JPWO2002024949A1 - 核酸解析方法 - Google Patents
核酸解析方法Info
- Publication number
- JPWO2002024949A1 JPWO2002024949A1 JP2002529541A JP2002529541A JPWO2002024949A1 JP WO2002024949 A1 JPWO2002024949 A1 JP WO2002024949A1 JP 2002529541 A JP2002529541 A JP 2002529541A JP 2002529541 A JP2002529541 A JP 2002529541A JP WO2002024949 A1 JPWO2002024949 A1 JP WO2002024949A1
- Authority
- JP
- Japan
- Prior art keywords
- nucleic acid
- internal standard
- extraction
- detection
- analyzed
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Granted
Links
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12Q—MEASURING OR TESTING PROCESSES INVOLVING ENZYMES, NUCLEIC ACIDS OR MICROORGANISMS; COMPOSITIONS OR TEST PAPERS THEREFOR; PROCESSES OF PREPARING SUCH COMPOSITIONS; CONDITION-RESPONSIVE CONTROL IN MICROBIOLOGICAL OR ENZYMOLOGICAL PROCESSES
- C12Q1/00—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions
- C12Q1/68—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions involving nucleic acids
- C12Q1/6844—Nucleic acid amplification reactions
- C12Q1/6851—Quantitative amplification
Landscapes
- Chemical & Material Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Organic Chemistry (AREA)
- Engineering & Computer Science (AREA)
- Zoology (AREA)
- Wood Science & Technology (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Health & Medical Sciences (AREA)
- Biophysics (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Immunology (AREA)
- Microbiology (AREA)
- Molecular Biology (AREA)
- Analytical Chemistry (AREA)
- Physics & Mathematics (AREA)
- Biotechnology (AREA)
- Biochemistry (AREA)
- Bioinformatics & Cheminformatics (AREA)
- General Engineering & Computer Science (AREA)
- General Health & Medical Sciences (AREA)
- Genetics & Genomics (AREA)
- Measuring Or Testing Involving Enzymes Or Micro-Organisms (AREA)
Abstract
Description
本発明は核酸の核酸解析方法、及び該方法を実施するためのキットに関する。詳細には、本発明の方法は、解析対象核酸の抽出工程、及び検出工程、場合によっては更に増幅工程を含み、それぞれ各工程において解析対象核酸と識別して検出可能な内部標準核酸を少なくとも一種類以上、解析対象核酸と同時に処理し、該内部標準核酸の検出結果から、各工程の成否を判定し、さらには該判定結果に基づき再解析を実施する。
背景技術
生物試料から遺伝子を単離し解析することは、分子生物学的研究にとって非常に有効な手段であるばかりでなく、医療分野においても盛んに利用されつつある。これまでにも遺伝子機能解析のため多くの遺伝子が生物個体、組織から単離、同定されている。また遺伝子増幅法として、ポリメラーゼ・チェイン・リアクション(PCR)法(Science:Vol.239、pp.487−491(1988))が開発され、存在量が非常に少ない遺伝子の単離や検出が可能となった。さらに、ヒトゲノム解析が急速に進展し、一塩基多型など遺伝子の変異と疾病または薬剤反応との関連付けが注目されている。このような遺伝子多型は分子生物学や遺伝学に留まらず、医学診断分野におけるオーダーメイド治療または投薬での利用が期待されている。
代表的な遺伝子の解析工程は、試料からの解析対象核酸の抽出工程及び検出工程から構成され、さらに該抽出工程と該検出工程の間に核酸増幅工程を含む場合もある。
核酸の抽出方法として広く知られているのは、プロテアーゼK等の蛋白質分解酵素や界面活性剤を加えて細胞を破壊および蛋白質を分解して核酸を遊離させ、フェノール/クロロホルムを添加し、遠心分離で核酸を水相に分配させた後、分取した水相にエタノールやイソプロパノール等を添加して核酸を不溶化させる、いわゆるプロテアーゼK/フェノール法(Molecular cloning:A Laboratory manual Appendix E3〜E4(New York:Cold Spring Harbor Laboratory、1989)である。しかし、本法は遠心分離を含むなど自動化には必ずしも適してはおらず、このような問題に対して、核酸の固体相への吸着特性を利用した方法が提案されており、例えばカオトロピック塩の存在下で核酸がガラスに結合することが、プロシーディング・オブ・ナショナル・アカデミー・オブ・サイエンス・オブ・ザ・ユーエスエイ、第76巻、615〜619頁(1979年)(Proc.Natl.Acad.Sci.USA76、615−619(1979))に記載されている。この核酸がある条件下において珪素酸化物(シリカ)に結合する特性を応用して、磁性シリカ粒子、シリカ粒子、シリカ繊維またはフィルター、およびこれらを含むスピンカラムまたはマイクロプレートなどによる核酸抽出キットや核酸抽出自動化装置が開示(特表平10−504834、特表平9−505724、特開平8−320274、特開平9−304385、特公2807090)されている。
核酸検出工程に用いられる方法、特に一塩基以上の配列が異なる核酸を検出する方法としては、例えばゲル電気泳動を用いた一本鎖DNA高次構造多型(SSCP)または制限酵素断片長多型(RFLP)、ガラスやシリコンウエハまたは各種ビーズに一本鎖核酸を固定化し、対象核酸とのハイブリダイゼーションを検出するマイクロアレイ法、DNAチップ法、ビーズアレイ法さらにパイロシーケンス法、インベーダー法、質量分析法、HPLC法などが、開発され広く利用されている。
核酸増幅方法としては、ポリメラーゼ連鎖反応(PCR)(米国特許4683195号および4683202号)、核酸配列基準増幅(NASBA)(欧州特許0、329、822号)などが公知であり利用されている。さらに、競合増幅または共増幅を利用した核酸の定量法が一般に知られている。この方法では、解析対象核酸と同一のプライマーと反応する数種類の内部標準核酸を同一容器内で増幅反応させ、既知量の該内部標準核酸を基準に対象核酸量を定量するものである(特表平8−107798、特表平8−501222、特表平11−123095、特表平11−506613)。
かかる従来技術は主に核酸増幅工程に内部標準核酸などと一般に称される解析対象核酸とは識別して検出可能な一定量の核酸を解析対象核酸と同時に増幅することによる、対象核酸量の定量に専ら利用されており、あくまでも解析対象核酸が正常に準備されていることを前提としている(特表平8−107798、特表平11−123095、特表平11−506613)。一方、特表平8−501222では抽出工程における対象核酸の抽出効率を反映させる方法や試料間の相互汚染を検出する方法が記載されているが、核酸増幅工程を含むことが必須であり、一連の核酸解析工程全体の成否および/またはどの工程で異常が生じたかを判定することは困難であった。
したがって、本発明は核酸の解析において、解析結果の信頼性の保証または向上を目的とした核酸解析方法を提供することを目的とする。
発明の開示
本発明は、解析対象核酸の抽出工程、及び検出工程、場合によっては該抽出工程と該検出工程の間に更に増幅工程を含む、核酸解析方法において、解析対象核酸および他の工程で使用される内部標準核酸とは識別して検出可能な一種類以上の内部標準核酸をそれぞれ各工程の実施前に試料に添加した後、対象核酸と同一容器内で各工程を実施し、核酸検出工程における各内部標準核酸の検出結果から各工程の成否を判定する方法を提供する。
すなわち、本発明は、解析対象核酸の抽出工程及び検出工程を含む核酸解析方法において、解析対象核酸と識別して検出可能な1種類以上の抽出用内部標準核酸を添加した後に核酸を抽出すること、及び上記検出工程による上記内部標準核酸の検出結果から抽出工程の成否を判定することを含む、核酸解析方法を提供する。
更に本発明は、解析対象核酸の抽出工程及び検出工程を含む核酸解析方法において、
解析対象核酸及び相互に識別して検出可能な1種類以上の抽出用内部標準核酸及び検出用内部標準核酸を添加した後に上記抽出工程及び検出工程を行うこと、そして上記検出工程による上記内部標準核酸の検出結果から抽出工程及び検出工程の成否を判定することを含む、核酸解析方法を提供する。
更にまた本発明は、解析対象核酸の抽出工程、増幅工程及び検出工程を含む核酸解析方法において、
解析対象核酸及び相互に識別して検出可能な1種類以上の抽出用内部標準核酸、増幅用内部標準核酸及び検出用内部標準核酸を添加した後に上記抽出工程及び検出工程を行うこと、そして上記検出工程による上記内部標準核酸の検出結果から抽出工程及び検出工程の成否を判定することを含む、核酸解析方法を提供する。
また、本発明は、解析対象核酸の抽出工程及び検出工程を含む核酸解析方法において、
(a)解析対象核酸を含有する試料に、該解析対象核酸と識別して検出可能な1種類以上の抽出用内部標準核酸を添加した後に核酸を抽出する核酸抽出工程、
(b)上記工程(a)において抽出された核酸を含有する試料に、上記解析対象核酸及び抽出用内部標準核酸と識別して検出可能な1種類以上の検出用内部標準核酸を添加した後に核酸を検出する核酸検出工程、及び
(c)核酸検出工程における上記の各内部標準核酸の検出結果から上記各工程の成否を判定する工程、
を含むことを特徴とする、核酸解析方法を提供する。
また、本発明は、解析対象核酸の抽出工程、増幅工程及び検出工程を含む核酸解析方法において、
(a)解析対象核酸を含有する試料に、解析対象核酸と同時に増幅可能であるが、該解析対象核酸と識別して検出可能な1種類以上の抽出用内部標準核酸を添加した後に核酸を抽出する核酸抽出工程、
(b)上記工程(a)において抽出された核酸を含有する試料に、上記解析対象核酸及び上記抽出用内部標準核酸と同時に増幅可能であるが、上記解析対象核酸及び上記抽出用内部標準核酸と識別して検出可能な1種類以上の増幅用内部標準核酸を添加した後に核酸を増幅する核酸増幅工程、
(c)上記工程(b)において増幅された核酸を含有する試料に、上記解析対象核酸、抽出用内部標準核酸、及び検出用内部標準核酸のいずれとも互いに識別して検出可能な1種類以上の検出用内部標準核酸を添加した後に核酸を検出する核酸検出工程、及び
(d)核酸検出工程における上記の各内部標準核酸の検出結果から上記各工程の成否を判定する工程、
を含むことを特徴とする、核酸解析方法を提供する。
さらに、本発明の核酸解析方法は、前記抽出工程、増幅工程または検出工程の成否判定結果に基づき、再度いずれかの工程から解析を実施することを特徴とする。
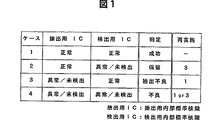
さらに、具体的には解析対象核酸を含む試料に解析対象核酸とは少なくとも一塩基以上配列の異なる一定量の抽出用内部標準核酸を添加し、その後核酸抽出工程を実施し、解析対象核酸及び抽出用内部標準核酸とは少なくとも一塩基以上配列の異なる一定量の検出用内部標準核酸を得られた核酸抽出物に添加し、その後一塩基以上配列の異なる核酸を識別検出可能な公知の核酸検出工程を実施する。その結果、図1に示すように各工程の成否を判定し、さらには該判定結果に基づき再解析を決定する。また、対象核酸を全く含まない試料(ブランク)を対象試料と同時処理することにより、試料の汚染(コンタミ)による偽陽性を監視し、再解析の判定に利用することもできる。この場合、ブランクで対象核酸が検出された場合はコンタミを生じており、抽出用内部標準核酸および検出用内部標準核酸の検出結果に係らず、除洗作業後再度、解析をやり直す。
以下、抽出用内部標準核酸及び検出用内部標準核酸の検出結果が正常であった場合及び正常でなかった場合の判定、及び正常でなかった場合に再実施の必要な工程について、図1を参照しながら説明する。
ケース1(抽出用内部標準核酸及び検出用内部標準核酸の検出結果が共に正常の場合):各工程は正常に実施され、解析対象核酸の核酸解析操作は、「成功」と判定する。
ケース2(抽出用内部標準核酸の検出結果が正常で、検出用内部標準核酸の検出結果が異常又は未検出の場合):解析対象核酸がブランクで検出されなかった場合、解析対象核酸の核酸解析操作は正常に実施された可能性が高いと考えられるが、該検出用内部標準核酸及び/又は該検出用内部標準核酸の添加機構が異常である可能性があり、「保留」と判定する。したがって、該検出用内部標準核酸を交換するか、該検出用内部標準核酸の添加機構を点検し、あるいはその双方を行い、図2に示す「再実施3」から再度実施する。
ケース3(抽出用内部標準核酸の検出結果が異常又は未検出で、検出用内部標準核酸の検出結果が正常の場合):核酸抽出工程が正常に実施されなかったと考えられ、「抽出不良」と判定し、図2に示す「再実施1」から再度実施する。特に、解析対象核酸が検出されなかった場合、偽陰性の可能性が極めて高いと考えられる。また、解析対象核酸が解析対象試料で検出された場合、該抽出用内部標準核酸及び/又は該抽出用内部標準核酸の添加機構が異常である可能性があり、該抽出用内部標準核酸を交換するか、該抽出用内部標準核酸の添加機構を点検し、あるいはその双方を行い、図2に示す「再実施1」から再度実施する。
ケース4(抽出用内部標準核酸及び検出用内部標準核酸の検出結果が共に異常又は未検出の場合):抽出用内部核酸及び検出用内部標準核酸が共に未検出の場合、核酸抽出工程および核酸検出工程が正常に実施されなかったと考えられ、「不良」と判定し、図2に示す「再実施1」から再度実施する。抽出用内部核酸が未検出ではない異常の場合、核酸検出工程が正常に実施されなかったと考えられ、「不良」と判定し、図2に示す「再実施3」から再度実施する。この再実施において「成功」の判定ができない場合は「再実施1」から再度実施する。
さらに、ケース2〜4において、再実施後、ケース1の「成功」と判定できない場合は、その判定結果に基づいて再実施を繰り返す。
本発明に用いられる核酸抽出工程には、上記プロテアーゼK/フェノール法、核酸の固体相への吸着特性を利用した方法、例えば磁性シリカ粒子、シリカ粒子、シリカ繊維またはフィルター、およびこれらを含むスピンカラムまたはマイクロプレートなどによる核酸抽出方法等の公知の方法を適宜使用することができるが、特にこれらに限定するものではない。
本発明に用いられる核酸検出工程には、公知の方法であるゲル電気泳動を用いた一本鎖DNA高次構造多型(SSCP)または制限酵素断片長多型(RFLP)、マイクロアレイ法、DNAチップ法、ビーズアレイ法さらにパイロシーケンス法、インベーダー法、質量分析法、HPLC法などがあり、少なくとも一塩基以上配列の異なる核酸を識別して検出可能であれば、利用できる。また、該抽出用内部標準核酸または該検出用内部標準核酸の検出信号は、各工程の成否の判定の他、該対象核酸の定量、塩基長測定または検出信号の補正など各種データ処理に用いることも可能である。
該核酸検出工程には、核酸検出に必要な試料の前処理、例えば、熱変性処理や各種標識処理や溶媒交換などを含み、検出用内部標準核酸の核酸抽出物への添加は該前処理前に実施されることが望ましい。
次に、該抽出工程と該検出工程の間に核酸増幅工程を含む核酸解析方法において、解析対象核酸を含む試料に、解析対象核酸と同時に増幅可能であるが、該解析対象核酸と少なくとも一塩基以上配列が異なる一定量の抽出用内部標準核酸を一種類以上添加し、核酸抽出工程を実施する。次に解析対象核酸と同時に増幅可能であるが、該解析対象核酸及び抽出用内部標準核酸と少なくとも一塩基以上配列が異なる一定量の増幅用内部標準核酸を一種類以上、得られた核酸抽出物に添加し、その後核酸増幅工程を実施する。次いで、解析対象核酸、抽出用内部標準核酸、及び増幅用内部標準核酸と少なくとも一塩基以上配列が異なる一定量の検出用内部標準核酸を一種類以上、得られた核酸増幅物に添加し、その後一塩基以上配列の異なる核酸を識別検出可能な公知の核酸検出工程を実施する。
その結果、図3に示すように、上記と同様に各工程の成否を判定し、さらには該判定結果に基づき再解析を決定する。また、解析対象核酸を含まないブランク(対照試料)を解析対象核酸と同時処理することにより、コンタミによる偽陽性を監視し、再解析の判定に利用することができる。この場合、ブランクで対象核酸が検出された場合コンタミを生じており、抽出用内部標準核酸および検出用内部標準核酸の結果に係らず、除洗作業後再度、解析をやり直す必要があることになる。
核酸増幅方法としては、ポリメラーゼ連鎖反応(PCR)、核酸配列基準増幅(NASBA)等の公知の方法を適宜用いれば良く、特に限定されるものではない。尚、増幅工程を含む場合、解析対象核酸と同時に増幅される抽出用内部標準核酸及び増幅用内部標準核酸の量は、検出用内部標準核酸と比較して少量にすることができるが、好ましい相対的量比は、使用する増幅方法及び検出方法に応じて異なり、特定されるものではない。
以下、抽出用内部標準核酸、増幅用内部標準核酸、及び検出用内部標準核酸の検出結果と、各工程の成否判定の関係を、図3を参照しながら説明する。
ケース1(抽出用内部標準核酸、増幅用内部標準核酸及び検出用内部標準核酸の検出結果がいずれも正常の場合):各工程は正常に実施され、解析対象核酸の核酸解析操作は、「成功」と判定する。
ケース2(抽出用内部標準核酸及び増幅用内部標準核酸の検出結果が正常であり、検出用内部標準核酸の検出結果が異常又は未検出の場合):解析対象核酸がブランクで検出されなかった場合、解析対象核酸の核酸解析操作は正常に実施された可能性が高いと考えられるが、該検出用内部標準核酸及び/又は該検出用内部標準核酸の添加機構が異常である可能性があり、「保留」と判定する。したがって、該検出用内部標準核酸を交換するか、該検出用内部標準核酸の添加機構を点検し、あるいはその双方を行い、図2に示す「再実施3」から再度実施する
ケース3(抽出用内部標準核酸及び検出用内部標準核酸の検出結果が正常であり、増幅用内部標準核酸の検出結果が異常又は未検出の場合):解析対象核酸がブランクで検出されなかった場合、解析対象核酸の核酸解析操作は正常に実施された可能性が高いと考えられるが、該増幅用内部標準核酸及び/又は該増幅用内部標準核酸の添加機構が異常である可能性があり、「保留」と判定する。したがって、該増幅用内部標準核酸を交換するか、該増幅用内部標準核酸の添加機構を点検し、あるいはその双方を行い、図2に示す「再実施2」から再度実施する。
ケース4(抽出用内部標準核酸の検出結果が正常であり、増幅用内部標準核酸及び検出用内部標準核酸の検出結果が異常又は未検出の場合):解析対象核酸がブランクで検出されなかった場合、解析対象核酸の核酸解析操作は正常に実施された可能性が高いと考えられるが、該増幅用内部標準核酸及び/又は該増幅用内部標準核酸の添加機構および該検出用内部標準核酸及び/又は該検出用内部標準核酸の添加機構が異常である可能性があり、「保留」と判定する。したがって、該増幅用内部標準核酸及び/又は該増幅用内部標準核酸の添加機構および該検出用内部標準核酸及び/又は該検出用内部標準核酸の添加機構の交換または点検を行い、図2に示す「再実施2」から再度実施する。
ケース5(抽出用内部標準核酸の検出結果が異常又は未検出で、増幅用内部標準核酸及び検出用内部標準核酸の検出結果が正常の場合):核酸抽出工程が正常に実施されなかったと考えられ、「抽出不良」と判定し、図2に示す「再実施1」から再度実施する。特に、解析対象核酸が検出されなかった場合、偽陰性の可能性が極めて高いと考えられる。また、解析対象核酸が解析対象試料で検出された場合、該抽出用内部標準核酸及び/又は該抽出用内部標準核酸の添加機構が異常である可能性があり、該抽出用内部標準核酸を交換するか、該抽出用内部標準核酸の添加機構を点検し、あるいはその双方を行い、図2に示す「再実施1」から再度実施する。
ケース6(抽出用内部標準核酸及び検出用内部標準核酸の検出結果が異常又は未検出であり、増幅用内部標準核酸の検出結果が正常の場合):核酸抽出工程が正常に実施されなかったと考えられ、「抽出不良」と判定し、さらに該検出用内部標準核酸及び/又は該検出用内部標準核酸の添加機構が異常である可能性があり、該検出用内部標準核酸を交換するか、該検出用内部標準核酸の添加機構を点検し、あるいはその双方を行い、図2に示す「再実施1」から再度実施する。また、解析対象核酸が解析対象試料で検出された場合、該抽出用内部標準核酸及び/又は該抽出用内部標準核酸の添加機構および検出用内部標準核酸及び/又は該検出用内部標準核酸の添加機構が異常である可能性があり、該抽出用内部標準核酸及び/又は該抽出用内部標準核酸の添加機構および検出用内部標準核酸及び/又は該検出用内部標準核酸の添加機構の交換または点検を行い、図2に示す「再実施1」から再度実施する。
ケース7(抽出用内部標準核酸及び増幅用内部標準核酸の検出結果が異常/又は未検出であり、検出用内部標準核酸の検出結果が正常の場合):増幅工程及び/又は核酸抽出工程が正常に実施されず、「抽出/増幅不良」と判定し、図2に示す「再実施1」から再度実施する。解析対象核酸が解析対象試料で検出された場合、該抽出用内部標準核酸及び/又は該抽出用内部標準核酸の添加機構および増幅用内部標準核酸及び/又は該増幅用内部標準核酸の添加機構が異常である可能性があり、該抽出用内部標準核酸及び/又は該抽出用内部標準核酸の添加機構および増幅用内部標準核酸及び/又は該増幅用内部標準核酸の添加機構の交換または点検を行い、図2に示す「再実施1」から再度実施する。
ケース8(抽出用内部標準核酸、増幅用内部標準核酸及び検出用内部標準核酸の検出結果がいずれも異常又は未検出の場合):抽出用内部標準核酸、増幅用内部標準核酸および検出用内部標準核酸とも未検出の場合、核酸抽出工程、核酸増幅工程および核酸検出工程が正常に実施されなかったと考えられ、「不良」と判定し、図2に示す「再実施1」から再度実施する。抽出用内部核酸および増幅用内部標準核酸とも未検出ではない異常の場合、核酸検出工程が正常に実施されなかったと考えられ、「不良」と判定し、図2に示す「再実施3」から再度実施する。この再実施において「成功」の判定ができない場合は「再実施1」から再度実施する。
さらに、ケース2〜8において、再実施後、ケース1の「成功」と判定できない場合は、その判定結果に基づいて再実施を繰り返す。
また、該内部標準核酸は一定量、つまり既知濃度で添加されることから、内部標準核酸の検出信号量に基づいて、対象核酸の定量や塩基長測定や検出信号の補正など各種データ処理を行うことが可能である。
増幅工程において、内部標準核酸を解析対象核酸と同時に増幅させる手段としては、広く知られている共通プライマーペアと呼ばれる解析対象核酸と同一のプライマー配列を内部標準核酸に包含する方法が、経済的かつ増幅安定性に優れているが、独立した複数の個別プライマーペアを用いても本発明は実施可能である。
さらに、内部標準核酸の塩基配列は対象核酸と少なくとも一塩基以上異なる必要があるが、増幅工程を含む場合やハイブリダイゼーションを利用したDNAチップなどを検出工程に利用する場合は、対象核酸と類似性が高い方が増幅効率や結合効率が同等になり易いため、再現性に優れており好適である。
本発明はまた、上記の本発明の核酸解析方法を実施するためのキットであって、
(i)抽出用内部標準核酸及び/又は抽出用内部標準核酸を含む抽出用試薬、及び
(ii)検出用内部標準核酸及び/又は検出用内部標準核酸を含む検出用試薬、を含むことを特徴とするキットを提供する。
本発明は更に、上記の核酸解析方法を実施するためのキットであって、
(i)抽出用内部標準核酸及び/又は抽出用内部標準核酸を含む抽出用試薬、
(ii)検出用内部標準核酸及び/又は検出用内部標準核酸を含む検出用試薬、及び
(iii)増幅用内部標準核酸及び/又は増幅用内部標準核酸を含む増幅用試薬、
を含むことを特徴とするキットを提供する。
上記キットにおいて、各内部標準核酸は、単独でキットに含まれていても良いが、溶媒、標識用試薬、プライマー等の、各工程において必要とされる他の試薬と共に含まれていても良い。試薬に含むことができる各成分については、当業者であれば容易に認識できるものであり、特に限定するものではない。
また、本発明に係るキットは、上記抽出用内部標準核酸が解析対象核酸と少なくとも1塩基以上配列の異なる一定量の核酸であり、上記検出用内部標準核酸が該解析対象核酸及び上記抽出用内部標準核酸のいずれとも少なくとも1塩基以上配列の異なる一定量の核酸であることを特徴とする。
また、上記キットが増幅用内部標準核酸及び/又は増幅用内部標準核酸を含む増幅用試薬を含む場合には、上記抽出用内部標準核酸が解析対象核酸と同時に増幅可能であるが、該解析対象核酸と少なくとも1塩基以上配列が異なる一定量の核酸であり、上記増幅用内部標準核酸が該解析対象核酸と同時に増幅可能であるが該解析対象核酸及び上記抽出用内部標準核酸と少なくとも1塩基以上配列が異なる一定量の核酸であり、上記検出用内部標準核酸が解析対象核酸、上記抽出用内部標準核酸及び上記増幅用内部標準核酸のいずれとも互いに少なくとも1塩基以上配列が異なる一定量の核酸であることを特徴とする。
これにより、本発明のキットを使用して本発明の核酸解析方法を実施する際に、1塩基以上配列の異なる核酸を識別可能な検出方法を使用することが可能であり、また、内部標準核酸の検出結果から、解析対象核酸の定量や塩基長測定や検出信号の補正など各種データ処理を行うことも可能となる。
発明を実施するための形態
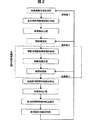
本発明の実施形態を表すフローチャートを図2に示す。
人の血液やその他の体液、組織または細胞、細菌、ウイルスなどの解析対象核酸を含む試料に、
抽出用内部標準核酸及び/又は抽出用内部標準核酸を含む抽出用試薬を試料に添加した後、解析対象核酸および抽出用内部標準核酸を同時に抽出する工程を実施し、
次に、検出用内部標準核酸及び/又は検出用内部標準核酸を含む検出用試薬を得られた核酸に添加した後、解析対象核酸、抽出用内部標準核酸、及び検出用内部標準核酸をそれぞれ識別して検出する工程を実施し、
各内部標準核酸の検出結果から前述のケースに従って各工程の成否を判定し、判定結果に基づいて該抽出工程又は核酸検出工程から、再実施を行う。
あるいはまた、上記解析対象核酸を含む試料に、
抽出用内部標準核酸及び/又は抽出用内部標準核酸を含む抽出用試薬を試料に添加した後、解析対象核酸および抽出用内部標準核酸を同時に抽出する工程を実施し、
増幅用内部標準核酸及び/又は増幅用内部標準核酸を含む増幅用試薬を核酸抽出物に添加した後、解析対象核酸、抽出用内部標準核酸、及び増幅用内部標準核酸を同時に増幅する工程を実施し、
検出用内部標準核酸及び/又は検出用内部標準核酸を含む検出用試薬を核酸増幅物に添加した後、解析対象核酸、抽出用内部標準核酸、検出用内部標準核酸、及び増幅用内部標準核酸をそれぞれ識別して検出する工程を実施し、
各内部標準核酸の検出結果から前述のケースに従って各工程の成否を判定し、判定結果に基づいて該抽出工程、増幅工程又は検出工程から再実施を行う。
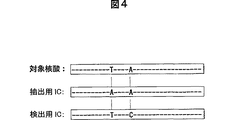
本発明に用いられる内部標準核酸の一例を図4に示す。具体的には、解析対象核酸を含む試料に、解析対象核酸とは少なくとも一塩基以上配列の異なる一定量の抽出用内部標準核酸を添加し、その後核酸抽出工程を実施し、解析対象核酸及び抽出用内部標準核酸とは少なくとも一塩基以上配列の異なる一定量の検出用内部標準核酸を得られた核酸抽出物に添加し、その後一塩基以上配列の異なる核酸を識別検出可能な核酸検出工程を実施する時に用いられる内部標準核酸の例である。解析対象核酸、抽出用内部標準核酸、及び検出用内部標準核酸の塩基長は同一であり、解析対象核酸塩基配列中の特定位置のチミン(T)がアデニン(A)であり、一塩基だけ異なる塩基配列を持つ核酸を抽出用内部標準核酸(抽出用IC)とし、解析対象核酸塩基配列中の別の特定位置のAがシトシン(C)であり、一塩基だけ異なる塩基配列を持つ核酸を検出用内部標準核酸(検出用IC)としたものである。この場合、抽出用ICと検出用ICは二塩基だけ異なる塩基配列を持つ核酸となり、一塩基以上配列の異なる核酸を識別検出可能な検出器により、異なる信号として検出される。
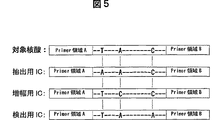
さらに、該抽出工程と該検出工程の間に核酸増幅工程を含む核酸解析方法において用いられる内部標準核酸の一例を図5に示す。この場合、本発明の方法は、具体的には解析対象核酸と同時に増幅可能であるが、該解析対象核酸と少なくとも一塩基以上配列が異なる、一定量の抽出用内部標準核酸を解析対象核酸を含む試料に添加し、核酸抽出工程を実施する。次いで、解析対象核酸と同時に増幅可能であるが、該解析対象核酸及び抽出用内部標準核酸と少なくとも一塩基以上配列が異なる一定量の増幅用内部標準核酸を得られた核酸抽出物に添加し、核酸増幅工程を実施する。その後、解析対象核酸、抽出用内部標準核酸、及び増幅用内部標準核酸と少なくとも一塩基以上配列が異なる一定量の検出用内部標準核酸を得られた核酸増幅物に添加し、一塩基以上配列の異なる核酸を識別検出可能な核酸検出工程を実施する。さらに、増幅工程において、内部標準核酸を対象核酸と同時に増幅させる手段として広く知られている共通プライマーペアど呼ばれる解析対象核酸と同一のプライマー配列を内部標準核酸に包含する方法を用いた例である。
図5に示すように、解析対象核酸塩基配列中の特定位置のTがAに一塩基だけ異なる塩基配列を持つ核酸を抽出用内部標準核酸(抽出用IC)とし、解析対象核酸塩基配列中の別の特定位置のAがCに一塩基だけ異なる塩基配列を持つ核酸を増幅用内部標準核酸(増幅用IC)とし、解析対象核酸塩基配列中のさらに別の特定位置のCがAに一塩基だけ異なる塩基配列を持つ核酸を検出用内部標準核酸(検出用IC)としたものである。この場合、抽出用ICと増幅用ICと検出用ICはそれぞれ二塩基ずつ異なる塩基配列を持つ核酸となり、一塩基以上配列の異なる核酸を識別検出可能な検出器により、異なる信号として検出される。さらに上記の塩基配列に差異を有する領域の両側に存在するプライマー領域A、プライマー領域Bは、解析対象核酸、及び各内部標準核酸と同一の塩基配列であることから、一種類のプライマーペアでそれぞれの塩基配列を増幅することが可能である。
本発明の核酸解析方法を実施したときに得られる結果の一例を図6に示す。図6は、解析対象核酸を含む試料に解析対象核酸と少なくとも一塩基以上配列が異なる一定量の抽出用内部標準核酸と、解析対象核酸及び抽出用内部標準核酸と少なくとも一塩基以上配列が異なる一定量の検出用内部標準核酸を用いて、一塩基以上配列の異なる核酸を識別検出可能な核酸検出工程としてゲル電気泳動を用いた一本鎖DNA高次構造多型(SSCP)を実施した時の電気泳動クロマトグラムの例である。SSCPはキャピラリー電気泳動装置を用いて、それぞれ蛍光標識した対象核酸、抽出用ICと検出用ICをレーザーで励起し、CCDカメラで蛍光スペクトルを測定した。
図6に示すように、「正常」のケースは、それぞれ抽出用IC、対象核酸、検出用ICとも所定のピーク強度が得られており、解析工程が正常に実施されたときのクロマトグラムの例である。一方、「異常1」のケースは、図1に示すケース3の一例である。抽出用ICの蛍光ピークが極めて小さく抽出用ICは異常であり、検出用ICの蛍光ピークは正常のケースと同じ検出時間に同等の蛍光強度を示しているので正常である。したがって、抽出不良と判断し、図2に示す再実施1を行う。「異常2」のケースは、図1に示すケース4の一例である。抽出用ICおよび検出用ICの蛍光ピークが広がり、抽出用ICおよび検出用ICは未検出ではないが異常である。特に、本ケースでは解析対象核酸の蛍光ピークも広がっているため、電気泳動による核酸分離能が低下していると考えられ、図2に示す再実施3を行う。
次に、本発明の核酸解析方法をDNAチップを用いて実施したときに得られる結果の一例を図7に示す。具体的には解析対象核酸と同時に増幅可能であるが、該解析対象核酸と少なくとも一塩基以上配列が異なる一定量の抽出用内部標準核酸、解析対象核酸と同時に増幅可能であるが、該解析対象核酸及び抽出用内部標準核酸と少なくとも一塩基以上配列が異なる一定量の増幅用内部標準核酸、および解析対象核酸、抽出用内部標準核酸、及び増幅用内部標準核酸と少なくとも一塩基以上配列が異なる一定量の検出用内部標準核酸を用いて、一塩基以上配列の異なる核酸を識別検出可能な核酸検出工程としてDNAチップを実施したときの例である。
DNAチップ上には、それぞれ抽出用IC1、抽出用IC2、抽出用IC3、増幅用IC、検出用ICおよび対象核酸Aと相補的な塩基配列を含有するプローブが固定化されている。このDNAチップ上で、それぞれ蛍光色素を標識した抽出用IC1、抽出用IC2、抽出用IC3、増幅用IC、検出用ICおよび対象核酸Aをハイブリダイズさせ、蛍光スペクトルを測定可能なDNAチップリーダーで検出した。
図7に示すように「正常」のケースはそれぞれ抽出用IC1、抽出用IC2、抽出用IC3、増幅用IC、検出用ICのいずれも表に示した所定のピーク強度(0.5、1.0又は1.5)が得られ、解析工程が正常に実施された例である。さらに、内部標準核酸の検出信号量に基づいて、対象核酸を定量する場合には、抽出用IC1、抽出用IC2、抽出用IC3の蛍光強度と既知の核酸量より、核酸濃度の検量線を作成し、対象核酸Aの蛍光強度から対象核酸の核酸量は2.4ngであると定量できる。
一方、「異常」のケースは図3のケース5に示した一例である。抽出用IC1、抽出用IC2、及び抽出用IC3の蛍光強度がそれぞれ0.1であり、それぞれの所定の蛍光強度である0.5、1.0又は1.5を下回っており、抽出用ICは異常である。その他の増幅用IC及び検出用ICの蛍光ピークは所定の蛍光強度と同じ強度を示しているので正常である。このとき対象核酸Aが検出されていないのは偽陰性の可能性が高いと考えられる。したがって、抽出不良と判断し、図2に示す再実施1を行う。
各内部標準核酸の検出信号量に基づいて、検出信号の補正を行ったデータ処理の一例を図8に示す。図6と同様、一塩基以上配列の異なる核酸を識別検出可能な核酸検出工程としてキャピラリー電気泳動装置を用いたSSCPを実施した時の電気泳動クロマトグラムの例である。
データ処理前に示したクロマトグラムは各レーンで内部核酸の検出時間にずれを生じている。このような時、対象核酸AとA’またはA”が同一ピークであるか、また対象核酸BとB’またはB”が同一ピークであるかを一目で判定することは困難である。そこで、本来既知の内部核酸は同じ検出時間になることからそれぞれのレーンの抽出用ICまたは検出用ICが同じ検出時間になるようにクロマトグラムを補正した結果がデータ処理後のクロマトグラムである。このようなデータ処理をすると対象核酸AとA’およびA”は同一ピークであり、対象核酸BとB”は同一ピークであるがB’は異なるピークであることが一目瞭然に判定できる。
産業上の利用可能性
本発明によれば、核酸解析を構成する抽出、増幅、及び検出の各工程での操作の成否を判定することが可能となり、得られる解析結果の信頼性を高めると共に、再検査を自動化することも可能となる。本効果は特に医療分野において遺伝子解析に基づいて実施される検査・診断の信頼性の向上に寄与する。
本明細書で引用した全ての刊行物、特許及び特許出願をそのまま参考として本明細書にとり入れるものとする。
【図面の簡単な説明】
図1は、抽出工程及び検出工程を含む本発明の方法における各工程の成否判定表を示す。
図2は、本発明の核酸解析方法のフローチャートを示す。
図3は、抽出工程、増幅工程、及び検出工程を含む本発明の方法における各工程の成否判定表を示す。
図4は、本発明の抽出用内部標準核酸および検出用内部標準核酸の一例を示す。
図5は、本発明の抽出用内部標準核酸、増幅用内部標準核酸、及び検出用内部標準核酸の一例を示す。
図6は、本発明の検出工程にゲル電気泳動を用いて一本鎖DNA高次構造多型を検出するために実施する本発明の方法における検出結果の一例を示す。
図7は、検出工程にDNAチップを用いた本発明の方法における検出結果を定量解析として示す一例を示す。
図8は、本発明の方法において検出工程にゲル電気泳動を用いて一本鎖DNA高次構造多型を検出するためのデータ処理の一例を示す。
Claims (11)
- 解析対象核酸の抽出工程及び検出工程を含む核酸解析方法において、
解析対象核酸と識別して検出可能な1種類以上の抽出用内部標準核酸を添加した後に核酸を抽出すること、及び上記検出工程による上記内部標準核酸の検出結果から抽出工程の成否を判定することを含む、核酸解析方法。 - 解析対象核酸の抽出工程及び検出工程を含む核酸解析方法において、
解析対象核酸及び相互に識別して検出可能な1種類以上の抽出用内部標準核酸及び検出用内部標準核酸を添加した後に上記抽出工程及び検出工程を行うこと、そして上記検出工程による上記内部標準核酸の検出結果から抽出工程及び検出工程の成否を判定することを含む、核酸解析方法。 - 解析対象核酸の抽出工程、増幅工程及び検出工程を含む核酸解析方法において、
解析対象核酸及び相互に識別して検出可能な1種類以上の抽出用内部標準核酸、増幅用内部標準核酸及び検出用内部標準核酸を添加した後に上記抽出工程及び検出工程を行うこと、そして上記検出工程による上記内部標準核酸の検出結果から抽出工程及び検出工程の成否を判定することを含む、核酸解析方法。 - 解析対象核酸の抽出工程及び検出工程を含む核酸解析方法において、
(a)解析対象核酸を含有する試料に、該解析対象核酸と識別して検出可能な1種類以上の抽出用内部標準核酸を添加した後に核酸を抽出する核酸抽出工程、
(b)上記工程(a)において抽出された核酸を含有する試料に、上記解析対象核酸及び抽出用内部標準核酸と識別して検出可能な1種類以上の検出用内部標準核酸を添加した後に核酸を検出する核酸検出工程、及び
(c)核酸検出工程における上記の各内部標準核酸の検出結果から上記各工程の成否を判定する工程、
を含むことを特徴とする、核酸解析方法。 - 解析対象核酸の抽出工程、増幅工程及び検出工程を含む核酸解析方法において、
(a)解析対象核酸を含有する試料に、解析対象核酸と同時に増幅可能であるが、該解析対象核酸と識別して検出可能な1種類以上の抽出用内部標準核酸を添加した後に核酸を抽出する核酸抽出工程、
(b)上記工程(a)において抽出された核酸を含有する試料に、上記解析対象核酸及び上記抽出用内部標準核酸と同時に増幅可能であるが、上記解析対象核酸及び上記抽出用内部標準核酸と識別して検出可能な1種類以上の増幅用内部標準核酸を添加した後に核酸を増幅する核酸増幅工程、
(c)上記工程(b)において増幅された核酸を含有する試料に、上記解析対象核酸、抽出用内部標準核酸、及び検出用内部標準核酸のいずれとも互いに識別して検出可能な1種類以上の検出用内部標準核酸を添加した後に核酸を検出する核酸検出工程、及び
(d)核酸検出工程における上記の各内部標準核酸の検出結果から上記各工程の成否を判定する工程、
を含むことを特徴とする、核酸解析方法。 - 請求項4又は5に記載の核酸解析方法において、上記核酸抽出工程、核酸増幅工程、及び核酸検出工程の成否判定結果に基づき、いずれかの工程から再度解析を実施することを特徴とする、核酸解析方法。
- 請求項4又は5に記載の核酸解析方法において、解析対象核酸を含まない対照試料を同時に処理し、その検出結果に基づいて判定を行うことを特徴とする、核酸解析方法。
- 請求項4から7に記載の核酸解析方法を実施するためのキットであって、
(i)抽出用内部標準核酸及び/又は抽出用内部標準核酸を含む抽出用試薬、及び
(ii)検出用内部標準核酸及び/又は検出用内部標準核酸を含む検出用試薬、を含むことを特徴とするキット。 - 請求項4から7記載の核酸解析方法を実施するためのキットであって、
(i)抽出用内部標準核酸及び/又は抽出用内部標準核酸を含む抽出用試薬、
(ii)検出用内部標準核酸及び/又は検出用内部標準核酸を含む検出用試薬、及び
(iii)増幅用内部標準核酸及び/又は増幅用内部標準核酸を含む増幅用試薬、
を含むことを特徴とするキット。 - 上記抽出用内部標準核酸が解析対象核酸と少なくとも1塩基以上配列の異なる一定量の核酸であり、上記検出用内部標準核酸が該解析対象核酸及び上記抽出用内部標準核酸のいずれとも少なくとも1塩基以上配列の異なる一定量の核酸であることを特徴とする、請求項8又は9に記載のキット。
- 上記抽出用内部標準核酸が解析対象核酸と同時に増幅可能であるが、該解析対象核酸と少なくとも1塩基以上配列が異なる一定量の核酸であり、上記増幅用内部標準核酸が該解析対象核酸と同時に増幅可能であるが該解析対象核酸及び上記抽出用内部標準核酸と少なくとも1塩基以上配列が異なる一定量の核酸であり、上記検出用内部標準核酸が解析対象核酸、上記抽出用内部標準核酸及び上記増幅用内部標準核酸のいずれとも互いに少なくとも1塩基以上配列が異なる一定量の核酸である、請求項9に記載のキット。
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| PCT/JP2000/006526 WO2002024949A1 (fr) | 2000-09-22 | 2000-09-22 | Procede d'analyse d'acide nucleique |
Related Child Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2005214419A Division JP2005348742A (ja) | 2005-07-25 | 2005-07-25 | 核酸解析方法 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JPWO2002024949A1 true JPWO2002024949A1 (ja) | 2004-01-29 |
| JP3752488B2 JP3752488B2 (ja) | 2006-03-08 |
Family
ID=11736503
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2002529541A Expired - Fee Related JP3752488B2 (ja) | 2000-09-22 | 2000-09-22 | 核酸解析方法 |
Country Status (4)
| Country | Link |
|---|---|
| US (1) | US7790368B1 (ja) |
| EP (1) | EP1319716B1 (ja) |
| JP (1) | JP3752488B2 (ja) |
| WO (1) | WO2002024949A1 (ja) |
Families Citing this family (20)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US7217542B2 (en) | 2002-10-31 | 2007-05-15 | Hewlett-Packard Development Company, L.P. | Microfluidic system for analyzing nucleic acids |
| JP2005180983A (ja) * | 2003-12-17 | 2005-07-07 | Hitachi High-Technologies Corp | 化学分析装置および化学分析用構造体 |
| CA2502549C (en) * | 2004-04-23 | 2016-02-16 | Becton, Dickinson And Company | Use of an extraction control in a method of extracting nucleic acids |
| US7981606B2 (en) | 2005-12-21 | 2011-07-19 | Roche Molecular Systems, Inc. | Control for nucleic acid testing |
| JP5063616B2 (ja) | 2006-02-03 | 2012-10-31 | インテジェニックス インコーポレイテッド | マイクロ流体デバイス |
| EP2109666A4 (en) * | 2007-02-05 | 2011-09-14 | Integenx Inc | MICROFLUIDIC AND NANOFLUIDIC DEVICES, SYSTEMS, AND APPLICATIONS |
| CN102803147B (zh) | 2009-06-05 | 2015-11-25 | 尹特根埃克斯有限公司 | 通用样品准备系统以及在一体化分析系统中的用途 |
| WO2012024658A2 (en) | 2010-08-20 | 2012-02-23 | IntegenX, Inc. | Integrated analysis system |
| CN113388605A (zh) | 2011-09-26 | 2021-09-14 | 凯杰有限公司 | 用于分离细胞外核酸的快速方法 |
| US10865440B2 (en) | 2011-10-21 | 2020-12-15 | IntegenX, Inc. | Sample preparation, processing and analysis systems |
| US20150136604A1 (en) | 2011-10-21 | 2015-05-21 | Integenx Inc. | Sample preparation, processing and analysis systems |
| WO2014063051A2 (en) * | 2012-10-18 | 2014-04-24 | Idexx Laboratories, Inc. | Nucleic acid amplification controls and kits and methods of use thereof |
| WO2014072367A1 (en) * | 2012-11-07 | 2014-05-15 | Qiagen Gmbh | Control for diagnostic assay |
| CN110560187B (zh) | 2013-11-18 | 2022-01-11 | 尹特根埃克斯有限公司 | 用于样本分析的卡盒和仪器 |
| US10208332B2 (en) | 2014-05-21 | 2019-02-19 | Integenx Inc. | Fluidic cartridge with valve mechanism |
| CN113092563A (zh) | 2014-10-22 | 2021-07-09 | 尹特根埃克斯有限公司 | 用于样品制备、处理和分析的系统和方法 |
| AU2016277476B2 (en) | 2015-06-10 | 2022-07-21 | Qiagen Gmbh | Method for isolating extracellular nucleic acids using anion exchange particles |
| EP4137583A1 (en) * | 2016-03-24 | 2023-02-22 | BioFire Diagnostics, LLC | Methods for quantitative amplification |
| US11185863B2 (en) | 2016-09-30 | 2021-11-30 | Koninklijke Philips N.V. | System for applying a reagent to a sample |
| WO2019163064A1 (ja) * | 2018-02-22 | 2019-08-29 | 学校法人 慶應義塾 | Pcr成否判定法 |
Family Cites Families (10)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US5096557A (en) | 1990-07-11 | 1992-03-17 | Genetype A.G. | Internal standard for electrophoretic separations |
| JP3594598B2 (ja) | 1993-07-09 | 2004-12-02 | アクゾ・ノベル・エヌ・ベー | 改良された核酸定量方法 |
| AT401270B (de) * | 1994-09-26 | 1996-07-25 | Immuno Ag | Verfahren zur quantifizierung von genomischer dna |
| CA2159044A1 (en) * | 1994-09-26 | 1996-03-27 | Falko-Guenter Falkner | Method of quantitating nucleic acids |
| WO1998004741A1 (en) * | 1996-07-26 | 1998-02-05 | Univera Pharmaceuticals, Inc. | Method of identifying aloe using pcr |
| WO1999002728A1 (en) | 1997-07-11 | 1999-01-21 | Brax Group Limited | Characterising nucleic acids |
| US6013444A (en) | 1997-09-18 | 2000-01-11 | Oligotrail, Llc | DNA bracketing locus compatible standards for electrophoresis |
| US5888740A (en) * | 1997-09-19 | 1999-03-30 | Genaco Biomedical Products, Inc. | Detection of aneuploidy and gene deletion by PCR-based gene- dose co-amplification of chromosome specific sequences with synthetic sequences with synthetic internal controls |
| US6258536B1 (en) * | 1998-12-01 | 2001-07-10 | Jonathan Oliner | Expression monitoring of downstream genes in the BRCA1 pathway |
| WO2000075377A2 (en) * | 1999-06-03 | 2000-12-14 | Jacques Schrenzel | Non-cognate hybridization system (nchs) |
-
2000
- 2000-09-22 WO PCT/JP2000/006526 patent/WO2002024949A1/ja active Application Filing
- 2000-09-22 US US09/958,727 patent/US7790368B1/en not_active Expired - Fee Related
- 2000-09-22 JP JP2002529541A patent/JP3752488B2/ja not_active Expired - Fee Related
- 2000-09-22 EP EP00961207.8A patent/EP1319716B1/en not_active Expired - Lifetime
Also Published As
| Publication number | Publication date |
|---|---|
| EP1319716B1 (en) | 2013-07-03 |
| WO2002024949A1 (fr) | 2002-03-28 |
| US7790368B1 (en) | 2010-09-07 |
| EP1319716A4 (en) | 2005-01-12 |
| EP1319716A1 (en) | 2003-06-18 |
| JP3752488B2 (ja) | 2006-03-08 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP3752488B2 (ja) | 核酸解析方法 | |
| JP4268944B2 (ja) | 核酸の検出あるいは定量方法 | |
| US7732138B2 (en) | Rapid genotyping analysis and the device thereof | |
| CN103946397B (zh) | 用于通用实时多重分析检测的双功能寡核苷酸探针 | |
| JP2005531314A (ja) | 配列の相違を検出する方法 | |
| Khan et al. | CRISPR-cas13 enzymology rapidly detects SARS-CoV-2 fragments in a clinical setting | |
| JP2023011943A (ja) | ハイブリッド多元ステップ核酸増幅 | |
| US20220290210A1 (en) | Extraction-free pathogen testing methods | |
| EP1426448A1 (en) | Method for lowering the effects of sequence variations in a diagnostic hybridization assay, probe for use in the assay and assay | |
| JP2005348742A (ja) | 核酸解析方法 | |
| JP4418450B2 (ja) | 生物学的dnaの検出 | |
| EP2660332B1 (en) | Positive control concept | |
| WO2011153385A2 (en) | Methods and systems for sequential determination of genetic mutations and/or variants | |
| Hue-Roye et al. | Principles of PCR-based assays | |
| JP2002171986A (ja) | 塩基多型の同定方法 | |
| US20050239086A1 (en) | Multiplex systems, methods, and kits for detecting and identifying nucleic acids | |
| EP3752636A1 (en) | Barcoded molecular standards | |
| Meaney et al. | Non-invasive prenatal diagnosis | |
| US20210395804A1 (en) | Sensitive and multiplexed detection of nucleic acids and proteins for large scale serological testing | |
| US20140073530A1 (en) | Rapid Genotyping Analysis and the Method Thereof | |
| JP4227139B2 (ja) | 生体試料の分析方法、反応液、及び分析装置 | |
| WO2022236193A2 (en) | Viral variant detection | |
| WO2021173310A1 (en) | Methods for detection of severe acute respiratory syndrome coronavirus 2 | |
| RU2402612C2 (ru) | Способ скрининга новорожденных на моногенные заболевания и биочип для осуществления этого способа | |
| CN114207146A (zh) | 组合的液相和固相dna扩增 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20050524 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20050725 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20051206 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20051212 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20081216 Year of fee payment: 3 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20091216 Year of fee payment: 4 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20101216 Year of fee payment: 5 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20101216 Year of fee payment: 5 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20111216 Year of fee payment: 6 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20111216 Year of fee payment: 6 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20121216 Year of fee payment: 7 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20131216 Year of fee payment: 8 |
|
| LAPS | Cancellation because of no payment of annual fees |