JP7676366B2 - 治療装置 - Google Patents
治療装置 Download PDFInfo
- Publication number
- JP7676366B2 JP7676366B2 JP2022511741A JP2022511741A JP7676366B2 JP 7676366 B2 JP7676366 B2 JP 7676366B2 JP 2022511741 A JP2022511741 A JP 2022511741A JP 2022511741 A JP2022511741 A JP 2022511741A JP 7676366 B2 JP7676366 B2 JP 7676366B2
- Authority
- JP
- Japan
- Prior art keywords
- shaft
- irradiation
- distal
- tip
- light
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61N—ELECTROTHERAPY; MAGNETOTHERAPY; RADIATION THERAPY; ULTRASOUND THERAPY
- A61N5/00—Radiation therapy
- A61N5/06—Radiation therapy using light
- A61N5/0613—Apparatus adapted for a specific treatment
- A61N5/062—Photodynamic therapy, i.e. excitation of an agent
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61N—ELECTROTHERAPY; MAGNETOTHERAPY; RADIATION THERAPY; ULTRASOUND THERAPY
- A61N5/00—Radiation therapy
- A61N5/06—Radiation therapy using light
- A61N5/0601—Apparatus for use inside the body
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61B—DIAGNOSIS; SURGERY; IDENTIFICATION
- A61B17/00—Surgical instruments, devices or methods
- A61B17/42—Gynaecological or obstetrical instruments or methods
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61N—ELECTROTHERAPY; MAGNETOTHERAPY; RADIATION THERAPY; ULTRASOUND THERAPY
- A61N5/00—Radiation therapy
- A61N5/06—Radiation therapy using light
- A61N5/0601—Apparatus for use inside the body
- A61N5/0603—Apparatus for use inside the body for treatment of body cavities
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61N—ELECTROTHERAPY; MAGNETOTHERAPY; RADIATION THERAPY; ULTRASOUND THERAPY
- A61N5/00—Radiation therapy
- A61N5/06—Radiation therapy using light
- A61N5/0601—Apparatus for use inside the body
- A61N5/0603—Apparatus for use inside the body for treatment of body cavities
- A61N2005/0611—Vagina
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61N—ELECTROTHERAPY; MAGNETOTHERAPY; RADIATION THERAPY; ULTRASOUND THERAPY
- A61N5/00—Radiation therapy
- A61N5/06—Radiation therapy using light
- A61N2005/0626—Monitoring, verifying, controlling systems and methods
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61N—ELECTROTHERAPY; MAGNETOTHERAPY; RADIATION THERAPY; ULTRASOUND THERAPY
- A61N5/00—Radiation therapy
- A61N5/06—Radiation therapy using light
- A61N2005/063—Radiation therapy using light comprising light transmitting means, e.g. optical fibres
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61N—ELECTROTHERAPY; MAGNETOTHERAPY; RADIATION THERAPY; ULTRASOUND THERAPY
- A61N5/00—Radiation therapy
- A61N5/06—Radiation therapy using light
- A61N2005/0632—Constructional aspects of the apparatus
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61N—ELECTROTHERAPY; MAGNETOTHERAPY; RADIATION THERAPY; ULTRASOUND THERAPY
- A61N5/00—Radiation therapy
- A61N5/06—Radiation therapy using light
- A61N2005/0658—Radiation therapy using light characterised by the wavelength of light used
- A61N2005/0659—Radiation therapy using light characterised by the wavelength of light used infrared
Landscapes
- Health & Medical Sciences (AREA)
- Engineering & Computer Science (AREA)
- Biomedical Technology (AREA)
- Life Sciences & Earth Sciences (AREA)
- Public Health (AREA)
- Veterinary Medicine (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Animal Behavior & Ethology (AREA)
- General Health & Medical Sciences (AREA)
- Radiology & Medical Imaging (AREA)
- Pathology (AREA)
- Surgery (AREA)
- Gynecology & Obstetrics (AREA)
- Pregnancy & Childbirth (AREA)
- Reproductive Health (AREA)
- Heart & Thoracic Surgery (AREA)
- Medical Informatics (AREA)
- Molecular Biology (AREA)
- Biophysics (AREA)
- Radiation-Therapy Devices (AREA)
- Surgical Instruments (AREA)
Description
上記目的を達成する本発明に係る治療装置の他の態様は、子宮頸がんの腫瘍細胞に結合した抗体-光感受性物質へ励起光を照射する治療装置であって、先端部および基端部を有する本体シャフトと、前記本体シャフトの先端側に配置され、流体が流入することで拡張可能な拡張部と、前記拡張部から先端側へ突出する先端シャフトと、前記先端シャフトおよび前記拡張部から前記抗体-光感受性物質の励起光を発光可能とする少なくとも1つの照射部と、を有し、前記拡張部の先端側に配置されて前記先端シャフトの基端部を囲む環状の補強部を有することを特徴とする。
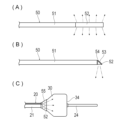
20 シャフト部
21 本体シャフト
22 照射用シャフト
22A 第3突き当て面(突き当て面)
23 流路用シャフト
24 先端シャフト
25 照射ルーメン
26 拡張ルーメン
30 拡張部
34 突き当て面
40 突出部
50 照射部
51 光ファイバ
52 発光部
70 補強部
72 第2突き当て面(突き当て面)
80 光出力装置
90 検出部
C 腫瘍細胞
CC 子宮頸管
I 内子宮口
O 外子宮口
U 子宮頸部
UC 子宮腔
UV 子宮膣部
V 膣
VF 膣円蓋
AV 前膣円蓋
RV 後膣円蓋
Claims (7)
- 子宮頸がんの腫瘍細胞に結合した抗体-光感受性物質へ励起光を照射する治療装置であって、
先端部および基端部を有する本体シャフトと、
前記本体シャフトの先端側に配置され、流体が流入することで拡張可能な拡張部と、
前記拡張部から先端側へ突出する先端シャフトと、
前記先端シャフトおよび前記拡張部から前記抗体-光感受性物質の励起光を発光可能とする少なくとも1つの照射部と、を有し、
前記拡張部の内部および前記先端シャフトの内部を連通し、前記照射部を移動可能に収容する照射ルーメンが形成されていることを特徴とする治療装置。 - 子宮頸がんの腫瘍細胞に結合した抗体-光感受性物質へ励起光を照射する治療装置であって、
先端部および基端部を有する本体シャフトと、
前記本体シャフトの先端側に配置され、流体が流入することで拡張可能な拡張部と、
前記拡張部から先端側へ突出する先端シャフトと、
前記先端シャフトおよび前記拡張部から前記抗体-光感受性物質の励起光を発光可能とする少なくとも1つの照射部と、を有し、
前記拡張部の先端側に配置されて前記先端シャフトの基端部を囲む環状の補強部を有することを特徴とする治療装置。 - 前記先端シャフトは、前記励起光を当該先端シャフトの軸心に対して略垂直方向へ照射し、
前記拡張部は、前記励起光を略先端方向へ照射することを特徴とする請求項1または2に記載の治療装置。 - 前記拡張部は、拡張状態において先端側へ向く突き当て面を有し、前記突き当て面の前記先端シャフトの軸心から離れた部位の一部が、先端側へ突出することを特徴とする請求項1~3のいずれか1項に記載の治療装置。
- 前記拡張部の先端側に配置されて前記先端シャフトの基端部を囲む環状の補強部を有することを特徴とする請求項1に記載の治療装置。
- 前記抗体-光感受性物質が発する蛍光を検出する検出部を有することを特徴とする請求項1~5のいずれか1項に記載の治療装置。
- 前記先端シャフトを摺動可能に収容する管状の内側シャフトと、
前記先端シャフトを含む照射用シャフトと、
前記本体シャフトの基端部が固定された移動操作部と、
前記移動操作部を摺動可能に保持するケーシングと、をさらに有し、
前記内側シャフトは、前記本体シャフトに固定され、
前記拡張部の先端部は、前記内側シャフトに固着され、
前記照射用シャフトは、前記ケーシングに固定され、
前記移動操作部が前記ケーシングに対して移動すると、前記照射用シャフトは移動せずに、前記本体シャフト、前記内側シャフトおよび前記拡張部が、前記ケーシングに対して前記本体シャフトの軸心方向に移動することを特徴とする請求項1~6のいずれか1項に記載の治療装置。
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2020060400 | 2020-03-30 | ||
| JP2020060400 | 2020-03-30 | ||
| PCT/JP2021/009428 WO2021199976A1 (ja) | 2020-03-30 | 2021-03-10 | 治療装置および治療方法 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JPWO2021199976A1 JPWO2021199976A1 (ja) | 2021-10-07 |
| JP7676366B2 true JP7676366B2 (ja) | 2025-05-14 |
Family
ID=77927181
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2022511741A Active JP7676366B2 (ja) | 2020-03-30 | 2021-03-10 | 治療装置 |
Country Status (4)
| Country | Link |
|---|---|
| US (1) | US20230001226A1 (ja) |
| JP (1) | JP7676366B2 (ja) |
| CN (1) | CN115397506A (ja) |
| WO (1) | WO2021199976A1 (ja) |
Families Citing this family (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2023144738A (ja) * | 2022-03-28 | 2023-10-11 | テルモ株式会社 | 膣内挿入デバイス、医療器具及び治療方法 |
| CN116115173A (zh) * | 2022-12-19 | 2023-05-16 | 青岛镭视光电科技有限公司 | 用于治疗宫颈癌的内窥镜探头 |
| CN116251302B (zh) * | 2023-03-11 | 2025-07-25 | 青岛镭视光电科技有限公司 | 治疗宫颈癌前病变的光动力治疗仪探头以及光动力治疗仪 |
| CN119236318A (zh) * | 2024-08-30 | 2025-01-03 | 北京英发光动技术有限公司 | 一种具有散热通道的光照治疗装置 |
Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US5947958A (en) | 1995-09-14 | 1999-09-07 | Conceptus, Inc. | Radiation-transmitting sheath and methods for its use |
| JP2018538077A (ja) | 2015-12-18 | 2018-12-27 | フォトキュア エイエスエイ | 光線力学的治療用装置 |
Family Cites Families (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US6572609B1 (en) * | 1999-07-14 | 2003-06-03 | Cardiofocus, Inc. | Phototherapeutic waveguide apparatus |
| US20030114434A1 (en) * | 1999-08-31 | 2003-06-19 | James Chen | Extended duration light activated cancer therapy |
| JP2009535116A (ja) * | 2006-04-25 | 2009-10-01 | ルーメックス, インク. | 光ワンドおよびバルーンカテーテル |
| WO2015160064A1 (ko) * | 2014-04-18 | 2015-10-22 | 부경대학교산학협력단 | 산광형 광섬유를 포함하는 프로브, 그 제조 방법 및 응용 |
| CN106794248B (zh) * | 2014-08-27 | 2020-01-14 | 富士胶片株式会社 | 光线力学疗法用组合物、杀菌方法、杀菌系统及杀菌系统的工作方法 |
| PT3432983T (pt) * | 2016-03-25 | 2024-06-17 | Inst Nat Sante Rech Med | Sistema para tratamento de uma cavidade do corpo de um paciente por terapia fotodinâmica e método de preparação de tal sistema |
-
2021
- 2021-03-10 JP JP2022511741A patent/JP7676366B2/ja active Active
- 2021-03-10 WO PCT/JP2021/009428 patent/WO2021199976A1/ja not_active Ceased
- 2021-03-10 CN CN202180025347.XA patent/CN115397506A/zh active Pending
-
2022
- 2022-09-13 US US17/943,780 patent/US20230001226A1/en active Pending
Patent Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US5947958A (en) | 1995-09-14 | 1999-09-07 | Conceptus, Inc. | Radiation-transmitting sheath and methods for its use |
| JP2018538077A (ja) | 2015-12-18 | 2018-12-27 | フォトキュア エイエスエイ | 光線力学的治療用装置 |
Also Published As
| Publication number | Publication date |
|---|---|
| US20230001226A1 (en) | 2023-01-05 |
| JPWO2021199976A1 (ja) | 2021-10-07 |
| WO2021199976A1 (ja) | 2021-10-07 |
| CN115397506A (zh) | 2022-11-25 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP7676366B2 (ja) | 治療装置 | |
| US5997571A (en) | Non-occluding phototherapy probe stabilizers | |
| US9113785B2 (en) | Fluid media for bio-sensitive applications | |
| JP3648555B2 (ja) | カラム状環境を照射する改良された光線治療用装置 | |
| EP2361549A2 (en) | System for analysis and treatment of a body lumen | |
| US11874455B2 (en) | Light irradiation device and light irradiation system | |
| US20230021096A1 (en) | Treatment apparatus and treatment method | |
| US20220047885A1 (en) | Light irradiation system, catheter, and light irradiation device | |
| US20220161046A1 (en) | Catheter and light irradiation system | |
| JP7735256B2 (ja) | 治療装置 | |
| US20230008437A1 (en) | Treatment Method and Treatment System | |
| JP7624650B2 (ja) | 光照射デバイス、及び、光照射システム | |
| JPWO2020138138A1 (ja) | 自然口拡張アプリケータ | |
| JP7735131B2 (ja) | 治療装置 | |
| JP7741622B2 (ja) | 光照射デバイス、及び、光照射システム | |
| WO2021066012A1 (ja) | 照射デバイスおよび治療方法 | |
| CN107213554A (zh) | 一种介入用的液态光传导装置 | |
| JP2024017698A (ja) | 医療デバイス、医療システム並びに、診断および治療方法 | |
| WO2023181811A1 (ja) | 医療デバイス | |
| JP2023048292A (ja) | 光照射システム | |
| JP2021166563A (ja) | 光学的治療装置及び光学的治療方法 | |
| JP2023140728A (ja) | 医療デバイス | |
| JP2023140729A (ja) | 医療デバイス | |
| WO2025070413A1 (ja) | 光照射デバイス | |
| HK1161065A (en) | System for analysis and treatment of a body lumen |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20231013 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20240827 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20241028 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20241226 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20250408 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20250430 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 7676366 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |