JP7520002B2 - ヒト血清アルブミンに結合する単一ドメイン抗体 - Google Patents
ヒト血清アルブミンに結合する単一ドメイン抗体 Download PDFInfo
- Publication number
- JP7520002B2 JP7520002B2 JP2021525805A JP2021525805A JP7520002B2 JP 7520002 B2 JP7520002 B2 JP 7520002B2 JP 2021525805 A JP2021525805 A JP 2021525805A JP 2021525805 A JP2021525805 A JP 2021525805A JP 7520002 B2 JP7520002 B2 JP 7520002B2
- Authority
- JP
- Japan
- Prior art keywords
- domain
- protein
- heavy chain
- antibody
- single variable
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies
- C07K16/18—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies
- C07K16/18—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans
- C07K16/28—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants
- C07K16/2878—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants against the NGF-receptor/TNF-receptor superfamily, e.g. CD27, CD30, CD40, CD95
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K2039/505—Medicinal preparations containing antigens or antibodies comprising antibodies
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/50—Immunoglobulins specific features characterized by immunoglobulin fragments
- C07K2317/51—Complete heavy chain or Fd fragment, i.e. VH + CH1
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/50—Immunoglobulins specific features characterized by immunoglobulin fragments
- C07K2317/56—Immunoglobulins specific features characterized by immunoglobulin fragments variable (Fv) region, i.e. VH and/or VL
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/50—Immunoglobulins specific features characterized by immunoglobulin fragments
- C07K2317/56—Immunoglobulins specific features characterized by immunoglobulin fragments variable (Fv) region, i.e. VH and/or VL
- C07K2317/565—Complementarity determining region [CDR]
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/50—Immunoglobulins specific features characterized by immunoglobulin fragments
- C07K2317/56—Immunoglobulins specific features characterized by immunoglobulin fragments variable (Fv) region, i.e. VH and/or VL
- C07K2317/569—Single domain, e.g. dAb, sdAb, VHH, VNAR or nanobody®
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/90—Immunoglobulins specific features characterized by (pharmaco)kinetic aspects or by stability of the immunoglobulin
- C07K2317/94—Stability, e.g. half-life, pH, temperature or enzyme-resistance
Landscapes
- Chemical & Material Sciences (AREA)
- Health & Medical Sciences (AREA)
- Organic Chemistry (AREA)
- Immunology (AREA)
- Medicinal Chemistry (AREA)
- Biophysics (AREA)
- General Health & Medical Sciences (AREA)
- Genetics & Genomics (AREA)
- Biochemistry (AREA)
- Molecular Biology (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Life Sciences & Earth Sciences (AREA)
- Peptides Or Proteins (AREA)
- Micro-Organisms Or Cultivation Processes Thereof (AREA)
- Medicinal Preparation (AREA)
- Medicines Containing Antibodies Or Antigens For Use As Internal Diagnostic Agents (AREA)
Description
MKWVTFISLL FLFSSAYSRG VFRRDAHKSE VAHRFKDLGE ENFKALVLIA FAQYLQQCPF EDHVKLVNEV TEFAKTCVAD ESAENCDKSL HTLFGDKLCT VATLRETYGE MADCCAKQEP ERNECFLQHK DDNPNLPRLV RPEVDVMCTA FHDNEETFLK KYLYEIARRH PYFYAPELLF FAKRYKAAFT ECCQAADKAA CLLPKLDELR DEGKASSAKQ GLKCASLQKF GERAFKAWAV ARLSQRFPKA EFAEVSKLVT DLTKVHTECC HGDLLECADD RADLAKYICE NQDSISSKLK ECCEKPLLEK SHCIAEVEND EMPADLPSLA ADFVGSKDVC KNYAEAKDVF LGMFLYEYAR RHPDYSVVLL LRLAKTYETT LEKCCAAADP HECYAKVFDE FKPLVEEPQN LIKQNCELFE QLGEYKFQNA LLVRYTKKVP QVSTPTLVEV SRNLGKVGSK CCKHPEAKRM PCAEDCLSVF LNQLCVLHEK TPVSDRVTKC CTESLVNGRP CFSALEVDET YVPKEFNAET FTFHADICTL SEKERQIKKQ TALVELVKHK PKATKEQLKA VMDDFAAFVE KCCKADDKET CFAEEGKKLV AASQAALGL
CDR1:HYAMH(配列番号2)
CDR2:GISWNGNKITYADSVKG(配列番号3)
CDR3:DSSLFIVGAPTFEH(配列番号4)
a)配列番号2又は配列番号2と1、2、3、4若しくは5個の差を有するアミノ酸配列を有するCDR1
b)配列番号3又は配列番号3と1、2、3、4、5、7、8、9、10、11、12、13、14、15、16若しくは17個の差を有するアミノ酸配列を有するCDR2、及び/又は
c)配列番号4又は配列番号4と1、2、3、4、5、6、7、8、9、10、11、12、13若しくは14個の差を有するアミノ酸配列を有するCDR3を含む。
E111→D;
R115→Q;
S100→H又はV;
V97→A;
K98→R;
13Q→H又はK;
16R→G;
19R→K;
23A→T;
24A→V;
H30→N又はD;
H31→E又はD;
G55→S;
G56→N;
K57→S、T、V、又はR;
T59→A、D、又はG;
K65R;
A89→V又はP及び/又は
I104→L。
・ ヒトにおいて1から72時間、例えば、2、4、6、8、若しくは10時間、例えば、10時間以上、例えば、10、11、12、14、14、15、16、17、18、19、20時間、例えば、約18時間、例えば、最高20時間、又は12、24、36、若しくは48時間の半減期(t1/2として表現される)を有し、及び/又は
・ 治療部分に連結した場合、得られる融合タンパク質に、ヒトにおいて1から72時間、例えば、10時間以上、例えば、2、4、6、8、若しくは10時間、例えば、10、11、12、14、14、15、16、17、18、19、20時間、例えば、約18時間、又は最高20時間、又は12、24、36、若しくは48時間の血清半減期を付与する。
GGCTTTGTGA GCGGATACAA TTATAATATG TGGAATTGTG AGCGCTCACA ATTCCACAAC GGTTTCCCTC TAGAAATAAT TTTGTTTAAC TTTTAGGAGG TAAAACATAT GAAGAAAACG GCAATCGCAA TCGCAGTCGC TCTGGCGGGT TTCGCAACTG TAGCGCAAGC CGAGGTGCAA CTGGTCGAGT CTGGTGGTGG TTTGGTGCAA CCTGGTAGAA GCTTGCGTTT GAGTTGTGCC GCTTCCGGCT TCACTTTCCA TCATTATGCT ATGCACTGGG TTCGTCAAGC TCCCGGAAAA GGTTTGGAGT GGGTTTCCGG AATTTCCTGG AATGGCAATA AGATTACGTA CGCTGATTCA GTGAAAGGAA GGTTTACAAT CAGTAGAGAT AATGCTAAAA ACTCATTGTA TCTACAAATG AACAGCCTAA GAGCAGAAGA TACCGCTCTG TACTACTGTG TTAGAGATAG CTCGTTATTC ATTGTAGGTG CACCAACTTT TGAACATTGG GGTCGGGGTA CTCTTGTGAC TGTCTCATCC GCGGCCGCAC ACCACCATCA TCACCACTAA CTCGAGCGCC TAATGAAAGC TTCCCCAAGG GCGACACCCC CTAATTAGCC CGGGCGAAAG GCCCAGTCTT TCGACTGAGC CTTTCGTTTT ATTTGATGCC TGGCAGTTCC CTACTCTCGC ATGGGGAGTC CCCACACTAC CATCGGCGCT ACGGCGTTTC ACTTCTGAGT TCGGCATGGA (配列番号16)
a)トランジェニック齧歯類、例えば、マウスをHSA抗原で免疫する工程であり、前記齧歯類が再配置されていないヒト重鎖V遺伝子を含む核酸構築物を発現しており、機能的な内在性軽若しくは重鎖を形成することができない工程と、
b)ヒト重鎖のみ抗体を単離する工程と、を含む方法も開示している。
a)トランジェニック齧歯類、例えば、マウスをHSA抗原で免疫する工程であり、前記齧歯類が再配置されていないヒト重鎖V遺伝子を含む核酸構築物を発現しており、機能的な内在性軽若しくは重鎖を形成することができない工程と、
b)前記齧歯類、例えば、マウスからVHドメイン配列を含む配列のライブラリーを作製する工程と、
c)前記ライブラリーからVHドメイン配列を含む配列を単離する工程と、を含む方法も開示している。
a)アミノ酸配列をコードする核酸配列のセット、収集物又はライブラリーを提供する工程と、
b)前記セット、収集物又はライブラリーを、HSAに結合する/親和性を有することができるアミノ酸配列についてスクリーニングする工程と、
c)HSAに結合する/親和性を有することができるアミノ酸配列を単離する工程と、を含むことができる。
Tg/TKOマウスの構築
内在性重及び軽鎖抗体の発現が抑制されているバックグラウンド内で生殖細胞系の構成の重鎖抗体トランスジェニック遺伝子座を有するマウス(三重ノックアウト、又はTKO)は以前に記載されたように作出された(国際公開第2004/076618号パンフレット及び国際公開第2003/000737号パンフレット、Renら、Genomics, 84, 686, 2004; Zouら、J. Immunol., 170, 1354, 2003)。簡単に説明すると、トランスジェニックマウスは、国際公開第2016/062990号パンフレットに記載されたようにCH1ドメインが欠如したマウス免疫グロブリン定常領域遺伝子、マウスエンハンサー及び調節領域と組み合わせて、過剰なヒトVH、D及びJ遺伝子を含む、酵母人工染色体(YAC)を用いた新鮮な受精卵母細胞の前核マイクロインジェクションの後に得られた。酵母人工染色体(YAC)は、酵母における非常に大きなDNA挿入物のクローニングのために採用することができるベクターである。天然の酵母染色体のように振る舞うために不可欠な3つのシス作用構造要素(自己複製配列(ARS)、セントロメア(CEN)、及び2つのテロメア(TEL))を全て含むだけでなく、大きなDNA挿入物を受け入れる能力によって、染色体のような安定性及び酵母細胞における伝達の忠実性に必要な最小サイズ(150kb)に達することができる。YACの構造及び使用は当技術分野ではよく知られている(例えば、Bruschi, C.V.及びGjuracic, K. Yeast Artificial Chromosomes, ENCYCLOPEDIA OF LIFE SCIENCES 2002 Macmillan Publishers Ltd, Nature Publishing Group / www.els.net)。
免疫用の抗原
免疫は、組換え精製タンパク質を使用した。組換えヒトHSAタンパク質は、Sigma社(カタログ番号A9731)から購入した。
免疫手順
8~12週齢の3匹のCrescendoマウスはそれぞれ、完全フロイントアジュバントで乳化して皮下に送達したHSA10μgで初回免疫を受け、その後、不完全フロイントアジュバントで乳化してまた皮下に投与したHSA10μgで、初回刺激に続いて週間隔で3回追加免疫を受けた。HSAの最終用量は、アジュバントの非存在下でリン酸緩衝生理食塩水に溶かして腹腔内投与した。初回免疫の28日後にマウスを致死処置し、上腕及び鼠径リンパ節、並びに脾臓をRNAlater(Qiagen社 カタログ番号76104)中に回収した。血清は、応答を試験するために収集し、保存した。
血清ELISA
Nunc社マキシソーププレートは、5μg/ml HSAのPBS溶液で4℃で一晩コーティングした。その後、プレートを0.05% Tween20を補給したPBSで洗浄し、続いてtween を添加していないPBSで洗浄し、3%脱脂粉乳(Marvel社)のPBS溶液で室温で少なくとも1時間ブロックした。3% Marvel/PBSに溶かした血清の希釈液をポリプロピレンチューブ又はプレートで調製し、室温で少なくとも1時間インキュベートしてから、ブロックされたELISAプレートに移し、そこで更に少なくとも1時間インキュベーションを行った。PBS/Tween及びPBSで洗浄後、PBS/3% Marvelで1:10000希釈に調製した、ビオチンをコンジュゲートしたヤギ抗マウスIgG、Fcガンマサブクラス1特異的抗体(Jackson社、115-065-205)の溶液を次に添加し、プレートを室温で少なくとも1時間インキュベートし、次いでPBS/Tween及びPBSで洗浄した。3% Marvel/PBSで1:1000に希釈したニュートラアビジン-HRP溶液(Pierce社31030)をELISAプレートに添加し、少なくとも30分間インキュベートした。更に洗浄した後、TMB基質(Sigma社カタログ番号T0440)を使用してELISAを発色させ、10分後にH2SO4 0.5M溶液の添加によって反応を停止させた。吸光度は、450nmで読み取ることにより判定した。陽性応答は、全マウスで認められた。
免疫マウスからのライブラリー作製
a.組織の処理、RNA抽出及びcDNA製造
脾臓、鼠径及び上腕リンパ節は、免疫した各動物からRNAlaterに収集した。各動物について、脾臓の1/3及び4つのリンパ節を別々に処理した。最初に、組織をホモジナイズし、組織を溶解マトリックスDビーズチューブ(MP Bio社カタログ番号116913100)に移した後、β-メルカプトエタノールを含有するRLT緩衝液(Qiagen RNeasyキット カタログ番号74104)600μlを添加してから、MP Bio Fastprepホモジナイザー(カタログ番号116004500)で、6m/s 40秒のサイクルを使用してホモジナイズした。ホモジナイズした組織を含有するチューブを氷に移し、10gで5分間微量遠心することによって残渣をペレットにした。上清400μlを取り出し、RT-PCRのために使用した。
ファージミドベクター、pUCG3をこれらの研究で使用した。示したように、NcoIやXhoIを用いた制限酵素消化、ライゲーション及び形質転換等の当技術分野で広く使用されている従来の方法を使用して、VHをpUCG3にクローニングすることができる。本明細書では、以下に説明したように、VHファージミドライブラリーを構築するために、PCRをベースにした代替方法を使用した。
HSA結合VHの単離のための選択戦略
ライブラリーファージストックの調製及びファージディスプレイ選択は、公開された方法(Antibody Engineering, Benny Lo編、第8章、161~176頁、2004)に従って実施した。ほとんどの場合、結合VHドメインを単離するために、パニングアプローチと組み合わせたファージディスプレイを使用した。しかし、様々な異なる選択方法が当技術分野ではよく記載されており、可溶性選択、ストレス下(例えば、熱)で実施される選択、及び過剰な抗原又は抗原反応性VHドメインを競合として添加し、高親和性VHドメインの回収を促すか、又は特定のエピトープから選択を遠ざける競合選択が含まれる。HSAで免疫したマウスからのライブラリーについては、HSAに対するパニング選択又は可溶性選択のいずれかを1回実施した。
標的結合のアッセイ
様々な選択によるVHは、以下のアッセイの1つ又は複数でスクリーニングしてHSAに結合するVHを特定した。
ライブラリーの選択後、細菌宿主が発現したVHドメインの粗抽出物を使用したELISAによって、HSA特異的VH抗体を特定した。小規模な細菌のペリプラズム抽出物は、ディープウェルプレートで増殖させた培養物1mlから調製した。開始培養物を使用して、0.1%(w/v)グルコース+アンピシリン100μg/mlを補給した2XTYブロス(Melford社、M2130)を含有する96ウェルディープウェルプレート(Fisher社、カタログ番号MPA-600-030X)に接種し、37℃にて250rpmで振とうした。OD600が0.6~1に達した時、IPTG(最終濃度1mM)及びアンピシリンを補給した2XTY 100μlを添加することによってVH生成を誘導し、培養物は250rpmで振とうしながら30℃で一晩増殖させた。大腸菌を3200rpmで10分間遠心分離することによってペレットにし、上清を廃棄した。細胞ペレットを氷冷抽出緩衝液(20%(w/v)スクロース、EDTA 1mM、50mMトリス-HCl pH8.0)150μlにゆっくりピペッティングすることによって再懸濁した。細胞を氷上で30分間インキュベートした後、4℃で4500rpmで15分間遠心分離した。上清をポリプロピレンプレートに移し、1×PBSTブロッキング液でインキュベーションした後、直接ELISAに使用した。
精製したVHは、ペリプラズム抽出液のニッケル-アガロースアフィニティークロマトグラフィー精製のためにVHC末端6×HISタグを使用することによって得られた。各VHの開始培養物は、2%(w/v)グルコース及びアンピシリン100μg/mlを補給した2XTY培地(2XTYブロス)(Melford社、カタログ番号M2103)中で、250rpmで振とうしながら30℃で一晩増殖させた。次に、この一晩培養したものを使用して2XTY培地50ml~200mlに接種し、250rpmで振とうしながら37℃で約6~8時間(OD600=0.6~1.0になるまで)インキュベートした。培養物を3200rpmで10分間遠心分離し、細胞ペレットをアンピシリン100μg/ml/IPTG 1mMを含有する新しい2XTYブロスに再懸濁した。振とうフラスコは、30℃で250rpmで一晩インキュベートした。培養物を再び3200rpmで10分間遠心分離し、上清を廃棄した。細胞ペレットを氷冷抽出緩衝液(20%(w/v)スクロース、EDTA 1mM、50mM トリス-HCl pH8.0又はMOPS 50mM)にゆっくりピペッティングすることによって再懸濁し、その後1:5に希釈した氷冷抽出緩衝液で更に希釈した。細胞を氷上で30分間インキュベートした後、4℃で4500rpmで15分間遠心分離した。上清を、イミダゾール(Sigma社、カタログ番号12399)10mM及び予め平衡化したニッケルアガロースビーズ(Qiagen社、Ni-NTA50%溶液、カタログ番号30210)を含有するチューブに移した。VH結合は4℃で2時間、ゆっくり振とうして進行させた。ビーズをポリプレップカラム(BioRad社カタログ番号731-1550)に移し、重力流を利用して上清を廃棄した。カラムをPBS/0.05% Tween(登録商標)で3回洗浄した後、PBS/イミダゾール20mM 5mlで3回洗浄した。VHは、PBS/イミダゾール250mMを使用してカラムから溶出させた。イミダゾールは、NAP-5カラム(GE Healthcare社、17-0853-01)で緩衝液交換し、PBSで溶出することによって、精製したVH調製物から除去した。精製したVHの収率は分光光度法で推定し、純度はSDS PAGEを使用して評価した。
ヒト、イヌ、及びマウス血清アルブミンとの結合研究は、ForteBio社 OCTET RED384装置を使用して実施した。血清アルブミン(HSA、CSA、MSA)は、アミン試薬カップリングキット(第2世代、ForteBio社)を使用したアミンカップリングによって、AR2Gバイオセンサーに結合させた。簡単に説明すると、AR2Gバイオセンサーを水で再水和した後、EDC/sNHS試薬を使用して10分間活性化した。活性化したバイオセンサーを、10mM酢酸ナトリウムpH5.0で10μg/mlに希釈した血清アルブミン(HSA、CSA、MSA)を含有するウェルに10分間浸漬した後、1MエタノールアミンpH8.5を使用して10分間遊離活性部位を不活性化した。次に、これらを10mMグリシンpH2.5に浸漬して表面を安定化した。その後、HSA及びCSAを付加したバイオセンサーを、1×アッセイ緩衝液(PBS/Tween-20 0.05%)に120秒間浸漬してベースラインを確立した後、血清アルブミンへの結合を起こさせる実験のために、所定の濃度のHumabody(登録商標)VHを含有するウェル(7点2倍希釈系列、最高濃度は50nM(HSAの場合)又は1500nM(MSA、CSA)に120秒かけて浸漬した。その後、バイオセンサーをアッセイ緩衝液を含有するウェルに移し、300秒かけてHumabody(登録商標)VHを血清アルブミンから解離させた。結合相互作用の動態及び親和性は、1:1結合モデルを使用してモデル化し、ForteBio解析ソフトウェアバージョン8.1以上を使用して算出した。異常な、又は適合しない曲線は解析から除外した。
VH単一ドメイン抗体は良好な安定性を示す
精製したVHをサイズ排除クロマトグラフィーに供した。簡単に説明すると、精製したVHを2mg/mlでPBS緩衝液に溶かし、4℃又は40℃で0~14日間保存した後、PDA検出器(280nmで検出)を備えたWaters H-Class Bio UPLCを使用して様々な時点で分析し、Waters ACQUITY BEH 125Å SECカラムで分離した。試料を10μlの体積で注入し、NaCl 200mM、100mMリン酸ナトリウムpH7.4+5%プロパン-1-オールを含有する移動相で、0.4ml/分の流速で流した。6分間データを収集し、保存後の試料中の単量体タンパク質のパーセンテージを算出した。
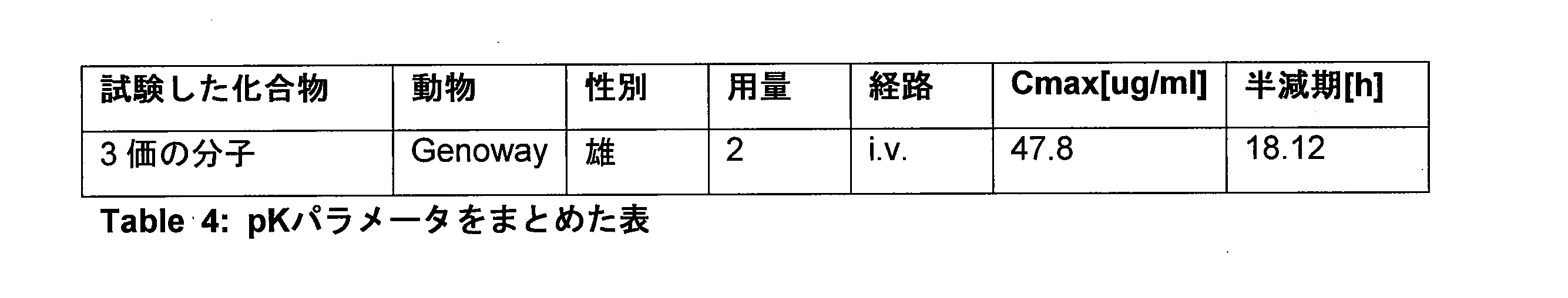
2重トランスジェニックヒト化FcRn/HSAマウスにおける半減期延長分子の単回静脈内投与の薬物動態分析
genOway(登録商標)によるヒト新生児Fc受容体/ヒトアルブミンマウスモデルを使用して実験を実行した。この2重ヒト化新生児Fc受容体(FcRn)/アルブミンマウスモデルは、自己由来受容体-リガンド相互作用を維持しており、ヒトにおける生理的薬物クリアランスを模倣しているため、アルブミンに連結した低分子及び従来の薬物動態を測定し最適化するので、並びに循環する生物製剤及びバイオシミラー薬物の半減期を研究し予測するための、独特で信頼性の高い手段となっている(Viuff D, Antunes F, Evans L, Cameron J, Dyrnesli H, Thue Ravn B, Stougaard M, Thiam K, Andersen B, Kjarulff S, Howard KA. 2016. 「Generation of a double transgenic humanized neonatal Fc receptor (FcRn)/albumin mouse to study the pharmacokinetics of albumin-linked drugs.」 J Control Release)。
Humabody(登録商標)1の結合部位の決定
ForteBio OCTET RED384装置を使用して、Humabody(登録商標)1VHとHSAドメインI、II、及びIIIとの間の相互作用を調べた。HSAドメインは、Albumin Bioscience社から購入した。簡単に説明すると、AR2Gバイオセンサーを水で再水和した後、EDC/sNHS試薬を使用して10分間活性化した。活性化したバイオセンサーを、10mM酢酸ナトリウムpH5.0で50μg/mlに希釈したHSAドメインを含有するウェルに5分間浸漬した後、1MエタノールアミンpH8.5を使用して遊離活性部位を10分かけて不活性化した。次に、これらを10mMグリシンpH2.5に浸漬して表面を安定化させた。その後、バイオセンサーに付加したドメインHSAを、1×アッセイ緩衝液(PBS/Tween-20 0.05%)に120秒間浸漬してベースラインを確立した後、HSAへの結合を起こさせるために300nMの所定濃度のHumabody(登録商標)1VHを含有するウェルに120秒かけて浸漬した。その後、バイオセンサーをアッセイ緩衝液を含有するウェルに移し、300秒かけてHumabody(登録商標)VHをHSAドメインから解離させた。
配列番号17
タンパク質
EVQLVESGGGVVQPGRSLRLSCAASGFSFSGYGMHWVRQAPGKGLEWVAYISYDGSNKYYADSVKGRFTISRDNSKNTLYLQMNSLRAEDTAVYYCAKDPAWGLRLGESSSYDFDIWGQGTMVTVSSGGGGSGGGGSGGGGSGGGGSGGGGSGGGGSEVQLVESGGGLVQPGGSLRLSCAASGFTLSNYWMNWVRQAPGKGLEWVANINQDGSERYYVDSVKGRFTISRDNAKNSLYLQMNSLRAEDTAVYYCARGGEGYGVDHYGLDVSGQGTTVTVSSGGGGSGGGGSGGGGSGGGGSGGGGSGGGGSEVQLVESGGGLVQPGRSLRLSCAASGFTFHHYAMHWVRQAPGKGLEWVSGISWNGNKITYADSVKGRFTISRDNAKNSLYLQMNSLRAEDTALYYCVRDSSLFIVGAPTFEHWGRGTLVTVSSGGGGSGGGGSGGGGSGGGGS
配列番号18のタンパク質をコードする核酸
GAGGTGCAGCTGGTGGAGTCTGGGGGAGGCGTGGTCCAGCCTGGGAGGTCCCTGAGACTCTCCTGTGCAGCCTCTGGATTCTCCTTCAGTGGCTATGGCATGCACTGGGTCCGCCAGGCTCCAGGCAAGGGACTGGAGTGGGTGGCATATATATCATATGATGGAAGTAATAAATACTATGCAGACTCCGTGAAGGGCCGATTCACCATCTCCAGAGACAATTCCAAGAACACGCTGTATCTGCAAATGAACAGCCTGAGAGCTGAGGACACGGCTGTGTATTACTGTGCGAAAGATCCGGCCTGGGGATTACGTTTGGGGGAGTCATCGTCCTATGATTTTGATATCTGGGGCCAAGGGACAATGGTCACCGTCTCCTCAGGTGGTGGCGGTTCAGGCGGAGGTGGCTCTGGAGGTGGAGGTTCAGGAGGTGGTGGTTCTGGCGGCGGTGGATCGGGTGGAGGTGGTAGTGAGGTGCAGTTAGTTGAGAGCGGAGGTGGTTTAGTTCAGCCGGGGGGCTCGCTTCGCCTGTCGTGCGCCGCCTCGGGATTCACATTATCAAACTACTGGATGAATTGGGTCCGCCAGGCTCCGGGCAAAGGTCTTGAGTGGGTGGCGAACATTAATCAGGACGGGAGCGAGCGTTATTACGTTGATTCGGTAAAAGGACGTTTCACTATCAGTCGTGACAACGCTAAAAATTCCTTGTACTTACAGATGAACTCACTTCGTGCTGAGGACACCGCAGTGTACTACTGTGCTCGCGGTGGTGAAGGATACGGCGTCGATCACTACGGCCTTGATGTATCAGGACAGGGGACTACAGTTACCGTCTCTTCCGGCGGAGGTGGCTCTGGAGGAGGCGGATCGGGGGGTGGAGGAAGTGGCGGCGGTGGTAGTGGAGGAGGTGGTTCTGGAGGCGGTGGCTCTGAAGTACAACTGGTTGAATCGGGTGGTGGATTGGTCCAACCTGGAAGATCATTGAGGCTTTCTTGTGCAGCTTCCGGATTCACCTTTCATCACTATGCTATGCACTGGGTGAGACAAGCCCCTGGTAAGGGCTTGGAATGGGTGTCCGGAATCTCCTGGAATGGTAACAAAATAACATATGCAGATTCCGTTAAGGGTAGATTTACTATTAGCCGTGATAATGCAAAAAACAGTTTATACTTGCAGATGAATTCCTTGAGGGCTGAGGATACAGCTCTTTACTATTGTGTGCGTGACTCATCGTTGTTCATTGTCGGAGCCCCAACTTTCGAACATTGGGGTAGAGGTACCCTAGTTACGGTTAGCTCAGGCGGAGGTGGCTCTGGAGGAGGCGGATCGGGGGGTGGAGGAAGTGGCGGCGGTGGTAGT
配列番号19
QVQLVESGGGLVHPGGSLKLSCAVSGFTFHHYAMHWVRQAPGKGLEWVSGISWNGNKITYADSVKGRFTISRDNAKNSLYLQMNSLRAEDTALYYCVRDSSLFIVGAPTFDHWGQGTLVTVSS
配列番号20
QVQLVESGGGLVHPGGSLKLSCAVSGFTFHHYAMHWVRQAPGKGLEWVSGISWNGNKITYADSVKGRFTISRDNAKNSLYLQMNSLRAEDTALYYCVRDSSLFIVGAPTFDHWGQGTLVTVSS
Claims (22)
- a)配列番号2を含むCDR1
b)配列番号3を含むCDR2、及び
c)配列番号4を含むCDR3を含む、
ヒト血清アルブミン(HSA)に結合する免疫グロブリンヒト単一可変重鎖ドメイン。 - 配列番号1を含む、請求項1に記載の免疫グロブリンヒト単一可変重鎖ドメイン。
- 請求項1又は2に記載の免疫グロブリンヒト単一可変重鎖ドメイン及び異なる標的に結合する少なくとも1つの第2の部分を含むタンパク質又は構築物。
- 治療部分を含む、請求項3に記載のタンパク質又は構築物。
- 前記治療部分が抗体又はその断片である、請求項4に記載のタンパク質又は構築物。
- 前記断片が、scFv、Fv、重鎖、又は単一ドメイン抗体である、請求項5に記載のタンパク質又は構築物。
- 前記単一ドメイン抗体が、単一可変重鎖ドメイン抗体である、請求項6に記載のタンパク質又は構築物。
- 前記免疫グロブリンヒト単一可変重鎖ドメインが、ペプチドリンカーによって治療部分に連結している、請求項3から7のいずれか一項に記載のタンパク質又は構築物。
- 前記ペプチドリンカーが(G4S)nであり、nが1から15である、請求項8に記載のタンパク質又は構築物。
- 前記免疫グロブリンヒト単一可変重鎖ドメインが前記タンパク質のN又はC末端に位置している、請求項3から9のいずれか一項に記載のタンパク質又は構築物。
- 前記免疫グロブリンヒト単一可変重鎖ドメインが前記タンパク質のC末端に位置しており、1から50個のアミノ酸のC末端伸長を含む、請求項10に記載のタンパク質又は構築物。
- タンパク質を請求項1又は2に記載の免疫グロブリンヒト単一可変重鎖ドメインに結合することを含む、タンパク質の半減期を延長する方法。
- 治療部分の半減期の延長における請求項1又は2に記載の免疫グロブリンヒト単一可変重鎖ドメインの使用であって、前記免疫グロブリンヒト単一可変重鎖ドメインが融合タンパク質において治療部分に連結している、使用。
- 請求項1若しくは2に記載の免疫グロブリンヒト単一可変重鎖ドメイン又は請求項3から11のいずれか一項に記載のタンパク質若しくは構築物を含む、医薬組成物。
- 請求項1又は2に記載の免疫グロブリンヒト単一可変重鎖ドメインをコードする核酸。
- 配列番号16を含む請求項15に記載の核酸。
- リンカーによって第2の核酸に連結している、請求項15又は16に記載の核酸。
- 前記第2の核酸が治療部分をコードしている、請求項17に記載の核酸。
- 前記リンカーが核酸リンカーである、請求項17又は18に記載の核酸。
- 請求項15から19のいずれか一項に記載の核酸を含むベクター。
- 請求項15から19のいずれか一項に記載の核酸又は請求項20に記載のベクターを含む宿主細胞。
- 請求項1又は2に記載の免疫グロブリンヒト単一可変重鎖ドメイン又は請求項3から11のいずれか一項に記載のタンパク質若しくは構築物又は請求項14に記載の医薬組成物を含むキット。
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| GBGB1818460.6A GB201818460D0 (en) | 2018-11-13 | 2018-11-13 | Single domain antibodies that bind human serum albumin |
| GB1818460.6 | 2018-11-13 | ||
| PCT/GB2019/053220 WO2020099871A1 (en) | 2018-11-13 | 2019-11-13 | Single domain antibodies that bind human serum albumin |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2022507307A JP2022507307A (ja) | 2022-01-18 |
| JP7520002B2 true JP7520002B2 (ja) | 2024-07-22 |
Family
ID=64739541
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2021525805A Active JP7520002B2 (ja) | 2018-11-13 | 2019-11-13 | ヒト血清アルブミンに結合する単一ドメイン抗体 |
Country Status (11)
| Country | Link |
|---|---|
| US (1) | US20210340233A1 (ja) |
| EP (1) | EP3880703A1 (ja) |
| JP (1) | JP7520002B2 (ja) |
| KR (1) | KR20210091254A (ja) |
| CN (1) | CN113412278B (ja) |
| AU (1) | AU2019378154A1 (ja) |
| CA (1) | CA3118640A1 (ja) |
| GB (1) | GB201818460D0 (ja) |
| IL (1) | IL282641A (ja) |
| SG (1) | SG11202103741RA (ja) |
| WO (1) | WO2020099871A1 (ja) |
Families Citing this family (11)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP3565842A1 (en) | 2017-01-06 | 2019-11-13 | Crescendo Biologics Limited | Single domain antibodies to programmed cell death (pd-1) |
| CN118955716A (zh) | 2017-11-13 | 2024-11-15 | 克雷森多生物制剂有限公司 | 结合cd137的单结构域抗体 |
| GB201802573D0 (en) | 2018-02-16 | 2018-04-04 | Crescendo Biologics Ltd | Therapeutic molecules that bind to LAG3 |
| CN109942704B (zh) * | 2019-04-12 | 2023-01-20 | 深圳普瑞金生物药业股份有限公司 | Hsa单域抗体、核酸及试剂盒 |
| CN117043184A (zh) * | 2021-04-01 | 2023-11-10 | 南京再明医药有限公司 | 抗人血清白蛋白(hsa)的纳米抗体及其应用 |
| TW202313685A (zh) * | 2021-06-07 | 2023-04-01 | 大陸商上海濟煜醫藥科技有限公司 | 抗人血清白蛋白的抗原結合蛋白 |
| GB202205589D0 (en) | 2022-04-14 | 2022-06-01 | Crescendo Biologics Ltd | Mesothelin binders |
| CN117088975B (zh) * | 2022-05-11 | 2024-06-25 | 东莞市朋志生物科技有限公司 | 抗白蛋白抗体、检测白蛋白的试剂和试剂盒 |
| AU2024221136A1 (en) | 2023-02-17 | 2025-10-02 | Ablynx N.V. | Polypeptides binding to the neonatal fc receptor |
| CN120025433A (zh) * | 2024-01-22 | 2025-05-23 | 寻济生物科技(北京)有限公司 | 一种抗白蛋白抗体或其抗原结合片段及其应用 |
| CN118685413B (zh) * | 2024-08-28 | 2025-02-07 | 杭州嘉因生物科技有限公司 | 下调内源性smn的诱导型稳定细胞株的构建及其应用 |
Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2010518062A (ja) | 2007-02-08 | 2010-05-27 | ドマンティス リミテッド | 血清アルブミンに対する抗体単一可変ドメイン |
| WO2017122018A1 (en) | 2016-01-12 | 2017-07-20 | Crescendo Biologics Limited | Molecules that bind prostate specific membrane antigen (psma) |
Family Cites Families (14)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| GB0115256D0 (en) | 2001-06-21 | 2001-08-15 | Babraham Inst | Mouse light chain locus |
| US20060073141A1 (en) * | 2001-06-28 | 2006-04-06 | Domantis Limited | Compositions and methods for treating inflammatory disorders |
| US20050271663A1 (en) * | 2001-06-28 | 2005-12-08 | Domantis Limited | Compositions and methods for treating inflammatory disorders |
| GB2398784B (en) | 2003-02-26 | 2005-07-27 | Babraham Inst | Removal and modification of the immunoglobulin constant region gene cluster of a non-human mammal |
| LT2949668T (lt) * | 2005-05-18 | 2019-11-11 | Ablynx Nv | Pagerinti nanokūnai tm prieš navikų nekrozės faktorių alfa |
| AU2007328900A1 (en) * | 2006-12-05 | 2008-06-12 | Ablynx N.V. | Peptides capable of binding to serum proteins |
| WO2012022703A2 (en) * | 2010-08-20 | 2012-02-23 | Glaxo Group Limited | Improved anti-serum albumin binding variants |
| AU2012273928A1 (en) * | 2011-06-23 | 2014-02-06 | Ablynx Nv | Immunoglobulin single variable domains directed against IgE |
| MX2014001883A (es) * | 2011-08-17 | 2014-05-27 | Glaxo Group Ltd | Proteinas y peptidos modificados. |
| WO2014111550A1 (en) * | 2013-01-17 | 2014-07-24 | Glaxosmithkline Intellectual Property Development Limited | Modified anti-serum albumin binding proteins |
| KR20170073647A (ko) | 2014-10-22 | 2017-06-28 | 크레센도 바이오로직스 리미티드 | 형질전환 마우스 |
| GB201500464D0 (en) * | 2015-01-12 | 2015-02-25 | Crescendo Biolog Ltd | Method of producing optimised therapeutic molecules |
| KR102530742B1 (ko) * | 2016-05-20 | 2023-05-09 | 하푼 테라퓨틱스, 인크. | 단일 도메인 혈청 알부민 결합 단백질 |
| WO2018224439A1 (en) * | 2017-06-05 | 2018-12-13 | Numab Innovation Ag | Novel anti-hsa antibodies |
-
2018
- 2018-11-13 GB GBGB1818460.6A patent/GB201818460D0/en not_active Ceased
-
2019
- 2019-11-13 KR KR1020217017911A patent/KR20210091254A/ko not_active Ceased
- 2019-11-13 CA CA3118640A patent/CA3118640A1/en active Pending
- 2019-11-13 JP JP2021525805A patent/JP7520002B2/ja active Active
- 2019-11-13 CN CN201980088164.5A patent/CN113412278B/zh active Active
- 2019-11-13 WO PCT/GB2019/053220 patent/WO2020099871A1/en not_active Ceased
- 2019-11-13 SG SG11202103741RA patent/SG11202103741RA/en unknown
- 2019-11-13 US US17/292,592 patent/US20210340233A1/en not_active Abandoned
- 2019-11-13 EP EP19809554.9A patent/EP3880703A1/en not_active Withdrawn
- 2019-11-13 AU AU2019378154A patent/AU2019378154A1/en active Pending
-
2021
- 2021-04-26 IL IL282641A patent/IL282641A/en unknown
Patent Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2010518062A (ja) | 2007-02-08 | 2010-05-27 | ドマンティス リミテッド | 血清アルブミンに対する抗体単一可変ドメイン |
| WO2017122018A1 (en) | 2016-01-12 | 2017-07-20 | Crescendo Biologics Limited | Molecules that bind prostate specific membrane antigen (psma) |
Also Published As
| Publication number | Publication date |
|---|---|
| CN113412278B (zh) | 2024-06-14 |
| JP2022507307A (ja) | 2022-01-18 |
| KR20210091254A (ko) | 2021-07-21 |
| SG11202103741RA (en) | 2021-05-28 |
| AU2019378154A1 (en) | 2021-05-20 |
| EP3880703A1 (en) | 2021-09-22 |
| GB201818460D0 (en) | 2018-12-26 |
| IL282641A (en) | 2021-06-30 |
| WO2020099871A1 (en) | 2020-05-22 |
| US20210340233A1 (en) | 2021-11-04 |
| CN113412278A (zh) | 2021-09-17 |
| CA3118640A1 (en) | 2020-05-22 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP7520002B2 (ja) | ヒト血清アルブミンに結合する単一ドメイン抗体 | |
| JP7450594B2 (ja) | 治療分子 | |
| JP7312168B2 (ja) | Cd137に結合するシングルドメイン抗体 | |
| KR102662387B1 (ko) | B7-h3 항체, 이의 항원-결합 단편 및 이의 의학적 용도 | |
| CN113840835B (zh) | 结合分子 | |
| IL282452A (en) | Antibodies with a light chain engineered histidine, and non-human animals that have been genetically modified to make them | |
| WO2022253302A1 (zh) | 靶向人血清白蛋白(hsa)的纳米抗体及其应用 | |
| JP2003284577A (ja) | 癌マーカー用生物合成結合蛋白質 | |
| CN107207581B (zh) | 用于制备优化的治疗分子的方法 | |
| JP7010491B2 (ja) | ヒト化抗rage抗体 | |
| US20250215616A1 (en) | Variable heavy chain only libraries, methods of preparation thereof, and uses thereof |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20220824 |
|
| A977 | Report on retrieval |
Free format text: JAPANESE INTERMEDIATE CODE: A971007 Effective date: 20230721 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20230724 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20231024 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20231218 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20240313 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20240610 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20240709 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 7520002 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |