JP7365332B2 - Cdk8/19阻害薬としての新規ヘテロ環式化合物 - Google Patents
Cdk8/19阻害薬としての新規ヘテロ環式化合物 Download PDFInfo
- Publication number
- JP7365332B2 JP7365332B2 JP2020506915A JP2020506915A JP7365332B2 JP 7365332 B2 JP7365332 B2 JP 7365332B2 JP 2020506915 A JP2020506915 A JP 2020506915A JP 2020506915 A JP2020506915 A JP 2020506915A JP 7365332 B2 JP7365332 B2 JP 7365332B2
- Authority
- JP
- Japan
- Prior art keywords
- compound
- cdk8
- bcd
- alkyl
- phenyl
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D413/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms
- C07D413/14—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms containing three or more hetero rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D403/00—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00
- C07D403/02—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00 containing two hetero rings
- C07D403/04—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00 containing two hetero rings directly linked by a ring-member-to-ring-member bond
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/41—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having five-membered rings with two or more ring hetero atoms, at least one of which being nitrogen, e.g. tetrazole
- A61K31/4164—1,3-Diazoles
- A61K31/4184—1,3-Diazoles condensed with carbocyclic rings, e.g. benzimidazoles
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/435—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom
- A61K31/4353—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom ortho- or peri-condensed with heterocyclic ring systems
- A61K31/437—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom ortho- or peri-condensed with heterocyclic ring systems the heterocyclic ring system containing a five-membered ring having nitrogen as a ring hetero atom, e.g. indolizine, beta-carboline
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/435—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom
- A61K31/4353—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom ortho- or peri-condensed with heterocyclic ring systems
- A61K31/4375—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom ortho- or peri-condensed with heterocyclic ring systems the heterocyclic ring system containing a six-membered ring having nitrogen as a ring heteroatom, e.g. quinolizines, naphthyridines, berberine, vincamine
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/435—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom
- A61K31/47—Quinolines; Isoquinolines
- A61K31/4709—Non-condensed quinolines and containing further heterocyclic rings
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/535—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with at least one nitrogen and one oxygen as the ring hetero atoms, e.g. 1,2-oxazines
- A61K31/5375—1,4-Oxazines, e.g. morpholine
- A61K31/5377—1,4-Oxazines, e.g. morpholine not condensed and containing further heterocyclic rings, e.g. timolol
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D401/00—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom
- C07D401/02—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom containing two hetero rings
- C07D401/04—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom containing two hetero rings directly linked by a ring-member-to-ring-member bond
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D401/00—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom
- C07D401/02—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom containing two hetero rings
- C07D401/06—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom containing two hetero rings linked by a carbon chain containing only aliphatic carbon atoms
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D401/00—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom
- C07D401/14—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom containing three or more hetero rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D403/00—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00
- C07D403/02—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00 containing two hetero rings
- C07D403/12—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00 containing two hetero rings linked by a chain containing hetero atoms as chain links
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D403/00—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00
- C07D403/14—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00 containing three or more hetero rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D413/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms
- C07D413/02—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms containing two hetero rings
- C07D413/10—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms containing two hetero rings linked by a carbon chain containing aromatic rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D471/00—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, at least one ring being a six-membered ring with one nitrogen atom, not provided for by groups C07D451/00 - C07D463/00
- C07D471/02—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, at least one ring being a six-membered ring with one nitrogen atom, not provided for by groups C07D451/00 - C07D463/00 in which the condensed system contains two hetero rings
- C07D471/04—Ortho-condensed systems
Description
「アルキル」とは、1~12個の炭素原子、より好ましくは、1~6個の炭素原子を有する脂肪族の直鎖または分鎖炭化水素基を意味する。分鎖とは、1つまたは複数の「低級アルキル」置換基を有するアルキル鎖を意味する。アルキル基の例としては、限定はしないが、メチル、エチル、n-プロピル、iso-プロピル、n-ブチル、iso-ブチル、sec-ブチル、tert-ブチル、n-ペンチル、2-ペンチル、3-ペンチル、neo-ペンチル、n-ヘキシルが挙げられる。アルキルは、同じ構造でも異なる構造でもよい置換基を有する場合がある。
「アルキルスルホニル」(-S(O)2-C1~C6アルキル)とは、スルホニル基-SO2-を介して適切な分子断片に結合している、上で定義したとおりの「アルキル」を意味する。アルキルスルホニルの例としては、限定はしないが、メチルスルホニル、エチルスルホニルなどが挙げられる。
「ハロ」または「ハロゲン」(Hal)とは、フルオロ、クロロ、ブロモ、およびヨードを意味する。
「置換基」とは、骨格(断片)に結合している化学基を意味する。
「溶媒和物」とは、1つまたは複数の溶媒分子を含んだ本発明の化合物または薬学的に許容されるその塩からなる分子の集合体である。溶媒分子は、レシピエントにとって安全であることがわかっている一般的な医薬用溶媒、たとえば、水、エタノール、エチレングリコールなどの分子である。メタノール、メチル-tert-ブチルエーテル、酢酸エチル、酢酸メチル、(S)-プロピレングリコールまたは(R)-プロピレングリコール、1,4-ブタンジオールなどの他の溶媒は、好ましい溶媒を得るための中間体の溶媒の生成に使用することができる。
溶媒和物および/または水和物は、結晶質形態で存在することが好ましい。
用語「結合」、「化学結合」、または「単結合」とは、結合によって繋げられる2つの原子が、より大きい下部構造の一部であるとみなされるとき、2つの原子または2つの部分(すなわち、基、断片)が化学的に結合することを指す。
用語「立体異性体」とは、同一の化学組成および同じ構造を有するが、原子またはその基の空間配置が異なる化合物を指す。立体異性体には、幾何異性体、鏡像異性体、ジアステエレオマーが含まれうる。
用語「ラセミ混合物」および「ラセミ体」とは、光学活性のない2つの鏡像異性体の等モル混合物を指す。鏡像異性体は、たとえば超臨界流体クロマトグラフィー(SFC)などのキラル分割によって、ラセミ混合物から別々に単離することができる。
用語「保護基」とは、アミノ基、カルボキシル基、ヒドロキシ基などの官能基の反応性をブロックするのに使用される基を指す。保護基の例としては、限定はしないが、tert-ブチルオキシカルボニル(Boc)、ベンジルオキシカルボニル(Cbz)、2-(トリメチルシリル)エトキシ)メチルアセタール(SEM)、トリアルキルシリル、アルキル(ジアリール)シリルまたはアルキルが挙げられる。
「医薬組成物」とは、本発明の化合物と、薬学的に許容される1種または複数の賦形剤とを含む組成物を意味する。賦形剤は、薬学的に許容され、薬理学的に適合する充填剤、溶媒、希釈剤、担体、佐剤、分配剤および検出剤(distributing and sensing agents)、送達剤、たとえば、保存剤、安定剤、充填剤、崩壊剤、湿潤剤(moistener)、乳化剤、懸濁化剤、増粘剤、甘味剤、着香剤、付香剤(aromatizing agent)、抗菌剤、殺かび剤、滑沢剤、および長期送達制御剤(prolonged delivery controller)からなる群から選択することができ、その選択および適切な割合は、投与の種類および方法ならびに投与量に応じて決まる。適切な懸濁化剤の例は、エトキシル化イソステアリルアルコール、ポリオキシエテン、ソルビトールおよびソルビトールエーテル、微結晶性セルロース、メタ水酸化アルミニウム、ベントナイト、寒天、およびトラガカント、またこれらの混合物である。たとえば、パラベン、クロロブタノール、ソルビン酸、および同様の化合物などの、種々の抗菌および殺かび剤によって、微生物の活動からの保護を実現することができる。組成物は、たとえば、糖、塩化ナトリウム、および同様の化合物などの等張剤も含有する場合がある。活性成分の吸収を遅くする薬剤、たとえば、モノステアリン酸アルミニウムやゼラチンによって、組成物の持続性作用を実現することができる。注射剤について、適切な担体、溶媒、希釈剤、および送達剤の例としては、水、エタノール、多価アルコール、およびこれらの混合物、(オリーブ油などの)自然の油および(オレイン酸エチルなどの)有機エステルが挙げられる。充填剤の例は、ラクトース、乳糖、クエン酸ナトリウム、炭酸カルシウム、リン酸カルシウムなどである。崩壊剤および分配剤(distributor)の例は、デンプン、アルギン酸およびその塩、シリケートなどである。適切な滑沢剤の例は、ステアリン酸マグネシウム、ラウリル硫酸ナトリウム、タルク、および高分子量ポリエチレングリコールである。活性成分を単独で、または別の活性化合物と組み合わせて、経口、舌下、経皮、筋肉内、静脈内、皮下、局所、または直腸投与するための医薬組成物は、伝統的な医薬用担体との混合物にした標準の投与形態として、ヒトおよび動物に投与することができる。適切な標準投与形態には、錠剤、ゼラチンカプセル剤、丸剤、粉末、顆粒、チューインガム、経口溶液または懸濁液などの経口形態;舌下および頬側投与形態;エアロゾル;植込錠;局所、経皮、皮下、筋肉内、静脈内、鼻腔内、または眼内形態、および直腸投与形態が含まれる。
「障害」とは、本発明の化合物による処置が恩恵をもたらすいずれかの状態を意味する。この用語は、哺乳動物を問題の障害に罹りやすくする病理学的状態を含めて、慢性および急性の障害または疾患を意味する。本明細書において処置対象となる障害の非限定的な例としては、腫瘍性疾患(oncological disease)、特に、乳がん、三種陰性乳がん(TNBC)、卵巣がん、転移性卵巣がん、胃がん、転移性胃がん、子宮内膜、唾液腺、肺、腎臓、または結腸がん;結腸直腸がん、黒色腫、転移性黒色腫、甲状腺、膵臓、前立腺、または膀胱がん;血液腫瘍性疾患、白血症(leucose)、急性骨髄性白血病、およびリンパ系悪性腫瘍、ニューロン、グリア、星状細胞、視床下部、および他の腺、マクロファージ、上皮、間質、および胞胚腔障害;炎症性、血管形成性、および免疫性障害が挙げられる。
本記述および後続の特許請求の範囲において、文脈からそうでないことが示されない限り、語「comprise」、「have」、「include」、または「comprises」、「comprising」、「has」、「having」、「includes」、「including」などの変形語、およびそのすべての文法的変異は、明記された完全体または完全体の群を含むが、他の完全体または完全体の群を除外しないことを示唆すると理解される。
式中、X1は、N、C、CHであり、
各X2、X3、X4は、独立に、C(H)m、NH、N、CR13、CHR13であり、
各L1、L2は、独立に、化学結合、-C(R6b)2-、-O-、-C(O)-、-C(O)-O-、-NH-、-C(=NR19)-であり、
各n、kは、独立に、0、1から選択され、
mは、0、1、2であり、
各R1、R3、R13は、独立に、H、Hal、シアノ、C1~C6アルキル、NH2であり、
各R2、R4は、独立に、
各X5、X6、X7は、独立に、C、CH、Nであり、
各L3、L4は、独立に、化学結合、-C(O)-、-O-、-CH2-、-NH-、-C(O)-NR7a-、-C(=NH)-であり、
p=0、1、2、3、4であり、
R5は、H;Hal;シアノ;C1~C6アルキル;C1~C6アルキルオキシ;C1~C6アルキルオキシC1~C6アルキル;NR15R16;非置換またはHal、C1~C6アルキル、C1~C6アルキルオキシ、NR15R16からなる群から選択される1つもしくはいくつかの置換基で置換されているアリール;非置換またはHal、C1~C6アルキル、C1~C6アルキルオキシ、NR15R16からなる群から選択される1つもしくはいくつかの置換基で置換されている、Nおよび/またはOから選択される1~2個のヘテロ原子を有する5~6員ヘテロシクリルであり、
各R6、R6a、R6bは、独立に、H、Hal、ヒドロキシ、C1~C6アルキル、C1~C6アルキルオキシであり、
各R7、R7aは、独立に、H、C1~C6アルキルであり、
各R8、R9は、独立に、H、C1~C6アルキル、-C(O)-NR21R22、-CN、-C(O)-OR20であり、または
R8およびR9は、これらが結合している炭素原子と一緒になって、窒素および/または酸素から選択される1~2個のヘテロ原子を有する5~6員ヘテロ環式環を形成しており、R8およびR9によって形成されるヘテロ環式環は、非置換でも、またはオキソ基、C1~C6アルキルから選択される1もしくは2つの置換基で置換されていてもよく、
各R10は、独立に、H、Hal、C1~C6アルキル、ヒドロキシ、シアノ、C1~C6アルキルオキシ、C1~C6アルキルオキシC1~C6アルキル、-NR23R24;非置換または1つもしくはいくつかのC1~C6アルキルで置換されている、N、O、および/またはSから選択される1~2個のヘテロ原子を有する5~6員ヘテロシクリル;非置換または1つもしくはいくつかのC1~C6アルキルで置換されている、N、O、および/またはSから選択される1~2個のヘテロ原子を有する5~6員ヘテロアリール;-S(O)2-C1~C6アルキルからなる群から選択され、
各R11、R12は、独立に、H;非置換またはヒドロキシ、C3~C6シクロアルキル、-NR23aR24aで置換されているC1~C6アルキル;C1~C6アルコキシC1~C6アルキル;C3~C6シクロアルキルであり、
各R14は、独立に、Hal、-C(O)NR17R18、C1~C6アルコキシであり、
各R15、R16、R19、R20、R21、R22、R23、R24、R23a、R24aは、独立に、H、C1~C6アルキルであり、
各R17、R18は、独立に、H、C1~C6アルキル;非置換またはHal、C1~C6アルキル、C1~C6アルコキシからなる群から選択される1つもしくはいくつかの置換基で置換されているアリールであり、
Halは、クロロ、ブロモ、ヨード、フルオロである。
別の一態様では、本発明は、各R3が、独立に、H、Halである、式Iの化合物に関する。
別の一態様では、本発明は、式I.1の化合物に関する。
mは、0、1であり、
X1は、N、C、CHであり、
各X2、X3は、独立に、C(H)m、NH、N、CR13、CHR13であり、
各L1、L2は、独立に、化学結合、-C(R6b)2-、-O-、-C(O)-、-C(O)-O-、-NH-、-C(=NR19)-であり、
各n、kは、独立に、0、1から選択され、
各R1、R3、R13は、独立に、H、Hal、シアノ、C1~C6アルキル、NH2であり、
各R2、R4は、独立に、
各X5、X6、X7は、独立に、C、CH、Nであり、
各L3、L4は、独立に、化学結合、-C(O)-、-O-、-CH2-、-NH-、-C(O)-NR7a-、-C(=NH)-であり、
p=0、1、2、3、4であり、
R5は、H;Hal;シアノ;C1~C6アルキル;C1~C6アルキルオキシ;C1~C6アルキルオキシC1~C6アルキル;NR15R16;非置換またはHal、C1~C6アルキル、C1~C6アルキルオキシ、NR15R16からなる群から選択される1つもしくはいくつかの置換基で置換されているアリール;非置換またはHal、C1~C6アルキル、C1~C6アルキルオキシ、NR15R16からなる群から選択される1つもしくはいくつかの置換基で置換されている、Nおよび/またはOから選択される1~2個のヘテロ原子を有する5~6員ヘテロシクリルであり、
各R6、R6a、R6bは、独立に、H、Hal、ヒドロキシ、C1~C6アルキル、C1~C6アルキルオキシであり、
各R7、R7aは、独立に、H、C1~C6アルキルであり、
各R8、R9は、独立に、H、C1~C6アルキル、-C(O)-NR21R22、-CN、-C(O)-OR20であり、または
R8およびR9は、これらが結合している炭素原子と一緒になって、窒素および/または酸素から選択される1~2個のヘテロ原子を有する5~6員ヘテロ環式環を形成しており、R8およびR9によって形成されるヘテロ環式環は、非置換でも、またはオキソ基、C1~C6アルキルから選択される1もしくは2つの置換基で置換されていてもよく、
各R10は、独立に、H、Hal、C1~C6アルキル、ヒドロキシ、シアノ、C1~C6アルキルオキシ、C1~C6アルキルオキシC1~C6アルキル、-NR23R24;非置換または1つもしくはいくつかのC1~C6アルキルで置換されている、N、O、および/またはSから選択される1~2個のヘテロ原子を有する5~6員ヘテロシクリル;非置換または1つもしくはいくつかのC1~C6アルキルで置換されている、N、O、および/またはSから選択される1~2個のヘテロ原子を有する5~6員ヘテロアリール;-S(O)2-C1~C6アルキルからなる群から選択され、
各R11、R12は、独立に、H;非置換またはヒドロキシ、C3~C6シクロアルキル、-NR23aR24aで置換されているC1~C6アルキル;C1~C6アルコキシC1~C6アルキル;C3~C6シクロアルキルであり、
各R14は、独立に、Hal、-C(O)NR17R18、C1~C6アルコキシであり、
各R15、R16、R19、R20、R21、R22、R23、R24、R23a、R24aは、独立に、H、C1~C6アルキルであり、
各R17、R18は、独立に、H、C1~C6アルキル;非置換またはHal、C1~C6アルキル、C1~C6アルコキシからなる群から選択される1つもしくはいくつかの置換基で置換されているアリールであり、
Halは、クロロ、ブロモ、ヨード、フルオロである。
別の一態様では、本発明は、各R3が、独立に、H、Halである、式I.1の化合物に関する。
別の一態様では、本発明は、式I.2の化合物に関する。
各X2、X3は、独立に、N、CR13であり、
各L1、L2は、独立に、化学結合、-C(R6b)2-、-O-、-C(O)-、-C(O)-O-、-NH-、-C(=NR19)-であり、
kは、0、1であり、
各R1、R3、R13は、独立に、H、Hal、シアノ、C1~C6アルキル、NH2であり、
各R2、R4は、独立に、
各X5、X6、X7は、独立に、C、CH、Nであり、
各L3、L4は、独立に、化学結合、-C(O)-、-O-、-CH2-、-NH-、-C(O)-NR7a-、-C(=NH)-であり、
p=0、1、2、3、4であり、
R5は、H;Hal;シアノ;C1~C6アルキル;C1~C6アルキルオキシ;C1~C6アルキルオキシC1~C6アルキル;NR15R16;非置換またはHal、C1~C6アルキル、C1~C6アルキルオキシ、NR15R16からなる群から選択される1つもしくはいくつかの置換基で置換されているアリール;非置換またはHal、C1~C6アルキル、C1~C6アルキルオキシ、NR15R16からなる群から選択される1つもしくはいくつかの置換基で置換されている、Nおよび/またはOから選択される1~2個のヘテロ原子を有する5~6員ヘテロシクリルであり、
各R6、R6a、R6bは、独立に、H、Hal、ヒドロキシ、C1~C6アルキル、C1~C6アルキルオキシであり、
各R7、R7aは、独立に、H、C1~C6アルキルであり、
各R8、R9は、独立に、H、C1~C6アルキル、-C(O)-NR21R22、-CN、-C(O)-OR20であり、または
R8およびR9は、これらが結合している炭素原子と一緒になって、窒素および/または酸素から選択される1~2個のヘテロ原子を有する5~6員ヘテロ環式環を形成しており、R8およびR9によって形成されるヘテロ環式環は、非置換でも、またはオキソ基、C1~C6アルキルから選択される1もしくは2つの置換基で置換されていてもよく、
各R10は、独立に、H、Hal、C1~C6アルキル、ヒドロキシ、シアノ、C1~C6アルキルオキシ、C1~C6アルキルオキシC1~C6アルキル、-NR23R24;非置換または1つもしくはいくつかのC1~C6アルキルで置換されている、N、O、および/またはSから選択される1~2個のヘテロ原子を有する5~6員ヘテロシクリル;非置換または1つもしくはいくつかのC1~C6アルキルで置換されている、N、O、および/またはSから選択される1~2個のヘテロ原子を有する5~6員ヘテロアリール;-S(O)2-C1~C6アルキルからなる群から選択され、
各R11、R12は、独立に、H;非置換またはヒドロキシ、C3~C6シクロアルキル、-NR23aR24aで置換されているC1~C6アルキル;C1~C6アルコキシC1~C6アルキル;C3~C6シクロアルキルであり、
各R14は、独立に、Hal、-C(O)NR17R18であり、
各R15、R16、R21、R22、R23、R24、R23a、R24aは、独立に、H、C1~C6アルキルであり、
各R17、R18は、独立に、H、C1~C6アルキル;非置換またはHal、C1~C6アルキル、C1~C6アルキルオキシからなる群から選択される1つもしくはいくつかの置換基で置換されているアリールであり、
各R19、R20は、独立に、H、C1~C6アルキルである。
別の一態様では、本発明は、式I.5aの化合物に関する。
別の一態様では、本発明は、式I.5の化合物に関する。
別の一態様では、本発明は、式I.6の化合物に関する。
各X1、X4は、独立に、C、CH、Nであり、
各L1、L2は、独立に、化学結合、-C(R6b)2-、-O-、-C(O)-、-NH-、-C(=NR19)-であり、
kは、0、1であり、
mは、1、2であり、
各R1、R3、R13は、独立に、H、Hal、シアノ、C1~C6アルキル、NH2であり、
各R2、R4は、独立に、
各X5、X6、X7は、独立に、C、CH、Nであり、
各L3、L4は、独立に、化学結合、-C(O)-、-O-、-CH2-、-NH-、-C(O)-NR7a-、-C(=NH)-であり、
p=0、1、2、3、4であり、
R5は、H;Hal;シアノ;C1~C6アルキル;C1~C6アルキルオキシ;C1~C6アルキルオキシC1~C6アルキル;NR15R16;非置換またはHal、C1~C6アルキル、C1~C6アルキルオキシ、NR15R16からなる群から選択される1つもしくはいくつかの置換基で置換されているアリール;非置換またはHal、C1~C6アルキル、C1~C6アルキルオキシ、NR15R16からなる群から選択される1つもしくはいくつかの置換基で置換されている、Nおよび/またはOから選択される1~2個のヘテロ原子を有する5~6員ヘテロシクリルであり、
各R6、R6a、R6bは、独立に、H、Hal、ヒドロキシ、C1~C6アルキル、C1~C6アルキルオキシであり、
各R7、R7aは、独立に、H、C1~C6アルキルであり、
各R8、R9は、独立に、H、C1~C6アルキル、-C(O)-NR21R22、-CN、-C(O)-OR20であり、または
R8およびR9は、これらが結合している炭素原子と一緒になって、窒素および/または酸素から選択される1~2個のヘテロ原子を有する5~6員ヘテロ環式環を形成しており、R8およびR9によって形成されるヘテロ環式環は、非置換でも、またはオキソ基、C1~C6アルキルから選択される1もしくは2つの置換基で置換されていてもよく、
各R10は、独立に、H、Hal、C1~C6アルキル、ヒドロキシ、シアノ、C1~C6アルキルオキシ、C1~C6アルキルオキシC1~C6アルキル、-NR23R24;非置換または1つもしくはいくつかのC1~C6アルキルで置換されている、N、O、および/またはSから選択される1~2個のヘテロ原子を有する5~6員ヘテロシクリル;非置換または1つもしくはいくつかのC1~C6アルキルで置換されている、N、O、および/またはSから選択される1~2個のヘテロ原子を有する5~6員ヘテロアリール;-S(O)2-C1~C6アルキルからなる群から選択され、
各R11、R12は、独立に、H;非置換またはヒドロキシ、C3~C6シクロアルキル、-NR23aR24aで置換されているC1~C6アルキル;C1~C6アルコキシC1~C6アルキル;C3~C6シクロアルキルであり、各R14は、独立に、Hal、-C(O)NR17R18、C1~C6アルコキシであり、
各R15、R16、R21、R22、R23、R24は、独立に、H、C1~C6アルキルであり、
各R17、R18は、独立に、H、C1~C6アルキル;非置換またはHal、C1~C6アルキル、C1~C6アルキルオキシからなる群から選択される1つもしくはいくつかの置換基で置換されているアリールであり、
各R19、R20は、独立に、H、C1~C6アルキルであり、
別の一態様では、本発明は、式I.7の化合物に関する。
別の一態様では、本発明は、式I.8の化合物に関する。
別の一態様では、本発明は、式I.9の化合物に関する。
別の一態様では、本発明は、式I.10の化合物に関する。
別の一態様では、本発明は、R5が、H;Hal;シアノ;C1~C6アルキル;C1~C6アルキルオキシ;C1~C6アルキルオキシC1~C6アルキル;NR15R16;非置換またはHal、C1~C6アルキル、C1~C6アルキルオキシ、NR15R16からなる群から選択される1つもしくはいくつかの置換基で置換されているフェニルであるアリール;非置換またはHal、C1~C6アルキル、C1~C6アルキルオキシ、NR15R16からなる群から選択される1つもしくはいくつかの置換基で置換されている4-モルホリニル、1-ピペリジニル、1-ピロリジニル、1-ピペラジニルである、Nおよび/またはOから選択される1~2個のヘテロ原子を有する5~6員ヘテロシクリルである、式I、I.1~I.10の化合物に関する。
別の一態様では、本発明は、式Iaの化合物:
式中、X1は、N、C、CHであり、
各X2、X3、X4は、独立に、C(H)m、NH、N、CR13であり、
各L1、L2は、独立に、化学結合、-C(R6)2-、-O-、-C(O)-、-NH-、-C(=NR19)-であり、
各n、kは、独立に、0、1から選択され、
mは、0、1、2であり、
各R1、R3、R13は、独立に、H、Hal、シアノ、C1~C6アルキルであり、
各R2、R4は、独立に、
各X5、X6、X7は、独立に、C、CH、Nであり、
各L3、L4は、独立に、化学結合、-C(O)-、-O-、-CH2-、-NH-、-C(O)-NR7-、-C(=NH)-であり、
p=0、1、2、3、4であり、
R5は、H;Hal;シアノ;C1~C6アルキル;C1~C6アルキルオキシ;C1~C6アルキルオキシC1~C6アルキル;NR15R16;非置換またはHal、C1~C6アルキル、C1~C6アルキルオキシ、NR15R16からなる群から選択される1つもしくはいくつかの置換基で置換されているアリール;非置換またはHal、C1~C6アルキル、C1~C6アルキルオキシ、NR15R16からなる群から選択される1つもしくはいくつかの置換基で置換されている、Nおよび/またはOから選択される1~2個のヘテロ原子を有する5~6員ヘテロシクリルであり、
各R6は、独立に、H、Hal、ヒドロキシ、C1~C6アルキルオキシであり、
各R7は、独立に、H、C1~C6アルキルであり、
各R8、R9は、独立に、H、C1~C6アルキル、-C(O)-NR21R22、-CN、-C(O)-OR20であり、または
R8およびR9は、これらが結合している炭素原子と一緒になって、窒素および/または酸素から選択される1~2個のヘテロ原子を有する5~6員ヘテロ環式環を形成しており、R8およびR9によって形成されるヘテロ環式環は、非置換でも、またはオキソ基、C1~C6アルキルから選択される1もしくは2つの置換基で置換されていてもよく、
各R10は、独立に、H、Hal、C1~C6アルキル、ヒドロキシ、シアノ、C1~C6アルキルオキシ、C1~C6アルキルオキシC1~C6アルキル、-NR23R24;非置換または1つもしくはいくつかのC1~C6アルキルで置換されている、N、O、および/またはSから選択される1~2個のヘテロ原子を有する5~6員ヘテロシクリル;非置換または1つもしくはいくつかのC1~C6アルキルで置換されている、N、O、および/またはSから選択される1~2個のヘテロ原子を有する5~6員ヘテロアリール;-S(O)2-C1~C6アルキルからなる群から選択され、
各R11、R12は、独立に、H、C1~C6アルキル、C1~C6アルコキシ、C1~C6アルキルオキシC1~C6アルキルであり、
各R14は、独立に、Hal、-C(O)NR17R18であり、
各R15、R16、R21、R22、R23、R24は、独立に、H、C1~C6アルキルであり、
各R17、R18は、独立に、H、C1~C6アルキル;非置換またはHal、C1~C6アルキル、C1~C6アルキルオキシからなる群から選択される1つもしくはいくつかの置換基で置換されているアリールであり、
各R19、R20は、独立に、H、C1~C6アルキルであり、
Halは、クロロ、ブロモ、ヨード、フルオロである。
別の一態様では、本発明は、各R1、R3が、独立に、H、Halである、式Iaの化合物に関する。
別の一態様では、本発明は、式Ia.1の化合物に関する。
mは、0、1であり、
X1、X2、X3、L1、L2、R1、R2、R3、R4、R13、n、k、
別の一態様では、本発明は、各R1、R3が、独立に、H、Halである、式Ia.1の化合物に関する。
本発明において記載する化合物は、薬学的に許容される塩として生成および/または使用することができる。薬学的に許容される塩の種類には、限定はしないが、遊離塩基形態の化合物を、塩酸、臭化水素酸、硫酸、硝酸、リン酸、メタリン酸などの薬学的に許容される無機酸、または酢酸、プロピオン酸、ヘキサン酸、シクロペンタンプロピオン酸、グリコール酸、ピルビン酸、乳酸、マロン酸、コハク酸、リンゴ酸、マレイン酸、フマル酸、トリフルオロ酢酸、酒石酸、クエン酸、安息香酸、3-(4-ヒドロキシベンゾイル)安息香酸、ケイ皮酸、マンデル酸、メタンスルホン酸、エタンスルホン酸、1,2-エタンジスルホン酸、2-ヒドロキシエタンスルホン酸、ベンゼンスルホン酸、トルエンスルホン酸、2-ナフタレンスルホン酸、4-メチルビシクロ-[2.2.2]オクタ-2-エン-l-カルボン酸、グルコヘプトン酸、4,4’-メチレンビス-3-ヒドロキシ-2-エン-l-カルボン酸、3-フェニルプロピオン酸、トリメチル酢酸、tert-ブチル酢酸、ラウリル硫酸、グルコン酸、グルタミン酸、ヒドロキシナフトエ酸、サリチル酸、ステアリン酸、ムコン酸などの有機酸と反応させることにより生成される酸付加塩;遊離塩基形態の化合物を、金属もしくはアンモニウムカチオン水酸化物、炭酸塩、もしくは炭酸水素塩などの薬学的に許容される無機塩基、または有機塩基と反応させることにより生成される塩基付加塩が含まれる。薬学的に許容される塩のカチオンとしては、限定はしないが、ナトリウム、カリウム、リチウム、マグネシウム、カルシウム、鉄、亜鉛、銅、マンガン、アルミニウムが挙げられ、有機塩基の例としては、限定はしないが、第一級、第二級、または第三級アミン(たとえば、イソプロピルアミン、トリメチルアミン、ジエチルアミン、トリエチルアミン、トリプロピルアミン)、天然に存在する置換アミンを始めとする置換アミン(たとえば、リシン、アルギニン、ヒスチジン、カフェイン、コリン)、環状アミン、ジシクロヘキシルアミン、プロカイン、エタノールアミン、2-ジエチルアミノエタノール、ヒドラバミン、エチレンジアミン、グルコサミン、メチルグルカミン、テオブロミン、プリン、ピペラジン、ピペリジン、N-エチルピペリジンが挙げられる。
ジメチルスルホキシド- DMSO
(±)-2.2’-ビス(ジフェニルホスフィノ)-1.1’-ジナフタレン- BINAP
4-メチル-ベンゼンスルホン酸- PTSA
4-ジメチルアミノピリジン- DMAP
N-(3-ジメチルアミノプロピル)-N’-エチルカルボジイミド塩酸塩- EDC’HCl
1-ヒドロキシベンゾトリアゾール水和物- HOBt
ジイソプロピルエチルアミン- DIPEA
N,N-ジメチルホルムアミド- DMF
テトラキス(トリフェニルホスフィン)パラジウム(0)- Pd(PPh3)4
テトラヒドロフラン- THF
2-ジシクロヘキシルホスフィノ-2’,4’,6’-トリイソプロピルビフェニル- XPhos
メチル-tert-ブチルエーテル- MTBE
ジフェニルホスホリルアジド- DPPA
2-(トリメチルシリル)エトキシメチルクロリド- SEMCl
本発明の化合物は、スキーム1に従って調製することができる。
各X1は、独立に、C、CH、Nであり、
各L1、L2は、独立に、化学結合、-C(R6)2-、-O-、-C(O)-、-NH-、-C(=NR19)-であり、
nは、0、1であり、
kは、0、1であり、
mは、1、2であり、
各R1、R3は、独立に、H、Hal、シアノ、C1~C6アルキルであり、
各R2、R4は、独立に、
各X5、X6、X7は、独立に、C、CH、Nであり、
各L3、L4は、独立に、化学結合、-C(O)-、-O-、-CH2-、-NH-、-C(O)-NR7-、-C(=NH)-であり、
p=0、1、2、3、4であり、
R5は、H;Hal;シアノ;C1~C6アルキル;C1~C6アルキルオキシ;C1~C6アルキルオキシC1~C6アルキル;NR15R16;非置換またはHal、C1~C6アルキル、C1~C6アルキルオキシ、NR15R16からなる群から選択される1つもしくはいくつかの置換基で置換されているアリール;非置換またはHal、C1~C6アルキル、C1~C6アルキルオキシ、NR15R16からなる群から選択される1つもしくはいくつかの置換基で置換されている、Nおよび/またはOから選択される1~2個のヘテロ原子を有する5~6員ヘテロシクリルであり、
各R6は、独立に、H、Hal、ヒドロキシ、C1~C6アルキルオキシであり、
各R7は、独立に、H、C1~C6アルキルであり、
各R8、R9は、独立に、H、C1~C6アルキル、-C(O)-NR21R22、-CN、-C(O)-OR20であり、または
R8およびR9は、これらが結合している炭素原子と一緒になって、窒素および/または酸素から選択される1~2個のヘテロ原子を有する5~6員ヘテロ環式環を形成しており、R8およびR9によって形成されるヘテロ環式環は、非置換でも、またはオキソ基、C1~C6アルキルから選択される1もしくは2つの置換基で置換されていてもよく、
各R10は、独立に、H、Hal、C1~C6アルキル、ヒドロキシ、シアノ、C1~C6アルキルオキシ、C1~C6アルキルオキシC1~C6アルキル、-NR23R24;非置換または1つもしくはいくつかのC1~C6アルキルで置換されている、N、O、および/またはSから選択される1~2個のヘテロ原子を有する5~6員ヘテロシクリル;非置換または1つもしくはいくつかのC1~C6アルキルで置換されている、N、O、および/またはSから選択される1~2個のヘテロ原子を有する5~6員ヘテロアリール;-S(O)2-C1~C6アルキルからなる群から選択され、
各R11、R12は、独立に、H、ヒドロキシ、C1~C6アルキル、C1~C6アルコキシ、C1~C6アルキルオキシC1~C6アルキルであり、
各R14は、独立に、Hal、-C(O)NR17R18であり、
各R15、R16、R21、R22、R23、R24は、独立に、H、C1~C6アルキルであり、
各R17、R18は、独立に、H、C1~C6アルキル;非置換またはHal、C1~C6アルキル、C1~C6アルキルオキシからなる群から選択される1つもしくはいくつかの置換基で置換されているアリールであり、
各R19、R20は、独立に、H、C1~C6アルキルであり、
各Yは、独立に、H、Hal、NH2、OH、-B(OH)2、-CON(Me)-OMe、-C(O)Clであり、
A、Wは、H、Hal、CN、-C(O)OH、-C(O)Clである。
化合物7の生成を伴う、化合物6と化合物Bの反応は、上述した、化合物1と化合物Bから化合物2を得るのに使用した方法の類推によって実施することができる。化合物7をハロゲン化物またはオキシハロゲン化リン、たとえば、POCl3、PBr3と反応させることにより、化合物2’を調製することができる。
tert-ブタノール中にて、加熱しながら、8をジフェニルホスホリルアジドと反応させることにより、化合物9を調製することができる。化合物10は、化合物9と化合物Cから、次の反応によって合成することができる。パラジウム触媒および塩基の存在下での、ハロゲン化アリール9とアリールボロン酸Cの鈴木反応(Y=-B(OH)2);パラジウム触媒および塩基の存在下での、ハロゲン化アリール9とアミンCのブッフバルト-ハートウィッグ反応(Y=H)。化合物10をHClやトリフルオロ酢酸などの強酸と反応させることにより、化合物11を調製することができる。化合物11から、亜硝酸ナトリウムとのジアゾ化反応に続いて、ヨウ化カリウムなどの適切な金属ハロゲン化物との反応によってジアゾニウム基をハロゲンに置換することにより、化合物5’を調製することができる。
シアン化亜鉛およびパラジウム触媒存在下でのシアン化反応によって、化合物2’から化合物12を調製することができる。化合物12を、アルカリの水-アルコール溶液の作用のもとで加熱しながら加水分解して、化合物13にすることができる。カルボン酸13を、カルボジイミドの関与によってアミド結合を得る方法に従ってアミンCと反応させることにより、化合物3’を調製することができる。
ニトリル12を、有機マグネシウム試薬の存在下でアミンCと反応させることにより、アミジン3’’を調製することができる。
上述した、化合物9と化合物Cから化合物10を調製するのに使用した方法の類推によって、化合物14から化合物15を調製することができる。化合物15をアルカリの水-アルコール溶液によって加水分解することにより、化合物16を合成することができる。化合物3’’’の生成を伴う化合物16と化合物Bの反応は、カルボジイミドおよび塩基の存在下で実施することができる。
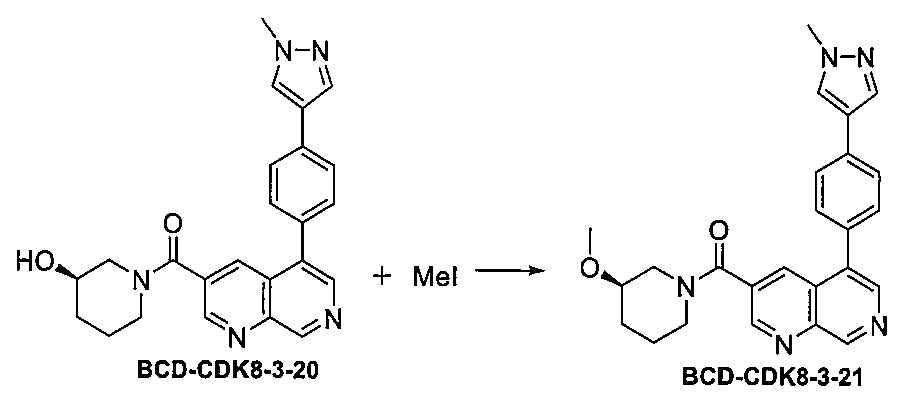
化合物17を、加熱しながらマロン酸と反応させることにより、化合物18を調製することができる。パラジウム触媒および塩基の存在下でのハロゲン化アリール18とアリールボロン酸Bの鈴木反応(Y=-B(OH)2)、またはパラジウム触媒および塩基の存在下でのハロゲン化アリール18とアミンBのブッフバルト-ハートウィッグ反応(Y=H)によって、化合物19を調製することができる。塩化チオニルなどの脱水ハロゲン化剤との反応によって、化合物20を調製することができる。化合物20をアミンCと反応させることにより、化合物21を調製することができる。
本発明の化合物は、スキーム8に従って調製することができる。
化合物23のアミンCとの反応を、DMSO中にて、カリウムtert-ブトキシドやジイソプロピルエチルアミンなどの塩基の存在下で実施すると、化合物24を得ることができる。化合物24を、有機リン配位子を有するパラジウム錯化合物などの触媒の存在下で化合物Bと反応させることにより、化合物25に変換することができる。化合物25から、Pd/Cでの水素還元反応に続いて、ギ酸のトリアルキルオルトエステルの作用のもとでの酸触媒作用による環化によって、化合物26を調製することができる。化合物29が得られる、置換ニトロ安息香酸28の化合物Bとの反応は、トリアルキルアミンやカルボジイミドなどの非求核性塩基の存在下で実施することができる。化合物25の生成を伴う、化合物29とアミンCの反応は、上述した、化合物23と化合物Cから化合物24を得るのに使用した方法の類推によって実施することができる。化合物24は、上述した、化合物25から化合物26を得るのに使用した方法の類推によって、化合物27に変換することができる。化合物27は、上述した、化合物24から化合物25を調製するのに使用した方法の類推によって、化合物26に変換することができる。
一態様では、本発明は、サイクリン依存性タンパク質キナーゼCDK8/19の活性化が介在する疾患または障害を処置するための方法であって、それを必要とする対象において、治療有効量の本発明の化合物もしくは薬学的に許容されるその塩または本発明の医薬組成物を投与するステップを含む方法に関する。
本明細書で使用するとき、化合物と他の1種または複数の治療薬に関しての用語「共投与」、「共投与される」、および「組み合わせて」は、次の事項:
・ 本発明の化合物と治療薬のそうした組合せの、処置を必要とする患者への同時投与[こうした成分を一緒に製剤して、前記成分を前記患者に対して実質的に同時に放出する単一剤形にする場合]、
・ 本発明の化合物と治療薬のそうした組合せの、処置を必要とする患者への実質的な同時投与[こうした成分を互いに別々に製剤して、前記患者に実質的に同時に投与され、その後前記成分が前記患者に対して実質的に同時に放出される別個の剤形にする場合]、
・ 本発明の化合物と治療薬のそうした組合せの、処置を必要とする患者への順次投与[こうした成分を互いに別々に製剤して、前記患者に各投与の間に有意な時間間隔をおいて連続的に投与され、その後前記成分が前記患者に対して実質的に異なる時期に放出される別個の剤形にする場合]、および
・ 本発明の化合物と治療薬のそうした組合せの、処置を必要とする患者への順次投与[こうした成分を一緒に製剤して、成分が前記患者に対して、同じおよび/または異なる時期に、併行して、連続して、かつ/または一部重複して放出されることになるように前記成分を制御されたかたちで放出する単一剤形にする場合]
を意味し、指し、包含し、各部分は、同じまたは異なる経路で投与される場合がある。
そのような薬物療法は、抗がん薬の1種または複数の投与を含むものでよい。抗がん薬の例としては、限定はしないが、アルキル化薬、アルキルスルホネート、ニトロソ尿素、またはトリアゼン;代謝拮抗薬 ホルモンおよび拮抗薬;白金化合物;抗がん抗生物質;トポイソメラーゼ阻害薬のいずれかが挙げられる。
抗がん薬の例としては、限定はしないが、次の薬剤、すなわち、微小管を標的とする薬物、たとえば、タキサン(たとえば、パクリタキセル、ドセタキセル、カバジタキセル、テゼタキセル(tezetaxel))、ビンカアルカロイド(たとえば、ビノレルビン、ビンブラスチン、ビンクリスチン、ビンデシン、ビンフルニン);分裂促進因子活性化タンパク質キナーゼシグナル伝達阻害薬(たとえば、U0126、PD98059、PD184352、PD0325901、ARRY-142886、SB239063、SP600125、BAY43-9006、ワートマニン、LY294002);mTOR阻害薬(たとえば、シロリムス、テムシロリムス、エベロリムス、リダフォロリムス);抗体(たとえば、リツキシマブ、トラスツズマブ、アレムツズマブ、ベシレソマブ、セツキシマブ、デノスマブ、イピリムマブ、ベバシズマブ、ペルツズマブ、ニボルマブ、オファツムマブ、パニツムマブ、トシツモマブ、カツマクソマブ、エロツズマブ、エプラツズマブ、ファーレツズマブ、モガムリズマブ、ネシツムマブ、ニモツズマブ、オビヌツズマブ、オカラツズマブ、オレゴボマブ、ラムシルマブ、リロツムマブ、シルツキシマブ、トシリズマブ、ザルツムマブ、ザノリムマブ、マツズマブ、ダロツズマブ、オナルツズマブ、ラコツモマブ(racotumomab)、タバルマブ、EDM-525797);キナーゼ阻害薬(ホスタマチニブ、エントスプレテニブ(entospletenib)、エルロチニブ、イマチニブ、ラパチニブ、ニロチニブ、パゾパニブ、ベムラフェニブ、ゲフィチニブ、クリゾチニブ、ダサチニブ、レゴラフェニブ、ルキソリチニブ、ソラフェニブ、スニチニブ、バンデタニブ、ボスチニブ、アキシチニブ、アファチニブ、アリセルチブ、ダブラフェニブ、ダコミチニブ、ジナシクリブ、ドビチニブ、ニンテダニブ、レンバチニブ、リニファニブ、リンシチニブ、マシチニブ、モテサニブ、ネラチニブ、オランチニブ、ポナチニブ、ラドチニブ、ティピファニブ、チバンチニブ、チボザニブ、トラメチニブ、アパチニブ、イブルチニブ、アカラブルチニブ、コビメチニブ、フェドラチニブ、ブリバニブアラニネート、セジラニブ、カボザンチニブ、イコチニブ、シパチニブ(cipatinib)、リゴサチブ、ピマセルチブ、ブパリシブ、イデラリシブ、ミドスタウリン、ペリホシン、XL-647);光増感剤(たとえば、タラポルフィン、テモポルフィン、ポルフィマーナトリウム);サイトカイン(たとえば、アルデスロイキン、インターフェロンアルファ、インターフェロンアルファ-2a、インターフェロンアルファ-2b、セルモロイキン、タソネルミン、組換え型インターロイキン2、オプレルベキン、組換え型インターフェロンベータ-1a);ワクチン(たとえば、ピシバニール、シプロイセルT、ビテスペン、エメペピムト-S、oncoVAX、リンドペピムト、troVAX、MGN-1601、MGN-1703);ビサントレン、デシタビン、ミトキサントロン、プロカルバジン、トラベクテジン、アムサクリン、ブロスタリシン、ミルテホシン、ロミデプシン、プリチデプシン、エリブリン、イクサベピロン、フォスブレタブリン、デニロイキンジフチトクス、イブリツモマブチウキセタン、プレドニムスチン、トラスツズマブエムタンシン、エストラムスチン、ゲムツズマブオゾガマイシン、アフリベルセプト、オポルツズマブモナトクス(oportuzumab monatox)、シントレデキンベスドトクス(cintredekin besudotox)、エドトレオチド、イノツズマブオゾガマイシン、ナプツモマブエスタフェナトクス、ビンタフォリド、ブレンツキシマブベドチン、ボルテゾミブ、イキサゾミブ、カルフィルゾミブ、レナリドミド、サリドマイド、ポマリドミド、ゾレドロン酸、イバンドロン酸、パミドロン酸、アリトレチノイン、トレチノイン、ペレチノイン、ベキサロテン、タミバロテン、イミキモド、レンチナン、ミファムルチド、ロムルチド、ペグアスパラガーゼ、ペントスタチン、エンドスタチン、シゾフィラン、ビスモデギブ、ボリノスタット、エンチノスタット、パノビノスタット、セレコキシブ、シレンギチド、エタニダゾール、ガネテスピブ、イドロノクシル(idronoksil)、イニパリブ、ロニダミン、ニモラゾール、プロコダゾール、タスキニモド、テロトリスタット、ベリノスタット、サイマルファシン、チラパザミン、トセドスタット、トラベデルセン、ウベニメクス、バルスポダール、ゲンジシン、レオリシン、レタスピマイシン、トレバナニブ、ビルリジンのいずれかが挙げられる。
患者の状態の改善が見出されれば、必要なら、維持量が投与される。その後、症状に応じて、投与量もしくは投与頻度または両方を、疾患または障害の改善が実現されるレベルまで減らすことができる。症状が再発すると、患者には、周期的な処置が長期的に必要となる場合がある。
非限定的に本発明は以下の態様を含む。
[態様1]
式Iの化合物:
[式中、X1は、N、C、CHであり、
各X2、X3、X4は、独立に、C(H)m、NH、N、CR13、CHR13であり、
各L1、L2は、独立に、化学結合、-C(R6b)2-、-O-、-C(O)-、-C(O)-O-、-NH-、-C(=NR19)-であり、
各n、kは、独立に、0、1から選択され、
mは、0、1、2であり、
各R1、R3、R13は、独立に、H、Hal、シアノ、C1~C6アルキル、NH2であり、
各R2、R4は、独立に、
各X5、X6、X7は、独立に、C、CH、Nであり、
各L3、L4は、独立に、化学結合、-C(O)-、-O-、-CH2-、-NH-、-C(O)-NR7a-、-C(=NH)-であり、
p=0、1、2、3、4であり、
R5は、H;Hal;シアノ;C1~C6アルキル;C1~C6アルキルオキシ;C1~C6アルキルオキシC1~C6アルキル;NR15R16;非置換またはHal、C1~C6アルキル、C1~C6アルコキシ、NR15R16からなる群から選択される1つもしくはいくつかの置換基で置換されているアリール;非置換またはHal、C1~C6アルキル、C1~C6アルキルオキシ、NR15R16からなる群から選択される1つもしくはいくつかの置換基で置換されている、Nおよび/またはOから選択される1~2個のヘテロ原子を有する5~6員ヘテロシクリルであり、
各R6、R6a、R6bは、独立に、H、Hal、ヒドロキシ、C1~C6アルキル、C1~C6アルキルオキシであり、
各R7、R7aは、独立に、H、C1~C6アルキルであり、
各R8、R9は、独立に、H、C1~C6アルキル、-C(O)-NR21R22、-CN、-C(O)-OR20であり、または
R8およびR9は、これらが結合している炭素原子と一緒になって、窒素および/または酸素から選択される1~2個のヘテロ原子を有する5~6員ヘテロ環式環を形成しており、R8およびR9によって形成されるヘテロ環式環は、非置換でも、またはオキソ基、C1~C6アルキルから選択される1もしくは2つの置換基で置換されていてもよく、
各R10は、独立に、H、Hal、C1~C6アルキル、ヒドロキシ、シアノ、C1~C6アルキルオキシ、C1~C6アルキルオキシC1~C6アルキル、-NR23R24;非置換または1つもしくはいくつかのC1~C6アルキルで置換されている、N、O、および/またはSから選択される1~2個のヘテロ原子を有する5~6員ヘテロシクリル;非置換または1つもしくはいくつかのC1~C6アルキルで置換されている、N、O、および/またはSから選択される1~2個のヘテロ原子を有する5~6員ヘテロアリール;-S(O)2-C1~C6アルキルからなる群から選択され、
各R11、R12は、独立に、H;非置換またはヒドロキシ、C3~C6シクロアルキル、-NR23aR24aで置換されているC1~C6アルキル;C1~C6アルコキシC1~C6アルキル;C3~C6シクロアルキルであり、
各R14は、独立に、Hal、-C(O)NR17R18、C1~C6アルコキシであり、
各R15、R16、R19、R20、R21、R22、R23、R24、R23a、R24aは、独立に、H、C1~C6アルキルであり、
各R17、R18は、独立に、H、C1~C6アルキル;非置換またはHal、C1~C6アルキル、C1~C6アルコキシからなる群から選択される1つもしくはいくつかの置換基で置換されているアリールであり、
各
Halは、クロロ、ブロモ、ヨード、フルオロである]。
[態様2]
式Iの化合物が、式I.1の化合物:
mは、0、1であり、
X1は、N、C、CHであり、
各X2、X3は、独立に、C(H)m、NH、N、CR13、CHR13であり、
各L1、L2は、独立に、化学結合、-C(R6b)2-、-O-、-C(O)-、-C(O)-O-、-NH-、-C(=NR19)-であり、
各n、kは、独立に、0、1から選択され、
各R1、R3、R13は、独立に、H、Hal、シアノ、C1~C6アルキル、NH2であり、
各R2、R4は、独立に、
各X5、X6、X7は、独立に、C、CH、Nであり、
各L3、L4は、独立に、化学結合、-C(O)-、-O-、-CH2-、-NH-、-C(O)-NR7a-、-C(=NH)-であり、
p=0、1、2、3、4であり、
R5は、H;Hal;シアノ;C1~C6アルキル;C1~C6アルキルオキシ;C1~C6アルキルオキシC1~C6アルキル;NR15R16;非置換またはHal、C1~C6アルキル、C1~C6アルキルオキシ、NR15R16からなる群から選択される1つもしくはいくつかの置換基で置換されているアリール;非置換またはHal、C1~C6アルキル、C1~C6アルキルオキシ、NR15R16からなる群から選択される1つもしくはいくつかの置換基で置換されている、Nおよび/またはOから選択される1~2個のヘテロ原子を有する5~6員ヘテロシクリルであり、
各R6、R6a、R6bは、独立に、H、Hal、ヒドロキシ、C1~C6アルキル、C1~C6アルキルオキシであり、
各R7、R7aは、独立に、H、C1~C6アルキルであり、
各R8、R9は、独立に、H、C1~C6アルキル、-C(O)-NR21R22、-CN、-C(O)-OR20であり、または
R8およびR9は、これらが結合している炭素原子と一緒になって、窒素および/または酸素から選択される1~2個のヘテロ原子を有する5~6員ヘテロ環式環を形成しており、R8およびR9によって形成されるヘテロ環式環は、非置換でも、またはオキソ基、C1~C6アルキルから選択される1もしくは2つの置換基で置換されていてもよく、
各R10は、独立に、H、Hal、C1~C6アルキル、ヒドロキシ、シアノ、C1~C6アルキルオキシ、C1~C6アルキルオキシC1~C6アルキル、-NR23R24;非置換または1つもしくはいくつかのC1~C6アルキルで置換されている、N、O、および/またはSから選択される1~2個のヘテロ原子を有する5~6員ヘテロシクリル;非置換または1つもしくはいくつかのC1~C6アルキルで置換されている、N、O、および/またはSから選択される1~2個のヘテロ原子を有する5~6員ヘテロアリール;-S(O)2-C1~C6アルキルからなる群から選択され、
各R11、R12は、独立に、H;非置換またはヒドロキシ、C3~C6シクロアルキル、-NR23aR24aで置換されているC1~C6アルキル;C1~C6アルコキシC1~C6アルキル;C3~C6シクロアルキルであり、
各R14は、独立に、Hal、-C(O)NR17R18、C1~C6アルコキシであり、
各R15、R16、R19、R20、R21、R22、R23、R24、R23a、R24aは、独立に、H、C1~C6アルキルであり、
各R17、R18は、独立に、H、C1~C6アルキル;非置換またはHal、C1~C6アルキル、C1~C6アルコキシからなる群から選択される1つもしくはいくつかの置換基で置換されているアリールであり、
各
Halは、クロロ、ブロモ、ヨード、フルオロである]である、態様1に記載の化合物。
[態様3]
各L1、L2が、独立に、化学結合、-C(O)-、-C(O)-O-、-NH-、-C(=NH)-である、態様1から2のいずれか一項に記載の化合物。
[態様4]
R5が、H;Hal;シアノ;C1~C6アルキル;C1~C6アルキルオキシ;C1~C6アルキルオキシC1~C6アルキル;NR15R16;非置換またはHal、C1~C6アルキル、C1~C6アルキルオキシ、NR15R16からなる群から選択される1つもしくはいくつかの置換基で置換されているフェニルであるアリール;非置換またはHal、C1~C6アルキル、C1~C6アルキルオキシ、NR15R16からなる群から選択される1つもしくはいくつかの置換基で置換されている4-モルホリニル、1-ピペリジニル、1-ピロリジニル、1-ピペラジニルである、Nおよび/またはOから選択される1~2個のヘテロ原子を有する5~6員ヘテロシクリルであり、
各R15、R16が、独立に、H、C1~C6アルキルである、態様1から2のいずれか一項に記載の化合物。
[態様5]
R10が、H、Hal、C1~C6アルキル、ヒドロキシ、シアノ、C1~C6アルキルオキシ、C1~C6アルキルオキシC1~C6アルキル、-NR23R24;非置換または1つもしくはいくつかのC1~C6アルキルで置換されている4-モルホリニル、1-ピペリジニル、1-ピロリジニル、1-ピペラジニルである、N、O、および/またはSから選択される1~2個のヘテロ原子を有する5~6員ヘテロシクリル;非置換または1つもしくはいくつかのC1~C6アルキルで置換されているチエニル、イミダゾリル、ピラゾリルである、N、O、および/またはSから選択される1~2個のヘテロ原子を有する5~6員ヘテロアリール;-S(O)2-C1~C6アルキルからなる群から独立に選択され、
各R23、R24は、独立に、H、C1~C6アルキルである、態様1から2のいずれか一項に記載の化合物。
[態様6]
式Iの化合物が、式Iaの化合物:
[式中、X1は、N、C、CHであり、
各X2、X3、X4は、独立に、C(H)m、NH、N、CR13であり、
各L1、L2は、独立に、化学結合、-C(R6)2-、-O-、-C(O)-、-NH-、-C(=NR19)-であり、
各n、kは、独立に、0、1から選択され、
mは、0、1、2であり、
各R1、R3、R13は、独立に、H、Hal、シアノ、C1~C6アルキルであり、
各R2、R4は、独立に、
各X5、X6、X7は、独立に、C、CH、Nであり、
各L3、L4は、独立に、化学結合、-C(O)-、-O-、-CH2-、-NH-、-C(O)-NR7-、-C(=NH)-であり、
p=0、1、2、3、4であり、
R5は、H;Hal;シアノ;C1~C6アルキル;C1~C6アルキルオキシ;C1~C6アルキルオキシC1~C6アルキル;NR15R16;非置換またはHal、C1~C6アルキル、C1~C6アルキルオキシ、NR15R16からなる群から選択される1つもしくはいくつかの置換基で置換されているアリール;非置換またはHal、C1~C6アルキル、C1~C6アルキルオキシ、NR15R16からなる群から選択される1つもしくはいくつかの置換基で置換されている、Nおよび/またはOから選択される1~2個のヘテロ原子を有する5~6員ヘテロシクリルであり、
各R6は、独立に、H、Hal、ヒドロキシ、C1~C6アルキルオキシであり、
各R7は、独立に、H、C1~C6アルキルであり、
各R8、R9は、独立に、H、C1~C6アルキル、-C(O)-NR21R22、-CN、-C(O)-OR20であり、または
R8およびR9は、これらが結合している炭素原子と一緒になって、窒素および/または酸素から選択される1~2個のヘテロ原子を有する5~6員ヘテロ環式環を形成しており、R8およびR9によって形成されるヘテロ環式環は、非置換でも、またはオキソ基、C1~C6アルキルから選択される1もしくは2つの置換基で置換されていてもよく、
各R10は、独立に、H、Hal、C1~C6アルキル、ヒドロキシ、シアノ、C1~C6アルキルオキシ、C1~C6アルキルオキシC1~C6アルキル、-NR23R24;非置換または1つもしくはいくつかのC1~C6アルキルで置換されている、N、O、および/またはSから選択される1~2個のヘテロ原子を有する5~6員ヘテロシクリル;非置換または1つもしくはいくつかのC1~C6アルキルで置換されている、N、O、および/またはSから選択される1~2個のヘテロ原子を有する5~6員ヘテロアリール;-S(O)2-C1~C6アルキルからなる群から選択され、
各R11、R12は、独立に、H、C1~C6アルキル、C1~C6アルコキシ、C1~C6アルキルオキシC1~C6アルキルであり、
各R14は、独立に、Hal、-C(O)NR17R18であり、
各R15、R16、R21、R22、R23、R24は、独立に、H、C1~C6アルキルであり、
各R17、R18は、独立に、H、C1~C6アルキル;非置換またはHal、C1~C6アルキル、C1~C6アルキルオキシからなる群から選択される1つもしくはいくつかの置換基で置換されているアリールであり、
各R19、R20は、独立に、H、C1~C6アルキルであり、
各
Halは、クロロ、ブロモ、ヨード、フルオロである]である、態様1に記載の化合物。
[態様7]
式Ia.1の化合物:
mは、0、1であり、
X1、X2、X3、L1、L2、R1、R2、R3、R4、R13、n、k、
[態様8]
各R3が、独立に、H、Halである、態様1から7のいずれか一項に記載の化合物。
[態様9]
1-(1-(4-((メチルスルホニル)カルバモイル)フェニル)-1H-ベンゾ[d]イミダゾール-6-イル)-N-フェニルアゼチジン-3-カルボキサミド(BCD-CDK8-1-1)
4-(6-(アゼチジン-1-カルボニル)-1H-ベンゾ[d]イミダゾール-1-イル)-N-(メチルスルホニル)ベンズアミド(BCD-CDK8-1-2)
(1-(4-(1H-ピラゾール-4-イル)フェニル)-1H-ベンゾ[d]イミダゾール-6-イル)(ピペリジン-1-イル)メタノン(BCD-CDK8-1-3)
(1-(1-(4-(1H-ピラゾール-4-イル)フェニル)-1H-ベンゾ[d]イミダゾール-6-イル)アゼチジン-3-イル)(モルホリノ)メタノン(BCD-CDK8-1-4)
(1-(4-(1H-ピラゾール-4-イル)フェニル)-1H-ベンゾ[d]イミダゾール-6-イル)(アゼチジン-1-イル)メタノン(BCD-CDK8-1-5)
メチル4-(6-(3-(フェニルカルバモイル)アゼチジン-1-イル)-1H-ベンゾ[d]イミダゾール-1-イル)ベンゾエート(BCD-CDK8-1-6E)
4-(6-(3-(フェニルカルバモイル)アゼチジン-1-イル)-1H-ベンゾ[d]イミダゾール-1-イル)安息香酸(BCD-CDK8-1-6A)
1-(1-(4-カルバモイルフェニル)-1H-ベンゾ[d]イミダゾール-6-イル)-N-フェニルアゼチジン-3-カルボキサミド(BCD-CDK8-1-6)
メチル-4-(6-(3-(フェニルカルバモイル)アゼチジン-1-イル)-4-フルオロ-1H-ベンゾ[d]イミダゾール-1-イル)ベンゾエート(BCD-CDK8-1-7E)
4-(-6-(3-(フェニルカルバモイル)アゼチジン-1-イル)-4-フルオロ-1H-ベンゾ[d]イミダゾール-1-イル)安息香酸(BCD-CDK8-1-7A)
1-(1-(4-カルバモイルフェニル)-4-フルオロ-1H-ベンゾ[d]イミダゾール-6-イル)-N-フェニルアゼチジン-3-カルボキサミド(BCD-CDK8-1-7)
(1-(1-(4-(1H-ピラゾール-4-イル)フェニル)-4-フルオロ-1H-ベンゾ[d]イミダゾール-6-イル)アゼチジン-3-イル)(モルホリノ)メタノン(BCD-CDK8-1-8)
(1-(1-(4-(ジメチルアミノ)フェニル)-1H-ベンゾ[d]イミダゾール-6-イル)アゼチジン-3-イル)(モルホリノ)メタノン(BCD-CDK8-1-9)
アゼチジン-1-イル(1-(4-(ジメチルアミノ)フェニル)-1H-ベンゾ[d]イミダゾール-6-イル)メタノン(BCD-CDK8-1-10)
(3-メトキシアゼチジン-1-イル)(1-(4-メトキシフェニル)-1H-ベンゾ[d]イミダゾール-6-イル)メタノン(BCD-CDK8-1-11)
(1-(1-(4-メトキシフェニル)-1H-ベンゾ[d]イミダゾール-6-イル)アゼチジン-3-イル)(モルホリノ)メタノン(BCD-CDK8-1-12)
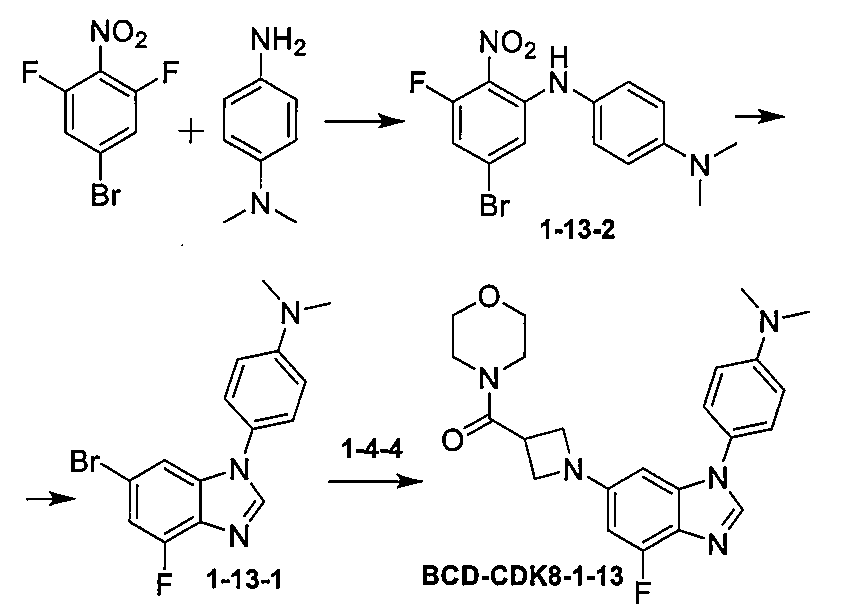
(1-(1-(4-(ジメチルアミノ)フェニル)-4-フルオロ-1H-ベンゾ[d]イミダゾール-6-イル)アゼチジン-3-イル)(モルホリノ)メタノン(BCD-CDK8-1-13)
(1-(1-(4-(1H-ピラゾール-4-イル)フェニル)-7-フルオロ-1H-ベンゾ[d]イミダゾール-6-イル)アゼチジン-3-イル)(モルホリノ)メタノン(BCD-CDK8-1-14)
メチル-4-(6-(アゼチジン-1-カルボニル)-7-フルオロ-1H-ベンゾ[d]イミダゾール-1-イル)ベンゾエート(BCD-CDK8-1-15E)
4-(6-(アゼチジン-1-カルボニル)-7-フルオロ-1H-ベンゾ[d]イミダゾール-1-イル)安息香酸(BCD-CDK8-1-15A)
4-(6-(アゼチジン-1-カルボニル)-7-フルオロ-1H-ベンゾ[d]イミダゾール-1-イル)ベンズアミド(BCD-CDK8-1-15)
(1-(4-(1-メチル-1H-ピラゾール-4-イル)フェニル)-1H-ベンゾ[d]イミダゾール-6-イル)(ピペリジン-1-イル)メタノン(BCD-CDK8-1-16)
(1-(1-(4-(1-メチル-1H-ピラゾール-4-イル)フェニル)-1H-ベンゾ[d]イミダゾール-6-イル)アゼチジン-3-イル)(モルホリノ)メタノン(BCD-CDK8-1-17)
アゼチジン-1-イル(1-(4-(1-メチル-1H-ピラゾール-4-イル)フェニル)-1H-ベンゾ[d]イミダゾール-6-イル)メタノン(BCD-CDK8-1-18)
(1-(1-(4-(1-メチル-1H-ピラゾール-4-イル)フェニル)-4-フルオロ-1H-ベンゾ[d]イミダゾール-6-イル)アゼチジン-3-イル)(モルホリノ)メタノン(BCD-CDK8-1-19)
(1-(1-(4-(1-メチル-1H-ピラゾール-4-イル)フェニル)-7-フルオロ-1H-ベンゾ[d]イミダゾール-6-イル)アゼチジン-3イル)(モルホリノ)メタノン(BCD-CDK8-1-20)
4-(6-((2-(クロロメチル)-3-オキソ-3-(フェニルアミノ)プロピル)アミノ)-4-フルオロ-1H-ベンゾ[d]イミダゾール-1-イル)ベンズアミド(BCD-CDK8-1-21A)
4-(6-((2-(クロロメチル)-3-オキソ-3-(フェニルアミノ)プロピル)アミノ)-4-フルオロ-1H-ベンゾ[d]イミダゾール-1-イル)安息香酸(BCD-CDK8-1-21)
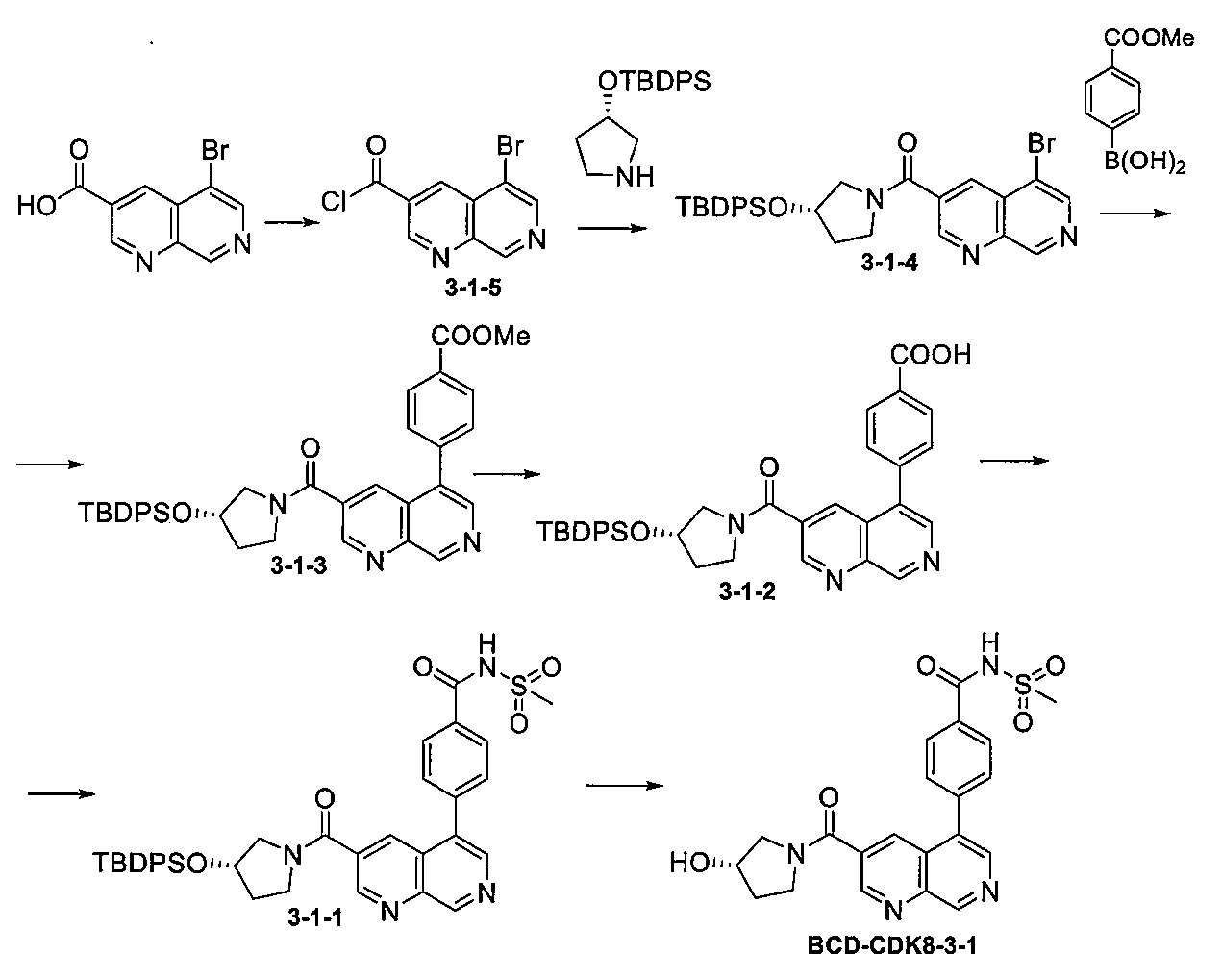
(S)-4-(3-(3-ヒドロキシピロリジン-1-カルボニル)-1,7-ナフチリジン-5-イル)-N-(メチルスルホニル)ベンズアミド(BCD-CDK8-3-1)
(R)-(5-(4-(1H-ピラゾール-4-イル)フェニル)-1,7-ナフチリジン-3-イル)(3-ヒドロキシピロリジン-1-イル)メタノン(BCD-CDK8-3-2)
(R)-(5-(4-(ジメチルアミノ)フェニル)-1,7-ナフチリジン-3-イル)(3-ヒドロキシピロリジン-1-イル)メタノン(BCD-CDK8-3-3)
(R)-(3-ヒドロキシピロリジン-1-イル)(5-(4-(1-メチル-1H-ピラゾール-4-イル)フェニル)-1,7-ナフチリジン-3-イル)メタノン(BCD-CDK8-3-4)
(R)-(3-ヒドロキシピロリジン-1-イル)(5-(4-モルホリノフェニル)-1,7-ナフチリジン-3-イル)メタノン(BCD-CDK8-3-5)
(R)-(3-ヒドロキシピロリジン-1-イル)(5-(4-メトキシフェニル)-1,7-ナフチリジン-3-イル)メタノン(BCD-CDK8-3-6)
(5-(4-(ジメチルアミノ)フェニル)-1,7-ナフチリジン-3-イル)(4-メチルピペラジン-1-イル)メタノン(BCD-CDK8-3-8)
(1-(5-(4-(1-メチル-1H-ピラゾール-4-イル)フェニル)-1,7-ナフチリジン-3-イル)アゼチジン-3-イル)(モルホリノ)メタノン(BCD-CDK8-3-9)
N-(メチルスルホニル)-4-(3-(ピペリジン-1-カルボニル)-1,7-ナフチリジン-5-イル)ベンズアミド(BCD-CDK8-3-11)
N,N-ジメチル-1-(5-(4-((メチルスルホニル)カルバモイル)フェニル)-1,7-ナフチリジン-3-イル)アゼチジン-3-カルボキサミド(BCD-CDK8-3-12)
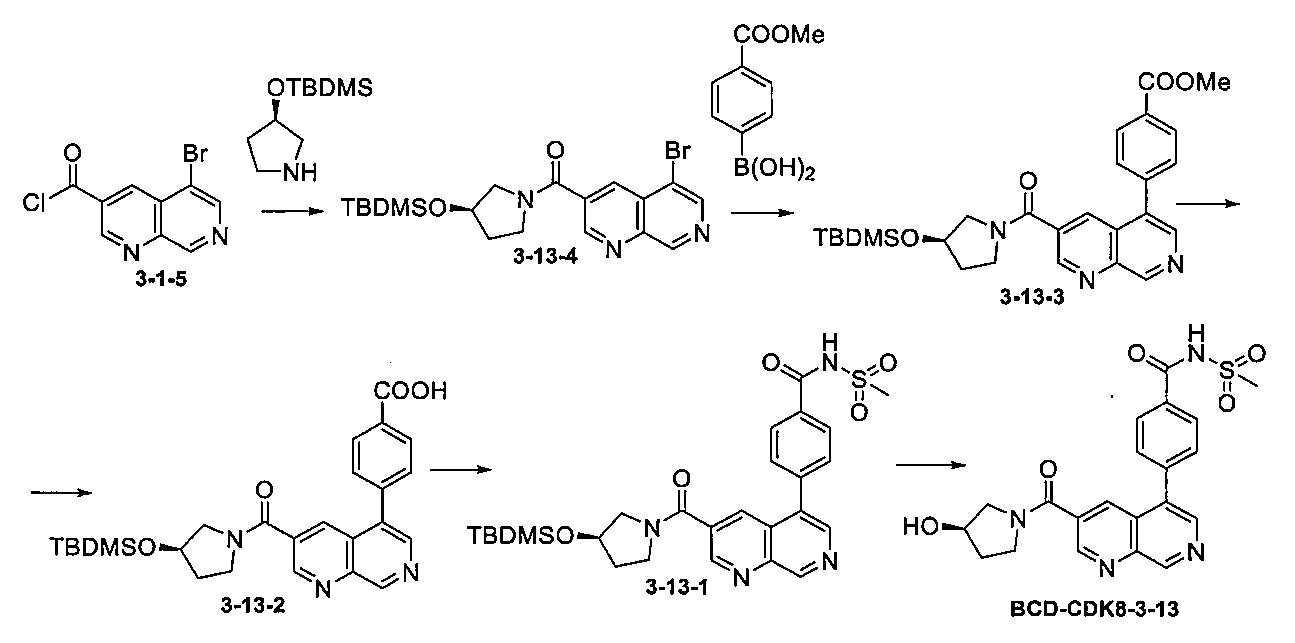
(R)-4-(3-(3-ヒドロキシピロリジン-1-カルボニル)-1,7-ナフチリジン-5-イル)-N-(メチルスルホニル)ベンズアミド(BCD-CDK8-3-13)
アゼチジン-1-イル(5-(4-(1-メチル-1H-ピラゾール-4-イル)フェニル)-1,7-ナフチリジン-3-イル)メタノン(BCD-CDK8-3-14)
(3-メトキシアゼチジン-1-イル)(5-(4-(1-メチル-1H-ピラゾール-4-イル)フェニル)-1,7-ナフチリジン-3-イル)メタノン(BCD-CDK8-3-15)
(5-(4-(1-メチル-1H-ピラゾール-4-イル)フェニル)-1,7-ナフチリジン-3-イル)(ピロリジン-1-イル)メタノン(BCD-CDK8-3-16)
1-(5-(4-(1-メチル-1H-ピラゾール-4-イル)フェニル)-1,7-ナフチリジン-3-イル)ピロリジン-2-オン(BCD-CDK8-3-17)
N-(2-メトキシエチル)-5-(4-(1-メチル-1H-ピラゾール-4-イル)フェニル)-1,7-ナフチリジン-3-カルボキサミド(BCD-CDK8-3-18)
(R)-(3-メトキシピロリジン-1-イル)(5-(4-(1-メチル-1H-ピラゾール-4-イル)フェニル)-1,7-ナフチリジン-3-イル)メタノン(BCD-CDK8-3-19)
(R)-3-(ヒドロキシピペリジン-1-イル)(5-(4-(1-メチル-1H-ピラゾール-4-イル)フェニル)-1,7-ナフチリジン-3-イル)メタノン(BCD-CDK8-3-20)
(R)-(3-メトキシピペリジン-1-イル)(5-(4-(1-メチル-1H-ピラゾール-4-イル)フェニル)-1,7-ナフチリジン-3-イル)メタノン(BCD-CDK8-3-21)
N,N-メチル-5-(4-(1-メチル-1H-ピラゾール-4-イル)フェニル)-1,7-ナフチリジン-3-カルボキサミド(BCD-CDK8-3-22)
N,N-ジエチル-5-(4-(1-メチル-1H-ピラゾール-4-イル)フェニル)-1,7-ナフチリジン-3-カルボキサミド(BCD-CDK8-3-23)
8-アミノ-N-(2-メトキシエチル)-5-(4-(1-メチル-1H-ピラゾール-4-イル)フェニル)-1,7-ナフチリジン-3-カルボキサミド(BCD-CDK8-3-24)
N-(2-メトキシエチル)-N-メチル-5-(4-(1-メチル-1H-ピラゾール-4-イル)フェニル)-1,7-ナフチリジン-3-カルボキサミド(BCD-CDK8-3-25)
(8-アミノ-5-(4-(1-メチル-1H-ピラゾール-4-イル)フェニル)-1,7-ナフチリジン-3-イル)(アゼチジン-1-イル)メタノン(BCD-CDK8-3-26)
(8-アミノ-5-(4-(1-メチル-1H-ピラゾール-4-イル)フェニル)-1,7-ナフチリジン-3-イル)(モルホリノ)メタノン(BCD-CDK8-3-27)
2-メトキシエチル-5-[4-(1-メチル-1H-ピラゾール-4-イル)フェニル]-1,7-ナフチリジン-3-カルボキシレート(BCD-CDK8-3-28)
2-メトキシエチル-8-アミノ-5-(4-(1-メチル-1H-ピラゾール-4-イル)フェニル)-1,7-ナフチリジン-3-カルボキシレート(BCD-CDK8-3-29)
(4-メチルピペラジン-1-イル)(5-(4-(1-メチル-1H-ピラゾール-4-イル)フェニル)-1,7-ナフチリジン-3-イル)メタノン(BCD-CDK8-3-30)
(8-アミノ-5-(4-(1-メチル-1H-ピラゾール-4-イル)フェニル)-1,7-ナフチリジン-3-イル)(4-メチルピペラジン-1-イル)メタノン(BCD-CDK8-3-31)
8-アミノ-N-(2-メトキシエチル)-N-メチル-5-(4-(1-メチル-1H-ピラゾール-4-イル)フェニル)-1,7-ナフチリジン-3-カルボキサミド(BCD-CDK8-3-32)
(5-(4-(1-メチル-1H-ピラゾール-4-イル)フェニル)-1,7-ナフチリジン-3-イル)(モルホリノ)メタノン(BCD-CDK8-3-33)
(8-アミノ-5-(4-(1-メチル-1H-ピラゾール-4-イル)フェニル)-1,7-ナフチリジン-3-イル)(3-メトキシアゼチジン-1-イル)メタノン(BCD-CDK8-3-34)
N-(2-(ジメチルアミノ)エチル)-N-メチル-5-(4-(1-メチル-1H-ピラゾール-4-イル)フェニル)-1,7-ナフチリジン-3-カルボキサミド(BCD-CDK8-3-35)
N-シクロプロピル-5-(4-(1-メチル-1H-ピラゾール-4-イル)フェニル)-1,7-ナフチリジン-3-カルボキサミド(BCD-CDK8-3-37)
8-アミノ-N-シクロプロピル-5-(4-(1-メチル-1H-ピラゾール-4-イル)フェニル)-1,7-ナフチリジン-3-カルボキサミド(BCD-CDK8-3-38)
N-(シクロプロピルメチル)-5-(4-(1-メチル-1H-ピラゾール-4-イル)フェニル)-1,7-ナフチリジン-3-カルボキサミド(BCD-CDK8-3-39)
8-アミノ-N-(シクロプロピルメチル)-5-(4-(1-メチル-1H-ピラゾール-4-イル)フェニル)-1,7-ナフチリジン-3-カルボキサミド(BCD-CDK8-3-40)
5-(4-(1H-イミダゾール-1-イル)フェニル)-N-(2-メトキシエチル)-1,7-ナフチリジン-3-イル)カルボキサミド(BCD-CDK8-3-41)
8-アミノ-N-(2-ヒドロキシエチル)-5-(4-(1-メチル-1H-ピラゾール-4-イル)フェニル)-1,7-ナフチリジン-3-カルボキサミド(BCD-CDK8-3-42)
(5-(4-(ジメチルアミノ)-3-ヒドロキシフェニル)-1H-ピロロ[2,3-b]ピリジン-3-イル)(ピリジン-2-イル)メタノン(BCD-CDK8-4-1)
5-(ジメチルアミノ)-2-(3-ピコリノイル-1H-ピロロ[2,3-b]ピリジン-5-イル)ベンズアミド(BCD-CDK8-4-2)
(5-(3-ヒドロキシ-4-モルホリノフェニル)-1H-ピロロ[2,3-b]ピリジン-3-イル)(ピリジン-2-イル)メタノン(BCD-CDK8-4-3)
5-メトキシ-2-(3-ピコリノイル-1H-ピロロ[2,3-b]ピリジン-5-イル)ベンズアミド(BCD-CDK8-4-4)
5-(4-(ジメチルアミノ)-3-ヒドロキシフェニル)-1H-ピロロ[2,3-b]ピリジン-3-イル)(ピリジン-3-イル)メタノン(BCD-CDK8-4-5)
5-(ジメチルアミノ)-2-(3-ニコチノイル-1H-ピロロ[2,3-b]ピリジン-5-イル)ベンズアミド(BCD-CDK8-4-6)
(5-(3-ヒドロキシ-4-モルホリノフェニル)-1H-ピロロ[2,3-b]ピリジン-3-イル)(ピリジン-3-イル)メタノン(BCD-CDK8-4-7)
5-メトキシ-2-(3-ニコチノイル-1H-ピロロ[2,3-b]ピリジン-5-イル)ベンズアミド(BCD-CDK8-4-8)
(5-(4-(ジメチルアミノ)-3-ヒドロキシフェニル)-1H-ピロロ[2,3-b]ピリジン-3-イル)(ピリジン-4-イル)メタノン(BCD-CDK8-4-9)
5-(ジメチルアミノ)-2-(3-イソニコチノイル-1H-ピロロ[2,3-b]ピリジン-5-イル)ベンズアミド(BCD-CDK8-4-10)
(5-(3-ヒドロキシ-4-モルホリノフェニル)-1H-ピロロ[2,3-b]ピリジン-3-イル)(ピリジン-4-イル)メタノン(BCD-CDK8-4-11)
2-(3-イソニコチノイル-1H-ピロロ[2,3-b]ピリジン-5-イル)-5-メトキシベンズアミド(BCD-CDK8-4-12)
5-メトキシ-2-(3-(3-メトキシベンゾイル)-1H-ピロロ[2,3-b]ピリジン-5-イル)ベンズアミド(BCD-CDK8-4-13)
(5-(4-(ジメチルアミノ)-3-メトキシフェニル)-1H-ピロロ[2,3-b]ピリジン-3-イル)(ピリジン-2-イル)メタノン(BCD-CDK8-4-21)
5-(ジメチルアミノ)-2-(3-ピコリノイル-1H-ピロロ[2,3-b]ピリジン-5-イル)ベンゾニトリル(BCD-CDK8-4-22)
(5-(3-メトキシ-4-モルホリノフェニル)-1H-ピロロ[2,3-b]ピリジン-3-イル)(ピリジン-2-イル)メタノン(BCD-CDK8-4-23)
5-メトキシ-2-(3-ピコリノイル-1H-ピロロ[2,3-b]ピリジン-5-イル)ベンゾニトリル(BCD-CDK8-4-24)
(5-(4-(ジメチルアミノ)-3-メトキシフェニル)-1H-ピロロ[2,3-b]ピリジン-3-イル)(ピリジン-3-イル)メタノン(BCD-CDK8-4-25)
5-(ジメチルアミノ)-2-(3-ニコチノイル-1H-ピロロ[2,3-b]ピリジン-5-イル)ベンゾニトリル(BCD-CDK8-4-26)
(5-(3-メトキシ-4-モルホリノフェニル)-1H-ピロロ[2,3-b]ピリジン-3-イル)(ピリジン-3-イル)メタノン(BCD-CDK8-4-27)
5-メトキシ-2-(3-ニコチノイル-1H-ピロロ[2,3-b]ピリジン-5-イル)ベンゾニトリル(BCD-CDK8-4-28)
(5-(4-(ジメチルアミノ)-3-メトキシフェニル)-1H-ピロロ[2,3-b]ピリジン-3-イル)(ピリジン-2-イル)メタノン(BCD-CDK8-4-29)
5-(ジメチルアミノ)-2-(3-イソニコチノイル-1H-ピロロ[2,3-b]ピリジン-5-イル)ベンゾニトリル(BCD-CDK8-4-30)
(5-(3-メトキシ-4-モルホリノフェニル)-1H-ピロロ[2,3-b]ピリジン-3-イル)(ピリジン-4-イル)メタノン(BCD-CDK8-4-31)
2-(3-イソニコチノイル-1H-ピロロ[2,3-b]ピリジン-5-イル)-5-メトキシベンゾニトリル(BCD-CDK8-4-32)
(5-(4-メトキシフェニル)-1H-ピロロ[2,3-b]ピリジン-3-イル)(ピリジン-4-イル)メタノン(BCD-CDK8-4-33)
(5-(4-(ジメチルアミノ)フェニル)-1H-ピロロ[2,3-b]ピリジン-3-イル)(3-メトキシフェニル)メタノン(BCD-CDK8-4-34)
5-メトキシ-2-(3-(3-メトキシベンゾイル)-1H-ピロロ[2,3-b]ピリジン-5-イル)ベンゾニトリル(BCD-CDK8-4-35)
(5-(4-モルホリノフェニル)-1H-ピロロ[2,3-b]ピリジン-3-イル)(ピリジン-2-イル)メタノン(BCD-CDK8-4-36)
(5-(4-モルホリノフェニル)-1H-ピロロ[2,3-b]ピリジン-3-イル)(ピリジン-3-イル)メタノン(BCD-CDK8-4-37)
(5-(4-モルホリノフェニル)-1H-ピロロ[2,3-b]ピリジン-3-イル)(ピリジン-4-イル)メタノン(BCD-CDK8-4-38)
(5-(4-(ジメチルアミノ)フェニル)-1H-ピロロ[2,3-b]ピリジン-3-イル)(ピリジン-3-イル)メタノン(BCD-CDK8-4-39)
(5-(4-(ジメチルアミノ)フェニル)-1H-ピロロ[2,3-b]ピリジン-3-イル)(ピリジン-4-イル)メタノン(BCD-CDK8-4-40)
N-(メチルスルホニル)-4-(4-(ピペリジン-1-カルボニル)キノリン-6-イル)ベンズアミド(BCD-CDK8-5-1)
4-(4-(ピペリジン-1-カルボニル)-2-クロロキノリン-6-イル)-N-(メチルスルホニル)ベンズアミド(BCD-CDK8-5-1Cl)
(R)-1-((6-(4-(ジメチルアミノ)フェニル)キノリン-4-イル)(イミノ)メチル)ピロリジン-3-オール(BCD-CDK8-5-2i)
(R)-(6-(4-(ジメチルアミノ)フェニル)キノリン-4-イル)(3-ヒドロキシピロリジン-1-イル)メタノン(BCD-CDK8-5-2)
モルホリノ(6-(4-モルホリノフェニル)キノリン-4-イル)メタンイミン(BCD-CDK8-5-3i)
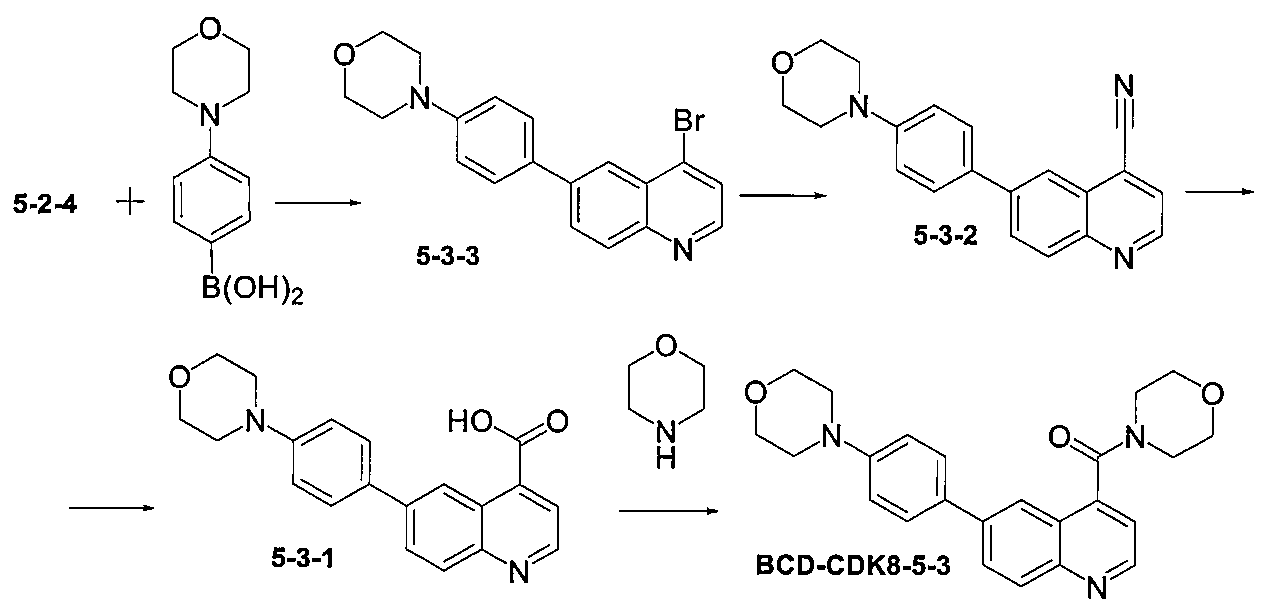
モルホリノ(6-(4-モルホリノフェニル)キノリン-4-イル)メタノン(BCD-CDK8-5-3)
(6-(4-(1H-ピラゾール-4-イル)フェニル)キノリン-4-イル)(ピペリジン-1-イル)メタンイミン(BCD-CDK8-5-4i)
(6-(4-(1H-ピラゾール-4-イル)フェニル)キノリン-4-イル)(ピペリジン-1-イル)メタノン(BCD-CDK8-5-4)
4-(4-(アゼチジン-1-カルボニル)キノリン-6-イル)-N-(メチルスルホニル)ベンズアミド(BCD-CDK8-5-5)
4-(4-(アゼチジン-1-カルボニル)-2-クロロキノリン-6-イル)-N-(メチルスルホニル)ベンズアミド(BCD-CDK8-5-5Cl)
1-(6-(4-メトキシフェニル)キノリン-4-イル)ピロリジン-2-オン(BCD-CDK8-5-6)
(S)-1-((6-(4-(ジメチルアミノ)フェニル)キノリン-4-イル)(イミノ)メチル)ピロリジン-3-オール(BCD-CDK8-5-7i)
(S)-(6-(4-(ジメチルアミノ)フェニル)キノリン-4-イル)(3-ヒドロキシピロリジン-1-イル)メタノン(BCD-CDK8-5-7)
(6-(4-(1-メチル-1H-ピラゾール-4-イル)フェニル)キノリン-4-イル)(ピペリジン-1-イル)メタンイミン(BCD-CDK8-5-8i)
(6-(4-(1-メチル-1H-ピラゾール-4-イル)フェニル)キノリン-4-イル)(ピペリジン-1-イル)メタノン(BCD-CDK8-5-8)
1-(4-(4-モルホリノフェニル)キノリン-6-イル)ピペリジン-4-カルボキサミド(BCD-CDK8-6-1)
(S)-4-(6-(3-ヒドロキシピロリジン-1-カルボニル)キノリン-4-イル)-N-(メチルスルホニル)ベンズアミド(BCD-CDK8-6-2)
4-メチル-1-(4-(4-((4-メチルピペラジン-1-イル)メチル)フェニル)キノリン-6-イル)ピペリジン-4-カルボキサミド(BCD-CDK8-6-3)
(4-(4-(1H-ピラゾール-4-イル)フェニル)キノリン-6-イル)(3-メトキシアゼチジン-1-イル)メタノン(BCD-CDK8-6-4)
4-(6-(アゼチジン-1-カルボニル)キノリン-4-イル)-N-(メチルスルホニル)ベンズアミド(BCD-CDK8-6-5)
N-(メチルスルホニル)-4-(6-(モルホリン-4-カルボニル)キノリン-4-イル)ベンズアミド(BCD-CDK8-6-6)
1-(4-(4-((4-メチルピペラジン-1-イル)メチル)フェニル)キノリン-6-イル)ピペリジン-4-カルボキサミド(BCD-CDK8-6-7)
4-メチル-1-(4-(4-モルホリノフェニル)キノリン-6-イル)ピペリジン-4-カルボキサミド(BCD-CDK8-6-8)
(R)-4-(6-(3-ヒドロキシピロリジン-1-カルボニル)キノリン-4-イル)-N-(メチルスルホニル)ベンズアミド(BCD-CDK8-6-9)
(3-メトキシアゼチジン-1-イル)(4-(4-(1-メチル-1H-ピラゾール-4-イル)フェニル)キノリン-6-イル)メタノン(BCD-CDK8-6-10)
アゼチジン-1-イル(4-(4-(1-メチル-1H-ピラゾール-4-イル)フェニル)キノリン-6-イル)メタノン(BCD-CDK8-6-11)
(4-(4-(1-メチル-1H-ピラゾール-4-イル)フェニル)キノリン-6-イル)(ピロリジン-1-イル)メタノン(BCD-CDK8-6-12)
1-(4-(4-(1-メチル-1H-ピラゾール-4-イル)フェニル)キノリン-6-イル)ピロリジン-2-オン(BCD-CDK8-6-13)
N-(2-メトキシエチル)-4-(4-(1-メチル-1H-ピラゾール-4-イル)フェニル)キノリン-6-カルボキサミド(BCD-CDK8-6-14)
である、態様1から2のいずれか一項に記載の化合物。
[態様10]
サイクリン依存性タンパク質キナーゼCDK8/19を、態様1から9のいずれかに記載の化合物と接触させるステップを含む、対象においてサイクリン依存性タンパク質キナーゼCDK8/19の生物活性を阻害するための方法。
[態様11]
治療有効量の態様1から9のいずれかに記載の化合物または薬学的に許容されるその塩と、薬学的に許容される1種または複数の賦形剤とを含む医薬組成物であって、サイクリン依存性タンパク質キナーゼCDK8/19の活性化が介在する疾患または障害を予防または処置するための、前記医薬組成物。
[態様12]
サイクリン依存性タンパク質キナーゼCDK8/19の活性化が介在する疾患または障害が、腫瘍性または血液腫瘍性である、サイクリン依存性タンパク質キナーゼCDK8/19の活性化が介在する疾患または障害を予防または処置するための、態様11に記載の医薬組成物。
[態様13]
腫瘍性または血液腫瘍性疾患が、結腸直腸がん、黒色腫、転移性黒色腫、乳がん、三種陰性乳がん(TNBC)、前立腺がん、転移性卵巣がん、転移性胃がん、白血症、急性骨髄性白血病、膵臓がんを含む群から選択される、態様12に記載の医薬組成物。
[態様14]
サイクリン依存性タンパク質キナーゼCDK8/19の活性化が介在する疾患または障害を処置するための方法であって、それを必要とする対象において、治療有効量の態様1から9のいずれかに記載の化合物もしくは薬学的に許容されるその塩、または態様11に記載の医薬組成物を投与するステップを含む方法。
[態様15]
サイクリン依存性タンパク質キナーゼCDK8/19の活性化が介在する疾患または障害が、腫瘍性または血液腫瘍性疾患である、態様14に記載の処置するための方法。
[態様16]
腫瘍性または血液腫瘍性疾患が、結腸直腸がん、黒色腫、転移性黒色腫、乳がん、三種陰性乳がん(TNBC)、前立腺がん、転移性卵巣がん、転移性胃がん、白血症、急性骨髄性白血病、膵臓がんを含む群から選択される、態様15に記載の処置するための方法。
[態様17]
それを必要とする対象において、サイクリン依存性タンパク質キナーゼCDK8/19の活性化が介在する疾患または障害を処置するための、態様1から9のいずれかに記載の化合物もしくは薬学的に許容されるその塩、または態様11に記載の医薬組成物の使用。
[態様18]
サイクリン依存性タンパク質キナーゼCDK8/19の活性化が介在する疾患または障害が、腫瘍性または血液腫瘍性疾患を含む、態様17に記載の使用。
[態様19]
腫瘍性および血液腫瘍性疾患が、結腸直腸がん、黒色腫、転移性黒色腫、乳がん、三種陰性乳がん(TNBC)、前立腺がん、転移性卵巣がん、転移性胃がん、白血症、急性骨髄性白血病、膵臓がんを含む群から選択される、態様18に記載の使用。
化合物BCD-CDK8-1-6eの調製方法
tert-ブチル-3-(フェニルカルバモイル)アゼチジン-1-カルボキシレート(500mg、1.81mmol)(WO2000/071518に記載のとおりに調製したもの)の5mLのジクロロメタン溶液に、トリフルオロ酢酸(0.70mL、7.5mmol)を加えた。混合物を12時間撹拌し、次いで、減圧蒸留によって溶媒を蒸発させた。残渣を減圧ロータリーエバポレーターによって45℃で乾燥させ、さらに精製することなく次のステップで使用した。
BCD-CDK8-1-6aの調製方法
BCD-CDK8-1-1の調製方法
化合物BCD-CDK8-1-6の調製方法
化合物BCD-CDK8-1-2の調製方法
化合物BCD-CDK8-1-2を、化合物BCD-CDK8-1-6aの代わりに1-2-1を使用しながら、化合物BCD-CDK8-1-1(実施例3)と似たようにして調製した。
化合物BCD-CDK8-1-3の調製方法
ステップ4. 1-3-3(650mg、2.58mmol)、1-3-4(746mg、2.58mmol)、およびDIPEA(0.675mL、3.87mmol)の20mLのDMSO溶液を、90℃で30時間加熱した。反応混合物を100mLの水中に注いだ。懸濁液を濾過し、沈殿を水で洗浄し、酢酸エチルに溶解させ、0.1M HCl溶液で洗浄した。有機相を減圧下で濃縮した。ヘキサン-酢酸エチル(2:1)を溶離液として使用するシリカゲルでのカラムクロマトグラフィーによって、生成物1-3-2を橙色の粉末として単離した。収率:712mg(53%)。
1-3-1(338mg、0.676mmol)およびフッ化テトラブチルアンモニウム(3.38mL、3.38mmol、THF中1M)の10mLのTHF溶液を、70℃で14時間撹拌した。反応混合物を減圧下で濃縮し、残渣を酢酸エチルに溶解させ、水で洗浄し、濃縮した。ジクロロメタン-酢酸エチル-メタノール(20:5:1)を溶離液として使用するシリカゲルでのカラムクロマトグラフィーによって、生成物を無色の粉末として単離した。収率:132mg(56%)。
化合物BCD-CDK8-1-16の調製方法
化合物BCD-CDK8-1-4の調製方法
化合物BCD-CDK8-1-17の調製方法
化合物BCD-CDK8-1-5の調製方法
ステップ2. 化合物1-5-1を、化合物1-1-1の代わりに化合物1-5-2を使用しながら、化合物BCD-CDK8-1-6e(実施例1、ステップ4)と似たようにして調製した。
化合物BCD-CDK8-1-18の調製方法
化合物BCD-CDK8-1-9の調製方法
化合物BCD-CDK8-1-10の調製方法
化合物BCD-CDK8-1-11の調製方法
化合物BCD-CDK8-1-12の調製方法
化合物BCD-CDK8-1-7eの調製方法
実施例17
化合物BCD-CDK8-1-7aの調製方法
化合物BCD-CDK8-1-7の調製方法
化合物BCD-CDK8-1-8の調製方法
化合物BCD-CDK8-1-19の調製方法
化合物BCD-CDK8-1-13の調製方法
化合物BCD-CDK8-1-14の調製方法
化合物BCD-CDK8-1-20の調製方法
化合物BCD-CDK8-1-15eの調製方法
化合物BCD-CDK8-1-15aの調製方法
化合物BCD-CDK8-1-15の調製方法
化合物BCD-CDK8-1-21aの調製方法
化合物BCD-CDK8-1-21の調製方法
化合物BCD-CDK8-5-2の調製方法
化合物BCD-CDK8-5-2iの調製方法
化合物BCD-CDK8-5-3の調製方法
化合物BCD-CDK8-5-3iの調製方法
化合物BCD-CDK8-5-4の調製方法
化合物BCD-CDK8-5-4iの調製方法
化合物BCD-CDK8-5-6の調製方法
化合物BCD-CDK8-5-7の調製方法
化合物BCD-CDK8-5-7iの調製方法
化合物BCD-CDK8-5-8の調製方法
化合物BCD-CDK8-5-8iの調製方法
化合物BCD-CDK8-5-1Clの調製方法
化合物BCD-CDK8-5-1の調製方法
化合物BCD-CDK8-5-5Clの調製方法
ステップ2. 化合物5-5Cl-1を、化合物BCD-CDK8-1-6eの代わりに化合物5-5Cl-2を使用しながら、化合物BCD-CDK8-1-6a(実施例2)と似たようにして調製した。
化合物BCD-CDK8-5-5の調製方法
化合物BCD-CDK8-6-1の調製方法
化合物BCD-CDK8-6-2の調製方法
化合物BCD-CDK8-6-3の調製方法
化合物BCD-CDK8-6-4の調製方法
化合物BCD-CDK8-6-5の調製方法
化合物BCD-CDK8-6-6の調製方法
化合物BCD-CDK8-6-7の調製方法
化合物BCD-CDK8-6-8の調製方法
化合物BCD-CDK8-6-9の調製方法
化合物BCD-CDK8-6-10の調製方法
化合物BCD-CDK8-6-11の調製方法
化合物BCD-CDK8-6-12の調製方法
化合物BCD-CDK8-6-13の調製方法
化合物BCD-CDK8-6-14の調製方法
化合物BCD-CDK8-3-1の調製方法
化合物BCD-CDK8-3-13の調製方法
ステップ3. 化合物3-13-2を、3-1-3の代わりに3-13-3を使用しながら、化合物3-1-2(実施例58、ステップ4)と似たようにして調製した。
ステップ5: 化合物BCD-CDK8-3-13を、3-1-1の代わりに3-13-1を使用しながら、BCD-CDK8-3-1(実施例58、ステップ6)と似たようにして調製した。
化合物BCD-CDK8-3-2の調製方法
ステップ3. 化合物BCD-CDK8-3-2を、5-4-1の代わりに3-2-1を使用しながら、BCD-CDK8-5-4(実施例33、ステップ6)と似たようにして調製した。
化合物BCD-CDK8-3-3の調製方法
化合物BCD-CDK8-3-4の調製方法
化合物BCD-CDK8-3-5の調製方法
化合物BCD-CDK8-3-6の調製方法
化合物BCD-CDK8-3-8の調製方法
化合物BCD-CDK8-3-9の調製方法
5-ブロモ-1,7-ナフチリジン-3-カルボン酸(2.22g、8.78mmol)(WO2015/014768に記載のとおりに調製したもの)、DPPA(2.27mL、10.5mmol)、トリエチルアミン(1.47mL、10.5mmol)を無水tert-ブタノール(50mL)に懸濁させた。混合物を8時間還流させた。反応混合物を減圧下で濃縮し、残渣を50mLの酢酸エチルに溶解させ、水(2×40mL)、飽和NaHCO3溶液(50mL)、および飽和NaCl溶液(50mL)で洗浄した。有機層をNa2SO4で乾燥させた。ジクロロメタン-メタノール(96:4)を溶離液として使用するシリカゲルでのカラムクロマトグラフィーによって、生成物3-9-4を淡黄色の粉末として単離した。収率:1.64g(58%)。
化合物BCD-CDK8-3-11の調製方法
ステップ3. 化合物3-11-1を、化合物3-1-3の代わりに3-11-2を使用しながら、化合物3-1-2(実施例58、ステップ4)と似たようにして調製した。
化合物BCD-CDK8-3-12の調製方法
ステップ3. 化合物3-12-3を、化合物3-9-2の代わりに化合物3-12-4を使用しながら、化合物3-9-1(実施例66、ステップ4)と似たようにして調製した。
化合物BCD-CDK8-3-14の調製方法
ステップ3. 化合物BCD-CDK8-3-14を、3-フルオロ-4-ニトロ安息香酸の代わりに化合物3-14-1を使用しながら、化合物1-2-4(実施例5、ステップ1)と似たようにして調製した。
化合物BCD-CDK8-3-15の調製方法
化合物BCD-CDK8-3-16の調製方法
化合物BCD-CDK8-3-17の調製方法
化合物BCD-CDK8-3-18の調製方法
化合物BCD-CDK8-4-24の調製方法
化合物BCD-CDK8-4-4の調製方法
化合物BCD-CDK8-4-28の調製方法
化合物BCD-CDK8-4-8の調製方法
化合物BCD-CDK8-4-32の調製方法
化合物BCD-CDK8-4-12の調製方法
化合物BCD-CDK8-4-21の調製方法
化合物BCD-CDK8-4-1の調製方法
化合物BCD-CDK8-4-25の調製方法
化合物BCD-CDK8-4-5の調製方法
化合物BCD-CDK8-4-29の調製方法
化合物BCD-CDK8-4-9の調製方法
化合物BCD-CDK8-4-22の調製方法
化合物BCD-CDK8-4-2の調製方法
化合物BCD-CDK8-4-26の調製方法
化合物BCD-CDK8-4-6の調製方法
化合物BCD-CDK8-4-30の調製方法
化合物BCD-CDK8-4-10の調製方法
化合物BCD-CDK8-4-23の調製方法
化合物BCD-CDK8-4-3の調製方法
化合物BCD-CDK8-4-27の調製方法
化合物BCD-CDK8-4-7の調製方法
化合物BCD-CDK8-4-31の調製方法
化合物BCD-CDK8-4-11の調製方法
化合物BCD-CDK8-4-35の調製方法
化合物BCD-CDK8-4-13の調製方法
化合物BCD-CDK8-4-33の調製方法
化合物BCD-CDK8-4-34の調製方法
化合物BCD-CDK8-4-36の調製方法
化合物BCD-CDK8-4-37の調製方法
化合物BCD-CDK8-4-38の調製方法
化合物BCD-CDK8-4-39の調製方法
化合物BCD-CDK8-4-40の調製方法
ステップ2. 化合物BCD-CDK8-4-40を、化合物4-24-1の代わりに4-40-1を使用しながら、化合物BCD-CDK8-4-24(実施例74、ステップ4)と似たようにして調製した。
化合物BCD-CDK8-3-19の調製方法
化合物BCD-CDK8-3-20の調製方法
化合物BCD-CDK8-3-21の調製方法
化合物BCD-CDK8-3-22の調製方法
化合物BCD-CDK8-3-23の調製方法
化合物BCD-CDK8-3-24の調製方法
化合物BCD-CDK8-3-25の調製方法
化合物BCD-CDK8-3-26の調製方法
化合物BCD-CDK8-3-33の調製方法
化合物BCD-CDK8-3-27の調製方法
化合物BCD-CDK8-3-28の調製方法
化合物BCD-CDK8-3-29の調製方法
化合物BCD-CDK8-3-30の調製方法
化合物BCD-CDK8-3-31の調製方法
化合物BCD-CDK8-3-32の調製方法
化合物BCD-CDK8-3-34の調製方法
化合物BCD-CDK8-3-35の調製方法
化合物BCD-CDK8-3-37の調製方法
化合物BCD-CDK8-3-38の調製方法
化合物BCD-CDK8-3-39の調製方法
化合物BCD-CDK8-3-40の調製方法
化合物BCD-CDK8-3-42の調製方法
化合物BCD-CDK8-3-41の調製方法
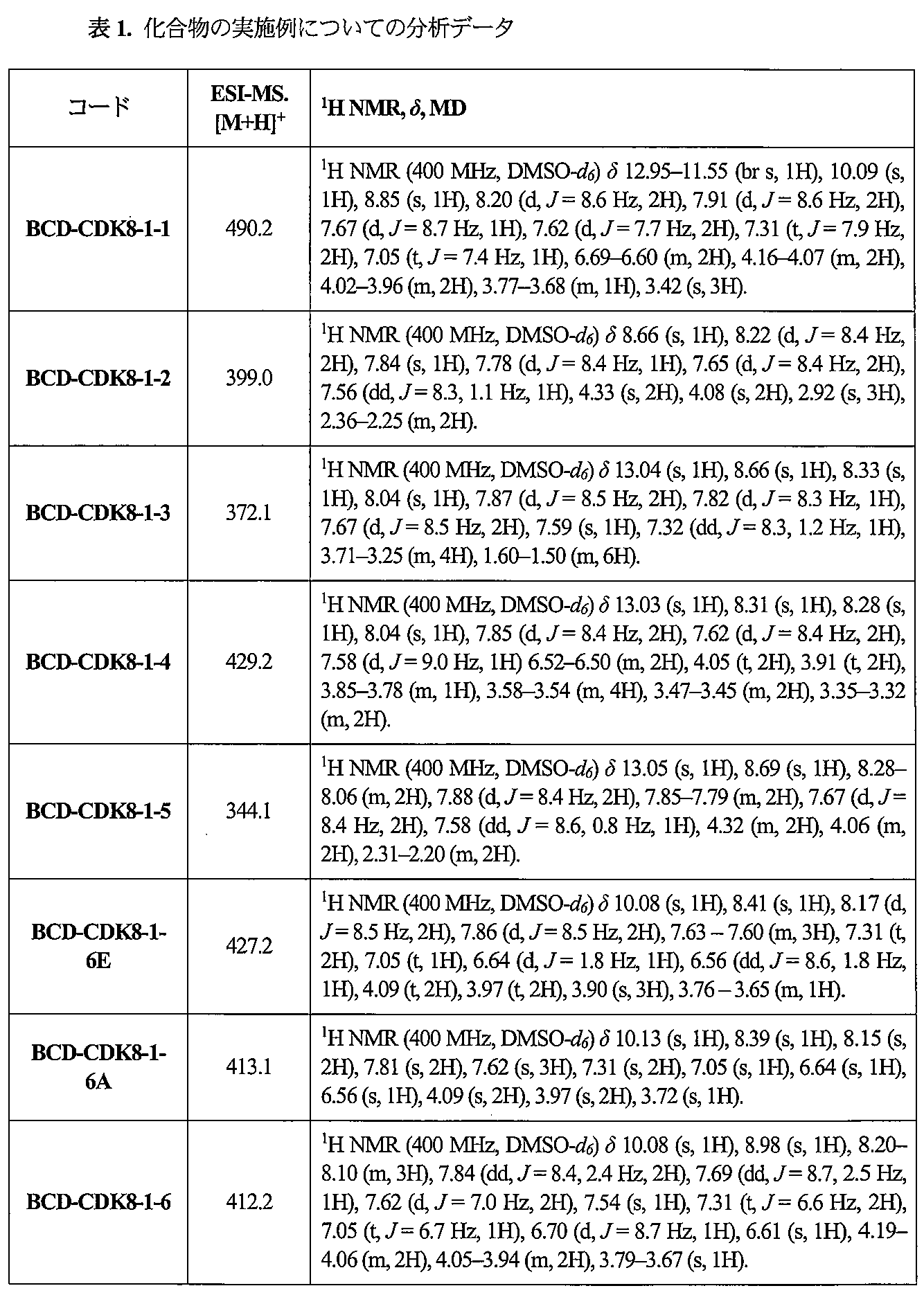
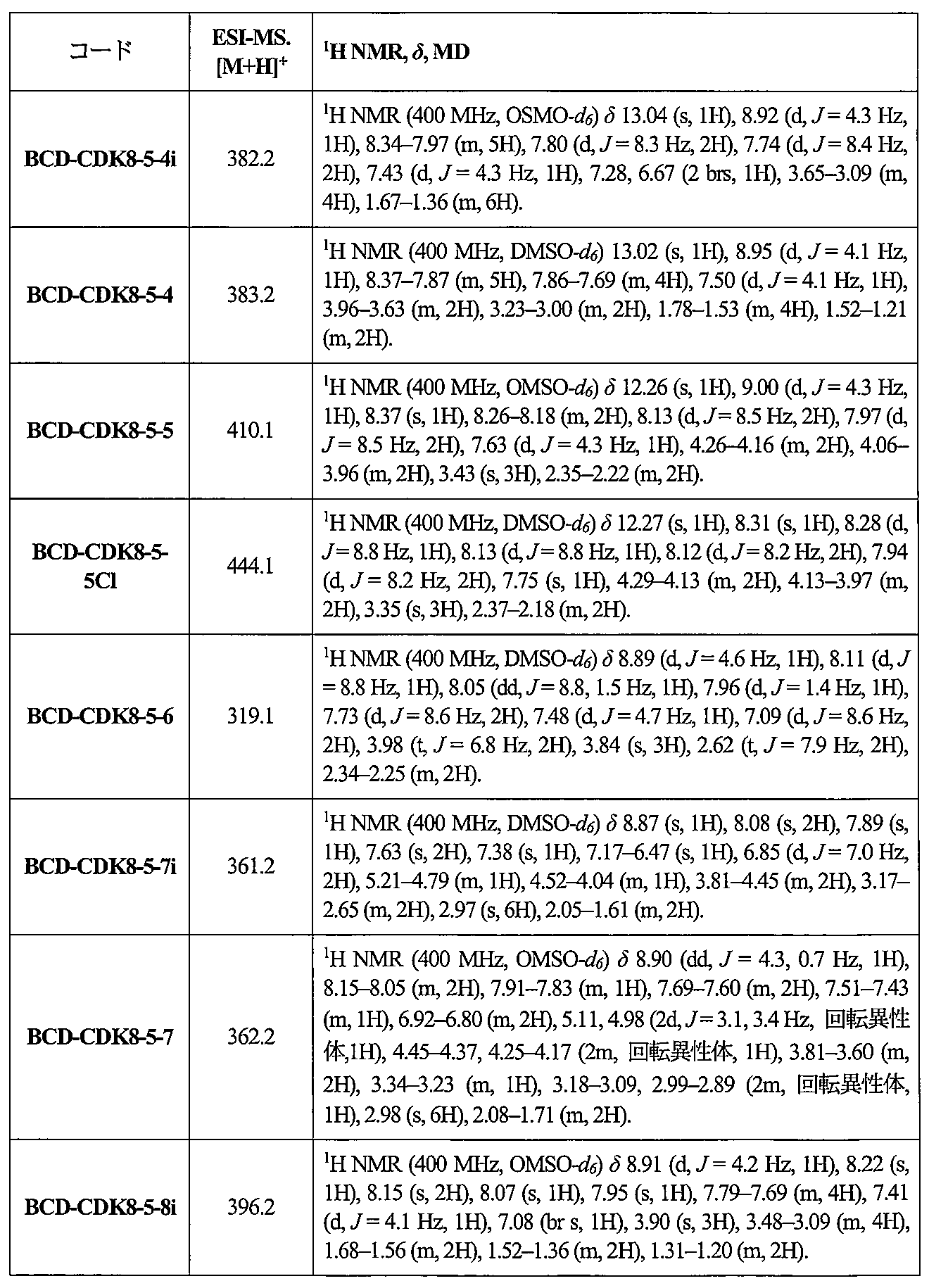
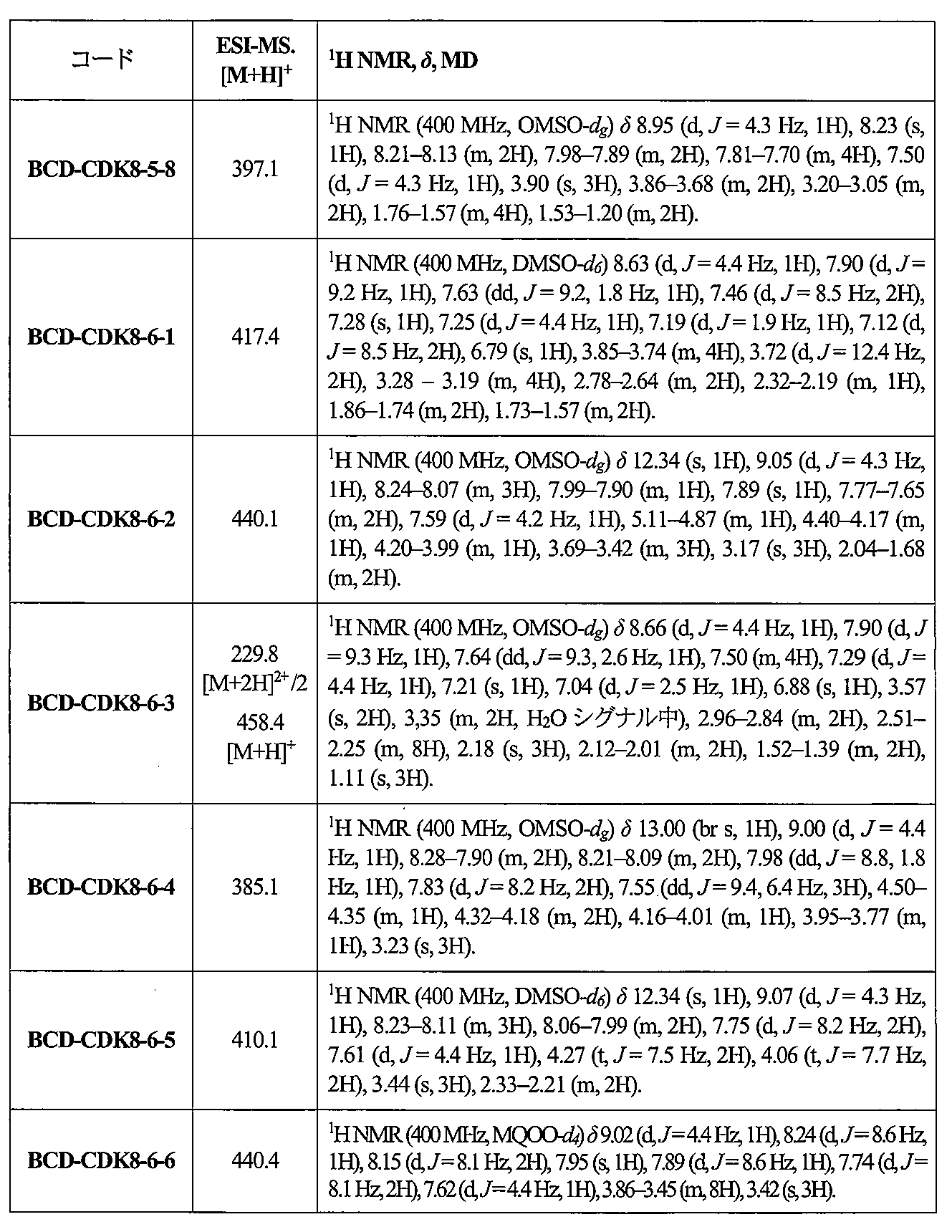
調製された化合物の分析
調製された化合物の純度および構造を、液体クロマトグラフィー-質量分析(LC-MS)および1H NMR分光測定によって確認した(表1)。
液体クロマトグラフィー-質量分析
化学的安定性の判定
模擬胃液およびヒト血漿において本明細書に記載の化合物の化学的安定性を明らかにした。
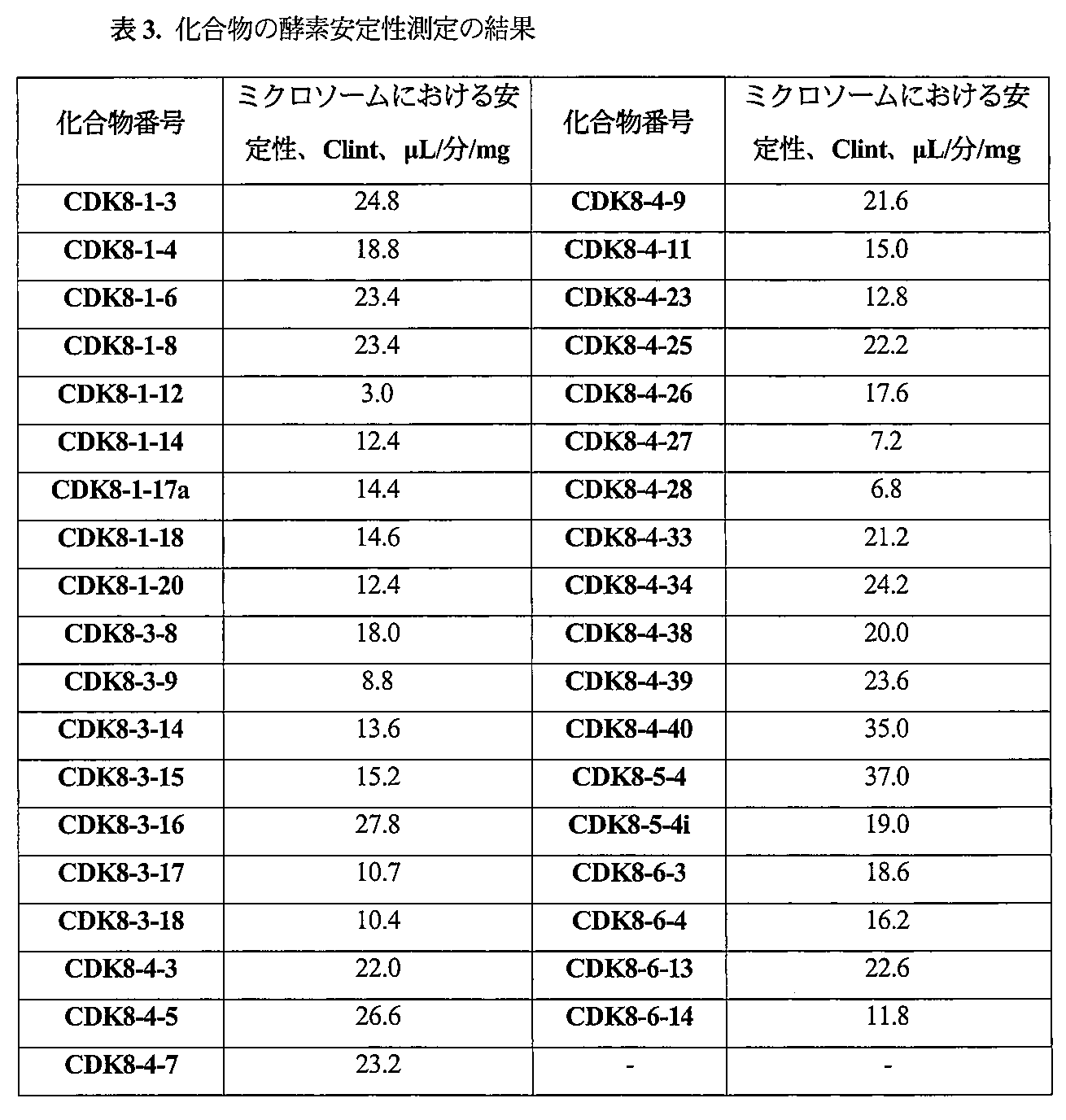
ヒト肝臓ミクロソームにおける酵素安定性の測定
候補物質の酵素安定性を測定することで、肝臓ミクロソームにおける酵素の作用に対する本化合物の安定性を推定することが可能になった。
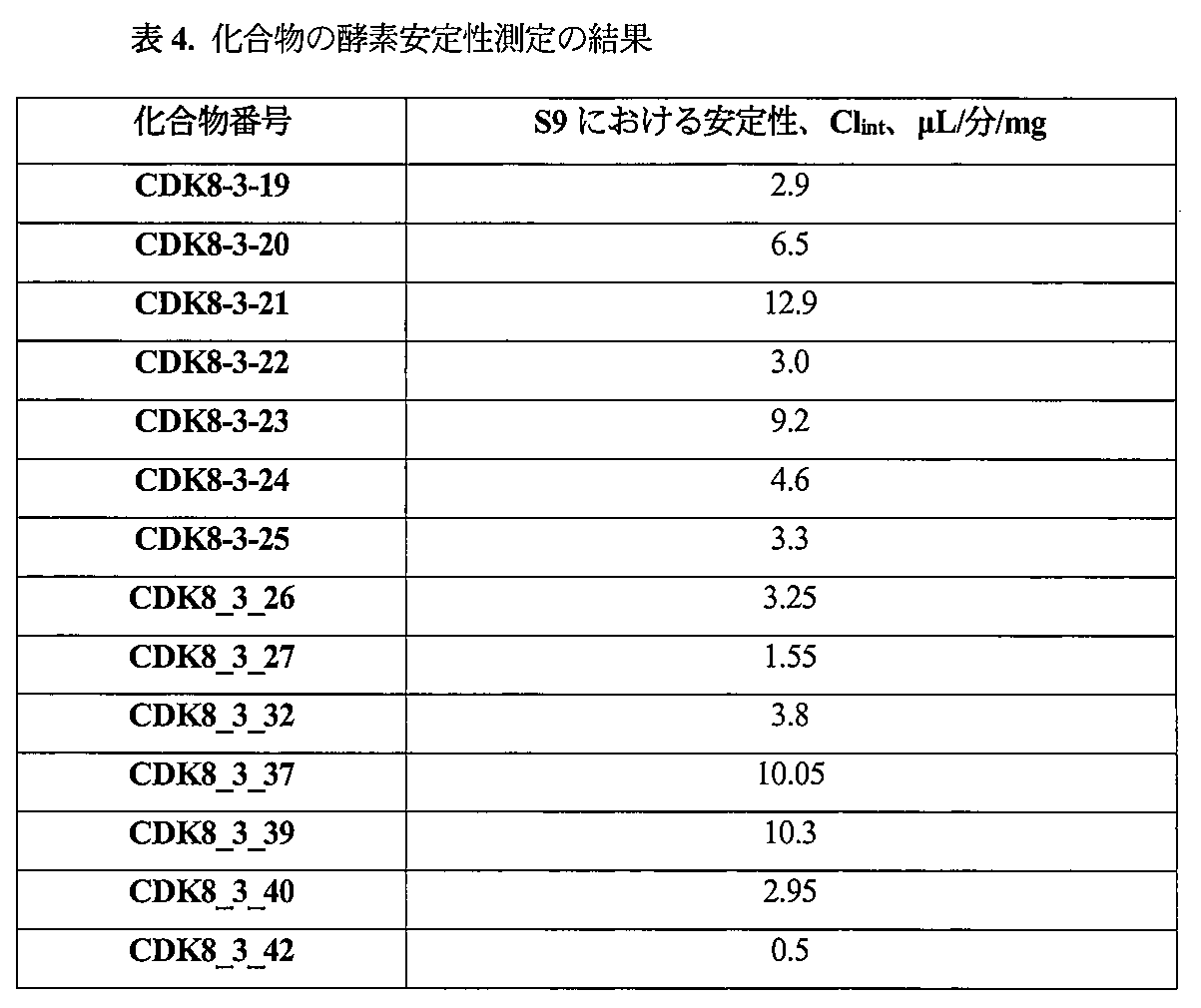
ヒト肝臓S9画分における酵素安定性の測定
候補物質の酵素安定性を測定することで、ヒト肝臓S9画分における酵素の作用に対する本化合物の安定性を推定することが可能になった。
Caco-2細胞単層への透過性の推定
Caco-2細胞単層への透過性を推定することで、物質が能動および受動両方の輸送によって生体膜を貫通しうる能力を評価することが可能になる。
Papp=(C(t)×V)/(C(0)×t×面積)、ここで、
Pappは、有効透過性定数(m/s)であり、
Vは、溶液体積(A→B試験では0.8ml、B→A試験では0.2ml)(ml)であり、
面積は、膜表面積(0.33cm2)(cm2)であり、
tは、保持時間(7200秒)(秒)であり、
C(0)は、初期溶液濃度(μM)であり、
C(t)は、2時間後の溶液濃度(A→B試験では、下方チャンバーウェルからのサンプル中の濃度、B→A試験では、上方チャンバーウェルからのサンプル中の濃度)(μM)である。
流出=Papp B-A/Papp A-B、ここで、
Papp A-Bは、直接分析A→Bの透過性の値であり、
Papp B-Aは、逆分析B→Aの透過性の値である。
in vitroでのCDK8感受性細胞株に対する抗増殖活性
本発明によるCDK8阻害薬の抗増殖活性を、連続細胞培養物MV4-11(二重表現型骨髄単球性白血病、ATCC(登録商標)CRL-9591(商標))、KG-1(急性骨髄性白血病、ATCC(登録商標)CCL-246(商標))、HL-60(急性前骨髄球性白血病、ATCC(登録商標)CCL-240(商標))での細胞ベースの試験において、生体染色剤AlamarBlue(ThermoFisher、#DAL1100)を使用して測定した。細胞を、10%FBS(Gibco、#16140-071)が加えられたRPMI-1640(PanEco、#C330p)培地で増殖させ、洗浄し、96ウェル培養プレート(Corning、#3599)において、10%FBS(Gibco、#16140-071)添加培養培地に、ウェルあたり100μmの培地中に約10×103細胞として再懸濁した。問題の化合物をDMSOに溶解させ、10%FBS(Gibco、#16140-071)添加培地で希釈して、最終濃度を0~100μMの範囲とした。次いで、希釈した化合物50μMを各ウェルに加え(最終DMSO濃度を1%未満とした)、5%CO2雰囲気中にて37℃で120時間インキュベートした。インキュベートした後、ウェル毎に15μLのAlamarBlue(ThermoFisher、#DAL1100)試薬を加え、オービタルシェーカー(Biosan、Latvia)において、プレートの中身を混合し、5%CO2雰囲気中にて37℃で3~5時間さらにインキュベートした。マイクロプレート分光光度計(Tecan Infinite M200Pro、スイス国)を使用し、540nmの励起波長(λEx)および590nmの発光波長(λEm)で蛍光シグナルを測定して、生細胞の数を推定した。
Claims (13)
- 式I.5aの化合物:
[式中、
各L1、L2は、独立に、化学結合、-C(R6b)2-、-O-、-C(O)-、-C(O)-O-、-NH-、-C(=NR19)-であり、
各R3、R13は、独立に、H、Hal、シアノ、C1~C6アルキル、NH2であり、
各R2、R4は、独立に、
各X5、X6、X7は、独立に、C、CH、Nであり、
各L3、L4は、独立に、化学結合、-C(O)-、-O-、-CH2-、-NH-、-C(O)-NR7a-、-C(=NH)-であり、
p=1であり、
R5は、H;Hal;シアノ;C1~C6アルキル;C1~C6アルキルオキシ;C1~C6アルキルオキシC1~C6アルキル;NR15R16;非置換またはHal、C1~C6アルキル、C1~C6アルコキシ、NR15R16からなる群から選択される1つもしくはいくつかの置換基で置換されているアリール;非置換またはHal、C1~C6アルキル、C1~C6アルキルオキシ、NR15R16からなる群から選択される1つもしくはいくつかの置換基で置換されている、Nおよび/またはOから選択される1~2個のヘテロ原子を有する5~6員ヘテロシクリルであり、
各R6、R6a、R6bは、独立に、H、Hal、ヒドロキシ、C1~C6アルキル、C1~C6アルキルオキシであり、
各R7、R7aは、独立に、H、C1~C6アルキルであり、
各R8、R9は、独立に、H、C1~C6アルキル、-C(O)-NR21R22、-CN、-C(O)-OR20であり、または
R8およびR9は、これらが結合している炭素原子と一緒になって、窒素および/または酸素から選択される1~2個のヘテロ原子を有する5~6員ヘテロ環式環を形成しており、R8およびR9によって形成されるヘテロ環式環は、非置換でも、またはオキソ基、C1~C6アルキルから選択される1もしくは2つの置換基で置換されていてもよく、
各R10は、独立に、H、C1~C6アルキル、ヒドロキシ、シアノ、C1~C6アルキルオキシ、C1~C6アルキルオキシC1~C6アルキル、-NR23R24;非置換または1つもしくはいくつかのC1~C6アルキルで置換されている、N、O、および/またはSから選択される1~2個のヘテロ原子を有する5~6員ヘテロシクリル;非置換または1つもしくはいくつかのC1~C6アルキルで置換されている、N、O、および/またはSから選択される1~2個のヘテロ原子を有する5~6員ヘテロアリール;-S(O)2-C1~C6アルキルからなる群から選択され、
R11は、独立に、非置換またはヒドロキシ、C3~C6シクロアルキル、-NR23aR24aで置換されているC1~C6アルキル;C1~C6アルコキシC1~C6アルキル;C3~C6シクロアルキルであり、
R12は、独立に、H;非置換またはヒドロキシ、C3~C6シクロアルキル、-NR23aR24aで置換されているC1~C6アルキル;C1~C6アルコキシC1~C6アルキル;C3~C6シクロアルキルであり、
各R14は、独立に、Hal、-C(O)NR17R18、C1~C6アルコキシであり、
各R15、R16、R19、R20、R21、R22、R23、R24、R23a、R24aは、独立に、H、C1~C6アルキルであり、
各R17、R18は、独立に、H、C1~C6アルキル;非置換またはHal、C1~C6アルキル、C1~C6アルコキシからなる群から選択される1つもしくはいくつかの置換基で置換されているアリールであり、
Halは、クロロ、ブロモ、ヨード、フルオロである]。 - 各L1、L2が、独立に、化学結合、-C(O)-、-C(O)-O-、-NH-、-C(=NH)-である、請求項1に記載の化合物。
- R5が、H;Hal;シアノ;C1~C6アルキル;C1~C6アルキルオキシ;C1~C6アルキルオキシC1~C6アルキル;NR15R16;非置換またはHal、C1~C6アルキル、C1~C6アルキルオキシ、NR15R16からなる群から選択される1つもしくはいくつかの置換基で置換されているフェニルであるアリール;非置換またはHal、C1~C6アルキル、C1~C6アルキルオキシ、NR15R16からなる群から選択される1つもしくはいくつかの置換基で置換されている4-モルホリニル、1-ピペリジニル、1-ピロリジニル、1-ピペラジニルである、Nおよび/またはOから選択される1~2個のヘテロ原子を有する5~6員ヘテロシクリルであり、
各R15、R16が、独立に、H、C1~C6アルキルである、請求項1から2のいずれか一項に記載の化合物。 - R10が、H、C1~C6アルキル、ヒドロキシ、シアノ、C1~C6アルキルオキシ、C1~C6アルキルオキシC1~C6アルキル、-NR23R24;非置換または1つもしくはいくつかのC1~C6アルキルで置換されている4-モルホリニル、1-ピペリジニル、1-ピロリジニル、1-ピペラジニルである、N、O、および/またはSから選択される1~2個のヘテロ原子を有する5~6員ヘテロシクリル;非置換または1つもしくはいくつかのC1~C6アルキルで置換されているチエニル、イミダゾリル、ピラゾリルである、N、O、および/またはSから選択される1~2個のヘテロ原子を有する5~6員ヘテロアリール;-S(O)2-C1~C6アルキルからなる群から独立に選択され、
各R23、R24は、独立に、H、C1~C6アルキルである、請求項1から2のいずれか一項に記載の化合物。 - 各R3が、独立に、H、Halである、請求項1から4のいずれか一項に記載の化合物。
- (S)-4-(3-(3-ヒドロキシピロリジン-1-カルボニル)-1,7-ナフチリジン-5-イル)-N-(メチルスルホニル)ベンズアミド(BCD-CDK8-3-1)
(R)-(5-(4-(1H-ピラゾール-4-イル)フェニル)-1,7-ナフチリジン-3-イル)(3-ヒドロキシピロリジン-1-イル)メタノン(BCD-CDK8-3-2)
(R)-(5-(4-(ジメチルアミノ)フェニル)-1,7-ナフチリジン-3-イル)(3-ヒドロキシピロリジン-1-イル)メタノン(BCD-CDK8-3-3)
(R)-(3-ヒドロキシピロリジン-1-イル)(5-(4-(1-メチル-1H-ピラゾール-4-イル)フェニル)-1,7-ナフチリジン-3-イル)メタノン(BCD-CDK8-3-4)
(R)-(3-ヒドロキシピロリジン-1-イル)(5-(4-モルホリノフェニル)-1,7-ナフチリジン-3-イル)メタノン(BCD-CDK8-3-5)
(R)-(3-ヒドロキシピロリジン-1-イル)(5-(4-メトキシフェニル)-1,7-ナフチリジン-3-イル)メタノン(BCD-CDK8-3-6)
(5-(4-(ジメチルアミノ)フェニル)-1,7-ナフチリジン-3-イル)(4-メチルピペラジン-1-イル)メタノン(BCD-CDK8-3-8)
(1-(5-(4-(1-メチル-1H-ピラゾール-4-イル)フェニル)-1,7-ナフチリジン-3-イル)アゼチジン-3-イル)(モルホリノ)メタノン(BCD-CDK8-3-9)
N-(メチルスルホニル)-4-(3-(ピペリジン-1-カルボニル)-1,7-ナフチリジン-5-イル)ベンズアミド(BCD-CDK8-3-11)
N,N-ジメチル-1-(5-(4-((メチルスルホニル)カルバモイル)フェニル)-1,7-ナフチリジン-3-イル)アゼチジン-3-カルボキサミド(BCD-CDK8-3-12)
(R)-4-(3-(3-ヒドロキシピロリジン-1-カルボニル)-1,7-ナフチリジン-5-イル)-N-(メチルスルホニル)ベンズアミド(BCD-CDK8-3-13)
アゼチジン-1-イル(5-(4-(1-メチル-1H-ピラゾール-4-イル)フェニル)-1,7-ナフチリジン-3-イル)メタノン(BCD-CDK8-3-14)
(3-メトキシアゼチジン-1-イル)(5-(4-(1-メチル-1H-ピラゾール-4-イル)フェニル)-1,7-ナフチリジン-3-イル)メタノン(BCD-CDK8-3-15)
(5-(4-(1-メチル-1H-ピラゾール-4-イル)フェニル)-1,7-ナフチリジン-3-イル)(ピロリジン-1-イル)メタノン(BCD-CDK8-3-16)
1-(5-(4-(1-メチル-1H-ピラゾール-4-イル)フェニル)-1,7-ナフチリジン-3-イル)ピロリジン-2-オン(BCD-CDK8-3-17)
N-(2-メトキシエチル)-5-(4-(1-メチル-1H-ピラゾール-4-イル)フェニル)-1,7-ナフチリジン-3-カルボキサミド(BCD-CDK8-3-18)
(R)-(3-メトキシピロリジン-1-イル)(5-(4-(1-メチル-1H-ピラゾール-4-イル)フェニル)-1,7-ナフチリジン-3-イル)メタノン(BCD-CDK8-3-19)
(R)-3-(ヒドロキシピペリジン-1-イル)(5-(4-(1-メチル-1H-ピラゾール-4-イル)フェニル)-1,7-ナフチリジン-3-イル)メタノン(BCD-CDK8-3-20)
(R)-(3-メトキシピペリジン-1-イル)(5-(4-(1-メチル-1H-ピラゾール-4-イル)フェニル)-1,7-ナフチリジン-3-イル)メタノン(BCD-CDK8-3-21)
N,N-メチル-5-(4-(1-メチル-1H-ピラゾール-4-イル)フェニル)-1,7-ナフチリジン-3-カルボキサミド(BCD-CDK8-3-22)
N,N-ジエチル-5-(4-(1-メチル-1H-ピラゾール-4-イル)フェニル)-1,7-ナフチリジン-3-カルボキサミド(BCD-CDK8-3-23)
8-アミノ-N-(2-メトキシエチル)-5-(4-(1-メチル-1H-ピラゾール-4-イル)フェニル)-1,7-ナフチリジン-3-カルボキサミド(BCD-CDK8-3-24)
N-(2-メトキシエチル)-N-メチル-5-(4-(1-メチル-1H-ピラゾール-4-イル)フェニル)-1,7-ナフチリジン-3-カルボキサミド(BCD-CDK8-3-25)
(8-アミノ-5-(4-(1-メチル-1H-ピラゾール-4-イル)フェニル)-1,7-ナフチリジン-3-イル)(アゼチジン-1-イル)メタノン(BCD-CDK8-3-26)
(8-アミノ-5-(4-(1-メチル-1H-ピラゾール-4-イル)フェニル)-1,7-ナフチリジン-3-イル)(モルホリノ)メタノン(BCD-CDK8-3-27)
2-メトキシエチル-5-[4-(1-メチル-1H-ピラゾール-4-イル)フェニル]-1,7-ナフチリジン-3-カルボキシレート(BCD-CDK8-3-28)
2-メトキシエチル-8-アミノ-5-(4-(1-メチル-1H-ピラゾール-4-イル)フェニル)-1,7-ナフチリジン-3-カルボキシレート(BCD-CDK8-3-29)
(4-メチルピペラジン-1-イル)(5-(4-(1-メチル-1H-ピラゾール-4-イル)フェニル)-1,7-ナフチリジン-3-イル)メタノン(BCD-CDK8-3-30)
(8-アミノ-5-(4-(1-メチル-1H-ピラゾール-4-イル)フェニル)-1,7-ナフチリジン-3-イル)(4-メチルピペラジン-1-イル)メタノン(BCD-CDK8-3-31)
8-アミノ-N-(2-メトキシエチル)-N-メチル-5-(4-(1-メチル-1H-ピラゾール-4-イル)フェニル)-1,7-ナフチリジン-3-カルボキサミド(BCD-CDK8-3-32)
(5-(4-(1-メチル-1H-ピラゾール-4-イル)フェニル)-1,7-ナフチリジン-3-イル)(モルホリノ)メタノン(BCD-CDK8-3-33)
(8-アミノ-5-(4-(1-メチル-1H-ピラゾール-4-イル)フェニル)-1,7-ナフチリジン-3-イル)(3-メトキシアゼチジン-1-イル)メタノン(BCD-CDK8-3-34)
N-(2-(ジメチルアミノ)エチル)-N-メチル-5-(4-(1-メチル-1H-ピラゾール-4-イル)フェニル)-1,7-ナフチリジン-3-カルボキサミド(BCD-CDK8-3-35)
N-シクロプロピル-5-(4-(1-メチル-1H-ピラゾール-4-イル)フェニル)-1,7-ナフチリジン-3-カルボキサミド(BCD-CDK8-3-37)
8-アミノ-N-シクロプロピル-5-(4-(1-メチル-1H-ピラゾール-4-イル)フェニル)-1,7-ナフチリジン-3-カルボキサミド(BCD-CDK8-3-38)
N-(シクロプロピルメチル)-5-(4-(1-メチル-1H-ピラゾール-4-イル)フェニル)-1,7-ナフチリジン-3-カルボキサミド(BCD-CDK8-3-39)
8-アミノ-N-(シクロプロピルメチル)-5-(4-(1-メチル-1H-ピラゾール-4-イル)フェニル)-1,7-ナフチリジン-3-カルボキサミド(BCD-CDK8-3-40)
5-(4-(1H-イミダゾール-1-イル)フェニル)-N-(2-メトキシエチル)-1,7-ナフチリジン-3-イル)カルボキサミド(BCD-CDK8-3-41)
8-アミノ-N-(2-ヒドロキシエチル)-5-(4-(1-メチル-1H-ピラゾール-4-イル)フェニル)-1,7-ナフチリジン-3-カルボキサミド(BCD-CDK8-3-42)
である、請求項1から2のいずれか一項に記載の化合物。 - 請求項1から6のいずれか一項に記載の化合物、または薬学的に許容されるその塩と、薬学的に許容される1種または複数の賦形剤とを含む医薬組成物。
- サイクリン依存性タンパク質キナーゼCDK8/19の活性化が介在する疾患または障害を予防または処置するための、請求項7に記載の医薬組成物。
- サイクリン依存性タンパク質キナーゼCDK8/19の活性化が介在する疾患または障害が、腫瘍性または血液腫瘍性である、請求項8に記載の医薬組成物。
- 腫瘍性または血液腫瘍性疾患が、結腸直腸がん、黒色腫、転移性黒色腫、乳がん、三種陰性乳がん(TNBC)、前立腺がん、転移性卵巣がん、転移性胃がん、白血症、急性骨髄性白血病、膵臓がんを含む群から選択される、請求項9に記載の医薬組成物。
- それを必要とする対象において、サイクリン依存性タンパク質キナーゼCDK8/19の活性化が介在する疾患または障害を処置するための医薬の製造における、請求項1から6のいずれか一項に記載の化合物もしくは薬学的に許容されるその塩、または請求項7に記載の医薬組成物の使用。
- サイクリン依存性タンパク質キナーゼCDK8/19の活性化が介在する疾患または障害が、腫瘍性または血液腫瘍性疾患を含む、請求項11に記載の使用。
- 腫瘍性および血液腫瘍性疾患が、結腸直腸がん、黒色腫、転移性黒色腫、乳がん、三種陰性乳がん(TNBC)、前立腺がん、転移性卵巣がん、転移性胃がん、白血症、急性骨髄性白血病、膵臓がんを含む群から選択される、請求項12に記載の使用。
Applications Claiming Priority (5)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| RU2017128123A RU2017128123A (ru) | 2017-08-07 | 2017-08-07 | Новые гетероциклические соединения как ингибиторы CDK8/19 |
| RU2017128123 | 2017-08-07 | ||
| RU2018108178 | 2018-03-06 | ||
| RU2018108178A RU2739489C2 (ru) | 2018-03-06 | 2018-03-06 | Новые гетероциклические соединения как ингибиторы CDK8/19 |
| PCT/RU2018/050089 WO2019031990A1 (ru) | 2017-08-07 | 2018-07-30 | Новые гетероциклические соединения как ингибиторы cdk8/19 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2020530020A JP2020530020A (ja) | 2020-10-15 |
| JP7365332B2 true JP7365332B2 (ja) | 2023-10-19 |
Family
ID=65272421
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2020506915A Active JP7365332B2 (ja) | 2017-08-07 | 2018-07-30 | Cdk8/19阻害薬としての新規ヘテロ環式化合物 |
Country Status (11)
| Country | Link |
|---|---|
| EP (1) | EP3666770A4 (ja) |
| JP (1) | JP7365332B2 (ja) |
| KR (1) | KR20200051626A (ja) |
| CN (1) | CN111670183A (ja) |
| AU (1) | AU2018312836B2 (ja) |
| BR (1) | BR112020002674A2 (ja) |
| CA (1) | CA3075477A1 (ja) |
| CO (1) | CO2020001326A2 (ja) |
| MX (1) | MX2020001531A (ja) |
| UY (1) | UY37837A (ja) |
| WO (1) | WO2019031990A1 (ja) |
Families Citing this family (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2019149738A1 (en) | 2018-01-31 | 2019-08-08 | Heparegenix Gmbh | Protein kinase mkk4 inhibitors for promoting liver regeneration or reducing or preventing hepatocyte death |
| EP3810139A1 (en) | 2018-06-21 | 2021-04-28 | HepaRegeniX GmbH | Tricyclic protein kinase inhibitors for promoting liver regeneration or reducing or preventing hepatocyte death |
| AU2019303986B2 (en) | 2018-07-16 | 2024-02-22 | Heparegenix Gmbh | Protein kinase inhibitors for promoting liver regeneration or reducing or preventing hepatocyte death |
| AR124379A1 (es) | 2020-12-17 | 2023-03-22 | Astrazeneca Ab | N-(2-(4-cianotiazolidin-3-il)-2-oxoetil)-quinolin-4-carboxamidas |
| CA3217423A1 (en) | 2021-06-16 | 2022-12-22 | Jeffrey M. Schkeryantz | Azetidinyl compounds comprising a carboxylic acid group for the treatment of neurodegenerative diseases |
| WO2023078337A1 (en) * | 2021-11-04 | 2023-05-11 | Insilico Medicine Ip Limited | Cdk8/19 dual inhibitors and methods of use |
Citations (9)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2008501696A (ja) | 2004-06-04 | 2008-01-24 | アンフォラ ディスカバリー コーポレーション | Atp利用酵素阻害活性を示すキノリンおよびイソキノリン系化合物、ならびにその組成物および使用 |
| WO2010012745A2 (en) | 2008-07-29 | 2010-02-04 | Boehringer Ingelheim International Gmbh | Benzimidazoles |
| JP2012525367A (ja) | 2009-04-30 | 2012-10-22 | ノバルティス アーゲー | イミダゾール誘導体およびサイクリン依存性キナーゼ類のモジュレーターとしてのその使用 |
| US20130165458A1 (en) | 2011-12-27 | 2013-06-27 | Development Center For Biotechnology | Quinazoline compounds as kinase inhibitors |
| WO2016009076A1 (en) | 2014-07-17 | 2016-01-21 | Merck Patent Gmbh | Novel naphthryidines and isoquinolines and their use as cdk8/19 inhibitors |
| WO2016041618A1 (en) | 2014-09-15 | 2016-03-24 | Merck Patent Gmbh | Substituted indazoles and related heterocycles |
| JP2016525142A (ja) | 2013-07-29 | 2016-08-22 | エフ.ホフマン−ラ ロシュ アーゲーF. Hoffmann−La Roche Aktiengesellschaft | 1,7−ナフチリジン誘導体 |
| WO2017040993A1 (en) | 2015-09-03 | 2017-03-09 | The Arizona Board Of Regents On Behalf Of The University Of Arizona | Small molecule inhibitors of dyrk1a and uses thereof |
| WO2017094026A1 (en) | 2015-11-30 | 2017-06-08 | Council Of Scientific & Industrial Research | 3-pyrimidinyl pyrrolo [2,3-b] pyridine as new anticancer agents and the process for the preparation thereof |
Family Cites Families (20)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US4492708A (en) * | 1982-09-27 | 1985-01-08 | Eli Lilly And Company | Antiviral benzimidazoles |
| DE4202526A1 (de) * | 1992-01-30 | 1993-08-05 | Bayer Ag | Neue 4-cinnolinyl- und 4-naphthyridinyl-dihydropyridine, verfahren zu ihrer herstellung und ihre verwendung in arzneimitteln |
| AU675484B2 (en) * | 1993-03-24 | 1997-02-06 | Neurosearch A/S | Benzimidazole compounds, their use and preparation |
| US5545653A (en) * | 1995-06-07 | 1996-08-13 | Eli Lilly And Company | Anti-viral compounds |
| WO2000071518A2 (en) | 1999-05-25 | 2000-11-30 | Sepracor, Inc. | Heterocyclic analgesic compounds and their use |
| DE60227794D1 (de) * | 2001-04-26 | 2008-09-04 | Eisai R&D Man Co Ltd | Stickstoffhaltige verbindung mit kondensiertem ring und pyrazolylgruppe als substituent und medizinische zusammensetzung davon |
| EA011034B1 (ru) | 2001-11-26 | 2008-12-30 | Кортекс Фармасеутикалс, Инк. | Соединения карбонилбензоксазина для усиления глутаматергических синаптических ответов |
| CA2550361C (en) * | 2003-12-19 | 2014-04-29 | Prabha Ibrahim | Compounds and methods for development of ret modulators |
| US8492378B2 (en) * | 2006-08-03 | 2013-07-23 | Takeda Pharmaceutical Company Limited | GSK-3β inhibitor |
| JP2010513519A (ja) | 2006-12-22 | 2010-04-30 | ミレニアム・ファーマシューティカルズ・インコーポレイテッド | キナーゼインヒビター活性を有するある種のピラゾリン誘導体 |
| GB0724340D0 (en) * | 2007-12-13 | 2008-01-30 | Univ Dundee | Novel Therapeutic Agents |
| AR072084A1 (es) * | 2008-06-12 | 2010-08-04 | Sanofi Aventis | Derivados de azacarbolinas, su preparacion y su utilizacion terapeutica como inhibidores de las quinasas pim |
| NZ603446A (en) | 2010-04-14 | 2014-05-30 | Array Biopharma Inc | 5, 7-substituted-imidazo [1, 2-c] pyrimidines as inhibitors of jak kinases |
| WO2012174312A2 (en) * | 2011-06-15 | 2012-12-20 | Glaxosmithkline Llc | Benzimidazole derivatives as antiviral agents |
| GB201202027D0 (en) * | 2012-02-06 | 2012-03-21 | Sareum Ltd | Pharmaceutical compounds |
| KR102138390B1 (ko) | 2012-08-21 | 2020-07-27 | 알데릭스, 인코포레이티드 | 체액 저류 또는 염 과부하와 연관된 장애 및 위장관 장애의 치료에서 nhe-매개된 역수송 저해를 위한 화합물 및 방법 |
| GB201403093D0 (en) * | 2014-02-21 | 2014-04-09 | Cancer Rec Tech Ltd | Therapeutic compounds and their use |
| JP6529085B2 (ja) * | 2014-04-18 | 2019-06-12 | 武田薬品工業株式会社 | 複素環化合物 |
| EP3183239B1 (en) * | 2014-08-22 | 2018-09-26 | Merck Patent GmbH | Indazoles |
| US9938273B2 (en) * | 2015-12-07 | 2018-04-10 | Plexxikon Inc. | Compounds and methods for kinase modulation, and indications therefor |
-
2018
- 2018-07-30 BR BR112020002674-3A patent/BR112020002674A2/pt unknown
- 2018-07-30 WO PCT/RU2018/050089 patent/WO2019031990A1/ru unknown
- 2018-07-30 KR KR1020207006919A patent/KR20200051626A/ko not_active Application Discontinuation
- 2018-07-30 JP JP2020506915A patent/JP7365332B2/ja active Active
- 2018-07-30 CA CA3075477A patent/CA3075477A1/en active Pending
- 2018-07-30 MX MX2020001531A patent/MX2020001531A/es unknown
- 2018-07-30 AU AU2018312836A patent/AU2018312836B2/en active Active
- 2018-07-30 EP EP18843992.1A patent/EP3666770A4/en active Pending
- 2018-07-30 CN CN201880065111.7A patent/CN111670183A/zh active Pending
- 2018-08-07 UY UY0001037837A patent/UY37837A/es unknown
-
2020
- 2020-02-06 CO CONC2020/0001326A patent/CO2020001326A2/es unknown
Patent Citations (9)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2008501696A (ja) | 2004-06-04 | 2008-01-24 | アンフォラ ディスカバリー コーポレーション | Atp利用酵素阻害活性を示すキノリンおよびイソキノリン系化合物、ならびにその組成物および使用 |
| WO2010012745A2 (en) | 2008-07-29 | 2010-02-04 | Boehringer Ingelheim International Gmbh | Benzimidazoles |
| JP2012525367A (ja) | 2009-04-30 | 2012-10-22 | ノバルティス アーゲー | イミダゾール誘導体およびサイクリン依存性キナーゼ類のモジュレーターとしてのその使用 |
| US20130165458A1 (en) | 2011-12-27 | 2013-06-27 | Development Center For Biotechnology | Quinazoline compounds as kinase inhibitors |
| JP2016525142A (ja) | 2013-07-29 | 2016-08-22 | エフ.ホフマン−ラ ロシュ アーゲーF. Hoffmann−La Roche Aktiengesellschaft | 1,7−ナフチリジン誘導体 |
| WO2016009076A1 (en) | 2014-07-17 | 2016-01-21 | Merck Patent Gmbh | Novel naphthryidines and isoquinolines and their use as cdk8/19 inhibitors |
| WO2016041618A1 (en) | 2014-09-15 | 2016-03-24 | Merck Patent Gmbh | Substituted indazoles and related heterocycles |
| WO2017040993A1 (en) | 2015-09-03 | 2017-03-09 | The Arizona Board Of Regents On Behalf Of The University Of Arizona | Small molecule inhibitors of dyrk1a and uses thereof |
| WO2017094026A1 (en) | 2015-11-30 | 2017-06-08 | Council Of Scientific & Industrial Research | 3-pyrimidinyl pyrrolo [2,3-b] pyridine as new anticancer agents and the process for the preparation thereof |
Non-Patent Citations (2)
| Title |
|---|
| ACS Med. Chem. Lett.,Vol.7, No.6,2016年,pp.573-578 |
| Bioorg. Med. Chem. Lett.,Vol.26,2016年,pp.1443-1451 |
Also Published As
| Publication number | Publication date |
|---|---|
| KR20200051626A (ko) | 2020-05-13 |
| JP2020530020A (ja) | 2020-10-15 |
| BR112020002674A2 (pt) | 2020-07-28 |
| CO2020001326A2 (es) | 2020-04-01 |
| EP3666770A4 (en) | 2021-04-07 |
| WO2019031990A1 (ru) | 2019-02-14 |
| UY37837A (es) | 2019-02-28 |
| EP3666770A1 (en) | 2020-06-17 |
| MX2020001531A (es) | 2020-03-20 |
| AU2018312836B2 (en) | 2022-12-08 |
| AU2018312836A1 (en) | 2020-03-26 |
| CN111670183A (zh) | 2020-09-15 |
| CA3075477A1 (en) | 2019-02-14 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP7365332B2 (ja) | Cdk8/19阻害薬としての新規ヘテロ環式化合物 | |
| KR20180094939A (ko) | 폴리시클릭 tlr7/8 안타고니스트 및 면역 질환의 치료에서 이들의 용도 | |
| US20200062760A1 (en) | Shp2 phosphatase inhibitors and methods of use thereof | |
| WO2016041618A1 (en) | Substituted indazoles and related heterocycles | |
| ES2720324T3 (es) | Piridil piperidinas | |
| EP3464295B1 (en) | Tricyclic heterocylic derivatives | |
| AU2015306458B2 (en) | Indazoles | |
| BR112021002090A2 (pt) | derivado azabicíclico opticamente ativo | |
| KR20210049895A (ko) | 고 활성 sting 단백질 작용제 화합물 | |
| CN111183142B (zh) | 硼酸衍生物 | |
| KR20150090044A (ko) | 아자퀴나졸린 카복사미드 유도체 | |
| JP7365396B2 (ja) | Cdk8/19阻害薬 | |
| RU2739489C2 (ru) | Новые гетероциклические соединения как ингибиторы CDK8/19 | |
| RU2763347C2 (ru) | Новые ингибиторы cdk8/19 | |
| TWI839374B (zh) | Cdk8/19抑制劑 | |
| EA041908B1 (ru) | Производные 1,7-нафтиридина и их применение в качестве ингибиторов cdk8/19 | |
| KR20230135541A (ko) | 신규한 화합물 및 이의 체크포인트 키나제 2 저해 용도 | |
| US20230348462A1 (en) | Imidazo[4,5-c]quinoline compounds and their use as atm kinase inhibitors | |
| CA3213823A1 (en) | Selective modulators of ataxia telangiectasia mutated (atm) kinase and uses thereof | |
| EA042225B1 (ru) | Ингибиторы cdk8/19 | |
| TW202120511A (zh) | 雜環化合物 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20210701 |
|
| A977 | Report on retrieval |
Free format text: JAPANESE INTERMEDIATE CODE: A971007 Effective date: 20220621 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20220624 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20220920 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20221122 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20221226 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20230412 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20230704 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20230928 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20231006 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 7365332 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |