JP7177073B2 - アッセイ用の光学系、デバイス、およびシステム - Google Patents
アッセイ用の光学系、デバイス、およびシステム Download PDFInfo
- Publication number
- JP7177073B2 JP7177073B2 JP2019543054A JP2019543054A JP7177073B2 JP 7177073 B2 JP7177073 B2 JP 7177073B2 JP 2019543054 A JP2019543054 A JP 2019543054A JP 2019543054 A JP2019543054 A JP 2019543054A JP 7177073 B2 JP7177073 B2 JP 7177073B2
- Authority
- JP
- Japan
- Prior art keywords
- sample
- optical
- imaging
- light
- camera
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
- 238000003556 assay Methods 0.000 title description 11
- 230000003287 optical effect Effects 0.000 claims description 336
- 238000003384 imaging method Methods 0.000 claims description 186
- 238000005286 illumination Methods 0.000 claims description 127
- 230000005284 excitation Effects 0.000 claims description 18
- 239000006096 absorbing agent Substances 0.000 claims description 15
- 230000031700 light absorption Effects 0.000 claims description 4
- 239000000523 sample Substances 0.000 description 538
- 238000000034 method Methods 0.000 description 149
- 125000006850 spacer group Chemical group 0.000 description 113
- 238000001514 detection method Methods 0.000 description 58
- 210000001519 tissue Anatomy 0.000 description 58
- 239000003795 chemical substances by application Substances 0.000 description 54
- 239000012491 analyte Substances 0.000 description 51
- 238000004422 calculation algorithm Methods 0.000 description 36
- 239000000835 fiber Substances 0.000 description 31
- 238000010186 staining Methods 0.000 description 29
- 238000003825 pressing Methods 0.000 description 28
- 210000004027 cell Anatomy 0.000 description 27
- -1 reservoirs Substances 0.000 description 26
- 230000008859 change Effects 0.000 description 24
- 238000010586 diagram Methods 0.000 description 24
- 239000012192 staining solution Substances 0.000 description 23
- WZUVPPKBWHMQCE-UHFFFAOYSA-N Haematoxylin Chemical compound C12=CC(O)=C(O)C=C2CC2(O)C1C1=CC=C(O)C(O)=C1OC2 WZUVPPKBWHMQCE-UHFFFAOYSA-N 0.000 description 22
- 238000012549 training Methods 0.000 description 22
- 230000008569 process Effects 0.000 description 21
- 238000010295 mobile communication Methods 0.000 description 19
- 230000006870 function Effects 0.000 description 18
- 239000013307 optical fiber Substances 0.000 description 18
- 238000004458 analytical method Methods 0.000 description 16
- 239000000427 antigen Substances 0.000 description 16
- 102000036639 antigens Human genes 0.000 description 16
- 108091007433 antigens Proteins 0.000 description 16
- 238000012545 processing Methods 0.000 description 15
- 239000000243 solution Substances 0.000 description 15
- 238000012360 testing method Methods 0.000 description 15
- 210000004369 blood Anatomy 0.000 description 14
- 239000008280 blood Substances 0.000 description 14
- 238000013461 design Methods 0.000 description 14
- 230000009977 dual effect Effects 0.000 description 13
- 238000007901 in situ hybridization Methods 0.000 description 13
- 238000003325 tomography Methods 0.000 description 12
- 230000002055 immunohistochemical effect Effects 0.000 description 11
- 239000000758 substrate Substances 0.000 description 11
- 238000000151 deposition Methods 0.000 description 10
- 239000007788 liquid Substances 0.000 description 10
- 108091032973 (ribonucleotides)n+m Proteins 0.000 description 9
- RBTBFTRPCNLSDE-UHFFFAOYSA-N 3,7-bis(dimethylamino)phenothiazin-5-ium Chemical compound C1=CC(N(C)C)=CC2=[S+]C3=CC(N(C)C)=CC=C3N=C21 RBTBFTRPCNLSDE-UHFFFAOYSA-N 0.000 description 9
- 239000003153 chemical reaction reagent Substances 0.000 description 9
- 239000012530 fluid Substances 0.000 description 9
- 229960000907 methylthioninium chloride Drugs 0.000 description 9
- 238000012546 transfer Methods 0.000 description 9
- 238000007398 colorimetric assay Methods 0.000 description 8
- 238000010205 computational analysis Methods 0.000 description 8
- 238000013527 convolutional neural network Methods 0.000 description 8
- 230000004807 localization Effects 0.000 description 8
- 230000009466 transformation Effects 0.000 description 8
- 238000004737 colorimetric analysis Methods 0.000 description 7
- NALREUIWICQLPS-UHFFFAOYSA-N 7-imino-n,n-dimethylphenothiazin-3-amine;hydrochloride Chemical compound [Cl-].C1=C(N)C=C2SC3=CC(=[N+](C)C)C=CC3=NC2=C1 NALREUIWICQLPS-UHFFFAOYSA-N 0.000 description 6
- 108020004414 DNA Proteins 0.000 description 6
- 206010036790 Productive cough Diseases 0.000 description 6
- 239000002981 blocking agent Substances 0.000 description 6
- 210000001175 cerebrospinal fluid Anatomy 0.000 description 6
- 210000002939 cerumen Anatomy 0.000 description 6
- 238000009826 distribution Methods 0.000 description 6
- MHMNJMPURVTYEJ-UHFFFAOYSA-N fluorescein-5-isothiocyanate Chemical compound O1C(=O)C2=CC(N=C=S)=CC=C2C21C1=CC=C(O)C=C1OC1=CC(O)=CC=C21 MHMNJMPURVTYEJ-UHFFFAOYSA-N 0.000 description 6
- 238000000799 fluorescence microscopy Methods 0.000 description 6
- 238000007490 hematoxylin and eosin (H&E) staining Methods 0.000 description 6
- 230000033001 locomotion Effects 0.000 description 6
- 238000010801 machine learning Methods 0.000 description 6
- 210000003097 mucus Anatomy 0.000 description 6
- 239000012188 paraffin wax Substances 0.000 description 6
- AFAIELJLZYUNPW-UHFFFAOYSA-N pararosaniline free base Chemical compound C1=CC(N)=CC=C1C(C=1C=CC(N)=CC=1)=C1C=CC(=N)C=C1 AFAIELJLZYUNPW-UHFFFAOYSA-N 0.000 description 6
- 239000008191 permeabilizing agent Substances 0.000 description 6
- 238000011002 quantification Methods 0.000 description 6
- 241000894007 species Species 0.000 description 6
- 210000003802 sputum Anatomy 0.000 description 6
- 208000024794 sputum Diseases 0.000 description 6
- AXDJCCTWPBKUKL-UHFFFAOYSA-N 4-[(4-aminophenyl)-(4-imino-3-methylcyclohexa-2,5-dien-1-ylidene)methyl]aniline;hydron;chloride Chemical compound Cl.C1=CC(=N)C(C)=CC1=C(C=1C=CC(N)=CC=1)C1=CC=C(N)C=C1 AXDJCCTWPBKUKL-UHFFFAOYSA-N 0.000 description 5
- 230000005540 biological transmission Effects 0.000 description 5
- 238000000339 bright-field microscopy Methods 0.000 description 5
- 238000003745 diagnosis Methods 0.000 description 5
- 239000000975 dye Substances 0.000 description 5
- YQGOJNYOYNNSMM-UHFFFAOYSA-N eosin Chemical compound [Na+].OC(=O)C1=CC=CC=C1C1=C2C=C(Br)C(=O)C(Br)=C2OC2=C(Br)C(O)=C(Br)C=C21 YQGOJNYOYNNSMM-UHFFFAOYSA-N 0.000 description 5
- ZBQZBWKNGDEDOA-UHFFFAOYSA-N eosin B Chemical compound O1C(=O)C2=CC=CC=C2C21C1=CC([N+]([O-])=O)=C(O)C(Br)=C1OC1=C2C=C([N+]([O-])=O)C(O)=C1Br ZBQZBWKNGDEDOA-UHFFFAOYSA-N 0.000 description 5
- SEACYXSIPDVVMV-UHFFFAOYSA-L eosin Y Chemical compound [Na+].[Na+].[O-]C(=O)C1=CC=CC=C1C1=C2C=C(Br)C(=O)C(Br)=C2OC2=C(Br)C([O-])=C(Br)C=C21 SEACYXSIPDVVMV-UHFFFAOYSA-L 0.000 description 5
- 238000002073 fluorescence micrograph Methods 0.000 description 5
- 238000004519 manufacturing process Methods 0.000 description 5
- 239000000463 material Substances 0.000 description 5
- 230000007246 mechanism Effects 0.000 description 5
- 108090000623 proteins and genes Proteins 0.000 description 5
- YBJHBAHKTGYVGT-ZKWXMUAHSA-N (+)-Biotin Chemical compound N1C(=O)N[C@@H]2[C@H](CCCCC(=O)O)SC[C@@H]21 YBJHBAHKTGYVGT-ZKWXMUAHSA-N 0.000 description 4
- JKYKXTRKURYNGW-UHFFFAOYSA-N 3,4-dihydroxy-9,10-dioxo-9,10-dihydroanthracene-2-sulfonic acid Chemical compound O=C1C2=CC=CC=C2C(=O)C2=C1C(O)=C(O)C(S(O)(=O)=O)=C2 JKYKXTRKURYNGW-UHFFFAOYSA-N 0.000 description 4
- ALJHHTHBYJROOG-UHFFFAOYSA-N 7-(dimethylamino)phenothiazin-3-one Chemical compound C1=CC(=O)C=C2SC3=CC(N(C)C)=CC=C3N=C21 ALJHHTHBYJROOG-UHFFFAOYSA-N 0.000 description 4
- MPVDXIMFBOLMNW-ISLYRVAYSA-N 7-hydroxy-8-[(E)-phenyldiazenyl]naphthalene-1,3-disulfonic acid Chemical compound OC1=CC=C2C=C(S(O)(=O)=O)C=C(S(O)(=O)=O)C2=C1\N=N\C1=CC=CC=C1 MPVDXIMFBOLMNW-ISLYRVAYSA-N 0.000 description 4
- CKLBXIYTBHXJEH-UHFFFAOYSA-J 75881-23-1 Chemical compound [Cl-].[Cl-].[Cl-].[Cl-].[Cu+2].[N-]1C(N=C2C3=CC=C(CSC(N(C)C)=[N+](C)C)C=C3C(N=C3C4=CC=C(CSC(N(C)C)=[N+](C)C)C=C4C(=N4)[N-]3)=N2)=C(C=C(CSC(N(C)C)=[N+](C)C)C=C2)C2=C1N=C1C2=CC(CSC(N(C)C)=[N+](C)C)=CC=C2C4=N1 CKLBXIYTBHXJEH-UHFFFAOYSA-J 0.000 description 4
- QFIIYGZAUXVPSZ-UHFFFAOYSA-N 8-(2,4-dihydroxy-6-methylanilino)-2-(2,4-dihydroxy-6-methylphenyl)imino-7-hydroxy-1,9-dimethyldibenzofuran-3-one Chemical compound CC1=CC(=CC(=C1NC2=C(C3=C(C=C2O)OC4=CC(=O)C(=NC5=C(C=C(C=C5C)O)O)C(=C43)C)C)O)O QFIIYGZAUXVPSZ-UHFFFAOYSA-N 0.000 description 4
- 208000005443 Circulating Neoplastic Cells Diseases 0.000 description 4
- 239000004214 Fast Green FCF Substances 0.000 description 4
- RZSYLLSAWYUBPE-UHFFFAOYSA-L Fast green FCF Chemical compound [Na+].[Na+].C=1C=C(C(=C2C=CC(C=C2)=[N+](CC)CC=2C=C(C=CC=2)S([O-])(=O)=O)C=2C(=CC(O)=CC=2)S([O-])(=O)=O)C=CC=1N(CC)CC1=CC=CC(S([O-])(=O)=O)=C1 RZSYLLSAWYUBPE-UHFFFAOYSA-L 0.000 description 4
- XXACTDWGHQXLGW-UHFFFAOYSA-M Janus Green B chloride Chemical compound [Cl-].C12=CC(N(CC)CC)=CC=C2N=C2C=CC(\N=N\C=3C=CC(=CC=3)N(C)C)=CC2=[N+]1C1=CC=CC=C1 XXACTDWGHQXLGW-UHFFFAOYSA-M 0.000 description 4
- WWKGVZASJYXZKN-UHFFFAOYSA-N Methyl violet 2B Chemical compound [Cl-].C1=CC(N(C)C)=CC=C1C(C=1C=CC(N)=CC=1)=C1C=CC(=[N+](C)C)C=C1 WWKGVZASJYXZKN-UHFFFAOYSA-N 0.000 description 4
- 108020005187 Oligonucleotide Probes Proteins 0.000 description 4
- 239000004218 Orcein Substances 0.000 description 4
- PLXBWHJQWKZRKG-UHFFFAOYSA-N Resazurin Chemical compound C1=CC(=O)C=C2OC3=CC(O)=CC=C3[N+]([O-])=C21 PLXBWHJQWKZRKG-UHFFFAOYSA-N 0.000 description 4
- FHNINJWBTRXEBC-UHFFFAOYSA-N Sudan III Chemical compound OC1=CC=C2C=CC=CC2=C1N=NC(C=C1)=CC=C1N=NC1=CC=CC=C1 FHNINJWBTRXEBC-UHFFFAOYSA-N 0.000 description 4
- 108010076830 Thionins Proteins 0.000 description 4
- ZHAFUINZIZIXFC-UHFFFAOYSA-N [9-(dimethylamino)-10-methylbenzo[a]phenoxazin-5-ylidene]azanium;chloride Chemical compound [Cl-].O1C2=CC(=[NH2+])C3=CC=CC=C3C2=NC2=C1C=C(N(C)C)C(C)=C2 ZHAFUINZIZIXFC-UHFFFAOYSA-N 0.000 description 4
- DEXKHGVSCDMMLD-UHFFFAOYSA-N [ClH]1N=CC=C1 Chemical compound [ClH]1N=CC=C1 DEXKHGVSCDMMLD-UHFFFAOYSA-N 0.000 description 4
- 238000010521 absorption reaction Methods 0.000 description 4
- DGOBMKYRQHEFGQ-UHFFFAOYSA-L acid green 5 Chemical compound [Na+].[Na+].C=1C=C(C(=C2C=CC(C=C2)=[N+](CC)CC=2C=C(C=CC=2)S([O-])(=O)=O)C=2C=CC(=CC=2)S([O-])(=O)=O)C=CC=1N(CC)CC1=CC=CC(S([O-])(=O)=O)=C1 DGOBMKYRQHEFGQ-UHFFFAOYSA-L 0.000 description 4
- CQPFMGBJSMSXLP-UHFFFAOYSA-M acid orange 7 Chemical compound [Na+].OC1=CC=C2C=CC=CC2=C1N=NC1=CC=C(S([O-])(=O)=O)C=C1 CQPFMGBJSMSXLP-UHFFFAOYSA-M 0.000 description 4
- KSCQDDRPFHTIRL-UHFFFAOYSA-N auramine O Chemical compound [H+].[Cl-].C1=CC(N(C)C)=CC=C1C(=N)C1=CC=C(N(C)C)C=C1 KSCQDDRPFHTIRL-UHFFFAOYSA-N 0.000 description 4
- QZKHGYGBYOUFGK-UHFFFAOYSA-L azocarmine B Chemical compound [Na+].[Na+].[O-]S(=O)(=O)C1=CC(S(=O)(=O)[O-])=CC=C1NC(C1=CC(=CC=C1C1=NC2=CC=CC=C22)S([O-])(=O)=O)=CC1=[N+]2C1=CC=CC=C1 QZKHGYGBYOUFGK-UHFFFAOYSA-L 0.000 description 4
- LUERODMRBLNCFK-UHFFFAOYSA-M azocarmine G Chemical compound [Na+].C1=CC(S(=O)(=O)[O-])=CC=C1NC(C1=CC(=CC=C1C1=NC2=CC=CC=C22)S([O-])(=O)=O)=CC1=[N+]2C1=CC=CC=C1 LUERODMRBLNCFK-UHFFFAOYSA-M 0.000 description 4
- BDFZFGDTHFGWRQ-UHFFFAOYSA-N basic brown 1 Chemical compound NC1=CC(N)=CC=C1N=NC1=CC=CC(N=NC=2C(=CC(N)=CC=2)N)=C1 BDFZFGDTHFGWRQ-UHFFFAOYSA-N 0.000 description 4
- 210000001124 body fluid Anatomy 0.000 description 4
- 235000012730 carminic acid Nutrition 0.000 description 4
- 230000006835 compression Effects 0.000 description 4
- 238000007906 compression Methods 0.000 description 4
- IQFVPQOLBLOTPF-HKXUKFGYSA-L congo red Chemical compound [Na+].[Na+].C1=CC=CC2=C(N)C(/N=N/C3=CC=C(C=C3)C3=CC=C(C=C3)/N=N/C3=C(C4=CC=CC=C4C(=C3)S([O-])(=O)=O)N)=CC(S([O-])(=O)=O)=C21 IQFVPQOLBLOTPF-HKXUKFGYSA-L 0.000 description 4
- 239000013078 crystal Substances 0.000 description 4
- 238000009792 diffusion process Methods 0.000 description 4
- IINNWAYUJNWZRM-UHFFFAOYSA-L erythrosin B Chemical compound [Na+].[Na+].[O-]C(=O)C1=CC=CC=C1C1=C2C=C(I)C(=O)C(I)=C2OC2=C(I)C([O-])=C(I)C=C21 IINNWAYUJNWZRM-UHFFFAOYSA-L 0.000 description 4
- 235000012732 erythrosine Nutrition 0.000 description 4
- 229940011411 erythrosine Drugs 0.000 description 4
- 239000004174 erythrosine Substances 0.000 description 4
- UKZQEOHHLOYJLY-UHFFFAOYSA-M ethyl eosin Chemical compound [K+].CCOC(=O)C1=CC=CC=C1C1=C2C=C(Br)C(=O)C(Br)=C2OC2=C(Br)C([O-])=C(Br)C=C21 UKZQEOHHLOYJLY-UHFFFAOYSA-M 0.000 description 4
- IDAQSADEMXDTKN-UHFFFAOYSA-L ethyl green Chemical compound [Cl-].[Br-].C1=CC([N+](C)(C)CC)=CC=C1C(C=1C=CC(=CC=1)N(C)C)=C1C=CC(=[N+](C)C)C=C1 IDAQSADEMXDTKN-UHFFFAOYSA-L 0.000 description 4
- 235000019240 fast green FCF Nutrition 0.000 description 4
- KHLVKKOJDHCJMG-QDBORUFSSA-L indigo carmine Chemical compound [Na+].[Na+].N/1C2=CC=C(S([O-])(=O)=O)C=C2C(=O)C\1=C1/NC2=CC=C(S(=O)(=O)[O-])C=C2C1=O KHLVKKOJDHCJMG-QDBORUFSSA-L 0.000 description 4
- 229960003988 indigo carmine Drugs 0.000 description 4
- 235000012738 indigotine Nutrition 0.000 description 4
- 239000004179 indigotine Substances 0.000 description 4
- 230000000670 limiting effect Effects 0.000 description 4
- 229940107698 malachite green Drugs 0.000 description 4
- FDZZZRQASAIRJF-UHFFFAOYSA-M malachite green Chemical compound [Cl-].C1=CC(N(C)C)=CC=C1C(C=1C=CC=CC=1)=C1C=CC(=[N+](C)C)C=C1 FDZZZRQASAIRJF-UHFFFAOYSA-M 0.000 description 4
- 239000002184 metal Substances 0.000 description 4
- 229940012189 methyl orange Drugs 0.000 description 4
- STZCRXQWRGQSJD-GEEYTBSJSA-M methyl orange Chemical compound [Na+].C1=CC(N(C)C)=CC=C1\N=N\C1=CC=C(S([O-])(=O)=O)C=C1 STZCRXQWRGQSJD-GEEYTBSJSA-M 0.000 description 4
- PGSADBUBUOPOJS-UHFFFAOYSA-N neutral red Chemical compound Cl.C1=C(C)C(N)=CC2=NC3=CC(N(C)C)=CC=C3N=C21 PGSADBUBUOPOJS-UHFFFAOYSA-N 0.000 description 4
- XJCPMUIIBDVFDM-UHFFFAOYSA-M nile blue A Chemical compound [Cl-].C1=CC=C2C3=NC4=CC=C(N(CC)CC)C=C4[O+]=C3C=C(N)C2=C1 XJCPMUIIBDVFDM-UHFFFAOYSA-M 0.000 description 4
- 239000002751 oligonucleotide probe Substances 0.000 description 4
- 235000019248 orcein Nutrition 0.000 description 4
- NTGBUUXKGAZMSE-UHFFFAOYSA-N phenyl n-[4-[4-(4-methoxyphenyl)piperazin-1-yl]phenyl]carbamate Chemical compound C1=CC(OC)=CC=C1N1CCN(C=2C=CC(NC(=O)OC=3C=CC=CC=3)=CC=2)CC1 NTGBUUXKGAZMSE-UHFFFAOYSA-N 0.000 description 4
- GVKCHTBDSMQENH-UHFFFAOYSA-L phloxine B Chemical compound [Na+].[Na+].[O-]C(=O)C1=C(Cl)C(Cl)=C(Cl)C(Cl)=C1C1=C2C=C(Br)C(=O)C(Br)=C2OC2=C(Br)C([O-])=C(Br)C=C21 GVKCHTBDSMQENH-UHFFFAOYSA-L 0.000 description 4
- 102000004169 proteins and genes Human genes 0.000 description 4
- CXZRDVVUVDYSCQ-UHFFFAOYSA-M pyronin B Chemical compound [Cl-].C1=CC(=[N+](CC)CC)C=C2OC3=CC(N(CC)CC)=CC=C3C=C21 CXZRDVVUVDYSCQ-UHFFFAOYSA-M 0.000 description 4
- INCIMLINXXICKS-UHFFFAOYSA-M pyronin Y Chemical compound [Cl-].C1=CC(=[N+](C)C)C=C2OC3=CC(N(C)C)=CC=C3C=C21 INCIMLINXXICKS-UHFFFAOYSA-M 0.000 description 4
- OARRHUQTFTUEOS-UHFFFAOYSA-N safranin Chemical compound [Cl-].C=12C=C(N)C(C)=CC2=NC2=CC(C)=C(N)C=C2[N+]=1C1=CC=CC=C1 OARRHUQTFTUEOS-UHFFFAOYSA-N 0.000 description 4
- 108700024661 strong silver Proteins 0.000 description 4
- 239000000126 substance Substances 0.000 description 4
- YCUVUDODLRLVIC-VPHDGDOJSA-N sudan black b Chemical compound C1=CC(=C23)NC(C)(C)NC2=CC=CC3=C1\N=N\C(C1=CC=CC=C11)=CC=C1\N=N\C1=CC=CC=C1 YCUVUDODLRLVIC-VPHDGDOJSA-N 0.000 description 4
- 229940099373 sudan iii Drugs 0.000 description 4
- ANRHNWWPFJCPAZ-UHFFFAOYSA-M thionine Chemical compound [Cl-].C1=CC(N)=CC2=[S+]C3=CC(N)=CC=C3N=C21 ANRHNWWPFJCPAZ-UHFFFAOYSA-M 0.000 description 4
- 229950003937 tolonium Drugs 0.000 description 4
- HNONEKILPDHFOL-UHFFFAOYSA-M tolonium chloride Chemical compound [Cl-].C1=C(C)C(N)=CC2=[S+]C3=CC(N(C)C)=CC=C3N=C21 HNONEKILPDHFOL-UHFFFAOYSA-M 0.000 description 4
- 206010003445 Ascites Diseases 0.000 description 3
- 206010050337 Cerumen impaction Diseases 0.000 description 3
- 101000649946 Homo sapiens Vacuolar protein sorting-associated protein 29 Proteins 0.000 description 3
- 208000002151 Pleural effusion Diseases 0.000 description 3
- 238000001069 Raman spectroscopy Methods 0.000 description 3
- 208000033809 Suppuration Diseases 0.000 description 3
- 102100028290 Vacuolar protein sorting-associated protein 29 Human genes 0.000 description 3
- 230000002378 acidificating effect Effects 0.000 description 3
- 210000004381 amniotic fluid Anatomy 0.000 description 3
- 210000001742 aqueous humor Anatomy 0.000 description 3
- 230000008901 benefit Effects 0.000 description 3
- 239000012472 biological sample Substances 0.000 description 3
- 210000001268 chyle Anatomy 0.000 description 3
- 210000004913 chyme Anatomy 0.000 description 3
- 238000013135 deep learning Methods 0.000 description 3
- 201000010099 disease Diseases 0.000 description 3
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 description 3
- 238000001035 drying Methods 0.000 description 3
- 238000005401 electroluminescence Methods 0.000 description 3
- 210000003060 endolymph Anatomy 0.000 description 3
- 238000005516 engineering process Methods 0.000 description 3
- 210000003743 erythrocyte Anatomy 0.000 description 3
- 210000003608 fece Anatomy 0.000 description 3
- 238000001914 filtration Methods 0.000 description 3
- 210000003811 finger Anatomy 0.000 description 3
- 239000000834 fixative Substances 0.000 description 3
- 210000004051 gastric juice Anatomy 0.000 description 3
- 230000036541 health Effects 0.000 description 3
- 210000004251 human milk Anatomy 0.000 description 3
- 235000020256 human milk Nutrition 0.000 description 3
- 238000003364 immunohistochemistry Methods 0.000 description 3
- 238000004020 luminiscence type Methods 0.000 description 3
- 239000011159 matrix material Substances 0.000 description 3
- 238000005259 measurement Methods 0.000 description 3
- 238000000386 microscopy Methods 0.000 description 3
- 238000012544 monitoring process Methods 0.000 description 3
- 210000002569 neuron Anatomy 0.000 description 3
- 150000007523 nucleic acids Chemical class 0.000 description 3
- 210000004049 perilymph Anatomy 0.000 description 3
- 238000005424 photoluminescence Methods 0.000 description 3
- 210000002381 plasma Anatomy 0.000 description 3
- 210000004915 pus Anatomy 0.000 description 3
- 210000003296 saliva Anatomy 0.000 description 3
- 238000010845 search algorithm Methods 0.000 description 3
- 210000002374 sebum Anatomy 0.000 description 3
- 210000000582 semen Anatomy 0.000 description 3
- 210000002966 serum Anatomy 0.000 description 3
- 210000004243 sweat Anatomy 0.000 description 3
- 210000001179 synovial fluid Anatomy 0.000 description 3
- 210000001138 tear Anatomy 0.000 description 3
- 238000000844 transformation Methods 0.000 description 3
- 230000032258 transport Effects 0.000 description 3
- 210000002700 urine Anatomy 0.000 description 3
- 210000004127 vitreous body Anatomy 0.000 description 3
- 210000004916 vomit Anatomy 0.000 description 3
- 230000008673 vomiting Effects 0.000 description 3
- OCKKUZVCJCWWHM-UHFFFAOYSA-L (7-amino-8-methylphenoxazin-3-ylidene)-diethylazanium;dichlorozinc;dichloride Chemical compound [Cl-].[Cl-].[Cl-].[Cl-].[Zn+2].CC1=C(N)C=C2OC3=CC(=[N+](CC)CC)C=CC3=NC2=C1.CC1=C(N)C=C2OC3=CC(=[N+](CC)CC)C=CC3=NC2=C1 OCKKUZVCJCWWHM-UHFFFAOYSA-L 0.000 description 2
- 102100028175 Abasic site processing protein HMCES Human genes 0.000 description 2
- 102000002260 Alkaline Phosphatase Human genes 0.000 description 2
- 108020004774 Alkaline Phosphatase Proteins 0.000 description 2
- 241000196324 Embryophyta Species 0.000 description 2
- 101001006387 Homo sapiens Abasic site processing protein HMCES Proteins 0.000 description 2
- 101100537375 Homo sapiens TMEM107 gene Proteins 0.000 description 2
- 108010001336 Horseradish Peroxidase Proteins 0.000 description 2
- 108020004711 Nucleic Acid Probes Proteins 0.000 description 2
- 208000005228 Pericardial Effusion Diseases 0.000 description 2
- 208000036071 Rhinorrhea Diseases 0.000 description 2
- 206010039101 Rhinorrhoea Diseases 0.000 description 2
- 102100036728 Transmembrane protein 107 Human genes 0.000 description 2
- 230000003044 adaptive effect Effects 0.000 description 2
- 230000001464 adherent effect Effects 0.000 description 2
- 230000003321 amplification Effects 0.000 description 2
- 238000013459 approach Methods 0.000 description 2
- 238000013528 artificial neural network Methods 0.000 description 2
- 229940052223 basic fuchsin Drugs 0.000 description 2
- 239000000090 biomarker Substances 0.000 description 2
- 229960002685 biotin Drugs 0.000 description 2
- 235000020958 biotin Nutrition 0.000 description 2
- 239000011616 biotin Substances 0.000 description 2
- 230000000903 blocking effect Effects 0.000 description 2
- 230000002759 chromosomal effect Effects 0.000 description 2
- 210000000349 chromosome Anatomy 0.000 description 2
- 125000000853 cresyl group Chemical group C1(=CC=C(C=C1)C)* 0.000 description 2
- 238000007405 data analysis Methods 0.000 description 2
- 230000001419 dependent effect Effects 0.000 description 2
- 230000000694 effects Effects 0.000 description 2
- 230000007613 environmental effect Effects 0.000 description 2
- 239000010408 film Substances 0.000 description 2
- 235000013305 food Nutrition 0.000 description 2
- 210000004211 gastric acid Anatomy 0.000 description 2
- 230000003100 immobilizing effect Effects 0.000 description 2
- 238000011532 immunohistochemical staining Methods 0.000 description 2
- 210000000265 leukocyte Anatomy 0.000 description 2
- 210000002751 lymph Anatomy 0.000 description 2
- 239000012528 membrane Substances 0.000 description 2
- 108020004999 messenger RNA Proteins 0.000 description 2
- 238000001000 micrograph Methods 0.000 description 2
- 239000000203 mixture Substances 0.000 description 2
- 238000003199 nucleic acid amplification method Methods 0.000 description 2
- 239000002853 nucleic acid probe Substances 0.000 description 2
- 108020004707 nucleic acids Proteins 0.000 description 2
- 102000039446 nucleic acids Human genes 0.000 description 2
- 210000004912 pericardial fluid Anatomy 0.000 description 2
- 230000000737 periodic effect Effects 0.000 description 2
- 230000010076 replication Effects 0.000 description 2
- 230000004044 response Effects 0.000 description 2
- 239000010865 sewage Substances 0.000 description 2
- 239000007787 solid Substances 0.000 description 2
- 230000007480 spreading Effects 0.000 description 2
- 238000003892 spreading Methods 0.000 description 2
- 210000003813 thumb Anatomy 0.000 description 2
- 239000013598 vector Substances 0.000 description 2
- 238000005406 washing Methods 0.000 description 2
- XOSXWYQMOYSSKB-UHFFFAOYSA-L water blue Chemical compound [Na+].[Na+].[O-]S(=O)(=O)C1=C(N)C(C)=CC(C(=C2C=CC(C=C2)=NC=2C=CC(=CC=2)S([O-])(=O)=O)C=2C=CC(NC=3C=CC(=CC=3)S(O)(=O)=O)=CC=2)=C1 XOSXWYQMOYSSKB-UHFFFAOYSA-L 0.000 description 2
- FWBHETKCLVMNFS-UHFFFAOYSA-N 4',6-Diamino-2-phenylindol Chemical compound C1=CC(C(=N)N)=CC=C1C1=CC2=CC=C(C(N)=N)C=C2N1 FWBHETKCLVMNFS-UHFFFAOYSA-N 0.000 description 1
- QRXMUCSWCMTJGU-UHFFFAOYSA-N 5-bromo-4-chloro-3-indolyl phosphate Chemical compound C1=C(Br)C(Cl)=C2C(OP(O)(=O)O)=CNC2=C1 QRXMUCSWCMTJGU-UHFFFAOYSA-N 0.000 description 1
- 102100028780 AP-1 complex subunit sigma-2 Human genes 0.000 description 1
- 102100031650 C-X-C chemokine receptor type 4 Human genes 0.000 description 1
- 102100022210 COX assembly mitochondrial protein 2 homolog Human genes 0.000 description 1
- 108020004635 Complementary DNA Proteins 0.000 description 1
- 108020004394 Complementary RNA Proteins 0.000 description 1
- 241000255581 Drosophila <fruit fly, genus> Species 0.000 description 1
- 108090000790 Enzymes Proteins 0.000 description 1
- 102000004190 Enzymes Human genes 0.000 description 1
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 1
- 102100029203 F-box only protein 8 Human genes 0.000 description 1
- 101100321670 Fagopyrum esculentum FA18 gene Proteins 0.000 description 1
- 238000010867 Hoechst staining Methods 0.000 description 1
- 241000282412 Homo Species 0.000 description 1
- 101100055680 Homo sapiens AP1S2 gene Proteins 0.000 description 1
- 101000922348 Homo sapiens C-X-C chemokine receptor type 4 Proteins 0.000 description 1
- 101000900446 Homo sapiens COX assembly mitochondrial protein 2 homolog Proteins 0.000 description 1
- 101100280298 Homo sapiens FAM162A gene Proteins 0.000 description 1
- 101100334493 Homo sapiens FBXO8 gene Proteins 0.000 description 1
- 101100257194 Homo sapiens SMIM8 gene Proteins 0.000 description 1
- 101000741917 Homo sapiens Serine/threonine-protein phosphatase 1 regulatory subunit 10 Proteins 0.000 description 1
- 101000911790 Homo sapiens Sister chromatid cohesion protein DCC1 Proteins 0.000 description 1
- 101000631695 Homo sapiens Succinate dehydrogenase assembly factor 3, mitochondrial Proteins 0.000 description 1
- 108020005198 Long Noncoding RNA Proteins 0.000 description 1
- 241001465754 Metazoa Species 0.000 description 1
- 206010028980 Neoplasm Diseases 0.000 description 1
- CTQNGGLPUBDAKN-UHFFFAOYSA-N O-Xylene Chemical compound CC1=CC=CC=C1C CTQNGGLPUBDAKN-UHFFFAOYSA-N 0.000 description 1
- 108091034117 Oligonucleotide Proteins 0.000 description 1
- 101100170008 Oryza sativa subsp. japonica DBB1 gene Proteins 0.000 description 1
- 229930040373 Paraformaldehyde Natural products 0.000 description 1
- 102100023788 Protein FAM162A Human genes 0.000 description 1
- 108020004518 RNA Probes Proteins 0.000 description 1
- 239000003391 RNA probe Substances 0.000 description 1
- 101100127688 Saccharomyces cerevisiae (strain ATCC 204508 / S288c) FAA1 gene Proteins 0.000 description 1
- 101100127690 Saccharomyces cerevisiae (strain ATCC 204508 / S288c) FAA2 gene Proteins 0.000 description 1
- 102100038743 Serine/threonine-protein phosphatase 1 regulatory subunit 10 Human genes 0.000 description 1
- 102100027040 Sister chromatid cohesion protein DCC1 Human genes 0.000 description 1
- 102100024789 Small integral membrane protein 8 Human genes 0.000 description 1
- 102100028996 Succinate dehydrogenase assembly factor 3, mitochondrial Human genes 0.000 description 1
- GYDJEQRTZSCIOI-UHFFFAOYSA-N Tranexamic acid Chemical compound NCC1CCC(C(O)=O)CC1 GYDJEQRTZSCIOI-UHFFFAOYSA-N 0.000 description 1
- 238000010817 Wright-Giemsa staining Methods 0.000 description 1
- JLCPHMBAVCMARE-UHFFFAOYSA-N [3-[[3-[[3-[[3-[[3-[[3-[[3-[[3-[[3-[[3-[[3-[[5-(2-amino-6-oxo-1H-purin-9-yl)-3-[[3-[[3-[[3-[[3-[[3-[[5-(2-amino-6-oxo-1H-purin-9-yl)-3-[[5-(2-amino-6-oxo-1H-purin-9-yl)-3-hydroxyoxolan-2-yl]methoxy-hydroxyphosphoryl]oxyoxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(5-methyl-2,4-dioxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(6-aminopurin-9-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(6-aminopurin-9-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(6-aminopurin-9-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(6-aminopurin-9-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxyoxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(5-methyl-2,4-dioxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(4-amino-2-oxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(5-methyl-2,4-dioxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(5-methyl-2,4-dioxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(6-aminopurin-9-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(6-aminopurin-9-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(4-amino-2-oxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(4-amino-2-oxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(4-amino-2-oxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(6-aminopurin-9-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(4-amino-2-oxopyrimidin-1-yl)oxolan-2-yl]methyl [5-(6-aminopurin-9-yl)-2-(hydroxymethyl)oxolan-3-yl] hydrogen phosphate Polymers Cc1cn(C2CC(OP(O)(=O)OCC3OC(CC3OP(O)(=O)OCC3OC(CC3O)n3cnc4c3nc(N)[nH]c4=O)n3cnc4c3nc(N)[nH]c4=O)C(COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3CO)n3cnc4c(N)ncnc34)n3ccc(N)nc3=O)n3cnc4c(N)ncnc34)n3ccc(N)nc3=O)n3ccc(N)nc3=O)n3ccc(N)nc3=O)n3cnc4c(N)ncnc34)n3cnc4c(N)ncnc34)n3cc(C)c(=O)[nH]c3=O)n3cc(C)c(=O)[nH]c3=O)n3ccc(N)nc3=O)n3cc(C)c(=O)[nH]c3=O)n3cnc4c3nc(N)[nH]c4=O)n3cnc4c(N)ncnc34)n3cnc4c(N)ncnc34)n3cnc4c(N)ncnc34)n3cnc4c(N)ncnc34)O2)c(=O)[nH]c1=O JLCPHMBAVCMARE-UHFFFAOYSA-N 0.000 description 1
- AXIKDPDWFVPGOD-UHFFFAOYSA-O [7-(dimethylamino)phenothiazin-3-ylidene]-dimethylazanium;2-(2,4,5,7-tetrabromo-3,6-dihydroxyxanthen-10-ium-9-yl)benzoic acid Chemical compound C1=CC(=[N+](C)C)C=C2SC3=CC(N(C)C)=CC=C3N=C21.OC(=O)C1=CC=CC=C1C1=C(C=C(Br)C(O)=C2Br)C2=[O+]C2=C1C=C(Br)C(O)=C2Br AXIKDPDWFVPGOD-UHFFFAOYSA-O 0.000 description 1
- 230000001133 acceleration Effects 0.000 description 1
- 239000002253 acid Substances 0.000 description 1
- 239000000853 adhesive Substances 0.000 description 1
- 230000001070 adhesive effect Effects 0.000 description 1
- 238000000149 argon plasma sintering Methods 0.000 description 1
- 239000011324 bead Substances 0.000 description 1
- 239000011230 binding agent Substances 0.000 description 1
- 239000012148 binding buffer Substances 0.000 description 1
- 230000033228 biological regulation Effects 0.000 description 1
- 238000001574 biopsy Methods 0.000 description 1
- 210000000601 blood cell Anatomy 0.000 description 1
- 238000009534 blood test Methods 0.000 description 1
- 239000010839 body fluid Substances 0.000 description 1
- 239000011449 brick Substances 0.000 description 1
- 239000000872 buffer Substances 0.000 description 1
- 238000010804 cDNA synthesis Methods 0.000 description 1
- 238000004364 calculation method Methods 0.000 description 1
- 201000011510 cancer Diseases 0.000 description 1
- 230000001413 cellular effect Effects 0.000 description 1
- 238000006243 chemical reaction Methods 0.000 description 1
- 238000004891 communication Methods 0.000 description 1
- 239000002299 complementary DNA Substances 0.000 description 1
- 239000003184 complementary RNA Substances 0.000 description 1
- 239000002361 compost Substances 0.000 description 1
- 150000001875 compounds Chemical class 0.000 description 1
- 238000004590 computer program Methods 0.000 description 1
- 239000004567 concrete Substances 0.000 description 1
- 238000010276 construction Methods 0.000 description 1
- 230000008094 contradictory effect Effects 0.000 description 1
- 238000012937 correction Methods 0.000 description 1
- 230000008021 deposition Effects 0.000 description 1
- 239000003599 detergent Substances 0.000 description 1
- 238000002405 diagnostic procedure Methods 0.000 description 1
- WZRZTHMJPHPAMU-UHFFFAOYSA-L disodium;(3e)-3-[(4-amino-3-sulfonatophenyl)-(4-amino-3-sulfophenyl)methylidene]-6-imino-5-methylcyclohexa-1,4-diene-1-sulfonate Chemical compound [Na+].[Na+].C1=C(S([O-])(=O)=O)C(=N)C(C)=CC1=C(C=1C=C(C(N)=CC=1)S([O-])(=O)=O)C1=CC=C(N)C(S(O)(=O)=O)=C1 WZRZTHMJPHPAMU-UHFFFAOYSA-L 0.000 description 1
- 238000006073 displacement reaction Methods 0.000 description 1
- 239000003651 drinking water Substances 0.000 description 1
- 235000020188 drinking water Nutrition 0.000 description 1
- 238000001493 electron microscopy Methods 0.000 description 1
- 229920005570 flexible polymer Polymers 0.000 description 1
- 238000007667 floating Methods 0.000 description 1
- GNBHRKFJIUUOQI-UHFFFAOYSA-N fluorescein Chemical compound O1C(=O)C2=CC=CC=C2C21C1=CC=C(O)C=C1OC1=CC(O)=CC=C21 GNBHRKFJIUUOQI-UHFFFAOYSA-N 0.000 description 1
- 238000002509 fluorescent in situ hybridization Methods 0.000 description 1
- 239000011521 glass Substances 0.000 description 1
- PCHJSUWPFVWCPO-UHFFFAOYSA-N gold Chemical compound [Au] PCHJSUWPFVWCPO-UHFFFAOYSA-N 0.000 description 1
- 238000005534 hematocrit Methods 0.000 description 1
- 238000009396 hybridization Methods 0.000 description 1
- 238000011065 in-situ storage Methods 0.000 description 1
- 238000005305 interferometry Methods 0.000 description 1
- 230000001926 lymphatic effect Effects 0.000 description 1
- 210000001161 mammalian embryo Anatomy 0.000 description 1
- 108091070501 miRNA Proteins 0.000 description 1
- 239000002679 microRNA Substances 0.000 description 1
- 238000012986 modification Methods 0.000 description 1
- 230000004048 modification Effects 0.000 description 1
- 238000012015 optical character recognition Methods 0.000 description 1
- 238000005457 optimization Methods 0.000 description 1
- 230000008520 organization Effects 0.000 description 1
- 229920002866 paraformaldehyde Polymers 0.000 description 1
- 239000002245 particle Substances 0.000 description 1
- 238000010827 pathological analysis Methods 0.000 description 1
- 230000010363 phase shift Effects 0.000 description 1
- 239000004033 plastic Substances 0.000 description 1
- 230000010287 polarization Effects 0.000 description 1
- 230000005855 radiation Effects 0.000 description 1
- 229910052704 radon Inorganic materials 0.000 description 1
- SYUHGPGVQRZVTB-UHFFFAOYSA-N radon atom Chemical compound [Rn] SYUHGPGVQRZVTB-UHFFFAOYSA-N 0.000 description 1
- 238000012124 rapid diagnostic test Methods 0.000 description 1
- 230000009467 reduction Effects 0.000 description 1
- 238000002310 reflectometry Methods 0.000 description 1
- 238000011160 research Methods 0.000 description 1
- PYWVYCXTNDRMGF-UHFFFAOYSA-N rhodamine B Chemical compound [Cl-].C=12C=CC(=[N+](CC)CC)C=C2OC2=CC(N(CC)CC)=CC=C2C=1C1=CC=CC=C1C(O)=O PYWVYCXTNDRMGF-UHFFFAOYSA-N 0.000 description 1
- 239000011435 rock Substances 0.000 description 1
- 239000004576 sand Substances 0.000 description 1
- 230000035945 sensitivity Effects 0.000 description 1
- 239000002689 soil Substances 0.000 description 1
- 238000007447 staining method Methods 0.000 description 1
- 230000003068 static effect Effects 0.000 description 1
- 210000002784 stomach Anatomy 0.000 description 1
- 238000003860 storage Methods 0.000 description 1
- 239000008399 tap water Substances 0.000 description 1
- 235000020679 tap water Nutrition 0.000 description 1
- JGVWCANSWKRBCS-UHFFFAOYSA-N tetramethylrhodamine thiocyanate Chemical compound [Cl-].C=12C=CC(N(C)C)=CC2=[O+]C2=CC(N(C)C)=CC=C2C=1C1=CC=C(SC#N)C=C1C(O)=O JGVWCANSWKRBCS-UHFFFAOYSA-N 0.000 description 1
- 239000010409 thin film Substances 0.000 description 1
- 230000036962 time dependent Effects 0.000 description 1
- 230000000007 visual effect Effects 0.000 description 1
- 239000001993 wax Substances 0.000 description 1
- 239000002023 wood Substances 0.000 description 1
- 239000008096 xylene Substances 0.000 description 1
Images
Classifications
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N21/00—Investigating or analysing materials by the use of optical means, i.e. using sub-millimetre waves, infrared, visible or ultraviolet light
- G01N21/84—Systems specially adapted for particular applications
- G01N21/8483—Investigating reagent band
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01L—CHEMICAL OR PHYSICAL LABORATORY APPARATUS FOR GENERAL USE
- B01L3/00—Containers or dishes for laboratory use, e.g. laboratory glassware; Droppers
- B01L3/50—Containers for the purpose of retaining a material to be analysed, e.g. test tubes
- B01L3/502—Containers for the purpose of retaining a material to be analysed, e.g. test tubes with fluid transport, e.g. in multi-compartment structures
- B01L3/5027—Containers for the purpose of retaining a material to be analysed, e.g. test tubes with fluid transport, e.g. in multi-compartment structures by integrated microfluidic structures, i.e. dimensions of channels and chambers are such that surface tension forces are important, e.g. lab-on-a-chip
- B01L3/502715—Containers for the purpose of retaining a material to be analysed, e.g. test tubes with fluid transport, e.g. in multi-compartment structures by integrated microfluidic structures, i.e. dimensions of channels and chambers are such that surface tension forces are important, e.g. lab-on-a-chip characterised by interfacing components, e.g. fluidic, electrical, optical or mechanical interfaces
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01L—CHEMICAL OR PHYSICAL LABORATORY APPARATUS FOR GENERAL USE
- B01L9/00—Supporting devices; Holding devices
- B01L9/52—Supports specially adapted for flat sample carriers, e.g. for plates, slides, chips
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N21/00—Investigating or analysing materials by the use of optical means, i.e. using sub-millimetre waves, infrared, visible or ultraviolet light
- G01N21/62—Systems in which the material investigated is excited whereby it emits light or causes a change in wavelength of the incident light
- G01N21/63—Systems in which the material investigated is excited whereby it emits light or causes a change in wavelength of the incident light optically excited
- G01N21/64—Fluorescence; Phosphorescence
- G01N21/645—Specially adapted constructive features of fluorimeters
- G01N21/6456—Spatial resolved fluorescence measurements; Imaging
- G01N21/6458—Fluorescence microscopy
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N21/00—Investigating or analysing materials by the use of optical means, i.e. using sub-millimetre waves, infrared, visible or ultraviolet light
- G01N21/75—Systems in which material is subjected to a chemical reaction, the progress or the result of the reaction being investigated
- G01N21/77—Systems in which material is subjected to a chemical reaction, the progress or the result of the reaction being investigated by observing the effect on a chemical indicator
- G01N21/78—Systems in which material is subjected to a chemical reaction, the progress or the result of the reaction being investigated by observing the effect on a chemical indicator producing a change of colour
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N21/00—Investigating or analysing materials by the use of optical means, i.e. using sub-millimetre waves, infrared, visible or ultraviolet light
- G01N21/84—Systems specially adapted for particular applications
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/483—Physical analysis of biological material
-
- G—PHYSICS
- G02—OPTICS
- G02B—OPTICAL ELEMENTS, SYSTEMS OR APPARATUS
- G02B21/00—Microscopes
- G02B21/0004—Microscopes specially adapted for specific applications
- G02B21/0008—Microscopes having a simple construction, e.g. portable microscopes
-
- G—PHYSICS
- G02—OPTICS
- G02B—OPTICAL ELEMENTS, SYSTEMS OR APPARATUS
- G02B21/00—Microscopes
- G02B21/0004—Microscopes specially adapted for specific applications
- G02B21/002—Scanning microscopes
- G02B21/0024—Confocal scanning microscopes (CSOMs) or confocal "macroscopes"; Accessories which are not restricted to use with CSOMs, e.g. sample holders
- G02B21/0052—Optical details of the image generation
- G02B21/0076—Optical details of the image generation arrangements using fluorescence or luminescence
-
- G—PHYSICS
- G02—OPTICS
- G02B—OPTICAL ELEMENTS, SYSTEMS OR APPARATUS
- G02B21/00—Microscopes
- G02B21/06—Means for illuminating specimens
- G02B21/08—Condensers
- G02B21/12—Condensers affording bright-field illumination
-
- G—PHYSICS
- G02—OPTICS
- G02B—OPTICAL ELEMENTS, SYSTEMS OR APPARATUS
- G02B21/00—Microscopes
- G02B21/16—Microscopes adapted for ultraviolet illumination ; Fluorescence microscopes
-
- G—PHYSICS
- G02—OPTICS
- G02B—OPTICAL ELEMENTS, SYSTEMS OR APPARATUS
- G02B21/00—Microscopes
- G02B21/24—Base structure
-
- G—PHYSICS
- G02—OPTICS
- G02B—OPTICAL ELEMENTS, SYSTEMS OR APPARATUS
- G02B7/00—Mountings, adjusting means, or light-tight connections, for optical elements
- G02B7/02—Mountings, adjusting means, or light-tight connections, for optical elements for lenses
- G02B7/023—Mountings, adjusting means, or light-tight connections, for optical elements for lenses permitting adjustment
-
- H—ELECTRICITY
- H04—ELECTRIC COMMUNICATION TECHNIQUE
- H04N—PICTORIAL COMMUNICATION, e.g. TELEVISION
- H04N23/00—Cameras or camera modules comprising electronic image sensors; Control thereof
- H04N23/50—Constructional details
- H04N23/51—Housings
-
- H—ELECTRICITY
- H04—ELECTRIC COMMUNICATION TECHNIQUE
- H04N—PICTORIAL COMMUNICATION, e.g. TELEVISION
- H04N23/00—Cameras or camera modules comprising electronic image sensors; Control thereof
- H04N23/50—Constructional details
- H04N23/55—Optical parts specially adapted for electronic image sensors; Mounting thereof
-
- H—ELECTRICITY
- H04—ELECTRIC COMMUNICATION TECHNIQUE
- H04N—PICTORIAL COMMUNICATION, e.g. TELEVISION
- H04N23/00—Cameras or camera modules comprising electronic image sensors; Control thereof
- H04N23/56—Cameras or camera modules comprising electronic image sensors; Control thereof provided with illuminating means
-
- H—ELECTRICITY
- H04—ELECTRIC COMMUNICATION TECHNIQUE
- H04N—PICTORIAL COMMUNICATION, e.g. TELEVISION
- H04N23/00—Cameras or camera modules comprising electronic image sensors; Control thereof
- H04N23/57—Mechanical or electrical details of cameras or camera modules specially adapted for being embedded in other devices
-
- H—ELECTRICITY
- H04—ELECTRIC COMMUNICATION TECHNIQUE
- H04N—PICTORIAL COMMUNICATION, e.g. TELEVISION
- H04N23/00—Cameras or camera modules comprising electronic image sensors; Control thereof
- H04N23/60—Control of cameras or camera modules
- H04N23/67—Focus control based on electronic image sensor signals
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01L—CHEMICAL OR PHYSICAL LABORATORY APPARATUS FOR GENERAL USE
- B01L2200/00—Solutions for specific problems relating to chemical or physical laboratory apparatus
- B01L2200/02—Adapting objects or devices to another
- B01L2200/025—Align devices or objects to ensure defined positions relative to each other
Landscapes
- Physics & Mathematics (AREA)
- Chemical & Material Sciences (AREA)
- Health & Medical Sciences (AREA)
- General Physics & Mathematics (AREA)
- Analytical Chemistry (AREA)
- Engineering & Computer Science (AREA)
- Life Sciences & Earth Sciences (AREA)
- Optics & Photonics (AREA)
- Signal Processing (AREA)
- Multimedia (AREA)
- General Health & Medical Sciences (AREA)
- Biochemistry (AREA)
- Immunology (AREA)
- Pathology (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Hematology (AREA)
- Biomedical Technology (AREA)
- Clinical Laboratory Science (AREA)
- Molecular Biology (AREA)
- Biophysics (AREA)
- Plasma & Fusion (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Dispersion Chemistry (AREA)
- Urology & Nephrology (AREA)
- Food Science & Technology (AREA)
- Medicinal Chemistry (AREA)
- Investigating, Analyzing Materials By Fluorescence Or Luminescence (AREA)
- Microscoopes, Condenser (AREA)
- Investigating Or Analysing Materials By Optical Means (AREA)
Description
この出願は、2017年2月8日に出願された米国仮特許出願第62/456.590号、2017年2月15日に出願された同第62/459,554号、および2017年2月16日に出願された同第62/460,075号、2017年2月8日に出願された第62/456,504号(ESX045PRV)、2017年2月16日に出願された第62/460,062号(ESX045PRV2)、および2017年2月9日に出願された第62/457,133号(ESX046PRV)(それらの全内容はあらゆる目的のために参照により本明細書に組み込まれる)に対する優先権を主張する。
とりわけ、本発明は、生物学的および化学的アッセイ、ならびに計算撮像を行うデバイスおよび方法に関する。
生物学的および化学的アッセイ(例えば、診断試験)では、多くの場合、撮像を含む簡単で高速かつ高感度のアッセイが必要である。本発明は、とりわけ、撮像を含む、簡単で高速かつ高感度のアッセイのためのデバイスおよび方法を提供する。
明視野および蛍光顕微鏡は、健康管理、疾患診断、科学教育などに広く応用されている試料のある特性を人々が検査できる非常に強力な技術である。しかしながら、従来、顕微鏡画像を撮影するには、一般の人々がアクセスが制限されている、高価な顕微鏡と、経験豊富な人員とが必要である。スマートフォンを明視野顕微鏡に変えることができる最近発明されたアクセサリがいくつか存在するが、明視野顕微鏡画像は試料の非常に限られた情報しか提供しない。
i.ホルダフレームと、
ii.ホルダフレームに取り外し可能に取り付けられている光学ボックスと、
を備え、
ホルダフレームが、モバイルデバイス上に取り外し可能に適合し、モバイルデバイスに組み込まれたカメラおよび照明源に光学ボックスを整列させるように構成され、
光学ボックスが、試料容器スロットおよび照明光学系を備える、光学アダプタ。
i.実施形態A1の光学アダプタと、
ii.第1のプレートおよび第2のプレートを備えるQMAXカードであって、第1のプレートおよび第2のプレートが、液体試料を200μm未満の均一な厚さの層に圧縮する、QMAXカードと、
iii.QMAXカードを収容し、光学ボックスにアサートされるように構成されたスライダと、
を備える、光学システム。
i.QMAXカードを受容しカメラの視野および焦点範囲の試料スライドに位置付けるように構成された、容器スロットと、
ii.試料の明視野顕微鏡画像を撮影するように構成された明視野照明光学系と、
iii.試料の蛍光顕微鏡画像を撮像するように構成された蛍光照明光学系と、
iv.光学ボックス内で内側および外側にスライドさせることにより、明視野照明光学系と蛍光照明光学系を切り替えるように構成されたレバーと、
を備える、先行する実施形態のいずれかに記載のアダプタまたはシステム。
比色アッセイは、健康監視、疾患診断、化学分析などに広く応用されている非常に強力な技術である。正確な比色アッセイ結果を得るための重要な要素は、色の変化を正確に定量化することである。従来、比色試験ストリップの色の変化は、色の変化を標準の色見本と比較することによって分析される。しかし、この比較は人間の目で行われ、環境の光条件によって容易に影響を受け、色の変化を定量化する精度が制限される。
比色アッセイは、健康監視、疾患診断、化学分析などに広く応用されている非常に強力な技術である。正確な比色アッセイ結果を得るための重要な要素は、色の変化を正確に定量化することである。従来、比色試験ストリップの色の変化は、色の変化を標準の色見本と比較することによって分析される。しかし、この比較は人間の目で行われ、環境の光条件によって容易に影響を受け、色の変化を定量化する精度が制限される。
1.ファイバリング照明器
光学アセンブリのいくつかの実施形態では、
A.側面照明リング(illunmring)ファイバの半径は10mmであり、
b.リングファイバの直径は、少なくとも5mm、10mm、15mm、20mm、25mm、30mm、40mm、50mm、60mm、80mm、もしくは100mm、またはいずれの2つの値間の範囲内であってよく、
c.リングファイバの断面の直径は、少なくとも0.5mm、1.0mm、1.5mm、2.0mm、2.5mm、3mm、4mm、5mm、6mm、8mm、もしくは10mm、またはいずれの2つの値間の範囲内であってよい。
d.外部イメージャレンズの直径は6mmであり、
e.イメージャレンズの直径は、少なくとも2mm、3mm、4mm、5mm、10mm、15mm、20mm、25mm、30mm、40mm、もしくは50mm、またはいずれの2つの値間の範囲内であってよい。
1.可動アーム上の第1の平面と光源との間の距離が、少なくとも0.5mm、2mm、4mm、8mm、10mm、20mm、50mm、100mm、またはいずれの2つの値間の範囲内であり得る、請求項3に記載の光学アセンブリ。
D-1.QMAX構造を有する断層撮影デバイス
ナノスケールの高解像度で生物学的検体のスライス可能な仮想3次元コピーを再構成する断層撮影デバイスが開示される。このデバイスは、図16-Aにあるように、撮像センサ、レンズ、およびQMAXデバイスからなる。
柱アレイは、各柱の上部に金属製のディスクを有する。金属製のディスクは、撮像センサによって撮影された画像の空間および高さの両方の較正についての較正信号を提供する。金属製のディスクの形状は、迅速な較正を容易にするように設計され得る。例えば、金属製のディスクの形状は、文字Eのようであってよく、このような柱アレイを図16-Bに示す。
断層撮影の目的は、生物学的検体のいくつかの投影を通して生物学的検体の3次元ボリュームを再構築することである。終端間の断層撮影には、光源、撮像、および3次元再構成が含まれる。
撮像センサによって捕捉される光は、検体から屈折する、検体から放射されるなどであり得る。
撮像部品は、撮像センサの投影を撮影する。投影は、異なる焦点距離、異なる角度、異なる照明などで撮影され得る。
(1)信号選択、これにより、撮影された画像の一部が選択される、
(2)信号強調、これにより、撮影された画像の一部または全体が強調される、
(3)信号変換、これにより、撮影された画像の一部または全体が、周波数表現、マルチスケール表現などの別の表現に変換される、
(4)信号複製、これにより、撮影された画像の一部が撮影された画像の別の部分、または撮影された画像の別の部分の表現に置き換えられる、
(5)または(1)~(4)の任意の組み合わせ(限定されないが、これらを含む)の目的のために使用することができる。
生物学的試料の3次元ボリュームをその投影から再構築することは、逆問題である。3次元体積再構成は、位相画像取得スキーム、逆投影スキーム、非線形近似スキーム、最適化スキームなどを用いることができる。
●焦点距離の計算
●位相画像取得
●高さ推定
●3次元ボリューム再構築
Lp=t×n
(1)画像もしくは画像ボリュームの一部が選択される信号選択、
(2)画像もしくは画像ボリュームの一部もしくは全体が強調される信号強調、
(3)画像もしくは画像ボリュームの一部もしくは全体が、周波数表現、マルチスケール表現などの別の表現に変換される信号変換、
(4)画像もしくは画像ボリュームの一部が、撮影された画像の別の部分、もしくは撮影された画像の別の部分の表現に置き換えられる信号複製、
(5)または(1)~(4)の任意の組み合わせ(限定されないが、これらを含む)のために、3次元ボリューム再構築に使用することができる。
DA1.QMAXデバイスと、イメージャと、を備える、試料撮像のためのデバイスであって、
(1)QMAXデバイスが、
第1のプレートと、第2のプレートと、スペーサと、を備え、
i.前記プレートが、異なる構成へと互いに対して移動可能であり、
ii.一方または両方のプレートが可撓性であり、
iii.プレートの各々が、そのそれぞれの内表面上に、変形可能な試料と接触するための試料接触領域を有し、
iv.プレートの一方または両方が、それぞれのプレートで固定される前記スペーサを備え、
v.スペーサが、所定の実質的に均一な高さ、および所定のスペーサ間距離を有し、
vi.スペーサの少なくとも1つが、試料接触領域内にあり、
構成のうちの1つは開放構成であり、開放構成では、2つのプレートが分離され、プレート間の間隔がスペーサによって調節されず、試料が、プレートの一方または両方に付着し、
構成のうちのもう1つは、開放構成において試料が付着した後に構成される閉鎖構成であり、閉鎖構成では、試料の少なくとも一部が、2つのプレートによって均一な厚さの層に圧縮され、層の均一な厚さが、2つのプレートの内表面によって限定され、プレートおよびスペーサによって調節され、
(2)イメージャが、均一な厚さの層の少なくとも一部から発せられる信号の画像を撮影するように構成されている、デバイス。
(1)QMAXデバイスが、第1のプレートと、第2のプレートと、スペーサと、を備え、
i.プレートが、異なる構成へと互いに対して移動可能であり、
ii.一方または両方のプレートが可撓性であり、
iii.プレートの各々が、そのそれぞれの内表面上に、変形可能な試料と接触するための試料接触領域を有し、
iv.プレートの一方または両方が、それぞれのプレートで固定されるスペーサを備え、
v.スペーサが、所定の実質的に均一な高さ、および所定のスペーサ間距離を有し、
vi.スペーサの少なくとも1つが、試料接触領域内にあり、
構成のうちの1つは開放構成であり、開放構成では、2つのプレートが分離され、プレート間の間隔がスペーサによって調節されず、試料が、プレートの一方または両方に付着し、
構成のうちのもう1つは、開放構成において前記試料が付着した後に構成される閉鎖構成であり、閉鎖構成では、試料の少なくとも一部が、2つのプレートによって均一な厚さの層に圧縮され、層の均一な厚さが、2つのプレートの内表面によって限定され、プレートおよびスペーサによって調節され、
(2)イメージャが、画像センサと、レンズと、を備え、
i.レンズが、均一な厚さの層の少なくとも一部から発せられる信号を集束させ、集束した信号を画像センサに投影するように構成されており、
ii.画像センサが、前記集束した信号の画像を撮影するように構成されており、
(3)ホルダが、QMAXデバイスとイメージャとの間の相対位置を調整するように構成されており、
(4)制御デバイスが、ホルダによって行われた位置調整を制御および/または推定し、前記画像を受信し、3次元ボリュームに再構築するためのハードウェアおよびソフトウェアを備える、システム。
(1)QMAXデバイスが、第1のプレートと、第2のプレートと、スペーサと、を備え、
i.プレートが、異なる構成へと互いに対して移動可能であり、
ii.一方または両方のプレートが可撓性であり、
iii.プレートの各々が、そのそれぞれの内表面上に、変形可能な試料と接触するための試料接触領域を有し、
iv.プレートの一方または両方が、それぞれのプレートで固定されるスペーサを備え、
v.スペーサが、所定の実質的に均一な高さ、および所定のスペーサ間距離を有し、
vi.スペーサの少なくとも1つが、試料接触領域内にあり、
構成のうちの1つは開放構成であり、開放構成では、2つのプレートが分離され、プレート間の間隔がスペーサによって調節されず、試料が、プレートの一方または両方に付着し、
構成のうちのもう1つは、開放構成において前記試料が付着した後に構成される閉鎖構成であり、閉鎖構成では、試料の少なくとも一部が、2つのプレートによって均一な厚さの層に圧縮され、層の均一な厚さが、2つのプレートの内表面によって限定され、プレートおよびスペーサによって調節され、
(2)イメージャが、焦点面を変更することが可能であり、画像センサと、レンズと、を備え、
i.レンズが、均一な厚さの層の少なくとも一部から発せられる信号を集束させ、集束した信号を画像センサに投影するように構成されており、
ii.画像センサが、前記集束した信号の画像を撮影するように構成されており、
iii.レンズが、単レンズ、またはいくつかのレンズで構成される複合レンズであり、
iv.レンズの少なくとも1つの素子レンズが、イメージセンサからの距離を変更してイメージャの焦点面を変更するように移動可能であり、
v.可動レンズが、コンピュータまたは手動で制御されるステッピングモーターおよび/または電磁力によって駆動され得、
かつ
(4)制御デバイスが、ホルダによって行われた位置調整を制御および/または推定し、前記画像を受信し、3次元ボリュームに再構築するためのハードウェアおよびソフトウェアを備える、システム。
(a)先行するデバイスまたはシステムの実施形態のいずれかに記載のQMAXデバイスに試料を付着させるステップと、
(b)(a)の後、QMAXデバイスの2つのプレートを使用して、試料の少なくとも一部を、プレートの試料接触表面によって限定される実質的に均一な厚さの層に圧縮するステップであって、層の均一な厚さがスペーサおよびプレートによって調節され、圧縮が、
2つのプレートを一緒にし、
並行してまたは順次のいずれかで、プレートの少なくとも一方の領域を適合押圧して、プレートを一緒に閉鎖構成へと押圧すること
を含み、適合押圧が、試料の少なくとも一部にわたってプレート上に実質的に均一な圧力を生じさせ、押圧が、プレートの試料接触表面間で試料の少なくとも一部を横方向に広げ、閉鎖構成が、均一な厚さ領域の層におけるプレート間の間隔がスペーサによって調節される構成である、前記ステップと、
(c)先行するデバイスまたはシステムの実施形態のいずれかに記載のイメージャを使用して、均一な厚さの層の少なくとも一部から発せられる信号の画像を撮影するステップと、
(d)QMAXデバイスとイメージャとの間の相対位置を調整し、ステップ(c)を繰り返すステップと、
(e)一連のステップ(c)の後、撮影された画像を、層の少なくとも一部の3次元ボリュームに再構築するステップであって、
適合押圧は、プレートの外表面の形状変化に関係なく、ある領域に適用される圧力を実質的に一定にする方法であり、
並行押圧は、目的の領域に同時に圧力を適用し、順次押圧は、目的の領域の一部に圧力を適用し、徐々に他の領域に移動する、前記ステップと、
を含む、方法。
(a)イメージャ内の可動レンズをコンピュータまたは手動で初期位置に制御するステップと、
(b)可動レンズの位置を焦点面の位置に対応させるステップと、
(c)イメージャの画像センサを使用して画像を撮影し、焦点面の位置を記録するステップと、
(d)可動レンズを次の位置に移動させる変位ステップをコンピュータまたは手動で追加するステップと、
(e)ステップ(b)~(d)を繰り返すステップと、
(f)一連のステップ(e)の後、異なる焦点面でいくつかの画像が撮影されるステップと、
を含む、方法。
i.一方または両方のプレートの試料接触領域が、各々がそれぞれの分析物に結合し、それを固定化する1つまたは複数の結合部位を備えるか、または
ii.一方または両方のプレートの試料接触領域が、各々が試薬(複数可)を収容する1つまたは複数の収容部位を備え、ステップ(c)の間または後に、試薬(複数可)が試料中に溶解および拡散し、試料が1つまたは複数の分析物を含むか、または
iii.分析物または標識が増幅部位から500nmである場合、各々分析物または分析物の標識からの信号を増幅することが可能である1つまたは複数の増幅部位、または
iv.i~iiiの任意の組み合わせである、先行する実施形態のいずれかに記載のデバイス。
(1)前記複数の較正柱が、閉鎖構成で2つのプレートの試料接触領域の間に設置され、互いに異なる高さを有し、これらはすべてスペーサの均一な高さよりも小さく、
(2)前記画像が、共通の光軸に沿った異なる焦点面で撮影され、
(3)制御デバイスが、(a)前記画像の各々の焦点スコアを計算するための、および(b)前記焦点スコアをルックアップテーブルと比較することにより、前記画像の各々が撮影される焦点面位置を推定するためのハードウェアとソフトウェアを備え、焦点スコアは、撮影された画像の各画素について計算された焦点の度合いのマトリックスであり、ルックアップテーブルは事前に決定されており、前記共通の光軸に沿った所定の焦点面位置の行、および対応する較正焦点スコアの行を含み、較正焦点スコアの各々は、対応する所定の焦点面で撮影された較正柱の画像に基づいて計算される、先行する実施形態のいずれかに記載のシステム。
(f)それらのそれぞれの再構成された3次元ボリュームに基づいて、赤血球、白血球、および/または血小板の容積を計算することをさらに含む、実施形態DC20に記載の方法。
(g)計算された容積に基づいて、平均赤血球容積(MCV)、ヘマトクリット、赤血球分布幅(RDW)、平均血小板容積(MPV)、血小板分布幅(PDW)、未熟血小板画分(IPF)、およびそれらの任意の組み合わせからなる群から選択される血液検査情報を決定することをさらに含む、実施形態DC21に記載の方法。
E-1.アッセイおよび撮像用QMAXデバイス
QMAXデバイス、イメージャ、およびコンピューティングユニットを備える、生物学的分析物の検出および位置特定のためのデバイスが開示される。QMAXデバイスで生物学的試料が推測される。試料に含まれる分析物の計数および位置は、本開示によって得られる。
開示される分析物の検出および位置特定は、機械学習のディープラーニングを用いる。機械学習アルゴリズムは、データから学習することができるアルゴリズムである。機械学習のより厳密な定義は、「Pによって測定されるTのタスクでのそのパフォーマンスがエクスペリエンスEによって向上する場合、タスクTのいくつかのクラスおよびパフォーマンス測定Pに関して、コンピュータプログラムはエクスペリエンスEから学習する」と言われている。それは、データから学習し、予測を行うことができるアルゴリズムの研究および構築を調査する。このようなアルゴリズムは、試料入力からモデルを構築することにより、データ駆動の予測または決定を行うことによって、後の厳密に静的なプログラム命令を克服する。
訓練段階では、注釈付きの訓練データが畳み込みニューラルネットワークに供給される。畳み込みニューラルネットワークは、既知のグリッドのようなトポロジーを有するデータを処理するための特殊な種類のニューラルネットワークである。例としては、一定の時間間隔で試料を取得する1Dグリッドとみなすことができる時系列データ、および画素の2Dグリッドとみなすことができる画像データが挙げられる。畳み込みネットワークは、実際のアプリケーションで非常に成功している。「畳み込みニューラルネットワーク」という名称は、ネットワークが畳み込みと呼ばれる数学的操作を用いることを示す。畳み込みは、特殊な種類の線形操作である。畳み込みネットワークは、それらの層の少なくとも1つで一般的な行列乗算の代わりに畳み込みを使用する単純なニューラルネットワークである。
予測段階では、検出コンポーネントが入力画像に適用され、位置特定コンポーネントがそれに続く。予測段階の出力は、各分析物の位置とともに、試料に含まれる分析物の計数である。
大域探索アルゴリズム(ヒートマップ)
入力:
ヒートマップ
出力:
軌跡
軌跡←{}
分類(ヒートマップ)
(ヒートマップは空ではない)とき{
s←表示(ヒートマップ)
D←{半径Rでのsとしてのディスク中心}
ヒートマップ=ヒートマップ¥D//ヒートマップからDを削除
軌跡にsを追加
}
●削除する項目がxrであり、その前の項目がxpであり、その次の項目がxfであると仮定する。
●前の項目xpについて、その次の項目を削除する項目の次の項目に再定義する。したがって、xpの次の項目が現在xfである。
●削除項目xrについて、その前の項目および次の項目の定義を解除し、順序付きリストから削除する。
●次の項目xfについて、その前の項目を削除した項目の前の項目に再定義する。したがって、xfの前の項目は現在xpである。
局所探索アルゴリズム(s、ヒートマップ)
入力:
s:開始位置(x、y)
ヒートマップ
出力:
s:局所ピークの位置。
値が>0の画素のみを考慮する。
網羅アルゴリズム(s、ヒートマップ)
入力:
s:局所ピークの位置。
ヒートマップ:
出力:
網羅:ピークで網羅された画素のセット:
位置特定アルゴリズム(ヒートマップ)
入力:
ヒートマップ
出力:
軌跡
軌跡←{}
画素←{ヒートマップからのすべての画素}
画素が空ではないとき{
s←画素からの任意の画素
s←局所探索(s、ヒートマップ)//sは現在局所ピークである
より良い局所ピークを得るために、sを取り囲む半径Rの局所領域をプローブする
r←網羅(s、ヒートマップ)
画素←画素¥r //網羅されているすべての画素を削除
軌跡にsを追加
EA1.データ分析のためのディープラーニングの方法であって、
(a)試験試料の画像を受信することであって、試料がQMAXデバイスに装填され、画像がQMAXデバイスに接続されたイメージャによって撮影され、画像が試験試料中の分析物からの検出可能な信号を含む、前記受信することと、
(b)検出モデルを用いて画像を分析し、画像の2Dデータアレイを生成することであって、2Dデータアレイが、画像内の各位置の分析物の確率データを含み、検出モデルが、
i.注釈付きデータセットを畳み込みニューラルネットワークに供給することであって、注釈付きデータセットが、試験試料と同じ種類であり、同じ分析物のための試料からである、前記供給すること、および
ii.畳み込みによる検出モデルを訓練および確立すること
を含む訓練プロセスを通して確立される、前記生成することと、
(c)2Dデータアレイを分析して、
i.信号リストプロセス、または
ii.局所探索プロセスにより局所信号ピークを検出することと、
(d)局所信号ピーク情報に基づいて分析物の量を計算することと、を含む、方法。
QMAXデバイスと、イメージャと、コンピューティングユニットと、を備える、データ分析のためのシステムであって、
(a)QMAXデバイスが、試験試料の少なくとも一部を非常に均一な厚さの層に圧縮するように構成されており、
(b)イメージャが、均一な厚さの層で試料の画像を生成するように構成され、画像が、試験試料中の分析物からの検出可能な信号を含み、
(c)コンピューティングユニットが、
i.イメージャから画像を受信し、
ii.検出モデルを用いて画像を分析し、画像の2Dデータアレイを生成し、ここで2Dデータアレイが、画像内の各位置の分析物の確率データを含み、検出モデルが、
注釈付きデータセットを畳み込みニューラルネットワークに供給することであって、注釈付きデータセットが、試験試料と同じ種類であり、同じ分析物のための試料からである、前記供給すること、および
畳み込みによる検出モデルを訓練および確立すること
を含む訓練プロセスを通して確立され、かつ
iii.(c)2Dデータアレイを分析して、信号リストプロセスまたは局所検索プロセスにより局所信号ピークを検出し、かつ
iv.局所信号ピーク情報に基づいて分析物の量を計算する
ように構成されている、システム。
i.2Dデータアレイから局所ピークを繰り返し検出することにより信号リストを確立し、検出された局所ピークを取り囲む局所領域を計算し、検出されたピークおよび局所領域データを順番に信号リストに移すことと、
ii.信号リストから最高信号および最高信号の周辺の信号を順次かつ繰り返し削除して、局所信号ピークを検出することと、を含む、実施形態EA1に記載の方法。
i.ランダムな点から開始して、2Dデータアレイの局所最大値を探索することと、
ii.値はより小さいが、ピークを取り囲む局所領域を計算することと、
iii.2Dデータアレイから局所最大値および周囲の小さい値を削除することと、
iv.ステップi~iiiを繰り返して、局所信号のピークを検出することと、を含む、実施形態EAの実施形態のいずれかに記載の方法。
F-1.組織染色および細胞撮像のためのQMAXデバイスの例
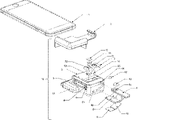
図18-Aは、ヒンジを有するまたは有さない一般的なQMAXデバイスの実施形態を示し、Q:定量化;M:拡大;A:試薬の添加;X:加速;圧縮調節オープンフロー(CROF)デバイスとも呼ばれる。一般的なQMAXデバイスは、第1のプレート10と、第2のプレート20とを備える。特に、パネル(A)は、第1のプレートがスペーサを有する、第1のプレート10および第2のプレート20の斜視図を示す。しかしながら、スペーサは、第2のプレート20(図示せず)または第1のプレート10および第2のプレート20(図示せず)の両方にも固定されることに留意されたい。パネル(B)は、開放構成で第1のプレート10上に試料90が付着する斜視図および断面図を示す。しかしながら、試料90は、第2のプレート20(図示せず)または第1のプレート10および第2のプレート20(図示せず)の両方にも付着することに留意されたい。パネル(c)は、(i)試料90を広げて(プレートの内表面間の試料の流れ)試料の厚さを低減するために第1のプレート10および第2のプレート20を使用する、および(ii)スペーサおよびプレートを使用して、QMAXデバイスの閉鎖構成で試料の厚さを調節することを図示する。各プレートの内表面は、1つもしくは複数の結合部位およびまたは収容部位(図示せず)を有してもよい。
i.光ルミネセンス、エレクトロルミネセンス、および電気化学ルミネセンスから選択されるルミネセンス、
ii.光の吸収、反射、透過、回折、散乱、または拡散、
iii.表面ラマン散乱、
iv.抵抗、静電容量、およびインダクタンスから選択される電気インピーダンス、
v.磁気緩和能、ならびに
vi.i~Vの任意の組み合わせからなる群から選択される。
いくつかの実施形態では、本発明のデバイスおよび方法は、試料で免疫組織化学を実施するのに有用である。
構成のうちの1つは開放構成であり、開放構成では、2つのプレートが完全または部分的に分離され、プレート間の間隔はスペーサによって調節されず、構成のうちのもう1つは、開放構成において試料およびIHC染色液が付着した後に構成される閉鎖構成であり、閉鎖構成では、試料の少なくとも一部は2つのプレート間にあり、染色液の少なくとも一部の層は試料の少なくとも一部と第2のプレートとの間にあり、染色液層の少なくとも一部の厚さは、プレート、試料、およびスペーサによって調節され、わずかなばらつきがあるが250μm以下である試料表面と第2のプレート表面との間の平均距離を有する。
いくつかの実施形態では、本発明のデバイスおよび方法は、H&E染色および特殊染色を実施するのに有用である。
いくつかの実施形態では、本発明のデバイスおよび方法は、組織学的試料でin situハイブリダイゼーション(ISH)を実施するのに有用である。
携帯電話を使用して組織試料を迅速に染色および分析するためのシステムも提供され、本システムは、
(a)上述の試料、染色液、およびデバイスと、
(b)モバイル通信デバイスであって、
i.試料を検出および/または撮像するための1つまたは複数のカメラ、
ii.検出された信号および/または試料の画像を受信および/または処理し、遠隔通信するための電子機器、信号プロセッサ、ハードウェア、およびソフトウェア
を備える、モバイル通信デバイスと、
(c)モバイル通信デバイスまたは外部源のいずれかからの光源と、
を備える。
(a)上述のシステムのデバイス上に組織試料および染色液を付着させ、2つのプレートを閉鎖構成に設置することと、
(b)撮像、データ処理、および通信のハードウェアおよびソフトウェアを有する携帯電話を得ることと、
(c)携帯電話によってCROFデバイスに付着した組織試料でアッセイして、結果を生成することと、
(d)携帯電話からの結果を携帯電話から離れた位置に通信することと、
を含む。
(a)組織試料を得ることと、
(b)染色液を得ることと、
(c)第1のプレートおよび第2のプレートを得ることであって、
プレートが、異なる構成へと互いに対して移動可能であり、
一方または両方のプレートが可撓性であり、
プレートの各々が、そのそれぞれの表面上に、組織試料またはIHC染色液と接触するための試料接触領域を有し、
第1のプレートの試料接触領域が滑らか5かつ平面であり、
第2のプレートの試料接触領域が、表面に固定され、所定の実質的に均一な高さおよび7μm~200μmの範囲の所定の一定のスペーサ間距離を有するスペーサを備える、
前記得ることと、
(c)プレートが開放構成に構成されているときに、組織試料および染色液をプレート上に付着させることであって、開放構成が、2つのプレートが部分的または完全にのいずれかに分離され、プレート間の間隔がスペーサによって調節されない構成である、前記付着させることと、
(d)(c)の後、2つのプレートを使用して、組織試料の少なくとも一部および染色液の少なくとも一部を閉鎖構成に圧縮することであって、
閉鎖構成では、試料の少なくとも一部は2つのプレート間にあり、染色液の少なくとも一部の層は試料の少なくとも一部と第2のプレートとの間にあり、染色液層の少なくとも一部の厚さは、プレート、試料、およびスペーサによって調節され、わずかなばらつきがあるが、250μm以下である試料表面と第2のプレート表面との間の平均距離を有する、
前記圧縮することと、
を含む。
(a)組織切片を得ることと、
(b)異なる構成へと互いに対して移動可能な第1および第2のプレートを得ることであって、各プレートが、実質的に平面である試料接触表面を有し、一方または両方のプレートが可撓性であり、プレートの一方または両方が、それぞれの試料接触表面で固定されているスペーサを含み、スペーサが、
i.所定の実質的に均一な高さ、
ii.実質的に均一な断面および平坦な上面を有する柱の形状、
iii.幅と高さとの比率が1以上、
iv.10μm~200μmの範囲である所定の一定のスペーサ間距離、
v.1%以上の充填率を有する、
前記得ることと、
(c)プレートが開放構成に構成されているときに、切片をプレートの一方または両方に付着させることであって、開放構成が、52つのプレートが部分的または完全にのいずれかに分離され、プレート間の間隔がスペーサによって調節されない構成である、前記付着させることと、
(d)(c)の後、2つのプレートを使用して、切片の少なくとも一部を、プレートの試料接触表面によって限定される実質的に均一な厚さの層に圧縮することであって、層の均一な厚さがスペーサおよびプレートによって調節され、10%未満のばらつきで1.8μm~3μmの範囲の平均値を有し、圧縮が、
2つのプレートを一緒にし、
並行してまたは順次のいずれかで、プレートの少なくとも一方の領域を適合押圧して、プレートを一緒に閉鎖構成へと押圧することを含み、適合押圧が、試料の少なくとも一部にわたってプレート上に実質的に均一な圧力を生じさせ、押圧が、プレートの試料接触表面間で試料の少なくとも一部を横方向に広げ、閉鎖構成が、均一な厚さ領域の層におけるプレート間の間隔がスペーサによって調節される構成である、
前記圧縮することと、
(e)プレートが閉鎖
構成である間に、均一な厚さの層の切片を分析することと、
を含み、
充填率は、全プレート面積に対するスペーサ接触面積の比率であり、
適合押圧は、プレートの外表面の形状変化に関係なく、ある領域に適用される圧力を実質的に一定にする方法であり、
並行押圧は、目的の領域に同時に圧力を適用し、順次押圧は、目的の領域の一部に圧力を適用し、徐々に他の領域に移動する。
FA1.組織試料を分析するためのデバイスであって、
第1のプレートと、第2のプレートと、スペーサと、を備え、
i.前記プレートが、異なる構成へと互いに対して移動可能であり、
ii.一方または両方のプレートが可撓性であり、
iii.プレートの各々が、そのそれぞれの内表面上に、染色液および/または標的分析物を含む疑いのある組織試料と接触するための試料接触領域を有し、
iv.プレートの一方または両方が、それぞれのプレートで固定されるスペーサを備え、
v.スペーサが、所定の実質的に均一な高さ、および所定のスペーサ間距離を有し、
vi.スペーサの少なくとも1つが、試料接触領域内にあり、
構成のうちの1つは開放構成であり、開放構成では、2つのプレートが部分的または全体的に分離され、プレート間の間隔がスペーサによって調節されず、染色液および試料が、プレートの一方または両方に付着し、
構成のうちのもう1つは、開放構成において染色液および試料が付着した後に構成される閉鎖構成であり、閉鎖構成では、試料の少なくとも一部が2つのプレート間にあり、染色液の少なくとも一部の層が試料の少なくとも一部と第2のプレートとの間にあり、染色液層の少なくとも一部の厚さが、プレート、試料、およびスペーサによって調節され、わずかなばらつきがあるが、250μm以下である試料表面と第2のプレート表面との間の平均距離を有する、デバイス。
第1のプレートと、第2のプレートと、スペーサと、を備え、
i.前記プレートが、異なる構成へと互いに対して移動可能であり、
ii.一方または両方のプレートが可撓性であり、
iii.プレートの各々が、そのそれぞれの内表面上に、移送溶液および/または標的分析物を含む疑いのある組織試料と接触するための試料接触領域を有し、
iv.プレートの一方または両方が、それぞれの試料接触領域上で乾燥され、移送溶液と接触すると、移送溶液に溶解し、組織試料を染色するように構成された染色剤を含み、
v.プレートの一方または両方が、それぞれのプレートで固定されるスペーサを備え、
vi.スペーサが、所定の実質的に均一な高さ、および所定のスペーサ間距離を有し、
vii.スペーサの少なくとも1つが、試料接触領域内にあり、
構成のうちの1つは開放構成であり、開放構成では、2つのプレートが部分的または全体的に分離され、プレート間の間隔がスペーサによって調節されず、染色液および試料が、プレートの一方または両方に付着し、
構成のうちのもう1つは、開放構成において染色液および試料が付着した後に構成される閉鎖構成であり、閉鎖構成では、試料の少なくとも一部が2つのプレート間にあり、移送溶液の少なくとも一部の層が試料の少なくとも一部と第2のプレートとの間にあり、移送溶液層の少なくとも一部の厚さが、プレート、試料、およびスペーサによって調節され、わずかなばらつきがあるが、250μm以下である試料表面と第2のプレート表面との間の平均距離を有する、デバイス。
(a)標的分析物を含む疑いのある組織試料および染色液を得るステップと、
(b)第1のプレートと、第2のプレートと、スペーサと、を得るステップであって、
i.プレートが、異なる構成へと互いに対して移動可能であり、
ii.一方または両方のプレートが可撓性であり、
iii.プレートの各々が、そのそれぞれの内表面上に、染色液および/または組織試料と接触するための試料接触領域を有し、
iv.プレートの一方または両方が、それぞれのプレートで固定されるスペーサを備え、
v.スペーサが、所定の実質的に均一な高さ、および所定のスペーサ間距離を有し、
vi.スペーサの少なくとも1つが、試料接触領域内にある、
前記得るステップと、
(c)プレートが開放構成にあるときに、プレートの一方または両方に染色液および組織試料を付着させるステップであって、
開放構成は、2つのプレートが部分的または全体的に分離され、2つのプレート間の間隔がスペーサによって調節されず、試料および染色液が、プレートの一方または両方に付着する構成である、
前記付着させるステップと、
(d)(c)の後、2つのプレートを合わせて、プレートを閉鎖構成へと押圧するステップであって、
押圧が、並行してまたは順次のいずれかで、プレートの少なくとも一方の領域を適合押圧して、プレートを一緒に閉鎖構成へと押圧することを含み、適合押圧が、試料の少なくとも一部にわたってプレート上に実質的に均一な圧力を生じさせ、押圧が、プレートの内表面間で試料の少なくとも一部を横方向に広げ、
構成のうちのもう1つは、開放構成において染色液および試料が付着した後に構成される閉鎖構成であり、閉鎖構成では、試料の少なくとも一部が2つのプレート間にあり、染色液の少なくとも一部の層が試料の少なくとも一部と第2のプレートとの間にあり、染色液層の少なくとも一部の厚さが、プレート、試料、およびスペーサによって調節され、わずかなばらつきがあるが、250μm以下である試料表面と第2のプレート表面との間の平均距離を有する、
前記押圧するステップと、
(e)プレートが閉鎖構成にあるときに標的分析物を分析するステップと、
を含む、方法。
(a)標的分析物を含む疑いのある組織試料および移送溶液を得るステップと、
(b)第1のプレートと、第2のプレートと、スペーサと、を得るステップであって、
i.プレートが、異なる構成へと互いに対して移動可能であり、
ii.一方または両方のプレートが可撓性であり、
iii.プレートの各々が、そのそれぞれの内表面上に、染色液および/または標的分析物を含む疑いのある組織試料と接触するための試料接触領域を有し、
iv.プレートの一方または両方が、それぞれの試料接触領域上にコーティングされ、移送溶液と接触すると、移送溶液に溶解し、組織試料を染色するように構成された染色剤を含み、
v.プレートの一方または両方が、それぞれのプレートで固定されるスペーサを備え、
vi.スペーサが、所定の実質的に均一な高さ、および所定のスペーサ間距離を有し、
vii.スペーサの少なくとも1つが、試料接触領域内にある、
前記得るステップと、
(c)プレートが開放構成にあるときに、プレートの一方または両方に染色液および組織試料を付着させるステップであって、
開放構成は、2つのプレートが部分的または全体的に分離され、2つのプレート間の間隔がスペーサによって調節されず、試料および染色液が、プレートの一方または両方に付着する構成である、前記付着させるステップと、
(d)(c)の後、2つのプレートを合わせて、プレートを閉鎖構成へと押圧するステップであって、
押圧が、並行してまたは順次のいずれかで、プレートの少なくとも一方の領域を適合押圧して、プレートを一緒に閉鎖構成へと押圧することを含み、適合押圧が、試料の少なくとも一部にわたってプレート上に実質的に均一な圧力を生じさせ、押圧が、プレートの内表面間で試料の少なくとも一部を横方向に広げ、
構成のうちのもう1つは、開放構成において染色液および試料が付着した後に構成される閉鎖構成であり、閉鎖構成では、試料の少なくとも一部が2つのプレート間にあり、染色液の少なくとも一部の層が試料の少なくとも一部と第2のプレートとの間にあり、染色液層の少なくとも一部の厚さが、プレート、試料、およびスペーサによって調節され、わずかなばらつきがあるが、250μm以下である試料表面と第2のプレート表面との間の平均距離を有する、
前記押圧するステップと、
(e)プレートが閉鎖構成にあるときに標的分析物を分析するステップと、
を含む、方法。
i.光ルミネセンス、エレクトロルミネセンス、および電気化学ルミネセンスから選択されるルミネセンス、
ii.光の吸収、反射、透過、回折、散乱、または拡散、
iii.表面ラマン散乱、
iv.抵抗、静電容量、およびインダクタンスから選択される電気インピーダンス、
v.磁気緩和能、ならびに
vi.i~Vの任意の組み合わせ
からなる群から選択される、実施形態FA21に記載のデバイス。
i.光ルミネセンス、エレクトロルミネセンス、および電気化学ルミネセンスから選択されるルミネセンス、
ii.光の吸収、反射、透過、回折、散乱、または拡散、
iii.表面ラマン散乱、
iv.抵抗、静電容量、およびインダクタンスから選択される電気インピーダンス、
v.磁気緩和能、ならびに
vi.i~Vの任意の組み合わせ
からなる群から選択される、実施形態FB21に記載のデバイス。
しかし最近では、デュアルカメラは最先端のスマートフォンでますます一般的になり、スマートフォンベースの撮像の可能性をさらに提示する。2つのカメラを使用することにより、試料の2つの異なる領域を同時に撮像でき、これは、はるかに大きな視野に相当する。さらに、各カメラを使用して、異なる解像度で顕微鏡撮像を行うことができる。例えば、1つのカメラは、低解像度だが試料内の大きな物体を撮像するためのより大きい視野で顕微鏡検査を行うことができ、もう1つのカメラは、高解像度だが小さな物体を撮像するためのより小さな視野で顕微鏡検査を行うことができる。これは、撮像用の試料が小さな物体と大きな物体との混在である場合に有用である。したがって、デュアルカメラに基づくスマートフォン撮像システムをユーザに提供することが非常に望ましい。
図19-Aは、デュアルカメラ撮像システムの概略図である。デュアルカメラ撮像システムは、2つの組み込まれたカメラモジュール、2つの外部レンズ、QMAXデバイス、および光源を有するモバイルコンピューティングデバイス(例えば、スマートフォン)を備える。各カメラモジュールは、内部レンズおよび画像センサを有する。QMAXデバイスは、2つのカメラモジュールの下に位置する。各外部レンズは、QMAXデバイスの試料が画像センサに明確に焦点を合わせることができる適切な高さで、QMAXデバイスとその対応する内部レンズとの間に設置される。各外部レンズは、その対応する内部レンズと整列される。撮像センサによって捕捉される光は、検体から屈折する、検体から放射されるなどであり得る。撮像センサによって捕捉される光は、可視波長を網羅し、QMAXデバイスの試料を通常または斜めの入射角で裏側または上側から照らすことができる。
一実施形態は、デュアルカメラ撮像システムが大きなFOV撮像に使用されることである。この実施形態では、両方のカメラによって撮影された画像は、同じ尺度または光学倍率を有する。これを実現するために、外部レンズ1の焦点距離fE1、内部レンズ1の焦点距離fN1、外部レンズ2の焦点距離fE2、および内部レンズ2の焦点距離fN2は、
レンズベースの撮像システムは、FOVのサイズと解像度との間でトレードオフがあるという本質的な欠点がある。大きなFOVを実現するには、撮像システムの解像度を犠牲にする必要がある。この問題は、大幅に異なるサイズスケールで試料が小さな物体と大きな物体との混在である場合により懸念される。十分な数の大きな物体を撮像するために、FOVを十分に大きくする必要があるが、小さな物体の詳細を得るための解像度が失われる。この問題を解決するために、この実施形態では、デュアルカメラ撮像システムを使用して、同じ試料でデュアル解像度撮影を実現する。この場合、カメラ1(または2)は低解像度および大きなFOV撮像に使用され、カメラ2(または1)は高解像度および小さなFOV撮像に使用される。
A1.デュアルレンズ撮像デバイスであって、
第1の外部レンズと、第2の外部レンズと、ハウジングユニットと、カードユニットと、を備え、
i.ハウジングユニットが、第1および第2の外部レンズ、ならびにカードユニットを収容し、デュアルレングス撮像デバイスをモバイルデバイスに接続するように構成されており、
ii.第1および第2の外部レンズが、モバイルデバイスの2つの内部レンズとそれぞれ整列するように構成されており、
iii.カードユニットが、試料を含む検体カードを収容するように構成されており、
カードユニットは、外部レンズと内部レンズとの間に位置付けられ、
外部レンズは、検体カードから屈折または放射される照明光をモバイルデバイスの画像センサに集束させ、画像センサが試料の画像を撮影できるように構成されている、デュアルレンズ撮像デバイス。
(a)実施形態A1のデュアルレンズ撮像デバイスと、
(b)デュアルレンズ撮像デバイスを介して試料の画像を撮影および処理するハードウェアおよびソフトウェアを備える、モバイルデバイスと、
を備える、デュアルレンズ撮像システム。
光源、単一のカメラ、およびコンピュータプロセッサを有する携帯撮像デバイスを使用して試料を撮像するための光学アダプタであって、
筐体と、
筐体内の空洞と、
空洞内のレバーと、
を備え、
レバーが、少なくとも1つの光学素子を備え、第1の位置と第2の位置との間で移動可能であるように構成され、(i)第1の位置では、撮像デバイスは、明視野モードで試料を撮像することが可能であり、(ii)第2の位置では、撮像デバイスは、蛍光励起モードで試料を撮像することが可能である、光学アダプタ。
筐体と、
カメラに視野を提供するように配置されたレンズと、
試料を受容しカメラの前記視野内に試料を位置付けるための筐体内の空洞であって、レンズが、カメラの視野内にあるときに試料によって屈折または放射される光を受光するように位置付けられている、空洞と、
空洞内のレバーと、
を備え、
レバーが、少なくとも1つの光学素子を備え、第1の位置と第2の位置との間で移動可能であるように構成され、(i)第1の位置では、撮像デバイスは、明視野モードで試料を撮像することが可能であり、(ii)第2の位置では、撮像デバイスは、蛍光励起モードで試料を撮像することが可能である、光学アダプタ。
筐体と、
試料を受容しカメラの視野内に試料を位置付けるための筐体内の空洞と、
空洞内のレバーと、
を備え、
レバーが、少なくとも1つの光学素子を備え、第1の位置と第2の位置との間で移動可能であるように構成され、(i)第1の位置では、撮像デバイスは、明視野モードで試料を撮像することが可能であり、(ii)第2の位置では、撮像デバイスは、蛍光励起モードで試料を撮像することが可能であり、
レバーが、第1の平面に沿って延在する第1の平面領域と、第1の平面領域から第1の方向に沿って横方向に変位し第2の平面に沿って延在する第2の平面領域と、を備え、第1の平面が、前記第2の平面から第2の方向に沿って異なる高さに配置され、第2の方向が、第1の方向と直交する、光学アダプタ。
筐体と、
試料を受容しカメラの視野内に試料を位置付けるための筐体内の空洞と、
空洞内のレバーと、
を備え、
レバーが、少なくとも1つの光学素子を備え、第1の位置と第2の位置との間で移動可能であるように構成され、(i)第1の位置では、撮像デバイスは、明視野モードで試料を撮像することが可能であり、(ii)第2の位置では、撮像デバイスは、蛍光励起モードで試料を撮像することが可能であり、
レバーが、第1の平面に沿って延在する第1の平面領域と、第1の平面領域から第1の方向に沿って横方向に変位し第2の平面に沿って延在する第2の平面領域と、を備え、第1の平面が、第2の平面から第2の方向に沿って異なる高さに配置され、第2の方向が、第1の方向と直交し、
第1の平面領域が、少なくとも1つの光学素子を備え、第2の平面領域が、少なくとも1つの光学素子を備える、光学アダプタ。
筐体と、
筐体内の空洞と、
空洞内のレバーと、
を備え、
レバーが、少なくとも1つの光学素子を備え、少なくとも3つの異なる位置の間で移動可能であるように構成され、(i)第1の位置では、撮像デバイスは、明視野モードで試料を撮像することが可能であり、(ii)第2の位置では、撮像デバイスは、蛍光励起モードで試料を撮像することが可能であり、(iii)第3の位置では、撮像デバイスは、試料の光吸収を測定することが可能である、光学アダプタ。
筐体と、
カメラに視野を提供するように構成されたレンズと、
試料を受容しカメラの視野内に試料を位置付けるための筐体内の空洞と、
筐体内の開口部であって、試料を照らすために光源から光源光を受光するように配置されている、開口部と、
空洞内のレバーと、
を備え、
レバーが、少なくとも1つの光学素子を備え、第1の位置と第2の位置との間で移動可能であるように構成され、(i)第1の位置では、撮像デバイスは、明視野モードで試料を撮像することが可能であり、(ii)第2の位置では、撮像デバイスは、蛍光励起モードで試料を撮像することが可能であり、蛍光励起モードでは、レンズは、試料が光源光によって照らされるときに試料によって放射される光を受光するように配置されている、光学アダプタ。
筐体と、
カメラに視野を提供するように構成されたレンズと、
試料を受容しカメラの視野内に試料を位置付けるための筐体内の空洞と、
空洞内のレバーと、
を備え、
レバーが、少なくとも1つの光学素子を備え、第1の位置と第2の位置との間で移動可能であるように構成され、(i)第1の位置では、撮像デバイスは、明視野モードで試料を撮像することが可能であり、(ii)第2の位置では、撮像デバイスは、蛍光励起モードで試料を撮像することが可能である、光学アダプタ。
筐体と、
筐体内の空洞と、
カメラに顕微鏡視野を提供するように構成されたレンズと、
空洞内の可動アームであって、可動アームが、第1の位置と第2の位置との間で切り替わるように構成可能であり、可動アームが第1の位置にあるとき、光学アセンブリは明視野モードにあり、可動アームが第2の位置にあるとき、光学アセンブリは蛍光励起モードにある、可動アームと、
を備える、光学アセンブリ。
空洞内の試料容器領域と、
筐体の側面上のスロットと、
を備え、スロットが、試料容器領域内に試料基板を受容しカメラの視野内に試料を位置付けるように配置されている、実施形態のいずれかに記載の光学アセンブリ。
光学アセンブリに結合するように構成された第1の側面および携帯電子デバイスに結合するように構成された第2の反対側の側面を備える携帯電話アタッチメントと、
を備え、携帯電子デバイスが、携帯電話である、システム。
筐体と、
筐体内の空洞と、
空洞内の複数の光学素子であって、筐体の第1の開口部から入る光を受光するように、および第1の開口部から入る光を第1の経路に沿って筐体の第2の開口部に向けて方向転換するように配置されている、複数の光学素子と、
筐体内の少なくとも2つの異なる位置で構成可能な可動アームと、
筐体内の少なくとも3つの異なる位置で構成可能な可動アームと、
を備え、
可動アームは、光を反射するための光反射体部分を備え、
可動アームは、光を均質化して光のコヒーレンスを破壊するための光拡散体を備え、
可動アームは、筐体の入口開口部と整列する開口部を備え、
可動アームが筐体内の第1の位置にあるとき、光反射体部分が、第1の開口部から入る光の複数の光学素子への入射を遮断するように、光反射体部分は筐体の入口開口部と複数の光学素子との間に位置付けられ、
可動アームが筐体内の第2の位置にあるとき、第1の開口部から入る光は、複数の光学素子に入射し、可動アームが筐体内の第3の位置にあるとき、第1の開口部から入る光は、可動アーム上の開口部を通過し、その後光拡散体に入射する、光学アセンブリ。
基板がスロット内に完全に挿入され、可動アームが筐体内の第2の位置にあるとき、第1の経路は試料基板と交差し、
試料基板がスロット内に完全に挿入され、可動アームが筐体内の第1の位置にあるとき、光反射体部分により反射された光は、試料基板へと方向転換され、
試料基板がスロット内に完全に挿入され、可動アームが筐体内の第3の位置にあるとき、光は第1の経路に沿って光拡散体に向かって進み、次に試料基板を照らす
ように、試料基板を受容するように配置されている、実施形態のいずれかに記載の光学アセンブリ。
光反射体部分の上に位置付けられた第1の容器と、
容器に装着された光学フィルタと、開口部部分の上に位置付けられた第2の容器と、容器に装着された光学フィルタと、
を備える、実施形態のいずれかに記載の光学アセンブリ。
光学アセンブリに結合するように構成された第1の側面を備え、携帯電話に結合するように構成された第2の反対側の側面を備える、携帯電話アタッチメントと、
を備え、携帯電話アタッチメントのサイズが調整可能である、システム。
カメラに顕微鏡視野を提供するように構成されたレンズと、
試料を受容し試料を前記顕微鏡視野内に位置付けるための容器と、
光源から光を受光するようにおよび容器を照らすように構成された光ファイバと、
を備える、光学アセンブリ。
光ファイバの第2の端面が、レンズの真下に位置する試料の領域を照らすように配置されている、実施形態のいずれかに記載の光学アセンブリ。
カメラに顕微鏡視野を提供するように構成されたレンズと、
試料を受容し試料を顕微鏡視野内に位置付けるための容器と、
レンズの光軸からオフセットされ、光源からの光を反射するようにおよび光軸に対して傾斜角の範囲にわたって試料を照らすように位置付けられたミラーと、
傾斜照明に応じて試料により放射される蛍光を通過させるために、試料とカメラとの間に位置付けられた波長フィルタと、
を備える、光学アセンブリ。
カメラに顕微鏡視野を提供するように構成されたレンズと、
試料を受容し試料を顕微鏡視野内に位置付けるための容器であって、
試料が、平面構造を備える試料ホルダによって支持され、容器が、平面構造を光源からの照明光の経路に部分的に延在するように位置付けて、照明光を平面構造に結合させかつ試料に蛍光を放射させるように構成されている、容器と、
照明に応じて試料により放射される蛍光を通過させるために、試料とカメラとの間に位置付けられた波長フィルタと、
を備える、光学アセンブリ。
第1のカメラモジュールに第1の顕微鏡視野を提供するように構成された第1のアセンブリレンズと、
第2のカメラモジュールに第2の顕微鏡視野を提供するように構成された第2のアセンブリレンズと、
試料を受容し試料を第1の顕微鏡視野内および第2の顕微鏡視野内に位置付けるための容器と、
を備える、光学アセンブリ。
第2のアセンブリレンズへの、または第2のアセンブリレンズからの第2の照明経路に配置される第2の光学フィルタと、
を備える、先行するいずれかの実施形態のいずれかに記載の光学アセンブリ。
第2のアセンブリレンズへの、または第2のアセンブリレンズからの第2の照明経路に配置される第2の偏光子と、
を備える、先行するいずれかの実施形態のいずれかに記載の光学アセンブリ。
カメラおよび少なくとも1つのレンズを備える撮像システムを使用して、試料の複数の画像を取得することであって、各画像が、試料の厚さ内の異なる物体平面に対応する、前記取得することと、
基準マークの1つ以上に基づいて、各画像を計算的に分析して対応する物体平面に関する情報を決定することと、
複数の画像および対応する物体平面に関する情報に基づいて、試料の3次元画像を計算的に構築することと、
を含む、撮像方法。
撮像システムに対して試料カートリッジを支持するための試料ホルダであって、2つのプレートを備える試料カートリッジが、スペーサのアレイによって互いに分離され、スペーサの少なくとも1つが基準マークを有し、撮像される試料が2つのプレート間で圧縮されるように構成されている、前記試料ホルダと、
試料ホルダおよびカメラに結合され、撮像システムを使用して試料の複数の画像を取得するように構成された、処理および制御システムであって、各画像が試料の厚さ内の異なる物体平面に対応する、前記処理および制御システムと、
を備え、
処理および制御システムは、
基準マークの1つ以上に基づいて、各画像を計算的に分析して対応する物体平面に関する情報を決定し、
複数の画像および対応する物体平面に関する情報に基づいて、試料の3次元画像を計算的に構築する
ようにさらに構成されている、撮像装置。
本発明は、様々な構成要素が互いに矛盾しない限り、複数の方法で組み合わせることができる様々な実施形態を含む。実施形態は、単一の発明出願とみなされるべきであり、各出願は、個別に独立しているものとしてではなく、参考文献として他の出願を有し、その全体およびすべての目的のためにも参照される。これらの実施形態は、現在の出願の開示だけでなく、本明細書で参照されるか、組み込まれるか、または優先権が主張される文書も含む。
本明細書で開示されるデバイス、システム、および方法の説明に使用される用語は、現在の出願、またはそれぞれ2016年8月10日および2016年9月14日に出願されたPCT出願(米国指定)第PCT/US2016/045437号および第PCT/US0216/051775号、2017年2月7日に出願された米国仮出願第62/456065号、2017年2月8日に出願された米国仮出願第62/426065号、2017年2月8日に出願された米国仮出願第62/456504号(これらの出願のすべてはすべての目的のためにそれらの全体が本明細書に組み込まれる)において定義されている。
本明細書で開示されるデバイス、システム、および方法は、試料の検出、分析、および定量化のために、Qカード、スペーサ、および均一な試料厚さの実施形態を含むか、または使用することができる。いくつかの実施形態では、Qカードは、試料の少なくとも一部を非常に均一性の層にするのに役立つスペーサを備える。スペーサの構造、材料、機能、変形、および寸法、ならびにスペーサおよび試料層の均一性は、本明細書に開示されるか、またはそれぞれ2016年8月10日および2016年9月14日に出願されたPCT出願(米国指定)第PCT/US2016/045437号および第PCT/US0216/051775号、2017年2月7日に出願された米国仮出願第62/456065号、2017年2月8日に出願された米国仮出願第62/426065号、2017年2月8日に出願された米国仮出願第62/456504号(これらの出願のすべてはすべての目的のためにそれらの全体が本明細書に組み込まれる)において列記、記載、および要約されている。
本明細書で開示されるデバイス、システム、および方法は、試料の検出、分析、および定量化のために、Qカードを含むか、または使用することができる。いくつかの実施形態では、Qカードは、Qカードの操作および試料の測定を容易にするのに役立つヒンジ、ノッチ、陥凹、およびスライダを備える。ヒンジ、ノッチ、陥凹、およびスライダの構造、材料、機能、変形、および寸法は、本明細書に開示されるか、またはそれぞれ2016年8月10日および2016年9月14日に出願されたPCT出願(米国指定)第PCT/US2016/045437号および第PCT/US0216/051775号、2017年2月7日に出願された米国仮出願第62/456065号、2017年2月8日に出願された米国仮出願第62/426065号、2017年2月8日に出願された米国仮出願第62/456504号(これらの出願のすべてはすべての目的のためにそれらの全体が本明細書に組み込まれる)において列記、記載、および要約されている。
本明細書で開示されるデバイス、システム、および方法は、試料の検出、分析、および定量化のために、Qカードを含むか、または使用することができる。いくつかの実施形態では、Qカードは、カードがスマートフォン検出システムによって読み取られることを可能にするスライダとともに使用される。Qカード、スライダ、およびスマートフォン検出システムの構造、材料、機能、変形、寸法、および接続は、本明細書に開示されるか、またはそれぞれ2016年8月10日および2016年9月14日に出願されたPCT出願(米国指定)第PCT/US2016/045437号および第PCT/US0216/051775号、2017年2月7日に出願された米国仮出願第62/456065号、2017年2月8日に出願された米国仮出願第62/426065号、2017年2月8日に出願された米国仮出願第62/456504号(これらの出願のすべてはすべての目的のためにそれらの全体が本明細書に組み込まれる)において列記、記載、および要約されている。
本明細書で開示されるデバイス、システム、および方法は、様々な種類の検出方法を含むか、または様々な種類の検出方法において使用され得る。検出方法は、本明細書に開示されるか、またはそれぞれ2016年8月10日および2016年9月14日に出願されたPCT出願(米国指定)第PCT/US2016/045437号および第PCT/US0216/051775号、2017年2月7日に出願された米国仮出願第62/456065号、2017年2月8日に出願された米国仮出願第62/426065号、2017年2月8日に出願された米国仮出願第62/456504号(これらの出願のすべてはすべての目的のためにそれらの全体が本明細書に組み込まれる)において列記、記載、および要約されている。
本明細書で開示されるデバイス、システム、および方法は、分析物検出に使用される様々な種類の標識を用いることができる。標識は、本明細書に開示されるか、またはそれぞれ2016年8月10日および2016年9月14日に出願されたPCT出願(米国指定)第PCT/US2016/045437号および第PCT/US0216/051775号、2017年2月7日に出願された米国仮出願第62/456065号、2017年2月8日に出願された米国仮出願第62/426065号、2017年2月8日に出願された米国仮出願第62/456504号(これらの出願のすべてはすべての目的のためにそれらの全体が本明細書に組み込まれる)において列記、記載、および要約されている。
本明細書に開示されるデバイス、システム、および方法は、様々な種類の分析物(バイオマーカーを含む)の操作および検出に適用することができる。分析物およびは、本明細書に開示されるか、またはそれぞれ2016年8月10日および2016年9月14日に出願されたPCT出願(米国指定)第PCT/US2016/045437号および第PCT/US0216/051775号、2017年2月7日に出願された米国仮出願第62/456065号、2017年2月8日に出願された米国仮出願第62/426065号、2017年2月8日に出願された米国仮出願第62/456504号(これらの出願のすべてはすべての目的のためにそれらの全体が本明細書に組み込まれる)において列記、記載、および要約されている。
本明細書で開示されるデバイス、システム、および方法は、様々な用途(分野および試料)に使用することができる。用途は、本明細書に開示されるか、またはそれぞれ2016年8月10日および2016年9月14日に出願されたPCT出願(米国指定)第PCT/US2016/045437号および第PCT/US0216/051775号、2017年2月7日に出願された米国仮出願第62/456065号、2017年2月8日に出願された米国仮出願第62/426065号、2017年2月8日に出願された米国仮出願第62/456504号(これらの出願のすべてはすべての目的のためにそれらの全体が本明細書に組み込まれる)において列記、記載、および要約されている。
本明細書で開示されるデバイス、システム、および方法は、データの転送、保存、および/または分析のためにクラウド技術を用いることができる。関連クラウド技術は、本明細書に開示されるか、またはそれぞれ2016年8月10日および2016年9月14日に出願されたPCT出願(米国指定)第PCT/US2016/045437号および第PCT/US0216/051775号、2017年2月7日に出願された米国仮出願第62/456065号、2017年2月8日に出願された米国仮出願第62/426065号、2017年2月8日に出願された米国仮出願第62/456504号(これらの出願のすべてはすべての目的のためにそれらの全体が本明細書に組み込まれる)において列記、記載、および要約されている。
本開示による本発明の主題のさらなる例は、以下に列挙される段落に記載される。
本発明はその詳細な説明と併せて説明されてきたが、前述の説明は、添付の特許請求の範囲によって定義される本発明の範囲を例示するものであり、限定するものではないことを理解されたい。
Claims (21)
- 光源、単一のカメラ、およびコンピュータプロセッサを有する携帯撮像デバイスを使用して試料を撮像するための光学アダプタであって、
筐体と、
前記筐体内の空洞と、
前記空洞内のレバーと、
を備え、
前記レバーが、少なくとも1つの光学素子を備え、第1の位置と第2の位置との間で移動可能であるように構成され、(i)前記第1の位置では、前記撮像デバイスは、明視野モードで試料を撮像することが可能であり、(ii)前記第2の位置では、前記撮像デバイスは、蛍光励起モードで前記試料を撮像することが可能であり、
前記レバーが、一緒に移動する第1のバーと第2のバーとをさらに備え、
前記第1のバーが、少なくとも1つの光学素子を備えた第1の平面を備え、
前記第2のバーが、少なくとも1つの光学素子を備えた第2の平面を備える、
光学アダプタ。 - 前記カメラに視野を提供するように配置されたレンズをさらに備える、請求項1に記載の光学アダプタ。
- 光源、単一のカメラ、およびコンピュータプロセッサを有する携帯撮像デバイスを使用して試料を撮像するための光学アダプタであって、
筐体と、
前記試料を受容し前記カメラの視野内に前記試料を位置付けるための前記筐体内の空洞と、
前記空洞内のレバーと、
を備え、
前記レバーが、少なくとも1つの光学素子を備え、第1の位置と第2の位置との間で移動可能であるように構成され、(i)前記第1の位置では、前記撮像デバイスは、明視野モードで試料を撮像することが可能であり、(ii)前記第2の位置では、前記撮像デバイスは、蛍光励起モードで前記試料を撮像することが可能であり、
前記レバーが、第1の平面に沿って延在する第1の平面領域と、前記第1の平面領域から第1の方向に沿って横方向に変位し第2の平面に沿って延在する第2の平面領域と、を備え、前記第1の平面が、前記第2の平面から第2の方向に沿って異なる高さに配置され、前記第2の方向が、前記第1の方向と直交する、光学アダプタ。 - 前記カメラに視野を提供するように配置されたレンズをさらに備える、請求項3に記載の光学アダプタ。
- 前記レバーが、少なくとも3つの異なる位置の間で移動可能であるように構成され、(i)第1の位置では、前記撮像デバイスは、明視野モードで試料を撮像することが可能であり、(ii)第2の位置では、前記撮像デバイスは、蛍光励起モードで前記試料を撮像することが可能であり、(iii)第3の位置では、前記撮像デバイスは、前記試料の光吸収を測定することが可能である、請求項1~4のいずれか一項に記載の光学アダプタ。
- 前記第1のバーが、帯域通過光学フィルタを備え、前記第2のバーが、前記第2のバーの前記第2の平面上に設置された光吸収体および前記第2のバーの傾斜面上に設置された反射ミラーを備え、かつ、前記フィルタと前記ミラーは蛍光照明光学系として動作する、請求項1または2に記載の光学アダプタ。
- 前記第1の平面は前記光源の下を移動し、前記第1の平面と前記光源との間の距離は0~5mmの範囲である、請求項1に記載の光学アダプタ。
- 前記レバーが異なる高さに前記第1の平面と前記第2の平面とを備え、前記第2のバーの一部は、画像平面と平行でなく、前記第2のバーの非平行部分の表面は、95%を超える高反射率の鏡面仕上げである、請求項1または2に記載の光学アダプタ。
- 蛍光照明光学系の光学素子が前記レバー上に設置されており、前記レバーが位置(ii)へとスライドすると、蛍光照明光学系素子は明視野照明光学系の光路を遮断し、照明光学系を蛍光照明光学系に切り替え、かつ、前記レバーが位置(i)へとスライドすると、前記レバー上に設置された前記蛍光照明光学系素子が光路から出て、照明光学系を明視野照明光学系に切り替える、請求項1または2に記載の光学アダプタ。
- 前記第2のバーの一部は、前記試料を撮像するための画像平面と平行ではない、請求項1または2に記載の光学アダプタ。
- 前記第2のバーの前記第2の平面が、画像平面と平行であり、前記試料から1mm~10mm離れている、請求項1または2に記載の光学アダプタ。
- 前記第2のバーの前記第2の平面が、画像平面と平行であり、前記第2の平面の表面が、高光吸収性であり、95%を超える光吸収率を有する、請求項1または2に記載の光学アダプタ。
- 前記レバー上に、前記レバーを前記アダプタに対してスライドさせたときに前記レバーを所定の位置で停止させるように構成された、ボールプランジャおよび溝を備える、請求項1または2に記載の光学アダプタ。
- 前記光学素子が、レンズ、フィルタ、ミラー、プリズム、またはビームスプリッタを含む、請求項1または2に記載の光学アダプタ。
- 第1の直角ミラーおよび第2の直角ミラーを含む複数の光学素子のセットをさらに備え、前記第1の直角ミラーおよび前記第2の直角ミラーが第1の経路にあり、前記光源からの光を反射して前記カメラに垂直に入射するように配置されている、請求項1または2に記載の光学アダプタ。
- ミラーおよび光吸収体を含む複数の光学素子の第2のセットをさらに備え、前記ミラーが光を反射して前記試料を斜めに照らし、前記光吸収体が前記蛍光励起モードにおいて第1の開口部からの外部光を吸収する、請求項1または2に記載の光学アダプタ。
- 光拡散体、第1の直角ミラー、および第2の直角ミラーを含む複数の光学素子のセットをさらに備え、前記第1の直角ミラーおよび第2の直角ミラーが第1の経路にあり、かつ前記光源からの光を前記光拡散体に向けて反射するように、およびその後前記カメラに垂直に入射するように配置されている、請求項1または2に記載の光学アダプタ。
- 前記第2のバーが前記第2の平面と傾斜面を備え、前記傾斜面の傾斜角が、少なくとも10度、30度、60度、80度、またはいずれの2つの値間の範囲内であり、前記傾斜角が、前記第2の平面と傾斜面との間の角度である、請求項1または2に記載の光学アダプタ。
- 前記第2のバーの前記第2の平面が傾斜面に接続されており、ミラーが前記傾斜面に設置されている、請求項1または2に記載の光学アダプタ。
- ロングパス光学フィルタをさらに備える、請求項1または2に記載の光学アダプタ。
- 前記筐体の第1の開口部から入る光を受光するように、および前記第1の開口部から入る光を第1の経路に沿って前記筐体の第2の開口部に向けて方向転換するように配置されている、複数の光学素子をさらに備える、請求項1または2に記載の光学アダプタ。
Applications Claiming Priority (17)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US201762456598P | 2017-02-08 | 2017-02-08 | |
| US201762456590P | 2017-02-08 | 2017-02-08 | |
| US201762456504P | 2017-02-08 | 2017-02-08 | |
| US62/456,504 | 2017-02-08 | ||
| US62/456,598 | 2017-02-08 | ||
| US62/456,590 | 2017-02-08 | ||
| US201762457133P | 2017-02-09 | 2017-02-09 | |
| US201762456904P | 2017-02-09 | 2017-02-09 | |
| US62/457,133 | 2017-02-09 | ||
| US62/456,904 | 2017-02-09 | ||
| US201762459554P | 2017-02-15 | 2017-02-15 | |
| US62/459,554 | 2017-02-15 | ||
| US201762460075P | 2017-02-16 | 2017-02-16 | |
| US201762460062P | 2017-02-16 | 2017-02-16 | |
| US62/460,062 | 2017-02-16 | ||
| US62/460,075 | 2017-02-16 | ||
| PCT/US2018/017504 WO2018148471A2 (en) | 2017-02-08 | 2018-02-08 | Optics, device, and system for assaying |
Publications (3)
| Publication Number | Publication Date |
|---|---|
| JP2020509403A JP2020509403A (ja) | 2020-03-26 |
| JP2020509403A5 JP2020509403A5 (ja) | 2021-03-18 |
| JP7177073B2 true JP7177073B2 (ja) | 2022-11-22 |
Family
ID=63107057
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2019543054A Active JP7177073B2 (ja) | 2017-02-08 | 2018-02-08 | アッセイ用の光学系、デバイス、およびシステム |
Country Status (5)
| Country | Link |
|---|---|
| EP (1) | EP3580597A4 (ja) |
| JP (1) | JP7177073B2 (ja) |
| CN (2) | CN116794819A (ja) |
| CA (1) | CA3053009A1 (ja) |
| WO (1) | WO2018148471A2 (ja) |
Families Citing this family (37)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP4321627A3 (en) | 2015-04-10 | 2024-04-17 | 10x Genomics Sweden AB | Spatially distinguished, multiplex nucleic acid analysis of biological specimens |
| US11719618B2 (en) * | 2018-08-28 | 2023-08-08 | Essenlix Corporation | Assay accuracy improvement |
| USD898221S1 (en) | 2018-11-15 | 2020-10-06 | Essenlix Corporation | Assay plate |
| USD897555S1 (en) | 2018-11-15 | 2020-09-29 | Essenlix Corporation | Assay card |
| USD898224S1 (en) | 2018-11-15 | 2020-10-06 | Essenlix Corporation | Assay plate with sample landing mark |
| USD898939S1 (en) | 2018-11-20 | 2020-10-13 | Essenlix Corporation | Assay plate with sample landing mark |
| USD893469S1 (en) | 2018-11-21 | 2020-08-18 | Essenlix Corporation | Phone holder |
| USD910202S1 (en) | 2018-11-21 | 2021-02-09 | Essenlix Corporation | Assay plate with sample landing mark |
| USD910203S1 (en) | 2018-11-27 | 2021-02-09 | Essenlix Corporation | Assay plate with sample landing mark |
| USD893470S1 (en) | 2018-11-28 | 2020-08-18 | Essenlix Corporation | Phone holder |
| USD912842S1 (en) | 2018-11-29 | 2021-03-09 | Essenlix Corporation | Assay plate |
| US20220064630A1 (en) | 2018-12-10 | 2022-03-03 | 10X Genomics, Inc. | Resolving spatial arrays using deconvolution |
| USD898222S1 (en) | 2019-01-18 | 2020-10-06 | Essenlix Corporation | Assay card |
| CN110297322A (zh) * | 2019-01-21 | 2019-10-01 | 福鼎市一雄光学仪器有限公司 | 内置光纤照明的手机高清近摄放大镜头装置 |
| CN111289443A (zh) * | 2019-07-03 | 2020-06-16 | 无锡市人民医院 | 一种便于进行循环利用的引流液比色卡及其比色方法 |
| WO2021003518A1 (en) * | 2019-07-11 | 2021-01-14 | Sensibility Pty Ltd | Machine learning based phone imaging system and analysis method |
| US20220276235A1 (en) * | 2019-07-18 | 2022-09-01 | Essenlix Corporation | Imaging based homogeneous assay |
| EP3798614A1 (en) * | 2019-09-30 | 2021-03-31 | IAssay, Inc. | Modular multiplex analysis devices and platforms |
| GB201918948D0 (en) | 2019-12-20 | 2020-02-05 | Oxford Immune Algorithmics Ltd | Portable device for imaging biological sample |
| CN113155555B (zh) * | 2020-01-23 | 2023-04-11 | 天津市政工程设计研究总院有限公司 | 用于模拟混凝土管廊的镁合金模型的制作方法 |
| US11768175B1 (en) | 2020-03-04 | 2023-09-26 | 10X Genomics, Inc. | Electrophoretic methods for spatial analysis |
| EP4153775B1 (en) | 2020-05-22 | 2024-07-24 | 10X Genomics, Inc. | Simultaneous spatio-temporal measurement of gene expression and cellular activity |
| US12031177B1 (en) | 2020-06-04 | 2024-07-09 | 10X Genomics, Inc. | Methods of enhancing spatial resolution of transcripts |
| EP4421186A3 (en) | 2020-06-08 | 2024-09-18 | 10X Genomics, Inc. | Methods of determining a surgical margin and methods of use thereof |
| AU2021288090A1 (en) * | 2020-06-10 | 2023-01-19 | 10X Genomics, Inc. | Fluid delivery methods |
| US20220020481A1 (en) | 2020-07-20 | 2022-01-20 | Abbott Laboratories | Digital pass verification systems and methods |
| CN116419709A (zh) * | 2020-08-23 | 2023-07-11 | 迈奥诊断公司 | 用于确定血红蛋白水平的设备和方法 |
| US20240033743A1 (en) * | 2020-09-18 | 2024-02-01 | 10X Genomics, Inc. | Sample handling apparatus and fluid delivery methods |
| CN112276370B (zh) * | 2020-11-27 | 2021-10-08 | 华中科技大学 | 一种基于空间光调制器的三维码激光标刻方法及系统 |
| WO2022119459A1 (en) * | 2020-12-03 | 2022-06-09 | Pictor Limited | Device and method of analyte detection |
| EP4121555A1 (en) | 2020-12-21 | 2023-01-25 | 10X Genomics, Inc. | Methods, compositions, and systems for capturing probes and/or barcodes |
| WO2022149162A1 (en) * | 2021-01-06 | 2022-07-14 | Scopgenx Private Limited | A compact portable multimodal microscopy |
| US20240151737A1 (en) * | 2021-02-18 | 2024-05-09 | Peek Technologies, Inc. | Configurable diagnostic platform systems and methods for performing chemical test assays |
| EP4421491A2 (en) | 2021-02-19 | 2024-08-28 | 10X Genomics, Inc. | Method of using a modular assay support device |
| WO2022256503A1 (en) | 2021-06-03 | 2022-12-08 | 10X Genomics, Inc. | Methods, compositions, kits, and systems for enhancing analyte capture for spatial analysis |
| CN113984759B (zh) * | 2021-09-24 | 2023-12-12 | 暨南大学 | 一种光学即时检测系统、体液玻片成晶与检测方法 |
| WO2024092682A1 (zh) * | 2022-11-04 | 2024-05-10 | 深圳华大智造科技股份有限公司 | 一种光学系统及检测方法 |
Citations (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2005099786A (ja) | 2003-08-29 | 2005-04-14 | Olympus Corp | 顕微鏡の光学素子切換装置 |
| JP2014503822A (ja) | 2010-12-21 | 2014-02-13 | ザ リージェンツ オブ ザ ユニバーシティ オブ カリフォルニア | 携帯デバイスにおける小型かつ広視野の蛍光画像化 |
| WO2016011534A1 (en) | 2014-07-24 | 2016-01-28 | University Health Network | Collection and analysis of data for diagnostic purposes |
| JP2016526687A (ja) | 2013-07-12 | 2016-09-05 | カルロバッツ,ネベン | トランスビジュアル感度を有する汎用迅速診断検査リーダー |
| JP2016161550A (ja) | 2015-03-05 | 2016-09-05 | アークレイ株式会社 | 比色測定用アダプタ |
Family Cites Families (10)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US7372985B2 (en) * | 2003-08-15 | 2008-05-13 | Massachusetts Institute Of Technology | Systems and methods for volumetric tissue scanning microscopy |
| DE102004034975A1 (de) * | 2004-07-16 | 2006-02-16 | Carl Zeiss Jena Gmbh | Verfahren zur Erfassung von Bildern einer Probe mit einem Mikroskop |
| JP5080186B2 (ja) * | 2007-09-26 | 2012-11-21 | 富士フイルム株式会社 | 分子分析光検出方法およびそれに用いられる分子分析光検出装置、並びにサンプルプレート |
| WO2009088930A2 (en) * | 2008-01-02 | 2009-07-16 | The Regents Of The University Of California | High numerical aperture telemicroscopy apparatus |
| CN103181154A (zh) * | 2010-10-29 | 2013-06-26 | 加利福尼亚大学董事会 | 用于成像的手机显微镜装置和方法 |
| MX366844B (es) * | 2013-12-12 | 2019-07-26 | Mes Medical Electronic Systems Ltd | Dispositivo casero de pruebas. |
| TWI551269B (zh) * | 2014-03-21 | 2016-10-01 | 財團法人工業技術研究院 | 攜帶型分析裝置以及系統 |
| TWI533025B (zh) * | 2014-07-07 | 2016-05-11 | 億觀生物科技股份有限公司 | 可攜式顯微鏡裝置 |
| CN204439554U (zh) * | 2015-03-27 | 2015-07-01 | 华南师范大学 | 智能手机宽场荧光成像器 |
| US10068145B2 (en) * | 2015-07-30 | 2018-09-04 | Fuji Xerox Co., Ltd. | Photographing system configured to hold a pill |
-
2018
- 2018-02-08 CN CN202310507084.7A patent/CN116794819A/zh active Pending
- 2018-02-08 WO PCT/US2018/017504 patent/WO2018148471A2/en unknown
- 2018-02-08 EP EP18751754.5A patent/EP3580597A4/en active Pending
- 2018-02-08 JP JP2019543054A patent/JP7177073B2/ja active Active
- 2018-02-08 CA CA3053009A patent/CA3053009A1/en active Pending
- 2018-02-08 CN CN201880020973.8A patent/CN111465882B/zh active Active
Patent Citations (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2005099786A (ja) | 2003-08-29 | 2005-04-14 | Olympus Corp | 顕微鏡の光学素子切換装置 |
| JP2014503822A (ja) | 2010-12-21 | 2014-02-13 | ザ リージェンツ オブ ザ ユニバーシティ オブ カリフォルニア | 携帯デバイスにおける小型かつ広視野の蛍光画像化 |
| JP2016526687A (ja) | 2013-07-12 | 2016-09-05 | カルロバッツ,ネベン | トランスビジュアル感度を有する汎用迅速診断検査リーダー |
| WO2016011534A1 (en) | 2014-07-24 | 2016-01-28 | University Health Network | Collection and analysis of data for diagnostic purposes |
| JP2016161550A (ja) | 2015-03-05 | 2016-09-05 | アークレイ株式会社 | 比色測定用アダプタ |
Also Published As
| Publication number | Publication date |
|---|---|
| WO2018148471A2 (en) | 2018-08-16 |
| CN111465882B (zh) | 2023-05-26 |
| WO2018148471A3 (en) | 2018-10-04 |
| CA3053009A1 (en) | 2018-08-16 |
| CN111465882A (zh) | 2020-07-28 |
| JP2020509403A (ja) | 2020-03-26 |
| EP3580597A4 (en) | 2021-05-05 |
| EP3580597A2 (en) | 2019-12-18 |
| CN116794819A (zh) | 2023-09-22 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP7177073B2 (ja) | アッセイ用の光学系、デバイス、およびシステム | |
| US11463608B2 (en) | Image-based assay using mark-assisted machine learning | |
| JP7084959B2 (ja) | 試料、特に血液を分析するための装置及びシステム、並びにそれらの使用方法 | |
| US11842483B2 (en) | Systems for cell shape estimation | |
| US12120407B2 (en) | Image-based assay using mark-assisted machine learning | |
| US20200302603A1 (en) | Method of computing tumor spatial and inter-marker heterogeneity | |
| Liu et al. | Pocket MUSE: an affordable, versatile and high-performance fluorescence microscope using a smartphone | |
| US11326989B2 (en) | Devices and methods for tissue and cell staining | |
| US8916390B2 (en) | Portable rapid diagnostic test reader | |
| US11885952B2 (en) | Optics, device, and system for assaying and imaging | |
| JP2018532999A (ja) | 蒸気凝縮液、特に呼気凝縮液を採取し分析する装置及びシステム、並びにそれらの使用方法 | |
| US20140356864A1 (en) | Analysis of colorimetric or fluorometric test assays | |
| Trueb et al. | Robust visualization and discrimination of nanoparticles by interferometric imaging | |
| US9255884B2 (en) | Fluorescence strip, fluorescence excitation device and portable fluorescence analysis system with the same | |
| WO2020041781A1 (en) | Enhanced, rapid, homogeneous, cell staining and assay | |
| Deshmukh et al. | A confirmatory test for sperm in sexual assault samples using a microfluidic-integrated cell phone imaging system | |
| US20220065795A1 (en) | System and methods for remote assessment of a sample assay for disease diagnostics | |
| Gordon et al. | Low cost microscope for malarial parasitemia quantification in microfluidically generated blood smears | |
| Spaziani et al. | SERS optrode for human thyroglobulin detection in liquid biopsy | |
| JP2023501279A (ja) | 患者の細胞の画像をラベル付けする方法、およびそのためのコンピュータ化システム |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| RD01 | Notification of change of attorney |
Free format text: JAPANESE INTERMEDIATE CODE: A7426 Effective date: 20191016 |
|
| RD04 | Notification of resignation of power of attorney |
Free format text: JAPANESE INTERMEDIATE CODE: A7424 Effective date: 20210121 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20210208 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20210208 |
|
| A871 | Explanation of circumstances concerning accelerated examination |
Free format text: JAPANESE INTERMEDIATE CODE: A871 Effective date: 20210208 |
|
| A975 | Report on accelerated examination |
Free format text: JAPANESE INTERMEDIATE CODE: A971005 Effective date: 20210210 |
|
| A977 | Report on retrieval |
Free format text: JAPANESE INTERMEDIATE CODE: A971007 Effective date: 20210526 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20210531 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20210827 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20211129 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20220117 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20220414 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20220713 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20220912 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20221011 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20221110 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 7177073 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |