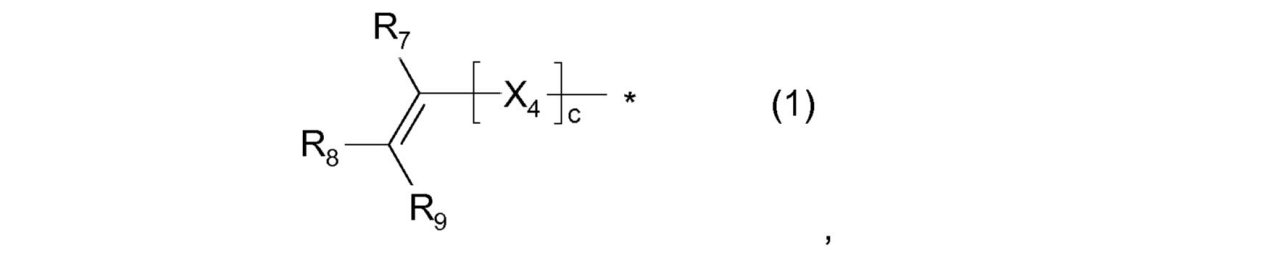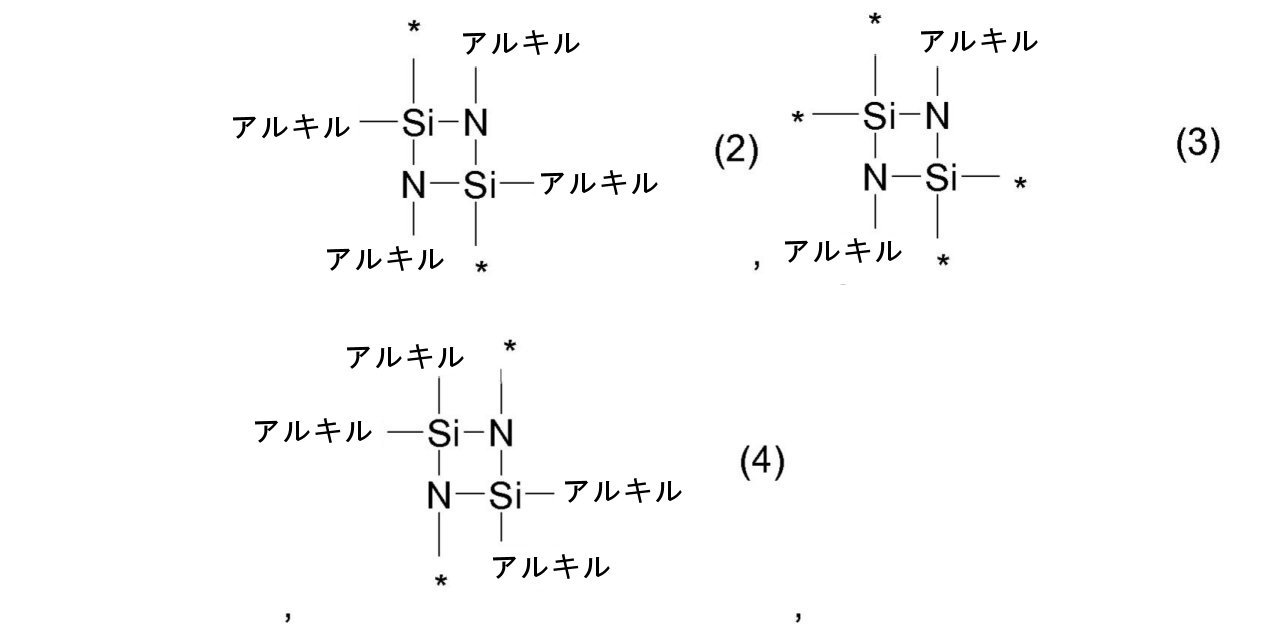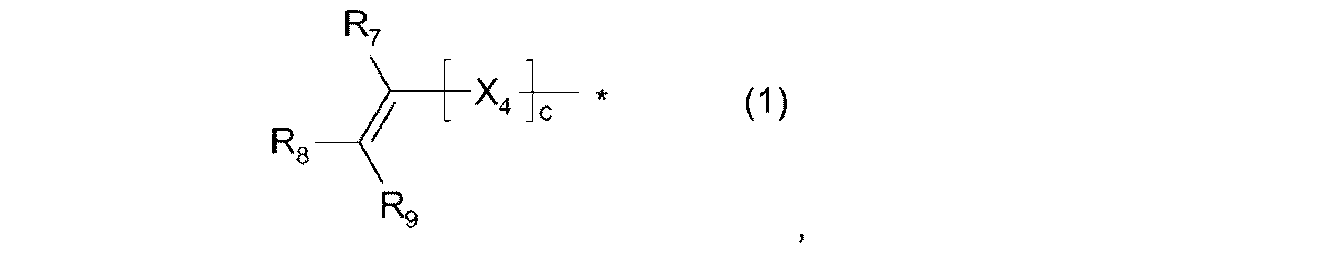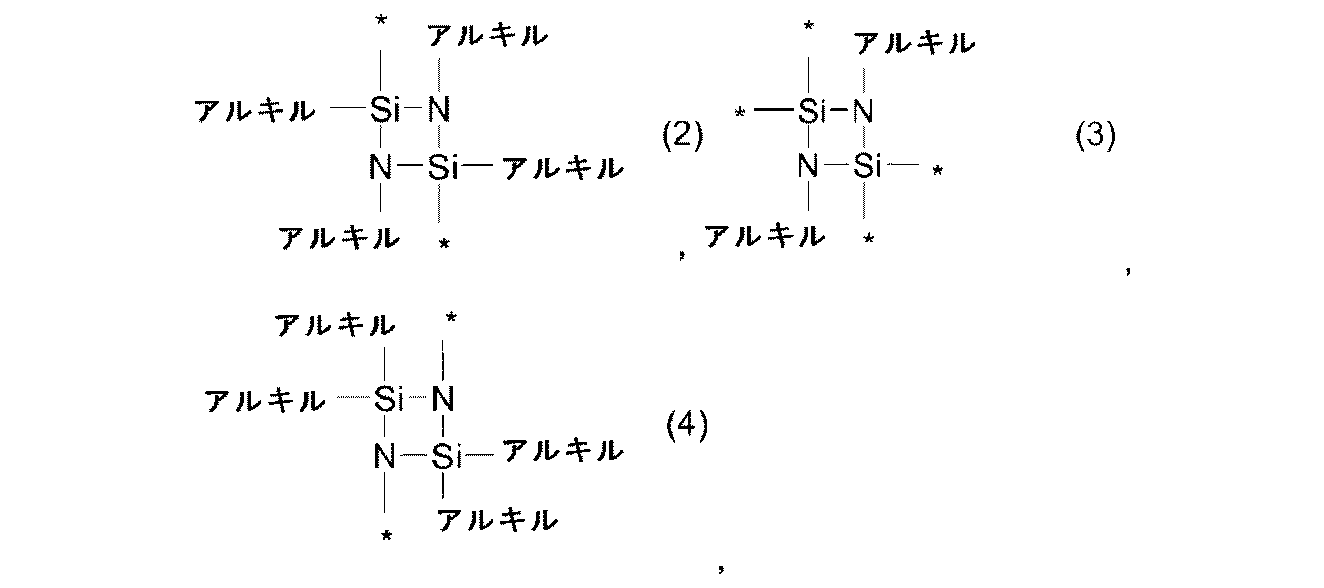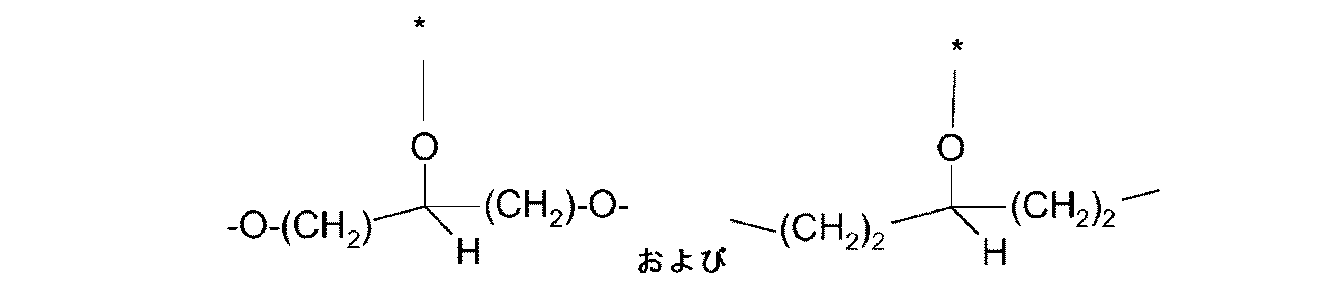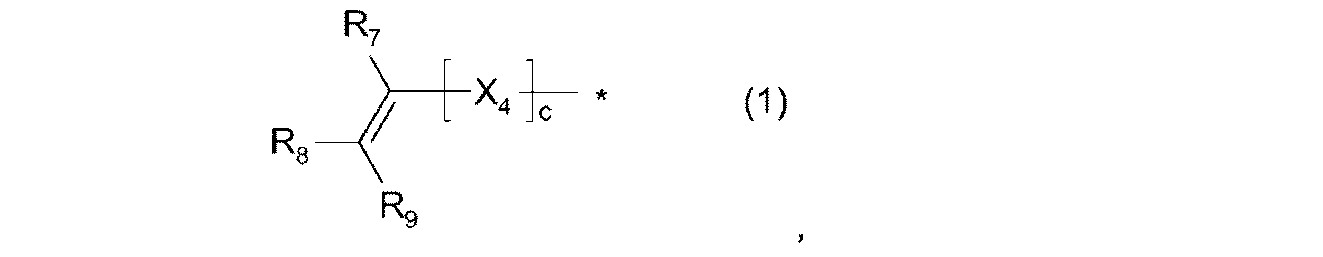JP7150737B2 - 光学活性デバイスのための化合物 - Google Patents
光学活性デバイスのための化合物 Download PDFInfo
- Publication number
- JP7150737B2 JP7150737B2 JP2019543965A JP2019543965A JP7150737B2 JP 7150737 B2 JP7150737 B2 JP 7150737B2 JP 2019543965 A JP2019543965 A JP 2019543965A JP 2019543965 A JP2019543965 A JP 2019543965A JP 7150737 B2 JP7150737 B2 JP 7150737B2
- Authority
- JP
- Japan
- Prior art keywords
- choh
- chcf
- atoms
- group
- linear
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D311/00—Heterocyclic compounds containing six-membered rings having one oxygen atom as the only hetero atom, condensed with other rings
- C07D311/02—Heterocyclic compounds containing six-membered rings having one oxygen atom as the only hetero atom, condensed with other rings ortho- or peri-condensed with carbocyclic rings or ring systems
- C07D311/04—Benzo[b]pyrans, not hydrogenated in the carbocyclic ring
- C07D311/06—Benzo[b]pyrans, not hydrogenated in the carbocyclic ring with oxygen or sulfur atoms directly attached in position 2
- C07D311/08—Benzo[b]pyrans, not hydrogenated in the carbocyclic ring with oxygen or sulfur atoms directly attached in position 2 not hydrogenated in the hetero ring
- C07D311/16—Benzo[b]pyrans, not hydrogenated in the carbocyclic ring with oxygen or sulfur atoms directly attached in position 2 not hydrogenated in the hetero ring substituted in position 7
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D407/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having oxygen atoms as the only ring hetero atoms, not provided for by group C07D405/00
- C07D407/02—Heterocyclic compounds containing two or more hetero rings, at least one ring having oxygen atoms as the only ring hetero atoms, not provided for by group C07D405/00 containing two hetero rings
- C07D407/12—Heterocyclic compounds containing two or more hetero rings, at least one ring having oxygen atoms as the only ring hetero atoms, not provided for by group C07D405/00 containing two hetero rings linked by a chain containing hetero atoms as chain links
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61F—FILTERS IMPLANTABLE INTO BLOOD VESSELS; PROSTHESES; DEVICES PROVIDING PATENCY TO, OR PREVENTING COLLAPSING OF, TUBULAR STRUCTURES OF THE BODY, e.g. STENTS; ORTHOPAEDIC, NURSING OR CONTRACEPTIVE DEVICES; FOMENTATION; TREATMENT OR PROTECTION OF EYES OR EARS; BANDAGES, DRESSINGS OR ABSORBENT PADS; FIRST-AID KITS
- A61F2/00—Filters implantable into blood vessels; Prostheses, i.e. artificial substitutes or replacements for parts of the body; Appliances for connecting them with the body; Devices providing patency to, or preventing collapsing of, tubular structures of the body, e.g. stents
- A61F2/02—Prostheses implantable into the body
- A61F2/14—Eye parts, e.g. lenses or corneal implants; Artificial eyes
- A61F2/16—Intraocular lenses
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D209/00—Heterocyclic compounds containing five-membered rings, condensed with other rings, with one nitrogen atom as the only ring hetero atom
- C07D209/02—Heterocyclic compounds containing five-membered rings, condensed with other rings, with one nitrogen atom as the only ring hetero atom condensed with one carbocyclic ring
- C07D209/04—Indoles; Hydrogenated indoles
- C07D209/08—Indoles; Hydrogenated indoles with only hydrogen atoms or radicals containing only hydrogen and carbon atoms, directly attached to carbon atoms of the hetero ring
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D209/00—Heterocyclic compounds containing five-membered rings, condensed with other rings, with one nitrogen atom as the only ring hetero atom
- C07D209/02—Heterocyclic compounds containing five-membered rings, condensed with other rings, with one nitrogen atom as the only ring hetero atom condensed with one carbocyclic ring
- C07D209/04—Indoles; Hydrogenated indoles
- C07D209/10—Indoles; Hydrogenated indoles with substituted hydrocarbon radicals attached to carbon atoms of the hetero ring
- C07D209/12—Radicals substituted by oxygen atoms
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D307/00—Heterocyclic compounds containing five-membered rings having one oxygen atom as the only ring hetero atom
- C07D307/77—Heterocyclic compounds containing five-membered rings having one oxygen atom as the only ring hetero atom ortho- or peri-condensed with carbocyclic rings or ring systems
- C07D307/78—Benzo [b] furans; Hydrogenated benzo [b] furans
- C07D307/79—Benzo [b] furans; Hydrogenated benzo [b] furans with only hydrogen atoms, hydrocarbon or substituted hydrocarbon radicals, directly attached to carbon atoms of the hetero ring
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D307/00—Heterocyclic compounds containing five-membered rings having one oxygen atom as the only ring hetero atom
- C07D307/77—Heterocyclic compounds containing five-membered rings having one oxygen atom as the only ring hetero atom ortho- or peri-condensed with carbocyclic rings or ring systems
- C07D307/78—Benzo [b] furans; Hydrogenated benzo [b] furans
- C07D307/79—Benzo [b] furans; Hydrogenated benzo [b] furans with only hydrogen atoms, hydrocarbon or substituted hydrocarbon radicals, directly attached to carbon atoms of the hetero ring
- C07D307/80—Radicals substituted by oxygen atoms
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D333/00—Heterocyclic compounds containing five-membered rings having one sulfur atom as the only ring hetero atom
- C07D333/50—Heterocyclic compounds containing five-membered rings having one sulfur atom as the only ring hetero atom condensed with carbocyclic rings or ring systems
- C07D333/52—Benzo[b]thiophenes; Hydrogenated benzo[b]thiophenes
- C07D333/54—Benzo[b]thiophenes; Hydrogenated benzo[b]thiophenes with only hydrogen atoms, hydrocarbon or substituted hydrocarbon radicals, directly attached to carbon atoms of the hetero ring
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D333/00—Heterocyclic compounds containing five-membered rings having one sulfur atom as the only ring hetero atom
- C07D333/50—Heterocyclic compounds containing five-membered rings having one sulfur atom as the only ring hetero atom condensed with carbocyclic rings or ring systems
- C07D333/52—Benzo[b]thiophenes; Hydrogenated benzo[b]thiophenes
- C07D333/54—Benzo[b]thiophenes; Hydrogenated benzo[b]thiophenes with only hydrogen atoms, hydrocarbon or substituted hydrocarbon radicals, directly attached to carbon atoms of the hetero ring
- C07D333/56—Radicals substituted by oxygen atoms
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D335/00—Heterocyclic compounds containing six-membered rings having one sulfur atom as the only ring hetero atom
- C07D335/04—Heterocyclic compounds containing six-membered rings having one sulfur atom as the only ring hetero atom condensed with carbocyclic rings or ring systems
- C07D335/06—Benzothiopyrans; Hydrogenated benzothiopyrans
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D401/00—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom
- C07D401/02—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom containing two hetero rings
- C07D401/12—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom containing two hetero rings linked by a chain containing hetero atoms as chain links
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D409/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having sulfur atoms as the only ring hetero atoms
- C07D409/02—Heterocyclic compounds containing two or more hetero rings, at least one ring having sulfur atoms as the only ring hetero atoms containing two hetero rings
- C07D409/12—Heterocyclic compounds containing two or more hetero rings, at least one ring having sulfur atoms as the only ring hetero atoms containing two hetero rings linked by a chain containing hetero atoms as chain links
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08F—MACROMOLECULAR COMPOUNDS OBTAINED BY REACTIONS ONLY INVOLVING CARBON-TO-CARBON UNSATURATED BONDS
- C08F124/00—Homopolymers of compounds having one or more unsaturated aliphatic radicals, each having only one carbon-to-carbon double bond, and at least one being terminated by a heterocyclic ring containing oxygen
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08F—MACROMOLECULAR COMPOUNDS OBTAINED BY REACTIONS ONLY INVOLVING CARBON-TO-CARBON UNSATURATED BONDS
- C08F126/00—Homopolymers of compounds having one or more unsaturated aliphatic radicals, each having only one carbon-to-carbon double bond, and at least one being terminated by a single or double bond to nitrogen or by a heterocyclic ring containing nitrogen
- C08F126/06—Homopolymers of compounds having one or more unsaturated aliphatic radicals, each having only one carbon-to-carbon double bond, and at least one being terminated by a single or double bond to nitrogen or by a heterocyclic ring containing nitrogen by a heterocyclic ring containing nitrogen
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08F—MACROMOLECULAR COMPOUNDS OBTAINED BY REACTIONS ONLY INVOLVING CARBON-TO-CARBON UNSATURATED BONDS
- C08F128/00—Homopolymers of compounds having one or more unsaturated aliphatic radicals, each having only one carbon-to-carbon double bond, and at least one being terminated by a bond to sulfur or by a heterocyclic ring containing sulfur
- C08F128/06—Homopolymers of compounds having one or more unsaturated aliphatic radicals, each having only one carbon-to-carbon double bond, and at least one being terminated by a bond to sulfur or by a heterocyclic ring containing sulfur by a heterocyclic ring containing sulfur
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Health & Medical Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Medicinal Chemistry (AREA)
- Polymers & Plastics (AREA)
- Ophthalmology & Optometry (AREA)
- Heart & Thoracic Surgery (AREA)
- General Health & Medical Sciences (AREA)
- Transplantation (AREA)
- Engineering & Computer Science (AREA)
- Biomedical Technology (AREA)
- Cardiology (AREA)
- Vascular Medicine (AREA)
- Life Sciences & Earth Sciences (AREA)
- Animal Behavior & Ethology (AREA)
- Oral & Maxillofacial Surgery (AREA)
- Public Health (AREA)
- Veterinary Medicine (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Addition Polymer Or Copolymer, Post-Treatments, Or Chemical Modifications (AREA)
- Nitrogen Condensed Heterocyclic Rings (AREA)
- Materials For Medical Uses (AREA)
- Pyrane Compounds (AREA)
- Prostheses (AREA)
- Plural Heterocyclic Compounds (AREA)
- Organic Low-Molecular-Weight Compounds And Preparation Thereof (AREA)
Description
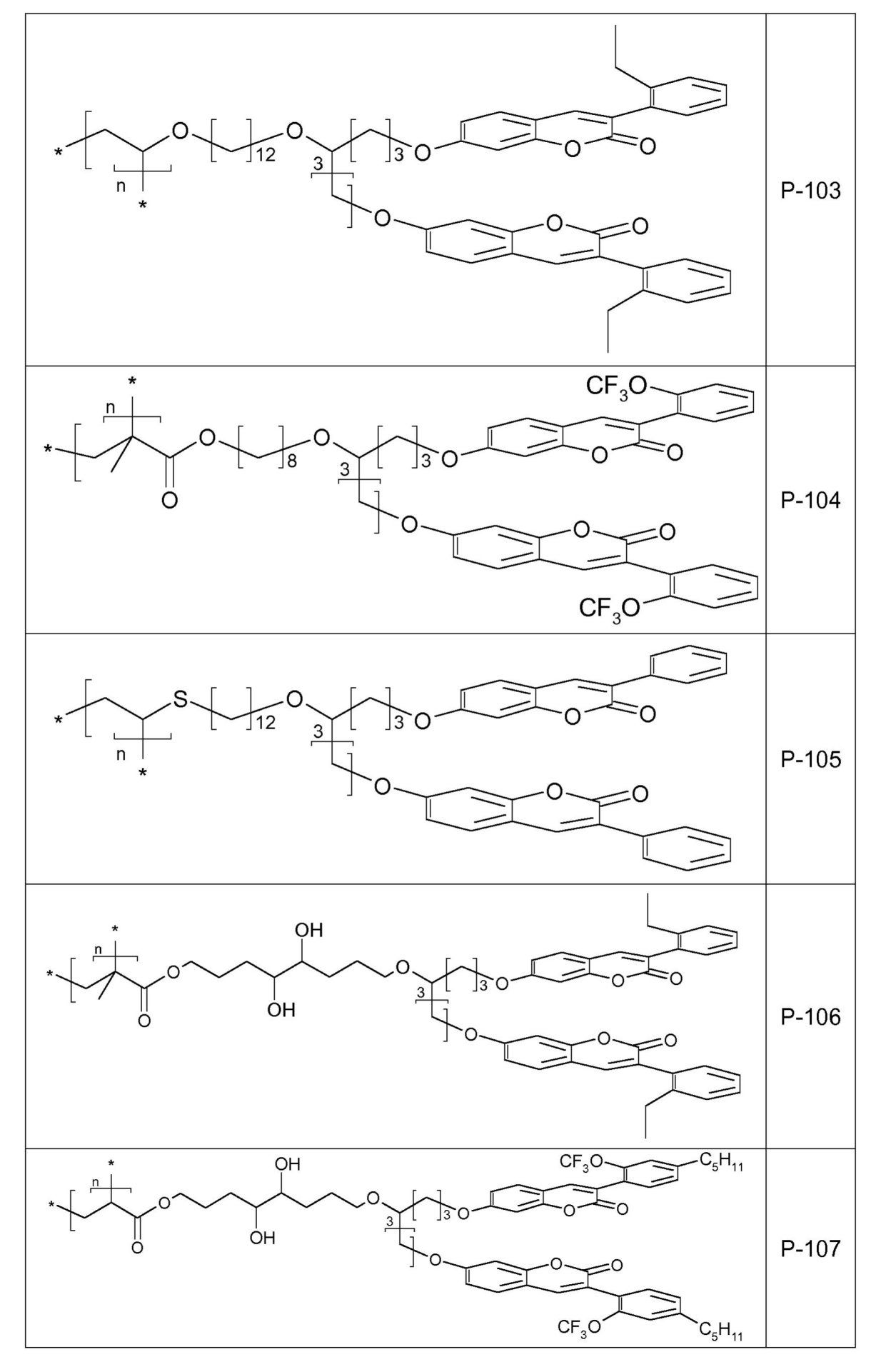
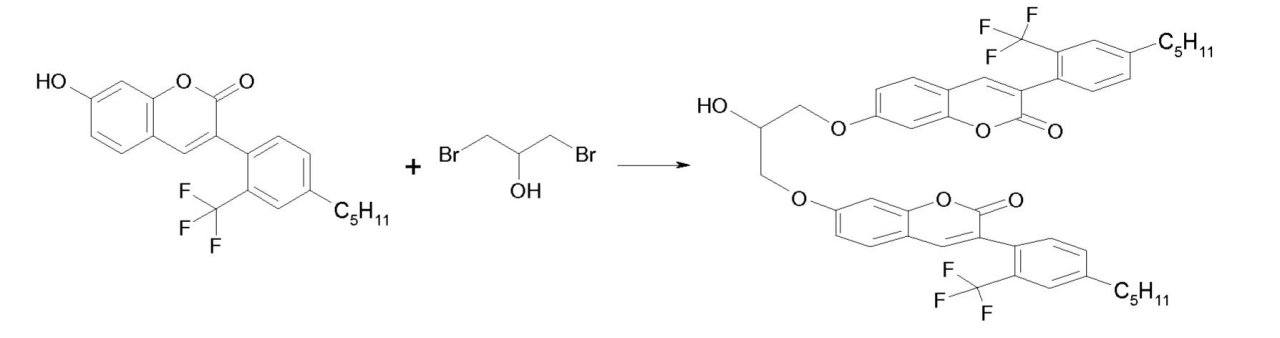
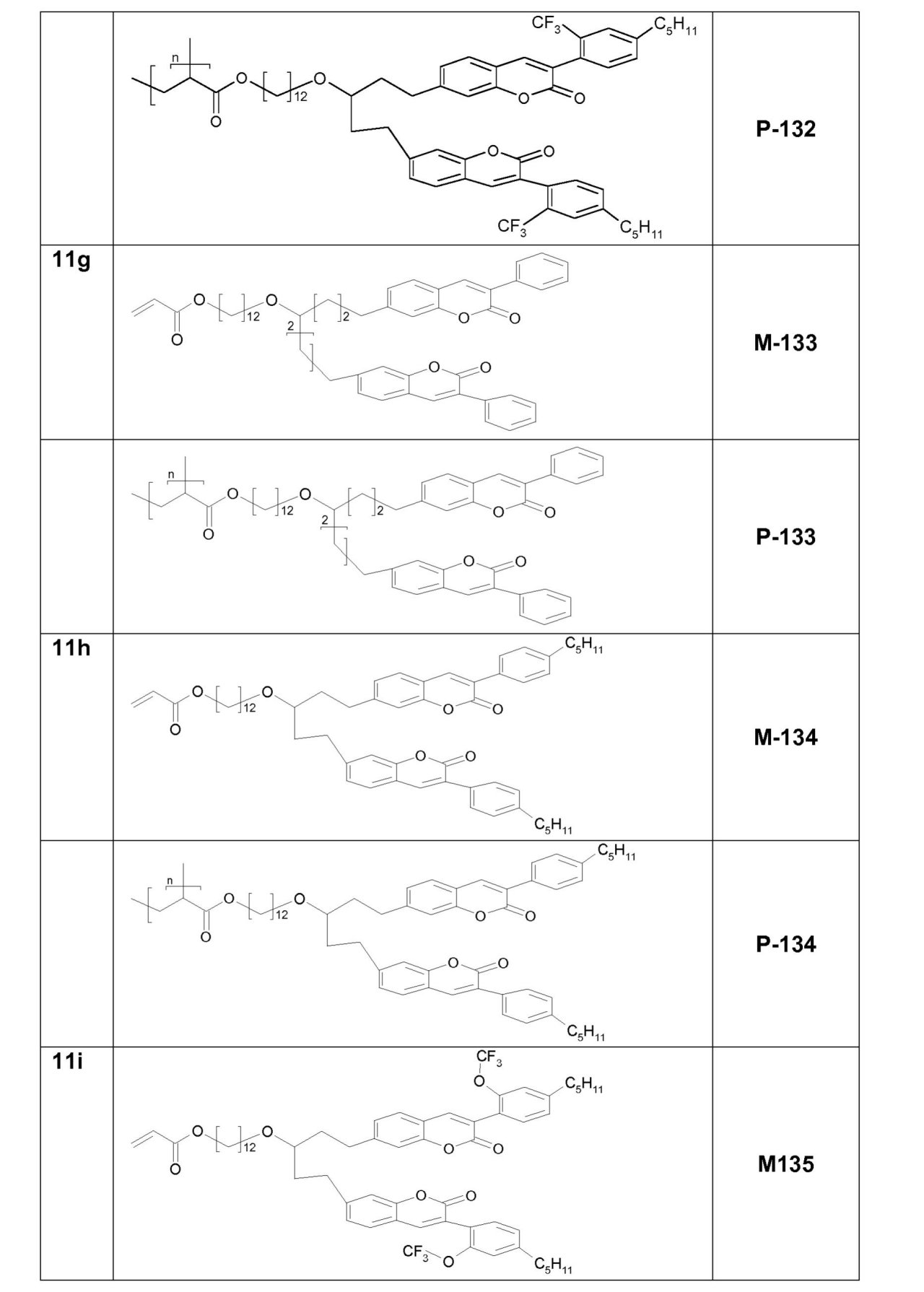
本発明は、新規化合物に、具体的に光活性単位を含む化合物であって、組成物および眼科用デバイスに具体的に好適な該新規化合物に、ならびにかかる化合物を含む組成物および眼科用デバイスに、関する。
白内障は、通常澄んでいる目の水晶体の混濁による視力の喪失に、極端には失明に繋がる目の疾患(an affection)の総称である。それは全世界における失明の主な原因であり、1億をも超える人々にその影響を及ぼしている。その主な原因が加齢であり、人口の平均年齢が上がりつつあるという事実のせいで、白内障の数は将来、実質的に上がり続けるであろうことが予想される。
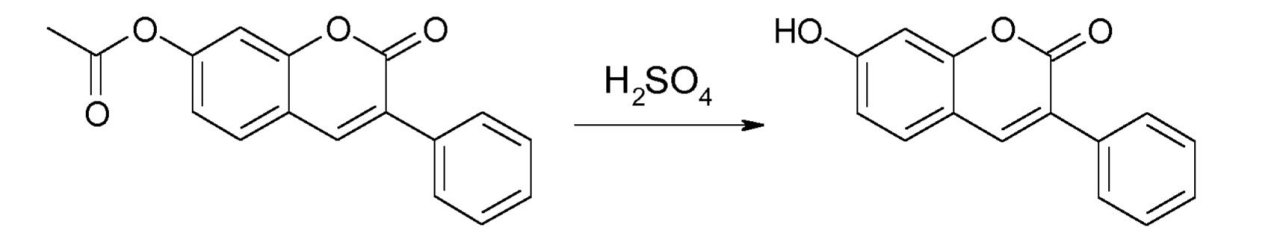
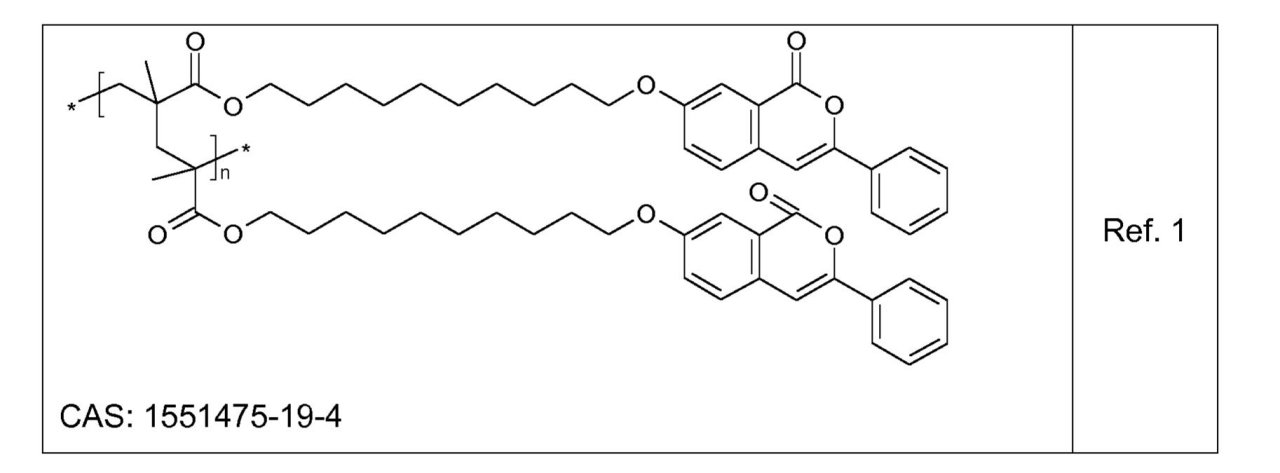
M. Schraub et al, European Polymer Journal 51 (2014) 21-27は、ポリメタクリラートを含有する3-フェニル-クマリンの光化学を記載する。
A. Bouquet et al, Tetrahedron, 1981, vol. 37, 75~81は、中性溶液中のまたは一級および三級アミンの存在下の数種のベンゾ[b]チオフェンの光化学的挙動を記載する。
4-アルキル-3-フェニル-2H-1-ベンゾピランー2-オンおよび関連化合物は、強力な殺虫剤として、Sangwan et al, Indian Journal of Chemistry, 1990, 29B, 294-296に記載されている。
光学特性が、好ましくは非侵襲的技法によって変化させられ得る化合物を提供することもまた、本出願の目的である。
本発明者らは今や、上の目的が、本出願の化合物および眼科用デバイスによる、個々にまたはいずれの組み合わせのいずれかによって達成され得ることを見出している。
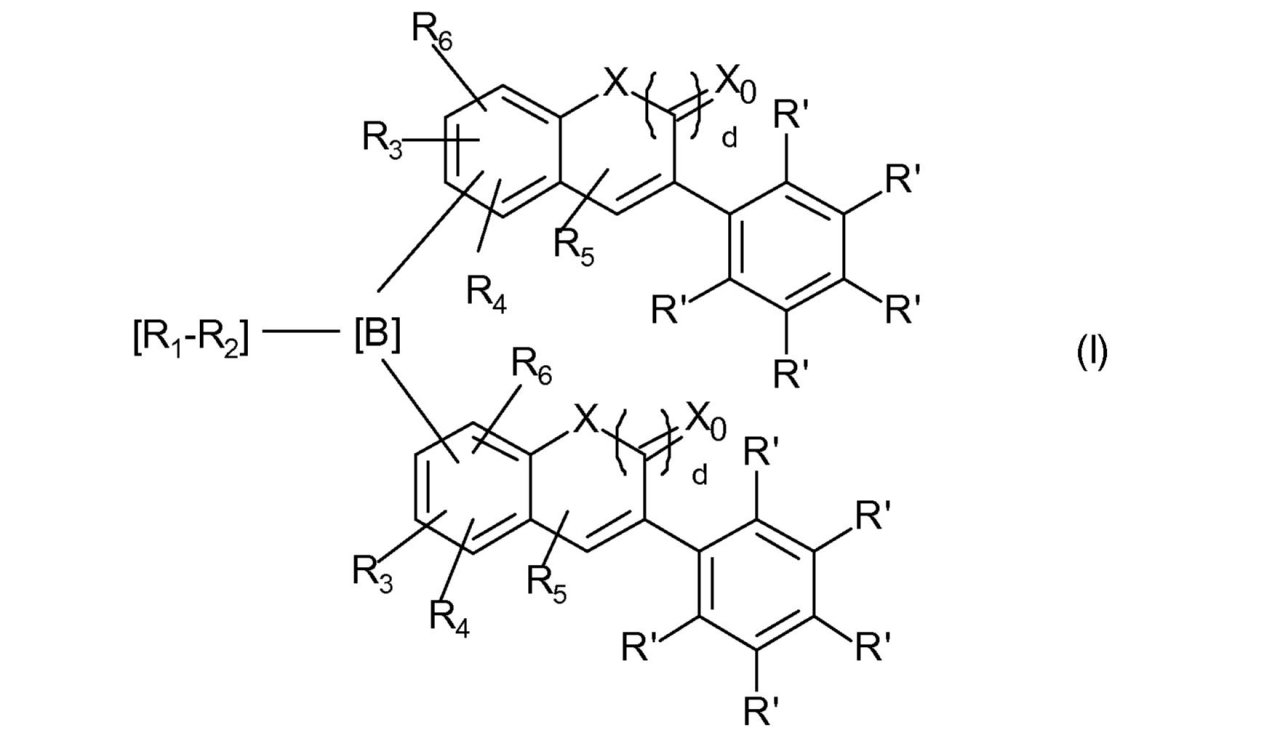
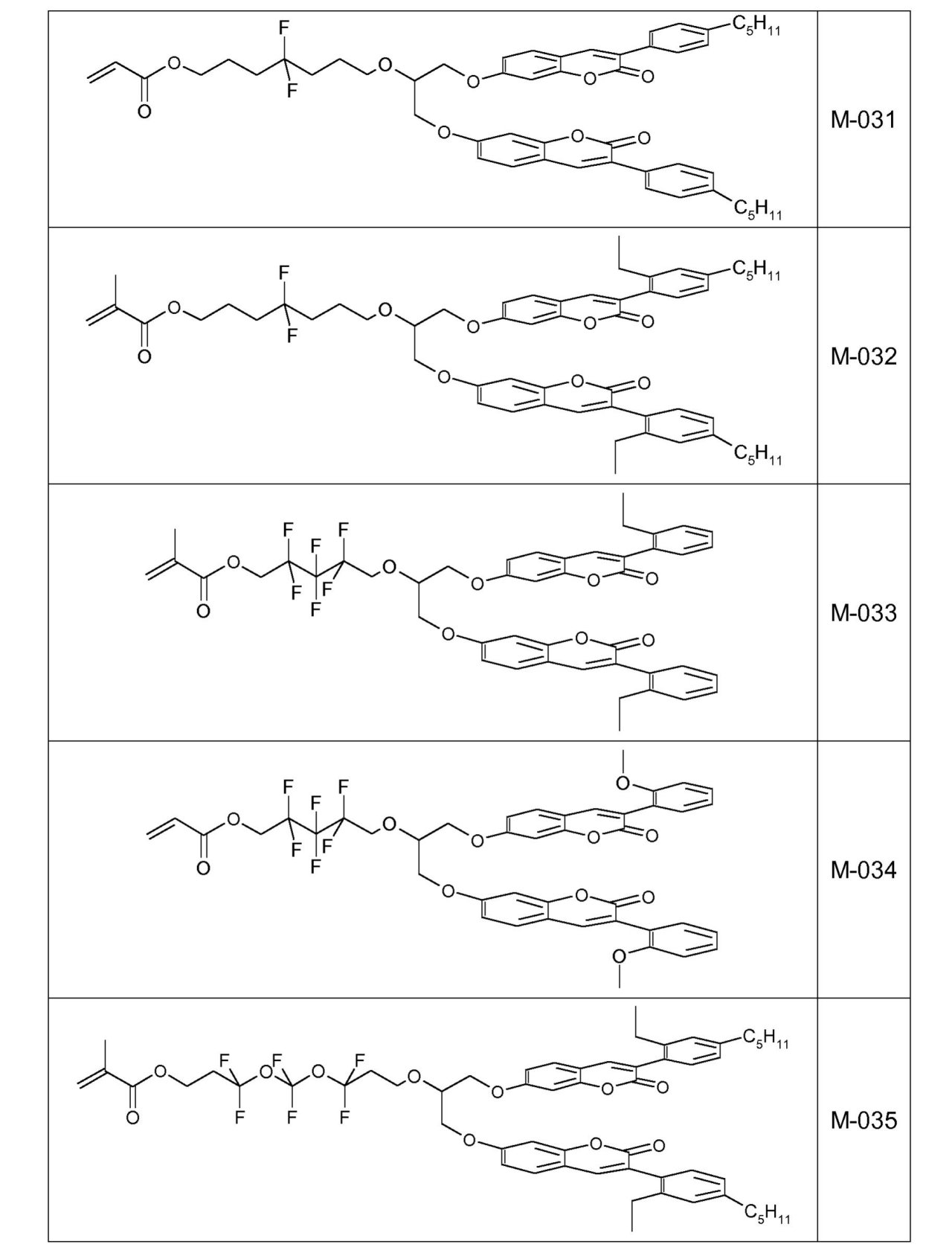
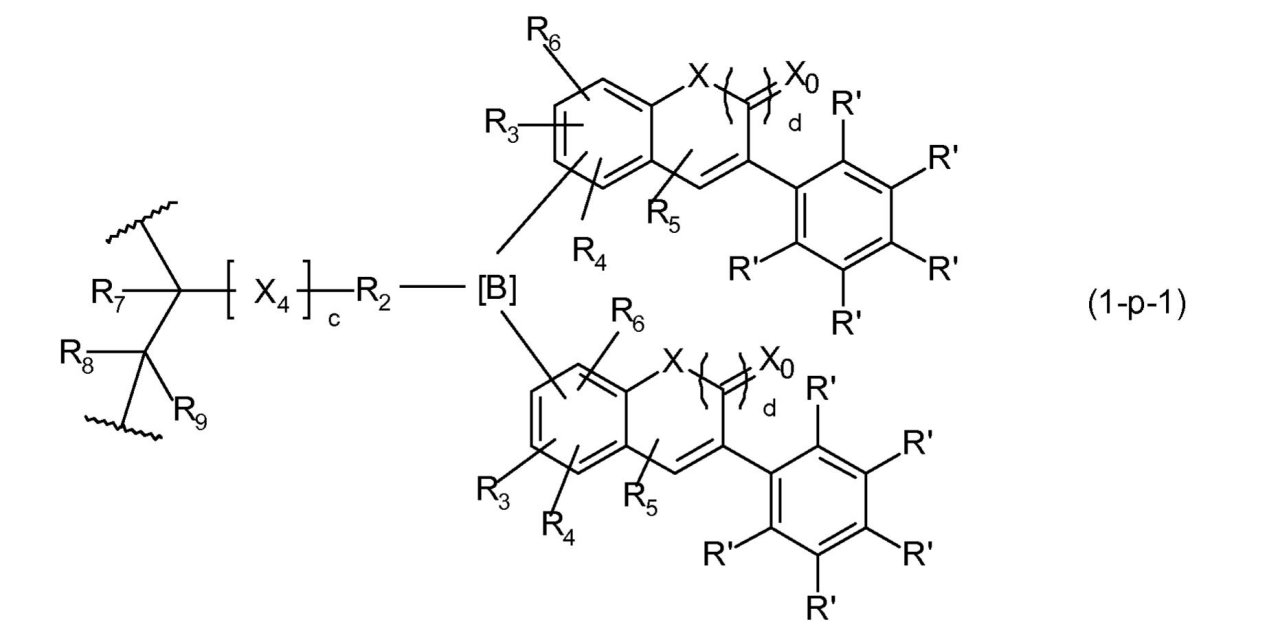
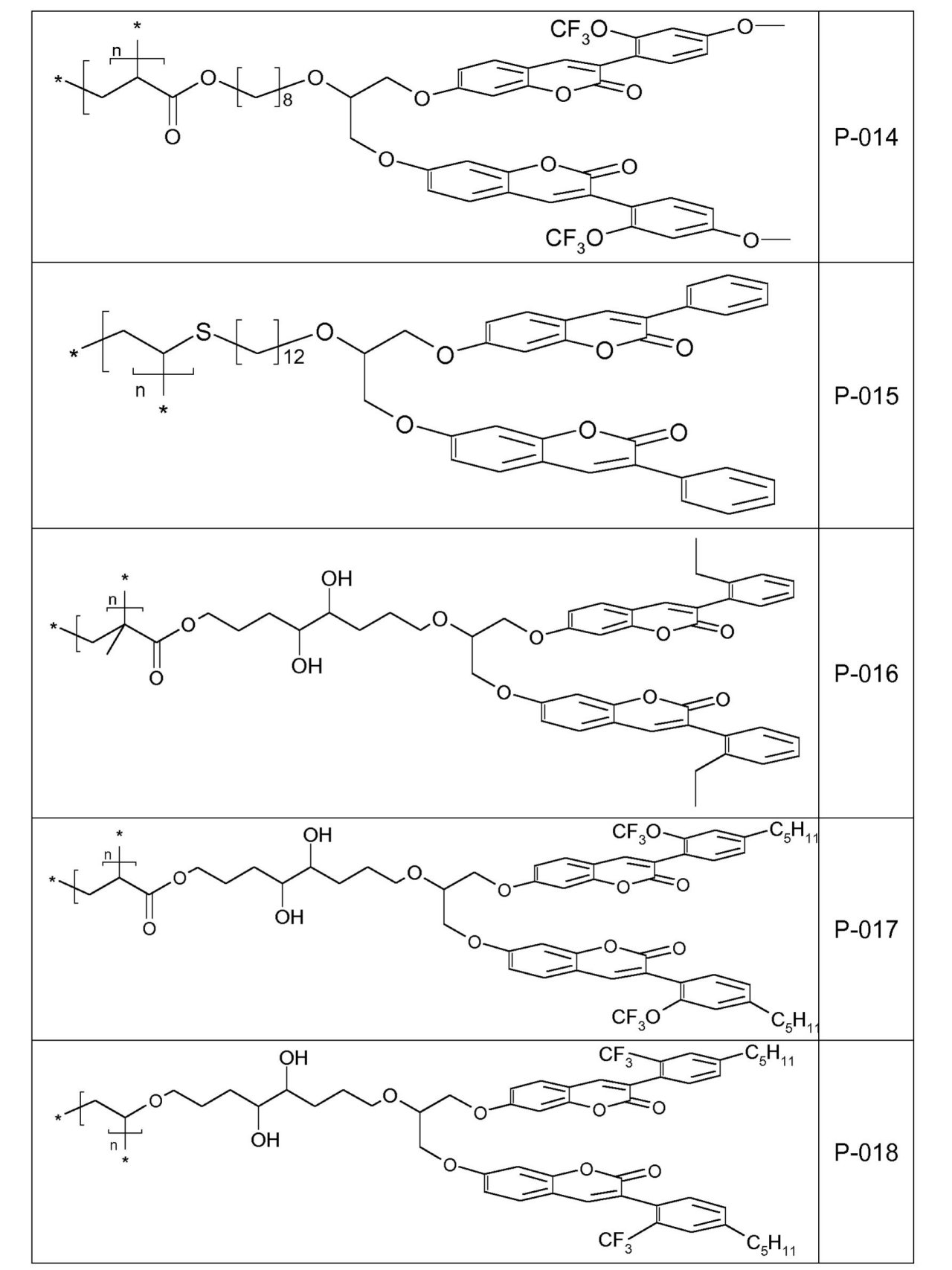
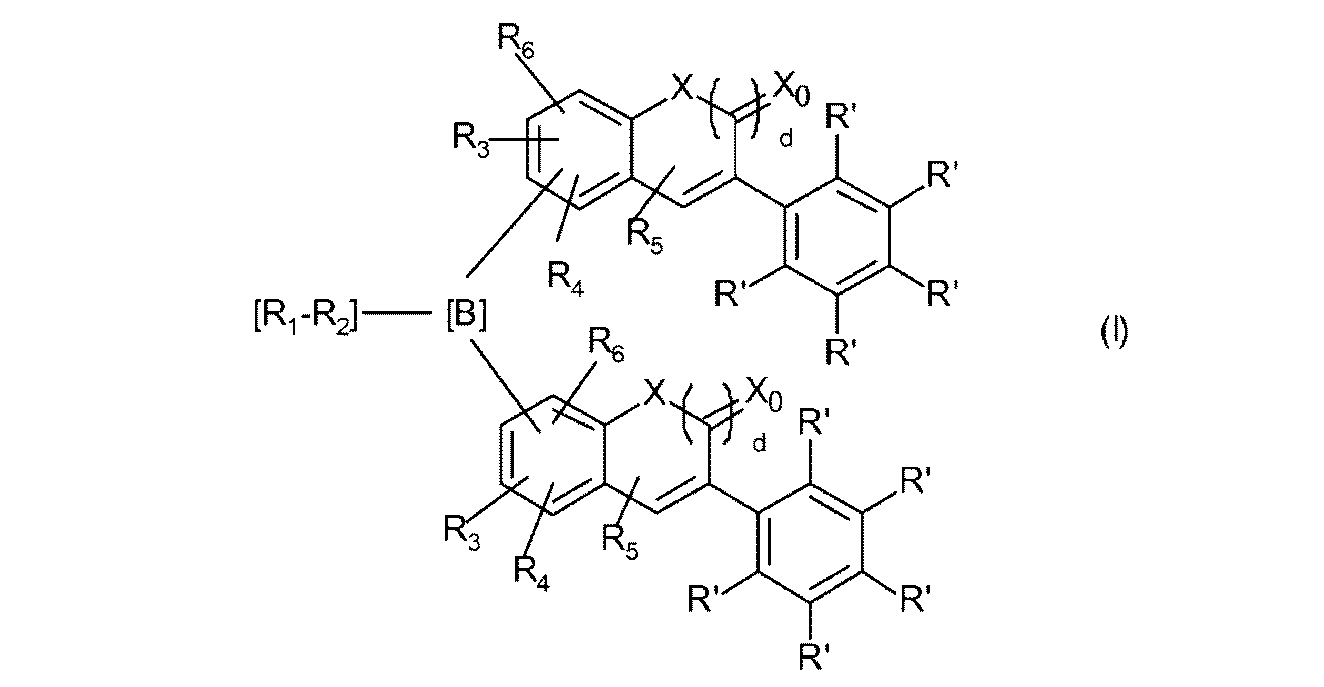
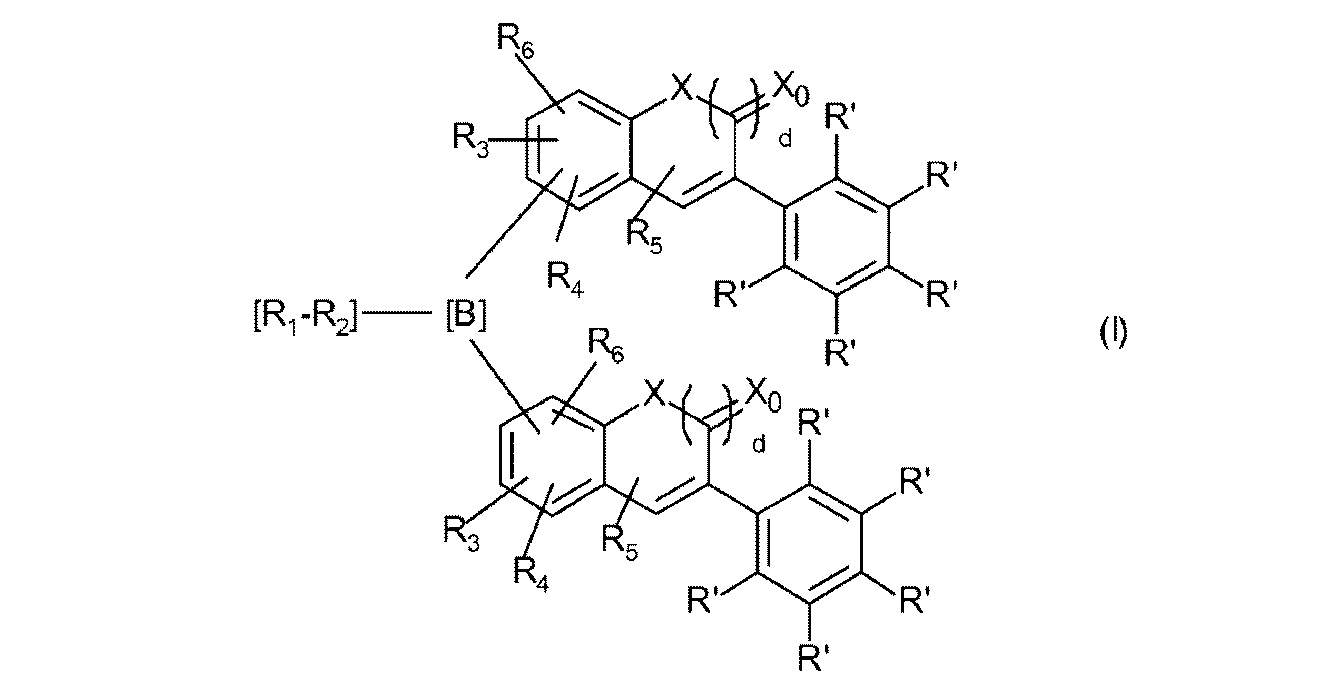
式中
X4は、O、S、C(=O)、C(=O)Oからなる群から選択され、
R7、R8、R9は出現毎に、互いに独立して、H、F、1~20個のC原子を有する線状もしくは分枝状の、非フッ素化されているか、部分的または全面的にフッ素化されたアルキル、あるいは6~14個のC原子をもつアリールからなる群から選択され、
cは、0または1である、
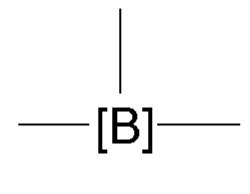
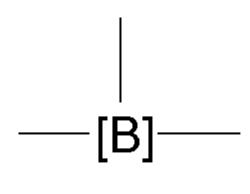
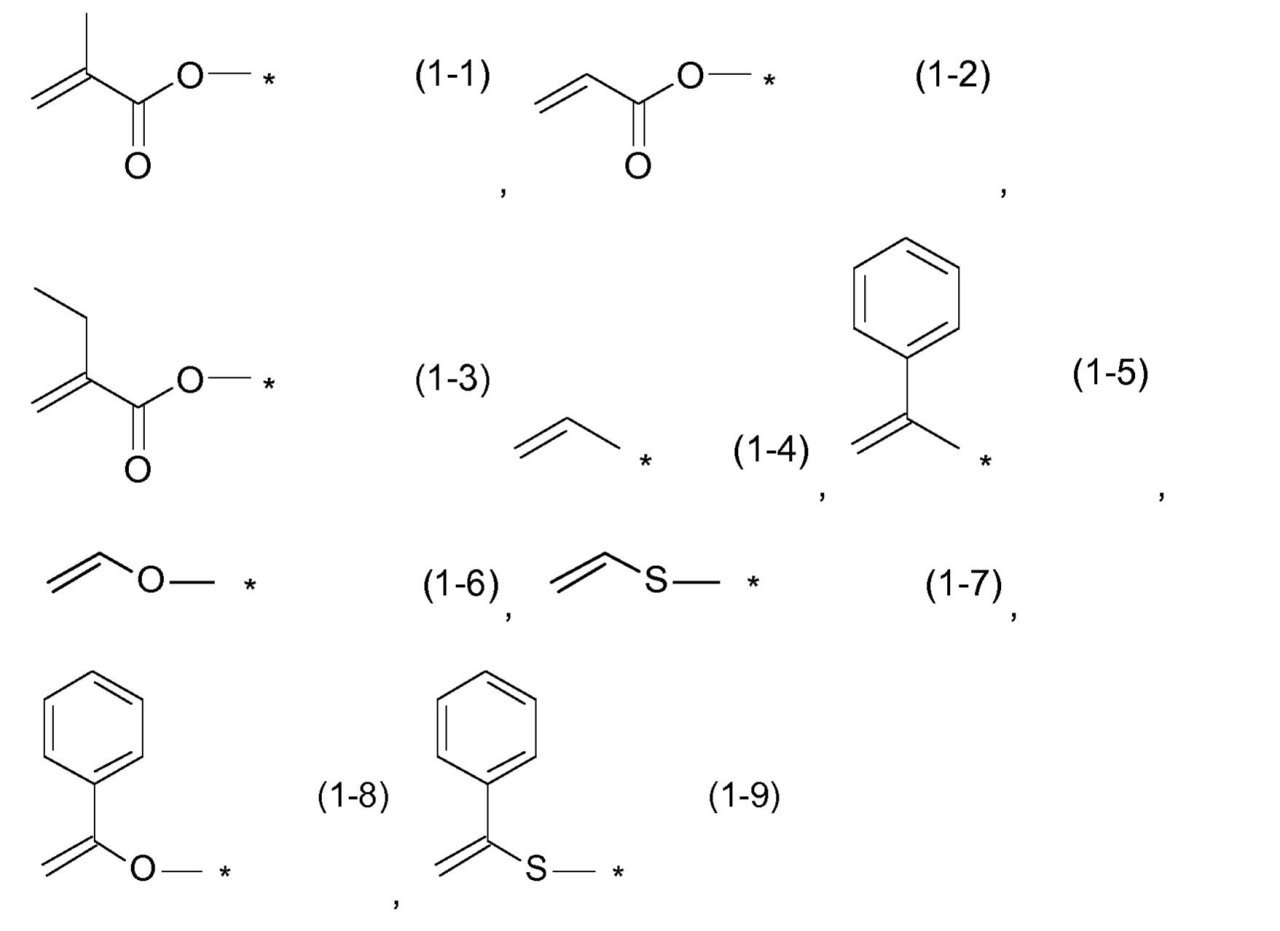
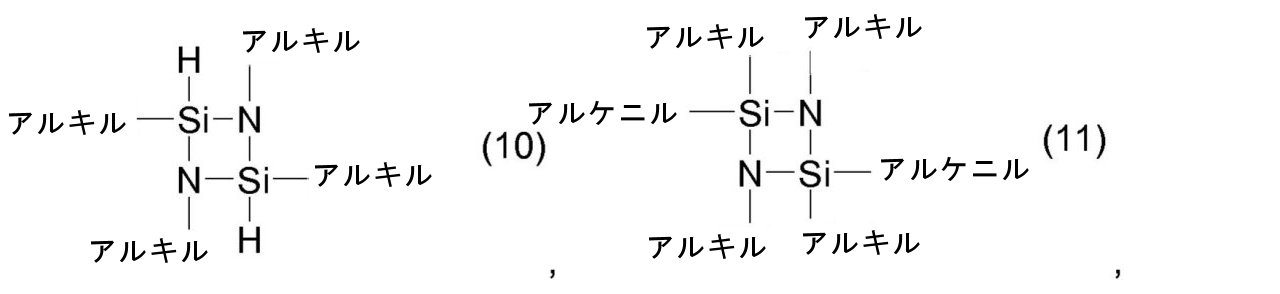
で表されるアルケニル基;
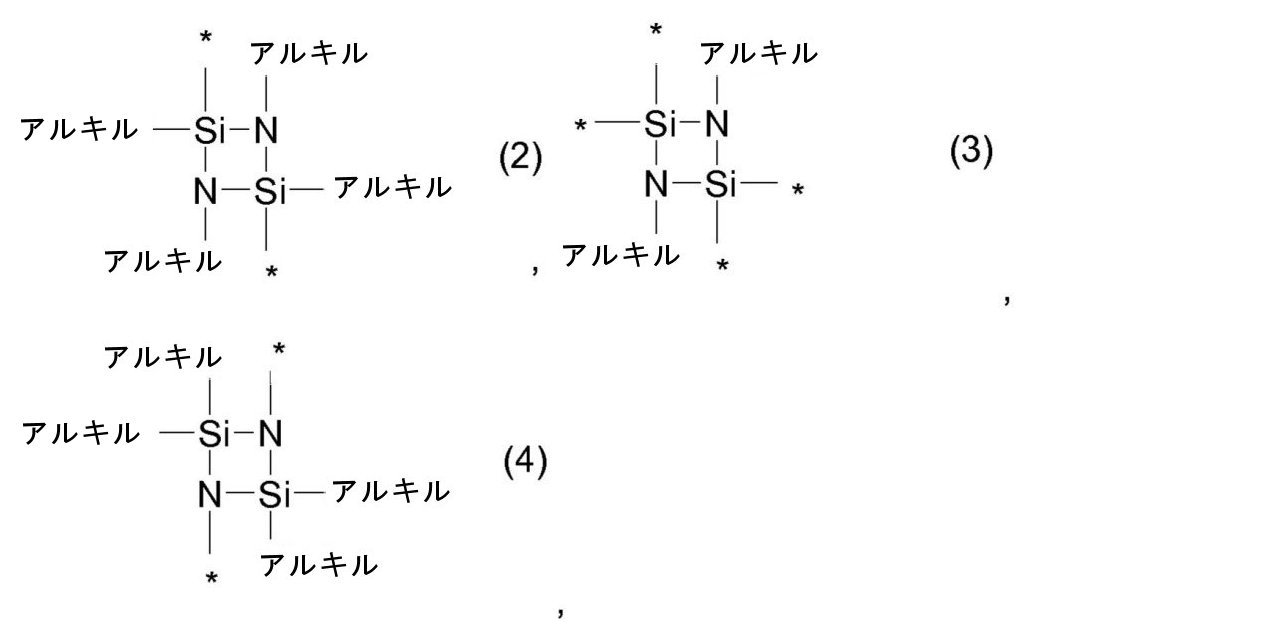
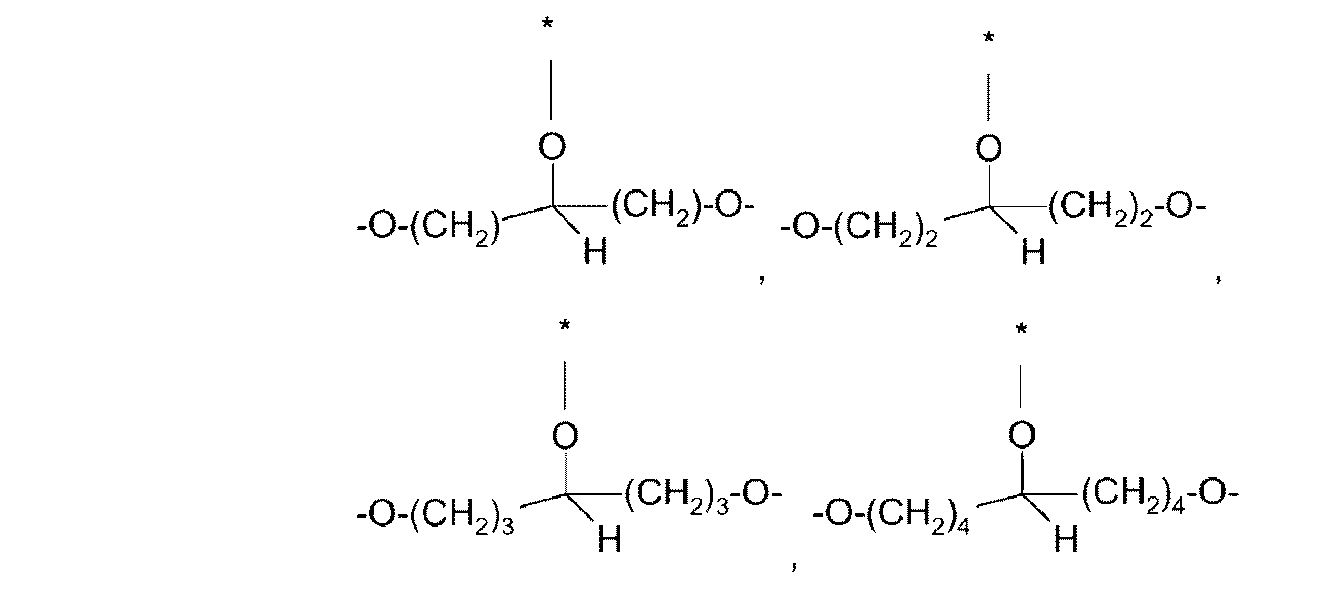
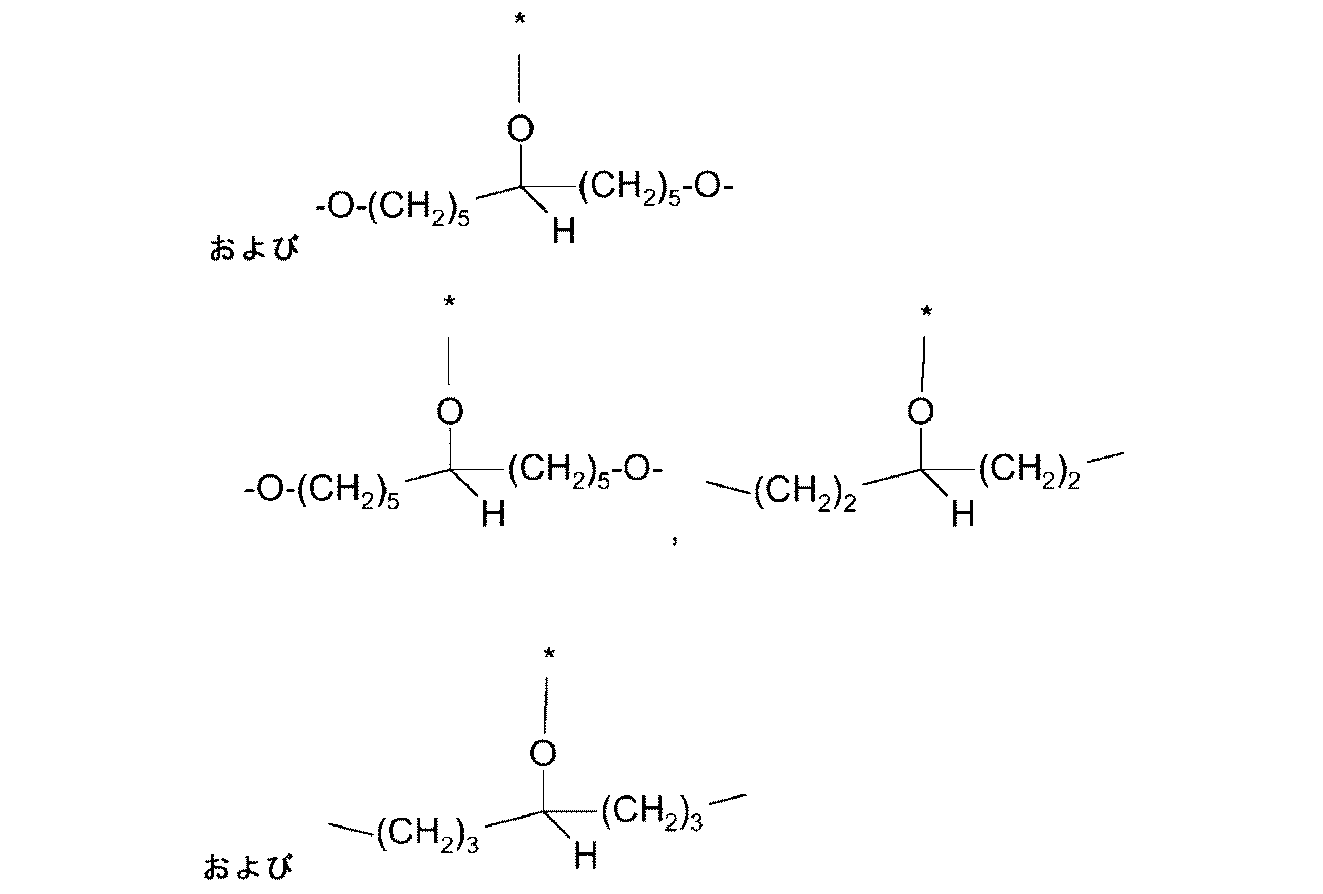
前記式中のアルキルは、出現毎に互いに独立して、1~6個のC原子を有する線状または分枝状のアルキル基を意味し、および星印「*」は、出現毎に互いに独立して、リンカー[-R2-]への繋がりを示す、
で表される、前記トリアルコキシシリル基または前記ジアルコキシアルキルシリル基
からなる群から選択される重合性基であり、
oは、1~20からなる群から選択され、
X1、X2、X3は、出現毎に独立して、O、SまたはNR0であり、
s、tは、0または1であり、
r、uは、出現毎に独立して、0~10からなる群から選択されるが、ここで-(C(R)2)p-X1-(C(R)2)q-(X2)s-(C(R)2)r-(X3)t-(C(R)2)u-について原子の全体数が、最大20原子までであり、
R3、R4、R5、R6は、出現毎に独立して、R’である。
- 式(I)で表される少なくとも1種の化合物および/または前に記載のとおりのオリゴマーもしくはポリマーを含む組成物を提供すること;
- 続いて、該組成物の物品を形成すること
というステップを含む。
- 少なくとも1種の重合された式(I)で表される化合物を含む物品を提供すること、および
- 続いて、該物品を、少なくとも200nmかつ最大でも1500nmの波長を有する照射にさらすこと
というステップを含む。
式(I)で表される化合物および本発明に従う式(I)で表される化合物の好ましい全態様は、全立体異性体または全ラセミ混合物を包含する。
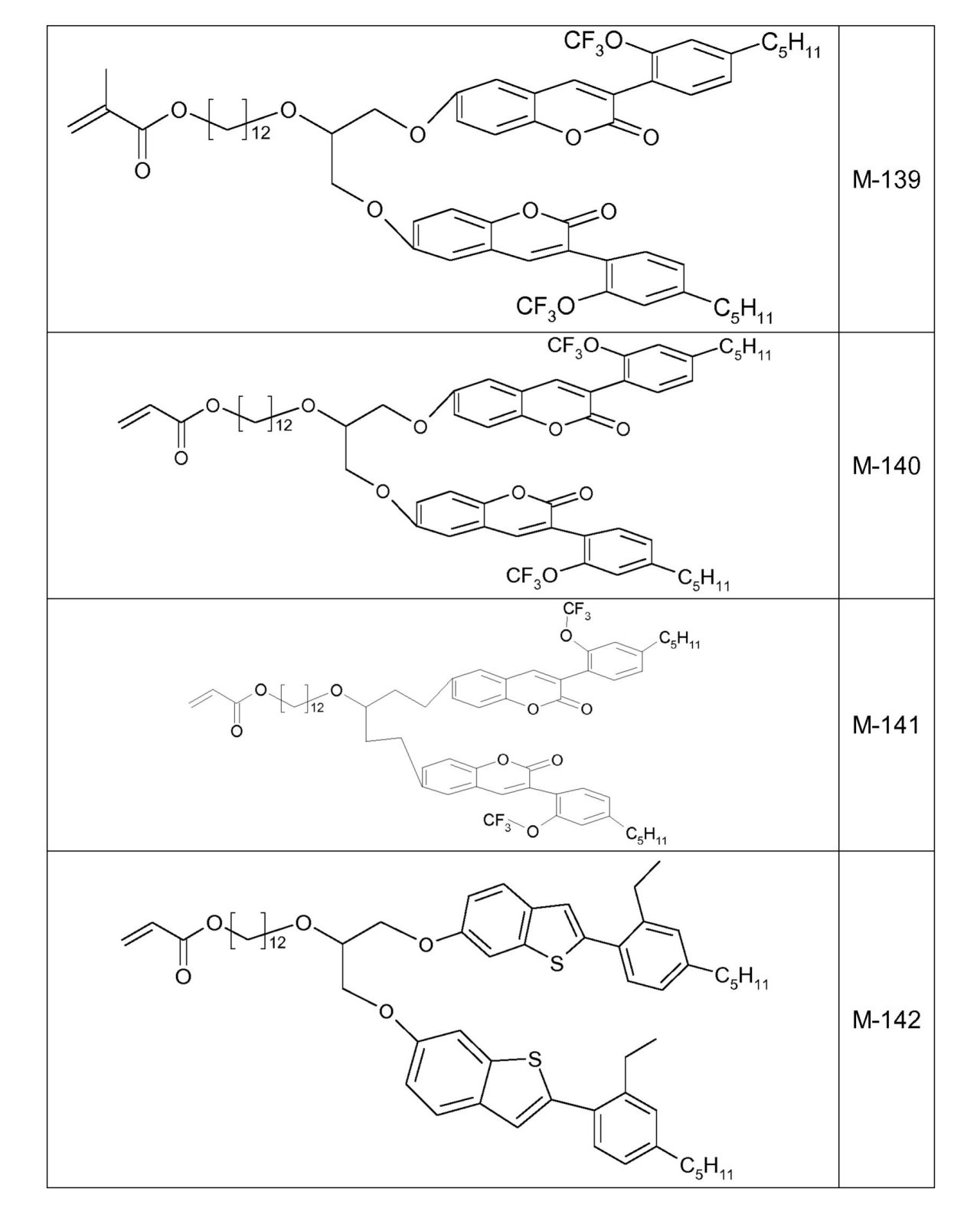
- 式(I)で表される化合物内に2つの発色団(例として2つのクマリン発色団)を有することによって、それらは、最適化された短距離充填および制御された配列を有し、よって、より速いかつより効率的な光反応を示し、
- リンカー-[R2]-および置換基R’によって表される特定の置換パターンを加えることによって、それらの融点またはガラス転移温度が減少し、よって、より良好に折り畳められるか、または折り曲げられるであろう。
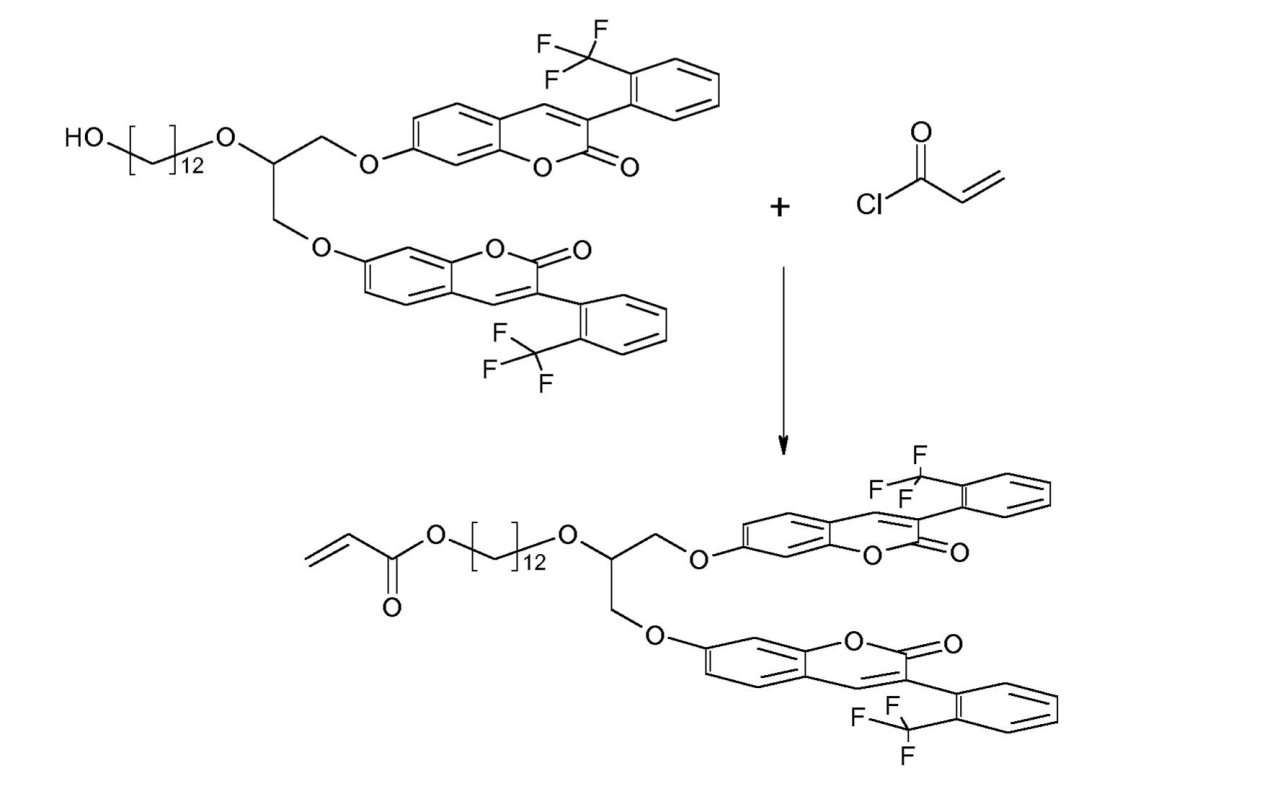
重合性基は、重合に供されるかまたは重合を起こし、よってオリゴマーまたはポリマーを形成し得る基である。
式中
X4は、O、S、C(=O)、C(=O)Oからなる群から選択され、
R7、R8、R9は、出現毎に互いに独立して、H、F、1~20個のC原子を有する線状もしくは分枝状の、フッ素化されていないか、部分的または全面的にフッ素化されたアルキル、あるいは6~14個のC原子をもつアリールからなる群から選択され、
cは、0または1である、
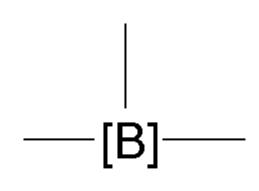
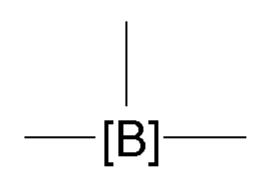
で表されるアルケニル基;
ここでアルキルが、出現毎に互いに独立して、1~6個のC原子を有する線状または分枝状のアルキル基を意味し、および星印「*」は、出現毎に互いに独立して、前に記載されたとおりのまたは前に好ましく記載されたとおりのリンカー[-R2-]への繋がりを示す、で表される、前記トリアルコキシシリル基または前記ジアルコキシアルキルシリル基
からなる群から選択される。
は、
に対応するが、ここで星印「*」は、前に記載されたとおりのまたは下に好ましく記載されたとおりのリンカー[-R2-R1]への繋がりを示す。
は、
に対応するが、ここで星印「*」は、前に記載されたとおりのまたは下に好ましく記載されたとおりのリンカー[-R2-R1]への繋がりを示す。
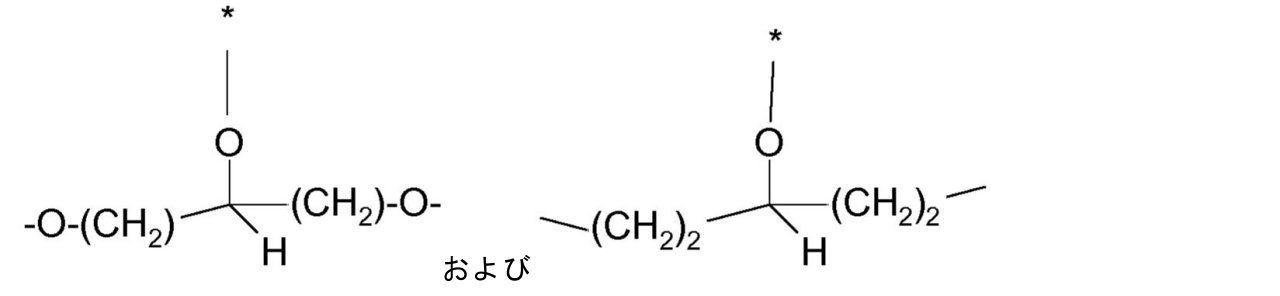
(ここでR1およびR2は、前に記載されたとおりのまたは下に好ましく記載されたとおりの意味を有する)を通して可視化され得るCH基へ結合されているO原子へ結合されている。
のO原子へ結合されている場合、具体的に好ましい。
のO原子へ結合されている場合、具体的に好ましい。
のO原子へ結合されている。
をもつ式(I)で表される化合物は、式(I-1)、
ここでR1、-R2-、R3、R4、R5、R6およびR’は、前に記載されたとおりのまたは下に好ましく記載されたとおりの意味を有する、
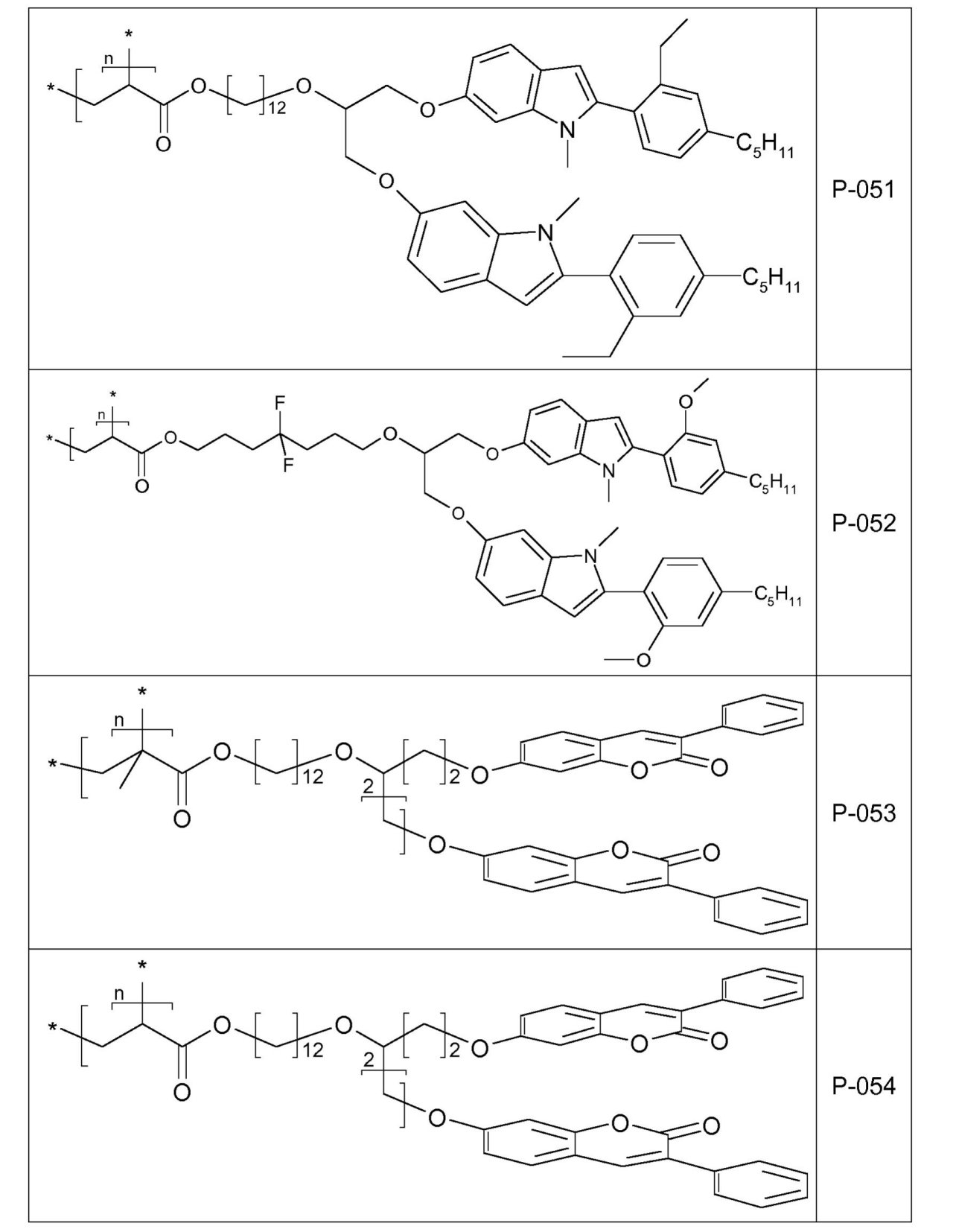
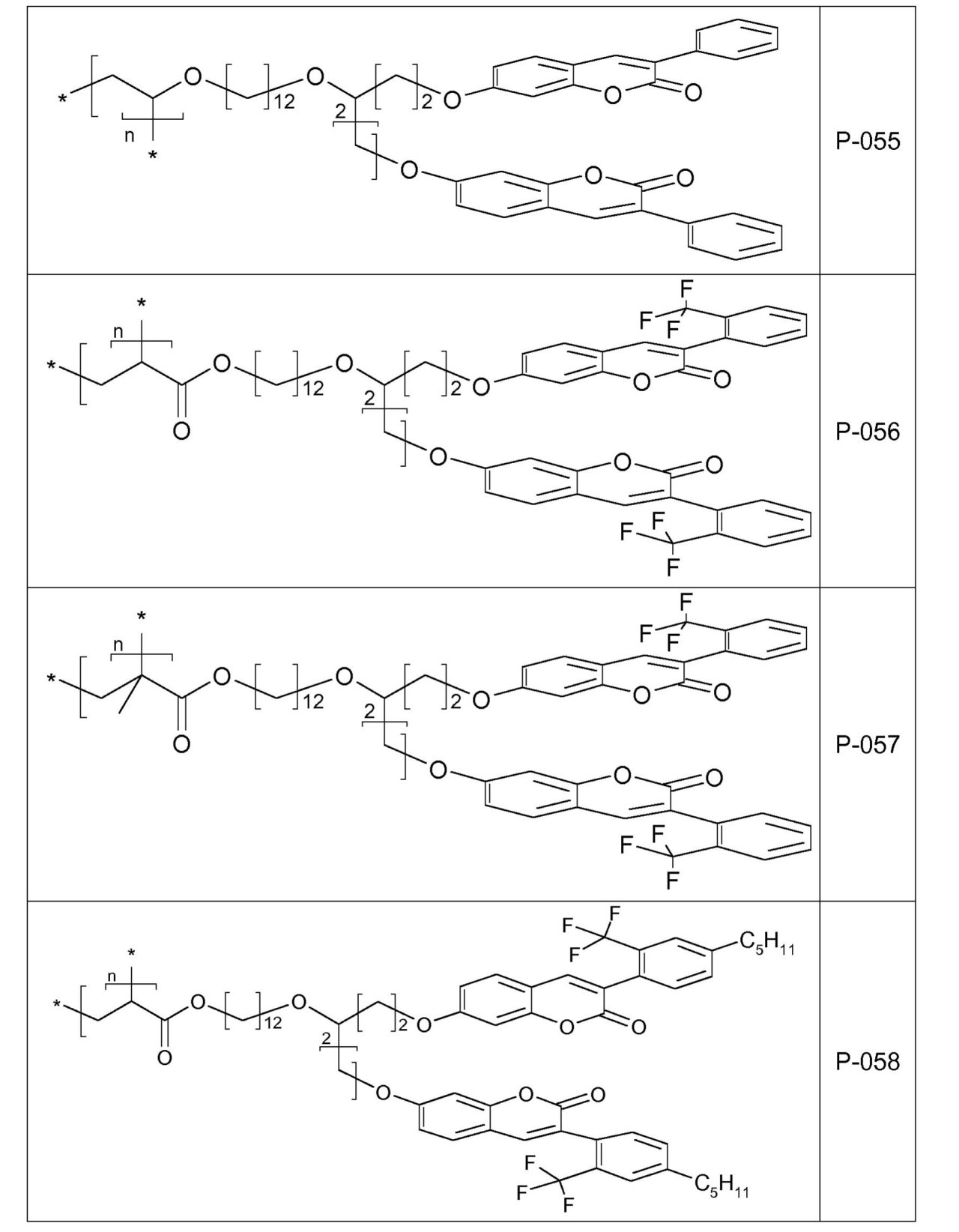
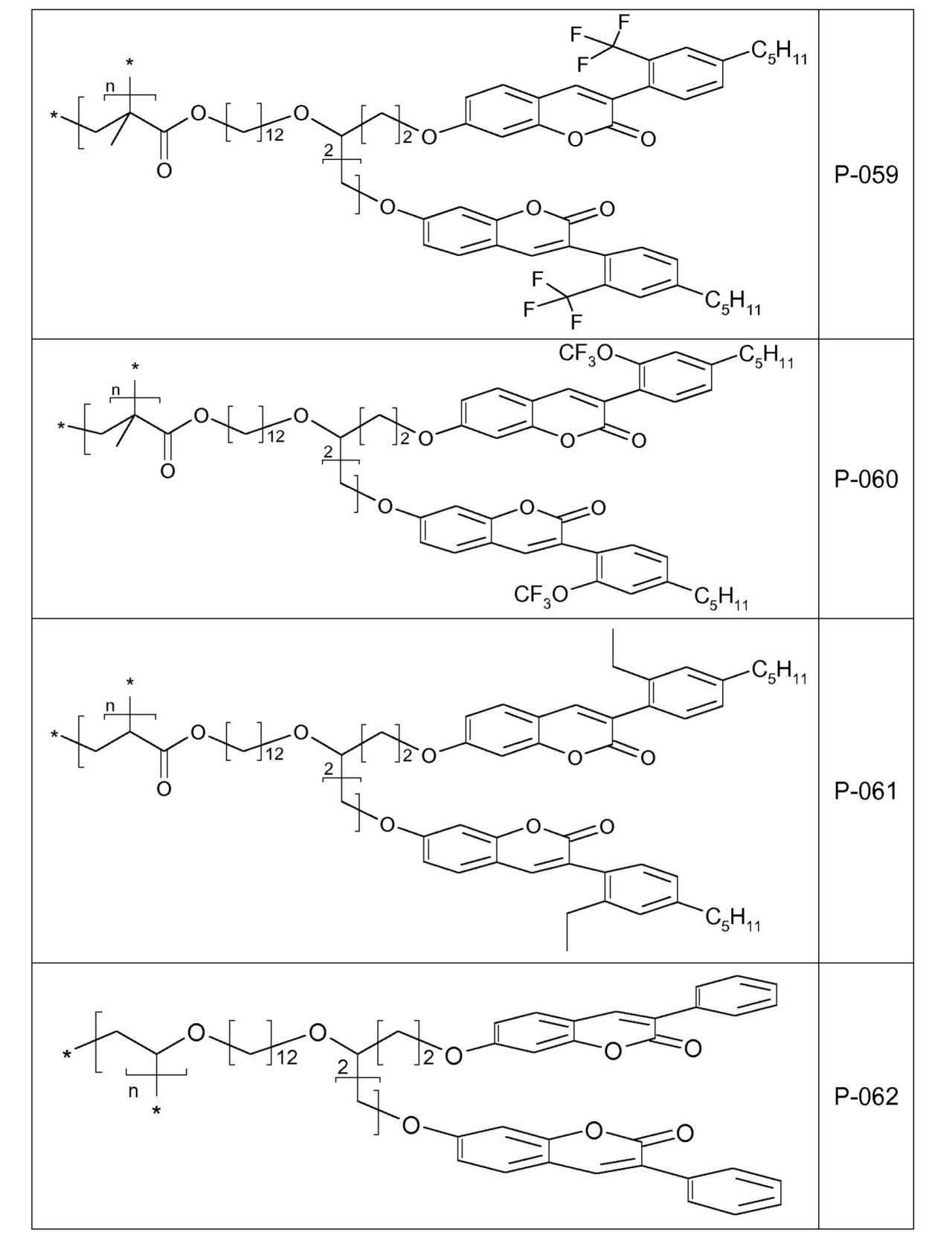
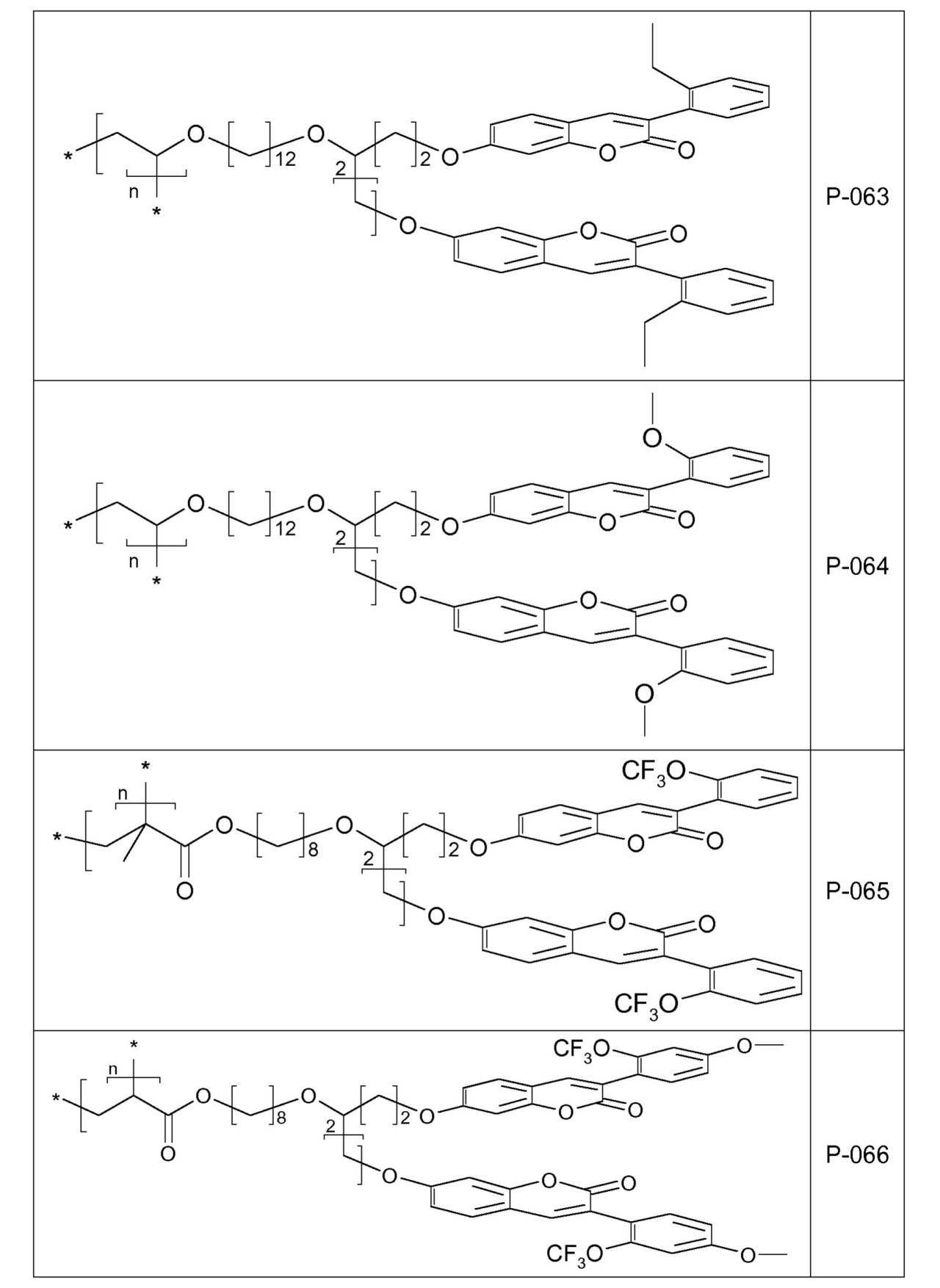
を通して表されるとおり、XおよびX0がともにOであり、かつdが1である場合の1-ベンゾピラン-2-オン環系(クマリンまたはクロメン-2-オン)を基にする。好ましくは、リンカー
は、1-ベンゾピラン-2-オン環系の位置7または6に結合されている。
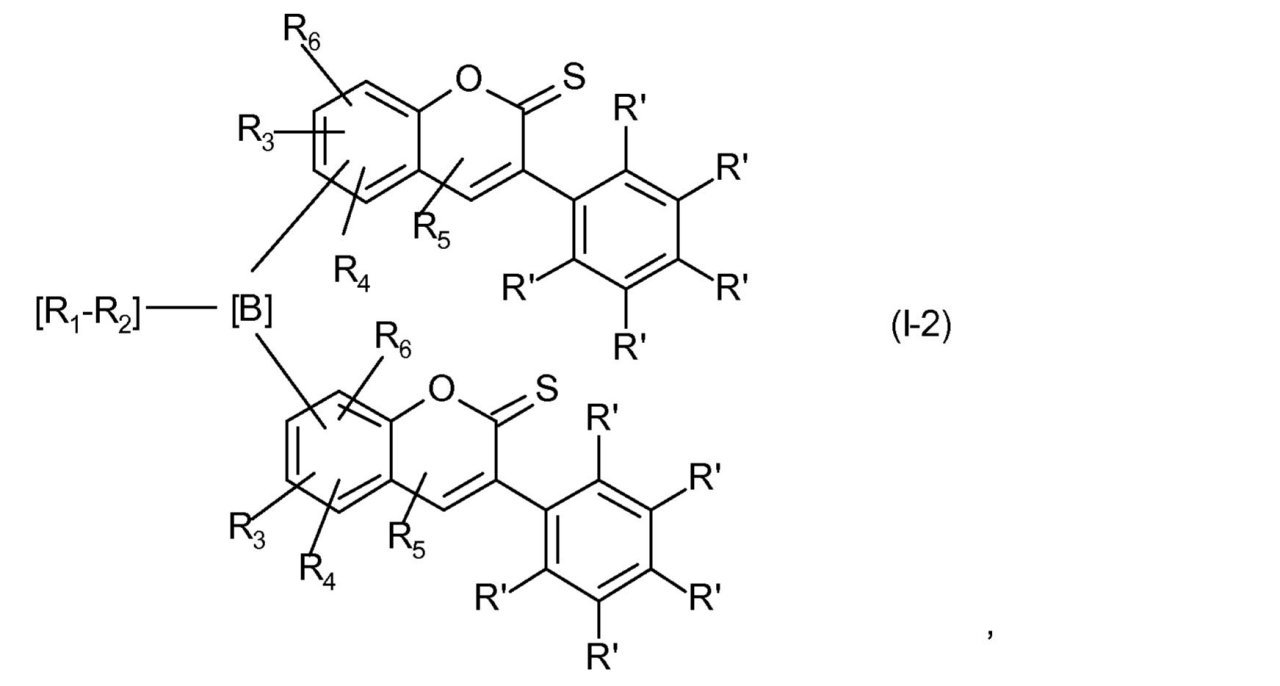
をもつ式(I)で表される化合物は、式(I-2)、
ここでR1、-R2-、R3、R4、R5、R6およびR’は、前に記載されたとおりのまたは下に好ましく記載されたとおりの意味を有する、
を通して表されるとおり、XがOであり、X0がSであり、かつdが1である場合の1-ベンゾピラン-2-チオン環系(チオクマリンまたはクロメン-2-チオン)を基にする。好ましくは、リンカー
は、1-ベンゾピラン-2-チオン環系の位置7または6に結合されている。
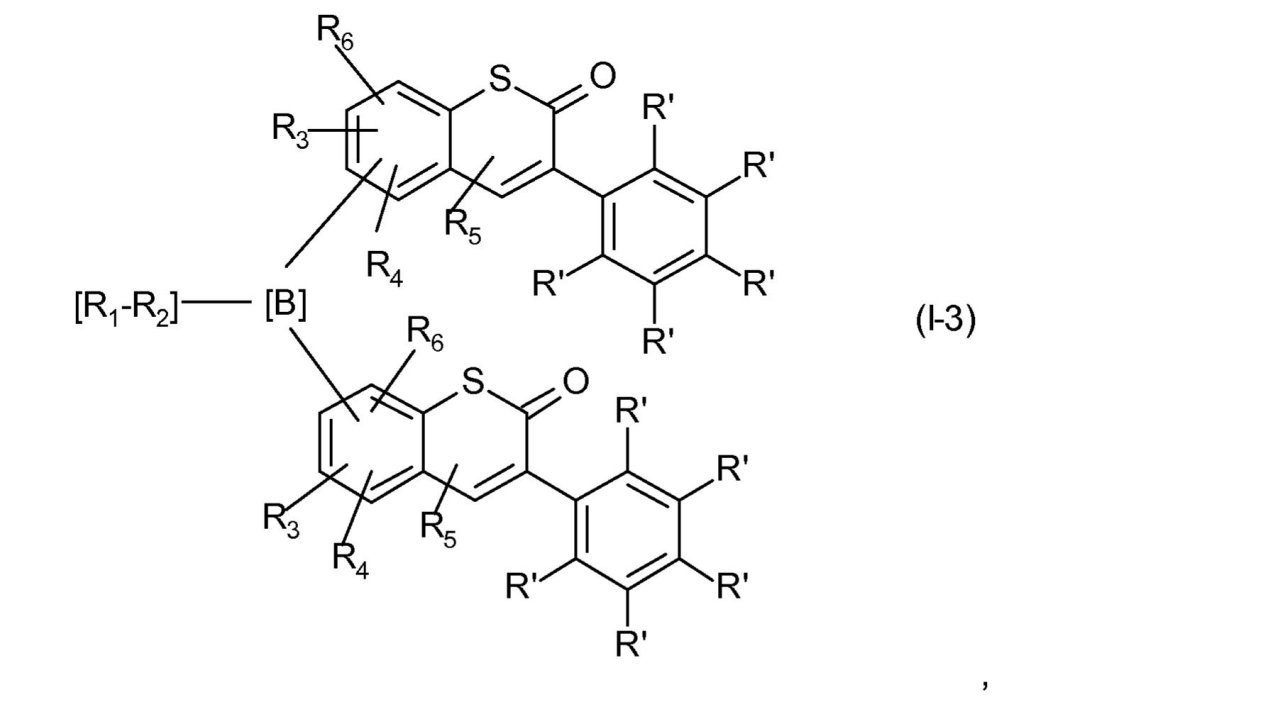
をもつ式(I)で表される化合物は、式(I-3)、
ここでR1、-R2-、R3、R4、R5、R6およびR’は、前に記載されたとおりのまたは下に好ましく記載されたとおりの意味を有する、
を通して表されるとおり、XがSであり、X0がOであり、かつdが1である場合のチオクロメン-2-オン環系を基にする。好ましくは、リンカー
は、チオクロメン-2-オン環系の位置7または6に結合されている。
をもつ式(I)で表される化合物は、式(I-4)、
ここでR1、-R2-、R3、R4、R5、R6およびR’は、前に記載されたとおりのまたは下に好ましく記載されたとおりの意味を有する、
を通して表されるとおり、XおよびX0がともにSであり、かつdが1である場合のチオクロメン-2-チオン環系を基にする。好ましくは、リンカー
は、チオクロメン-2-チオン環系の位置7または6に結合されている。
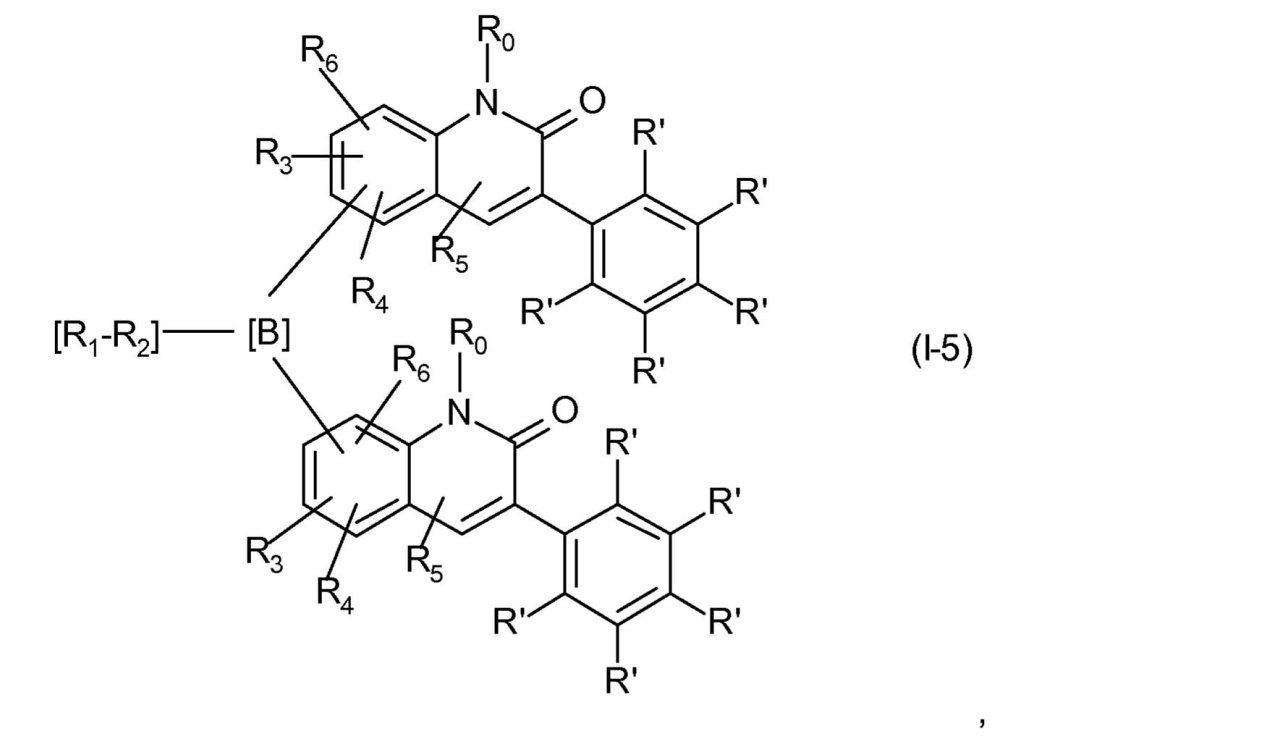
をもつ式(I)で表される化合物は、式(I-5)、
ここでR1、-R2-、R3、R4、R5、R6、R0およびR’は、前に記載されたとおりのまたは下に好ましく記載されたとおりの意味を有する、
を通して表されるとおり、XがNR0であり、X0がOであり、かつdが1である場合のキノリン-2-オン環系を基にする。好ましくは、リンカー
は、キノリン-2-オン環系の位置7または6に結合されている。
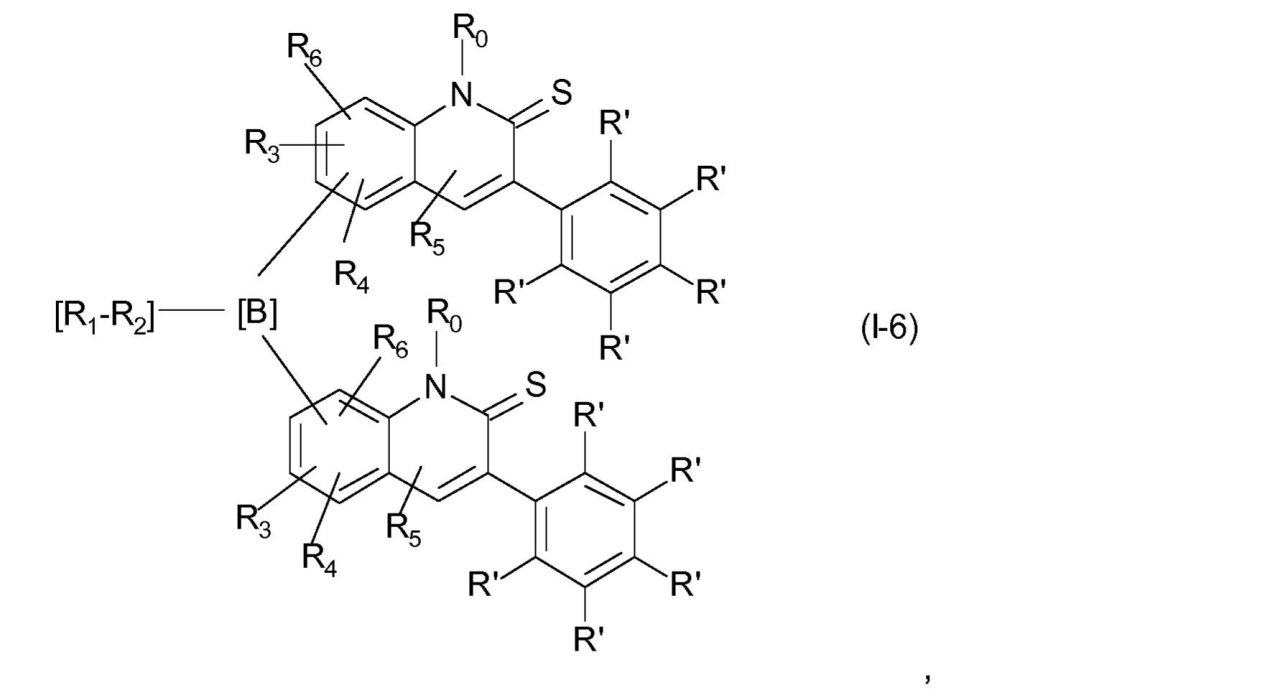
をもつ式(I)で表される化合物は、式(I-6)、
ここでR1、-R2-、R3、R4、R5、R6、R0およびR’は、前に記載されたとおりのまたは下に好ましく記載されたとおりの意味を有する、
を通して表されるとおり、XがNR0であり、X0がSであり、かつdが1である場合のキノリン-2-チオン環系を基にする。好ましくは、リンカー
は、キノリン-2-チオン環系の位置7または6に結合されている。
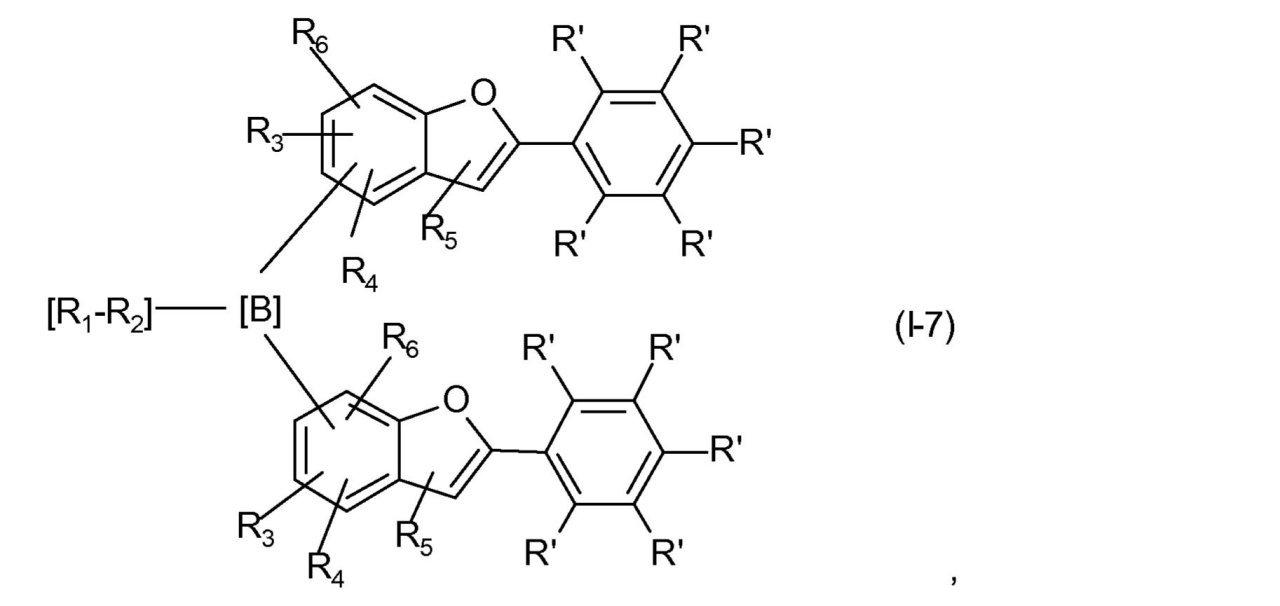
をもつ式(I)で表される化合物は、式(I-7)、
ここでR1、-R2-、R3、R4、R5、R6およびR’は、前に記載されたとおりのまたは下に好ましく記載されたとおりの意味を有する、
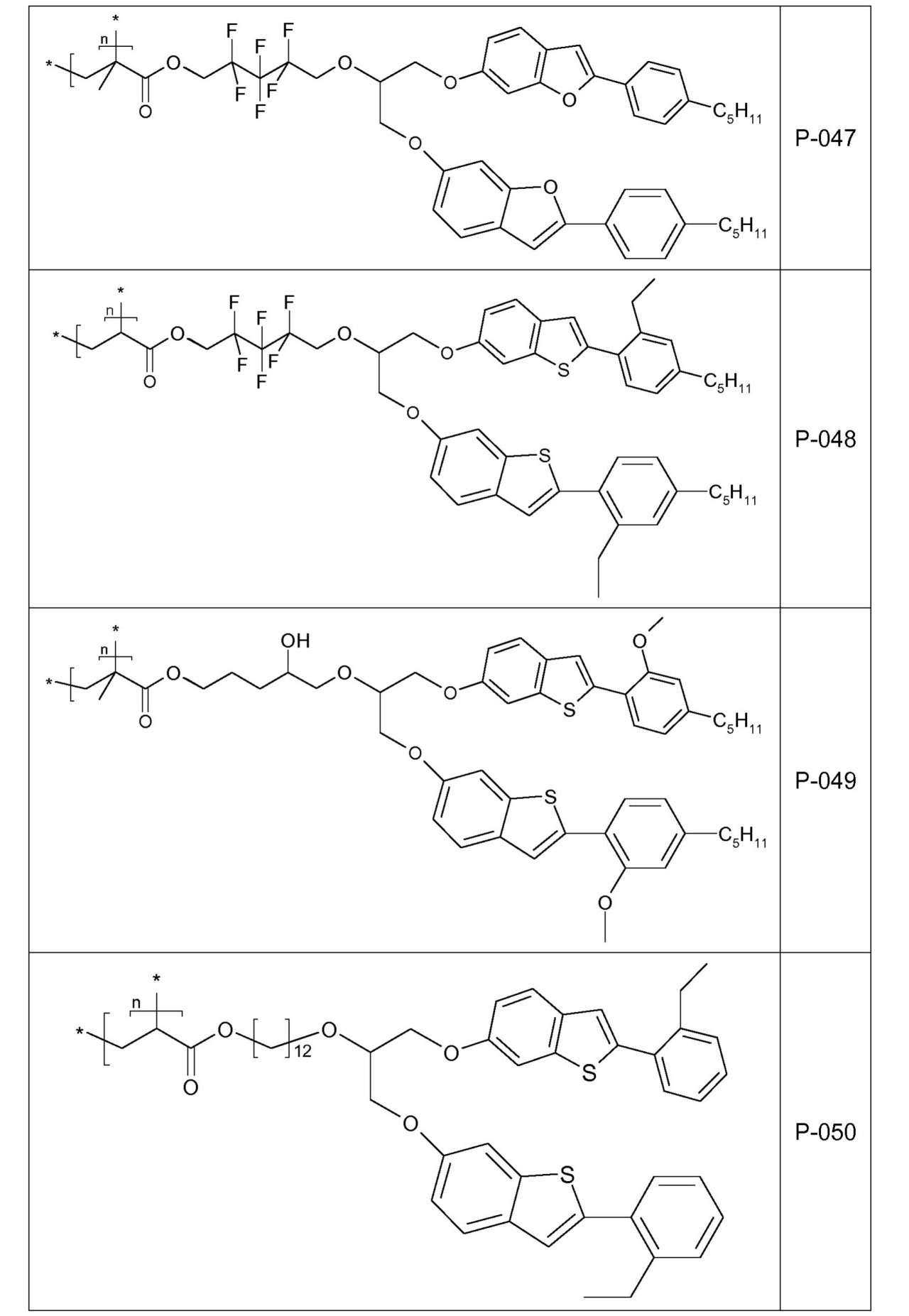
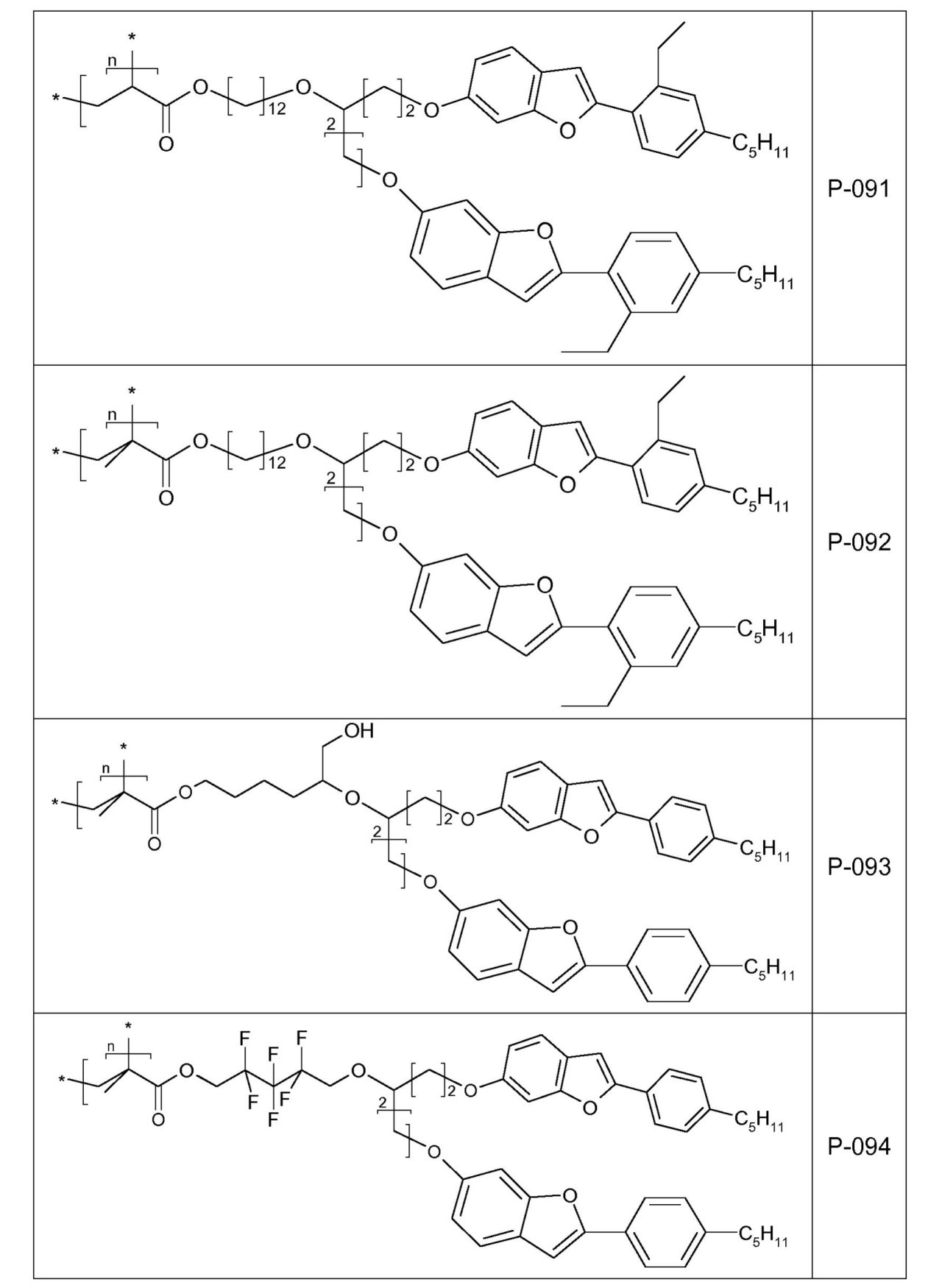
を通して表されるとおり、XがOであり、かつdが0である場合のベンゾ[b]フラン環系を基にする。好ましくは、リンカー
は、ベンゾ[b]フラン環系の位置6または5に結合されている。
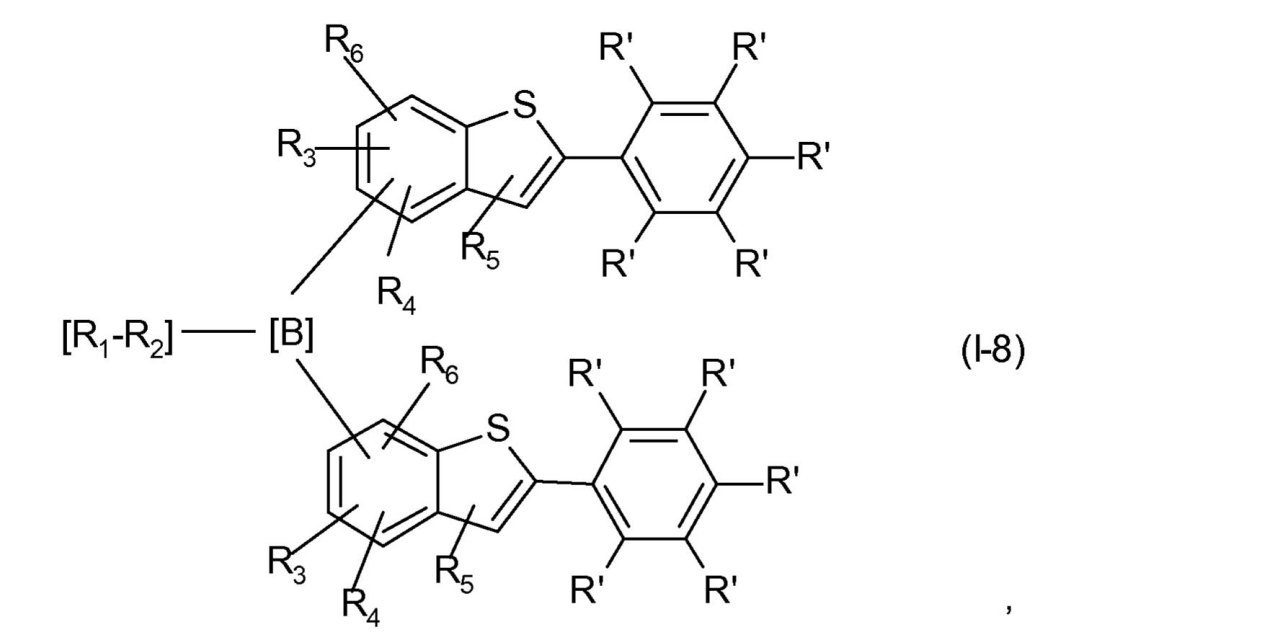
をもつ式(I)で表される化合物は、式(I-8)、
ここでR1、-R2-、R3、R4、R5、R6およびR’は、前に記載されたとおりのまたは下に好ましく記載されたとおりの意味を有する、
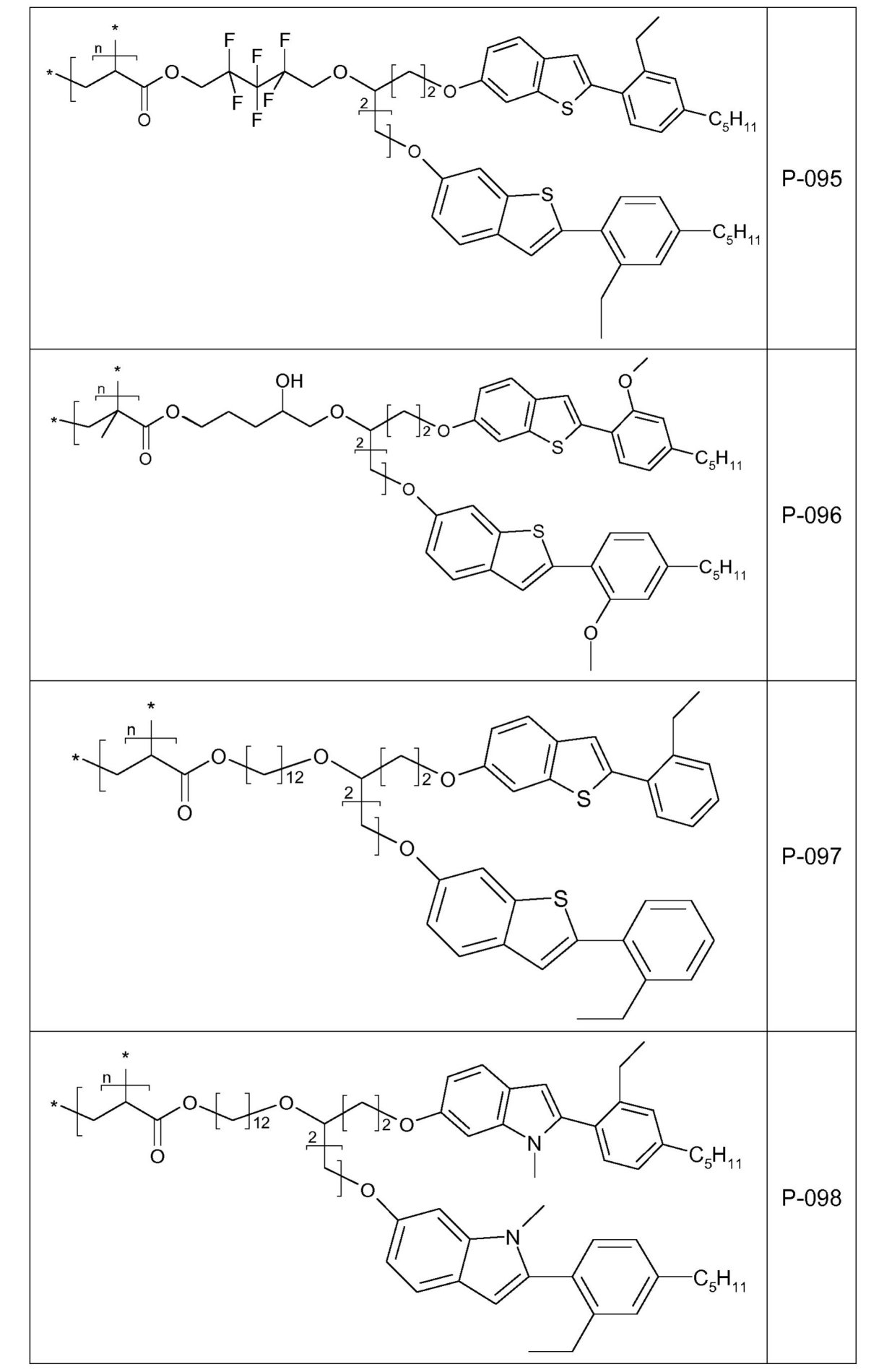
を通して表されるとおり、XがSであり、かつdが0である場合のベンゾ[b]チオフェン環系を基にする。好ましくは、リンカー
は、ベンゾ[b]チオフェン環系の位置6または5に結合されている。
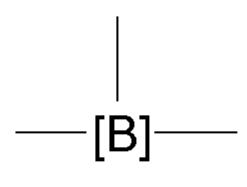
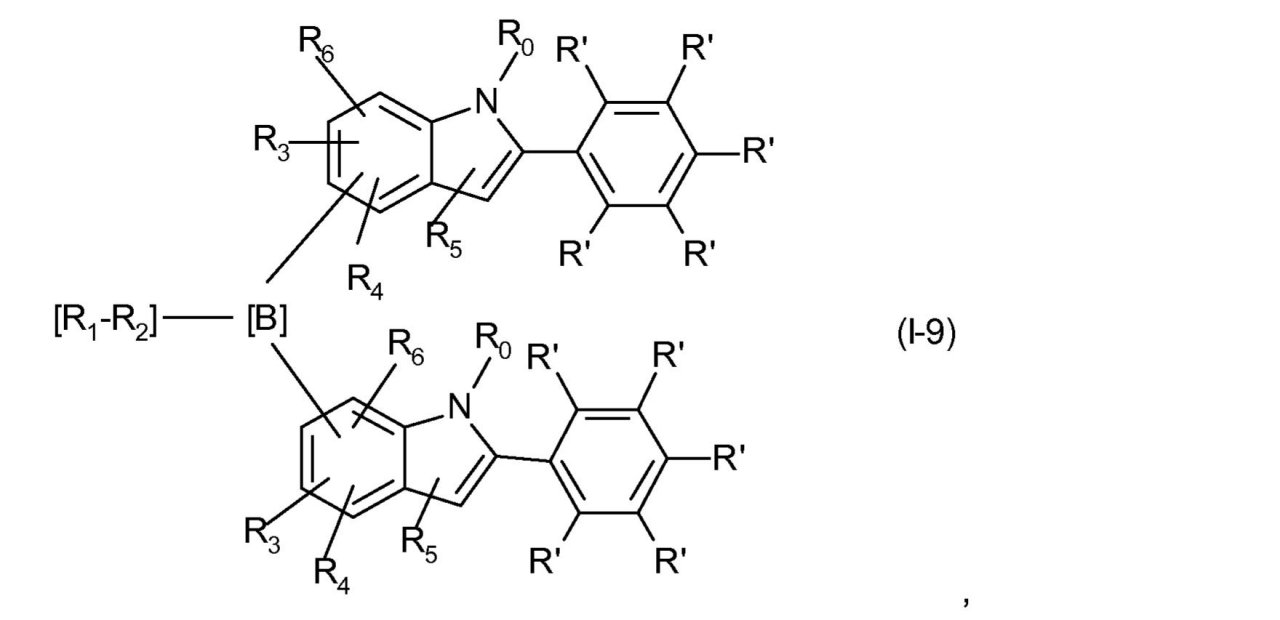
をもつ式(I)で表される化合物は、式(I-9)、
ここでR1、-R2-、R3、R4、R5、R6、R0およびR’は、前に記載されたとおりのまたは下に好ましく記載されたとおりの意味を有する、
を通して表されるとおり、dが0であり、かつXがNR0である場合のベンゾ[b]ピロール環系を基にする。好ましくは、リンカー
は、ベンゾ[b]ピロール環系の位置6または5に結合されている。
XがNR0である場合、R0は、具体的に好ましくは、エチル、イソ-プロピル、2-メチル-プロピル、n-ペンチルまたは4-メチル-ペンチルである。
をもつ式(I)で表される化合物は、好ましくは、式(I-1)、(I-2)、(I-3)、(I-4)、(I-5)および(I-6)(ここでR1、-R2-、R3、R4、R5、R6、R0およびR’は、前に記載されたとおりのまたは下に好ましく記載されたとおりの意味を有する)で表され、dが1であるときに得られる化合物である。
をもつ式(I)で表される化合物は、式(I-1)(ここでR1、-R2-、R3、R4、R5、R6およびR’は、前に記載されたとおりのまたは下に好ましく記載されたとおりの意味を有する)を通して表されるとき、dが1であり、かつXおよびX0がOであるときに、具体的に好ましい。
、ペンタフルオロエトキシ、2-ヒドロキシ-エチル、3-ヒドロキシ-プロピル、4-ヒドロキシ-ブチル、および5-ヒドロキシ-ペンチルからなる群から選択される。
前に定義されたとおりのまたは前に好ましく定義されたとおりのリンカー
をもつ式(I)、(I-1)、(I-2)、(I-3)、(I-4)、(I-5)、(I-6)、(I-7)、(I-8)および(I-9)で表される化合物は、出現毎に独立した置換基R’の選択を通して築かれたそれらの置換パターンを通すのがさらに好ましい。
のO原子へ結合されている。
したがって、本発明はさらに、前に記載のとおりのまたは前に好ましく記載されたとおりの式(I)で表される化合物を対象にするが、式中少なくとも2個のR’がHではない。
のO原子へ結合されている。
したがって、本発明はさらに、前に記載のとおりのまたは前に好ましく記載されたとおりの式(I)で表される化合物を対象にするが、式中少なくとも4個のR’がHではない。
のO原子へ結合されている。
R3、R4、R5およびR6は、好ましくはHまたはFである。R3、R4、R5およびR6は、具体的に好ましくはHである。
および置換基をもつ式(I)、(I-1)~(I-9)で表される化合物は、前に記載のとおりのまたは前もしくは下に好ましく記載されたとおりの重合性基を有し、および少なくとも1個の連結要素[-R2-]を有する。
Rは、極めて具体的に好ましくは、Hである。
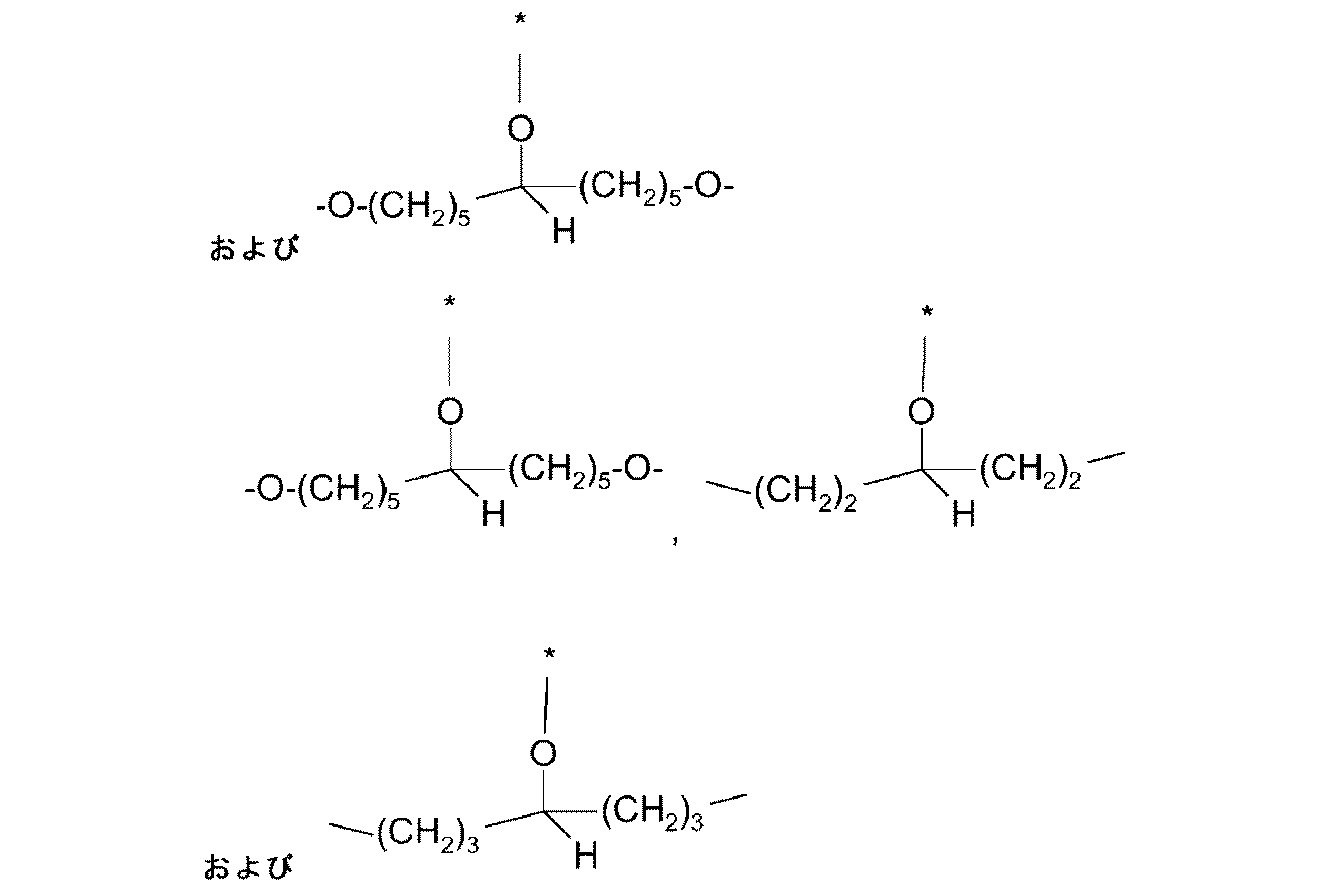
-(CH2)3-、-(CH2)4-、-(CH2)5-、-(CH2)6-、
-(CH2)7-、-(CH2)8-、-(CH2)9-、-(CH2)10-、
-(CH2)11-、-(CH2)12-、-(CH2)13-、-(CH2)14-、
-(CH2)15-、-(CH2)16-、-(CH2)17-、-(CH2)18-、
-(CH2)19-、-(CH2)20-、-(CHCH3)-、
-(CHCH3)2-、-(CHCH3)3-、-(CHCH3)4-、
-(CHCH3)5-、-(CHCH3)6-、-(CHCH3)7-、
-(CHCH3)8-、-(CHCH3)9-、-(CHCH3)10-、
-(CHCH3)11-、-(CHCH3)12-、-(CHCH3)13-、
-(CHCH3)14-、-(CHCH3)15-、-(CHCH3)16-、
-(CHCH3)17-、-(CHCH3)18-、-(CHCH3)19-、
-(CHCH3)20-、-(C(CH3)2)-、-(C(CH3)2)2-、
-(C(CH3)2)3-、-(C(CH3)2)4-、-(C(CH3)2)5-、
-(C(CH3)2)6-、-(C(CH3)2)7-、-(C(CH3)2)8-、
-(C(CH3)2)9-、-(C(CH3)2)10-、
-(C(CH3)2)11-、-(C(CH3)2)12-、
-(C(CH3)2)13-、-(C(CH3)2)14-、
-(C(CH3)2)15-、-(C(CH3)2)16-、
-(C(CH3)2)17-、-(C(CH3)2)18-、
-(C(CH3)2)19-、-(C(CH3)2)20-、
-(CHC2H5)4-、-(CHC2H5)5-、-(CHC2H5)6-、
-(CHC2H5)7-、-(CHC2H5)8-、-(CHC2H5)9-、
-(CHC2H5)10-、-(CHC2H5)11-、-(CHC2H5)12-、
-(CHC2H5)13-、-(CHC2H5)14-、-(CHC2H5)15-、
-(CHC2H5)16-、-(CHC2H5)17-、-(CHC2H5)18-、
-(CHC2H5)19-、-(CHC2H5)20-、
-(CH2)-(CHCH3)-(CH2)-、
-(CH2)-(CHCH3)-(CH2)2-、
-(CH2)-(CHCH3)-(CH2)3-、
-(CH2)-(CHCH3)-(CH2)11-、
-(CH2)2-(CHCH3)-(CH2)-、
-(CH2)3-(CHCH3)-(CH2)-、
-(CH2)11-(CHCH3)-(CH2)-、
-(CH2)2-O-(CH2)2-、-(CH2)3-O-(CH2)3-、
-(CH2)2-O-(CH2)2-O-(CH2)2-、
-(CH2)3-O-(CH2)3-O-(CH2)3-、
-(CH2)2-O-(CH2)2-O-(CH2)6-、
-(CH2)6-O-(CH2)2-O-(CH2)2-、
-(CH2)2-O-(CH2)2-O-(CH2)8-、
-(CH2)8-O-(CH2)2-O-(CH2)2-、
-(CH2)2-S-(CH2)2-S-(CH2)2-、
-(CH2)3-S-(CH2)3-S-(CH2)3-、
-(CH2)2-S-(CH2)2-S-(CH2)6-、
-(CH2)6-S-(CH2)2-S-(CH2)2-、
-(CH2)2-S-(CH2)2-S-(CH2)8-、
-(CH2)8-S-(CH2)2-S-(CH2)2-、
-(CH2)2-(NCH3)-(CH2)2-、
-(CH2)3-(NCH3)-(CH2)3-、
-(CH2)2-(NCH3)-(CH2)2-(NCH3)-(CH2)2-、
-(CH2)3-(NCH3)-(CH2)3-(NCH3)-(CH2)3-、
-(CH2)2-(NCH3)-(CH2)2-(NCH3)-(CH2)6-、
-(CH2)6-(NCH3)-(CH2)2-(NCH3)-(CH2)2-、
-(CH2)2-(NCH3)-(CH2)2-(NCH3)-(CH2)8-、および
-(CH2)8-(NCH3)-(CH2)2-(NCH3)-(CH2)2-、
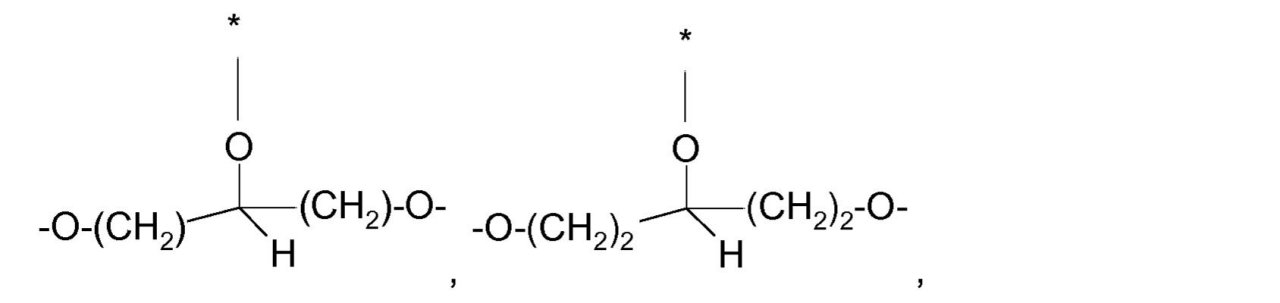
-(CH2)-(CHOH)-(CH2)-、
-(CH2)-(CHOH)-(CH2)2-、
-(CH2)-(CHOH)-(CH2)3-、
-(CH2)-(CHOH)-(CH2)4-、
-(CH2)-(CHOH)-(CH2)5-、
-(CH2)-(CHOH)-(CH2)6-、
-(CH2)-(CHOH)-(CH2)7-、
-(CH2)-(CHOH)-(CH2)8-、
-(CH2)2-(CHOH)-(CH2)-、
-(CH2)3-(CHOH)-(CH2)-、
-(CH2)4-(CHOH)-(CH2)-、
-(CH2)5-(CHOH)-(CH2)-、
-(CH2)6-(CHOH)-(CH2)-、
-(CH2)7-(CHOH)-(CH2)-、
-(CH2)8-(CHOH)-(CH2)-、
-(CH2)2-(CHOH)-(CH2)2-、
-(CH2)3-(CHOH)-(CH2)3-、
-(CH2)4-(CHOH)-(CH2)4-、
-(CH2)5-(CHOH)-(CH2)5-、
-(CH2)-[CH(CH2OH)]-、
-(CH2)-[CH(CH2OH)]-(CH2)-、
-(CH2)-[CH(CH2OH)]-(CH2)2-、
-(CH2)-[CH(CH2OH)]-(CH2)3-、
-(CH2)-[CH(CH2OH)]-(CH2)4-、
-(CH2)-[CH(CH2OH)]-(CH2)5-、
-(CH2)-[CH(CH2OH)]-(CH2)6-、
-(CH2)-[CH(CH2OH)]-(CH2)7-、
-(CH2)-[CH(CH2OH)]-(CH2)8-、
-(CH2)2-[CH(CH2OH)]-(CH2)-、
-(CH2)3-[CH(CH2OH)]-(CH2)-、
-(CH2)4-[CH(CH2OH)]-(CH2)-、
-(CH2)5-[CH(CH2OH)]-(CH2)-、
-(CH2)6-[CH(CH2OH)]-(CH2)-、
-(CH2)7-[CH(CH2OH)]-(CH2)-、
-(CH2)8-[CH(CH2OH)]-(CH2)-、
-(CH2)2-[CH(CH2OH)]-(CH2)2-、
-(CH2)3-[CH(CH2OH)]-(CH2)3-、
-(CH2)4-[CH(CH2OH)]-(CH2)4-、
-(CH2)5-[CH(CH2OH)]-(CH2)5-、
-(CH2)2-(CHOH)-(CHOH)-(CH2)2-、
-(CH2)3-(CHOH)-(CHOH)-(CH2)3-、
-(CH2)4-(CHOH)-(CHOH)-(CH2)4-、
-(CH2)-(CHOH)-(CHOH)-(CH2)3-、
-(CH2)-(CHOH)-(CHOH)-(CH2)4-、
-(CH2)-(CHOH)-(CHOH)-(CH2)5-、
-(CH2)-(CHOH)-(CHOH)-(CH2)6-、
-(CH2)-(CHOH)-(CHOH)-(CH2)7-、
-(CH2)3-(CHOH)-(CHOH)-(CH2)-、
-(CH2)4-(CHOH)-(CHOH)-(CH2)-、
-(CH2)5-(CHOH)-(CHOH)-(CH2)-、
-(CH2)6-(CHOH)-(CHOH)-(CH2)-、
-(CH2)7-(CHOH)-(CHOH)-(CH2)-、
-(CH2)2-(CHOH)-(CHOH)-(CH2)3-、
-(CH2)2-(CHOH)-(CHOH)-(CH2)4-、
-(CH2)2-(CHOH)-(CHOH)-(CH2)5-、
-(CH2)2-(CHOH)-(CHOH)-(CH2)6-、
-(CH2)3-(CHOH)-(CHOH)-(CH2)2-、
-(CH2)4-(CHOH)-(CHOH)-(CH2)2-、
-(CH2)5-(CHOH)-(CHOH)-(CH2)2-、
-(CH2)6-(CHOH)-(CHOH)-(CH2)2-、
-(CH2)3-(CHOH)-(CHOH)-(CH2)4-、
-(CH2)4-(CHOH)-(CHOH)-(CH2)3-、
-(CH2)3-(CHOH)-(CHOH)-(CH2)5-、
-(CH2)5-(CHOH)-(CHOH)-(CH2)3-、
-(CH2)2-(CHOH)-(CH2)-(CHOH)-(CH2)2-、
-(CH2)3-(CHOH)-(CH2)-(CHOH)-(CH2)3-、
-(CH2)4-(CHOH)-(CH2)-(CHOH)-(CH2)4-、
-(CH2)-(CHOH)-(CH2)-(CHOH)-(CH2)3-、
-(CH2)-(CHOH)-(CH2)-(CHOH)-(CH2)4-、
-(CH2)-(CHOH)-(CH2)-(CHOH)-(CH2)5-、
-(CH2)-(CHOH)-(CH2)-(CHOH)-(CH2)6-、
-(CH2)-(CHOH)-(CH2)-(CHOH)-(CH2)7-、
-(CH2)3-(CHOH)-(CH2)-(CHOH)-(CH2)-、
-(CH2)4-(CHOH)-(CH2)-(CHOH)-(CH2)-、
-(CH2)5-(CHOH)-(CH2)-(CHOH)-(CH2)-、
-(CH2)6-(CHOH)-(CH2)-(CHOH)-(CH2)-、
-(CH2)7-(CHOH)-(CH2)-(CHOH)-(CH2)-、
-(CH2)2-(CHOH)-(CH2)-(CHOH)-(CH2)3-、
-(CH2)2-(CHOH)-(CH2)-(CHOH)-(CH2)4-、
-(CH2)2-(CHOH)-(CH2)-(CHOH)-(CH2)5-、
-(CH2)2-(CHOH)-(CH2)-(CHOH)-(CH2)6-、
-(CH2)3-(CHOH)-(CH2)-(CHOH)-(CH2)2-、
-(CH2)4-(CHOH)-(CH2)-(CHOH)-(CH2)2-、
-(CH2)5-(CHOH)-(CH2)-(CHOH)-(CH2)2-、
-(CH2)6-(CHOH)-(CH2)-(CHOH)-(CH2)2-、
-(CH2)3-(CHOH)-(CH2)-(CHOH)-(CH2)4-、
-(CH2)4-(CHOH)-(CH2)-(CHOH)-(CH2)3-、
-(CH2)2-(CHOH)-(CH2)2-(CHOH)-(CH2)2-、
-(CH2)3-(CHOH)-(CH2)2-(CHOH)-(CH2)3-、
-(CH2)4-(CHOH)-(CH2)2-(CHOH)-(CH2)4-、
-(CH2)-(CHOH)-(CH2)2-(CHOH)-(CH2)3-、
-(CH2)-(CHOH)-(CH2)2-(CHOH)-(CH2)4-、
-(CH2)-(CHOH)-(CH2)2-(CHOH)-(CH2)5-、
-(CH2)-(CHOH)-(CH2)2-(CHOH)-(CH2)6-、
-(CH2)-(CHOH)-(CH2)2-(CHOH)-(CH2)7-、
-(CH2)3-(CHOH)-(CH2)2-(CHOH)-(CH2)-、
-(CH2)4-(CHOH)-(CH2)2-(CHOH)-(CH2)-、
-(CH2)5-(CHOH)-(CH2)2-(CHOH)-(CH2)-、
-(CH2)6-(CHOH)-(CH2)2-(CHOH)-(CH2)-、
-(CH2)7-(CHOH)-(CH2)2-(CHOH)-(CH2)-、
-(CH2)2-(CHOH)-(CH2)2-(CHOH)-(CH2)3-、
-(CH2)2-(CHOH)-(CH2)2-(CHOH)-(CH2)4-、
-(CH2)2-(CHOH)-(CH2)2-(CHOH)-(CH2)5-、
-(CH2)2-(CHOH)-(CH2)2-(CHOH)-(CH2)6-、
-(CH2)3-(CHOH)-(CH2)2-(CHOH)-(CH2)2-、
-(CH2)4-(CHOH)-(CH2)2-(CHOH)-(CH2)2-、
-(CH2)5-(CHOH)-(CH2)2-(CHOH)-(CH2)2-、
-(CH2)6-(CHOH)-(CH2)2-(CHOH)-(CH2)2-、
-(CH2)3-(CHOH)-(CH2)2-(CHOH)-(CH2)4-、
-(CH2)4-(CHOH)-(CH2)2-(CHOH)-(CH2)3-、
-(CH2)2-(CHOH)-(CH2)-[CH(CH2OH)]-(CH2)2-、
-(CH2)3-(CHOH)-(CH2)-[CH(CH2OH)]-(CH2)3-、
-(CH2)4-(CHOH)-(CH2)-[CH(CH2OH)]-(CH2)4-、
-(CH2)-(CHOH)-(CH2)-[CH(CH2OH)]-(CH2)3-、
-(CH2)-(CHOH)-(CH2)-[CH(CH2OH)]-(CH2)4-、
-(CH2)-(CHOH)-(CH2)-[CH(CH2OH)]-(CH2)5-、
-(CH2)-(CHOH)-(CH2)-[CH(CH2OH)]-(CH2)6-、
-(CH2)-(CHOH)-(CH2)-[CH(CH2OH)]-(CH2)7-、
-(CH2)3-(CHOH)-(CH2)-[CH(CH2OH)]-(CH2)-、
-(CH2)4-(CHOH)-(CH2)-[CH(CH2OH)]-(CH2)-、
-(CH2)5-(CHOH)-(CH2)-[CH(CH2OH)]-(CH2)-、
-(CH2)6-(CHOH)-(CH2)-[CH(CH2OH)]-(CH2)-、
-(CH2)7-(CHOH)-(CH2)-[CH(CH2OH)]-(CH2)-、
-(CH2)2-(CHOH)-(CH2)-[CH(CH2OH)]-(CH2)3-、
-(CH2)2-(CHOH)-(CH2)-[CH(CH2OH)]-(CH2)4-、
-(CH2)2-(CHOH)-(CH2)-[CH(CH2OH)]-(CH2)5-、
-(CH2)2-(CHOH)-(CH2)-[CH(CH2OH)]-(CH2)6-、
-(CH2)3-(CHOH)-(CH2)-[CH(CH2OH)]-(CH2)2-、
-(CH2)4-(CHOH)-(CH2)-[CH(CH2OH)]-(CH2)2-、
-(CH2)5-(CHOH)-(CH2)-[CH(CH2OH)]-(CH2)2-、
-(CH2)6-(CHOH)-(CH2)-[CH(CH2OH)]-(CH2)2-、
-(CH2)3-(CHOH)-(CH2)-[CH(CH2OH)]-(CH2)4-、
-(CH2)4-(CHOH)-(CH2)-[CH(CH2OH)]-(CH2)3-、
-(CH2)2-(CHOH)-(CH2)2-[CH(CH2OH)]-(CH2)2-、
-(CH2)3-(CHOH)-(CH2)2-[CH(CH2OH)]-(CH2)3-、
-(CH2)4-(CHOH)-(CH2)2-[CH(CH2OH)]-(CH2)4-、
-(CH2)-(CHOH)-(CH2)2-[CH(CH2OH)]-(CH2)3-、
-(CH2)-(CHOH)-(CH2)2-[CH(CH2OH)]-(CH2)4-、
-(CH2)-(CHOH)-(CH2)2-[CH(CH2OH)]-(CH2)5-、
-(CH2)-(CHOH)-(CH2)2-[CH(CH2OH)]-(CH2)6-、
-(CH2)-(CHOH)-(CH2)2-[CH(CH2OH)]-(CH2)7-、
-(CH2)3-(CHOH)-(CH2)2-[CH(CH2OH)]-(CH2)-、
-(CH2)4-(CHOH)-(CH2)2-[CH(CH2OH)]-(CH2)-、
-(CH2)5-(CHOH)-(CH2)2-[CH(CH2OH)]-(CH2)-、
-(CH2)6-(CHOH)-(CH2)2-[CH(CH2OH)]-(CH2)-、
-(CH2)7-(CHOH)-(CH2)2-[CH(CH2OH)]-(CH2)-、
-(CH2)2-(CHOH)-(CH2)2-[CH(CH2OH)]-(CH2)3-、
-(CH2)2-(CHOH)-(CH2)2-[CH(CH2OH)]-(CH2)4-、
-(CH2)2-(CHOH)-(CH2)2-[CH(CH2OH)]-(CH2)5-、
-(CH2)2-(CHOH)-(CH2)2-[CH(CH2OH)]-(CH2)6-、
-(CH2)3-(CHOH)-(CH2)2-[CH(CH2OH)]-(CH2)2-、
-(CH2)4-(CHOH)-(CH2)2-[CH(CH2OH)]-(CH2)2-、
-(CH2)5-(CHOH)-(CH2)2-[CH(CH2OH)]-(CH2)2-、
-(CH2)6-(CHOH)-(CH2)2-[CH(CH2OH)]-(CH2)2-、
-(CH2)3-(CHOH)-(CH2)2-[CH(CH2OH)]-(CH2)4-、
-(CH2)4-(CHOH)-(CH2)2-[CH(CH2OH)]-(CH2)3-、
-(CH2)2-[CH(CH2OH)]-(CH2)2-(CHOH)-(CH2)2-、
-(CH2)3-[CH(CH2OH)]-(CH2)2-(CHOH)-(CH2)3-、
-(CH2)4-[CH(CH2OH)]-(CH2)2-(CHOH)-(CH2)4-、
-(CH2)-[CH(CH2OH)]-(CH2)2-(CHOH)-(CH2)3-、
-(CH2)-[CH(CH2OH)]-(CH2)2-(CHOH)-(CH2)4-、
-(CH2)-[CH(CH2OH)]-(CH2)2-(CHOH)-(CH2)5-、
-(CH2)-[CH(CH2OH)]-(CH2)2-(CHOH)-(CH2)6-、
-(CH2)-[CH(CH2OH)]-(CH2)2-(CHOH)-(CH2)7-、
-(CH2)3-[CH(CH2OH)]-(CH2)2-(CHOH)-(CH2)-、
-(CH2)4-[CH(CH2OH)]-(CH2)2-(CHOH)-(CH2)-、
-(CH2)5-[CH(CH2OH)]-(CH2)2-(CHOH)-(CH2)-、
-(CH2)6-[CH(CH2OH)]-(CH2)2-(CHOH)-(CH2)-、
-(CH2)7-[CH(CH2OH)]-(CH2)2-(CHOH)-(CH2)-、
-(CH2)2-[CH(CH2OH)]-(CH2)2-(CHOH)-(CH2)3-、
-(CH2)2-[CH(CH2OH)]-(CH2)2-(CHOH)-(CH2)4-、
-(CH2)2-[CH(CH2OH)]-(CH2)2-(CHOH)-(CH2)5-、
-(CH2)2-[CH(CH2OH)]-(CH2)2-(CHOH)-(CH2)6-、
-(CH2)3-[CH(CH2OH)]-(CH2)2-(CHOH)-(CH2)2-、
-(CH2)4-[CH(CH2OH)]-(CH2)2-(CHOH)-(CH2)2-、
-(CH2)5-[CH(CH2OH)]-(CH2)2-(CHOH)-(CH2)2-、
-(CH2)6-[CH(CH2OH)]-(CH2)2-(CHOH)-(CH2)2-、
-(CH2)3-[CH(CH2OH)]-(CH2)2-(CHOH)-(CH2)4-、
-(CH2)4-[CH(CH2OH)]-(CH2)2-(CHOH)-(CH2)3-、
-(CH2)2-[CH(CH2OH)]-(CH2)-(CHOH)-(CH2)2-、
-(CH2)3-[CH(CH2OH)]-(CH2)-(CHOH)-(CH2)3-、
-(CH2)4-[CH(CH2OH)]-(CH2)-(CHOH)-(CH2)4-、
-(CH2)-[CH(CH2OH)]-(CH2)-(CHOH)-(CH2)3-、
-(CH2)-[CH(CH2OH)]-(CH2)-(CHOH)-(CH2)4-、
-(CH2)-[CH(CH2OH)]-(CH2)-(CHOH)-(CH2)5-、
-(CH2)-[CH(CH2OH)]-(CH2)-(CHOH)-(CH2)6-、
-(CH2)-[CH(CH2OH)]-(CH2)-(CHOH)-(CH2)7-、
-(CH2)3-[CH(CH2OH)]-(CH2)-(CHOH)-(CH2)-、
-(CH2)4-[CH(CH2OH)]-(CH2)-(CHOH)-(CH2)-、
-(CH2)5-[CH(CH2OH)]-(CH2)-(CHOH)-(CH2)-、
-(CH2)6-[CH(CH2OH)]-(CH2)-(CHOH)-(CH2)-、
-(CH2)7-[CH(CH2OH)]-(CH2)-(CHOH)-(CH2)-、
-(CH2)2-[CH(CH2OH)]-(CH2)-(CHOH)-(CH2)3-、
-(CH2)2-[CH(CH2OH)]-(CH2)-(CHOH)-(CH2)4-、
-(CH2)2-[CH(CH2OH)]-(CH2)-(CHOH)-(CH2)5-、
-(CH2)2-[CH(CH2OH)]-(CH2)-(CHOH)-(CH2)6-、
-(CH2)3-[CH(CH2OH)]-(CH2)-(CHOH)-(CH2)2-、
-(CH2)4-[CH(CH2OH)]-(CH2)-(CHOH)-(CH2)2-、
-(CH2)5-[CH(CH2OH)]-(CH2)-(CHOH)-(CH2)2-、
-(CH2)6-[CH(CH2OH)]-(CH2)-(CHOH)-(CH2)2-、
-(CH2)3-[CH(CH2OH)]-(CH2)-(CHOH)-(CH2)4-、
-(CH2)4-[CH(CH2OH)]-(CH2)-(CHOH)-(CH2)3-、
-(CH2)2-(CHOH)-(CHOH)-(CH2)-(CHOH)-(CHOH)-(CH2)2-、
-(CH2)3-(CHOH)-(CHOH)-(CH2)-(CHOH)-(CHOH)-(CH2)3-、
-(CH2)4-(CHOH)-(CHOH)-(CH2)-(CHOH)-(CHOH)-(CH2)4-、
-(CH2)-(CHOH)-(CHOH)-(CH2)-(CHOH)-(CHOH)-(CH2)3-、
-(CH2)-(CHOH)-(CHOH)-(CH2)-(CHOH)-(CHOH)-(CH2)4-、
-(CH2)-(CHOH)-(CHOH)-(CH2)-(CHOH)-(CHOH)-(CH2)5-、
-(CH2)-(CHOH)-(CHOH)-(CH2)-(CHOH)-(CHOH)-(CH2)6-、
-(CH2)-(CHOH)-(CHOH)-(CH2)-(CHOH)-(CHOH)-(CH2)7-、
-(CH2)3-(CHOH)-(CHOH)-(CH2)-(CHOH)-(CHOH)-(CH2)-、
-(CH2)4-(CHOH)-(CHOH)-(CH2)-(CHOH)-(CHOH)-(CH2)-、
-(CH2)5-(CHOH)-(CHOH)-(CH2)-(CHOH)-(CHOH)-(CH2)-、
-(CH2)6-(CHOH)-(CHOH)-(CH2)-(CHOH)-(CHOH)-(CH2)-、
-(CH2)7-(CHOH)-(CHOH)-(CH2)-(CHOH)-(CHOH)-(CH2)-、
-(CH2)2-(CHOH)-(CHOH)-(CH2)-(CHOH)-(CHOH)-(CH2)3-、
-(CH2)2-(CHOH)-(CHOH)-(CH2)-(CHOH)-(CHOH)-(CH2)4-、
-(CH2)2-(CHOH)-(CHOH)-(CH2)-(CHOH)-(CHOH)-(CH2)5-、
-(CH2)2-(CHOH)-(CHOH)-(CH2)-(CHOH)-(CHOH)-(CH2)6-、
-(CH2)3-(CHOH)-(CHOH)-(CH2)-(CHOH)-(CHOH)-(CH2)2-、
-(CH2)4-(CHOH)-(CHOH)-(CH2)-(CHOH)-(CHOH)-(CH2)2-、
-(CH2)5-(CHOH)-(CHOH)-(CH2)-(CHOH)-(CHOH)-(CH2)2-、
-(CH2)6-(CHOH)-(CHOH)-(CH2)-(CHOH)-(CHOH)-(CH2)2-、
-(CH2)3-(CHOH)-(CHOH)-(CH2)-(CHOH)-(CHOH)-(CH2)4-、
-(CH2)4-(CHOH)-(CHOH)-(CH2)-(CHOH)-(CHOH)-(CH2)3-、
-(CH2)3-(CHOH)-(CHOH)-(CH2)-(CHOH)-(CHOH)-(CH2)5-、
-(CH2)5-(CHOH)-(CHOH)-(CH2)-(CHOH)-(CHOH)-(CH2)3-、
-(CH2)2-(CHOH)-(CH2)-O-(CH2)2-O-(CH2)-(CHOH)-(CH2)2-、
-(CH2)3-(CHOH)-(CH2)-O-(CH2)2-O-(CH2)-(CHOH)-(CH2)3-、
-(CH2)4-(CHOH)-(CH2)-O-(CH2)2-O-(CH2)-(CHOH)-(CH2)4-、
-(CH2)-(CHOH)-(CH2)-O-(CH2)2-O-(CH2)-(CHOH)-(CH2)3-、
-(CH2)-(CHOH)-(CH2)-O-(CH2)2-O-(CH2)-(CHOH)-(CH2)4-、
-(CH2)-(CHOH)-(CH2)-O-(CH2)2-O-(CH2)-(CHOH)-(CH2)5-、
-(CH2)-(CHOH)-(CH2)-O-(CH2)2-O-(CH2)-(CHOH)-(CH2)6-、
-(CH2)-(CHOH)-(CH2)-O-(CH2)2-O-(CH2)-(CHOH)-(CH2)7-、
-(CH2)3-(CHOH)-(CH2)-O-(CH2)2-O-(CH2)-(CHOH)-(CH2)-、
-(CH2)4-(CHOH)-(CH2)-O-(CH2)2-O-(CH2)-(CHOH)-(CH2)-、
-(CH2)5-(CHOH)-(CH2)-O-(CH2)2-O-(CH2)-(CHOH)-(CH2)-、
-(CH2)6-(CHOH)-(CH2)-O-(CH2)2-O-(CH2)-(CHOH)-(CH2)-、
-(CH2)7-(CHOH)-(CH2)-O-(CH2)2-O-(CH2)-(CHOH)-(CH2)-、
-(CH2)2-(CHOH)-(CH2)-O-(CH2)2-O-(CH2)-(CHOH)-(CH2)3-、
-(CH2)2-(CHOH)-(CH2)-O-(CH2)2-O-(CH2)-(CHOH)-(CH2)4-、
-(CH2)2-(CHOH)-(CH2)-O-(CH2)2-O-(CH2)-(CHOH)-(CH2)5-、
-(CH2)2-(CHOH)-(CH2)-O-(CH2)2-O-(CH2)-(CHOH)-(CH2)6-、
-(CH2)3-(CHOH)-(CH2)-O-(CH2)2-O-(CH2)-(CHOH)-(CH2)2-、
-(CH2)4-(CHOH)-(CH2)-O-(CH2)2-O-(CH2)-(CHOH)-(CH2)2-、
-(CH2)5-(CHOH)-(CH2)-O-(CH2)2-O-(CH2)-(CHOH)-(CH2)2-、
-(CH2)6-(CHOH)-(CH2)-O-(CH2)2-O-(CH2)-(CHOH)-(CH2)2-、
-(CH2)3-(CHOH)-(CH2)-O-(CH2)2-O-(CH2)-(CHOH)-(CH2)4-、
-(CH2)4-(CHOH)-(CH2)-O-(CH2)2-O-(CH2)-(CHOH)-(CH2)3-、
-(CH2)3-(CHOH)-(CH2)-O-(CH2)2-O-(CH2)-(CHOH)-(CH2)5-、
-(CH2)5-(CHOH)-(CH2)-O-(CH2)2-O-(CH2)-(CHOH)-(CH2)3-、
-(CH2)2-(CHOH)-(CH2)-O-(CH2)3-O-(CH2)-(CHOH)-(CH2)2-、
-(CH2)3-(CHOH)-(CH2)-O-(CH2)3-O-(CH2)-(CHOH)-(CH2)3-、
-(CH2)4-(CHOH)-(CH2)-O-(CH2)3-O-(CH2)-(CHOH)-(CH2)4-、
-(CH2)-(CHOH)-(CH2)-O-(CH2)3-O-(CH2)-(CHOH)-(CH2)3-、
-(CH2)-(CHOH)-(CH2)-O-(CH2)3-O-(CH2)-(CHOH)-(CH2)4-、
-(CH2)-(CHOH)-(CH2)-O-(CH2)3-O-(CH2)-(CHOH)-(CH2)5-、
-(CH2)-(CHOH)-(CH2)-O-(CH2)3-O-(CH2)-(CHOH)-(CH2)6-、
-(CH2)-(CHOH)-(CH2)-O-(CH2)3-O-(CH2)-(CHOH)-(CH2)7-、
-(CH2)3-(CHOH)-(CH2)-O-(CH2)3-O-(CH2)-(CHOH)-(CH2)-、
-(CH2)4-(CHOH)-(CH2)-O-(CH2)3-O-(CH2)-(CHOH)-(CH2)-、
-(CH2)5-(CHOH)-(CH2)-O-(CH2)3-O-(CH2)-(CHOH)-(CH2)-、
-(CH2)6-(CHOH)-(CH2)-O-(CH2)3-O-(CH2)-(CHOH)-(CH2)-、
-(CH2)7-(CHOH)-(CH2)-O-(CH2)3-O-(CH2)-(CHOH)-(CH2)-、
-(CH2)2-(CHOH)-(CH2)-O-(CH2)3-O-(CH2)-(CHOH)-(CH2)3-、
-(CH2)2-(CHOH)-(CH2)-O-(CH2)3-O-(CH2)-(CHOH)-(CH2)4-、
-(CH2)2-(CHOH)-(CH2)-O-(CH2)3-O-(CH2)-(CHOH)-(CH2)5-、
-(CH2)2-(CHOH)-(CH2)-O-(CH2)3-O-(CH2)-(CHOH)-(CH2)6-、
-(CH2)3-(CHOH)-(CH2)-O-(CH2)3-O-(CH2)-(CHOH)-(CH2)2-、
-(CH2)4-(CHOH)-(CH2)-O-(CH2)3-O-(CH2)-(CHOH)-(CH2)2-、
-(CH2)5-(CHOH)-(CH2)-O-(CH2)3-O-(CH2)-(CHOH)-(CH2)2-、
-(CH2)6-(CHOH)-(CH2)-O-(CH2)3-O-(CH2)-(CHOH)-(CH2)2-、
-(CH2)3-(CHOH)-(CH2)-O-(CH2)3-O-(CH2)-(CHOH)-(CH2)4-、
-(CH2)4-(CHOH)-(CH2)-O-(CH2)3-O-(CH2)-(CHOH)-(CH2)3-、
-(CH2)3-(CHOH)-(CH2)-O-(CH2)3-O-(CH2)-(CHOH)-(CH2)5-、
-(CH2)5-(CHOH)-(CH2)-O-(CH2)3-O-(CH2)-(CHOH)-(CH2)3-、
-(CH2)2-(CHOH)-(CH2)-O-(CH2)4-O-(CH2)-(CHOH)-(CH2)2-、
-(CH2)3-(CHOH)-(CH2)-O-(CH2)4-O-(CH2)-(CHOH)-(CH2)3-、
-(CH2)4-(CHOH)-(CH2)-O-(CH2)4-O-(CH2)-(CHOH)-(CH2)4-、
-(CH2)-(CHOH)-(CH2)-O-(CH2)4-O-(CH2)-(CHOH)-(CH2)3-、
-(CH2)-(CHOH)-(CH2)-O-(CH2)4-O-(CH2)-(CHOH)-(CH2)4-、
-(CH2)-(CHOH)-(CH2)-O-(CH2)4-O-(CH2)-(CHOH)-(CH2)5-、
-(CH2)-(CHOH)-(CH2)-O-(CH2)4-O-(CH2)-(CHOH)-(CH2)6-、
-(CH2)-(CHOH)-(CH2)-O-(CH2)4-O-(CH2)-(CHOH)-(CH2)7-、
-(CH2)3-(CHOH)-(CH2)-O-(CH2)4-O-(CH2)-(CHOH)-(CH2)-、
-(CH2)4-(CHOH)-(CH2)-O-(CH2)4-O-(CH2)-(CHOH)-(CH2)-、
-(CH2)5-(CHOH)-(CH2)-O-(CH2)4-O-(CH2)-(CHOH)-(CH2)-、
-(CH2)6-(CHOH)-(CH2)-O-(CH2)4-O-(CH2)-(CHOH)-(CH2)-、
-(CH2)7-(CHOH)-(CH2)-O-(CH2)4-O-(CH2)-(CHOH)-(CH2)-、
-(CH2)2-(CHOH)-(CH2)-O-(CH2)4-O-(CH2)-(CHOH)-(CH2)3-、
-(CH2)2-(CHOH)-(CH2)-O-(CH2)4-O-(CH2)-(CHOH)-(CH2)4-、
-(CH2)2-(CHOH)-(CH2)-O-(CH2)4-O-(CH2)-(CHOH)-(CH2)5-、
-(CH2)2-(CHOH)-(CH2)-O-(CH2)4-O-(CH2)-(CHOH)-(CH2)6-、
-(CH2)3-(CHOH)-(CH2)-O-(CH2)4-O-(CH2)-(CHOH)-(CH2)2-、
-(CH2)4-(CHOH)-(CH2)-O-(CH2)4-O-(CH2)-(CHOH)-(CH2)2-、
-(CH2)5-(CHOH)-(CH2)-O-(CH2)4-O-(CH2)-(CHOH)-(CH2)2-、
-(CH2)6-(CHOH)-(CH2)-O-(CH2)4-O-(CH2)-(CHOH)-(CH2)2-、
-(CH2)3-(CHOH)-(CH2)-O-(CH2)4-O-(CH2)-(CHOH)-(CH2)4-、
-(CH2)4-(CHOH)-(CH2)-O-(CH2)4-O-(CH2)-(CHOH)-(CH2)3-、
-(CH2)3-(CHOH)-(CH2)-O-(CH2)4-O-(CH2)-(CHOH)-(CH2)5-、
-(CH2)5-(CHOH)-(CH2)-O-(CH2)4-O-(CH2)-(CHOH)-(CH2)3-、
-(CH2)2-(CHOH)-(CH2)-O-(CH2)5-O-(CH2)-(CHOH)-(CH2)2-、
-(CH2)3-(CHOH)-(CH2)-O-(CH2)5-O-(CH2)-(CHOH)-(CH2)3-、
-(CH2)4-(CHOH)-(CH2)-O-(CH2)5-O-(CH2)-(CHOH)-(CH2)4-、
-(CH2)-(CHOH)-(CH2)-O-(CH2)5-O-(CH2)-(CHOH)-(CH2)3-、
-(CH2)-(CHOH)-(CH2)-O-(CH2)5-O-(CH2)-(CHOH)-(CH2)4-、
-(CH2)-(CHOH)-(CH2)-O-(CH2)5-O-(CH2)-(CHOH)-(CH2)5-、
-(CH2)-(CHOH)-(CH2)-O-(CH2)5-O-(CH2)-(CHOH)-(CH2)6-、
-(CH2)-(CHOH)-(CH2)-O-(CH2)5-O-(CH2)-(CHOH)-(CH2)7-、
-(CH2)3-(CHOH)-(CH2)-O-(CH2)5-O-(CH2)-(CHOH)-(CH2)-、
-(CH2)4-(CHOH)-(CH2)-O-(CH2)5-O-(CH2)-(CHOH)-(CH2)-、
-(CH2)5-(CHOH)-(CH2)-O-(CH2)5-O-(CH2)-(CHOH)-(CH2)-、
-(CH2)6-(CHOH)-(CH2)-O-(CH2)5-O-(CH2)-(CHOH)-(CH2)-、
-(CH2)7-(CHOH)-(CH2)-O-(CH2)5-O-(CH2)-(CHOH)-(CH2)-、
-(CH2)2-(CHOH)-(CH2)-O-(CH2)5-O-(CH2)-(CHOH)-(CH2)3-、
-(CH2)2-(CHOH)-(CH2)-O-(CH2)5-O-(CH2)-(CHOH)-(CH2)4-、
-(CH2)2-(CHOH)-(CH2)-O-(CH2)5-O-(CH2)-(CHOH)-(CH2)5-、
-(CH2)2-(CHOH)-(CH2)-O-(CH2)5-O-(CH2)-(CHOH)-(CH2)6-、
-(CH2)3-(CHOH)-(CH2)-O-(CH2)5-O-(CH2)-(CHOH)-(CH2)2-、
-(CH2)4-(CHOH)-(CH2)-O-(CH2)5-O-(CH2)-(CHOH)-(CH2)2-、
-(CH2)5-(CHOH)-(CH2)-O-(CH2)5-O-(CH2)-(CHOH)-(CH2)2-、
-(CH2)6-(CHOH)-(CH2)-O-(CH2)5-O-(CH2)-(CHOH)-(CH2)2-、
-(CH2)3-(CHOH)-(CH2)-O-(CH2)5-O-(CH2)-(CHOH)-(CH2)4-、
-(CH2)4-(CHOH)-(CH2)-O-(CH2)5-O-(CH2)-(CHOH)-(CH2)3-、
-(CH2)3-(CHOH)-(CH2)-O-(CH2)5-O-(CH2)-(CHOH)-(CH2)5-、
-(CH2)5-(CHOH)-(CH2)-O-(CH2)5-O-(CH2)-(CHOH)-(CH2)3-、
-(CH2)2-(CHOH)-(CH2)-O-(CH2)6-O-(CH2)-(CHOH)-(CH2)2-、
-(CH2)3-(CHOH)-(CH2)-O-(CH2)6-O-(CH2)-(CHOH)-(CH2)3-、
-(CH2)4-(CHOH)-(CH2)-O-(CH2)6-O-(CH2)-(CHOH)-(CH2)4-、
-(CH2)-(CHOH)-(CH2)-O-(CH2)6-O-(CH2)-(CHOH)-(CH2)3-、
-(CH2)-(CHOH)-(CH2)-O-(CH2)6-O-(CH2)-(CHOH)-(CH2)4-、
-(CH2)-(CHOH)-(CH2)-O-(CH2)6-O-(CH2)-(CHOH)-(CH2)5-、
-(CH2)-(CHOH)-(CH2)-O-(CH2)6-O-(CH2)-(CHOH)-(CH2)6-、
-(CH2)-(CHOH)-(CH2)-O-(CH2)6-O-(CH2)-(CHOH)-(CH2)7-、
-(CH2)3-(CHOH)-(CH2)-O-(CH2)6-O-(CH2)-(CHOH)-(CH2)-、
-(CH2)4-(CHOH)-(CH2)-O-(CH2)6-O-(CH2)-(CHOH)-(CH2)-、
-(CH2)5-(CHOH)-(CH2)-O-(CH2)6-O-(CH2)-(CHOH)-(CH2)-、
-(CH2)6-(CHOH)-(CH2)-O-(CH2)6-O-(CH2)-(CHOH)-(CH2)-、
-(CH2)7-(CHOH)-(CH2)-O-(CH2)6-O-(CH2)-(CHOH)-(CH2)-、
-(CH2)2-(CHOH)-(CH2)-O-(CH2)6-O-(CH2)-(CHOH)-(CH2)3-、
-(CH2)2-(CHOH)-(CH2)-O-(CH2)6-O-(CH2)-(CHOH)-(CH2)4-、
-(CH2)2-(CHOH)-(CH2)-O-(CH2)6-O-(CH2)-(CHOH)-(CH2)5-、
-(CH2)2-(CHOH)-(CH2)-O-(CH2)6-O-(CH2)-(CHOH)-(CH2)6-、
-(CH2)3-(CHOH)-(CH2)-O-(CH2)6-O-(CH2)-(CHOH)-(CH2)2-、
-(CH2)4-(CHOH)-(CH2)-O-(CH2)6-O-(CH2)-(CHOH)-(CH2)2-、
-(CH2)5-(CHOH)-(CH2)-O-(CH2)6-O-(CH2)-(CHOH)-(CH2)2-、
-(CH2)6-(CHOH)-(CH2)-O-(CH2)6-O-(CH2)-(CHOH)-(CH2)2-、
-(CH2)3-(CHOH)-(CH2)-O-(CH2)6-O-(CH2)-(CHOH)-(CH2)4-、
-(CH2)4-(CHOH)-(CH2)-O-(CH2)6-O-(CH2)-(CHOH)-(CH2)3-、
-(CH2)3-(CHOH)-(CH2)-O-(CH2)6-O-(CH2)-(CHOH)-(CH2)5-、および
-(CH2)5-(CHOH)-(CH2)-O-(CH2)6-O-(CH2)-(CHOH)-(CH2)3-、
-(CH2)-(CF2)-(CH2)-、
-(CH2)-(CF2)-(CH2)2-、
-(CH2)-(CF2)-(CH2)3-、
-(CH2)-(CF2)-(CH2)4-、
-(CH2)-(CF2)-(CH2)5-、
-(CH2)-(CF2)-(CH2)6-、
-(CH2)-(CF2)-(CH2)7-、
-(CH2)-(CF2)-(CH2)8-、
-(CH2)-(CF2)-(CH2)9-、
-(CH2)-(CF2)-(CH2)10-、
-(CH2)2-(CF2)-(CH2)-、
-(CH2)3-(CF2)-(CH2)-、
-(CH2)4-(CF2)-(CH2)-、
-(CH2)5-(CF2)-(CH2)-、
-(CH2)6-(CF2)-(CH2)-、
-(CH2)7-(CF2)-(CH2)-、
-(CH2)8-(CF2)-(CH2)-、
-(CH2)9-(CF2)-(CH2)-、
-(CH2)10-(CF2)-(CH2)-、
-(CH2)2-(CF2)-(CH2)2-、
-(CH2)3-(CF2)-(CH2)3-、
-(CH2)4-(CF2)-(CH2)4-、
-(CH2)5-(CF2)-(CH2)5-、
-(CH2)2-(CF2)-(CH2)-、
-(CH2)2-(CF2)-(CH2)3-、
-(CH2)2-(CF2)-(CH2)4-、
-(CH2)2-(CF2)-(CH2)5-、
-(CH2)2-(CF2)-(CH2)6-、
-(CH2)2-(CF2)-(CH2)7-、
-(CH2)2-(CF2)-(CH2)8-、
-(CH2)2-(CF2)-(CH2)9-、
-(CH2)3-(CF2)-(CH2)-、
-(CH2)3-(CF2)-(CH2)2-、
-(CH2)3-(CF2)-(CH2)4-、
-(CH2)3-(CF2)-(CH2)5-、
-(CH2)3-(CF2)-(CH2)6-、
-(CH2)3-(CF2)-(CH2)7-、
-(CH2)3-(CF2)-(CH2)8-、
-(CH2)4-(CF2)-(CH2)-、
-(CH2)4-(CF2)-(CH2)2-、
-(CH2)4-(CF2)-(CH2)3-、
-(CH2)4-(CF2)-(CH2)5-、
-(CH2)4-(CF2)-(CH2)6-、
-(CH2)4-(CF2)-(CH2)7-、
-(CH2)5-(CF2)-(CH2)-、
-(CH2)5-(CF2)-(CH2)2-、
-(CH2)5-(CF2)-(CH2)3-、
-(CH2)5-(CF2)-(CH2)4-、
-(CH2)5-(CF2)-(CH2)6-、
-(CH2)6-(CF2)-(CH2)-、
-(CH2)6-(CF2)-(CH2)2-、
-(CH2)6-(CF2)-(CH2)3-、
-(CH2)6-(CF2)-(CH2)4-、
-(CH2)6-(CF2)-(CH2)5-、
-(CH2)-(CF2)2-(CH2)-、
-(CH2)-(CF2)2-(CH2)2-、
-(CH2)-(CF2)2-(CH2)3-、
-(CH2)-(CF2)2-(CH2)4-、
-(CH2)-(CF2)2-(CH2)5-、
-(CH2)-(CF2)2-(CH2)6-、
-(CH2)-(CF2)2-(CH2)7-、
-(CH2)-(CF2)2-(CH2)8-、
-(CH2)-(CF2)2-(CH2)9-、
-(CH2)2-(CF2)2-(CH2)-、
-(CH2)3-(CF2)2-(CH2)-、
-(CH2)4-(CF2)2-(CH2)-、
-(CH2)5-(CF2)2-(CH2)-、
-(CH2)6-(CF2)2-(CH2)-、
-(CH2)7-(CF2)2-(CH2)-、
-(CH2)8-(CF2)2-(CH2)-、
-(CH2)9-(CF2)2-(CH2)-、
-(CH2)2-(CF2)2-(CH2)2-、
-(CH2)3-(CF2)2-(CH2)3-、
-(CH2)4-(CF2)2-(CH2)4-、
-(CH2)5-(CF2)2-(CH2)5-、
-(CH2)2-(CF2)2-(CH2)-、
-(CH2)2-(CF2)2-(CH2)3-、
-(CH2)2-(CF2)2-(CH2)4-、
-(CH2)2-(CF2)2-(CH2)5-、
-(CH2)2-(CF2)2-(CH2)6-、
-(CH2)2-(CF2)2-(CH2)7-、
-(CH2)2-(CF2)2-(CH2)8-、
-(CH2)3-(CF2)2-(CH2)-、
-(CH2)3-(CF2)2-(CH2)2-、
-(CH2)3-(CF2)2-(CH2)4-、
-(CH2)3-(CF2)2-(CH2)5-、
-(CH2)3-(CF2)2-(CH2)6-、
-(CH2)3-(CF2)2-(CH2)7-、
-(CH2)4-(CF2)2-(CH2)-、
-(CH2)4-(CF2)2-(CH2)2-、
-(CH2)4-(CF2)2-(CH2)3-、
-(CH2)4-(CF2)2-(CH2)5-、
-(CH2)4-(CF2)2-(CH2)6-、
-(CH2)5-(CF2)2-(CH2)-、
-(CH2)5-(CF2)2-(CH2)2-、
-(CH2)5-(CF2)2-(CH2)3-、
-(CH2)5-(CF2)2-(CH2)4-、
-(CH2)6-(CF2)2-(CH2)-、
-(CH2)6-(CF2)2-(CH2)2-、
-(CH2)6-(CF2)2-(CH2)3-、
-(CH2)6-(CF2)2-(CH2)4-、
-(CH2)-(CF2)3-(CH2)-、
-(CH2)-(CF2)3-(CH2)2-、
-(CH2)-(CF2)3-(CH2)3-、
-(CH2)-(CF2)3-(CH2)4-、
-(CH2)-(CF2)3-(CH2)5-、
-(CH2)-(CF2)3-(CH2)6-、
-(CH2)-(CF2)3-(CH2)7-、
-(CH2)-(CF2)3-(CH2)8-、
-(CH2)2-(CF2)3-(CH2)-、
-(CH2)3-(CF2)3-(CH2)-、
-(CH2)4-(CF2)3-(CH2)-、
-(CH2)5-(CF2)3-(CH2)-、
-(CH2)6-(CF2)3-(CH2)-、
-(CH2)7-(CF2)3-(CH2)-、
-(CH2)8-(CF2)3-(CH2)-、
-(CH2)2-(CF2)3-(CH2)2-、
-(CH2)3-(CF2)3-(CH2)3-、
-(CH2)4-(CF2)3-(CH2)4-、
-(CH2)2-(CF2)3-(CH2)-、
-(CH2)2-(CF2)3-(CH2)3-、
-(CH2)2-(CF2)3-(CH2)4-、
-(CH2)2-(CF2)3-(CH2)5-、
-(CH2)2-(CF2)3-(CH2)6-、
-(CH2)2-(CF2)3-(CH2)7-、
-(CH2)3-(CF2)3-(CH2)-、
-(CH2)3-(CF2)3-(CH2)2-、
-(CH2)3-(CF2)3-(CH2)4-、
-(CH2)3-(CF2)3-(CH2)5-、
-(CH2)3-(CF2)3-(CH2)6-、
-(CH2)4-(CF2)3-(CH2)-、
-(CH2)4-(CF2)3-(CH2)2-、
-(CH2)4-(CF2)3-(CH2)3-、
-(CH2)4-(CF2)3-(CH2)5-、
-(CH2)5-(CF2)3-(CH2)-、
-(CH2)5-(CF2)3-(CH2)2-、
-(CH2)5-(CF2)3-(CH2)3-、
-(CH2)5-(CF2)3-(CH2)4-、
-(CH2)6-(CF2)3-(CH2)-、
-(CH2)6-(CF2)3-(CH2)2-、
-(CH2)6-(CF2)3-(CH2)3-、
-(CH2)-(CF2)4-(CH2)-、
-(CH2)-(CF2)4-(CH2)2-、
-(CH2)-(CF2)4-(CH2)3-、
-(CH2)-(CF2)4-(CH2)4-、
-(CH2)-(CF2)4-(CH2)5-、
-(CH2)-(CF2)4-(CH2)6-、
-(CH2)-(CF2)4-(CH2)7-、
-(CH2)-(CF2)4-(CH2)8-、
-(CH2)-(CF2)4-(CH2)9-、
-(CH2)-(CF2)4-(CH2)10-、
-(CH2)2-(CF2)4-(CH2)-、
-(CH2)3-(CF2)4-(CH2)-、
-(CH2)4-(CF2)4-(CH2)-、
-(CH2)5-(CF2)4-(CH2)-、
-(CH2)6-(CF2)4-(CH2)-、
-(CH2)7-(CF2)4-(CH2)-、
-(CH2)2-(CF2)4-(CH2)2-、
-(CH2)3-(CF2)4-(CH2)3-、
-(CH2)4-(CF2)4-(CH2)4-、
-(CH2)5-(CF2)4-(CH2)5-、
-(CH2)2-(CF2)4-(CH2)3-、
-(CH2)2-(CF2)4-(CH2)4-、
-(CH2)2-(CF2)4-(CH2)5-、
-(CH2)2-(CF2)4-(CH2)6-、
-(CH2)3-(CF2)4-(CH2)2-、
-(CH2)3-(CF2)4-(CH2)4-、
-(CH2)4-(CF2)4-(CH2)2-、
-(CH2)4-(CF2)4-(CH2)3-、
-(CH2)5-(CF2)4-(CH2)2-、
-(CH2)5-(CF2)4-(CH2)3-、
-(CH2)6-(CF2)4-(CH2)2-、
-(CH2)-(CF2)5-(CH2)-、
-(CH2)-(CF2)5-(CH2)2-、
-(CH2)-(CF2)5-(CH2)3-、
-(CH2)-(CF2)5-(CH2)4-、
-(CH2)-(CF2)5-(CH2)5-、
-(CH2)-(CF2)5-(CH2)6-、
-(CH2)2-(CF2)5-(CH2)-、
-(CH2)3-(CF2)5-(CH2)-、
-(CH2)4-(CF2)5-(CH2)-、
-(CH2)5-(CF2)5-(CH2)-、
-(CH2)6-(CF2)5-(CH2)-、
-(CH2)2-(CF2)5-(CH2)2-、
-(CH2)3-(CF2)5-(CH2)3-、
-(CH2)4-(CF2)5-(CH2)4-、
-(CH2)2-(CF2)5-(CH2)3-、
-(CH2)2-(CF2)5-(CH2)4-、
-(CH2)2-(CF2)5-(CH2)5-、
-(CH2)2-(CF2)5-(CH2)6-、
-(CH2)3-(CF2)5-(CH2)2-、
-(CH2)3-(CF2)5-(CH2)4-、
-(CH2)4-(CF2)5-(CH2)2-、
-(CH2)4-(CF2)5-(CH2)3-、
-(CH2)5-(CF2)5-(CH2)2-、
-(CH2)-(CHCF3)-(CH2)-、
-(CH2)-(CHCF3)-(CH2)2-、
-(CH2)-(CHCF3)-(CH2)3-、
-(CH2)-(CHCF3)-(CH2)4-、
-(CH2)-(CHCF3)-(CH2)5-、
-(CH2)-(CHCF3)-(CH2)6-、
-(CH2)-(CHCF3)-(CH2)7-、
-(CH2)-(CHCF3)-(CH2)8-、
-(CH2)-(CHCF3)-(CH2)9-、
-(CH2)-(CHCF3)-(CH2)10-、
-(CH2)2-(CHCF3)-(CH2)-、
-(CH2)3-(CHCF3)-(CH2)-、
-(CH2)4-(CHCF3)-(CH2)-、
-(CH2)5-(CHCF3)-(CH2)-、
-(CH2)6-(CHCF3)-(CH2)-、
-(CH2)7-(CHCF3)-(CH2)-、
-(CH2)8-(CHCF3)-(CH2)-、
-(CH2)9-(CHCF3)-(CH2)-、
-(CH2)10-(CHCF3)-(CH2)-、
-(CH2)2-(CHCF3)-(CH2)2-、
-(CH2)3-(CHCF3)-(CH2)3-、
-(CH2)4-(CHCF3)-(CH2)4-、
-(CH2)5-(CHCF3)-(CH2)5-、
-(CH2)2-(CHCF3)-(CH2)3-、
-(CH2)2-(CHCF3)-(CH2)4-、
-(CH2)2-(CHCF3)-(CH2)5-、
-(CH2)2-(CHCF3)-(CH2)6-、
-(CH2)2-(CHCF3)-(CH2)7-、
-(CH2)2-(CHCF3)-(CH2)8-、
-(CH2)2-(CHCF3)-(CH2)9-、
-(CH2)3-(CHCF3)-(CH2)2-、
-(CH2)3-(CHCF3)-(CH2)4-、
-(CH2)3-(CHCF3)-(CH2)5-、
-(CH2)3-(CHCF3)-(CH2)6-、
-(CH2)3-(CHCF3)-(CH2)7-、
-(CH2)3-(CHCF3)-(CH2)8-、
-(CH2)4-(CHCF3)-(CH2)2-、
-(CH2)4-(CHCF3)-(CH2)3-、
-(CH2)4-(CHCF3)-(CH2)5-、
-(CH2)4-(CHCF3)-(CH2)6-、
-(CH2)4-(CHCF3)-(CH2)7-、
-(CH2)5-(CHCF3)-(CH2)2-、
-(CH2)5-(CHCF3)-(CH2)3-、
-(CH2)5-(CHCF3)-(CH2)4-、
-(CH2)5-(CHCF3)-(CH2)6-、
-(CH2)6-(CHCF3)-(CH2)2-、
-(CH2)6-(CHCF3)-(CH2)3-、
-(CH2)6-(CHCF3)-(CH2)4-、
-(CH2)6-(CHCF3)-(CH2)5-、
-(CH2)-(CHCF3)2-(CH2)-、
-(CH2)-(CHCF3)2-(CH2)2-、
-(CH2)-(CHCF3)2-(CH2)3-、
-(CH2)-(CHCF3)2-(CH2)4-、
-(CH2)-(CHCF3)2-(CH2)5-、
-(CH2)-(CHCF3)2-(CH2)6-、
-(CH2)-(CHCF3)2-(CH2)7-、
-(CH2)-(CHCF3)2-(CH2)8-、
-(CH2)-(CHCF3)2-(CH2)9-、
-(CH2)2-(CHCF3)2-(CH2)-、
-(CH2)3-(CHCF3)2-(CH2)-、
-(CH2)4-(CHCF3)2-(CH2)-、
-(CH2)5-(CHCF3)2-(CH2)-、
-(CH2)6-(CHCF3)2-(CH2)-、
-(CH2)7-(CHCF3)2-(CH2)-、
-(CH2)8-(CHCF3)2-(CH2)-、
-(CH2)9-(CHCF3)2-(CH2)-、
-(CH2)2-(CHCF3)2-(CH2)2-、
-(CH2)3-(CHCF3)2-(CH2)3-、
-(CH2)4-(CHCF3)2-(CH2)4-、
-(CH2)5-(CHCF3)2-(CH2)5-、
-(CH2)2-(CHCF3)2-(CH2)3-、
-(CH2)2-(CHCF3)2-(CH2)4-、
-(CH2)2-(CHCF3)2-(CH2)5-、
-(CH2)2-(CHCF3)2-(CH2)6-、
-(CH2)2-(CHCF3)2-(CH2)7-、
-(CH2)2-(CHCF3)2-(CH2)8-、
-(CH2)3-(CHCF3)2-(CH2)2-、
-(CH2)3-(CHCF3)2-(CH2)4-、
-(CH2)3-(CHCF3)2-(CH2)5-、
-(CH2)3-(CHCF3)2-(CH2)6-、
-(CH2)3-(CHCF3)2-(CH2)7-、
-(CH2)4-(CHCF3)2-(CH2)2-、
-(CH2)4-(CHCF3)2-(CH2)3-、
-(CH2)4-(CHCF3)2-(CH2)5-、
-(CH2)4-(CHCF3)2-(CH2)6-、
-(CH2)5-(CHCF3)2-(CH2)2-、
-(CH2)5-(CHCF3)2-(CH2)3-、
-(CH2)5-(CHCF3)2-(CH2)4-、
-(CH2)6-(CHCF3)2-(CH2)2-、
-(CH2)6-(CHCF3)2-(CH2)3-、
-(CH2)6-(CHCF3)2-(CH2)4-、
-(CH2)-(CHCF3)3-(CH2)-、
-(CH2)-(CHCF3)3-(CH2)2-、
-(CH2)-(CHCF3)3-(CH2)3-、
-(CH2)-(CHCF3)3-(CH2)4-、
-(CH2)-(CHCF3)3-(CH2)5-、
-(CH2)-(CHCF3)3-(CH2)6-、
-(CH2)-(CHCF3)3-(CH2)7-、
-(CH2)-(CHCF3)3-(CH2)8-、
-(CH2)2-(CHCF3)3-(CH2)-、
-(CH2)3-(CHCF3)3-(CH2)-、
-(CH2)4-(CHCF3)3-(CH2)-、
-(CH2)5-(CHCF3)3-(CH2)-、
-(CH2)6-(CHCF3)3-(CH2)-、
-(CH2)7-(CHCF3)3-(CH2)-、
-(CH2)8-(CHCF3)3-(CH2)-、
-(CH2)2-(CHCF3)3-(CH2)2-、
-(CH2)3-(CHCF3)3-(CH2)3-、
-(CH2)4-(CHCF3)3-(CH2)4-、
-(CH2)2-(CHCF3)3-(CH2)3-、
-(CH2)2-(CHCF3)3-(CH2)4-、
-(CH2)2-(CHCF3)3-(CH2)5-、
-(CH2)2-(CHCF3)3-(CH2)6-、
-(CH2)2-(CHCF3)3-(CH2)7-、
-(CH2)3-(CHCF3)3-(CH2)2-、
-(CH2)3-(CHCF3)3-(CH2)4-、
-(CH2)3-(CHCF3)3-(CH2)5-、
-(CH2)3-(CHCF3)3-(CH2)6-、
-(CH2)4-(CHCF3)3-(CH2)2-、
-(CH2)4-(CHCF3)3-(CH2)3-、
-(CH2)4-(CHCF3)3-(CH2)5-、
-(CH2)5-(CHCF3)3-(CH2)2-、
-(CH2)5-(CHCF3)3-(CH2)3-、
-(CH2)5-(CHCF3)3-(CH2)4-、
-(CH2)6-(CHCF3)3-(CH2)2-、
-(CH2)6-(CHCF3)3-(CH2)3-、
-(CH2)-(CHCF3)4-(CH2)-、
-(CH2)-(CHCF3)4-(CH2)2-、
-(CH2)-(CHCF3)4-(CH2)3-、
-(CH2)-(CHCF3)4-(CH2)4-、
-(CH2)-(CHCF3)4-(CH2)5-、
-(CH2)-(CHCF3)4-(CH2)6-、
-(CH2)-(CHCF3)4-(CH2)7-、
-(CH2)-(CHCF3)4-(CH2)8-、
-(CH2)-(CHCF3)4-(CH2)9-、
-(CH2)-(CHCF3)4-(CH2)10-、
-(CH2)2-(CHCF3)4-(CH2)-、
-(CH2)3-(CHCF3)4-(CH2)-、
-(CH2)4-(CHCF3)4-(CH2)-、
-(CH2)5-(CHCF3)4-(CH2)-、
-(CH2)6-(CHCF3)4-(CH2)-、
-(CH2)7-(CHCF3)4-(CH2)-、
-(CH2)2-(CHCF3)4-(CH2)2-、
-(CH2)3-(CHCF3)4-(CH2)3-、
-(CH2)4-(CHCF3)4-(CH2)4-、
-(CH2)5-(CHCF3)4-(CH2)5-、
-(CH2)2-(CHCF3)4-(CH2)3-、
-(CH2)2-(CHCF3)4-(CH2)4-、
-(CH2)2-(CHCF3)4-(CH2)5-、
-(CH2)2-(CHCF3)4-(CH2)6-、
-(CH2)3-(CHCF3)4-(CH2)2-、
-(CH2)3-(CHCF3)4-(CH2)4-、
-(CH2)4-(CHCF3)4-(CH2)2-、
-(CH2)4-(CHCF3)4-(CH2)3-、
-(CH2)5-(CHCF3)4-(CH2)2-、
-(CH2)5-(CHCF3)4-(CH2)3-、
-(CH2)6-(CHCF3)4-(CH2)2-、
-(CH2)-(CHCF3)5-(CH2)-、
-(CH2)-(CHCF3)5-(CH2)2-、
-(CH2)-(CHCF3)5-(CH2)3-、
-(CH2)-(CHCF3)5-(CH2)4-、
-(CH2)-(CHCF3)5-(CH2)5-、
-(CH2)-(CHCF3)5-(CH2)6-、
-(CH2)2-(CHCF3)5-(CH2)-、
-(CH2)3-(CHCF3)5-(CH2)-、
-(CH2)4-(CHCF3)5-(CH2)-、
-(CH2)5-(CHCF3)5-(CH2)-、
-(CH2)6-(CHCF3)5-(CH2)-、
-(CH2)2-(CHCF3)5-(CH2)2-、
-(CH2)3-(CHCF3)5-(CH2)3-、
-(CH2)4-(CHCF3)5-(CH2)4-、
-(CH2)2-(CHCF3)5-(CH2)3-、
-(CH2)2-(CHCF3)5-(CH2)4-、
-(CH2)2-(CHCF3)5-(CH2)5-、
-(CH2)2-(CHCF3)5-(CH2)6-、
-(CH2)3-(CHCF3)5-(CH2)2-、
-(CH2)3-(CHCF3)5-(CH2)4-、
-(CH2)4-(CHCF3)5-(CH2)2-、
-(CH2)4-(CHCF3)5-(CH2)3-、
-(CH2)5-(CHCF3)5-(CH2)2-、
-(CH2)-[C(CH3)CF3]-、
-(CH2)-[C(CH3)CF3]-(CH2)-、
-(CH2)-[C(CH3)CF3]-(CH2)2-、
-(CH2)-[C(CH3)CF3]-(CH2)3-、
-(CH2)-[C(CH3)CF3]-(CH2)4-、
-(CH2)-[C(CH3)CF3]-(CH2)5-、
-(CH2)-[C(CH3)CF3]-(CH2)6-、
-(CH2)-[C(CH3)CF3]-(CH2)7-、
-(CH2)-[C(CH3)CF3]-(CH2)8-、
-(CH2)-[C(CH3)CF3]-(CH2)9-、
-(CH2)-[C(CH3)CF3]-(CH2)10-、
-(CH2)2-[C(CH3)CF3]-(CH2)-、
-(CH2)3-[C(CH3)CF3]-(CH2)-、
-(CH2)4-[C(CH3)CF3]-(CH2)-、
-(CH2)5-[C(CH3)CF3]-(CH2)-、
-(CH2)6-[C(CH3)CF3]-(CH2)-、
-(CH2)7-[C(CH3)CF3]-(CH2)-、
-(CH2)8-[C(CH3)CF3]-(CH2)-、
-(CH2)9-[C(CH3)CF3]-(CH2)-、
-(CH2)10-[C(CH3)CF3]-(CH2)-、
-(CH2)2-[C(CH3)CF3]-(CH2)2-、
-(CH2)3-[C(CH3)CF3]-(CH2)3-、
-(CH2)4-[C(CH3)CF3]-(CH2)4-、
-(CH2)5-[C(CH3)CF3]-(CH2)5-、
-(CH2)2-[C(CH3)CF3]-(CH2)3-、
-(CH2)2-[C(CH3)CF3]-(CH2)4-、
-(CH2)2-[C(CH3)CF3]-(CH2)5-、
-(CH2)2-[C(CH3)CF3]-(CH2)6-、
-(CH2)2-[C(CH3)CF3]-(CH2)7-、
-(CH2)2-[C(CH3)CF3]-(CH2)8-、
-(CH2)2-[C(CH3)CF3]-(CH2)9-、
-(CH2)3-[C(CH3)CF3]-(CH2)2-、
-(CH2)3-[C(CH3)CF3]-(CH2)4-、
-(CH2)3-[C(CH3)CF3]-(CH2)5-、
-(CH2)3-[C(CH3)CF3]-(CH2)6-、
-(CH2)3-[C(CH3)CF3]-(CH2)7-、
-(CH2)3-[C(CH3)CF3]-(CH2)8-、
-(CH2)4-[C(CH3)CF3]-(CH2)2-、
-(CH2)4-[C(CH3)CF3]-(CH2)3-、
-(CH2)4-[C(CH3)CF3]-(CH2)5-、
-(CH2)4-[C(CH3)CF3]-(CH2)6-、
-(CH2)4-[C(CH3)CF3]-(CH2)7-、
-(CH2)5-[C(CH3)CF3]-(CH2)2-、
-(CH2)5-[C(CH3)CF3]-(CH2)3-、
-(CH2)5-[C(CH3)CF3]-(CH2)4-、
-(CH2)5-[C(CH3)CF3]-(CH2)6-、
-(CH2)6-[C(CH3)CF3]-(CH2)2-、
-(CH2)6-[C(CH3)CF3]-(CH2)3-、
-(CH2)6-[C(CH3)CF3]-(CH2)4-、
-(CH2)6-[C(CH3)CF3]-(CH2)5-、
-(CH2)-[C(CH3)CF3]2-、
-(CH2)-[C(CH3)CF3]2-(CH2)-、
-(CH2)-[C(CH3)CF3]2-(CH2)2-、
-(CH2)-[C(CH3)CF3]2-(CH2)3-、
-(CH2)-[C(CH3)CF3]2-(CH2)4-、
-(CH2)-[C(CH3)CF3]2-(CH2)5-、
-(CH2)-[C(CH3)CF3]2-(CH2)6-、
-(CH2)-[C(CH3)CF3]2-(CH2)7-、
-(CH2)-[C(CH3)CF3]2-(CH2)8-、
-(CH2)-[C(CH3)CF3]2-(CH2)9-、
-(CH2)2-[C(CH3)CF3]2-(CH2)-、
-(CH2)3-[C(CH3)CF3]2-(CH2)-、
-(CH2)4-[C(CH3)CF3]2-(CH2)-、
-(CH2)5-[C(CH3)CF3]2-(CH2)-、
-(CH2)6-[C(CH3)CF3]2-(CH2)-、
-(CH2)7-[C(CH3)CF3]2-(CH2)-、
-(CH2)8-[C(CH3)CF3]2-(CH2)-、
-(CH2)9-[C(CH3)CF3]2-(CH2)-、
-(CH2)2-[C(CH3)CF3]2-(CH2)2-、
-(CH2)3-[C(CH3)CF3]2-(CH2)3-、
-(CH2)4-[C(CH3)CF3]2-(CH2)4-、
-(CH2)5-[C(CH3)CF3]2-(CH2)5-、
-(CH2)2-[C(CH3)CF3]2-(CH2)3-、
-(CH2)2-[C(CH3)CF3]2-(CH2)4-、
-(CH2)2-[C(CH3)CF3]2-(CH2)5-、
-(CH2)2-[C(CH3)CF3]2-(CH2)6-、
-(CH2)2-[C(CH3)CF3]2-(CH2)7-、
-(CH2)2-[C(CH3)CF3]2-(CH2)8-、
-(CH2)3-[C(CH3)CF3]2-(CH2)2-、
-(CH2)3-[C(CH3)CF3]2-(CH2)4-、
-(CH2)3-[C(CH3)CF3]2-(CH2)5-、
-(CH2)3-[C(CH3)CF3]2-(CH2)6-、
-(CH2)3-[C(CH3)CF3]2-(CH2)7-、
-(CH2)4-[C(CH3)CF3]2-(CH2)2-、
-(CH2)4-[C(CH3)CF3]2-(CH2)3-、
-(CH2)4-[C(CH3)CF3]2-(CH2)5-、
-(CH2)4-[C(CH3)CF3]2-(CH2)6-、
-(CH2)5-[C(CH3)CF3]2-(CH2)2-、
-(CH2)5-[C(CH3)CF3]2-(CH2)3-、
-(CH2)5-[C(CH3)CF3]2-(CH2)4-、
-(CH2)6-[C(CH3)CF3]2-(CH2)2-、
-(CH2)6-[C(CH3)CF3]2-(CH2)3-、
-(CH2)6-[C(CH3)CF3]2-(CH2)4-、
-(CH2)-[C(CH3)CF3]3-、
-(CH2)-[C(CH3)CF3]3-(CH2)-、
-(CH2)-[C(CH3)CF3]3-(CH2)2-、
-(CH2)-[C(CH3)CF3]3-(CH2)3-、
-(CH2)-[C(CH3)CF3]3-(CH2)4-、
-(CH2)-[C(CH3)CF3]3-(CH2)5-、
-(CH2)-[C(CH3)CF3]3-(CH2)6-、
-(CH2)-[C(CH3)CF3]3-(CH2)7-、
-(CH2)-[C(CH3)CF3]3-(CH2)8-、
-(CH2)2-[C(CH3)CF3]3-(CH2)-、
-(CH2)3-[C(CH3)CF3]3-(CH2)-、
-(CH2)4-[C(CH3)CF3]3-(CH2)-、
-(CH2)5-[C(CH3)CF3]3-(CH2)-、
-(CH2)6-[C(CH3)CF3]3-(CH2)-、
-(CH2)7-[C(CH3)CF3]3-(CH2)-、
-(CH2)8-[C(CH3)CF3]3-(CH2)-、
-(CH2)2-[C(CH3)CF3]3-(CH2)2-、
-(CH2)3-[C(CH3)CF3]3-(CH2)3-、
-(CH2)4-[C(CH3)CF3]3-(CH2)4-、
-(CH2)2-[C(CH3)CF3]3-(CH2)3-、
-(CH2)2-[C(CH3)CF3]3-(CH2)4-、
-(CH2)2-[C(CH3)CF3]3-(CH2)5-、
-(CH2)2-[C(CH3)CF3]3-(CH2)6-、
-(CH2)2-[C(CH3)CF3]3-(CH2)7-、
-(CH2)3-[C(CH3)CF3]3-(CH2)2-、
-(CH2)3-[C(CH3)CF3]3-(CH2)4-、
-(CH2)3-[C(CH3)CF3]3-(CH2)5-、
-(CH2)3-[C(CH3)CF3]3-(CH2)6-、
-(CH2)4-[C(CH3)CF3]3-(CH2)2-、
-(CH2)4-[C(CH3)CF3]3-(CH2)3-、
-(CH2)4-[C(CH3)CF3]3-(CH2)5-、
-(CH2)5-[C(CH3)CF3]3-(CH2)2-、
-(CH2)5-[C(CH3)CF3]3-(CH2)3-、
-(CH2)5-[C(CH3)CF3]3-(CH2)4-、
-(CH2)6-[C(CH3)CF3]3-(CH2)2-、
-(CH2)6-[C(CH3)CF3]3-(CH2)3-、
-(CH2)-[C(CH3)CF3]4-、
-(CH2)-[C(CH3)CF3]4-(CH2)-、
-(CH2)-[C(CH3)CF3]4-(CH2)2-、
-(CH2)-[C(CH3)CF3]4-(CH2)3-、
-(CH2)-[C(CH3)CF3]4-(CH2)4-、
-(CH2)-[C(CH3)CF3]4-(CH2)5-、
-(CH2)-[C(CH3)CF3]4-(CH2)6-、
-(CH2)-[C(CH3)CF3]4-(CH2)7-、
-(CH2)-[C(CH3)CF3]4-(CH2)8-、
-(CH2)-[C(CH3)CF3]4-(CH2)9-、
-(CH2)-[C(CH3)CF3]4-(CH2)10-、
-(CH2)2-[C(CH3)CF3]4-(CH2)-、
-(CH2)3-[C(CH3)CF3]4-(CH2)-、
-(CH2)4-[C(CH3)CF3]4-(CH2)-、
-(CH2)5-[C(CH3)CF3]4-(CH2)-、
-(CH2)6-[C(CH3)CF3]4-(CH2)-、
-(CH2)7-[C(CH3)CF3]4-(CH2)-、
-(CH2)2-[C(CH3)CF3]4-(CH2)2-、
-(CH2)3-[C(CH3)CF3]4-(CH2)3-、
-(CH2)4-[C(CH3)CF3]4-(CH2)4-、
-(CH2)5-[C(CH3)CF3]4-(CH2)5-、
-(CH2)2-[C(CH3)CF3]4-(CH2)3-、
-(CH2)2-[C(CH3)CF3]4-(CH2)4-、
-(CH2)2-[C(CH3)CF3]4-(CH2)5-、
-(CH2)2-[C(CH3)CF3]4-(CH2)6-、
-(CH2)3-[C(CH3)CF3]4-(CH2)2-、
-(CH2)3-[C(CH3)CF3]4-(CH2)4-、
-(CH2)4-[C(CH3)CF3]4-(CH2)2-、
-(CH2)4-[C(CH3)CF3]4-(CH2)3-、
-(CH2)5-[C(CH3)CF3]4-(CH2)2-、
-(CH2)5-[C(CH3)CF3]4-(CH2)3-、
-(CH2)6-[C(CH3)CF3]4-(CH2)2-、
-(CH2)-[C(CH3)CF3]5-、
-(CH2)-[C(CH3)CF3]5-(CH2)-、
-(CH2)-[C(CH3)CF3]5-(CH2)2-、
-(CH2)-[C(CH3)CF3]5-(CH2)3-、
-(CH2)-[C(CH3)CF3]5-(CH2)4-、
-(CH2)-[C(CH3)CF3]5-(CH2)5-、
-(CH2)-[C(CH3)CF3]5-(CH2)6-、
-(CH2)2-[C(CH3)CF3]5-(CH2)-、
-(CH2)3-[C(CH3)CF3]5-(CH2)-、
-(CH2)4-[C(CH3)CF3]5-(CH2)-、
-(CH2)5-[C(CH3)CF3]5-(CH2)-、
-(CH2)6-[C(CH3)CF3]5-(CH2)-、
-(CH2)2-[C(CH3)CF3]5-(CH2)2-、
-(CH2)3-[C(CH3)CF3]5-(CH2)3-、
-(CH2)4-[C(CH3)CF3]5-(CH2)4-、
-(CH2)2-[C(CH3)CF3]5-(CH2)3-、
-(CH2)2-[C(CH3)CF3]5-(CH2)4-、
-(CH2)2-[C(CH3)CF3]5-(CH2)5-、
-(CH2)2-[C(CH3)CF3]5-(CH2)6-、
-(CH2)3-[C(CH3)CF3]5-(CH2)2-、
-(CH2)3-[C(CH3)CF3]5-(CH2)4-、
-(CH2)4-[C(CH3)CF3]5-(CH2)2-、
-(CH2)4-[C(CH3)CF3]5-(CH2)3-、
-(CH2)5-[C(CH3)CF3]5-(CH2)2-、
-(CH2)-[CH(CH2CF3)]-、
-(CH2)-[CH(CH2CF3)]-(CH2)-、
-(CH2)-[CH(CH2CF3)]-(CH2)2-、
-(CH2)-[CH(CH2CF3)]-(CH2)3-、
-(CH2)-[CH(CH2CF3)]-(CH2)4-、
-(CH2)-[CH(CH2CF3)]-(CH2)5-、
-(CH2)-[CH(CH2CF3)]-(CH2)6-、
-(CH2)-[CH(CH2CF3)]-(CH2)7-、
-(CH2)-[CH(CH2CF3)]-(CH2)8-、
-(CH2)-[CH(CH2CF3)]-(CH2)9-、
-(CH2)-[CH(CH2CF3)]-(CH2)10-、
-(CH2)2-[CH(CH2CF3)]-(CH2)-、
-(CH2)3-[CH(CH2CF3)]-(CH2)-、
-(CH2)4-[CH(CH2CF3)]-(CH2)-、
-(CH2)5-[CH(CH2CF3)]-(CH2)-、
-(CH2)6-[CH(CH2CF3)]-(CH2)-、
-(CH2)7-[CH(CH2CF3)]-(CH2)-、
-(CH2)8-[CH(CH2CF3)]-(CH2)-、
-(CH2)9-[CH(CH2CF3)]-(CH2)-、
-(CH2)10-[CH(CH2CF3)]-(CH2)-、
-(CH2)2-[CH(CH2CF3)]-(CH2)2-、
-(CH2)3-[CH(CH2CF3)]-(CH2)3-、
-(CH2)4-[CH(CH2CF3)]-(CH2)4-、
-(CH2)5-[CH(CH2CF3)]-(CH2)5-、
-(CH2)2-[CH(CH2CF3)]-(CH2)3-、
-(CH2)2-[CH(CH2CF3)]-(CH2)4-、
-(CH2)2-[CH(CH2CF3)]-(CH2)5-、
-(CH2)2-[CH(CH2CF3)]-(CH2)6-、
-(CH2)2-[CH(CH2CF3)]-(CH2)7-、
-(CH2)2-[CH(CH2CF3)]-(CH2)8-、
-(CH2)2-[CH(CH2CF3)]-(CH2)9-、
-(CH2)3-[CH(CH2CF3)]-(CH2)2-、
-(CH2)3-[CH(CH2CF3)]-(CH2)4-、
-(CH2)3-[CH(CH2CF3)]-(CH2)5-、
-(CH2)3-[CH(CH2CF3)]-(CH2)6-、
-(CH2)3-[CH(CH2CF3)]-(CH2)7-、
-(CH2)3-[CH(CH2CF3)]-(CH2)8-、
-(CH2)4-[CH(CH2CF3)]-(CH2)2-、
-(CH2)4-[CH(CH2CF3)]-(CH2)3-、
-(CH2)4-[CH(CH2CF3)]-(CH2)5-、
-(CH2)4-[CH(CH2CF3)]-(CH2)6-、
-(CH2)4-[CH(CH2CF3)]-(CH2)7-、
-(CH2)5-[CH(CH2CF3)]-(CH2)2-、
-(CH2)5-[CH(CH2CF3)]-(CH2)3-、
-(CH2)5-[CH(CH2CF3)]-(CH2)4-、
-(CH2)5-[CH(CH2CF3)]-(CH2)6-、
-(CH2)6-[CH(CH2CF3)]-(CH2)2-、
-(CH2)6-[CH(CH2CF3)]-(CH2)3-、
-(CH2)6-[CH(CH2CF3)]-(CH2)4-、
-(CH2)6-[CH(CH2CF3)]-(CH2)5-、
-(CH2)-[CH(CH2CF3)]2-、
-(CH2)-[CH(CH2CF3)]2-(CH2)-、
-(CH2)-[CH(CH2CF3)]2-(CH2)2-、
-(CH2)-[CH(CH2CF3)]2-(CH2)3-、
-(CH2)-[CH(CH2CF3)]2-(CH2)4-、
-(CH2)-[CH(CH2CF3)]2-(CH2)5-、
-(CH2)-[CH(CH2CF3)]2-(CH2)6-、
-(CH2)-[CH(CH2CF3)]2-(CH2)7-、
-(CH2)-[CH(CH2CF3)]2-(CH2)8-、
-(CH2)-[CH(CH2CF3)]2-(CH2)9-、
-(CH2)2-[CH(CH2CF3)]2-(CH2)-、
-(CH2)3-[CH(CH2CF3)]2-(CH2)-、
-(CH2)4-[CH(CH2CF3)]2-(CH2)-、
-(CH2)5-[CH(CH2CF3)]2-(CH2)-、
-(CH2)6-[CH(CH2CF3)]2-(CH2)-、
-(CH2)7-[CH(CH2CF3)]2-(CH2)-、
-(CH2)8-[CH(CH2CF3)]2-(CH2)-、
-(CH2)9-[CH(CH2CF3)]2-(CH2)-、
-(CH2)2-[CH(CH2CF3)]2-(CH2)2-、
-(CH2)3-[CH(CH2CF3)]2-(CH2)3-、
-(CH2)4-[CH(CH2CF3)]2-(CH2)4-、
-(CH2)5-[CH(CH2CF3)]2-(CH2)5-、
-(CH2)2-[CH(CH2CF3)]2-(CH2)3-、
-(CH2)2-[CH(CH2CF3)]2-(CH2)4-、
-(CH2)2-[CH(CH2CF3)]2-(CH2)5-、
-(CH2)2-[CH(CH2CF3)]2-(CH2)6-、
-(CH2)2-[CH(CH2CF3)]2-(CH2)7-、
-(CH2)2-[CH(CH2CF3)]2-(CH2)8-、
-(CH2)3-[CH(CH2CF3)]2-(CH2)2-、
-(CH2)3-[CH(CH2CF3)]2-(CH2)4-、
-(CH2)3-[CH(CH2CF3)]2-(CH2)5-、
-(CH2)3-[CH(CH2CF3)]2-(CH2)6-、
-(CH2)3-[CH(CH2CF3)]2-(CH2)7-、
-(CH2)4-[CH(CH2CF3)]2-(CH2)2-、
-(CH2)4-[CH(CH2CF3)]2-(CH2)3-、
-(CH2)4-[CH(CH2CF3)]2-(CH2)5-、
-(CH2)4-[CH(CH2CF3)]2-(CH2)6-、
-(CH2)5-[CH(CH2CF3)]2-(CH2)2-、
-(CH2)5-[CH(CH2CF3)]2-(CH2)3-、
-(CH2)5-[CH(CH2CF3)]2-(CH2)4-、
-(CH2)6-[CH(CH2CF3)]2-(CH2)2-、
-(CH2)6-[CH(CH2CF3)]2-(CH2)3-、
-(CH2)6-[CH(CH2CF3)]2-(CH2)4-、
-(CH2)-[CH(CH2CF3)]3-、
-(CH2)-[CH(CH2CF3)]3-(CH2)-、
-(CH2)-[CH(CH2CF3)]3-(CH2)2-、
-(CH2)-[CH(CH2CF3)]3-(CH2)3-、
-(CH2)-[CH(CH2CF3)]3-(CH2)4-、
-(CH2)-[CH(CH2CF3)]3-(CH2)5-、
-(CH2)-[CH(CH2CF3)]3-(CH2)6-、
-(CH2)-[CH(CH2CF3)]3-(CH2)7-、
-(CH2)-[CH(CH2CF3)]3-(CH2)8-、
-(CH2)2-[CH(CH2CF3)]3-(CH2)-、
-(CH2)3-[CH(CH2CF3)]3-(CH2)-、
-(CH2)4-[CH(CH2CF3)]3-(CH2)-、
-(CH2)5-[CH(CH2CF3)]3-(CH2)-、
-(CH2)6-[CH(CH2CF3)]3-(CH2)-、
-(CH2)7-[CH(CH2CF3)]3-(CH2)-、
-(CH2)8-[CH(CH2CF3)]3-(CH2)-、
-(CH2)2-[CH(CH2CF3)]3-(CH2)2-、
-(CH2)3-[CH(CH2CF3)]3-(CH2)3-、
-(CH2)4-[CH(CH2CF3)]3-(CH2)4-、
-(CH2)2-[CH(CH2CF3)]3-(CH2)3-、
-(CH2)2-[CH(CH2CF3)]3-(CH2)4-、
-(CH2)2-[CH(CH2CF3)]3-(CH2)5-、
-(CH2)2-[CH(CH2CF3)]3-(CH2)6-、
-(CH2)2-[CH(CH2CF3)]3-(CH2)7-、
-(CH2)3-[CH(CH2CF3)]3-(CH2)2-、
-(CH2)3-[CH(CH2CF3)]3-(CH2)4-、
-(CH2)3-[CH(CH2CF3)]3-(CH2)5-、
-(CH2)3-[CH(CH2CF3)]3-(CH2)6-、
-(CH2)4-[CH(CH2CF3)]3-(CH2)2-、
-(CH2)4-[CH(CH2CF3)]3-(CH2)3-、
-(CH2)4-[CH(CH2CF3)]3-(CH2)5-、
-(CH2)5-[CH(CH2CF3)]3-(CH2)2-、
-(CH2)5-[CH(CH2CF3)]3-(CH2)3-、
-(CH2)5-[CH(CH2CF3)]3-(CH2)4-、
-(CH2)6-[CH(CH2CF3)]3-(CH2)2-、
-(CH2)6-[CH(CH2CF3)]3-(CH2)3-、
-(CH2)-[CH(CH2CF3)]4-、
-(CH2)-[CH(CH2CF3)]4-(CH2)-、
-(CH2)-[CH(CH2CF3)]4-(CH2)2-、
-(CH2)-[CH(CH2CF3)]4-(CH2)3-、
-(CH2)-[CH(CH2CF3)]4-(CH2)4-、
-(CH2)-[CH(CH2CF3)]4-(CH2)5-、
-(CH2)-[CH(CH2CF3)]4-(CH2)6-、
-(CH2)-[CH(CH2CF3)]4-(CH2)7-、
-(CH2)-[CH(CH2CF3)]4-(CH2)8-、
-(CH2)-[CH(CH2CF3)]4-(CH2)9-、
-(CH2)-[CH(CH2CF3)]4-(CH2)10-、
-(CH2)2-[CH(CH2CF3)]4-(CH2)-、
-(CH2)3-[CH(CH2CF3)]4-(CH2)-、
-(CH2)4-[CH(CH2CF3)]4-(CH2)-、
-(CH2)5-[CH(CH2CF3)]4-(CH2)-、
-(CH2)6-[CH(CH2CF3)]4-(CH2)-、
-(CH2)7-[CH(CH2CF3)]4-(CH2)-、
-(CH2)2-[CH(CH2CF3)]4-(CH2)2-、
-(CH2)3-[CH(CH2CF3)]4-(CH2)3-、
-(CH2)4-[CH(CH2CF3)]4-(CH2)4-、
-(CH2)5-[CH(CH2CF3)]4-(CH2)5-、
-(CH2)2-[CH(CH2CF3)]4-(CH2)3-、
-(CH2)2-[CH(CH2CF3)]4-(CH2)4-、
-(CH2)2-[CH(CH2CF3)]4-(CH2)5-、
-(CH2)2-[CH(CH2CF3)]4-(CH2)6-、
-(CH2)3-[CH(CH2CF3)]4-(CH2)2-、
-(CH2)3-[CH(CH2CF3)]4-(CH2)4-、
-(CH2)4-[CH(CH2CF3)]4-(CH2)2-、
-(CH2)4-[CH(CH2CF3)]4-(CH2)3-、
-(CH2)5-[CH(CH2CF3)]4-(CH2)2-、
-(CH2)5-[CH(CH2CF3)]4-(CH2)3-、
-(CH2)6-[CH(CH2CF3)]4-(CH2)2-、
-(CH2)-[CH(CH2CF3)5-、
-(CH2)-[CH(CH2CF3)]5-(CH2)-、
-(CH2)-[CH(CH2CF3)]5-(CH2)2-、
-(CH2)-[CH(CH2CF3)]5-(CH2)3-、
-(CH2)-[CH(CH2CF3)]5-(CH2)4-、
-(CH2)-[CH(CH2CF3)]5-(CH2)5-、
-(CH2)-[CH(CH2CF3)]5-(CH2)6-、
-(CH2)2-[CH(CH2CF3)]5-(CH2)-、
-(CH2)3-[CH(CH2CF3)]5-(CH2)-、
-(CH2)4-[CH(CH2CF3)]5-(CH2)-、
-(CH2)5-[CH(CH2CF3)]5-(CH2)-、
-(CH2)6-[CH(CH2CF3)]5-(CH2)-、
-(CH2)2-[CH(CH2CF3)]5-(CH2)2-、
-(CH2)3-[CH(CH2CF3)]5-(CH2)3-、
-(CH2)4-[CH(CH2CF3)]5-(CH2)4-、
-(CH2)2-[CH(CH2CF3)]5-(CH2)3-、
-(CH2)2-[CH(CH2CF3)]5-(CH2)4-、
-(CH2)2-[CH(CH2CF3)]5-(CH2)5-、
-(CH2)2-[CH(CH2CF3)]5-(CH2)6-、
-(CH2)3-[CH(CH2CF3)]5-(CH2)2-、
-(CH2)3-[CH(CH2CF3)]5-(CH2)4-、
-(CH2)4-[CH(CH2CF3)]5-(CH2)2-、
-(CH2)4-[CH(CH2CF3)]5-(CH2)3-、
-(CH2)5-[CH(CH2CF3)]5-(CH2)2-、
-(CH2)-[C(CH3)(CH2CF3)]-、
-(CH2)-[C(CH3)(CH2CF3)]-(CH2)-、
-(CH2)-[C(CH3)(CH2CF3)]-(CH2)2-、
-(CH2)-[C(CH3)(CH2CF3)]-(CH2)3-、
-(CH2)-[C(CH3)(CH2CF3)]-(CH2)4-、
-(CH2)-[C(CH3)(CH2CF3)]-(CH2)5-、
-(CH2)-[C(CH3)(CH2CF3)]-(CH2)6-、
-(CH2)-[C(CH3)(CH2CF3)]-(CH2)7-、
-(CH2)-[C(CH3)(CH2CF3)]-(CH2)8-、
-(CH2)-[C(CH3)(CH2CF3)]-(CH2)9-、
-(CH2)-[C(CH3)(CH2CF3)]-(CH2)10-、
-(CH2)2-[C(CH3)(CH2CF3)]-(CH2)-、
-(CH2)3-[C(CH3)(CH2CF3)]-(CH2)-、
-(CH2)4-[C(CH3)(CH2CF3)]-(CH2)-、
-(CH2)5-[C(CH3)(CH2CF3)]-(CH2)-、
-(CH2)6-[C(CH3)(CH2CF3)]-(CH2)-、
-(CH2)7-[C(CH3)(CH2CF3)]-(CH2)-、
-(CH2)8-[C(CH3)(CH2CF3)]-(CH2)-、
-(CH2)9-[C(CH3)(CH2CF3)]-(CH2)-、
-(CH2)10-[C(CH3)(CH2CF3)]-(CH2)-、
-(CH2)2-[C(CH3)(CH2CF3)]-(CH2)2-、
-(CH2)3-[C(CH3)(CH2CF3)]-(CH2)3-、
-(CH2)4-[C(CH3)(CH2CF3)]-(CH2)4-、
-(CH2)5-[C(CH3)(CH2CF3)]-(CH2)5-、
-(CH2)2-[C(CH3)(CH2CF3)]-(CH2)3-、
-(CH2)2-[C(CH3)(CH2CF3)]-(CH2)4-、
-(CH2)2-[C(CH3)(CH2CF3)]-(CH2)5-、
-(CH2)2-[C(CH3)(CH2CF3)]-(CH2)6-、
-(CH2)2-[C(CH3)(CH2CF3)]-(CH2)7-、
-(CH2)2-[C(CH3)(CH2CF3)]-(CH2)8-、
-(CH2)2-[C(CH3)(CH2CF3)]-(CH2)9-、
-(CH2)3-[C(CH3)(CH2CF3)]-(CH2)2-、
-(CH2)3-[C(CH3)(CH2CF3)]-(CH2)4-、
-(CH2)3-[C(CH3)(CH2CF3)]-(CH2)5-、
-(CH2)3-[C(CH3)(CH2CF3)]-(CH2)6-、
-(CH2)3-[C(CH3)(CH2CF3)]-(CH2)7-、
-(CH2)3-[C(CH3)(CH2CF3)]-(CH2)8-、
-(CH2)4-[C(CH3)(CH2CF3)]-(CH2)2-、
-(CH2)4-[C(CH3)(CH2CF3)]-(CH2)3-、
-(CH2)4-[C(CH3)(CH2CF3)]-(CH2)5-、
-(CH2)4-[C(CH3)(CH2CF3)]-(CH2)6-、
-(CH2)4-[C(CH3)(CH2CF3)]-(CH2)7-、
-(CH2)5-[C(CH3)(CH2CF3)]-(CH2)2-、
-(CH2)5-[C(CH3)(CH2CF3)]-(CH2)3-、
-(CH2)5-[C(CH3)(CH2CF3)]-(CH2)4-、
-(CH2)5-[C(CH3)(CH2CF3)]-(CH2)6-、
-(CH2)6-[C(CH3)(CH2CF3)]-(CH2)2-、
-(CH2)6-[C(CH3)(CH2CF3)]-(CH2)3-、
-(CH2)6-[C(CH3)(CH2CF3)]-(CH2)4-、
-(CH2)6-[C(CH3)(CH2CF3)]-(CH2)5-、
-(CH2)-[C(CH3)(CH2CF3)]2-、
-(CH2)-[C(CH3)(CH2CF3)]2-(CH2)-、
-(CH2)-[C(CH3)(CH2CF3)]2-(CH2)2-、
-(CH2)-[C(CH3)(CH2CF3)]2-(CH2)3-、
-(CH2)-[C(CH3)(CH2CF3)]2-(CH2)4-、
-(CH2)-[C(CH3)(CH2CF3)]2-(CH2)5-、
-(CH2)-[C(CH3)(CH2CF3)]2-(CH2)6-、
-(CH2)-[C(CH3)(CH2CF3)]2-(CH2)7-、
-(CH2)-[C(CH3)(CH2CF3)]2-(CH2)8-、
-(CH2)-[C(CH3)(CH2CF3)]2-(CH2)9-、
-(CH2)2-[C(CH3)(CH2CF3)]2-(CH2)-、
-(CH2)3-[C(CH3)(CH2CF3)]2-(CH2)-、
-(CH2)4-[C(CH3)(CH2CF3)]2-(CH2)-、
-(CH2)5-[C(CH3)(CH2CF3)]2-(CH2)-、
-(CH2)6-[C(CH3)(CH2CF3)]2-(CH2)-、
-(CH2)7-[C(CH3)(CH2CF3)]2-(CH2)-、
-(CH2)8-[C(CH3)(CH2CF3)]2-(CH2)-、
-(CH2)9-[C(CH3)(CH2CF3)]2-(CH2)-、
-(CH2)2-[C(CH3)(CH2CF3)]2-(CH2)2-、
-(CH2)3-[C(CH3)(CH2CF3)]2-(CH2)3-、
-(CH2)4-[C(CH3)(CH2CF3)]2-(CH2)4-、
-(CH2)5-[C(CH3)(CH2CF3)]2-(CH2)5-、
-(CH2)2-[C(CH3)(CH2CF3)]2-(CH2)3-、
-(CH2)2-[C(CH3)(CH2CF3)]2-(CH2)4-、
-(CH2)2-[C(CH3)(CH2CF3)]2-(CH2)5-、
-(CH2)2-[C(CH3)(CH2CF3)]2-(CH2)6-、
-(CH2)2-[C(CH3)(CH2CF3)]2-(CH2)7-、
-(CH2)2-[C(CH3)(CH2CF3)]2-(CH2)8-、
-(CH2)3-[C(CH3)(CH2CF3)]2-(CH2)2-、
-(CH2)3-[C(CH3)(CH2CF3)]2-(CH2)4-、
-(CH2)3-[C(CH3)(CH2CF3)]2-(CH2)5-、
-(CH2)3-[C(CH3)(CH2CF3)]2-(CH2)6-、
-(CH2)3-[C(CH3)(CH2CF3)]2-(CH2)7-、
-(CH2)4-[C(CH3)(CH2CF3)]2-(CH2)2-、
-(CH2)4-[C(CH3)(CH2CF3)]2-(CH2)3-、
-(CH2)4-[C(CH3)(CH2CF3)]2-(CH2)5-、
-(CH2)4-[C(CH3)(CH2CF3)]2-(CH2)6-、
-(CH2)5-[C(CH3)(CH2CF3)]2-(CH2)2-、
-(CH2)5-[C(CH3)(CH2CF3)]2-(CH2)3-、
-(CH2)5-[C(CH3)(CH2CF3)]2-(CH2)4-、
-(CH2)6-[C(CH3)(CH2CF3)]2-(CH2)2-、
-(CH2)6-[C(CH3)(CH2CF3)]2-(CH2)3-、
-(CH2)6-[C(CH3)(CH2CF3)]2-(CH2)4-、
-(CH2)-[C(CH3)(CH2CF3)]3-、
-(CH2)-[C(CH3)(CH2CF3)]3-(CH2)-、
-(CH2)-[C(CH3)(CH2CF3)]3-(CH2)2-、
-(CH2)-[C(CH3)(CH2CF3)]3-(CH2)3-、
-(CH2)-[C(CH3)(CH2CF3)]3-(CH2)4-、
-(CH2)-[C(CH3)(CH2CF3)]3-(CH2)5-、
-(CH2)-[C(CH3)(CH2CF3)]3-(CH2)6-、
-(CH2)-[C(CH3)(CH2CF3)]3-(CH2)7-、
-(CH2)-[C(CH3)(CH2CF3)]3-(CH2)8-、
-(CH2)2-[C(CH3)(CH2CF3)]3-(CH2)-、
-(CH2)3-[C(CH3)(CH2CF3)]3-(CH2)-、
-(CH2)4-[C(CH3)(CH2CF3)]3-(CH2)-、
-(CH2)5-[C(CH3)(CH2CF3)]3-(CH2)-、
-(CH2)6-[C(CH3)(CH2CF3)]3-(CH2)-、
-(CH2)7-[C(CH3)(CH2CF3)]3-(CH2)-、
-(CH2)8-[C(CH3)(CH2CF3)]3-(CH2)-、
-(CH2)2-[C(CH3)(CH2CF3)]3-(CH2)2-、
-(CH2)3-[C(CH3)(CH2CF3)]3-(CH2)3-、
-(CH2)4-[C(CH3)(CH2CF3)]3-(CH2)4-、
-(CH2)2-[C(CH3)(CH2CF3)]3-(CH2)3-、
-(CH2)2-[C(CH3)(CH2CF3)]3-(CH2)4-、
-(CH2)2-[C(CH3)(CH2CF3)]3-(CH2)5-、
-(CH2)2-[C(CH3)(CH2CF3)]3-(CH2)6-、
-(CH2)2-[C(CH3)(CH2CF3)]3-(CH2)7-、
-(CH2)3-[C(CH3)(CH2CF3)]3-(CH2)2-、
-(CH2)3-[C(CH3)(CH2CF3)]3-(CH2)4-、
-(CH2)3-[C(CH3)(CH2CF3)]3-(CH2)5-、
-(CH2)3-[C(CH3)(CH2CF3)]3-(CH2)6-、
-(CH2)4-[C(CH3)(CH2CF3)]3-(CH2)2-、
-(CH2)4-[C(CH3)(CH2CF3)]3-(CH2)3-、
-(CH2)4-[C(CH3)(CH2CF3)]3-(CH2)5-、
-(CH2)5-[C(CH3)(CH2CF3)]3-(CH2)2-、
-(CH2)5-[C(CH3)(CH2CF3)]3-(CH2)3-、
-(CH2)5-[C(CH3)(CH2CF3)]3-(CH2)4-、
-(CH2)6-[C(CH3)(CH2CF3)]3-(CH2)2-、
-(CH2)6-[C(CH3)(CH2CF3)]3-(CH2)3-、
-(CH2)-[C(CH3)(CH2CF3)]4-、
-(CH2)-[C(CH3)(CH2CF3)]4-(CH2)-、
-(CH2)-[C(CH3)(CH2CF3)]4-(CH2)2-、
-(CH2)-[C(CH3)(CH2CF3)]4-(CH2)3-、
-(CH2)-[C(CH3)(CH2CF3)]4-(CH2)4-、
-(CH2)-[C(CH3)(CH2CF3)]4-(CH2)5-、
-(CH2)-[C(CH3)(CH2CF3)]4-(CH2)6-、
-(CH2)-[C(CH3)(CH2CF3)]4-(CH2)7-、
-(CH2)-[C(CH3)(CH2CF3)]4-(CH2)8-、
-(CH2)-[C(CH3)(CH2CF3)]4-(CH2)9-、
-(CH2)-[C(CH3)(CH2CF3)]4-(CH2)10-、
-(CH2)2-[C(CH3)(CH2CF3)]4-(CH2)-、
-(CH2)3-[C(CH3)(CH2CF3)]4-(CH2)-、
-(CH2)4-[C(CH3)(CH2CF3)]4-(CH2)-、
-(CH2)5-[C(CH3)(CH2CF3)]4-(CH2)-、
-(CH2)6-[C(CH3)(CH2CF3)]4-(CH2)-、
-(CH2)7-[C(CH3)(CH2CF3)]4-(CH2)-、
-(CH2)2-[C(CH3)(CH2CF3)]4-(CH2)2-、
-(CH2)3-[C(CH3)(CH2CF3)]4-(CH2)3-、
-(CH2)4-[C(CH3)(CH2CF3)]4-(CH2)4-、
-(CH2)5-[C(CH3)(CH2CF3)]4-(CH2)5-、
-(CH2)2-[C(CH3)(CH2CF3)]4-(CH2)3-、
-(CH2)2-[C(CH3)(CH2CF3)]4-(CH2)4-、
-(CH2)2-[C(CH3)(CH2CF3)]4-(CH2)5-、
-(CH2)2-[C(CH3)(CH2CF3)]4-(CH2)6-、
-(CH2)3-[C(CH3)(CH2CF3)]4-(CH2)2-、
-(CH2)3-[C(CH3)(CH2CF3)]4-(CH2)4-、
-(CH2)4-[C(CH3)(CH2CF3)]4-(CH2)2-、
-(CH2)4-[C(CH3)(CH2CF3)]4-(CH2)3-、
-(CH2)5-[C(CH3)(CH2CF3)]4-(CH2)2-、
-(CH2)5-[C(CH3)(CH2CF3)]4-(CH2)3-、
-(CH2)6-[C(CH3)(CH2CF3)]4-(CH2)2-、
-(CH2)-[C(CH3)(CH2CF3)]5-、
-(CH2)-[C(CH3)(CH2CF3)]5-(CH2)-、
-(CH2)-[C(CH3)(CH2CF3)]5-(CH2)2-、
-(CH2)-[C(CH3)(CH2CF3)]5-(CH2)3-、
-(CH2)-[C(CH3)(CH2CF3)]5-(CH2)4-、
-(CH2)-[C(CH3)(CH2CF3)]5-(CH2)5-、
-(CH2)-[C(CH3)(CH2CF3)]5-(CH2)6-、
-(CH2)2-[C(CH3)(CH2CF3)]5-(CH2)-、
-(CH2)3-[C(CH3)(CH2CF3)]5-(CH2)-、
-(CH2)4-[C(CH3)(CH2CF3)]5-(CH2)-、
-(CH2)5-[C(CH3)(CH2CF3)]5-(CH2)-、
-(CH2)6-[C(CH3)(CH2CF3)]5-(CH2)-、
-(CH2)2-[C(CH3)(CH2CF3)]5-(CH2)2-、
-(CH2)3-[C(CH3)(CH2CF3)]5-(CH2)3-、
-(CH2)4-[C(CH3)(CH2CF3)]5-(CH2)4-、
-(CH2)2-[C(CH3)(CH2CF3)]5-(CH2)3-、
-(CH2)2-[C(CH3)(CH2CF3)]5-(CH2)4-、
-(CH2)2-[C(CH3)(CH2CF3)]5-(CH2)5-、
-(CH2)2-[C(CH3)(CH2CF3)]5-(CH2)6-、
-(CH2)3-[C(CH3)(CH2CF3)]5-(CH2)2-、
-(CH2)3-[C(CH3)(CH2CF3)]5-(CH2)4-、
-(CH2)4-[C(CH3)(CH2CF3)]5-(CH2)2-、
-(CH2)4-[C(CH3)(CH2CF3)]5-(CH2)3-、
-(CH2)5-[C(CH3)(CH2CF3)]5-(CH2)2-、
-(CH2)2-(CF2)-O-(CF2)-O-(CF2)-(CH2)2-、
-(CH2)3-(CF2)-O-(CF2)-O-(CF2)-(CH2)3-、
-(CH2)4-(CF2)-O-(CF2)-O-(CF2)-(CH2)4-、
-(CH2)-(CF2)-O-(CF2)-O-(CF2)-(CH2)2-、
-(CH2)-(CF2)-O-(CF2)-O-(CF2)-(CH2)3-、
-(CH2)-(CF2)-O-(CF2)-O-(CF2)-(CH2)4-、
-(CH2)-(CF2)-O-(CF2)-O-(CF2)-(CH2)5-、
-(CH2)-(CF2)-O-(CF2)-O-(CF2)-(CH2)6-、
-(CH2)-(CF2)-O-(CF2)-O-(CF2)-(CH2)7-、
-(CH2)2-(CF2)-O-(CF2)-O-(CF2)-(CH2)-、
-(CH2)3-(CF2)-O-(CF2)-O-(CF2)-(CH2)-、
-(CH2)4-(CF2)-O-(CF2)-O-(CF2)-(CH2)-、
-(CH2)5-(CF2)-O-(CF2)-O-(CF2)-(CH2)-、
-(CH2)6-(CF2)-O-(CF2)-O-(CF2)-(CH2)-、
-(CH2)7-(CF2)-O-(CF2)-O-(CF2)-(CH2)-、
-(CH2)2-(CF2)-O-(CF2)-O-(CF2)-(CH2)3-、
-(CH2)2-(CF2)-O-(CF2)-O-(CF2)-(CH2)4-、
-(CH2)2-(CF2)-O-(CF2)-O-(CF2)-(CH2)5-、
-(CH2)2-(CF2)-O-(CF2)-O-(CF2)-(CH2)6-、
-(CH2)3-(CF2)-O-(CF2)-O-(CF2)-(CH2)2-、
-(CH2)4-(CF2)-O-(CF2)-O-(CF2)-(CH2)2-、
-(CH2)5-(CF2)-O-(CF2)-O-(CF2)-(CH2)2-、
-(CH2)6-(CF2)-O-(CF2)-O-(CF2)-(CH2)2-、
-(CH2)3-(CF2)-O-(CF2)-O-(CF2)-(CH2)4-、
-(CH2)4-(CF2)-O-(CF2)-O-(CF2)-(CH2)3-、
-(CH2)3-(CF2)-O-(CF2)-O-(CF2)-(CH2)5-、
-(CH2)5-(CF2)-O-(CF2)-O-(CF2)-(CH2)3-、
-(CH2)2-(CF2)-O-(CF2)2-O-(CF2)-(CH2)2-、
-(CH2)3-(CF2)-O-(CF2)2-O-(CF2)-(CH2)3-、
-(CH2)4-(CF2)-O-(CF2)2-O-(CF2)-(CH2)4-、
-(CH2)-(CF2)-O-(CF2)2-O-(CF2)-(CH2)2-、
-(CH2)-(CF2)-O-(CF2)2-O-(CF2)-(CH2)3-、
-(CH2)-(CF2)-O-(CF2)2-O-(CF2)-(CH2)4-、
-(CH2)-(CF2)-O-(CF2)2-O-(CF2)-(CH2)5-、
-(CH2)-(CF2)-O-(CF2)2-O-(CF2)-(CH2)6-、
-(CH2)-(CF2)-O-(CF2)2-O-(CF2)-(CH2)7-、
-(CH2)2-(CF2)-O-(CF2)2-O-(CF2)-(CH2)-、
-(CH2)3-(CF2)-O-(CF2)2-O-(CF2)-(CH2)-、
-(CH2)4-(CF2)-O-(CF2)2-O-(CF2)-(CH2)-、
-(CH2)5-(CF2)-O-(CF2)2-O-(CF2)-(CH2)-、
-(CH2)6-(CF2)-O-(CF2)2-O-(CF2)-(CH2)-、
-(CH2)7-(CF2)-O-(CF2)2-O-(CF2)-(CH2)-、
-(CH2)2-(CF2)-O-(CF2)2-O-(CF2)-(CH2)3-、
-(CH2)2-(CF2)-O-(CF2)2-O-(CF2)-(CH2)4-、
-(CH2)2-(CF2)-O-(CF2)2-O-(CF2)-(CH2)5-、
-(CH2)2-(CF2)-O-(CF2)2-O-(CF2)-(CH2)6-、
-(CH2)3-(CF2)-O-(CF2)2-O-(CF2)-(CH2)2-、
-(CH2)4-(CF2)-O-(CF2)2-O-(CF2)-(CH2)2-、
-(CH2)5-(CF2)-O-(CF2)2-O-(CF2)-(CH2)2-、
-(CH2)6-(CF2)-O-(CF2)2-O-(CF2)-(CH2)2-、
-(CH2)3-(CF2)-O-(CF2)2-O-(CF2)-(CH2)4-、
-(CH2)4-(CF2)-O-(CF2)2-O-(CF2)-(CH2)3-、
-(CH2)3-(CF2)-O-(CF2)2-O-(CF2)-(CH2)5-、
-(CH2)5-(CF2)-O-(CF2)2-O-(CF2)-(CH2)3-、
-(CH2)2-(CF2)2-O-(CF2)2-O-(CF2)2-(CH2)2-、
-(CH2)3-(CF2)2-O-(CF2)2-O-(CF2)2-(CH2)3-、
-(CH2)4-(CF2)2-O-(CF2)2-O-(CF2)2-(CH2)4-、
-(CH2)-(CF2)2-O-(CF2)2-O-(CF2)2-(CH2)2-、
-(CH2)-(CF2)2-O-(CF2)2-O-(CF2)2-(CH2)3-、
-(CH2)-(CF2)2-O-(CF2)2-O-(CF2)2-(CH2)3-、
-(CH2)-(CF2)2-O-(CF2)2-O-(CF2)2-(CH2)4-、
-(CH2)-(CF2)2-O-(CF2)2-O-(CF2)2-(CH2)5-、
-(CH2)-(CF2)2-O-(CF2)2-O-(CF2)2-(CH2)6-、
-(CH2)-(CF2)2-O-(CF2)2-O-(CF2)2-(CH2)7-、
-(CH2)2-(CF2)2-O-(CF2)2-O-(CF2)2-(CH2)-、
-(CH2)3-(CF2)2-O-(CF2)2-O-(CF2)2-(CH2)-、
-(CH2)4-(CF2)2-O-(CF2)2-O-(CF2)2-(CH2)-、
-(CH2)5-(CF2)2-O-(CF2)2-O-(CF2)2-(CH2)-、
-(CH2)6-(CF2)2-O-(CF2)2-O-(CF2)2-(CH2)-、
-(CH2)7-(CF2)2-O-(CF2)2-O-(CF2)2-(CH2)-、
-(CH2)2-(CF2)2-O-(CF2)2-O-(CF2)2-(CH2)3-、
-(CH2)2-(CF2)2-O-(CF2)2-O-(CF2)2-(CH2)4-、
-(CH2)2-(CF2)2-O-(CF2)2-O-(CF2)2-(CH2)5-、
-(CH2)2-(CF2)2-O-(CF2)2-O-(CF2)2-(CH2)6-、
-(CH2)3-(CF2)2-O-(CF2)2-O-(CF2)2-(CH2)2-、
-(CH2)4-(CF2)2-O-(CF2)2-O-(CF2)2-(CH2)2-、
-(CH2)5-(CF2)2-O-(CF2)2-O-(CF2)2-(CH2)2-、
-(CH2)6-(CF2)2-O-(CF2)2-O-(CF2)2-(CH2)2-、
-(CH2)3-(CF2)2-O-(CF2)2-O-(CF2)2-(CH2)4-、
-(CH2)4-(CF2)2-O-(CF2)2-O-(CF2)2-(CH2)3-、
-(CH2)3-(CF2)2-O-(CF2)2-O-(CF2)2-(CH2)5-、
-(CH2)5-(CF2)2-O-(CF2)2-O-(CF2)2-(CH2)3-、
-(CH2)2-(CF2)-O-(CF2)-O-(CF2)-O-(CF2)-(CH2)2-、
-(CH2)3-(CF2)-O-(CF2)-O-(CF2)-O-(CF2)-(CH2)3-、
-(CH2)4-(CF2)-O-(CF2)-O-(CF2)-O-(CF2)-(CH2)4-、
-(CH2)-(CF2)-O-(CF2)-O-(CF2)-O-(CF2)-(CH2)2-、
-(CH2)-(CF2)-O-(CF2)-O-(CF2)-O-(CF2)-(CH2)3-、
-(CH2)-(CF2)-O-(CF2)-O-(CF2)-O-(CF2)-(CH2)4-、
-(CH2)-(CF2)-O-(CF2)-O-(CF2)-O-(CF2)-(CH2)5-、
-(CH2)-(CF2)-O-(CF2)-O-(CF2)-O-(CF2)-(CH2)6-、
-(CH2)-(CF2)-O-(CF2)-O-(CF2)-O-(CF2)-(CH2)7-、
-(CH2)2-(CF2)-O-(CF2)-O-(CF2)-O-(CF2)-(CH2)-、
-(CH2)3-(CF2)-O-(CF2)-O-(CF2)-O-(CF2)-(CH2)-、
-(CH2)4-(CF2)-O-(CF2)-O-(CF2)-O-(CF2)-(CH2)-、
-(CH2)5-(CF2)-O-(CF2)-O-(CF2)-O-(CF2)-(CH2)-、
-(CH2)6-(CF2)-O-(CF2)-O-(CF2)-O-(CF2)-(CH2)-、
-(CH2)7-(CF2)-O-(CF2)-O-(CF2)-O-(CF2)-(CH2)-、
-(CH2)2-(CF2)-O-(CF2)-O-(CF2)-O-(CF2)-(CH2)3-、
-(CH2)2-(CF2)-O-(CF2)-O-(CF2)-O-(CF2)-(CH2)4-、
-(CH2)2-(CF2)-O-(CF2)-O-(CF2)-O-(CF2)-(CH2)5-、
-(CH2)2-(CF2)-O-(CF2)-O-(CF2)-O-(CF2)-(CH2)6-、
-(CH2)3-(CF2)-O-(CF2)-O-(CF2)-O-(CF2)-(CH2)2-、
-(CH2)4-(CF2)-O-(CF2)-O-(CF2)-O-(CF2)-(CH2)2-、
-(CH2)5-(CF2)-O-(CF2)-O-(CF2)-O-(CF2)-(CH2)2-、
-(CH2)6-(CF2)-O-(CF2)-O-(CF2)-O-(CF2)-(CH2)2-、
-(CH2)3-(CF2)-O-(CF2)-O-(CF2)-O-(CF2)-(CH2)4-、
-(CH2)4-(CF2)-O-(CF2)-O-(CF2)-O-(CF2)-(CH2)3-、
-(CH2)3-(CF2)-O-(CF2)-O-(CF2)-O-(CF2)-(CH2)5-、
-(CH2)5-(CF2)-O-(CF2)-O-(CF2)-O-(CF2)-(CH2)3-、
-(CH2)2-(CF2)2-O-(CF2)2-O-(CF2)2-O-(CF2)2-(CH2)2-、
-(CH2)3-(CF2)2-O-(CF2)2-O-(CF2)2-O-(CF2)2-(CH2)3-、
-(CH2)4-(CF2)2-O-(CF2)2-O-(CF2)2-O-(CF2)2-(CH2)4-、
-(CH2)-(CF2)2-O-(CF2)2-O-(CF2)2-O-(CF2)2-(CH2)2-、
-(CH2)-(CF2)2-O-(CF2)2-O-(CF2)2-O-(CF2)2-(CH2)3-、
-(CH2)-(CF2)2-O-(CF2)2-O-(CF2)2-O-(CF2)2-(CH2)4-、
-(CH2)-(CF2)2-O-(CF2)2-O-(CF2)2-O-(CF2)2-(CH2)5-、
-(CH2)-(CF2)2-O-(CF2)2-O-(CF2)2-O-(CF2)2-(CH2)6-、
-(CH2)-(CF2)2-O-(CF2)2-O-(CF2)2-O-(CF2)2-(CH2)7-、
-(CH2)2-(CF2)2-O-(CF2)2-O-(CF2)2-O-(CF2)2-(CH2)-、
-(CH2)3-(CF2)2-O-(CF2)2-O-(CF2)2-O-(CF2)2-(CH2)-、
-(CH2)4-(CF2)2-O-(CF2)2-O-(CF2)2-O-(CF2)2-(CH2)-、
-(CH2)5-(CF2)2-O-(CF2)2-O-(CF2)2-O-(CF2)2-(CH2)-、
-(CH2)6-(CF2)2-O-(CF2)2-O-(CF2)2-O-(CF2)2-(CH2)-、
-(CH2)7-(CF2)2-O-(CF2)2-O-(CF2)2-O-(CF2)2-(CH2)-、
-(CH2)2-(CF2)2-O-(CF2)2-O-(CF2)2-O-(CF2)2-(CH2)3-、
-(CH2)2-(CF2)2-O-(CF2)2-O-(CF2)2-O-(CF2)2-(CH2)4-、
-(CH2)2-(CF2)2-O-(CF2)2-O-(CF2)2-O-(CF2)2-(CH2)5-、
-(CH2)2-(CF2)2-O-(CF2)2-O-(CF2)2-O-(CF2)2-(CH2)6-、
-(CH2)3-(CF2)2-O-(CF2)2-O-(CF2)2-O-(CF2)2-(CH2)2-、
-(CH2)4-(CF2)2-O-(CF2)2-O-(CF2)2-O-(CF2)2-(CH2)2-、
-(CH2)5-(CF2)2-O-(CF2)2-O-(CF2)2-O-(CF2)2-(CH2)2-、
-(CH2)6-(CF2)2-O-(CF2)2-O-(CF2)2-O-(CF2)2-(CH2)2-、
-(CH2)3-(CF2)2-O-(CF2)2-O-(CF2)2-O-(CF2)2-(CH2)4-、
-(CH2)4-(CF2)2-O-(CF2)2-O-(CF2)2-O-(CF2)2-(CH2)3-、
-(CH2)3-(CF2)2-O-(CF2)2-O-(CF2)2-O-(CF2)2-(CH2)5-、
-(CH2)5-(CF2)2-O-(CF2)2-O-(CF2)2-O-(CF2)2-(CH2)3-、
-(CH2)12-、-(CH2)13-、
-(CH2)-(CHOH)-(CH2)-、
-(CH2)-(CHOH)-(CH2)4-、
-(CH2)4-(CHOH)-(CH2)-、
-(CH2)-[CH(CH2OH)]-(CH2)-、
-(CH2)-[CH(CH2OH)]-(CH2)4-、
-(CH2)2-[CH(CH2OH)]-(CH2)-、
-(CH2)3-(CHOH)-(CHOH)-(CH2)3-、
-(CH2)3-(CHOH)-(CHOH)-(CH2)4-、
-(CH2)3-(CHOH)-(CH2)-(CHOH)-(CH2)3-、
-(CH2)-(CHOH)-(CH2)2-(CHOH)-(CH2)-、
-(CH2)-(CHOH)-(CH2)-[CH(CH2OH)]-(CH2)3-、
-(CH2)-(CHOH)-(CH2)2-[CH(CH2OH)]-(CH2)-、
-(CH2)-(CHOH)-(CHOH)-(CH2)-(CHOH)-(CHOH)-(CH2)3-、
-(CH2)2-(CHOH)-(CHOH)-(CH2)-(CHOH)-(CHOH)-(CH2)3-、
-(CH2)-(CHOH)-(CH2)-O-(CH2)2-O-(CH2)-(CHOH)-(CH2)-、
-(CH2)-(CHOH)-(CH2)-O-(CH2)6-O-(CH2)-(CHOH)-(CH2)-、
-(CH2)3-(CF2)-(CH2)3-、-(CH2)5-(CF2)-(CH2)6-、
-(CH2)6-(CF2)-(CH2)5-、-(CH2)-(CF2)3-(CH2)-、
-(CH2)2-(CF2)4-(CH2)2-、-(CH2)-[CH(CF3)]-(CH2)-、
-(CH2)-[C(CH3)CF3]-(CH2)-、-(CH2)-[CH(CH2CF3)]-(CH2)-、
-(CH2)-[C(CH3)(CH2CF3)]-(CH2)-、
-(CH2)2-(CF2)-O-(CF2)-O-(CF2)-(CH2)2-、
-(CH2)-(CF2)-O-(CF2)-O-(CF2)-O-(CF2)-(CH2)-、
である。
-(CH2)11-、-(CH2)12-、-(CH2)13-、
-(CH2)-(CHOH)-(CH2)-、
-(CH2)-(CHOH)-(CH2)4-、
-(CH2)4-(CHOH)-(CH2)-、
-(CH2)-[CH(CH2OH)]-(CH2)-、
-(CH2)-[CH(CH2OH)]-(CH2)4-、
-(CH2)2-[CH(CH2OH)]-(CH2)-、
-(CH2)3-(CHOH)-(CHOH)-(CH2)3-、
-(CH2)3-(CHOH)-(CHOH)-(CH2)4-、
-(CH2)3-(CHOH)-(CH2)-(CHOH)-(CH2)3-、
-(CH2)-(CHOH)-(CH2)2-(CHOH)-(CH2)-、
-(CH2)-(CHOH)-(CH2)-[CH(CH2OH)]-(CH2)3-、
-(CH2)-(CHOH)-(CH2)2-[CH(CH2OH)]-(CH2)-、
-(CH2)-(CHOH)-(CHOH)-(CH2)-(CHOH)-(CHOH)-(CH2)3-、
-(CH2)2-(CHOH)-(CHOH)-(CH2)-(CHOH)-(CHOH)-(CH2)3-、
-(CH2)3-(CF2)-(CH2)3-、-(CH2)-(CF2)3-(CH2)-、
-(CH2)2-(CF2)4-(CH2)2-、
-(CH2)-[CH(CF3)]-(CH2)-、
-(CH2)-[C(CH3)CF3]-(CH2)-、
-(CH2)-[CH(CH2CF3)]-(CH2)-、
-(CH2)-[C(CH3)(CH2CF3)]-(CH2)-、
である。
-(CH2)11-、-(CH2)12-、-(CH2)13-、とくに-(CH2)12-である。
および前に記載のとおりのまたは前もしくは下に好ましく記載されるとおりの重合性基を有する置換基をもつ式(I)、(I-1)、(I-2)、(I-3)、(I-4)、(I-5)、(I-6)、(I-7)、(I-8)および(I-9)で表される化合物は、置換基-R2-が-(C(R)2)o-に対応し、およびRおよびoが前に記載のとおりのまたは前に好ましく記載されたとおりの意味を有する場合、好ましい。
式中
X4は、O、S、C(=O)、C(=O)Oからなる群から選択され、
R7、R8、R9は、出現毎に互いに独立して、H、F、1~20個のC原子を有する線状もしくは分枝状の、フッ素化されていないか、部分的または全面的にフッ素化されたアルキル、あるいは6~14個のC原子をもつアリールからなる群から選択され、および
cは、0または1であり、
星印「*」は、-R2-への結合を示す、
で表されるアルケニル基から選択される重合性基である場合、具体的に好ましく選択される。
好ましくは、R7は、H、メチル、エチルまたはフェニルである。
好ましくは、X4は、C(=O)またはC(=O)Oである。
好ましい基R1は、好ましくは、連結要素-R2-で表される好ましい基と組み合わせられる。
-(CH2)8-R1、-(CH2)11-R1、-(CH2)12-R1、
-(CH2)13-R1、-(CH2)-(CHOH)-(CH2)-R1、
-(CH2)-(CHOH)-(CH2)4-R1、
-(CH2)4-(CHOH)-(CH2)-R1、
-(CH2)-[CH(CH2OH)]-(CH2)-R1、
-(CH2)-[CH(CH2OH)]-(CH2)4-R1、
-(CH2)2-[CH(CH2OH)]-(CH2)-R1、
-(CH2)3-(CHOH)-(CHOH)-(CH2)3-R1、
-(CH2)3-(CHOH)-(CHOH)-(CH2)4-R1、
-(CH2)3-(CHOH)-(CH2)-(CHOH)-(CH2)3-R1、
-(CH2)-(CHOH)-(CH2)2-(CHOH)-(CH2)-R1、
-(CH2)-(CHOH)-(CH2)-[CH(CH2OH)]-(CH2)3-R1、
-(CH2)-(CHOH)-(CH2)2-[CH(CH2OH)]-(CH2)-R1、
-(CH2)-(CHOH)-(CHOH)-(CH2)-(CHOH)-(CHOH)-(CH2)3-R1、
-(CH2)2-(CHOH)-(CHOH)-(CH2)-(CHOH)-(CHOH)-(CH2)3-R1、
-(CH2)3-(CF2)-(CH2)3-R1、
-(CH2)-(CF2)3-(CH2)-R1、
-(CH2)2-(CF2)4-(CH2)2-R1、
-(CH2)-[CH(CF3)]-(CH2)-R1、
-(CH2)-[C(CH3)CF3]-(CH2)-R1、
-(CH2)-[CH(CH2CF3)]-(CH2)-R1、
-(CH2)-[C(CH3)(CH2CF3)]-(CH2)-R1、
からなる群から選択され、式中R1は、トリエトキシシリル、ジエトキシメチルシリル、または式(1-1)、(1-2)、(1-3)、(1-4)、(1-5)、(1-6)、(1-7)、(1-8)もしくは(1-9)で表されるアルケニルからなる群から選択されるか、あるいは式中R1は、好ましくは、式(1-1)、(1-2)または(1-3)で表されるアルケニルからなる群から選択される。
第2タイプの反応は、ウィリアムソンのエーテル合成である。
第3タイプの反応は、ウィリアムソンのエーテル合成である。
第4タイプの反応は、エステル化反応である。
第2タイプの反応は、ウィリアムソンのエーテル合成である。
第3タイプの反応は、ウィリアムソンのエーテル合成である。
第4タイプの反応は、エステル化反応である。
で表される構成単位M0を含み、式中
-R2-、R3、R4、R5、R6、R7、R8、R9、X、X0、R’、
X4およびcは、前に記載されたとおりのもしくは好ましく記載されたとおりの意味または好ましい意味を有する。有機化学の分野における当業者には知られているとおり、組み合わせは、2個のO原子または1個のO原子と1個のS原子とが互いに直接連結されている場合が除かれる。
(式中アルキル基および/またはアルコキシ基は、出現毎に互いに独立して、1~6個のC原子を有する線状または分枝状であり、およびここでアルケニル基は、出現毎に独立して、2~4個のC原子を有する線状である)で表されるシランからなる群から選択される1種以上のモノマーの重合によって導かれる。
(式中アルキル基および/またはアルコキシ基は、出現毎に互いに独立して、1~6個のC原子を有する線状または分枝状であり、およびここでアルケニル基は、出現毎に独立して、2~4個のC原子を有する線状である)で表されるシランからなる群から選択される1以上のモノマーの重合によって導き出される。
光開始剤の好適な例は、ジメチルアミノベンゾアート/カンファキノンである。
- 本明細書に定義されたとおりの式(I)で表される少なくとも1種の化合物、および/または本明細書に定義されたとおりのオリゴマーもしくはポリマーを含む組成物を提供すること;および
- 続いて、該組成物の物品を形成すること
というステップを含むプロセスによって形成されてもよい。
- 本明細書に定義されるとおりの物品を提供すること;および
- 続いて、該物品を、少なくとも200nmかつ最大でも1500nmの波長を有する照射にさらすこと
というステップを含む。
以下の例は、限定せずに本化合物の利点を示すことを意図する。
そのように示されない限り、合成はすべて、乾燥させた(すなわち水がない)溶媒を使用して不活性雰囲気下で実行する。溶媒および試薬は、商業的な供給元から購入する。
例1:
酢酸3-フェニル-クマリン-7-イルエステルの合成のための概論&一般合成手順(GSP1):
2g(14.2mmol)2,4-ジヒドロキシ-ベンズアルデヒドおよび3.1g(14.2mmol)4ブロモフェニル-酢酸を、4.5ml 無水酢酸および4.4ml ピリジンに溶解する。バッチを135℃にて72h撹拌し、次いで室温まで冷却する。沈殿した固体を吸引濾別し、水でゆすいで中性にする(rinsed neutral with water)。残渣を40℃にて真空乾燥する。3-(4-ブロモフェニル)-2-オキソ-2H-クロメン-7-イルアセタートの収量は4.9g(13.6mmol)(理論上の96%)である。
フェノール誘導体へのアセタート誘導体の脱保護のための概論&一般合成手順(GSP2):
7.0mmol 酢酸3-フェニル-クマリン-7-イルエステルを、14ml エタノールと10ml 硫酸(20%、aq.)との混合物に懸濁し、2h還流する。バッチを次いで、室温まで冷却し、沈殿した固体を吸引濾別して、水でゆすいで中性にする。収量は6.8mmolであり、理論上の97%である。
ハロゲン化2-オキソ-3-フェニル-2H-クロメン-7-イルアセタート誘導体の鈴木(Suzuki)カップリングのための概論&一般合成手順(GSP3):
3.0g(8.4mmol)の酢酸3-(4-ブロモフェニル)-クマリン-7-イルエステル、1.0g(8.8mmol)のボロン酸n-ペンチル、および3.7g(17.5mmol)のリン酸三カリウム三水和物を、80mlのトルエンに溶解し、脱気する。171mg(0.4mmol)の2-ジシクロヘキシルホスフィノ-2’,6’-ジメトキシ-1,1’-ビフェニル[S-Phos]および47mg(0.2mmol)の酢酸パラジウム(II)を加える。続いて反応混合物を、保護ガス雰囲気下110℃にて24h撹拌する。冷却された溶液を、酢酸エチルで希釈して水で洗浄し、乾燥して蒸発させた。産物を、シリカゲル上のカラムクロマトグラフィー(ヘプタン/酢酸エチル)によって精製する。収率:2.5g(7.1mmol)、理論上の85%。
メチルエーテル誘導体の、対応するフェノール誘導体への脱保護のための概論&一般合成手順(GSP4):
10ml DCM中3-(2-エチル-4-ペンチルフェニル)-7-メトキシ-2H-クロメン-2-オン(300mg、0.973mmol)の溶液へ、BCl3(2.0当量)を0℃にて加える。溶液を室温まで終夜加温し、さらに1時間還流させる。反応混合物を室温まで冷却させた後、これを氷/水の混合物上へ注ぎ、EEで抽出し、MgSO4で乾燥させて蒸発させる。残渣を、ヘプタン/EEを溶離液として使用するカラムクロマトグラフィーを介して精製する。182.3mg(0.51mmol)の3-(2-エチル-4-ペンチルフェニル)-7-ヒドロキシ-2H-クロメン-2-オンを単離する(理論上の83%)。
1H NMR (500 MHz,DMSO-d6) δ 10.58 (s,1H),7.85 (s,1H),7.54 (d,2H,J = 8.5 Hz),7.16 7.06 (m,3H),7.10 (d,1H,j = 2.2 Hz),6.81 (dd,1H,J = 8.5 Hz,J = 2.3 Hz),6.76 (d,1H,J = 2.3 Hz),2.63 (q,2H,J = 7.6 Hz),2.49-2.45 (m,2H),1.21 (t,3H,J = 7.6 Hz),1.07 (t,3H,J = 7.5 Hz).
7-[3-ヒドロキシ-5-[3-[4-ペンチル-2-(トリフルオロメチル)フェニル]クマリン-7-イル]ペンタ-1,4-ジイニル]-3-[4-ペンチル-2-(トリフルオロメチル)フェニル]クマリンの合成のための概論&一般合成手順(GSP5.3):
7-[3-ヒドロキシ-5-[3-[4-ペンチル-2-(トリフルオロメチル)フェニル]クマリン-7-イル]ペンチル]-3-[4-ペンチル-2-(トリフルオロメチル)フェニル]クマリンの合成のための概論&一般合成手順(GSP5.4):
モノマーの溶媒重合のための概論&一般合成手順(GSP8):
対応するモノマーを、撹拌子のあるシュレンク管(Schlenck-tube)中乾燥N,N-ジメチルホルムアミドに溶解する。溶液を脱気して、凍結-排気-解凍のサイクルを3回実施する。その後、アゾイソブチロニトリル(AIBN、0.05当量)を一回で(in one portion)、脱気された溶液へ加え、これを最低でも3日間、油浴中で最大65℃まで加熱する。溶液を室温まで冷却し、次いでこれを液滴として、撹拌しながら冷メタノール(100ml メタノール/100mg モノマー)中へ注ぐ。沈殿したポリマーをフリット上で回収するか、または溶液を数回遠心分離することで最終ポリマー材料を得る。
例11dに記載のとおりの12-((1,3-ビス((3-(2-(トリフルオロメチル)-4-(ペンチル)フェニル)クマリン-7-イル)オキシ)プロパン-2-イル)オキシ)ドデシルアクリラート、メタクリル酸メチル、開始剤のアゾビスイソブチロニトリル(0.04eq)、およびクロスリンカーのエチレングリコールジメタクリラート(0.1~0.4eq)の種々の比率での組成物を、3サイクルの凍結-ポンプでの吸出(pump)-解凍によって脱気する。
例15 - 光誘起屈折率変化およびガラス転移温度
相転移温度を、密封したアルミニウムパン中、-100℃から200℃まで20K/minでの第2加熱ラン(the second heating run)における加熱の間、TA Instruments Q2000示差走査熱量計で決定する。素材の照射は、Coherent Avia 355-7000 UV-Laserで実施する。
の590nmでの屈折率(n)を、照射前後にSchmidt+Haensch AR12上で測定する。以下
の表は、照射前後の屈折率ならびに屈折率の変化(最大のΔn)を示す。
引用されたポリマーのための期待される値を以下の表に与える:
(1) 式(I)
Xは、O、SまたはNR 0 であり、
X 0 は、OまたはSであり、
dは、0または1であり、
Rは、出現毎に独立して、H、F、OH、1~4個のC原子を有する線状もしくは分枝状のアルキル基、1~4個のC原子を有する線状もしくは分枝状のヒドロキシアルキル基、あるいは1~4個のC原子を有する線状もしくは分枝状の、部分的または全体的にフッ素化されたアルキル基からなる群から選択され、
R’は、出現毎に独立して、H、F、1~20個のC原子を有する線状もしくは分枝状の、ハロゲン化されていないか、部分的または全面的にハロゲン化されたアルキル基、1~20個のC原子を有する線状もしくは分枝状のヒドロキシアルキル基、3~6個のC原子を有する、ハロゲン化されていないか、部分的または全面的にハロゲン化されたシクロアルキル基、1~20個のC原子を有する線状もしくは分枝状の、ハロゲン化されていないか、部分的または全面的にハロゲン化されたアルコキシ基、あるいは1~20個のC原子を有する線状もしくは分枝状の、ハロゲン化されていないか、部分的または全面的にハロゲン化されたチオアルキル基からなる群から選択され、
R 0 は、出現毎に独立して、1~10個のC原子を有する線状もしくは分枝状のアルキル基、または3~6個のC原子を有するシクロアルキル基からなる群から選択され、
R 1 は、式(1)、
X 4 は、O、S、C(=O)、C(=O)Oからなる群から選択され、
R 7 、R 8 、R 9 は出現毎に、互いに独立して、H、F、1~20個のC原子を有する線状もしくは分枝状の、非フッ素化されているか、部分的または全面的にフッ素化されたアルキル、あるいは6~14個のC原子をもつアリールからなる群から選択され、
cは、0または1である、
で表されるアルケニル基;
トリアルコキシシリル基またはジアルコキシアルキルシリル基であって、当該基中のアルキル基および/またはアルコキシ基は、各々独立して、1~6個のC原子を有する線状または分枝状である;およびシリル基は、式(2)、(3)または(4)、
で表される、前記トリアルコキシシリル基または前記ジアルコキシアルキルシリル基
からなる群から選択される重合性基であり、
-R 2 -は、-(C(R) 2 ) o -、-(C(R) 2 ) p -X 1 -(C(R) 2 ) q -(X 2 ) s -(C(R) 2 ) r -(X 3 ) t -(C(R) 2 ) u -、またはHとは異なる少なくとも1個のRで置換された5個もしくは6個のC原子を有するシクロアルキレン基であり、
oは、1~20からなる群から選択され、
X 1 、X 2 、X 3 は、出現毎に独立して、O、SまたはNR 0 であり、
s、tは、0または1であり、
p、qは、出現毎に独立して、1~10からなる群から選択され、ならびに
r、uは、出現毎に独立して、0~10からなる群から選択されるが、ここで-(C(
R) 2 ) p -X 1 -(C(R) 2 ) q -(X 2 ) s -(C(R) 2 ) r -(X 3 ) t -(C(R) 2 ) u -について原子の全体数が、最大20原子までであり、
R 3 、R 4 、R 5 、R 6 は、出現毎に独立して、R’である、
で表される化合物。
(2)
に対応する、実施態様1に記載の化合物。
(3) dが、1である、実施態様1または2に記載の化合物。
(4) dが1であり、ならびにXおよびX 0 が、Oである、実施態様1~3のいずれかに記載の化合物。
(5) 少なくとも1個のR’が、Hではない、実施態様1~4のいずれかに記載の化合物。
(6) 少なくとも2個のR’が、Hではない、実施態様1~5のいずれかに記載の化合物。
(7) 少なくとも4個のR’が、Hではない、実施態様1~6のいずれかに記載の化合物。
(8) 置換基R 3 、R 4 、R 5 、R 6 が、出現毎に同一である、実施態様1~7のいずれかに記載の化合物。
(9) R 2 が、-(C(R) 2 ) o -であり、ならびにRおよびoが、実施態様1に提示されるとおりの意味を有する、実施態様1~8のいずれかに記載の化合物。
(10) R 1 が、アクリルラジカルまたはメタクリルラジカルである、実施態様1~9のいずれかに記載の化合物。
(11) 実施態様1~10のいずれかに記載されるとおりの重合された式(I)で表される化合物を含む、オリゴマーまたはポリマー。
(12) 実施態様1~10のいずれかに記載の式(I)で表される少なくとも1個の化合物および/または実施態様11に記載のオリゴマーもしくはポリマーを含む、組成物。
(13) 実施態様1~10のいずれかに記載の少なくとも1種の重合された式(I)で表される化合物、または実施態様11に記載の少なくとも1種のオリゴマーもしくはポリマーを含む、物品。
(14) 該物品が、目用インプラントへ変換され得る素材、または目用インプラント、好ましくは眼内レンズである、実施態様13に記載の物品。
(15) 実施態様13または14に記載の物品を形成するプロセスであって、該プロセスが、
- 実施態様1~10のいずれかに記載の式(I)で表される少なくとも1種の化合物および/または実施態様11に記載のオリゴマーもしくはポリマーを含む組成物を提供すること;
- 続いて、該組成物の物品を形成すること
というステップを含む、前記プロセス。
(16) 実施態様13または14に記載の物品の光学特性を変化させるプロセスであって、該プロセスが、
- 実施態様13または14に記載の物品を提供すること、および
- 続いて、該物品を、少なくとも200nmかつ最大でも1500nmの波長を有する照射にさらすこと
というステップを含む、前記プロセス。
Claims (15)
- 重合された式(I)で表される化合物を含む、オリゴマーまたはポリマーを含む、組成物。
Xは、O、SまたはNR0であり、
X0は、OまたはSであり、
dは、0または1であり、
Rは、出現毎に独立して、H、F、OH、1~4個のC原子を有する線状もしくは分枝状のアルキル基、1~4個のC原子を有する線状もしくは分枝状のヒドロキシアルキル基、あるいは1~4個のC原子を有する線状もしくは分枝状の、部分的または全体的にフッ素化されたアルキル基からなる群から選択され、
R’は、出現毎に独立して、H、F、1~20個のC原子を有する線状もしくは分枝状の、ハロゲン化されていないか、部分的または全面的にハロゲン化されたアルキル基、1~20個のC原子を有する線状もしくは分枝状のヒドロキシアルキル基、3~6個のC原子を有する、ハロゲン化されていないか、部分的または全面的にハロゲン化されたシクロアルキル基、1~20個のC原子を有する線状もしくは分枝状の、ハロゲン化されていないか、部分的または全面的にハロゲン化されたアルコキシ基、あるいは1~20個のC原子を有する線状もしくは分枝状の、ハロゲン化されていないか、部分的または全面的にハロゲン化されたチオアルキル基からなる群から選択され、
R0は、出現毎に独立して、1~10個のC原子を有する線状もしくは分枝状のアルキル基、または3~6個のC原子を有するシクロアルキル基からなる群から選択され、
R1は、式(1)、
X4は、C(=O)Oであり、
R7、R8、R9は出現毎に、互いに独立して、H、F、1~20個のC原子を有する線状もしくは分枝状の、非フッ素化されているか、部分的または全面的にフッ素化されたアルキル、あるいは6~14個のC原子をもつアリールからなる群から選択され、
cは、1である、
で表されるアルケニル基である、重合性基であり、
-R2-は、-(C(R)2)o-、-(C(R)2)p-X1-(C(R)2)q-(X2)s-(C(R)2)r-(X3)t-(C(R)2)u-、またはHとは異なる少なくとも1個のRで置換された5個もしくは6個のC原子を有するシクロアルキレン基であり、
oは、1~20からなる群から選択され、
X1、X2、X3は、出現毎に独立して、O、SまたはNR0であり、
s、tは、0または1であり、
p、qは、出現毎に独立して、1~10からなる群から選択され、ならびに
r、uは、出現毎に独立して、0~10からなる群から選択されるが、ここで-(C(
R)2)p-X1-(C(R)2)q-(X2)s-(C(R)2)r-(X3)t-(C(R)2)u-について原子の全体数が、最大20原子までであり、
R3、R4、R5、R6は、出現毎に独立して、R’である。 - dが、1である、請求項1または2に記載の組成物。
- dが1であり、ならびにXおよびX0が、Oである、請求項1~3のいずれか一項に記載の組成物。
- 少なくとも1個のR’が、Hではない、請求項1~4のいずれか一項に記載の組成物。
- 少なくとも2個のR’が、Hではない、請求項1~5のいずれか一項に記載の組成物。
- 少なくとも4個のR’が、Hではない、請求項1~6のいずれか一項に記載の組成物。
- 置換基R3、R4、R5、R6が、出現毎に同一である、請求項1~7のいずれか一項に記載の組成物。
- R2が、-(C(R)2)o-であり、ならびにRおよびoが、請求項1に提示されるとおりの意味を有する、請求項1~8のいずれか一項に記載の組成物。
- R1が、アクリルラジカルまたはメタクリルラジカルである、請求項1~9のいずれか一項に記載の組成物。
- 請求項1~10のいずれか一項に記載の組成物を含む、物品。
- 該物品が、目用インプラントへ変換され得る素材、または目用インプラントである、請求項11に記載の物品。
- 該物品が、眼内レンズである、請求項11に記載の物品。
- 請求項11~13のいずれか一項に記載の物品を形成するプロセスであって、該プロセスが、
- 請求項1~10のいずれか一項に記載の組成物を提供すること;
- 続いて、該組成物の物品を形成すること
というステップを含む、前記プロセス。 - 請求項11~13のいずれか一項に記載の物品の光学特性を変化させるプロセスであって、該プロセスが、
- 請求項11~13のいずれか一項に記載の物品を提供すること、および
- 続いて、該物品を、少なくとも200nmかつ最大でも1500nmの波長を有する照射にさらすこと
というステップを含む、前記プロセス。
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2022154662A JP7528170B2 (ja) | 2017-02-15 | 2022-09-28 | 光学活性デバイスのためのビス化合物 |
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| EP17156327.3A EP3363794A1 (en) | 2017-02-15 | 2017-02-15 | Bis-compounds for optically active devices |
| EP17156327.3 | 2017-02-15 | ||
| PCT/EP2018/053621 WO2018149850A1 (en) | 2017-02-15 | 2018-02-14 | Bis-compounds for optically active devices |
Related Child Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2022154662A Division JP7528170B2 (ja) | 2017-02-15 | 2022-09-28 | 光学活性デバイスのためのビス化合物 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2020508986A JP2020508986A (ja) | 2020-03-26 |
| JP7150737B2 true JP7150737B2 (ja) | 2022-10-11 |
Family
ID=58046588
Family Applications (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2019543965A Active JP7150737B2 (ja) | 2017-02-15 | 2018-02-14 | 光学活性デバイスのための化合物 |
| JP2022154662A Active JP7528170B2 (ja) | 2017-02-15 | 2022-09-28 | 光学活性デバイスのためのビス化合物 |
Family Applications After (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2022154662A Active JP7528170B2 (ja) | 2017-02-15 | 2022-09-28 | 光学活性デバイスのためのビス化合物 |
Country Status (13)
| Country | Link |
|---|---|
| US (1) | US11001576B2 (ja) |
| EP (2) | EP3363794A1 (ja) |
| JP (2) | JP7150737B2 (ja) |
| CN (1) | CN110300747B (ja) |
| AU (1) | AU2018222556B2 (ja) |
| BR (1) | BR112019014963A8 (ja) |
| CA (1) | CA3053434A1 (ja) |
| ES (1) | ES2848058T3 (ja) |
| HU (1) | HUE053267T2 (ja) |
| MX (1) | MX393092B (ja) |
| PL (1) | PL3583101T3 (ja) |
| PT (1) | PT3583101T (ja) |
| WO (1) | WO2018149850A1 (ja) |
Families Citing this family (10)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP3133065A1 (en) | 2015-08-21 | 2017-02-22 | Merck Patent GmbH | Compounds for optically active devices |
| EP3363786A1 (en) | 2017-02-15 | 2018-08-22 | Merck Patent GmbH | Compounds for optically active devices |
| EP3363793A1 (en) * | 2017-02-15 | 2018-08-22 | Merck Patent GmbH | Hydrophobic compounds for optically active devices |
| MX2021011159A (es) | 2019-04-18 | 2021-10-22 | Johnson & Johnson Surgical Vision Inc | Compuestos para dispositivos opticamente activos. |
| US20220202566A1 (en) | 2019-04-26 | 2022-06-30 | Merck Patent Gmbh | System and method |
| US20230203214A1 (en) | 2020-05-20 | 2023-06-29 | Merck Patent Gmbh | Azacoumarin and azathiocoumarin derivatives for use in optically active devices |
| WO2022012798A1 (en) | 2020-07-15 | 2022-01-20 | Merck Patent Gmbh | Optically active devices |
| EP4015512A1 (en) | 2020-12-16 | 2022-06-22 | AMO Ireland | Optically active devices |
| EP4036085A1 (en) | 2021-01-27 | 2022-08-03 | AMO Ireland | Compounds for optically active ophthalmic devices |
| US20260109796A1 (en) | 2024-10-17 | 2026-04-23 | Johnson & Johnson Surgical Vision, Inc. | Materials and methods for light adjustable ophthalmic devices |
Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2009070172A1 (en) | 2007-11-30 | 2009-06-04 | Henkel Ag & Co. Kgaa | Curable resins containing acetal, ketal, acetal ester, or ketal ester linkages |
| JP2011505932A (ja) | 2007-12-11 | 2011-03-03 | *アクリテック ゲーエムベーハー | 眼科用組成物及びその使用 |
Family Cites Families (14)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US5290892A (en) | 1990-11-07 | 1994-03-01 | Nestle S.A. | Flexible intraocular lenses made from high refractive index polymers |
| IT1247476B (it) * | 1991-06-14 | 1994-12-17 | Fidia Spa | Derivati della cumarina. |
| US5331073A (en) | 1992-11-09 | 1994-07-19 | Allergan, Inc. | Polymeric compositions and intraocular lenses made from same |
| JP3206004B2 (ja) | 1995-06-07 | 2001-09-04 | アルコン ラボラトリーズ, インコーポレイテッド | 改良された高屈折率の眼科用レンズ材料 |
| DE19955836C1 (de) * | 1999-11-19 | 2001-05-17 | Norbert Hampp | Ophthalmologisches Implantat |
| US6852793B2 (en) * | 2002-06-19 | 2005-02-08 | Bausch & Lomb Incorporated | Low water content, high refractive index, flexible, polymeric compositions |
| DE102005045540A1 (de) | 2005-09-23 | 2007-03-29 | Hampp, Norbert, Prof. Dr. | Intraokularlinse |
| JP2011507987A (ja) | 2007-12-11 | 2011-03-10 | *アクリテック ゲーエムベーハー | 共重合体及び眼科用組成物 |
| JP5402266B2 (ja) | 2008-06-10 | 2014-01-29 | 三菱化学株式会社 | 光反応性組成物、光学材料、ホログラム記録層形成用組成物、ホログラム記録材料およびホログラム記録媒体 |
| CN102197109B (zh) * | 2008-10-29 | 2014-05-14 | 默克专利股份有限公司 | 液晶显示器 |
| DE102008063742A1 (de) * | 2008-12-18 | 2010-07-01 | *Acri.Tec Gmbh | Farbstoff, ophthalmologische Zusammensetzung und ophthalmologische Linse |
| TWI583673B (zh) * | 2010-04-02 | 2017-05-21 | 艾爾康股份有限公司 | 可調整之發色團化合物及併合該化合物之材料 |
| TWI473823B (zh) * | 2010-06-21 | 2015-02-21 | Novartis Ag | 具有經降低的閃光之高折射率、丙烯酸系眼科裝置材料 |
| EP3133065A1 (en) | 2015-08-21 | 2017-02-22 | Merck Patent GmbH | Compounds for optically active devices |
-
2017
- 2017-02-15 EP EP17156327.3A patent/EP3363794A1/en not_active Ceased
-
2018
- 2018-02-14 AU AU2018222556A patent/AU2018222556B2/en active Active
- 2018-02-14 MX MX2019009606A patent/MX393092B/es unknown
- 2018-02-14 CA CA3053434A patent/CA3053434A1/en active Pending
- 2018-02-14 PL PL18705880T patent/PL3583101T3/pl unknown
- 2018-02-14 US US16/485,847 patent/US11001576B2/en active Active
- 2018-02-14 HU HUE18705880A patent/HUE053267T2/hu unknown
- 2018-02-14 ES ES18705880T patent/ES2848058T3/es active Active
- 2018-02-14 EP EP18705880.5A patent/EP3583101B1/en active Active
- 2018-02-14 CN CN201880011909.3A patent/CN110300747B/zh active Active
- 2018-02-14 WO PCT/EP2018/053621 patent/WO2018149850A1/en not_active Ceased
- 2018-02-14 JP JP2019543965A patent/JP7150737B2/ja active Active
- 2018-02-14 PT PT187058805T patent/PT3583101T/pt unknown
- 2018-02-14 BR BR112019014963A patent/BR112019014963A8/pt active Search and Examination
-
2022
- 2022-09-28 JP JP2022154662A patent/JP7528170B2/ja active Active
Patent Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2009070172A1 (en) | 2007-11-30 | 2009-06-04 | Henkel Ag & Co. Kgaa | Curable resins containing acetal, ketal, acetal ester, or ketal ester linkages |
| JP2011505932A (ja) | 2007-12-11 | 2011-03-03 | *アクリテック ゲーエムベーハー | 眼科用組成物及びその使用 |
Also Published As
| Publication number | Publication date |
|---|---|
| EP3583101B1 (en) | 2020-10-28 |
| BR112019014963A8 (pt) | 2023-01-10 |
| BR112019014963A2 (pt) | 2020-04-07 |
| EP3583101A1 (en) | 2019-12-25 |
| MX393092B (es) | 2025-03-24 |
| AU2018222556A1 (en) | 2019-10-03 |
| ES2848058T3 (es) | 2021-08-05 |
| AU2018222556B2 (en) | 2022-03-03 |
| JP2022173419A (ja) | 2022-11-18 |
| PT3583101T (pt) | 2021-01-29 |
| CN110300747A (zh) | 2019-10-01 |
| US11001576B2 (en) | 2021-05-11 |
| WO2018149850A1 (en) | 2018-08-23 |
| MX2019009606A (es) | 2019-11-08 |
| JP2020508986A (ja) | 2020-03-26 |
| HUE053267T2 (hu) | 2021-06-28 |
| CA3053434A1 (en) | 2018-08-23 |
| EP3363794A1 (en) | 2018-08-22 |
| CN110300747B (zh) | 2023-03-28 |
| US20200062739A1 (en) | 2020-02-27 |
| PL3583101T3 (pl) | 2021-04-06 |
| JP7528170B2 (ja) | 2024-08-05 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP7150737B2 (ja) | 光学活性デバイスのための化合物 | |
| JP7528169B2 (ja) | 光学活性デバイスのための化合物 | |
| JP7150738B2 (ja) | 光学活性デバイスのための疎水性化合物 | |
| ES2848071T3 (es) | Compuestos hidrófilos para dispositivos ópticamente activos | |
| ES2850898T3 (es) | Compuestos hidrófobos para dispositivos ópticamente activos |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20210212 |
|
| A977 | Report on retrieval |
Free format text: JAPANESE INTERMEDIATE CODE: A971007 Effective date: 20211223 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20220111 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20220411 |
|
| A711 | Notification of change in applicant |
Free format text: JAPANESE INTERMEDIATE CODE: A711 Effective date: 20220411 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20220519 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20220608 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20220830 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20220928 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 7150737 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |