JP7101694B2 - 腰痛のための抗生物質製剤 - Google Patents
腰痛のための抗生物質製剤 Download PDFInfo
- Publication number
- JP7101694B2 JP7101694B2 JP2019547196A JP2019547196A JP7101694B2 JP 7101694 B2 JP7101694 B2 JP 7101694B2 JP 2019547196 A JP2019547196 A JP 2019547196A JP 2019547196 A JP2019547196 A JP 2019547196A JP 7101694 B2 JP7101694 B2 JP 7101694B2
- Authority
- JP
- Japan
- Prior art keywords
- pharmaceutical composition
- pain
- vancomycin
- poloxamer
- injectable pharmaceutical
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/535—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with at least one nitrogen and one oxygen as the ring hetero atoms, e.g. 1,2-oxazines
- A61K31/5375—1,4-Oxazines, e.g. morpholine
- A61K31/5377—1,4-Oxazines, e.g. morpholine not condensed and containing further heterocyclic rings, e.g. timolol
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K38/00—Medicinal preparations containing peptides
- A61K38/04—Peptides having up to 20 amino acids in a fully defined sequence; Derivatives thereof
- A61K38/14—Peptides containing saccharide radicals; Derivatives thereof, e.g. bleomycin, phleomycin, muramylpeptides or vancomycin
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/06—Organic compounds, e.g. natural or synthetic hydrocarbons, polyolefins, mineral oil, petrolatum or ozokerite
- A61K47/08—Organic compounds, e.g. natural or synthetic hydrocarbons, polyolefins, mineral oil, petrolatum or ozokerite containing oxygen, e.g. ethers, acetals, ketones, quinones, aldehydes, peroxides
- A61K47/10—Alcohols; Phenols; Salts thereof, e.g. glycerol; Polyethylene glycols [PEG]; Poloxamers; PEG/POE alkyl ethers
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/30—Macromolecular organic or inorganic compounds, e.g. inorganic polyphosphates
- A61K47/34—Macromolecular compounds obtained otherwise than by reactions only involving carbon-to-carbon unsaturated bonds, e.g. polyesters, polyamino acids, polysiloxanes, polyphosphazines, copolymers of polyalkylene glycol or poloxamers
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K49/00—Preparations for testing in vivo
- A61K49/04—X-ray contrast preparations
- A61K49/0433—X-ray contrast preparations containing an organic halogenated X-ray contrast-enhancing agent
- A61K49/0438—Organic X-ray contrast-enhancing agent comprising an iodinated group or an iodine atom, e.g. iopamidol
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K49/00—Preparations for testing in vivo
- A61K49/04—X-ray contrast preparations
- A61K49/0433—X-ray contrast preparations containing an organic halogenated X-ray contrast-enhancing agent
- A61K49/0447—Physical forms of mixtures of two different X-ray contrast-enhancing agents, containing at least one X-ray contrast-enhancing agent which is a halogenated organic compound
- A61K49/0457—Semi-solid forms, ointments, gels, hydrogels
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K49/00—Preparations for testing in vivo
- A61K49/04—X-ray contrast preparations
- A61K49/0433—X-ray contrast preparations containing an organic halogenated X-ray contrast-enhancing agent
- A61K49/0447—Physical forms of mixtures of two different X-ray contrast-enhancing agents, containing at least one X-ray contrast-enhancing agent which is a halogenated organic compound
- A61K49/0461—Dispersions, colloids, emulsions or suspensions
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/0012—Galenical forms characterised by the site of application
- A61K9/0019—Injectable compositions; Intramuscular, intravenous, arterial, subcutaneous administration; Compositions to be administered through the skin in an invasive manner
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/0012—Galenical forms characterised by the site of application
- A61K9/0019—Injectable compositions; Intramuscular, intravenous, arterial, subcutaneous administration; Compositions to be administered through the skin in an invasive manner
- A61K9/0024—Solid, semi-solid or solidifying implants, which are implanted or injected in body tissue
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/06—Ointments; Bases therefor; Other semi-solid forms, e.g. creams, sticks, gels
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/08—Solutions
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/14—Particulate form, e.g. powders, Processes for size reducing of pure drugs or the resulting products, Pure drug nanoparticles
- A61K9/141—Intimate drug-carrier mixtures characterised by the carrier, e.g. ordered mixtures, adsorbates, solid solutions, eutectica, co-dried, co-solubilised, co-kneaded, co-milled, co-ground products, co-precipitates, co-evaporates, co-extrudates, co-melts; Drug nanoparticles with adsorbed surface modifiers
- A61K9/146—Intimate drug-carrier mixtures characterised by the carrier, e.g. ordered mixtures, adsorbates, solid solutions, eutectica, co-dried, co-solubilised, co-kneaded, co-milled, co-ground products, co-precipitates, co-evaporates, co-extrudates, co-melts; Drug nanoparticles with adsorbed surface modifiers with organic macromolecular compounds
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61L—METHODS OR APPARATUS FOR STERILISING MATERIALS OR OBJECTS IN GENERAL; DISINFECTION, STERILISATION OR DEODORISATION OF AIR; CHEMICAL ASPECTS OF BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES; MATERIALS FOR BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES
- A61L27/00—Materials for grafts or prostheses or for coating grafts or prostheses
- A61L27/14—Macromolecular materials
- A61L27/18—Macromolecular materials obtained otherwise than by reactions only involving carbon-to-carbon unsaturated bonds
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61L—METHODS OR APPARATUS FOR STERILISING MATERIALS OR OBJECTS IN GENERAL; DISINFECTION, STERILISATION OR DEODORISATION OF AIR; CHEMICAL ASPECTS OF BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES; MATERIALS FOR BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES
- A61L27/00—Materials for grafts or prostheses or for coating grafts or prostheses
- A61L27/50—Materials characterised by their function or physical properties, e.g. injectable or lubricating compositions, shape-memory materials, surface modified materials
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61L—METHODS OR APPARATUS FOR STERILISING MATERIALS OR OBJECTS IN GENERAL; DISINFECTION, STERILISATION OR DEODORISATION OF AIR; CHEMICAL ASPECTS OF BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES; MATERIALS FOR BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES
- A61L27/00—Materials for grafts or prostheses or for coating grafts or prostheses
- A61L27/50—Materials characterised by their function or physical properties, e.g. injectable or lubricating compositions, shape-memory materials, surface modified materials
- A61L27/52—Hydrogels or hydrocolloids
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61L—METHODS OR APPARATUS FOR STERILISING MATERIALS OR OBJECTS IN GENERAL; DISINFECTION, STERILISATION OR DEODORISATION OF AIR; CHEMICAL ASPECTS OF BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES; MATERIALS FOR BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES
- A61L27/00—Materials for grafts or prostheses or for coating grafts or prostheses
- A61L27/50—Materials characterised by their function or physical properties, e.g. injectable or lubricating compositions, shape-memory materials, surface modified materials
- A61L27/54—Biologically active materials, e.g. therapeutic substances
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61L—METHODS OR APPARATUS FOR STERILISING MATERIALS OR OBJECTS IN GENERAL; DISINFECTION, STERILISATION OR DEODORISATION OF AIR; CHEMICAL ASPECTS OF BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES; MATERIALS FOR BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES
- A61L27/00—Materials for grafts or prostheses or for coating grafts or prostheses
- A61L27/50—Materials characterised by their function or physical properties, e.g. injectable or lubricating compositions, shape-memory materials, surface modified materials
- A61L27/58—Materials at least partially resorbable by the body
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/04—Centrally acting analgesics, e.g. opioids
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P29/00—Non-central analgesic, antipyretic or antiinflammatory agents, e.g. antirheumatic agents; Non-steroidal antiinflammatory drugs [NSAID]
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
- A61P31/04—Antibacterial agents
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08L—COMPOSITIONS OF MACROMOLECULAR COMPOUNDS
- C08L71/00—Compositions of polyethers obtained by reactions forming an ether link in the main chain; Compositions of derivatives of such polymers
- C08L71/02—Polyalkylene oxides
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K2300/00—Mixtures or combinations of active ingredients, wherein at least one active ingredient is fully defined in groups A61K31/00 - A61K41/00
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61L—METHODS OR APPARATUS FOR STERILISING MATERIALS OR OBJECTS IN GENERAL; DISINFECTION, STERILISATION OR DEODORISATION OF AIR; CHEMICAL ASPECTS OF BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES; MATERIALS FOR BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES
- A61L2300/00—Biologically active materials used in bandages, wound dressings, absorbent pads or medical devices
- A61L2300/40—Biologically active materials used in bandages, wound dressings, absorbent pads or medical devices characterised by a specific therapeutic activity or mode of action
- A61L2300/404—Biocides, antimicrobial agents, antiseptic agents
- A61L2300/406—Antibiotics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61L—METHODS OR APPARATUS FOR STERILISING MATERIALS OR OBJECTS IN GENERAL; DISINFECTION, STERILISATION OR DEODORISATION OF AIR; CHEMICAL ASPECTS OF BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES; MATERIALS FOR BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES
- A61L2400/00—Materials characterised by their function or physical properties
- A61L2400/06—Flowable or injectable implant compositions
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61L—METHODS OR APPARATUS FOR STERILISING MATERIALS OR OBJECTS IN GENERAL; DISINFECTION, STERILISATION OR DEODORISATION OF AIR; CHEMICAL ASPECTS OF BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES; MATERIALS FOR BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES
- A61L2430/00—Materials or treatment for tissue regeneration
- A61L2430/38—Materials or treatment for tissue regeneration for reconstruction of the spine, vertebrae or intervertebral discs
Landscapes
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Animal Behavior & Ethology (AREA)
- Veterinary Medicine (AREA)
- Public Health (AREA)
- General Health & Medical Sciences (AREA)
- Epidemiology (AREA)
- Medicinal Chemistry (AREA)
- Pharmacology & Pharmacy (AREA)
- Engineering & Computer Science (AREA)
- Dermatology (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Transplantation (AREA)
- Oral & Maxillofacial Surgery (AREA)
- Bioinformatics & Cheminformatics (AREA)
- General Chemical & Material Sciences (AREA)
- Biomedical Technology (AREA)
- Organic Chemistry (AREA)
- Dispersion Chemistry (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Neurosurgery (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Pain & Pain Management (AREA)
- Gastroenterology & Hepatology (AREA)
- Immunology (AREA)
- Oil, Petroleum & Natural Gas (AREA)
- Molecular Biology (AREA)
- Rheumatology (AREA)
- Neurology (AREA)
- Communicable Diseases (AREA)
- Oncology (AREA)
- Inorganic Chemistry (AREA)
- Polymers & Plastics (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
- Medicinal Preparation (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Medicines Containing Antibodies Or Antigens For Use As Internal Diagnostic Agents (AREA)
Description
いくつかの実施形態では、本発明の医薬組成物は、有効量の少なくとも1種の抗生物質を含む。抗生物質は、バンコマイシン及びリネゾリドから選択され得る。一実施形態では、抗生物質は、バンコマイシン塩又は遊離塩基を含むバンコマイシンである。バンコマイシンは、組成物の重量又は体積に基づいて、約1%~約50%で医薬組成物に負荷され得る。いくつかの態様では、バンコマイシンは、組成物の重量又は体積に基づいて、約1%~約30%又は約1%~約20%又は約2.5%~約20%で負荷され得る。一態様では、組成物は、1%(10mg/ml)、2.5%(25mg/ml)、5%(50mg/ml)、10%(100mg/ml)、20%(200mg/ml)又は50%(500mg/ml)のバンコマイシンを負荷され得る。別の実施形態では、抗生物質はリネゾリドである。リネゾリドは、組成物の重量又は体積に基づいて、約1%~50%で医薬組成物に負荷され得る。いくつかの態様では、リネゾリドは、組成物の重量又は体積に基づいて、約1%~約20%又は約2.5%~約20%で負荷され得る。一態様では、組成物は、約1%(10mg/ml)、2.5%(25mg/ml)、5%(50mg/ml)、10%(100mg/ml)、20%(200mg/ml)又は50%(500mg/ml)のリネゾリドを含むことができる。
本発明の医薬組成物及び製剤は、抗生物質構成成分を1種以上の薬学的に許容され得る担体又は賦形剤と組み合わせて含んでおり、疼痛を治療し、予防し、寛解させ又は緩和する。医薬組成物及び製剤は、場合により1種以上の追加の活性物質、例えば治療的及び/又は予防的活性物質を含むことができる。
活性成分
背景技術で記載したように、腰痛は、多くの場合、腰椎椎間板ヘルニア後のモディック変化に密接に関係している。多くの場合、腰椎椎間板ヘルニアの核組織内に嫌気性細菌が認められるため、活性成分としての少なくとも1種の抗生物質を含む本発明の医薬組成物は、腰痛を有する患者、又は腰痛を発症する危険性のある患者に投与され得る。いくつかの実施形態では、治療薬が投与される対象は、骨、関節、靱帯若しくは腱に、又は骨、関節、靱帯若しくは腱の付近に、疼痛を患う又は疼痛を発症する危険性がある。
特定の実施形態では、標的細菌は、プロピオニバウテリウム・アクネス(P.acnes)、コリネバクテリウム・プロピンキウム(Corynebaterium propinquum)又はスタフィロコッカス(Staphylococcus)属のもの等の嫌気性細菌である。
I.コンパニオン薬物
コンパニオン(即ち、組み合わせで提供される薬物)薬物を本発明の活性成分と共に投与することができる。特定の実施形態では、アスピリン、イブプロフェン、ケトプロフェン、ナプロキセン、セファコキシブ、ロフェコキシブ、パレコキシブ、セレコキシブ、バルデコキシブ及びインドメタシン等の抗炎症薬薬物も投与される。特定の実施形態では、アセトアミノフェン、モルヒネ、オキシコドン及びコデイン等の疼痛緩和薬も投与される。コンパニオン薬物は、店頭の疼痛緩和パッチ、薬物及び/又は軟膏も含むことができる。
以前の研究は、バンコマイシン及びリネゾリドを含む抗生物質を封入したポロキサマーを、抗生物質の制御放出及び徐放に使用して、細菌増殖の阻害におけるその有効性を増大させることができることを示しているが(ベイリースら著、インターナショナル・ジャーナル・オブ・ファーマシューティックス、1999年、第192巻(2):p.183~193;ベイリースら著、アンチミクロバイアル・エージェンツ・アンド・ケモセラピー(Antimicrob Agents Chemother.)、2000年、第44巻(4):p.1093~1096;カロレヴィッチら著、ポリマーズ・イン・メディスン、2011年、第41巻(4)p.3~15;及びリーら著、ジャーナル・オブ・コントロール・リリース、2004年、第96巻(1):p.1~7)、これらの以前の研究のいずれも、例えば造影剤等の他の医薬担体の添加による効果を研究していない。本発明で実施した実験では、疾病部位へのその送達を監視するために、バンコマイシン又はリネゾリドを含む製剤に造影剤イオヘキソールを添加することによって、組成物の放射線可視性が増大することが示された。
本発明は、本明細書で論じた抗生物質組成物を疾病部位(1つ又は複数)に投与して、疼痛を治療し、予防し、寛解させ又は緩和し、及び同時に頸椎、胸椎、腰椎又は仙椎における細菌感染を排除する医薬製剤を提供する。製剤は、1種以上の薬学的に許容され得る担体又は賦形剤と組み合わせた抗生物質組成物及び複合体を含むことができる。医薬品の調製及び/又は製造における一般的な留意事項は、例えばレミントン(Remington)著:サイエンス・アンド・プラクティス・オブ・ファーマシー(The Science and Practice of Pharmacy)第21版、リッピンコット・ウィリアムズ・アンド・ウィルキンス(Lippincott Williams & Wilkins)、2005年(その内容は、参照により本明細書に組み込まれる)に見出すことができる。
熱感受性ヒドロゲル
薬物送達に使用される熱感受性ヒドロゲル生体材料。特に、生理学的温度付近の溶液-ゲル転移温度を有する注射用熱感受性ヒドロゲルが有用である。熱感受性ヒドロゲルは、低温(例えば室温)で液体である。インビボでの注射によって、ヒドロゲルは体温で非流動/硬質ゲルを形成した。溶液からゲルへの相転移温度は、下限臨界溶液温度(LCST)と称されている。ゲルは、数時間又は数日で分解する。製剤中の構成成分の濃度を変化させることにより、ゲルのLCST又は分解速度等の特性を微調整することができる。医薬品を組み込んだ後、ヒドロゲルシステムは、その場で持続薬物放出デポーとして機能することができる。注射用熱感受性ヒドロゲルシステムは、薬物調製の単純さ、薬物用の保護環境、長期かつ局所的な薬物送達、及び適用の容易さを含む多数の利点を有する。
医薬製剤は、薬学的に許容され得る賦形剤を更に含むことができ、本明細書で使用される賦形剤は、所望の特定の剤形に適した任意の及び全ての溶媒、分散媒体、希釈剤又は他の液体ビヒクル、分散物又は縣濁補助剤、表面活性剤、等張剤、増粘又は乳化剤、保存剤、固体結合剤、滑沢剤等を含むが、それらに限定されない。医薬組成物を製剤化するための様々な賦形剤、及び組成物を調製するための技術は、当該技術分野で既知である(レミントン著:サイエンス・アンド・プラクティス・オブ・ファーマシー、第21版、A.R.ジェンナーロ(Gennaro)、リッピンコット・ウィリアムズ・アンド・ウィルキンス、ボルチモア(Baltimore)、MD、2006年参照;参照により本明細書に組み込まれる)。任意の従来の賦形剤媒体が、例えば任意の望ましくない生物学的効果を生じる、又は別様に医薬組成物の任意の他の構成成分と有害な方法で相互作用することにより、物質又はその誘導体と適合性を有し得ない場合を除いて、従来の賦形剤媒体の使用が本開示の範囲内で想定され得る。
例示的な顆粒化及び/又は分散剤は、ジャガイモ澱粉、トウモロコシ澱粉、タピオカ澱粉、澱粉グリコール酸ナトリウム、粘土、アルギン酸、グァーガム、シトラスパルプ、寒天、ベントナイト、セルロース及び木製品、天然スポンジ、陽イオン交換樹脂、炭酸カルシウム、ケイ酸塩、炭酸ナトリウム、架橋ポリ(ビニルピロリドン)(クロスポビドン)、カルボキシメチル澱粉ナトリウム(澱粉グリコール酸ナトリウム)、カルボキシメチルセルロース、架橋カルボキシメチルセルロースナトリウム(クロスカルメロースナトリウム)、メチルセルロース、アルファ化澱粉(澱粉1500)、微結晶澱粉、水不溶性澱粉、カルボキシメチルセルロースカルシウム、ケイ酸マグネシウムアルミニウム(ビーガム(VEEGUM)(登録商標))、ラウリル硫酸ナトリウム、第4級アンモニウム化合物等、及び/又はそれらの組み合わせを含むが、それらに限定されない。
製剤
本明細書に記載される医薬組成物の製剤は、既知の方法又は薬学の分野で今後開発される任意の方法により調製することができる。一般に、そのような調製方法は、活性成分をコンジュゲート及び/又は1種以上の他の付属成分と関連させるステップを含む。
いくつかの実施形態では、医薬製剤は、治療的活性薬剤として抗生物質を含むことができる。抗生物質は、β-ラクタム類、オキサゾリジノン、アミノグリコシド、糖ペプチド、リポペプチド、グリシルシクリン、バンコマイシン、リネゾリド、エリスロマイシン、リファンピシン、シプロフロキサシン、フシジン酸、テトラサイクリン、クリンダマイシン、ドキシサイクリン、ミノサイクリン、イミペナム、レボフロキサシン、ガチフロキサシン、モキシフロキサシン、オキシテトラサイクリン、クロラムフェニコール、セフォタキシム、テイコプラニン、オフロキサシン、メトロニダゾール、ホスホマイシン、ピペラシリン、メロペネム、トレゾリド、ラデゾリド、トブラマイシン、レタパムリン、ダプトマイシン、テラバンシン、セフタロリン、セフトビプロ、オリチタバンシン(ortitavancin)、ダルババンシン、テイコプラニン、キヌプリスチン/ダルホプリスチン、ダプトマイシン、セフトビプロール、ダルババンシン、テラバンシン、オリタバンシン、ソリスロマイシン及びイクラプリム又はそれらの組み合わせを含むことができるが、それらに限定されない。いくつかの態様では、抗生物質は、バンコマイシン又はリネゾリドである。
本発明の少なくとも1種の抗生物質を含む医薬組成物及び/又は製剤は、治療的有効な結果をもたらす任意の経路により投与することができる。必要とする正確な量は、対象の種、年齢、及び全体的な状態、疾病の重篤さ、特定の組成物、その投与モード、その活性モード等に応じて、対象によって変動するであろう。
細胞、器官及び組織に対する多数回投与のための当該技術分野で既知の方法及び装置を、本発明の実施形態として本明細書に開示した方法及び組成物に関連して使用することが想定される。これらには、例えば、多数の針を有する方法及び装置、例えばルーメン又はカテーテルを使用するハイブリッド装置、並びに熱、電流又は放射線駆動機構を使用する装置が含まれる。
生体適合性:本明細書で使用されるとき、用語「生体適合性」は、損傷、毒性又は免疫系による拒絶の危険性が殆ど又は全くなく、生細胞、組織、器官又は系と適合性であることを意味する。
生物学的に活性な:本明細書で使用されるとき、表現「生物学的に活性な」は、生物系及び/又は生物内で活性を有する任意の物質の特性を指す。例えば、生物に投与された際、その生物に対して生物学的効果を有する物質は、生物学的に活性であると見なされる。特定の実施形態では、本発明の核酸分子は、核酸分子の一部が生物学的に活性であり、又は生物学的に関連すると考えられる活性を模倣する場合でも、生物学的に活性と見なされ得る。
ヒドロゲル:本明細書で使用されるとき、用語「ヒドロゲル」は、水不溶性の、架橋されたポリマー鎖の3次元ネットワーク及びポリマー鎖間の間隙を満たす水と見なされる。架橋により水不溶性が促進され、必要な機械的強度及び物理的完全性が提供される。ヒドロゲルは殆ど水である(水の質量分率は、ポリマーの質量分率よりも遥かに大きい)。ヒドロゲルがかなりの量の水を保持する能力は、ポリマー鎖が少なくとも中程度の親水性の特性を有する筈であることを示唆している。
患者:本明細書で使用されるとき、用語「患者」は、治療を模索し若しくは治療の必要があり、治療を要求し、治療を受けており、今後治療を受け得る対象、又は特定の疾病若しくは状態のために訓練された専門家によるケアを受けている対象を指す。
薬学的に許容され得る:本明細書で使用されるとき、表現「薬学的に許容され得る」は、健全な医学的判断の範囲内で、過剰な毒性、刺激作用、アレルギー応答又は他の問題又は合併症を有することなく、適切な利益/リスク比に見合って、ヒト及び動物の組織と接触させて使用するのに好適な、化合物、材料、組成物及び/又は剤形を指すように本明細書で使用される。
合成:用語「合成」は、人の手により生成、調製及び/又は製造されることを意味する。
治療する:本明細書で使用されるとき、用語「治療する」は、特定の疾病、疾患及び/又は状態の1つ以上の症状又は特徴を、部分的に又は完全に、軽減し、寛解させ、改善し、緩和し、それらの発症を遅延させ、それらの進行を阻害し、それらの重篤さを低減し、及び/又はそれらの発生率を低減することを指す。例えば、癌を「治療する」は、腫瘍の生存、成長及び/又は伝播を阻害することを指し得る。治療は、疾病、疾患及び/又は状態に関連した病態を発症する危険性を低減する目的で、疾病、疾患及び/若しくは状態の徴候を示さない対象、並びに/又は疾病、疾患及び/若しくは状態の初期徴候のみを示す対象に投与されてもよい。
当業者は、単に日常的な実験を用いて、本発明による本明細書に記載される特定の実施形態の多数の等価物を認識し又は確認することができるであろう。本発明の範囲は、上記の明細書に限定されず、添付の特許請求の範囲に示すように限定されるものとする。
(実施例)
実施例1:スタフィロコッカス・アウレウス(S.aureus)椎間板内感染の羊モデル
スタフィロコッカス・アウレウス(S.aureus)椎間板内感染の羊モデルを開発して、抗生物質製剤のインビボ有効性を試験した。研究開始時におよそ35~40kg+の雄のシャロレー(Charollais)又はサフォーク(Suffolk)交雑羊を、動物科学的処置法(Animal(Scientific Procedure)Act)1986の下で内務省(Home Office)ガイドラインに従って収容し、水へのアクセス下で少なくとも7日間順化させた。これらの羊モデルには、抗生物質を添加していない羊濃厚飼料が給餌され、更に飼料(乾草/麦わら)が提供された。
2.5×106CFU/mlの凍結グリセロール/リン酸緩衝生理食塩水ストックから、2×104CFU/mlに希釈することにより細菌接種材料(ATCC 29213)を調製する:
1.2 注射用製剤の調製
0.2mlの製剤を18G1”又は1.5”針を使用してシリンジ内に引き込む。必要に応じて、シリンジを引き出し及び引き込んで、気泡を除去してもよい。次いで、針を25G4.69”投与針と交換し、0.1mlの用量を残してプライミングする。直ちに使用しない場合、プライミングしたシリンジを冷蔵庫内に放置するが、30分以内に使用する必要がある。
共局所投与
単一の20G3.5”脊椎針を各椎間板の髄核の縁内に直接配置する。針の位置を確認した後、用量溶液をプライミングした第2の25G4.69”針を第1の針内に挿入し、先端を髄核の中央に配置する。第2の針の位置を確認した後、各椎間板に細菌を注射する。次いで内側針を除去する。細菌投与時点から1時間後の直前に、新たな用量溶液をプライミングした新たな25G4.69”針を20G3.5”内に挿入し、髄核の中央に位置付ける。第2の治療は、第1の用量の1時間後に、この針により付与された用量である。
細菌感染:単一の20G3.5”脊椎針を各椎間板の髄核の縁内に直接配置する。針の位置を確認した後、用量溶液をプライミングした第2の25G4.69”針を第1の針内に挿入し、先端を髄核の中央に配置する。第2の針の位置を確認した後、各椎間板に細菌を注射する。次いで針を除去する。動物を脊椎の反対側へのアクセスのために再配置する。
各製剤用量をゆっくり付与するためには、用量溶液をシリンジ/針関節から漏出させることなく、十分な力を用いて用量を連続して首尾よく送達し、送達には30~60秒を必要とする。
1.4 注射技術:予防的投与
注射の順序は、第1の注射が抗生物質の製剤であり、第2の注射が細菌接種材料を含むように逆転されてもよい。抗生物質と細菌の投与間の時間は、数時間、数日、数週間又は数カ月であってもよい。第2の注射は、共局在し又は控えめであってもよく、例えば第1の注射と同じ椎間板側に注射され、又は第1の注射の反対側の椎間板側に注射されてもよい。
各投与の直前及び直後に各羊を撮影して画像を捕捉する。順序の詳細を記録する。適格者により各IVD注射の投与直後の視覚的評価を行う。注射は:良好、漏洩なし;最小限の漏洩;中程度の漏洩;大量の漏洩のいずれかとして採点/記録される。
投与後の設定時点で羊を殺す。注射した椎間板を解体し、髄核を各椎間板から取り出す。加えて、追加の未治療椎間板を採取して、対照組織を提供する。この椎間板は、対照サンプルと治療サンプルとの間にコンタミネーションが存在しないことを確実にするよう注意して、特定の動物の治療椎間板の全ての後に取り出す。
実施例1の羊椎間板内感染モデルを使用して、治療的に投与されたバンコマイシンのインビボ有効性を評価した。結果は、バンコマイシン治療がない場合、椎間板内に注射された1×103CFUのスタフィロコッカス・アウレウス(S.aureus)が、椎間板1グラム当たりおよそ108CFUに増殖したことを示す。0.5%ヒアルロン酸を含むオムニパーク(Omnipaque)(登録商標)中で、200mg/mlバンコマイシン又は50mg/mlバンコマイシンで製剤化されたバンコマイシンは、共局在又は控えめの注射として、感染の1時間後に注射された。
実施例1に記載した予防モデルを使用して、バンコマイシンが細菌の投与前に椎間板全体に拡散する時間を与えられた場合、より有効であるという仮説を試験した。
4.1 材料
この研究に使用した活性化合物及び材料の詳細を、表2に列挙する。
4.2 バンコマイシンヒドロゲル製剤及び製剤の開発
他の箇所で記載された低温方法によりポロキサマーヒドロゲルを調製した(シュモルカ(Schmolka).人工皮膚(Artificial skin).I.熱傷の治療のためのプルロニックF-127ゲルの調製及び特性(Preparation and properties of pluronic F-127 gels for treatment of burns).ジャーナル・オブ・バイオメディカル・マテリアル・リサーチ(Journal of Biomedical Materials Research)、p.571~582、1972年)。バンコマイシン塩酸塩を最終標的濃度50mg/mL、75mg/mL又は100mg/mLでオムニパークに加えた。次いで、薬物溶液をAPIが完全に溶解するまでおよそ2時間撹拌又は超音波処理し、pHを1M HCl及び/又はNaOHでpH6に調整した。次いで、ポロキサマー407(w/w)又はポロキサマー407及びポロキサマー188(w/w)の組み合わせを薬物溶液に加えて所望のポリマー濃度を達成した。澄んだ溶液が得られるまで製剤を72時間冷蔵庫内で保存した。並行して、対照サンプルを調製し、結果をバンコマイシン負荷サンプルと比較した。
調製した製剤の熱可逆性挙動を、異なる温度での管反転法(tube inversion method)により視覚的に評価した。調製したヒドロゲルを収容するバイアルをインキュベータに移動し、温度を2℃/10分の速度で上昇させた。温度の各上昇時に、バイアルをインキュベータから取り出し、反転して液体-ゲル挙動を評価した。
シリンジ通過性及び注射可能性を、25ゲージ、11.91cm(4.69インチ)針に通して、及び注射に必要な圧力/力等のパラメータにより評価し、流れの一様性を以下のように4つのカテゴリーに分類した:1=注射:不可能;流れ:流れなし;2=注射:困難;流れ:一滴ずつ、3=注射:中程度;流れ:連続的;4=注射:容易;流れ:連続的。加えて、各製剤100μlを、針を有し及び有さないシリンジを通してバイアル内に引き込んだ後に重量を比較することにより、用量測定の正確性を確認した。いくつかの場合、暖かいオレンジを使用して25ゲージ、11.91cm(4.69インチ)針を通して注射可能性を評価し、良好、可能又は不可能として分類したことを記す。
以前の作業では、25%及び30%(w/w)のバンコマイシンポロキサマー407製剤のレオロジー特性が臨床的投与を制限し得ることが示唆された。従って、羊注射に好適な25ゲージ、11.91cm(4.69インチ)針を通した椎間板内投与により送達できる、より高い注射可能性/シリンジ通過性特性を有する製剤を開発する必要があった。本明細書に記載される製剤最適化作業では、ポロキサマー188(5%~50%(w/w))を加えた又は加えていない、濃度5%~18%の(w/w)のポロキサマー407を使用した。
5.2 リネゾリドナノ懸濁液製剤
リネゾリド(分子量、337.346g/mol)を抗菌試験薬として選択し、ポロキサマー熱可逆性ヒドロゲルを開発する能力について探究した。リネゾリド負荷50及び200mg/mLを有するナノ懸濁液を開発する能力を評価するために、粒子サイズ、多分散性及び均質性を含む、製剤の短期の物理的安定性を評価した。次いで、異なる濃度のポロキサマー407及び188を加え、ゾル-ゲル転移温度及び注射可能性/シリンジ通過性を評価した。
この作業には、ダイオードアレイ検出器を備えたアジレント(Agilent)1100 HPLCシステムを使用した。サンプルをHPLCアンバーバイアル内に配置し、実験全体を通して室温で保管した。2つの標準(標準A及び標準B)を移動相中で0.1mg/mlで調製し、APIが完全に溶解するまで約45分間超音波処理し、次いで0.22μm PTFEシリンジフィルターで濾過した後、HPLCに注入した。システム適合性試験(SST)を行って、システムの良好な性能を評価した。2つのブランクを注入してベースラインの品質を決定した(即ち、任意のマトリクス干渉を廃棄した)。標準Aを5回注入し、標準Bを2回注入し、両標準に関するピークの平均面積及び%RSDを計算して、注入の併行精度を評価した。最終的に、標準アグリーメントを以下の等式により記載されるように計算した。
表7に示すように、API(50mg/mL及び200mg/mL)を分散媒体に添加し、530RPMで8時間の湿式ボールミルによりナノ懸濁液を生成した。
他の箇所に記載された低温方法によりポロキサマーヒドロゲルを調製した(シュモルカ、ジャーナル・オブ・バイオメディカル・マテリアル・リサーチ、p.571~582、1972年)。ポロキサマー407(w/w)又はポロキサマー407及び188(w/w)の組み合わせを、撹拌下で4℃に保たれた、調製したナノ懸濁液に徐々に加えた。澄んだ溶液が得られるまで製剤を冷蔵庫内に72時間保管した。並行して、対照サンプルを調製し、結果をリネゾリド負荷サンプルと比較した。
調製したリネゾリド製剤の熱可逆性挙動を、異なる温度での管反転法により視覚的に評価した。調製したヒドロゲルを収容するバイアルをインキュベータに移動し、温度を2℃/10分の速度で上昇させた。温度の2℃の各上昇時に、バイアルをインキュベータから取り出し、反転して液体-ゲル挙動を評価した。
シリンジ通過性及び注射可能性を、製剤を閉鎖バイアル内で30分間保管した後、25ゲージ11.91cm(4.69インチ)針に通して評価した。注射に必要な圧力/力等のパラメータ及び流れの一様性を、4つのカテゴリーに分類した:1=注射:不可能;流れ:流れなし;2=注射:困難;流れ:一滴ずつ、3=注射:中程度;流れ:連続的;4=注射:容易;流れ:連続的(表9)。加えて、各製剤100μlを、25ゲージ11.91cm(4.69インチ)針を有し及び有さないシリンジを通してバイアル内に引き込んだ後に重量を比較することにより、用量測定の正確性を確認した。いくつかの場合、暖かいオレンジを使用して25ゲージ、11.91cm(4.69インチ)針を通して注射可能性を評価し、良好、可能又は不可能として分類したことを留意する必要がある。
社会科学ソフトウエアの統計パッケージ(SPSsバージョン16.0、SPSS社、シカゴ、USA)を使用して統計評価を行った。全データをスチューデントのt検定により分析した。p<0.05の場合に、統計的に有意な差異を規定した。値は平均±標準偏差(SD)n=3として表した。
管反転法は、プラセボポロキサマー407製剤が熱可逆性特性を示し、ゾル-ゲル転移温度30℃で、濃度20%(w/w)で、液体から半固体ゲルに転移することを示した。一方、濃度20%(w/w)未満の製剤は、逆転熱ゲル化を示さず、22℃~36℃で液体又は粘稠液体として挙動した(表9)。データはリネゾリドの添加によりポロキサマー407製剤のゾル-ゲル転移温度が低下することを示唆する(例えば、対照16%ポロキサマー407、対、16%ポロキサマー407+50mg/mLリネゾリド)。
リネゾリドは、中程度の水溶性を有し、殆どの製剤中でマイクロ/ナノ結晶のサスペンス(suspense)を形成する。異なる賦形剤を、それらのリネゾリドの可溶化能力に関してスクリーニングする。多様な賦形剤の存在下、リネゾリド結晶形II及びIIIの可溶性を水中で試験した。リネゾリド(約10mg/mlロット)を賦形剤に加え、溶液に溶解させた。澄んだ溶液が得られた場合、リネゾリドの他のロットを加えた。この工程は飽和溶液が得られるまで継続した。溶液を濾過し、定量HPLC-UVアッセイを用いて可溶性リネゾリドの品質を見積もった。加えたリネゾリドの質量と、可溶性リネゾリド濃度を下記の表11に示す。目標は>50mg/ml可溶性リネゾリドを達成することであった。賦形剤スクリーニングにより、クレプトース(Kleptose)、キャプティソール(Captisol)、PEG300及びPEG400が最も高い可溶性を有する賦形剤であることが特定された。50%オムニパーク(w/v)溶液中のクレプトース(登録商標)及びキャプティソール(登録商標)(20及び30%w/v)に関する37℃での可溶性を表12に示す。キャプティソール(登録商標)20%及び30%w/v溶液は、各々およそ30及び40mg/mLで飽和した。クレプトース(登録商標)20及び30%w/vは、これまでの所、各々40及び50mg/mLで、両方の形態に関してより高い可溶性を示した。特に、30%クレプトース(w/v)は、50%オムニパーク(v/v)中で目標>50mg/mlまでリネゾリドを可溶化することができる。
リネゾリド、クレプトース又はキャプトソール(Captosol)、オムニパーク及びポロキサマー407を含む熱感受性ヒドロゲル製剤を調製し、好適なゾル-ゲル転移に関して試験する。実施例6に記載した低温方法を用いて、ポロキサマー407又はポロキサマー407及び188の組み合わせのヒドロゲルを調製する。濃度20%~30%のクレプトース又はキャプティソールをポロキサマー溶液に加える。クレプトース又はキャプティソールを含む溶液にリネゾリド結晶(例えば、II型及びIII型)を、リネゾリドが溶液に完全に溶解するまで加える。製剤を澄んだ溶液が得られるまで冷蔵庫内に72時間保管し、又は代替的に数時間以内の溶解を可能にするよう高せん断を用いて急速に混合してもよい。並行して、対照サンプルを調製し、結果をリネゾリド負荷サンプルと比較する。
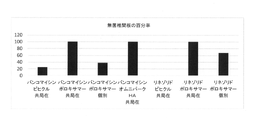
100マイクロリットルのポロキサマー製剤を寒天円板内に埋め込んだ。寒天構造の周囲の媒体中への負荷化合物の放出を測定する。このアッセイはポロキサマー注射を含む椎間板を模倣する。高速液体クロマトグラフィー(HPLC)を用いて、72時間に亘り放出された抗生物質の質量を決定した。図2に示すように、72時間後に92%のバンコマイシン投与量(灰色)及び57%のリネゾリド投与量(黒色)が計上された。リネゾリドの溶解及び続く拡散は、この製剤における中程度の徐放の要素に寄与し得る。
ヒドロゲルの注射可能性をインビトロ及びエクスビボの両方で決定して、ヒドロゲルがインビボ評価に好適であることを確認した。冷蔵庫での保管から取り出した後、バンコマイシン及びリネゾリド製剤の両方は室温で3時間まで、液体及び注射可能の状態に留まる。
治療的投与を伴う実施例1のスタフィロコッカス・アウレウス(S.aureus)脊椎円板感染モデルをこの研究に使用した。
(付記)
好ましい実施形態として、上記実施形態から把握できる技術的思想について、以下に記載する。
[項目1]
(a)有効量の抗生物質;
(b)熱感受性ヒドロゲル;
(c)放射線造影剤;
(d)少なくとも1種の薬学的に許容され得る賦形剤を含む、腰痛を緩和及び/又は治療するための注射用医薬組成物。
[項目2]
前記熱感受性ヒドロゲルが、生分解性及び生体適合性ポリマーから構成されている、項目1に記載の注射用医薬組成物。
[項目3]
前記ポリマーがポロキサマーである、項目2に記載の注射用医薬組成物。
[項目4]
前記ポロキサマーがポロキサマー407であり、前記ポロキサマー407は、前記組成物の重量又は体積に基づいて、約2%~約20%存在する、項目3に記載の注射用医薬組成物。
[項目5]
更にポロキサマー188を含み、前記ポロキサマー188は、前記組成物の約5重量%~約20重量%存在する、項目4に記載の注射用医薬組成物。
[項目6]
前記組成物が、約4℃~約25℃の温度で水溶液である、項目1~5のいずれか一項に記載の注射用医薬組成物。
[項目7]
前記水溶液が、約32℃~約38の温度でゲル化する、項目6に記載の注射用医薬組成物。
[項目8]
前記水溶液が、室温で少なくとも3時間残存する、項目6又は7に記載の注射用医薬組成物。
[項目9]
前記抗生物質が、バンコマイシン及びリネゾリドから選択される、項目1~8のいずれか一項に記載の注射用医薬組成物。
[項目10]
前記抗生物質がリネゾリドである、項目9に記載の注射用医薬組成物。
[項目11]
前記抗生物質がバンコマイシンである、項目9に記載の注射用医薬組成物。
[項目12]
前記組成物が、前記組成物の重量又は体積に基づいて、15%~35%の濃度のシクロデキストリンを更に含む、項目10に記載の注射用医薬組成物。
[項目13]
リネゾリドの濃度が、前記組成物の重量又は体積に基づいて、約1%~約20%である、項目10又は12に記載の注射用医薬組成物。
[項目14]
バンコマイシンの濃度が、前記組成物の重量又は体積に基づいて、約1%~約30である、項目11に記載の注射用医薬組成物。
[項目15]
前記組成物が、総用量1mg~200mgのリネゾリドを含む、項目10又は12に記載の注射用医薬組成物。
[項目16]
前記組成物が、総用量1mg~600mgのバンコマイシンを含む、項目11に記載の注射用医薬組成物。
[項目17]
前記造影剤が、イオヘキソール、イオパミドール、イオキシラン、イオプロミド、イオジキサノール、イオベルソール、ジアトリゾエート、メトリゾエート、イオキサグレート等からなる群から選択される、項目1~16のいずれか一項に記載の注射用医薬組成物。
[項目18]
前記注射用医薬組成物が、脊椎に関連した骨、関節、靱帯又は腱への投与のために製剤化されている、項目1~17のいずれか一項に記載の注射用医薬組成物。
[項目19]
前記脊椎に関連した前記骨、関節、靱帯又は腱が、頸椎、胸椎、腰椎又は仙椎に関連している、項目18に記載の注射用医薬組成物。
[項目20]
項目1~19のいずれか一項に記載の注射用医薬組成物を投与することを含む、対象における疼痛の治療又は予防方法。
[項目21]
前記疼痛が、急性疼痛、亜急性疼痛、慢性疼痛、局所疼痛、神経根疼痛又は関連痛である、項目20に記載の方法。
[項目22]
前記疼痛が、腰痛又は頸部痛である、項目21に記載の方法。
[項目23]
前記腰痛又は頸部痛が、モディック変化又は骨浮腫に関連している、項目22に記載の方法。
[項目24]
前記対象が、以前に椎間板ヘルニアを有する、項目23に記載の方法。
[項目25]
前記対象が、細菌感染が疑われる又は細菌感染を有する、項目20~24のいずれか一項に記載の方法。
[項目26]
前記注射用医薬組成物が、椎間板、椎間腔、関節内腔、靱帯、腱、腱及び骨接合部、又は骨浮腫に隣接した部位内に注射される、項目20~25のいずれか一項に記載の方法。
[項目27]
前記注射用医薬組成物が、モディック変化若しくは骨浮腫の部位に隣接して、又は前記部位内に注射される、項目20~25のいずれか一項に記載の方法。
[項目28]
対象における疼痛の緩和又は寛解と、前記対象の頸椎、胸椎、腰椎又は仙椎における細菌感染の排除とを同時に行う方法であって、項目1~19のいずれか一項に記載の注射用医薬組成物を、感染した椎骨内、椎骨の付近、又は椎骨の周囲の領域に注射により投与することを含む、方法。
Claims (21)
- 腰痛を緩和及び/又は治療するための注射用医薬組成物であって、
(a)バンコマイシン及びリネゾリドから選択される有効量の抗生物質;
(b)ポロキサマー407からなる熱感受性ヒドロゲルであって、前記ポロキサマー407が、前記組成物の重量又は体積に基づいて、2%~20%存在する熱感受性ヒドロゲル;
(c)非イオン性放射線造影剤イオヘキソール;及び
(d)少なくとも1種の薬学的に許容され得る賦形剤
を含む、注射用医薬組成物。 - 更にポロキサマー188を含み、前記ポロキサマー188は、前記組成物の5重量%~20重量%存在する、請求項1に記載の注射用医薬組成物。
- 前記組成物が、約4℃~約25℃の温度で、注射可能な水溶液の状態である、請求項1又は2に記載の注射用医薬組成物。
- 前記組成物が、約32℃~約38℃の温度で、ゲルである、請求項3に記載の注射用医薬組成物。
- 前記組成物が、冷蔵庫での保管から取り出した後、室温で少なくとも3時間、前記注射可能な水溶液の状態に留まる、請求項3又は4に記載の注射用医薬組成物。
- 前記抗生物質がリネゾリドであり、
前記組成物が、前記組成物の重量又は体積に基づいて、15%~35%の濃度のシクロデキストリンを更に含む、請求項1に記載の注射用医薬組成物。 - リネゾリドの濃度が、前記組成物の重量又は体積に基づいて、約1%~約20%である、請求項6に記載の注射用医薬組成物。
- 前記抗生物質がバンコマイシンであり、バンコマイシンの濃度が、前記組成物の重量又は体積に基づいて、約1%~約30である、請求項1~5のいずれか一項に記載の注射用医薬組成物。
- 前記組成物が、総用量1mg~200mgのリネゾリドを含む、請求項6に記載の注射用医薬組成物。
- 前記組成物が、総用量1mg~600mgのバンコマイシンを含む、請求項8に記載の注射用医薬組成物。
- 前記注射用医薬組成物が、脊椎に関連した骨、関節、靱帯又は腱への投与のために製剤化されている、請求項1~10のいずれか一項に記載の注射用医薬組成物。
- 前記脊椎に関連した前記骨、関節、靱帯又は腱が、頸椎、胸椎、腰椎又は仙椎に関連している、請求項11に記載の注射用医薬組成物。
- 対象における疼痛の治療又は予防に使用するための請求項1~12のいずれか一項に記載の注射用医薬組成物。
- 前記疼痛が、急性疼痛、亜急性疼痛、慢性疼痛、局所疼痛、神経根疼痛又は関連痛である、請求項13に記載の注射用医薬組成物。
- 前記疼痛が、腰痛又は頸部痛である、請求項14に記載の注射用医薬組成物。
- 前記腰痛又は頸部痛が、モディック変化又は骨浮腫に関連している、請求項15に記載の注射用医薬組成物。
- 前記対象が、以前に椎間板ヘルニアを有する、請求項16に記載の注射用医薬組成物。
- 前記対象が、細菌感染が疑われる又は細菌感染を有する、請求項13~17のいずれか一項に記載の注射用医薬組成物。
- 前記注射用医薬組成物が、椎間板、椎間腔、関節内腔、靱帯、腱、腱及び骨接合部、又は骨浮腫に隣接した部位内に注射される、請求項13~18のいずれか一項に記載の注射用医薬組成物。
- 前記注射用医薬組成物が、モディック変化若しくは骨浮腫の部位に隣接して、又は前記部位内に注射される、請求項13~19のいずれか一項に記載の注射用医薬組成物。
- 対象における疼痛の緩和又は寛解と、前記対象の頸椎、胸椎、腰椎又は仙椎における細菌感染の排除とを同時に行う方法に使用するための注射用医薬組成物であって、感染した椎骨内、椎骨の付近、又は椎骨の周囲の領域に注射により投与される、請求項1~12のいずれか一項に記載の注射用医薬組成物。
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2022108095A JP7418858B2 (ja) | 2016-11-16 | 2022-07-05 | 腰痛のための抗生物質製剤 |
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US201662423112P | 2016-11-16 | 2016-11-16 | |
| US62/423,112 | 2016-11-16 | ||
| PCT/GB2017/053447 WO2018091895A1 (en) | 2016-11-16 | 2017-11-16 | Antibiotic formulations for lower back pain |
Related Child Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2022108095A Division JP7418858B2 (ja) | 2016-11-16 | 2022-07-05 | 腰痛のための抗生物質製剤 |
Publications (3)
| Publication Number | Publication Date |
|---|---|
| JP2020500221A JP2020500221A (ja) | 2020-01-09 |
| JP2020500221A5 JP2020500221A5 (ja) | 2021-01-07 |
| JP7101694B2 true JP7101694B2 (ja) | 2022-07-15 |
Family
ID=60582616
Family Applications (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2019547196A Active JP7101694B2 (ja) | 2016-11-16 | 2017-11-16 | 腰痛のための抗生物質製剤 |
| JP2022108095A Active JP7418858B2 (ja) | 2016-11-16 | 2022-07-05 | 腰痛のための抗生物質製剤 |
Family Applications After (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2022108095A Active JP7418858B2 (ja) | 2016-11-16 | 2022-07-05 | 腰痛のための抗生物質製剤 |
Country Status (8)
| Country | Link |
|---|---|
| US (3) | US20190343761A1 (ja) |
| EP (2) | EP3998092B1 (ja) |
| JP (2) | JP7101694B2 (ja) |
| KR (1) | KR102615354B1 (ja) |
| CN (2) | CN109982729B (ja) |
| DK (1) | DK3541442T3 (ja) |
| ES (1) | ES2909236T3 (ja) |
| WO (1) | WO2018091895A1 (ja) |
Cited By (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2021503462A (ja) * | 2017-11-16 | 2021-02-12 | ペルシカ ファーマシューティカルズ リミテッドPersica Pharmaceuticals Ltd. | リネゾリド製剤 |
| JP7418858B2 (ja) | 2016-11-16 | 2024-01-22 | ペルシカ ファーマシューティカルズ リミテッド | 腰痛のための抗生物質製剤 |
Families Citing this family (7)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| USRE48948E1 (en) | 2008-04-18 | 2022-03-01 | Warsaw Orthopedic, Inc. | Clonidine compounds in a biodegradable polymer |
| EP3679928A1 (fr) * | 2019-01-08 | 2020-07-15 | Atlangram | Composition pharmaceutique de type gel pour traiter/prevenir une infection |
| WO2021191903A1 (en) * | 2020-03-26 | 2021-09-30 | Bone Sci. Bio Ltd. | Pharmaceutical compositions comprising amphiphilic peptides and methods of use thereof |
| CN111467302A (zh) * | 2020-04-13 | 2020-07-31 | 徐州医科大学 | 一种可诱导局部亚低温治疗颅脑外伤的可注射温度敏感性制冷水凝胶 |
| US20240032965A1 (en) * | 2020-11-24 | 2024-02-01 | Discgenics, Inc. | Methods and systems for treatment of intervertebral disc by intradiscal micro-needle insertion |
| CN112957333B (zh) * | 2021-02-05 | 2022-11-22 | 海南通用康力制药有限公司 | 注射用磷酸特地唑胺及其制备方法 |
| WO2024069049A1 (en) * | 2022-09-26 | 2024-04-04 | Desentum Oy | Thermosensitive hydrogel composition |
Citations (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2009538285A (ja) | 2006-05-26 | 2009-11-05 | バクスター・インターナショナル・インコーポレイテッド | 骨造成のための注射用フィブリン組成物 |
| JP2013508116A (ja) | 2009-10-27 | 2013-03-07 | スパイン ウェイブ,インコーポレーテッド | 放射線不透過性の注入可能核ヒドロゲル組成物 |
| JP2013508381A (ja) | 2009-10-21 | 2013-03-07 | オトノミ―,インク. | ポロクサマーを包含する製剤のゲル化温度の調節 |
| JP2016533354A (ja) | 2013-10-21 | 2016-10-27 | メーロ エス.アール.エル. | 腰痛治療のための抗菌剤を含有する生体再吸収性組成物 |
Family Cites Families (26)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US5628734A (en) | 1995-03-23 | 1997-05-13 | Hatfalvi; Bela I. | Spinal needle with curved distal end and method of using said needle in a spinal injection to prevent post dural puncture headache |
| US5702717A (en) | 1995-10-25 | 1997-12-30 | Macromed, Inc. | Thermosensitive biodegradable polymers based on poly(ether-ester)block copolymers |
| HUP0200915A3 (en) * | 1996-11-21 | 2002-10-28 | Du Pont | Production of vegetable gels |
| SE515072C2 (sv) | 1999-07-09 | 2001-06-05 | Reachin Technologies Ab | Haptisk återgivning av komplexa grafiska miljöer |
| US6500153B1 (en) | 2001-07-13 | 2002-12-31 | Children's And Women's Health Centre Of British Columbia | Syringe and needle for preventing inadvertent drug injection |
| KR100517643B1 (ko) | 2003-07-25 | 2005-09-28 | 한국과학기술연구원 | 온도 감응성 폴리포스파젠계 고분자, 이의 제조방법 및이를 이용한 주입형 온도 감응성 폴리포스파젠 하이드로젤 |
| WO2005032650A1 (en) | 2003-10-03 | 2005-04-14 | Medtronic, Inc. | Kit for implantation of therapy elements |
| US7367961B2 (en) | 2004-09-10 | 2008-05-06 | Depuy Spine, Inc. | Intradiscal injection of autologous interferon |
| US7850656B2 (en) | 2005-04-29 | 2010-12-14 | Warsaw Orthopedic, Inc. | Devices and methods for delivering medical agents |
| KR100784485B1 (ko) | 2006-01-18 | 2007-12-11 | 한국과학기술연구원 | 생분해성 온도 감응성 폴리포스파젠계 하이드로젤, 그의제조방법 및 그의 용도 |
| JP5839189B2 (ja) * | 2008-07-21 | 2016-01-06 | オトノミ—,インク. | 耳の不調の治療用の制御放出性の抗菌性組成物および方法 |
| KR101001855B1 (ko) | 2008-10-22 | 2010-12-17 | 한국과학기술연구원 | 생분해성 및 생체친화성이 우수한 조직재생용 주입형 온도감응성 플루로닉 유도체 하이드로겔 및 이의 제조방법 |
| US20120277199A1 (en) * | 2009-10-21 | 2012-11-01 | Otonomy, Inc. | Modulation of Gel Temperature of Poloxamer-Containing Formulations |
| EP2343046A1 (en) | 2010-01-08 | 2011-07-13 | Nirvana's Tree House B.V. | Functionalised triblock copolymers and compositions containing such polymers |
| LT2658525T (lt) | 2010-12-29 | 2017-12-11 | Medincell | Biologiškai skaidomos vaistų tiekimo kompozicijos |
| CA2852068A1 (en) * | 2011-10-12 | 2013-04-18 | Derek OVERSTREET | In situ forming hydrogel and method using same |
| TWI473627B (zh) | 2012-02-17 | 2015-02-21 | Taipei Veterans General Hospital | 用於幹細胞療法注射傳輸系統的雙性幾丁質奈米膠 |
| CN103126973B (zh) * | 2013-02-01 | 2015-02-18 | 安徽四正医药科技有限公司 | 用于血管瘤治疗的多糖水凝胶液体栓塞剂及其制备方法 |
| US9789073B2 (en) | 2013-03-14 | 2017-10-17 | Pathak Holdings, Llc | Compositions, methods and devices for local drug delivery |
| US10682415B2 (en) | 2013-07-22 | 2020-06-16 | Wisconsin Alumni Research Foundation | Thermogel formulation for combination drug delivery |
| MX2016000964A (es) | 2013-07-22 | 2016-08-03 | Imprimis Pharmaceuticals Inc | Composiciones farmaceuticas para la administracion intraocular que comprenden un agente antibacteriano y un agente antiinflamatorio. |
| EP3052528B1 (en) | 2013-10-02 | 2017-11-22 | AO Technology AG | Thermosensitive hyaluronic acid conjugates and methods for the preparation thereof |
| US20160287710A1 (en) | 2013-11-12 | 2016-10-06 | Margit Maria JANAT-AMSBURY | Glycol chitin based thermosensitive hydrogel for vaginal delivery of progesterone |
| CN105744969B (zh) * | 2014-01-31 | 2019-12-31 | 雪松-西奈医学中心 | 用于最优主动脉瓣膜复合体成像和对准的猪尾装置 |
| US9364545B2 (en) | 2014-06-19 | 2016-06-14 | Taipei Medical University | Thermosensitive injectable hydrogel for drug delivery |
| JP7101694B2 (ja) * | 2016-11-16 | 2022-07-15 | ペルシカ ファーマシューティカルズ リミテッド | 腰痛のための抗生物質製剤 |
-
2017
- 2017-11-16 JP JP2019547196A patent/JP7101694B2/ja active Active
- 2017-11-16 DK DK17809337.3T patent/DK3541442T3/da active
- 2017-11-16 CN CN201780070772.4A patent/CN109982729B/zh active Active
- 2017-11-16 WO PCT/GB2017/053447 patent/WO2018091895A1/en unknown
- 2017-11-16 ES ES17809337T patent/ES2909236T3/es active Active
- 2017-11-16 EP EP21215487.6A patent/EP3998092B1/en active Active
- 2017-11-16 EP EP17809337.3A patent/EP3541442B1/en active Active
- 2017-11-16 KR KR1020197014015A patent/KR102615354B1/ko active IP Right Grant
- 2017-11-16 US US16/461,434 patent/US20190343761A1/en not_active Abandoned
- 2017-11-16 CN CN202210363334.XA patent/CN114712303A/zh active Pending
-
2021
- 2021-01-06 US US17/142,559 patent/US20210128454A1/en not_active Abandoned
-
2022
- 2022-07-05 JP JP2022108095A patent/JP7418858B2/ja active Active
- 2022-10-19 US US17/969,554 patent/US20230149297A1/en active Pending
Patent Citations (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2009538285A (ja) | 2006-05-26 | 2009-11-05 | バクスター・インターナショナル・インコーポレイテッド | 骨造成のための注射用フィブリン組成物 |
| JP2013508381A (ja) | 2009-10-21 | 2013-03-07 | オトノミ―,インク. | ポロクサマーを包含する製剤のゲル化温度の調節 |
| JP2013508116A (ja) | 2009-10-27 | 2013-03-07 | スパイン ウェイブ,インコーポレーテッド | 放射線不透過性の注入可能核ヒドロゲル組成物 |
| JP2016533354A (ja) | 2013-10-21 | 2016-10-27 | メーロ エス.アール.エル. | 腰痛治療のための抗菌剤を含有する生体再吸収性組成物 |
Non-Patent Citations (1)
| Title |
|---|
| Journal of biomedical materials research. Part A,2010年,Vol. 92, No. 1, pp. 378-85. |
Cited By (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP7418858B2 (ja) | 2016-11-16 | 2024-01-22 | ペルシカ ファーマシューティカルズ リミテッド | 腰痛のための抗生物質製剤 |
| JP2021503462A (ja) * | 2017-11-16 | 2021-02-12 | ペルシカ ファーマシューティカルズ リミテッドPersica Pharmaceuticals Ltd. | リネゾリド製剤 |
| JP7251813B2 (ja) | 2017-11-16 | 2023-04-04 | ペルシカ ファーマシューティカルズ リミテッド | リネゾリド製剤 |
Also Published As
| Publication number | Publication date |
|---|---|
| ES2909236T3 (es) | 2022-05-05 |
| JP7418858B2 (ja) | 2024-01-22 |
| DK3541442T3 (da) | 2022-03-14 |
| US20210128454A1 (en) | 2021-05-06 |
| JP2022133382A (ja) | 2022-09-13 |
| KR20190084979A (ko) | 2019-07-17 |
| CN109982729A (zh) | 2019-07-05 |
| US20230149297A1 (en) | 2023-05-18 |
| EP3998092C0 (en) | 2024-02-14 |
| CN109982729B (zh) | 2022-04-22 |
| WO2018091895A1 (en) | 2018-05-24 |
| CN114712303A (zh) | 2022-07-08 |
| EP3541442B1 (en) | 2022-01-19 |
| US20190343761A1 (en) | 2019-11-14 |
| JP2020500221A (ja) | 2020-01-09 |
| EP3541442A1 (en) | 2019-09-25 |
| EP3998092A1 (en) | 2022-05-18 |
| EP3998092B1 (en) | 2024-02-14 |
| KR102615354B1 (ko) | 2023-12-21 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP7101694B2 (ja) | 腰痛のための抗生物質製剤 | |
| Tao et al. | Injectable chitosan-based thermosensitive hydrogel/nanoparticle-loaded system for local delivery of vancomycin in the treatment of osteomyelitis | |
| Zakaria et al. | Newly developed topical cefotaxime sodium hydrogels: antibacterial activity and in vivo evaluation | |
| AU2016213722A1 (en) | Solid dispersion of rifaximin | |
| US20230143410A1 (en) | Linezolid formulations | |
| Gao et al. | Evaluating accessibility of intravenously administered nanoparticles at the lesion site in rat and pig contusion models of spinal cord injury | |
| Phipps et al. | Intraosseous delivery of bone morphogenic protein-2 using a self-assembling peptide hydrogel | |
| Rudnik-Jansen et al. | Safety of intradiscal delivery of triamcinolone acetonide by a poly (esteramide) microsphere platform in a large animal model of intervertebral disc degeneration | |
| JP6813357B2 (ja) | 薬物送達システム | |
| TWI835758B (zh) | 利奈唑胺(linezolid)調合物 | |
| Kamel et al. | Injectable hydrogel scaffolds composed of Nanocellulose derived from sugarcane bagasse and combined with calcium for Bone regeneration | |
| Rastogi et al. | Evaluation of a perforated drug delivery system in mice for prolonged and constant release of a hydrophilic drug | |
| US20180311376A1 (en) | A Medical Composition and a Medical Hydrogel for Use in the Prevention and/or Treatment of a Disease of the Facet Joints and/or for Use in the Replacement and/or Regeneration of Articular Facets | |
| Florczyk et al. | Innovative Vancomycin-Loaded Hydrogel-Based Systems–New Opportunities for the Antibiotic Therapy | |
| WO2023062080A1 (en) | Low back pain treatment | |
| Ranjan et al. | Osteomyelitis: Therapeutic Management using Nanomedicines | |
| KR20220003551A (ko) | 스타틴 및 히알루론산 유도체를 포함하는 약학적 조성물 | |
| Zakaria et al. | Research Article Newly Developed Topical Cefotaxime Sodium Hydrogels: Antibacterial Activity and In Vivo Evaluation |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20201113 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20201113 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20211207 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20220221 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20220607 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20220705 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 7101694 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |