JP7036723B2 - 眼疾患の処置のための組成物および方法 - Google Patents
眼疾患の処置のための組成物および方法 Download PDFInfo
- Publication number
- JP7036723B2 JP7036723B2 JP2018529249A JP2018529249A JP7036723B2 JP 7036723 B2 JP7036723 B2 JP 7036723B2 JP 2018529249 A JP2018529249 A JP 2018529249A JP 2018529249 A JP2018529249 A JP 2018529249A JP 7036723 B2 JP7036723 B2 JP 7036723B2
- Authority
- JP
- Japan
- Prior art keywords
- mrna
- seq
- intron
- aso
- protein
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N15/00—Mutation or genetic engineering; DNA or RNA concerning genetic engineering, vectors, e.g. plasmids, or their isolation, preparation or purification; Use of hosts therefor
- C12N15/09—Recombinant DNA-technology
- C12N15/11—DNA or RNA fragments; Modified forms thereof; Non-coding nucleic acids having a biological activity
- C12N15/113—Non-coding nucleic acids modulating the expression of genes, e.g. antisense oligonucleotides; Antisense DNA or RNA; Triplex- forming oligonucleotides; Catalytic nucleic acids, e.g. ribozymes; Nucleic acids used in co-suppression or gene silencing
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P27/00—Drugs for disorders of the senses
- A61P27/02—Ophthalmic agents
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N15/00—Mutation or genetic engineering; DNA or RNA concerning genetic engineering, vectors, e.g. plasmids, or their isolation, preparation or purification; Use of hosts therefor
- C12N15/09—Recombinant DNA-technology
- C12N15/11—DNA or RNA fragments; Modified forms thereof; Non-coding nucleic acids having a biological activity
- C12N15/111—General methods applicable to biologically active non-coding nucleic acids
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N15/00—Mutation or genetic engineering; DNA or RNA concerning genetic engineering, vectors, e.g. plasmids, or their isolation, preparation or purification; Use of hosts therefor
- C12N15/09—Recombinant DNA-technology
- C12N15/11—DNA or RNA fragments; Modified forms thereof; Non-coding nucleic acids having a biological activity
- C12N15/113—Non-coding nucleic acids modulating the expression of genes, e.g. antisense oligonucleotides; Antisense DNA or RNA; Triplex- forming oligonucleotides; Catalytic nucleic acids, e.g. ribozymes; Nucleic acids used in co-suppression or gene silencing
- C12N15/1138—Non-coding nucleic acids modulating the expression of genes, e.g. antisense oligonucleotides; Antisense DNA or RNA; Triplex- forming oligonucleotides; Catalytic nucleic acids, e.g. ribozymes; Nucleic acids used in co-suppression or gene silencing against receptors or cell surface proteins
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2310/00—Structure or type of the nucleic acid
- C12N2310/10—Type of nucleic acid
- C12N2310/11—Antisense
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2310/00—Structure or type of the nucleic acid
- C12N2310/30—Chemical structure
- C12N2310/31—Chemical structure of the backbone
- C12N2310/315—Phosphorothioates
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2310/00—Structure or type of the nucleic acid
- C12N2310/30—Chemical structure
- C12N2310/32—Chemical structure of the sugar
- C12N2310/321—2'-O-R Modification
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2320/00—Applications; Uses
- C12N2320/30—Special therapeutic applications
- C12N2320/33—Alteration of splicing
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12Q—MEASURING OR TESTING PROCESSES INVOLVING ENZYMES, NUCLEIC ACIDS OR MICROORGANISMS; COMPOSITIONS OR TEST PAPERS THEREFOR; PROCESSES OF PREPARING SUCH COMPOSITIONS; CONDITION-RESPONSIVE CONTROL IN MICROBIOLOGICAL OR ENZYMOLOGICAL PROCESSES
- C12Q1/00—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions
- C12Q1/68—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions involving nucleic acids
- C12Q1/6876—Nucleic acid products used in the analysis of nucleic acids, e.g. primers or probes
- C12Q1/6883—Nucleic acid products used in the analysis of nucleic acids, e.g. primers or probes for diseases caused by alterations of genetic material
Landscapes
- Health & Medical Sciences (AREA)
- Engineering & Computer Science (AREA)
- Life Sciences & Earth Sciences (AREA)
- Genetics & Genomics (AREA)
- Biomedical Technology (AREA)
- Organic Chemistry (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Chemical & Material Sciences (AREA)
- Zoology (AREA)
- Molecular Biology (AREA)
- Biotechnology (AREA)
- General Engineering & Computer Science (AREA)
- Wood Science & Technology (AREA)
- General Health & Medical Sciences (AREA)
- Biophysics (AREA)
- Microbiology (AREA)
- Biochemistry (AREA)
- Plant Pathology (AREA)
- Physics & Mathematics (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Chemical Kinetics & Catalysis (AREA)
- General Chemical & Material Sciences (AREA)
- Medicinal Chemistry (AREA)
- Ophthalmology & Optometry (AREA)
- Pharmacology & Pharmacy (AREA)
- Animal Behavior & Ethology (AREA)
- Public Health (AREA)
- Veterinary Medicine (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Micro-Organisms Or Cultivation Processes Thereof (AREA)
Description
本出願は、2015年12月14日出願の米国仮特許出願第62/267,259号、および2016年4月6日出願の米国仮特許出願第62/318,958号の利益を主張するものであり、該出願は全体として参照によって本明細書に組み込まれる。
本出願は配列表を包含しており、これは、EFS-Webを介してASCIIフォーマットで提出され、その全体が引用により本明細書に組み込まれる。2016年12月12日に作成されたASCIIのコピーは、47991-713_601_SL.txtのファイル名であり、15,418,644バイトのサイズである。
NO28、(e)SEQ ID NO29、(f)SEQ ID NO30あるいはSEQ ID NO31、(g)SEQ ID NO 32あるいはSEQ ID NO 33、(h)SEQ ID NO 34、SEQ ID NO 35、SEQ ID NO 36、あるいはSEQ ID NO 37、(i)SEQ ID NO 38、SEQ ID NO 39、あるいはSEQ ID NO 40、(j)SEQ ID NO 41、(k)SEQ ID NO 42、SEQ ID NO 43、SEQ ID NO 44、SEQ ID NO 45、SEQ ID NO 46、SEQ ID NO 47、SEQ ID NO 48、SEQ ID NO 49、SEQ ID NO 50、SEQ ID NO 51、あるいはSEQ ID NO 52、(l)SEQ ID NO 53、(m)SEQ ID NO 54あるいはSEQ ID NO 55、(n)SEQ ID NO 56、(o)SEQ ID NO 57あるいはSEQ ID NO 58、(p)SEQ ID NO 59、(q)SEQ ID NO 60あるいはSEQ ID NO 61、(r)SEQ ID NO62、(s)SEQ ID NO63あるいはSEQ ID NO64、(t)SEQ ID NO65、SEQ ID NO66、SEQ ID NO67、SEQ ID NO68、SEQ ID NO69、SEQ ID NO70、SEQ ID NO71、SEQ ID NO72、SEQ ID NO73、SEQ ID NO74、SEQ ID NO75、SEQ ID NO76、SEQ ID NO77、SEQ ID NO78、SEQ ID NO79、あるいはSEQ ID NO80、(u)SEQ ID NO81、(v)SEQ ID NO82、または(w)SEQ ID NO83に対して、少なくとも約80%、85%、90%、95%、97%、あるいは100%の配列同一性を備えた配列を含む。いくつかの実施形態において、RIC mRNA前駆体は、(a)SEQ ID NO1、(b)SEQ ID NO2、(c)SEQ ID NO3、(d)SEQ ID NO4、(e)SEQ ID NO5、(f)SEQ ID NO6、(g)SEQ ID NO7、(h)SEQ ID NO 8、(i)SEQ ID NO 9、(j)SEQ ID NO 10、(k)SEQ ID NO 11、(l)SEQ ID NO 12、(m)SEQ ID NO 13、(n)SEQ ID NO 14、(o)SEQ ID NO 15、(p)SEQ ID NO 16、(q)SEQ ID NO 17、(r)SEQ ID NO 18、(s)SEQ ID NO 19、(t)SEQ ID NO 20、(u)SEQ ID NO 21、(v)SEQ ID NO 22、(w)SEQ ID NO 23に対して、少なくとも約80%、85%、90%、95%、97%、あるいは100%の配列同一性を備えた遺伝子配列によってコードされる。いくつかの実施形態において、アンチセンスオリゴマーはRIC mRNA前駆体の一部を標的とし、これは、以下の内部の保持されたイントロンにある:(a)保持されたイントロンの5’スプライス部位に対する+6から+100の領域;(b)保持されたイントロンの3’スプライス部位に対する-16から-100の領域。いくつかの実施形態において、アンチセンスオリゴマーは、少なくとも1つの保持されたイントロンの5’スプライス部位の約100ヌクレオチド下流から、少なくとも1つの保持されたイントロンの3’スプライス部位の約100ヌクレオチド上流までの領域内にあるRIC mRNA前駆体の一部を標的とする。いくつかの実施形態において、RIC mRNA前駆体の標的部分は、以下の内部にある:(a)保持されたイントロンの5’スプライス部位に隣接するエクソン中の+2e~-4eの領域;あるいは(b)保持されたイントロンの3’スプライス部位に隣接するエクソン中の+2e~-4eの領域。
本明細書で言及されるすべての公報、特許、および特許出願は、個々の公報、特許、特許出願が引用によって組み込まれるように具体的且つ個別に示される程度まで、引用によって本明細書に組み込まれる。
ROM1(網膜外節膜タンパク質(retinal outer segment membrane protein)1)は、杆体細胞外節膜タンパク質1をコードする。この遺伝子は、光受容体に特異的な遺伝子ファミリーのメンバーであり、眼の光受容体の円板縁(disk rim)に見られる内在性膜タンパク質をコードする。このタンパク質は、ホモ二量体を形成することができるか、または別の光受容体とヘテロ二量体化することができる(retinal degeneration slow(RDS))。ROM1は、円板形態形成(disk morphogenesis)にとって不可欠であり、外節円板(outer segment disks)の安定化および圧縮またはリムの湾曲の維持に関係する接着分子としても機能し得る。この遺伝子における特定の欠損は、変性眼疾患網膜色素変性に関係している。
網膜色素変性7(RP7)は、色素性網膜症のグループに属する網膜ジストロフィーである。網膜色素変性は、眼底検査で目に見える網膜色素沈着物、および杆体光受容細胞の一次損失と、続く錐体光受容体の二次損失を特徴とする。患者は、典型的に、夜間視力の失明および中間周辺視野の損失を有している。罹患した個体は、疾病を進行させるにつれ、遠周辺視野を失い、最終的に中心視力も失う。この疾患は、ROM1を含む別々の遺伝子座に影響を与える突然変異によって引き起こされ得る。網膜色素変性7の2遺伝子形態は、PRPH2遺伝子の突然変異に起因し、ROM1遺伝子のヌル突然変異が報告された。
TEAD1は、転写エンハンサー因子TEF-1をコードする。転写エンハンサー因子TEF-1は、増殖の制限およびアポトーシスの促進による臓器サイズの調整および腫瘍抑制に関係する経路である、Hippoシグナル伝達経路において重要な役割を果たす転写因子である。この経路のコアはキナーゼカスケードで構成され、ここで調節タンパク質SAV1と複合したMST1/MST2は、YAP1腫瘍性タンパク質およびWWTR1/TAZを順にリン酸化および不活性化する、調節タンパク質MOB1と複合したLATS1/2をリン酸化および活性化する。TEAD1は、YAP1およびWWTR1/TAZの遺伝子発現を媒介することにより作用し、それによって、細胞増殖、遊走および上皮間葉転換(EMT)の誘発を調節する。TEAD1は、特異的且つ協働的にSPHおよびGT-IIC「enhansons」(5’-GTGGAATGT-3’)に結合し、細胞特異的な方法でインビボでの転写を活性化する。活性化機能は、限定する細胞特異的な転写仲介因子(TIF)によって媒介されるように見える。TEAD1はまた、心臓発達に関係し、M-CATモチーフに結合する。
Sveinsson網脈絡膜萎縮は、TEAドメインファミリーメンバー-1遺伝子TEAD1の突然変異によって引き起こされる。らせん状乳頭周囲脈絡網膜変性または優性限局性萎縮(atrophia areata)とも呼ばれる、Sveinsson網脈絡膜萎縮(SCRA)は、網膜および脈絡膜に関係する視神経円板から放散する左右対称性の病変を特徴とする、常染色体優性眼疾患である。
RDH5は、11-シスレチノールデヒドロゲナーゼをコードする。この酵素は、短鎖デヒドロゲナーゼ/還元酵素(SDR)ファミリーに属している。このレチノールデヒドロゲナーゼは、視覚色素の普遍的な発色団である、11-シスレチンアルデヒドの生合成における最終工程を触媒するように機能する。この遺伝子の突然変異は、錐体および杆体の光色素の再生の遅延を特徴とする夜盲のまれな形態である、常染色体劣性白点状眼底を引き起こす。選択的スプライシングは、結果として複数の転写変異体をもたらす。この遺伝子と隣接する上流のBLOC1S1(リソソーム細胞小器官複合体-1、サブユニット1の新生)遺伝子との間に、読み過し転写も存在する。
白点状眼底は、錐体および杆体の光色素の再生の遅延を特徴とする夜盲のまれな形態である。神鳥斑点網膜疾患のこの形態は、中間周辺部(midperiphery)における最大の密度を有する且つ黄斑とは無関係の眼底全体にわたる離散的な一様の白点を特徴とする。夜盲が生じる。常染色体優性遺伝および常染色体劣性遺伝の両方が示唆されてきた。
NR2E3は、NR2E3(核受容体サブファミリー2、グループE、メンバー3)としても知られる、光受容細胞に特異的な核受容体(PNR)をコードする。NR2E3は、網膜の光受容細胞の核受容体である。NR2E3は、杆体発達の活性化因子および錐体発達の抑制因子である転写因子である。NR2E3は、ロドプシン、M-オプシン、S-オプシンおよび杆体に特異的なホスホジエステラーゼβサブユニットを含む、多くの杆体および錐体に特異的な遺伝子のプロモーター領域に結合する。NR2E3は、ロドプシン発現を増強し、M-錐体オプシン発現およびS錐体オプシン発現を抑制する。
網膜色素変性37は、NR2E3遺伝子のホモ接合型またはヘテロ接合の突然変異によって引き起こされる。網膜色素変性37(RP37)は、色素性網膜症のグループに属する網膜ジストロフィーである。網膜色素変性は、網膜における杆体光受容細胞の進行性変性が原因で重度の視覚障害を引き起こす、遺伝性の変性眼疾患である。網膜ジストロフィーのこの形態は、年齢とは無関係の初期症状を明らかにし、それ故、網膜色素変性の診断が、早期乳児期から後期成人期までのどこかで下される。網膜色素変性の初期段階の患者はまず、杆体光受容体の衰弱によって周辺および暗所視が損なわれたことに気づく。進行性の杆体変性に続いて、隣接した網膜色素上皮(RPE)の異常および錐体光受容細胞の悪化が生じる。辺縁視が漸増的に損なわれるにつれ、患者は、進行性の「トンネル状視野」を経験し、最終的に失明する。罹患した個体はさらに、欠陥のある明暗順応、夜盲症(夜盲)、および眼底における骨棘の蓄積を経験し得る。
PAX6は、無虹彩タイプIIタンパク質(AN2)またはoculorhombinとしても知られている、ペアードボックスタンパク質Pax-6をコードする。ペアードボックス遺伝子ファミリーのメンバーである、PAX6は、眼発生(oculogenesis)および他の進行プロセスに関係する転写制御因子をコードする。Pax6は、胚発生の間に存在する転写因子である。コードされたタンパク質は、DNAに結合する及び遺伝子転写の制御因子とし機能すると知られている、2つの異なる結合部位を含んでいる。PAX6は、眼および脳の発達の重要な調節遺伝子である。脳内では、タンパク質は、臭いを処理する専門の細胞の進行に関係している。転写因子として、Pax6は、組織の適切な発達を確かなものとするために遺伝子発現パターンを活性化及び/又は非活性化する。
無虹彩は、染色体11p13上のPAX6遺伝子のヘテロ接合突然変異によって引き起こされる。PAX6遺伝子の280を超える突然変異が、虹彩の欠如である無虹彩を引き起こすことが分かった。これらの突然変異のほとんどは、異常に短い、非機能性PAX6タンパク質の産生につながる。結果として、他の遺伝子の活性を調節するPAX6タンパク質はより少なくなる。
視神経のコロボーマは、PAX6遺伝子の突然変異によって引き起こされる。視神経のコロボーマは、視神経の下面に欠陥がある視神経円板の先天異常である。罹患した眼の視力は損なわれ、その程度は、欠陥のサイズに左右され、典型的に視力よりも視野に影響する。さらに、患者の3分の1に現われる漿液性網膜剥離のリスクが増加する。網膜剥離が生じた場合、それは、通常治療可能ではなく、すべて視界が眼の罹患した領域において失われる、これは黄斑に関係するかもしれないし、関係しないかもしれない。
眼コロボーマは、染色体11p13上のPAX6遺伝子のヘテロ接合突然変異によって引き起こされる。コロボーマは、胚発生中の眼の発達異常に起因する眼の先天性欠損である。それは、あらゆる眼組織の先天的欠陥として定義され、典型的に眼裂の異常閉鎖と一致した部位で組織または間隙が存在しないことを示している。融合不全は、眼の下部分の1つ又は複数の領域のコロボーマにつながりかねず、これは、毛様体、網膜、および脈絡膜を含む、虹彩から視神経までの、亀裂が横切った眼球の部分に影響を与える。コロボーマはまた、発達的な眼の異常の相関したスペクトルの一部として小さな( 小眼球(microphthalmic))眼または欠損した(無眼球(anophthalmic))眼に頻繁に関連付けられ、片眼または両眼の眼に影響を与えかねない。
前上葉異常及び/又は白内障(FVH1)を伴う又は伴わない中心窩形成不全-1は、染色体11p13上のPAX6遺伝子のヘテロ接合突然変異によって引き起こされる。中心窩形成不全は、推定される中心窩領域の連続した(continuity of)すべての神経感覚網膜層を有する中心窩陥凹の欠如として定義される。分離された主体(isolated entity)としての中心窩形成不全は、まれな現象であり、通常、無虹彩、小眼球、白皮症、または色覚異常などの、他の視覚障害に関連して記載される。報告された中心窩形成不全のすべてのケースには、視力の低下および眼振が伴う。
両側性視神経形成不全は、PAX6遺伝子の突然変異によって引き起こされ得る。視神経形成不全は、視神経の未発達から生じる病状である。この疾病は、最も一般的な先天性視神経異常である。すべての視神経軸索が適切に発達するとは限らないため、視神経円板は異常に小さく見える。それは、しばしば、内分泌障害(ホルモン欠乏症)、発達遅延、および脳奇形に関連付けられる。網膜から脳への視覚信号の伝達の要因である視神経には、平均的な人においておよそ120万の神経線維がある。しかしながら、視神経形成不全と診断された人においては、神経は顕著により少ない。視神経形成不全は、一側性(片眼)または両側性(両眼)であり得るが、ほとんどの場合、両側性を示す(80%)。一側性の場合は、より良い視力を有する傾向があるため、典型的に、両側性視神経形成不全の人より遅い年齢で診断される。視力は、光覚弁なしからほぼ正常な視力までの範囲であり得る。
CRXは、錐体杆体ホメオボックスタンパク質をコードする。錐体杆体ホメオボックスタンパク質は、光受容細胞の分化において役割を果たす、光受容体に特異的な転写因子である。このホメオドメインタンパク質は、正常な錐体および杆体の機能の維持に必要である。錐体杆体ホメオボックスタンパク質は、オプシン遺伝子を含む幾つかの光受容体に特異的な遺伝子の上流で見られる配列5’-TAATC[CA]-3’を結合する及びトランス活性化する転写因子である。CRXは、NRL、RORBおよびRAXなどの他の転写因子と相乗的に、光受容体に特異的な遺伝子の転写を調節するように作用し、哺乳動物の光受容体の維持にとって不可欠である。
錐体杆体ジストロフィー-2(CORD2)は、染色体19q13上のCRX遺伝子のヘテロ接合突然変異によって引き起こされる。錐体杆体ジストロフィー2(CORD2)は、優位に黄斑領域にある眼底検査で目に見える網膜色素沈着物、および錐体光受容体の初期欠損に続く杆体変性を特徴とする、遺伝性網膜ジストロフィーである。これは、視力および中心視野における感受性の低下につながり、その後、辺縁視が損失する。視力の深刻な損失が、網膜色素変性よりも早く生じる。
レーバー先天黒内障-7は、染色体19q13上のCRX遺伝子のヘテロ接合またはホモ接合の突然変異によって引き起こされ得る。レーバー先天黒内障は、視力損失、眼振、および重度の網膜機能不全を特徴とする、早発性の小児期の網膜ジストロフィーのグループを含む。患者は、通常出生時に深刻な視力損失および振子様眼振を示す。網膜電図(ERG)応答は、通常記録不可能である。他の臨床所見は、高い遠視、光不快(photodysphoria)、眼指兆候(oculodigital sign)、円錐角膜、白内障、および眼底に対する可変性外観(variable appearance to the fundus)を含み得る。
FSCN2はファスシン-2をコードする。この遺伝子は、ファスシンタンパク質ファミリーのメンバーをコードする。ファスシンは、アクチンを動的細胞伸長(dynamic cell extensions)内の糸状束(filamentous bundles)へと架橋する。このファミリーは、光受容体円板の形態形成において役割を果たすと提案されている。この遺伝子の突然変異は、結果として、常染色体優性の網膜色素変性および黄斑変性の1つの形態をもたらす。異なるアイソフォームをコードする複数の転写変異体も発見された。
網膜色素変性30は、染色体17q25上の網膜ファスシン遺伝子(FSCN2)の突然変異によって引き起こされる。網膜色素変性30(RP30)は、色素性網膜症のグループに属する網膜ジストロフィーである。網膜色素変性は、眼底検査で目に見える網膜色素沈着物および続く錐体光受容体の二次損失を特徴とする。患者は、典型的に夜間視力の失明および中間周辺視野の損失を有している。患者の疾病が進行するにつれ、患者は遠周辺視野を失い、最終的に中心視力も失う。
ABCA4は、ABCA4またはABCRとしても知られるサブファミリーA(ABC1)、メンバー4である、ATP結合カセットをコードする。ABCA4は、多細胞真核生物に独占的に見られるATP結合カセット輸送体遺伝子のサブファミリーA(ABC1)のメンバーである。ABCA4タンパク質は、光受容体において産生される。ABCA4タンパク質は、眼に入る光が脳に伝達される電気信号に変換されるプロセスである、光伝達後に活性である。光伝達は、有毒物質の形成につながる可能性がある。ABCA4タンパク質は、光受容細胞から、N-レチニリデン-PEと呼ばれる、これらの物質のうちの1つを除去する。
シュタルガルト病-1(STGD1)は、染色体1p22上のABCA4遺伝子(601691)のホモ接合または複合ヘテロ接合の突然変異によって引き起こされる。シュタルガルト黄斑変性は、進行性の視力損失を引き起こす遺伝性の眼障害である。この障害は網膜に影響を与える。具体的には、シュタルガルト黄斑変性は、黄斑と呼ばれる網膜の中心近くの小さな領域に影響を与える。黄斑は、読書、運転、および顔認識などの詳細なタスクに必要とされる鋭い中心視の原因である。シュタルガルト黄斑変性を有する人のほとんどにおいて、脂肪性の黄色色素(リポフスチン)が黄斑の基礎となる細胞に蓄積される。経時的に、この物質の異常な蓄積は、はっきりとした中心視にとって重要な細胞を損傷させかねない。中心視損失に加えて、シュタルガルト黄斑変性を有する人は、少ない光で誘導することを困難にし得る夜間視力の問題を有している。罹患した個体の中には色覚を損なったものもいた。シュタルガルト黄斑変性の徴候および症状は、典型的に小児期後期から成人早期に現われ、経時的に悪化する。
網膜色素変性-19(RP19)は、染色体1p22上のABCR遺伝子(ABCA4)のホモ接合または複合ヘテロ接合の突然変異によって引き起こされ得る。網膜色素変性は、辺縁視の進行性の損失および中心視損失を引き起こしかねない夜間視力の困難性を特徴とする遺伝性の眼障害である。網膜色素変性に関連付けられた多くの遺伝子がある。タイプ19は、染色体1p21-p13上の遺伝的欠陥に関連付けられる。網膜色素変性-19は、夜盲、辺縁視の損失、進行性の網膜変性、トンネル状視野、進行性の視力損失、夜間または少ない光での視力減退、進行した段階での中心視の損失、および網膜色素上皮の斑点を特徴とする。
加齢黄斑変性-2(ARMD2)は、染色体1p22上のABCA4遺伝子における変更によって与えられる。加齢黄斑変性は、先進国の高齢者の視力損失の主要原因である眼疾患である。視力損失は、通常、60年代または70年代の人において顕著となり、経時的に悪化する傾向がある。加齢黄斑変性は、主として、読書、運転、および顔認識などの詳細なタスクに必要とされる中心視に影響を与える。この状態での視力損失は、光および色を検出する眼の後ろの組織(網膜)における光感知細胞の段階的な悪化に起因する。具体的には、加齢黄斑変性は、中心視の原因である、黄斑と呼ばれる網膜の中心近くの小さな領域に影響を与える。側(辺縁)視および夜間視力は、一般に影響を受けない。研究者は、乾燥型および湿潤型として知られる、2つの主要なタイプの加齢黄斑変性について記載した。乾燥型は、はるかにより一般的であり、加齢黄斑変性のすべての症例の85~90パーセントを占めている。それは、網膜下のドルーゼンと呼ばれる黄色がかった沈着物の蓄積およびゆっくり進行する視力損失を特徴とする。その状態は、典型的には両眼の視力に影響を与えるが、視力損失は、しばしば片眼ずつ生じる。加齢黄斑変性の湿潤型は、急速に悪化しかねない重度の視力損失に関係している。その状態のこの湿潤型は、黄斑の真下の異常で脆弱な血管の成長を特徴とする。これらの血管は血液および体液を漏出し、これによって黄斑が損傷し、中心視は、ぼやけて、歪んだように見える。
錐体杆体ジストロフィー-3(CORD3)は、染色体1p22上のABCA4のホモ接合または複合ヘテロ接合の突然変異によって引き起こされる。錐体杆体ジストロフィーは、色素性網膜症のグループに属する遺伝性網膜ジストロフィーである。錐体杆体ジストロフィーの有病率は、40,000分の1と推定される。錐体杆体ジストロフィーは、黄斑領域に優位に局在化された、眼底検査で目に見える、網膜色素沈着物を特徴とする。杆体光受容体の一次損失およびその後の錐体光受容体における二次損失に起因する、杆体錐体ジストロフィー(RCD)とも呼ばれる典型的な網膜色素変性(RP)とは対照的に、錐体杆体ジストロフィーは、反対の一連の事象(opposite sequence of events)を反映している。錐体杆体ジストロフィーは、一次的な錐体の関与、または時に錐体および杆体両方の同時の損失を特徴とし、これは、錐体杆体ジストロフィーの以下の主症状を説明するものである:視力の低下、色覚異常、光嫌悪(photoaversion)および中心視野の感受性の低下、その後の辺縁視の進行性の損失および夜盲。錐体杆体ジストロフィーの臨床経過は、一般により深刻なものであって、RCDの臨床経過より急速であり、初期の法的盲および無能力につながる。しかしながら、末期では、錐体杆体ジストロフィーはRCDと変わりない。錐体杆体ジストロフィーは、最も頻繁に非症候性であるが、バルデー-ビードル症候群および脊髄小脳失調症7型(SCA7)などの、幾つかの症候群の一部であり得る。非症候性の錐体杆体ジストロフィーは、遺伝学的に異質である(10のクローン化遺伝子および3つの遺伝子座がこれまでに同定されている)。錐体杆体ジストロフィーの病態形成に関係している4つの主要な原因となる遺伝子は、ABCA4(これはシュタルガルト病および常染色体劣性の錐体杆体ジストロフィーの30~60%も引き起こす)、CRXおよびGUCY2D(これは常染色体優性の錐体杆体ジストロフィーの多くの報告された症例の要因である)、およびRPGR(これはX連鎖性RPの約2/3およびX連鎖性錐体杆体ジストロフィーの未決定のパーセンテージを引き起こす)である。RPまたは黄斑ジストロフィーを引き起こし得る、遺伝子の高度に有害な突然変異はまた、錐体杆体ジストロフィーにつながり得る。錐体杆体ジストロフィーの診断は、病歴、眼底検査および網膜電図に基づいている。幾つかの遺伝子に対して分子診断が行われ得、遺伝相談が常に勧められる。現在、その疾患の進化を止める又は視力を回復させる治療はなく、視力予後は乏しい。管理は、変性プロセスを遅らせること、合併症を処置すること、および患者が失明の社会学的および心理学的な効果に対処するのを助けることに向けられている。
<MYOC>
MYOC遺伝子はミオシリンをコードする。ミオシリンは、小柱網および毛様体に見られ、眼内圧を調節する。それはまた、様々なタイプの筋肉に見られる。ミオシリンの機能は、十分に理解されていないが、毛様体の筋組織におけるその作用によって眼内圧を制御する助けとなり得る。研究者は、ミオシリンが、タンパク質複合体の部分として他のタンパク質と一緒に機能すると考えている。ミオシリンは、CYP1B1遺伝子の産物である、シトクロムP450タンパク質の形態を含む多くの他のタンパク質と相互作用し得る。
GLC1Aと指定される原発開放隅角緑内障(POAG)は、染色体1q上のMYOC遺伝子のヘテロ接合の突然変異によって引き起こされる。POAGに関連する症状はない。眼内の圧力はゆっくり上昇し、角膜は腫脹なしで適合する。角膜が腫脹した場合には、症状が現れ、角膜の腫脹は、通常、何かが調子悪いという信号である。しかし、そうではないため、この疾患はしばしば検出されない。これは無痛であり、患者は、しばしば、ゆっくり視力を失っていることをその疾患の後期段階まで気づかない。しかしながら、視力が損なわれときには、損傷が回復不能となっている。緑内障は、眼と脳をつなぐ視神経が進行的に損傷される眼障害のグループである。この損傷は、側(辺縁)視の低下および最終的な失明につながりかねない。他の徴候および症状は、眼球突出、涙の過剰分泌、および光に対する異常な感受性(羞明)を含み得る。用語「早発性の緑内障」は、障害が40歳より前に現われるときに使用され得る。緑内障を有する人のほとんどにおいて、視神経に対する損傷は、眼内の圧力(眼内圧)の上昇によって引き起こされる。眼内圧は、眼に入る体液と眼を出る体液との間のバランスに左右される。通常、緑内障は、高齢者において進行し、障害を進行させるリスクは、高血圧(高血圧症)および真性糖尿病の他に、家族歴を含む、様々な病状による影響を受け得る。早発性の緑内障のリスクは、主として遺伝に左右される。眼内の体液の排出を妨害する構造的異常は、出生時に存在し、通常、生後1年の間に明らかになり得る。そのような異常は、症候群と呼ばれる、多くの体組織に影響を与える遺伝病の一部であり得る。緑内障は、他の関連する異常なしで5歳よりも前に現われる場合、原発先天緑内障と呼ばれる。他の個体は、最も一般的な緑内障の成体形である、原発開放隅角緑内障の早発を経験する。原発開放隅角緑内障は、小児期または成人早期の間に発症する場合、若年性解放隅角緑内障と呼ばれる。
TCF4は、TCF4をコードするか、または時に免疫グロブリン転写因子2と呼ばれる。TCF4は、ホモ二量体または他のbHLHタンパク質を有するヘテロ二量体として機能する、広く発現されたベーシック・ヘリックス・ループ・ヘリックス(bHLH)タンパク質である。これらの二量体は、エフリュッシ(E)ボックス配列でDNAを結合する。選択的スプライシングは、それらの細胞内局在性およびトランス活性化能力が異なる多数のN末端で別々のTCF4アイソフォームを産生する。TCF4タンパク質は、免疫グロブリンエンハンサーのミュー-E5/カッパ-E2モチーフに結合する転写因子として作用する。TCF4は、SSTR2-INR、またはソマトスタチン受容体2イニシエーター要素上で通常見られる、E-ボックス(5’-CANNTG-3’)に結合することによって転写を活性化する。TCF4は、主として、DNAへの結合によって神経の分化を開始することによる妊娠中の胎児の神経学的発達に関係している。それは、初期発生中に中枢神経系、体節、および生殖隆起において見られる。発生の後期に、それは、甲状腺、胸腺、および腎臓において見られ、成人期には、リンパ球、筋肉、および胃腸系において見られる。
フックス角膜内皮ジストロフィー-3(FECD3)は、染色体18q22上のTCF4遺伝子におけるヘテロ接合のイントロン性の三塩基反復配列伸長(CTG)nによって引き起こされる。遅発性フックス角膜内皮ジストロフィー(FECD)は、40年を超える人口のおよそ4%に影響を与える変性障害である。それは、角膜内皮によって分泌されたコラーゲンに富んだ基底層であるデスメ膜のごく小さい屈折性の突起物(microscopic refractile excrescences)である、グッテー(guttae)の進行性の形成による他の角膜疾患とは区別される。通常、FECDが内皮細胞機能を深刻に損なわせるのに、発症から20年間かかり、これは、実質浮腫および視覚障害につながる。この疾病の第1の症状は、典型的に、通常その日におさまる朝の霧視である。経時的に、罹患した個体は視力を失っていく。フックス内皮ジストロフィーを有する人はまた、明るい光に敏感になる。フックス内皮ジストロフィーは、角膜と呼ばれる眼の最前面に特異的に影響を与える。眼の検査中に検出可能である、グッテーと呼ばれる沈着物は、角膜の真中に形成され、最終的に広がる。これらのグッテーは、角膜における細胞の損失の一因となり、視力の問題につながる。小水疱が角膜上で発達し、これは、破裂して眼痛を引き起こし得る。フックス内皮ジストロフィーの徴候および症状は、通常、40代または50代の人において始まる。この疾病の非常にまれな早発性の異型は、20代の人の視力に影響を与え始める。
MFSD8は、MFSD8としても知られている主要促進物質スーパーファミリードメイン含有8(Major facilitator superfamily domain containing 8)をコードする。MFSD8タンパク質は、細胞リソソームにおいて見られる。MFSD8タンパク質は、第2次能動輸送タンパク質の主要促進物質スーパーファミリーと呼ばれる、関連するタンパク質の大きなグループに属する。このファミリーにおけるタンパク質は、特定の分子を細胞内の構造間で、または細胞内および細胞外へと移動させる。MFSD8タンパク質は分子を輸送する傾向にあるが、それが移動させる特有の分子は知られていない。MFSD8タンパク質は、恐らくリソソームの膜にわたって物質を輸送する。
中央錐体が関係する黄斑ジストロフィー(CCMD)は、染色体4q28上のMFSD8遺伝子の複合ヘテロ接合の突然変異によって引き起こされる。これは、主として錐体ジストロフィーであるが、高齢患者においては杆体損傷の証拠がある。中心視力の軽度の減少は、30代から60代の個体において顕著である。わずかな色素の変化および色覚異常が、これらの症状の発症で文書化され、標的黄斑症および中心窩の重度の萎縮が存在し得る。辺縁が正常である末梢で拡張する中心暗点(enlarging central scotoma with normal periphery)が、時に識別され得る。他の患者は、蒼白な(pale)視神経円板を有する乳頭周囲の領域に対して萎縮性の様相(atrophic appearance)を有している。MFSD8遺伝子(4q28.2)のミスセンス突然変異およびナンセンス突然変異に対する複合ヘテロ接合性が、常染色体劣性遺伝を示唆するDutch同胞群のメンバーの中から見つけられた。
CTNS遺伝子は、通称シスチノシン(cystinosin)をコードする。このタンパク質は、物質を消化し再利用する細胞の区画であるリソソームの膜内に位置する。リソソームの内部で消化されたタンパク質は、より小さなアミノ酸に分割される。その後、アミノ酸は、輸送タンパク質によってリソソームから除去される。シスチノシンは、アミノ酸シスチンをリソソームから特異的に移動させる輸送タンパク質である。
眼性非腎症性シスチン症は、染色体17p13にマッピングするシスチノシン(CTNS)をコードする遺伝子の突然変異によって引き起こされる。古典的な腎症性タイプのシスチン症の異型である、眼性非腎症性シスチン症は、腎臓病ではないが角膜のシスチン結晶による羞明を特徴とする常染色体劣性のリソソーム蓄積症である。シスチン症を引き起こす原因である80を超える異なる突然変異が、CTNS遺伝子において特定された。最も一般的な突然変異は、CTNS遺伝子の大部分の欠失(時に57-kb欠失と呼ばれる)であり、結果としてシスチノシンの完全な損失をもたらす。この欠失は、ヨーロッパ系の人におけるシスチン症の症例のおよそ50パーセントの原因である。他の突然変異は、結果として、その正常な輸送機能を実行することができない異常に短いタンパク質の産生をもたらす。CTNS遺伝子の非常に小さな領域を変化させる突然変異によって、輸送タンパク質は、その通常の活性のいくらかを保持することが可能になり、結果としてシスチン症のより軽度な形態がもたらされ得る。
NXNL1は、ヌクレオレドキシン様1(NXNL1)をコードする。NXNL1は、錐体細胞の生存率に役割を果たし、錐体変性を遅らせ得る。NXNL1は、杆体の変性には役割を果たさないようである。NXNL1に関連する疾患は、レーバー先天黒内障およびバルデー-ビードル症候群を含む。レーバー先天黒内障は、主として網膜に影響を与える眼障害である。この疾病を有する個体は、典型的に乳児期に開始する重度の視力障害を有している。他の特徴は、羞明、眼の不随意運動(眼振)、および極端な遠眼を含む。瞳孔はまた通常光に反応しない。さらに、角膜は、円錐形であり得、異常に薄い(円錐角膜)。フランスシェッティの眼指兆候(Franceschetti's oculo-digital sign)は、レーバー先天黒内障の特性である。この徴候は、指関節または指での眼のつっつき、圧迫、およびこすりから成る。この疾病の少なくとも13のタイプが記載され、これらは、それらの遺伝子的原因、視力損失のパターン、および関連する眼異常によって判別される。
OPTN遺伝子は、コイルドコイル含有タンパク質オプチニューリンをコードする。オプチニューリンは、正常眼圧緑内障および成人発症の原発開放隅角緑内障において役割を果たし得る。オプチニューリンは、アデノウイルスE3-14.7Kタンパク質と相互作用し、腫瘍壊死因子αまたはFasリガンド経路を利用して、アポトーシス、炎症または血管収縮を媒介し得る。オプチニューリンはまた、細胞の形態形成および膜輸送、小胞輸送、並びにRAB8、ハンチンチン、および転写因子IIIAタンパク質とのその相互作用による転写活性化において機能し得る。選択的スプライシングは、結果として同じタンパク質をコードする複数の転写変異体をもたらす。
原発開放隅角緑内障(POAG)は、視神経および視野の欠陥の特定パターンを特徴とする。前眼房の角は解放しており、通常、眼内圧は上昇する。しかしながら、緑内障は、どれほどの眼内圧であっても生じ得る。該疾患は、後期まで一般に無症候性であり、それまでには相当且つ回復不能な視神経損傷が既に生じている。該疾患は、OPTN遺伝子に影響を与える突然変異によって引き起こされる。
筋萎縮性側索硬化症12(ALS12)は、脳における上位運動ニューロンおよび脳幹および脊髄における下位運動ニューロンに影響を与える神経変性障害であり、結果として致命的な麻痺につながる。感覚異常は存在しない。該疾患の病理学的特徴は、運動性ニューロンの損失による皮質脊髄路の蒼白、残存する運動性ニューロン内のユビキチン陽性の封入体の存在、および病理学的凝集体の沈着を含む。筋萎縮性側索硬化症の病因は、多因子性の傾向があり、遺伝的および環境的な要因の両方を含む。該疾患は、症例の5-10%において遺伝性である。
RLBP1遺伝子は、生理学的リガンドとしての11-シス-レチンアルデヒドまたは11-シス-レチナールを運ぶ36-kD水溶性タンパク質をコードする。RLBP1タンパク質は、視覚サイクルの機能性成分であり得る。この遺伝子の突然変異は、重度の杆体錐体ジストロフィー、ボスニア型ジストロフィー(非症候性の常染色体劣性の網膜色素変性)および白点状網膜炎に関係している。
ボスニア型の網膜ジストロフィー(BRD)は、白点状網膜炎の一種である。罹患した個体は、白点状網膜炎および黄斑変性と一致した特徴を有する幼児期早期からの夜盲を示す。該疾患は、RLBP1遺伝子に影響を与える突然変異によって引き起こされる。
白点状眼底は、典型的に幼児期早期に現れる、夜盲および明るい光に対する暴露後の暗順応の遅れを特徴とする網膜障害である。罹患した個体の眼底は、網膜色素上皮における複数の小さい、白い又は浅黄色の点を含有し、これは黄斑を含んでいるかもしれないし、含んでいないかもしれない。これらの点は変わらないままであることができ、より顕著になるか、あるいは老化中に消え、新しい点がまた現われ得る。罹患した個体の暗順応曲線は、錐体および杆体の感受性の回復の延長を特色とし、網膜電図の錐体および杆体の振幅は、暗順応の30-40分後に著しく低減されるが、長時間の適応後に正常または正常に近いレベルになり、白点状眼底を有する個体のおよそ38%が広範囲な錐体機能不全であることが示された。白点状眼底の患者において、RLBP1遺伝子の突然変異も報告された。
白点状網膜炎(RPA)は、夜盲および暗順応の遅れを引き起こす、網膜の後側の白い斑点(white flecks)の凝集を特徴とする神鳥斑点網膜疾患の形態である。これは、進行性である及び網膜の一般化された萎縮に進化する白点状眼底とは異なる。該疾患は、RLBP1遺伝子に影響を与える突然変異によって引き起こされる。
RPE65遺伝子は「網膜色素上皮に特異的なタンパク質65kDa」とも呼ばれる。RPE65遺伝子は、正視にとって不可欠なRPE65タンパク質をコードする。RPE65タンパク質は、網膜色素上皮(RPE)において産生される。RPEは、眼の後部に並ぶ光感応組織である網膜を支持し、それに栄養を与える。RPE65タンパク質は、視覚サイクルと呼ばれる多段階プロセスに関係し、これによって、眼に入る光を脳に伝達される電気信号へと変換する。光は、網膜における感光色素に当たると、11-シス-レチナール(ビタミンAの形態)をオール-トランスレチナールに変化させる。この転換は、電気信号を生成する一連の化学反応を引き起こす。その後、RPE65タンパク質は、視覚サイクルを再び始めることができるように、オール-トランスレチナールを11-シス-レチナールに変換するのを助ける。
レーバー先天黒内障は、主として、光および色を検出する眼の後ろの特殊な組織である網膜に影響を与える眼障害である。この障害を有する人は、典型的に、乳児期に開始する重度の視力障害を有している。視力障害は、安定する傾向があるが、経時的に非常にゆっくりと悪化し得る。
網膜色素変性症20は色素性網膜炎の群に属する網膜ジストロフィーである。網膜色素変性症は、眼底検査で目視可能な網膜色素沈着物、および杆体光受容細胞の一次損失と続く錐体光受容体の二次損失によって特徴づけられる。患者は、典型的には夜間視力の失明、および中間周辺視野の損失を有する。それらの疾患の進行で、彼らは遠方の周辺視野、そして最終的には中心視覚を同様に失う。
LRAT遺伝子、すなわちレシチンレチノールアシルトランスフェラーゼ(ホスファチジルコリン--レチノールO-アシルトランスフェラ-ゼ)は、小胞体に局所化したLRATタンパク質をコードし、触媒作用でエステル化のオール-トランス-レチノールをオール-トランス-レチニルエステルへと変える。この反応は、視覚系でのビタミンA物質代謝の重要な工程である。この遺伝子における突然変異は、早発性の重度の網膜ジストロフィーおよびレーバー先天黒内障14に関係してきた。選択的スプライシングは、結果として多数の転写変異体をもたらす。LRATタンパク質は、ホスファチジルコリンのsn-1の位置からオール-トランス-レチノールまでアシル基を転移させ、オール-トランス-レチニルエステルを産生する。レチニルエステルはビタミンAの貯蔵形態である。LRATは視覚において重大な役割を果たす。LRATは、網膜色素上皮においてオール-トランス-レチニルエステルを11-シス-レチノールへと処理するイソメロヒドロラーゼのための、そのエステルの基質を提供し;その処理では、膜結合性のアルコールデヒドロゲナーゼにより、11-シス-レチノールは酸化され、かつロドプシンおよび錐体光色素に関する発色団である11-シス-レチンアルデヒドに転換される。
レーバー先天黒内障14(LCA14)は網膜の重度のジストロフィーであり、典型的には生後1年で明らかとなる。視覚機能は通常貧弱であり、かつしばしば眼振、不活発な瞳孔反応またはほぼ存在しない瞳孔反応、羞明、高遠視、および円錐角膜を伴う。その疾患は、LRAT遺伝子に影響を与える突然変異によって引き起こされる。
網膜色素変性症は進行性の視力喪失を引き起こす関連する眼科疾患の群である。これらの疾患は、目の後部にある光に敏感な組織の層である網膜に影響を与える。網膜色素変性症の人々において、網膜の光を感知する細胞が徐々に悪化するとともに、視力喪失が生じる。網膜色素変性症の初発症候は、通常夜間視力の損失であり、それは幼年期において明白となる。夜間視力の問題は、弱光における運転を困難にする可能性がある。その後、その疾患は盲点が側視(周辺視野)内で発展する原因となる。経時的に、これらの盲点はトンネル状視野を生成するように統合する。その疾患は、数年または数十年間にわたって進行し、読書、運動、および顔を認識することなどの細かい作業のために必要である中心視覚に影響を与える。成年期において、網膜色素変性症の多くの人々が法的盲(legally blind)となる。
レチノールデヒドロゲナーゼ8(オール-トランス-)はRDH8遺伝子によってコードされた酵素である。オール-トランス-レチノールデヒドロゲナーゼ(RDH8)は、オール-トランス-レチナールをNADPHの存在下においてオール-トランス-レチノールへ還元する視覚サイクル酵素である。その酵素は、短連鎖デヒドロゲナーゼ/還元酵素のファミリーのメンバーで、光受容体の外節に位置し;従って、光受容体レチノールデヒドロゲナーゼとしても公知である。これは、漂白され加水分解されたロドプシンの産生物であるオール-トランス-レチナールを減少させることにより、ロドプシン再生経路を開始することによる視覚サイクルにおいて重要である。
RDH12遺伝子、すなわちレチノールデヒドロゲナーゼ12(オール-トランス-/9-シス/11-シス)は、最も高い活性が9-シスおよびオール-トランス-レチノールに対するNADPH依存のレチナールレダクターゼである、RDH12タンパク質をコードする。コードされた酵素は、さらに短連鎖アルデヒドの代謝において役割を果たすが、ステロイドデヒドロゲナーゼ活性を示さない。この遺伝子の欠損は、レーバー先天黒内障13型および網膜色素変性症53の原因となる。
レーバー先天黒内障13(LCA13)は、網膜の重度のジストロフィーであり、典型的には生後1年で明らかになる。視覚機能は通常貧弱であり、かつしばしば眼振、不活発な瞳孔反応またはほぼ存在しない瞳孔反応、羞明、高遠視、および円錐角膜を伴う。場合によっては、レーバー先天黒内障13は、染色体14q23.3の、光受容体に特異的なレチナールデヒドデヒドロゲナーゼ遺伝子RDH12におけるホモ接合または複合ヘテロ接合の突然変異によって引き起こされうる。
網膜色素変性症53(RP53)は色素性網膜炎の群に属する網膜ジストロフィーである。網膜色素変性症は、眼底検査で目視可能な網膜色素沈着物、および杆体光受容細胞の一次損失と続く錐体光受容体の二次損失によって特徴づけられる。患者は、典型的には夜間視力の失明、および中間周辺視野の損失を有する。それらの疾患の進行で、彼らは遠方の周辺視野、そして最終的には中心視覚を同様に失う。
RGR遺伝子は、推定網膜のGタンパク質共役受容体をコードする。その遺伝子は、7つの膜貫通型のGタンパク質共役受容体の1ファミリーのオプシンサブファミリーのメンバーである。レチンアルデヒドと結合する他のオプシンのように、それは7番目の膜貫通ドメイン中に保存されたリシン残基を含む。そのタンパク質は、オール-トランス-レチナールが11-シス-レチナールとなる転換を触媒するように、フォトイソメラーゼ(photoisomerase)として作用する。逆異性化が、網膜の光受容細胞においてロドプシンにより生じる。タンパク質は、網膜の光受容細胞、網膜色素上皮、およびミュラー細胞に隣接している組織において排他的に発現する。この遺伝子は、常染色体劣性および常染色体優性の網膜色素変性症(それぞれarRPおよびadRP)に関係することもある。選択的スプライシングは、結果として様々なアイソフォームをコードする多数の転写変異体をもたらす。網膜のGタンパク質共役受容体(RGR)は、網膜の光受容細胞(すなわち網膜色素上皮とミュラー細胞)に隣接している細胞において排他的に見られるロドプシンホモログである。それは、11-シス-レチナールではなくオール-トランス-レチナールに優先的に結合し、通常ロドプシンにおいて見られる。哺乳動物において、光の光子は、RGR内のオール-トランス-レチナールを11-シス-レチナールに転換するが、光受容細胞において逆異性化反応がロドプシン内で生じる。
網膜色素変性症44(RP44)は色素性網膜炎の群に属する網膜ジストロフィーである。網膜色素変性症は、眼底検査で目視可能な網膜色素沈着物、および杆体光受容細胞の一次損失と続く錐体光受容体の二次損失によって特徴づけられる。患者は、典型的には夜間視力の失明、および中間周辺視野の損失を有する。それらの疾患の進行で、彼らは遠方の周辺視野、そして最終的には中心視覚を同様に失う。その疾患は、RGR遺伝子に影響を与える突然変異によって引き起こされる。
CNGA3または環状ヌクレオチドゲートチャネルα3遺伝子は、錐体光受容体の環状ヌクレオチドゲート(CNG)チャネルの1部分(αサブユニット)をコードする。これらのチャネルは排他的に錐体中で見られ、網膜内に位置する。錐体は、色覚を含む明るい光(明所視)中の視覚を提供する。
色覚異常-2は常染色体劣性の障害であり、かつ杆体の一色型色覚異常または完全色盲とも呼ばれる完全な色覚障害であって、羞明、視力低下、眼振、および色を区別する能力が完全に無いこと(the complete inability to discriminate between colors)によって特徴づけられる珍しい先天性の常染色体劣性の障害である。網膜電図検査の記録は、色覚異常において、杆体光受容体の機能は正常であり、錐体光受容体の応答が存在しないことを示す。
PER1遺伝子は、ヒトにおけるピリオド概日性タンパク質ホモログ1のタンパク質をコードする。PER1は、中枢の概日時計遺伝子(例えばCLOCK)の発現を抑制する核中の概日リズムおよび機能の主要制御因子である。PER1の存在量、核移行、および転写抑制の周期性は、PER1のリン酸化、ユビキチン化およびプロテアソーム分解によって調整される。
IDUA遺伝子は、α-L-イズロニダーゼと呼ばれる酵素をコードし、この酵素は大きな糖分子(例えばグリコサミノグリカン)(GAG)の分解にとって不可欠である。加水分解を通して、α-L-イズロニダーゼは、硫酸化されていないα-L-イズロン酸分解するために水分子を使用し、その水分子はヘパラン硫酸およびデルマタン硫酸中に存在する。α-L-イズロニダーゼはリソソーム中に位置しうる。IDUA遺伝子中の100を超える突然変異が、ムコ多糖症I型(MPS I)を引き起こすと分かってきた。MPS Iを引き起こすたいていの突然変異は、α-L-イズロニダーゼの機能を弱めるか、または完全に除く。ある突然変異が重度か弱毒化したMPS Iを引き起こしたかどうかは、通常測定することができないが;しかしながら、α-L-イズロニダーゼも生成しない人々は、重症のこの障害を有する。
ムコ多糖症I型(MPS I)は多くの身体各部に影響を与える疾病である。この障害は、一旦、以下の3つの独立した症候群に分けられた:重度のものから軽度なものの順に表記して、ハーラー症候群(MPS I-H)、ハーラー-シャイエ症候群(MPS I-H/S)、およびシャイエ症候群(MPS I-S)。これら3つの症候群のそれぞれの間に多くの重複が存在するため、MPS Iは現在重度のタイプおよび弱毒化したタイプに分類される。
ハーラー-シャイエ症候群は、2つの両極のハーラー症候群およびシャイエ症候群との間の、ムコ多糖症1型(MPS1)の中間形であり、珍しいリソソーム蓄積症であり、骨格変形および運動発達の遅延によって特徴づけられる。MPS Iの罹患率は1/100,000と見積もられており、ハーラー-シャイエ症候群は症例の23%、すなわちおよそ1/435,000の罹患率である。ハーラー-シャイエ症候群の患者は、正常な又はほとんど正常な知能有するが、様々な度合いの物理的な機能障害を示す。患者は、低身長、多発異骨症(multiple dysostosis)、胸部の腰椎後彎、様々な度合いの進行性の粗大化顔貌、心筋症および弁異常、脳感覚の(neurosensorial)聴覚消失、扁桃腺肥大および咽頭扁桃肥大、ならびに鼻汁を含む、様々な度合いに筋骨格の変質を生後1年で示す。水頭症は、2歳の後に生じる場合がある。角膜混濁は2~4歳の間で見られ、視力を回復するためには角膜移植が必要である。他の徴候は、臓器肥大、ヘルニア、および多毛症を含むこともある。
ALMS1遺伝子はALMS1タンパク質をコードする。ALMS1遺伝子は、位置13における染色体2の短(p)腕に位置付けられる。ALMS1タンパク質は、聴力、視力、体重の調節、ならびに心臓、腎臓、肺、および肝臓の機能において役割を果たすかもしれない。膵臓が、血糖レベルを制御するのを助けるホルモンであるインスリンをどのように調整するかにも影響しうる。
アルストレーム症候群は、多くの体組織に影響を与える珍しい疾病である。この疾病の徴候および症状の多くは幼児期あるいは幼児期早期に始まるが、いくらかは年取ってから現われる。アルストレーム症候群は、進行性の視力および聴力の喪失、心筋(拡張型心筋症)を拡大させ弱める心臓病の形態、肥満、2型真性糖尿病、および低身長によって特徴づけられる。この障害はまた、肝臓、腎臓、膀胱、および肺に関する重いまたは生命を脅かす医学的問題を引き起こす場合がある。アルストレーム症候群のある程度の個体は、黒色表皮腫と呼ばれる皮膚疾病を持ち、その疾病は、本体の皮膚の重なりおよびしわをもたらし、皮膚が厚く、浅黒く、手ざわりがよくなる。アルストレーム症候群の徴候および症状は重症度が異なり、かつ全ての影響を受けた個体は、障害の特長の全てを有する。
実施形態では、本明細書の方法は、細胞核中で、ROM1、TEAD1、RDH5、NR2E3、PAX6、CRX、FSCN2、ABCA4、MYOC、TCF4、MFSD8、CTNS、NXNL1、OPTN、RLBP1、RPE65、LRAT、RDH8、RDH12、RGR、CNGA3、ALMS1、PER1、またはIDUAの遺伝子から転写され、かつROM1、TEAD1、RDH5、NR2E3、PAX6、CRX、FSCN2、ABCA4、MYOC、TCF4、MFSD8、CTNS、NXNL1、OPTN、RLBP1、RPE65、LRAT、RDH8、RDH12、RGR、CNGA3、ALMS1、PER1、またはIDUAのタンパク質をコードする保持されたイントロン含有mRNA前駆体(RIC mRNA前駆体)の存在を活用する。成熟し完全にスプライシングされたROM1、TEAD1、RDH5、NR2E3、PAX6、CRX、FSCN2、ABCA4、MYOC、TCF4、MFSD8、CTNS、NXNL1、OPTN、RLBP1、RPE65、LRAT、RDH8、RDH12、RGR、CNGA3、ALMS1、PER1、またはIDUAのmRNAを産生するためのROM1、TEAD1、RDH5、NR2E3、PAX6、CRX、FSCN2、ABCA4、MYOC、TCF4、MFSD8、CTNS、NXNL1、OPTN、RLBP1、RPE65、LRAT、RDH8、RDH12、RGR、CNGA3、ALMS1、PER1、またはIDUAのRIC mRNA種のスプライシングは、保持されたイントロンのスプライシングアウトを刺激するASOを使用して誘発させることができる。結果としてもたらされる成熟したROM1、TEAD1、RDH5、NR2E3、PAX6、CRX、FSCN2、ABCA4、MYOC、TCF4、MFSD8、CTNS、NXNL1、OPTN、RLBP1、RPE65、LRAT、RDH8、RDH12、RGR、CNGA3、ALMS1、PER1、またはIDUAのmRNAは、細胞質へ輸送され、そして翻訳され、それによって、患者の細胞において、ROM1、TEAD1、RDH5、NR2E3、PAX6、CRX、FSCN2、ABCA4、MYOC、TCF4、MFSD8、CTNS、NXNL1、OPTN、RLBP1、RPE65、LRAT、RDH8、RDH12、RGR、CNGA3、ALMS1、PER1またはIDUAタンパク質を増加させ、かつROM1、TEAD1、RDH5、NR2E3、PAX6、CRX、FSCN2、ABCA4、MYOC、TCF4、MFSD8、CTNS、NXNL1、OPTN、RLBP1、RPE65、LRAT、RDH8、RDH12、RGR、CNGA3、ALMS1、PER1、またはIDUAの不足によって引き起こる眼の疾患または疾病の症状を緩和させることができる。この方法は、以下で更に説明され、核内遺伝子出力の標的化増大(TANGO)として知られる。
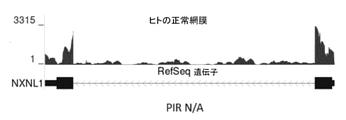
ROM1、TEAD1、RDH5、NR2E3、PAX6、CRX、FSCN2、ABCA4、MYOC、TCF4、MFSD8、CTNS、NXNL1、OPTN、RLBP1、RPE65、LRAT、RDH8、RDH12、RGR、CNGA3、ALMS1、PER1、またはIDUAの遺伝子は、イントロン保持事象に対して分析されうる。RNA配列決定(RNAseq)は、UCSCゲノムブラウザにおいて視覚化することができ、ARPE-19において発現され、細胞質または核分画のいずれかにおいて局地化されたROM1、TEAD1、RDH5、NR2E3、PAX6、CRX、FSCN2、ABCA4、MYOC、TCF4、MFSD8、CTNS、NXNL1、OPTN、RLBP1、RPE65、LRAT、RDH8、RDH12、RGR、CNGA3、ALMS1、PER1、またはIDUAの転写産物を示す。保持されたイントロン含有mRNA前駆体の転写産物は、核に保持され、細胞質には輸送されない。
いくつかの実施形態では、本明細書に開示されるASOは、ABCA4ゲノム配列から転写されたRIC mRNA前駆体(ABCA4 RIC mRNA前駆体)を標的とする。いくつかの実施形態では、ABCA4ゲノム配列はSEQ ID NO:1である。いくつかの実施形態では、ABCA4 RIC mRNA前駆体は、SEQ ID NO:24である。いくつかの実施形態では、ABCA4 RIC mRNA前駆体の転写産物は、保持されたイントロン40、および/または38、および/または36、および/または44、および/または39を含む。いくつかの実施形態では、ABCA4 RIC mRNA前駆体の転写産物が保持されたイントロン40を含むとき、本明細書に開示されるASOはSEQ ID NO:26674を標的とする。いくつかの実施形態では、ABCA4 RIC mRNA前駆体の転写産物が保持されたイントロン38を含むとき、本明細書に開示されるASOはSEQ ID NO:26706を標的とする。いくつかの実施形態では、ABCA4 RIC mRNA前駆体の転写産物が保持されたイントロン36を含むとき、本明細書に開示されるASOはSEQ ID NO:26656を標的とする。いくつかの実施形態では、ABCA4 RIC mRNA前駆体の転写産物が保持されたイントロン44を含むとき、本明細書に開示されるASOはSEQ ID NO:26681を標的とする。いくつかの実施形態では、ABCA4 RIC mRNA前駆体の転写産物が保持されたイントロン39を含むとき、本明細書に開示されるASOはSEQ ID NO:26664を標的とする。いくつかの実施形態では、ABCA4 RIC mRNA前駆体の転写産物が保持されたイントロン40を含むとき、ASOはSEQ ID NO:84-315のいずれか1つに係る配列を有する。いくつかの実施形態では、ABCA4 RIC mRNA前駆体の転写産物が保持されたイントロン38を含むとき、ASOはSEQ ID NO:316-543のいずれか1つに係る配列を有する。いくつかの実施形態では、ABCA4 RIC mRNA前駆体の転写産物が保持されたイントロン36を含むとき、ASOはSEQ ID NO:544-774のいずれか1つに係る配列を有する。いくつかの実施形態では、ABCA4 RIC mRNA前駆体の転写産物が保持されたイントロン44を含むとき、ASOはSEQ ID NO:775-1016のいずれか1つに係る配列を有する。いくつかの実施形態では、ABCA4 RIC mRNA前駆体の転写産物が保持されたイントロン39を含むとき、ASOはSEQ ID NO:1017-1126のいずれか1つに係る配列を有する。いくつかの実施形態では、ASOは、ABCA4 RIC mRNA前駆体の配列を標的とする。
いくつかの実施形態では、本明細書に開示されるASOは、RPE65ゲノム配列から転写されたRIC mRNA前駆体(RPE65 RIC mRNA前駆体)を標的とする。いくつかの実施形態では、RPE65ゲノム配列はSEQ ID NO:2である。いくつかの実施形態では、RPE65 RIC mRNA前駆体は、SEQ ID NO:25である。いくつかの実施形態では、RPE65 RIC mRNA前駆体の転写産物は、保持されたイントロン9および/または10を含む。いくつかの実施形態では、RPE65 RIC mRNA前駆体の転写産物が保持されたイントロン9を含むとき、本明細書に開示されるASOはSEQ ID NO:26691を標的とする。いくつかの実施形態では、RPE65 RIC mRNA前駆体の転写産物が保持されたイントロン10を含むとき、本明細書に開示されるASOはSEQ ID NO:26671を標的とする。いくつかの実施形態では、RPE65 RIC mRNA前駆体の転写産物が保持されたイントロン9を含むとき、ASOはSEQ ID NO:1127-1293のいずれか1つに係る配列を有する。いくつかの実施形態では、RPE65 RIC mRNA前駆体の転写産物が保持されたイントロン10を含むとき、ASOはSEQ ID NO:1294-1528のいずれか1つに係る配列を有する。いくつかの実施形態では、ASOは、PRE65 RIC mRNA前駆体の配列を標的とする。
いくつかの実施形態では、本明細書に開示されるASOは、MYOCゲノム配列から転写されたRIC mRNA前駆体(MYOC RIC mRNA前駆体)を標的とする。いくつかの実施形態では、MYOCゲノム配列はSEQ ID NO:3である。いくつかの実施形態では、MYOC RIC mRNA前駆体は、SEQ ID NO:26である。いくつかの実施形態では、MYOC RIC mRNA前駆体の転写産物は保持されたイントロン1および/または2を含む。いくつかの実施形態では、MYOC RIC mRNA前駆体の転写産物が保持されたイントロン1を含むとき、本明細書に開示されるASOは、SEQ ID NO:26669を標的とする。いくつかの実施形態では、MYOC RIC mRNA前駆体の転写産物が保持されたイントロン2を含むとき、本明細書に開示されるASOは、SEQ ID NO:26696を標的とする。いくつかの実施形態では、MYOC RIC mRNA前駆体の転写産物が保持されたイントロン1を含むとき、ASOはSEQ ID NO:1529-1855のいずれか1つに係る配列を有する。いくつかの実施形態では、MYOC RIC mRNA前駆体の転写産物が保持されたイントロン2を含むとき、ASOはSEQ ID NO:1856-2318のいずれか1つに係る配列を有する。いくつかの実施形態では、ASOは、MYOC RIC mRNA前駆体の配列を標的とする。
いくつかの実施形態では、本明細書に開示されるASOは、CNGA3ゲノム配列から転写されたRIC mRNA前駆体(CNGA3 RIC mRNA前駆体)を標的とする。いくつかの実施形態では、CNGA3ゲノム配列はSEQ ID NO:4である。いくつかの実施形態では、CNGA3 RIC mRNA前駆体は、SEQ ID NO:27または28である。いくつかの実施形態では、CNGA3 RIC mRNA前駆体の転写産物は保持されたイントロン6および/または5を含む。いくつかの実施形態では、CNGA3 RIC mRNA前駆体の転写産物が保持されたイントロン6を含むとき、本明細書に開示されるASOはSEQ ID NO:26711を標的とする。いくつかの実施形態では、CNGA3 RIC mRNA前駆体の転写産物が保持されたイントロン5を含むとき、本明細書に開示されるASOはSEQ ID NO:26711を標的とする。いくつかの実施形態では、CNGA3 RIC mRNA前駆体の転写産物が保持されたイントロン6を含むとき、ASOはSEQ ID NO:2319-2544のいずれか1つに係る配列を有する。いくつかの実施形態では、CNGA3 RIC mRNA前駆体の転写産物が保持されたイントロン5を含むとき、ASOはSEQ ID NO:2545-2770のいずれか1つに係る配列を有する。いくつかの実施形態では、ASOは、CNGA3 RIC mRNA前駆体の配列を標的とする。
いくつかの実施形態では、本明細書に開示されるASOは、MFSD8ゲノム配列から転写されたRIC mRNA前駆体(MFSD8 RIC mRNA前駆体)を標的とする。いくつかの実施形態では、MFSD8ゲノム配列はSEQ ID NO:5である。いくつかの実施形態では、MFSD8 RIC mRNA前駆体は、SEQ ID NO:29である。いくつかの実施形態では、MFSD8 RIC mRNA前駆体の転写産物は保持されたイントロン11および/または12を含む。いくつかの実施形態では、MFSD8 RIC mRNA前駆体の転写産物が保持されたイントロン11を含むとき、本明細書に開示されるASOはSEQ ID NO:26703を標的とする。いくつかの実施形態では、MFSD8 RIC mRNA前駆体の転写産物が保持されたイントロン12を含むとき、本明細書に開示されるASOはSEQ ID NO:26708を標的とする。いくつかの実施形態では、MFSD8 RIC mRNA前駆体の転写産物が保持されたイントロン11を含むとき、ASOはSEQ ID NO:2771-2852のいずれか1つに係る配列を有する。いくつかの実施形態では、MFSD8 RIC mRNA前駆体の転写産物が保持されたイントロン12を含むとき、ASOはSEQ ID NO:2853-3631のいずれか1つに係る配列を有する。いくつかの実施形態では、ASOは、MFSD8 RIC mRNA前駆体の配列を標的とする。
いくつかの実施形態では、本明細書に開示されるASOは、IDUAゲノム配列から転写されたRIC mRNA前駆体(IDUA RIC mRNA前駆体)を標的とする。いくつかの実施形態では、IDUAゲノム配列はSEQ ID NO:6である。いくつかの実施形態では、IDUA RIC mRNA前駆体は、SEQ ID NO:30または31である。いくつかの実施形態では、IDUA RIC mRNA前駆体の転写産物は保持されたイントロン3、および/または4、および/または5、および/または6、および/または7を含む。いくつかの実施形態では、IDUA RIC mRNA前駆体の転写産物が保持されたイントロン3を含むとき、本明細書に開示されるASOは、SEQ ID NO:26668を標的とする。いくつかの実施形態では、IDUA RIC mRNA前駆体の転写産物が保持されたイントロン4を含むとき、本明細書に開示されるASOは、SEQ ID NO:26679を標的とする。いくつかの実施形態では、IDUA RIC mRNA前駆体の転写産物が保持されたイントロン5を含むとき、本明細書に開示されるASOは、SEQ ID NO:26700を標的とする。いくつかの実施形態では、IDUA RIC mRNA前駆体の転写産物が保持されたイントロン6を含むとき、本明細書に開示されるASOは、SEQ ID NO:26655を標的とする。いくつかの実施形態では、IDUA RIC mRNA前駆体の転写産物が保持されたイントロン7を含むとき、本明細書に開示されるASOは、SEQ ID NO:26663を標的とする。いくつかの実施形態では、IDUA RIC mRNA前駆体の転写産物が保持されたイントロン3を含むとき、ASOはSEQ ID NO:3632-3697または4038-4103のいずれか1つに係る配列を有する。いくつかの実施形態では、IDUA RIC mRNA前駆体の転写産物が保持されたイントロン4を含むとき、ASOはSEQ ID NO:3698-3813または4104-4219のいずれか1つに係る配列を有する。いくつかの実施形態では、IDUA RIC mRNA前駆体の転写産物が保持されたイントロン5を含むとき、ASOはSEQ ID NO:3814-3879または4220-4285のいずれか1つに係る配列を有する。いくつかの実施形態では、IDUA RIC mRNA前駆体の転写産物が保持されたイントロン6を含むとき、ASOはSEQ ID NO:3880-3952または4286-4358のいずれか1つに係る配列を有する。いくつかの実施形態では、IDUA RIC mRNA前駆体の転写産物が保持されたイントロン7を含むとき、ASOはSEQ ID NO:3953-4037または4359-4443のいずれか1つに係る配列を有する。いくつかの実施形態では、ASOは、IDUA RIC mRNA前駆体の配列を標的とする。
いくつかの実施形態では、本明細書に開示されるASOは、LRATゲノム配列から転写されたRIC mRNA前駆体(LRAT RIC mRNA前駆体)を標的とする。いくつかの実施形態では、LRATゲノム配列はSEQ ID NO:7である。いくつかの実施形態では、LRAT RIC mRNA前駆体は、SEQ ID NO:32または33である。いくつかの実施形態では、LRAT RIC mRNA前駆体の転写産物は、保持されたイントロン2を含む。いくつかの実施形態では、LRAT RIC mRNA前駆体の転写産物が保持されたイントロン2を含むとき、本明細書に開示されるASOはSEQ ID NO:26685を標的とする。いくつかの実施形態では、LRAT RIC mRNA前駆体の転写産物が保持されたイントロン2を含むとき、ASOはSEQ ID NO:4444-6647のいずれか1つに係る配列を有する。いくつかの実施形態では、ASOは、LRAT RIC mRNA前駆体の配列を標的とする。
いくつかの実施形態では、本明細書に開示されるASOは、OPTNゲノム配列から転写されたRIC mRNA前駆体(OPTN RIC mRNA前駆体)を標的とする。いくつかの実施形態では、OPTNゲノム配列はSEQ ID NO:8である。いくつかの実施形態では、OPTN RIC mRNA前駆体はSEQ ID NO:34、35、36、または37である。いくつかの実施形態では、OPTN RIC mRNA前駆体の転写産物は保持されたイントロン9または8または7を含む。いくつかの実施形態では、OPTN RIC mRNA前駆体の転写産物が保持されたイントロン9を含むとき、本明細書に開示されるASOはSEQ ID NO:26714を標的とする。いくつかの実施形態では、OPTN RIC mRNA前駆体の転写産物が保持されたイントロン8を含むとき、本明細書に開示されるASOはSEQ ID NO:26714を標的とする。いくつかの実施形態では、OPTN RIC mRNA前駆体の転写産物が保持されたイントロン7を含むとき、本明細書に開示されるASOはSEQ ID NO:26714を標的とする。いくつかの実施形態では、OPTN RIC mRNA前駆体の転写産物が保持されたイントロン9を含むとき、ASOはSEQ ID NO:6648-6880または7114-7346のいずれか1つに係る配列を有する。いくつかの実施形態では、OPTN RIC mRNA前駆体の転写産物が保持されたイントロン8を含むとき、ASOはSEQ ID NO:6881-7113のいずれか1つに係る配列を有する。いくつかの実施形態では、OPTN RIC mRNA前駆体の転写産物が保持されたイントロン7を含むとき、ASOはSEQ ID NO:7347-7579のいずれか1つに係る配列を有する。いくつかの実施形態では、ASOは、OPTN RIC mRNA前駆体の配列を標的とする。
いくつかの実施形態では、本明細書に開示されるASOは、RGRゲノム配列から転写されたRIC mRNA前駆体(RGR RIC mRNA前駆体)を標的とする。いくつかの実施形態では、RGRゲノム配列はSEQ ID NO:9である。いくつかの実施形態では、RGR RIC mRNA前駆体はSEQ ID NO:38、39、または40である。いくつかの実施形態では、RGR RIC mRNA前駆体の転写産物は保持されたイントロン1および/または2を含む。いくつかの実施形態では、RGR RIC mRNA前駆体の転写産物が保持されたイントロン1を含むとき、本明細書に開示されるASOはSEQ ID NO:26657を標的とする。いくつかの実施形態では、RGR RIC mRNA前駆体の転写産物が保持されたイントロン2を含むとき、本明細書に開示されるASOはSEQ ID NO:26687または26683を標的とする。いくつかの実施形態では、RGR RIC mRNA前駆体の転写産物が保持されたイントロン1を含むとき、ASOはSEQ ID NO:7580-7806、8041-8267、または8500-8726のいずれか1つに係る配列を有する。いくつかの実施形態では、RGR RIC mRNA前駆体の転写産物が保持されたイントロン2を含むとき、ASOはSEQ ID NO:7807-8040、8268-8499、または8727-8958のいずれか1つに係る配列を有する。いくつかの実施形態では、ASOは、RGR RIC mRNA前駆体の配列を標的とする。
いくつかの実施形態では、本明細書に開示されるASOは、TEAD1ゲノム配列から転写されたRIC mRNA前駆体(TEAD1 RIC mRNA前駆体)を標的とする。いくつかの実施形態では、TEAD1ゲノム配列はSEQ ID NO:10である。いくつかの実施形態では、TEAD1 RIC mRNA前駆体はSEQ ID NO:41である。いくつかの実施形態では、TEAD1 RIC mRNA前駆体の転写産物は、保持されたイントロン4を含む。いくつかの実施形態では、TEAD1 RIC mRNA前駆体の転写産物が保持されたイントロン4を含むとき、本明細書に開示されるASOはSEQ ID NO:26672を標的とする。いくつかの実施形態では、TEAD1 RIC mRNA前駆体の転写産物が保持されたイントロン4を含むとき、ASOはSEQ ID NO:8959-9163のいずれか1つに係る配列を有する。いくつかの実施形態では、ASOは、TEAD1 RIC mRNA前駆体の配列を標的とする。
いくつかの実施形態では、本明細書に開示されるASOは、PAX6ゲノム配列から転写されたRIC mRNA前駆体(PAX6 RIC mRNA前駆体)を標的とする。いくつかの実施形態では、PAX6ゲノム配列はSEQ ID NO:11である。いくつかの実施形態では、PAX6 RIC mRNA前駆体は、SEQ ID NO:42、43、44、45、46、47、48、49、50、51、または52である。いくつかの実施形態では、PAX6 RIC mRNA前駆体の転写産物は保持されたイントロン2および/または3、または、1および/または3および/または4、または、3および/または4および/または5、または、4および/または5および/または6、または、4および/または6および/または7、または、2および/または3および/または4を含む。いくつかの実施形態では、PAX6 RIC mRNA前駆体の転写産物が保持されたイントロン1を含むとき、本明細書に開示されるASOはSEQ ID NO:26707を標的とする。いくつかの実施形態では、PAX6 RIC mRNA前駆体の転写産物が保持されたイントロン2を含むとき、本明細書に開示されるASOはSEQ ID NO:26697または26694を標的とする。いくつかの実施形態では、PAX6 RIC mRNA前駆体の転写産物が保持されたイントロン3を含むとき、本明細書に開示されるASOはSEQ ID NO:26677、26678、26694、または26659を標的とする。いくつかの実施形態では、PAX6 RIC mRNA前駆体の転写産物が保持されたイントロン4を含むとき、本明細書に開示されるASOはSEQ ID NO:26713、26659、または26694を標的とする。いくつかの実施形態では、PAX6 RIC mRNA前駆体の転写産物が保持されたイントロン5を含むとき、本明細書に開示されるASOはSEQ ID NO:26713または26659を標的とする。いくつかの実施形態では、PAX6 RIC mRNA前駆体の転写産物が保持されたイントロン6を含むとき、本明細書に開示されるASOはSEQ ID NO:26713または26678を標的とする。いくつかの実施形態では、PAX6 RIC mRNA前駆体の転写産物が保持されたイントロン7を含むとき、本明細書に開示されるASOはSEQ ID NO:26713を標的とする。いくつかの実施形態では、PAX6 RIC mRNA前駆体の転写産物が保持されたイントロン1を含むとき、ASOはSEQ ID NO:9508-9774のいずれか1つに係る配列を有する。いくつかの実施形態では、PAX6 RIC mRNA前駆体の転写産物が保持されたイントロン2を含むとき、ASOはSEQ ID NO:9164-9296または13581-13780のいずれか1つに係る配列を有する。いくつかの実施形態では、PAX6 RIC mRNA前駆体の転写産物が保持されたイントロン3を含むとき、ASOはSEQ ID NO:9297-9507、9775-9841、10053-10252、または13781-14012のいずれか1つに係る配列を有する。いくつかの実施形態では、PAX6 RIC前駆体mRNAの転写産物が保持されたイントロン4を含むとき、ASOは、SEQ ID NO:9842-10052、10253-10484、10696-10895、11339-11538、11982-12181、12460-12659、13103-13302、14013-14423、または14702-14901のいずれか1つに係る配列を有する。いくつかの実施形態では、PAX6 RIC mRNA前駆体の転写産物が保持されたイントロン5を含むとき、ASOはSEQ ID NO:10485-10695、10896-11127、11539-11770、または12660-12891のいずれか1つに係る配列を有する。いくつかの実施形態では、PAX6 RIC mRNA前駆体の転写産物が保持されたイントロン6を含むとき、ASOは、SEQ ID NO:11128-11338、11771-11981、12182-12248、12892-13102、13303-13369、14424-14490、または14902-14968のいずれか1つに係る配列を有する。いくつかの実施形態では、PAX6 RIC mRNA前駆体の転写産物が保持されたイントロン7を含むとき、ASOはSEQ ID NO:12249-12459、13370-13580、14491-14701、または14969-15179のいずれか1つに係る配列を有する。いくつかの実施形態では、ASOは、PAX6 RIC mRNA前駆体の配列を標的とする。
いくつかの実施形態では、本明細書に開示されるASOは、ROM1ゲノム配列から転写されたRIC mRNA前駆体(ROM1 RIC mRNA前駆体)を標的とする。いくつかの実施形態では、ROM1ゲノム配列はSEQ ID NO:12である。いくつかの実施形態では、ROM1 RIC mRNA前駆体はSEQ ID NO:53である。いくつかの実施形態では、ROM1 RIC mRNA前駆体の転写産物は保持されたイントロン1を含む。いくつかの実施形態では、ROM1 RIC mRNA前駆体の転写産物が保持されたイントロン1を含むとき、本明細書に開示されるASOはSEQ ID NO:26665を標的とする。いくつかの実施形態では、ROM1 RIC mRNA前駆体の転写産物が保持されたイントロン1を含むとき、ASOはSEQ ID NO:15180-15486のいずれか1つに係る配列を有する。いくつかの実施形態では、ASOは、ROM1 RIC mRNA前駆体の配列を標的とする。
いくつかの実施形態では、本明細書に開示されるASOは、RDH5ゲノム配列から転写されたRIC mRNA前駆体(RDH5 RIC mRNA前駆体)を標的とする。いくつかの実施形態では、RDH5ゲノム配列はSEQ ID NO:13である。いくつかの実施形態では、RDH5 RIC mRNA前駆体はSEQ ID NO:54または55である。いくつかの実施形態では、RDH5 RIC mRNA前駆体の転写産物は保持されたイントロン1および/または2を含む。いくつかの実施形態では、RDH5 RIC mRNA前駆体の転写産物が保持されたイントロン1を含むとき、本明細書に開示されるASOはSEQ ID NO:26704または26709を標的とする。いくつかの実施形態では、RDH5 RIC mRNA前駆体の転写産物が保持されたイントロン2を含むとき、本明細書に開示されるASOはSEQ ID NO:26666または26684を標的とする。いくつかの実施形態では、RDH5 RIC mRNA前駆体の転写産物が保持されたイントロン1を含むとき、ASOはSEQ ID NO:15487-15700または15845-16057のいずれか1つに係る配列を有する。いくつかの実施形態では、RDH5 RIC mRNA前駆体の転写産物が保持されたイントロン2を含むとき、ASOはSEQ ID NO:15701-15844または16058-16202のいずれか1つに係る配列を有する。いくつかの実施形態では、ASOは、RDH5 RIC mRNA前駆体の配列を標的とする。
いくつかの実施形態では、本明細書に開示されるASOは、RDH12ゲノム配列から転写されたRIC mRNA前駆体(RDH12 RIC mRNA前駆体)を標的とする。いくつかの実施形態では、RDH12ゲノム配列はSEQ ID NO:14である。いくつかの実施形態では、RDH12 RIC mRNA前駆体はSEQ ID NO:56である。いくつかの実施形態では、RDH12 RIC mRNA前駆体の転写産物は、保持されたイントロン7を含む。いくつかの実施形態では、RDH12 RIC mRNA前駆体の転写産物が保持されたイントロン7を含むとき、本明細書に開示されるASOはSEQ ID NO:26693を標的とする。いくつかの実施形態では、RDH12 RIC mRNA前駆体の転写産物が保持されたイントロン7を含むとき、ASOはSEQ ID NO:16203-16458のいずれか1つに係る配列を有する。いくつかの実施形態では、ASOは、RDH12 RIC mRNA前駆体の配列を標的とする。
幾つかの実施形態では、本明細書に開示されるASOは、NR2E3ゲノム配列から転写されたRIC mRNA前駆体(NR2E3 RIC mRNA前駆体)を標的とする。いくつかの実施形態では、NR2E3ゲノム配列はSEQ ID NO:15である。いくつかの実施形態では、NR2E3 RIC mRNA前駆体は、SEQ ID NO:57または58である。いくつかの実施形態では、NR2E3 RIC mRNA前駆体の転写産物は保持されたイントロン1、および/または2、および/または3、および/または4、および/または5、および/または6、および/または7を含む。いくつかの実施形態では、NR2E3 RIC mRNA前駆体の転写産物が保持されたイントロン1を含むとき、本明細書に開示されるASOはSEQ ID NO:26702を標的とする。いくつかの実施形態では、NR2E3 RIC mRNA前駆体の転写産物が保持されたイントロン2を含むとき、本明細書に開示されるASOはSEQ ID NO:26660を標的とする。いくつかの実施形態では、NR2E3 RIC mRNA前駆体の転写産物が保持されたイントロン3を含むとき、本明細書に開示されるASOはSEQ ID NO:26705を標的とする。いくつかの実施形態では、NR2E3 RIC mRNA前駆体の転写産物が保持されたイントロン4を含むとき、本明細書に開示されるASOはSEQ ID NO:26698を標的とする。いくつかの実施形態では、NR2E3 RIC mRNA前駆体の転写産物が保持されたイントロン5を含むとき、本明細書に開示されるASOはSEQ ID NO:26658を標的とする。いくつかの実施形態では、NR2E3 RIC mRNA前駆体の転写産物が保持されたイントロン6を含むとき、本明細書に開示されるASOはSEQ ID NO:26676を標的とする。いくつかの実施形態では、NR2E3 RIC mRNA前駆体の転写産物が保持されたイントロン7を含むとき、本明細書に開示されるASOはSEQ ID NO:26712または26701を標的とする。いくつかの実施形態では、NR2E3 RIC mRNA前駆体の転写産物が保持されたイントロン1を含むとき、ASOはSEQ ID NO:16459-1661または17255-17457のいずれか1つに係る配列を有する。いくつかの実施形態では、NR2E3 RIC mRNA前駆体の転写産物が保持されたイントロン2を含むとき、ASOはSEQ ID NO:16662-16272または17458-17523のいずれか1つに係る配列を有する。いくつかの実施形態では、NR2E3 RIC mRNA前駆体の転写産物が保持されたイントロン3を含むとき、ASOはSEQ ID NO:16728-16798または17524-17594のいずれか1つに係る配列を有する。いくつかの実施形態では、NR2E3 RIC mRNA前駆体の転写産物が保持されたイントロン4を含むとき、ASOはSEQ ID NO:16799-16890または17595-17686のいずれか1つに係る配列を有する。いくつかの実施形態では、NR2E3 RIC mRNA前駆体の転写産物が保持されたイントロン5を含むとき、ASOはSEQ ID NO:16891-17127または17687-17923のいずれか1つに係る配列を有する。いくつかの実施形態では、NR2E3 RIC mRNA前駆体の転写産物が保持されたイントロン6を含むとき、ASOはSEQ ID NO:17128-17169または17924-17965.のいずれか1つに係る配列を有する。いくつかの実施形態では、NR2E3 RIC mRNA前駆体の転写産物が保持されたイントロン7を含むとき、ASOはSEQ ID NO:17170-17254または17966-18209のいずれか1つに係る配列を有する。いくつかの実施形態では、ASOは、NR2E3 RIC mRNA前駆体の配列を標的とする。
いくつかの実施形態では、本明細書に開示されるASOは、RLBP1ゲノム配列から転写されたRIC mRNA前駆体(RLBP1 RIC mRNA前駆体)を標的とする。いくつかの実施形態では、RLBP1ゲノム配列はSEQ ID NO:16である。いくつかの実施形態では、RLBP1 RIC mRNA前駆体はSEQ ID NO:59である。いくつかの実施形態では、RLBP1 RIC mRNA前駆体の転写産物が保持されたイントロン2および/または5を含む。いくつかの実施形態では、RLBP1 RIC mRNA前駆体の転写産物が保持されたイントロン2を含むとき、本明細書に開示されるASOはSEQ ID NO:26673を標的とする。いくつかの実施形態では、RLBP1 RIC mRNA前駆体の転写産物が保持されたイントロン5を含むとき、本明細書に開示されるASOはSEQ ID NO:26667を標的とする。いくつかの実施形態では、RLBP1 RIC mRNA前駆体の転写産物が保持されたイントロン2を含むとき、ASOはSEQ ID NO:18210-18383のいずれか1つに係る配列を有する。いくつかの実施形態では、RLBP1 RIC mRNA前駆体の転写産物が保持されたイントロン5を含むとき、ASOはSEQ ID NO:18384-18638のいずれか1つに係る配列を有する。いくつかの実施形態では、ASOは、RLBP1 RIC mRNA前駆体の配列を標的とする。
いくつかの実施形態では、本明細書に開示されるASOは、CTNSゲノム配列から転写されたRIC mRNA前駆体(CTNS RIC mRNA前駆体)を標的とする。いくつかの実施形態では、CTNSゲノム配列はSEQ ID NO:17である。いくつかの実施形態では、CTNS RIC mRNA前駆体はSEQ ID NO:60または61である。いくつかの実施形態では、CTNS RIC mRNA前駆体の転写産物は保持されたイントロン9および/または10を含む。いくつかの実施形態では、CTNS RIC mRNA前駆体の転写産物が保持されたイントロン9を含むとき、本明細書に開示されるASOはSEQ ID NO:26690を標的とする。いくつかの実施形態では、CTNS RIC mRNA前駆体の転写産物が保持されたイントロン10を含むとき、本明細書に開示されるASOはSEQ ID NO:26692を標的とする。いくつかの実施形態では、CTNS RIC mRNA前駆体の転写産物が保持されたイントロン9を含むとき、ASOはSEQ ID NO:18639-18861または19087-19309のいずれか1つに係る配列を有する。いくつかの実施形態では、CTNS RIC mRNA前駆体の転写産物が保持されたイントロン10を含むとき、ASOはSEQ ID NO:18862-19086または19310-19534のいずれか1つに係る配列を有する。いくつかの実施形態では、ASOは、CTNS RIC mRNA前駆体の配列を標的とする。
いくつかの実施形態では、本明細書に開示されるASOは、PER1ゲノム配列から転写されたRIC mRNA前駆体(PER1 RIC mRNA前駆体)を標的とする。いくつかの実施形態では、PER1ゲノム配列はSEQ ID NO:18である。いくつかの実施形態では、PER1 RIC mRNA前駆体はSEQ ID NO:62である。いくつかの実施形態では、PER1 RIC mRNA前駆体の転写産物は保持されたイントロン1および/または14を含む。いくつかの実施形態では、PER1 RIC mRNA前駆体の転写産物が保持されたイントロン1を含むとき、本明細書に開示されるASOはSEQ ID NO:26682を標的とする。いくつかの実施形態では、PER1 RIC mRNA前駆体の転写産物が保持されたイントロン14を含むとき、本明細書に開示されるASOはSEQ ID NO:26710を標的とする。いくつかの実施形態では、PER1 RIC mRNA前駆体の転写産物が保持されたイントロン1を含むとき、ASOはSEQ ID NO:19535-19782のいずれか1つに係る配列を有する。いくつかの実施形態では、PER1 RIC mRNA前駆体の転写産物が保持されたイントロン14を含むとき、ASOはSEQ ID NO:19783-19845のいずれか1つに係る配列を有する。いくつかの実施形態では、ASOは、PER1 RIC mRNA前駆体の配列を標的とする。
いくつかの実施形態では、本明細書に開示されるASOは、FSCN2ゲノム配列から転写されたRIC mRNA前駆体(FSCN2 RIC mRNA前駆体)を標的とする。いくつかの実施形態では、FSCN2ゲノム配列はSEQ ID NO:19である。いくつかの実施形態では、FSCN2 RIC mRNA前駆体はSEQ ID NO:63または64である。いくつかの実施形態では、FSCN2 RIC mRNA前駆体の転写産物は保持されたイントロン1および/または3を含む。いくつかの実施形態では、FSCN2 RIC mRNA前駆体の転写産物が保持されたイントロン1を含むとき、本明細書に開示されるASOはSEQ ID NO:26670を標的とする。いくつかの実施形態では、FSCN2 RIC mRNA前駆体の転写産物が保持されたイントロン3を含むとき、本明細書に開示されるASOはSEQ ID NO:26662または26661を標的とする。いくつかの実施形態では、FSCN2 RIC mRNA前駆体の転写産物が保持されたイントロン1を含むとき、ASOはSEQ ID NO:19846-20232または20348-20734のいずれか1つに係る配列を有する。いくつかの実施形態では、FSCN2 RIC mRNA前駆体の転写産物が保持されたイントロン3を含むとき、ASOはSEQ ID NO:20233-20347または20735-20849のいずれか1つに係る配列を有する。いくつかの実施形態では、ASOは、FSCN2 RIC mRNA前駆体の配列を標的とする。
いくつかの実施形態では、本明細書に開示されるASOは、TCF4ゲノム配列 から転写されたRIC mRNA前駆体(TCF4 RIC mRNA前駆体)を標的とする。いくつかの実施形態では、TCF4ゲノム配列はSEQ ID NO:20である。いくつかの実施形態では、TCF4 RIC mRNA前駆体は、SEQ ID NO:65、66、67、68、69、70、71、72、73、74、75、76、77、78、79、または80である。いくつかの実施形態では、TCF4 RIC mRNA前駆体の転写産物は保持されたイントロン9、12、14、16、15、17、または11を含む。いくつかの実施形態では、TCF4 RIC mRNA前駆体の転写産物が保持されたイントロン9を含むとき、本明細書に開示されるASOはSEQ ID NO:26688を標的とする。いくつかの実施形態では、TCF4 RIC mRNA前駆体の転写産物が保持されたイントロン12を含むとき、本明細書に開示されるASOはSEQ ID NO:26688または26689を標的とする。いくつかの実施形態では、TCF4 RIC mRNA前駆体の転写産物が保持されたイントロン14を含むとき、本明細書に開示されるASOはSEQ ID NO:26688を標的とする。いくつかの実施形態では、TCF4 RIC mRNA前駆体の転写産物が保持されたイントロン16を含むとき、本明細書に開示されるASOはSEQ ID NO:26688または26689を標的とする。いくつかの実施形態では、TCF4 RIC mRNA前駆体の転写産物が保持されたイントロン15を含むとき、本明細書に開示されるASOはSEQ ID NO:26688または26689を標的とする。いくつかの実施形態では、TCF4 RIC mRNA前駆体の転写産物が保持されたイントロン17を含むとき、本明細書に開示されるASOはSEQ ID NO:26689を標的とする。いくつかの実施形態では、TCF4 RIC mRNA前駆体の転写産物が保持されたイントロン11を含むとき、本明細書に開示されるASOはSEQ ID NO:26689を標的とする。いくつかの実施形態では、TCF4 RIC mRNA前駆体の転写産物が保持されたイントロン9を含むとき、ASOはSEQ ID NO:20860-21577のいずれか1つに係る配列を有する。いくつかの実施形態では、TCF4 RIC mRNA前駆体の転写産物が保持されたイントロン12を含むとき、ASOはSEQ ID NO:21578-22063または22790-23031のいずれか1つに係る配列を有する。いくつかの実施形態では、TCF4 RIC mRNA前駆体の転写産物が保持されたイントロン14を含むとき、ASOはSEQ ID NO:22064-22305のいずれか1つに係る配列を有する。いくつかの実施形態では、TCF4 RIC mRNA前駆体の転写産物が保持されたイントロン16を含むとき、ASOはSEQ ID NO:22306-22547、23276-23519、24006-24249、または24494-24737のいずれか1つに係る配列を有する。いくつかの実施形態では、TCF4 RIC mRNA前駆体の転写産物が保持されたイントロン15を含むとき、ASOはSEQ ID NO:22548-22789、23032-23275、または23510-23761のいずれか1つに係る配列を有する。いくつかの実施形態では、TCF4 RIC mRNA前駆体の転写産物が保持されたイントロン17を含むとき、ASOはSEQ ID NO:23762-24005のいずれか1つに係る配列を有する。いくつかの実施形態では、TCF4 RIC mRNA前駆体の転写産物が保持されたイントロン11を含むとき、ASOはSEQ ID NO:24250-24493のいずれか1つに係る配列を有する。いくつかの実施形態では、ASOは、TCF4 RIC mRNA前駆体の配列を標的とする。
いくつかの実施形態では、本明細書に開示されるASOは、RDH8ゲノム配列から転写されたRIC mRNA前駆体(RDH8 RIC mRNA前駆体)を標的とする。いくつかの実施形態では、RDH8ゲノム配列はSEQ ID NO:21である。いくつかの実施形態では、RDH8 RIC mRNA前駆体は、SEQ ID NO:81である。いくつかの実施形態では、RDH8 RIC mRNA前駆体の転写産物は保持されたイントロン4を含む。いくつかの実施形態では、RDH8 RIC mRNA前駆体の転写産物が保持されたイントロン4を含むとき、本明細書に開示されるASOはSEQ ID NO:26680を標的とする。いくつかの実施形態では、RDH8 RIC mRNA前駆体の転写産物が保持されたイントロン4を含むとき、ASOはSEQ ID NO:24738-24873のいずれか1つに係る配列を有する。いくつかの実施形態では、ASOは、RDH8 RIC mRNA前駆体の配列を標的とする。
いくつかの実施形態では、本明細書に開示されるASOは、NXNL1ゲノム配列から転写されたRIC mRNA前駆体(NXNL1 RIC mRNA前駆体)を標的とする。いくつかの実施形態では、NXNL1ゲノム配列はSEQ ID NO:22である。いくつかの実施形態では、NXNL1 RIC mRNA前駆体はSEQ ID NO:82である。いくつかの実施形態では、NXNL1 RIC mRNA前駆体の転写産物は保持されたイントロン1を含む。いくつかの実施形態では、NXNL1 RIC mRNA前駆体の転写産物が保持されたイントロン1を含むとき、本明細書に開示されるASOはSEQ ID NO:26699を標的とする。いくつかの実施形態では、NXNL1 RIC mRNA前駆体の転写産物が保持されたイントロン1を含むとき、ASOはSEQ ID NO:24874-25231のいずれか1つに係る配列を有する。いくつかの実施形態では、ASOは、NXNL1 RIC mRNA前駆体の配列を標的とする。
いくつかの実施形態では、本明細書に開示されるASOは、CRXゲノム配列から転写されたRIC mRNA前駆体(CRX RIC mRNA前駆体)を標的とする。いくつかの実施形態では、CRXゲノム配列はSEQ ID NO:23である。いくつかの実施形態では、CRX RIC mRNA前駆体はSEQ ID NO:83である。いくつかの実施形態では、CRX RIC mRNA前駆体の転写産物は、保持されたイントロン1、および/または2、および/または3を含む。いくつかの実施形態では、CRX RIC mRNA前駆体の転写産物が保持されたイントロン1を含むとき、本明細書に開示されるASOはSEQ ID NO:26675を標的とする。いくつかの実施形態では、CRX RIC mRNA前駆体の転写産物が保持されたイントロン2を含むとき、本明細書に開示されるASOはSEQ ID NO:26695を標的とする。いくつかの実施形態では、CRX RIC mRNA前駆体の転写産物が保持されたイントロン3を含むとき、本明細書に開示されるASOはSEQ ID NO:26686を標的とする。いくつかの実施形態では、CRX RIC mRNA前駆体の転写産物が保持されたイントロン1を含むとき、ASOはSEQ ID NO:25232-25465のいずれか1つに係る配列を有する。いくつかの実施形態では、CRX RIC mRNA前駆体の転写産物が保持されたイントロン2を含むとき、ASOはSEQ ID NO:25466-25695のいずれか1つに係る配列を有する。いくつかの実施形態では、CRX RIC mRNA前駆体の転写産物が保持されたイントロン3を含むとき、ASOはSEQ ID NO:25696-26654のいずれか1つに係る配列を有する。いくつかの実施形態では、ASOは、CRX RIC mRNA前駆体の配列を標的とする。
a.第1の変異対立遺伝子であって、
i)ROM1、TEAD1、RDH5、NR2E3、PAX6、CRX、FSCN2、ABCA4、MYOC、TCF4、MFSD8、CTNS、NXNL1、OPTN、RLBP1、RPE65、LRAT、RDH8、RDH12、RGR、CNGA3、ALMS1、PER1またはIDUAタンパク質が、野生型対立遺伝子からの産生と比較して、減少したレベルで産生され、
ii)ROM1、TEAD1、RDH5、NR2E3、PAX6、CRX、FSCN2、ABCA4、MYOC、TCF4、MFSD8、CTNS、NXNL1、OPTN、RLBP1、RPE65、LRAT、RDH8、RDH12、RGR、CNGA3、ALMS1、PER1またはIDUAタンパク質が、同等の野生型タンパク質と比較して機能が低下した形態で産生され、または
iii)ROM1、TEAD1、RDH5、NR2E3、PAX6、CRX、FSCN2、ABCA4、MYOC、TCF4、MFSD8、CTNS、NXNL1、OPTN、RLBP1、RPE65、LRAT、RDH8、RDH12、RGR、CNGA3、ALMS1、PER1またはIDUAタンパク質、または機能的RNAが産生されない、第1の変異対立遺伝子;および
b.第2の変異対立遺伝子であって、
i)ROM1、TEAD1、RDH5、NR2E3、PAX6、CRX、FSCN2、ABCA4、MYOC、TCF4、MFSD8、CTNS、NXNL1、OPTN、RLBP1、RPE65、LRAT、RDH8、RDH12、RGR、CNGA3、ALMS1、PER1またはIDUAタンパク質が、野生型対立遺伝子からの産生と比較して減少したレベルで産生され、
ii)ROM1、TEAD1、RDH5、NR2E3、PAX6、CRX、FSCN2、ABCA4、MYOC、TCF4、MFSD8、CTNS、NXNL1、OPTN、RLBP1、RPE65、LRAT、RDH8、RDH12、RGR、CNGA3、ALMS1、PER1またはIDUAタンパク質が、同等の野生型タンパク質と比較して機能が低下した形態で産生され、または
iii)ROM1、TEAD1、RDH5、NR2E3、PAX6、CRX、FSCN2、ABCA4、MYOC、TCF4、MFSD8、CTNS、NXNL1、OPTN、RLBP1、RPE65、LRAT、RDH8、RDH12、RGR、CNGA3、ALMS1、PER1またはIDUAタンパク質が産生されない、第2の変異対立遺伝子を有し;
ここで、RIC mRNA前駆体は、第1の対立遺伝子および/または第2の対立遺伝子から転写される。これらの実施形態では、ASOは、第1の対立遺伝子または第2の対立遺伝子から転写されたRIC mRNA前駆体の標的部分に結合することで、RIC mRNA前駆体からの保持されたイントロンの構成的スプライシングを誘導し、ROM1、TEAD1、RDH5、NR2E3、PAX6、CRX、FSCN2、ABCA4、MYOC、TCF4、MFSD8、CTNS、NXNL1、OPTN、RLBP1、RPE65、LRAT、RDH8、RDH12、RGR、CNGA3、ALMS1、PER1またはIDUAタンパク質をコードするmRNAレベルの増加を引き起こし、被験体の細胞における標的タンパク質または機能的RNAの発現の増加をもたらす。これらの実施形態では、RIC mRNA前駆体からの保持されたイントロンの構成的スプライシングの結果として生じる、発現レベルの増加を有する標的タンパク質あるいは機能的RNAは、同等の野性型タンパク質と比較して機能性の低い形態(部分的機能的)、あるいは同等の野性型タンパク質と比較して完全な機能性を有する形態(完全機能的)、のいずれかであり得る。
前述したように、実施形態では、核内遺伝子出力の標的とされた増強(TANGO)は、ROM1、TEAD1、RDH5、NR2E3、PAX6、CRX、FSCN2、ABCA4、MYOC、TCF4、MFSD8、CTNS、NXNL1、OPTN、RLBP1、RPE65、LRAT、RDH8、RDH12、RGR、CNGA3、ALMS1、PER1またはIDUAタンパク質の発現を増加させるために、本発明の方法において使用され得る。これらの実施形態では、ROM1、TEAD1、RDH5、NR2E3、PAX6、CRX、FSCN2、ABCA4、MYOC、TCF4、MFSD8、CTNS、NXNL1、OPTN、RLBP1、RPE65、LRAT、RDH8、RDH12、RGR、CNGA3、ALMS1、PER1またはIDUAタンパク質をコードする、保持されたイントロン含有mRNA前駆体(RIC mRNA前駆体)は、細胞の核内にある。保持されたイントロン、5’スプライス部位に隣接するエクソン、および3’スプライス部位に隣接するエクソンを含み、ROM1、TEAD1、RDH5、NR2E3、PAX6、CRX、FSCN2、ABCA4、MYOC、TCF4、MFSD8、CTNS、NXNL1、OPTN、RLBP1、RPE65、LRAT、RDH8、RDH12、RGR、CNGA3、ALMS1、PER1またはIDUAタンパク質をコードする、ROM1、TEAD1、RDH5、NR2E3、PAX6、CRX、FSCN2、ABCA4、MYOC、TCF4、MFSD8、CTNS、NXNL1、OPTN、RLBP1、RPE65、LRAT、RDH8、RDH12、RGR、CNGA3、ALMS1、PER1またはIDUA mRNA前駆体を有する細胞は、RIC mRNA前駆体の標的部分に相補的なアンチセンスオリゴマー(ASO)と接触させることができる。RIC mRNA前駆体の標的部分へのASOのハイブリダイゼーションは、結果として、保持されたイントロンのスプライス部位(5’スプライス部位あるいは3’スプライス部位)のスプライシングを増強することができ、その後に標的タンパク質産生を増加させる。
本明細書に提供される方法とアンチセンスオリゴヌクレオチド組成物は、ROM1、TEAD1、RDH5、NR2E3、PAX6、CRX、FSCN2、ABCA4、MYOC、TCF4、MFSD8、CTNS、NXNL1、OPTN、RLBP1、RPE65、LRAT、RDH8、RDH12、RGR、CNGA3、ALMS1、PER1、またはIDUAのタンパク質をコードするmRNAのレベル、またはROM1、TEAD1、RDH5、NR2E3、PAX6、CRX、FSCN2、ABCA4、MYOC、TCF4、MFSD8、CTNS、NXNL1、OPTN、RLBP1、RPE65、LRAT、RDH8、RDH12、RGR、CNGA3、ALMS1、PER1、またはIDUAのタンパク質をコードする成熟mRNAのレベルを増加させることにより、細胞における、例えば、ROM1、TEAD1、RDH5、NR2E3、PAX6、CRX、FSCN2、ABCA4、MYOC、TCF4、MFSD8、CTNS、NXNL1、OPTN、RLBP1、RPE65、LRAT、RDH8、RDH12、RGR、CNGA3、ALMS1、PER1、またはIDUAのタンパク質の量又は活性が不足している被験体における、ROM1、TEAD1、RDH5、NR2E3、PAX6、CRX、FSCN2、ABCA4、MYOC、TCF4、MFSD8、CTNS、NXNL1、OPTN、RLBP1、RPE65、LRAT、RDH8、RDH12、RGR、CNGA3、ALMS1、PER1、またはIDUAのタンパク質の発現を増加させるのに有用である。特に、本明細書に記載されるような方法と組成物は、ROM1、TEAD1、RDH5、NR2E3、PAX6、CRX、FSCN2、ABCA4、MYOC、TCF4、MFSD8、CTNS、NXNL1、OPTN、RLBP1、RPE65、LRAT、RDH8、RDH12、RGR、CNGA3、ALMS1、PER1、またはIDUAのタンパク質をコードする、ROM1、TEAD1、RDH5、NR2E3、PAX6、CRX、FSCN2、ABCA4、MYOC、TCF4、MFSD8、CTNS、NXNL1、OPTN、RLBP1、RPE65、LRAT、RDH8、RDH12、RGR、CNGA3、ALMS1、PER1、またはIDUAのRIC mRNA前駆体からの保持されたイントロンの構成的スプライシングを誘発することができ、それにより、ROM1、TEAD1、RDH5、NR2E3、PAX6、CRX、FSCN2、ABCA4、MYOC、TCF4、MFSD8、CTNS、NXNL1、OPTN、RLBP1、RPE65、LRAT、RDH8、RDH12、RGR、CNGA3、ALMS1、PER1、またはIDUAのタンパク質をコードするmRNAのレベル、或いはROM1、TEAD1、RDH5、NR2E3、PAX6、CRX、FSCN2、ABCA4、MYOC、TCF4、MFSD8、CTNS、NXNL1、OPTN、RLBP1、RPE65、LRAT、RDH8、RDH12、RGR、CNGA3、ALMS1、PER1、またはIDUAのタンパク質をコードする成熟mRNAのレベルを増加させ、および、ROM1、TEAD1、RDH5、NR2E3、PAX6、CRX、FSCN2、ABCA4、MYOC、TCF4、MFSD8、CTNS、NXNL1、OPTN、RLBP1、RPE65、LRAT、RDH8、RDH12、RGR、CNGA3、ALMS1、PER1、またはIDUAのタンパク質の発現を増加させる。
本開示の1つの態様は、ROM1、TEAD1、RDH5、NR2E3、PAX6、CRX、FSCN2、ABCA4、MYOC、TCF4、MFSD8、CTNS、NXNL1、OPTN、RLBP1、RPE65、LRAT、RDH8、RDH12、RGR、CNGA3、ALMS1、PER1、またはIDUAのRIC mRNA前駆体の標的部分に結合することによりスプライシングを増強するアンチセンスオリゴマーを含む組成物である。本明細書で使用されるように、用語「ASO」と「アンチセンスオリゴマー」は、交換可能に使用され、且つ、ワトソン-クリック型塩基対またはゆらぎ塩基対(G-U)により、標的核酸(例えばROM1、TEAD1、RDH5、NR2E3、PAX6、CRX、FSCN2、ABCA4、MYOC、TCF4、MFSD8、CTNS、NXNL1、OPTN、RLBP1、RPE65、LRAT、RDH8、RDH12、RGR、CNGA3、ALMS1、PER1、またはIDUAのRIC mRNA前駆体)配列にハイブリダイズする、核酸塩基を含むポリヌクレオチドなどのオリゴマーを指す。ASOは、標的配列に相補的な又はほぼ相補的(例えば、標的配列に結合し、スプライス部位でスプライシングを増強させるのに十分な相補性)である正確な配列を有し得る。ASOは、標的核酸(例えば、mRNA前駆体の転写産物の標的部分)に結合し(ハイブリダイズし)、生理学的条件下でハイブリダイズされたままであるように設計されている。典型的に、ASOは、意図した(標的とされた)核酸配列以外の部位にハイブリダイズする場合、標的核酸でない限られた数の配列に(標的核酸以外の少数の部位に)ハイブリダイズする。ASOの設計は、mRNA前駆体の転写産物の標的部分の核酸配列、或いはゲノムまたは細胞のmRNA前駆体またはトランスクリプトームにおける他の場所での十分に類似した核酸配列の発生を考慮に入れることができ、その結果、ASOが他の部位に結合し「オフターゲット」効果を引き起こす可能性は限定される。例えば、発明の名称「Reducing Nonsense-Mediated mRNA Decay」のWO2015/035091として公開されたPCT国際出願番号PCT/US2014/054151におけるものなどの、当業者に既知のアンチセンスオリゴマーは、本明細書に記載される方法を実施するために使用され得る。
記載された組成物のアンチセンスオリゴヌクレオチドを含み、上記方法のいずれかにおいて使用するための医薬組成物または医薬製剤は、医薬品産業において周知の従来技術に従って調製することができ、且つ公開文献においても記載されている。実施形態において、被験体を処置するための医薬組成物または医薬製剤は、上記のような任意のアンチセンスオリゴマー、またはその薬学的に許容可能な塩、溶媒和物、水和物、またはエステルの有効量、および薬学的に許容可能な希釈剤を含む。医薬製剤のアンチセンスオリゴマーはさらに、薬学的に許容可能な賦形剤、希釈剤または担体を含み得る。
本明細書に提供される組成物のうちのいずれかが個体に投与されうる。「個体」は、「被験体」または「患者」と交換可能に使用されてもよい。個体は哺乳動物でもよく、例えば人間、または、人類以外の霊長類、げっ歯類、ウサギ、ラット、マウス、馬、ロバ、ヤギ、猫、犬、雌牛、ブタ、あるいは羊などの動物である。実施形態では、個体はヒトである。実施形態では、個体は胎児、胚、または小児である。他の実施形態では、個体は植物などの別の真核生物であってもよい。いくつかの実施形態では、本明細書で提供される化合物は細胞にエクスビボで投与される。
標的イントロンにおいて特異的にROM1、TEAD1、RDH5、NR2E3、PAX6、CRX、FSCN2、ABCA4、MYOC、TCF4、MFSD8、CTNS、NXNL1、OPTN、RLBP1、RPE65、LRAT、RDH8、RDH12、RGR、CNGA3、ALMS1、PER1またはIDUA RIC mRNA前駆体のスプライシングを増強する付加的なASOを特定する(判定する)方法も本発明の範囲内である。mRNA前駆体の標的領域内で様々なヌクレオチドに特異的にハイブリダイズするASOは、標的イントロンのスプライシングの速度および/または程度を改善するASOを特定する(判定する)ためにスクリーニングされてもよい。いくつかの実施形態では、ASOはスプライシング抑制因子/サイレンサーの結合部位をブロックまたは妨害することがある。当該技術分野において既知の任意の方法が、イントロンの標的領域にハイブリダイズされた時に所望の効果(例えばスプライシング、タンパク質または機能的なRNA生産の向上)をもたらすASOを特定する(判定する)ために使用されてもよい。これらの方法はまた、保持されたイントロンに隣接するエクソン中、または保持されていないイントロン中の標的領域へ結合することにより、保持されたイントロンのスプライシングを増強するASOの特定のために使用することができる。使用されうる方法の一例が下記に提供される。
本明細書は以下の発明の態様を包含する。
[1]
被験体の細胞により標的タンパク質または機能的RNAの発現を増加させることによって、必要としている被験体の眼疾患を処置する方法であって、該細胞は、保持されたイントロン含有mRNA前駆体(RIC mRNA前駆体)を有し、該RIC mRNA前駆体は、保持されたイントロン、5’スプライス部位に隣接しているエクソン、および3’スプライス部位に隣接しているエクソンを含み、ここで、RIC mRNA前駆体は、標的タンパク質または機能的RNAをコードし、該方法は、被験体の細胞を、標的タンパク質または機能的RNAをコードするRIC mRNA前駆体の標的部分に相補的なアンチセンスオリゴマー(ASO)と接触させる工程を含み、それによって、保持されたイントロンは、標的タンパク質または機能的RNAをコードするRIC mRNA前駆体から構成的にスプライシングされ、それにより、被験体の細胞内で、標的タンパク質または機能的RNAをコードするmRNAのレベルを増加させ、標的タンパク質または機能的RNAの発現を増加させる、方法。
[2]
眼疾患は、網膜色素変性症-7、Sveinsson網脈絡膜萎縮、白点状眼底、網膜色素変性症37、無虹彩症、視神経コロボーマ、眼コロボーマ、中心窩形成不全-1、両側性視神経形成不全、錐体杆体ジストロフィー-2、レーバー先天黒内障-7、網膜色素変性症30、シュタルガルト病-1、網膜色素変性症-19、加齢黄斑変性-2、錐体杆体ジストロフィー-3、原発開放隅角緑内障、フックス角膜内皮ジストロフィー-3、中央錐体が関係する黄斑ジストロフィー、眼性非腎症性シスチン蓄積症、レーバー先天黒内障、原発開放隅角緑内障、筋萎縮性側索硬化症12、ボスニア型の網膜ジストロフィー、白点状眼底、白点状網膜炎、レーバー先天黒内障2、網膜色素変性症20、レーバー先天黒内障14、網膜色素変性症、オール-トランスレチナール(例えばSTGD1)の遅いクリアランスまたは蓄積による眼疾患、レーバー先天黒内障13、網膜色素変性症44、色覚異常-2、時差ぼけ、アルストレーム症候群、弱毒化MPS-1(ハーラー-シャイエ症候群およびシャイエ症候群)、またはバルデー・ビードル症候群である、[1]に記載の方法。
[3]
標的タンパク質の発現を増加させる方法であって、ここで、該標的タンパク質は、保持されたイントロン含有mRNA前駆体(RIC mRNA前駆体)を有する細胞によってROM1、TEAD1、RDH5、NR2E3、PAX6、CRX、FSCN2、ABCA4、MYOC、TCF4、MFSD8、CTNS、NXNL1、OPTN、RLBP1、RPE65、LRAT、RDH8、RDH12、RGR、CNGA3、ALMS1、PER1、またはIDUAのスプライシング効率を改善し、ROM1、TEAD1、RDH5、NR2E3、PAX6、CRX、FSCN2、ABCA4、MYOC、TCF4、MFSD8、CTNS、NXNL1、OPTN、RLBP1、RPE65、LRAT、RDH8、RDH12、RGR、CNGA3、ALMS1、PER1、またはIDUAの発現であり、RIC mRNA前駆体は、保持されたイントロン、保持されたイントロンの5’スプライス部位に隣接するエクソン、保持されたイントロンの3’スプライス部位に隣接するエクソンを含み、該RIC mRNA前駆体は、ROM1、TEAD1、RDH5、NR2E3、PAX6、CRX、FSCN2、ABCA4、MYOC、TCF4、MFSD8、CTNS、NXNL1、OPTN、RLBP1、RPE65、LRAT、RDH8、RDH12、RGR、CNGA3、ALMS1、PER1、またはIDUAタンパク質のスプライシング効率を改善することによって、ROM1、TEAD1、RDH5、NR2E3、PAX6、CRX、FSCN2、ABCA4、MYOC、TCF4、MFSD8、CTNS、NXNL1、OPTN、RLBP1、RPE65、LRAT、RDH8、RDH12、RGR、CNGA3、ALMS1、PER1、またはIDUAの発現をコードし、該方法は、ROM1、TEAD1、RDH5、NR2E3、PAX6、CRX、FSCN2、ABCA4、MYOC、TCF4、MFSD8、CTNS、NXNL1、OPTN、RLBP1、RPE65、LRAT、RDH8、RDH12、RGR、CNGA3、ALMS1、PER1、またはIDUAタンパク質のスプライシング効率を改善することによって、ROM1、TEAD1、RDH5、NR2E3、PAX6、CRX、FSCN2、ABCA4、MYOC、TCF4、MFSD8、CTNS、NXNL1、OPTN、RLBP1、RPE65、LRAT、RDH8、RDH12、RGR、CNGA3、ALMS1、PER1、またはIDUAの発現をコードするRIC mRNA前駆体の標的部分へ相補的なアンチセンスオリゴマー(ASO)と、細胞とを接触させ、それによって、保持されたイントロンは、ROM1、TEAD1、RDH5、NR2E3、PAX6、CRX、FSCN2、ABCA4、MYOC、TCF4、MFSD8、CTNS、NXNL1、OPTN、RLBP1、RPE65、LRAT、RDH8、RDH12、RGR、CNGA3、ALMS1、PER1、またはIDUAタンパク質のスプライシング効率の改善によって、ROM1、TEAD1、RDH5、NR2E3、PAX6、CRX、FSCN2、ABCA4、MYOC、TCF4、MFSD8、CTNS、NXNL1、OPTN、RLBP1、RPE65、LRAT、RDH8、RDH12、RGR、CNGA3、ALMS1、PER1、またはIDUA発現をコードするRIC mRNA前駆体から構成的にスプライシングされ、それにより、ROM1、TEAD1、RDH5、NR2E3、PAX6、CRX、FSCN2、ABCA4、MYOC、TCF4、MFSD8、CTNS、NXNL1、OPTN、RLBP1、RPE65、LRAT、RDH8、RDH12、RGR、CNGA3、ALMS1、PER1、またはIDUAタンパク質をコードするmRNAのレベルを増加させる工程と、細胞において、ROM1、TEAD1、RDH5、NR2E3、PAX6、CRX、FSCN2、ABCA4、MYOC、TCF4、MFSD8、CTNS、NXNL1、OPTN、RLBP1、RPE65、LRAT、RDH8、RDH12、RGR、CNGA3、ALMS1、PER1、またはIDUAタンパク質のスプライシング効率を改善することによって、ROM1、TEAD1、RDH5、NR2E3、PAX6、CRX、FSCN2、ABCA4、MYOC、TCF4、MFSD8、CTNS、NXNL1、OPTN、RLBP1、RPE65、LRAT、RDH8、RDH12、RGR、CNGA3、ALMS1、PER1、またはIDUAの発現を増加させる工程と、を含み、ここで、標的タンパク質は、ROM1、TEAD1、RDH5、NR2E3、PAX6、CRX、FSCN2、ABCA4、MYOC、TCF4、MFSD8、CTNS、NXNL1、OPTN、RLBP1、RPE65、LRAT、RDH8、RDH12、RGR、CNGA3、ALMS1、PER1、またはIDUAである、方法。
[4]
標的タンパク質は、ROM1、TEAD1、RDH5、NR2E3、PAX6、CRX、FSCN2、ABCA4、MYOC、TCF4、MFSD8、CTNS、NXNL1、OPTN、RLBP1、RPE65、LRAT、RDH8、RDH12、RGR、CNGA3、ALMS1、PER1、またはIDUAである、[1]または[2]に記載の方法。
[5]
標的タンパク質または機能的RNAは、被験体において量または活性が不足している標的タンパク質または機能的RNAを機能的に増強または交換する、補償タンパク質または補償する機能的RNAである、[1]または[2]に記載の方法。
[6]
細胞は、不足した量または活性のROM1、TEAD1、RDH5、NR2E3、PAX6、CRX、FSCN2、ABCA4、MYOC、TCF4、MFSD8、CTNS、NXNL1、OPTN、RLBP1、RPE65、LRAT、RDH8、RDH12、RGR、CNGA3、ALMS1、PER1、またはIDUAタンパク質によって引き起こされた疾病を有する被験体内にある、またはその被験体由来である、[3]に記載の方法。
[7]
標的タンパク質の量の不足は標的タンパク質のハプロ不全によって引き起こされ、ここで被験体は、機能的な標的タンパク質をコードする第1の対立遺伝子、および標的タンパク質が産生されない第2の対立遺伝子、または非機能的な標的タンパク質をコードする第2の対立遺伝子を有し、アンチセンスオリゴマーは、第1の対立遺伝子から転写されたRIC mRNA前駆体の標的部分に結合する、[1]から[6]のいずれか1つに記載の方法。
[8]
被験体は、標的タンパク質の量または機能の不足に起因する障害により引き起こされた疾病を有し、ここで被験体は、
(a)第1の変異対立遺伝子であって、そこから、
(i)標的タンパク質が野生型対立遺伝子からの産生と比較して低下したレベルで産生されるか、
(ii)標的タンパク質が同等の野生型タンパク質と比較して低下した機能を有する形態で産生されるか、または
(iii)標的タンパク質が産生されない、第1の変異対立遺伝子と、
(b)第2の変異対立遺伝子であって、そこから、
(i)標的タンパク質が野生型対立遺伝子からの産生と比較して低下したレベルで産生されるか、
(ii)標的タンパク質が同等の野生型タンパク質と比較して低下した機能を有する形態で産生されるか、または
(iii)標的タンパク質が産生されない、第2の変異対立遺伝子と、を有し、
ここで、被験体は、第1の変異対立遺伝子(a)(iii)を有するとき、第2の変異対立遺伝子は(b)(i)または(b)(ii)であり、かつ被験体が第2の変異対立遺伝子(b)(iii)を有するとき、第1の変異対立遺伝子は(a)(i)あるいは(a)(ii)であり、およびここで、RIC mRNA前駆体は、(a)(i)もしくは(a)(ii)である第1の変異対立遺伝子から、および/または(b)(i)もしくは(b)(ii)である第2の変異対立遺伝子から転写される、[1]から[6]のいずれか1つに記載の方法。
[9]
標的タンパク質が、同等の野生型タンパク質と比較して機能が低下した形態で産生される、[8]に記載の方法。
[10]
標的タンパク質が、同等の野生型タンパク質と比較して完全に機能的である形態で産生される、[8]に記載の方法。
[11]
RIC mRNA前駆体の標的部分は、保持されたイントロンの5’スプライス部位に対する+6から保持されたイントロンの3’スプライス部位に対する-16の領域内の保持されたイントロンにある、[1]から[10]のいずれか1つに記載の方法。
[12]
RIC mRNA前駆体の標的部分が、保持されたイントロンの5’スプライス部位に対する+69から保持されたイントロンの3’スプライス部位に対する-79の領域内の保持されたイントロンにある、[1]から[10]のいずれか1つに記載の方法。
[13]
標的タンパク質は、(a)ABCA4、(b)RPE65、(c)MYOC、(d)CNGA3、(e)MFSD8、(f)IDUA、(g)LRAT、(h)OPTN、(i)RGR、(j)TEAD1、(k)PAX6、(l)ROM1、(m)RDH5、(n)RDH12、(o)NR2E3、(p)RLBP1、(q)CTNS、(r)PER1、(s)FSCN2、(t)TCF4、(u)RDH8、(v)NXNL1、または(w)CRXである、[1]から[12]のいずれか1つに記載の方法。
[14]
RIC mRNA前駆体の標的部分は、
(a)SEQ ID NO 84-1126のいずれか1つ、
(b)SEQ ID NO 1127-1528のいずれか1つ、
(c)SEQ ID NO 1529-2318のいずれか1つ、
(d)SEQ ID NO 2319-2770のいずれか1つ、
(e)SEQ ID NO 2771-3631のいずれか1つ、
(f)SEQ ID NO 3632-4443のいずれか1つ、
(g)SEQ ID NO 4444-6647のいずれか1つ、
(h)SEQ ID NO 6648-7579のいずれか1つ、
(i)SEQ ID NO 7580-8958のいずれか1つ、
(j)SEQ ID NO 8959-9163のいずれか1つ、
(k)SEQ ID NO 9164-15179のいずれか1つ、
(l)SEQ ID NO 15180-15486のいずれか1つ、
(m)SEQ ID NO 15487-16202のいずれか1つ、
(n)SEQ ID NO 16203-16458のいずれか1つ、
(o)SEQ ID NO 16459-18209のいずれか1つ、
(p)SEQ ID NO 18210-18638のいずれか1つ、
(q)SEQ ID NO 18639-19534のいずれか1つ、
(r)SEQ ID NO 19535-19845のいずれか1つ、
(s)SEQ ID NO 19846-20849のいずれか1つ、
(t)SEQ ID NO 20850-24737のいずれか1つ、
(u)SEQ ID NO 24738-24873のいずれか1つ、
(v)SEQ ID NO 24874-25231のいずれか1つ、または
(w)SEQ ID NO 25232-26654のいずれか1つに、
少なくとも約80%、85%、90%、95%、97%、または100%相補的な配列を含む、[13]に記載の方法。
[15]
RIC mRNA前駆体の標的部分は、
(a)SEQ ID NO 26674、SEQ ID NO 26706、SEQ ID NO 26656、SEQ ID NO 26681、もしくはSEQ ID NO 26664、
(b)SEQ ID NO 26691、もしくはSEQ ID NO 26671、
(c)SEQ ID NO 26669、もしくはSEQ ID NO 26696、
(d)SEQ ID NO 26711、
(e)SEQ ID NO 26703、もしくはSEQ ID NO 26708、
(f) SEQ ID NO 26668、SEQ ID NO 26679、SEQ ID NO 26700、SEQ ID NO 26655、もしくはSEQ ID NO 26663、
(g)SEQ ID NO 26685、
(h)SEQ ID NO 26714、
(i)SEQ ID NO 26657、SEQ ID NO 26687、もしくはSEQ ID NO 26683、
(j)SEQ ID NO 26672、
(k)SEQ ID NO 26697、SEQ ID NO 26677、SEQ ID NO 26707、SEQ ID NO 26678、SEQ ID NO 26713、SEQ ID NO 26694、もしくはSEQ ID NO 26659、
(l)SEQ ID NO 26665、
(m)SEQ ID NO 26704、SEQ ID NO 26666、SEQ ID NO 26709、もしくはSEQ ID NO 26684、
(n)SEQ ID NO 26693、
(o)SEQ ID NO 26702、SEQ ID NO 26660、SEQ ID NO 26705、SEQ ID NO 26698、SEQ ID NO 26658、SEQ ID NO 26676、SEQ ID NO 26712、もしくはSEQ ID NO 26701、
(p)SEQ ID NO 26673、もしくはSEQ ID NO 26667、
(q)SEQ ID NO 26690、もしくはSEQ ID NO 26692、
(r)SEQ ID NO 26682、もしくはSEQ ID NO 26710、
(s)SEQ ID NO 26670、SEQ ID NO 26662、もしくはSEQ ID NO 26661、
(t)SEQ ID NO 26688、もしくはSEQ ID NO 26689、
(u)SEQ ID NO 26680、
(v)SEQ ID NO 26699、もしくは、
(w)SEQ ID NO 26695、もしくはSEQ ID NO 26686
の少なくとも8つの近接する核酸を含む領域に対して、少なくとも80%、85%、90%、95%、97%、もしくは100%の配列同一性を備えた配列を含む、[13]または[14]に記載の方法。
[16]
ASOは、
(a)SEQ ID NO 84-1126のいずれか1つ、
(b)SEQ ID NO 1127-1528のいずれか1つ、
(c)SEQ ID NO 1529-2318のいずれか1つ、
(d)SEQ ID NO 2319-2770のいずれか1つ、
(e)SEQ ID NO 2771-3631のいずれか1つ、
(f)SEQ ID NO 3632-4443のいずれか1つ、
(g)SEQ ID NO 4444-6647のいずれか1つ、
(h)SEQ ID NO 6648-7579のいずれか1つ、
(i)SEQ ID NO 7580-8958のいずれか1つ、
(j)SEQ ID NO 8959-9163のいずれか1つ、
(k)SEQ ID NO 9164-15179のいずれか1つ、
(l)SEQ ID NO 15180-15486のいずれか1つ、
(m)SEQ ID NO 15487-16202のいずれか1つ、
(n)SEQ ID NO 16203-16458のいずれか1つ、
(o)SEQ ID NO 16459-18209のいずれか1つ、
(p)SEQ ID NO 18210-18638のいずれか1つ、
(q)SEQ ID NO 18639-19534のいずれか1つ、
(r)SEQ ID NO 19535-19845のいずれか1つ、
(s)SEQ ID NO 19846-20849のいずれか1つ、
(t)SEQ ID NO 20850-24737のいずれか1つ、
(u)SEQ ID NO 24738-24873のいずれか1つ、
(v)SEQ ID NO 24874-25231のいずれか1つ、または
(w)SEQ ID NO 25232-26654のいずれか1つ
に対する、少なくとも約80%、85%、90%、95%、97%、あるいは100%の配列同一性を備えた配列を含む、[13]から[15]のいずれか1つに記載の方法。
[17]
RIC mRNA前駆体は、
(a)SEQ ID NO 24、
(b)SEQ ID NO 25、
(c)SEQ ID NO 26、
(d)SEQ ID NO 27、もしくはSEQ ID NO 28、
(e)SEQ ID NO 29、
(f)SEQ ID NO 30、もしくはSEQ ID NO 31、
(g)SEQ ID NO 32、もしくはSEQ ID NO 33、
(h)SEQ ID NO 34、SEQ ID NO 35、SEQ ID NO 36、もしくはSEQ ID NO 37、
(i)SEQ ID NO 38、SEQ ID NO 39、もしくはSEQ ID NO 40、
(j)SEQ ID NO 41、
(k)SEQ ID NO 42、SEQ ID NO 43、SEQ ID NO 44、SEQ ID NO 45、SEQ ID NO 46、SEQ ID NO 47、SEQ ID NO 48、SEQ ID NO 49、SEQ ID NO 50、SEQ ID NO 51、もしくはSEQ ID NO 52、
(l)SEQ ID NO 53、
(m)SEQ ID NO 54、もしくはSEQ ID NO 55、
(n)SEQ ID NO 56、
(o)SEQ ID NO 57、またはSEQ ID NO 58、
(p)SEQ ID NO 59、
(q)SEQ ID NO 60、もしくはSEQ ID NO 61、
(r)SEQ ID NO 62、
(s)SEQ ID NO 63、もしくはSEQ ID NO 64、
(t)SEQ ID NO 65、SEQ ID NO 66、SEQ ID NO 67、SEQ ID NO 68、SEQ ID NO 69、SEQ ID NO 70、SEQ ID NO 71、SEQ ID NO 72、SEQ ID NO 73、SEQ ID NO 74、SEQ ID NO 75、SEQ ID NO 76、SEQ ID NO 77、SEQ ID NO 78、SEQ ID NO 79、もしくはSEQ ID NO 80、
(u)SEQ ID NO 81、
(v)SEQ ID NO 82、または、
(w)SEQ ID NO 83
に対して、少なくとも約80%、85%、90%、95%、97%、もしくは100%の配列同一性を備えた配列を含む、[13]から[16]のいずれか1つに記載の方法。
[18]
RIC mRNA前駆体は、
(a)SEQ ID NO 1、
(b)SEQ ID NO 2、
(c)SEQ ID NO 3、
(d)SEQ ID NO 4、
(e)SEQ ID NO 5、
(f)SEQ ID NO 6、
(g)SEQ ID NO 7、
(h)SEQ ID NO 8、
(i)SEQ ID NO 9、
(j)SEQ ID NO 10、
(k)SEQ ID NO 11、
(l)SEQ ID NO 12、
(m)SEQ ID NO 13、
(n)SEQ ID NO 14、
(o)SEQ ID NO 15、
(p)SEQ ID NO 16、
(q)SEQ ID NO 17、
(r)SEQ ID NO 18、
(s)SEQ ID NO 19、
(t)SEQ ID NO 20、
(u)SEQ ID NO 21、
(v)SEQ ID NO 22、
(w)SEQ ID NO 23
に対して、少なくとも約80%、85%、90%、95%、97%、もしくは100%の配列同一性を備えた遺伝子配列によりコードされる、[13]から[17]のいずれか1つに記載の方法。
[19]
RIC mRNA前駆体の標的部分は、
(a)保持されたイントロンの5’スプライス部位に対する+6から+100の領域内;または
(b)保持されたイントロンの3’スプライス部位に対する-16から-100の領域
内の保持されたイントロンにある、[1]から[18]のいずれか1つに記載の方法。
[20]
アンチセンスオリゴマーが、少なくとも1つの保持されたイントロンの5’スプライス部位の約100ヌクレオチド下流から、少なくとも1つの保持されたイントロンの3’スプライス部位の約100ヌクレオチド上流の領域内にある、RIC mRNA前駆体の一部を標的とする、[1]から[18]のいずれか1つに記載の組成物。
[21]
RIC mRNA前駆体の標的部分は、(a)保持されたイントロンの5’スプライス部位に隣接しているエクソンにおける+2eから-4eの領域内;
または(b)保持されたイントロンの3’スプライス部位に隣接しているエクソンにおける+2eから-4eの領域内にある、[1]から[18]のいずれか1つに記載の方法。
[22]
アンチセンスオリゴマーは、機能的RNAまたは標的タンパク質をコードする遺伝子から転写されたmRNA前駆体の選択的スプライシングを調節することにより、標的タンパク質または機能的RNAの量を増加させない、[1]から[20]のいずれか1つに記載の方法。
[23]
アンチセンスオリゴマーは、標的タンパク質または機能的RNAをコードする遺伝子の変異から結果として生じる異常スプライシングを調節することにより、標的タンパク質または機能的RNAの量を増加させない、[1]から[22]のいずれか1つに記載の方法。
[24]
RIC mRNA前駆体は、全長mRNA前駆体の部分的スプライシングまたは野生型mRNA前駆体の部分的スプライシングによって産生された、[1]から[23]のいずれか1つに記載の方法。
[25]
標的タンパク質または機能的RNAをコードするmRNAは、全長成熟mRNAまたは野生型成熟mRNAである、[1]から[24]のいずれか1つに記載の方法。
[26]
産生される標的タンパク質は全長タンパク質または野生型タンパク質である、[1]から[25]のいずれか1つに記載の方法。
[27]
アンチセンスオリゴマーと接触させられた細胞内で産生された標的タンパク質または機能的RNAをコードするmRNAの総量は、対照細胞内で産生された標的タンパク質または機能的RNAをコードするmRNAの総量と比較して、約1.1倍から約10倍、約1.5倍から約10倍、約2倍から約10倍、約3倍から約10倍、約4倍から約10倍、約1.1倍から約5倍、約1.1倍から約6倍、約1.1倍から約7倍、約1.1倍から約8倍、約1.1倍から約9倍、約2倍から約5倍、約2倍から約6倍、約2倍から約7倍、約2倍から約8倍、約2倍から約9倍、約3倍から約6倍、約3倍から約7倍、約3倍から約8倍、約3倍から約9倍、約4倍から約7倍、約4倍から約8倍、約4倍から約9倍、少なくとも約1.1倍、少なくとも約1.5倍、少なくとも約2倍、少なくとも約2.5倍、少なくとも約3倍、少なくとも約3.5倍、少なくとも4倍、少なくとも約5倍、または少なくとも約10倍増加する、[1]から[26]のいずれか1つに記載の方法。
[28]
アンチセンスオリゴマーと接触させられた細胞によって産生された標的タンパク質の総量は、対照細胞内で産生された標的タンパク質の総量と比較して、約1.1倍から約10倍、約1.5倍から約10倍、約2倍から約10倍、約3倍から約10倍、約4倍から約10倍、約1.1倍から約5倍、約1.1倍から約6倍、約1.1倍から約7倍、約1.1倍から約8倍、約1.1倍から約9倍、約2倍から約5倍、約2倍から約6倍、約2倍から約7倍、約2倍から約8倍、約2倍から約9倍、約3倍から約6倍、約3倍から約7倍、約3倍から約8倍、約3倍から約9倍、約4倍から約7倍、約4倍から約8倍、約4倍から約9倍、少なくとも約1.1倍、少なくとも約1.5倍、少なくとも約2倍、少なくとも約2.5倍、少なくとも約3倍、少なくとも約3.5倍、少なくとも4倍、少なくとも約5倍、または少なくとも約10倍増加する、[1]から[27]のいずれか1つに記載の方法。
[29]
アンチセンスオリゴマーは、ホスホロチオエート結合またはホスホロジアミデート結合を含む骨格修飾を含む、[1]から[28]のいずれか1つに記載の方法。
[30]
アンチセンスオリゴマーは、ホスホロジアミデートモルホリノ、ロックド核酸、ペプチド核酸、2’-Oメチル部分、2’-フルオロ部分、または2’-O-メトキシエチル部分を含む、[1]から[29]のいずれか1つに記載の方法。
[31]
アンチセンスオリゴマーは、少なくとも1つの修飾された糖部を含む、[1]から[30]のいずれか1つに記載の方法。
[32]
各糖部は修飾された糖部である、[31]のいずれか1つに記載の方法。
[33]
アンチセンスオリゴマーは、8から50の核酸塩基、8から40の核酸塩基、8から35の核酸塩基、8から30の核酸塩基、8から25の核酸塩基、8から20の核酸塩基、8から15の核酸塩基、9から50の核酸塩基、9から40の核酸塩基、9から35の核酸塩基、9から30の核酸塩基、9から25の核酸塩基、9から20の核酸塩基、9から15の核酸塩基、10から50の核酸塩基、10から40の核酸塩基、10から35の核酸塩基、10から30の核酸塩基、10から25の核酸塩基、10から20の核酸塩基、10から15の核酸塩基、11から50の核酸塩基、11から40の核酸塩基、11から35の核酸塩基、11から30の核酸塩基、11から25の核酸塩基、11から20の核酸塩基、11から15の核酸塩基、12から50の核酸塩基、12から40の核酸塩基、12から35の核酸塩基、12から30の核酸塩基、12から25の核酸塩基、12から20の核酸塩基、または12から15の核酸塩基から成る、[1]から[32]のいずれか1つに記載の方法。
[34]
アンチセンスオリゴマーは、タンパク質をコードするRIC mRNA前駆体の標的部分に、少なくとも80%、少なくとも85%、少なくとも90%、少なくとも95%、少なくとも98%、少なくとも99%、または100%相補的である、[1]から[33]のいずれか1つに記載の方法。
[35]
細胞は、標的タンパク質または機能的RNAをコードする遺伝子から転写されたRIC mRNA前駆体の集団を含み、ここでRIC mRNA前駆体の集団は、2つ以上の保持されたイントロンを含み、アンチセンスオリゴマーは、RIC mRNA前駆体の集団において最も豊富な保持されたイントロンに結合する、[1]から[34]のいずれか1つに記載の方法。
[36]
最も豊富な保持されたイントロンに対するアンチセンスオリゴマーの結合は、標的タンパク質または機能的RNAをコードするmRNAを産生するために、RIC mRNA前駆体の集団からの2つ以上の保持されたイントロンからのスプライシングアウトを誘発する、[35]に記載の方法。
[37]
細胞は、標的タンパク質または機能的RNAをコードする遺伝子から転写されたRIC mRNA前駆体の集団を含み、ここでRIC mRNA前駆体の集団は、2つ以上の保持されたイントロンを含み、アンチセンスオリゴマーは、RIC mRNA前駆体の集団において2番目に豊富な保持されたイントロンに結合する、[1]から[34]のいずれか1つに記載の方法。
[38]
2番目に豊富な保持されたイントロンに対するアンチセンスオリゴマーの結合は、標的タンパク質または機能的RNAをコードするmRNAを産生するために、RIC mRNA前駆体の集団からの2つ以上の保持されたイントロンからのスプライシングアウトを誘発する、[37]に記載の方法。
[39]
疾病は疾患また障害である、[6]から[38]のいずれか1つに記載の方法。
[40]
疾患または障害は、網膜色素変性症-7、Sveinsson網脈絡膜萎縮、白点状眼底、網膜色素変性症37、無虹彩症、視神経コロボーマ、眼コロボーマ、中心窩形成不全-1、両側性視神経形成不全、錐体杆体ジストロフィー-2、レーバー先天黒内障-7、網膜色素変性症30、シュタルガルト病-1、網膜色素変性症-19、加齢黄斑変性-2、錐体杆体ジストロフィー-3、原発開放隅角緑内障、フックス角膜内皮ジストロフィー-3、中央錐体が関係する黄斑ジストロフィー、眼性非腎症性シスチン蓄積症、レーバー先天黒内障、原発開放隅角緑内障、筋萎縮性側索硬化症12、ボスニア型の網膜ジストロフィー、白点状眼底、白点状網膜炎、レーバー先天黒内障2、網膜色素変性症20、レーバー先天黒内障14、網膜色素変性症、オール-トランスレチナール(例えばSTGD1)の遅いクリアランスまたは蓄積による眼疾患、レーバー先天黒内障13、網膜色素変性症44、色覚異常-2、時差ぼけ、アルストレーム症候群、弱毒化MPS-1(ハーラー-シャイエ症候群およびシャイエ症候群)、またはバルデー・ビードル症候群である、[39]に記載の方法。
[41]
標的タンパク質およびRIC mRNA前駆体は、ROM1、TEAD1、RDH5、NR2E3、PAX6、CRX、FSCN2、ABCA4、MYOC、TCF4、MFSD8、CTNS、NXNL1、OPTN、RLBP1、RPE65、LRAT、RDH8、RDH12、RGR、CNGA3、ALMS1、PER1またはIDUAの遺伝子によってコードされる、[40]に記載の方法。
[42]
タンパク質の発現を評価する工程をさらに含む、[1]から[41]のいずれか1つに記載の方法。
[43]
アンチセンスオリゴマーは、ROM1、TEAD1、RDH5、NR2E3、PAX6、CRX、FSCN2、ABCA4、MYOC、TCF4、MFSD8、CTNS、NXNL1、OPTN、RLBP1、RPE65、LRAT、RDH8、RDH12、RGR、CNGA3、ALMS1、PER1またはIDUAのRIC mRNA前駆体の標的部分へ結合する、[1]から[42]のいずれか1つに記載の方法。
[44]
被験体はヒトである、[1]から[43]のいずれか1つに記載の方法。
[45]
被験体はヒト以外の動物である、[1]から[43]のいずれか1つに記載の方法。
[46]
被験体は胎児、胚、または小児である、[1]から[44]のいずれか1つに記載の方法。
[47]
細胞はエスクビボにある、[1]から[45]のいずれか1つに記載の方法。
[48]
アンチセンスオリゴマーは、被験体の硝子体内注射、網膜下注射、局所投与、移植、腹腔内注射、筋肉内注射、皮下注射、または静脈内注射によって投与される、[1]から[45]のいずれか1つに記載の方法。
[49]
5’スプライス部位に隣接しているエクソンの-3eから-1eおよび保持されたイントロンの+1から+6における9つのヌクレオチドは、対応する野生型配列と同一である、[1]から[48]のいずれか1つに記載の方法。
[50]
保持されたイントロンの-15から-1および3’スプライス部位に隣接しているエクソンの+1eにおける16のヌクレオチドは、対応する野生型配列と同一である、[1]から[49]のいずれか1つに記載の方法。
[51]
[1]から[50]のいずれか1つの方法で使用される、アンチセンスオリゴマー。
[52]
SEQ ID NO 84-26[654]のいずれか1つに対して、少なくとも約80%、85%、90%、95%、97%、または100%の配列同一性を有する配列を含む、アンチセンスオリゴマー。
[53]
[51]または[52]のアンチセンスオリゴマーおよび賦形剤を含む、医薬組成物。
[54]
硝子体内注射、網膜下注射、局所投与、移植、腹腔内注射、筋肉内注射、皮下注射、または静脈内注射によって[53]の医薬組成物を投与することにより、それらを必要としている被験体を処置する方法。
[55]
不足しているタンパク質または不足している機能的RNAに関連する、処置を必要としている被験体における、網膜色素変性症-7、Sveinsson網脈絡膜萎縮、白点状眼底、網膜色素変性症37、無虹彩症、視神経コロボーマ、眼コロボーマ、中心窩形成不全-1、両側性視神経形成不全、錐体杆体ジストロフィー-2、レーバー先天黒内障-7、網膜色素変性症30、シュタルガルト病-1、網膜色素変性症-19、加齢黄斑変性-2、錐体杆体ジストロフィー-3、原発開放隅角緑内障、フックス角膜内皮ジストロフィー-3、中央錐体が関係する黄斑ジストロフィー、眼性非腎症性シスチン蓄積症、レーバー先天黒内障、原発開放隅角緑内障、筋萎縮性側索硬化症12、ボスニア型の網膜ジストロフィー、白点状眼底、白点状網膜炎、レーバー先天黒内障2、網膜色素変性症20、レーバー先天黒内障14、網膜色素変性症、オール-トランスレチナール(例えばSTGD1)の遅いクリアランスまたは蓄積による眼疾患、レーバー先天黒内障13、網膜色素変性症44、色覚異常-2、時差ぼけ、アルストレーム症候群、弱毒化MPS-1(ハーラー-シャイエ症候群およびシャイエ症候群)、またはバルデー・ビードル症候群を処置するための細胞により、標的タンパク質または機能的RNAの発現を増加させる方法で使用されるためのアンチセンスオリゴマーを含む組成物であって、ここで、不足しているタンパク質または不足している機能的RNAは、被験体において量あるいは活性が不足しており、ここで、アンチセンスオリゴマーは、標的タンパク質または機能的RNAをコードする、保持されたイントロン含有mRNA前駆体(RIC mRNA前駆体)の構成的のスプライシングを増強し、ここで、標的タンパク質は:
(a)不足しているタンパク質;または
(b)被験体において不足しているタンパク質を機能的に増強または交換する、補償タンパク質であり、
ここで、機能的RNAは:
(a)不足しているRNA;または
(b)被験体において不足している機能的RNAを機能的に増強または交換する、補償する機能的RNAであり、
ここで、RIC mRNA前駆体は、保持されたイントロン、5’スプライス部位に隣接しているエクソン、および3’スプライス部位に隣接しているエクソンを含み、保持されたイントロンは、標的タンパク質または機能的RNAをコードするRIC mRNA前駆体からスプライシングされ、それによって、被験体において標的タンパク質または機能的RNAの産生または活性を増加させる、組成物。
[56]
処置を必要とする被験体におけるROM1、TEAD1、RDH5、NR2E3、PAX6、CRX、FSCN2、ABCA4、MYOC、TCF4、MFSD8、CTNS、NXNL1、OPTN、RLBP1、RPE65、LRAT、RDH8、RDH12、RGR、CNGA3、ALMS1、PER1またはIDUAのタンパク質に関連する疾病を処置する方法で使用されるアンチセンスオリゴマーを含む組成物であって、該方法は、被験体の細胞によって、ROM1、TEAD1、RDH5、NR2E3、PAX6、CRX、FSCN2、ABCA4、MYOC、TCF4、MFSD8、CTNS、NXNL1、OPTN、RLBP1、RPE65、LRAT、RDH8、RDH12、RGR、CNGA3、ALMS1、PER1またはIDUAのタンパク質の発現を増加させる工程を含み、ここで、細胞は、保持されたイントロン、保持されたイントロンの5’スプライス部位に隣接するエクソン、保持されたイントロンの3’スプライス部位に隣接するエクソンを含む保持されたイントロン含有mRNA前駆体を有し、およびRIC mRNA前駆体は、ROM1、TEAD1、RDH5、NR2E3、PAX6、CRX、FSCN2、ABCA4、MYOC、TCF4、MFSD8、CTNS、NXNL1、OPTN、RLBP1、RPE65、LRAT、RDH8、RDH12、RGR、CNGA3、ALMS1、PER1またはIDUAのタンパク質をコードし、該方法は、細胞をアンチセンスオリゴマーと接触させる工程であって、それによって、保持されたイントロンは、ROM1、TEAD1、RDH5、NR2E3、PAX6、CRX、FSCN2、ABCA4、MYOC、TCF4、MFSD8、CTNS、NXNL1、OPTN、RLBP1、RPE65、LRAT、RDH8、RDH12、RGR、CNGA3、ALMS1、PER1またはIDUAのタンパク質をコードするRIC mRNA前駆体の転写産物から構成的にスプライシングされ、それにより標的タンパク質または機能的RNAをコードするmRNAのレベルを増加させる工程と、被験体の細胞においてROM1、TEAD1、RDH5、NR2E3、PAX6、CRX、FSCN2、ABCA4、MYOC、TCF4、MFSD8、CTNS、NXNL1、OPTN、RLBP1、RPE65、LRAT、RDH8、RDH12、RGR、CNGA3、ALMS1、PER1、またはIDUAのタンパク質の発現を増加させる工程を含む、組成物。
[57]
標的タンパク質は、ROM1、TEAD1、RDH5、NR2E3、PAX6、CRX、FSCN2、ABCA4、MYOC、TCF4、MFSD8、CTNS、NXNL1、OPTN、RLBP1、RPE65、LRAT、RDH8、RDH12、RGR、CNGA3、ALMS1、PER1、またはIDUAである、[56]に記載の組成物。
[58]
疾病は疾患また障害である、[56]または[57]に記載の組成物。
[59]
疾患または障害は、網膜色素変性症-7、Sveinsson網脈絡膜萎縮、白点状眼底、網膜色素変性症37、無虹彩症、視神経コロボーマ、眼コロボーマ、中心窩形成不全-1、両側性視神経形成不全、錐体杆体ジストロフィー-2、レーバー先天黒内障-7、網膜色素変性症30、シュタルガルト病-1、網膜色素変性症-19、加齢黄斑変性-2、錐体杆体ジストロフィー-3、原発開放隅角緑内障、フックス角膜内皮ジストロフィー-3、中央錐体が関係する黄斑ジストロフィー、眼性非腎症性シスチン蓄積症、レーバー先天黒内障、原発開放隅角緑内障、筋萎縮性側索硬化症12、ボスニア型の網膜ジストロフィー、白点状眼底、白点状網膜炎、レーバー先天黒内障2、網膜色素変性症20、レーバー先天黒内障14、網膜色素変性症、オール-トランスレチナール(例えばSTGD1)の遅いクリアランスまたは蓄積による眼疾患、レーバー先天黒内障13、網膜色素変性症44、色覚異常-2、時差ぼけ、アルストレーム症候群、弱毒化MPS-1(ハーラー-シャイエ症候群およびシャイエ症候群)、またはバルデー・ビードル症候群である、[58]に記載の組成物。
[60]
標的タンパク質およびRIC mRNA前駆体は、ROM1、TEAD1、RDH5、NR2E3、PAX6、CRX、FSCN2、ABCA4、MYOC、TCF4、MFSD8、CTNS、NXNL1、OPTN、RLBP1、RPE65、LRAT、RDH8、RDH12、RGR、CNGA3、ALMS1、PER1またはIDUAの遺伝子によってコードされる、[59]に記載の組成物。
[61]
アンチセンスオリゴマーは、保持されたイントロンの5’スプライス部位に対する+6から保持されたイントロンの3’スプライス部位に対する-16の領域内の保持されたイントロンにあるRIC mRNA前駆体の一部を標的とする、[55]から[60]のいずれか1つに記載の組成物。
[62]
RIC mRNA前駆体の標的部分は、保持されたイントロンの5’スプライス部位に対する+69から保持されたイントロンの3’スプライス部位に対する-79の領域内の保持されたイントロンにある、[55]から[60]のいずれか1つに記載の組成物。
[63]
標的タンパク質は、(a)ABCA4、(b)RPE65、(c)MYOC、(d)CNGA3、(e)MFSD8、(f)IDUA、(g)LRAT、(h)OPTN、(i)RGR、(j)TEAD1、(k)PAX6、(l)ROM1、(m)RDH5、(n)RDH12、(o)NR2E3、(p)RLBP1、(q)CTNS、(r)PER1、(s)FSCN2、(t)TCF4、(u)RDH8、(v)NXNL1、または(w)CRXである、[55]から[62]のいずれか1つに記載の組成物。
[64]
RIC mRNA前駆体の標的部分は、
(a)SEQ ID NO 84-1126のいずれか1つ、
(b)SEQ ID NO 1127-1528のいずれか1つ、
(c)SEQ ID NO 1529-2318のいずれか1つ、
(d)SEQ ID NO 2319-2770のいずれか1つ、
(e)SEQ ID NO 2771-3631のいずれか1つ、
(f)SEQ ID NO 3632-4443のいずれか1つ、
(g)SEQ ID NO 4444-6647のいずれか1つ、
(h)SEQ ID NO 6648-7579のいずれか1つ、
(i)SEQ ID NO 7580-8958のいずれか1つ、
(j)SEQ ID NO 8959-9163のいずれか1つ、
(k)SEQ ID NO 9164-15179のいずれか1つ、
(l)SEQ ID NO 15180-15486のいずれか1つ、
(m)SEQ ID NO 15487-16202のいずれか1つ、
(n)SEQ ID NO 16203-16458のいずれか1つ、
(o)SEQ ID NO 16459-18209のいずれか1つ、
(p)SEQ ID NO 18210-18638のいずれか1つ、
(q)SEQ ID NO 18639-19534のいずれか1つ、
(r)SEQ ID NO 19535-19845のいずれか1つ、
(s)SEQ ID NO 19846-20849のいずれか1つ、
(t)SEQ ID NO 20850-24737のいずれか1つ、
(u)SEQ ID NO 24738-24873のいずれか1つ、
(v)SEQ ID NO 24874-25231のいずれか1つ、または
(w)SEQ ID NO 25232-26654のいずれか1つに
少なくとも約80%、85%、90%、95%、97%、または100%相補的な配列を含む、[63]に記載の組成物。
[65]
RIC mRNA前駆体の標的部分は、
(a) SEQ ID NO 26674、SEQ ID NO 26706、SEQ ID NO 26656、SEQ ID NO 26681、もしくはSEQ ID NO 26664、
(b)SEQ ID NO 26691、もしくはSEQ ID NO 26671、
(c)SEQ ID NO 26669、もしくはSEQ ID NO 26696、
(d)SEQ ID NO 26711、
(e)SEQ ID NO 26703、もしくはSEQ ID NO 26708、
(f) SEQ ID NO 26668、SEQ ID NO 26679、SEQ ID NO 26700、SEQ ID NO 26655、もしくはSEQ ID NO 26663、
(g)SEQ ID NO 26685、
(h)SEQ ID NO 26714、
(i)SEQ ID NO 26657、SEQ ID NO 26687、もしくはSEQ ID NO 26683、
(j)SEQ ID NO 26672、
(k)SEQ ID NO 26697、SEQ ID NO 26677、SEQ ID NO 26707、SEQ ID NO 26678、SEQ ID NO 26713、SEQ ID NO 26694、もしくはSEQ ID NO 26659、
(l)SEQ ID NO 26665、
(m)SEQ ID NO 26704、SEQ ID NO 26666、SEQ ID NO 26709、もしくはSEQ ID NO 26684、
(n)SEQ ID NO 26693、
(o)SEQ ID NO 26702、SEQ ID NO 26660、SEQ ID NO 26705、SEQ ID NO 26698、SEQ ID NO 26658、SEQ ID NO 26676、SEQ ID NO 26712、もしくはSEQ ID NO 26701、
(p)SEQ ID NO 26673、もしくはSEQ ID NO 26667、
(q)SEQ ID NO 26690、もしくはSEQ ID NO 26692、
(r)SEQ ID NO 26682、もしくはSEQ ID NO 26710、
(s)SEQ ID NO 26670、SEQ ID NO 26662、もしくはSEQ ID NO 26661、
(t)SEQ ID NO 26688、もしくはSEQ ID NO 26689、
(u)SEQ ID NO 26680、
(v)SEQ ID NO 26699、もしくは、
(w)SEQ ID NO 26695、もしくはSEQ ID NO 26686
の少なくとも8つの近接する核酸を含む領域に対して、少なくとも80%、85%、90%、95%、97%、もしくは100%の配列同一性を備えた配列を含む、[63]または[64]に記載の組成物。
[66]
ASOは、
(a)SEQ ID NO 84-1126のいずれか1つ、
(b)SEQ ID NO 1127-1528のいずれか1つ、
(c)SEQ ID NO 1529-2318のいずれか1つ、
(d)SEQ ID NO 2319-2770のいずれか1つ、
(e)SEQ ID NO 2771-3631のいずれか1つ、
(f)SEQ ID NO 3632-4443のいずれか1つ、
(g)SEQ ID NO 4444-6647のいずれか1つ、
(h)SEQ ID NO 6648-7579のいずれか1つ、
(i)SEQ ID NO 7580-8958のいずれか1つ、
(j)SEQ ID NO 8959-9163のいずれか1つ、
(k)SEQ ID NO 9164-15179のいずれか1つ、
(l)SEQ ID NO 15180-15486のいずれか1つ、
(m)SEQ ID NO 15487-16202のいずれか1つ、
(n)SEQ ID NO 16203-16458のいずれか1つ、
(o)SEQ ID NO 16459-18209のいずれか1つ、
(p)SEQ ID NO 18210-18638のいずれか1つ、
(q)SEQ ID NO 18639-19534のいずれか1つ、
(r)SEQ ID NO 19535-19845のいずれか1つ、
(s)SEQ ID NO 19846-20849のいずれか1つ、
(t)SEQ ID NO 20850-24737のいずれか1つ、
(u)SEQ ID NO 24738-24873のいずれか1つ、
(v)SEQ ID NO 24874 -25231のいずれか1つ、または
(w)SEQ ID NO 25232-26654のいずれか1つ
に対して、少なくとも約80%、85%、90%、95%、97%、もしくは100%の配列同一性を備えた配列を含む、[63]から[65]のいずれか1つに記載の組成物。
[67]
RIC mRNA前駆体は、
(a)SEQ ID NO 24、
(b)SEQ ID NO 25、
(c)SEQ ID NO 26、
(d)SEQ ID NO 27、もしくはSEQ ID NO 28、
(e)SEQ ID NO 29、
(f)SEQ ID NO 30、もしくはSEQ ID NO 31、
(g)SEQ ID NO 32、もしくはSEQ ID NO 33、
(h)SEQ ID NO 34、SEQ ID NO 35、SEQ ID NO 36、もしくはSEQ ID NO 37、
(i)SEQ ID NO 38、SEQ ID NO 39、もしくはSEQ ID NO 40、
(j)SEQ ID NO 41、
(k)SEQ ID NO 42、SEQ ID NO 43、SEQ ID NO 44、SEQ ID NO 45、SEQ ID NO 46、SEQ ID NO 47、SEQ ID NO 48、SEQ ID NO 49、SEQ ID NO 50、SEQ ID NO 51,もしくはSEQ ID NO 52、
(l)SEQ ID NO 53、
(m)SEQ ID NO 54、もしくはSEQ ID NO 55、
(n)SEQ ID NO 56、
(o)SEQ ID NO 57、またはSEQ ID NO 58、
(p)SEQ ID NO 59、
(q)SEQ ID NO 60、もしくはSEQ ID NO 61、
(r)SEQ ID NO 62、
(s)SEQ ID NO 63、もしくはSEQ ID NO 64、
(t)SEQ ID NO 65、SEQ ID NO 66、SEQ ID NO 67、SEQ ID NO 68、SEQ ID NO 69、SEQ ID NO 70、SEQ ID NO 71、SEQ ID NO 72、SEQ ID NO 73、SEQ ID NO 74、SEQ ID NO 75、SEQ ID NO 76、SEQ ID NO 77、SEQ ID NO 78、SEQ ID NO 79、もしくはSEQ ID NO 80、
(u)SEQ ID NO 81、
(v)SEQ ID NO 82、または、
(w)SEQ ID NO 83
に対して、少なくとも約80%、85%、90%、95%、97%、もしくは100%の配列同一性を備えた配列を含む、[63]から[66]のいずれか1つに記載の組成物。
[68]
RIC mRNA前駆体は、
(a)SEQ ID NO 1、
(b)SEQ ID NO 2、
(c)SEQ ID NO 3、
(d)SEQ ID NO 4、
(e)SEQ ID NO 5、
(f)SEQ ID NO 6、
(g)SEQ ID NO 7、
(h)SEQ ID NO 8、
(i)SEQ ID NO 9、
(j)SEQ ID NO 10、
(k)SEQ ID NO 11、
(l)SEQ ID NO 12、
(m)SEQ ID NO 13、
(n)SEQ ID NO 14、
(o)SEQ ID NO 15、
(p)SEQ ID NO 16、
(q)SEQ ID NO 17、
(r)SEQ ID NO 18、
(s)SEQ ID NO 19、
(t)SEQ ID NO 20、
(u)SEQ ID NO 21、
(v)SEQ ID NO 22、
(w)SEQ ID NO 23
に対して、少なくとも約80%、85%、90%、95%、97%、あるいは100%の配列同一性を備えた遺伝子配列によってコードされる、[63]から[67]のいずれか1つに記載の組成物。
[69]
アンチセンスオリゴマーは、(a)保持されたイントロンの5’スプライス部位に対する+6から+100の領域内;
または(b)保持されたイントロンの3’スプライス部位に対する-16から-100の領域内の保持されたイントロンにあるRIC mRNA前駆体の一部を標的とする、[55]から[68]のいずれか1つに記載の組成物。
[70]
アンチセンスオリゴマーは、少なくとも1つの保持されたイントロンの5’スプライス部位の約100ヌクレオチド下流から少なくとも1つの保持されたイントロンの3’スプライス部位の約100ヌクレオチド上流の領域内にあるRIC mRNA前駆体の一部を標的とする、[55]から[68]のいずれか1つに記載の組成物。
[71]
RIC mRNA前駆体の標的部分は、(a)保持されたイントロンの5’スプライス部位に隣接しているエクソンにおける+2eから-4eの領域内;
または(b)保持されたイントロンの3’スプライス部位に隣接しているエクソンにおける+2eから-4eの領域内にある、[55]から[68]のいずれか1つに記載の組成物。
[72]
アンチセンスオリゴマーは、標的タンパク質または機能的RNAをコードする遺伝子から転写されたmRNA前駆体の選択的スプライシングを調節することにより標的タンパク質または機能的RNAの量を増加させない、[55]から[71]のいずれか1つに記載の組成物。
[73]
アンチセンスオリゴマーは、標的タンパク質または機能的RNAをコードする遺伝子の変異から結果として生じる異常スプライシングを調節することにより標的タンパク質または機能的RNAの量を増加させない、[55]から[72]のいずれか1つに記載の組成物。
[74]
RIC mRNA前駆体は、全長mRNA前駆体または野生型mRNA前駆体からの部分的スプライシングによって産生された、[55]から[73]のいずれか1つに記載の組成物。
[75]
標的タンパク質または機能的RNAをコードするmRNAは、全長成熟mRNAまたは野生型成熟mRNAである、[55]から[74]のいずれか1つに記載の組成物。
[76]
産生される標的タンパク質は、全長タンパク質または野生型タンパク質である、[55]から[75]のいずれか1つに記載の組成物。
[77]
保持されたイントロンは律速イントロンである、[55]から[76]のいずれか1つに記載の組成物。
[78]
保持されたイントロンは、RIC mRNA前駆体において最も豊富な保持されたイントロンである、[55]から[77]のいずれか1つに記載の組成物。
[79]
保持されたイントロンは、RIC mRNA前駆体において2番目に豊富な保持されたイントロンである、[55]から[77]のいずれか1つに記載の組成物。
[80]
アンチセンスオリゴマーは、ホスホロチオエート結合またはホスホロジアミデート結合を含む骨格修飾を含む、[55]から[79]のいずれか1つに記載の組成物。
[81]
アンチセンスオリゴマーはアンチセンスオリゴヌクレオチドである、[55]から[80]のいずれか1つに記載の組成物。
[82]
アンチセンスオリゴマーは、ホスホロジアミデートモルホリノ、ロックド核酸、ペプチド核酸、2’-O-メチル部分、2’-フルオロ部分、または2’-O-メトキシエチル部分を含む、[55]から[81]のいずれか1つに記載の組成物。
[83]
アンチセンスオリゴマーは少なくとも1つの修飾された糖部を含む、[55]から[82]のいずれか1つに記載の組成物。
[84]
各糖部は修飾された糖部である、[83]に記載の組成物。
[85]
アンチセンスオリゴマーは、8から50の核酸塩基、8から40の核酸塩基、8から35の核酸塩基、8から30の核酸塩基、8から25の核酸塩基、8から20の核酸塩基、8から15の核酸塩基、9から50の核酸塩基、9から40の核酸塩基、9から35の核酸塩基、9から30の核酸塩基、9から25の核酸塩基、9から20の核酸塩基、9から15の核酸塩基、10から50の核酸塩基、10から40の核酸塩基、10から35の核酸塩基、10から30の核酸塩基、10から25の核酸塩基、10から20の核酸塩基、10から15の核酸塩基、11から50の核酸塩基、11から40の核酸塩基、11から35の核酸塩基、11から30の核酸塩基、11から25の核酸塩基、11から20の核酸塩基、11から15の核酸塩基、12から50の核酸塩基、12から40の核酸塩基、12から35の核酸塩基、12から30の核酸塩基、12から25の核酸塩基、12から20の核酸塩基、または12から15の核酸塩基から成る、[55]から[84]のいずれか1つに記載の組成物。
[86]
アンチセンスオリゴマーは、タンパク質をコードするRIC mRNA前駆体の標的部分に、少なくとも80%、少なくとも85%、少なくとも90%、少なくとも95%、少なくとも98%、少なくとも99%、または100%相補的である、[55]から[85]のいずれか1つに記載の組成物。
[87]
アンチセンスオリゴマーは、ROM1、TEAD1、RDH5、NR2E3、PAX6、CRX、FSCN2、ABCA4、MYOC、TCF4、MFSD8、CTNS、NXNL1、OPTN、RLBP1、RPE65、LRAT、RDH8、RDH12、RGR、CNGA3、ALMS1、PER1またはIDUAのRIC mRNA前駆体の標的部分へ結合する、[55]から[86]のいずれか1つに記載の組成物。
[88]
[55]から[87]の組成物のいずれかのアンチセンスオリゴマー、および賦形剤を含む、医薬組成物。
[89]
硝子体内注射、網膜下注射、局所投与、移植、腹腔内注射、筋肉内注射、皮下注射、または静脈内注射によって[88]の医薬組成物を投与することにより、必要としている被験体を処置する方法。
[90]
医薬組成物であって、該医薬組成物は:不足しているROM1、TEAD1、RDH5、NR2E3、PAX6、CRX、FSCN2、ABCA4、MYOC、TCF4、MFSD8、CTNS、NXNL1、OPTN、RLBP1、RPE65、LRAT、RDH8、RDH12、RGR、CNGA3、ALMS1、PER1、またはIDUAのmRNAの転写産物の標的配列にハイブリダイズするアンチセンスオリゴマーであって、ここで、該不足しているROM1、TEAD1、RDH5、NR2E3、PAX6、CRX、FSCN2、ABCA4、MYOC、TCF4、MFSD8、CTNS、NXNL1、OPTN、RLBP1、RPE65、LRAT、RDH8、RDH12、RGR、CNGA3、ALMS1、PER1、またはIDUAのmRNAの転写産物は、保持されたイントロンを含み、該アンチセンスオリゴマーは、不足しているROM1、TEAD1、RDH5、NR2E3、PAX6、CRX、FSCN2、ABCA4、MYOC、TCF4、MFSD8、CTNS、NXNL1、OPTN、RLBP1、RPE65、LRAT、RDH8、RDH12、RGR、CNGA3、ALMS1、PER1、またはIDUAのmRNAの転写産物からの保持されたイントロンのスプライシングアウトを誘発する、アンチセンスオリゴマーと、薬学的に許容可能な賦形剤と、を含む、医薬組成物。
[91]
不足しているROM1、TEAD1、RDH5、NR2E3、PAX6、CRX、FSCN2、ABCA4、MYOC、TCF4、MFSD8、CTNS、NXNL1、OPTN、RLBP1、RPE65、LRAT、RDH8、RDH12、RGR、CNGA3、ALMS1、PER1、またはIDUAのRIC mRNA前駆体の転写産物である、[90]に記載の医薬組成物。
[92]
ROM1、TEAD1、RDH5、NR2E3、PAX6、CRX、FSCN2、ABCA4、MYOC、TCF4、MFSD8、CTNS、NXNL1、OPTN、RLBP1、RPE65、LRAT、RDH8、RDH12、RGR、CNGA3、ALMS1、PER1、またはIDUAのRIC mRNA前駆体の標的部分は、保持されたイントロンの5’スプライス部位に対する+500から保持されたイントロンの3’スプライス部位に対する-500の領域内の保持されたイントロンにある、[90]または[91]に記載の医薬組成物。
[93]
ROM1、TEAD1、RDH5、NR2E3、PAX6、CRX、FSCN2、ABCA4、MYOC、TCF4、MFSD8、CTNS、NXNL1、OPTN、RLBP1、RPE65、LRAT、RDH8、RDH12、RGR、CNGA3、ALMS1、PER1、またはIDUAのRIC mRNA前駆体の転写産物は、SEQ ID NO:1-[23]のいずれか1つに対して少なくとも約80%、85%、90%、95%、96%、97%、98%、99%、あるいは100%の配列同一性を備えた遺伝子配列によってコードされる、[90]または[91]に記載の医薬組成物。
[94]
ROM1、TEAD1、RDH5、NR2E3、PAX6、CRX、FSCN2、ABCA4、MYOC、TCF4、MFSD8、CTNS、NXNL1、OPTN、RLBP1、RPE65、LRAT、RDH8、RDH12、RGR、CNGA3、ALMS1、PER1、またはIDUAのRIC mRNA前駆体の転写産物は、SEQ ID NO:24-[83]のいずれか1つに対して少なくとも約80%、85%、90%、95%、96%、97%、98%、99%、あるいは100%の配列同一性を備えた配列を含む、[90]または[91]に記載の医薬組成物。
[95]
アンチセンスオリゴマーは、ホスホロチオエート結合またはホスホロジアミデート結合を含む骨格修飾を含む、[90]に記載の医薬組成物。
[96]
アンチセンスオリゴマーはアンチセンスオリゴヌクレオチドである、[90]に記載の医薬化合物。
[97]
アンチセンスオリゴマーは、ホスホロジアミデートモルホリノ、ロックド核酸、ペプチド核酸、2’-O-メチル部分、2’-フルオ部分ロ、または2’-O-メトキシエチル部分を含む、[90]に記載の医薬組成物。
[98]
アンチセンスオリゴマーは少なくとも1つの修飾された糖部を含む、[90]に記載の医薬組成物。
[99]
アンチセンスオリゴマーは、8から50の核酸塩基、8から40の核酸塩基、8から35の核酸塩基、8から30の核酸塩基、8から25の核酸塩基、8から20の核酸塩基、8から15の核酸塩基、9から50の核酸塩基、9から40の核酸塩基、9から35の核酸塩基、9から30の核酸塩基、9から25の核酸塩基、9から20の核酸塩基、9から15の核酸塩基、10から50の核酸塩基、10から40の核酸塩基、10から35の核酸塩基、10から30の核酸塩基、10から25の核酸塩基、10から20の核酸塩基、10から15の核酸塩基、11から50の核酸塩基、11から40の核酸塩基、11から35の核酸塩基、11から30の核酸塩基、11から25の核酸塩基、11から20の核酸塩基、11から15の核酸塩基、12から50の核酸塩基、12から40の核酸塩基、12から35の核酸塩基、12から30の核酸塩基、12から25の核酸塩基、12から20の核酸塩基、または12から15の核酸塩基を含む、[90]に記載の医薬組成物。
[100]
アンチセンスオリゴマーは、ROM1、TEAD1、RDH5、NR2E3、PAX6、CRX、FSCN2、ABCA4、MYOC、TCF4、MFSD8、CTNS、NXNL1、OPTN、RLBP1、RPE65、LRAT、RDH8、RDH12、RGR、CNGA3、ALMS1、PER1、またはIDUAのRIC mRNA前駆体の転写産物の標的部分に、少なくとも80%、少なくとも85%、少なくとも90%、少なくとも95%、少なくとも98%、少なくとも99%、または100%相補的である、[90]または[91]に記載の医薬組成物。
[101]
ROM1、TEAD1、RDH5、NR2E3、PAX6、CRX、FSCN2、ABCA4、MYOC、TCF4、MFSD8、CTNS、NXNL1、OPTN、RLBP1、RPE65、LRAT、RDH8、RDH12、RGR、CNGA3、ALMS1、PER1、またはIDUAのRIC mRNA前駆体の転写産物の標的部分は、SEQ ID NO:26655-26714から選択される配列内にある、[90]または[91]に記載の医薬組成物。
[102]
アンチセンスオリゴマーは、SEQ ID NO:84-26[654]のいずれか1つに対して、少なくとも約80%、85%、90%、91%、92%、93%、94%、95%、96%、97%、98%、または99%の配列同一性であるヌクレオチド配列を含む、[90]に記載の医薬組成物。
[103]
アンチセンスオリゴマーは、SEQ ID NO:84-26654から選択されるヌクレオチド配列を含む、[90]に記載の医薬組成物。
[104]
医薬組成物は、髄腔内注射、脳室内注射、腹腔内注射、筋肉内注射、皮下注射、または静脈内注射のために製剤される、[90]から[103]のいずれか1つに記載の医薬組成物。
[105]
保持されたイントロンの除去を促進するために、不足しているROM1、TEAD1、RDH5、NR2E3、PAX6、CRX、FSCN2、ABCA4、MYOC、TCF4、MFSD8、CTNS、NXNL1、OPTN、RLBP1、RPE65、LRAT、RDH8、RDH12、RGR、CNGA3、ALMS1、PER1またはIDUAのmRNAの転写産物の処理を誘発し、ROM1、TEAD1、RDH5、NR2E3、PAX6、CRX、FSCN2、ABCA4、MYOC、TCF4、MFSD8、CTNS、NXNL1、OPTN、RLBP1、RPE65、LRAT、RDH8、RDH12、RGR、CNGA3、ALMS1、PER1、またはIDUAのタンパク質の機能的形態をコードする、完全に処理されたROM1、TEAD1、RDH5、NR2E3、PAX6、CRX、FSCN2、ABCA4、MYOC、TCF4、MFSD8、CTNS、NXNL1、OPTN、RLBP1、RPE65、LRAT、RDH8、RDH12、RGR、CNGA3、ALMS1、PER1またはIDUAのmRNAの転写産物を産生する方法であって、該方法は:
(a)アンチセンスオリゴマーを被験体の標的細胞と接触させる工程と;
(b)アンチセンスオリゴマーを、不足しているROM1、TEAD1、RDH5、NR2E3、PAX6、CRX、FSCN2、ABCA4、MYOC、TCF4、MFSD8、CTNS、NXNL1、OPTN、RLBP1、RPE65、LRAT、RDH8、RDH12、RGR、CNGA3、ALMS1、PER1またはIDUAのmRNAの転写産物にハイブリダイズする工程であって、ここで、不足しているROM1、TEAD1、RDH5、NR2E3、PAX6、CRX、FSCN2、ABCA4、MYOC、TCF4、MFSD8、CTNS、NXNL1、OPTN、RLBP1、RPE65、LRAT、RDH8、RDH12、RGR、CNGA3、ALMS1、PER1、またはIDUAのmRNAの転写産物は、ROM1、TEAD1、RDH5、NR2E3、PAX6、CRX、FSCN2、ABCA4、MYOC、TCF4、MFSD8、CTNS、NXNL1、OPTN、RLBP1、RPE65、LRAT、RDH8、RDH12、RGR、CNGA3、ALMS1、PER1、またはIDUAのタンパク質の機能的形態をコード可能であり、少なくとも1つの保持されたイントロンを含む、工程と;
(c)ROM1、TEAD1、RDH5、NR2E3、PAX6、CRX、FSCN2、ABCA4、MYOC、TCF4、MFSD8、CTNS、NXNL1、OPTN、RLBP1、RPE65、LRAT、RDH8、RDH12、RGR、CNGA3、ALMS1、PER1、またはIDUAのタンパク質の機能的形態をコードする、完全に処理されたROM1、TEAD1、RDH5、NR2E3、PAX6、CRX、FSCN2、ABCA4、MYOC、TCF4、MFSD8、CTNS、NXNL1、OPTN、RLBP1、RPE65、LRAT、RDH8、RDH12、RGR、CNGA3、ALMS1、PER1またはIDUAのmRNAの転写産物を産生するために、不足しているROM1、TEAD1、RDH5、NR2E3、PAX6、CRX、FSCN2、ABCA4、MYOC、TCF4、MFSD8、CTNS、NXNL1、OPTN、RLBP1、RPE65、LRAT、RDH8、RDH12、RGR、CNGA3、ALMS1、PER1またはIDUAのmRNAの転写産物から少なくとも1つの保持されたイントロンを取り除く工程と;
(d)完全に処理されたROM1、TEAD1、RDH5、NR2E3、PAX6、CRX、FSCN2、ABCA4、MYOC、TCF4、MFSD8、CTNS、NXNL1、OPTN、RLBP1、RPE65、LRAT、RDH8、RDH12、RGR、CNGA3、ALMS1、PER1またはIDUAのmRNAの転写産物から、ROM1、TEAD1、RDH5、NR2E3、PAX6、CRX、FSCN2、ABCA4、MYOC、TCF4、MFSD8、CTNS、NXNL1、OPTN、RLBP1、RPE65、LRAT、RDH8、RDH12、RGR、CNGA3、ALMS1、PER1、またはIDUAのタンパク質の機能的形態を翻訳する工程と;
を含む、方法。
[106]
保持されたイントロンは保持されたイントロン全体である、[105]に記載の方法。
[107]
不足しているROM1、TEAD1、RDH5、NR2E3、PAX6、CRX、FSCN2、ABCA4、MYOC、TCF4、MFSD8、CTNS、NXNL1、OPTN、RLBP1、RPE65、LRAT、RDH8、RDH12、RGR、CNGA3、ALMS1、PER1、またはIDUAのmRNAの転写産物は、ROM1、TEAD1、RDH5、NR2E3、PAX6、CRX、FSCN2、ABCA4、MYOC、TCF4、MFSD8、CTNS、NXNL1、OPTN、RLBP1、RPE65、LRAT、RDH8、RDH12、RGR、CNGA3、ALMS1、PER1、またはIDUAのRIC mRNA前駆体の転写産物である、[105]または[106]に記載の方法。
[108]
ROM1、TEAD1、RDH5、NR2E3、PAX6、CRX、FSCN2、ABCA4、MYOC、TCF4、MFSD8、CTNS、NXNL1、OPTN、RLBP1、RPE65、LRAT、RDH8、RDH12、RGR、CNGA3、ALMS1、PER1、またはIDUAタンパク質の量または活性の不足によって引き起こされた疾病を抱える被験体を処置する方法であって、該方法は、SEQ ID NO:84-26[654]のいずれか1つに対して、少なくとも約80%、85%、90%、91%、92%、93%、94%、95%、96%、97%、98%、または99%の配列同一性を備えるヌクレオチド配列を含むアンチセンスオリゴマーを、被験体へ投与する工程を含む、方法。
本発明は、以下の実施例によってより具体的に例示されるだろう。しかしながら、本発明がどんな方法でもこれらの実施例によって制限されていないことが理解されるべきである。
実施例1:次世代配列決定を用いるRNAseqによるROM1、TEAD1、RDH5、PAX6、FSCN2、MYOC、TCF4、MFSD8、CTNS、OPTN、RLBP1、RPE65、LRAT、RDH8、RDH12、RGR、CNGA3、ALMS1、PER1、およびIDUA転写産物におけるイントロン保持事象の特定
イントロン保持事象を特定するための、ROM1、TEAD1、RDH5、PAX6、FSCN2、MYOC、TCF4、MFSD8、CTNS、OPTN、RLBP1、RPE65、LRAT、RDH8、RDH12、RGR、CNGA3、ALMS1、PER1、およびIDUA遺伝子により産生される転写産物のスナップショットを明らかにするために次世代配列決定を用いて全トランスクリプトームショットガン配列を実行した。このために、細胞の核および細胞質の分画からのpolyA+ RNAを、IlluminaのTruSeq Stranded mRNAライブラリPrepキットを用いて構築されたcDNAライブラリから分離した。ARPE-19細胞または星状細胞がほとんどの分析に使用され、(RDH8とRDH12についての)あるケースでは、ヒト網膜トランスクリプトームデータが使用された(Farkas, et al.,2013, “Transcriptome analyses of the human retina identify unprecedented transcript diversity and 3.5 Mb of novel transcribed sequence via significant alternative splicing and novel genes,” BMC Genomics 14:486、該文献は参照により本明細書に組み込まれる)。ライブラリを対末端配列決定(pair-end sequenced)し、結果として、ヒトゲノムにマッピングされうる100ヌクレオチドの読み取りをもたらした。マッピングされた読み取りは(UCSC Genome Informatics Group (Center for Biomolecular Science & Engineering, University of California, Santa Cruz, 1156 High Street, Santa Cruz, CA 95064)によって操作され、かつ、例えばRosenbloom, et al., 2015,”The UCSC Genome Browser database: 2015 update,”Nucleic Acids Research 43, Database Issue doi: 10.1093/nar/gku1177に記載された)UCSCのゲノムブラウザを使用して視覚化され、読み取りの範囲および数はピーク信号によって推論される。ピークの高さは、特定の領域における読取密度によって与えられた発現のレベルを示している。ピークをエクソン領域およびイントロン領域に一致させられるように、(読み取りシグナルの下に)UCSCゲノムブラウザによってP遺伝子の模式図(縮尺通りに描かれている)が提供される。このディスプレイに基づいて、細胞の核分画においては高い読取密度を有するが、細胞質分画においては読み取りが非常に低いかまったく無いイントロンを特定した。これは、これらのイントロンが保持されたこと、および、イントロンを含む転写産物が核内に残っていることを示し、かつ、この保持されたRIC mRNA前駆体が、細胞質に排出されないので、非生産的であることを示唆している。
イントロン保持事象を特定するために本明細書で記載されたCRX、ABCA4、MYOC、およびNXNL1遺伝子によって生成された転写産物のスナップショットを明らかにするために、次世代配列決定を使用して、全トランスクリプトームのショットガン配列決定を実行した。このために、THLE-3(ヒト肝上皮)細胞の核および細胞質の分画からのpolyA+ RNAを分離し、IlluminaのTruSeq Stranded mRNAライブラリPrepキットを用いてcDNAライブラリを構築した。ライブラリは対末端配列形成され、ヒトゲノムにマッピングされた100ヌクレオチドの読み取りをもたらす。マッピングされた読み取りは(UCSC Genome Informatics Group (Center for Biomolecular Science & Engineering, University of California, Santa Cruz,1156 High Street,Santa Cruz, CA 95064)によって操作され、かつ、例えばRosenbloom, et al.,2015,”The UCSC Genome Browser database: 2015 update,”Nucleic Acids Research 43, Database Issue doi: 10.1093/nar/gku1177に記載された)UCSCのゲノムブラウザを使用して視覚化され、読み取りの範囲および数はピーク信号によって推論される。ピークの高さは、特定の領域における読取密度によって与えられた発現のレベルを示している。ピークをエクソン領域およびイントロン領域に一致させられるように、UCSCゲノムブラウザによって遺伝子の模式図が提供される。このディスプレイに基づいて、THLE-3細胞の核分画においては高い読取密度を有するが、これらの細胞の細胞質分画においては読み取りが非常に低いかまったく無いイントロンを特定した。これは、これらのイントロンが保持されたこと、および、イントロン含有転写産物が核内に残っていることを示し、かつ、この保持されたRIC mRNA前駆体が細胞質に排出されないので、非生産的であることを示唆している。
ASOウォークは、本明細書に記述された方法を使用して、保持されたイントロンを標的とするように設計された。例えばヌクレオチド+6から+69に及ぶイントロン5’スプライス部位のすぐ下流の領域と、例えばイントロンのヌクレオチド-16から-79に及ぶイントロン3’スプライス部位すぐ上流の領域とが、2’-O-Me RNA、PS骨格、5ヌクレオチド間隔でシフトした18mer ASOで標的とされた。表1は、設計された例示的なASOおよびそれらの標的配列を列挙する。
ASOを用いた標的遺伝子イントロンスプライシング効率の増加を判定するために、本明細書に記述された方法を使用した。ARPE-19細胞、すなわちヒトの網膜上皮細胞株(American Type Culture Collection (ATCC),USA)を偽トランスフェクトし、または表1に記載の標的化ASOでトランスフェクトした。細胞を、供給元の仕様書に従って、Lipofectamine RNAiMaxトランスフェクション試薬(Thermo Fisher)を用いてトランスフェクトする。簡潔に述べると、ASOを96ウェル組織培養プレートに播種し、Opti-MEMで希釈したRNAiMaxと組み合わせる。トリプシンを用いて細胞を剥離し、完全培地に再懸濁し、約25,000個の細胞をASOトランスフェクション混合物に加える。トランスフェクション実験は三通りのプレート複製において実行される。最終的なASO濃度は80nMであった。供給元の仕様書に従って、培地をトランスフェクションの6時間後に交換し、細胞をCells-to-Ct溶解試薬を用い、DNAse(Thermo Fisher)で試薬を補充し、24時間で採取する。供給元の仕様書に従い、cDNAをCells-to-Ct RT試薬(Thermo Fisher)で生成される。対象のイントロンでのスプライシングの量を定量化するために、対応するエクソン-エクソンジャンクション(Thermo Fisher)に及ぶプローブでTaqmanアッセイを用いて、定量PCRが実行される。Taqmanアッセイは、QuantStudio 7Flex Real-Time PCRシステム(Thermo Fisher)上で、供給元の仕様書に従い実行される。標的遺伝子アッセイ値を、RPL32(deltaCt)およびプレート一致偽トランスフェクションサンプル(delta-delta Ct)に対して正規化し、モック定量(2 ^-(delta-delta Ct)に対して倍率変化を生成する。3つのプレート複製のモック(mock)に対する平均倍率変化をプロットする(図4、図6および図7)。標的遺伝子発現を増加させるいくつかのASOが特定され、図4、図6および図7に示されるように、その標的イントロンでのスプライシングの増加が示唆された。標的イントロンの保持を確認する全トランスクリプトームデータ(図3および図5)と共に、これらの結果は、ASOが律速イントロンのスプライシング効率を改善し得ることを確認する。
ASOを用いた標的遺伝子イントロンスプライシング効率の増加を判定するために、本明細書に記述された方法を使用した。ARPE-19細胞、すなわちヒトの網膜上皮細胞株(American Type Culture Collection (ATCC),USA)を偽トランスフェクトし、または表1に記載の標的化ASOでトランスフェクトした。細胞を、供給元の仕様書に従って、Lipofectamine RNAiMaxトランスフェクション試薬(Thermo Fisher)を用いてトランスフェクトする。簡潔に述べると、ASOを96ウェル組織培養プレートに播種し、Opti-MEMで希釈したRNAiMaxと組み合わせる。トリプシンを用いて細胞を剥離し、完全培地に再懸濁し、約25,000個の細胞をASOトランスフェクション混合物に加える。トランスフェクション実験は三通りのプレート複製において実行される。最終的なASO濃度は80nMであった。供給元の仕様書に従って、培地をトランスフェクションの6時間後に交換し、細胞をCells-to-Ct溶解試薬を用い、DNAse(Thermo Fisher)で試薬を補充し、24時間で採取する。供給元の仕様書に従い、cDNAをCells-to-Ct RT試薬(Thermo Fisher)で生成される。対象のイントロンでのスプライシングの量を定量化するために、対応するエクソン-エクソンジャンクション(Thermo Fisher)に及ぶプローブでTaqmanアッセイを用いて、定量PCRが実行される。Taqmanアッセイは、QuantStudio 7Flex Real-Time PCRシステム(Thermo Fisher)上で、供給元の仕様書に従い実行される。標的遺伝子アッセイ値を、RPL32(deltaCt)およびプレート一致偽トランスフェクションサンプル(delta-delta Ct)に対して正規化し、モック定量(2 ^-(delta-delta Ct)に対して倍率変化を生成する。3つのプレート複製のモック(mock)に対する平均倍率変化をプロットする(図10)。標的遺伝子発現を増加させるいくつかのASOが特定され、図10に示されるように、その標的イントロンでのスプライシングの増加が示唆された。標的イントロンの保持を確認する全トランスクリプトームデータ(図8および図9)と共に、これらの結果は、ASOが律速イントロンのスプライシング効率を改善し得ることを確認する。
ASOを用いた標的遺伝子イントロンスプライシング効率の増加を判定するために、本明細書に記述された方法を使用した。ARPE-19細胞、すなわちヒトの網膜上皮細胞株(American Type Culture Collection (ATCC),USA)を偽トランスフェクトし、または表1に記載の標的化ASOでトランスフェクトした。細胞を、供給元の仕様書に従って、Lipofectamine RNAiMaxトランスフェクション試薬(Thermo Fisher)を用いてトランスフェクトする。簡潔に述べると、ASOを96ウェル組織培養プレートに播種し、Opti-MEMで希釈したRNAiMaxと組み合わせる。トリプシンを用いて細胞を剥離し、完全培地に再懸濁し、約25,000個の細胞をASOトランスフェクション混合物に加える。トランスフェクション実験は三通りのプレート複製において実行される。最終的なASO濃度は80nMであった。供給元の仕様書に従って、培地をトランスフェクションの6時間後に交換し、細胞をCells-to-Ct溶解試薬を用い、DNAse(Thermo Fisher)で試薬を補充し、24時間で採取する。供給元の仕様書に従い、cDNAをCells-to-Ct RT試薬(Thermo Fisher)で生成される。対象のイントロンでのスプライシングの量を定量化するために、対応するエクソン-エクソンジャンクション(Thermo Fisher)に及ぶプローブでTaqmanアッセイを用いて、定量PCRが実行される。Taqmanアッセイは、QuantStudio 7Flex Real-Time PCRシステム(Thermo Fisher)上で、供給元の仕様書に従い実行される。標的遺伝子アッセイ値を、RPL32(deltaCt)およびプレート一致偽トランスフェクションサンプル(delta-delta Ct)に対して正規化し、モック定量(2 ^-(delta-delta Ct)に対して倍率変化を生成する。3つのプレート複製のモック(mock)に対する平均倍率変化をプロットする(図12)。標的遺伝子発現を増加させるいくつかのASOが特定され、図12に示されるように、その標的イントロンでのスプライシングの増加が示唆された。標的イントロンの保持を確認する全トランスクリプトームデータ(図11)と共に、これらの結果は、ASOが律速イントロンのスプライシング効率を改善し得ることを確認する。
ASOを用いた標的遺伝子イントロンスプライシング効率の増加を判定するために、本明細書に記述された方法を使用した。ARPE-19細胞、すなわちヒトの網膜上皮細胞株(American Type Culture Collection (ATCC),USA)を偽トランスフェクトし、または表1に記載の標的化ASOでトランスフェクトした。細胞を、供給元の仕様書に従って、Lipofectamine RNAiMaxトランスフェクション試薬(Thermo Fisher)を用いてトランスフェクトする。簡潔に述べると、ASOを96ウェル組織培養プレートに播種し、Opti-MEMで希釈したRNAiMaxと組み合わせる。トリプシンを用いて細胞を剥離し、完全培地に再懸濁し、約25,000個の細胞をASOトランスフェクション混合物に加える。トランスフェクション実験は三通りのプレート複製において実行される。最終的なASO濃度は80nMであった。供給元の仕様書に従って、培地をトランスフェクションの6時間後に交換し、細胞をCells-to-Ct溶解試薬を用い、DNAse(Thermo Fisher)で試薬を補充し、24時間で採取する。供給元の仕様書に従い、cDNAをCells-to-Ct RT試薬(Thermo Fisher)で生成される。対象のイントロンでのスプライシングの量を定量化するために、対応するエクソン-エクソンジャンクション(Thermo Fisher)に及ぶプローブでTaqmanアッセイを用いて、定量PCRが実行される。Taqmanアッセイは、QuantStudio 7Flex Real-Time PCRシステム(Thermo Fisher)上で、供給元の仕様書に従い実行される。標的遺伝子アッセイ値を、RPL32(deltaCt)およびプレート一致偽トランスフェクションサンプル(delta-delta Ct)に対して正規化し、モック定量(2 ^-(delta-delta Ct)に対して倍率変化を生成する。3つのプレート複製のモック(mock)に対する平均倍率変化をプロットする(図14)。標的遺伝子発現を増加させるいくつかのASOが特定され、図14に示されるように、その標的イントロンでのスプライシングの増加が示唆された。標的イントロンの保持を確認する全トランスクリプトームデータ(図13および図15)と共に、これらの結果は、ASOが律速イントロンのスプライシング効率を改善し得ることを確認する。
ASOを用いた標的遺伝子イントロンスプライシング効率の増加を判定するために、本明細書に記述された方法を使用した。ARPE-19細胞、すなわちヒトの網膜上皮細胞株(American Type Culture Collection (ATCC),USA)を偽トランスフェクトし、または表1に記載の標的化ASOでトランスフェクトした。細胞を、供給元の仕様書に従って、Lipofectamine RNAiMaxトランスフェクション試薬(Thermo Fisher)を用いてトランスフェクトする。簡潔に述べると、ASOを96ウェル組織培養プレートに播種し、Opti-MEMで希釈したRNAiMaxと組み合わせる。トリプシンを用いて細胞を剥離し、完全培地に再懸濁し、約25,000個の細胞をASOトランスフェクション混合物に加える。トランスフェクション実験は三通りのプレート複製において実行される。最終的なASO濃度は80nMであった。供給元の仕様書に従って、培地をトランスフェクションの6時間後に交換し、細胞をCells-to-Ct溶解試薬を用い、DNAse(Thermo Fisher)で試薬を補充し、24時間で採取する。供給元の仕様書に従い、cDNAをCells-to-Ct RT試薬(Thermo Fisher)で生成される。対象のイントロンでのスプライシングの量を定量化するために、対応するエクソン-エクソンジャンクション(Thermo Fisher)に及ぶプローブでTaqmanアッセイを用いて、定量PCRが実行される。Taqmanアッセイは、QuantStudio 7Flex Real-Time PCRシステム(Thermo Fisher)上で、供給元の仕様書に従い実行される。標的遺伝子アッセイ値を、RPL32(deltaCt)およびプレート一致偽トランスフェクションサンプル(delta-delta Ct)に対して正規化し、モック定量(2 ^-(delta-delta Ct)に対して倍率変化を生成する。3つのプレート複製のモック(mock)に対する平均倍率変化をプロットする(図17)。標的遺伝子発現を増加させるいくつかのASOが特定され、図17に示されるように、その標的イントロンでのスプライシングの増加が示唆された。標的イントロンの保持を確認する全トランスクリプトームデータ(図16)と共に、これらの結果は、ASOが律速イントロンのスプライシング効率を改善し得ることを確認する。
ASOを用いた標的遺伝子イントロンスプライシング効率の増加を判定するために、本明細書に記述された方法を使用した。ARPE-19細胞、すなわちヒトの網膜上皮細胞株(American Type Culture Collection (ATCC),USA)を偽トランスフェクトし、または表1に記載の標的化ASOでトランスフェクトした。細胞を、供給元の仕様書に従って、Lipofectamine RNAiMaxトランスフェクション試薬(Thermo Fisher)を用いてトランスフェクトする。簡潔に述べると、ASOを96ウェル組織培養プレートに播種し、Opti-MEMで希釈したRNAiMaxと組み合わせる。トリプシンを用いて細胞を剥離し、完全培地に再懸濁し、約25,000個の細胞をASOトランスフェクション混合物に加える。トランスフェクション実験は三通りのプレート複製において実行される。最終的なASO濃度は80nMであった。供給元の仕様書に従って、培地をトランスフェクションの6時間後に交換し、細胞をCells-to-Ct溶解試薬を用い、DNAse(Thermo Fisher)で試薬を補充し、24時間で採取する。供給元の仕様書に従い、cDNAをCells-to-Ct RT試薬(Thermo Fisher)で生成される。対象のイントロンでのスプライシングの量を定量化するために、対応するエクソン-エクソンジャンクション(Thermo Fisher)に及ぶプローブでTaqmanアッセイを用いて、定量PCRが実行される。Taqmanアッセイは、QuantStudio 7Flex Real-Time PCRシステム(Thermo Fisher)上で、供給元の仕様書に従い実行される。標的遺伝子アッセイ値を、RPL32(deltaCt)およびプレート一致偽トランスフェクションサンプル(delta-delta Ct)に対して正規化し、モック定量(2 ^-(delta-delta Ct)に対して倍率変化を生成する。3つのプレート複製のモック(mock)に対する平均倍率変化をプロットする(図29および図32)。標的遺伝子発現を増加させるいくつかのASOが特定され、図29および図32に示されるように、その標的イントロンでのスプライシングの増加が示唆された。これらの結果は、ASOが律速イントロンのスプライシング効率を改善しうることを確認する。
ASOを用いた標的遺伝子イントロンスプライシング効率の増加を判定するために、本明細書に記述された方法を使用した。ARPE-19細胞、すなわちヒトの網膜上皮細胞株(American Type Culture Collection (ATCC),USA)を偽トランスフェクトし、または表1に記載の標的化ASOでトランスフェクトした。細胞を、供給元の仕様書に従って、Lipofectamine RNAiMaxトランスフェクション試薬(Thermo Fisher)を用いてトランスフェクトする。簡潔に述べると、ASOを96ウェル組織培養プレートに播種し、Opti-MEMで希釈したRNAiMaxと組み合わせる。トリプシンを用いて細胞を剥離し、完全培地に再懸濁し、約25,000個の細胞をASOトランスフェクション混合物に加える。トランスフェクション実験は三通りのプレート複製において実行される。最終的なASO濃度は80nMであった。供給元の仕様書に従って、培地をトランスフェクションの6時間後に交換し、細胞をCells-to-Ct溶解試薬を用い、DNAse(Thermo Fisher)で試薬を補充し、24時間で採取する。供給元の仕様書に従い、cDNAをCells-to-Ct RT試薬(Thermo Fisher)で生成される。対象のイントロンでのスプライシングの量を定量化するために、対応するエクソン-エクソンジャンクション(Thermo Fisher)に及ぶプローブでTaqmanアッセイを用いて、定量PCRが実行された。Taqmanアッセイは、QuantStudio 7Flex Real-Time PCRシステム(Thermo Fisher)上で、供給元の仕様書に従い実行される。標的遺伝子アッセイ値を、RPL32(deltaCt)およびプレート一致偽トランスフェクションサンプル(delta-delta Ct)に対して正規化し、モック定量(2 ^-(delta-delta Ct)に対して倍率変化を生成する。3つのプレート複製のモック(mock)に対する平均倍率変化をプロットする(図36)。標的遺伝子発現を増加させるいくつかのASOが特定され、図36に示されるように、その標的イントロンでのスプライシングの増加が示唆された。標的イントロンの保持を確認する全体のトランスクリプトームデータ(図35、図37、図38、図39および図40)とともに、これらの結果は、ASOが律速イントロンのスプライシング効率を改善しうることを確認する。
ASOを用いた標的遺伝子イントロンスプライシング効率の増加を判定するために、本明細書に記述された方法を使用した。ARPE-19細胞、すなわちヒトの網膜上皮細胞株(American Type Culture Collection (ATCC),USA)を偽トランスフェクトし、または表1に記載の標的化ASOでトランスフェクトした。細胞を、供給元の仕様書に従って、Lipofectamine RNAiMaxトランスフェクション試薬(Thermo Fisher)を用いてトランスフェクトする。簡潔に述べると、ASOを96ウェル組織培養プレートに播種し、Opti-MEMで希釈したRNAiMaxと組み合わせる。トリプシンを用いて細胞を剥離し、完全培地に再懸濁し、約25,000個の細胞をASOトランスフェクション混合物に加える。トランスフェクション実験は三通りのプレート複製において実行される。最終的なASO濃度は80nMであった。供給元の仕様書に従って、培地をトランスフェクションの6時間後に交換し、細胞をCells-to-Ct溶解試薬を用い、DNAse(Thermo Fisher)で試薬を補充し、24時間で採取する。供給元の仕様書に従い、cDNAをCells-to-Ct RT試薬(Thermo Fisher)で生成される。対象のイントロンでのスプライシングの量を定量化するために、対応するエクソン-エクソンジャンクション(Thermo Fisher)に及ぶプローブでTaqmanアッセイを用いて、定量PCRが実行される。Taqmanアッセイは、QuantStudio 7Flex Real-Time PCRシステム(Thermo Fisher)上で、供給元の仕様書に従い実行される。標的遺伝子アッセイ値を、RPL32(deltaCt)およびプレート一致偽トランスフェクションサンプル(delta-delta Ct)に対して正規化し、モック定量(2 ^-(delta-delta Ct)に対して倍率変化を生成する。3つのプレート複製のモックの平均倍率変化がプロットされる(図43)。いくつかのASOが標的遺伝子の発現を増加させると特定され、図43に示されるように、標的イントロンにおけるスプライシングの増加が示された。標的イントロン(図41および図42)の保持を確認する全トランスクリプトームデータと共に、これらの結果は、ASOが律速イントロンのスプライシング効率を改善し得ることを確認する。
Claims (12)
- OPTNタンパク質をコードする保持されたイントロン含有mRNA前駆体(RIC mRNA前駆体)の標的部分に相補的なアンチセンスオリゴマー(ASO)であって、RIC mRNA前駆体は保持されたイントロンを含み、ASOのRIC mRNA前駆体の標的部分との結合が、RIC mRNA前駆体を発現する細胞内で、保持されたイントロンをRIC mRNA前駆体から構成的にスプライシングさせることにより、細胞内で、OPTNタンパク質をコードする成熟mRNAのレベルを増加させ、RIC mRNA前駆体の標的部分は保持されたイントロン内にあり、保持されたイントロンはイントロン7であり、RIC mRNA前駆体の標的部分は:
(a)保持されたイントロン7の5’スプライス部位に対して+6から+31;
(b)保持されたイントロン7の5’スプライス部位に対して+41から+51;または
(c)保持されたイントロン7の3’スプライス部位に対して-61から-16、
から選択される領域内である、前記ASO。 - RIC mRNA前駆体が、SEQ ID NO:34、35、36、又は37に少なくとも80%、85%、90%、95%、97%、あるいは100%の配列同一性を備えた配列を含む、請求項1に記載のASO。
- RIC mRNA前駆体の標的部分が、SEQ ID NO:26714の少なくとも8つの隣接する核酸を含む領域に少なくとも80%、85%、90%、95%、97%、あるいは100%の配列同一性を備えた配列を含む、請求項1又は2に記載のASO。
- OPTNタンパク質が:
i)同等の野性型タンパク質と比較して、機能が低下した形態;又は
ii)同等の野性型タンパク質と比較して、十分に機能的な形態、
で生成される、請求項1~3のいずれか1項に記載のASO。 - ASOが、ホスホロチオエート結合若しくはホスホロジアミデート結合を含む骨格修飾;又は修飾された糖部若しくは糖アナログを含み、該修飾された糖部若しくは糖アナログが、必要に応じて、ホスホロジアミデートモルホリノ、ロックド核酸、ペプチド核酸、2’-O-メチル、2’-フルオロ、又は2’-O-メトキシエチル部分を含む、請求項1~4のいずれか1項に記載のASO。
- ASOが、8~50の核酸塩基から成る、請求項1~5のいずれかに記載のASO。
- 請求項1~6のいずれか1項に記載のASOを含むポリヌクレオチドを結合させたウイルスベクター。
- 被験体においてOPTNタンパク質の量又は機能が不足していることを特徴とする疾患又は疾病を処置するための医薬組成物であって、請求項1~6のいずれかに記載のASO又は請求項7に記載のウイルスベクターを含む、前記医薬組成物。
- 処置される被験体においてOPTNタンパク質の量又は活性が不足している、請求項8に記載の医薬組成物。
- OPTNタンパク質の量の不足は、OPTNタンパク質のハプロ不全によって引き起こされ、ここで被験体は、機能的なOPTNタンパク質をコードする第1の対立遺伝子、及びOPTNタンパク質が生成されない第2の対立遺伝子又は非機能的なOPTNタンパク質をコードする第2の対立遺伝子を有し、ASOは、第1の対立遺伝子から転写されたRIC mRNA前駆体の標的部分に結合する、請求項8又は9に記載の医薬組成物。
- 被験体は、
(a)
(i)OPTNタンパク質が野生型対立遺伝子からの生成と比較して、減少したレベルで生成される、
(ii)OPTNタンパク質が同等の野性型タンパク質と比較して機能が低下した形態で生成される、あるいは、
(iii)OPTNタンパク質が生成されない、
第1の変異対立遺伝子と、
(b)
(i)OPTNタンパク質が野生型対立遺伝子からの生成と比較して、減少したレベルで生成される、
(ii)OPTNタンパク質が同等の野性型タンパク質と比較して機能が低下した形態で生成される、あるいは、
(iii)OPTNタンパク質が生成されない、
第2の変異対立遺伝子とを有し、
ここで、被験体が第1の変異対立遺伝子(a)(iii)を有するとき、第2の変異対立遺伝子は(b)(i)あるいは(b)(ii)であり、被験体が第2の変異対立遺伝子(b)(iii)を有するとき、第1の変異対立遺伝子は(a)(i)あるいは(a)(ii)であり、ここで、RIC mRNA前駆体は、(a)(i)あるいは(a)(ii)である第1の変異対立遺伝子、又は(b)(i)あるいは(b)(ii)である第2の変異対立遺伝子から転写される、請求項8~10のいずれかに記載の医薬組成物。 - くも膜下腔内注射、脳室内注射、腹腔内注射、筋肉内注射、皮下注射、あるいは静脈内注射による投与用である、請求項8~11のいずれかに記載の医薬組成物。
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2022000109A JP2022046724A (ja) | 2015-12-14 | 2022-01-04 | 眼疾患の処置のための組成物および方法 |
Applications Claiming Priority (5)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US201562267259P | 2015-12-14 | 2015-12-14 | |
| US62/267,259 | 2015-12-14 | ||
| US201662318958P | 2016-04-06 | 2016-04-06 | |
| US62/318,958 | 2016-04-06 | ||
| PCT/US2016/066691 WO2017106370A1 (en) | 2015-12-14 | 2016-12-14 | Compositions and methods for treatment of eye diseases |
Related Child Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2022000109A Division JP2022046724A (ja) | 2015-12-14 | 2022-01-04 | 眼疾患の処置のための組成物および方法 |
Publications (3)
| Publication Number | Publication Date |
|---|---|
| JP2019500348A JP2019500348A (ja) | 2019-01-10 |
| JP2019500348A5 JP2019500348A5 (ja) | 2020-01-30 |
| JP7036723B2 true JP7036723B2 (ja) | 2022-03-15 |
Family
ID=59057531
Family Applications (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2018529249A Active JP7036723B2 (ja) | 2015-12-14 | 2016-12-14 | 眼疾患の処置のための組成物および方法 |
| JP2022000109A Pending JP2022046724A (ja) | 2015-12-14 | 2022-01-04 | 眼疾患の処置のための組成物および方法 |
Family Applications After (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2022000109A Pending JP2022046724A (ja) | 2015-12-14 | 2022-01-04 | 眼疾患の処置のための組成物および方法 |
Country Status (4)
| Country | Link |
|---|---|
| EP (1) | EP3390634A4 (ja) |
| JP (2) | JP7036723B2 (ja) |
| CA (1) | CA3005128A1 (ja) |
| WO (1) | WO2017106370A1 (ja) |
Families Citing this family (20)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| GB201410693D0 (en) | 2014-06-16 | 2014-07-30 | Univ Southampton | Splicing modulation |
| JP6867945B2 (ja) | 2014-10-03 | 2021-05-12 | コールド スプリング ハーバー ラボラトリー | 核内遺伝子出力の標的とされた増強 |
| SG11201802870RA (en) | 2015-10-09 | 2018-05-30 | Univ Southampton | Modulation of gene expression and screening for deregulated protein expression |
| US11096956B2 (en) | 2015-12-14 | 2021-08-24 | Stoke Therapeutics, Inc. | Antisense oligomers and uses thereof |
| EP3933041B1 (en) | 2015-12-14 | 2024-01-31 | Cold Spring Harbor Laboratory | Antisense oligomers for treatment of autosomal dominant retardation |
| BR112019014841A2 (pt) | 2017-01-23 | 2020-04-28 | Regeneron Pharma | rna guia, uso do rna guia, rna antissentido, sirna ou shrna, uso do rna antissentido, do sirna ou do shrna, ácido nucleico isolado, vetor, composição, célula, e, métodos para modificar um gene hsd17b13 em uma célula, para diminuir a expressão de um gene hsd17b13 em uma célula, para modificar uma célula e para tratar um indivíduo que não é portador da variante de hsd17b13 |
| EP3610029A1 (en) | 2017-04-11 | 2020-02-19 | Regeneron Pharmaceuticals, Inc. | Assays for screening activity of modulators of members of the hydroxysteroid (17-beta) dehydrogenase (hsd17b) family |
| GB201706009D0 (en) * | 2017-04-13 | 2017-05-31 | Proqr Therapeutics Ii Bv | Antisense oligonucleotides for the treatment of stargardt disease |
| SG10202108375XA (en) | 2017-08-25 | 2021-09-29 | Stoke Therapeutics Inc | Antisense oligomers for treatment of conditions and diseases |
| CA3078883A1 (en) | 2017-10-11 | 2019-04-18 | Regeneron Pharmaceuticals, Inc. | Inhibition of hsd17b13 in the treatment of liver disease in patients expressing the pnpla3 i148m variation |
| EP3700570A4 (en) * | 2017-10-23 | 2021-08-04 | Stoke Therapeutics, Inc. | ANTISENSE OLIGOMERS FOR THE TREATMENT OF CONDITIONS AND DISEASES BASED ON THE DECLINE OF NON-SENSE MEDIATION RNA |
| RU177889U1 (ru) * | 2017-11-30 | 2018-03-15 | Общество с ограниченной ответственностью "Вертикаль-М" (ООО "Вертикаль-М") | Дренаж для хирургического лечения глаукомы |
| JP2021520837A (ja) * | 2018-04-17 | 2021-08-26 | ザ トラスティーズ オブ ザ ユニバーシティ オブ ペンシルバニア | トランススプライシング分子 |
| CA3103429A1 (en) * | 2018-06-14 | 2019-12-19 | Don W. Cleveland | Compounds and methods for increasing stmn2 expression |
| PE20220013A1 (es) | 2018-07-03 | 2022-01-11 | Hoffmann La Roche | Oligonucleotidos para modular la expresion de tau |
| EP3914712A1 (en) * | 2019-01-25 | 2021-12-01 | Nayan Therapeutics, Inc. | Nr2e3 expression reducing oligonucleotides, compositions containing the same, and methods of their use |
| WO2021034985A1 (en) * | 2019-08-19 | 2021-02-25 | Stoke Therapeutics, Inc. | Compositions and methods for modulating splicing and protein expression |
| JP2023525799A (ja) | 2020-05-11 | 2023-06-19 | ストーク セラピューティクス,インク. | 状態及び疾患の治療のためのopa1アンチセンスオリゴマー |
| WO2023104693A1 (en) * | 2021-12-07 | 2023-06-15 | F. Hoffmann-La Roche Ag | Antisense oligonucleotides targeting actl6b |
| WO2023160454A1 (zh) * | 2022-02-25 | 2023-08-31 | 北京中因科技有限公司 | 表达盒组合及其应用 |
Family Cites Families (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP2630241B1 (en) * | 2010-10-22 | 2018-10-17 | CuRNA, Inc. | Treatment of alpha-l-iduronidase (idua) related diseases by inhibition of natural antisense transcript to idua |
| US10260069B2 (en) * | 2013-02-04 | 2019-04-16 | Ionis Pharmaceuticals, Inc. | Selective antisense compounds and uses thereof |
| US10647983B2 (en) * | 2013-09-04 | 2020-05-12 | Cold Spring Harbor Laboratory | Reducing nonsense-mediated mRNA decay |
| GB201410693D0 (en) * | 2014-06-16 | 2014-07-30 | Univ Southampton | Splicing modulation |
| JP6867945B2 (ja) * | 2014-10-03 | 2021-05-12 | コールド スプリング ハーバー ラボラトリー | 核内遺伝子出力の標的とされた増強 |
-
2016
- 2016-12-14 CA CA3005128A patent/CA3005128A1/en active Pending
- 2016-12-14 EP EP16876610.3A patent/EP3390634A4/en active Pending
- 2016-12-14 WO PCT/US2016/066691 patent/WO2017106370A1/en active Application Filing
- 2016-12-14 JP JP2018529249A patent/JP7036723B2/ja active Active
-
2022
- 2022-01-04 JP JP2022000109A patent/JP2022046724A/ja active Pending
Non-Patent Citations (2)
| Title |
|---|
| Journal of the Neurological Sciences,Vol.309,2011年,p.16-17 |
| NATURE,2010年,Vol 465,p.223-227 |
Also Published As
| Publication number | Publication date |
|---|---|
| JP2022046724A (ja) | 2022-03-23 |
| JP2019500348A (ja) | 2019-01-10 |
| CA3005128A1 (en) | 2017-06-22 |
| EP3390634A1 (en) | 2018-10-24 |
| EP3390634A4 (en) | 2019-08-14 |
| WO2017106370A1 (en) | 2017-06-22 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP7036723B2 (ja) | 眼疾患の処置のための組成物および方法 | |
| US20220118000A1 (en) | Antisense oligomers and uses thereof | |
| JP7049249B2 (ja) | 中枢神経系疾患の処置のための組成物および方法 | |
| Richardson et al. | The zebrafish eye—a paradigm for investigating human ocular genetics | |
| JP6395058B2 (ja) | ハンチンチン対する、組成物及びその使用 | |
| den Hollander et al. | Leber congenital amaurosis: genes, proteins and disease mechanisms | |
| Wang et al. | ABCB6 mutations cause ocular coloboma | |
| JP7054675B2 (ja) | 網膜色素変性症18と網膜色素変性症13の処置のための組成物と方法 | |
| Graw | Cataract mutations and lens development | |
| EP2900821B1 (en) | Peptide-linked morpholino antisense oligonucleotides for treatment of myotonic dystrophy | |
| CA3137740A1 (en) | Oligonucleotide compositions and methods of use thereof | |
| Lentz et al. | Deafness and retinal degeneration in a novel USH1C knock‐in mouse model | |
| JP2019500345A (ja) | 肝臓病の処置のための組成物および方法 | |
| CN108291225A (zh) | 单链反义寡核苷酸在预防或治疗涉及三核苷酸重复扩增的遗传疾病中的用途 | |
| Guziewicz et al. | Molecular consequences of BEST1 gene mutations in canine multifocal retinopathy predict functional implications for human bestrophinopathies | |
| Palmer et al. | Expression of Gtf2ird1, the Williams syndrome-associated gene, during mouse development | |
| CN113134076A (zh) | 一种利用转录因子再生具备功能的视网膜神经节细胞的方法 | |
| JP2018524982A (ja) | マイクロrna‐328アンチセンス組成物及び治療用途 | |
| WO2022166815A1 (zh) | 用于治疗增殖性玻璃体视网膜病变的双链核酸分子及其应用 | |
| CN107532181A (zh) | Mirna模拟物和它们在治疗感觉病患中的用途 | |
| JP2022530403A (ja) | エクソンスキッピング戦略による網膜ジストロフィーの処置方法 | |
| JP2018526031A (ja) | NRARP遺伝子の発現を阻害するためのsiRNA、並びにそのための方法及び組成物におけるそれらの使用 | |
| Su et al. | Single-cell transcriptome atlas of spontaneous dry age-related macular degeneration in macaques | |
| Wang et al. | Modeling Cone/Cone–Rod Dystrophy Pathology by AAV-Mediated Overexpression of Mutant CRX Protein in the Mouse Retina | |
| KR20220048954A (ko) | Acta2 억제제를 유효성분으로 포함하는 망막 또는 맥락막 질환 치료용 조성물 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20180806 |
|
| RD03 | Notification of appointment of power of attorney |
Free format text: JAPANESE INTERMEDIATE CODE: A7423 Effective date: 20190531 |
|
| RD04 | Notification of resignation of power of attorney |
Free format text: JAPANESE INTERMEDIATE CODE: A7424 Effective date: 20190603 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20191213 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20191213 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20200819 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A821 Effective date: 20200819 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20201105 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20210205 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20210430 |
|
| A02 | Decision of refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A02 Effective date: 20210830 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20220104 |
|
| C60 | Trial request (containing other claim documents, opposition documents) |
Free format text: JAPANESE INTERMEDIATE CODE: C60 Effective date: 20220104 |
|
| A911 | Transfer to examiner for re-examination before appeal (zenchi) |
Free format text: JAPANESE INTERMEDIATE CODE: A911 Effective date: 20220113 |
|
| C21 | Notice of transfer of a case for reconsideration by examiners before appeal proceedings |
Free format text: JAPANESE INTERMEDIATE CODE: C21 Effective date: 20220114 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20220215 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20220303 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 7036723 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |