JP7030302B2 - ボロン酸またはボロン酸エステル、もしくはそれらを用いて多環芳香族化合物または多環芳香族多量体化合物を製造する方法 - Google Patents
ボロン酸またはボロン酸エステル、もしくはそれらを用いて多環芳香族化合物または多環芳香族多量体化合物を製造する方法 Download PDFInfo
- Publication number
- JP7030302B2 JP7030302B2 JP2017111692A JP2017111692A JP7030302B2 JP 7030302 B2 JP7030302 B2 JP 7030302B2 JP 2017111692 A JP2017111692 A JP 2017111692A JP 2017111692 A JP2017111692 A JP 2017111692A JP 7030302 B2 JP7030302 B2 JP 7030302B2
- Authority
- JP
- Japan
- Prior art keywords
- ring
- carbon atoms
- bonded
- aryl
- compound
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
- 150000001875 compounds Chemical class 0.000 title claims description 240
- -1 boronic acid ester Chemical class 0.000 title claims description 139
- ZADPBFCGQRWHPN-UHFFFAOYSA-N boronic acid Chemical compound OBO ZADPBFCGQRWHPN-UHFFFAOYSA-N 0.000 title claims description 37
- 238000004519 manufacturing process Methods 0.000 title claims description 16
- 125000004432 carbon atom Chemical group C* 0.000 claims description 167
- 125000003118 aryl group Chemical group 0.000 claims description 149
- 125000001072 heteroaryl group Chemical group 0.000 claims description 115
- 125000000217 alkyl group Chemical group 0.000 claims description 99
- 229910052739 hydrogen Inorganic materials 0.000 claims description 84
- 239000001257 hydrogen Substances 0.000 claims description 84
- UFHFLCQGNIYNRP-UHFFFAOYSA-N Hydrogen Chemical compound [H][H] UFHFLCQGNIYNRP-UHFFFAOYSA-N 0.000 claims description 78
- 229910052736 halogen Chemical group 0.000 claims description 72
- 150000002367 halogens Chemical group 0.000 claims description 70
- 229910052799 carbon Inorganic materials 0.000 claims description 55
- OKTJSMMVPCPJKN-UHFFFAOYSA-N Carbon Chemical compound [C] OKTJSMMVPCPJKN-UHFFFAOYSA-N 0.000 claims description 50
- 239000000463 material Substances 0.000 claims description 38
- 125000003545 alkoxy group Chemical group 0.000 claims description 31
- 238000000034 method Methods 0.000 claims description 23
- 125000004986 diarylamino group Chemical group 0.000 claims description 21
- 125000005240 diheteroarylamino group Chemical group 0.000 claims description 18
- 125000004104 aryloxy group Chemical group 0.000 claims description 17
- YZCKVEUIGOORGS-OUBTZVSYSA-N Deuterium Chemical group [2H] YZCKVEUIGOORGS-OUBTZVSYSA-N 0.000 claims description 16
- 229910052805 deuterium Inorganic materials 0.000 claims description 15
- IVDFJHOHABJVEH-UHFFFAOYSA-N pinacol Chemical compound CC(C)(O)C(C)(C)O IVDFJHOHABJVEH-UHFFFAOYSA-N 0.000 claims description 14
- ZOXJGFHDIHLPTG-UHFFFAOYSA-N Boron Chemical compound [B] ZOXJGFHDIHLPTG-UHFFFAOYSA-N 0.000 claims description 13
- 229910052796 boron Inorganic materials 0.000 claims description 13
- 239000000539 dimer Substances 0.000 claims description 12
- 125000002496 methyl group Chemical group [H]C([H])([H])* 0.000 claims description 12
- 125000000999 tert-butyl group Chemical group [H]C([H])([H])C(*)(C([H])([H])[H])C([H])([H])[H] 0.000 claims description 12
- 125000000843 phenylene group Chemical group C1(=C(C=CC=C1)*)* 0.000 claims description 11
- 125000002947 alkylene group Chemical group 0.000 claims description 10
- 125000004957 naphthylene group Chemical group 0.000 claims description 10
- 239000013638 trimer Substances 0.000 claims description 10
- 239000002253 acid Substances 0.000 claims description 8
- 125000005842 heteroatom Chemical group 0.000 claims description 8
- 125000004435 hydrogen atom Chemical group [H]* 0.000 claims description 7
- 150000001491 aromatic compounds Chemical class 0.000 claims description 4
- 125000005843 halogen group Chemical group 0.000 claims description 3
- 150000001721 carbon Chemical group 0.000 claims 9
- YXFVVABEGXRONW-UHFFFAOYSA-N Toluene Chemical compound CC1=CC=CC=C1 YXFVVABEGXRONW-UHFFFAOYSA-N 0.000 description 183
- 239000010410 layer Substances 0.000 description 82
- 238000006243 chemical reaction Methods 0.000 description 42
- 239000007787 solid Substances 0.000 description 33
- 239000002904 solvent Substances 0.000 description 31
- 125000001424 substituent group Chemical group 0.000 description 29
- IMNFDUFMRHMDMM-UHFFFAOYSA-N N-Heptane Chemical compound CCCCCCC IMNFDUFMRHMDMM-UHFFFAOYSA-N 0.000 description 28
- 239000003480 eluent Substances 0.000 description 28
- 239000000243 solution Substances 0.000 description 26
- 239000000203 mixture Substances 0.000 description 25
- 239000012299 nitrogen atmosphere Substances 0.000 description 25
- 239000012044 organic layer Substances 0.000 description 25
- 230000015572 biosynthetic process Effects 0.000 description 23
- 238000003786 synthesis reaction Methods 0.000 description 23
- WYURNTSHIVDZCO-UHFFFAOYSA-N Tetrahydrofuran Chemical compound C1CCOC1 WYURNTSHIVDZCO-UHFFFAOYSA-N 0.000 description 22
- MZRVEZGGRBJDDB-UHFFFAOYSA-N N-Butyllithium Chemical compound [Li]CCCC MZRVEZGGRBJDDB-UHFFFAOYSA-N 0.000 description 20
- 125000001997 phenyl group Chemical group [H]C1=C([H])C([H])=C(*)C([H])=C1[H] 0.000 description 19
- OKKJLVBELUTLKV-UHFFFAOYSA-N Methanol Chemical compound OC OKKJLVBELUTLKV-UHFFFAOYSA-N 0.000 description 18
- VSCWAEJMTAWNJL-UHFFFAOYSA-K aluminium trichloride Chemical compound Cl[Al](Cl)Cl VSCWAEJMTAWNJL-UHFFFAOYSA-K 0.000 description 18
- VLKZOEOYAKHREP-UHFFFAOYSA-N n-Hexane Chemical compound CCCCCC VLKZOEOYAKHREP-UHFFFAOYSA-N 0.000 description 17
- VYPSYNLAJGMNEJ-UHFFFAOYSA-N Silicium dioxide Chemical compound O=[Si]=O VYPSYNLAJGMNEJ-UHFFFAOYSA-N 0.000 description 16
- 239000000741 silica gel Substances 0.000 description 16
- 229910002027 silica gel Inorganic materials 0.000 description 16
- 239000010409 thin film Substances 0.000 description 16
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 16
- 238000002347 injection Methods 0.000 description 15
- 239000007924 injection Substances 0.000 description 15
- 238000005160 1H NMR spectroscopy Methods 0.000 description 12
- XEKOWRVHYACXOJ-UHFFFAOYSA-N Ethyl acetate Chemical compound CCOC(C)=O XEKOWRVHYACXOJ-UHFFFAOYSA-N 0.000 description 12
- SECXISVLQFMRJM-UHFFFAOYSA-N N-Methylpyrrolidone Chemical compound CN1CCCC1=O SECXISVLQFMRJM-UHFFFAOYSA-N 0.000 description 12
- 238000005481 NMR spectroscopy Methods 0.000 description 12
- ILAHWRKJUDSMFH-UHFFFAOYSA-N boron tribromide Chemical compound BrB(Br)Br ILAHWRKJUDSMFH-UHFFFAOYSA-N 0.000 description 12
- 230000005525 hole transport Effects 0.000 description 12
- BWHMMNNQKKPAPP-UHFFFAOYSA-L potassium carbonate Chemical compound [K+].[K+].[O-]C([O-])=O BWHMMNNQKKPAPP-UHFFFAOYSA-L 0.000 description 12
- 239000011541 reaction mixture Substances 0.000 description 11
- 239000004065 semiconductor Substances 0.000 description 11
- 239000000758 substrate Substances 0.000 description 11
- YLQBMQCUIZJEEH-UHFFFAOYSA-N Furan Chemical group C=1C=COC=1 YLQBMQCUIZJEEH-UHFFFAOYSA-N 0.000 description 10
- JGFZNNIVVJXRND-UHFFFAOYSA-N N,N-Diisopropylethylamine (DIPEA) Chemical compound CCN(C(C)C)C(C)C JGFZNNIVVJXRND-UHFFFAOYSA-N 0.000 description 10
- 150000001642 boronic acid derivatives Chemical class 0.000 description 10
- KWGKDLIKAYFUFQ-UHFFFAOYSA-M lithium chloride Chemical compound [Li+].[Cl-] KWGKDLIKAYFUFQ-UHFFFAOYSA-M 0.000 description 10
- IUYHWZFSGMZEOG-UHFFFAOYSA-M magnesium;propane;chloride Chemical compound [Mg+2].[Cl-].C[CH-]C IUYHWZFSGMZEOG-UHFFFAOYSA-M 0.000 description 10
- 239000012046 mixed solvent Substances 0.000 description 10
- MRWWWZLJWNIEEJ-UHFFFAOYSA-N 4,4,5,5-tetramethyl-2-propan-2-yloxy-1,3,2-dioxaborolane Chemical compound CC(C)OB1OC(C)(C)C(C)(C)O1 MRWWWZLJWNIEEJ-UHFFFAOYSA-N 0.000 description 9
- 0 CC1(C)c2cc(N(c3ccccc3)c3ccccc3)ccc2-c2cc(Oc3cccc(N(c4ccccc4)c4ccccc4)c3*)ccc12 Chemical compound CC1(C)c2cc(N(c3ccccc3)c3ccccc3)ccc2-c2cc(Oc3cccc(N(c4ccccc4)c4ccccc4)c3*)ccc12 0.000 description 9
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 9
- 239000007788 liquid Substances 0.000 description 9
- 239000000047 product Substances 0.000 description 9
- 238000010898 silica gel chromatography Methods 0.000 description 9
- HEDRZPFGACZZDS-UHFFFAOYSA-N Chloroform Chemical compound ClC(Cl)Cl HEDRZPFGACZZDS-UHFFFAOYSA-N 0.000 description 8
- MVPPADPHJFYWMZ-UHFFFAOYSA-N chlorobenzene Chemical compound ClC1=CC=CC=C1 MVPPADPHJFYWMZ-UHFFFAOYSA-N 0.000 description 8
- 125000005647 linker group Chemical group 0.000 description 8
- UHOVQNZJYSORNB-UHFFFAOYSA-N monobenzene Natural products C1=CC=CC=C1 UHOVQNZJYSORNB-UHFFFAOYSA-N 0.000 description 8
- WHXSMMKQMYFTQS-UHFFFAOYSA-N Lithium Chemical compound [Li] WHXSMMKQMYFTQS-UHFFFAOYSA-N 0.000 description 7
- KDLHZDBZIXYQEI-UHFFFAOYSA-N Palladium Chemical compound [Pd] KDLHZDBZIXYQEI-UHFFFAOYSA-N 0.000 description 7
- 239000003153 chemical reaction reagent Substances 0.000 description 7
- 230000005669 field effect Effects 0.000 description 7
- 229910052744 lithium Inorganic materials 0.000 description 7
- WGOPGODQLGJZGL-UHFFFAOYSA-N lithium;butane Chemical compound [Li+].CC[CH-]C WGOPGODQLGJZGL-UHFFFAOYSA-N 0.000 description 7
- 239000002841 Lewis acid Substances 0.000 description 6
- CTQNGGLPUBDAKN-UHFFFAOYSA-N O-Xylene Chemical compound CC1=CC=CC=C1C CTQNGGLPUBDAKN-UHFFFAOYSA-N 0.000 description 6
- 238000001816 cooling Methods 0.000 description 6
- 150000007517 lewis acids Chemical class 0.000 description 6
- 229910000027 potassium carbonate Inorganic materials 0.000 description 6
- 239000002243 precursor Substances 0.000 description 6
- 238000000746 purification Methods 0.000 description 6
- 238000010992 reflux Methods 0.000 description 6
- 239000008096 xylene Substances 0.000 description 6
- VEXZGXHMUGYJMC-UHFFFAOYSA-N Hydrochloric acid Chemical compound Cl VEXZGXHMUGYJMC-UHFFFAOYSA-N 0.000 description 5
- 125000000609 carbazolyl group Chemical group C1(=CC=CC=2C3=CC=CC=C3NC12)* 0.000 description 5
- 239000012043 crude product Substances 0.000 description 5
- 238000005886 esterification reaction Methods 0.000 description 5
- 230000005281 excited state Effects 0.000 description 5
- 239000010408 film Substances 0.000 description 5
- UBJFKNSINUCEAL-UHFFFAOYSA-N lithium;2-methylpropane Chemical compound [Li+].C[C-](C)C UBJFKNSINUCEAL-UHFFFAOYSA-N 0.000 description 5
- 238000004768 lowest unoccupied molecular orbital Methods 0.000 description 5
- 239000002244 precipitate Substances 0.000 description 5
- 238000007740 vapor deposition Methods 0.000 description 5
- RFFLAFLAYFXFSW-UHFFFAOYSA-N 1,2-dichlorobenzene Chemical compound ClC1=CC=CC=C1Cl RFFLAFLAYFXFSW-UHFFFAOYSA-N 0.000 description 4
- IJGRMHOSHXDMSA-UHFFFAOYSA-N Atomic nitrogen Chemical compound N#N IJGRMHOSHXDMSA-UHFFFAOYSA-N 0.000 description 4
- KWYHDKDOAIKMQN-UHFFFAOYSA-N N,N,N',N'-tetramethylethylenediamine Chemical compound CN(C)CCN(C)C KWYHDKDOAIKMQN-UHFFFAOYSA-N 0.000 description 4
- JUJWROOIHBZHMG-UHFFFAOYSA-N Pyridine Chemical compound C1=CC=NC=C1 JUJWROOIHBZHMG-UHFFFAOYSA-N 0.000 description 4
- 125000005620 boronic acid group Chemical class 0.000 description 4
- 150000002148 esters Chemical group 0.000 description 4
- 230000005284 excitation Effects 0.000 description 4
- 239000005457 ice water Substances 0.000 description 4
- 239000012212 insulator Substances 0.000 description 4
- 125000001624 naphthyl group Chemical group 0.000 description 4
- 239000011368 organic material Substances 0.000 description 4
- 239000002994 raw material Substances 0.000 description 4
- 230000009257 reactivity Effects 0.000 description 4
- MFRIHAYPQRLWNB-UHFFFAOYSA-N sodium tert-butoxide Chemical compound [Na+].CC(C)(C)[O-] MFRIHAYPQRLWNB-UHFFFAOYSA-N 0.000 description 4
- 238000003756 stirring Methods 0.000 description 4
- JOXIMZWYDAKGHI-UHFFFAOYSA-N toluene-4-sulfonic acid Chemical compound CC1=CC=C(S(O)(=O)=O)C=C1 JOXIMZWYDAKGHI-UHFFFAOYSA-N 0.000 description 4
- OISVCGZHLKNMSJ-UHFFFAOYSA-N 2,6-dimethylpyridine Chemical compound CC1=CC=CC(C)=N1 OISVCGZHLKNMSJ-UHFFFAOYSA-N 0.000 description 3
- HRZTZLCMURHWFY-UHFFFAOYSA-N 2-bromo-1,3-difluorobenzene Chemical compound FC1=CC=CC(F)=C1Br HRZTZLCMURHWFY-UHFFFAOYSA-N 0.000 description 3
- UCFSYHMCKWNKAH-UHFFFAOYSA-N 4,4,5,5-tetramethyl-1,3,2-dioxaborolane Chemical compound CC1(C)OBOC1(C)C UCFSYHMCKWNKAH-UHFFFAOYSA-N 0.000 description 3
- 239000007848 Bronsted acid Substances 0.000 description 3
- YMWUJEATGCHHMB-UHFFFAOYSA-N Dichloromethane Chemical compound ClCCl YMWUJEATGCHHMB-UHFFFAOYSA-N 0.000 description 3
- VMHLLURERBWHNL-UHFFFAOYSA-M Sodium acetate Chemical compound [Na+].CC([O-])=O VMHLLURERBWHNL-UHFFFAOYSA-M 0.000 description 3
- ZMANZCXQSJIPKH-UHFFFAOYSA-N Triethylamine Chemical compound CCN(CC)CC ZMANZCXQSJIPKH-UHFFFAOYSA-N 0.000 description 3
- 230000003190 augmentative effect Effects 0.000 description 3
- 239000002585 base Substances 0.000 description 3
- 238000004440 column chromatography Methods 0.000 description 3
- 230000000052 comparative effect Effects 0.000 description 3
- 230000003111 delayed effect Effects 0.000 description 3
- 238000011161 development Methods 0.000 description 3
- 230000005684 electric field Effects 0.000 description 3
- 125000001495 ethyl group Chemical group [H]C([H])([H])C([H])([H])* 0.000 description 3
- 239000000706 filtrate Substances 0.000 description 3
- 238000010438 heat treatment Methods 0.000 description 3
- 125000001041 indolyl group Chemical group 0.000 description 3
- 125000001449 isopropyl group Chemical group [H]C([H])([H])C([H])(*)C([H])([H])[H] 0.000 description 3
- 238000005259 measurement Methods 0.000 description 3
- SKTCDJAMAYNROS-UHFFFAOYSA-N methoxycyclopentane Chemical compound COC1CCCC1 SKTCDJAMAYNROS-UHFFFAOYSA-N 0.000 description 3
- 229910052763 palladium Inorganic materials 0.000 description 3
- 125000001484 phenothiazinyl group Chemical group C1(=CC=CC=2SC3=CC=CC=C3NC12)* 0.000 description 3
- 125000001644 phenoxazinyl group Chemical group C1(=CC=CC=2OC3=CC=CC=C3NC12)* 0.000 description 3
- 125000003367 polycyclic group Chemical group 0.000 description 3
- 239000001632 sodium acetate Substances 0.000 description 3
- 235000017281 sodium acetate Nutrition 0.000 description 3
- 239000000126 substance Substances 0.000 description 3
- YJTKZCDBKVTVBY-UHFFFAOYSA-N 1,3-Diphenylbenzene Chemical group C1=CC=CC=C1C1=CC=CC(C=2C=CC=CC=2)=C1 YJTKZCDBKVTVBY-UHFFFAOYSA-N 0.000 description 2
- IANQTJSKSUMEQM-UHFFFAOYSA-N 1-benzofuran Chemical group C1=CC=C2OC=CC2=C1 IANQTJSKSUMEQM-UHFFFAOYSA-N 0.000 description 2
- FCEHBMOGCRZNNI-UHFFFAOYSA-N 1-benzothiophene Chemical group C1=CC=C2SC=CC2=C1 FCEHBMOGCRZNNI-UHFFFAOYSA-N 0.000 description 2
- BMIBJCFFZPYJHF-UHFFFAOYSA-N 2-methoxy-5-methyl-3-(4,4,5,5-tetramethyl-1,3,2-dioxaborolan-2-yl)pyridine Chemical compound COC1=NC=C(C)C=C1B1OC(C)(C)C(C)(C)O1 BMIBJCFFZPYJHF-UHFFFAOYSA-N 0.000 description 2
- PQQFODIEQBDFRE-UHFFFAOYSA-N 6-(3-bromo-2-chlorophenoxy)-9,9-dimethyl-N,N-diphenylfluoren-2-amine Chemical compound BrC=1C(=C(OC=2C=C3C=4C=CC(=CC=4C(C3=CC=2)(C)C)N(C2=CC=CC=C2)C2=CC=CC=C2)C=CC=1)Cl PQQFODIEQBDFRE-UHFFFAOYSA-N 0.000 description 2
- UJOBWOGCFQCDNV-UHFFFAOYSA-N 9H-carbazole Chemical group C1=CC=C2C3=CC=CC=C3NC2=C1 UJOBWOGCFQCDNV-UHFFFAOYSA-N 0.000 description 2
- CSCPPACGZOOCGX-UHFFFAOYSA-N Acetone Chemical compound CC(C)=O CSCPPACGZOOCGX-UHFFFAOYSA-N 0.000 description 2
- NLXLAEXVIDQMFP-UHFFFAOYSA-N Ammonia chloride Chemical compound [NH4+].[Cl-] NLXLAEXVIDQMFP-UHFFFAOYSA-N 0.000 description 2
- CPELXLSAUQHCOX-UHFFFAOYSA-M Bromide Chemical compound [Br-] CPELXLSAUQHCOX-UHFFFAOYSA-M 0.000 description 2
- WKBOTKDWSSQWDR-UHFFFAOYSA-N Bromine atom Chemical compound [Br] WKBOTKDWSSQWDR-UHFFFAOYSA-N 0.000 description 2
- BCOVNNCVNRBOLX-UHFFFAOYSA-N C1(=CC=CC=C1)N(C1=CC=C(C=C1)C=1C(=CC=C(C=1)OC)C(=O)OC)C1=CC=CC=C1 Chemical compound C1(=CC=CC=C1)N(C1=CC=C(C=C1)C=1C(=CC=C(C=1)OC)C(=O)OC)C1=CC=CC=C1 BCOVNNCVNRBOLX-UHFFFAOYSA-N 0.000 description 2
- VEXZGXHMUGYJMC-UHFFFAOYSA-M Chloride anion Chemical compound [Cl-] VEXZGXHMUGYJMC-UHFFFAOYSA-M 0.000 description 2
- ZAMOUSCENKQFHK-UHFFFAOYSA-N Chlorine atom Chemical compound [Cl] ZAMOUSCENKQFHK-UHFFFAOYSA-N 0.000 description 2
- 229940126062 Compound A Drugs 0.000 description 2
- XDTMQSROBMDMFD-UHFFFAOYSA-N Cyclohexane Chemical compound C1CCCCC1 XDTMQSROBMDMFD-UHFFFAOYSA-N 0.000 description 2
- PXGOKWXKJXAPGV-UHFFFAOYSA-N Fluorine Chemical compound FF PXGOKWXKJXAPGV-UHFFFAOYSA-N 0.000 description 2
- NLDMNSXOCDLTTB-UHFFFAOYSA-N Heterophylliin A Natural products O1C2COC(=O)C3=CC(O)=C(O)C(O)=C3C3=C(O)C(O)=C(O)C=C3C(=O)OC2C(OC(=O)C=2C=C(O)C(O)=C(O)C=2)C(O)C1OC(=O)C1=CC(O)=C(O)C(O)=C1 NLDMNSXOCDLTTB-UHFFFAOYSA-N 0.000 description 2
- CPELXLSAUQHCOX-UHFFFAOYSA-N Hydrogen bromide Chemical compound Br CPELXLSAUQHCOX-UHFFFAOYSA-N 0.000 description 2
- AFVFQIVMOAPDHO-UHFFFAOYSA-N Methanesulfonic acid Chemical compound CS(O)(=O)=O AFVFQIVMOAPDHO-UHFFFAOYSA-N 0.000 description 2
- JLTDJTHDQAWBAV-UHFFFAOYSA-N N,N-dimethylaniline Chemical compound CN(C)C1=CC=CC=C1 JLTDJTHDQAWBAV-UHFFFAOYSA-N 0.000 description 2
- ZLMJMSJWJFRBEC-UHFFFAOYSA-N Potassium Chemical compound [K] ZLMJMSJWJFRBEC-UHFFFAOYSA-N 0.000 description 2
- NINIDFKCEFEMDL-UHFFFAOYSA-N Sulfur Chemical compound [S] NINIDFKCEFEMDL-UHFFFAOYSA-N 0.000 description 2
- DTQVDTLACAAQTR-UHFFFAOYSA-N Trifluoroacetic acid Chemical compound OC(=O)C(F)(F)F DTQVDTLACAAQTR-UHFFFAOYSA-N 0.000 description 2
- 125000000641 acridinyl group Chemical group C1(=CC=CC2=NC3=CC=CC=C3C=C12)* 0.000 description 2
- 150000001412 amines Chemical class 0.000 description 2
- RDOXTESZEPMUJZ-UHFFFAOYSA-N anisole Chemical compound COC1=CC=CC=C1 RDOXTESZEPMUJZ-UHFFFAOYSA-N 0.000 description 2
- MWPLVEDNUUSJAV-UHFFFAOYSA-N anthracene Chemical compound C1=CC=CC2=CC3=CC=CC=C3C=C21 MWPLVEDNUUSJAV-UHFFFAOYSA-N 0.000 description 2
- QVGXLLKOCUKJST-UHFFFAOYSA-N atomic oxygen Chemical compound [O] QVGXLLKOCUKJST-UHFFFAOYSA-N 0.000 description 2
- WPYMKLBDIGXBTP-UHFFFAOYSA-N benzoic acid Chemical compound OC(=O)C1=CC=CC=C1 WPYMKLBDIGXBTP-UHFFFAOYSA-N 0.000 description 2
- 125000002619 bicyclic group Chemical group 0.000 description 2
- 230000033228 biological regulation Effects 0.000 description 2
- 238000009835 boiling Methods 0.000 description 2
- 239000003054 catalyst Substances 0.000 description 2
- 230000008859 change Effects 0.000 description 2
- 239000000460 chlorine Substances 0.000 description 2
- 229910052801 chlorine Inorganic materials 0.000 description 2
- 239000013078 crystal Substances 0.000 description 2
- NNBZCPXTIHJBJL-UHFFFAOYSA-N decalin Chemical compound C1CCCC2CCCCC21 NNBZCPXTIHJBJL-UHFFFAOYSA-N 0.000 description 2
- 238000000354 decomposition reaction Methods 0.000 description 2
- TXCDCPKCNAJMEE-UHFFFAOYSA-N dibenzofuran Chemical group C1=CC=C2C3=CC=CC=C3OC2=C1 TXCDCPKCNAJMEE-UHFFFAOYSA-N 0.000 description 2
- IYYZUPMFVPLQIF-ALWQSETLSA-N dibenzothiophene Chemical group C1=CC=CC=2[34S]C3=C(C=21)C=CC=C3 IYYZUPMFVPLQIF-ALWQSETLSA-N 0.000 description 2
- ZUOUZKKEUPVFJK-UHFFFAOYSA-N diphenyl Chemical group C1=CC=CC=C1C1=CC=CC=C1 ZUOUZKKEUPVFJK-UHFFFAOYSA-N 0.000 description 2
- USIUVYZYUHIAEV-UHFFFAOYSA-N diphenyl ether Chemical compound C=1C=CC=CC=1OC1=CC=CC=C1 USIUVYZYUHIAEV-UHFFFAOYSA-N 0.000 description 2
- DMBHHRLKUKUOEG-UHFFFAOYSA-N diphenylamine Chemical compound C=1C=CC=CC=1NC1=CC=CC=C1 DMBHHRLKUKUOEG-UHFFFAOYSA-N 0.000 description 2
- 238000005401 electroluminescence Methods 0.000 description 2
- 230000032050 esterification Effects 0.000 description 2
- 229910052731 fluorine Inorganic materials 0.000 description 2
- 239000011737 fluorine Substances 0.000 description 2
- 150000002431 hydrogen Chemical class 0.000 description 2
- 230000003301 hydrolyzing effect Effects 0.000 description 2
- KLRHPHDUDFIRKB-UHFFFAOYSA-M indium(i) bromide Chemical compound [Br-].[In+] KLRHPHDUDFIRKB-UHFFFAOYSA-M 0.000 description 2
- 230000003993 interaction Effects 0.000 description 2
- ZCSHNCUQKCANBX-UHFFFAOYSA-N lithium diisopropylamide Chemical compound [Li+].CC(C)[N-]C(C)C ZCSHNCUQKCANBX-UHFFFAOYSA-N 0.000 description 2
- 230000004807 localization Effects 0.000 description 2
- 229910052751 metal Inorganic materials 0.000 description 2
- 239000002184 metal Substances 0.000 description 2
- 238000006263 metalation reaction Methods 0.000 description 2
- ZICRWXFGZCVTBZ-UHFFFAOYSA-N methyl 2-hydroxy-4-methoxybenzoate Chemical compound COC(=O)C1=CC=C(OC)C=C1O ZICRWXFGZCVTBZ-UHFFFAOYSA-N 0.000 description 2
- GYVGXEWAOAAJEU-UHFFFAOYSA-N n,n,4-trimethylaniline Chemical compound CN(C)C1=CC=C(C)C=C1 GYVGXEWAOAAJEU-UHFFFAOYSA-N 0.000 description 2
- 229910052757 nitrogen Inorganic materials 0.000 description 2
- 150000002894 organic compounds Chemical class 0.000 description 2
- 238000007122 ortho-metalation reaction Methods 0.000 description 2
- 125000002971 oxazolyl group Chemical group 0.000 description 2
- 229910052760 oxygen Inorganic materials 0.000 description 2
- 239000001301 oxygen Substances 0.000 description 2
- PIBWKRNGBLPSSY-UHFFFAOYSA-L palladium(II) chloride Chemical compound Cl[Pd]Cl PIBWKRNGBLPSSY-UHFFFAOYSA-L 0.000 description 2
- ANRQGKOBLBYXFM-UHFFFAOYSA-M phenylmagnesium bromide Chemical compound Br[Mg]C1=CC=CC=C1 ANRQGKOBLBYXFM-UHFFFAOYSA-M 0.000 description 2
- 229910052698 phosphorus Inorganic materials 0.000 description 2
- 239000011591 potassium Substances 0.000 description 2
- 229910052700 potassium Inorganic materials 0.000 description 2
- 230000008569 process Effects 0.000 description 2
- LVTJOONKWUXEFR-FZRMHRINSA-N protoneodioscin Natural products O(C[C@@H](CC[C@]1(O)[C@H](C)[C@@H]2[C@]3(C)[C@H]([C@H]4[C@@H]([C@]5(C)C(=CC4)C[C@@H](O[C@@H]4[C@H](O[C@H]6[C@@H](O)[C@@H](O)[C@@H](O)[C@H](C)O6)[C@@H](O)[C@H](O[C@H]6[C@@H](O)[C@@H](O)[C@@H](O)[C@H](C)O6)[C@H](CO)O4)CC5)CC3)C[C@@H]2O1)C)[C@H]1[C@H](O)[C@H](O)[C@H](O)[C@@H](CO)O1 LVTJOONKWUXEFR-FZRMHRINSA-N 0.000 description 2
- AOJFQRQNPXYVLM-UHFFFAOYSA-N pyridin-1-ium;chloride Chemical compound [Cl-].C1=CC=[NH+]C=C1 AOJFQRQNPXYVLM-UHFFFAOYSA-N 0.000 description 2
- UMJSCPRVCHMLSP-UHFFFAOYSA-N pyridine Natural products COC1=CC=CN=C1 UMJSCPRVCHMLSP-UHFFFAOYSA-N 0.000 description 2
- 125000000168 pyrrolyl group Chemical group 0.000 description 2
- 239000000376 reactant Substances 0.000 description 2
- 238000007363 ring formation reaction Methods 0.000 description 2
- 238000013341 scale-up Methods 0.000 description 2
- 125000003107 substituted aryl group Chemical group 0.000 description 2
- 238000000967 suction filtration Methods 0.000 description 2
- 229910052717 sulfur Inorganic materials 0.000 description 2
- 239000011593 sulfur Substances 0.000 description 2
- IMNIMPAHZVJRPE-UHFFFAOYSA-N triethylenediamine Chemical compound C1CN2CCN1CC2 IMNIMPAHZVJRPE-UHFFFAOYSA-N 0.000 description 2
- WJKHJLXJJJATHN-UHFFFAOYSA-N triflic anhydride Chemical compound FC(F)(F)S(=O)(=O)OS(=O)(=O)C(F)(F)F WJKHJLXJJJATHN-UHFFFAOYSA-N 0.000 description 2
- WRECIMRULFAWHA-UHFFFAOYSA-N trimethyl borate Chemical compound COB(OC)OC WRECIMRULFAWHA-UHFFFAOYSA-N 0.000 description 2
- ODHXBMXNKOYIBV-UHFFFAOYSA-N triphenylamine Chemical compound C1=CC=CC=C1N(C=1C=CC=CC=1)C1=CC=CC=C1 ODHXBMXNKOYIBV-UHFFFAOYSA-N 0.000 description 2
- GETTZEONDQJALK-UHFFFAOYSA-N (trifluoromethyl)benzene Chemical compound FC(F)(F)C1=CC=CC=C1 GETTZEONDQJALK-UHFFFAOYSA-N 0.000 description 1
- JYEUMXHLPRZUAT-UHFFFAOYSA-N 1,2,3-triazine Chemical group C1=CN=NN=C1 JYEUMXHLPRZUAT-UHFFFAOYSA-N 0.000 description 1
- WSLDOOZREJYCGB-UHFFFAOYSA-N 1,2-Dichloroethane Chemical group ClCCCl WSLDOOZREJYCGB-UHFFFAOYSA-N 0.000 description 1
- 125000000355 1,3-benzoxazolyl group Chemical group O1C(=NC2=C1C=CC=C2)* 0.000 description 1
- RYHBNJHYFVUHQT-UHFFFAOYSA-N 1,4-Dioxane Chemical compound C1COCCO1 RYHBNJHYFVUHQT-UHFFFAOYSA-N 0.000 description 1
- XJKSTNDFUHDPQJ-UHFFFAOYSA-N 1,4-diphenylbenzene Chemical group C1=CC=CC=C1C1=CC=C(C=2C=CC=CC=2)C=C1 XJKSTNDFUHDPQJ-UHFFFAOYSA-N 0.000 description 1
- GTIWFNAUYPVPAT-UHFFFAOYSA-N 1-bromo-2-chloro-3-fluorobenzene Chemical compound FC1=CC=CC(Br)=C1Cl GTIWFNAUYPVPAT-UHFFFAOYSA-N 0.000 description 1
- HYZJCKYKOHLVJF-UHFFFAOYSA-N 1H-benzimidazole Chemical group C1=CC=C2NC=NC2=C1 HYZJCKYKOHLVJF-UHFFFAOYSA-N 0.000 description 1
- BAXOFTOLAUCFNW-UHFFFAOYSA-N 1H-indazole Chemical group C1=CC=C2C=NNC2=C1 BAXOFTOLAUCFNW-UHFFFAOYSA-N 0.000 description 1
- KFDNQUWMBLVQNB-UHFFFAOYSA-N 2-[2-[bis(carboxymethyl)amino]ethyl-(carboxymethyl)amino]acetic acid;sodium Chemical compound [Na].[Na].[Na].[Na].OC(=O)CN(CC(O)=O)CCN(CC(O)=O)CC(O)=O KFDNQUWMBLVQNB-UHFFFAOYSA-N 0.000 description 1
- UXGVMFHEKMGWMA-UHFFFAOYSA-N 2-benzofuran Chemical group C1=CC=CC2=COC=C21 UXGVMFHEKMGWMA-UHFFFAOYSA-N 0.000 description 1
- 125000006176 2-ethylbutyl group Chemical group [H]C([H])([H])C([H])([H])C([H])(C([H])([H])*)C([H])([H])C([H])([H])[H] 0.000 description 1
- XWKFPIODWVPXLX-UHFFFAOYSA-N 2-methyl-5-methylpyridine Natural products CC1=CC=C(C)N=C1 XWKFPIODWVPXLX-UHFFFAOYSA-N 0.000 description 1
- HORNXRXVQWOLPJ-UHFFFAOYSA-N 3-chlorophenol Chemical compound OC1=CC=CC(Cl)=C1 HORNXRXVQWOLPJ-UHFFFAOYSA-N 0.000 description 1
- OGGKVJMNFFSDEV-UHFFFAOYSA-N 3-methyl-n-[4-[4-(n-(3-methylphenyl)anilino)phenyl]phenyl]-n-phenylaniline Chemical compound CC1=CC=CC(N(C=2C=CC=CC=2)C=2C=CC(=CC=2)C=2C=CC(=CC=2)N(C=2C=CC=CC=2)C=2C=C(C)C=CC=2)=C1 OGGKVJMNFFSDEV-UHFFFAOYSA-N 0.000 description 1
- 125000004920 4-methyl-2-pentyl group Chemical group CC(CC(C)*)C 0.000 description 1
- ZCYVEMRRCGMTRW-UHFFFAOYSA-N 7553-56-2 Chemical compound [I] ZCYVEMRRCGMTRW-UHFFFAOYSA-N 0.000 description 1
- KDCGOANMDULRCW-UHFFFAOYSA-N 7H-purine Chemical group N1=CNC2=NC=NC2=C1 KDCGOANMDULRCW-UHFFFAOYSA-N 0.000 description 1
- LLAXDWLRVWTADE-UHFFFAOYSA-N 9,9-dimethyl-n,n-diphenylfluoren-2-amine Chemical compound C1=C2C(C)(C)C3=CC=CC=C3C2=CC=C1N(C=1C=CC=CC=1)C1=CC=CC=C1 LLAXDWLRVWTADE-UHFFFAOYSA-N 0.000 description 1
- 229910016569 AlF 3 Inorganic materials 0.000 description 1
- 238000006443 Buchwald-Hartwig cross coupling reaction Methods 0.000 description 1
- VWLZTPGDSWOVBY-UHFFFAOYSA-N C1(=CC=CC=C1)N(C=1C=CC=C(C=1)C1=C(C=CC(=C1)OC)C(C)(C)O)C1=CC=CC=C1 Chemical compound C1(=CC=CC=C1)N(C=1C=CC=C(C=1)C1=C(C=CC(=C1)OC)C(C)(C)O)C1=CC=CC=C1 VWLZTPGDSWOVBY-UHFFFAOYSA-N 0.000 description 1
- PSXLCTPHDAEPLK-UHFFFAOYSA-N CC(C)[Mg] Chemical compound CC(C)[Mg] PSXLCTPHDAEPLK-UHFFFAOYSA-N 0.000 description 1
- PFTKFQKGNHJXQH-UHFFFAOYSA-N Cc(c(Oc1ccccc1)ccc1)c1Oc1ccccc1 Chemical compound Cc(c(Oc1ccccc1)ccc1)c1Oc1ccccc1 PFTKFQKGNHJXQH-UHFFFAOYSA-N 0.000 description 1
- 229910021591 Copper(I) chloride Inorganic materials 0.000 description 1
- KRHYYFGTRYWZRS-UHFFFAOYSA-N Fluorane Chemical compound F KRHYYFGTRYWZRS-UHFFFAOYSA-N 0.000 description 1
- 239000007818 Grignard reagent Substances 0.000 description 1
- 229910021617 Indium monochloride Inorganic materials 0.000 description 1
- BZLVMXJERCGZMT-UHFFFAOYSA-N Methyl tert-butyl ether Chemical compound COC(C)(C)C BZLVMXJERCGZMT-UHFFFAOYSA-N 0.000 description 1
- 229920000557 Nafion® Polymers 0.000 description 1
- 240000007594 Oryza sativa Species 0.000 description 1
- 235000007164 Oryza sativa Nutrition 0.000 description 1
- ISWSIDIOOBJBQZ-UHFFFAOYSA-N Phenol Chemical compound OC1=CC=CC=C1 ISWSIDIOOBJBQZ-UHFFFAOYSA-N 0.000 description 1
- OAICVXFJPJFONN-UHFFFAOYSA-N Phosphorus Chemical compound [P] OAICVXFJPJFONN-UHFFFAOYSA-N 0.000 description 1
- XUIMIQQOPSSXEZ-UHFFFAOYSA-N Silicon Chemical group [Si] XUIMIQQOPSSXEZ-UHFFFAOYSA-N 0.000 description 1
- PMZURENOXWZQFD-UHFFFAOYSA-L Sodium Sulfate Chemical compound [Na+].[Na+].[O-]S([O-])(=O)=O PMZURENOXWZQFD-UHFFFAOYSA-L 0.000 description 1
- FZWLAAWBMGSTSO-UHFFFAOYSA-N Thiazole Chemical group C1=CSC=N1 FZWLAAWBMGSTSO-UHFFFAOYSA-N 0.000 description 1
- YTPLMLYBLZKORZ-UHFFFAOYSA-N Thiophene Chemical group C=1C=CSC=1 YTPLMLYBLZKORZ-UHFFFAOYSA-N 0.000 description 1
- 238000006887 Ullmann reaction Methods 0.000 description 1
- 229910021536 Zeolite Inorganic materials 0.000 description 1
- 229910007926 ZrCl Inorganic materials 0.000 description 1
- TWWQCBRELPOMER-UHFFFAOYSA-N [4-(n-phenylanilino)phenyl]boronic acid Chemical compound C1=CC(B(O)O)=CC=C1N(C=1C=CC=CC=1)C1=CC=CC=C1 TWWQCBRELPOMER-UHFFFAOYSA-N 0.000 description 1
- MBHHMGSRTLPOFQ-UHFFFAOYSA-M [Li].CC1(C(N(CCC1)[Mg]Cl)(C)C)C Chemical compound [Li].CC1(C(N(CCC1)[Mg]Cl)(C)C)C MBHHMGSRTLPOFQ-UHFFFAOYSA-M 0.000 description 1
- 125000004054 acenaphthylenyl group Chemical group C1(=CC2=CC=CC3=CC=CC1=C23)* 0.000 description 1
- 150000007513 acids Chemical class 0.000 description 1
- 239000000654 additive Substances 0.000 description 1
- 230000000996 additive effect Effects 0.000 description 1
- 238000005576 amination reaction Methods 0.000 description 1
- 125000003277 amino group Chemical group 0.000 description 1
- 235000019270 ammonium chloride Nutrition 0.000 description 1
- 239000007864 aqueous solution Substances 0.000 description 1
- 125000004429 atom Chemical group 0.000 description 1
- IOJUPLGTWVMSFF-UHFFFAOYSA-N benzothiazole Chemical group C1=CC=C2SC=NC2=C1 IOJUPLGTWVMSFF-UHFFFAOYSA-N 0.000 description 1
- QRUDEWIWKLJBPS-UHFFFAOYSA-N benzotriazole Chemical group C1=CC=C2N[N][N]C2=C1 QRUDEWIWKLJBPS-UHFFFAOYSA-N 0.000 description 1
- 235000010290 biphenyl Nutrition 0.000 description 1
- 239000004305 biphenyl Substances 0.000 description 1
- MYIAPBDBTMDUDP-UHFFFAOYSA-N bis(trifluoromethylsulfonyl)methylsulfonyl-trifluoromethane Chemical compound FC(F)(F)S(=O)(=O)C(S(=O)(=O)C(F)(F)F)S(=O)(=O)C(F)(F)F MYIAPBDBTMDUDP-UHFFFAOYSA-N 0.000 description 1
- 150000001639 boron compounds Chemical class 0.000 description 1
- GDTBXPJZTBHREO-UHFFFAOYSA-N bromine Substances BrBr GDTBXPJZTBHREO-UHFFFAOYSA-N 0.000 description 1
- 229910052794 bromium Inorganic materials 0.000 description 1
- 239000006227 byproduct Substances 0.000 description 1
- 238000005266 casting Methods 0.000 description 1
- XOYLJNJLGBYDTH-UHFFFAOYSA-M chlorogallium Chemical compound [Ga]Cl XOYLJNJLGBYDTH-UHFFFAOYSA-M 0.000 description 1
- 125000000259 cinnolinyl group Chemical group N1=NC(=CC2=CC=CC=C12)* 0.000 description 1
- 238000000576 coating method Methods 0.000 description 1
- 239000003086 colorant Substances 0.000 description 1
- 229940125904 compound 1 Drugs 0.000 description 1
- 238000007796 conventional method Methods 0.000 description 1
- OXBLHERUFWYNTN-UHFFFAOYSA-M copper(I) chloride Chemical compound [Cu]Cl OXBLHERUFWYNTN-UHFFFAOYSA-M 0.000 description 1
- 238000005859 coupling reaction Methods 0.000 description 1
- ZOCHARZZJNPSEU-UHFFFAOYSA-N diboron Chemical compound B#B ZOCHARZZJNPSEU-UHFFFAOYSA-N 0.000 description 1
- HNPSIPDUKPIQMN-UHFFFAOYSA-N dioxosilane;oxo(oxoalumanyloxy)alumane Chemical compound O=[Si]=O.O=[Al]O[Al]=O HNPSIPDUKPIQMN-UHFFFAOYSA-N 0.000 description 1
- 238000010894 electron beam technology Methods 0.000 description 1
- 238000006266 etherification reaction Methods 0.000 description 1
- 238000002474 experimental method Methods 0.000 description 1
- 239000012467 final product Substances 0.000 description 1
- 125000003983 fluorenyl group Chemical group C1(=CC=CC=2C3=CC=CC=C3CC12)* 0.000 description 1
- UQSQSQZYBQSBJZ-UHFFFAOYSA-N fluorosulfonic acid Chemical compound OS(F)(=O)=O UQSQSQZYBQSBJZ-UHFFFAOYSA-N 0.000 description 1
- 239000011521 glass Substances 0.000 description 1
- 150000004795 grignard reagents Chemical class 0.000 description 1
- 238000009499 grossing Methods 0.000 description 1
- 125000005241 heteroarylamino group Chemical group 0.000 description 1
- 125000000623 heterocyclic group Chemical group 0.000 description 1
- 238000004770 highest occupied molecular orbital Methods 0.000 description 1
- 229910000042 hydrogen bromide Inorganic materials 0.000 description 1
- IXCSERBJSXMMFS-UHFFFAOYSA-N hydrogen chloride Substances Cl.Cl IXCSERBJSXMMFS-UHFFFAOYSA-N 0.000 description 1
- 229910000041 hydrogen chloride Inorganic materials 0.000 description 1
- 229910000040 hydrogen fluoride Inorganic materials 0.000 description 1
- 230000007062 hydrolysis Effects 0.000 description 1
- 238000006460 hydrolysis reaction Methods 0.000 description 1
- 125000002887 hydroxy group Chemical group [H]O* 0.000 description 1
- 125000002883 imidazolyl group Chemical group 0.000 description 1
- 150000003949 imides Chemical class 0.000 description 1
- 239000012535 impurity Substances 0.000 description 1
- APHGZSBLRQFRCA-UHFFFAOYSA-M indium(1+);chloride Chemical compound [In]Cl APHGZSBLRQFRCA-UHFFFAOYSA-M 0.000 description 1
- 238000003402 intramolecular cyclocondensation reaction Methods 0.000 description 1
- 239000011630 iodine Substances 0.000 description 1
- 229910052740 iodine Inorganic materials 0.000 description 1
- 125000000959 isobutyl group Chemical group [H]C([H])([H])C([H])(C([H])([H])[H])C([H])([H])* 0.000 description 1
- 125000000904 isoindolyl group Chemical group C=1(NC=C2C=CC=CC12)* 0.000 description 1
- 238000002955 isolation Methods 0.000 description 1
- 125000001972 isopentyl group Chemical group [H]C([H])([H])C([H])(C([H])([H])[H])C([H])([H])C([H])([H])* 0.000 description 1
- 125000002183 isoquinolinyl group Chemical group C1(=NC=CC2=CC=CC=C12)* 0.000 description 1
- CTAPFRYPJLPFDF-UHFFFAOYSA-N isoxazole Chemical group C=1C=NOC=1 CTAPFRYPJLPFDF-UHFFFAOYSA-N 0.000 description 1
- 238000003475 lamination Methods 0.000 description 1
- 150000002605 large molecules Chemical group 0.000 description 1
- 238000004895 liquid chromatography mass spectrometry Methods 0.000 description 1
- 239000004973 liquid crystal related substance Substances 0.000 description 1
- YNESATAKKCNGOF-UHFFFAOYSA-N lithium bis(trimethylsilyl)amide Chemical compound [Li+].C[Si](C)(C)[N-][Si](C)(C)C YNESATAKKCNGOF-UHFFFAOYSA-N 0.000 description 1
- ANYSGBYRTLOUPO-UHFFFAOYSA-N lithium tetramethylpiperidide Chemical compound [Li]N1C(C)(C)CCCC1(C)C ANYSGBYRTLOUPO-UHFFFAOYSA-N 0.000 description 1
- MCVFFRWZNYZUIJ-UHFFFAOYSA-M lithium;trifluoromethanesulfonate Chemical compound [Li+].[O-]S(=O)(=O)C(F)(F)F MCVFFRWZNYZUIJ-UHFFFAOYSA-M 0.000 description 1
- 239000011777 magnesium Substances 0.000 description 1
- IWCVDCOJSPWGRW-UHFFFAOYSA-M magnesium;benzene;chloride Chemical compound [Mg+2].[Cl-].C1=CC=[C-]C=C1 IWCVDCOJSPWGRW-UHFFFAOYSA-M 0.000 description 1
- NXPHGHWWQRMDIA-UHFFFAOYSA-M magnesium;carbanide;bromide Chemical compound [CH3-].[Mg+2].[Br-] NXPHGHWWQRMDIA-UHFFFAOYSA-M 0.000 description 1
- 239000011159 matrix material Substances 0.000 description 1
- 238000001465 metallisation Methods 0.000 description 1
- 229940098779 methanesulfonic acid Drugs 0.000 description 1
- UZKWTJUDCOPSNM-UHFFFAOYSA-N methoxybenzene Substances CCCCOC=C UZKWTJUDCOPSNM-UHFFFAOYSA-N 0.000 description 1
- DVSDBMFJEQPWNO-UHFFFAOYSA-N methyllithium Chemical compound C[Li] DVSDBMFJEQPWNO-UHFFFAOYSA-N 0.000 description 1
- 239000011259 mixed solution Substances 0.000 description 1
- 125000002950 monocyclic group Chemical group 0.000 description 1
- VGGNVBNNVSIGKG-UHFFFAOYSA-N n,n,2-trimethylaziridine-1-carboxamide Chemical compound CC1CN1C(=O)N(C)C VGGNVBNNVSIGKG-UHFFFAOYSA-N 0.000 description 1
- 125000004108 n-butyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 1
- 125000003136 n-heptyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 1
- 125000001280 n-hexyl group Chemical group C(CCCCC)* 0.000 description 1
- 125000000740 n-pentyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 1
- 125000004123 n-propyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])* 0.000 description 1
- 125000001971 neopentyl group Chemical group [H]C([*])([H])C(C([H])([H])[H])(C([H])([H])[H])C([H])([H])[H] 0.000 description 1
- YCWSUKQGVSGXJO-NTUHNPAUSA-N nifuroxazide Chemical group C1=CC(O)=CC=C1C(=O)N\N=C\C1=CC=C([N+]([O-])=O)O1 YCWSUKQGVSGXJO-NTUHNPAUSA-N 0.000 description 1
- 238000010534 nucleophilic substitution reaction Methods 0.000 description 1
- 125000005447 octyloxy group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])O* 0.000 description 1
- 150000002900 organolithium compounds Chemical class 0.000 description 1
- 230000010355 oscillation Effects 0.000 description 1
- 238000013021 overheating Methods 0.000 description 1
- 229930184652 p-Terphenyl Natural products 0.000 description 1
- 125000005582 pentacene group Chemical group 0.000 description 1
- 125000001147 pentyl group Chemical group C(CCCC)* 0.000 description 1
- 230000002093 peripheral effect Effects 0.000 description 1
- 125000002080 perylenyl group Chemical group C1(=CC=C2C=CC=C3C4=CC=CC5=CC=CC(C1=C23)=C45)* 0.000 description 1
- 125000001828 phenalenyl group Chemical group C1(C=CC2=CC=CC3=CC=CC1=C23)* 0.000 description 1
- YNPNZTXNASCQKK-UHFFFAOYSA-N phenanthrene Chemical group C1=CC=C2C3=CC=CC=C3C=CC2=C1 YNPNZTXNASCQKK-UHFFFAOYSA-N 0.000 description 1
- 125000001791 phenazinyl group Chemical group C1(=CC=CC2=NC3=CC=CC=C3N=C12)* 0.000 description 1
- 125000004437 phosphorous atom Chemical group 0.000 description 1
- 239000011574 phosphorus Substances 0.000 description 1
- LFSXCDWNBUNEEM-UHFFFAOYSA-N phthalazine Chemical group C1=NN=CC2=CC=CC=C21 LFSXCDWNBUNEEM-UHFFFAOYSA-N 0.000 description 1
- 230000000704 physical effect Effects 0.000 description 1
- 125000002924 primary amino group Chemical group [H]N([H])* 0.000 description 1
- CPNGPNLZQNNVQM-UHFFFAOYSA-N pteridine Chemical group N1=CN=CC2=NC=CN=C21 CPNGPNLZQNNVQM-UHFFFAOYSA-N 0.000 description 1
- 125000003373 pyrazinyl group Chemical group 0.000 description 1
- 125000003226 pyrazolyl group Chemical group 0.000 description 1
- 125000005581 pyrene group Chemical group 0.000 description 1
- PBMFSQRYOILNGV-UHFFFAOYSA-N pyridazine Chemical group C1=CC=NN=C1 PBMFSQRYOILNGV-UHFFFAOYSA-N 0.000 description 1
- 125000000714 pyrimidinyl group Chemical group 0.000 description 1
- 125000002294 quinazolinyl group Chemical group N1=C(N=CC2=CC=CC=C12)* 0.000 description 1
- 125000002943 quinolinyl group Chemical group N1=C(C=CC2=CC=CC=C12)* 0.000 description 1
- XSCHRSMBECNVNS-UHFFFAOYSA-N quinoxaline Chemical group N1=CC=NC2=CC=CC=C21 XSCHRSMBECNVNS-UHFFFAOYSA-N 0.000 description 1
- 238000001226 reprecipitation Methods 0.000 description 1
- 235000009566 rice Nutrition 0.000 description 1
- 125000002914 sec-butyl group Chemical group [H]C([H])([H])C([H])([H])C([H])(*)C([H])([H])[H] 0.000 description 1
- 238000000926 separation method Methods 0.000 description 1
- 229910052710 silicon Inorganic materials 0.000 description 1
- QRUBYZBWAOOHSV-UHFFFAOYSA-M silver trifluoromethanesulfonate Chemical compound [Ag+].[O-]S(=O)(=O)C(F)(F)F QRUBYZBWAOOHSV-UHFFFAOYSA-M 0.000 description 1
- 239000002356 single layer Substances 0.000 description 1
- 150000003384 small molecules Chemical class 0.000 description 1
- 239000011734 sodium Substances 0.000 description 1
- 238000004528 spin coating Methods 0.000 description 1
- 238000004544 sputter deposition Methods 0.000 description 1
- 125000000547 substituted alkyl group Chemical group 0.000 description 1
- 238000006467 substitution reaction Methods 0.000 description 1
- 239000002887 superconductor Substances 0.000 description 1
- 239000000725 suspension Substances 0.000 description 1
- 238000001308 synthesis method Methods 0.000 description 1
- 230000002194 synthesizing effect Effects 0.000 description 1
- 239000013076 target substance Substances 0.000 description 1
- 125000001973 tert-pentyl group Chemical group [H]C([H])([H])C([H])([H])C(*)(C([H])([H])[H])C([H])([H])[H] 0.000 description 1
- 125000003831 tetrazolyl group Chemical group 0.000 description 1
- 125000001425 triazolyl group Chemical group 0.000 description 1
- IMFACGCPASFAPR-UHFFFAOYSA-N tributylamine Chemical compound CCCCN(CCCC)CCCC IMFACGCPASFAPR-UHFFFAOYSA-N 0.000 description 1
- 125000002889 tridecyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 description 1
- ITMCEJHCFYSIIV-UHFFFAOYSA-N triflic acid Chemical compound OS(=O)(=O)C(F)(F)F ITMCEJHCFYSIIV-UHFFFAOYSA-N 0.000 description 1
- 125000001889 triflyl group Chemical group FC(F)(F)S(*)(=O)=O 0.000 description 1
- 125000006617 triphenylamine group Chemical group 0.000 description 1
- 125000005580 triphenylene group Chemical group 0.000 description 1
- 239000001226 triphosphate Substances 0.000 description 1
- 235000011178 triphosphate Nutrition 0.000 description 1
- UNXRWKVEANCORM-UHFFFAOYSA-N triphosphoric acid Chemical compound OP(O)(=O)OP(O)(=O)OP(O)(O)=O UNXRWKVEANCORM-UHFFFAOYSA-N 0.000 description 1
- PXXNTAGJWPJAGM-UHFFFAOYSA-N vertaline Natural products C1C2C=3C=C(OC)C(OC)=CC=3OC(C=C3)=CC=C3CCC(=O)OC1CC1N2CCCC1 PXXNTAGJWPJAGM-UHFFFAOYSA-N 0.000 description 1
- 239000010457 zeolite Substances 0.000 description 1
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07F—ACYCLIC, CARBOCYCLIC OR HETEROCYCLIC COMPOUNDS CONTAINING ELEMENTS OTHER THAN CARBON, HYDROGEN, HALOGEN, OXYGEN, NITROGEN, SULFUR, SELENIUM OR TELLURIUM
- C07F5/00—Compounds containing elements of Groups 3 or 13 of the Periodic Table
- C07F5/02—Boron compounds
- C07F5/022—Boron compounds without C-boron linkages
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07F—ACYCLIC, CARBOCYCLIC OR HETEROCYCLIC COMPOUNDS CONTAINING ELEMENTS OTHER THAN CARBON, HYDROGEN, HALOGEN, OXYGEN, NITROGEN, SULFUR, SELENIUM OR TELLURIUM
- C07F5/00—Compounds containing elements of Groups 3 or 13 of the Periodic Table
- C07F5/02—Boron compounds
- C07F5/025—Boronic and borinic acid compounds
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07F—ACYCLIC, CARBOCYCLIC OR HETEROCYCLIC COMPOUNDS CONTAINING ELEMENTS OTHER THAN CARBON, HYDROGEN, HALOGEN, OXYGEN, NITROGEN, SULFUR, SELENIUM OR TELLURIUM
- C07F5/00—Compounds containing elements of Groups 3 or 13 of the Periodic Table
- C07F5/02—Boron compounds
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y02—TECHNOLOGIES OR APPLICATIONS FOR MITIGATION OR ADAPTATION AGAINST CLIMATE CHANGE
- Y02E—REDUCTION OF GREENHOUSE GAS [GHG] EMISSIONS, RELATED TO ENERGY GENERATION, TRANSMISSION OR DISTRIBUTION
- Y02E10/00—Energy generation through renewable energy sources
- Y02E10/50—Photovoltaic [PV] energy
- Y02E10/549—Organic PV cells
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Electroluminescent Light Sources (AREA)
- Heterocyclic Carbon Compounds Containing A Hetero Ring Having Nitrogen And Oxygen As The Only Ring Hetero Atoms (AREA)
- Organic Low-Molecular-Weight Compounds And Preparation Thereof (AREA)
Description
A環、B環およびC環は、それぞれ独立して、アリール環またはヘテロアリール環であり、これらの環における少なくとも1つの水素は置換されていてもよく、
Y1はエステル化されていてもよい-B(OH)2であり、
X1およびX2は、それぞれ独立して、-O-、>N-Ar、-S-または-Se-であり、ここで、前記N-ArのArは置換されていてもよいアリール、置換されていてもよいヘテロアリールまたは置換されていてもよいアルキルであり、前記N-ArのArは連結基または単結合により前記A環、B環および/またはC環と結合していてもよく、そして、
式(1)で表される化合物または構造における少なくとも1つの水素が重水素で置換されていてもよい。)
Y1はエステル化されていてもよい-B(OH)2であり、
X1およびX2は、それぞれ独立して、-O-、>N-Ar、-S-または-Se-であり、ここで、前記N-ArのArはアルキルまたはハロゲンで置換されていてもよいアリール、アルキルまたはハロゲンで置換されていてもよいヘテロアリールもしくはアルキルまたはハロゲンで置換されていてもよいアルキルであり、前記N-ArのArは-O-、-S-、>C(R)2または単結合により前記A環、B環および/またはC環と結合していてもよく、また、前記>C(R)2のRはそれぞれ独立して水素またはアルキルであり、このアルキルにおける少なくとも1つの水素はハロゲンで置換されていてもよく、
式(1)で表される化合物または構造における少なくとも1つの水素が重水素で置換されていてもよく、そして、
前記多量体化合物は2量体化合物または3量体化合物である、
項1に記載する化合物または多量体化合物。
R1、R2、R3、R4、R5、R6、R7、R8、R9、R10およびR11は、それぞれ独立して、水素、アリール、ヘテロアリール、ジアリールアミノ、ジヘテロアリールアミノ、アリールヘテロアリールアミノ、アルキル、アルコキシ、アリールオキシまたはハロゲンであり、これらにおける少なくとも1つの水素はアリール、ヘテロアリール、アルキルまたはハロゲンで置換されていてもよく、また、R1~R11のうちの隣接する基同士が結合してa環、b環またはc環と共にアリール環またはヘテロアリール環を形成していてもよく、形成された環における少なくとも1つの水素はアリール、ヘテロアリール、ジアリールアミノ、ジヘテロアリールアミノ、アリールヘテロアリールアミノ、アルキル、アルコキシ、アリールオキシまたはハロゲンで置換されていてもよく、これらにおける少なくとも1つの水素はアリール、ヘテロアリール、アルキルまたはハロゲンで置換されていてもよく、
Y1はエステル化されていてもよい-B(OH)2であり、
X1およびX2は、それぞれ独立して、-O-、>N-Ar、-S-または-Se-であり、ここで、前記N-ArのArは炭素数6~12のアリール、炭素数2~15のヘテロアリールまたは炭素数1~6のアルキルであり、これらにおける少なくとも1つの水素はハロゲンで置換されていてもよく、前記N-ArのArは-O-、-S-、>C(R)2または単結合により前記a環、b環および/またはc環と結合していてもよく、また、前記>C(R)2のRはそれぞれ独立して炭素数1~6のアルキルであり、このアルキルにおける少なくとも1つの水素はハロゲンで置換されていてもよく、そして、
式(2)で表される化合物における少なくとも1つの水素が重水素で置換されていてもよい。)
Y1は-B(OH)2がエステル化された基であり、
X1およびX2は、それぞれ独立して、-O-、>N-Arまたは-S-であり、ここで、前記N-ArのArは炭素数6~10のアリールまたは炭素数1~4のアルキルであり、これらにおける少なくとも1つの水素はハロゲンで置換されていてもよく、そして、
式(2)で表される化合物における少なくとも1つの水素が重水素で置換されていてもよい、
項3に記載する化合物。
A環、B環およびC環は、それぞれ独立して、アリール環またはヘテロアリール環であり、これらの環における少なくとも1つの水素は置換されていてもよく、
Y1はエステル化されていてもよい-B(OH)2であり、
X1およびX2は、それぞれ独立して、-O-、>N-Ar、-S-または-Se-であり、ここで、前記N-ArのArは置換されていてもよいアリール、置換されていてもよいヘテロアリールまたは置換されていてもよいアルキルであり、前記N-ArのArは連結基または単結合により前記A環、B環および/またはC環と結合していてもよく、そして、
上記構造式における少なくとも1つの水素が重水素で置換されていてもよい。)
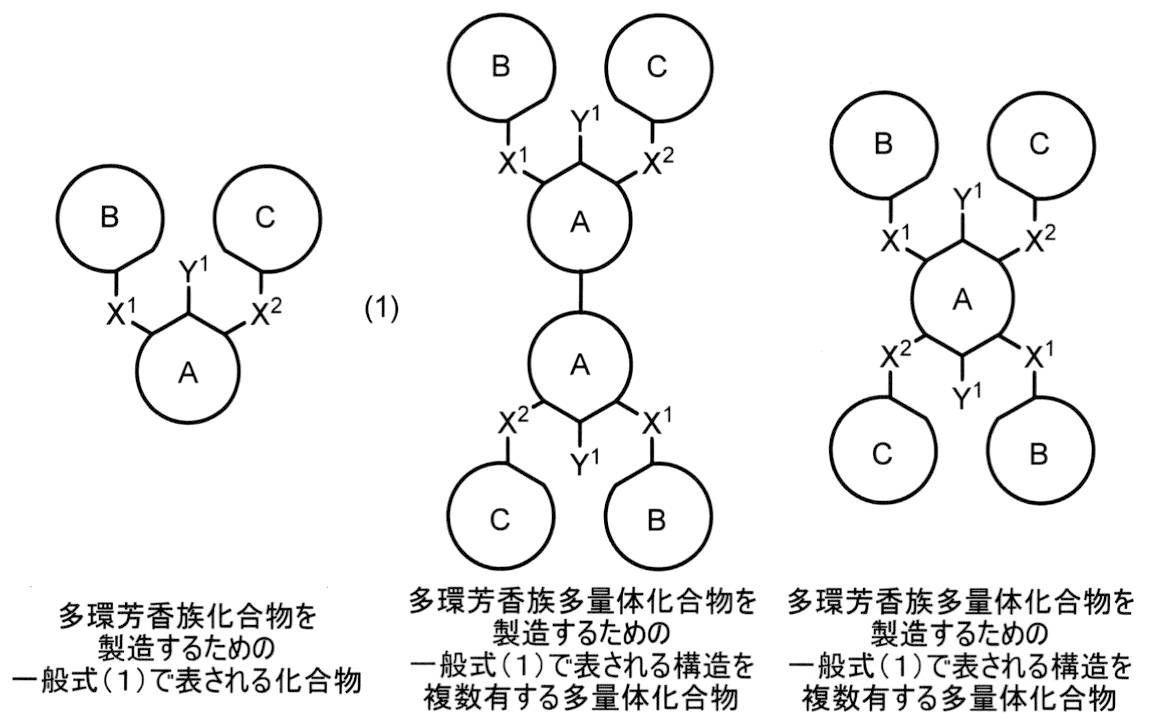
本発明を概略的に説明すると、本発明の一態様は、下記一般式(1)で表される化合物、および、下記一般式(1)で表される構造を複数有する多量体化合物に関する。なお、多量体化合物については、多量化の数や態様により化合物構造が異なるため、下記多量体化合物は一例であり、中央の多量体化合物は2つの式(1)で表される構造が単結合で結合してできた化合物であり、右側の多量体化合物は環Aを共有するようにして2つの式(1)で表される構造が結合してできた化合物である。また、式中の符号は上記項1で定義するものと同じである。
本願発明は、下記一般式(1)で表される化合物、または下記一般式(1)で表される構造を複数有する多量体化合物である。本願発明は、好ましくは、下記一般式(2)で表される化合物、または下記一般式(2)で表される構造を複数有する多量体化合物である。なお、下記式(1)中のY1、X1およびX2は上記項1で定義するものと同じであり、下記式(2)中のY1、X1、X2およびR1~R11は上記項3で定義するものと同じである。
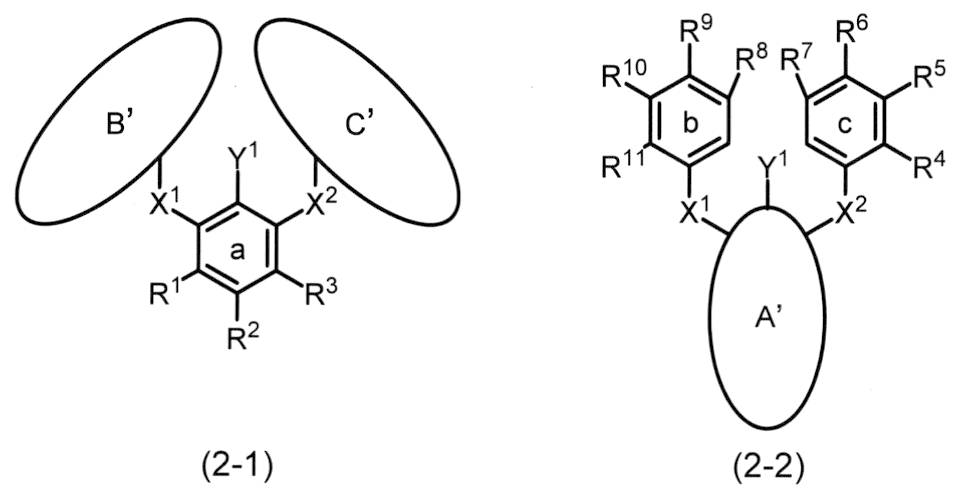
この規定は、下記式(2-3-1)で表される、X1やX2が縮合環B’および縮合環C’に取り込まれた環構造を有する化合物で表現できる。すなわち、例えば一般式(2)におけるb環(またはc環)であるベンゼン環に対してX1(またはX2)を取り込むようにして他の環が縮合して形成されるB’環(またはC’環)を有する化合物である。形成されてできた縮合環B’(または縮合環C’)は例えばフェノキサジン環、フェノチアジン環またはアクリジン環である。
また、上記規定は、下記式(2-3-2)や式(2-3-3)で表される、X1および/またはX2が縮合環A’に取り込まれた環構造を有する化合物でも表現できる。すなわち、例えば一般式(2)におけるa環であるベンゼン環に対してX1(および/またはX2)を取り込むようにして他の環が縮合して形成されるA’環を有する化合物である。形成されてできた縮合環A’は例えばフェノキサジン環、フェノチアジン環またはアクリジン環である。
なお、下記式中のY1、X1、X2およびR1~R11は上記項3で定義するものと同じである。
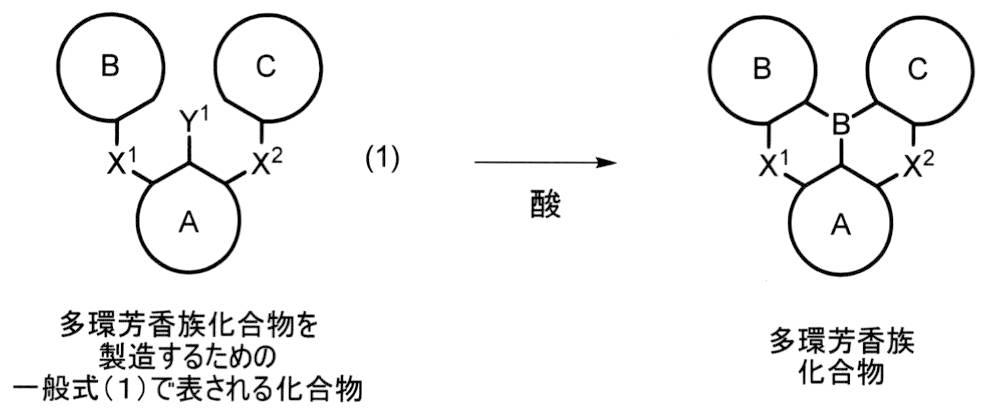
一般式(1)または(2)で表される化合物(ボロン酸またはボロン酸エステル)は、基本的には、A環(a環)とB環(b環)およびC環(c環)とを結合基(X1およびX2)で結合させることで中間体を製造し(第1反応)、その後にY1基を導入することで、まずボロン酸エステルを製造することができ、これを加水分解することでそのボロン酸を製造することができる。第1反応では、例えばエーテル化反応であれば、求核置換反応、ウルマン反応といった一般的反応が利用でき、アミノ化反応で有ればブッフバルト-ハートウィッグ反応といった一般的反応が利用できる。なお、以下に示す各スキーム中の構造式における符号は上記した定義と同じである。
次に、一般式(1)等で表されるボロン酸またはボロン酸エステルを用いて、多環芳香族化合物および多環芳香族多量体化合物を製造する方法について説明する。なお、以下に示す各スキーム中の構造式における符号は上記した定義と同じである。
本発明で製造される多環芳香族化合物および多環芳香族多量体化合物は、有機デバイス用材料として用いることができる。有機デバイスとしては、例えば、有機電界発光素子、有機電界効果トランジスタまたは有機薄膜太陽電池などがあげられる。
本発明で製造される多環芳香族化合物および多環芳香族多量体化合物は、有機電界発光素子の各層を構成する材料として用いることができる。以下に、本実施形態に係る有機EL素子について図面に基づいて詳細に説明する。図1は、本実施形態に係る有機EL素子を示す概略断面図である。
本発明で製造される多環芳香族化合物および多環芳香族多量体化合物は、有機電界効果トランジスタを構成する材料として用いることができる。有機電界効果トランジスタは、電圧入力によって発生させた電界により電流を制御するトランジスタのことであり、ソース電極とドレイン電極の他にゲート電極が設けられている。ゲート電極に電圧を印加すると電界が生じ、ソース電極とドレイン電極間を流れる電子(あるいはホール)の流れを任意にせき止めて電流を制御することができるものである。電界効果トランジスタは、単なるトランジスタ(バイポーラトランジスタ)に比べて小型化が容易であり、集積回路などを構成する素子としてよく用いられている。
(1)基板/ゲート電極/絶縁体層/ソース電極・ドレイン電極/有機半導体活性層
(2)基板/ゲート電極/絶縁体層/有機半導体活性層/ソース電極・ドレイン電極
(3)基板/有機半導体活性層/ソース電極・ドレイン電極/絶縁体層/ゲート電極
(4)基板/ソース電極・ドレイン電極/有機半導体活性層/絶縁体層/ゲート電極
このように構成された有機電界効果トランジスタは、アクティブマトリックス駆動方式の液晶ディスプレイや有機エレクトロルミネッセンスディスプレイの画素駆動スイッチング素子等として適用できる。
本発明で製造される多環芳香族化合物および多環芳香族多量体化合物は、有機薄膜太陽電池を構成する材料として用いることができる。有機薄膜太陽電池は、ガラスなどの透明基板上にITOなどの陽極、ホール輸送層、光電変換層、電子輸送層、陰極が積層された構造を有する。光電変換層は陽極側にp型半導体層を有し、陰極側にn型半導体層を有している。本発明で製造される多環芳香族化合物および多環芳香族多量体化合物は、その物性に応じて、ホール輸送層、p型半導体層、n型半導体層、電子輸送層の材料として用いることが可能である。本発明で製造される多環芳香族化合物および多環芳香族多量体化合物は、有機薄膜太陽電池においてホール輸送材料や電子輸送材料として機能しうる。有機薄膜太陽電池は、上記の他にホールブロック層、電子ブロック層、電子注入層、ホール注入層、平滑化層などを適宜備えていてもよい。有機薄膜太陽電池には、有機薄膜太陽電池に用いられる既知の材料を適宜選択して組み合わせて用いることができる。
1H-NMR(400MHz,CDCl3):δ=7.18~7.16(m,8H)、7.05~7.02(m,4H)、6.95~6.92(m,12H)、6.86~6.84(m,2H)、6.44(s,2H)、1.27(s,36H)、0.54(s,12H).
1H-NMR(400MHz,CDCl3):δ=7.31~7.25(m,6H)、7.05~6.98(m,5H)、6.71(d,2H)、1.08(s,12H).
1H-NMR(400MHz,CDCl3):δ=8.13(d,2H)、7.69(d,2H)、7.57(d,2H)、7.40~7.39(m,4H)、7.36~7.33(m,4H)7.29~7.26(m,2H)7.09~7.07(m,6H)1.11(s,12H).
1H-NMR(400MHz,CDCl3):δ=7.49(d,2H)、7.30~7.22(m,13H)、7.17(d,2H)、7.13~7.11(m,8H)、7.03~6.99(m,6H)、6.93(dd,2H)、6.67(d,2H)、1.39(s,12H)、1.14(s,12H).
MS(ACPI) m/z=488(M+MeOH)
1H-NMR(400MHz,CDCl3):δ=7.49(d,1H)、7.30~7.08(m,19H)、7.04~6.99(m,6H)、6.94(dd,1H)、6.77(d,1H)、6.73(d,1H)、1.39(s,6H)、0.93(s,12H).
1H-NMR(400MHz,CDCl3):δ=7.49(d,1H)、7.29~7.10(m,15H)、7.01(d,8H)、6.93(dd,1H)、6.75(d,1H)、6.69(d,1H)、1.39(s,6H)、1.28(s,18H)、0.96(s,12H).
<化合物(1-1-98)を用いた多環芳香族化合物Aの合成>
化合物(1-1-98)(8.7g)、塩化アルミニウム(12.5g)、N,N-ジイソプロピルエチルアミン(DIPEA)(6.0g)およびクロロベンゼン(44ml)の入ったフラスコを、窒素雰囲気下、120℃で1時間撹拌した。室温まで冷却した反応混合液を氷水(200ml)に注ぎ、トルエンを加え有機層を抽出した。有機層の溶媒を減圧留去し得られた固体をクロロホルムに溶解させ、シリカゲルショートパスカラム(溶離液:トルエン)に通した。溶媒を減圧留去して得られた粗精製物をシクロペンチルメチルエーテルおよびソルミックスA-11を用いて再沈殿させることで、黄色固体として多環芳香族化合物A(6.2g、収率70%)を得た。
1H-NMR(400MHz,CDCl3):δ=8.95(d,2H)、7.45(dd,6H)、7.13(d,4H)、7.08-7.04(m,4H)、6.95-6.88(m,6H)、6.75(d,2H)、5.56(s,2H)、1.46(s,18H)、1.33(s,18H).
<化合物(1-3-139)を用いた多環芳香族化合物Bの合成>
化合物(1-3-139)(22.8g)、塩化アルミニウム(23.5g)およびクロロベンゼン(230ml)の入ったフラスコを、窒素雰囲気下、130℃で2時間撹拌した。室温まで冷却した反応混合液を0℃の氷水(1L)に注ぎ、トルエン(500ml)を加え有機層を抽出した。有機層の溶媒を減圧留去して得られた固体をソルミックスA-11(500ml)を用いて洗浄することで、淡黄色固体として多環芳香族化合物B(14.2g、収率60%)を得た。
1H-NMR(400MHz,CDCl3):δ=8.69(dd,2H)、7.79(t,1H)、7.70(ddd,2H)、7.54(dt,2H)、7.38(ddd,2H)、7.22(d,2H).
<化合物(1-3-252)を用いた多環芳香族化合物Cの合成>
化合物(1-3-252)(124g)、塩化アルミニウム(131.3g)およびトルエン(620ml)の入ったフラスコを、窒素雰囲気下、90℃で1時間撹拌した。室温まで冷却した反応混合液を5℃の酢酸ナトリウム水溶液に注ぎ、有機層を抽出した。溶媒を減圧留去して得られた粗生成物をo-ジクロロベンゼンおよび酢酸エチルを用いて再沈澱させることで、黄色固体として多環芳香族化合物C(91g、収率63%)を得た。
1H-NMR(400MHz,CDCl3):δ=8.73(d,2H)、8.17(d,2H)、8.01(d,2H)、7.74(m,4H)、7.60(d,2H)、7.58(s,2H)、7.53(d,2H)、7.40-7.48(m,4H)、7.32(t,2H).
<化合物(1-3-386)を用いた多環芳香族化合物Dの合成>
1H-NMR(400MHz,CDCl3):δ=8.64(s,2H)、7.75(m,3H)、7.69(d,2H)、7.30(t,8H)、7.25(s,2H)、7.20(m,10H)、7.08(m,6H)、1.58(s,12H).
<化合物(1-3-439)を用いた多環芳香族化合物Eの合成>
化合物(1-3-439)(29.5g)、塩化アルミニウム(25.8g)およびクロロベンゼン(290ml)の入ったフラスコを、窒素雰囲気下、110℃で2時間撹拌した。反応終了後、室温まで冷却した反応混合液を0℃の氷水(1L)に注ぎ、トルエン(500ml)を加え有機層を抽出した。有機層の溶媒を減圧留去して得られた固体をソルミックスA-11(500ml)を用いて洗浄することで、淡黄色固体として多環芳香族化合物E(12.3g、収率41%)を得た。
1H-NMR(400MHz,CDCl3):δ=8.51(dd,2H)、7.81(t,1H)、7.56(d,2H)、7.36(dd,2H)、7.38(m,2H).
<化合物(1-2-340)を用いた多環芳香族化合物Fの合成>
化合物(1-2-340)(21.5g)およびトルエン(215ml)の入ったフラスコに塩化アルミニウム(19.2g)およびN,N-ジイソプロピルエチルアミン(DIPEA)(3.7g)を加え、3時間還流した。その後、室温まで冷却した反応混合液を氷水(250ml)に注ぎ、トルエンを加え有機層を抽出した。有機層の溶媒を減圧留去し得られた固体をNH2シリカゲルでショートカラム精製(溶離液:トルエン/ヘプタン=1/4(容量比))を行った後、メタノールで数回再沈殿した。得られた粗製品をシリカゲルでカラム精製(溶離液:トルエン/ヘプタン=1/2(容量比))を行い、黄色固体として多環芳香族化合物F(15.5g、収率71%)を得た。
1H-NMR(400MHz,CDCl3):δ=8.94(dd,1H)、8.70(s,1H)、7.74~7.69(m,4H)、7.62(t,1H)、7.53~7.47(m,2H)、7.38(dd,2H)、7.33~7.28(m,5H)、7.24(d,1H)、7.18(dd,4H)、7.09~7.05(m,4H)、6.80(d,1H)、6.30(d,1H)、1.58(s,6H).
<前駆体の臭化物と三臭化ホウ素を用いた多環芳香族化合物Dの合成>
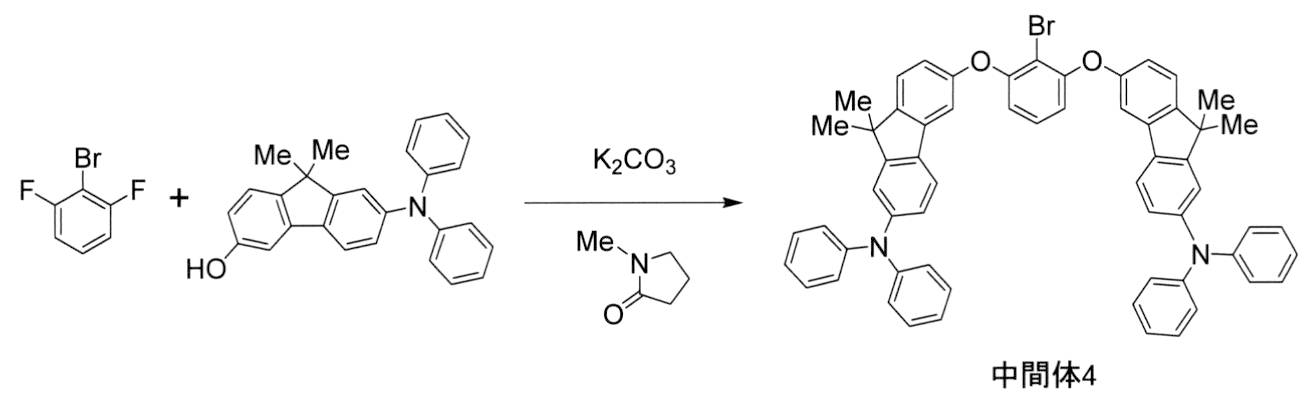
窒素雰囲気下、前駆体の臭化物である中間体4(11.0g)およびキシレン(60.5ml)の入ったフラスコを-40℃まで冷却し、2.6Mのn-ブチルリチウムヘキサン溶液(5.1ml)を滴下した。滴下終了後、この温度で0.5時間撹拌した後、60℃まで昇温して3時間撹拌した。その後、反応液を減圧して低沸点の成分を留去した後、-40℃まで冷却して三臭化ホウ素(4.3g)を加えた。室温まで昇温して0.5時間撹拌した後、0℃まで冷却してN,N-ジイソプロピルエチルアミン(3.8g)を添加し、125℃で8時間加熱撹拌した。反応液を室温まで冷却し、酢酸ナトリウム水溶液を加えて反応を停止させた後、トルエンを加えて分液した。有機層をシリカゲルショートパスカラム、次いでシリカゲルカラムクロマトグラフィー(溶離液:へプタン/トルエン=4/1混合溶媒(容量比))、更に活性炭カラムクロマトグラフィー(溶離液:トルエン)で精製し、多環芳香族化合物D(1.2g、収率12%)を得た。
<前駆体の塩化物と三臭化ホウ素を用いた多環芳香族化合物Fの合成>
窒素雰囲気下、前駆体の塩化物である中間体6(5.0g)およびキシレン(100ml)の入ったフラスコを-40℃まで冷却し、2.6Mのs-ブチルリチウムヘキサン溶液(9.3ml)を滴下した。滴下終了後、この温度で0.5時間撹拌した後、60℃まで昇温して3時間撹拌した。その後、反応液を減圧して低沸点の成分を留去した後、-40℃まで冷却して三臭化ホウ素(7.1g)を加えた。室温まで昇温して0.5時間撹拌した後、0℃まで冷却してN,N-ジイソプロピルエチルアミン(2.6g)を添加し、125℃で8時間加熱撹拌した。反応液を室温まで冷却し、酢酸ナトリウム水溶液を加えて反応を停止させた後、トルエンを加えて分液した。有機層をシリカゲルショートパスカラム、次いでシリカゲルカラムクロマトグラフィー(溶離液:へプタン/トルエン=4/1混合溶媒(容量比))、更に活性炭カラムクロマトグラフィー(溶離液:トルエン)で精製し、多環芳香族化合物F(0.8g、収率16%)を得た。
101 基板
102 陽極
103 正孔注入層
104 正孔輸送層
105 発光層
106 電子輸送層
107 電子注入層
108 陰極
Claims (12)
- 下記一般式(1)で表される化合物、または下記一般式(1)で表される単位構造を複数有する多量体化合物。
Y 1 、X 1 、およびX 2 は、A環における炭素原子に結合し、かつY 1 が結合する炭素とX 1 が結合する炭素とは隣接し、Y 1 が結合する炭素とX 2 が結合する炭素とは隣接しており、
A環、B環、およびC環は、それぞれ独立して、炭素数6~30のアリール環または炭素数2~30のヘテロアリール環であり、これらの環における少なくとも1つの水素は、アリール、ヘテロアリール、ジアリールアミノ、ジヘテロアリールアミノ、アリールヘテロアリールアミノ、アルキル、アルコキシ、アリールオキシ、またはハロゲンで置換されていてもよく、
Y1はボロン酸(-B(OH)2)またはボロン酸エステルであり、
X1およびX2は、それぞれ独立して、-O-、>N-Ar、-S-、または-Se-であり、ただし、X1およびX2の両方が-O-であることはなく、ここで、前記>N-ArのArは、アリール、ヘテロアリール、またはアルキルであり、これらの基における少なくとも1つの水素は、アリール、ヘテロアリール、アルキル、またはハロゲンで置換されていてもよく、前記>N-ArのArは、-O-、-S-、>C(R)2、または単結合により、前記A環、B環、および/またはC環と結合していてもよく、前記>C(R)2のRは、それぞれ独立して、水素またはアルキルであり、当該アルキルにおける少なくとも1つの水素はハロゲンで置換されていてもよく、
式(1)で表される化合物または単位構造における少なくとも1つの水素は、重水素で置換されていてもよく、そして、
前記多量体化合物の場合は、前記単位構造が単結合、炭素数1~3のアルキレン基、フェニレン基、またはナフチレン基で複数結合した形態、前記単位構造におけるA環、B環、またはC環を複数の単位構造で共有するようにして結合した形態、または、前記単位構造におけるA環、B環、またはC環同士が縮合するようにして結合した形態である。) - Y 1 、X 1 、およびX 2 は、A環における炭素原子に結合し、かつY 1 が結合する炭素とX 1 が結合する炭素とは隣接し、Y 1 が結合する炭素とX 2 が結合する炭素とは隣接しており、
A環、B環、およびC環は、それぞれ独立して、炭素数6~30のアリール環または炭素数2~30のヘテロアリール環であり、これらの環における少なくとも1つの水素は、炭素数6~30のアリール、炭素数2~30のヘテロアリール、ジアリールアミノ(ただしアリールは炭素数6~16のアリール)、ジヘテロアリールアミノ(ただしヘテロアリールは炭素数6~15のヘテロアリール)、アリールヘテロアリールアミノ(ただしアリールは炭素数6~16のアリール、ヘテロアリールは炭素数6~15のヘテロアリール)、炭素数1~24のアルキル、炭素数1~24のアルコキシ、炭素数6~30のアリールオキシ、またはハロゲンで置換されていてもよく、
Y1はボロン酸(-B(OH)2)またはボロン酸エステルであり、
X1およびX2は、それぞれ独立して、-O-、>N-Ar、-S-、または-Se-であり、ただし、X1およびX2の両方が-O-であることはなく、ここで、前記>N-ArのArは、炭素数6~30のアリール、炭素数2~30のヘテロアリール、または炭素数1~24のアルキルであり、これらの基における少なくとも1つの水素は、炭素数6~16のアリール、炭素数6~15のヘテロアリール、炭素数1~6のアルキル、またはハロゲンで置換されていてもよく、前記>N-ArのArは、-O-、-S-、>C(R)2、または単結合により、前記A環、B環、および/またはC環と結合していてもよく、前記>C(R)2のRは、それぞれ独立して、水素または炭素数1~6のアルキルであり、当該アルキルにおける少なくとも1つの水素はハロゲンで置換されていてもよく、
式(1)で表される化合物または単位構造における少なくとも1つの水素は、重水素で置換されていてもよく、
前記多量体化合物の場合は、前記単位構造が単結合、炭素数1~3のアルキレン基、フェニレン基、またはナフチレン基で複数結合した形態、前記単位構造におけるA環、B環、またはC環を複数の単位構造で共有するようにして結合した形態、または、前記単位構造におけるA環、B環、またはC環同士が縮合するようにして結合した形態であり、そして、
前記多量体化合物は、2量体化合物または3量体化合物である、
請求項1に記載する化合物または多量体化合物。 - 下記一般式(2)で表される化合物、または下記一般式(2)で表される単位構造を複数有する多量体化合物。
Y 1 、X 1 、およびX 2 は、a環における炭素原子に結合し、かつY 1 が結合する炭素とX 1 が結合する炭素とは隣接し、Y 1 が結合する炭素とX 2 が結合する炭素とは隣接しており、
R1、R2、R3、R4、R5、R6、R7、R8、R9、R10、およびR11は、それぞれ独立して、水素、炭素数6~30のアリール、炭素数2~30のヘテロアリール、ジアリールアミノ(ただしアリールは炭素数6~16のアリール)、ジヘテロアリールアミノ(ただしヘテロアリールは炭素数6~15のヘテロアリール)、アリールヘテロアリールアミノ(ただしアリールは炭素数6~16のアリール、ヘテロアリールは炭素数6~15のヘテロアリール)、炭素数1~24のアルキル、炭素数1~24のアルコキシ、炭素数6~30のアリールオキシ、またはハロゲンであり、これらの基における少なくとも1つの水素は、炭素数6~16のアリール、炭素数6~15のヘテロアリール、炭素数1~6のアルキル、またはハロゲンで置換されていてもよく、また、R1~R11のうちの隣接する基同士が結合して、a環、b環、またはc環と共に、炭素数9~30のアリール環または炭素数6~30のヘテロアリール環を形成していてもよく、形成された環における少なくとも1つの水素は、炭素数6~30のアリール、炭素数2~30のヘテロアリール、ジアリールアミノ(ただしアリールは炭素数6~16のアリール)、ジヘテロアリールアミノ(ただしヘテロアリールは炭素数6~15のヘテロアリール)、アリールヘテロアリールアミノ(ただしアリールは炭素数6~16のアリール、ヘテロアリールは炭素数6~15のヘテロアリール)、炭素数1~24のアルキル、炭素数1~24のアルコキシ、炭素数6~30のアリールオキシ、またはハロゲンで置換されていてもよく、これらの基における少なくとも1つの水素は、炭素数6~16のアリール、炭素数6~15のヘテロアリール、炭素数1~6のアルキル、またはハロゲンで置換されていてもよく、
Y1はボロン酸(-B(OH)2)またはボロン酸エステルであり、
X1およびX2は、それぞれ独立して、-O-、>N-Ar、-S-、または-Se-であり、ただし、X1およびX2の両方が-O-であることはなく、ここで、前記>N-ArのArは、炭素数6~12のアリール、炭素数2~15のヘテロアリール、または炭素数1~6のアルキルであり、これらの基における少なくとも1つの水素はハロゲンで置換されていてもよく、前記>N-ArのArは、-O-、-S-、>C(R)2、または単結合により、前記a環、b環、および/またはc環と結合していてもよく、前記>C(R)2のRは、それぞれ独立して、炭素数1~6のアルキルであり、当該アルキルにおける少なくとも1つの水素はハロゲンで置換されていてもよく、
式(2)で表される化合物または単位構造における少なくとも1つの水素は、重水素で置換されていてもよく、
前記多量体化合物の場合は、前記単位構造が単結合、炭素数1~3のアルキレン基、フェニレン基、またはナフチレン基で複数結合した形態、前記単位構造におけるa環、b環、またはc環を複数の単位構造で共有するようにして結合した形態、または、前記単位構造におけるa環、b環、またはc環同士が縮合するようにして結合した形態であり、そして、
前記多量体化合物は、2量体化合物または3量体化合物である。) - Y 1 、X 1 、およびX 2 は、a環における炭素原子に結合し、かつY 1 が結合する炭素とX 1 が結合する炭素とは隣接し、Y 1 が結合する炭素とX 2 が結合する炭素とは隣接しており、
R1、R2、R3、R4、R5、R6、R7、R8、R9、R10、およびR11は、それぞれ独立して、水素、炭素数6~30のアリール、炭素数2~30のヘテロアリール、ジアリールアミノ(ただしアリールは炭素数6~12のアリール)、またはハロゲンであり、これらの基における少なくとも1つの水素はハロゲンで置換されていてもよく、また、R1~R11のうちの隣接する基同士が結合して、a環、b環、またはc環と共に、炭素数9~16のアリール環または炭素数6~15のヘテロアリール環を形成していてもよく、形成された環における少なくとも1つの水素は、炭素数6~10のアリールまたはハロゲンで置換されていてもよく、この炭素数6~10のアリールにおける少なくとも1つの水素はハロゲンで置換されていてもよく、
Y1はボロン酸エステルであり、
X1およびX2は、それぞれ独立して、-O-、>N-Ar、または-S-であり、ただし、X1およびX2の両方が-O-であることはなく、ここで、前記>N-ArのArは、炭素数6~10のアリールまたは炭素数1~4のアルキルであり、これらの基における少なくとも1つの水素はハロゲンで置換されていてもよく、
式(2)で表される化合物または単位構造における少なくとも1つの水素は、重水素で置換されていてもよく、
前記多量体化合物の場合は、前記単位構造が単結合、炭素数1~3のアルキレン基、フェニレン基、またはナフチレン基で複数結合した形態、前記単位構造におけるa環、b環、またはc環を複数の単位構造で共有するようにして結合した形態、または、前記単位構造におけるa環、b環、またはc環同士が縮合するようにして結合した形態であり、そして、
前記多量体化合物は、2量体化合物または3量体化合物である、
請求項3に記載する化合物。 - 下記一般式(1)で表される化合物、または下記一般式(1)で表される単位構造を複数有する多量体化合物に、酸を作用させて、下記一般式(3)で表される多環芳香族化合物、または下記一般式(3)で表される単位構造を複数有する多環芳香族多量体化合物を製造する方法。
Y 1 、X 1 、およびX 2 は、A環における炭素原子に結合し、かつY 1 が結合する炭素とX 1 が結合する炭素とは隣接し、Y 1 が結合する炭素とX 2 が結合する炭素とは隣接しており、
X 1 およびB(ホウ素)はB環における隣接する炭素原子に結合し、X 2 およびB(ホウ素)はC環における隣接する炭素原子に結合しており、
A環、B環、およびC環は、それぞれ独立して、炭素数6~30のアリール環または炭素数2~30のヘテロアリール環であり、これらの環における少なくとも1つの水素は、アリール、ヘテロアリール、ジアリールアミノ、ジヘテロアリールアミノ、アリールヘテロアリールアミノ、アルキル、アルコキシ、アリールオキシ、またはハロゲンで置換されていてもよく、
Y1はボロン酸(-B(OH)2)またはボロン酸エステルであり、
X1およびX2は、それぞれ独立して、-O-、>N-Ar、-S-、または-Se-であり、ここで、前記>N-ArのArは、アリール、ヘテロアリール、またはアルキルであり、これらの基における少なくとも1つの水素は、アリール、ヘテロアリール、アルキル、またはハロゲンで置換されていてもよく、前記>N-ArのArは、-O-、-S-、>C(R)2、または単結合により、前記A環、B環、および/またはC環と結合していてもよく、前記>C(R)2のRは、それぞれ独立して、水素またはアルキルであり、当該アルキルにおける少なくとも1つの水素はハロゲンで置換されていてもよく、
式(1)で表される化合物または単位構造、および式(3)で表される化合物または単位構造における少なくとも1つの水素は、重水素で置換されていてもよく、そして、
前記多量体化合物および多環芳香族多量体化合物の場合は、前記単位構造が単結合、炭素数1~3のアルキレン基、フェニレン基、またはナフチレン基で複数結合した形態、前記単位構造におけるA環、B環、またはC環を複数の単位構造で共有するようにして結合した形態、または、前記単位構造におけるA環、B環、またはC環同士が縮合するようにして結合した形態である。) - 上記式(1)および式(3)中、
Y 1 、X 1 、およびX 2 は、A環における炭素原子に結合し、かつY 1 が結合する炭素とX 1 が結合する炭素とは隣接し、Y 1 が結合する炭素とX 2 が結合する炭素とは隣接しており、
X 1 およびB(ホウ素)はB環における隣接する炭素原子に結合し、X 2 およびB(ホウ素)はC環における隣接する炭素原子に結合しており、
A環、B環、およびC環は、それぞれ独立して、炭素数6~30のアリール環または炭素数2~30のヘテロアリール環であり、これらの環における少なくとも1つの水素は、炭素数6~30のアリール、炭素数2~30のヘテロアリール、ジアリールアミノ(ただしアリールは炭素数6~16のアリール)、ジヘテロアリールアミノ(ただしヘテロアリールは炭素数6~15のヘテロアリール)、アリールヘテロアリールアミノ(ただしアリールは炭素数6~16のアリール、ヘテロアリールは炭素数6~15のヘテロアリール)、炭素数1~24のアルキル、炭素数1~24のアルコキシ、炭素数6~30のアリールオキシ、またはハロゲンで置換されていてもよく、
Y1はボロン酸(-B(OH)2)またはボロン酸エステルであり、
X1およびX2は、それぞれ独立して、-O-、>N-Ar、-S-、または-Se-であり、ここで、前記>N-ArのArは、炭素数6~30のアリール、炭素数2~30のヘテロアリール、または炭素数1~24のアルキルであり、これらの基における少なくとも1つの水素は、炭素数6~16のアリール、炭素数6~15のヘテロアリール、炭素数1~6のアルキル、またはハロゲンで置換されていてもよく、前記>N-ArのArは、-O-、-S-、>C(R)2、または単結合により、前記A環、B環、および/またはC環と結合していてもよく、前記>C(R)2のRは、それぞれ独立して、水素または炭素数1~6のアルキルであり、当該アルキルにおける少なくとも1つの水素はハロゲンで置換されていてもよく、
式(1)で表される化合物または単位構造、および式(3)で表される化合物または単位構造における少なくとも1つの水素は、重水素で置換されていてもよく、
前記多量体化合物および多環芳香族多量体化合物の場合は、前記単位構造が単結合、炭素数1~3のアルキレン基、フェニレン基、またはナフチレン基で複数結合した形態、前記単位構造におけるA環、B環、またはC環を複数の単位構造で共有するようにして結合した形態、または、前記単位構造におけるA環、B環、またはC環同士が縮合するようにして結合した形態であり、そして、
前記多量体化合物および多環芳香族多量体化合物は、2量体化合物または3量体化合物である、
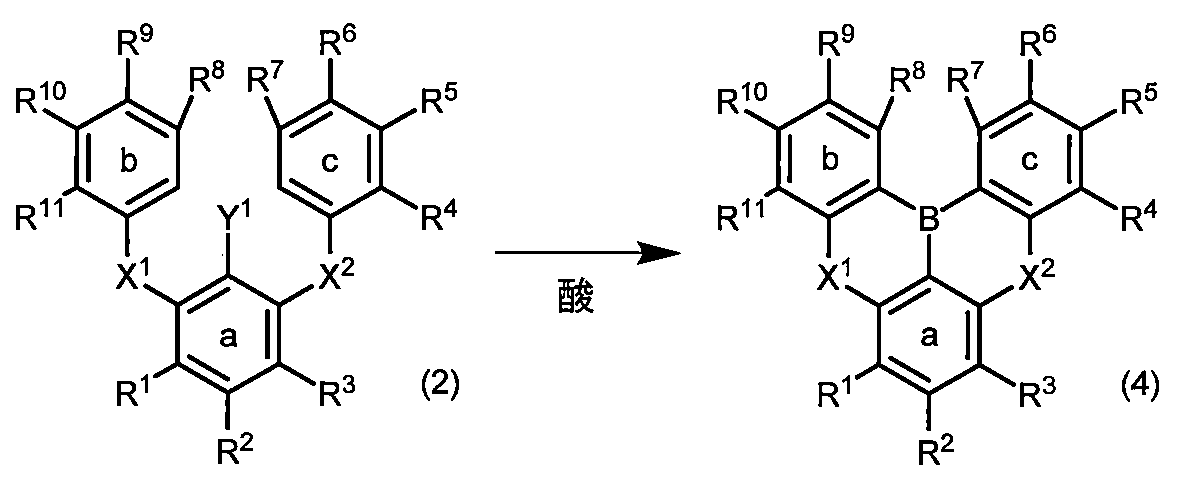
請求項7に記載する製造方法。 - 下記一般式(2)で表される化合物、または下記一般式(2)で表される単位構造を複数有する多量体化合物に、酸を作用させて、下記一般式(4)で表される多環芳香族化合物、または下記一般式(4)で表される単位構造を複数有する多環芳香族多量体化合物を製造する方法。
Y 1 、X 1 、およびX 2 は、a環における炭素原子に結合し、かつY 1 が結合する炭素とX 1 が結合する炭素とは隣接し、Y 1 が結合する炭素とX 2 が結合する炭素とは隣接しており、
X 1 およびB(ホウ素)はb環における隣接する炭素原子に結合し、X 2 およびB(ホウ素)はc環における隣接する炭素原子に結合しており、
R1、R2、R3、R4、R5、R6、R7、R8、R9、R10、およびR11は、それぞれ独立して、水素、炭素数6~30のアリール、炭素数2~30のヘテロアリール、ジアリールアミノ(ただしアリールは炭素数6~16のアリール)、ジヘテロアリールアミノ(ただしヘテロアリールは炭素数6~15のヘテロアリール)、アリールヘテロアリールアミノ(ただしアリールは炭素数6~16のアリール、ヘテロアリールは炭素数6~15のヘテロアリール)、炭素数1~24のアルキル、炭素数1~24のアルコキシ、炭素数6~30のアリールオキシ、またはハロゲンであり、これらの基における少なくとも1つの水素は、炭素数6~16のアリール、炭素数6~15のヘテロアリール、炭素数1~6のアルキル、またはハロゲンで置換されていてもよく、また、R1~R11のうちの隣接する基同士が結合して、a環、b環、またはc環と共に、炭素数9~30のアリール環または炭素数6~30のヘテロアリール環を形成していてもよく、形成された環における少なくとも1つの水素は、炭素数6~30のアリール、炭素数2~30のヘテロアリール、ジアリールアミノ(ただしアリールは炭素数6~16のアリール)、ジヘテロアリールアミノ(ただしヘテロアリールは炭素数6~15のヘテロアリール)、アリールヘテロアリールアミノ(ただしアリールは炭素数6~16のアリール、ヘテロアリールは炭素数6~15のヘテロアリール)、炭素数1~24のアルキル、炭素数1~24のアルコキシ、炭素数6~30のアリールオキシ、またはハロゲンで置換されていてもよく、これらの基における少なくとも1つの水素は、炭素数6~16のアリール、炭素数6~15のヘテロアリール、炭素数1~6のアルキル、またはハロゲンで置換されていてもよく、
Y1はボロン酸(-B(OH)2)またはボロン酸エステルであり、
X1およびX2は、それぞれ独立して、-O-、>N-Ar、-S-、または-Se-であり、ここで、前記>N-ArのArは、炭素数6~12のアリール、炭素数2~15のヘテロアリール、または炭素数1~6のアルキルであり、これらの基における少なくとも1つの水素はハロゲンで置換されていてもよく、前記>N-ArのArは、-O-、-S-、>C(R)2、または単結合により、前記a環、b環、および/またはc環と結合していてもよく、前記>C(R)2のRは、それぞれ独立して、炭素数1~6のアルキルであり、当該アルキルにおける少なくとも1つの水素はハロゲンで置換されていてもよく、
式(2)で表される化合物または単位構造、および式(4)で表される化合物または単位構造における少なくとも1つの水素は、重水素で置換されていてもよく、
前記多量体化合物および多環芳香族多量体化合物の場合は、前記単位構造が単結合、炭素数1~3のアルキレン基、フェニレン基、またはナフチレン基で複数結合した形態、前記単位構造におけるa環、b環、またはc環を複数の単位構造で共有するようにして結合した形態、または、前記単位構造におけるa環、b環、またはc環同士が縮合するようにして結合した形態であり、そして、
前記多量体化合物および多環芳香族多量体化合物は、2量体化合物または3量体化合物である。) - 上記式(2)および式(4)中、
Y 1 、X 1 、およびX 2 は、a環における炭素原子に結合し、かつY 1 が結合する炭素とX 1 が結合する炭素とは隣接し、Y 1 が結合する炭素とX 2 が結合する炭素とは隣接しており、
X 1 およびB(ホウ素)はb環における隣接する炭素原子に結合し、X 2 およびB(ホウ素)はc環における隣接する炭素原子に結合しており、
R1、R2、R3、R4、R5、R6、R7、R8、R9、R10、およびR11は、それぞれ独立して、水素、炭素数6~30のアリール、炭素数2~30のヘテロアリール、ジアリールアミノ(ただしアリールは炭素数6~12のアリール)、またはハロゲンであり、これらの基における少なくとも1つの水素はハロゲンで置換されていてもよく、また、R1~R11のうちの隣接する基同士が結合して、a環、b環、またはc環と共に、炭素数9~16のアリール環または炭素数6~15のヘテロアリール環を形成していてもよく、形成された環における少なくとも1つの水素は、炭素数6~10のアリールまたはハロゲンで置換されていてもよく、この炭素数6~10のアリールにおける少なくとも1つの水素はハロゲンで置換されていてもよく、
Y1はボロン酸エステルであり、
X1およびX2は、それぞれ独立して、-O-、>N-Ar、または-S-であり、ここで、前記>N-ArのArは、炭素数6~10のアリールまたは炭素数1~4のアルキルであり、これらの基における少なくとも1つの水素はハロゲンで置換されていてもよく、
式(2)で表される化合物または単位構造、および式(4)で表される化合物または単位構造における少なくとも1つの水素は、重水素で置換されていてもよく、
前記多量体化合物および多環芳香族多量体化合物の場合は、前記単位構造が単結合、炭素数1~3のアルキレン基、フェニレン基、またはナフチレン基で複数結合した形態、前記単位構造におけるa環、b環、またはc環を複数の単位構造で共有するようにして結合した形態、または、前記単位構造におけるa環、b環、またはc環同士が縮合するようにして結合した形態であり、そして、
前記多量体化合物および多環芳香族多量体化合物は、2量体化合物または3量体化合物である、
請求項9に記載する製造方法。 - 請求項1に記載の化合物(ただし、X1およびX2の両方が-O-である場合も含む)または多量体化合物(ただし、X1およびX2の両方が-O-である場合も含む)を含む、下記一般式(3)で表される多環芳香族化合物または下記一般式(3)で表される単位構造を複数有する多環芳香族多量体化合物の製造材料。
Y 1 、X 1 、およびX 2 は、A環における炭素原子に結合し、かつY 1 が結合する炭素とX 1 が結合する炭素とは隣接し、Y 1 が結合する炭素とX 2 が結合する炭素とは隣接しており、
X 1 およびB(ホウ素)はB環における隣接する炭素原子に結合し、X 2 およびB(ホウ素)はC環における隣接する炭素原子に結合しており、
A環、B環、およびC環は、それぞれ独立して、炭素数6~30のアリール環または炭素数2~30のヘテロアリール環であり、これらの環における少なくとも1つの水素は、アリール、ヘテロアリール、ジアリールアミノ、ジヘテロアリールアミノ、アリールヘテロアリールアミノ、アルキル、アルコキシ、アリールオキシ、またはハロゲンで置換されていてもよく、
Y 1 はボロン酸(-B(OH) 2 )またはボロン酸エステルであり、
X 1 およびX 2 は、それぞれ独立して、-O-、>N-Ar、-S-、または-Se-であり、ここで、前記>N-ArのArは、アリール、ヘテロアリール、またはアルキルであり、これらの基における少なくとも1つの水素は、アリール、ヘテロアリール、アルキル、またはハロゲンで置換されていてもよく、前記>N-ArのArは、-O-、-S-、>C(R) 2 、または単結合により、前記A環、B環、および/またはC環と結合していてもよく、前記>C(R) 2 のRは、それぞれ独立して、水素またはアルキルであり、当該アルキルにおける少なくとも1つの水素はハロゲンで置換されていてもよく、
式(3)で表される化合物または単位構造における少なくとも1つの水素は、重水素で置換されていてもよく、そして、
前記多量体化合物および多環芳香族多量体化合物の場合は、前記単位構造が単結合、炭素数1~3のアルキレン基、フェニレン基、またはナフチレン基で複数結合した形態、前記単位構造におけるA環、B環、またはC環を複数の単位構造で共有するようにして結合した形態、または、前記単位構造におけるA環、B環、またはC環同士が縮合するようにして結合した形態である。)
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2016212093 | 2016-10-28 | ||
| JP2016212093 | 2016-10-28 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2018076281A JP2018076281A (ja) | 2018-05-17 |
| JP7030302B2 true JP7030302B2 (ja) | 2022-03-07 |
Family
ID=62079610
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2017111692A Active JP7030302B2 (ja) | 2016-10-28 | 2017-06-06 | ボロン酸またはボロン酸エステル、もしくはそれらを用いて多環芳香族化合物または多環芳香族多量体化合物を製造する方法 |
Country Status (3)
| Country | Link |
|---|---|
| JP (1) | JP7030302B2 (ja) |
| KR (2) | KR102426597B1 (ja) |
| CN (2) | CN108017662A (ja) |
Families Citing this family (9)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2020017931A1 (ko) * | 2018-07-19 | 2020-01-23 | 주식회사 엘지화학 | 다환 화합물 및 이를 포함하는 유기 발광 소자 |
| WO2020045681A1 (ja) * | 2018-08-31 | 2020-03-05 | 学校法人関西学院 | 多環芳香族化合物の発光材料を用いた有機電界発光素子 |
| KR20200094262A (ko) | 2019-01-29 | 2020-08-07 | 삼성디스플레이 주식회사 | 유기 전계 발광 소자 및 유기 전계 발광 소자용 다환 화합물 |
| KR20200107028A (ko) | 2019-03-05 | 2020-09-16 | 삼성디스플레이 주식회사 | 유기 전계 발광 소자 및 유기 전계 발광 소자용 다환 화합물 |
| KR20210014834A (ko) | 2019-07-30 | 2021-02-10 | 삼성디스플레이 주식회사 | 유기금속 화합물 및 이를 포함한 유기 발광 소자 |
| KR20210018574A (ko) | 2019-08-05 | 2021-02-18 | 삼성디스플레이 주식회사 | 유기금속 화합물 및 이를 포함한 유기 발광 소자 |
| KR20210065258A (ko) | 2019-11-26 | 2021-06-04 | 삼성디스플레이 주식회사 | 화합물 및 이를 포함하는 발광 소자 |
| CN112194612A (zh) * | 2020-10-15 | 2021-01-08 | 濮阳惠成电子材料股份有限公司 | 光电材料中间体n-(7-溴-9,9-二甲基芴-2-基)咔唑的合成方法 |
| WO2024132993A1 (de) | 2022-12-19 | 2024-06-27 | Merck Patent Gmbh | Materialien für elektronische vorrichtungen |
Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2012115394A2 (ko) | 2011-02-24 | 2012-08-30 | 덕산하이메탈(주) | 화합물 및 이를 이용한 유기전기소자, 그 전자장치 |
| JP2013229285A (ja) | 2011-12-15 | 2013-11-07 | Fujifilm Corp | 金属錯体色素、光電変換素子、色素増感太陽電池、色素溶液および化合物 |
| WO2013185871A1 (en) | 2012-06-12 | 2013-12-19 | Merck Patent Gmbh | Compounds for electronic devices |
Family Cites Families (8)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP3735703B2 (ja) | 1999-12-21 | 2006-01-18 | 大阪大学長 | エレクトロルミネッセンス素子 |
| US20040131881A1 (en) | 2002-12-31 | 2004-07-08 | Eastman Kodak Company | Complex fluorene-containing compounds for use in OLED devices |
| JP2005170911A (ja) | 2003-12-15 | 2005-06-30 | Idemitsu Kosan Co Ltd | 芳香族化合物およびそれを用いた有機エレクトロルミネッセンス素子 |
| DE102010009903A1 (de) | 2010-03-02 | 2011-09-08 | Merck Patent Gmbh | Verbindungen für elektronische Vorrichtungen |
| KR101982749B1 (ko) * | 2011-02-24 | 2019-05-28 | 덕산네오룩스 주식회사 | 화합물 및 이를 이용한 유기전기소자, 그 전자장치 |
| CN103502252A (zh) | 2011-03-03 | 2014-01-08 | 国立大学法人九州大学 | 新型化合物、电荷输送材料和有机器件 |
| US9166176B2 (en) * | 2011-03-10 | 2015-10-20 | Kyoto University | Polycyclic aromatic compound |
| TWI636056B (zh) | 2014-02-18 | 2018-09-21 | 學校法人關西學院 | 多環芳香族化合物及其製造方法、有機元件用材料及其應用 |
-
2017
- 2017-06-06 JP JP2017111692A patent/JP7030302B2/ja active Active
- 2017-07-19 KR KR1020170091589A patent/KR102426597B1/ko active IP Right Grant
- 2017-10-27 CN CN201711020839.1A patent/CN108017662A/zh active Pending
- 2017-10-27 CN CN202210849129.4A patent/CN115197253A/zh active Pending
-
2022
- 2022-07-22 KR KR1020220090759A patent/KR20220110677A/ko not_active Application Discontinuation
Patent Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2012115394A2 (ko) | 2011-02-24 | 2012-08-30 | 덕산하이메탈(주) | 화합물 및 이를 이용한 유기전기소자, 그 전자장치 |
| JP2013229285A (ja) | 2011-12-15 | 2013-11-07 | Fujifilm Corp | 金属錯体色素、光電変換素子、色素増感太陽電池、色素溶液および化合物 |
| WO2013185871A1 (en) | 2012-06-12 | 2013-12-19 | Merck Patent Gmbh | Compounds for electronic devices |
Non-Patent Citations (2)
| Title |
|---|
| Angew.Chem.Int.Ed.,2015年,Vol.54,pp.3033-3037 |
| J.Org.Chem.,2013年,Vol.78,pp.6350-6355 |
Also Published As
| Publication number | Publication date |
|---|---|
| KR20220110677A (ko) | 2022-08-09 |
| KR102426597B1 (ko) | 2022-07-27 |
| CN108017662A (zh) | 2018-05-11 |
| CN115197253A (zh) | 2022-10-18 |
| JP2018076281A (ja) | 2018-05-17 |
| KR20180046851A (ko) | 2018-05-09 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP7030302B2 (ja) | ボロン酸またはボロン酸エステル、もしくはそれらを用いて多環芳香族化合物または多環芳香族多量体化合物を製造する方法 | |
| CN109155368B (zh) | 有机电场发光元件、显示装置及照明装置 | |
| KR102618236B1 (ko) | 중수소 치환 다환 방향족 화합물 | |
| KR102701483B1 (ko) | 유기 전계 발광 소자 | |
| CN107851724B (zh) | 有机电场发光元件、显示装置及照明装置 | |
| CN110692146B (zh) | 有机电场发光元件及显示装置或照明装置 | |
| WO2020054676A1 (ja) | 有機電界発光素子 | |
| WO2018150832A1 (ja) | 有機電界発光素子 | |
| WO2019009052A1 (ja) | 多環芳香族化合物 | |
| JP2015188099A (ja) | 有機電界発光素子用材料、有機電界発光素子、表示装置、及び照明装置 | |
| CN112601753B (zh) | 氟取代多环芳香族化合物、有机器件用材料、有机电致发光元件、显示装置以及照明装置 | |
| WO2013150674A1 (ja) | ベンゾフルオレン化合物、該化合物を用いた発光層用材料および有機電界発光素子 | |
| KR102007337B1 (ko) | 벤조플루오렌 화합물, 이 화합물을 사용한 발광층용 재료 및 유기 전계 발광 소자 | |
| JP6041058B2 (ja) | アントラセン系化合物、発光層用材料、これを用いた有機電界発光素子、表示装置および照明装置 | |
| JP2020136675A (ja) | 有機電界発光素子 | |
| JP2020200254A (ja) | 多環芳香族化合物 | |
| CN110249442B (zh) | 化合物 | |
| JP7454810B2 (ja) | 多環芳香族化合物 | |
| JP2023134566A (ja) | 有機電界発光素子 | |
| JP7018171B2 (ja) | アルケニル基を有する多環芳香族化合物およびその多量体 | |
| KR20230007944A (ko) | 안트라센 화합물 | |
| KR20220021418A (ko) | 다환방향족 화합물 | |
| JP2021177526A (ja) | 有機電界発光素子 | |
| JP2022090294A (ja) | 多環芳香族化合物 | |
| KR102714696B1 (ko) | 불소 치환 다환 방향족 화합물 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| AA64 | Notification of invalidation of claim of internal priority (with term) |
Free format text: JAPANESE INTERMEDIATE CODE: A241764 Effective date: 20170704 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20170726 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20200110 |
|
| A977 | Report on retrieval |
Free format text: JAPANESE INTERMEDIATE CODE: A971007 Effective date: 20201210 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20201222 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20210217 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20210416 |
|
| A711 | Notification of change in applicant |
Free format text: JAPANESE INTERMEDIATE CODE: A711 Effective date: 20210426 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20210706 |
|
| AA91 | Notification that invitation to amend document was cancelled |
Free format text: JAPANESE INTERMEDIATE CODE: A971091 Effective date: 20210810 Free format text: JAPANESE INTERMEDIATE CODE: A971091 Effective date: 20210727 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20210817 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20211111 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20220125 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20220214 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 7030302 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |