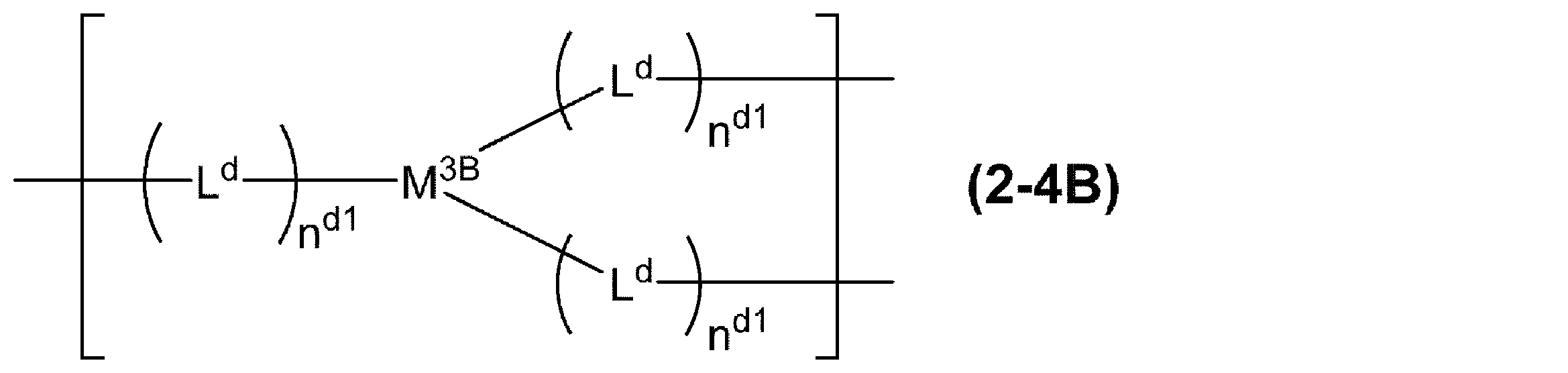JP7017907B2 - 発光素子 - Google Patents
発光素子 Download PDFInfo
- Publication number
- JP7017907B2 JP7017907B2 JP2017219443A JP2017219443A JP7017907B2 JP 7017907 B2 JP7017907 B2 JP 7017907B2 JP 2017219443 A JP2017219443 A JP 2017219443A JP 2017219443 A JP2017219443 A JP 2017219443A JP 7017907 B2 JP7017907 B2 JP 7017907B2
- Authority
- JP
- Japan
- Prior art keywords
- group
- atom
- ring
- formula
- layer
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
- 0 CN(N(*)*)N(*)* Chemical compound CN(N(*)*)N(*)* 0.000 description 15
- YVWPHVUJIZFMNR-PZUCLOCMSA-N C/C(/C=C(\C)/N(c1ccccc1)c(cc1)ccc1-c(cc1)ccc1N(c1ccc(C=C)cc1)c1cc(C)ccc1)=C/C=C Chemical compound C/C(/C=C(\C)/N(c1ccccc1)c(cc1)ccc1-c(cc1)ccc1N(c1ccc(C=C)cc1)c1cc(C)ccc1)=C/C=C YVWPHVUJIZFMNR-PZUCLOCMSA-N 0.000 description 1
- GMRSXGNVTNZWFA-UHFFFAOYSA-N CC(C(OCCc1cccc(N(c2ccccc2)c(cc2)ccc2N(c2ccccc2)c2cccc(CCOC(C(C)=C)=O)c2)c1)=O)=C Chemical compound CC(C(OCCc1cccc(N(c2ccccc2)c(cc2)ccc2N(c2ccccc2)c2cccc(CCOC(C(C)=C)=O)c2)c1)=O)=C GMRSXGNVTNZWFA-UHFFFAOYSA-N 0.000 description 1
- MVCZOLWLICYNQS-UHFFFAOYSA-N CCCCCCc1cc(C2(C(C=C3C)=C4C3=C2C=C4C)c2cc(CCCCCC)cc(CCCCCC)c2)cc(C)c1 Chemical compound CCCCCCc1cc(C2(C(C=C3C)=C4C3=C2C=C4C)c2cc(CCCCCC)cc(CCCCCC)c2)cc(C)c1 MVCZOLWLICYNQS-UHFFFAOYSA-N 0.000 description 1
- KLKNYXQEQYZZCP-UHFFFAOYSA-N CCCc(cccc1C(C)CC)c1N Chemical compound CCCc(cccc1C(C)CC)c1N KLKNYXQEQYZZCP-UHFFFAOYSA-N 0.000 description 1
- ARZUXEDWORFCJU-UHFFFAOYSA-N CC[N]1(=C)=C(C)C1 Chemical compound CC[N]1(=C)=C(C)C1 ARZUXEDWORFCJU-UHFFFAOYSA-N 0.000 description 1
- OZBHXHWJZJGBLQ-UHFFFAOYSA-N Cc1cc(-c2cc(-c3ccccc3)cc(-c3ccccc3)c2)cc(-c2cc(-c3ccccc3)cc(-c3ccccc3)c2)c1 Chemical compound Cc1cc(-c2cc(-c3ccccc3)cc(-c3ccccc3)c2)cc(-c2cc(-c3ccccc3)cc(-c3ccccc3)c2)c1 OZBHXHWJZJGBLQ-UHFFFAOYSA-N 0.000 description 1
- JGBRYZVVUGRWOL-UHFFFAOYSA-N Cc1nc(-c2cc(-c3ccccc3)cc(-c3ccccc3)c2)cc(-c2cc(-c3ccccc3)cc(-c3ccccc3)c2)n1 Chemical compound Cc1nc(-c2cc(-c3ccccc3)cc(-c3ccccc3)c2)cc(-c2cc(-c3ccccc3)cc(-c3ccccc3)c2)n1 JGBRYZVVUGRWOL-UHFFFAOYSA-N 0.000 description 1
- WARCRYXKINZHGQ-UHFFFAOYSA-N NNC(c1ccccc1)=O Chemical compound NNC(c1ccccc1)=O WARCRYXKINZHGQ-UHFFFAOYSA-N 0.000 description 1
- AWXGSYPUMWKTBR-UHFFFAOYSA-N c(cc1)cc(c2ccccc22)c1[n]2-c(cc1)ccc1N(c(cc1)ccc1-[n]1c2ccccc2c2c1cccc2)c(cc1)ccc1-[n]1c(cccc2)c2c2c1cccc2 Chemical compound c(cc1)cc(c2ccccc22)c1[n]2-c(cc1)ccc1N(c(cc1)ccc1-[n]1c2ccccc2c2c1cccc2)c(cc1)ccc1-[n]1c(cccc2)c2c2c1cccc2 AWXGSYPUMWKTBR-UHFFFAOYSA-N 0.000 description 1
- SDHNJSIZTIODFW-UHFFFAOYSA-N c(cc1)cc(c2ccccc22)c1[n]2-c(cc1c2c3)ccc1[s]c2ccc3-[n]1c2ccccc2c2ccccc12 Chemical compound c(cc1)cc(c2ccccc22)c1[n]2-c(cc1c2c3)ccc1[s]c2ccc3-[n]1c2ccccc2c2ccccc12 SDHNJSIZTIODFW-UHFFFAOYSA-N 0.000 description 1
- UFWDOFZYKRDHPB-UHFFFAOYSA-N c(cc1)cc(c2ccccc22)c1[n]2-c1cc(-c2nc(-c3cccc(-[n]4c(cccc5)c5c5c4cccc5)c3)ccc2)ccc1 Chemical compound c(cc1)cc(c2ccccc22)c1[n]2-c1cc(-c2nc(-c3cccc(-[n]4c(cccc5)c5c5c4cccc5)c3)ccc2)ccc1 UFWDOFZYKRDHPB-UHFFFAOYSA-N 0.000 description 1
Landscapes
- Electroluminescent Light Sources (AREA)
Description
[1]陽極と、陰極と、前記陽極及び前記陰極の間に設けられた第1の有機層及び第2の有機層と、を有し、
前記第1の有機層が、式(1)で表される金属錯体を含有する層Aであり、
前記第2の有機層が、
式(2)で表される金属錯体から水素原子1個以上を除いた基を有する構成単位を含む高分子化合物、及び、前記高分子化合物の架橋体のうち、少なくとも1種を含有する層B、又は、
式(2)で表される金属錯体及び架橋基を有する化合物の架橋体を含有する層C’である、発光素子。
[式中、
Mは、ロジウム原子、パラジウム原子、イリジウム原子又は白金原子を表す。
n1は1以上の整数を表し、n2は0以上の整数を表し、n1+n2は2又は3である。
Mがロジウム原子又はイリジウム原子の場合、n1+n2は3であり、Mがパラジウム原子又は白金原子の場合、n1+n2は2である。
E1は、炭素原子又は窒素原子を表す。E1が複数存在する場合、それらは同一でも異なっていてもよい。
環Bは、芳香族炭化水素環又は芳香族複素環を表し、これらの環は置換基を有していてもよい。該置換基が複数存在する場合、それらは互いに結合して、それぞれが結合する原子とともに環を形成していてもよい。環Bが複数存在する場合、それらは同一でも異なっていてもよい。
Z1Aは、=N-で表される基又は=C(RZ1A)-で表される基を表す。Z1Aが複数存在する場合、それらは同一であっても異なっていてもよい。RZ1Aは、水素原子、アルキル基、シクロアルキル基、アルコキシ基、シクロアルコキシ基、アリール基、アリールオキシ基、1価の複素環基、置換アミノ基又はハロゲン原子を表し、これらの基は置換基を有していてもよい。
R1は、シクロアルキル基、アルコキシ基、シクロアルコキシ基、アリール基、アリールオキシ基、1価の複素環基、置換アミノ基、ハロゲン原子又は炭素原子数2以上30以下のアルキル基を表し、これらの基は置換基を有していてもよい。R1が複数存在する場合、それらは同一でも異なっていてもよい。
Ar1Aは、式(Ar-1A)で表される基を表す。Ar1Aが複数存在する場合、それらは同一でも異なっていてもよい。
A1-G1-A2は、アニオン性の2座配位子を表す。A1及びA2は、それぞれ独立に、炭素原子、酸素原子又は窒素原子を表し、これらの原子は環を構成する原子であってもよい。G1は、単結合、又は、A1及びA2とともに2座配位子を構成する原子団を表す。A1-G1-A2が複数存在する場合、それらは同一でも異なっていてもよい。]
[式中、
環Aは、芳香族炭化水素環又は芳香族複素環を表し、これらの環は置換基を有していてもよい。該置換基が複数存在する場合、それらは互いに結合して、それぞれが結合する原子とともに環を形成していてもよい。
R2及びR3は、それぞれ独立に、アルキル基、シクロアルキル基、アルコキシ基、シクロアルコキシ基、アリール基、アリールオキシ基、1価の複素環基、置換アミノ基又はハロゲン原子を表し、これらの基は置換基を有していてもよい。]
[式中、
M2は、ロジウム原子、パラジウム原子、イリジウム原子又は白金原子を表す。
n3は1以上の整数を表し、n4は0以上の整数を表し、n3+n4は2又は3である。
M2がロジウム原子又はイリジウム原子の場合、n3+n4は3であり、M2がパラジウム原子又は白金原子の場合、n3+n4は2である。
E4は、炭素原子又は窒素原子を表す。E4が複数存在する場合、それらは同一でも異なっていてもよい。
環L1は、6員の芳香族複素環を表し、この環は置換基を有していてもよい。該置換基が複数存在する場合、それらは互いに結合して、それぞれが結合する原子とともに環を形成していてもよい。環L1が複数存在する場合、それらは同一でも異なっていてもよい。
環L2は、芳香族炭化水素環又は芳香族複素環を表し、これらの環は置換基を有していてもよい。該置換基が複数存在する場合、それらは互いに結合して、それぞれが結合する原子とともに環を形成していてもよい。環L2が複数存在する場合、それらは同一でも異なっていてもよい。
環L1が有していてもよい置換基と環L2が有していてもよい置換基とは、互いに結合して、それぞれが結合する原子とともに環を形成していてもよい。
A3-G2-A4は、アニオン性の2座配位子を表す。A3及びA4は、それぞれ独立に、炭素原子、酸素原子又は窒素原子を表し、これらの原子は環を構成する原子であってもよい。G2は、単結合、又は、A3及びA4とともに2座配位子を構成する原子団を表す。A3-G2-A4が複数存在する場合、それらは同一でも異なっていてもよい。]
[2]前記式(1)で表される金属錯体が、式(1-1)で表される金属錯体である、[1]に記載の発光素子。
[式中、
M、Z1A、n1、n2、R1、Ar1A及びA1-G1-A2は、前記と同じ意味を表す。
環B1は、ベンゼン環、ピリジン環又はジアザベンゼン環を表し、E1B、E2B、E3B及びE4Bは、それぞれ独立に、窒素原子又は炭素原子を表す。E1B、E2B、E3B及びE4Bが複数存在する場合、それらはそれぞれ同一でも異なっていてもよい。E1Bが窒素原子の場合、R1Bは存在しない。E2Bが窒素原子の場合、R2Bは存在しない。E3Bが窒素原子の場合、R3Bは存在しない。E4Bが窒素原子の場合、R4Bは存在しない。
R1B、R2B、R3B及びR4Bは、それぞれ独立に、水素原子、アルキル基、シクロアルキル基、アルコキシ基、シクロアルコキシ基、アリール基、アリールオキシ基、1価の複素環基、置換アミノ基又はハロゲン原子を表し、これらの基は置換基を有していてもよい。R1B、R2B、R3B及びR4Bが複数存在する場合、それらはそれぞれ同一でも異なっていてもよい。R1BとR2B、R2BとR3B、及び、R3BとR4Bは、それぞれ結合して、それぞれが結合する原子とともに環を形成していてもよい。]
[3]陽極と、陰極と、前記陽極及び前記陰極の間に設けられた第1の有機層及び第2の有機層と、を有し、
前記第1の有機層及び前記第2の有機層が、発光層であり、
前記第1の有機層が、式(1’)で表される金属錯体を含有する層A’である、発光素子。
[式中、
Mは、ロジウム原子、パラジウム原子、イリジウム原子又は白金原子を表す。
n1は1以上の整数を表し、n2は0以上の整数を表し、n1+n2は2又は3である。
Mがロジウム原子又はイリジウム原子の場合、n1+n2は3であり、Mがパラジウム原子又は白金原子の場合、n1+n2は2である。
E1は、炭素原子又は窒素原子を表す。E1が複数存在する場合、それらは同一でも異なっていてもよい。
環Bは、芳香族炭化水素環又は芳香族複素環を表し、これらの環は置換基を有していてもよい。該置換基が複数存在する場合、それらは互いに結合して、それぞれが結合する原子とともに環を形成していてもよい。環Bが複数存在する場合、それらは同一でも異なっていてもよい。
Z1Aは、=N-で表される基又は=C(RZ1A)-で表される基を表す。Z1Aが複数存在する場合、それらは同一であっても異なっていてもよい。RZ1Aは、水素原子、アルキル基、シクロアルキル基、アルコキシ基、シクロアルコキシ基、アリール基、アリールオキシ基、1価の複素環基、置換アミノ基又はハロゲン原子を表し、これらの基は置換基を有していてもよい。
R1’は、炭素原子数2以上30以下のアルキル基を表し、該基は置換基を有していてもよい。R1が複数存在する場合、それらは同一でも異なっていてもよい。
Ar1Aは、前記式(Ar-1A)で表される基を表す。Ar1Aが複数存在する場合、それらは同一でも異なっていてもよい。
A1-G1-A2は、アニオン性の2座配位子を表す。A1及びA2は、それぞれ独立に、炭素原子、酸素原子又は窒素原子を表し、これらの原子は環を構成する原子であってもよい。G1は、単結合、又は、A1及びA2とともに2座配位子を構成する原子団を表す。A1-G1-A2が複数存在する場合、それらは同一でも異なっていてもよい。]
[4]前記第2の有機層が、
前記式(2)で表される金属錯体から水素原子1個以上を除いた基を有する構成単位を含む高分子化合物、及び、前記高分子化合物の架橋体のうち、少なくとも1種を含有する層B、又は、
前記式(2)で表される金属錯体を含有する層Cである、[3]に記載の発光素子。
[5]陽極と、陰極と、前記陽極及び前記陰極の間に設けられた第1の有機層及び第2の有機層と、を有し、
前記第1の有機層が、前記式(1’)で表される金属錯体を含有する層A’であり、
前記第2の有機層が、
前記式(2)で表される金属錯体から水素原子1個以上を除いた基を有する構成単位を含む高分子化合物、及び、前記高分子化合物の架橋体のうち、少なくとも1種を含有する層B、又は、
前記式(2)で表される金属錯体を含有する層C
である、発光素子。
[6]前記第2の有機層が、前記層Bであり、
前記高分子化合物が、架橋基を有する構成単位を更に含む、[1]、[2]、[4]及び[5]のいずれかに記載の発光素子。
[7]前記第2の有機層が、前記層Bであり、
前記構成単位が、式(2-1B)で表される構成単位、式(2-2B)で表される構成単位、式(2-3B)で表される構成単位又は式(2-4B)で表される構成単位である、[1]、[2]及び[4]~[6]のいずれかに記載の発光素子。
[式中、
M1Bは、式(2)で表される金属錯体から水素原子1個を除いた基を表す。
LCは、酸素原子、硫黄原子、-N(RA)-、-C(RB)2-、-C(RB)=C(RB)-、-C≡C-、アリーレン基又は2価の複素環基を表し、これらの基は置換基を有していてもよい。RAは、水素原子、アルキル基、シクロアルキル基、アリール基又は1価の複素環基を表し、これらの基は置換基を有していてもよい。RBは、水素原子、アルキル基、シクロアルキル基、アルコキシ基、シクロアルコキシ基、アリール基又は1価の複素環基を表し、これらの基は置換基を有していてもよい。複数存在するRBは、同一でも異なっていてもよく、互いに結合して、それぞれが結合する炭素原子とともに環を形成していてもよい。LCが複数存在する場合、それらは同一でも異なっていてもよい。
nc1は0以上の整数を表す。]
[式中、
M1Bは前記と同じ意味を表す。
Ld及びLeは、それぞれ独立に、酸素原子、硫黄原子、-N(RA)-、-C(RB)2-、-C(RB)=C(RB)-、-C≡C-、アリーレン基又は2価の複素環基を表し、これらの基は置換基を有していてもよい。RA及びRBは、前記と同じ意味を表す。Ld及びLeが複数存在する場合、それらはそれぞれ同一でも異なっていてもよい。
nd1及びne1は、それぞれ独立に、0以上の整数を表す。複数存在するnd1は、同一でも異なっていてもよい。
Ar1Mは、芳香族炭化水素基又は複素環基を表し、これらの基は置換基を有していてもよい。]
[式中、
Ld及びnd1は、前記と同じ意味を表す。
M2Bは、式(2)で表される金属錯体から水素原子2個を除いた基を表す。]
[式中、
Ld及びnd1は、前記と同じ意味を表す。
M3Bは、式(2)で表される金属錯体から水素原子3個を除いた基を表す。]
[8]前記第2の有機層が、前記層B又は前記層C’であり、
前記架橋基が、架橋基A群から選ばれる架橋基である、[1]、[2]又は[6]に記載の発光素子。
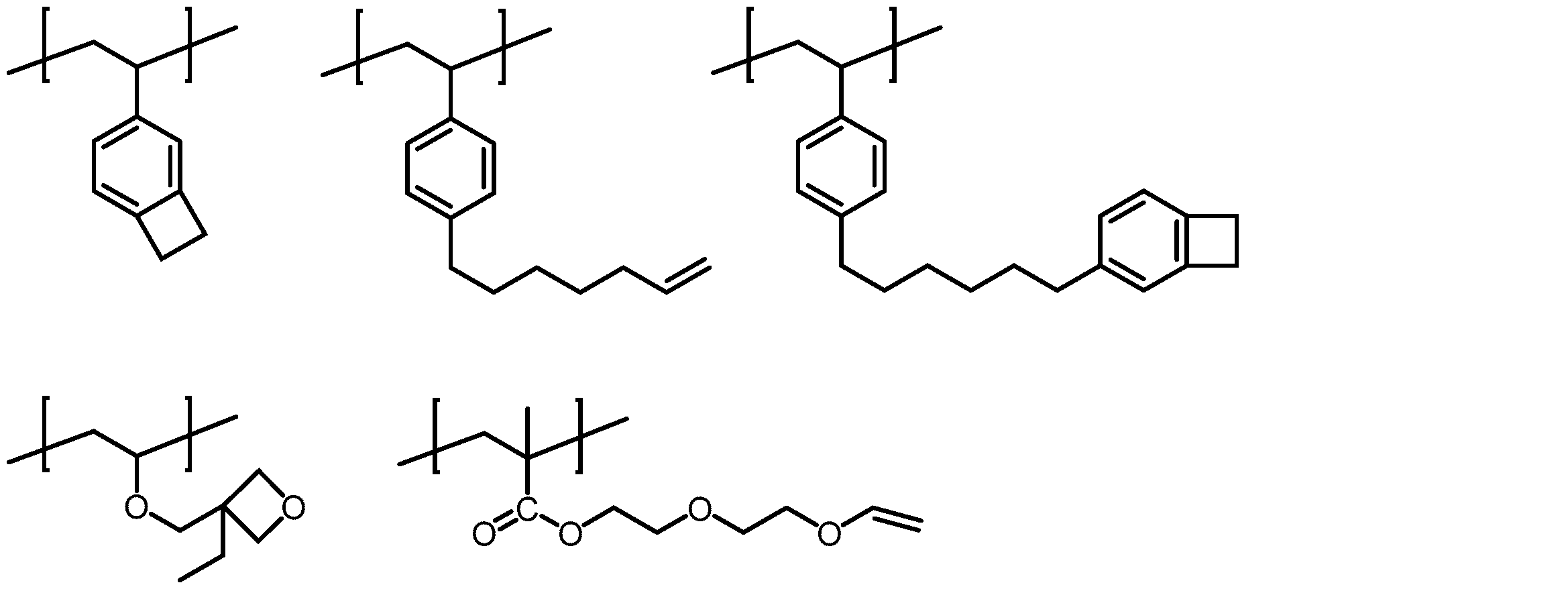
(架橋基A群)
[式中、RXLは、メチレン基、酸素原子又は硫黄原子を表し、nXLは、0~5の整数を表す。RXLが複数存在する場合、それらは同一でも異なっていてもよい。複数存在するnXLは、同一でも異なっていてもよい。*1は結合位置を表す。これらの架橋基は置換基を有していてもよい。]
[9]前記式(Ar-1A)で表される基が、式(Ar-2A)で表される基である、[1]~[8]のいずれかに記載の発光素子。
[式中、R2及びR3は、前記と同じ意味を表す。
環A1は、ベンゼン環、ピリジン環又はジアザベンゼン環を表し、E1A、E2A及びE3Aは、それぞれ独立に、窒素原子又は炭素原子を表す。E1Aが窒素原子の場合、R1Aは存在しない。E2Aが窒素原子の場合、R2Aは存在しない。E3Aが窒素原子の場合、R3Aは存在しない。
R1A、R2A及びR3Aは、それぞれ独立に、水素原子、アルキル基、シクロアルキル基、アルコキシ基、シクロアルコキシ基、アリール基、アリールオキシ基、1価の複素環基、置換アミノ基又はハロゲン原子を表し、これらの基は置換基を有していてもよい。R1AとR2A、及び、R2AとR3Aは、それぞれ結合して、それぞれが結合する原子とともに環を形成していてもよい。]
[10]前記式(2)で表される金属錯体が、式(2-B)で表される金属錯体である、[1]~[9]のいずれかに記載の発光素子。
[式中、
M2、n3、n4及びA3-G2-A4は、前記と同じ意味を表す。
環L1Bは、ピリジン環又はピリミジン環を表し、環L2Bは、ベンゼン環、ピリジン環又はジアザベンゼン環を表し、E11B、E12B、E13B、E14B、E21B、E22B、E23B及びE24Bは、それぞれ独立に、窒素原子又は炭素原子を表す。E11B、E12B、E13B、E14B、E21B、E22B、E23B及びE24Bが複数存在する場合、それらはそれぞれ同一でも異なっていてもよい。E11Bが窒素原子の場合、R11Bは存在しない。E12Bが窒素原子の場合、R12Bは存在しない。E13Bが窒素原子の場合、R13Bは存在しない。E14Bが窒素原子の場合、R14Bは存在しない。E21Bが窒素原子の場合、R21Bは存在しない。E22Bが窒素原子の場合、R22Bは存在しない。E23Bが窒素原子の場合、R23Bは存在しない。E24Bが窒素原子の場合、R24Bは存在しない。
R11B、R12B、R13B、R14B、R21B、R22B、R23B及びR24Bは、それぞれ独立に、水素原子、アルキル基、シクロアルキル基、アルコキシ基、シクロアルコキシ基、アリール基、アリールオキシ基、1価の複素環基、置換アミノ基又はハロゲン原子を表し、これらの基は置換基を有していてもよい。R11B、R12B、R13B、R14B、R21B、R22B、R23B及びR24Bが複数存在する場合、それらはそれぞれ同一でも異なっていてもよい。R11BとR12B、R12BとR13B、R13BとR14B、R11BとR21B、R21BとR22B、R22BとR23B、及び、R23BとR24Bは、それぞれ結合して、それぞれが結合する原子とともに環を形成していてもよい。]
[11]前記式(2-B)で表される金属錯体が、式(2-B1)で表される金属錯体、式(2-B2)で表される金属錯体、式(2-B3)で表される金属錯体、式(2-B4)で表される金属錯体又は式(2-B5)で表される金属錯体である、[10]に記載の発光素子。
[式中、
M2、n3、n4、R11B、R12B、R13B、R14B、R21B、R22B、R23B、R24B及びA3-G2-A4は、前記と同じ意味を表す。
n31及びn32は、それぞれ独立に、1以上の整数を表し、n31+n32は2又は3である。M2がロジウム原子又はイリジウム原子の場合、n31+n32は3であり、M2がパラジウム原子又は白金原子の場合、n31+n32は2である。
R15B、R16B、R17B及びR18Bは、それぞれ独立に、水素原子、アルキル基、シクロアルキル基、アルコキシ基、シクロアルコキシ基、アリール基、アリールオキシ基、1価の複素環基、置換アミノ基又はハロゲン原子を表し、これらの基は置換基を有していてもよい。R15B、R16B、R17B及びR18Bが複数存在する場合、それらはそれぞれ同一でも異なっていてもよい。R15BとR16B、R16BとR17B、及び、R17BとR18Bは、それぞれ結合して、それぞれが結合する原子とともに環を形成していてもよい。]
[12]前記第1の有機層が、式(H-1)で表される化合物、及び/又は、式(Y)で表される構成単位を含む高分子化合物を更に含有する、[1]~[11]のいずれかに記載の発光素子。
[式中、
ArH1及びArH2は、それぞれ独立に、アリール基又は1価の複素環基を表し、これらの基は置換基を有していてもよい。
nH1及びnH2は、それぞれ独立に、0又は1を表す。nH1が複数存在する場合、それらは同一でも異なっていてもよい。複数存在するnH2は、同一でも異なっていてもよい。
nH3は、0以上10以下の整数を表す。
LH1は、アリーレン基、2価の複素環基、又は、-[C(RH11)2]nH11-で表される基を表し、これらの基は置換基を有していてもよい。LH1が複数存在する場合、それらは同一でも異なっていてもよい。nH11は、1以上10以下の整数を表す。RH11は、水素原子、アルキル基、シクロアルキル基、アルコキシ基、シクロアルコキシ基、アリール基又は1価の複素環基を表し、これらの基は置換基を有していてもよい。複数存在するRH11は、同一でも異なっていてもよく、互いに結合して、それぞれが結合する炭素原子とともに環を形成していてもよい。
LH2は、-N(-LH21-RH21)-で表される基を表す。LH2が複数存在する場合、それらは同一でも異なっていてもよい。LH21は、単結合、アリーレン基又は2価の複素環基を表し、これらの基は置換基を有していてもよい。RH21は、水素原子、アルキル基、シクロアルキル基、アリール基又は1価の複素環基を表し、これらの基は置換基を有していてもよい。]
[式中、ArY1は、アリーレン基、2価の複素環基、又は、アリーレン基と2価の複素環基とが直接結合した2価の基を表し、これらの基は置換基を有していてもよい。]
[13]前記第1の有機層が、正孔輸送材料、正孔注入材料、電子輸送材料、電子注入材料、発光材料及び酸化防止剤からなる群より選ばれる少なくとも1種を更に含有する、[1]~[12]のいずれかに記載の発光素子。
[14]前記第1の有機層と前記第2の有機層とが隣接している、[1]~[13]のいずれかに記載の発光素子。
[15]前記第2の有機層が、前記陽極及び前記第1の有機層との間に設けられた層である、[1]~[14]のいずれかに記載の発光素子。
本明細書で共通して用いられる用語は、特記しない限り、以下の意味である。
アルキル基は、置換基を有していてもよい。アルキル基としては、例えば、メチル基、エチル基、プロピル基、イソプロピル基、ブチル基、2-ブチル基、イソブチル基、tert-ブチル基、ペンチル基、イソアミル基、2-エチルブチル基、ヘキシル基、ヘプチル基、オクチル基、2-エチルヘキシル基、3-プロピルヘプチル基、デシル基、3,7-ジメチルオクチル基、2-エチルオクチル基、2-ヘキシルデシル基、ドデシル基等が挙げられる。また、アルキル基は、これらの基における水素原子の一部又は全部が、シクロアルキル基、アルコキシ基、シクロアルコキシ基、アリール基、フッ素原子等で置換された基であってもよい。このようなアルキル基としては、例えば、トリフルオロメチル基、ペンタフルオロエチル基、パーフルオロブチル基、パーフルオロヘキシル基、パーフルオロオクチル基、3-フェニルプロピル基、3-(4-メチルフェニル)プロピル基、3-(3,5-ジ-ヘキシルフェニル)プロピル基、6-エチルオキシヘキシル基が挙げられる。
「シクロアルキル基」の炭素原子数は、置換基の炭素原子数を含めないで、通常3~50であり、好ましくは3~30であり、より好ましくは4~20である。
シクロアルキル基は、置換基を有していてもよい。シクロアルキル基としては、例えば、シクロヘキシル基、シクロヘキシルメチル基、シクロヘキシルエチル基が挙げられる。
アリール基は、置換基を有していてもよい。アリール基としては、例えば、フェニル基、1-ナフチル基、2-ナフチル基、1-アントラセニル基、2-アントラセニル基、9-アントラセニル基、1-ピレニル基、2-ピレニル基、4-ピレニル基、2-フルオレニル基、3-フルオレニル基、4-フルオレニル基、2-フェニルフェニル基、3-フェニルフェニル基、4-フェニルフェニル基等が挙げられる。また、アリール基は、これらの基における水素原子の一部又は全部が、アルキル基、シクロアルキル基、アルコキシ基、シクロアルコキシ基、アリール基、フッ素原子等で置換された基であってもよい。
アルコキシ基は、置換基を有していてもよい。アルコキシ基としては、例えば、メトキシ基、エトキシ基、プロピルオキシ基、イソプロピルオキシ基、ブチルオキシ基、イソブチルオキシ基、tert-ブチルオキシ基、ペンチルオキシ基、ヘキシルオキシ基、ヘプチルオキシ基、オクチルオキシ基、2-エチルヘキシルオキシ基、ノニルオキシ基、デシルオキシ基、3,7-ジメチルオクチルオキシ基、ラウリルオキシ基等が挙げられる。また、アルコキシ基は、これらの基における水素原子の一部又は全部が、シクロアルキル基、アルコキシ基、シクロアルコキシ基、アリール基、フッ素原子等で置換された基であってもよい。
「シクロアルコキシ基」の炭素原子数は、置換基の炭素原子数を含めないで、通常3~40であり、好ましくは4~10である。
シクロアルコキシ基は、置換基を有していてもよい。シクロアルコキシ基としては、例えば、シクロヘキシルオキシ基が挙げられる。
アリールオキシ基は、置換基を有していてもよい。アリールオキシ基としては、例えば、フェノキシ基、1-ナフチルオキシ基、2-ナフチルオキシ基、1-アントラセニルオキシ基、9-アントラセニルオキシ基、1-ピレニルオキシ基等が挙げられる。また、アリールオキシ基は、これらの基における水素原子の一部又は全部が、アルキル基、シクロアルキル基、アルコキシ基、シクロアルコキシ基、フッ素原子等で置換された基であってもよい。
「芳香族複素環式化合物」は、オキサジアゾール、チアジアゾール、チアゾール、オキサゾール、チオフェン、ピロール、ホスホール、フラン、ピリジン、ピラジン、ピリミジン、トリアジン、ピリダジン、キノリン、イソキノリン、カルバゾール、ジベンゾホスホール等の複素環自体が芳香族性を示す化合物、及び、フェノキサジン、フェノチアジン、ジベンゾボロール、ジベンゾシロール、ベンゾピラン等の複素環自体は芳香族性を示さなくとも、複素環に芳香環が縮環されている化合物を意味する。
1価の複素環基は、置換基を有していてもよい。1価の複素環基としては、例えば、チエニル基、ピロリル基、フリル基、ピリジニル基、ピペリジニル基、キノリニル基、イソキノリニル基、ピリミジニル基、トリアジニル基等が挙げられる。また、1価の複素環基は、これらの基における水素原子の一部又は全部が、アルキル基、シクロアルキル基、アルコキシ基、シクロアルコキシ基等で置換された基であってもよい。
置換アミノ基としては、二置換アミノ基が好ましい。二置換アミノ基としては、例えば、ジアルキルアミノ基、ジシクロアルキルアミノ基及びジアリールアミノ基が挙げられる。
二置換アミノ基としては、例えば、ジメチルアミノ基、ジエチルアミノ基、ジフェニルアミノ基、ビス(4-メチルフェニル)アミノ基、ビス(4-tert-ブチルフェニル)アミノ基、ビス(3,5-ジ-tert-ブチルフェニル)アミノ基が挙げられる。
「シクロアルケニル基」の炭素原子数は、置換基の炭素原子数を含めないで、通常3~30であり、好ましくは4~20である。
アルケニル基及びシクロアルケニル基は、置換基を有していてもよい。アルケニル基としては、例えば、ビニル基、1-プロペニル基、2-プロペニル基、2-ブテニル基、3-ブテニル基、3-ペンテニル基、4-ペンテニル基、1-ヘキセニル基、5-ヘキセニル基、7-オクテニル基、及び、これらの基における水素原子の一部又は全部が置換基で置換された基が挙げられる。シクロアルケニル基としては、例えば、シクロヘキセニル基、シクロヘキサジエニル基、シクロオクタトリエニル基、ノルボルニレニル基、及び、これらの基における水素原子の一部又は全部が置換基で置換された基が挙げられる。
「シクロアルキニル基」の炭素原子数は、置換基の炭素原子を含めないで、通常4~30であり、好ましくは4~20である。
アルキニル基及びシクロアルキニル基は、置換基を有していてもよい。アルキニル基としては、例えば、エチニル基、1-プロピニル基、2-プロピニル基、2-ブチニル基、3-ブチニル基、3-ペンチニル基、4-ペンチニル基、1-ヘキシニル基、5-ヘキシニル基、及び、これらの基における水素原子の一部又は全部が置換基で置換された基が挙げられる。シクロアルキニル基としては、例えば、シクロオクチニル基等が挙げられる。
アリーレン基は、置換基を有していてもよい。アリーレン基としては、例えば、フェニレン基、ナフタレンジイル基、アントラセンジイル基、フェナントレンジイル基、ジヒドロフェナントレンジイル基、ナフタセンジイル基、フルオレンジイル基、ピレンジイル基、ペリレンジイル基、クリセンジイル基、及び、これらの基における水素原子の一部又は全部が置換基で置換された基が挙げられる。アリーレン基は、好ましくは、式(A-1)~式(A-20)で表される基である。アリーレン基は、これらの基が複数結合した基を含む。
2価の複素環基は、置換基を有していてもよい。2価の複素環基としては、例えば、ピリジン、ジアザベンゼン、トリアジン、アザナフタレン、ジアザナフタレン、カルバゾール、ジベンゾフラン、ジベンゾチオフェン、ジベンゾシロール、フェノキサジン、フェノチアジン、アクリジン、ジヒドロアクリジン、フラン、チオフェン、アゾール、ジアゾール又はトリアゾールから、環を構成する炭素原子又はヘテロ原子に直接結合している水素原子のうち2個の水素原子を除いた2価の基が挙げられる。また、2価の複素環基は、これらの基における水素原子の一部又は全部が置換基で置換された基であってもよい。2価の複素環基は、好ましくは、式(AA-1)~式(AA-34)で表される基である。2価の複素環基は、これらの基が複数結合した基を含む。
本実施形態の第1の発光素子は、陽極と、陰極と、陽極及び陰極の間に設けられた第1の有機層及び第2の有機層と、を有する発光素子である。
第1の有機層は、式(1)で表される金属錯体を含有する層Aである。層Aは、式(1)で表される金属錯体の1種を単独で含有していてもよく、2種以上を含有していてもよい。式(1)で表される金属錯体を含有する層Aは、式(1’)で表される金属錯体を含有する層A’であることが好ましい。すなわち、式(1)で表される金属錯体は式(1’)で表される金属錯体であることが好ましい。層A’は、式(1’)で表される金属錯体の1種を単独で含有していてもよく、2種以上を含有していてもよい。
式(1)で表される金属錯体及び式(1’)で表される金属錯体は、通常、室温(25℃)で燐光発光性を示す金属錯体であり、好ましくは、室温で三重項励起状態からの発光を示す金属錯体である。
環Bにおける芳香族炭化水素環としては、ベンゼン環、ナフタレン環、インデン環、フルオレン環、フェナントレン環、ジヒドロフェナントレン環及びこれらの環が縮合した環が挙げられる。環Bにおける芳香族炭化水素環は、好ましくは、ベンゼン環、ナフタレン環、インデン環、フルオレン環、フェナントレン環又はジヒドロフェナントレン環であり、より好ましくは、ベンゼン環、フルオレン環又はジヒドロフェナントレン環であり、更に好ましくは、ベンゼン環であり、これらの環は置換基を有していてもよい。
環Bにおける芳香族複素環としては、ピロール環、ジアゾール環、フラン環、チオフェン環、ピリジン環、ジアザベンゼン環、アザナフタレン環、ジアザナフタレン環、インドール環、ベンゾジアゾール環、ベンゾフラン環、ベンゾチオフェン環、カルバゾール環、ジベンゾフラン環、ジベンゾチオフェン環及びこれらの環に芳香環が縮合した環が挙げられる。環Bにおける芳香族複素環は、好ましくは、ピロール環、ジアゾール環、フラン環、チオフェン環、ピリジン環、ジアザベンゼン環、アザナフタレン環、ジアザナフタレン環、インドール環、ベンゾジアゾール環、ベンゾフラン環、ベンゾチオフェン環、カルバゾール環、ジベンゾフラン環又はジベンゾチオフェン環であり、より好ましくは、ピリジン環、ジアザベンゼン環、カルバゾール環、ジベンゾフラン環又はジベンゾチオフェン環であり、更に好ましくは、ピリジン環又はジアザベンゼン環であり、これらの環は置換基を有していてもよい。
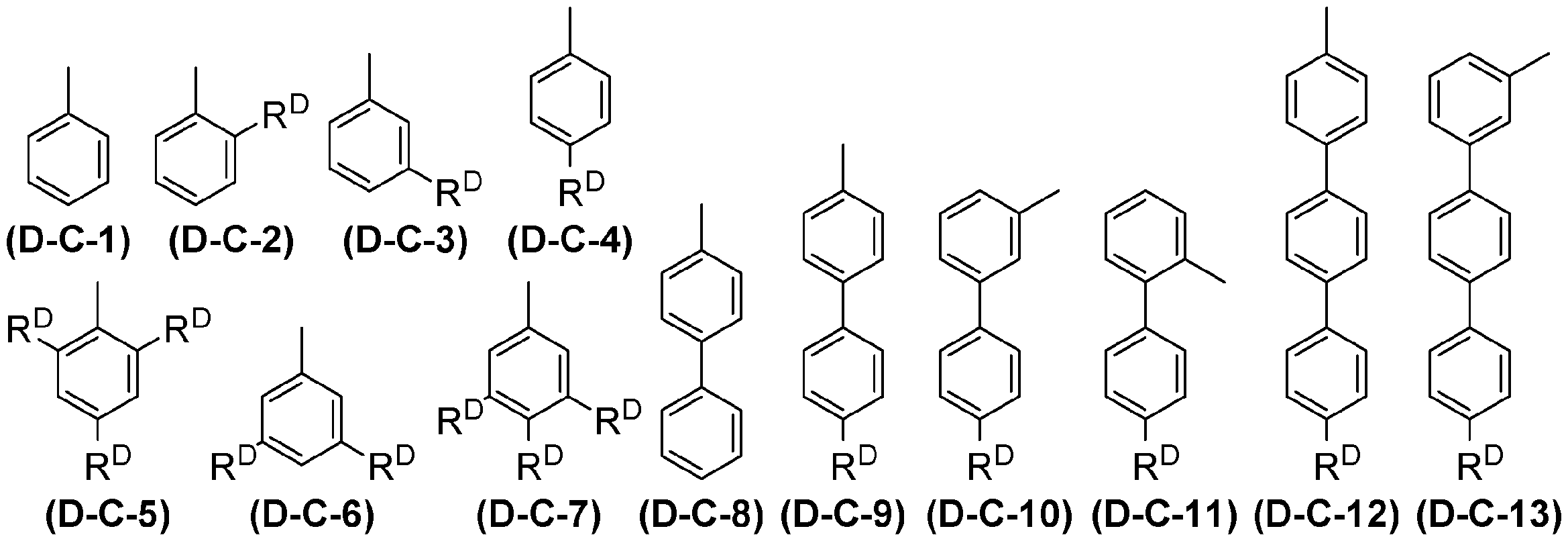
mDA1、mDA2及びmDA3は、それぞれ独立に、0以上の整数を表す。
GDAは、窒素原子、芳香族炭化水素基又は複素環基を表し、これらの基は置換基を有していてもよい。
ArDA1、ArDA2及びArDA3は、それぞれ独立に、アリーレン基又は2価の複素環基を表し、これらの基は置換基を有していてもよい。ArDA1、ArDA2及びArDA3が複数存在する場合、それらはそれぞれ同一でも異なっていてもよい。
TDAは、アリール基又は1価の複素環基を表し、これらの基は置換基を有していてもよい。複数存在するTDAは、同一でも異なっていてもよい。
mDA1、mDA2、mDA3、mDA4、mDA5、mDA6及びmDA7は、それぞれ独立に、0以上の整数を表す。
GDAは、窒素原子、芳香族炭化水素基又は複素環基を表し、これらの基は置換基を有していてもよい。複数存在するGDAは、同一でも異なっていてもよい。
ArDA1、ArDA2、ArDA3、ArDA4、ArDA5、ArDA6及びArDA7は、それぞれ独立に、アリーレン基又は2価の複素環基を表し、これらの基は置換基を有していてもよい。ArDA1、ArDA2、ArDA3、ArDA4、ArDA5、ArDA6及びArDA7が複数存在する場合、それらはそれぞれ同一でも異なっていてもよい。
TDAは、アリール基又は1価の複素環基を表し、これらの基は置換基を有していてもよい。複数存在するTDAは、同一でも異なっていてもよい。
mDA1は、0以上の整数を表す。
ArDA1は、アリーレン基又は2価の複素環基を表し、これらの基は置換基を有していてもよい。ArDA1が複数存在する場合、それらは同一でも異なっていてもよい。
TDAは、アリール基又は1価の複素環基を表し、これらの基は置換基を有していてもよい。
*は、式(D-A)におけるArDA1、式(D-B)におけるArDA1、式(D-B)におけるArDA2、又は、式(D-B)におけるArDA3との結合を表す。
**は、式(D-A)におけるArDA2、式(D-B)におけるArDA2、式(D-B)におけるArDA4、又は、式(D-B)におけるArDA6との結合を表す。
***は、式(D-A)におけるArDA3、式(D-B)におけるArDA3、式(D-B)におけるArDA5、又は、式(D-B)におけるArDA7との結合を表す。
RDAは、水素原子、アルキル基、シクロアルキル基、アルコキシ基、シクロアルコキシ基、アリール基又は1価の複素環基を表し、これらの基は更に置換基を有していてもよい。RDAが複数存在する場合、それらは同一でも異なっていてもよい。
RDAは前記と同じ意味を表す。
RDBは、水素原子、アルキル基、シクロアルキル基、アリール基又は1価の複素環基を表し、これらの基は置換基を有していてもよい。RDBが複数存在する場合、それらは同一でも異なっていてもよい。
Rp1、Rp2、Rp3及びRp4は、それぞれ独立に、アルキル基、シクロアルキル基、アルコキシ基、シクロアルコキシ基又はハロゲン原子を表す。Rp1、Rp2及びRp4が複数存在する場合、それらはそれぞれ同一であっても異なっていてもよい。
np1は、0~5の整数を表し、np2は0~3の整数を表し、np3は0又は1を表し、np4は0~4の整数を表す。複数存在するnp1は、同一でも異なっていてもよい。
Rp1、Rp2及びRp3は、それぞれ独立に、アルキル基、シクロアルキル基、アルコキシ基、シクロアルコキシ基又はハロゲン原子を表す。Rp1及びRp2が複数存在する場合、それらはそれぞれ同一でも異なっていてもよい。
np1は0~5の整数を表し、np2は0~3の整数を表し、np3は0又は1を表す。np1及びnp2が複数存在する場合、それらはそれぞれ同一でも異なっていてもよい。
Rp4、Rp5及びRp6は、それぞれ独立に、アルキル基、シクロアルキル基、アルコキシ基、シクロアルコキシ基又はハロゲン原子を表す。Rp4、Rp5及びRp6が複数存在する場合、それらはそれぞれ同一であっても異なっていてもよい。
np4は、0~4の整数を表し、np5は0~5の整数を表し、np6は0~5の整数を表す。
すなわち、R1は、R1’であることが好ましい。
環Aにおける芳香族炭化水素環の例及び好ましい範囲は、環Bにおける芳香族炭化水素環の例及び好ましい範囲と同じである。環Aにおける芳香族複素環の例及び好ましい範囲は、環Bにおける芳香族炭化水素環の例及び好ましい範囲と同じである。
R2Aは、特に好ましくは、水素原子、アルキル基又はアリール基であり、とりわけ好ましくは、アルキル基又はアリール基であり、殊更に好ましくは、アルキル基であり、これらの基は置換基を有していてもよい。
環A1がジアザベンゼン環である場合、E1A及びE3Aが窒素原子であるピリミジン環が好ましい。
環A1は、ベンゼン環が好ましい。
A1-G1-A2で表されるアニオン性の2座配位子としては、例えば、下記式で表される配位子が挙げられる。但し、A1-G1-A2で表されるアニオン性の2座配位子は、添え字n1でその数を定義されている配位子とは異なる。
*は、Mと結合する部位を表す。
RL1は、水素原子、アルキル基、シクロアルキル基、アリール基、1価の複素環基又はハロゲン原子を表し、これらの基は置換基を有していてもよい。複数存在するRL1は、同一でも異なっていてもよい。
RL2は、アルキル基、シクロアルキル基、アリール基、1価の複素環基又はハロゲン原子を表し、これらの基は置換基を有していてもよい。
式(1)で表される金属錯体は、本実施形態の発光素子の外部量子効率がより優れるので、好ましくは、式(1-1)で表される金属錯体である。
式(1’)で表される金属錯体は、本実施形態の発光素子の外部量子効率がより優れるので、好ましくは、式(1’-1)で表される金属錯体である。
R2Bは、特に好ましくは、水素原子、アルキル基又はアリール基であり、とりわけ好ましくは、水素原子又はアリール基であり、殊更に好ましくは、水素原子であり、これらの基は更に置換基を有していてもよい。
環B1がジアザベンゼン環である場合、環B1は、E2B及びE4Bが窒素原子であるピリミジン環、又は、E1B及びE3Bが窒素原子であるピリミジン環であることが好ましく、E2B及びE4Bが窒素原子であるピリミジン環であることがより好ましい。
環B1は、ベンゼン環であることが好ましい。
式(1’-1)で表される金属錯体は、本実施形態の発光素子の外部量子効率がより優れるので、式(1’-2)で表される金属錯体であることが好ましい。
ZAは、-CH=で表される基又は-N=で表される基を表す。ZAが複数存在する場合、それらは同一でも異なっていてもよい。ZAは、好ましくは-N=で表される基である。
ZBは、-O-で表される基又は-S-で表される基を表す。
式(1)で表される金属錯体は、例えば、配位子となる化合物と金属化合物とを反応させる方法により製造することができる。必要に応じて、金属錯体の配位子の官能基変換反応を行ってもよい。
n1’は、1又は2を表す。Mがロジウム原子又はイリジウム原子の場合、n1’は2であり、Mがパラジウム原子又は白金原子の場合、n1’は1である。
本実施形態の発光素子の外部量子効率がより優れるので、第1の有機層は、式(1)又は式(1’)で表される金属錯体と、正孔注入性、正孔輸送性、電子注入性及び電子輸送性のうちの少なくとも1つの機能を有するホスト材料とを含有する層であることが好ましい。第1の有機層は、ホスト材料の1種を単独で含有していてもよく、2種以上を含有していてもよい。
ホスト材料として好ましい低分子化合物(以下、「低分子ホスト」と言う。)に関して説明する。
nH3は、通常、0以上10以下の整数であり、好ましくは0以上5以下の整数であり、更に好ましくは1以上3以下の整数であり、特に好ましくは1である。
nH11は、好ましくは1以上5以下の整数であり、より好ましく1以上3以下の整数であり、更に好ましく1である。
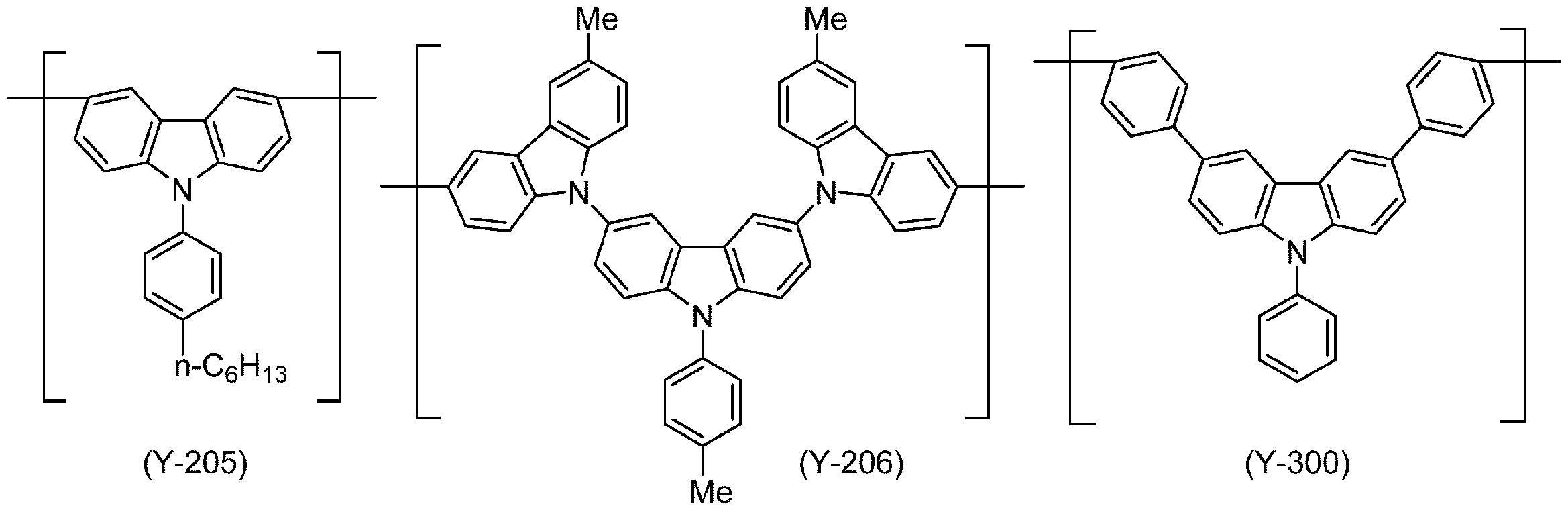
ホスト化合物として好ましい高分子化合物(以下、「高分子ホスト」と言う。)は、好ましくは、式(Y)で表される構成単位を含む高分子化合物である。
aX1及びaX2は、それぞれ独立に、0以上の整数を表す。
ArX1及びArX3は、それぞれ独立に、アリーレン基又は2価の複素環基を表し、これらの基は置換基を有していてもよい。
ArX2及びArX4は、それぞれ独立に、アリーレン基、2価の複素環基、又は、アリーレン基と2価の複素環基とが直接結合した2価の基を表し、これらの基は置換基を有していてもよい。ArX2及びArX4が複数存在する場合、それらは同一でも異なっていてもよい。
RX1、RX2及びRX3は、それぞれ独立に、水素原子、アルキル基、シクロアルキル基、アリール基又は1価の複素環基を表し、これらの基は置換基を有していてもよい。RX2及びRX3が複数存在する場合、それらは同一でも異なっていてもよい。
aX2は、本実施形態の発光素子の外部量子効率がより優れるので、好ましくは2以下であり、より好ましくは0である。
高分子ホストは、ケミカルレビュー(Chem.Rev.),第109巻,897-1091頁(2009年)等に記載の公知の重合方法を用いて製造することができ、Suzuki反応、Yamamoto反応、Buchwald反応、Stille反応、Negishi反応及びKumada反応等の遷移金属触媒を用いるカップリング反応により重合させる方法が例示される。
第1の有機層は、式(1)又は式(1’)で表される金属錯体と、前述のホスト材料、正孔輸送材料、正孔注入材料、電子輸送材料、電子注入材料、発光材料(但し、式(1)で表される金属錯体とは異なる。)及び酸化防止剤からなる群から選ばれる少なくとも1種とを含む組成物(以下、「第1の組成物」ともいう。)を含有する層であってもよい。
正孔輸送材料は、低分子化合物と高分子化合物とに分類され、好ましくは高分子化合物である。正孔輸送材料は、架橋基を有していてもよい。
電子輸送材料は、低分子化合物と高分子化合物とに分類される。電子輸送材料は、架橋基を有していてもよい。
正孔注入材料及び電子注入材料は、各々、低分子化合物と高分子化合物とに分類される。正孔注入材料及び電子注入材料は、架橋基を有していてもよい。
正孔注入材料又は電子注入材料が導電性高分子を含む場合、導電性高分子の電気伝導度は、好ましくは、1×10-5S/cm~1×103S/cmである。導電性高分子の電気伝導度をかかる範囲とするために、導電性高分子に適量のイオンをドープすることができる。
発光材料(但し、式(1)で表される金属錯体とは異なる。)は、低分子化合物と高分子化合物とに分類される。発光材料は、架橋基を有していてもよい。
酸化防止剤は、例えば、式(1)又は式(1’)で表される金属錯体を溶解可能な少なくとも一種の溶媒に可溶であり、発光及び電荷輸送を阻害しない化合物であることが好ましい。酸化防止剤としては、例えば、フェノール系酸化防止剤、リン系酸化防止剤が挙げられる。
式(1)又は式(1’)で表される金属錯体と、溶媒とを含有する組成物(以下、「第1のインク」ともいう。)は、スピンコート法、キャスティング法、マイクログラビアコート法、グラビアコート法、バーコート法、ロールコート法、ワイヤーバーコート法、ディップコート法、スプレーコート法、スクリーン印刷法、フレキソ印刷法、オフセット印刷法、インクジェット印刷法、キャピラリーコート法、ノズルコート法等の湿式法に好適に使用することができる。
次に、第2の有機層の好ましい実施形態の1つである層Bについて説明する。
層Bは、式(2)で表される金属錯体から、該金属錯体を構成する炭素原子又はヘテロ原子に直接結合する1個以上の水素原子を取り除いた基を有する構成単位(以下、「金属錯体構成単位」ともいう。)を含む高分子化合物(以下、「層Bの高分子化合物」ともいう。)、及び、層Bの高分子化合物の架橋体のうち、少なくとも1種を含有する層である。
層Bにおいて、層Bの高分子化合物及び層Bの高分子化合物の架橋体は、それぞれ、1種単独で含有されていても、2種以上含有されていてもよい。
式(2)で表される金属錯体は、通常、室温(25℃)で燐光発光性を示す金属錯体であり、好ましくは、室温で三重項励起状態からの発光を示す金属錯体である。
環L1としては、例えば、ピリジン環、ジアザベンゼン環、キノリン環及びイソキノリン環が挙げられ、ピリジン環、ピリミジン環、キノリン環又はイソキノリン環が好ましく、ピリジン環、キノリン環又はイソキノリン環がより好ましく、ピリジン環又はイソキノリン環が更に好ましく、ピリジン環が特に好ましく、これらの環は置換基を有していてもよい。
環L1及び環L2が有していてもよい置換基における1価の複素環基の例及び好ましい範囲は、Bが有していてもよい置換基における1価の複素環基の例及び好ましい範囲と同じである。
環L1及び環L2が有していてもよい置換基における置換アミノ基の例及び好ましい範囲は、Bが有していてもよい置換基における置換アミノ基の例及び好ましい範囲と同じである。
環L2が有していてもよい置換基が複数存在する場合、それらは互いに結合して、それぞれが結合する原子とともに環を形成していてもよいが、環を形成しないことが好ましい。
環L1が有していてもよい置換基と、環L2が有していてもよい置換基とは、互いに結合して、それぞれが結合する原子とともに環を形成していてもよいが、環を形成しないことが好ましい。
式(2)で表される金属錯体は、本実施形態の発光素子の外部量子効率がより優れるので、式(2-B)で表される金属錯体であることが好ましい。
環L1Bは、ピリジン環であることが好ましい。
環L2Bがジアザベンゼン環である場合、E21B及びE23Bが窒素原子であるピリミジン環、又は、E22B及びE24Bが窒素原子であるピリミジン環が好ましく、E22B及びE24Bが窒素原子であるピリミジン環がより好ましい。
環L2Bは、ベンゼン環であることが好ましい。
また、上記以外の入手方法として、例えば、「Journal of the American Chemical Society,Vol.107,1431-1432(1985)」、「Journal of the American Chemical Society,Vol.106,6647-6653(1984)」、特表2004-530254号公報、特開2008-179617号公報、特開2011-105701号公報、特表2007-504272号公報、国際公開第2006/121811号、特開2013-147450号公報に記載されている方法に従って合成することができる。
金属錯体構成単位は、本実施形態の発光素子の外部量子効率が優れ、かつ、合成が容易なため、好ましくは、式(2)で表される金属錯体から1個以上5個以下の水素原子を除いた基を含む構成単位であり、より好ましくは、式(2)で表される金属錯体から1個以上3個以下の水素原子を除いた基を含む構成単位であり、更に好ましくは式(2-1B)で表される構成単位、式(2-2B)で表される構成単位、式(2-3B)で表される構成単位又は式(2-4B)で表される構成単位であり、特に好ましくは式(2-1B)で表される構成単位、式(2-2B)で表される構成単位又は式(2-3B)で表される構成単位であり、とりわけ好ましくは式(2-3B)で表される構成単位である。
RAは、アリール基又は1価の複素環基であることが好ましく、アリール基であることがより好ましく、これらの基は置換基を有していてもよい。
M2、E4、環L1、環L2及びA3-G2-A4は、前記と同じ意味を表す。
環L11は、6員の芳香族複素環を表し、これらの環は置換基を有していてもよい。該置換基が複数存在する場合、それらは同一でも異なっていてもよく、互いに結合して、それぞれが結合する原子とともに環を形成していてもよい。
環L12は、芳香族炭化水素環又は芳香族複素環を表し、これらの環は置換基を有していてもよい。該置換基が複数存在する場合、それらは同一でも異なっていてもよく、互いに結合して、それぞれが結合する原子とともに環を形成していてもよい。
但し、環L11及び環L12の一方は、1つの結合手を有する。
n11及びn12は、それぞれ独立に、0以上の整数を表す。但し、n11+n12は1又は2である。M2がロジウム原子又はイリジウム原子の場合、n11+n12は2であり、M2がパラジウム原子又は白金原子の場合、n11+n12は1である。
Ldは、-C(RB)2-、アリーレン基又は2価の複素環基であることが好ましく、アリーレン基又は2価の複素環基であることがより好ましく、アリーレン基であることが更に好ましく、式(A-1)又は(A-2)で表される基であることが特に好ましく、これらの基は置換基を有していてもよい。
M2Bは、式(BM-2)又は(BM-3)で表される基であることがより好ましく、式(BM-2)で表される基であることが更に好ましい。
M2、E4、環L1、環L2、環L11、環L12及びA3-G2-A4は前記と同じ意味を表す。複数存在する環L11は、同一でも異なっていてもよい。複数存在する環L12は、同一でも異なっていてもよい。
n13及びn14は、それぞれ独立に、0以上の整数を表す。但し、n13+n14は0又は1である。M2がロジウム原子又はイリジウム原子の場合、n13+n14は1であり、M2がパラジウム原子又は白金原子の場合、n13+n14は0である。
M2、E4、環L1、環L2、A3-G2-A4、n11及びn12は、前記と同じ意味を表す。
環L13は、6員の芳香族複素環を表し、これらの環は置換基を有していてもよい。該置換基が複数存在する場合、それらは同一でも異なっていてもよく、互いに結合して、それぞれが結合する原子とともに環を形成していてもよい。
環L14は、芳香族炭化水素環又は芳香族複素環を表し、これらの環は置換基を有していてもよい。該置換基が複数存在する場合、それらは同一でも異なっていてもよく、互いに結合して、それぞれが結合する原子とともに環を形成していてもよい。
但し、環L13及び環L14の一方は2つの結合手を有するか、又は、環L13及び環L14は、それぞれ、結合手を1つずつ有する。
M3Bは、式(BM-4)で表される基であることが好ましい。
M2、E4、環L11、環L12、環L13及び環L14は、前記と同じ意味を表す。
n15は0又は1を表す。n16は1又は3を表す。但し、M2がロジウム原子又はイリジウム原子の場合、n15は0であり、かつ、n16は3である。M2がパラジウム原子又は白金原子の場合、n15は1であり、かつ、n16は1である。
RDは、前記と同じ意味を表す。
Deは式(D-A)、(D-B)又は(D-C)で表される基を表す。
すなわち、層Bの高分子化合物の架橋体は、層B’の高分子化合物の架橋体であることが好ましい。
層B’の高分子化合物が式(Y)で表される構成単位を含み、ArY1がアリーレン基である場合、層B’の高分子化合物に含まれる式(Y)で表される構成単位は、本実施形態の発光素子の輝度寿命がより優れるので、層B’の高分子化合物に含まれる構成単位の合計量に対して、好ましくは0.5~90モル%であり、より好ましくは30~80モル%である。
層B’の高分子化合物が式(Y)で表される構成単位を含み、ArY1が2価の複素環基、又は、アリーレン基と2価の複素環基とが直接結合した2価の基である場合、層B’の高分子化合物に含まれる式(Y)で表される構成単位は、本実施形態の発光素子の電荷輸送性がより優れるので、層B’の高分子化合物に含まれる構成単位の合計量に対して、好ましくは0.5~50モル%であり、より好ましくは3~30モル%である。
架橋基を有する構成単位において、架橋基は、本実施形態の発光素子の外部量子効率が優れるので、架橋基A群から選ばれる架橋基であることが好ましい。
nAは0~5の整数を表し、nは1又は2を表す。nAが複数存在する場合、それらは同一でも異なっていてもよい。
Ar3は、芳香族炭化水素基又は複素環基を表し、これらの基は置換基を有していてもよい。
LAは、アルキレン基、シクロアルキレン基、アリーレン基、2価の複素環基、-NR’-で表される基、酸素原子又は硫黄原子を表し、これらの基は置換基を有していてもよい。R’は、水素原子、アルキル基、シクロアルキル基、アリール基又は1価の複素環基を表し、これらの基は置換基を有していてもよい。LAが複数存在する場合、それらは同一でも異なっていてもよい。
Xは、架橋基A群から選ばれる架橋基を表す。Xが複数存在する場合、それらは同一でも異なっていてもよい。
Ar3で表される芳香族炭化水素基のn個の置換基を除いたアリーレン基部分としては、好ましくは、式(A-1)~式(A-20)で表される基であり、より好ましくは、式(A-1)、式(A-2)、式(A-6)~式(A-10)、式(A-19)又は式(A-20)で表される基であり、さらに好ましくは、式(A-1)、式(A-2)、式(A-7)、式(A-9)又は式(A-19)で表される基であり、これらの基は置換基を有していてもよい。
Ar3で表される複素環基のn個の置換基を除いた2価の複素環基部分としては、好ましくは、式(AA-1)~式(AA-34)で表される基である。
LAで表されるシクロアルキレン基の炭素原子数は、置換基の炭素原子数を含めないで、通常3~20である。
アルキレン基及びシクロアルキレン基としては、例えば、メチレン基、エチレン基、プロピレン基、ブチレン基、ヘキシレン基、シクロヘキシレン基、オクチレン基が挙げられ、これらの基は置換基を有していてもよい。
式(Z)で表される構成単位は、層B’の高分子化合物中に、1種のみ含まれていてもよく、2種以上含まれていてもよい。
mAは0~5の整数を表し、mは1~4の整数を表し、cは0又は1の整数を表す。mAが複数存在する場合、それらは同一でも異なっていてもよい。
Ar5は、芳香族炭化水素基、複素環基、又は、芳香族炭化水素環と複素環とが直接結合した基を表し、これらの基は置換基を有していてもよい。
Ar4及びAr6は、それぞれ独立に、アリーレン基又は2価の複素環基を表し、これらの基は置換基を有していてもよい。
Ar4、Ar5及びAr6はそれぞれ、該基が結合している窒素原子に結合している該基以外の基と、直接結合又は酸素原子若しくは硫黄原子を介して結合して、環を形成していてもよい。
KAは、アルキレン基、シクロアルキレン基、アリーレン基、2価の複素環基、-NR’-で表される基、酸素原子又は硫黄原子を表し、これらの基は置換基を有していてもよい。R’は、水素原子、アルキル基、シクロアルキル基、アリール基又は1価の複素環基を表し、これらの基は置換基を有していてもよい。KAが複数存在する場合、それらは同一でも異なっていてもよい。
X’は、架橋基A群から選ばれる架橋基、水素原子、アルキル基、シクロアルキル基、アリール基又は1価の複素環基を表し、これらの基は置換基を有していてもよい。X’が複数存在する場合、それらは同一でも異なっていてもよい。但し、少なくとも1つのX’は、架橋基A群から選ばれる架橋基である。
式(Z)で表される構成単位としては、例えば、式(Z-1)~式(Z-30)で表される構成単位が挙げられ、式(Z’)で表される構成単位としては、例えば、式(Z’-1)~式(Z’-9)で表される構成単位が挙げられる。これらの中でも、層B’の高分子化合物の架橋性が優れるので、好ましくは式(Z-1)~式(Z-30)で表される構成単位であり、より好ましくは式(Z-1)~式(Z-15)、式(Z-19)、式(Z-20)、式(Z-23)、式(Z-25)又は式(Z-30)で表される構成単位であり、更に好ましくは式(Z-1)~式(Z-9)又は式(Z-30)で表される構成単位である。
層Bの高分子化合物及び層B’の高分子化合物は、前述の高分子ホストの製造方法と同様の方法で製造することができる。上記以外の製造方法として、例えば、特開2003-171659号公報、国際公開第2006/003000号、特開2010-43243号公報、特開2011-105701号公報、国際公開第2013/021180号、特開2015-174931号公報、特開2015-174932号公報に記載されている方法に従って合成することができる。
層Bは、層Bの高分子化合物(又はその架橋体)と、正孔輸送材料、正孔注入材料、電子輸送材料、電子注入材料、発光材料及び酸化防止剤からなる群から選ばれる少なくとも1種の材料とを含む組成物(以下、「層Bの組成物」ともいう。)を含有する層であってもよい。
層Bは、層B’の高分子化合物(又はその架橋体)と、正孔輸送材料、正孔注入材料、電子輸送材料、電子注入材料、発光材料及び酸化防止剤からなる群から選ばれる少なくとも1種の材料とを含む組成物(以下、「層B’の組成物」ともいう。)を含有する層であってもよい。
層Bは、例えば、層Bの高分子化合物と、溶媒とを含有する組成物(以下、「層Bのインク」ともいう。)、又は、層B’の高分子化合物と、溶媒とを含有する組成物(以下、「層B’のインク」ともいう。)を用いて形成することができる。層Bのインク及び層B’のインクは、第1のインクの項で説明した湿式法に好適に使用することができる。層Bのインク及び層B’のインクの粘度の好ましい範囲は、第1のインクの粘度の好ましい範囲と同じである。層Bのインク及び層B’のインクに含有される溶媒の例及び好ましい範囲は、第1のインクに含有される溶媒の例及び好ましい範囲と同じである。
次に、第2の有機層の好ましい実施形態の1つである層Cについて説明する。
層Cは、式(2)で表される金属錯体と、架橋基を有する化合物の架橋体とを含有する層C’であることが好ましい。層C’において、式(2)で表される金属錯体及び架橋基を有する化合物の架橋体は、それぞれ、1種単独で含有されていても、2種以上含有されていてもよい。
層C’の高分子化合物における架橋基A群から選ばれる少なくとも1種の架橋基を有する構成単位の定義、例及び好ましい範囲は、層B’の高分子化合物における架橋基A群から選ばれる少なくとも1種の架橋基を有する構成単位の定義、例及び好ましい範囲と同じである。
層C’の高分子化合物は、前述の高分子ホストの製造方法と同様の方法で製造することができる。
層C’の低分子化合物は、式(3)で表される低分子化合物が好ましい。
mB1、mB2及びmB3は、それぞれ独立に、0以上の整数を表す。複数存在するmB1は、同一でも異なっていてもよい。mB3が複数存在する場合、それらは同一でも異なっていてもよい。
Ar7は、芳香族炭化水素基、複素環基、又は、芳香族炭化水素環と複素環とが直接結合した基を表し、これらの基は置換基を有していてもよい。Ar7が複数存在する場合、それらは同一でも異なっていてもよい。
LB1は、アルキレン基、シクロアルキレン基、アリーレン基、2価の複素環基、-N(R’’’)-で表される基、酸素原子又は硫黄原子を表し、これらの基は置換基を有していてもよい。R’’’は、水素原子、アルキル基、シクロアルキル基、アリール基又は1価の複素環基を表し、これらの基は置換基を有していてもよい。LB1が複数存在する場合、それらは同一でも異なっていてもよい。
X’’は、架橋基、水素原子、アルキル基、シクロアルキル基、アリール基又は1価の複素環基を表し、これらの基は置換基を有していてもよい。複数存在するX’’は、同一でも異なっていてもよい。但し、複数存在するX’’のうち、少なくとも1つは、架橋基である。
層Cは、式(2)で表される金属錯体と、正孔輸送材料、正孔注入材料、電子輸送材料、電子注入材料、発光材料及び酸化防止剤からなる群から選ばれる少なくとも1種とを含む組成物(以下、「層Cの組成物」ともいう。)を含有する層であってもよい。但し、式(2)で表される金属錯体と、正孔輸送材料、正孔注入材料、電子輸送材料、電子注入材料及び発光材料とは異なる。
層C’は、式(2)で表される金属錯体と、架橋基を有する化合物の架橋体と、正孔輸送材料、正孔注入材料、電子輸送材料、電子注入材料、発光材料及び酸化防止剤からなる群から選ばれる少なくとも1種とを含む組成物(以下、「層C’の組成物」ともいう。)を含有する層であってもよい。但し、式(2)で表される金属錯体及び架橋基を有する化合物の架橋体と、正孔輸送材料、正孔注入材料、電子輸送材料、電子注入材料及び発光材料とは異なる。
層Cは、例えば、式(2)で表される金属錯体と、溶媒とを含有する組成物(以下、「層Cのインク」ともいう。)を用いて形成することができる。層C’は、例えば、式(2)で表される金属錯体と、架橋基を有する化合物と、溶媒とを含有する組成物(以下、「層C’のインク」ともいう。)を用いて形成することができる。層Cのインク及び層C’のインクは、第1のインクの項で説明した湿式法に好適に使用することができる。層Cのインク及び層C’のインクの粘度の好ましい範囲は、第1のインクの粘度の好ましい範囲と同じである。層Cのインク及び層C’のインクに含有される溶媒の例及び好ましい範囲は、第1のインクに含有される溶媒の例及び好ましい範囲と同じである。
本実施形態の発光素子は、陽極、陰極、第1の有機層及び第2の有機層以外の層を有していてもよい。
本実施形態の発光素子において、第2の有機層は、本実施形態の発光素子の外部量子効率がより優れるので、陽極及び第1の有機層の間に設けられた層であることが好ましい。
本実施形態の発光素子は、第1の有機層が層A’である場合、第2の有機層は層B又は層Cであり、本実施形態の発光素子の外部量子効率がより優れるので、好ましくは層B又は層C’であり、より好ましくは層Bである。
本実施形態の発光素子において、第2の有機層は、通常、正孔輸送層、発光層(即ち、第1の発光層とは別個の発光層であり、以下、「第2の発光層」と言う。)又は電子輸送層であり、好ましくは正孔輸送層又は第2の発光層であり、更に好ましくは第2の発光層である。
例えば、第1の発光層が層Aであり、且つ、第2の発光層が層Bである場合、層Aにおける式(1)で表される金属錯体の含有量と、層Bにおける層Bの高分子化合物又は層Bの高分子化合物の架橋体の含有量とを調整することにより、発光色を調整することが可能であり、発光色を白色に調整することも可能である。
(D2)陽極/正孔輸送層(第2の有機層)/第1の発光層(第1の有機層)/陰極
(D3)陽極/正孔注入層/第2の発光層(第2の有機層)/第1の発光層(第1の有機層)/陰極
(D4)陽極/正孔注入層/第2の発光層(第2の有機層)/第1の発光層(第1の有機層)/電子輸送層/陰極
(D5)陽極/正孔注入層/第2の発光層(第2の有機層)/第1の発光層(第1の有機層)/電子注入層/陰極
(D6)陽極/正孔注入層/第2の発光層(第2の有機層)/第1の発光層(第1の有機層)/電子輸送層/電子注入層/陰極
(D7)陽極/正孔注入層/正孔輸送層(第2の有機層)/第1の発光層(第1の有機層)/陰極
(D8)陽極/正孔注入層/正孔輸送層(第2の有機層)/第1の発光層(第1の有機層)/電子輸送層/陰極
(D9)陽極/正孔注入層/正孔輸送層(第2の有機層)/第1の発光層(第1の有機層)/電子注入層/陰極
(D10)陽極/正孔注入層/正孔輸送層(第2の有機層)/第1の発光層(第1の有機層)/電子輸送層/電子注入層/陰極
(D11)陽極/正孔注入層/正孔輸送層/第2の発光層(第2の有機層)/第1の発光層(第1の有機層)/電子輸送層/電子注入層/陰極
(D12)陽極/正孔注入層/正孔輸送層(第2の有機層)/第1の発光層(第1の有機層)/第2の発光層/電子輸送層/電子注入層/陰極
(D13)陽極/正孔注入層/正孔輸送層/第1の発光層(第1の有機層)/第2の発光層(第2の有機層)/電子輸送層/電子注入層/陰極
(D14)陽極/正孔注入層/正孔輸送層/第1の発光層(第1の有機層)/電子輸送層(第2の有機層)/電子注入層/陰極
(D15)陽極/正孔注入層/正孔輸送層(第2の有機層)/第2の発光層/第1の発光層(第1の有機層)/電子輸送層/電子注入層/陰極
陽極、正孔注入層、正孔輸送層、第2の発光層、電子輸送層、電子注入層及び陰極が複数存在する場合、それらを構成する材料はそれぞれ同一でも異なっていてもよい。
第2の発光層は、第2の有機層又は発光材料を含有する層である。第2の発光層が発光材料を含有する層である場合、第2の発光層に含有される発光材料としては、例えば、前述の第1の組成物が含有していてもよい発光材料が挙げられる。第2の発光層に含有される発光材料は、1種単独で含有されていても、2種以上が含有されていてもよい。
正孔輸送層は、第2の有機層又は正孔輸送材料を含有する層である。正孔輸送層が正孔輸送材料を含有する層である場合、正孔輸送材料としては、例えば、前述の第1の組成物が含有していてもよい正孔輸送材料が挙げられる。正孔輸送層に含有される正孔輸送材料は、1種単独で含有されていても、2種以上が含有されていてもよい。
電子輸送層は、第2の有機層又は電子輸送材料を含有する層であり、好ましくは、電子輸送材料を含有する層である。電子輸送層が電子輸送材料を含有する層である場合、電子輸送層に含有される電子輸送材料としては、例えば、前述の第1の組成物が含有していてもよい電子輸送材料が挙げられる。電子輸送層に含有される電子輸送材料は、1種単独で含有されていても、2種以上が含有されていてもよい。
正孔注入層は、正孔注入材料を含有する層である。正孔注入層に含有される正孔注入材料としては、例えば、前述の第1の組成物が含有していてもよい正孔注入材料が挙げられる。正孔注入層に含有される正孔注入材料は、1種単独で含有されていても、2種以上が含有されていてもよい。
発光素子における基板は、電極の形成及び有機層の形成の際に、化学的に変化しない基板であることが好ましい。基板は、例えば、ガラス、プラスチック、シリコン等の材料からなる基板であってよい。不透明な基板を使用する場合には、基板から最も遠くにある電極が透明又は半透明であることが好ましい。
本実施形態の発光素子において、第1の有機層、第2の有機層、その他の層の形成方法としては、低分子化合物を用いる場合、例えば、粉末からの真空蒸着法、溶液又は溶融状態からの成膜による方法が挙げられ、高分子化合物を用いる場合、例えば、溶液又は溶融状態からの成膜による方法が挙げられる。
加熱の時間は、通常、0.1分~1000分であり、好ましくは0.5分~500分であり、より好ましくは1分~120分であり、更に好ましくは10分~60分である。
発光素子を用いて面状の発光を得るためには、面状の陽極と陰極が重なり合うように配置すればよい。パターン状の発光を得るためには、面状の発光素子の表面にパターン状の窓を設けたマスクを設置する方法、非発光部にしたい層を極端に厚く形成し実質的に非発光とする方法、陽極若しくは陰極、又は両方の電極をパターン状に形成する方法がある。これらのいずれかの方法でパターンを形成し、いくつかの電極を独立にON/OFFできるように配置することにより、数字、文字等を表示できるセグメントタイプの表示装置が得られる。ドットマトリックス表示装置とするためには、陽極と陰極を共にストライプ状に形成して直交するように配置すればよい。複数の種類の発光色の異なる高分子化合物を塗り分ける方法、カラーフィルター又は蛍光変換フィルターを用いる方法により、部分カラー表示、マルチカラー表示が可能となる。ドットマトリックス表示装置は、パッシブ駆動も可能であるし、TFT等と組み合わせてアクティブ駆動も可能である。これらの表示装置は、コンピュータ、テレビ、携帯端末等のディスプレイに用いることができる。面状の発光素子は、液晶表示装置のバックライト用の面状光源、又は、面状の照明用光源として好適に用いることができる。フレキシブルな基板を用いれば、曲面状の光源及び表示装置としても使用できる。
[測定条件]
測定する高分子化合物を約0.05質量%の濃度でテトラヒドロフラン(THF)に溶解させ、SECに10μL注入した。SECの移動相としてTHFを用い、2.0mL/分の流量で流した。カラムとして、PLgel MIXED-B(ポリマーラボラトリーズ製)を用いた。検出器にはUV-VIS検出器(島津製作所製、商品名:SPD-10Avp)を用いた。
測定試料を約2mg/mLの濃度になるようにクロロホルム又はテトラヒドロフランに溶解させ、LC-MS(Agilent製、商品名:1100LCMSD)に約1μL注入した。LC-MSの移動相には、アセトニトリル及びテトラヒドロフランの比率を変化させながら用い、0.2mL/分の流量で流した。カラムは、L-column 2 ODS(3μm)(化学物質評価研究機構製、内径:2.1mm、長さ:100mm、粒径3μm)を用いた。
5~10mgの測定試料を約0.5mLの重クロロホルム(CDCl3)、重テトラヒドロフラン、重ジメチルスルホキシド、重アセトン、重N,N-ジメチルホルムアミド、重トルエン、重メタノール、重エタノール、重2-プロパノール又は重塩化メチレンに溶解させ、NMR装置(バリアン(Varian,Inc.)製、商品名:INOVA300若しくはMERCURY 400VX、又は、ブルカー製、商品名:AVANCE600)を用いて測定した。
化合物M1、M2及びM3は、国際公開第2013/146806号に記載の方法に従って合成した。
金属錯体R1は、特開2008-179617号公報に記載の方法に従って合成した。
金属錯体RM1は、国際公開第2009/157424号に記載の方法に従って合成した。
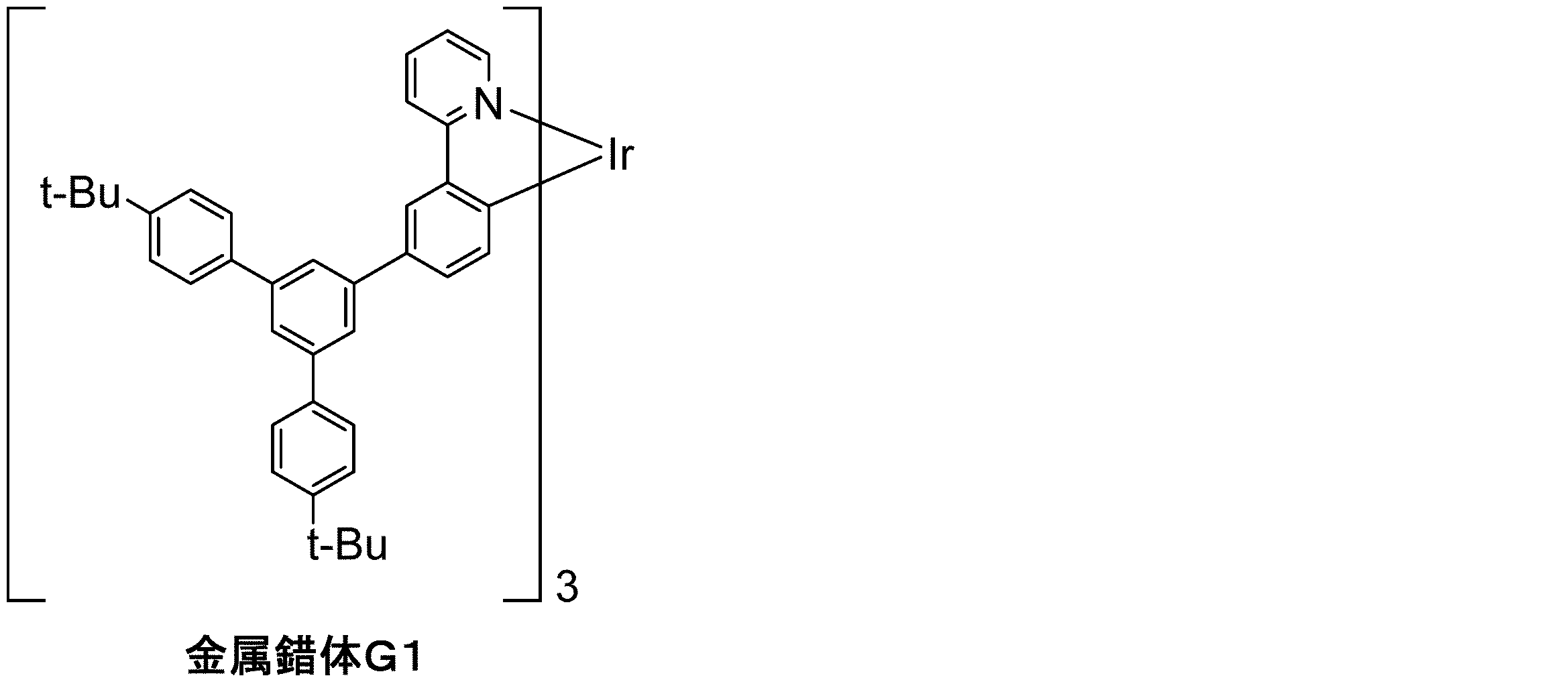
金属錯体G1は、国際公開第2009/131255号に記載の方法に準じて合成した。
(工程1)反応容器内を不活性ガス雰囲気とした後、化合物M1(0.800g)、化合物M2(0.149g)、化合物M3(1.66g)、ジクロロビス(トリス-o-メトキシフェニルホスフィン)パラジウム(1.4mg)及びトルエン(45mL)を加え、100℃に加熱した。
(工程2)反応液に、20質量%水酸化テトラエチルアンモニウム水溶液(16mL)を滴下し、7時間還流させた。
(工程3)反応後、そこに、2-エチルフェニルボロン酸(90mg)及びジクロロビス(トリス-o-メトキシフェニルホスフィン)パラジウム(1.3mg)を加え、17.5時間還流させた。
(工程4)その後、そこに、ジエチルジチアカルバミン酸ナトリウム水溶液を加え、85℃で2時間撹拌した。冷却後、反応液を、3.6質量%塩酸、2.5質量%アンモニア水、水で洗浄し、得られた溶液をメタノールに滴下したところ、沈澱が生じた。沈殿物をトルエンに溶解させ、アルミナカラム、シリカゲルカラムの順番で通すことにより精製した。得られた溶液をメタノールに滴下し、撹拌した後、得られた沈殿物をろ取し、乾燥させることにより、高分子化合物HTL-1を1.64g得た。高分子化合物HTL-1のMnは3.5×104であり、Mwは2.2×105であった。
(工程1)反応容器内を不活性ガス雰囲気とした後、化合物M1(2.52g)、化合物M2(0.470g)、化合物M3(4.90g)、金属錯体RM1(0.530g)、ジクロロビス(トリス-o-メトキシフェニルホスフィン)パラジウム(4.2mg)及びトルエン(158mL)を加え、100℃に加熱した。
(工程2)反応液に、20質量%水酸化テトラエチルアンモニウム水溶液(16mL)を滴下し、8時間還流させた。
(工程3)反応後、そこに、フェニルボロン酸(116mg)及びジクロロビス(トリス-o-メトキシフェニルホスフィン)パラジウム(4.2mg)を加え、15時間還流させた。
(工程4)その後、そこに、ジエチルジチアカルバミン酸ナトリウム水溶液を加え、85℃で2時間撹拌した。冷却後、反応液を、3.6質量%塩酸、2.5質量%アンモニア水、水で洗浄し、得られた溶液をメタノールに滴下したところ、沈澱が生じた。沈殿物をトルエンに溶解させ、アルミナカラム、シリカゲルカラムの順番で通すことにより精製した。得られた溶液をメタノールに滴下し、撹拌した後、得られた沈殿物をろ取し、乾燥させることにより、高分子化合物EML-1を6.02g得た。高分子化合物EML-1のMnは3.8×104であり、Mwは4.5×105であった。
(高分子化合物ET1aの合成)
高分子化合物ET1aは、特開2012-33845号公報に記載の方法に従って合成した化合物ET1-1、及び、特開2012-33845号公報に記載の方法に従って合成した化合物ET1-2を用いて、特開2012-33845号公報に記載の方法に従って合成した。
反応容器内を不活性ガス雰囲気とした後、高分子化合物ET1a(200mg)、テトラヒドロフラン(20mL)及びエタノール(20mL)を加え、55℃に加熱した。その後、そこへ、水(2mL)に溶解させた水酸化セシウム(200mg)を加え、55℃で6時間撹拌した。その後、室温まで冷却した後、減圧濃縮することにより、固体を得た。得られた固体を水で洗浄した後、減圧乾燥させることにより、高分子化合物ET1(150mg、薄黄色固体)を得た。得られた高分子化合物ET1のNMRスペクトルにより、高分子化合物ET1aのエチルエステル部位のエチル基由来のシグナルが完全に消失していることを確認した。
金属錯体B1は、以下の方法で合成した。
反応容器内を窒素雰囲気とした後、化合物L1-2(50g)及び塩化チオニル(100mL)を加え、還流下、3時間撹拌した。その後、反応混合物を室温まで冷却した後、塩化チオニルを減圧留去することにより、反応混合物L1-2’を得た。
反応容器内を窒素雰囲気とした後、化合物L1-1(47g)及びテトラヒドロフラン(1L)を加え、0℃に冷却した。そこへ、トリエチルアミン(54mL)をゆっくり加え、0℃で45分間撹拌した。そこへ、(反応混合物L1-2’の合成)で得られた反応混合物L1-2’(全量)をゆっくりと加えた。その後、室温で16時間撹拌した。得られた反応液をろ過した後、得られたろ液を減圧濃縮することにより、粗生成物を得た。得られた粗生成物を、酢酸エチル及びヘキサンの混合溶媒で洗浄した後、減圧乾燥させることにより、化合物L1-3(50g)を得た。化合物L1-3のHPLC面積百分率値は95.2%であった。上記操作を繰り返し行うことにより、必要量の化合物L1-3を得た。
LC-MS(APCI,positive):m/z=263[M+H]+
1H-NMR(300MHz,CDCl3):δ(ppm)=0.84(t,9H),1.64(q,6H),7.39-7.54(m,3H),7.81-7.84(m,2H),8.72-8.74(m,1H),9.66-9.68(m,1H).
反応容器内を窒素雰囲気とした後、化合物L1-3(58g)及びトルエン(600mL)を加え、室温で撹拌した。そこへ、五塩化リン(92g)をゆっくりと加えた後、110℃で3時間撹拌した。その後、得られた反応液を室温まで冷却し、そこへ、化合物L1-4(78.2g)及びp-トルエンスルホン酸(3g)を加えた。その後、130℃で4日間撹拌した後、反応液を室温まで冷却した。得られた反応液を減圧濃縮し、そこへ、酢酸エチル(2L)を加えた後、10質量%炭酸水素ナトリウム水溶液で洗浄した。得られた有機層を硫酸マグネシウムで乾燥させた後、ろ過し、得られたろ液を減圧濃縮することにより、粗生成物を得た。この粗生成物をシリカゲルカラムクロマトグラフィー(メタノール及びクロロホルムの混合溶媒)により精製し、更に、アセトニトリルを用いて晶析を行った後、減圧乾燥させることにより、化合物L1-5(6g)を得た。化合物L1-5のHPLC面積百分率値は99.1%であった。
LC-MS(APCI,positive):m/z=404[M+H]+
1H-NMR(400MHz,CDCl3):δ(ppm)=0.83(t,9H),1.34(s,9H),1.64(q,6H),1.96(s,6H),7.12(s,2H),7.20-7.23(m,2H),7.28-7.34(m,3H).
反応容器内を窒素雰囲気とした後、トリス(アセチルアセトナト)イリジウム(III)(1.4g)、化合物L1-5(4.6g)及びペンタデカン(2mL)を加え、300℃で18時間撹拌した。その後、得られた反応液を室温まで冷却し、そこへ、トルエンを加え、溶解させた後、減圧濃縮させることにより、粗生成物を得た。得られた粗生成物をシリカゲルカラムクロマトグラフィー(ヘプタン及び酢酸エチルの混合溶媒)により精製し、更に、アセトニトリル及びトルエンの混合溶媒を用いて晶析を行った後、減圧乾燥させることにより、金属錯体B1(2.8g)を得た。金属錯体B1のHPLC面積百分率値は99.5%以上であった。
1H-NMR(600MHz,THF-d8):δ(ppm)=7.30(s,6H),6.90(d,3H),6.44-6.48(m,3H),6.22-6.26(m,3H),5.77(d,3H),2.10(s,9H),1.89(s,9H),1.56(s,18H),1.38(s,27H),0.73(t,27H).
金属錯体B2は、以下の方法で合成した。
反応容器内を窒素雰囲気とした後、化合物L1-1(500g)、テトラヒドロフラン(5L)及びトリエチルアミン(585mL)を加え、0℃で撹拌した。そこへ、化合物L2-1を滴下した後、室温で16時間撹拌した。得られた反応液をろ過した後、得られたろ液を減圧濃縮することにより、固体を得た。得られた固体を酢酸エチルで洗浄した後、減圧乾燥させることにより、化合物L2-2(500g)を得た。化合物L2-2のHPLC面積百分率値は99.4%であった。
1H-NMR(400MHz,CDCl3):δ(ppm)=1.22(d,6H),2.54-2.63(m,1H),7.40-7.56(m,3H),7.80-7.83(m,2H),9.06(s,1H),9.42(s,1H).
反応容器内を窒素雰囲気とした後、化合物L2-2(40g)、ジクロロベンゼン(400mL)及び化合物L1-4(85g)を加え、-10℃で撹拌した。そこへ、五塩化リン(22mL)を滴下した。その後、-10℃で30分間撹拌し、更に、室温で1時間撹拌した後、185℃で18時間撹拌した。その後、得られた反応液を室温まで冷却し、減圧濃縮した。得られた反応混合物を塩化メチレン及びイオン交換水で抽出した。得られた有機層を硫酸マグネシウムで乾燥させ、ろ過し、得られたろ液を減圧濃縮することにより、粗生成物を得た。得られた粗生成物をシリカゲルカラムクロマトグラフィー(ヘプタン及び酢酸エチルの混合溶媒)により精製し、更に、アセトニトリルを用いて晶析を行った後、減圧乾燥させることにより、化合物L2-3(10g)を得た。化合物L2-3のHPLC面積百分率値は99.4%であった。
1H-NMR(400MHz,CDCl3):δ(ppm)=1.32(d,6H),1.35(s,9H),1.94(s,6H),2.55-2.62(m,1H),7.17(s,2H),7.22-7.33(m,3H),7.39-7.41(m,2H).
反応容器内を窒素雰囲気とした後、トリス(アセチルアセトナト)イリジウム(III)(3.5g)、化合物L2-3(10g)及びペンタデカン(2mL)を加え、285℃で18時間撹拌した。その後、得られた反応液を室温まで冷却し、シリカゲルカラムクロマトグラフィー(ヘプタン及び酢酸エチルの混合溶媒)及びシリカゲルカラムクロマトグラフィー(塩化メチレン及び酢酸エチルの混合溶媒)により精製し、更に、ヘプタン及びトルエンの混合溶媒を用いて晶析を行った。その後、得られた固体を減圧乾燥させることにより、金属錯体B2(1.2g)を得た。金属錯体B2のHPLC面積百分率値は99.5%以上であった。上記操作を繰り返し行うことにより、必要量の金属錯体B2を得た。
1H-NMR(600MHz,THF-d8):δ(ppm)=7.35(brs,3H),7.34(brs,3H),6.86(dd,3H),6.49(td,3H),6.33(td,3H),6.13(d,3H),2.53(spt,3H),2.15(s,9H),1.90(s,9H),1.39(s,27H),1.23(d,9H),1.11(d,9H).
金属錯体B3は、以下の方法で合成した。
反応容器内を窒素雰囲気とした後、化合物L1-1(50g)及びN-メチル-2-ピロリドン(200mL)を加え、0℃で撹拌した。そこへ、N-メチル-2-ピロリドン(40mL)に溶解させた化合物L3-1(40g)を滴下した後、室温で18時間撹拌した。その後、得られた反応液をイオン交換水(1.2L)に注ぐことにより、沈殿物が得られた。得られた沈殿物をろ取し、更に、1M塩酸水溶液、イオン交換水及びヘプタンで順次洗浄した。その後、得られた固体を減圧乾燥することにより、化合物L3-2(43g、白色固体)を得た。
1H-NMR(600MHz、CDCl3)δ(ppm)=9.64(br,1H),8.90(br,1H),7.86(d,2H),7.56(t,1H),7.45(t,2H),7.02-7.08(m,3H),2.41(s,6H).
反応容器内を窒素雰囲気とした後、化合物L3-2(43g)及びトルエン(740mL)を加え、室温で撹拌した。そこへ、五塩化リン(67g)を少しずつ加えた後、110℃で21時間撹拌した。得られた反応液を室温まで冷却した後、氷水(500mL)に注ぎ、2時間撹拌し、水層を除去した。得られた有機層をイオン交換水、10質量%炭酸水素ナトリウム水溶液で洗浄し、更に、得られた有機層を硫酸マグネシウムで乾燥させた後、ろ過した。得られたろ液を減圧濃縮することにより、化合物L3-3(40g)を得た。
反応容器内を窒素雰囲気とした後、化合物L3-3(40g)、化合物L3-4(32g)及びキシレン(800mL)を加え、室温で撹拌した。そこへ、p-トルエンスルホン酸(3g)を加え、120℃で116時間撹拌した。その後、得られた反応液を室温まで冷却した後、そこへ、イオン交換水(800mL)を加え、室温で1時間撹拌した。その後、水層を除去した後、得られた有機層を5質量%炭酸水素ナトリウム水溶液で洗浄した。得られた有機層を硫酸マグネシウムで乾燥させた後、ろ過し、得られたろ液を減圧濃縮することにより、粗生成物を得た。得られた粗生成物をシリカゲルカラムクロマトグラフィー(ヘプタン及び酢酸エチルの混合溶媒)及びシリカゲルカラムクロマトグラフィー(アセトニトリル及びテトラヒドロフラン)により順次精製することにより、化合物L3-5(1.3g、白色固体)を得た。化合物L3-5のHPLC面積百分率値は99.5%以上であった。上記操作を繰り返し行うことにより、必要量の化合物L3-5を得た。
1H-NMR(600MHz、THF-d8)δ(ppm)=7.42(d,2H),7.30(t,1H),7.24(t,2H),7.15(t,1H),6.98(d,2H),6.85(s,2H),2.51(t,2H),2.07(s,6H),1.81(s,6H),1.56(m,2H),1.26-1.32(m,6H),0.88(t,3H).
反応容器内を窒素雰囲気とした後、トリス(アセチルアセトナト)イリジウム(III)(0.6g)、化合物L3-5(2.0g)及びトリデカン(2mL)を加え、250℃で120時間攪拌した。その後、得られた反応液を室温まで冷却した後、シリカゲルカラムクロマトグラフィー(ヘプタン及び酢酸エチルの混合溶媒)により精製し、更に、塩化メチレン及びアセトニトリルの混合溶媒を用いて晶析を行った。得られた固体を減圧乾燥することにより、金属錯体B3(0.6g、黄色固体)を得た。金属錯体B3のHPLC面積百分率値は99.2%であった。
1H-NMR(600MHz、THF-d8)δ(ppm)=7.04-7.08(m,6H),6.93(s,3H),6.92(s,3H),6.88(d,3H),6.84(d,3H),6.61(t,3H),6.43(t,3H),6.29(d,3H),2.57(t,6H),2.12(s,9H),1.95(s,9H),1.82(s,9H),1.70(s,9H),1.62(m,6H),1.28-1.36(m,18H),0.89(t,9H).
金属錯体B4は、以下の方法で合成した。
反応容器内を窒素雰囲気とした後、化合物L1-1(100g)、トリエチルアミン(114mL)及びテトラヒドロフラン(1.5L)を加え、0℃で撹拌した。そこへ、化合物L4-1(52mL)を滴下した後、室温で16時間撹拌した。その後、得られた反応液をろ過した後、得られたろ液を濃縮することにより、粗生成物を得た。得られた粗生成物を、酢酸エチルを用いて晶析した後、減圧乾燥することにより、化合物L4-2(70g)を得た。化合物L4-2のHPLC面積百分率値は98.7%であった。
LC-MS(APCI,positive):m/z=179[M+H]+
1H-NMR(300MHz、DMSO-d6)δ(ppm)=10.26(br,1H),9.86(br,1H),7.83-7.86(m,2H),7.45-7.56(m,3H),1.90(s,3H).
反応容器内を窒素雰囲気とした後、化合物L4-2(70g)及びキシレン(700mL)を加え、室温で撹拌した。そこへ、五塩化リン(123g)を少しずつ加え、130℃で2時間撹拌した後、室温に冷却した。そこへ、化合物L4-3(70g)を少しずつ加えた後、130℃で8時間撹拌した。その後、得られた反応液を室温まで冷却した後、減圧濃縮した。そこへ、酢酸エチルを加え、得られた有機層をイオン交換水、10質量%炭酸水素ナトリウム水溶液、飽和食塩水で順次洗浄した。得られた有機層を硫酸ナトリウムで乾燥させた後、ろ過し、得られたろ液を減圧濃縮することにより、粗生成物を得た。得られた粗生成物をシリカゲルカラムクロマトグラフィー(ヘキサン及び酢酸エチルの混合溶媒)により精製し、更に、N,N-ジメチルホルムアミド及び水の混合溶媒を用いて晶析を行った。得られた固体を減圧乾燥することにより、化合物L4-4(70g、白色固体)を得た。化合物L4-4のHPLC面積百分率値は99.2%であった。
LC-MS(APCI,positive):m/z=320[M+H]+
1H-NMR(400MHz、CDCl3)δ(ppm)=7.53-7.58(m,1H),7.48(d,2H),7.33(d,2H),7.28-7.30(m,1H),7.21-7.25(m,2H),2.39(q,2H),2.26(s,3H),1.14(d,6H),0.87(d,6H).
反応容器内を窒素雰囲気とした後、トリス(アセチルアセトナト)イリジウム(III)(1.2g)、化合物L4-4(4.0g)及びトリデカン(1mL)を加え、280℃で18時間攪拌した。その後、得られた反応液を室温まで冷却した後、シリカゲルカラムクロマトグラフィー(酢酸エチル及びメタノールの混合溶媒)により精製し、更に、トルエン及びアセトニトリルの混合溶媒を用いて晶析した。得られた固体を減圧乾燥することにより、金属錯体B4(1.7g、黄色固体)を得た。金属錯体B4のHPLC面積百分率値は99.5%以上であった。
1H-NMR(600MHz、THF-d8)δ(ppm)=7.56(t,3H),7.42(dd,3H),7.40(dd,3H),6.87(dd,3H),6.52(td,3H),6.35(td,3H),6.17(dd,3H),2.83(hept,3H),2.34(hept,3H),2.10(s,9H),1.23(d,9H),0.98(d,9H),0.96(d,9H),0.92(d,9H).
金属錯体B5は、以下の方法で合成した。
反応容器内を窒素雰囲気とした後、化合物L1-1(200g)、トリエチルアミン(225mL)及びテトラヒドロフラン(3L)を加え、0℃に冷却した。そこへ、化合物L5-1(198g)を滴下した後、室温で16時間撹拌した。得られた反応液をろ過した後、得られたろ液を減圧濃縮することにより、粗生成物を得た。得られた粗生成物を酢酸エチルで洗浄した後、減圧乾燥させることにより、化合物L5-2(172g)を得た。化合物L5-2のHPLC面積百分率値は99.2%であった。
1H-NMR(400MHz,DMSO-d6):δ(ppm)=0.88(t,3H),1.18(s,6H),1.57(q,2H),7.47-7.58(m,3H),7.89-7.91(m,2H),9.51(s,1H),10.20(s,1H).
反応容器内を窒素雰囲気とした後、化合物L5-2(100g)及びトルエン(700mL)を加え、室温で撹拌した。そこへ、五塩化リン(178g)を少しずつ加え、110℃で18時間撹拌した後、室温に冷却した。得られた反応液を濃縮することにより、粗生成物L5-2’(65g)を得た。その後、反応容器内を再度、窒素雰囲気とした後、トルエン(1L)、化合物L1-4(43g)及びp-トルエンスルホン酸(6.5g)を加え、110で3日間撹拌した。その後、得られた反応液を室温まで冷却した後、減圧濃縮した。そこへ、酢酸エチルを加え、得られた有機層をイオン交換水で洗浄した。得られた有機層を硫酸ナトリウムで乾燥させた後、ろ過し、得られたろ液を減圧濃縮することにより、粗生成物を得た。得られた粗生成物をシリカゲルカラムクロマトグラフィー(ヘキサン及び酢酸エチルの混合溶媒)により精製し、更に、アセトニトリル及び酢酸エチルの混合溶媒を用いて晶析を行った。得られた固体を逆相カラムクロマトグラフィーにより精製した後、減圧乾燥することにより、化合物L5-3(16g)を得た。化合物L5-3のHPLC面積百分率値は99.4%であった。
LC-MS(APCI,positive):m/z=376[M+H]+
1H-NMR(400MHz,CDCl3):δ(ppm)=0.89(t,3H),1.19(s,6H),1.33(s,9H),1.71(q,2H), 1.97(s,6H),7.12(s,2H),7.19-7.23(m,2H),7.27-7.28(m,1H),7.33-7.36(m,2H).
反応容器内を窒素雰囲気とした後、トリス(アセチルアセトナト)イリジウム(III)(1.5g)、化合物L5-3(4.0g)及びトリデカン(2mL)を加え、280℃で28時間攪拌した。その後、得られた反応液を室温まで冷却した後、シリカゲルカラムクロマトグラフィー(へプタン及び酢酸エチルの混合溶媒)により精製し、更に、トルエン及びメタノールの混合溶媒を用いて晶析した。得られた固体を減圧乾燥することにより、金属錯体B5(1.0g、黄色固体)を得た。金属錯体B5のHPLC面積百分率値は99.5%以上であった。
1H-NMR(600MHz,THF-d8):δ(ppm)=7.31(s,6H),6.91(d,3H),6.48(td,3H),6.24-6.30(m,3H),5.87(d,3H),2.12-2.15(m,9H),1.94(s,9H),1.58-1.66(m,3H),1.50-1.57(m,3H),1.38(s,27H),1.12-1.16(m,9H),1.04-1.08(m,9H),0.84(t,9H).
金属錯体B6は、以下の方法で合成した。
反応容器内を窒素雰囲気とした後、4-ブロモ-2,6-ジメチルアニリン(100g)、トリエチルアミン(253mL)及びテトラヒドロフラン(1.5L)を加え、0℃に冷却した。そこへ、化合物L5-1(124mL)をゆっくりと滴下した後、室温で16時間撹拌した。得られた反応液をろ過した後、得られたろ液を減圧濃縮することにより、粗生成物を得た。得られた粗生成物をアセトニトリルを用いて晶析を行った後、減圧乾燥させることにより、化合物L9-1(125g)を得た。化合物L9-1のHPLC面積百分率値は98.7%であった。
1H-NMR(400MHz,CDCl3):δ(ppm)=0.96(t,3H),1.29(s,6H),1.68(q,2H),2.16(s,6H),6.93(brs,1H),7.08(s,2H).
反応容器内を窒素雰囲気とした後、化合物L9-1(120g)、モノクロロベンゼン(1.2L)、2-フルオロピリジン(43g)及びトリフルオロメタンスルホン酸無水物(125g)を加え、室温で撹拌した。そこへ、化合物L8-2(95.2g)を加え、室温で1時間撹拌した後、90℃で18時間撹拌し、更に、130℃で12時間撹拌した。その後、得られた反応液を室温まで冷却し、そこへ、酢酸エチルを加えた。得られた反応液を10質量%炭酸水素ナトリウム水溶液で洗浄し、更に、イオン交換水で2回洗浄した。得られた有機層を硫酸マグネシウムで乾燥させた後、ろ過し、得られたろ液を減圧濃縮することにより、粗生成物を得た。得られた粗生成物をアセトニトリルを用いて晶析を行った後、減圧乾燥させることにより、化合物L9-2(70g)を得た。化合物L9-2のHPLC面積百分率値は99.5%以上であった。
1H-NMR(400MHz,CDCl3):δ(ppm)=0.89(t,3H),1.22(s,6H),1.71(q,2H),1.99(s,6H),7.11-7.14(m,2H),7.37(s,2H),7.46-7.49(m,1H),7.64-7.65(m,1H).
反応容器内を窒素雰囲気とした後、化合物L9-2(60g)、フェニルボロン酸(38.3g)、トルエン(600mL)、トリス(ジベンジリデンアセトン)ジパラジウム(0)(Pd2(dba)3)(2.3g)、2-ジシクロヘキシルホスフィノ-2’,6’-ジメトキシビフェニル(SPhos)(2.1g)を加え、60℃に昇温した。そこへ、25質量%のテトラエチルアンモニウムヒドロキシド水溶液(300mL)を加えた後、加熱還流下で18時間攪拌した。その後、得られた反応液をセライトを敷いたろ過器でろ過した後、セライトを酢酸エチルで洗浄した。得られたろ液から水層を除去した後、得られた有機層をイオン交換水で洗浄した。得られた有機層を硫酸マグネシウムで乾燥させた後、ろ過し、得られたろ液を減圧濃縮することにより、粗生成物を得た。得られた粗生成物を、アセトニトリルを用いて晶析し、更に、アセトニトリル及びトルエンの混合溶媒を用いて晶析を行った。得られた固体を、シリカゲルカラムクロマトグラフィー(ヘキサン及び酢酸エチルの混合溶媒)、及び、逆相カラムクロマトグラフィー(水及びアセトニトリルの混合溶媒)により、順次精製した後、減圧乾燥することにより、化合物L9-3(34g)を得た。化合物L9-3のHPLC面積百分率値は99.5%以上であった。
1H-NMR(400MHz,CDCl3):δ(ppm)=0.95(t,3H),1.29(s,6H),1.79(q,2H),2.01(s,6H),7.26-7.31(m,5H),7.36-7.57(m,8H),7.65-7.69(m,3H).
反応容器内を窒素雰囲気とした後、トリス(アセチルアセトナト)イリジウム(III)(1.3g)、化合物L9-3(5.0g)及びペンタデカン(2mL)を加え、300℃で24時間撹拌した。その後、反応液を50℃まで冷却し、そこへ、トルエンを加えた。その後、得られた反応液を室温にまで冷却した後、イオン交換水で洗浄した。得られた有機層を減圧濃縮することにより、固体を得た。得られた固体をシリカゲルカラムクロマトグラフィー(塩化メチレン及び酢酸エチルの混合溶媒)により精製し、更に、アセトニトリル及びトルエンの混合溶媒を用いて晶析を行った後、減圧乾燥させることにより、金属錯体B6(0.65g)を得た。金属錯体B6のHPLC面積百分率値は99.5%以上であった。
1H-NMR(600MHz,THF-d8):δ(ppm)=7.77(dd,6H),7.65(s,6H),7.50(t,6H),7.41(tt,3H),7.25(d,3H),7.11(dd,6H),6.98-7.02(m,9H),6.93-6.97(m,3H),6.33(d,3H),2.27(s,9H),2.13(s,9H),1.75-1.79(m,4H),1.64-1.70(m,4H),1.30(s,9H),1.22(s,9H),1.00(t,9H).
金属錯体B7は、以下の方法で合成した。
反応容器内を窒素雰囲気とした後、金属錯体B2(2.2g)及び塩化メチレン(30mL)を加え、0℃で撹拌した。そこへ、N-ブロモスクシンイミド(0.95g)を15分間かけてゆっくりと加えた後、反応液を0℃から室温にゆっくりと昇温し、更に、室温で20時間撹拌した。その後、そこへ、メタノール(100mL)を加えた後、15分間撹拌することにより、沈殿物が得られた。得られた沈殿物をろ取し、更に、メタノールで洗浄した後、減圧乾燥させることにより、金属錯体B7’(2.1g)を得た。金属錯体B7’のHPLC面積百分率値は99.3%であった。
LC-MS(APCI,positive):m/z=1468[M+H]+
反応容器内を窒素雰囲気とした後、金属錯体B7’(1.0g)、化合物L7-1(1.2g)、トルエン(50mL)、トリス(ジベンジリデンアセトン)ジパラジウム(0)(Pd2(dba)3)(9.4mg)、2-ジシクロヘキシルホスフィノ-2’,6’-ジメトキシビフェニル(SPhos)(8.4mg)を加え、80℃に昇温した。その後、そこへ、20質量%のテトラエチルアンモニウムヒドロキシド水溶液(1.8mL)を加え、加熱還流下で20時間攪拌した。その後、得られた反応液を室温まで冷却し、水層を除去した後、得られた有機層をシリカゲルを敷いたろ過器でろ過した。得られたろ液を減圧濃縮することで固体を得た。得られた固体をシリカゲルカラムクロマトグラフィー(塩化メチレン及び酢酸エチルの混合溶媒)で精製し、更に、アセトニトリル及びトルエンの混合溶媒を用いて晶析を行った後、減圧乾燥させることにより、金属錯体B7(0.72g)を得た。金属錯体B7のHPLC面積百分率値は99.5%以上であった。
1H-NMR(600MHz,THF-d8):δ(ppm)=7.57-7.61(m,15H),7.49(d,12H),7.43(d,6H),7.27(d,3H),7.23(d,3H),7.21(d,3H),7.09(dd,3H),6.65(d,3H),2.61(spt,3H),2.24(s,9H),2.08(s,9H),1.38(s,54H),1.28(d,9H),1.18(d,9H),0.93(s,27H).
金属錯体B8は、以下の方法で合成した。
反応容器内を窒素雰囲気とした後、化合物L1-4(200g)、トリエチルアミン(472mL)及びテトラヒドロフラン(2L)を加え、0℃に冷却した。そこへ、化合物L5-1(228g)をゆっくりと滴下した後、室温で16時間撹拌した。得られた反応液をろ過した後、得られたろ液を減圧濃縮することにより、粗生成物を得た。得られた粗生成物を酢酸エチルで洗浄した後、減圧乾燥させることにより、化合物L8-1(205g)を得た。化合物L8-1のHPLC面積百分率値は99.5%以上であった。
LC-MS(APPI,positive):m/z=276[M+H]+
1H-NMR(400MHz,CDCl3):δ(ppm)=1.01(t,3H),1.31(s,6H),1.33(s,9H),1.70(q,2H),2.23(s,6H),6.84-7.09(m,3H).
反応容器内を窒素雰囲気とした後、化合物L8-1(115g)、モノクロロベンゼン(1.2L)、2-フルオロピリジン(44.6g)及びトリフルオロメタンスルホン酸無水物(130g)を加え、室温で撹拌した。そこへ、化合物L8-2(23g)を加え、室温で1時間撹拌した後、90℃で18時間撹拌した。その後、得られた反応液を室温まで冷却し、そこへ、クロロホルムを加えた。得られた反応液を10質量%炭酸水素ナトリウム水溶液で洗浄し、更に、イオン交換水で2回洗浄した。得られた有機層を硫酸マグネシウムで乾燥させた後、ろ過し、得られたろ液を減圧濃縮することにより、粗生成物を得た。得られた粗生成物をシリカゲルカラムクロマトグラフィー(ヘキサン及び酢酸エチルの混合溶媒)により精製し、更に、アセトニトリルを用いて晶析を行った後、減圧乾燥させることにより、化合物L8-3(100g)を得た。化合物L8-3のHPLC面積百分率値は99.5%以上であった。
LC-MS(APCI,positive):m/z=454[M+H]+
1H-NMR(400MHz,DMSO-d6):δ(ppm)=0.79(t,3H),1.12(s,6H),1.31(s,9H),1.62(q,2H),1.91(s,6H),7.16(s,2H),7.27-7.39(m,3H),7.56(d,1H).
反応容器内を窒素雰囲気とした後、化合物L8-3(50g)、化合物L8-4(22g)、トルエン(500mL)、トリス(ジベンジリデンアセトン)ジパラジウム(0)(Pd2(dba)3)(1g)、2-ジシクロヘキシルホスフィノ-2’,6’-ジメトキシビフェニル(SPhos)(0.9g)を加え、60℃に昇温した。そこへ、25質量%のテトラエチルアンモニウムヒドロキシド水溶液(260mL)を加えた後、加熱還流下で18時間攪拌した。その後、得られた反応液をセライトを敷いたろ過器でろ過した後、セライトを酢酸エチルで洗浄した。得られたろ液から水層を除去した後、得られた有機層をイオン交換水で洗浄した。得られた有機層を硫酸マグネシウムで乾燥させた後、ろ過し、得られたろ液を減圧濃縮することにより、粗生成物を得た。得られた粗生成物をシリカゲルカラムクロマトグラフィー(ヘキサン及び酢酸エチルの混合溶媒)により精製し、更に、アセトニトリルを用いて晶析を行った後、減圧乾燥させることにより、化合物L8-5(36g)を得た。化合物L8-5のHPLC面積百分率値は99.5%以上であった。
LC-MS(APCI,positive):m/z=508[M+H]+
1H-NMR(400MHz,CDCl3):δ(ppm)=0.92(t,3H),1.23(s,6H),1.35(s,9H),1.37(s,9H),1.73(q,2H),2.01(s,6H),7.19(d,2H),7.20(s,2H),7.26-7.28(m,1H),7.34-7.39(m,3H),7.51-7.54(m,1H),7.69-7.72(m,1H).
反応容器内を窒素雰囲気とした後、トリス(アセチルアセトナト)イリジウム(III)(2.1g)、化合物L8-5(8.6g)及びペンタデカン(3mL)を加え、300℃で24時間撹拌した。その後、反応液を室温まで冷却することにより、固体が析出した。析出した固体をろ取し、得られた固体をシリカゲルカラムクロマトグラフィー(塩化メチレン及び酢酸エチルの混合溶媒)により精製し、更に、アセトニトリル及び塩化メチレンの混合溶媒を用いて晶析を行った後、減圧乾燥させることにより、金属錯体B8(4.0g)を得た。金属錯体B8のHPLC面積百分率値は99.5%以上であった。
LC-MS(ESI,positive):m/z=1713[M+H]+
1H-NMR(600MHz,THF-d8):δ(ppm)=0.92(t,9H),1.11(s,9H),1.22(s,9H),1.27(s,27H),1.42(s,27H),1.56-1.62(m,3H),1.64-1.72(m,3H),2.02(s,9H),2.18(s,9H),6.24(d,3H),6.92(dd,3H),7.04(d,6H),7.15(d,3H),7.19(d,6H),7.38(d,6H).
(陽極及び正孔注入層の形成)
ガラス基板にスパッタ法により45nmの厚みでITO膜を付けることにより陽極を形成した。該陽極上に、ポリチオフェン・スルホン酸系の正孔注入剤であるAQ-1200(Plextronics社製)をスピンコート法により35nmの厚さで成膜し、大気雰囲気下において、ホットプレート上で170℃、15分間加熱することにより正孔注入層を形成した。
キシレンに、高分子化合物EML-1を0.7質量%の濃度で溶解させた。得られたキシレン溶液を用いて、正孔注入層の上にスピンコート法により20nmの厚さで成膜し、窒素ガス雰囲気下において、ホットプレート上で180℃、60分間加熱させることにより第2の有機層(第2の発光層)を形成した。
トルエンに、化合物HM-1及び金属錯体B1(化合物HM-1/金属錯体B1=75質量%/25質量%)を2質量%の濃度で溶解させた。得られたトルエン溶液を用いて、第2の有機層の上にスピンコート法により75nmの厚さで成膜し、窒素ガス雰囲気下において、130℃、10分間加熱させることにより第1の有機層(第1の発光層)を形成した。化合物HM-1は、Luminescence Technology社より購入したものを用いた。
2,2,3,3,4,4,5,5-オクタフルオロ-1-ペンタノールに、高分子化合物ET1を0.25質量%の濃度で溶解させた。得られた2,2,3,3,4,4,5,5-オクタフルオロ-1-ペンタノール溶液を用いて、第1の有機層の上にスピンコート法により10nmの厚さで成膜し、窒素ガス雰囲気下において、130℃、10分間加熱させることにより電子輸送層を形成した。
電子輸送層を形成した基板を蒸着機内において、1.0×10-4Pa以下にまで減圧した後、陰極として、電子輸送層の上にフッ化ナトリウムを約4nm、次いで、フッ化ナトリウム層の上にアルミニウムを約80nm蒸着した。蒸着後、ガラス基板を用いて封止することにより、発光素子D1を作製した。
発光素子D1に電圧を印加することにより、470nm、495nm及び595nmに発光スペクトルの極大発光波長を有するEL発光が観測された。470nm及び495nmの発光は、金属錯体B1に由来する発光であり、595nmの発光は、高分子化合物EML-1に由来する発光であった。また、100cd/m2における外部量子効率は18.6[%]であり、色度座標(x,y)は(0.45,0.38)であった。
実施例D1の(第2の有機層の形成)における、「高分子化合物EML-1」に代えて、「高分子化合物HTL-1及び金属錯体R1(高分子化合物HTL-1/金属錯体R1=65質量%/35質量%)」を用いた以外は実施例D1と同様にして、発光素子D2を作製した。
実施例D1の(第1の有機層の形成)における、「化合物HM-1及び金属錯体B1(化合物HM-1/金属錯体B1=75質量%/25質量%)」に代えて、「化合物HM-1及び金属錯体B3(化合物HM-1/金属錯体B3=75質量%/25質量%)」を用いた以外は実施例D1と同様にして、発光素子D3を作製した。
実施例D1の(第1の有機層の形成)における、「化合物HM-1及び金属錯体B1(化合物HM-1/金属錯体B1=75質量%/25質量%)」に代えて、「化合物HM-1及び金属錯体B5(化合物HM-1/金属錯体B5=75質量%/25質量%)」を用いた以外は実施例D1と同様にして、発光素子D4を作製した。
実施例D1の(第1の有機層の形成)における、「化合物HM-1及び金属錯体B1(化合物HM-1/金属錯体B1=75質量%/25質量%)」に代えて、「化合物HM-1及び金属錯体B6(化合物HM-1/金属錯体B6=75質量%/25質量%)」を用いた以外は実施例D1と同様にして、発光素子D5を作製した。
実施例D1の(第1の有機層の形成)における、「化合物HM-1及び金属錯体B1(化合物HM-1/金属錯体B1=75質量%/25質量%)」に代えて、「化合物HM-1及び金属錯体B7(化合物HM-1/金属錯体B7=75質量%/25質量%)」を用いた以外は実施例D1と同様にして、発光素子D6を作製した。
実施例D1の(第1の有機層の形成)における、「化合物HM-1及び金属錯体B1(化合物HM-1/金属錯体B1=75質量%/25質量%)」に代えて、「化合物HM-1及び金属錯体B8(化合物HM-1/金属錯体B8=75質量%/25質量%)」を用いた以外は実施例D1と同様にして、発光素子D7を作製した。
実施例D1における(第2の有機層の形成)を、下記(第2の有機層の形成-CD1)に変更し、更に、実施例D1における(第1の有機層の形成)を下記(第1の有機層の形成-CD1)に変更したこと以外は実施例D1と同様にして、発光素子CD1を作製した。
キシレンに、高分子化合物HTL-1を0.7質量%の濃度で溶解させた。得られたキシレン溶液を用いて、正孔注入層の上にスピンコート法により20nmの厚さで成膜し、窒素ガス雰囲気下において、ホットプレート上で180℃、60分間加熱させることにより第2の有機層(正孔輸送層)を形成した。
トルエンに、化合物HM-1、金属錯体B1及び金属錯体R1(化合物HM-1/金属錯体B1/金属錯体R1=74質量%/25質量%/1質量%)を2質量%の濃度で溶解させた。得られたトルエン溶液を用いて、第2の有機層の上にスピンコート法により75nmの厚さで成膜し、窒素ガス雰囲気下において、130℃、10分間加熱させることにより第1の有機層(発光層)を形成した。
発光素子CD1に電圧を印加することにより、465nm、495nm及び590nmに発光スペクトルの極大発光波長を有するEL発光が観測された。465nm及び495nmの発光は、金属錯体B1に由来する発光であり、590nmの発光は、金属錯体R1に由来する発光であった。100cd/m2における外部量子効率は2.6[%]であり、色度座標(x,y)は(0.53,0.40)であった。
実施例D1の(第1の有機層の形成)における、「化合物HM-1及び金属錯体B1(化合物HM-1/金属錯体B1=75質量%/25質量%)」に代えて、「化合物HM-1、金属錯体B5及び金属錯体G1(化合物HM-1/金属錯体B5/金属錯体G1=74質量%/25質量%/1質量%)」を用いた以外は実施例D1と同様にして、発光素子D8を作製した。
実施例D1の(第1の有機層の形成)における、「化合物HM-1及び金属錯体B1(化合物HM-1/金属錯体B1=75質量%/25質量%)」に代えて、「化合物HM-1、金属錯体B2及び金属錯体G1(化合物HM-1/金属錯体B2/金属錯体G1=74質量%/25質量%/1質量%)」を用いた以外は実施例D1と同様にして、発光素子D9を作製した。
実施例D1の(第1の有機層の形成)における、「化合物HM-1及び金属錯体B1(化合物HM-1/金属錯体B1=75質量%/25質量%)」に代えて、「化合物HM-1、金属錯体B1及び金属錯体G1(化合物HM-1/金属錯体B1/金属錯体G1=74質量%/25質量%/1質量%)」を用いた以外は実施例D1と同様にして、発光素子D10を作製した。
実施例D1の(第1の有機層の形成)における、「化合物HM-1及び金属錯体B1(化合物HM-1/金属錯体B1=75質量%/25質量%)」に代えて、「化合物HM-1、金属錯体B6及び金属錯体G1(化合物HM-1/金属錯体B6/金属錯体G1=74質量%/25質量%/1質量%)」を用いた以外は実施例D1と同様にして、発光素子D11を作製した。
また、20cd/m2における外部量子効率は17.6[%]であり、色度座標(x,y)は(0.46,0.46)であった。
実施例D1の(第1の有機層の形成)における、「化合物HM-1及び金属錯体B1(化合物HM-1/金属錯体B1=75質量%/25質量%)」に代えて、「化合物HM-1、金属錯体B7及び金属錯体G1(化合物HM-1/金属錯体B7/金属錯体G1=74質量%/25質量%/1質量%)」を用いた以外は実施例D1と同様にして、発光素子D12を作製した。
また、20cd/m2における外部量子効率は20.8[%]であり、色度座標(x,y)は(0.47,0.44)であった。
実施例D1の(第1の有機層の形成)における、「化合物HM-1及び金属錯体B1(化合物HM-1/金属錯体B1=75質量%/25質量%)」に代えて、「化合物HM-1、金属錯体B8及び金属錯体G1(化合物HM-1/金属錯体B8/金属錯体G1=74質量%/25質量%/1質量%)」を用いた以外は実施例D1と同様にして、発光素子D13を作製した。
また、20cd/m2における外部量子効率は19.2[%]であり、色度座標(x,y)は(0.45,0.45)であった。
実施例D1の(第1の有機層の形成)における、「化合物HM-1及び金属錯体B1(化合物HM-1/金属錯体B1=75質量%/25質量%)」に代えて、「化合物HM-1、金属錯体B4及び金属錯体G1(化合物HM-1/金属錯体B4/金属錯体G1=74質量%/25質量%/1質量%)」を用いた以外は実施例D1と同様にして、発光素子CD2を作製した。
Claims (15)
- 陽極と、陰極と、前記陽極及び前記陰極の間に設けられた第1の有機層及び第2の有機層と、を有し、
前記第1の有機層が、式(1)で表される金属錯体を含有する層Aであり、
前記第2の有機層が、
式(2)で表される金属錯体から水素原子1個以上を除いた基を有する構成単位を含む高分子化合物、及び、前記高分子化合物の架橋体のうち、少なくとも1種を含有する層B、又は、
式(2)で表される金属錯体及び架橋基を有する化合物の架橋体を含有する層C’である、発光素子。
[式中、
Mは、ロジウム原子、パラジウム原子、イリジウム原子又は白金原子を表す。
n1は1以上の整数を表し、n2は0以上の整数を表し、n1+n2は2又は3である。
Mがロジウム原子又はイリジウム原子の場合、n1+n2は3であり、Mがパラジウム原子又は白金原子の場合、n1+n2は2である。
E1は、炭素原子又は窒素原子を表す。E1が複数存在する場合、それらは同一でも異なっていてもよい。
環Bは、芳香族炭化水素環又は芳香族複素環を表し、これらの環は置換基を有していてもよい。該置換基が複数存在する場合、それらは互いに結合して、それぞれが結合する原子とともに環を形成していてもよい。環Bが複数存在する場合、それらは同一でも異なっていてもよい。
Z1Aは、=N-で表される基又は=C(RZ1A)-で表される基を表す。Z1Aが複数存在する場合、それらは同一であっても異なっていてもよい。RZ1Aは、水素原子、アルキル基、シクロアルキル基、アルコキシ基、シクロアルコキシ基、アリール基、アリールオキシ基、1価の複素環基、置換アミノ基又はハロゲン原子を表し、これらの基は置換基を有していてもよい。
R1は、炭素原子数5以上30以下のアルキル基を表し、該基は置換基を有していてもよい。R1が複数存在する場合、それらは同一でも異なっていてもよい。
Ar1Aは、式(Ar-1A)で表される基を表す。Ar1Aが複数存在する場合、それらは同一でも異なっていてもよい。
A1-G1-A2は、アニオン性の2座配位子を表す。A1及びA2は、それぞれ独立に、炭素原子、酸素原子又は窒素原子を表し、これらの原子は環を構成する原子であってもよい。G1は、単結合、又は、A1及びA2とともに2座配位子を構成する原子団を表す。A1-G1-A2が複数存在する場合、それらは同一でも異なっていてもよい。]
[式中、
環Aは、芳香族炭化水素環又は芳香族複素環を表し、これらの環は置換基を有していてもよい。該置換基が複数存在する場合、それらは互いに結合して、それぞれが結合する原子とともに環を形成していてもよい。
R2及びR3は、それぞれ独立に、アルキル基、シクロアルキル基、アルコキシ基、シクロアルコキシ基、アリール基、アリールオキシ基、1価の複素環基、置換アミノ基又はハロゲン原子を表し、これらの基は置換基を有していてもよい。]
[式中、
M2は、ロジウム原子、パラジウム原子、イリジウム原子又は白金原子を表す。
n3は1以上の整数を表し、n4は0以上の整数を表し、n3+n4は2又は3である。
M2がロジウム原子又はイリジウム原子の場合、n3+n4は3であり、M2がパラジウム原子又は白金原子の場合、n3+n4は2である。
E4は、炭素原子又は窒素原子を表す。E4が複数存在する場合、それらは同一でも異なっていてもよい。
環L1は、6員の芳香族複素環を表し、この環は置換基を有していてもよい。該置換基が複数存在する場合、それらは互いに結合して、それぞれが結合する原子とともに環を形成していてもよい。環L1が複数存在する場合、それらは同一でも異なっていてもよい。
環L2は、芳香族炭化水素環又は芳香族複素環を表し、これらの環は置換基を有していてもよい。該置換基が複数存在する場合、それらは互いに結合して、それぞれが結合する原子とともに環を形成していてもよい。環L2が複数存在する場合、それらは同一でも異なっていてもよい。
環L1が有していてもよい置換基と環L2が有していてもよい置換基とは、互いに結合して、それぞれが結合する原子とともに環を形成していてもよい。
A3-G2-A4は、アニオン性の2座配位子を表す。A3及びA4は、それぞれ独立に、炭素原子、酸素原子又は窒素原子を表し、これらの原子は環を構成する原子であってもよい。G2は、単結合、又は、A3及びA4とともに2座配位子を構成する原子団を表す。A3-G2-A4が複数存在する場合、それらは同一でも異なっていてもよい。] - 前記式(1)で表される金属錯体が、式(1-1)で表される金属錯体である、請求項1に記載の発光素子。
[式中、
M、Z1A、n1、n2、R1、Ar1A及びA1-G1-A2は、前記と同じ意味を表す。
環B1は、ベンゼン環、ピリジン環又はジアザベンゼン環を表し、E1B、E2B、E3B及びE4Bは、それぞれ独立に、窒素原子又は炭素原子を表す。E1B、E2B、E3B及びE4Bが複数存在する場合、それらはそれぞれ同一でも異なっていてもよい。E1Bが窒素原子の場合、R1Bは存在しない。E2Bが窒素原子の場合、R2Bは存在しない。E3Bが窒素原子の場合、R3Bは存在しない。E4Bが窒素原子の場合、R4Bは存在しない。
R1B、R2B、R3B及びR4Bは、それぞれ独立に、水素原子、アルキル基、シクロアルキル基、アルコキシ基、シクロアルコキシ基、アリール基、アリールオキシ基、1価の複素環基、置換アミノ基又はハロゲン原子を表し、これらの基は置換基を有していてもよい。R1B、R2B、R3B及びR4Bが複数存在する場合、それらはそれぞれ同一でも異なっていてもよい。R1BとR2B、R2BとR3B、及び、R3BとR4Bは、それぞれ結合して、それぞれが結合する原子とともに環を形成していてもよい。] - 陽極と、陰極と、前記陽極及び前記陰極の間に設けられた第1の有機層及び第2の有機層と、を有し、
前記第1の有機層及び前記第2の有機層が、発光層であり、
前記第1の有機層が、式(1’)で表される金属錯体を含有する層A’である、発光素子。
[式中、
Mは、ロジウム原子、パラジウム原子、イリジウム原子又は白金原子を表す。
n1は1以上の整数を表し、n2は0以上の整数を表し、n1+n2は2又は3である。
Mがロジウム原子又はイリジウム原子の場合、n1+n2は3であり、Mがパラジウム原子又は白金原子の場合、n1+n2は2である。
E1は、炭素原子又は窒素原子を表す。E1が複数存在する場合、それらは同一でも異なっていてもよい。
環Bは、芳香族炭化水素環又は芳香族複素環を表し、これらの環は置換基を有していてもよい。該置換基が複数存在する場合、それらは互いに結合して、それぞれが結合する原子とともに環を形成していてもよい。環Bが複数存在する場合、それらは同一でも異なっていてもよい。
Z1Aは、=N-で表される基又は=C(RZ1A)-で表される基を表す。Z1Aが複数存在する場合、それらは同一であっても異なっていてもよい。RZ1Aは、水素原子、アルキル基、シクロアルキル基、アルコキシ基、シクロアルコキシ基、アリール基、アリールオキシ基、1価の複素環基、置換アミノ基又はハロゲン原子を表し、これらの基は置換基を有していてもよい。
R1’は、炭素原子数5以上30以下のアルキル基を表し、該基は置換基を有していてもよい。R 1’ が複数存在する場合、それらは同一でも異なっていてもよい。
Ar1Aは、式(Ar-1A)で表される基を表す。Ar1Aが複数存在する場合、それらは同一でも異なっていてもよい。
A1-G1-A2は、アニオン性の2座配位子を表す。A1及びA2は、それぞれ独立に、炭素原子、酸素原子又は窒素原子を表し、これらの原子は環を構成する原子であってもよい。G1は、単結合、又は、A1及びA2とともに2座配位子を構成する原子団を表す。A1-G1-A2が複数存在する場合、それらは同一でも異なっていてもよい。]
[式中、
環Aは、芳香族炭化水素環又は芳香族複素環を表し、これらの環は置換基を有していてもよい。該置換基が複数存在する場合、それらは互いに結合して、それぞれが結合する原子とともに環を形成していてもよい。
R2及びR3は、それぞれ独立に、アルキル基、シクロアルキル基、アルコキシ基、シクロアルコキシ基、アリール基、アリールオキシ基、1価の複素環基、置換アミノ基又はハロゲン原子を表し、これらの基は置換基を有していてもよい。] - 前記第2の有機層が、
式(2)で表される金属錯体から水素原子1個以上を除いた基を有する構成単位を含む高分子化合物、及び、前記高分子化合物の架橋体のうち、少なくとも1種を含有する層B、又は、
式(2)で表される金属錯体を含有する層Cである、請求項3に記載の発光素子。
[式中、
M2は、ロジウム原子、パラジウム原子、イリジウム原子又は白金原子を表す。
n3は1以上の整数を表し、n4は0以上の整数を表し、n3+n4は2又は3である。
M2がロジウム原子又はイリジウム原子の場合、n3+n4は3であり、M2がパラジウム原子又は白金原子の場合、n3+n4は2である。
E4は、炭素原子又は窒素原子を表す。E4が複数存在する場合、それらは同一でも異なっていてもよい。
環L1は、6員の芳香族複素環を表し、この環は置換基を有していてもよい。該置換基が複数存在する場合、それらは互いに結合して、それぞれが結合する原子とともに環を形成していてもよい。環L1が複数存在する場合、それらは同一でも異なっていてもよい。
環L2は、芳香族炭化水素環又は芳香族複素環を表し、これらの環は置換基を有していてもよい。該置換基が複数存在する場合、それらは互いに結合して、それぞれが結合する原子とともに環を形成していてもよい。環L2が複数存在する場合、それらは同一でも異なっていてもよい。
環L1が有していてもよい置換基と環L2が有していてもよい置換基とは、互いに結合して、それぞれが結合する原子とともに環を形成していてもよい。
A3-G2-A4は、アニオン性の2座配位子を表す。A3及びA4は、それぞれ独立に、炭素原子、酸素原子又は窒素原子を表し、これらの原子は環を構成する原子であってもよい。G2は、単結合、又は、A3及びA4とともに2座配位子を構成する原子団を表す。A3-G2-A4が複数存在する場合、それらは同一でも異なっていてもよい。] - 陽極と、陰極と、前記陽極及び前記陰極の間に設けられた第1の有機層及び第2の有機層と、を有し、
前記第1の有機層が、式(1’)で表される金属錯体を含有する層A’であり、
前記第2の有機層が、
式(2)で表される金属錯体から水素原子1個以上を除いた基を有する構成単位を含む高分子化合物、及び、前記高分子化合物の架橋体のうち、少なくとも1種を含有する層B、又は、
式(2)で表される金属錯体を含有する層C
である、発光素子。
[式中、
Mは、ロジウム原子、パラジウム原子、イリジウム原子又は白金原子を表す。
n1は1以上の整数を表し、n2は0以上の整数を表し、n1+n2は2又は3である。
Mがロジウム原子又はイリジウム原子の場合、n1+n2は3であり、Mがパラジウム原子又は白金原子の場合、n1+n2は2である。
E1は、炭素原子又は窒素原子を表す。E1が複数存在する場合、それらは同一でも異なっていてもよい。
環Bは、芳香族炭化水素環又は芳香族複素環を表し、これらの環は置換基を有していてもよい。該置換基が複数存在する場合、それらは互いに結合して、それぞれが結合する原子とともに環を形成していてもよい。環Bが複数存在する場合、それらは同一でも異なっていてもよい。
Z1Aは、=N-で表される基又は=C(RZ1A)-で表される基を表す。Z1Aが複数存在する場合、それらは同一であっても異なっていてもよい。RZ1Aは、水素原子、アルキル基、シクロアルキル基、アルコキシ基、シクロアルコキシ基、アリール基、アリールオキシ基、1価の複素環基、置換アミノ基又はハロゲン原子を表し、これらの基は置換基を有していてもよい。
R1’は、炭素原子数5以上30以下のアルキル基を表し、該基は置換基を有していてもよい。R 1’ が複数存在する場合、それらは同一でも異なっていてもよい。
Ar1Aは、式(Ar-1A)で表される基を表す。Ar1Aが複数存在する場合、それらは同一でも異なっていてもよい。
A1-G1-A2は、アニオン性の2座配位子を表す。A1及びA2は、それぞれ独立に、炭素原子、酸素原子又は窒素原子を表し、これらの原子は環を構成する原子であってもよい。G1は、単結合、又は、A1及びA2とともに2座配位子を構成する原子団を表す。A1-G1-A2が複数存在する場合、それらは同一でも異なっていてもよい。]
[式中、
環Aは、芳香族炭化水素環又は芳香族複素環を表し、これらの環は置換基を有していてもよい。該置換基が複数存在する場合、それらは互いに結合して、それぞれが結合する原子とともに環を形成していてもよい。
R2及びR3は、それぞれ独立に、アルキル基、シクロアルキル基、アルコキシ基、シクロアルコキシ基、アリール基、アリールオキシ基、1価の複素環基、置換アミノ基又はハロゲン原子を表し、これらの基は置換基を有していてもよい。]
[式中、
M2は、ロジウム原子、パラジウム原子、イリジウム原子又は白金原子を表す。
n3は1以上の整数を表し、n4は0以上の整数を表し、n3+n4は2又は3である。
M2がロジウム原子又はイリジウム原子の場合、n3+n4は3であり、M2がパラジウム原子又は白金原子の場合、n3+n4は2である。
E4は、炭素原子又は窒素原子を表す。E4が複数存在する場合、それらは同一でも異なっていてもよい。
環L1は、6員の芳香族複素環を表し、この環は置換基を有していてもよい。該置換基が複数存在する場合、それらは互いに結合して、それぞれが結合する原子とともに環を形成していてもよい。環L1が複数存在する場合、それらは同一でも異なっていてもよい。
環L2は、芳香族炭化水素環又は芳香族複素環を表し、これらの環は置換基を有していてもよい。該置換基が複数存在する場合、それらは互いに結合して、それぞれが結合する原子とともに環を形成していてもよい。環L2が複数存在する場合、それらは同一でも異なっていてもよい。
環L1が有していてもよい置換基と環L2が有していてもよい置換基とは、互いに結合して、それぞれが結合する原子とともに環を形成していてもよい。
A3-G2-A4は、アニオン性の2座配位子を表す。A3及びA4は、それぞれ独立に、炭素原子、酸素原子又は窒素原子を表し、これらの原子は環を構成する原子であってもよい。G2は、単結合、又は、A3及びA4とともに2座配位子を構成する原子団を表す。A3-G2-A4が複数存在する場合、それらは同一でも異なっていてもよい。] - 前記第2の有機層が、前記層Bであり、
前記高分子化合物が、架橋基を有する構成単位を更に含む、請求項1、2、4及び5のいずれか一項に記載の発光素子。 - 前記第2の有機層が、前記層Bであり、
前記構成単位が、式(2-1B)で表される構成単位、式(2-2B)で表される構成単位、式(2-3B)で表される構成単位又は式(2-4B)で表される構成単位である、請求項1、2及び4~6のいずれか一項に記載の発光素子。
[式中、
M1Bは、式(2)で表される金属錯体から水素原子1個を除いた基を表す。
LCは、酸素原子、硫黄原子、-N(RA)-、-C(RB)2-、-C(RB)=C(RB)-、-C≡C-、アリーレン基又は2価の複素環基を表し、これらの基は置換基を有していてもよい。RAは、水素原子、アルキル基、シクロアルキル基、アリール基又は1価の複素環基を表し、これらの基は置換基を有していてもよい。RBは、水素原子、アルキル基、シクロアルキル基、アルコキシ基、シクロアルコキシ基、アリール基又は1価の複素環基を表し、これらの基は置換基を有していてもよい。複数存在するRBは、同一でも異なっていてもよく、互いに結合して、それぞれが結合する炭素原子とともに環を形成していてもよい。LCが複数存在する場合、それらは同一でも異なっていてもよい。
nc1は0以上の整数を表す。]
[式中、
M1Bは前記と同じ意味を表す。
Ld及びLeは、それぞれ独立に、酸素原子、硫黄原子、-N(RA)-、-C(RB)2-、-C(RB)=C(RB)-、-C≡C-、アリーレン基又は2価の複素環基を表し、これらの基は置換基を有していてもよい。RA及びRBは、前記と同じ意味を表す。Ld及びLeが複数存在する場合、それらはそれぞれ同一でも異なっていてもよい。
nd1及びne1は、それぞれ独立に、0以上の整数を表す。複数存在するnd1は、同一でも異なっていてもよい。
Ar1Mは、芳香族炭化水素基又は複素環基を表し、これらの基は置換基を有していてもよい。]
[式中、
Ld及びnd1は、前記と同じ意味を表す。
M2Bは、式(2)で表される金属錯体から水素原子2個を除いた基を表す。]
[式中、
Ld及びnd1は、前記と同じ意味を表す。
M3Bは、式(2)で表される金属錯体から水素原子3個を除いた基を表す。] - 前記式(Ar-1A)で表される基が、式(Ar-2A)で表される基である、請求項1~8のいずれか一項に記載の発光素子。
[式中、R2及びR3は、前記と同じ意味を表す。
環A1は、ベンゼン環、ピリジン環又はジアザベンゼン環を表し、E1A、E2A及びE3Aは、それぞれ独立に、窒素原子又は炭素原子を表す。E1Aが窒素原子の場合、R1Aは存在しない。E2Aが窒素原子の場合、R2Aは存在しない。E3Aが窒素原子の場合、R3Aは存在しない。
R1A、R2A及びR3Aは、それぞれ独立に、水素原子、アルキル基、シクロアルキル基、アルコキシ基、シクロアルコキシ基、アリール基、アリールオキシ基、1価の複素環基、置換アミノ基又はハロゲン原子を表し、これらの基は置換基を有していてもよい。R1AとR2A、及び、R2AとR3Aは、それぞれ結合して、それぞれが結合する原子とともに環を形成していてもよい。] - 前記式(2)で表される金属錯体が、式(2-B)で表される金属錯体である、請求項1~9のいずれか一項に記載の発光素子。
[式中、
M2、n3、n4及びA3-G2-A4は、前記と同じ意味を表す。
環L1Bは、ピリジン環又はピリミジン環を表し、環L2Bは、ベンゼン環、ピリジン環又はジアザベンゼン環を表し、E11B、E12B、E13B、E14B、E21B、E22B、E23B及びE24Bは、それぞれ独立に、窒素原子又は炭素原子を表す。E11B、E12B、E13B、E14B、E21B、E22B、E23B及びE24Bが複数存在する場合、それらはそれぞれ同一でも異なっていてもよい。E11Bが窒素原子の場合、R11Bは存在しない。E12Bが窒素原子の場合、R12Bは存在しない。E13Bが窒素原子の場合、R13Bは存在しない。E14Bが窒素原子の場合、R14Bは存在しない。E21Bが窒素原子の場合、R21Bは存在しない。E22Bが窒素原子の場合、R22Bは存在しない。E23Bが窒素原子の場合、R23Bは存在しない。E24Bが窒素原子の場合、R24Bは存在しない。
R11B、R12B、R13B、R14B、R21B、R22B、R23B及びR24Bは、それぞれ独立に、水素原子、アルキル基、シクロアルキル基、アルコキシ基、シクロアルコキシ基、アリール基、アリールオキシ基、1価の複素環基、置換アミノ基又はハロゲン原子を表し、これらの基は置換基を有していてもよい。R11B、R12B、R13B、R14B、R21B、R22B、R23B及びR24Bが複数存在する場合、それらはそれぞれ同一でも異なっていてもよい。R11BとR12B、R12BとR13B、R13BとR14B、R11BとR21B、R21BとR22B、R22BとR23B、及び、R23BとR24Bは、それぞれ結合して、それぞれが結合する原子とともに環を形成していてもよい。] - 前記式(2-B)で表される金属錯体が、式(2-B1)で表される金属錯体、式(2-B2)で表される金属錯体、式(2-B3)で表される金属錯体、式(2-B4)で表される金属錯体又は式(2-B5)で表される金属錯体である、請求項10に記載の発光素子。
[式中、
M2、n3、n4、R11B、R12B、R13B、R14B、R21B、R22B、R23B、R24B及びA3-G2-A4は、前記と同じ意味を表す。
n31及びn32は、それぞれ独立に、1以上の整数を表し、n31+n32は2又は3である。M2がロジウム原子又はイリジウム原子の場合、n31+n32は3であり、M2がパラジウム原子又は白金原子の場合、n31+n32は2である。
R15B、R16B、R17B及びR18Bは、それぞれ独立に、水素原子、アルキル基、シクロアルキル基、アルコキシ基、シクロアルコキシ基、アリール基、アリールオキシ基、1価の複素環基、置換アミノ基又はハロゲン原子を表し、これらの基は置換基を有していてもよい。R15B、R16B、R17B及びR18Bが複数存在する場合、それらはそれぞれ同一でも異なっていてもよい。R15BとR16B、R16BとR17B、及び、R17BとR18Bは、それぞれ結合して、それぞれが結合する原子とともに環を形成していてもよい。] - 前記第1の有機層が、式(H-1)で表される化合物、及び/又は、式(Y)で表される構成単位を含む高分子化合物を更に含有する、請求項1~11のいずれか一項に記載の発光素子。
[式中、
ArH1及びArH2は、それぞれ独立に、アリール基又は1価の複素環基を表し、これらの基は置換基を有していてもよい。
nH1及びnH2は、それぞれ独立に、0又は1を表す。nH1が複数存在する場合、それらは同一でも異なっていてもよい。複数存在するnH2は、同一でも異なっていてもよい。
nH3は、0以上10以下の整数を表す。
LH1は、アリーレン基、2価の複素環基、又は、-[C(RH11)2] nH11 -で表される基を表し、これらの基は置換基を有していてもよい。LH1が複数存在する場合、それらは同一でも異なっていてもよい。nH11は、1以上10以下の整数を表す。RH11は、水素原子、アルキル基、シクロアルキル基、アルコキシ基、シクロアルコキシ基、アリール基又は1価の複素環基を表し、これらの基は置換基を有していてもよい。複数存在するRH11は、同一でも異なっていてもよく、互いに結合して、それぞれが結合する炭素原子とともに環を形成していてもよい。
LH2は、-N(-LH21-RH21)-で表される基を表す。LH2が複数存在する場合、それらは同一でも異なっていてもよい。LH21は、単結合、アリーレン基又は2価の複素環基を表し、これらの基は置換基を有していてもよい。RH21は、水素原子、アルキル基、シクロアルキル基、アリール基又は1価の複素環基を表し、これらの基は置換基を有していてもよい。]
[式中、ArY1は、アリーレン基、2価の複素環基、又は、アリーレン基と2価の複素環基とが直接結合した2価の基を表し、これらの基は置換基を有していてもよい。] - 前記第1の有機層が、正孔輸送材料、正孔注入材料、電子輸送材料、電子注入材料、発光材料及び酸化防止剤からなる群より選ばれる少なくとも1種を更に含有する、請求項1~12のいずれか一項に記載の発光素子。
- 前記第1の有機層と前記第2の有機層とが隣接している、請求項1~13のいずれか一項に記載の発光素子。
- 前記第2の有機層が、前記陽極及び前記第1の有機層の間に設けられた層である、請求項1~14のいずれか一項に記載の発光素子。
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2016221919 | 2016-11-14 | ||
| JP2016221919 | 2016-11-14 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2018085505A JP2018085505A (ja) | 2018-05-31 |
| JP7017907B2 true JP7017907B2 (ja) | 2022-02-09 |
Family
ID=62237732
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2017219443A Active JP7017907B2 (ja) | 2016-11-14 | 2017-11-14 | 発光素子 |
Country Status (1)
| Country | Link |
|---|---|
| JP (1) | JP7017907B2 (ja) |
Families Citing this family (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| GB2550203A (en) * | 2016-05-13 | 2017-11-15 | Sumitomo Chemical Co | Light-emitting compound |
| JP6589032B1 (ja) * | 2018-10-25 | 2019-10-09 | 住友化学株式会社 | 発光素子 |
Citations (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2012046479A (ja) | 2009-11-02 | 2012-03-08 | Semiconductor Energy Lab Co Ltd | 有機金属錯体、発光素子、表示装置、電子機器、及び照明装置 |
| JP2013199473A (ja) | 2012-02-24 | 2013-10-03 | Semiconductor Energy Lab Co Ltd | 燐光性有機金属イリジウム錯体、発光素子、発光装置、電子機器、および照明装置 |
| WO2015151914A1 (ja) | 2014-04-04 | 2015-10-08 | コニカミノルタ株式会社 | 有機金属錯体の合成方法及び当該合成方法により合成された化合物を用いた有機エレクトロルミネッセンス素子 |
| WO2015163174A1 (ja) | 2014-04-25 | 2015-10-29 | 住友化学株式会社 | 発光素子 |
-
2017
- 2017-11-14 JP JP2017219443A patent/JP7017907B2/ja active Active
Patent Citations (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2012046479A (ja) | 2009-11-02 | 2012-03-08 | Semiconductor Energy Lab Co Ltd | 有機金属錯体、発光素子、表示装置、電子機器、及び照明装置 |
| JP2013199473A (ja) | 2012-02-24 | 2013-10-03 | Semiconductor Energy Lab Co Ltd | 燐光性有機金属イリジウム錯体、発光素子、発光装置、電子機器、および照明装置 |
| WO2015151914A1 (ja) | 2014-04-04 | 2015-10-08 | コニカミノルタ株式会社 | 有機金属錯体の合成方法及び当該合成方法により合成された化合物を用いた有機エレクトロルミネッセンス素子 |
| WO2015163174A1 (ja) | 2014-04-25 | 2015-10-29 | 住友化学株式会社 | 発光素子 |
Also Published As
| Publication number | Publication date |
|---|---|
| JP2018085505A (ja) | 2018-05-31 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP2021120952A (ja) | 組成物の製造方法 | |
| JP6468289B2 (ja) | 発光素子 | |
| JP6610536B2 (ja) | 発光素子およびそれに用いる組成物 | |
| WO2015145871A1 (ja) | 高分子化合物およびそれを用いた発光素子 | |
| JP7020420B2 (ja) | 発光素子 | |
| JP6881430B2 (ja) | 発光素子及び該発光素子に用いる高分子化合物 | |
| WO2015159744A1 (ja) | 組成物およびそれを用いた発光素子 | |
| JP2018083941A (ja) | 組成物及びそれを用いた発光素子 | |
| CN110574497B (zh) | 组合物和使用了该组合物的发光元件 | |
| JP6877976B2 (ja) | 発光素子 | |
| JP6826930B2 (ja) | 発光素子 | |
| JP6754774B2 (ja) | 発光素子 | |
| JP2017125087A (ja) | 高分子化合物及びそれを用いた発光素子 | |
| JP6642428B2 (ja) | 高分子化合物およびそれを用いた発光素子 | |
| JP7017907B2 (ja) | 発光素子 | |
| JP2020138934A (ja) | 金属錯体及び前記金属錯体を含む組成物 | |
| JP2018083940A (ja) | 組成物及びそれを用いた発光素子 | |
| JP6468928B2 (ja) | 高分子化合物およびそれを用いた発光素子 | |
| KR20190047099A (ko) | 발광 소자 | |
| JP6851189B2 (ja) | 発光素子及び金属錯体 | |
| JP7017908B2 (ja) | 発光素子 | |
| JPWO2019208648A1 (ja) | 発光素子 | |
| JP6941711B2 (ja) | 金属錯体及びそれを含有する発光素子 | |
| JP7192339B2 (ja) | 発光素子 | |
| JP6804465B2 (ja) | 組成物及びそれを用いた発光素子 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| AA64 | Notification of invalidation of claim of internal priority (with term) |
Free format text: JAPANESE INTERMEDIATE CODE: A241764 Effective date: 20171219 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20180125 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20200908 |
|
| A977 | Report on retrieval |
Free format text: JAPANESE INTERMEDIATE CODE: A971007 Effective date: 20210428 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20210511 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20210810 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20210831 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20211015 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20220118 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20220128 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 7017907 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |