JP6964191B2 - 新規な乳酸菌およびその使用 - Google Patents
新規な乳酸菌およびその使用 Download PDFInfo
- Publication number
- JP6964191B2 JP6964191B2 JP2020524353A JP2020524353A JP6964191B2 JP 6964191 B2 JP6964191 B2 JP 6964191B2 JP 2020524353 A JP2020524353 A JP 2020524353A JP 2020524353 A JP2020524353 A JP 2020524353A JP 6964191 B2 JP6964191 B2 JP 6964191B2
- Authority
- JP
- Japan
- Prior art keywords
- bifidobacterium longum
- lactobacillus plantarum
- lactic acid
- inflammatory
- kccm12089p
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
- JVTAAEKCZFNVCJ-UHFFFAOYSA-N lactic acid Chemical compound CC(O)C(O)=O JVTAAEKCZFNVCJ-UHFFFAOYSA-N 0.000 title description 166
- 241000894006 Bacteria Species 0.000 title description 85
- 239000004310 lactic acid Substances 0.000 title description 83
- 235000014655 lactic acid Nutrition 0.000 title description 83
- 240000006024 Lactobacillus plantarum Species 0.000 claims description 99
- 241001608472 Bifidobacterium longum Species 0.000 claims description 98
- 229940009291 bifidobacterium longum Drugs 0.000 claims description 97
- 235000013965 Lactobacillus plantarum Nutrition 0.000 claims description 92
- 229940072205 lactobacillus plantarum Drugs 0.000 claims description 92
- 239000000203 mixture Substances 0.000 claims description 51
- 208000027866 inflammatory disease Diseases 0.000 claims description 42
- 206010046914 Vaginal infection Diseases 0.000 claims description 33
- 201000008100 Vaginitis Diseases 0.000 claims description 33
- 206010061218 Inflammation Diseases 0.000 claims description 29
- 230000004054 inflammatory process Effects 0.000 claims description 29
- 108020004465 16S ribosomal RNA Proteins 0.000 claims description 19
- 230000002265 prevention Effects 0.000 claims description 19
- 206010009887 colitis Diseases 0.000 claims description 18
- 239000008194 pharmaceutical composition Substances 0.000 claims description 17
- 230000036541 health Effects 0.000 claims description 14
- 235000013376 functional food Nutrition 0.000 claims description 12
- 206010003246 arthritis Diseases 0.000 claims description 10
- 201000003146 cystitis Diseases 0.000 claims description 6
- FWMNVWWHGCHHJJ-SKKKGAJSSA-N 4-amino-1-[(2r)-6-amino-2-[[(2r)-2-[[(2r)-2-[[(2r)-2-amino-3-phenylpropanoyl]amino]-3-phenylpropanoyl]amino]-4-methylpentanoyl]amino]hexanoyl]piperidine-4-carboxylic acid Chemical compound C([C@H](C(=O)N[C@H](CC(C)C)C(=O)N[C@H](CCCCN)C(=O)N1CCC(N)(CC1)C(O)=O)NC(=O)[C@H](N)CC=1C=CC=CC=1)C1=CC=CC=C1 FWMNVWWHGCHHJJ-SKKKGAJSSA-N 0.000 claims description 5
- 201000004624 Dermatitis Diseases 0.000 claims description 5
- 208000004232 Enteritis Diseases 0.000 claims description 5
- 201000005569 Gout Diseases 0.000 claims description 5
- 206010065390 Inflammatory pain Diseases 0.000 claims description 5
- 208000008589 Obesity Diseases 0.000 claims description 5
- 206010033645 Pancreatitis Diseases 0.000 claims description 5
- 206010040047 Sepsis Diseases 0.000 claims description 5
- 201000002661 Spondylitis Diseases 0.000 claims description 5
- 208000006673 asthma Diseases 0.000 claims description 5
- 206010006451 bronchitis Diseases 0.000 claims description 5
- 206010012601 diabetes mellitus Diseases 0.000 claims description 5
- 208000006454 hepatitis Diseases 0.000 claims description 5
- 231100000283 hepatitis Toxicity 0.000 claims description 5
- 206010023332 keratitis Diseases 0.000 claims description 5
- 201000008383 nephritis Diseases 0.000 claims description 5
- 235000020824 obesity Nutrition 0.000 claims description 5
- 201000001245 periodontitis Diseases 0.000 claims description 5
- 206010034674 peritonitis Diseases 0.000 claims description 5
- 230000001225 therapeutic effect Effects 0.000 claims description 5
- 201000008827 tuberculosis Diseases 0.000 claims description 5
- 208000000143 urethritis Diseases 0.000 claims description 5
- 239000003814 drug Substances 0.000 claims description 4
- 229940079593 drug Drugs 0.000 claims description 3
- 230000006872 improvement Effects 0.000 claims description 2
- 208000007882 Gastritis Diseases 0.000 claims 4
- 208000013223 septicemia Diseases 0.000 claims 4
- 230000000694 effects Effects 0.000 description 32
- 241000207201 Gardnerella vaginalis Species 0.000 description 30
- 210000004027 cell Anatomy 0.000 description 23
- 210000001215 vagina Anatomy 0.000 description 16
- 238000010171 animal model Methods 0.000 description 14
- 241000699670 Mus sp. Species 0.000 description 13
- 102000003896 Myeloperoxidases Human genes 0.000 description 13
- 108090000235 Myeloperoxidases Proteins 0.000 description 13
- 230000001965 increasing effect Effects 0.000 description 11
- MZOFCQQQCNRIBI-VMXHOPILSA-N (3s)-4-[[(2s)-1-[[(2s)-1-[[(1s)-1-carboxy-2-hydroxyethyl]amino]-4-methyl-1-oxopentan-2-yl]amino]-5-(diaminomethylideneamino)-1-oxopentan-2-yl]amino]-3-[[2-[[(2s)-2,6-diaminohexanoyl]amino]acetyl]amino]-4-oxobutanoic acid Chemical compound OC[C@@H](C(O)=O)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](CCCN=C(N)N)NC(=O)[C@H](CC(O)=O)NC(=O)CNC(=O)[C@@H](N)CCCCN MZOFCQQQCNRIBI-VMXHOPILSA-N 0.000 description 10
- 108060008682 Tumor Necrosis Factor Proteins 0.000 description 10
- 102000000852 Tumor Necrosis Factor-alpha Human genes 0.000 description 10
- 210000002540 macrophage Anatomy 0.000 description 10
- -1 D-fluctose Chemical compound 0.000 description 9
- 239000000243 solution Substances 0.000 description 9
- 239000006228 supernatant Substances 0.000 description 9
- OKTJSMMVPCPJKN-UHFFFAOYSA-N Carbon Chemical compound [C] OKTJSMMVPCPJKN-UHFFFAOYSA-N 0.000 description 8
- 229910052799 carbon Inorganic materials 0.000 description 8
- 235000021109 kimchi Nutrition 0.000 description 8
- 238000000034 method Methods 0.000 description 8
- 102000004127 Cytokines Human genes 0.000 description 7
- 108090000695 Cytokines Proteins 0.000 description 7
- 241000186660 Lactobacillus Species 0.000 description 7
- 239000002158 endotoxin Substances 0.000 description 7
- 229940039696 lactobacillus Drugs 0.000 description 7
- 210000002429 large intestine Anatomy 0.000 description 7
- 229920006008 lipopolysaccharide Polymers 0.000 description 7
- 239000002609 medium Substances 0.000 description 7
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 6
- 241000699666 Mus <mouse, genus> Species 0.000 description 6
- DNIAPMSPPWPWGF-UHFFFAOYSA-N Propylene glycol Chemical compound CC(O)CO DNIAPMSPPWPWGF-UHFFFAOYSA-N 0.000 description 6
- 239000012980 RPMI-1640 medium Substances 0.000 description 6
- 210000000683 abdominal cavity Anatomy 0.000 description 6
- 239000003795 chemical substances by application Substances 0.000 description 6
- 210000003608 fece Anatomy 0.000 description 6
- 235000013305 food Nutrition 0.000 description 6
- 239000007788 liquid Substances 0.000 description 6
- 238000005259 measurement Methods 0.000 description 6
- 239000002773 nucleotide Substances 0.000 description 6
- 125000003729 nucleotide group Chemical group 0.000 description 6
- 238000002360 preparation method Methods 0.000 description 6
- WQZGKKKJIJFFOK-GASJEMHNSA-N Glucose Natural products OC[C@H]1OC(O)[C@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-GASJEMHNSA-N 0.000 description 5
- PEDCQBHIVMGVHV-UHFFFAOYSA-N Glycerine Chemical compound OCC(O)CO PEDCQBHIVMGVHV-UHFFFAOYSA-N 0.000 description 5
- 108010057466 NF-kappa B Proteins 0.000 description 5
- 102000003945 NF-kappa B Human genes 0.000 description 5
- 230000000844 anti-bacterial effect Effects 0.000 description 5
- 230000003078 antioxidant effect Effects 0.000 description 5
- SRBFZHDQGSBBOR-UHFFFAOYSA-N beta-D-Pyranose-Lyxose Natural products OC1COC(O)C(O)C1O SRBFZHDQGSBBOR-UHFFFAOYSA-N 0.000 description 5
- WQZGKKKJIJFFOK-SVZMEOIVSA-N (+)-Galactose Chemical compound OC[C@H]1OC(O)[C@H](O)[C@@H](O)[C@H]1O WQZGKKKJIJFFOK-SVZMEOIVSA-N 0.000 description 4
- NHJVRSWLHSJWIN-UHFFFAOYSA-N 2,4,6-trinitrobenzenesulfonic acid Chemical compound OS(=O)(=O)C1=C([N+]([O-])=O)C=C([N+]([O-])=O)C=C1[N+]([O-])=O NHJVRSWLHSJWIN-UHFFFAOYSA-N 0.000 description 4
- 241000193818 Atopobium Species 0.000 description 4
- 241001633064 Atopobium vaginae Species 0.000 description 4
- FBPFZTCFMRRESA-FSIIMWSLSA-N D-Glucitol Natural products OC[C@H](O)[C@H](O)[C@@H](O)[C@H](O)CO FBPFZTCFMRRESA-FSIIMWSLSA-N 0.000 description 4
- FBPFZTCFMRRESA-JGWLITMVSA-N D-glucitol Chemical compound OC[C@H](O)[C@@H](O)[C@H](O)[C@H](O)CO FBPFZTCFMRRESA-JGWLITMVSA-N 0.000 description 4
- 102100029064 Serine/threonine-protein kinase WNK1 Human genes 0.000 description 4
- 229930006000 Sucrose Natural products 0.000 description 4
- CZMRCDWAGMRECN-UGDNZRGBSA-N Sucrose Chemical compound O[C@H]1[C@H](O)[C@@H](CO)O[C@@]1(CO)O[C@@H]1[C@H](O)[C@@H](O)[C@H](O)[C@@H](CO)O1 CZMRCDWAGMRECN-UGDNZRGBSA-N 0.000 description 4
- 101710124574 Synaptotagmin-1 Proteins 0.000 description 4
- PYMYPHUHKUWMLA-LMVFSUKVSA-N aldehydo-D-ribose Chemical compound OC[C@@H](O)[C@@H](O)[C@@H](O)C=O PYMYPHUHKUWMLA-LMVFSUKVSA-N 0.000 description 4
- WQZGKKKJIJFFOK-VFUOTHLCSA-N beta-D-glucose Chemical compound OC[C@H]1O[C@@H](O)[C@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-VFUOTHLCSA-N 0.000 description 4
- 235000013361 beverage Nutrition 0.000 description 4
- 238000012258 culturing Methods 0.000 description 4
- 230000003247 decreasing effect Effects 0.000 description 4
- 201000010099 disease Diseases 0.000 description 4
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 description 4
- HHEAADYXPMHMCT-UHFFFAOYSA-N dpph Chemical compound [O-][N+](=O)C1=CC([N+](=O)[O-])=CC([N+]([O-])=O)=C1[N]N(C=1C=CC=CC=1)C1=CC=CC=C1 HHEAADYXPMHMCT-UHFFFAOYSA-N 0.000 description 4
- 238000002474 experimental method Methods 0.000 description 4
- 239000000796 flavoring agent Substances 0.000 description 4
- 235000013355 food flavoring agent Nutrition 0.000 description 4
- 238000009472 formulation Methods 0.000 description 4
- 238000003119 immunoblot Methods 0.000 description 4
- 208000015181 infectious disease Diseases 0.000 description 4
- 230000000813 microbial effect Effects 0.000 description 4
- 230000001766 physiological effect Effects 0.000 description 4
- 102000004169 proteins and genes Human genes 0.000 description 4
- 108090000623 proteins and genes Proteins 0.000 description 4
- 238000011084 recovery Methods 0.000 description 4
- 230000002829 reductive effect Effects 0.000 description 4
- 239000000600 sorbitol Substances 0.000 description 4
- 235000010356 sorbitol Nutrition 0.000 description 4
- 239000005720 sucrose Substances 0.000 description 4
- 210000001519 tissue Anatomy 0.000 description 4
- OWEGMIWEEQEYGQ-UHFFFAOYSA-N 100676-05-9 Natural products OC1C(O)C(O)C(CO)OC1OCC1C(O)C(O)C(O)C(OC2C(OC(O)C(O)C2O)CO)O1 OWEGMIWEEQEYGQ-UHFFFAOYSA-N 0.000 description 3
- 241000193830 Bacillus <bacterium> Species 0.000 description 3
- 208000004926 Bacterial Vaginosis Diseases 0.000 description 3
- FBPFZTCFMRRESA-KVTDHHQDSA-N D-Mannitol Chemical compound OC[C@@H](O)[C@@H](O)[C@H](O)[C@H](O)CO FBPFZTCFMRRESA-KVTDHHQDSA-N 0.000 description 3
- GUBGYTABKSRVRQ-PICCSMPSSA-N Maltose Natural products O[C@@H]1[C@@H](O)[C@H](O)[C@@H](CO)O[C@@H]1O[C@@H]1[C@@H](CO)OC(O)[C@H](O)[C@H]1O GUBGYTABKSRVRQ-PICCSMPSSA-N 0.000 description 3
- 241000124008 Mammalia Species 0.000 description 3
- 229930195725 Mannitol Natural products 0.000 description 3
- 239000000654 additive Substances 0.000 description 3
- 238000004458 analytical method Methods 0.000 description 3
- PYMYPHUHKUWMLA-UHFFFAOYSA-N arabinose Natural products OCC(O)C(O)C(O)C=O PYMYPHUHKUWMLA-UHFFFAOYSA-N 0.000 description 3
- GUBGYTABKSRVRQ-QUYVBRFLSA-N beta-maltose Chemical compound OC[C@H]1O[C@H](O[C@H]2[C@H](O)[C@@H](O)[C@H](O)O[C@@H]2CO)[C@H](O)[C@@H](O)[C@@H]1O GUBGYTABKSRVRQ-QUYVBRFLSA-N 0.000 description 3
- DLRVVLDZNNYCBX-ZZFZYMBESA-N beta-melibiose Chemical compound O[C@@H]1[C@@H](O)[C@@H](O)[C@@H](CO)O[C@@H]1OC[C@@H]1[C@@H](O)[C@H](O)[C@@H](O)[C@H](O)O1 DLRVVLDZNNYCBX-ZZFZYMBESA-N 0.000 description 3
- 230000007423 decrease Effects 0.000 description 3
- 230000006870 function Effects 0.000 description 3
- 230000002538 fungal effect Effects 0.000 description 3
- 238000000265 homogenisation Methods 0.000 description 3
- 239000000411 inducer Substances 0.000 description 3
- 230000028709 inflammatory response Effects 0.000 description 3
- 239000004615 ingredient Substances 0.000 description 3
- 238000002955 isolation Methods 0.000 description 3
- 239000000594 mannitol Substances 0.000 description 3
- 235000010355 mannitol Nutrition 0.000 description 3
- 239000000546 pharmaceutical excipient Substances 0.000 description 3
- 239000002504 physiological saline solution Substances 0.000 description 3
- 239000000047 product Substances 0.000 description 3
- 235000020183 skimmed milk Nutrition 0.000 description 3
- 235000000346 sugar Nutrition 0.000 description 3
- 239000000725 suspension Substances 0.000 description 3
- 238000012360 testing method Methods 0.000 description 3
- 210000004291 uterus Anatomy 0.000 description 3
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 3
- VOXZDWNPVJITMN-ZBRFXRBCSA-N 17β-estradiol Chemical compound OC1=CC=C2[C@H]3CC[C@](C)([C@H](CC4)O)[C@@H]4[C@@H]3CCC2=C1 VOXZDWNPVJITMN-ZBRFXRBCSA-N 0.000 description 2
- 102000007469 Actins Human genes 0.000 description 2
- 108010085238 Actins Proteins 0.000 description 2
- PLXMOAALOJOTIY-FPTXNFDTSA-N Aesculin Natural products OC[C@@H]1[C@@H](O)[C@H](O)[C@@H](O)[C@H](O)[C@H]1Oc2cc3C=CC(=O)Oc3cc2O PLXMOAALOJOTIY-FPTXNFDTSA-N 0.000 description 2
- 229920001817 Agar Polymers 0.000 description 2
- GUBGYTABKSRVRQ-XLOQQCSPSA-N Alpha-Lactose Chemical compound O[C@@H]1[C@@H](O)[C@@H](O)[C@@H](CO)O[C@H]1O[C@@H]1[C@@H](CO)O[C@H](O)[C@H](O)[C@H]1O GUBGYTABKSRVRQ-XLOQQCSPSA-N 0.000 description 2
- ZHGNHOOVYPHPNJ-UHFFFAOYSA-N Amigdalin Chemical compound FC(F)(F)C(=O)OCC1OC(OCC2OC(OC(C#N)C3=CC=CC=C3)C(OC(=O)C(F)(F)F)C(OC(=O)C(F)(F)F)C2OC(=O)C(F)(F)F)C(OC(=O)C(F)(F)F)C(OC(=O)C(F)(F)F)C1OC(=O)C(F)(F)F ZHGNHOOVYPHPNJ-UHFFFAOYSA-N 0.000 description 2
- CIWBSHSKHKDKBQ-JLAZNSOCSA-N Ascorbic acid Chemical compound OC[C@H](O)[C@H]1OC(=O)C(O)=C1O CIWBSHSKHKDKBQ-JLAZNSOCSA-N 0.000 description 2
- 241000186000 Bifidobacterium Species 0.000 description 2
- WNBCMONIPIJTSB-BGNCJLHMSA-N Cichoriin Natural products O([C@H]1[C@H](O)[C@@H](O)[C@@H](O)[C@@H](CO)O1)c1c(O)cc2c(OC(=O)C=C2)c1 WNBCMONIPIJTSB-BGNCJLHMSA-N 0.000 description 2
- 108020004414 DNA Proteins 0.000 description 2
- RTZKZFJDLAIYFH-UHFFFAOYSA-N Diethyl ether Chemical compound CCOCC RTZKZFJDLAIYFH-UHFFFAOYSA-N 0.000 description 2
- 238000008157 ELISA kit Methods 0.000 description 2
- 239000004386 Erythritol Substances 0.000 description 2
- UNXHWFMMPAWVPI-UHFFFAOYSA-N Erythritol Natural products OCC(O)C(O)CO UNXHWFMMPAWVPI-UHFFFAOYSA-N 0.000 description 2
- RFSUNEUAIZKAJO-ARQDHWQXSA-N Fructose Chemical compound OC[C@H]1O[C@](O)(CO)[C@@H](O)[C@@H]1O RFSUNEUAIZKAJO-ARQDHWQXSA-N 0.000 description 2
- 241000282412 Homo Species 0.000 description 2
- GUBGYTABKSRVRQ-QKKXKWKRSA-N Lactose Natural products OC[C@H]1O[C@@H](O[C@H]2[C@H](O)[C@@H](O)C(O)O[C@@H]2CO)[C@H](O)[C@@H](O)[C@H]1O GUBGYTABKSRVRQ-QKKXKWKRSA-N 0.000 description 2
- 241001465754 Metazoa Species 0.000 description 2
- 102100038280 Prostaglandin G/H synthase 2 Human genes 0.000 description 2
- 108050003267 Prostaglandin G/H synthase 2 Proteins 0.000 description 2
- KAESVJOAVNADME-UHFFFAOYSA-N Pyrrole Chemical compound C=1C=CNC=1 KAESVJOAVNADME-UHFFFAOYSA-N 0.000 description 2
- 239000012083 RIPA buffer Substances 0.000 description 2
- 239000012979 RPMI medium Substances 0.000 description 2
- NGFMICBWJRZIBI-JZRPKSSGSA-N Salicin Natural products O([C@H]1[C@H](O)[C@@H](O)[C@@H](O)[C@H](CO)O1)c1c(CO)cccc1 NGFMICBWJRZIBI-JZRPKSSGSA-N 0.000 description 2
- FAPWRFPIFSIZLT-UHFFFAOYSA-M Sodium chloride Chemical compound [Na+].[Cl-] FAPWRFPIFSIZLT-UHFFFAOYSA-M 0.000 description 2
- 244000299461 Theobroma cacao Species 0.000 description 2
- 108091023040 Transcription factor Proteins 0.000 description 2
- 102000040945 Transcription factor Human genes 0.000 description 2
- TVXBFESIOXBWNM-UHFFFAOYSA-N Xylitol Natural products OCCC(O)C(O)C(O)CCO TVXBFESIOXBWNM-UHFFFAOYSA-N 0.000 description 2
- 238000002835 absorbance Methods 0.000 description 2
- 239000008186 active pharmaceutical agent Substances 0.000 description 2
- 239000000443 aerosol Substances 0.000 description 2
- 239000008272 agar Substances 0.000 description 2
- NGFMICBWJRZIBI-UHFFFAOYSA-N alpha-salicin Natural products OC1C(O)C(O)C(CO)OC1OC1=CC=CC=C1CO NGFMICBWJRZIBI-UHFFFAOYSA-N 0.000 description 2
- 210000000436 anus Anatomy 0.000 description 2
- 239000003125 aqueous solvent Substances 0.000 description 2
- 230000033228 biological regulation Effects 0.000 description 2
- 230000037396 body weight Effects 0.000 description 2
- 239000001506 calcium phosphate Substances 0.000 description 2
- 229910000389 calcium phosphate Inorganic materials 0.000 description 2
- 235000011010 calcium phosphates Nutrition 0.000 description 2
- 150000001720 carbohydrates Chemical class 0.000 description 2
- 235000014633 carbohydrates Nutrition 0.000 description 2
- 235000019219 chocolate Nutrition 0.000 description 2
- 235000009508 confectionery Nutrition 0.000 description 2
- 238000007796 conventional method Methods 0.000 description 2
- 239000012228 culture supernatant Substances 0.000 description 2
- 230000034994 death Effects 0.000 description 2
- 238000004925 denaturation Methods 0.000 description 2
- 230000036425 denaturation Effects 0.000 description 2
- 235000015872 dietary supplement Nutrition 0.000 description 2
- 239000003085 diluting agent Substances 0.000 description 2
- POULHZVOKOAJMA-UHFFFAOYSA-N dodecanoic acid Chemical compound CCCCCCCCCCCC(O)=O POULHZVOKOAJMA-UHFFFAOYSA-N 0.000 description 2
- 239000002552 dosage form Substances 0.000 description 2
- 239000003937 drug carrier Substances 0.000 description 2
- 238000001962 electrophoresis Methods 0.000 description 2
- 239000000839 emulsion Substances 0.000 description 2
- UNXHWFMMPAWVPI-ZXZARUISSA-N erythritol Chemical compound OC[C@H](O)[C@H](O)CO UNXHWFMMPAWVPI-ZXZARUISSA-N 0.000 description 2
- 235000019414 erythritol Nutrition 0.000 description 2
- 229940009714 erythritol Drugs 0.000 description 2
- XHCADAYNFIFUHF-TVKJYDDYSA-N esculin Chemical compound O[C@@H]1[C@@H](O)[C@H](O)[C@@H](CO)O[C@H]1OC(C(=C1)O)=CC2=C1OC(=O)C=C2 XHCADAYNFIFUHF-TVKJYDDYSA-N 0.000 description 2
- 229940093496 esculin Drugs 0.000 description 2
- AWRMZKLXZLNBBK-UHFFFAOYSA-N esculin Natural products OC1OC(COc2cc3C=CC(=O)Oc3cc2O)C(O)C(O)C1O AWRMZKLXZLNBBK-UHFFFAOYSA-N 0.000 description 2
- 239000000284 extract Substances 0.000 description 2
- 239000003889 eye drop Substances 0.000 description 2
- 229940012356 eye drops Drugs 0.000 description 2
- 239000003885 eye ointment Substances 0.000 description 2
- 238000000855 fermentation Methods 0.000 description 2
- 230000004151 fermentation Effects 0.000 description 2
- 239000012530 fluid Substances 0.000 description 2
- 235000003599 food sweetener Nutrition 0.000 description 2
- 239000000499 gel Substances 0.000 description 2
- 150000004676 glycans Chemical class 0.000 description 2
- 235000011187 glycerol Nutrition 0.000 description 2
- 230000012010 growth Effects 0.000 description 2
- 230000009422 growth inhibiting effect Effects 0.000 description 2
- 230000001939 inductive effect Effects 0.000 description 2
- 230000002401 inhibitory effect Effects 0.000 description 2
- 239000008101 lactose Substances 0.000 description 2
- HQKMJHAJHXVSDF-UHFFFAOYSA-L magnesium stearate Chemical compound [Mg+2].CCCCCCCCCCCCCCCCCC([O-])=O.CCCCCCCCCCCCCCCCCC([O-])=O HQKMJHAJHXVSDF-UHFFFAOYSA-L 0.000 description 2
- 238000004519 manufacturing process Methods 0.000 description 2
- 210000004379 membrane Anatomy 0.000 description 2
- 239000012528 membrane Substances 0.000 description 2
- HEBKCHPVOIAQTA-UHFFFAOYSA-N meso ribitol Natural products OCC(O)C(O)C(O)CO HEBKCHPVOIAQTA-UHFFFAOYSA-N 0.000 description 2
- 244000005700 microbiome Species 0.000 description 2
- 210000004877 mucosa Anatomy 0.000 description 2
- 239000002674 ointment Substances 0.000 description 2
- 235000008390 olive oil Nutrition 0.000 description 2
- 239000004006 olive oil Substances 0.000 description 2
- 229920001282 polysaccharide Polymers 0.000 description 2
- 239000005017 polysaccharide Substances 0.000 description 2
- 239000003755 preservative agent Substances 0.000 description 2
- 230000004044 response Effects 0.000 description 2
- 230000002441 reversible effect Effects 0.000 description 2
- NGFMICBWJRZIBI-UJPOAAIJSA-N salicin Chemical compound O[C@@H]1[C@@H](O)[C@H](O)[C@@H](CO)O[C@H]1OC1=CC=CC=C1CO NGFMICBWJRZIBI-UJPOAAIJSA-N 0.000 description 2
- 229940120668 salicin Drugs 0.000 description 2
- 239000000523 sample Substances 0.000 description 2
- 210000002966 serum Anatomy 0.000 description 2
- 239000007787 solid Substances 0.000 description 2
- 239000000126 substance Substances 0.000 description 2
- 239000000829 suppository Substances 0.000 description 2
- 239000000375 suspending agent Substances 0.000 description 2
- 239000003765 sweetening agent Substances 0.000 description 2
- 208000024891 symptom Diseases 0.000 description 2
- 239000006188 syrup Substances 0.000 description 2
- 235000020357 syrup Nutrition 0.000 description 2
- 229940124597 therapeutic agent Drugs 0.000 description 2
- 229940071127 thioglycolate Drugs 0.000 description 2
- CWERGRDVMFNCDR-UHFFFAOYSA-M thioglycolate(1-) Chemical compound [O-]C(=O)CS CWERGRDVMFNCDR-UHFFFAOYSA-M 0.000 description 2
- 238000002054 transplantation Methods 0.000 description 2
- QORWJWZARLRLPR-UHFFFAOYSA-H tricalcium bis(phosphate) Chemical compound [Ca+2].[Ca+2].[Ca+2].[O-]P([O-])([O-])=O.[O-]P([O-])([O-])=O QORWJWZARLRLPR-UHFFFAOYSA-H 0.000 description 2
- RULSWEULPANCDV-PIXUTMIVSA-N turanose Chemical compound OC[C@@H](O)[C@@H](O)[C@@H](C(=O)CO)O[C@H]1O[C@H](CO)[C@@H](O)[C@H](O)[C@H]1O RULSWEULPANCDV-PIXUTMIVSA-N 0.000 description 2
- 229930003231 vitamin Natural products 0.000 description 2
- 235000013343 vitamin Nutrition 0.000 description 2
- 239000011782 vitamin Substances 0.000 description 2
- 229940088594 vitamin Drugs 0.000 description 2
- 239000000080 wetting agent Substances 0.000 description 2
- 239000000811 xylitol Substances 0.000 description 2
- 235000010447 xylitol Nutrition 0.000 description 2
- HEBKCHPVOIAQTA-SCDXWVJYSA-N xylitol Chemical compound OC[C@H](O)[C@@H](O)[C@H](O)CO HEBKCHPVOIAQTA-SCDXWVJYSA-N 0.000 description 2
- 229960002675 xylitol Drugs 0.000 description 2
- HDTRYLNUVZCQOY-UHFFFAOYSA-N α-D-glucopyranosyl-α-D-glucopyranoside Natural products OC1C(O)C(O)C(CO)OC1OC1C(O)C(O)C(O)C(CO)O1 HDTRYLNUVZCQOY-UHFFFAOYSA-N 0.000 description 1
- XDIYNQZUNSSENW-UUBOPVPUSA-N (2R,3S,4R,5R)-2,3,4,5,6-pentahydroxyhexanal Chemical compound OC[C@@H](O)[C@@H](O)[C@H](O)[C@@H](O)C=O.OC[C@@H](O)[C@@H](O)[C@H](O)[C@@H](O)C=O XDIYNQZUNSSENW-UUBOPVPUSA-N 0.000 description 1
- JKMHFZQWWAIEOD-UHFFFAOYSA-N 2-[4-(2-hydroxyethyl)piperazin-1-yl]ethanesulfonic acid Chemical compound OCC[NH+]1CCN(CCS([O-])(=O)=O)CC1 JKMHFZQWWAIEOD-UHFFFAOYSA-N 0.000 description 1
- JRBJSXQPQWSCCF-UHFFFAOYSA-N 3,3'-Dimethoxybenzidine Chemical compound C1=C(N)C(OC)=CC(C=2C=C(OC)C(N)=CC=2)=C1 JRBJSXQPQWSCCF-UHFFFAOYSA-N 0.000 description 1
- YRNWIFYIFSBPAU-UHFFFAOYSA-N 4-[4-(dimethylamino)phenyl]-n,n-dimethylaniline Chemical compound C1=CC(N(C)C)=CC=C1C1=CC=C(N(C)C)C=C1 YRNWIFYIFSBPAU-UHFFFAOYSA-N 0.000 description 1
- FHVDTGUDJYJELY-UHFFFAOYSA-N 6-{[2-carboxy-4,5-dihydroxy-6-(phosphanyloxy)oxan-3-yl]oxy}-4,5-dihydroxy-3-phosphanyloxane-2-carboxylic acid Chemical compound O1C(C(O)=O)C(P)C(O)C(O)C1OC1C(C(O)=O)OC(OP)C(O)C1O FHVDTGUDJYJELY-UHFFFAOYSA-N 0.000 description 1
- 208000035143 Bacterial infection Diseases 0.000 description 1
- 241000186018 Bifidobacterium adolescentis Species 0.000 description 1
- 238000009010 Bradford assay Methods 0.000 description 1
- 241000222122 Candida albicans Species 0.000 description 1
- 206010008342 Cervix carcinoma Diseases 0.000 description 1
- LZZYPRNAOMGNLH-UHFFFAOYSA-M Cetrimonium bromide Chemical compound [Br-].CCCCCCCCCCCCCCCC[N+](C)(C)C LZZYPRNAOMGNLH-UHFFFAOYSA-M 0.000 description 1
- 206010009944 Colon cancer Diseases 0.000 description 1
- 229920000858 Cyclodextrin Polymers 0.000 description 1
- GUBGYTABKSRVRQ-CUHNMECISA-N D-Cellobiose Chemical compound O[C@@H]1[C@@H](O)[C@H](O)[C@@H](CO)O[C@H]1O[C@@H]1[C@@H](CO)OC(O)[C@H](O)[C@H]1O GUBGYTABKSRVRQ-CUHNMECISA-N 0.000 description 1
- RFSUNEUAIZKAJO-VRPWFDPXSA-N D-Fructose Natural products OC[C@H]1OC(O)(CO)[C@@H](O)[C@@H]1O RFSUNEUAIZKAJO-VRPWFDPXSA-N 0.000 description 1
- ZZZCUOFIHGPKAK-UHFFFAOYSA-N D-erythro-ascorbic acid Natural products OCC1OC(=O)C(O)=C1O ZZZCUOFIHGPKAK-UHFFFAOYSA-N 0.000 description 1
- RGHNJXZEOKUKBD-SQOUGZDYSA-M D-gluconate Chemical compound OC[C@@H](O)[C@@H](O)[C@H](O)[C@@H](O)C([O-])=O RGHNJXZEOKUKBD-SQOUGZDYSA-M 0.000 description 1
- 150000008151 D-glucosides Chemical class 0.000 description 1
- WQZGKKKJIJFFOK-QTVWNMPRSA-N D-mannopyranose Chemical compound OC[C@H]1OC(O)[C@@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-QTVWNMPRSA-N 0.000 description 1
- SRBFZHDQGSBBOR-SOOFDHNKSA-N D-ribopyranose Chemical compound O[C@@H]1COC(O)[C@H](O)[C@@H]1O SRBFZHDQGSBBOR-SOOFDHNKSA-N 0.000 description 1
- SRBFZHDQGSBBOR-IOVATXLUSA-N D-xylopyranose Chemical compound O[C@@H]1COC(O)[C@H](O)[C@H]1O SRBFZHDQGSBBOR-IOVATXLUSA-N 0.000 description 1
- 238000007400 DNA extraction Methods 0.000 description 1
- 102000016928 DNA-directed DNA polymerase Human genes 0.000 description 1
- 108010014303 DNA-directed DNA polymerase Proteins 0.000 description 1
- 229920001353 Dextrin Polymers 0.000 description 1
- 239000004375 Dextrin Substances 0.000 description 1
- KCXVZYZYPLLWCC-UHFFFAOYSA-N EDTA Chemical compound OC(=O)CN(CC(O)=O)CCN(CC(O)=O)CC(O)=O KCXVZYZYPLLWCC-UHFFFAOYSA-N 0.000 description 1
- LVGKNOAMLMIIKO-UHFFFAOYSA-N Elaidinsaeure-aethylester Natural products CCCCCCCCC=CCCCCCCCC(=O)OCC LVGKNOAMLMIIKO-UHFFFAOYSA-N 0.000 description 1
- LYCAIKOWRPUZTN-UHFFFAOYSA-N Ethylene glycol Chemical compound OCCO LYCAIKOWRPUZTN-UHFFFAOYSA-N 0.000 description 1
- 229930091371 Fructose Natural products 0.000 description 1
- 239000005715 Fructose Substances 0.000 description 1
- 108010010803 Gelatin Proteins 0.000 description 1
- 229920000084 Gum arabic Polymers 0.000 description 1
- 239000007995 HEPES buffer Substances 0.000 description 1
- UETNIIAIRMUTSM-UHFFFAOYSA-N Jacareubin Natural products CC1(C)OC2=CC3Oc4c(O)c(O)ccc4C(=O)C3C(=C2C=C1)O UETNIIAIRMUTSM-UHFFFAOYSA-N 0.000 description 1
- 241001026509 Kata Species 0.000 description 1
- 240000001929 Lactobacillus brevis Species 0.000 description 1
- 235000013957 Lactobacillus brevis Nutrition 0.000 description 1
- 241000394636 Lactobacillus mucosae Species 0.000 description 1
- 241000186604 Lactobacillus reuteri Species 0.000 description 1
- 241000186612 Lactobacillus sakei Species 0.000 description 1
- 239000012741 Laemmli sample buffer Substances 0.000 description 1
- 239000005639 Lauric acid Substances 0.000 description 1
- 229920000168 Microcrystalline cellulose Polymers 0.000 description 1
- OVRNDRQMDRJTHS-UHFFFAOYSA-N N-acelyl-D-glucosamine Natural products CC(=O)NC1C(O)OC(CO)C(O)C1O OVRNDRQMDRJTHS-UHFFFAOYSA-N 0.000 description 1
- OVRNDRQMDRJTHS-FMDGEEDCSA-N N-acetyl-beta-D-glucosamine Chemical compound CC(=O)N[C@H]1[C@H](O)O[C@H](CO)[C@@H](O)[C@@H]1O OVRNDRQMDRJTHS-FMDGEEDCSA-N 0.000 description 1
- MBLBDJOUHNCFQT-LXGUWJNJSA-N N-acetylglucosamine Natural products CC(=O)N[C@@H](C=O)[C@@H](O)[C@H](O)[C@H](O)CO MBLBDJOUHNCFQT-LXGUWJNJSA-N 0.000 description 1
- AYRXSINWFIIFAE-UHFFFAOYSA-N O6-alpha-D-Galactopyranosyl-D-galactose Natural products OCC1OC(OCC(O)C(O)C(O)C(O)C=O)C(O)C(O)C1O AYRXSINWFIIFAE-UHFFFAOYSA-N 0.000 description 1
- 206010030113 Oedema Diseases 0.000 description 1
- 240000007594 Oryza sativa Species 0.000 description 1
- 235000007164 Oryza sativa Nutrition 0.000 description 1
- 102000003992 Peroxidases Human genes 0.000 description 1
- 239000002202 Polyethylene glycol Substances 0.000 description 1
- 241000288906 Primates Species 0.000 description 1
- 238000011529 RT qPCR Methods 0.000 description 1
- MUPFEKGTMRGPLJ-RMMQSMQOSA-N Raffinose Natural products O(C[C@H]1[C@@H](O)[C@H](O)[C@@H](O)[C@@H](O[C@@]2(CO)[C@H](O)[C@@H](O)[C@@H](CO)O2)O1)[C@@H]1[C@H](O)[C@@H](O)[C@@H](O)[C@@H](CO)O1 MUPFEKGTMRGPLJ-RMMQSMQOSA-N 0.000 description 1
- 244000088415 Raphanus sativus Species 0.000 description 1
- 235000006140 Raphanus sativus var sativus Nutrition 0.000 description 1
- 208000019802 Sexually transmitted disease Diseases 0.000 description 1
- 229920002472 Starch Polymers 0.000 description 1
- 102000000591 Tight Junction Proteins Human genes 0.000 description 1
- 108010002321 Tight Junction Proteins Proteins 0.000 description 1
- HDTRYLNUVZCQOY-WSWWMNSNSA-N Trehalose Natural products O[C@@H]1[C@@H](O)[C@@H](O)[C@@H](CO)O[C@@H]1O[C@@H]1[C@H](O)[C@@H](O)[C@@H](O)[C@@H](CO)O1 HDTRYLNUVZCQOY-WSWWMNSNSA-N 0.000 description 1
- 101710162629 Trypsin inhibitor Proteins 0.000 description 1
- 229940122618 Trypsin inhibitor Drugs 0.000 description 1
- MUPFEKGTMRGPLJ-UHFFFAOYSA-N UNPD196149 Natural products OC1C(O)C(CO)OC1(CO)OC1C(O)C(O)C(O)C(COC2C(C(O)C(O)C(CO)O2)O)O1 MUPFEKGTMRGPLJ-UHFFFAOYSA-N 0.000 description 1
- 208000006105 Uterine Cervical Neoplasms Diseases 0.000 description 1
- 229930003268 Vitamin C Natural products 0.000 description 1
- 239000000205 acacia gum Substances 0.000 description 1
- 235000010489 acacia gum Nutrition 0.000 description 1
- 230000002378 acidificating effect Effects 0.000 description 1
- 230000004913 activation Effects 0.000 description 1
- 239000004480 active ingredient Substances 0.000 description 1
- 230000000996 additive effect Effects 0.000 description 1
- 235000013334 alcoholic beverage Nutrition 0.000 description 1
- 150000001298 alcohols Chemical class 0.000 description 1
- 229940072056 alginate Drugs 0.000 description 1
- 235000010443 alginic acid Nutrition 0.000 description 1
- 229920000615 alginic acid Polymers 0.000 description 1
- HDTRYLNUVZCQOY-LIZSDCNHSA-N alpha,alpha-trehalose Chemical compound O[C@@H]1[C@@H](O)[C@H](O)[C@@H](CO)O[C@@H]1O[C@@H]1[C@H](O)[C@@H](O)[C@H](O)[C@@H](CO)O1 HDTRYLNUVZCQOY-LIZSDCNHSA-N 0.000 description 1
- 239000003242 anti bacterial agent Substances 0.000 description 1
- 230000003110 anti-inflammatory effect Effects 0.000 description 1
- 229940088710 antibiotic agent Drugs 0.000 description 1
- 229940121375 antifungal agent Drugs 0.000 description 1
- 239000003429 antifungal agent Substances 0.000 description 1
- PYMYPHUHKUWMLA-WDCZJNDASA-N arabinose Chemical compound OC[C@@H](O)[C@@H](O)[C@H](O)C=O PYMYPHUHKUWMLA-WDCZJNDASA-N 0.000 description 1
- 230000001580 bacterial effect Effects 0.000 description 1
- 208000022362 bacterial infectious disease Diseases 0.000 description 1
- 230000009286 beneficial effect Effects 0.000 description 1
- 230000008901 benefit Effects 0.000 description 1
- 239000011230 binding agent Substances 0.000 description 1
- 230000001164 bioregulatory effect Effects 0.000 description 1
- 235000008429 bread Nutrition 0.000 description 1
- 239000000872 buffer Substances 0.000 description 1
- 239000004067 bulking agent Substances 0.000 description 1
- 239000000378 calcium silicate Substances 0.000 description 1
- 229910052918 calcium silicate Inorganic materials 0.000 description 1
- 235000012241 calcium silicate Nutrition 0.000 description 1
- OYACROKNLOSFPA-UHFFFAOYSA-N calcium;dioxido(oxo)silane Chemical compound [Ca+2].[O-][Si]([O-])=O OYACROKNLOSFPA-UHFFFAOYSA-N 0.000 description 1
- 244000309466 calf Species 0.000 description 1
- 229940095731 candida albicans Drugs 0.000 description 1
- 229940041514 candida albicans extract Drugs 0.000 description 1
- 239000002775 capsule Substances 0.000 description 1
- 150000004649 carbonic acid derivatives Chemical class 0.000 description 1
- 210000004534 cecum Anatomy 0.000 description 1
- 239000001913 cellulose Substances 0.000 description 1
- 235000010980 cellulose Nutrition 0.000 description 1
- 229920002678 cellulose Polymers 0.000 description 1
- 238000005119 centrifugation Methods 0.000 description 1
- 201000010881 cervical cancer Diseases 0.000 description 1
- 230000008859 change Effects 0.000 description 1
- 235000013351 cheese Nutrition 0.000 description 1
- 239000007795 chemical reaction product Substances 0.000 description 1
- 229940110456 cocoa butter Drugs 0.000 description 1
- 235000019868 cocoa butter Nutrition 0.000 description 1
- 239000000084 colloidal system Substances 0.000 description 1
- 210000001072 colon Anatomy 0.000 description 1
- 208000029742 colonic neoplasm Diseases 0.000 description 1
- 239000003086 colorant Substances 0.000 description 1
- 238000012790 confirmation Methods 0.000 description 1
- 239000006071 cream Substances 0.000 description 1
- 210000004748 cultured cell Anatomy 0.000 description 1
- 235000013365 dairy product Nutrition 0.000 description 1
- 230000007123 defense Effects 0.000 description 1
- 235000019425 dextrin Nutrition 0.000 description 1
- 239000008121 dextrose Substances 0.000 description 1
- 150000002016 disaccharides Chemical class 0.000 description 1
- 239000007884 disintegrant Substances 0.000 description 1
- 239000003792 electrolyte Substances 0.000 description 1
- 239000003623 enhancer Substances 0.000 description 1
- 150000002148 esters Chemical class 0.000 description 1
- 229960005309 estradiol Drugs 0.000 description 1
- LVGKNOAMLMIIKO-QXMHVHEDSA-N ethyl oleate Chemical compound CCCCCCCC\C=C/CCCCCCCC(=O)OCC LVGKNOAMLMIIKO-QXMHVHEDSA-N 0.000 description 1
- 229940093471 ethyl oleate Drugs 0.000 description 1
- 230000029142 excretion Effects 0.000 description 1
- 230000002349 favourable effect Effects 0.000 description 1
- 235000021107 fermented food Nutrition 0.000 description 1
- 230000001605 fetal effect Effects 0.000 description 1
- 239000000945 filler Substances 0.000 description 1
- 235000012041 food component Nutrition 0.000 description 1
- 239000005417 food ingredient Substances 0.000 description 1
- 239000003205 fragrance Substances 0.000 description 1
- 230000008014 freezing Effects 0.000 description 1
- 238000007710 freezing Methods 0.000 description 1
- 235000012055 fruits and vegetables Nutrition 0.000 description 1
- 235000020510 functional beverage Nutrition 0.000 description 1
- 239000008273 gelatin Substances 0.000 description 1
- 229920000159 gelatin Polymers 0.000 description 1
- 235000019322 gelatine Nutrition 0.000 description 1
- 235000011852 gelatine desserts Nutrition 0.000 description 1
- DLRVVLDZNNYCBX-CQUJWQHSSA-N gentiobiose Chemical compound O[C@@H]1[C@@H](O)[C@H](O)[C@@H](CO)O[C@H]1OC[C@@H]1[C@@H](O)[C@H](O)[C@@H](O)C(O)O1 DLRVVLDZNNYCBX-CQUJWQHSSA-N 0.000 description 1
- 229940050410 gluconate Drugs 0.000 description 1
- 239000008103 glucose Substances 0.000 description 1
- 239000008187 granular material Substances 0.000 description 1
- 235000015243 ice cream Nutrition 0.000 description 1
- 238000000338 in vitro Methods 0.000 description 1
- 230000006698 induction Effects 0.000 description 1
- 230000002757 inflammatory effect Effects 0.000 description 1
- 230000005764 inhibitory process Effects 0.000 description 1
- 239000007972 injectable composition Substances 0.000 description 1
- 229910052500 inorganic mineral Inorganic materials 0.000 description 1
- 239000007928 intraperitoneal injection Substances 0.000 description 1
- 238000001990 intravenous administration Methods 0.000 description 1
- 229940001882 lactobacillus reuteri Drugs 0.000 description 1
- 239000000865 liniment Substances 0.000 description 1
- 239000012669 liquid formulation Substances 0.000 description 1
- 229940057995 liquid paraffin Drugs 0.000 description 1
- 244000144972 livestock Species 0.000 description 1
- 239000006210 lotion Substances 0.000 description 1
- 239000012139 lysis buffer Substances 0.000 description 1
- 229960003511 macrogol Drugs 0.000 description 1
- 235000019359 magnesium stearate Nutrition 0.000 description 1
- 235000013372 meat Nutrition 0.000 description 1
- 230000008018 melting Effects 0.000 description 1
- 238000002844 melting Methods 0.000 description 1
- 229920000609 methyl cellulose Polymers 0.000 description 1
- 239000001923 methylcellulose Substances 0.000 description 1
- 235000010981 methylcellulose Nutrition 0.000 description 1
- LXCFILQKKLGQFO-UHFFFAOYSA-N methylparaben Chemical compound COC(=O)C1=CC=C(O)C=C1 LXCFILQKKLGQFO-UHFFFAOYSA-N 0.000 description 1
- 239000008108 microcrystalline cellulose Substances 0.000 description 1
- 229940016286 microcrystalline cellulose Drugs 0.000 description 1
- 235000019813 microcrystalline cellulose Nutrition 0.000 description 1
- 239000011707 mineral Substances 0.000 description 1
- 235000010755 mineral Nutrition 0.000 description 1
- 235000010446 mineral oil Nutrition 0.000 description 1
- 239000002480 mineral oil Substances 0.000 description 1
- 150000002772 monosaccharides Chemical class 0.000 description 1
- 210000004400 mucous membrane Anatomy 0.000 description 1
- 229950006780 n-acetylglucosamine Drugs 0.000 description 1
- 231100000956 nontoxicity Toxicity 0.000 description 1
- 235000012149 noodles Nutrition 0.000 description 1
- 210000000056 organ Anatomy 0.000 description 1
- 150000007524 organic acids Chemical class 0.000 description 1
- 235000005985 organic acids Nutrition 0.000 description 1
- 230000008520 organization Effects 0.000 description 1
- 238000007911 parenteral administration Methods 0.000 description 1
- 239000006072 paste Substances 0.000 description 1
- 229920003175 pectinic acid Polymers 0.000 description 1
- 108040007629 peroxidase activity proteins Proteins 0.000 description 1
- 239000008363 phosphate buffer Substances 0.000 description 1
- 239000006187 pill Substances 0.000 description 1
- 235000013550 pizza Nutrition 0.000 description 1
- 229920001223 polyethylene glycol Polymers 0.000 description 1
- 229920000136 polysorbate Polymers 0.000 description 1
- 239000001267 polyvinylpyrrolidone Substances 0.000 description 1
- 229920000036 polyvinylpyrrolidone Polymers 0.000 description 1
- 235000013855 polyvinylpyrrolidone Nutrition 0.000 description 1
- 239000013641 positive control Substances 0.000 description 1
- 239000000843 powder Substances 0.000 description 1
- 239000002244 precipitate Substances 0.000 description 1
- 230000008569 process Effects 0.000 description 1
- 230000035755 proliferation Effects 0.000 description 1
- 230000000069 prophylactic effect Effects 0.000 description 1
- QELSKZZBTMNZEB-UHFFFAOYSA-N propylparaben Chemical compound CCCOC(=O)C1=CC=C(O)C=C1 QELSKZZBTMNZEB-UHFFFAOYSA-N 0.000 description 1
- 229960003415 propylparaben Drugs 0.000 description 1
- 230000001681 protective effect Effects 0.000 description 1
- 238000000746 purification Methods 0.000 description 1
- 238000011002 quantification Methods 0.000 description 1
- MUPFEKGTMRGPLJ-ZQSKZDJDSA-N raffinose Chemical compound O[C@H]1[C@H](O)[C@@H](CO)O[C@@]1(CO)O[C@@H]1[C@H](O)[C@@H](O)[C@H](O)[C@@H](CO[C@@H]2[C@@H]([C@@H](O)[C@@H](O)[C@@H](CO)O2)O)O1 MUPFEKGTMRGPLJ-ZQSKZDJDSA-N 0.000 description 1
- 238000011160 research Methods 0.000 description 1
- 230000033764 rhythmic process Effects 0.000 description 1
- 235000009566 rice Nutrition 0.000 description 1
- 150000003839 salts Chemical class 0.000 description 1
- 239000012723 sample buffer Substances 0.000 description 1
- 235000013580 sausages Nutrition 0.000 description 1
- HFHDHCJBZVLPGP-UHFFFAOYSA-N schardinger α-dextrin Chemical compound O1C(C(C2O)O)C(CO)OC2OC(C(C2O)O)C(CO)OC2OC(C(C2O)O)C(CO)OC2OC(C(O)C2O)C(CO)OC2OC(C(C2O)O)C(CO)OC2OC2C(O)C(O)C1OC2CO HFHDHCJBZVLPGP-UHFFFAOYSA-N 0.000 description 1
- 230000028327 secretion Effects 0.000 description 1
- 230000035945 sensitivity Effects 0.000 description 1
- 235000011888 snacks Nutrition 0.000 description 1
- 239000011780 sodium chloride Substances 0.000 description 1
- 239000007901 soft capsule Substances 0.000 description 1
- 235000014214 soft drink Nutrition 0.000 description 1
- 235000014347 soups Nutrition 0.000 description 1
- 241000894007 species Species 0.000 description 1
- 239000007921 spray Substances 0.000 description 1
- 239000003381 stabilizer Substances 0.000 description 1
- 239000008107 starch Substances 0.000 description 1
- 235000019698 starch Nutrition 0.000 description 1
- 238000007920 subcutaneous administration Methods 0.000 description 1
- 150000005846 sugar alcohols Chemical class 0.000 description 1
- 150000008163 sugars Chemical class 0.000 description 1
- NCEXYHBECQHGNR-QZQOTICOSA-N sulfasalazine Chemical compound C1=C(O)C(C(=O)O)=CC(\N=N\C=2C=CC(=CC=2)S(=O)(=O)NC=2N=CC=CC=2)=C1 NCEXYHBECQHGNR-QZQOTICOSA-N 0.000 description 1
- 229960001940 sulfasalazine Drugs 0.000 description 1
- NCEXYHBECQHGNR-UHFFFAOYSA-N sulfasalazine Natural products C1=C(O)C(C(=O)O)=CC(N=NC=2C=CC(=CC=2)S(=O)(=O)NC=2N=CC=CC=2)=C1 NCEXYHBECQHGNR-UHFFFAOYSA-N 0.000 description 1
- 230000001629 suppression Effects 0.000 description 1
- 239000004094 surface-active agent Substances 0.000 description 1
- 230000002459 sustained effect Effects 0.000 description 1
- 238000013268 sustained release Methods 0.000 description 1
- 239000012730 sustained-release form Substances 0.000 description 1
- 239000003826 tablet Substances 0.000 description 1
- 239000000454 talc Substances 0.000 description 1
- 229910052623 talc Inorganic materials 0.000 description 1
- 235000012222 talc Nutrition 0.000 description 1
- 235000013616 tea Nutrition 0.000 description 1
- 229940126585 therapeutic drug Drugs 0.000 description 1
- 239000002562 thickening agent Substances 0.000 description 1
- 238000011200 topical administration Methods 0.000 description 1
- 231100000419 toxicity Toxicity 0.000 description 1
- 230000001988 toxicity Effects 0.000 description 1
- 239000002753 trypsin inhibitor Substances 0.000 description 1
- 241001148471 unidentified anaerobic bacterium Species 0.000 description 1
- 235000015112 vegetable and seed oil Nutrition 0.000 description 1
- 239000008158 vegetable oil Substances 0.000 description 1
- 235000019154 vitamin C Nutrition 0.000 description 1
- 239000011718 vitamin C Substances 0.000 description 1
- 150000003722 vitamin derivatives Chemical class 0.000 description 1
- 238000005406 washing Methods 0.000 description 1
- 238000001262 western blot Methods 0.000 description 1
- 239000012138 yeast extract Substances 0.000 description 1
Images
Classifications
-
- A—HUMAN NECESSITIES
- A23—FOODS OR FOODSTUFFS; TREATMENT THEREOF, NOT COVERED BY OTHER CLASSES
- A23L—FOODS, FOODSTUFFS, OR NON-ALCOHOLIC BEVERAGES, NOT COVERED BY SUBCLASSES A21D OR A23B-A23J; THEIR PREPARATION OR TREATMENT, e.g. COOKING, MODIFICATION OF NUTRITIVE QUALITIES, PHYSICAL TREATMENT; PRESERVATION OF FOODS OR FOODSTUFFS, IN GENERAL
- A23L33/00—Modifying nutritive qualities of foods; Dietetic products; Preparation or treatment thereof
- A23L33/10—Modifying nutritive qualities of foods; Dietetic products; Preparation or treatment thereof using additives
- A23L33/135—Bacteria or derivatives thereof, e.g. probiotics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K35/00—Medicinal preparations containing materials or reaction products thereof with undetermined constitution
- A61K35/66—Microorganisms or materials therefrom
- A61K35/74—Bacteria
- A61K35/741—Probiotics
- A61K35/744—Lactic acid bacteria, e.g. enterococci, pediococci, lactococci, streptococci or leuconostocs
- A61K35/745—Bifidobacteria
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K35/00—Medicinal preparations containing materials or reaction products thereof with undetermined constitution
- A61K35/66—Microorganisms or materials therefrom
- A61K35/74—Bacteria
- A61K35/741—Probiotics
- A61K35/744—Lactic acid bacteria, e.g. enterococci, pediococci, lactococci, streptococci or leuconostocs
- A61K35/747—Lactobacilli, e.g. L. acidophilus or L. brevis
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P19/00—Drugs for skeletal disorders
- A61P19/08—Drugs for skeletal disorders for bone diseases, e.g. rachitism, Paget's disease
- A61P19/10—Drugs for skeletal disorders for bone diseases, e.g. rachitism, Paget's disease for osteoporosis
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/24—Antidepressants
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P3/00—Drugs for disorders of the metabolism
- A61P3/04—Anorexiants; Antiobesity agents
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N1/00—Microorganisms, e.g. protozoa; Compositions thereof; Processes of propagating, maintaining or preserving microorganisms or compositions thereof; Processes of preparing or isolating a composition containing a microorganism; Culture media therefor
- C12N1/20—Bacteria; Culture media therefor
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N1/00—Microorganisms, e.g. protozoa; Compositions thereof; Processes of propagating, maintaining or preserving microorganisms or compositions thereof; Processes of preparing or isolating a composition containing a microorganism; Culture media therefor
- C12N1/20—Bacteria; Culture media therefor
- C12N1/205—Bacterial isolates
-
- A—HUMAN NECESSITIES
- A23—FOODS OR FOODSTUFFS; TREATMENT THEREOF, NOT COVERED BY OTHER CLASSES
- A23V—INDEXING SCHEME RELATING TO FOODS, FOODSTUFFS OR NON-ALCOHOLIC BEVERAGES AND LACTIC OR PROPIONIC ACID BACTERIA USED IN FOODSTUFFS OR FOOD PREPARATION
- A23V2002/00—Food compositions, function of food ingredients or processes for food or foodstuffs
-
- A—HUMAN NECESSITIES
- A23—FOODS OR FOODSTUFFS; TREATMENT THEREOF, NOT COVERED BY OTHER CLASSES
- A23V—INDEXING SCHEME RELATING TO FOODS, FOODSTUFFS OR NON-ALCOHOLIC BEVERAGES AND LACTIC OR PROPIONIC ACID BACTERIA USED IN FOODSTUFFS OR FOOD PREPARATION
- A23V2200/00—Function of food ingredients
- A23V2200/30—Foods, ingredients or supplements having a functional effect on health
- A23V2200/32—Foods, ingredients or supplements having a functional effect on health having an effect on the health of the digestive tract
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K35/00—Medicinal preparations containing materials or reaction products thereof with undetermined constitution
- A61K2035/11—Medicinal preparations comprising living procariotic cells
- A61K2035/115—Probiotics
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12R—INDEXING SCHEME ASSOCIATED WITH SUBCLASSES C12C - C12Q, RELATING TO MICROORGANISMS
- C12R2001/00—Microorganisms ; Processes using microorganisms
- C12R2001/01—Bacteria or Actinomycetales ; using bacteria or Actinomycetales
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12R—INDEXING SCHEME ASSOCIATED WITH SUBCLASSES C12C - C12Q, RELATING TO MICROORGANISMS
- C12R2001/00—Microorganisms ; Processes using microorganisms
- C12R2001/01—Bacteria or Actinomycetales ; using bacteria or Actinomycetales
- C12R2001/225—Lactobacillus
- C12R2001/25—Lactobacillus plantarum
Description
具体的には、本発明の薬学組成物に含まれるラクトバチルス・プランタラムNK3は、その生菌体、その死菌体、その培養物、その破砕物またはその抽出物であってもよいが、炎症疾患の予防または治療の効果を達成できるラクトバチルス・プランタラムNK3の形態であれば、特に制限されない。
具体的には、本発明の薬学組成物に含まれるビフィドバクテリウム・ロンガムNK49は、その生菌体、その死菌体、その培養物、その破砕物またはその抽出物であってもよいが、炎症疾患の予防または治療の効果を達成できるラクトバチルス・プランタラムNK3の形態であれば、特に制限されない。
具体的には、前記炎症疾患は膣炎であってもよい。
具体的には、前記炎症疾患は大腸炎であってもよい。
ヒトの糞便をGAM液体培地(GAM broth;Nissui Pharmaceutical、Japan)に入れて懸濁した。その後、上澄みを取ってBL寒天培地(BL agar medium;Nissui Pharmaceutical、Japan)に移植し、37℃で約48時間嫌気的に培養した後、コロニー(colony)を形成した菌株を分離した。
白菜キムチ、大根キムチまたはネギギムチを各々破砕し、破砕上澄みを取ってMRS寒天培地(MRS agar medium;Difco、USA)に移植し、37℃で約48時間嫌気的に培養した後、コロニー(colony)を形成した菌株を分離した。
ヒトの糞便またはキムチから分離した菌株の生理学的特性および16S rDNA配列を分析して菌株の種を確定し、菌株名を付与した。付与された乳酸菌の菌株名は下記表1の通りである。具体的には、キムチから分離した乳酸菌は、5種のラクトバチルス・プランタラム(Lactobacillus plantarum)(表1の管理番号1〜5)、5種のラクトバチルス・ブレビス(Lactobacillus brevis)(表1の管理番号6〜10)、5種のラクトバチルス・サケイ(Lactobacillus sakei)(表1の管理番号11〜15)、および5種のラクトバチルス・カルバタス(Lactobacillus curvatus)(表1の管理番号16〜20)であった。ヒトの糞便から分離した乳酸菌は、5種のラクトバチルス・ラムノサス(Lactobacillus rhamnosus)(表1の管理番号21〜25)、5種のラクトバチルス・プランタラム(Lactobacillus plantarum)(表1の管理番号26〜30)、5種のラクトバチルス・ロイテリ(Lactobacillus reuteri)(表1の管理番号31〜35)、4種のラクトバチルス・ジョンソニー(Lactobacillus johnsonii)(表1の管理番号36〜39)、3種のラクトバチルス・ムコサエ(Lactobacillus mucosae)(表1の管理番号40〜42)、3種のビフィドバクテリウム・アドレセンティス(Bifidobacterium adolescentis)(表1の管理番号43〜45)、および5種のビフィドバクテリウム・ロンガム(Bifidobacterium longum)(表1の管理番号46〜50)であった。
前記表1に記載された菌株のうちラクトバチルス・プランタラム(Lactobacillus plantarum)NK3(受託番号KCCM12089P)は、グラム陽性桿菌であることが確認された。また、ラクトバチルス・プランタラム(Lactobacillus plantarum)NK3の16S rDNAは、配列番号1の塩基配列を有することが明らかになった。ラクトバチルス・プランタラム(Lactobacillus plantarum)NK3の16S rDNA塩基配列をBLAST検索で比較した結果、同一な16S rDNA塩基配列を有するラクトバチルス・プランタラム(Lactobacillus plantarum)菌株は検索されず、公知のラクトバチルス・プランタラム(Lactobacillus plantarum)菌株の16S rDNA配列と99%の相同性を示すことを確認した。
前記表1に記載された菌株のうちビフィドバクテリウム・ロンガム(Bifidobacterium longum)NK49(受託番号KCCM12088P)は、グラム陽性桿菌であることが確認された。また、ビフィドバクテリウム・ロンガム(Bifidobacterium longum)NK49の16S rDNAは、配列番号2の塩基配列を有することが明らかになった。ビフィドバクテリウム・ロンガム(Bifidobacterium longum)NK49の16S rDNA塩基配列をBLAST検索で比較した結果、同一な16S rDNA塩基配列を有するビフィドバクテリウム・ロンガム(Bifidobacterium longum)菌株は検索されず、公知のビフィドバクテリウム・ロンガム(Bifidobacterium longum)菌株の16S rDNA配列と99%の相同性を示すことを確認した。
DPPH(2,2−Diphenyl−1−picrylhydrazyl)を0.2mM濃度になるようにエタノールに溶かしてDPPH溶液を製造した。前記DPPH溶液0.1mLに乳酸菌の懸濁液(1×106CFU/mL)またはビタミンC溶液(1g/mL)を入れて20分間37℃で培養した。培養液を3000rpmで5分間遠心分離して上澄みを得た。その後、517nmで上澄みの吸光度を測定して、分離した乳酸菌の抗酸化活性を計算した。各乳酸菌別の抗酸化活性は下記表4の通りである。
C57BL/6マウス(male、6週齢、20〜23g)の腹腔に滅菌された4%チオグリコレート(thioglycolate)2mLを投与した。96時間の経過後にマウスを麻酔し、マウスの腹腔にRPMI 1640培地8mLを投与した。5〜10分後にマウスの腹腔内のRPMI培地(マクロファージ)を抜き取り、1000gで10分間遠心分離し、さらにRPMI 1640培地で2回洗浄した。前記マクロファージを各ウェル当たりに0.5×106の数で24−ウェルプレートに敷き、分離した乳酸菌(最終処理濃度:1×104CFU/mL、以下同一)と炎症反応誘導物質であるリポポリサッカライド(lipopolysaccharide、LPS)を2時間または24時間処理した後に上澄みおよび細胞を得た。得られた細胞をRIPAバッファ(Gibco社)に入れて均質化した。24時間処理した培養上澄みにおいてTNF−α、IL−10などのサイトカイン発現量を、2時間処理して得られた細胞からp65(NF−kB)、p−p65(phosphor−NF−kB)およびβ−actinの発現量を免疫ブロット法(immunoblotting)により測定した。各乳酸菌別の炎症指標の発現レベルは下記表4の通りである。
大腸癌細胞であるCaco2細胞を韓国細胞株バンクから分譲してRPMI 1640培地で48時間培養した後、Caco2細胞をウェル当たりに2×106の量になるように12−ウェルプレートに分株した。各ウェルにLPS 1μgを単独で処理するか、またはLPS 1μgと乳酸菌1×104CFUを共に処理した後、24時間培養した。その後、各ウェルから培養された細胞を集め、免疫ブロット法(immunoblotting)により密着結合タンパク質(tight junction protein)であるZO−1の発現量を測定した。各乳酸菌別のZO−1の発現量は下記表5の通りである。
分離した乳酸菌の活性を評価した結果、分離した乳酸菌のうち新規な乳酸菌であるラクトバチルス・プランタラム(Lactobacillus plantarum)NK3およびビフィドバクテリウム・ロンガム(Bifidobacterium longum)NK49が密着結合タンパク質であるZO−1の発現量を増加させつつ、抗酸化活性および炎症反応の抑制効果に優れることを確認した(表4および表5)。
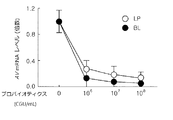
その結果、ラクトバチルス・プランタラム(Lactobacillus plantarum)NK3またはビフィドバクテリウム・ロンガム(Bifidobacterium longum)NK49を処理した全ての群において、NF−kBの活性が抑制され、TNF−αの発現量が抑制されることを確認した(図1および図2)。
GAM培地に、分離した新規な乳酸菌であるラクトバチルス・プランタラム(Lactobacillus plantarum)NK3およびビフィドバクテリウム・ロンガム(Bifidobacterium longum)NK49(1×106、1×107、1×108CFU/mL)と共にガードネレラ・バギナリス(Gardnerella vaginalis)またはアトポビウム・バギナエ(Atopobium vaginae)(1×106CFU/mL)を移植した。37℃、嫌気的条件でBHI brothに酵母抽出物(yeast extract)(1%)、マルトース(maltose)(0.1%)、グルコース(glucose)(0.1%)および馬血清(horse serum)(10%)を添加したBHIS培地において24時間培養して抗菌力を測定した。
C57BL/6マウス(雌、19〜22g、6週齢)を1群当たりに6匹ずつ用いて実験を行った。前記マウスにβ−estradiol 17−benzoate(Sigma社、MO、米国)0.125mgをオリーブオイルに溶かして皮下注射した。3日後、ガードネレラ・バギナリス(Gardnerella vaginalis)(1×108CFU/mouse)をマウスの膣内に移植した。移植して8日目から14日間、毎日1回ずつ1×109CFU/mouseの分離した新規な乳酸菌であるラクトバチルス・プランタラム(Lactobacillus plantarum)NK3、ビフィドバクテリウム・ロンガム(Bifidobacterium longum)NK49またはこれらの1:1の混合物を経口または膣内に直接投与した。乳酸菌を投与して7日目(移植して14日目)に最後に投与し、24時間後に動物モデルを犠牲死させて実験を行った。
上記のようにガードネレラ・バギナリス(Gardnerella vaginalis)をマウスの膣に移植した結果、膣と子宮に浮腫を伴った炎症が発生した。しかし、新規な乳酸菌であるラクトバチルス・プランタラム(Lactobacillus plantarum)NK3、ビフィドバクテリウム・ロンガム(Bifidobacterium longum)NK49またはこれらの混合物を経口または膣内に投与した結果、膣と子宮の外観上の炎症が有意に減少することを確認した(図6)。
新規な乳酸菌を上記のように投与してから24時間および48時間に、滅菌された生理食塩水0.5mlで膣内を洗い出した。洗い出した膣洗浄液をQiagen DNA purification kitを用いて分離した後、PCRにより乳酸菌およびガードネレラ・バギナリス(Gardnerella vaginalis)菌株を定量した。
50mMリン酸緩衝液(phosphate buffer、pH6.0)1mlに上記のように洗い出した膣洗浄液を加えて超音波処理した。溶かして凍らせる過程を3回実施した後に遠心分離した。上層液100μLにO−ジアニシジン(o−dianisidine、0.129mg/mL)398μLを加えた。H2O2の最終濃度を0.0005%に合わせた後、25℃および492nm条件で経時的(time course)にミエロペルオキシダーゼ(myeloperoxidase、MPO)の活性を測定した。
前記犠牲死させた動物モデルの大腸または膣粘膜組織にlysis buffer(20mM HEPES、1.5mM MgCl2、0.4mM NaCl、1mM EDTA、1mM dithiotheitol、0.5mM phenyl methyl sulfonyl fluoride、20μg/mLトリプシン阻害剤、1% nonidet p−40、20%グリセロール)を入れて均質化(homogenize)した。Bradford assayによりタンパク質を定量して、タンパク質50μg/μLが含まれるように検体を製造した。前記検体に電気泳動サンプルバッファ(Laemmli sample buffer 950μL+βMe 50μL)10μg/μLを加えた後、100℃で3分間変性(denaturation)させ、電気泳動(150V、30mA)を行った。電気泳動したゲルを30Vにおいて2時間メンブレンにトランスファー(transfer)した。前記メンブレンを5% skim milk/PBS−T(0.05% tween 20/PBS)に15mL入れ、1時間揺すった。1次抗体10μg/μLに1% skim milk/PBS−T 10mLを入れて12時間反応させた後、PBS−T溶液で5分間3回洗浄した。そして、各サイトカインおよび転写因子に対する2次抗体10μg/μLに1% skim milk/PBS−T 20mLを入れて1時間揺すって反応させた。PBS−T溶液で5分間3回洗浄した後、最後にECL溶液で発光させた。
マウスの膣を滅菌された生理食塩水0.5mlで膣内を2回洗い出した。洗い出した膣洗浄液を集めて遠心分離(10,000g、10分間)し、沈殿物をbacterial genomic DNA extraction kit(QIAGEN DNeasy Feces kit;Qiagen、Hilden、Germany)を用いてDNAを抽出した。抽出されたDNA 10ngをQiagen thermal cyclerにおいて下記のプライマーを入れ、SYBER premixを入れて、DNA polymerase activation(95℃、30秒間)、denaturation(95℃、5秒間)およびamplification(63℃、30秒間)を38回繰り返してPCRを行った。
乳酸菌 (Lactobacilli) reverse(5’−3’) CTT GTA CAC ACC GCC CGT(配列番号4);
Control 16S rDNA forward(5’−3’) AGA GTT TGA TCC TGG CTC AG(配列番号5);および
Control 16S rDNA reverse(5’−3’) AAG GAG GTG WTC CAR CC(配列番号6)。
大腸組織100mgに0.5%ヘキサデシルトリメチルアンモニウム臭化物(hexadecyl trimethyl ammonium bromide)含有10mMリン酸カルシウム緩衝液(potassium phosphate buffer、pH7.0)200μLを入れ、均質化(homogenization)した。4℃および10,000gの条件で10分間遠心分離して上澄みを得た。上澄み50μLを0.95mLの反応液(1.6mMテトラメチルベンジジン(tetramethyl benzidine)と0.1mM H2O2含有)に入れ、37℃で反応させつつ、650nmで経時的に吸光度を測定した。前記ミエロペルオキシダーゼ活性は、反応物として生じたH2O2 1μmol/mLを1ユニットに計算した。
ウェスタンブロット法を利用して、p−p65、p65、COX−2およびβ−actinのような炎症反応指標物質を測定した。具体的には、前記ミエロペルオキシダーゼ(Myeloperoxidase、MPO)活性測定実験と同様の方法により得られた上澄み50μgを取り、免疫ブロット法を行った。また、サイトカイン(IL−17、TNF−α)の発現量は、ELISA kitを用いて測定した。
それにより、新規な乳酸菌は、毒性を示さず、且つ、大腸炎の予防および治療に効果があることを確認した。
本発明の発明者らは、ラクトバチルス・プランタラム(Lactobacillus plantarum)NK3を2017年8月4日に公認寄託機関である韓国微生物保存センター(アドレス:大韓民国、ソウル西大門区弘済内2街ギル45ユリムビル)に特許寄託してKCCM12089Pの受託番号を与えられた。
また、本発明の発明者らは、ビフィドバクテリウム・ロンガム(Bifidobacterium longum)NK49を2017年8月4日に公認寄託機関である韓国微生物保存センター(アドレス:大韓民国、ソウル西大門区弘済内2街ギル45ユリムビル)に特許寄託してKCCM12088Pの受託番号を与えられた。
Claims (18)
- ラクトバチルス・プランタラムNK3(Lactobacillus plantarum NK3) KCCM12089P。
- ビフィドバクテリウム・ロンガムNK49(Bifidobacterium longum NK49) KCCM12088P。
- 前記ラクトバチルス・プランタラムNK3(Lactobacillus plantarum NK3) KCCM12089Pは、配列番号1の16S rDNA塩基配列を含む、請求項1に記載のラクトバチルス・プランタラムNK3(Lactobacillus plantarum NK3) KCCM12089P。
- 前記ビフィドバクテリウム・ロンガムNK49(Bifidobacterium longum NK49) KCCM12088Pは、配列番号2の16S rDNA塩基配列を含む、請求項2に記載のビフィドバクテリウム・ロンガムNK49(Bifidobacterium longum NK49) KCCM12088P。
- ラクトバチルス・プランタラムNK3(Lactobacillus plantarum NK3) KCCM12089P、ビフィドバクテリウム・ロンガムNK49(Bifidobacterium longum NK49) KCCM12088Pまたはこれらの混合物を含む炎症疾患の予防または治療用の薬学組成物。
- 前記ラクトバチルス・プランタラムNK3(Lactobacillus plantarum NK3) KCCM12089Pは、その生菌体、その死菌体、その培養物またはその破砕物である、請求項5に記載の炎症疾患の予防または治療用の薬学組成物。
- 前記ビフィドバクテリウム・ロンガムNK49(Bifidobacterium longum NK49) KCCM12088Pは、その生菌体、その死菌体、その培養物またはその破砕物である、請求項5に記載の炎症疾患の予防または治療用の薬学組成物。
- 前記炎症疾患は、関節炎、痛風、肝炎、喘息、肥満、角膜炎、胃炎、腸炎、腎臓炎、大腸炎、糖尿、結核、気管支炎、胸膜炎、腹膜炎、脊椎炎、膵臓炎、炎症痛、尿道炎、膀胱炎、膣炎、動脈硬化症、敗血症、火傷、皮膚炎、歯周炎および歯肉炎を含む群より選択されるいずれか一つ以上である、請求項5に記載の炎症疾患の予防または治療用の薬学組成物。
- 前記炎症疾患は大腸炎または膣炎である、請求項5に記載の炎症疾患の予防または治療用の薬学組成物。
- ラクトバチルス・プランタラムNK3(Lactobacillus plantarum NK3) KCCM12089P、ビフィドバクテリウム・ロンガムNK49(Bifidobacterium longum NK49) KCCM12088Pまたはこれらの混合物を含む炎症疾患の予防または改善用の健康機能食品。
- 前記ラクトバチルス・プランタラムNK3(Lactobacillus plantarum NK3) KCCM12089Pは、その生菌体、その死菌体、その培養物またはその破砕物である、請求項10に記載の炎症疾患の予防または改善用の健康機能食品。
- 前記ビフィドバクテリウム・ロンガムNK49(Bifidobacterium longum NK49) KCCM12088Pは、その生菌体、その死菌体、その培養物またはその破砕物である、請求項10に記載の炎症疾患の予防または改善用の健康機能食品。
- 前記炎症疾患は、関節炎、痛風、肝炎、喘息、肥満、角膜炎、胃炎、腸炎、腎臓炎、大腸炎、糖尿、結核、気管支炎、胸膜炎、腹膜炎、脊椎炎、膵臓炎、炎症痛、尿道炎、膀胱炎、膣炎、動脈硬化症、敗血症、火傷、皮膚炎、歯周炎および歯肉炎を含む群より選択されるいずれか一つ以上である、請求項10に記載の炎症疾患の予防または改善用の健康機能食品。
- 前記炎症疾患は大腸炎または膣炎である、請求項10に記載の炎症疾患の予防または改善用の健康機能食品。
- 炎症疾患の治療のための薬剤を製造するためのラクトバチルス・プランタラムNK3(Lactobacillus plantarum NK3) KCCM12089P、ビフィドバクテリウム・ロンガムNK49(Bifidobacterium longum NK49) KCCM12088Pまたはこれらの混合物の使用。
- 前記炎症疾患は、関節炎、痛風、肝炎、喘息、肥満、角膜炎、胃炎、腸炎、腎臓炎、大腸炎、糖尿、結核、気管支炎、胸膜炎、腹膜炎、脊椎炎、膵臓炎、炎症痛、尿道炎、膀胱炎、膣炎、動脈硬化症、敗血症、火傷、皮膚炎、歯周炎および歯肉炎を含む群より選択されるいずれか一つ以上である、請求項15に記載の使用。
- 炎症疾患の治療に用いるためのラクトバチルス・プランタラムNK3(Lactobacillus plantarum NK3) KCCM12089P、ビフィドバクテリウム・ロンガムNK49(Bifidobacterium longum NK49) KCCM12088Pまたはこれらの混合物を含む組成物。
- 前記炎症疾患は、関節炎、痛風、肝炎、喘息、肥満、角膜炎、胃炎、腸炎、腎臓炎、大腸炎、糖尿、結核、気管支炎、胸膜炎、腹膜炎、脊椎炎、膵臓炎、炎症痛、尿道炎、膀胱炎、膣炎、動脈硬化症、敗血症、火傷、皮膚炎、歯周炎および歯肉炎を含む群より選択されるいずれか一つ以上である、請求項17に記載の組成物。
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| KR10-2017-0145420 | 2017-11-02 | ||
| KR20170145420 | 2017-11-02 | ||
| PCT/KR2018/004590 WO2019088379A1 (ko) | 2017-11-02 | 2018-04-19 | 신규 유산균 및 이의 용도 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2021501586A JP2021501586A (ja) | 2021-01-21 |
| JP6964191B2 true JP6964191B2 (ja) | 2021-11-10 |
Family
ID=66332068
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2020524353A Active JP6964191B2 (ja) | 2017-11-02 | 2018-04-19 | 新規な乳酸菌およびその使用 |
Country Status (10)
| Country | Link |
|---|---|
| US (3) | US11554146B2 (ja) |
| EP (1) | EP3875576A4 (ja) |
| JP (1) | JP6964191B2 (ja) |
| KR (2) | KR102151666B1 (ja) |
| CN (1) | CN113302279A (ja) |
| AU (2) | AU2018358456B2 (ja) |
| BR (1) | BR112021008358A2 (ja) |
| CA (1) | CA3081210C (ja) |
| SG (1) | SG11202104408UA (ja) |
| WO (2) | WO2019088379A1 (ja) |
Families Citing this family (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN108624520B (zh) * | 2017-03-16 | 2022-01-25 | 景岳生物科技股份有限公司 | 促进骨质再生的植物乳杆菌菌株gmnl-662及其组合物 |
| CN116829164A (zh) * | 2020-12-16 | 2023-09-29 | 株式会社明治 | 用于改善脑组织炎症的组合物 |
| KR102533469B1 (ko) * | 2021-01-05 | 2023-05-17 | 연세대학교 산학협력단 | 염증성 장 질환의 예방 또는 치료용 조성물 |
| EP4304557A1 (en) * | 2021-03-12 | 2024-01-17 | MarvelBiome, Inc. | Methods and uses of microbiome compositions, components, or metabolites for treating eye disorders |
| KR102488062B1 (ko) * | 2021-03-19 | 2023-01-12 | 서원대학교산학협력단 | 녹용 발효추출물을 포함하는 여성 갱년기 운동성 감소의 예방 또는 치료용 조성물 |
| KR102445903B1 (ko) * | 2021-07-06 | 2022-09-22 | 롯데제과 주식회사 | 혈당 상승 저해 및 스트레스 조절 효과가 우수한 열처리된 락토바실러스 플랜타럼 lrcc5314 균주 및 용도 |
Family Cites Families (12)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| KR102000514B1 (ko) | 2013-04-03 | 2019-10-01 | 프로비 아베 | 골다공증의 치료 또는 예방에 사용되는 프로바이오틱 스트레인 |
| ITMI20130794A1 (it) | 2013-05-14 | 2014-11-15 | Probiotical Spa | Composizione comprendente batteri lattici per uso nel trattamento preventivo e/o curativo delle vaginosi batteriche. |
| KR101638984B1 (ko) | 2013-05-29 | 2016-07-13 | 바이오제닉스코리아 주식회사 | 나노형 김치 유산균 |
| WO2015122717A1 (ko) | 2014-02-17 | 2015-08-20 | 경희대학교 산학협력단 | 비만 억제 효능을 갖는 신규 유산균 및 이의 용도 |
| KR101709246B1 (ko) | 2014-05-30 | 2017-02-22 | 일동후디스 주식회사 | 다시마 및 복합 유산균을 이용한 항비만용 신바이오틱스 조성물 |
| KR101690738B1 (ko) | 2014-08-25 | 2016-12-29 | 고려대학교 산학협력단 | 발효 율피 추출물을 유효성분으로 포함하는 항당뇨 조성물 |
| WO2017037089A1 (en) | 2015-08-31 | 2017-03-09 | Nestec S.A. | Methods and compositions using bifidobacterium longum to treat or prevent depressive symptoms |
| KR20170032815A (ko) | 2015-09-15 | 2017-03-23 | 경희대학교 산학협력단 | 신규 유산균 및 퇴행성 뇌질환 또는 인지기능의 예방, 개선 또는 치료용 조성물 |
| KR101824147B1 (ko) | 2015-11-10 | 2018-01-31 | 경남과학기술대학교 산학협력단 | 증진된 생리활성을 갖는 콩 발효조성물 및 이를 포함하는 갱년기 또는 폐경기 증상 개선용 건강기능성 식품 |
| KR101750468B1 (ko) * | 2016-03-04 | 2017-06-27 | 주식회사 메디오젠 | 락토바실러스 퍼멘툼 mg901 또는 락토바실러스 플란타룸 mg989를 포함하는 조성물 |
| KR101784847B1 (ko) * | 2016-05-10 | 2017-10-13 | 주식회사 하우동천 | 질염 예방 및 치료용 유산균 함유 조성물 및 이의 용도 |
| KR20160085235A (ko) | 2016-06-28 | 2016-07-15 | 바이오제닉스코리아 주식회사 | 면역증진 및 장내환경개선용 건강기능성 아이스크림 |
-
2018
- 2018-04-19 AU AU2018358456A patent/AU2018358456B2/en active Active
- 2018-04-19 WO PCT/KR2018/004590 patent/WO2019088379A1/ko active Application Filing
- 2018-04-19 JP JP2020524353A patent/JP6964191B2/ja active Active
- 2018-04-19 CA CA3081210A patent/CA3081210C/en active Active
- 2018-04-19 US US16/760,689 patent/US11554146B2/en active Active
- 2018-11-01 KR KR1020180132834A patent/KR102151666B1/ko active IP Right Grant
-
2019
- 2019-04-30 US US17/290,516 patent/US20230181657A1/en active Pending
- 2019-04-30 EP EP19877635.3A patent/EP3875576A4/en active Pending
- 2019-04-30 BR BR112021008358-8A patent/BR112021008358A2/pt unknown
- 2019-04-30 CN CN201980086597.7A patent/CN113302279A/zh active Pending
- 2019-04-30 WO PCT/KR2019/005239 patent/WO2020091166A1/ko unknown
- 2019-04-30 SG SG11202104408UA patent/SG11202104408UA/en unknown
-
2020
- 2020-08-28 KR KR1020200108963A patent/KR102173547B1/ko active IP Right Grant
-
2021
- 2021-11-15 AU AU2021269282A patent/AU2021269282B2/en active Active
-
2022
- 2022-12-13 US US18/065,497 patent/US20230181656A1/en active Pending
Also Published As
| Publication number | Publication date |
|---|---|
| AU2021269282A1 (en) | 2021-12-09 |
| AU2018358456A1 (en) | 2020-05-28 |
| CA3081210A1 (en) | 2019-05-09 |
| KR102173547B1 (ko) | 2020-11-03 |
| AU2018358456B2 (en) | 2021-10-28 |
| US20230181656A1 (en) | 2023-06-15 |
| JP2021501586A (ja) | 2021-01-21 |
| AU2021269282B2 (en) | 2023-08-17 |
| WO2019088379A1 (ko) | 2019-05-09 |
| EP3875576A1 (en) | 2021-09-08 |
| CA3081210C (en) | 2023-04-11 |
| WO2020091166A1 (ko) | 2020-05-07 |
| SG11202104408UA (en) | 2021-05-28 |
| US20210260140A1 (en) | 2021-08-26 |
| US20230181657A1 (en) | 2023-06-15 |
| US11554146B2 (en) | 2023-01-17 |
| KR102151666B1 (ko) | 2020-09-04 |
| KR20200104848A (ko) | 2020-09-04 |
| BR112021008358A2 (pt) | 2021-08-03 |
| EP3875576A4 (en) | 2022-03-02 |
| CN113302279A (zh) | 2021-08-24 |
| KR20190050294A (ko) | 2019-05-10 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP6964191B2 (ja) | 新規な乳酸菌およびその使用 | |
| JP2022000040A (ja) | 代謝障害を処置するための低温殺菌アッカーマンシアの使用 | |
| KR102128287B1 (ko) | 아커만시아 뮤시니필라 eb-amdk19 균주 및 그의 용도 | |
| KR102487131B1 (ko) | 신규 유산균 및 이의 용도 | |
| WO2022140401A1 (en) | Lactobacillus compositions and methods for prevention and treatment of microbial infection | |
| JP2014047212A (ja) | ラクトバチラス‐プランタルムcmu995菌株の使用方法 | |
| JP2019508486A (ja) | 胃腸炎の処置及び予防のためのフィーカリバクテリウム・プラウスニッツィcncm i−4573株 | |
| KR102543494B1 (ko) | 신규 프로바이오틱스 및 이의 용도 | |
| KR101957211B1 (ko) | 조산 및 질염 원인균에 대한 항균 활성, 성병 원인 바이러스에 대한 항바이러스 활성 및 질내 부착능이 우수한 락토바실러스 속 균주 및 이의 용도 | |
| WO2018112739A1 (zh) | 一种假小链状双歧杆菌及其培养方法和应用 | |
| KR101770035B1 (ko) | 상엽 추출물을 유효성분으로 포함하는 IL-1β에 의한 관절염의 예방 또는 개선용 조성물 | |
| JP2023519233A (ja) | 肝機能改善または脂肪蓄積抑制の微生物、及びその用途 | |
| WO2012103785A1 (zh) | 唾液乳杆菌及其代谢物的制备方法和组合物以及应用 | |
| JP2020022488A (ja) | 多様な機能性を有する新規乳酸菌およびその用途 | |
| CN117004503B (zh) | 一株唾液联合乳杆菌mb1及其在制备助睡眠和调理肠胃食品药品中的应用 | |
| CN115466699B (zh) | 熊猫源唾液乳杆菌及在治疗或预防炎症性肠病中的应用 | |
| KR20230128540A (ko) | 균주, 조성물 및 사용 방법 | |
| ES2891536T3 (es) | Cepa Bifidobacterium animalis AMT30 y composición que contiene la cepa de Bifidobacterium animalis AMT30 | |
| WO2022250192A1 (ko) | 항염증 활성이 우수한 김치 유래 신균주 락토바실러스 퍼멘텀 및 이를 포함하는 염증성 질환의 예방 또는 치료용 조성물 | |
| CN116785277B (zh) | 染料木黄酮在制备调控肠道菌丰度的制剂中的应用 | |
| KR20240026346A (ko) | 신규 유산균 및 이의 용도 | |
| JP2007091704A (ja) | IgE産生抑制剤、IgE産生抑制用飲食品、抗アレルギー剤および抗アレルギー用飲食品 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A821 Effective date: 20200701 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20200728 |
|
| A80 | Written request to apply exceptions to lack of novelty of invention |
Free format text: JAPANESE INTERMEDIATE CODE: A801 Effective date: 20200728 Free format text: JAPANESE INTERMEDIATE CODE: A80 Effective date: 20200728 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20210727 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20210813 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20211005 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20211018 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 6964191 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |