JP6936073B2 - 硫化物固体電解質 - Google Patents
硫化物固体電解質 Download PDFInfo
- Publication number
- JP6936073B2 JP6936073B2 JP2017153385A JP2017153385A JP6936073B2 JP 6936073 B2 JP6936073 B2 JP 6936073B2 JP 2017153385 A JP2017153385 A JP 2017153385A JP 2017153385 A JP2017153385 A JP 2017153385A JP 6936073 B2 JP6936073 B2 JP 6936073B2
- Authority
- JP
- Japan
- Prior art keywords
- solid electrolyte
- sulfide solid
- lithium
- electrolyte according
- crystal structure
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
Images
Classifications
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y02—TECHNOLOGIES OR APPLICATIONS FOR MITIGATION OR ADAPTATION AGAINST CLIMATE CHANGE
- Y02E—REDUCTION OF GREENHOUSE GAS [GHG] EMISSIONS, RELATED TO ENERGY GENERATION, TRANSMISSION OR DISTRIBUTION
- Y02E60/00—Enabling technologies; Technologies with a potential or indirect contribution to GHG emissions mitigation
- Y02E60/10—Energy storage using batteries
Landscapes
- Conductive Materials (AREA)
- Secondary Cells (AREA)
- Battery Electrode And Active Subsutance (AREA)
- Primary Cells (AREA)
Description
現在市販されているリチウムイオン電池は、可燃性の有機溶媒を含む電解液が使用されているため、短絡時の温度上昇を抑える安全装置の取り付けや短絡防止のための構造・材料面での改善が必要となる。これに対し、電解液を固体電解質に変えて、電池を全固体化したリチウムイオン電池は、電池内に可燃性の有機溶媒を用いないので、安全装置の簡素化が図れ、製造コストや生産性に優れると考えられている。
アルジロダイト型結晶構造は、安定性が高い結晶であり、また、イオン伝導度の高いものも存在する。しかしながら、量産化可能な製造方法の開発やイオン伝導度のさらなる改善が求められている。
また、本発明の一実施形態によれば、上記硫化物固体電解質と、活物質を含む電極合材が提供される。
また、本発明の一実施形態によれば、上記硫化物固体電解質及び上記電極合材のうち少なくとも1つを含むリチウムイオン電池が提供される。
2θ=25.2±0.5deg及び29.7±0.5degの回折ピークは、アルジロダイト型結晶構造に由来するピークである。アルジロダイト型結晶構造は、PS4 3−を主たる骨格の単位構造とし、その周辺にリチウム元素(Li)で囲まれた硫黄元素(S)やハロゲン元素(X)が配置されている構造である。
アルジロダイト型結晶構造の回折ピークは、例えば、2θ=15.3±0.5deg、17.7±0.5deg、31.1.±0.5deg、44.9±0.5deg、47.7±0.5degにも現れることがある。本態様の硫化物固体電解質は、これらのピークを有していてもよい。
5.0≦a≦7.5 ・・・(A)
6.5≦a+c≦7.5 ・・・(B)
0.5≦a−b≦1.5 ・・・(C)
(式中、b>0且つc≧0を満たす。)
X1:F、Cl、O
X2:Br
X3:I、Se、Te
元素Xにおいて、元素X1の占めるモル比が最も大きい場合、上記式(A)は、5.0≦a≦6.5であることが好ましく、5.2≦a≦6.1であることがより好ましい。また、元素Xにおいて、元素X2の占めるモル比が最も大きい場合、上記式(A)は、5.2≦a<≦6.8であることが好ましく、5.3≦a<≦6.6であることがより好ましい。また、元素Xにおいて、元素X3の占めるモル比が最も大きい場合、上記式(A)は、5.5≦a≦7.2であることが好ましく、5.5≦a≦7.0であることがより好ましい。
上記式(C)は、0.6≦a−b≦1.3であることが好ましく、0.7≦a−b≦1.3であることがより好ましい。
5.0≦a≦7.1 ・・・(A’)
6.5≦a+c<7.1 ・・・(B’)
1.0<a−b≦1.5 ・・・(C’)
(式中、b>0且つc≧0を満たす。)
上記式(C’)は、1.0<a−b≦1.4であることが好ましく、1.0<a−b≦1.3であることがより好ましい。
元素Xにおいて、元素X1の占めるモル比が最も大きい場合、上記式(A’)は、5.2≦a≦6.5であることが好ましく、5.25≦a≦6.4であることがより好ましい。また、元素Xにおいて、元素X2の占めるモル比が最も大きい場合、上記式(A’)は、5.2≦a≦6.8であることが好ましく、5.3≦a≦6.6であることがより好ましい。また、元素Xにおいて、元素X3の占めるモル比が最も大きい場合、上記式(A’)は、5.5≦a≦7.0であることが好ましく、5.5≦a≦6.8であることがより好ましい。
Lia(P1−αMα)SbXc (4)
(式中、Mは、Si、Ge、Sn、Pb、B、Al、Ga、As、Sb及びBiからなる群より選択される1以上の元素であり、Xは、F、Cl、Br、I、O、Se及びTeからなる群から選択される1以上の元素である。a〜cは下記式(1)〜(3)を満たす。αは0≦α≦0.3である。)
5.0≦a≦7.5 ・・・(1)
6.5≦a+c≦7.5 ・・・(2)
0.5≦a−b≦1.5 ・・・(3)
(式中、b>0且つc≧0を満たす。)
αは0が好ましい。
上記式(3)は、0.6≦a−b≦1.3であることが好ましく、0.7≦a−b≦1.3であることがより好ましい。
元素Xにおいて、元素X1の占めるモル比が最も大きい場合、上記式(1)は、5.0≦a≦6.5であることが好ましく、5.2≦a≦6.1であることがより好ましい。また、元素Xにおいて、元素X2の占めるモル比が最も大きい場合、上記式(1)は、5.2≦a<≦6.8であることが好ましく、5.3≦a<≦6.6であることがより好ましい。また、元素Xにおいて、元素X3の占めるモル比が最も大きい場合、上記式(1)は、5.5≦a≦7.2であることが好ましく、5.5≦a≦7.0であることがより好ましい。
5.0≦a≦7.1 ・・・(1’)
6.5≦a+c<7.1 ・・・(2’)
1.0<a−b≦1.5 ・・・(3’)
(式中、b>0且つc≧0を満たす。)
上記式(3’)は、1.0<a−b≦1.4であることが好ましく、1.0<a−b≦1.3であることがより好ましい。
元素Xにおいて、元素X1の占めるモル比が最も大きい場合、上記式(1’)は、5.2≦a≦6.5であることが好ましく、5.25≦a≦6.4であることがより好ましい。また、元素Xにおいて、元素X2の占めるモル比が最も大きい場合、上記式(1’)は、5.2≦a≦6.8であることが好ましく、5.3≦a≦6.6であることがより好ましい。また、元素Xにおいて、元素X3の占めるモル比が最も大きい場合、上記式(1’)は、5.5≦a≦7.0であることが好ましく、5.5≦a≦6.8であることがより好ましい。
各元素のモル比は、例えば原料における各元素の含有量を調製することにより制御できる。
0<IA/IB<0.1 (5)
(式中、IAは2θ=17.6±0.4deg及び2θ=18.1±0.4degのうちアルジロダイト型結晶構造の回折ピークではないものの回折ピークの強度を表し、IBは2θ=29.7±0.5degの回折ピークの強度を表す。)
なお、2θ=17.6±0.4deg及び2θ=18.1±0.4degのいずれかは、通常、比較的ピーク強度の強いアルジロダイト型結晶構造の回折ピークと重なるため測定できない場合がある。従って、2θ=17.6±0.4deg及び2θ=18.1±0.4degのうちアルジロダイト型結晶構造の回折ピークではないものとは、通常、観測されるこれら2つのピークのうち強度の弱い方を意味する。
0<IC/IB<0.100・・・(6)
(式中、ICは2θ=14.4±0.5degの回折ピークの強度を表し、IBは2θ=29.7±0.5degの回折ピークの強度を表す。)
本発明の第1の態様に係る硫化物固体電解質も固体31P−NMR測定において、110±5ppmにピークを有すると好ましい。
本態様の硫化物固体電解質は、新結晶構造がP2S6ユニットを含む構造から構成されるため、アルジロダイト型結晶構造中のS欠陥構造が少なくなり、高イオン伝導度が得られると考えられる。
上記半値幅は実施例に記載の方法で確認できる。
以下、本発明の第1の態様に係る硫化物固体電解質と本発明の第2の態様に係る硫化物固体電解質をまとめて「本発明の硫化物固体電解質」という。
上記硫化リチウムは、特に制限なく使用できるが、高純度のものが好ましい。硫化リチウムは、例えば、特開平7−330312号公報、特開平9−283156号公報、特開2010−163356号公報、特開2011−84438号公報に記載の方法により製造することができる。
具体的には、炭化水素系有機溶媒中で水酸化リチウムと硫化水素とを70℃〜300℃で反応させて、水硫化リチウムを生成し、次いでこの反応液を脱硫化水素化することにより硫化リチウムを合成できる(特開2010−163356号公報)。
また、水溶媒中で水酸化リチウムと硫化水素とを10℃〜100℃で反応させて、水硫化リチウムを生成し、次いでこの反応液を脱硫化水素化することにより硫化リチウムを合成できる(特開2011−84438号公報)。
Ml−Xm (7)
Xは、フッ素(F)、塩素(Cl)、臭素(Br)、及びヨウ素(I)から選択されるハロゲン元素が好ましい。
また、lは1又は2の整数であり、mは1〜10の整数である。mが2〜10の整数の場合、すなわち、Xが複数存在する場合は、Xは同じであってもよいし、異なっていてもよい。例えば、後述するSiBrCl3は、mが4であって、XはBrとClという異なる元素からなるものである。
ハロゲン化合物は、上記の化合物の中から一種を単独で用いてもよく、二種以上を組み合わせて用いてもよい。すなわち上記の化合物の少なくとも1つを用いることができる。また、この場合において、ハロゲン元素は、上記のハロゲン元素の中から一種を単独で用いてもよく、二種以上を組み合わせて用いてもよい。
例えば、本発明の硫化物固体電解質の原料として、硫化リチウム、五硫化二リン、ハロゲン化リチウムを使用する場合には、投入原料のモル比を、硫化リチウム:五硫化二リン:ハロゲン化リチウム=37〜88:8〜25:0.1〜50とすることができる。
尚、中間体がガラス(非晶質)成分を含むことは、XRD測定において非晶質成分に起因するブロードなピーク(ハローパターン)の存在により確認できる。
また、本実施形態では、特許文献1のように原料を550℃で6日間も加熱する必要はないため、量産性が高い。
ガラス成分を含む中間体を製造し、原子レベルで材料成分を混ぜ合わせることで、ガラス成分を含む中間体の熱処理中に、ハロゲンがスムーズにアルジロダイト結晶構造のサイトに入ることができる。
粉砕メディアであるボールは、例えば、ジルコニア製ボールを使用した場合、その直径は0.2〜20mmが好ましい。
本実施形態では、中間体を熱処理することにより、アルジロダイト型結晶構造を含む硫化物固体電解質を得るが、熱処理の温度を高くすると、アルジロダイト型結晶構造の形成が進行しやすく、結晶性が高くなるため、イオン伝導度が向上する。一方、熱処理の温度を高くし過ぎると、新規の結晶構造が増加するため、アルジロダイト型結晶構造の形成が阻害される。本発明では熱処理温度を上記範囲で調整して適切な条件とすることが好ましい。
従来技術(例えば、特許文献2〜5)では、硫化水素気流下で原料混合物を焼成している。これにより、焼成時に硫黄が補完されると考える。一方、本発明では硫化水素不存在下で熱処理することが好ましい。この場合、従来技術の固体電解質よりも硫黄の含有量が少ない硫化物固体電解質が得られると考えている。本発明における新規結晶構造は、P2S6 4−を主の単位構造とするものであり、アルジロダイト構造と比して、Sの元素比が少ない構造であると推察されるため、上述の条件が好ましい。
本発明の一実施形態の電極合材は、上述した本発明の硫化物固体電解質と、活物質を含む。又は、本発明の硫化物固体電解質により製造される。活物質として負極活物質を使用すると負極合材となる。一方、正極活物質を使用すると正極合材となる。
本発明の硫化物固体電解質に負極活物質を配合することにより負極合材が得られる。
負極活物質としては、例えば、炭素材料、金属材料等を使用することができる。これらのうち2種以上からなる複合体も使用できる。また、今後開発される負極活物質も使用することができる。
また、負極活物質は電子伝導性を有していることが好ましい。
炭素材料としては、グラファイト(例えば、人造黒鉛)、黒鉛炭素繊維、樹脂焼成炭素、熱分解気相成長炭素、コークス、メソカーボンマイクロビーズ(MCMB)、フルフリルアルコール樹脂焼成炭素、ポリアセン、ピッチ系炭素繊維、気相成長炭素繊維、天然黒鉛及び難黒鉛化性炭素等が挙げられる。
金属材料としては、金属単体、合金、金属化合物が挙げられる。当該金属単体としては、金属ケイ素、金属スズ、金属リチウム、金属インジウム、金属アルミニウムが挙げられる。当該合金としては、ケイ素、スズ、リチウム、インジウム及びアルミニウムのうち少なくとも1つを含む合金が挙げられる。当該金属化合物としては、金属酸化物が挙げられる。金属酸化物は、例えば酸化ケイ素、酸化スズ、酸化アルミニウムである。
負極合材における負極活物質の含有量が少なすぎると電気容量が小さくなる。また、負極活物質が電子伝導性を有し、導電助剤を含まないか、又は少量の導電助剤しか含まない場合には、負極内の電子伝導性(電子伝導パス)が低下し、レート特性が低くなるおそれや、負極活物質の利用率が下がり、電気容量が低下するおそれがあると考える。一方、負極合材における負極活物質の含有量が多すぎると、負極内のイオン伝導性(イオン伝導パス)が低下し、レート特性が低くなるおそれや、負極活物質の利用率が下がり、電気容量が低下するおそれがあると考える。
負極活物質の電子伝導性が低い場合には、導電助剤を添加することが好ましい。導電助剤は、導電性を有していればよく、その電子伝導度は、好ましくは1×103S/cm以上であり、より好ましくは1×105S/cm以上である。
導電助剤の具体例としては、好ましくは炭素材料、ニッケル、銅、アルミニウム、インジウム、銀、コバルト、マグネシウム、リチウム、クロム、金、ルテニウム、白金、ベリリウム、イリジウム、モリブデン、ニオブ、オスニウム、ロジウム、タングステン及び亜鉛からなる群より選択される少なくとも1つの元素を含む物質であり、より好ましくは導電性が高い炭素単体、炭素単体以外の炭素材料;ニッケル、銅、銀、コバルト、マグネシウム、リチウム、ルテニウム、金、白金、ニオブ、オスニウム又はロジウムを含む金属単体、混合物又は化合物である。
なお、炭素材料の具体例としては、ケッチェンブラック、アセチレンブラック、デンカブラック、サーマルブラック、チャンネルブラック等のカーボンブラック;黒鉛、炭素繊維、活性炭等が挙げられ、これらは単独でも2種以上でも併用可能である。なかでも、電子伝導性が高いアセチレンブラック、デンカブラック、ケッチェンブラックが好適である。
結着剤としては、ポリテトラフルオロエチレン(PTFE)、ポリフッ化ビニリデン(PVDF)、フッ素ゴム等の含フッ素樹脂、あるいはポリプロピレン、ポリエチレン等の熱可塑性樹脂、エチレン−プロピレン−ジエンゴム(EPDM)、スルホン化EPDM、天然ブチルゴム(NBR)等を単独で、あるいは2種以上の混合物として用いることができる。また、水系バインダーであるセルロース系やスチレンブタジエンゴム(SBR)の水分散体等を用いることもできる。
混合方法は特に限定されないが、例えば、乳鉢、ボールミル、ビーズミル、ジェットミル、遊星ボールミル、振動ボールミル、サンドミル、カッターミルを用いて混合する乾式混合;及び有機溶媒中に原料を分散させた後に、乳鉢、ボールミル、ビーズミル、遊星ボールミル、振動ボールミル、サンドミル、フィルミックスを用いて混合し、その後溶媒を除去する湿式混合を適用することができる。これらのうち、負極活物質粒子を破壊しないために湿式混合が好ましい。
本発明の固体電解質に正極活物質を配合することにより正極合材が得られる。
正極活物質は、リチウムイオンの挿入脱離が可能な物質であり、電池分野において正極活物質として公知のものが使用できる。また、今後開発される正極活物質も使用することができる。
金属酸化物は、例えば遷移金属酸化物である。具体的には、V2O5、V6O13、LiCoO2、LiNiO2、LiMnO2、LiMn2O4、Li(NiaCobMnc)O2(ここで、0<a<1、0<b<1、0<c<1、a+b+c=1)、LiNi1−YCoYO2、LiCo1−YMnYO2、LiNi1−YMnYO2(ここで、0≦Y<1)、Li(NiaCobMnc)O4(0<a<2、0<b<2、0<c<2、a+b+c=2)、LiMn2−ZNiZO4、LiMn2−ZCoZO4(ここで、0<Z<2)、LiCoPO4、LiFePO4、CuO、Li(NiaCobAlc)O2(ここで、0<a<1、0<b<1、0<c<1、a+b+c=1)等が挙げられる。
金属硫化物としては、硫化チタン(TiS2)、硫化モリブデン(MoS2)、硫化鉄(FeS、FeS2)、硫化銅(CuS)及び硫化ニッケル(Ni3S2)等が挙げられる。
その他、金属酸化物としては、酸化ビスマス(Bi2O3)、鉛酸ビスマス(Bi2Pb2O5)等が挙げられる。
非金属硫化物としては、有機ジスルフィド化合物、カーボンスルフィド化合物等が挙げられる。
上記の他、セレン化ニオブ(NbSe3)、金属インジウム、硫黄も正極活物質として使用できる。
導電助剤は、負極合材と同様である。
本発明の一実施形態のリチウムイオン電池は、上述した本発明の硫化物固体電解質及び電極合材のうち少なくとも1つを含む。又は、本発明の硫化物固体電解質及び電極合材のうち少なくとも1つにより製造される。
リチウムイオン電池の構成は特に限定されないが、一般に、負極層、電解質層及び正極層をこの順に積層した構造を有する。以下、リチウムイオン電池の各層について説明する。
負極層は、好ましくは本発明の負極合材から製造される層である。
又は、負極層は、好ましくは本発明の負極合材を含む層である。
負極層の厚さは、100nm以上5mm以下が好ましく、1μm以上3mm以下がより好ましく、5μm以上1mm以下がさらに好ましい。
負極層は公知の方法により製造することができ、例えば、塗布法、静電法(静電スプレー法、静電スクリーン法等)により製造することができる。
電解質層は、固体電解質を含む層又は固体電解質から製造された層である。当該固体電解質は特に限定されないが、好ましくは本発明の硫化物固体電解質である。
電解質層は、固体電解質のみからなってもよく、さらにバインダーを含んでもよい。当該バインダーとしては、本発明の負極合材の結着剤と同じものが使用できる。
電解質層の固体電解質は、融着していてもよい。融着とは、固体電解質粒子の一部が溶解し、溶解した部分が他の固体電解質粒子と一体化することを意味する。また、電解質層は、固体電解質の板状体であってもよく、当該板状体は、固体電解質粒子の一部又は全部が溶解し、板状体になっている場合も含む。
電解質層は、公知の方法により製造することができ、例えば、塗布法、静電法(静電スプレー法、静電スクリーン法等)により製造することができる。
正極層は、正極活物質を含む層であり、好ましくは本発明の正極合材を含む層又は本発明の正極合材から製造された層である。
正極層の厚さは、0.01mm以上10mm以下であることが好ましい。
正極層は、公知の方法により製造することができ、例えば、塗布法、静電法(静電スプレー法、静電スクリーン法等)により製造することができる。
本実施形態のリチウムイオン電池は、好ましくは集電体をさらに備える。例えば負極集電体は負極層の電解質層側とは反対側に、正極集電体は正極層の電解質層側とは反対側に設ける。
集電体として、銅、マグネシウム、ステンレス鋼、チタン、鉄、コバルト、ニッケル、亜鉛、アルミニウム、ゲルマニウム、インジウム、リチウム、又はこれらの合金等からなる板状体や箔状体等が使用できる。
また、接合面にイオン伝導性を有する活物質や、イオン伝導性を阻害しない接着物質を介して接合してもよい。
接合においては、固体電解質の結晶構造が変化しない範囲で加熱融着してもよい。
また、本実施形態のリチウムイオン電池は、上述した各部材を順次形成することでも製造できる。公知の方法により製造することができ、例えば、塗布法、静電法(静電スプレー法、静電スクリーン法等)により製造することができる。
なお、評価方法は以下のとおりである。
(1)イオン伝導度測定と電子伝導性測定
各例で製造した硫化物固体電解質を、錠剤成形機に充填し、ミニプレス機を用いて407MPa(プレス表示値22MPa)の圧力を加え成形体とした。電極としてカーボンを成形体の両面に乗せ、再度錠剤成形機にて圧力を加えることで、測定用の成形体(直径約10mm、厚み0.1〜0.2cm)を作製した。この成形体について交流インピーダンス測定によりイオン伝導度を測定した。イオン伝導度の値は25℃における数値を採用した。
なお、本実施例で用いたイオン伝導度の測定方法では、イオン伝導度が1.0×10−6S/cm未満の場合には、イオン伝導度を正確に測ることができないため、測定不能とした。
また、この成形体について直流電気測定により電子伝導度を測定した。電子伝導度の値は25℃における数値を採用した。なお、5Vの電圧を印加したときの電子伝導度が1.0×10−6S/cm未満の場合、電子伝導性は測定不能とした。
各例で製造した硫化物固体電解質の粉末から、直径10mm、高さ0.1〜0.3cmの円形ペレットを成形して試料とした。この試料を、XRD用気密ホルダーを用いて空気に触れさせずに測定した。回折ピークの2θ位置は、XRD解析プログラムJADEを用いて重心法にて決定した。
株式会社リガクの粉末X線回折測定装置SmartLabを用いて以下の条件にて実施した。
管電圧:45kV
管電流:200mA
X線波長:Cu−Kα線(1.5418Å)
光学系:平行ビーム法
スリット構成:ソーラースリット5°、入射スリット1mm、受光スリット1mm
検出器:シンチレーションカウンター
測定範囲:2θ=10−60deg
ステップ幅、スキャンスピード:0.02deg、1deg/分
測定結果より結晶相の存在を確認するためのピーク位置の解析では、XRD解析プログラムJADEを用い、3次式近似によりベースラインを引いて、ピーク位置を求めた。
回折ピークの強度においては、2θ=29.7deg±0.5degに存在するアルジロダイト型結晶構造の回折ピークの強度(IB)、2θ=17.6±0.4degかつ18.1±0.4degに存在するLi3PS4結晶構造の回折ピークの強度(IA)、及び2θ=14.4±0.5degに存在する新規の結晶構造の回折ピークの強度(IC)を次の手順で決定した。
実測データの5点のデータの移動平均によりスムージングを行い、17.5〜18.5degの間の最低強度点をバックグランドとして実測データから差し引いた。その後、17.0〜17.8deg及び17.9〜18.5degの実測データの最大値間の実測データの最大値を算出し、その小さい方のピーク強度をLi3PS4結晶構造の回折ピークの強度(IA)とした。また、アルジロダイト型結晶構造は29.0〜32.0degの実測データの最大値を回折ピークの強度(IB)とした。また、2θ=14.0〜15.0degにあるピークを特定し、ピークトップの強度を回折ピークの強度(IC)とした。各回折ピークの強度から、強度比(IA/IB)及び強度比(IC/IB)を計算した。
各例で製造した硫化物固体電解質の粉末を秤量し、アルゴン雰囲気中で、バイアル瓶に採取した。バイアル瓶にKOHアルカリ水溶液を入れ、硫黄分の捕集に注意しながらサンプルを溶解し、適宜希釈、測定溶液とした。これを、パッシェンルンゲ型ICP−OES装置(SPECTRO社製SPECTRO ARCOS)にて測定し、組成を決定した。
検量線溶液は、Li、P、S、Ge、SiはICP測定用1000mg/L標準溶液を、Cl、Brはイオンクロマトグラフ用1000mg/L標準溶液を、Iはよう化カリウム(試薬特級)を用いて調製した。
各試料で2つの測定溶液を調整し、各測定溶液で5回の測定を行い、平均値を算出した。その2つの測定溶液の測定値の平均で組成を決定した。
各例で製造した硫化物固体電解質の粉末約60mgをNMR試料管へ充填し、下記の装置及び条件にて固体31PNMRスペクトルを得た。
装置:ECZ400R装置(株式会社JEOL RESONANCE製)
観測核:31P
観測周波数:161.944MHz
測定温度:室温
パルス系列:シングルパルス(90°パルスを使用)
90°パルス幅:3.8μ
FID測定後、次のパルス印加までの待ち時間 300秒
マジックアングル回転の回転数 12kHz
積算回数 64回
測定範囲:250ppm〜−150ppm
31PNMRスペクトルの測定において、化学シフトは、外部基準として(NH4)2HPO4(化学シフト1.33ppm)を用いることで得た。
各例で製造した硫化物固体電解質の粉末約100mgをガラスキャピラリに充填して紫外線硬化性樹脂で密封し、下記装置及び条件にて顕微ラマン測定を行った。各サンプルで、サンプルの異なる位置で5回の測定を行い、得られたプロファイルを平均化したプロファイルを使用した。
装置:Almega(サーモフィッシャーサイエンティフィック株式会社製)
レーザ: 532 nm
レーザ出力レベル: 10%
レーザ偏光: 平行
グレーティング: 2400lines/mm
分光器アパーチャ: 25μmピンホール
測定範囲:90〜1300 cm−1
露光時間: 10秒
露光回数: 20
バックグラウンド露光回数: 20
測定回数:5
(硫化リチウム(Li2S)の製造)
撹拌機付きの500mLセパラブルフラスコに、不活性ガス下で乾燥したLiOH無水物(本荘ケミカル社製)を200g仕込んだ。窒素気流下にて昇温し、内部温度を200℃に保持した。窒素ガスを硫化水素ガス(住友精化)に切り替え、500mL/minの流量にし、LiOH無水物と硫化水素を反応させた。
反応により発生する水分はコンデンサーにより凝縮して回収した。反応を6時間行った時点で水が144mL回収された。さらに3時間反応を継続したが、水の発生は見られなかった。
生成物粉末を回収して、純度及びXRDを測定した。その結果、純度は98.5%であり、XRDではLi2Sのピークパターンが確認できた。
製造例1で製造した硫化リチウム(純度98.5%)、五硫化二リン(サーモフォス社製、純度99.9%以上)及び塩化リチウム(シグマアルドリッチ社製、純度99%)を出発原料に用いた(以下、全ての実施例において、各出発原料の純度は同様である)。硫化リチウム(Li2S)、五硫化二リン(P2S5)、及び塩化リチウム(LiCl)のmol比(Li2S:P2S5:LiCl)が46.8:12.7:40.5となるように、各原料を混合した。具体的には、硫化リチウム0.483g、五硫化二リン0.632g、塩化リチウム0.385gを混合し、原料混合物とした。
実施例1の中間体のXRDパターンを図1に示す。遊星型ボールミルによる処理により、原料がガラス化したことを示すハローパターンが確認できる。原料の一部が残存しているものの大部分はガラスとなっていた。
上記中間体の粉末約1.5gをAr雰囲気下のグローブボックス内で、タンマン管(PT2,東京硝子機器株式会社製)内に詰め、石英ウールでタンマン管の口を塞ぎ、さらにSUS製の密閉容器で大気が入らないよう封をした。その後、密閉容器を電気炉(FUW243PA、アドバンテック社製)内に入れ熱処理した。具体的には、室温から500℃まで2.5℃/minで昇温し(3時間で500℃に昇温)、500℃で8時間保持した。その後、徐冷し、硫化物固体電解質を得た。
原料組成、製造条件及び評価結果を表1に示す。
硫化物固体電解質をICP分析し、各元素のモル比を測定した。結果を表2に示す。
得られた硫化物固体電解質のXRDパターンを図2に示す。2θ=15.6、18.0、25.6,30.1、31.5、45.2、48,1degにアルジロダイト型結晶構造に由来するピークが観測された。また、2θ=14.4、29.2、33.8degに新規結晶構造に由来するピークが観測された。一方、Li3PS4結晶構造由来の回折ピークは観測されなかった。
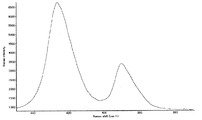
得られた硫化物固体電解質のラマン測定結果を図4に示す。430cm−1付近にアルジロダイト構造に由来したピークと、390cm−1付近に新規結晶構造に由来するピークが観測された。
遊星型ボールミルによる処理時間を60時間とした他は、実施例1と同様にして硫化物固体電解質を作製し、評価した。結果を表1及び2に示す。
XRDの測定結果、2θ=15.5、18.0、25.6、30.1、31.5、45.1、48.1degにアルジロダイト型結晶構造に由来するピークが観測された。2θ=14.4、29.2、33.8degに新規結晶構造に由来するピークが観測された。一方、Li3PS4結晶構造由来の回折ピークは観測されなかった。なお、電子伝導性は10−6S/cm未満であった。
原料組成及びメカニカルミリング条件及び熱処理条件を表1に示すように変更した他は、実施例2と同様にして硫化物固体電解質を作製した。
なお、実施例5の熱処理はAr流通下で実施した。具体的に、Ar雰囲気下のグローブボックス内で中間体をシール機能付きのガラス管内に詰め、大気が入らないように、ガラス管の先端を専用治具で封をした。その後、ガラス管を電気炉内にセットした。専用治具を電気炉内にある継手に差し入れて、ガス流通管に繋ぎ、Arを0.5L/minで流通しながら熱処理した。具体的には、室温から500℃まで3℃/minで昇温し、500℃で8時間保持した。その後、徐冷し、硫化物固体電解質を得た。
実施例4〜6についても、2θ=25.2±0.5deg及び29.7±0.5degにそれぞれアルジロダイト型結晶構造に由来するピークが観測され、且つ、2θ=14.4±0.5deg及び33.8±0.5degにそれぞれ新規結晶構造に由来するピークが観測された。
比較例1では、2θ=15.5、25.6、30.0、30.4、45.2、48.1degにアルジロダイト型結晶構造に由来するピークが観測された。一方、新規結晶構造に由来するピークは観測されなかった。また、2θ=17.6、18.2degにLi3PS4結晶構造に由来するピークが観測され、IA/IB=0.16であった(IAは2θ=17.6±0.4deg及び2θ=18.1±0.4degのうちアルジロダイト型結晶構造に起因する回折ピークではないものの回折ピークの強度を表し、IBは2θ=29.7±0.5degの回折ピークの強度を表す。)。なお、電子伝導性は10−6S/cm未満であった。
原料粉末の処理について、表1に示す原料を遊星型ボールミルで原料の結晶性を維持できる程度に混合し、混合粉末とした。
得られた混合粉末のXRDパターンを図7に示す。XRDパターンから、原料であるLi2S、P2S5、LiClのピークが確認でき、原料粉末の結晶性が維持されていた。
上記混合粉末の熱処理時に硫化水素を導入した。具体的に、Ar雰囲気下のグローブボックス内で、混合粉末約1.5gをシール機能付きのガラス管内に詰め、大気が入らないように、ガラス管の先端を専用治具で封をした。その後、ガラス管を電気炉内にセットした。専用治具を電気炉内にある継手に差し入れて、ガス流通管に繋ぎ、硫化水素を0.5L/minで流通しながら熱処理した。具体的には、室温から500℃まで3℃/minで昇温し、500℃で4時間保持した。その後、徐冷し、硫化物固体電解質を得た。
硫化物固体電解質の製造条件及び評価結果を表1及び2に示す。
実施例1で用いた硫化リチウム、五硫化二リン及び塩化リチウムと、臭化リチウム(LiBr:シグマアルドリッチ社製、純度99%)を出発原料に用いた。mol比(Li2S:P2S5:LiCl:LiBr)が46.8:12.7:35.4:5.1となるように、各原料を混合した。具体的には、硫化リチウム0.476g、五硫化二リン0.594g、塩化リチウム0.332g、臭化リチウム0.097gを混合し、原料混合物とした。
原料混合物を変更した他は、実施例1と同様にして硫化物固体電解質を作製した。
硫化物固体電解質のσは、9.8mS/cmであった。なお、電子伝導性は10−6S/cm未満であった。
XRD測定の結果、アルジロダイト型結晶構造に由来するピークが観測され、新規結晶構造に由来するピークが観察された。ピーク強度比は、0.006であった。
ICP分析の結果、モル比a(Li/P)は、5.3、モル比b(S/P)は4.4、モル比c((Cl+Br)/P)は1.6であった。
実施例7で用いた硫化リチウム、五硫化二リン、塩化リチウム及び臭化リチウムと、ヨウ化リチウムとを出発原料に用いた。mol比(Li2S:P2S5:LiCl:LiBr:LiI)が46.8:12.7:32.9:5.1:2.5となるように、各原料を混合した。具体的には、硫化リチウム0.460g、五硫化二リン0.575g、塩化リチウム0.298g、臭化リチウム0.094g、ヨウ化リチウム0.072gを混合し、原料混合物とした。
原料混合物を変更した他は、実施例1と同様にして硫化物固体電解質を作製した。
硫化物固体電解質のσは、9.0mS/cmであった。なお、電子伝導性は10−6S/cm未満であった。
XRD測定の結果、アルジロダイト型結晶構造に由来するピークが観測され、新規結晶構造に由来するピークが観察された。ピーク強度比は、0.009であった。
ICP分析の結果、モル比a(Li/P)は、5.3、モル比b(S/P)は4.4、モル比c((Cl+Br+I)/P)は1.6であった。
実施例1で使用した用いた硫化リチウム、五硫化二リン及び塩化リチウムと、硫化ゲルマニウム(IV)(GeS2:高純度科学研究所社製、純度99%)を出発原料に用いた。mol比(Li2S:P2S5:GeS2:LiCl)が46.9:11.1:2.5:39.5となるように、各原料を混合した。具体的には、硫化リチウム0.487g、五硫化二リン0.558g、硫化ゲルマニウム(IV)0.076g、塩化リチウム0.378gを混合し、原料混合物とした。
原料混合物を変更した他は、実施例1と同様にして硫化物固体電解質を作製した。
硫化物固体電解質のσは、7.2mS/cmであった。なお、電子伝導性は10−6S/cm未満であった。
XRD測定の結果、アルジロダイト型結晶構造に由来するピークが観測され、新規結晶構造に由来するピークが観察された。ピーク強度比は、0.020であった。
ICP分析の結果、モル比a(Li/(P+Ge))は5.3、モル比b(S/(P+Ge))は4.3、モル比c(Cl/(P+Ge))は1.6であった。
実施例1で使用した用いた硫化リチウム、五硫化二リン及び塩化リチウムと、二硫化珪素(SiS2:高純度科学研究所社製)を出発原料に用いた。mol比(Li2S:P2S5:SiS2:LiCl)が46.9:11.1:2.5:39.5となるように、各原料を混合した。具体的には、硫化リチウム0.495g、五硫化二リン0.567g、二硫化珪素0.052g、塩化リチウム0.385gを混合し、原料混合物とした。
原料混合物を変更した他は、実施例1と同様にして硫化物固体電解質を作製した。
硫化物固体電解質のσは、7.1mS/cmであった。なお、電子伝導性は10−6S/cm未満であった。
XRD測定の結果、アルジロダイト型結晶構造に由来するピークが観測され、新規結晶構造に由来するピークが観察された。ピーク強度比は、0.021であった。
ICP分析の結果、モル比a(Li/(P+Si))は5.3、モル比b(S/(P+Si))は4.3、モル比c(Cl/(P+Si))は1.6であった。
Claims (16)
- リチウム、リン、硫黄及びハロゲン元素を含み、
アルジロダイト型結晶構造を含み、
CuKα線を使用した粉末X線回折測定において2θ=14.4±0.5deg及び33.8±0.5degに回折ピークを有する硫化物固体電解質。 - CuKα線を使用した粉末X線回折において、2θ=25.2±0.5deg及び29.7±0.5degに回折ピークを有する、請求項1に記載の硫化物固体電解質。
- さらに、CuKα線を使用した粉末X線回折において、2θ=29.1±0.5degの回折ピークを有する、請求項1に記載の硫化物固体電解質。
- さらに、CuKα線を使用した粉末X線回折において、2θ=15.3±0.5deg、17.7±0.5deg、31.1±0.5deg、44.9±0.5deg及び47.7±0.5degの回折ピークの少なくとも1つを有する、請求項1〜3のいずれかに記載の硫化物固体電解質。
- 前記回折ピークの範囲が中央値の±0.3degである、請求項1〜4のいずれかに記載の硫化物固体電解質。
- 前記ハロゲン元素が塩素又は臭素である請求項1〜5のいずれかに記載の硫化物固体電解質。
- 硫黄を除くカルコゲン元素及びハロゲン元素からなる群より選択される1種以上の元素Xを含み、リチウムのリンに対するモル比a(Li/P)、硫黄のリンに対するモル比b(S/P)及び元素Xのリンに対するモル比c(X/P)が、下記式(A)〜(C)を満たす請求項1〜6のいずれかに記載の硫化物固体電解質。
5.0≦a≦7.5 ・・・(A)
6.5≦a+c≦7.5 ・・・(B)
0.5≦a−b≦1.5 ・・・(C)
(式中、b>0且つc>0を満たす。) - 前記元素XがF、Cl、Br及びIから選択される1以上のハロゲン元素である、請求項7に記載の硫化物固体電解質。
- 下記式(4)で表される組成を有する請求項1〜6のいずれかに記載の硫化物固体電解質。
Lia(P1−αMα)SbXc (4)
(式(4)中、Mは、Si、Ge、Sn、Pb、B、Al、Ga、As、Sb及びBiからなる群より選択される1以上の元素であり、Xは、F、Cl、Br、I、O、Se及びTeからなる群から選択される1以上の元素である。a〜cは下記式(1)〜(3)を満たす。αは0≦α≦0.3である。)
5.0≦a≦7.5 ・・・(1)
6.5≦a+c≦7.5 ・・・(2)
0.5≦a−b≦1.5 ・・・(3)
(式中、b>0且つc>0を満たす。) - 前記XがF、Cl、Br及びIから選択される1以上のハロゲン元素である、請求項9に記載の硫化物固体電解質。
- CuKα線を使用した粉末X線回折において、2θ=17.6±0.4deg及び2θ=18.1±0.4degに回折ピーク(アルジロダイト型結晶構造に起因するピークではない)を有しないか、有する場合には下記式(5)を満たす、請求項1〜10のいずれかに記載の硫化物固体電解質。
0<IA/IB<0.1 (5)
(式中、IAは2θ=17.6±0.4deg及び2θ=18.1±0.4degのうちアルジロダイト型結晶構造に起因する回折ピークではないものの回折ピークの強度を表し、IBは2θ=29.7±0.5degの回折ピークの強度を表す。) - 固体31P−NMR測定において、110±5ppmにピークを有する請求項1〜11のいずれかに記載の硫化物固体電解質。
- CuKα線を使用した粉末X線回折において、下記式(6)を満たす、請求項2〜12のいずれかに記載の硫化物固体電解質。
0<IC/IB<0.100・・・(6)
(式中、ICは2θ=14.4±0.5degの回折ピークの強度を表し、IBは2θ=29.7±0.5degの回折ピークの強度を表す。) - ラマン分光測定において380cm−1〜395cm−1の範囲内にピークを有する、請求項1〜13のいずれかに記載の硫化物固体電解質。
- 請求項1〜14のいずれかに記載の硫化物固体電解質と、活物質を含む電極合材。
- 請求項1〜14のいずれかに記載の硫化物固体電解質及び請求項15に記載の電極合材のうち少なくとも1つを含むリチウムイオン電池。
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2021137768A JP7258089B2 (ja) | 2016-08-12 | 2021-08-26 | 硫化物固体電解質 |
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2016158995 | 2016-08-12 | ||
| JP2016158995 | 2016-08-12 |
Related Child Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2021137768A Division JP7258089B2 (ja) | 2016-08-12 | 2021-08-26 | 硫化物固体電解質 |
Publications (3)
| Publication Number | Publication Date |
|---|---|
| JP2018029058A JP2018029058A (ja) | 2018-02-22 |
| JP2018029058A5 JP2018029058A5 (ja) | 2020-03-12 |
| JP6936073B2 true JP6936073B2 (ja) | 2021-09-15 |
Family
ID=61248583
Family Applications (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2017153385A Active JP6936073B2 (ja) | 2016-08-12 | 2017-08-08 | 硫化物固体電解質 |
| JP2021137768A Active JP7258089B2 (ja) | 2016-08-12 | 2021-08-26 | 硫化物固体電解質 |
Family Applications After (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2021137768A Active JP7258089B2 (ja) | 2016-08-12 | 2021-08-26 | 硫化物固体電解質 |
Country Status (1)
| Country | Link |
|---|---|
| JP (2) | JP6936073B2 (ja) |
Families Citing this family (23)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP6936073B2 (ja) * | 2016-08-12 | 2021-09-15 | 出光興産株式会社 | 硫化物固体電解質 |
| CN112331910A (zh) * | 2017-07-07 | 2021-02-05 | 三井金属矿业株式会社 | 锂二次电池的固体电解质及该固体电解质用硫化物系化合物 |
| WO2019131725A1 (ja) * | 2017-12-28 | 2019-07-04 | 三井金属鉱業株式会社 | 固体電解質 |
| KR102063159B1 (ko) * | 2018-07-17 | 2020-01-08 | 한국과학기술연구원 | 셀레늄을 포함하는 리튬 이온 전도성 황화물계 고체전해질 및 이의 제조방법 |
| US20200087155A1 (en) * | 2018-09-19 | 2020-03-19 | Blue Current, Inc. | Lithium oxide argyrodites |
| JP2020061304A (ja) * | 2018-10-11 | 2020-04-16 | 古河機械金属株式会社 | 硫化物系無機固体電解質材料用の五硫化二リン組成物 |
| KR20220088689A (ko) * | 2019-10-29 | 2022-06-28 | 미쓰이금속광업주식회사 | 고체 전해질 및 그것을 사용한 전극 합제, 고체 전해질층, 고체 전지 |
| EP4053948A4 (en) * | 2019-10-29 | 2022-11-30 | Mitsui Mining & Smelting Co., Ltd. | SOLID ELECTROLYTE, AND MIXTURE OF ELECTRODES, SOLID ELECTROLYTE LAYER AND SOLID ELECTROLYTE BATTERY, EACH USING SUCH SOLID ELECTROLYTE |
| CN114556492A (zh) * | 2019-10-29 | 2022-05-27 | 三井金属矿业株式会社 | 固体电解质和使用其的电极合剂、固体电解质层、固态电池 |
| JP6935041B1 (ja) | 2019-12-11 | 2021-09-15 | 三井金属鉱業株式会社 | 硫化物固体電解質 |
| JP7301005B2 (ja) * | 2020-01-08 | 2023-06-30 | Jx金属株式会社 | 硫化物系固体電解質及び全固体リチウムイオン電池 |
| EP4129901A4 (en) * | 2020-03-23 | 2024-05-01 | Mitsui Mining & Smelting Co Ltd | SULFIDE SOLID ELECTROLYTE AND ELECTRODE MIXTURE, SOLID ELECTROLYTE LAYER AND BODY BATTERY |
| US20230343996A1 (en) * | 2020-07-09 | 2023-10-26 | Mitsui Mining & Smelting Co., Ltd. | Method for producing lithium sulfide |
| EP4206124A1 (en) * | 2020-08-28 | 2023-07-05 | Mitsui Mining & Smelting Co., Ltd. | Active material, method for producing same, electrode mixture and battery |
| JP7477414B2 (ja) * | 2020-09-24 | 2024-05-01 | Jx金属株式会社 | 硫化物系固体電解質及び全固体リチウムイオン電池 |
| EP4242267A1 (en) * | 2020-11-09 | 2023-09-13 | Idemitsu Kosan Co.,Ltd. | Resin composition, binder for battery, electrode mixture layer for battery, electrolyte layer, sheet for battery, battery, and resin composition production method |
| CN112510254B (zh) * | 2020-11-30 | 2022-07-19 | 北京理工大学 | 一种新型硫化物固态电解质及其制备方法和用途 |
| CN113471521B (zh) * | 2021-06-30 | 2022-08-19 | 国联汽车动力电池研究院有限责任公司 | 一种无机硫化物固体电解质及其制备方法 |
| CN113363569B (zh) * | 2021-06-30 | 2023-05-05 | 国联汽车动力电池研究院有限责任公司 | 一种高稳定性无机硫化物固体电解质及其制备方法 |
| KR20230006324A (ko) * | 2021-07-02 | 2023-01-10 | 삼성에스디아이 주식회사 | 전고체 이차전지용 황화물계 고체 전해질, 그 제조방법 및 이를 포함하는 전고체 이차전지 |
| CN114852980B (zh) * | 2022-04-22 | 2024-04-05 | 武汉理工大学 | 一种锂电池用固态电解质材料及其制备方法 |
| KR20240028949A (ko) * | 2022-08-25 | 2024-03-05 | 주식회사 엘지화학 | 고체 전해질 및 이를 포함하는 전고체 전지 |
| WO2024101239A1 (ja) * | 2022-11-11 | 2024-05-16 | 古河機械金属株式会社 | 硫化物系無機固体電解質材料の製造方法、硫化リン組成物の製造方法、硫化リン組成物の評価方法および硫化リン組成物 |
Family Cites Families (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2015011937A1 (ja) * | 2013-07-25 | 2015-01-29 | 三井金属鉱業株式会社 | リチウムイオン電池用硫化物系固体電解質 |
| JP2016134316A (ja) * | 2015-01-20 | 2016-07-25 | 出光興産株式会社 | 固体電解質 |
| JP6936073B2 (ja) | 2016-08-12 | 2021-09-15 | 出光興産株式会社 | 硫化物固体電解質 |
-
2017
- 2017-08-08 JP JP2017153385A patent/JP6936073B2/ja active Active
-
2021
- 2021-08-26 JP JP2021137768A patent/JP7258089B2/ja active Active
Also Published As
| Publication number | Publication date |
|---|---|
| JP7258089B2 (ja) | 2023-04-14 |
| JP2021192375A (ja) | 2021-12-16 |
| JP2018029058A (ja) | 2018-02-22 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP6936073B2 (ja) | 硫化物固体電解質 | |
| US11264642B2 (en) | Sulfide solid electrolyte | |
| JP7187637B2 (ja) | 硫化物固体電解質の製造方法 | |
| JP7102453B2 (ja) | 硫化物固体電解質 | |
| JP6934042B2 (ja) | 硫化物固体電解質粒子 | |
| US20220367907A1 (en) | Sulfide solid electrolyte | |
| JP7013456B2 (ja) | 硫化物固体電解質 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20200131 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20200131 |
|
| A977 | Report on retrieval |
Free format text: JAPANESE INTERMEDIATE CODE: A971007 Effective date: 20201021 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20201201 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20210128 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20210315 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20210803 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20210826 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 6936073 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |