JP6445874B2 - 酸性ガス吸収剤、酸性ガス除去方法および酸性ガス除去装置 - Google Patents
酸性ガス吸収剤、酸性ガス除去方法および酸性ガス除去装置 Download PDFInfo
- Publication number
- JP6445874B2 JP6445874B2 JP2015005378A JP2015005378A JP6445874B2 JP 6445874 B2 JP6445874 B2 JP 6445874B2 JP 2015005378 A JP2015005378 A JP 2015005378A JP 2015005378 A JP2015005378 A JP 2015005378A JP 6445874 B2 JP6445874 B2 JP 6445874B2
- Authority
- JP
- Japan
- Prior art keywords
- carbon dioxide
- acid gas
- gas
- absorption
- mol
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Expired - Fee Related
Links
Images
Classifications
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01D—SEPARATION
- B01D53/00—Separation of gases or vapours; Recovering vapours of volatile solvents from gases; Chemical or biological purification of waste gases, e.g. engine exhaust gases, smoke, fumes, flue gases, aerosols
- B01D53/14—Separation of gases or vapours; Recovering vapours of volatile solvents from gases; Chemical or biological purification of waste gases, e.g. engine exhaust gases, smoke, fumes, flue gases, aerosols by absorption
- B01D53/1493—Selection of liquid materials for use as absorbents
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01D—SEPARATION
- B01D53/00—Separation of gases or vapours; Recovering vapours of volatile solvents from gases; Chemical or biological purification of waste gases, e.g. engine exhaust gases, smoke, fumes, flue gases, aerosols
- B01D53/14—Separation of gases or vapours; Recovering vapours of volatile solvents from gases; Chemical or biological purification of waste gases, e.g. engine exhaust gases, smoke, fumes, flue gases, aerosols by absorption
- B01D53/1456—Removing acid components
- B01D53/1475—Removing carbon dioxide
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01D—SEPARATION
- B01D2252/00—Absorbents, i.e. solvents and liquid materials for gas absorption
- B01D2252/20—Organic absorbents
- B01D2252/204—Amines
- B01D2252/20431—Tertiary amines
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01D—SEPARATION
- B01D2252/00—Absorbents, i.e. solvents and liquid materials for gas absorption
- B01D2252/20—Organic absorbents
- B01D2252/204—Amines
- B01D2252/20436—Cyclic amines
- B01D2252/20447—Cyclic amines containing a piperazine-ring
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01D—SEPARATION
- B01D2252/00—Absorbents, i.e. solvents and liquid materials for gas absorption
- B01D2252/20—Organic absorbents
- B01D2252/204—Amines
- B01D2252/20478—Alkanolamines
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01D—SEPARATION
- B01D2252/00—Absorbents, i.e. solvents and liquid materials for gas absorption
- B01D2252/50—Combinations of absorbents
- B01D2252/504—Mixtures of two or more absorbents
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01D—SEPARATION
- B01D2252/00—Absorbents, i.e. solvents and liquid materials for gas absorption
- B01D2252/60—Additives
- B01D2252/602—Activators, promoting agents, catalytic agents or enzymes
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y02—TECHNOLOGIES OR APPLICATIONS FOR MITIGATION OR ADAPTATION AGAINST CLIMATE CHANGE
- Y02C—CAPTURE, STORAGE, SEQUESTRATION OR DISPOSAL OF GREENHOUSE GASES [GHG]
- Y02C20/00—Capture or disposal of greenhouse gases
- Y02C20/40—Capture or disposal of greenhouse gases of CO2
Landscapes
- Chemical & Material Sciences (AREA)
- Engineering & Computer Science (AREA)
- Analytical Chemistry (AREA)
- General Chemical & Material Sciences (AREA)
- Oil, Petroleum & Natural Gas (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Catalysts (AREA)
- Treating Waste Gases (AREA)
- Gas Separation By Absorption (AREA)
- Carbon And Carbon Compounds (AREA)
Description
この酸性ガスを吸収した酸性ガス吸収剤から酸性ガスを脱離させて、この酸性ガス吸収剤を再生する再生器とを有し、
前記の再生器で再生した前記の酸性ガス吸収剤を前記の吸収器にて再利用すること、を特徴とするものである。
実施形態の酸性ガス吸収剤は、下記の一般式(1)で表される第3級アルカノールアミンと、第1級アミンおよび第2級アミンからなる群から選ばれた反応促進剤とを含有すること、を特徴とするものである。
従来より、アミン化合物が有する立体障害は、酸性ガス吸収時の生成物に対する影響が大きく、低反応熱を示す重炭酸イオンの生成に有利に働くことが知られている。例えば分岐構造を有するN−イソプロピルアミノエタノールは、二酸化炭素の吸収反応に対して低反応熱性を示すことが報告されている。しかしながら、例えば2−アミノ−2−メチル−1−プロパノールアミンのように立体障害が大きいアミンは融点が比較的高く、CO2吸収するとさらに凝固しやすいという課題がある。さらに吸収能力を高めるために他アミンを1種類以上混合することが知られているが、その際に室温で固体であるアミンを混合すると、混合した吸収液はさらに凝固しやすくなる。
2−(ジメチルアミノ)−2−メチル−1−プロパノール、
2−(ジメチルアミノ)−2−エチル−1−プロパノール、
2−(ジメチルアミノ)−2−プロピル−1−プロパノール、
2−(ジメチルアミノ)−2−イソプロピル−1−プロパノール、
2−(ジメチルアミノ)−2−ブチル−1−プロパノール、
2−(ジメチルアミノ)−2−sec−ブチル−1−プロパノール、
2−(ジメチルアミノ)−2−tert−ブチル−1−プロパノール、
2−(N−メチル−N−エチルアミノ)−2−メチル−1−プロパノール、
2−(N−メチル−N−エチルアミノ)−2−エチル−1−プロパノール、
2−(N−メチル−N−エチルアミノ)−2−プロピル−1−プロパノール、
2−(N−メチル−N−エチルアミノ)−2−イソプロピル−1−プロパノール、
2−(N−メチル−N−エチルアミノ)−2−ブチル−1−プロパノール、
2−(N−メチル−N−エチルアミノ)−2−sec−ブチル−1−プロパノール、
2−(N−メチル−N−エチルアミノ)−2−tert−ブチル−1−プロパノール、
2−(ジエチルアミノ)−2−メチル−1−プロパノール、
2−(ジエチルアミノ)−2−エチル−1−プロパノール、
2−(ジエチルアミノ)−2−プロピル−1−プロパノール
2−(ジエチルアミノ)−2−イソプロピル−1−プロパノール、
2−(ジエチルアミノ)−2−ブチル−1−プロパノール、
2−(ジエチルアミノ)−2−sec−ブチル−1−プロパノール、
2−(ジエチルアミノ)−2−tert−ブチル−1−プロパノール、
2−(N−メチル−N−プロピルアミノ)−2−メチル−1−プロパノール、
2−(N−メチル−N−プロピルアミノ)−2−エチル−1−プロパノール、
2−(N−メチル−N−プロピルアミノ)−2−プロピル−1−プロパノール、
2−(N−メチル−N−プロピルアミノ)−2−イソプロピル−1−プロパノール、
2−(N−メチル−N−プロピルアミノ)−2−ブチル−1−プロパノール、
2−(N−メチル−N−プロピルアミノ)−2−sec−ブチル−1−プロパノール、
2−(N−メチル−N−プロピルアミノ)−2−tert−ブチル−1−プロパノール、
2−(N−メチル−N−イソプロピルアミノ)−2−メチル−1−プロパノール、
2−(N−メチル−N−イソプロピルアミノ)−2−エチル−1−プロパノール、
2−(N−メチル−N−イソプロピルアミノ)−2−プロピル−1−プロパノール、
2−(N−メチル−N−イソプロピルアミノ)−2−イソプロピル−1−プロパノール、
2−(N−メチル−N−イソプロピルアミノ)−2−ブチル−1−プロパノール、
2−(N−メチル−N−イソプロピルアミノ)−2−sec−ブチル−1−プロパノール、
2−(N−メチル−N−イソプロピルアミノ)−2−tert−ブチル−1−プロパノール、
2−(N−エチル−N−プロピルアミノ)−2−メチル−1−プロパノール、
2−(N−エチル−N−プロピルアミノ)−2−エチル−1−プロパノール、
2−(N−エチル−N−プロピルアミノ)−2−プロピル−1−プロパノール、
2−(N−エチル−N−プロピルアミノ)−2−イソプロピル−1−プロパノール、
2−(N−エチル−N−プロピルアミノ)−2−ブチル−1−プロパノール、
2−(N−エチル−N−プロピルアミノ)−2−sec−ブチル−1−プロパノール、
2−(N−エチル−N−プロピルアミノ)−2−tert−ブチル−1−プロパノール、
2−(N−エチル−N−イソプロピルアミノ)−2−メチル−1−プロパノール、
2−(N−エチル−N−イソプロピルアミノ)−2−エチル−1−プロパノール、
2−(N−エチル−N−イソプロピルアミノ)−2−プロピル−1−プロパノール、
2−(N−エチル−N−イソプロピルアミノ)−2−イソプロピル−1−プロパノール、
2−(N−エチル−N−イソプロピルアミノ)−2−ブチル−1−プロパノール、
2−(N−エチル−N−イソプロピルアミノ)−2−sec−ブチル−1−プロパノール、
2−(N−エチル−N−イソプロピルアミノ)−2−tert−ブチル−1−プロパノール、
2−(N−プロピル−N−プロピルアミノ)−2−メチル−1−プロパノール、
2−(N−プロピル−N−プロピルアミノ)−2−エチル−1−プロパノール、
2−(N−プロピル−N−プロピルアミノ)−2−プロピル−1−プロパノール、
2−(N−プロピル−N−プロピルアミノ)−2−イソプロピル−1−プロパノール、
2−(N−プロピル−N−プロピルアミノ)−2−ブチル−1−プロパノール、
2−(N−プロピル−N−プロピルアミノ)−2−sec−ブチル−1−プロパノール、
2−(N−プロピル−N−プロピルアミノ)−2−tert−ブチル−1−プロパノール、
2−(N−プロピル−N−イソプロピルアミノ)−2−メチル−1−プロパノール、
2−(N−プロピル−N−イソプロピルアミノ)−2−エチル−1−プロパノール、
2−(N−プロピル−N−イソプロピルアミノ)−2−プロピル−1−プロパノール、
2−(N−プロピル−N−イソプロピルアミノ)−2−イソプロピル−1−プロパノール、
2−(N−プロピル−N−イソプロピルアミノ)−2−ブチル−1−プロパノール、
2−(N−プロピル−N−イソプロピルアミノ)−2−sec−ブチル−1−プロパノール、
2−(N−プロピル−N−イソプロピルアミノ)−2−tert−ブチル−1−プロパノール、
2−(ジメチルアミノ)−2−メチル−1−ブタノール、
2−(ジメチルアミノ)−2−エチル−1−ブタノール、
2−(ジメチルアミノ)−2−プロピル−1−ブタノール、
2−(ジメチルアミノ)−2−イソプロピル−1−ブタノール、
2−(ジメチルアミノ)−2−ブチル−1−ブタノール、
2−(ジメチルアミノ)−2−sec−ブチル−1−ブタノール、
2−(ジメチルアミノ)−2−tert−ブチル−1−ブタノール、
2−(N−メチル−N−エチルアミノ)−2−メチル−1−ブタノール、
2−(N−メチル−N−エチルアミノ)−2−エチル−1−ブタノール、
2−(N−メチル−N−エチルアミノ)−2−プロピル−1−ブタノール、
2−(N−メチル−N−エチルアミノ)−2−イソプロピル−1−ブタノール、
2−(N−メチル−N−エチルアミノ)−2−ブチル−1−ブタノール、
2−(N−メチル−N−エチルアミノ)−2−sec−ブチル−1−ブタノール、
2−(N−メチル−N−エチルアミノ)−2−tert−ブチル−1−ブタノール、
2−(ジエチルアミノ)−2−メチル−1−ブタノール、
2−(ジエチルアミノ)−2−エチル−1−ブタノール、
2−(ジエチルアミノ)−2−プロピル−1−ブタノール
2−(ジエチルアミノ)−2−イソプロピル−1−ブタノール、
2−(ジエチルアミノ)−2−ブチル−1−ブタノール、
2−(ジエチルアミノ)−2−sec−ブチル−ブタノール、
2−(ジエチルアミノ)−2−tert−ブチル−1−ブタノール、
などを挙げることができる。
本発明の実施形態の酸性ガス吸収剤は、第1級アミンおよび第2級アミンからなる群から選ばれた反応促進剤とさらに含有する。
モノエタノールアミン、
2−アミノ−2−メチル−1−プロパノール、
2−アミノ−2−メチル−1,3−ジプロパノール、
ジエタノールアミン、
2−メチルアミノエタノール、
2−エチルアミノエタノール、
2−プロピルアミノエタノール、
n−ブチルアミノエタノール、
2−(イソプロピルアミノ)エタノール、
3−エチルアミノプロパノール等が挙げられる。
アゼチジン、
2−メチルアゼチジン、
2−エチルアゼチジン、
2−アゼチジルメタノール、
2−(2−アミノエチル)アゼチジン、
ピロリジン、
2−メチルピロリジン、
2−エチルピロリジン、
2−ピロリジルメタノール、
2−(2−アミノエチル)ピロリジン、
ピペリジン、
2−メチルピペリジン、
2−エチルピペリジン、
3−メチルピペリジン、
3−エチルピペリジン、
2−ピペリジンメタノール、
2−ピペリジンエタノール、
3−ピペリジンメタノール、
3−ピペリジンエタノール、
4−ピペリジンメタノール、
4−ピペリジンエタノール、
2−(2−アミノエチル)ピロリジン、
ヘキサヒドロ−1H−アゼピン、
ピペラジン、ピぺラジン誘導体
などを挙げることができる。
本発明の実施形態による酸性ガス吸収剤は、一般式(1)で表される第3級アルカノールアミンと、第1級アミンおよび第2級アミンからなる群から選ばれた反応促進剤とを含むものであって、例えば水等の溶媒と、必要に応じて各種の補助材料等と混合したうえで、例えば酸性ガス吸収方法ないし酸性ガス吸収装置の酸性ガス吸収剤として好適なものである。ここで、補助材料の具体例には、例えば、酸化防止剤、pH調整剤、消泡剤、防食剤等が包含される。
本発明の実施形態による酸性ガスの除去方法は、酸性ガスを含有するガスと、上述の実施形態による酸性ガス吸収剤とを接触させて、前記の酸性ガスを含むガスから酸性ガスを除去すること、を特徴とするものである。
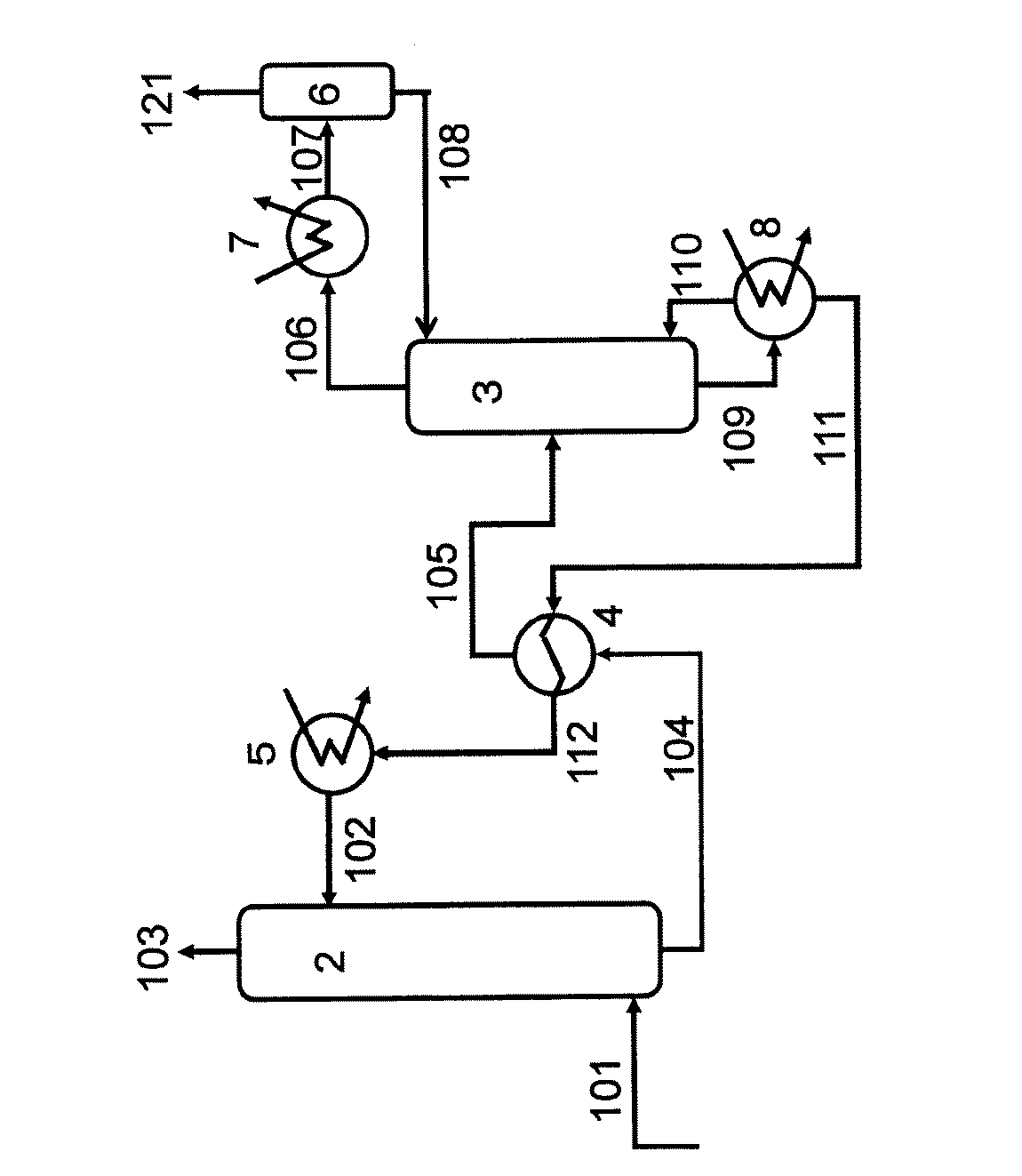
本発明の実施形態による酸性ガス除去装置は、酸性ガスを含有するガスと前述した特定の本発明の実施形態による酸性ガス吸収剤とを接触させ、この酸性ガス吸収剤に酸性ガスを吸収させることにより前記の酸性ガスを含有するガスから酸性ガスを除去する吸収器と、この酸性ガスを吸収した酸性ガス吸収剤から酸性ガスを脱離させて、この酸性ガス吸収剤を再生する再生器と、を有し、前記の再生器で再生した前記の酸性ガス吸収剤を前記の吸収器にて再利用する酸性ガス除去装置であること、を特徴とするものである。
2−(ジメチルアミノ)−2−メチル−1−プロパノール(DMAMP)を40質量%、ピペラジン(PZ)を3質量%となるように水に溶解させ、50mlの水溶液(以下、吸収液と示す。)とした。この吸収液を試験管に充填して40℃に加熱し、二酸化炭素10体積%、窒素(N2)ガス90体積%含む混合ガスを流速500mL/minで3時間通気して、試験管出口でのガス中の二酸化炭素濃度を赤外線式ガス濃度測定装置(株式会社島津製作所製、商品名「CGT−7000」)を用いて測定し、吸収性能を評価した。試験管内のアミン水溶液へのガス導入口には、1/8インチのテフロン(登録商標)チューブ(内径:1.59mm、外径:3.17mm)を用いて行った。
その結果、二酸化炭素吸収前および40℃で二酸化炭素吸収させた吸収液共に凝固しなかった。
2−(ジメチルアミノ)−2−メチル−1−プロパノールを40質量%、ピペラジンを5質量%となるよう水に溶解させた以外は、実施例1と同様にして吸収液(水溶液)を調製し、実施例1と同様の装置を用い、同一条件下で二酸化炭素吸収量、二酸化炭素吸収速度、および凝固性を測定した。
また、二酸化炭素吸収前および40℃で二酸化炭素吸収させた吸収液共に凝固しなかった。
2−(ジメチルアミノ)−2−メチル−1−プロパノールを40質量%、ピペラジンを15質量%となるよう水に溶解させた以外は、実施例1と同様にして吸収液(水溶液)を調製し、実施例1と同様の装置を用い、同一条件下で二酸化炭素吸収量、二酸化炭素吸収速度、および凝固性を測定した。
また、二酸化炭素吸収前および40℃で二酸化炭素吸収させた吸収液共に凝固した。
2−(ジメチルアミノ)−2−メチル−1−プロパノールを30質量%、ピペラジンを5質量%となるよう水に溶解させた以外は、実施例1と同様にして吸収液(水溶液)を調製し、実施例1と同様の装置を用い、同一条件下で二酸化炭素吸収量、二酸化炭素吸収速度、および凝固性を測定した。
また、二酸化炭素吸収前および40℃で二酸化炭素吸収させた吸収液共に凝固しなかった。
2−(ジメチルアミノ)−2−メチル−1−プロパノールを60質量%、ピペラジンを5質量%となるよう水に溶解させた以外は、実施例1と同様にして吸収液を調製し、実施例1と同様の装置を用い、同一条件下で二酸化炭素吸収量、二酸化炭素吸収速度、および凝固性を測定した。
また、CO2吸収前の吸収液は凝固し、40℃で二酸化炭素吸収させた吸収液は凝固しなかった。
2−(ジメチルアミノ)−2−メチル−1−プロパノールを15質量%、ピペラジンを5質量%となるよう水に溶解させた以外は、実施例1と同様にして吸収液(水溶液)を調製し、実施例1と同様の装置を用い、同一条件下で二酸化炭素吸収量、二酸化炭素吸収速度、および凝固性を測定した。
また、二酸化炭素吸収前および40℃で二酸化炭素吸収させた吸収液共に凝固しなかった。
2−(エチルメチルアミノ)−2−メチル−1−プロパノール(EMAMP)を40質量%、ピペラジンを5質量%となるよう水に溶解させた以外は、実施例1と同様にして吸収液(水溶液)を調製し、実施例1と同様の装置を用い、同一条件下で二酸化炭素吸収量、二酸化炭素吸収速度、および凝固性を測定した。
2−(ジメチルアミノ)−2−エチル−1−プロパノール(DMAEP)を40質量%、ピペラジンを5質量%となるよう水に溶解させた以外は、実施例1と同様にして吸収液(水溶液)を調製し、実施例1と同様の装置を用い、同一条件下で二酸化炭素吸収量、二酸化炭素吸収速度、および凝固性を測定した。
2−(ジエチルアミノ)−2−メチル−1−プロパノール(DEAMP)を40質量%、ピペラジンを5質量%となるよう水に溶解させた以外は、実施例1と同様にして吸収液(水溶液)を調製し、実施例1と同様の装置を用い、同一条件下で二酸化炭素吸収量、二酸化炭素吸収速度、および凝固性を測定した。
2−(ジメチルアミノ)−2−メチル−1−プロパノールを40質量%、1−メチルピペラジン(1MPZ)を5質量%となるよう水に溶解させた以外は、実施例1と同様にして吸収液(水溶液)を調製し、実施例1と同様の装置を用い、同一条件下で二酸化炭素吸収量、二酸化炭素吸収速度、および凝固性を測定した。
2−(ジメチルアミノ)−2−メチル−1−プロパノールを40質量%、2−メチルピペラジン(2MPZ)を5質量%となるよう水に溶解させた以外は、実施例1と同様にして吸収液(水溶液)を調製し、実施例1と同様の装置を用い、同一条件下で二酸化炭素吸収量、二酸化炭素吸収速度、および凝固性を測定した。
2−(ジメチルアミノ)−2−メチル−1−プロパノールを40質量%、2,5−ジメチルピペラジン(25DMPZ)を5質量%となるよう水に溶解させた以外は、実施例1と同様にして吸収液(水溶液)を調製し、実施例1と同様の装置を用い、同一条件下で二酸化炭素吸収量、二酸化炭素吸収速度、および凝固性を測定した。
2−(ジメチルアミノ)−2−メチル−1−プロパノールを40質量%、2,6−ジメチルピペラジン(26DMPZ)を5質量%となるよう水に溶解させた以外は、実施例1と同様にして吸収液(水溶液)を調製し、実施例1と同様の装置を用い、同一条件下で二酸化炭素吸収量、二酸化炭素吸収速度、および凝固性を測定した。
2−(ジメチルアミノ)−2−メチル−1−プロパノールを40質量%、モノエタノールアミン(MEA)を5質量%となるよう水に溶解させた以外は、実施例1と同様にして吸収液(水溶液)を調製し、実施例1と同様の装置を用い、同一条件下で二酸化炭素吸収量、二酸化炭素吸収速度、および凝固性を測定した。
2−(ジメチルアミノ)−2−メチル−1−プロパノールを40質量%、2−メチルアミノエタノール(MAE)を5質量%となるよう水に溶解させた以外は、実施例1と同様にして吸収液(水溶液)を調製し、実施例1と同様の装置を用い、同一条件下で二酸化炭素吸収量、二酸化炭素吸収速度、および凝固性を測定した。
2−(ジメチルアミノ)−2−メチル−1−プロパノールを40質量%、2−エチルアミノエタノール(EAE)を5質量%となるよう水に溶解させた以外は、実施例1と同様にして吸収液(水溶液)を調製し、実施例1と同様の装置を用い、同一条件下で二酸化炭素吸収量、二酸化炭素吸収速度、および凝固性を測定した。
2−アミノ−2−メチル−1−プロパノールを40質量%、ピペラジンを5質量%となるよう水に溶解させた以外は、実施例1と同様にして吸収液を調製し、実施例1と同様の装置を用い、同一条件下で二酸化炭素吸収量、二酸化炭素吸収速度、および凝固性を測定した。
2−(ジメチルアミノ)−2−メチル−1−プロパノールを40質量%となるよう水に溶解させた以外は、実施例1と同様にして吸収液を調製し、実施例1と同様の装置を用い、同一条件下で二酸化炭素吸収量、二酸化炭素吸収速度、および凝固性を測定した。
Claims (3)
- 2−(ジメチルアミノ)−2−メチル−1−プロパノール、2−(エチルメチルアミノ)−2−メチル−1−プロパノール、2−(ジメチルアミノ)−2−エチル−1−プロパノールおよび2−(ジエチルアミノ)−2−メチル−1−プロパノールからなる群より選ばれる少なくとも一種の第3級アルカノールアミンと、ピペラジン、2−メチルピペラジン、2,5−ジメチルピペラジンおよび2,6−ジメチルピペラジンからなる群より選ばれる少なくとも一種の反応促進剤とを含有してなり、前記の第3級アルカノールアミンの含有量が20〜55質量%であり、前記の反応促進剤の含有量が1〜10質量%であることを特徴とする、酸性ガス吸収剤。
- 酸性ガスを含有するガスと、請求項1に記載の酸性ガス吸収剤とを接触させて、前記の酸性ガスを含むガスから酸性ガスを除去することを特徴とする、酸性ガスの除去方法。
- 酸性ガスを含有するガスと、請求項1に記載の酸性ガス吸収剤とを接触させ、この酸性ガス吸収剤に酸性ガスを吸収させることにより前記の酸性ガスを含有するガスから酸性ガスを除去する吸収器と、
この酸性ガスを吸収した酸性ガス吸収剤から酸性ガスを脱離させて、この酸性ガス吸収剤を再生する再生器とを有し、
前記の再生器で再生した前記の酸性ガス吸収剤を前記の吸収器にて再利用することを特徴とする、酸性ガス除去装置。
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2015005378A JP6445874B2 (ja) | 2015-01-14 | 2015-01-14 | 酸性ガス吸収剤、酸性ガス除去方法および酸性ガス除去装置 |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2015005378A JP6445874B2 (ja) | 2015-01-14 | 2015-01-14 | 酸性ガス吸収剤、酸性ガス除去方法および酸性ガス除去装置 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2016129877A JP2016129877A (ja) | 2016-07-21 |
| JP6445874B2 true JP6445874B2 (ja) | 2018-12-26 |
Family
ID=56415061
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2015005378A Expired - Fee Related JP6445874B2 (ja) | 2015-01-14 | 2015-01-14 | 酸性ガス吸収剤、酸性ガス除去方法および酸性ガス除去装置 |
Country Status (1)
| Country | Link |
|---|---|
| JP (1) | JP6445874B2 (ja) |
Families Citing this family (8)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| AU2019295364B2 (en) * | 2018-06-26 | 2024-10-31 | Carbon Clean Solutions Limited | Solvent and process for removing carbon dioxide from a gaseous mixture having high carbon dioxide partial pressures |
| GB201813839D0 (en) | 2018-06-26 | 2018-10-10 | Carbon Clean Solutions Ltd | System and process of capturing carbon dioxide from flue gases |
| US12134067B2 (en) | 2018-07-02 | 2024-11-05 | Carbon Clean Solutions Limited | Method and a system for the removal of carbon dioxide from solvents |
| CN109351125A (zh) * | 2018-09-20 | 2019-02-19 | 湖南大学 | 一种用于降低富co2胺溶液再生能耗的新型催化解吸塔 |
| CN109529547A (zh) * | 2018-12-24 | 2019-03-29 | 大连理工大学 | 可降低吸湿性影响的捕集混合气体中二氧化碳的脱碳溶液 |
| CN111875504B (zh) * | 2020-07-27 | 2021-05-18 | 中国科学院过程工程研究所 | 一种环己基双胺类离子液体及其在二氧化硫吸收中的应用 |
| JP7637524B2 (ja) * | 2021-02-04 | 2025-02-28 | 株式会社トクヤマ | 吸収液および分離回収方法 |
| CN118904025B (zh) * | 2024-07-23 | 2025-02-18 | 中国石油大学(北京) | 一种利用电场辅助醇胺解吸co2的方法 |
Family Cites Families (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| UA24004A1 (uk) * | 1988-05-24 | 1998-08-31 | Сосьєте Насьональ Елф Акітен (Продюксьон) | Абсорбеhт для очищеhhя промислових газів від кислих компоhеhтів та спосіб очищеhhя промислових газів від кислих компоhеhтів |
| JP2966719B2 (ja) * | 1994-03-18 | 1999-10-25 | 関西電力株式会社 | ガス中の硫化水素を選択的に除去する方法 |
| JP3197183B2 (ja) * | 1995-03-16 | 2001-08-13 | 関西電力株式会社 | 燃焼排ガス中の二酸化炭素を除去する方法 |
| JP3233802B2 (ja) * | 1994-12-15 | 2001-12-04 | 関西電力株式会社 | 燃焼排ガス中の炭酸ガスと窒素酸化物を除去する方法 |
| DE10210729A1 (de) * | 2002-03-12 | 2003-10-02 | Basf Ag | Verfahren zum Entsäuern eines Fluidstroms und Waschflüssigkeit zur Verwendung in einem derartigen Verfahren |
-
2015
- 2015-01-14 JP JP2015005378A patent/JP6445874B2/ja not_active Expired - Fee Related
Also Published As
| Publication number | Publication date |
|---|---|
| JP2016129877A (ja) | 2016-07-21 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP5659127B2 (ja) | 酸性ガス吸収剤、酸性ガス除去方法および酸性ガス除去装置 | |
| JP6445874B2 (ja) | 酸性ガス吸収剤、酸性ガス除去方法および酸性ガス除去装置 | |
| JP5659084B2 (ja) | 酸性ガス吸収剤、酸性ガス除去方法および酸性ガス除去装置 | |
| JP5868795B2 (ja) | 酸性ガス吸収剤、酸性ガス除去方法および酸性ガス除去装置 | |
| EP2468385B1 (en) | Acid gas absorbent, acid gas removal method and acid gas removal device | |
| JP6383262B2 (ja) | 酸性ガス吸収剤、酸性ガスの除去方法および酸性ガス除去装置 | |
| JP6173817B2 (ja) | 酸性ガス吸収剤、酸性ガス除去方法及び酸性ガス除去装置 | |
| JP6479543B2 (ja) | 酸性ガス吸収剤、酸性ガスの除去方法および酸性ガスの除去装置 | |
| US9724642B2 (en) | Acid gas absorbent, acid gas removal device, and acid gas removal method | |
| JP2015029987A (ja) | 酸性ガス吸収剤、酸性ガス除去方法及び酸性ガス除去装置 | |
| JP2018122278A (ja) | 酸性ガス吸収剤、酸性ガス除去方法および酸性ガス除去装置 | |
| JP7185421B2 (ja) | 酸性ガス吸収剤、酸性ガスの除去方法および酸性ガス除去装置 | |
| JP2017196547A (ja) | 酸性ガス吸収剤、酸性ガスの除去方法および酸性ガス除去装置 | |
| JP2017121610A (ja) | 酸性ガス吸収剤、酸性ガス除去方法および酸性ガス除去装置 | |
| JP2017035669A (ja) | 酸性ガス吸収剤、酸性ガス除去方法および酸性ガス除去装置 | |
| JP2015071136A (ja) | 酸性ガス吸収剤、酸性ガス除去方法及び酸性ガス除去装置 | |
| JP2015112574A (ja) | 酸性ガス吸収剤、酸性ガス除去方法及び酸性ガス除去装置 | |
| JP7204391B2 (ja) | 酸性ガス吸収剤、酸性ガスの除去方法及び酸性ガス除去装置 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20170731 |
|
| A711 | Notification of change in applicant |
Free format text: JAPANESE INTERMEDIATE CODE: A712 Effective date: 20171121 |
|
| A711 | Notification of change in applicant |
Free format text: JAPANESE INTERMEDIATE CODE: A711 Effective date: 20171122 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20180216 |
|
| A977 | Report on retrieval |
Free format text: JAPANESE INTERMEDIATE CODE: A971007 Effective date: 20180214 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20180412 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20180706 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20181102 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20181130 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 6445874 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| LAPS | Cancellation because of no payment of annual fees |