JP6230138B2 - 生体組織試料の加工システムおよび加工方法 - Google Patents
生体組織試料の加工システムおよび加工方法 Download PDFInfo
- Publication number
- JP6230138B2 JP6230138B2 JP2016526272A JP2016526272A JP6230138B2 JP 6230138 B2 JP6230138 B2 JP 6230138B2 JP 2016526272 A JP2016526272 A JP 2016526272A JP 2016526272 A JP2016526272 A JP 2016526272A JP 6230138 B2 JP6230138 B2 JP 6230138B2
- Authority
- JP
- Japan
- Prior art keywords
- tissue
- processing container
- container
- assembly
- tissue processing
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
Images
Classifications
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N35/00—Automatic analysis not limited to methods or materials provided for in any single one of groups G01N1/00 - G01N33/00; Handling materials therefor
- G01N35/0099—Automatic analysis not limited to methods or materials provided for in any single one of groups G01N1/00 - G01N33/00; Handling materials therefor comprising robots or similar manipulators
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12M—APPARATUS FOR ENZYMOLOGY OR MICROBIOLOGY; APPARATUS FOR CULTURING MICROORGANISMS FOR PRODUCING BIOMASS, FOR GROWING CELLS OR FOR OBTAINING FERMENTATION OR METABOLIC PRODUCTS, i.e. BIOREACTORS OR FERMENTERS
- C12M23/00—Constructional details, e.g. recesses, hinges
- C12M23/50—Means for positioning or orientating the apparatus
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12M—APPARATUS FOR ENZYMOLOGY OR MICROBIOLOGY; APPARATUS FOR CULTURING MICROORGANISMS FOR PRODUCING BIOMASS, FOR GROWING CELLS OR FOR OBTAINING FERMENTATION OR METABOLIC PRODUCTS, i.e. BIOREACTORS OR FERMENTERS
- C12M33/00—Means for introduction, transport, positioning, extraction, harvesting, peeling or sampling of biological material in or from the apparatus
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12M—APPARATUS FOR ENZYMOLOGY OR MICROBIOLOGY; APPARATUS FOR CULTURING MICROORGANISMS FOR PRODUCING BIOMASS, FOR GROWING CELLS OR FOR OBTAINING FERMENTATION OR METABOLIC PRODUCTS, i.e. BIOREACTORS OR FERMENTERS
- C12M33/00—Means for introduction, transport, positioning, extraction, harvesting, peeling or sampling of biological material in or from the apparatus
- C12M33/08—Means for introduction, transport, positioning, extraction, harvesting, peeling or sampling of biological material in or from the apparatus by vibration
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12M—APPARATUS FOR ENZYMOLOGY OR MICROBIOLOGY; APPARATUS FOR CULTURING MICROORGANISMS FOR PRODUCING BIOMASS, FOR GROWING CELLS OR FOR OBTAINING FERMENTATION OR METABOLIC PRODUCTS, i.e. BIOREACTORS OR FERMENTERS
- C12M33/00—Means for introduction, transport, positioning, extraction, harvesting, peeling or sampling of biological material in or from the apparatus
- C12M33/14—Means for introduction, transport, positioning, extraction, harvesting, peeling or sampling of biological material in or from the apparatus with filters, sieves or membranes
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12M—APPARATUS FOR ENZYMOLOGY OR MICROBIOLOGY; APPARATUS FOR CULTURING MICROORGANISMS FOR PRODUCING BIOMASS, FOR GROWING CELLS OR FOR OBTAINING FERMENTATION OR METABOLIC PRODUCTS, i.e. BIOREACTORS OR FERMENTERS
- C12M41/00—Means for regulation, monitoring, measurement or control, e.g. flow regulation
- C12M41/12—Means for regulation, monitoring, measurement or control, e.g. flow regulation of temperature
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12M—APPARATUS FOR ENZYMOLOGY OR MICROBIOLOGY; APPARATUS FOR CULTURING MICROORGANISMS FOR PRODUCING BIOMASS, FOR GROWING CELLS OR FOR OBTAINING FERMENTATION OR METABOLIC PRODUCTS, i.e. BIOREACTORS OR FERMENTERS
- C12M41/00—Means for regulation, monitoring, measurement or control, e.g. flow regulation
- C12M41/48—Automatic or computerized control
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12M—APPARATUS FOR ENZYMOLOGY OR MICROBIOLOGY; APPARATUS FOR CULTURING MICROORGANISMS FOR PRODUCING BIOMASS, FOR GROWING CELLS OR FOR OBTAINING FERMENTATION OR METABOLIC PRODUCTS, i.e. BIOREACTORS OR FERMENTERS
- C12M45/00—Means for pre-treatment of biological substances
- C12M45/02—Means for pre-treatment of biological substances by mechanical forces; Stirring; Trituration; Comminuting
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12M—APPARATUS FOR ENZYMOLOGY OR MICROBIOLOGY; APPARATUS FOR CULTURING MICROORGANISMS FOR PRODUCING BIOMASS, FOR GROWING CELLS OR FOR OBTAINING FERMENTATION OR METABOLIC PRODUCTS, i.e. BIOREACTORS OR FERMENTERS
- C12M45/00—Means for pre-treatment of biological substances
- C12M45/09—Means for pre-treatment of biological substances by enzymatic treatment
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12M—APPARATUS FOR ENZYMOLOGY OR MICROBIOLOGY; APPARATUS FOR CULTURING MICROORGANISMS FOR PRODUCING BIOMASS, FOR GROWING CELLS OR FOR OBTAINING FERMENTATION OR METABOLIC PRODUCTS, i.e. BIOREACTORS OR FERMENTERS
- C12M47/00—Means for after-treatment of the produced biomass or of the fermentation or metabolic products, e.g. storage of biomass
- C12M47/04—Cell isolation or sorting
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N5/00—Undifferentiated human, animal or plant cells, e.g. cell lines; Tissues; Cultivation or maintenance thereof; Culture media therefor
- C12N5/06—Animal cells or tissues; Human cells or tissues
- C12N5/0602—Vertebrate cells
- C12N5/069—Vascular Endothelial cells
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N35/00—Automatic analysis not limited to methods or materials provided for in any single one of groups G01N1/00 - G01N33/00; Handling materials therefor
- G01N35/02—Automatic analysis not limited to methods or materials provided for in any single one of groups G01N1/00 - G01N33/00; Handling materials therefor using a plurality of sample containers moved by a conveyor system past one or more treatment or analysis stations
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2506/00—Differentiation of animal cells from one lineage to another; Differentiation of pluripotent cells
- C12N2506/02—Differentiation of animal cells from one lineage to another; Differentiation of pluripotent cells from embryonic cells
- C12N2506/025—Differentiation of animal cells from one lineage to another; Differentiation of pluripotent cells from embryonic cells from extra-embryonic cells, e.g. trophoblast, placenta
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N35/00—Automatic analysis not limited to methods or materials provided for in any single one of groups G01N1/00 - G01N33/00; Handling materials therefor
- G01N2035/00346—Heating or cooling arrangements
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N35/00—Automatic analysis not limited to methods or materials provided for in any single one of groups G01N1/00 - G01N33/00; Handling materials therefor
- G01N35/00584—Control arrangements for automatic analysers
- G01N35/00722—Communications; Identification
- G01N2035/00891—Displaying information to the operator
Landscapes
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Engineering & Computer Science (AREA)
- Chemical & Material Sciences (AREA)
- Wood Science & Technology (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Zoology (AREA)
- Organic Chemistry (AREA)
- Biomedical Technology (AREA)
- Biotechnology (AREA)
- Genetics & Genomics (AREA)
- Biochemistry (AREA)
- General Health & Medical Sciences (AREA)
- Microbiology (AREA)
- General Engineering & Computer Science (AREA)
- Sustainable Development (AREA)
- Molecular Biology (AREA)
- Analytical Chemistry (AREA)
- Cell Biology (AREA)
- Physics & Mathematics (AREA)
- Computer Hardware Design (AREA)
- Vascular Medicine (AREA)
- Mechanical Engineering (AREA)
- Immunology (AREA)
- General Physics & Mathematics (AREA)
- Pathology (AREA)
- Thermal Sciences (AREA)
- Robotics (AREA)
- Clinical Laboratory Science (AREA)
- Apparatus Associated With Microorganisms And Enzymes (AREA)
- Sampling And Sample Adjustment (AREA)
- Micro-Organisms Or Cultivation Processes Thereof (AREA)
Description
この開示の一実施の形態では、前記制御装置は、組織の加工に必要なパラメータを供給するために表示装置と入力ボタンを有するユーザインタフェースを備える。
a)無菌状態の確実な実現:手作業による接続がリスク要因となり、細胞単離システムの無菌状態や無菌の性質を危うくするかもしれない。不適切な取り扱いによって、細菌による汚染や、細胞単離システムの閉鎖特性に欠陥が生じる可能性がある。ロボット工学および同期作動バルブで実現した、この開示の導管を用いないシステムにより、細菌による汚染のおそれを除去する閉じた無菌の流路が確実に実現される。
b)不正確な接続から生じる手作業のミスの除去:最小限の人的介在。ロボット工学で実現したシステムは、最小限の手作業による介入で作動され、手作業ミスの確率と汚染の可能性が減少する。
c)導管を用いないシステムはポンプを使用しないので、SVF/細胞が圧力による歪やそれによって引き起こされる損壊を被ることがない。
a)異なる生体組織のための異なる工程は、異なるソフトウェアを入力して、同じハードウェアを用いて取り扱うことができる。
b)今後、軌道や攪拌速度などの現行工程に改良を加えることにより、最終生成物の収率/生存能力を向上させる。
c)今後、現行工程に修正を加えることにより、同じ組織から異なる細胞の個体群を得る。
a.組織加工容器のバルブを組織貯蔵容器のバルブに接続することにより、所定量の組織試料(例えば、脂肪組織)を該組織加工容器に供給する。この開示の任意の一実施の形態では、組織加工容器と組織採取缶の間に導管を接続することにより、上記組織を該組織加工容器に供給する。
b.それから、組織加工容器のバルブを洗浄緩衝溶液が含まれた貯蔵容器のバルブに接続することにより、該貯蔵容器の洗浄緩衝溶液を該組織加工容器に供給する。
c.それから、ロボット操作アセンブリを援用して該組織加工容器で混合物を攪拌することにより、組織試料を洗浄緩衝溶液で洗浄するが、該ロボット操作アセンブリが該組織加工容器を所定の軌道で移動させる。
d.該組織加工容器でその混合物を相分離させることにより、該混合物は初期脂肪上部分画と初期水下部分画に分離するが、この相分離は、該ロボット操作アセンブリがその温浸室をX軸に対して90°の角度で傾けることにより行う。
e.前ステップで得た初期水分画を廃物収集装置に配置するが、ステップb〜eを1〜6回、好ましくは3〜4回繰り返す。
f.該組織加工容器のバルブを温浸緩衝剤が含まれた容器のバルブに接続することにより、該温浸緩衝剤容器に含まれた所定量の温浸緩衝剤を該組織加工容器に送る。
g.該組織加工容器で上記混合物を所定の回数で攪拌することにより、上記初期脂肪上部分画と上記温浸緩衝剤を混合して温浸工程を行う。温浸工程中は、制御装置にインタフェースで接続された加熱素子と温度センサを援用して、囲い部で所定の温度が維持される。
h.該組織加工容器で上記混合物の相分離を行うことによって、その混合物をSVFを含有する最終脂肪上部分画と最終水下部分画に分離する。
i.上記ロボット操作アセンブリが該組織加工容器を搬送して前ステップで得た最終水下部分画を細胞濃縮装置に供給することにより、その最終水下部分画を細胞濃縮装置に導く。当該最終水下部分画を供給するために、該組織加工容器のバルブを該細胞濃縮装置のバルブに接続する。
j.その最終水分画が濾過アセンブリを含む上記細胞濃縮装置内で濾過されるが、SVF細胞を含有する最終水分画を濃縮するために任意に赤血球の除去を行う。
それから、上記最終のSVF細胞懸濁液から温浸酵素を除去するために、該SVF濃縮物を洗浄緩衝溶液で洗浄する。このSVF洗浄は以下のように行う。
a.上記組織加工容器の最終脂肪分画を上記廃物収集装置に配置する。
b.それから、該組織加工容器を所定量の洗浄緩衝溶液で満たし、任意に攪拌によりすすぎ洗浄を行って残余の組織と酵素を除去する。そして、洗浄緩衝剤を該廃物収集装置に配置する。
c.上記すすぎ洗浄を行った組織加工容器を洗浄緩衝溶液で再度満たしてから、そのSVF濃縮物を濾過により洗浄するために、上記細胞濃縮装置に供給する(洗浄緩衝剤を上記濾過装置の室のいずれか1つに供給してもよい)。
d.温浸酵素を完全に除去して最終のSVF生成物を得るために、ステップcを1回または複数回実行してもよい。
a.上記ロボットアームが上記組織加工容器を廃棄置場に廃棄する。
b.該ロボットアームが上記ハンド交換置場から洗浄容器を取り出す。この洗浄容器は、組織加工容器、または任意の他の形状および大きさを有する容器であってもよい。
c.その洗浄容器を洗浄緩衝溶液で満たしてから、当該SVF濃縮物を濾過により洗浄するために、上記細胞濃縮装置に供給する(洗浄緩衝剤を上記濾過装置の室のいずれか1つに供給してもよい。好ましくは、SVF濃縮物を含有する最終室に直接に供給してもよい。)。
d.温浸酵素を完全に除去して最終のSVF生成物を得るために、ステップcを1回または複数回実行してもよい。
1.導管を用いないシステム:この開示に記載のロボット工学で実現したシステムは、導管を用いずに作動する。導管を用いないシステムは以下の利点を提供する。
a)無菌状態の確実な実現:手作業による接続がリスク要因となり、細胞単離システムの無菌状態や無菌の性質を危うくするおそれがある。不適切な取り扱いによって、細菌による汚染や、細胞単離システムの閉鎖特性に欠陥が生じる可能性がある。ロボット工学および同期作動バルブで実現した、この開示の導管を用いないシステムにより、細菌による汚染のおそれを除去する閉じた無菌の流路が確実に実現される。
b)不正確な接続から生じる手作業のミスの除去:最小限の人的介在。ロボット工学で実現したシステムは、最小限の手作業による介入で作動され、手作業ミスの確率と汚染の可能性が減少する。
c)導管を用いないシステムはポンプを使用しないので、SVF/細胞が圧力による歪やそれによって引き起こされる損壊を被ることがない。
a)異なる生体組織のための異なる工程は、異なるソフトウェアを入力して、同じハードウェアを用いて取り扱うことができる。
b)今後、軌道や攪拌速度などの現行工程に改良を加えることにより、最終生成物の収率/生存能力を向上させる。
c)今後、現行工程に修正を加えることにより、同じ組織から異なる細胞の個体群を得る。
本明細書において実質的にいかなる複数および/または単数の用語の使用に関しても、当業者は、当該文脈および/または適用に適切であるように、複数から単数におよび/または単数から複数に解釈することができる。その種々の単数/複数置換は、明らかにするために本明細書において明確に記載してよい。
501 システムの基礎
502 加熱素子
503 囲い部
505a〜505f 貯蔵容器
506 表示モニター
507 細胞濃縮装置
508 廃物収集装置
511 制御装置
512 RFID接続モジュール
513 キャスター車輪
514 洗浄容器
515 バルブアセンブリ
516 貯蔵容器の注出口
517 掴み部
703 組織加工容器
703a 組織加工容器の注入/注出口
701 釣合いおもり
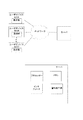
100 ロボット操作アセンブリ
101 ロボット操作アセンブの基礎
102 第1のモータ
105 第1の“Y”形状フォーク
107 第2のモータ
108 第2の“Y”形状フォーク
110 第3のモータ
111 第3の“Y”形状フォーク
111a 第4のモータ
112 攪拌リンク
113および115 十字形リンクモータ
117 容器保持器
S1〜S6 位置センサ
Claims (21)
- 組織の加工を行う自動化システム(500)であって、
組織試料、緩衝溶液、酵素および試薬の少なくとも1つをそれぞれ貯蔵する複数の容器(505)と、
組織の加工を行う組織加工容器(703)と、
前記組織加工容器(703)に連結され、前記組織加工容器(703)を前記複数の容器(505)のそれぞれに向けて搬送し、組織試料、緩衝溶液、酵素および試薬の少なくとも1つを重力の作用で収集するために該組織加工容器(703)の注入口を該複数の容器(505)のそれぞれの注出口(516)に位置合わせして、前記組織加工容器(703)を多数の平面内に移動し、洗浄工程、温浸工程、相分離工程およびこれらの工程の組合せの少なくとも1つを行い、温浸した前記組織試料から水分画と脂肪分画を分離するように構成したロボット操作アセンブリ(100)と、
前記ロボット操作アセンブリ(100)にインタフェースで接続され、該ロボット操作アセンブリ(100)の動作を制御して前記組織の加工を行う制御装置(511)と、
を備えることを特徴とするシステム。 - 前記組織は、脂肪組織、胎盤組織および臍帯組織の少なくとも1つから選択する哺乳類の組織である、ことを特徴とする請求項1に記載のシステム。
- 前記脂肪組織を加工することにより間質血管分画(SVF)細胞を単離し、また胎盤および臍帯組織から多能幹/間質細胞を単離する、ことを特徴とする請求項2に記載のシステム。
- 細胞を単離するために温浸した組織の水分画を濾過するように構成され、前記組織加工容器(703)から水分画組織試料を受け取る細胞濃縮装置(507)をさらに備える、ことを特徴とする請求項1に記載のシステム。
- 前記細胞濃縮装置(507)は、フィルタアセンブリ、スピナーおよび遠心分離アセンブリの少なくとも1つである、ことを特徴とする請求項4に記載のシステム。
- 前記組織加工容器(703)から組織の水分画と組織の脂肪分画の少なくとも1つを受け取る廃物収集装置(508)を備える、ことを特徴とする請求項1に記載のシステム。
- 室(503)に収納されていることを特徴とする請求項1に記載のシステム。
- 前記制御装置(511)は、組織の加工に必要なパラメータを供給するための表示装置(506)と、入力ボタンを有するユーザインタフェースを備える、ことを特徴とする請求項1に記載のシステム。
- 室(503)の温度を測定かつ調節するために前記室(503)内に設けられる少なくとも1つの温度センサ(504)を備え、前記温度センサ(504)は前記制御装置(511)にインタフェースで接続される、ことを特徴とする請求項1に記載のシステム。
- 室(503)内に設けた少なくとも1つの加熱素子(502)を備え、前記加熱素子(502)は、前記室(503)の温度を所定の制限内に維持するために前記制御装置(511)にインタフェースで接続されて前記組織加工容器(703)を加熱する、ことを特徴とする請求項1に記載のシステム。
- 前記複数の容器(505)のそれぞれの注出口(516)と前記組織加工容器(703)の注入口に、バルブアセンブリ(515)を設ける、ことを特徴とする請求項1に記載のシステム。
- 前記バルブアセンブリ(515)は、前記制御装置(511)にインタフェースで接続される、ことを特徴とする請求項11に記載のシステム。
- 前記ロボット操作アセンブリ(100)に連結するように構成された洗浄容器(514)を備える、ことを特徴とする請求項1に記載のシステム。
- 前記ロボット操作アセンブリ(100)は、
前記洗浄容器(514)を前記複数の容器(505)に向けて搬送し、洗浄緩衝溶液を収集するために該洗浄容器(514)の注入口を洗浄緩衝溶液を貯蔵している容器の注出口に位置合わせして、
前記洗浄容器(514)を細胞濃縮装置(507)に向けて搬送し、水分画組織試料を洗浄するために、前記細胞濃縮装置(507)に洗浄緩衝溶液が供給されるように該洗浄容器(514)の注出口を該細胞濃縮装置(507)の注入口に位置合わせするように構成した、ことを特徴とする請求項13に記載のシステム。 - 前記複数の容器(505)のそれぞれと前記組織加工容器(703)は、無線周波数識別タグを具備する、ことを特徴とする請求項1に記載のシステム。
- 前記ロボット操作アセンブリ(100)は複数のセンサ(S)を備える、ことを特徴とする請求項1に記載のシステム。
- 前記複数のセンサ(S)は、前記ロボット操作アセンブリ(100)の動作を所定の軌道で制御するために前記制御装置(511)にインタフェースで接続される、ことを特徴とする請求項16に記載のシステム。
- 請求項1に記載の自動化システム(500)を用いて組織の加工を行う方法であって、
a.前記ロボット操作アセンブリが前記組織加工容器(703)の注入口を組織試料と洗浄緩衝溶液との少なくとも1つを貯蔵する前記容器(505)の注出口(516)に位置合わせして、前記組織加工容器(703)に前記組織試料または前記洗浄緩衝溶液を重力の作用で受け取り、
b.その混合物を前記ロボット操作アセンブリ(100)によって前記組織加工容器(703)で攪拌することにより洗浄緩衝溶液で組織試料を洗浄して、該ロボット操作アセンブリ(100)が該組織加工容器(703)を多数の平面内に移動し、
c.該混合物を相分離させて初期脂肪上部分画と初期水下部分画を得るために、前記ロボット操作アセンブリ(100)が前記組織加工容器(703)をX軸に対して90°の角度で傾け、
d.前記ロボット操作アセンブリ(100)が廃物収集装置(508)の注入口を前記組織加工容器(703)の注出口に位置合わせして、ステップ(c)で得た初期水下部分画を重力の作用で廃物収集装置(508)に配置し、
e.前記ロボット操作アセンブリ(100)が前記組織加工容器(703)の注入口を温浸緩衝溶液を貯蔵する温浸緩衝剤容器の注出口に位置合わせして、前記温浸緩衝剤容器に含まれた所定量の温浸緩衝剤を重力の作用で前記組織加工容器(703)に受け取り、
f.その混合物を前記ロボット操作アセンブリ(100)によって前記組織加工容器(703)で攪拌することにより上記脂肪上部分画を温浸緩衝剤で温浸して、該ロボット操作アセンブリ(100)が該組織加工容器(703)を多数の平面内に移動し、
g.前記組織加工容器(703)で該混合物を相分離させて最終脂肪上部分画と最終水下部分画を得るために、前記ロボット操作アセンブリ(100)が該組織加工容器(703)をX軸に対して90°の角度で傾けることを含む、ことを特徴とする方法。 - 前記ロボット操作アセンブリ(100)の位置をセンサによって検出し、前記制御装置(511)が該ロボット操作アセンブリ(100)を統制して前記組織加工容器(703)を前記複数の容器と前記廃物収集装置(508)のそれぞれに向けて搬送することを含む、ことを特徴とする請求項18に記載の方法。
- 前記組織加工容器(703)が前記複数の容器(505)と前記廃物収集装置(508)の少なくとも1つに位置合わせされたことを制御装置(511)によって検出し、バルブアセンブリを作動させることを含む、ことを特徴とする請求項18に記載の方法。
- 生体組織試料の加工のために用いる請求項1に記載の自動化システム。
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| IN5151/CHE/2013 | 2013-11-13 | ||
| IN5151CH2013 IN2013CH05151A (ja) | 2013-11-13 | 2014-11-12 | |
| PCT/IB2014/065975 WO2015071829A1 (en) | 2013-11-13 | 2014-11-12 | A system and method for processing of biological tissue samples |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2016537972A JP2016537972A (ja) | 2016-12-08 |
| JP6230138B2 true JP6230138B2 (ja) | 2017-11-15 |
Family
ID=52014189
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2016526272A Active JP6230138B2 (ja) | 2013-11-13 | 2014-11-12 | 生体組織試料の加工システムおよび加工方法 |
Country Status (10)
| Country | Link |
|---|---|
| US (1) | US9726687B2 (ja) |
| EP (1) | EP3068870B1 (ja) |
| JP (1) | JP6230138B2 (ja) |
| KR (1) | KR101844697B1 (ja) |
| CN (1) | CN105722973A (ja) |
| BR (1) | BR112016010760A2 (ja) |
| ES (1) | ES2787888T3 (ja) |
| IN (1) | IN2013CH05151A (ja) |
| MX (1) | MX2016006215A (ja) |
| WO (1) | WO2015071829A1 (ja) |
Families Citing this family (13)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US11174458B2 (en) | 2007-04-23 | 2021-11-16 | Koligo Therapeutics, Inc. | Cell separation apparatus and methods of use |
| DE102014214076A1 (de) * | 2014-07-18 | 2016-01-21 | Hamilton Bonaduz Ag | Fluidleitungsanordnung, umfassend eine Mehrzahl von Fluidleitungselementen, Ventilleitungsanordnung, umfassend eine Fluidleitungsanordnung und eine Schaltanordnung, und Handhabungsanordnung mit einer Ventilleitungsanordnung |
| KR20210061347A (ko) * | 2018-08-23 | 2021-05-27 | 테라셀 컨설팅 에스피알엘 | 조직 매트릭스를 생성하기 위해 생물학적 조직을 처리하는 자동화 공정 |
| CN113660961A (zh) * | 2018-12-13 | 2021-11-16 | 科力果疗法公司 | 细胞分离装置及使用方法 |
| CN110229785A (zh) * | 2019-06-17 | 2019-09-13 | 白晋 | 一种利用血管内皮祖细胞提升脂肪移植成功率的方法 |
| JP2022536542A (ja) | 2019-06-17 | 2022-08-17 | デカ・プロダクツ・リミテッド・パートナーシップ | 細胞および組織の調製のためのシステムならびに方法 |
| DK3789305T3 (da) * | 2019-09-05 | 2022-03-28 | Skan Ag | Anlæg med en indeslutning til aseptisk omfyldning af et pulver |
| CN110511863B (zh) * | 2019-09-29 | 2024-03-12 | 深圳赛动生物自动化有限公司 | 细胞离心分装装置及其工作方法 |
| EP4136208A1 (en) * | 2020-04-22 | 2023-02-22 | CellUnite GmbH | Modular cell processing |
| IT202000011926A1 (it) * | 2020-05-21 | 2021-11-21 | Univ Degli Studi Di Bari Aldo Moro | Dispositivo e metodo per l'estrazione di cellule staminali da tessuto adiposo |
| US11987787B2 (en) | 2020-07-22 | 2024-05-21 | AVITA Medical Americas, LLC | Devices, methods, and kits for preparing a cell suspension |
| CN112940914A (zh) * | 2021-01-29 | 2021-06-11 | 赵彬 | 一种促进表皮干细胞分化和生长的实验装置 |
| US11879121B2 (en) | 2021-04-20 | 2024-01-23 | CisNovo | Tissue disaggregation system and methods |
Family Cites Families (8)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CA2463673C (en) * | 2001-10-19 | 2009-01-13 | Monogen, Inc. | Filtration system and method for obtaining a cytology layer |
| US9144583B2 (en) | 2002-03-29 | 2015-09-29 | Tissue Genesis, Inc. | Cell separation apparatus and methods of use |
| WO2004073846A1 (en) * | 2003-02-19 | 2004-09-02 | The Horticulture And Food Research Institute Of New Zealand Limited | Tissue disintegrator and sample processing system |
| BRPI0411798A (pt) | 2003-06-25 | 2006-08-08 | Macropore Biosurgery Inc | sistemas e métodos para separar e concentrar células regenerativas do tecido |
| ES2892751T3 (es) | 2006-01-18 | 2022-02-04 | Coimmune Inc | Sistemas y métodos para el procesamiento de muestras en un recipiente cerrado y dispositivos relacionados |
| JP5890623B2 (ja) * | 2011-06-28 | 2016-03-22 | 株式会社安川電機 | 液体処理システム及び液体処理方法 |
| AU2012303719B2 (en) * | 2011-08-29 | 2016-05-26 | Stempeutics Research Private Limited | A system for isolating stromal vascular fraction (SVF) cells from the adipose tissue and a method thereof |
| KR20140147805A (ko) * | 2011-12-07 | 2014-12-30 | 아바스템 바이오메디컬 코퍼레이션 | 지방조직으로부터 비지방 세포의 단리를 위한 방법 및 장치 |
-
2014
- 2014-11-12 BR BR112016010760A patent/BR112016010760A2/pt not_active Application Discontinuation
- 2014-11-12 IN IN5151CH2013 patent/IN2013CH05151A/en unknown
- 2014-11-12 WO PCT/IB2014/065975 patent/WO2015071829A1/en active Application Filing
- 2014-11-12 ES ES14809124T patent/ES2787888T3/es active Active
- 2014-11-12 CN CN201480061538.1A patent/CN105722973A/zh active Pending
- 2014-11-12 US US15/032,845 patent/US9726687B2/en active Active
- 2014-11-12 JP JP2016526272A patent/JP6230138B2/ja active Active
- 2014-11-12 KR KR1020167012177A patent/KR101844697B1/ko active IP Right Grant
- 2014-11-12 MX MX2016006215A patent/MX2016006215A/es active IP Right Grant
- 2014-11-12 EP EP14809124.2A patent/EP3068870B1/en active Active
Also Published As
| Publication number | Publication date |
|---|---|
| JP2016537972A (ja) | 2016-12-08 |
| ES2787888T3 (es) | 2020-10-19 |
| KR20160065975A (ko) | 2016-06-09 |
| EP3068870B1 (en) | 2020-01-15 |
| US20160252537A1 (en) | 2016-09-01 |
| EP3068870A1 (en) | 2016-09-21 |
| IN2013CH05151A (ja) | 2015-09-04 |
| CN105722973A (zh) | 2016-06-29 |
| US9726687B2 (en) | 2017-08-08 |
| MX2016006215A (es) | 2016-08-19 |
| KR101844697B1 (ko) | 2018-04-02 |
| WO2015071829A1 (en) | 2015-05-21 |
| BR112016010760A2 (pt) | 2017-10-10 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP6230138B2 (ja) | 生体組織試料の加工システムおよび加工方法 | |
| AU2012303719B2 (en) | A system for isolating stromal vascular fraction (SVF) cells from the adipose tissue and a method thereof | |
| JP2023518207A (ja) | 細胞処理のためのシステム、デバイス、及び方法 | |
| AU2012303719A1 (en) | A system for isolating stromal vascular fraction (SVF) cells from the adipose tissue and a method thereof | |
| EP2943562B1 (en) | A system for extraction of cells from a sample of tissue | |
| JP7037510B2 (ja) | 衝撃波または機械的衝撃を使用する、細胞の分離、解離、および/または脱凝集 | |
| JP5898788B2 (ja) | 植物インフィルトレーション装置 | |
| Ochs et al. | Advances in automation for the production of clinical-grade mesenchymal stromal cells: the AUTOSTEM robotic platform | |
| US20190358633A1 (en) | Fluidic devices for closed cell culture applications under current Good Manufacturing Practice | |
| CN215288820U (zh) | 脂肪干细胞提取装置 | |
| Bartel | Stem Cells and Cell Therapy: Autologous Cell Manufacturing | |
| US10913931B1 (en) | Apparatus and method for harvesting and preparing viable stem cells | |
| US11535822B2 (en) | Device for isolating stem cells from fetal tissues | |
| CN219603592U (zh) | 一种自动化的类器官液体分装系统 | |
| CN219194991U (zh) | 一种细胞药物培育无菌隔离器 | |
| CN113789297A (zh) | 一种规模化制备鸡胚成纤维细胞的方法 | |
| CN115612614A (zh) | 一种类器官处理前的液体分装系统 | |
| WAKITANI et al. | Development of automatic cell culture system for cell therapy and regenerative medicine—Robotized system for high quality cell product preparation— | |
| JP2019198240A (ja) | ロボット装置を備えた細胞増殖装置 | |
| JP2019198239A (ja) | 互いに独立したサブユニットを有する細胞増殖装置 | |
| JP2018023325A (ja) | 培養方法 | |
| JPS5950310B2 (ja) | 培養容器の搬送装置 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20170228 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20170529 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20171003 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20171012 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 6230138 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |