JP6182368B2 - リグニン分解物の製造方法 - Google Patents
リグニン分解物の製造方法 Download PDFInfo
- Publication number
- JP6182368B2 JP6182368B2 JP2013131931A JP2013131931A JP6182368B2 JP 6182368 B2 JP6182368 B2 JP 6182368B2 JP 2013131931 A JP2013131931 A JP 2013131931A JP 2013131931 A JP2013131931 A JP 2013131931A JP 6182368 B2 JP6182368 B2 JP 6182368B2
- Authority
- JP
- Japan
- Prior art keywords
- lignin
- mass
- raw material
- degradation product
- water
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
Description
リグノセルロース原料から高収率でリグニンを分離する方法として、一般に、製紙会社などで主に使用されているクラフト蒸解法が知られている(例えば、特許文献1参照)。
そこで本発明は、低着色で、かつ溶媒溶解性を有する、汎用性の高いリグニン分解物を、高収率で製造することができるリグニン分解物の製造方法を提供することを課題とする。
[1]下記工程(1)〜(3)を有する、リグニン分解物の製造方法。
工程(1):リグノセルロース原料を酵素により糖化処理して糖化残渣を得る工程
工程(2):工程(1)で得られた糖化残渣を、リンのオキソ酸を含む水溶媒中、またはリンのオキソ酸と20℃の水に対する溶解度が90g/L以上の有機溶媒と水とを含む混合溶媒中で加熱処理して、リグニン分解物を含有する加熱処理液を得る工程
工程(3):工程(2)で得られた加熱処理液を固液分離して、不溶分を除去し、リグニン分解物を得る工程
[2]前記[1]の方法により得られたリグニン分解物。
本発明のリグニン分解物の製造方法は、下記工程(1)〜(3)を有する。
工程(1):リグノセルロース原料を酵素により糖化処理して糖化残渣を得る工程
工程(2):工程(1)で得られた糖化残渣を、リンのオキソ酸を含む水溶媒中、またはリンのオキソ酸と20℃の水に対する溶解度が90g/L以上の有機溶媒と水とを含む混合溶媒中で加熱処理して、リグニン分解物を含有する加熱処理液を得る工程
工程(3):工程(2)で得られた加熱処理液を固液分離して、不溶分を除去し、リグニン分解物を得る工程
すなわち、前記工程(1)においてリグノセルロース原料を酵素糖化することにより、リグノセルロース原料に含まれる多糖類が分解されて、リグニンと多糖類の絡み合いが緩和されて、リグニンの自由度が大幅に向上した糖化残渣が得られる。次に前記工程(2)においてこの糖化残渣をリグニンと親和性の高い溶媒に浸漬することで、リグニンが膨潤し、溶媒中の水分子がリグニン分子内部まで浸潤する。この状態で加熱すると、リグニンが変性を受けない比較的穏和な条件でリグニン分子鎖が縮合することなく切断され、溶媒溶解性を有する、低変性のリグニン分解物を高収率で得ることができる。さらに、前記工程(2)において前記溶媒とともにリンのオキソ酸を用いることで、リグニン分子鎖の過度な切断や官能基の分解を極力低減し、リグニンの構造変化に伴う着色を抑制できる。
工程(1)は、リグノセルロース原料を酵素により糖化処理して糖化残渣を得る工程である。
工程(1)において使用されるリグノセルロース原料とは、セルロース、ヘミセルロース及びリグニンを含む植物系のバイオマスをいう。
リグノセルロース原料としては、カラマツやヌクスギなどの針葉樹、アブラヤシ、ヒノキなどの広葉樹から得られる木材チップなどの各種木材;木材から製造されるウッドパルプ、綿の種子の周囲の繊維から得られるコットンリンターパルプなどのパルプ類;バガス(サトウキビの搾りかす)、稲わら、とうもろこし茎・葉、パーム空果房(Empty Fruit Bunch、以下「EFB」という)などの植物茎・葉・果房類;籾殻、パーム殻、ココナッツ殻などの植物殻類;新聞紙、ダンボール、雑誌、上質紙などの紙類;ジャイアントケルプ、コンブ、ワカメ、ノリ、マクサ、スピルリナ、ドナリエラ、クロレラ、セネデスムスなどの藻類などが挙げられる。これらのリグノセルロース原料は、1種単独でも、又は2種以上を組み合わせて用いてもよい。
これらのうち、リグニン分解物の収率向上、糖化効率の向上の観点、入手容易性及び原料コストの観点から、木材、紙類、植物茎・葉・果房類、植物殻類、及び藻類が好ましく、針葉樹チップ、広葉樹チップ、バガス、稲わら、とうもろこし茎・葉、EFB、籾殻、パーム殻、ココナッツ殻、紙類、及び藻類がより好ましく、バガス、EFB、及びアブラヤシの幹から得られる木材チップが更に好ましく、バガスがより更に好ましい。
リグノセルロース原料は、糖化効率の向上、リグニン分解物の収率向上及びリグニンの変性抑制の観点から、酵素で糖化処理する前に、前処理されていることが好ましい。好ましい前処理としては、粉砕処理又は水熱処理が挙げられる。前処理としては、リグニンの変性抑制の観点からは、粉砕処理が好ましく、前処理時間の短縮、及びリグニン分解物の収率向上の観点からは、水熱処理が好ましい。
リグノセルロース原料の前処理として粉砕処理することにより、リグノセルロース原料を小粒子化し、リグノセルロース原料に含まれるセルロースの結晶構造が破壊されるので、糖化効率が向上する。
粉砕処理を行う場合、リグノセルロース原料中の水分量は、リグノセルロース原料の粉砕効率、及びリグニン分解物の収率向上の観点から、リグノセルロース原料の乾燥質量に対して好ましくは40質量%以下、より好ましくは30質量%以下、更に好ましくは20質量%以下、更に好ましくは10質量%以下、更に好ましくは5質量%以下である。なお、リグノセルロース原料中の水分量を0質量%にすることは困難であるため、生産性の観点から、該水分量はリグノセルロース原料の乾燥重量に対して、好ましくは0.01質量%以上、より好ましくは0.1質量%以上、更に好ましくは0.5質量%以上、更に好ましくは1質量%以上である。
リグノセルロース原料中の水分量は、市販の赤外線水分計などを用いて測定することができ、具体的には実施例に記載の方法により測定することができる。
粉砕機の具体例としては、高圧圧縮ロールミルや、ロール回転ミルなどのロールミル、リングローラーミル、ローラーレースミル又はボールレースミルなどの竪型ローラーミル、転動ボールミル、振動ボールミル、振動ロッドミル、振動チューブミル、遊星ボールミル又は遠心流動化ミルなどの容器駆動式媒体ミル、塔式粉砕機、攪拌槽式ミル、流通槽式ミル又はアニュラー式ミルなどの媒体攪拌式ミル、高速遠心ローラーミルやオングミルなどの圧密せん断ミル、乳鉢、石臼、マスコロイダー、フレットミル、エッジランナーミル、ナイフミル、ピンミル、カッターミルなどが挙げられる。これらの中では、リグノセルロース原料の粉砕効率、及び生産性の観点から、容器駆動式媒体ミル又は媒体攪拌式ミルが好ましく、容器駆動式媒体ミルがより好ましく、振動ボールミル、振動ロッドミル又は振動チューブミルなどの振動ミルが更に好ましく、振動ロッドミルがより更に好ましい。
粉砕処理に用いられる塩基性化合物としては、水酸化ナトリウム、水酸化カリウム、水酸化リチウムなどのアルカリ金属水酸化物、水酸化マグネシウム、水酸化カルシウムなどのアルカリ土類金属水酸化物、酸化ナトリウム、酸化カリウムなどのアルカリ金属酸化物、酸化マグネシウム、酸化カルシウムなどのアルカリ土類金属酸化物、硫化ナトリウム、硫化カリウムなどのアルカリ金属硫化物、硫化マグネシウム、硫化カルシウムなどのアルカリ土類金属硫化物などが挙げられる。これらのうち、酵素糖化率向上の観点から、アルカリ金属水酸化物又はアルカリ土類金属水酸化物を用いることがより好ましく、アルカリ金属水酸化物を用いることが更に好ましく、水酸化ナトリウム又は水酸化カリウムを用いることがより更に好ましい。これらの塩基性化合物は、単独で又は2種以上を組み合わせて用いることができる。
粉砕処理時の水分量は、リグノセルロース原料の乾燥質量に対する水分量を意味し、乾燥処理などによりリグノセルロース原料、塩基性化合物に含まれる水分量を低減することや、粉砕処理時に水を添加して水分量を上げることなどにより、適宜調整することができる。
水熱処理とは、加圧条件下で高温の水溶液をリグノセルロース原料に作用させる処理である。水熱処理は、公知の反応装置を用いて行うことができ、用いられる反応装置に特に制限はない。
水熱処理方法としては、バッチ式、連続式のどちらでもよい。
なお、水熱処理で得られたリグノセルロース原料は、湿潤状態のものでもよく、さらに乾燥処理して得られたものでもよいが、糖化効率向上の観点から、湿潤状態のものが好ましい。
工程(1)の糖化処理に用いられる酵素としては、糖化効率の向上、及びリグニン分解物の収率向上、及びリグニンの変性抑制の観点から、セルラーゼやヘミセルラーゼが挙げられる。これらの酵素は、単独で又は2種以上を組み合わせて用いることができる。
ここで、セルラーゼとは、セルロースのβ−1,4−グルカンのグリコシド結合を加水分解する酵素を指し、エンドグルカナーゼ、エクソグルカナーゼまたはセロビオハイドロラーゼ、及びβ−グルコシダーゼなどと称される酵素の総称である。本発明に使用されるセルラーゼとしては、市販のセルラーゼ製剤や、動物、植物、微生物由来のものが含まれる。
これらの中で、糖化効率の向上、及びリグニン分解物の収率向上の観点から、好ましくはトリコデルマ リーゼ(Trichoderma reesei)、トリコデルマ ビリデ(Trichoderma viride)、あるいはフミコーラ インソレンス(Humicola insolens)由来のセルラーゼ、例えばセルクラスト1.5L(ノボザイムズ社製、商品名)、TP−60(明治製菓株式会社製、商品名)、CellicCTec2(ノボザイムズ社製、商品名)、Accellerase DUET(ジェネンコア社製、商品名)、あるいはウルトラフロL(ノボザイムズ社製、商品名)が挙げられる。
例えば、前記酵素を使用し、リグノセルロース原料を基質とする場合は、0.5〜20%(w/v)の基質懸濁液に対して前記酵素を0.001〜15%(v/v)となるように添加し、pH2〜10の緩衝液中、反応温度10℃以上90℃以下で、反応時間30分以上、5日間以下で反応させることにより糖化処理を行うことができる。
上記緩衝液のpHは、用いる酵素の種類により適宜選択することが好ましく、好ましくはpH3以上、より好ましくはpH4以上、そして好ましくはpH7以下、より好ましくはpH6以下である。
また、上記反応温度は、用いる酵素の種類により適宜選択することが好ましく、好ましくは20℃以上、より好ましくは40℃以上であり、そして好ましくは70℃以下、より好ましくは60℃以下である。
さらに、上記反応時間は、用いる酵素の種類により適宜選択することが好ましく、好ましくは0.5日間以上であり、そして好ましくは3日間以下、より好ましくは2日間以下である。
リグノセルロース原料を酵素により糖化処理することにより、糖化残渣が得られる。ここで糖化残渣とは、酵素糖化処理後の混合物を遠心分離等の固液分離手段により分離した、固形成分のことである。この固形成分は、水で数回洗浄することで水溶性の多糖類を除去できる。その後、湿潤状態で次の工程(2)を行ってもよいし、乾燥させることで、糖化残渣を粉末化してもよい。生産効率向上の観点からは、湿潤状態で次の工程(2)を行うことが好ましい。また、乾燥処理を行う場合は、リグニンの変性抑制の観点から、100℃以下で乾燥することが好ましく、凍結乾燥することがより好ましい。
工程(2)は、前述の糖化残渣を、リンのオキソ酸を含む水溶媒中、またはリンのオキソ酸と20℃の水に対する溶解度が90g/L以上の有機溶媒と水とを含む混合溶媒中で加熱処理して、リグニン分解物を含有する加熱処理液を得る工程である。当該溶媒においては、リグニン分解物を高収率で得る観点から、20℃の水に対する溶解度が90g/L以上の有機溶媒と水とを含む混合溶媒が好ましい。
工程(2)に用いる水溶媒は、溶媒として20℃の水に対する溶解度が90g/L以上の有機溶媒を含まない。
工程(2)において、水溶媒又は前記混合溶媒に、酸としてリンのオキソ酸から選ばれる1種以上を含有させることにより、低着色のリグニン分解物を高収率で得ることができる。本発明において、リンのオキソ酸とは、リン−酸素結合を有する塩をいい、例えば、次亜リン酸、ホスフィン酸、亜リン酸、ホスホン酸、リン酸、メタリン酸、及びピロリン酸が挙げられる。これらは、リンのオキソ酸塩として用いることができ、例えば、アルカリ金属塩、アルカリ土類金属塩、アンモニウム塩、有機アミン塩等が挙げられる。これらの中では、リグニン分解物を高収率で得る観点からリン酸が好ましく、低着色のリグニン分解物を高収率で得る観点からホスホン酸が好ましい。
工程(2)で用いる水溶媒又は前記混合溶媒に用いる水としては、特に制限はないが、蒸留水、イオン交換水又は純水等が挙げられる。溶媒として水を用いることにより、糖化残渣の膨潤と分子鎖の開裂が促進され、リグニンとセルロース及びヘミセルロースとの交絡を容易に解くことができ、リグニン分解物の抽出効率を向上させることができる。
工程(2)で水と共に用いる有機溶媒は、糖化残渣に含まれるセルロース及びヘミセルロースからリグニンを容易に分離し(以下、単に「リグニン分離性」ともいう。)、リグニン分解物の抽出効率を向上させる観点から、20℃の水に対する溶解度が90g/L以上であり、好ましくは100g/L以上、より好ましくは120g/L以上である。20℃の水に対する溶解度が90g/L以上の有機溶媒を用いることにより、混合溶媒とリグニンとの親和性が向上し、リグニンとセルロース及びヘミセルロースとの交絡を容易に解くことができ、リグニン分解物の抽出効率を向上させることができる。
前記有機溶媒としては、リグニン分離性及びリグニン分解物の抽出効率向上の観点から、アルコール類、ニトリル類、エーテル類及びケトン類からなる群から選ばれる1種以上が好ましい。
前記有機溶媒は、リグニン分解物の抽出効率向上の観点から、SP値が8〜23であることが好ましく、より好ましくは8〜16、更に好ましくは9〜13である。
ここで、「SP値」とは、溶解性パラメーター(Solubility Parameter;SP値)を意味し、Fedorsの方法〔Robert F.Fedors, Polymer Engineering and Science, 14, 147-154 (1974)〕により、下記のFedorsの式に基づいて求められた値δ[(cal/cm3)1/2]であり、化合物の化学構造の原子または原子団の蒸発エネルギーの総和(Δei)とモル体積の総和(Δvi)の比の平方根から求められる。
Fedorsの式: δ=(ΣΔei/ΣΔvi)1/2
前記アルコール類としては、メタノール、エタノール、ジエチレングリコール、n−プロパノール、イソプロパノール、2−ブタノール、イソブタノール、t−ブチルアルコールなどが挙げられる。
前記ニトリル類としては、アセトニトリルなどが挙げられる。
前記エーテル類としては、ジオキサンなどが挙げられる。
前記ケトン類としては、アセトン、メチルエチルケトンなどが挙げられる。
上記で例示した有機溶媒は、いずれも20℃の水に対する溶解度が90g/L以上である。これらの有機溶媒は、単独で又は2種以上を組み合わせて用いることができる。
これらの有機溶媒のうち、リグニン分離性及びリグニン分解物の抽出効率向上、安全性の観点から、エタノール、イソプロパノール、2−ブタノール、t−ブタノール、アセトン及びメチルエチルケトンからなる群から選ばれる1種以上が好ましく、より好ましくはエタノール、イソプロパノール及びアセトンからなる群から選ばれる1種以上であり、更に好ましくはイソプロパノール及びアセトンからなる群から選ばれる1種以上であり、更に好ましくはアセトンである。
用いられるラジカル捕捉剤としては、ヒドロキノン、ベンゾキノン、メトキノン、フェノール等の芳香族系ラジカル捕捉剤、トリブチルアミン、ジフェニルアミン、フェノチアジンおよびフェニル−α−ナフチルアミン等のアミン系ラジカル捕捉剤、2,2,6,6−テトラメチルピペリジン−1−オキシル等の安定化フリーラジカル系ラジカル捕捉剤、L−アスコルビン酸、エリソルビン酸、α−トコフェロールおよびクロロゲン酸等の有機酸系ラジカル捕捉剤、(+)−カテキン、エピカテキン、エピガロカテキン、エピガロカテキンガラートおよびエピガロカテキンガラート等のカテキン系ラジカル捕捉剤、及び分子状水素などが挙げられる。
工程(2)で用いる混合溶媒中の前記有機溶媒の含有量は、リグニン分離性及びリグニン分解物の抽出率向上の観点から、好ましくは0.01質量%以上、より好ましくは10質量%以上、更に好ましくは30質量%以上、更に好ましくは40質量%以上であり、そして好ましくは90質量%以下、より好ましくは70質量%以下であり、更に好ましくは60質量%以下であり、更に好ましくは50質量%以下である。
リンのオキソ酸の含有量は、リグニン分解物の収率向上、生成するリグニン分解物の分子量制御及び低着色のリグニン分解物を得る観点から、工程(2)で用いる水溶媒又は混合溶媒に対して、好ましくは0.01質量%以上、より好ましくは0.1質量%以上、更に好ましくは0.3質量%以上、更に好ましくは1質量%以上であり、そして好ましくは15質量%以下、より好ましくは10質量%以下、更に好ましくは8質量%以下、更に好ましくは5質量%以下である。
工程(2)で用いられる加熱装置としては、リグニンの変性抑制及びリグニン分解物の収率向上の観点から、オートクレーブ又はマイクロ波加熱装置が好ましい。
工程(3)は、前記工程(2)で得られたリグニン分解物を含有する加熱処理液を固液分離して、不溶分を除去し、リグニン分解物を得る工程である。
リグニン分解物を得る方法としては、工程(2)で得られた加熱処理液を固液分離し、不溶分を除去し、液体分に含まれるリグニン分解物を得る工程を少なくとも含む方法であれば、特に限定されない。リグニン分解物を得る方法としては、ろ過、遠心分離などの固液分離の他に、溶媒留去、洗浄、乾燥等の工程を適宜組み合わせることができる。また前記工程(2)でリンのオキソ酸を添加するため、リグニン分解後のpHに応じて中和する工程を含む。これらの工程は、常法により行うことができる。例えば、前記工程(2)で得られた加熱処理液の固液分離により不溶分を除去し、液体分に含まれる前記有機溶媒及び水を減圧留去し、得られた残渣を水洗し、リグニン分解物を得る方法が挙げられる。溶媒留去後の残渣を水洗することで、水溶性の多糖類等を除去することができ、リグニン分解物のリグニン純度を高めることができる。中和に用いる塩基としては、前記粉砕処理に用いられる塩基性化合物と同じものが挙げられる。
本発明の製造方法により得られるリグニン分解物は、低着色で、かつ溶媒溶解性を有する。このため、例えば、抗菌剤、農薬、及び熱硬化性樹脂、セメント分散剤、蓄電池用分散剤、香粧品用途の添加剤、その他の機能性材料として利用することができる。
本発明の製造方法により得られるリグニン分解物の重量平均分子量は、例えば、2,000以上、40,000以下の範囲であり、リグニン分解物の用途に応じて、適宜分子量を選択して使用することができる。なお、重量平均分子量は、実施例記載の方法により測定される。
また、本発明の製造方法により得られるリグニン分解物の変性度の指標であるアルデヒド収率は、低分子芳香族化合物への変換の観点から、好ましくは10%以上、より好ましくは12.5%以上、更に好ましくは15%以上、より更に好ましくは20%以上である。なお、前記アルデヒド収率は、実施例に記載のアルカリニトロベンゼン酸化法により測定される値であり、アルデヒド収率の値が高いほど、リグニン分解物の変性度が低いことを示す。
また、本発明の製造方法により得られるリグニン分解物の着色度の指標であるL値(明度)は、低分子芳香族化合物への変換の観点から、好ましくは45以上、より好ましくは50以上、更に好ましくは55以上である。なお、L値は、実施例に記載の色差計によって測定される値であり、L値が高いほど明度が高く、白色に近いことを示す。
[1]下記工程(1)〜(3)を有する、リグニン分解物の製造方法。
工程(1):リグノセルロース原料を酵素により糖化処理して糖化残渣を得る工程
工程(2):工程(1)で得られた糖化残渣を、リンのオキソ酸を含む水溶媒中、またはリンのオキソ酸と20℃の水に対する溶解度が90g/L以上の有機溶媒と水とを含む混合溶媒中で加熱処理して、リグニン分解物を含有する加熱処理液を得る工程
工程(3):工程(2)で得られた加熱処理液を固液分離して、不溶分を除去し、リグニン分解物を得る工程
[3]工程(2)の加熱処理温度が、好ましくは40℃以上、より好ましくは60℃以上、更に好ましくは80℃以上、更に好ましくは90℃以上であり、そして、好ましくは300℃以下、より好ましくは200℃以下、更に好ましくは150℃以下、更に好ましくは130℃以下である、上記[1]又は[2]に記載のリグニン分解物の製造方法。
[4]前記混合溶媒における前記有機溶媒と水の比率〔有機溶媒/水〕(質量比)が、好ましくは90/10〜0.01/99.99、より好ましくは90/10〜10/90、更に好ましくは70/30〜30/70、更に好ましくは、60/40〜40/60、更に好ましくは50/50〜40/60である、上記[1]〜[3]のいずれかに記載のリグニン分解物の製造方法。
[5]水溶媒、または前記混合溶媒の使用量が、糖化残渣の固形分に対し、好ましくは2質量倍以上、より好ましくは5質量倍以上、更に好ましくは10質量倍以上、更に好ましくは15質量倍以上であり、そして好ましくは40質量倍以下、より好ましくは30質量倍以下である、上記[1]〜[4]のいずれかに記載のリグニン分解物の製造方法。
[6]酵素が、好ましくはセルラーゼ及びヘミセルラーゼからなる群から選ばれる1種以上、より好ましくはセロビオハイドロラーゼ、β−グルコシダーゼ、エンドグルカナーゼ及びヘミセルラーゼからなる群から選ばれる1種以上、更に好ましくはセロビオハイドロラーゼ、及びエンドグルカナーゼからなる群から選ばれる1種以上である、上記[1]〜[5]のいずれかに記載のリグニン分解物の製造方法。
[7]リグノセルロース原料が、好ましくは針葉樹チップ、広葉樹チップ、バガス、稲わら、とうもろこし茎・葉、パーム空果房(EFB)、籾殻、パーム殻、ココナッツ殻、紙類及び藻類からなる群から選ばれる1種以上、より好ましくは、バガス、EFB、又はアブラヤシの幹から得られる木材チップ、更に好ましはバガスである、上記[1]〜[6]に記載のリグニン分解物の製造方法。
[9] 粉砕処理における、リグノセルロース原料中の水分量が、リグノセルロース原料の乾燥質量に対して、好ましくは40質量%以下、より好ましくは30質量%以下、更に好ましくは20質量%以下、更に好ましくは10質量%以下、更に好ましくは5質量%以下であり、そして好ましくは0.01質量%以上、より好ましくは0.1質量%以上、更に好ましくは0.5質量%以上、更に好ましくは1質量%以上である、上記[8]に記載のリグニン分解物の製造方法。
[10] 粉砕時間が、好ましくは1分以上、より好ましくは2分以上、更に好ましくは5分以上であり、そして好ましくは12時間以下、より好ましくは6時間以下、更に好ましくは3時間以下、更に好ましくは2時間以下である、上記[8]又は[9]に記載のリグニン分解物の製造方法。
[11] 塩基性化合物の存在下で粉砕処理する、上記[8]〜[10]のいずれかに記載のリグニン分解物の製造方法。
[12] 粉砕処理時の水分量が、リグノセルロース原料の乾燥質量に対して0.1質量%以上、より好ましくは0.5質量%以上、更に好ましくは1質量%以上、更に好ましくは2質量%以上であり、そして、好ましくは40質量%以下、より好ましくは35質量%以下、更に好ましくは30質量%以下、更に好ましくは25質量%以下、更に好ましくは20質量%以下である、上記[8]〜[11]のいずれかに記載のリグニン分解物の製造方法。
[14] 有機溶媒が、好ましくはエタノール、イソプロパノール、2−ブタノール、t−ブタノール、アセトン及びメチルエチルケトンからなる群から選ばれる1種以上、より好ましくはエタノール、イソプロパノール及びアセトンからなる群から選ばれる1種以上であり、更に好ましくはイソプロパノール及びアセトンからなる群から選ばれる1種以上であり、更に好ましくはアセトンである、[1]〜[13]のいずれかに記載のリグニン分解物の製造方法。
[15] 工程(2)における加熱処理の時間が、好ましくは1分以上、より好ましくは2分以上、更に好ましくは10分以上であり、そして好ましくは6時間以下、より好ましくは4時間以下、更に好ましくは3時間以下である[1]〜[14]のいずれかに記載のリグニン分解物の製造方法。
[16] 上記[1]〜[15]のいずれかに記載の製造方法により得られたリグニン分解物。
[17]リグニン分解物のL値(明度)が、好ましくは45以上、より好ましくは50以上、更に好ましくは55以上である、上記[16]に記載のリグニン分解物。
粉砕したリグノセルロース原料を、エタノール−ジクロロエタン混合溶剤(1:1、質量比)で6時間ソックスレー抽出を行い、抽出後のサンプルを60℃で真空乾燥した。得られた試料2.5gに水150mL、亜塩素酸ナトリウム1.0g及び酢酸0.2mLを添加し、70〜80℃で1時間加温した。引き続き亜塩素酸ナトリウム及び酢酸を添加して加温する操作を、試料が白く脱色するまで3〜4回繰り返し行った。白色の残渣をグラスフィルター(1G−3)でろ過し、冷水及びアセトンで洗浄した後、105℃で恒量になるまで乾燥し、残渣質量を求めた。下記式によりホロセルロース含有量を算出し、これをセルロース含有量とした。
セルロース含有量(質量%)=[残渣質量(g)/リグノセルロース原料の採取量(g:乾燥原料換算)]×100
AGUモル数は、リグノセルロース原料中のホロセルロースをすべてセルロースと仮定して、以下の式に基づき算出した。
AGUモル数=ホロセルロース質量(g)/162
リグノセルロース原料の水分量の測定には、赤外線水分計「FD−610」(株式会社ケット科学研究所製)を使用した。150℃にて測定を行い、30秒間の質量変化率が0.1%以下となる点を測定の終点とした。測定された水分量の値を、リグノセルロース原料の乾燥質量に対する質量%に換算した。
X線回折強度は、株式会社リガク製の「Rigaku RINT 2500VC X-RAY diffractometer」を用いて以下の条件で測定し、以下計算式(1)に基づいてセルロースI型結晶化度を算出した。
測定条件は、X線源:Cu/Kα−radiation,管電圧:40kv,管電流:120mA,測定範囲:2θ=5〜45°で測定した。測定用サンプルは面積320mm2×厚さ1mmのペレットを圧縮し作製した。X線のスキャンスピードは10°/minで測定した。
〔セルロースI型結晶化度〕
セルロースI型結晶化度は、X線回折法による回折強度値からSegal法により算出したもので、下記計算式(1)により定義される。
セルロースI型結晶化度(%)=〔(I22.6−I18.5)/I22.6〕×100 (1)
〔I22.6は、X線回折における格子面(002面)(回折角2θ=22.6°)の回折強度、I18.5は、アモルファス部(回折角2θ=18.5°)の回折強度を示す〕
平均粒径は、レーザー回折/散乱式粒度分布測定装置「LA−950」(株式会社堀場製作所製)を用いて測定した。測定条件は、粒径測定前に超音波で1分間処理し、測定時の分散媒体として水を用い、体積基準のメジアン径を、室温にて測定した。
リグノセルロース原料中のリグニン含有量は、下記式により算出した。なお、工程(2)の初期基質である酵素糖化残渣、および工程(2)の最終残渣についても、リグニン含有量の測定方法は同様である。
リグニン含有量(g)=〔真の酸不溶性リグニン含率(%)+酸可溶性リグニン含率(%)〕×試料採取量(乾基準)(g)/100
ここで、真の酸不溶性リグニン含率及び酸可溶性リグニン含率は、以下に示す方法により算出した。
真の酸不溶性リグニン含率は、下記式により、粗酸不溶性リグニン中の灰分率を差し引いて算出した。
真の酸不溶性リグニン含率(%)=粗酸不溶性リグニン含率(%)×〔100−灰分率(%)〕/100
粉砕したリグノセルロース原料を、60℃で真空乾燥した。この乾燥試料300mgをバイアルに入れ、72%硫酸を3ml加えて30℃の水浴中で1時間適宜撹拌した。その後、水84mlを加えて耐圧瓶に移し、オートクレーブを用いて120℃で1時間処理を行った。その後、試料が70℃以下にならないうちに取り出し、予め恒量を測定しておいた1G−3のガラスフィルターを用いて吸引ろ過を行った。ろ液(A)は保管し、残渣が付着したガラスフィルターはよく水洗した後、105℃で乾燥して、恒量を測定し、粗酸不溶性リグニン採取量(乾基準)を求めた。
粗酸不溶性リグニン含率(%)=〔リグニン残査質量(g)/試料採取量(乾基準)(g)〕×100
粗酸不溶性リグニンを予め恒量を測定したるつぼに移し、575℃で12時間保持し、その後冷却して、るつぼの恒量を測定し、灰化後試料質量を求め、下記式により灰分率を求めた。
灰分率(%)=〔灰化後試料質量(g)/粗酸不溶性リグニン採取量(乾基準)(g)〕×100
酸可溶性リグニンの測定は以下の方法により行った。
ろ液(A)を100mlに定容し、UV−Vis吸光光度計を用いて、205nmにおける吸光度を測定した。この時、吸光度が0.3〜0.8になるように適宜希釈した。
酸可溶性リグニン含率(%)=d×v×(As−Ab)/(a×w)×100
d:希釈倍率、v:ろ液定容量(L)、As:試料溶液の吸光度、Ab:ブランク溶液の吸光度、a:リグニンの吸光係数、w:試料採取量(乾基準)(g)
リグニンの吸光係数(a)は、参考資料(「リグニン化学研究法」、ユニ出版株式会社発行)において、既報の平均値として記載されている値110L/g/cmを用いた。
リグニン抽出率は下記のように算出した。
(酵素糖化残渣の場合)
リグニン抽出率(質量%)=〔(酵素糖化残渣の仕込み質量(g)×酵素糖化残渣中のリグニン含量(%))―(工程(2)で得られた最終残渣の質量(g)×工程(2)で得られた最終残渣のリグニン含率(%))〕/〔酵素糖化残渣の仕込み質量(g)×酵素糖化残渣中のリグニン含量(%)〕×100×K
K(%)=〔酵素糖化残渣の回収量(g)×酵素糖化残渣中のリグニン含量(%)〕/〔リグノセルロース原料の仕込み質量(g)×リグノセルロース原料中のリグニン含量(%)〕
なお、工程(2)で得られた最終残渣とは、工程(2)で得られる加熱処理液中の不溶分のことである。
リグニン抽出率(質量%)=〔クラフト蒸解リグニンの回収量(g)×クラフト蒸解リグニン中のリグニン含量(%)〕/〔リグノセルロース原料の仕込み質量(g)×リグノセルロース原料中のリグニン含量(%)〕
本方法で製造したリグニン分解物の重量平均分子量を、ゲルクロマトグラフィー法により下記条件で測定した。
東ソー株式会社製GPC装置(HLC−8120GPC)に、東ソー株式会社製カラム(TSK−GEL、α−M)2本とガードカラムを連結した。溶離液として60mmol/LのH3PO4と50mmol/LのLiBrを添加したN,N−ジメチルホルムアミドを、毎分1mlの流速で流し、40℃の恒温槽中でカラムを安定させた。そこに試料溶液100μlを注入して測定を行った。試料の分子量は、あらかじめ作成した検量線に基づき算出した。このときの検量線には、数種類の単分散ポリスチレン〔東ソー株式会社製のA−500(分子量5.0×102)、F−10(分子量9.64×104)、F−850(分子量8.42×106)、Pressure Chemical社製(分子量4.0×103、3.0×104、9.29×105)〕を標準試料として作成したものを用いた。
リグニン分解物又は試薬のリグニン変性度は、参考資料(「リグニン化学研究法」、ユニ出版株式会社発行)に記載のアルカリニトロベンゼン酸化法を用いて、アルデヒド収率を指標に評価した。具体的には下記の方法により測定した。
リグニン分解物又は試薬50mgを秤量した。試料、2M 水酸化ナトリウム水溶液7ml、ニトロベンゼン0.4mlを20mlのバイアルに入れ、900rpmで撹拌しながら170℃で2.5時間加熱した。反応終了後冷却し、10mlのジエチルエーテルで3回抽出し、ニトロベンゼン還元物と余分なニトロベンゼンを除去した。残った水層側に濃塩酸を加えてpH1に調整し、さらに10mlのジエチルエーテルで3回抽出した。このジエチルエーテル抽出液を減圧下で留去し、酸化混合物を得た。この混合物をジクロロメタン20mLでメスアップした。うち2mlをミリポアHVHP膜(日本ミリポア株式会社製、孔径0.45μm)でろ過し、ガスクロマトグラフィ(GC)に供した。
3つのアルデヒド量を合算し、アルデヒド収量とした。仕込み試料中のリグニン質量でアルデヒド収量を割ることで、アルデヒド収率(%)を算出し、リグニン変性度の指標とした。
アルデヒド収率が高いほど、低変性なリグニン分解物であることを示している。
得られたリグニン分解物1mgをバイアルに採取し、溶媒を1ml添加し、撹拌してリグニンの溶媒溶解性を目視で評価した。溶媒としてジメチルスルホキシド(DMSO)、又はジメチルホルムアミド(DMF)を用いた。
得られたリグニン分解物又は試薬1mgを乳鉢で磨り潰して微粒化を確認した後、バイアル(株式会社マルエム製、スクリュー管、No.3)に100mg採取した。次に、色差計(コニカミノルタ株式会社製、CR−200)の検出部を天井に向けて固定し、サンプルの入ったバイアルの底辺を色差計の検出部に密着させた上でL値を3回測定し、得られた値の平均値を求めた。L値は明度を示すため、L値が高いほど白く、L値が低いほど黒いことを表している。
(前処理)
リグノセルロース原料として、バガス(サトウキビの搾りかす、水分量7.0%)を減圧乾燥機「VO−320」(アドバンテック東洋株式会社製)の中に入れ、窒素流通下の条件で2時間減圧乾燥し、水分量2.0%、ホロセルロース含有量71.3質量%、リグニン含有量22.8%の乾燥バガスを得た。
得られた乾燥バガス100gと、粒径0.7mmの粒状の水酸化ナトリウム「トーソーパール」(東ソー株式会社製)8.8g(ホロセルロースを構成するAGU1モルに対し0.5モル相当量)とを、バッチ式振動ミル「MB−1」(中央化工機株式会社製:容器全容積3.5L、ロッドとして、φ30mm、長さ218mm、断面形状が円形のSUS304製ロッド、ロッド充填率57%)に投入し、水冷しながら2時間粉砕処理して粉砕バガス(セルロースI型結晶化度2%、平均粒径56.6μm)を得た。得られた粉砕バガス100g(塩基性化合物を除いた乾燥原料換算)を、1.0M 塩酸で中和した。
粉砕バガス100gを2.0Lの100mM酢酸緩衝液(pH5.0)に投入し、セルラーゼ・ヘミセルラーゼ製剤「Cellic CTec 2」(ノボザイム社製)を20mL添加し、50℃に保ちながら600rpmで撹拌し酵素糖化を行った。24時間後に反応を終了させ、遠心分離により上清と糖化残渣に分離した。糖化残渣は洗浄・遠心分離を繰り返し行い、凍結乾燥させた。上述の方法により糖化残渣のリグニン含有量を測定した。
糖化残渣(絶乾質量250mg)を反応容器(容量5mL)に取り、最終的にアセトン/水(50/50,質量比)の混合溶媒が4.8gとなり、かつ、混合溶媒に対してリン酸濃度が1.8質量%となるように、リン酸水溶液、アセトン、水を加えて密閉した後、120℃で30分間、圧力は成り行きとし、900rpmで撹拌しながらマイクロ波加熱装置Initiator 60(バイオタージ・ジャパン株式会社製)を用いてマイクロ波加熱を行い、加熱処理液を得た。
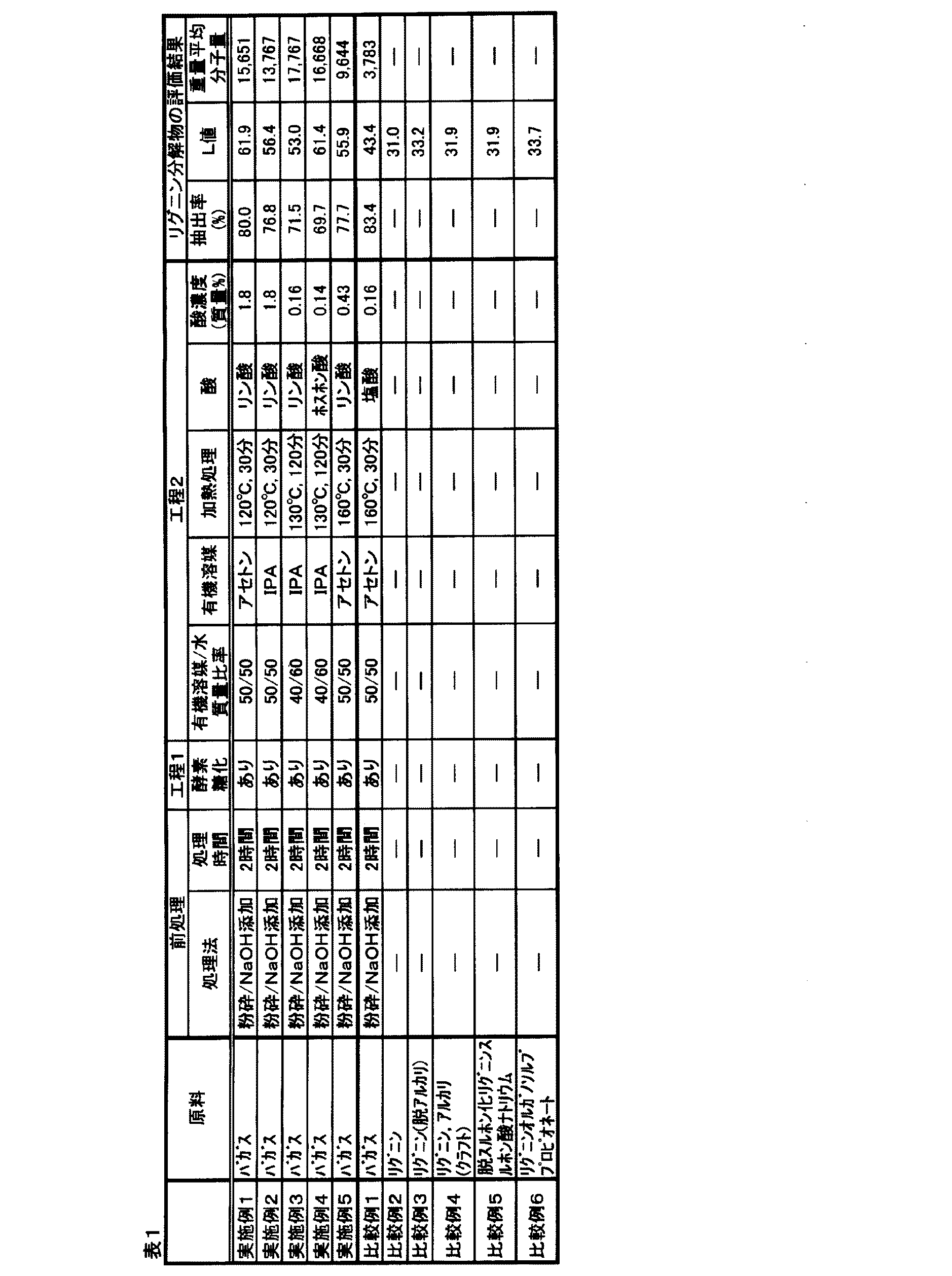
工程(2)で得られた加熱処理液は、遠心分離により抽出液と残渣に分離され、残渣をアセトン、水、及びアセトン/水混合溶媒で抽出液が透明になるまで洗浄した。遠心分離及び洗浄により得られた抽出液を集め、抽出液のpHが5.0〜6.0となるように適宜水酸化ナトリウムで中和した後、抽出液に含まれる溶媒を減圧留去した。得られた固形分を再度水で洗浄し、水不溶分を凍結乾燥してリグニン分解物を得た。上述の方法で、リグニンの抽出率、リグニン分解物のL値および重量平均分子量を測定した。結果を表1に示す。
工程(2)で、有機溶媒をイソプロパノールとした以外は、実施例1と同様の条件で行った。結果を表1に示す。
工程(2)で、糖化残渣(絶乾質量500mg)とし、イソプロパノール/水の質量比を40/60とし、リン酸濃度を0.16質量%とし(混合溶媒のpH4.5)、反応温度130℃で120分処理した以外は、実施例2と同様の条件で行った。結果を表1に示す。
工程(2)で、リン酸の代わりにホスホン酸を0.14質量%添加した以外は、実施例3と同様の条件で行った。結果を表1に示す。
工程(2)で、リン酸濃度を0.43質量%とし、反応温度160℃で30分処理した以外は、実施例1と同様の条件で行った。結果を表1に示す。
工程(2)で、混合溶媒中に塩酸(濃度1.0M)を240μL添加し、反応温度160℃で30分間処理した以外は、実施例1と同様の条件で行った。結果を表1に示す。
リグニン(関東化学;試薬)を用いて、上述の方法により、リグニン分解物のL値を測定した。結果を表1に示す。
リグニン(脱アルカリ)(東京化成工業株式会社;試薬「Lignin(Dealkali)」)を用いた以外は、比較例2と同様の条件で行った。結果を表1に示す。
リグニン、アルカリ(クラフト)(シグマ−アルドリッチ社製;試薬「Lignin、alkali(Kraft)」)を用いた以外は、比較例2と同様の条件で行った。結果を表1に示す。
脱スルホン化リグニンスルホン酸ナトリウム(シグマ−アルドリッチ社製;試薬「Lignosulfonic acid、sodium salt、desulfonated」)を用いた以外は、比較例2と同様の条件で行った。結果を表1に示す。
リグニンオルガノソルブプロピオネート(Sigma−Aldrich;試薬「Lignin、organosolv、propionate」)を用いた以外は、比較例2と同様の条件で行った。結果を表1に示す。
Claims (8)
- 下記工程(1)〜(3)を有する、リグニン分解物の製造方法。
工程(1):リグノセルロース原料を酵素により糖化処理して糖化残渣を得る工程
工程(2):工程(1)で得られた糖化残渣を、リンのオキソ酸を含む水溶媒中、またはリンのオキソ酸と20℃の水に対する溶解度が90g/L以上の有機溶媒と水とを含む混合溶媒中で加熱処理して、リグニン分解物を含有する加熱処理液を得る工程
工程(3):工程(2)で得られた加熱処理液を固液分離して、不溶分を除去し、リグニン分解物を得る工程 - 前記リンのオキソ酸の含有量が、工程(2)で用いる水溶媒又は混合溶媒に対して、0.01質量%以上、15質量%以下である、請求項1に記載のリグニン分解物の製造方法。
- 工程(2)の加熱処理温度が、80℃以上、150℃以下である、請求項1又は2に記載のリグニン分解物の製造方法。
- 前記混合溶媒における前記有機溶媒と水の比率〔有機溶媒/水〕(質量比)が、90/10〜10/90である、請求項1〜3のいずれかに記載のリグニン分解物の製造方法。
- 工程(2)で用いる前記水溶媒、または前記混合溶媒の使用量が、糖化残渣の固形分に対し、2質量倍以上、40質量倍以下である、請求項1〜4のいずれかに記載のリグニン分解物の製造方法。
- 酵素が、セロビオハイドロラーゼ、β−グルコシダーゼ、エンドグルカナーゼ及びヘミセルラーゼからなる群から選ばれる1種以上である、請求項1〜5のいずれかに記載のリグニン分解物の製造方法。
- リグノセルロース原料が、針葉樹チップ、広葉樹チップ、バガス、稲わら、とうもろこし茎・葉、パーム空果房(EFB)、籾殻、パーム殻、ココナッツ殻、紙類、及び藻類からなる群から選ばれる1種以上である、請求項1〜6のいずれかに記載のリグニン分解物の製造方法。
- リグノセルロース原料を、酵素で糖化処理する前に粉砕処理する、請求項1〜7のいずれかに記載のリグニン分解物の製造方法。
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2013131931A JP6182368B2 (ja) | 2013-06-24 | 2013-06-24 | リグニン分解物の製造方法 |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2013131931A JP6182368B2 (ja) | 2013-06-24 | 2013-06-24 | リグニン分解物の製造方法 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2015006998A JP2015006998A (ja) | 2015-01-15 |
| JP6182368B2 true JP6182368B2 (ja) | 2017-08-16 |
Family
ID=52337609
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2013131931A Active JP6182368B2 (ja) | 2013-06-24 | 2013-06-24 | リグニン分解物の製造方法 |
Country Status (1)
| Country | Link |
|---|---|
| JP (1) | JP6182368B2 (ja) |
Families Citing this family (8)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2016171275A1 (ja) * | 2015-04-24 | 2016-10-27 | 花王株式会社 | 樹脂用添加剤 |
| CN107531954B (zh) | 2015-04-24 | 2020-04-28 | 花王株式会社 | 树脂用添加剂 |
| FI127740B (en) | 2015-05-29 | 2019-01-15 | Upm Kymmene Corp | Method and apparatus for forming a lignin fraction and lignin composition and use thereof |
| US11134679B2 (en) | 2016-04-11 | 2021-10-05 | Kao Corporation | Method for growing plant |
| US11279877B2 (en) | 2016-04-11 | 2022-03-22 | Kao Corporation | Method for improving soil |
| CN109890890B (zh) * | 2016-10-26 | 2022-02-22 | 花王株式会社 | 橡胶组合物 |
| BE1025161B1 (fr) * | 2017-04-20 | 2018-11-26 | Galactic S.A. | Procede de production simultanee d'acide lactique et d'alcool ou biogaz au depart de cereales |
| JP6974988B2 (ja) * | 2017-09-05 | 2021-12-01 | 花王株式会社 | 植物収量向上剤 |
Family Cites Families (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US8663392B2 (en) * | 2008-03-14 | 2014-03-04 | Virginia Tech Intellectual Properties, Inc. | Method and apparatus for lignocellulose pretreatment using a super-cellulose-solvent and highly volatile solvents |
| CN101285106B (zh) * | 2008-06-10 | 2010-08-18 | 南京工业大学 | 一种高效水解木质纤维素类生物质同时制备多组分糖液及木质素的方法 |
| CA2800234C (en) * | 2010-03-08 | 2018-08-28 | Forestry And Forest Products Research Institute | Lignin-based enzyme stabilizer |
| JP5720131B2 (ja) * | 2010-07-06 | 2015-05-20 | 王子ホールディングス株式会社 | リグニンの製造方法及びその組成物 |
| JP5685959B2 (ja) * | 2011-01-26 | 2015-03-18 | 王子ホールディングス株式会社 | リグノセルロース含有バイオマスからの有価物の製造方法 |
-
2013
- 2013-06-24 JP JP2013131931A patent/JP6182368B2/ja active Active
Also Published As
| Publication number | Publication date |
|---|---|
| JP2015006998A (ja) | 2015-01-15 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP6007081B2 (ja) | リグニン分解物の製造方法 | |
| JP6182368B2 (ja) | リグニン分解物の製造方法 | |
| Palamae et al. | Cellulose and hemicellulose recovery from oil palm empty fruit bunch (EFB) fibers and production of sugars from the fibers | |
| Michelin et al. | Liquid hot water pretreatment of multi feedstocks and enzymatic hydrolysis of solids obtained thereof | |
| Luo et al. | High efficiency and clean separation of eucalyptus components by glycolic acid pretreatment | |
| EP2652193B1 (en) | Treatment | |
| Hu et al. | Impact of pseudolignin versus dilute acid-pretreated lignin on enzymatic hydrolysis of cellulose | |
| Valladares-Diestra et al. | Citric acid assisted hydrothermal pretreatment for the extraction of pectin and xylooligosaccharides production from cocoa pod husks | |
| JP6247030B2 (ja) | 紫外線吸収剤 | |
| JP2008271962A (ja) | 糖の製造方法 | |
| Tang et al. | Fibrous agricultural biomass as a potential source for bioconversion to vanillic acid | |
| Shankar et al. | Fungal-integrated second-generation lignocellulosic biorefinery: utilization of agricultural biomass for co-production of lignocellulolytic enzymes, mushroom, fungal polysaccharides, and bioethanol | |
| Nlandu et al. | Flax nanofibrils production via supercritical carbon dioxide pre‐treatment and enzymatic hydrolysis | |
| JP6182369B2 (ja) | リグニン分解物の製造方法 | |
| JP6349518B2 (ja) | リグニン分解物の製造方法 | |
| JP2012016285A (ja) | リグニンの製造方法及びその組成物 | |
| Poolakkalody et al. | Evaluating the biofuel potential of perennial grass, Pennisetum polystachion based on aqueous 1-ethyl, 3-methylimidazolium acetate ([EMIM][Ac]) pretreatment | |
| AU2013237533B2 (en) | Process for the production of organic compounds from plant species | |
| Kumagai et al. | Improvement of enzymatic saccharification of Populus and switchgrass by combined pretreatment with steam and wet disk milling | |
| JP2013221149A (ja) | リグニン分解物の製造方法 | |
| JP2014117207A (ja) | 糖の製造方法 | |
| JP6474150B2 (ja) | バイオマス原料の糖化方法 | |
| JP2011055732A (ja) | 樹皮原料から糖類を製造する方法 | |
| Deba et al. | Biosugar production from oil palm mesocarp fiber (OPMF) using Viscozyme | |
| Sunar et al. | Pretreatment of sugarcane bagasse using ionic liquid for enhanced enzymatic saccharification and lignin recovery: process optimization by response surface methodology |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20160307 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20161129 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20170130 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20170704 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20170724 |
|
| R151 | Written notification of patent or utility model registration |
Ref document number: 6182368 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R151 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |