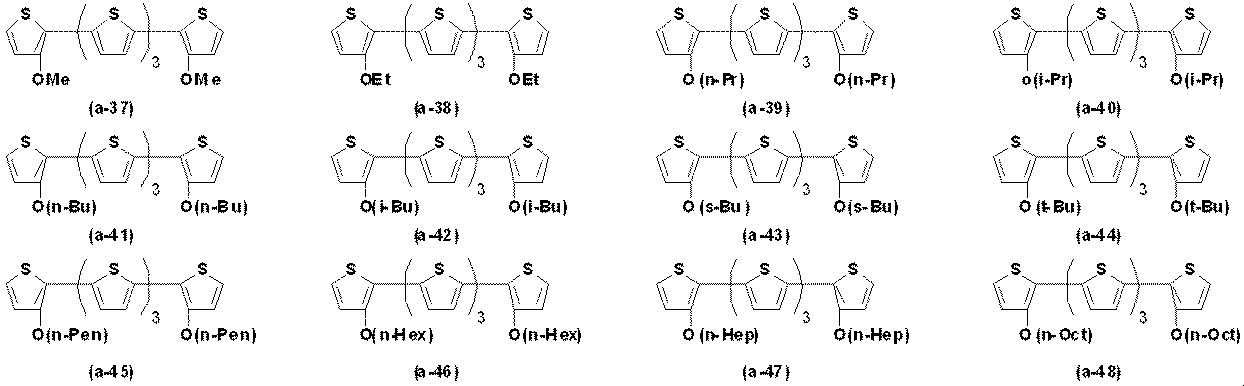JP6132016B2 - 電荷輸送性ワニス - Google Patents
電荷輸送性ワニス Download PDFInfo
- Publication number
- JP6132016B2 JP6132016B2 JP2015517001A JP2015517001A JP6132016B2 JP 6132016 B2 JP6132016 B2 JP 6132016B2 JP 2015517001 A JP2015517001 A JP 2015517001A JP 2015517001 A JP2015517001 A JP 2015517001A JP 6132016 B2 JP6132016 B2 JP 6132016B2
- Authority
- JP
- Japan
- Prior art keywords
- group
- carbon atoms
- bis
- substituted
- charge transporting
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
- 0 CBr/I1=C/CCCC(c2ccc(*3=CC3)[s]2)SC1 Chemical compound CBr/I1=C/CCCC(c2ccc(*3=CC3)[s]2)SC1 0.000 description 2
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D519/00—Heterocyclic compounds containing more than one system of two or more relevant hetero rings condensed among themselves or condensed with a common carbocyclic ring system not provided for in groups C07D453/00 or C07D455/00
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D333/00—Heterocyclic compounds containing five-membered rings having one sulfur atom as the only ring hetero atom
- C07D333/02—Heterocyclic compounds containing five-membered rings having one sulfur atom as the only ring hetero atom not condensed with other rings
- C07D333/04—Heterocyclic compounds containing five-membered rings having one sulfur atom as the only ring hetero atom not condensed with other rings not substituted on the ring sulphur atom
- C07D333/26—Heterocyclic compounds containing five-membered rings having one sulfur atom as the only ring hetero atom not condensed with other rings not substituted on the ring sulphur atom with hetero atoms or with carbon atoms having three bonds to hetero atoms with at the most one bond to halogen, e.g. ester or nitrile radicals, directly attached to ring carbon atoms
- C07D333/30—Hetero atoms other than halogen
- C07D333/32—Oxygen atoms
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01B—CABLES; CONDUCTORS; INSULATORS; SELECTION OF MATERIALS FOR THEIR CONDUCTIVE, INSULATING OR DIELECTRIC PROPERTIES
- H01B1/00—Conductors or conductive bodies characterised by the conductive materials; Selection of materials as conductors
- H01B1/06—Conductors or conductive bodies characterised by the conductive materials; Selection of materials as conductors mainly consisting of other non-metallic substances
- H01B1/12—Conductors or conductive bodies characterised by the conductive materials; Selection of materials as conductors mainly consisting of other non-metallic substances organic substances
- H01B1/124—Intrinsically conductive polymers
- H01B1/127—Intrinsically conductive polymers comprising five-membered aromatic rings in the main chain, e.g. polypyrroles, polythiophenes
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K50/00—Organic light-emitting devices
- H10K50/10—OLEDs or polymer light-emitting diodes [PLED]
- H10K50/14—Carrier transporting layers
- H10K50/15—Hole transporting layers
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/10—Organic polymers or oligomers
- H10K85/111—Organic polymers or oligomers comprising aromatic, heteroaromatic, or aryl chains, e.g. polyaniline, polyphenylene or polyphenylene vinylene
- H10K85/113—Heteroaromatic compounds comprising sulfur or selene, e.g. polythiophene
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Physics & Mathematics (AREA)
- Spectroscopy & Molecular Physics (AREA)
- Electroluminescent Light Sources (AREA)
- Life Sciences & Earth Sciences (AREA)
- Engineering & Computer Science (AREA)
- Materials Engineering (AREA)
- Wood Science & Technology (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Heterocyclic Carbon Compounds Containing A Hetero Ring Having Oxygen Or Sulfur (AREA)
- Nitrogen And Oxygen Or Sulfur-Condensed Heterocyclic Ring Systems (AREA)
- Heterocyclic Compounds Containing Sulfur Atoms (AREA)
Description
この電荷輸送性薄膜の着色は、有機EL素子の色純度および色再現性を低下させることが知られている。
しかも、このような着色は、3色発光法、白色法および色変換法などの有機ELディスプレイにおける種々のフルカラー化技術において問題になり、有機EL素子を安定に生産する際の著しい障害になる。
このような事情から、有機EL素子の電荷輸送性薄膜は、可視領域での透過率が高く、高透明性を有することが望まれており、本発明者らは、それに鑑み、各種ウェットプロセスに適用可能であるとともに、有機EL素子の正孔注入層に適用した場合に優れたEL素子特性を実現できる透明性に優れた薄膜を与える電荷輸送性材料を開発してきている(特許文献1参照)。
なお、特許文献2には、オリゴチオフェン誘導体およびヘテロポリ酸を用いたワニスは、具体的に開示されていない。
1. 式(2)で表されるオリゴチオフェン誘導体からなる電荷輸送性物質と、ヘテロポリ酸からなるドーパント物質と、有機溶媒とを含むことを特徴とする電荷輸送性ワニス、
2. 前記R 1 およびR 2 が、互いに独立して、水素原子(ただし、R 1 およびR 2 が、同時に水素原子になる場合を除く。)、またはZ 1 で置換されていてもよい炭素数6〜20のアルキル基である、または、いずれも−OY 1 基(ただし、Y 1 は炭素数1〜20のアルキル基である。)であり、かつこれらが互いに結合したものである1の電荷輸送性ワニス、
3. 1または2の電荷輸送性ワニスを用いて作製される電荷輸送性薄膜、
4. 3の電荷輸送性薄膜を有する電子デバイス、
5. 3の電荷輸送性薄膜を有する有機エレクトロルミネッセンス素子、
6. 前記電荷輸送性薄膜が、正孔注入層または正孔輸送層である5の有機エレクトロルミネッセンス素子、
7. 1または2の電荷輸送性ワニスを基材上に塗布して焼成することを特徴とする電荷輸送性薄膜の製造方法、
8. 3の電荷輸送性薄膜を用いることを特徴とする有機エレクトロルミネッセンス素子の製造方法
を提供する。
本発明の電荷輸送性ワニスを用いることで、高い透明性および導電性を備えた電荷輸送性薄膜が得られ、この薄膜を、特に有機EL素子の正孔注入層に適用することで、高い発光効率を有し、かつ、耐久性に優れた有機EL素子を得ることができる。
また、本発明の電荷輸送性ワニスは、スピンコート法やスリットコート法など、大面積に成膜可能な各種ウェットプロセスを用いた場合でも電荷輸送性に優れた薄膜を再現性よく製造できるため、近年の有機EL素子の分野における進展にも十分対応できる。
さらに、本発明の電荷輸送性ワニスから得られる薄膜は、帯電防止膜や有機薄膜太陽電池の陽極バッファ層等としても使用できる。
本発明に係る電荷輸送性ワニスは、式(1)で表されるオリゴチオフェン誘導体からなる電荷輸送性物質と、ヘテロポリ酸からなるドーパント物質と、有機溶媒とを含む。
ここで、電荷輸送性とは、導電性と同義であり、正孔輸送性と同義である。電荷輸送性物質は、それ自体に電荷輸送性があるものでもよく、電子受容性物質と共に用いた際に電荷輸送性があるものでもよい。電荷輸送性ワニスは、それ自体に電荷輸送性があるものでもよく、それにより得られる固形膜が電荷輸送性を有するものでもよい。
また、オリゴチオフェン誘導体の有機溶媒への溶解性を向上させる観点から、n1〜n3は、好ましくはn1+n2+n3≦8、より好ましくはn1+n2+n3≦7、より一層好ましくはn1+n2+n3≦6、さらに好ましくはn1+n2+n3≦5を満たす。
すなわち、本発明で用いるオリゴチオフェン誘導体は、具体的には、例えば、下記スキーム1および2によって、合成することができ、また、特に、両末端に、アルキル基、アルケニル基、アルキニル基、アリール基またはヘテロアリール基を有するオリゴチオフェン誘導体(式(1’))は、下記スキーム3によって、合成することもできる。
擬ハロゲン基としては、メタンスルホニルオキシ基、トリフルオロメタンスルホニルオキシ基、ノナフルオロブタンスルホニルオキシ基等の(フルオロ)アルキルスルホニルオキシ基;ベンゼンスルホニルオキシ基、トルエンスルホニルオキシ基等の芳香族スルホニルオキシ基などが挙げられる。
スキーム2において、式(6)〜(8)で表されるチオフェン誘導体の仕込みは、通常、式(7)で表されるチオフェン誘導体に対し、式(6)で表されるチオフェン誘導体、式(8)で表されるチオフェン誘導体それぞれ0.5〜1.5当量程度であるが、0.9〜1.3当量程度が好適である。
スキーム3において、式(9)で表されるチオフェン誘導体および式(10)〜(11)で表される化合物の仕込みは、通常、式(9)で表されるチオフェン誘導体に対し、式(10)で表される化合物、式(11)で表される化合物それぞれ0.5〜1.5当量程度であるが、0.9〜1.3当量程度が好適である。
また、配位子が同時に使用される場合の配位子の使用量は、使用する金属錯体に対し、0.1〜5当量程度でよいが、1〜4当量程度が好適である。
反応終了後は、常法に従って後処理をして、式(1)または(1’)で表されるオリゴチオフェン誘導体を得ることができる。
一方、式(3)、(5)、(7)、(10)および(11)で表される化合物は、市販品を用いることもできるし、一般的に用いられる手法に従い、各化合物に対応する構造を有する、チオフェン、アルカン、アルケン、アルキン、アレーンまたはチオフェン以外のヘテロアレーンをハロゲン化または擬ハロゲン化することで得ることができる。
なお、式中、「Me」はメチル基を、「Et」はエチル基を、「n−Pr」はn−プロピル基を、「i−Pr」はi−プロピル基を、「n−Bu」はn−ブチル基を、「i−Bu」はイソブチル基を、「s−Bu」はs−ブチル基を、「t−Bu」はt−ブチル基を、「n−Pen」はn−ペンチル基を、「n−Hex」はn−ヘキシル基を、「n−Hep」はn−ヘプチル基を、「n−Oct」はn−オクチル基を、「Ph」はフェニル基を、「Ar1」は4−(ジフェニルアミノ)フェニル基を、それぞれ示す。
すなわち、例えば、一般的には、リンタングステン酸は化学式H3(PW12O40)・nH2Oで、リンモリブデン酸は化学式H3(PMo12O40)・nH2Oでそれぞれ示されるが、定量分析において、この式中のP(リン)、O(酸素)またはW(タングステン)もしくはMo(モリブデン)の数が多く、または少ないものであっても、それが市販品として入手したもの、あるいは、公知の合成方法に従い適切に合成したものである限り、本発明において用いることができる。この場合、本発明に規定されるヘテロポリ酸の質量とは、合成物や市販品中における純粋なリンタングステン酸の質量(リンタングステン酸含量)ではなく、市販品として入手可能な形態および公知の合成法にて単離可能な形態において、水和水やその他の不純物等を含んだ状態での全質量を意味する。
その他の電荷輸送性物として好適に用い得るアニリン誘導体としては、例えば、式(12)で表されるものが挙げられる。
とりわけ、その他のドーパント物質としては、アリールスルホン酸化合物が好ましく、有機溶媒への溶解性を考慮すると、その分子量は、好ましく3000以下、より好ましくは2000以下、より一層好ましくは1000以下である。
A2は、ナフタレン環またはアントラセン環を表すが、ナフタレン環が好ましい。
A3は、2〜4価のパーフルオロビフェニル基を表し、lは、A1とA3との結合数を示し、2≦l≦4を満たす整数であるが、A3が2価のパーフルオロビフェニル基であり、かつ、lが2であることが好ましい。
mは、A2に結合するスルホン酸基数を表し、1≦m≦4を満たす整数であるが、2が最適である。
kは、ナフタレン環に結合するスルホン酸基数を表し、1≦k≦4を満たす整数であるが、2〜4が好ましく、2が最適である。
その他、ハロゲン原子、炭素数1〜20のアルキル基の例としては上記と同様のものが挙げられるが、ハロゲン原子としては、フッ素原子が好ましい。
なお、パーフルオロアルキル基とは、アルキル基の水素原子全てがフッ素原子に置換された基であり、パーフルオロアルケニル基とは、アルケニル基の水素原子全てがフッ素原子に置換された基である。
このような高溶解性溶媒としては、例えば、N,N−ジメチルホルムアミド、N,N−ジメチルアセトアミド、N−メチルピロリドン、1,3−ジメチル−2−イミダゾリジノン、ジエチレングリコールモノメチルエーテル、プロピレングリコールモノメチルエーテル等の有機溶媒を用いることができる。これらの溶媒は1種単独で、または2種以上混合して用いることができ、その使用量は、ワニスに使用する溶媒全体に対して5〜100質量%とすることができる。
なお、電荷輸送性物質およびドーパント物質は、いずれも上記溶媒に完全に溶解しているか、均一に分散している状態となっていることが好ましく、完全に溶解していることがより好ましい。
高粘度有機溶媒としては、特に限定されるものではなく、例えば、シクロヘキサノール、エチレングリコール、エチレングリコールジクリシジルエーテル、1,3−オクチレングリコール、ジエチレングリコール、ジプロピレングリコール、トリエチレングリコール、トリプロピレングリコール、1,3−ブタンジオール、2,3−ブタンジオール、1,4−ブタンジオール、プロピレングリコール、へキシレングリコール等が挙げられる。これらの溶媒は単独で用いてもよく、2種以上混合して用いてもよい。
本発明のワニスに用いられる溶媒全体に対する高粘度有機溶媒の添加割合は、固体が析出しない範囲内であることが好ましく、固体が析出しない限りにおいて、添加割合は、5〜80質量%が好ましい。
このような溶媒としては、例えば、エチレングリコールモノブチルエーテル、ジエチレングリコールジエチルエーテル、ジエチレングリコールジメチルエーテル、ジエチレングリコールモノエチルエーテルアセテート、ジエチレングリコールモノブチルエーテルアセテート、ジプロピレングリコールモノメチルエーテル、プロピレングリコールモノメチルエーテルアセテート、ジエチレングリコールモノエチルエーテル、ジアセトンアルコール、γ−ブチロラクトン、エチルラクテート、n−ヘキシルアセテート等が挙げられるが、これらに限定されるものではない。これらの溶媒は1種単独で、または2種以上混合して用いることができる。
また、本発明における電荷輸送性ワニスの固形分濃度は、ワニスの粘度および表面張力等や、作製する薄膜の厚み等を勘案して適宜設定されるものではあるが、通常、0.1〜10.0質量%程度であり、ワニスの塗布性を向上させることを考慮すると、好ましくは0.5〜5.0質量%、より好ましくは1.0〜3.0質量%である。
ワニスの塗布方法としては、特に限定されるものではなく、ディップ法、スピンコート法、転写印刷法、ロールコート法、刷毛塗り、インクジェット法、スプレー法等が挙げられ、塗布方法に応じてワニスの粘度および表面張力を調節することが好ましい。
なお、焼成の際、より高い均一成膜性を発現させたり、基材上で反応を進行させたりする目的で、2段階以上の温度変化をつけてもよく、加熱は、例えば、ホットプレートやオーブン等、適当な機器を用いて行えばよい。
使用する電極基板は、洗剤、アルコール、純水等による液体洗浄を予め行って浄化しておくことが好ましく、例えば、陽極基板では使用直前にUVオゾン処理、酸素−プラズマ処理等の表面処理を行うことが好ましい。ただし陽極材料が有機物を主成分とする場合、表面処理を行わなくともよい。
上記の方法により、陽極基板上に本発明の電荷輸送性ワニスを塗布して焼成し、電極上に正孔注入層を作製する。これを真空蒸着装置内に導入し、正孔輸送層、発光層、電子輸送層/ホールブロック層、電子注入層、陰極金属を順次蒸着してOLED素子とする。なお、必要に応じて、発光層と正孔輸送層との間に電子ブロック層を設けてよい。
なお、金属陽極を構成するその他の金属としては、例えば、スカンジウム、チタン、バナジウム、クロム、マンガン、鉄、コバルト、ニッケル、銅、亜鉛、ガリウム、イットリウム、ジルコニウム、ニオブ、モリブデン、ルテニウム、ロジウム、パラジウム、カドニウム、インジウム、スカンジウム、ランタン、セリウム、プラセオジム、ネオジム、プロメチウム、サマリウム、ユウロピウム、ガドリニウム、テルビウム、ジスプロシウム、ホルミウム、エルビウム、ツリウム、イッテルビウム、ハフニウム、タリウム、タングステン、レニウム、オスミウム、イリジウム、プラチナ、金、チタン、鉛、ビスマスやそれらの合金等が挙げられる。
陰極材料としては、アルミニウム、マグネシウム−銀合金、アルミニウム−リチウム合金、リチウム、ナトリウム、カリウム、セシウム等が挙げられる。
電子ブロック層を形成する材料としては、トリス(フェニルピラゾール)イリジウム等が挙げられる。
上記OLED素子作製において、正孔輸送層、発光層、電子輸送層、電子注入層の真空蒸着操作を行う代わりに、正孔輸送性高分子層、発光性高分子層を順次形成することによって本発明の電荷輸送性ワニスによって形成される電荷輸送性薄膜を有するPLED素子を作製することができる。
具体的には、陽極基板上に本発明の電荷輸送性ワニスを塗布して上記の方法により正孔注入層を作製し、その上に正孔輸送性高分子層、発光性高分子層を順次形成し、さらに陰極電極を蒸着してPLED素子とする。
正孔輸送性高分子層および発光性高分子層の形成法としては、正孔輸送性高分子材料もしくは発光性高分子材料、またはこれらにドーパント物質を加えた材料に溶媒を加えて溶解するか、均一に分散し、正孔注入層または正孔輸送性高分子層の上に塗布した後、それぞれ焼成することで成膜する方法が挙げられる。
塗布方法としては、特に限定されるものではなく、インクジェット法、スプレー法、ディップ法、スピンコート法、転写印刷法、ロールコート法、刷毛塗り等が挙げられる。なお、塗布は、窒素、アルゴン等の不活性ガス下で行うことが好ましい。
焼成する方法としては、不活性ガス下または真空中、オーブンまたはホットプレートで加熱する方法が挙げられる。
(1)基板洗浄:長州産業(株)製 基板洗浄装置(減圧プラズマ方式)
(2)ワニスの塗布:ミカサ(株)製 スピンコーターMS−A100
(3)膜厚測定:(株)小坂研究所製 微細形状測定機サーフコーダET−4000
(4)透過率測定:(株)島津製作所社製 可視紫外線吸収スペクトル測定装置UV−3100PC
(5)EL素子の作製:長州産業(株)製 多機能蒸着装置システムC−E2L1G1−N
(6)EL素子の輝度等の測定:(有)テック・ワールド製 I−V−L測定システム
(7)EL素子の寿命測定(半減期等の測定および予想半減期の見積):(株)イーエッチシー製 有機EL輝度寿命評価システムPEL−105S
撹拌後、イオン交換水およびノルマルヘキサンを加え分液し、得られた有機層を更にイオン交換水で2回洗浄した後、硫酸ナトリウムを用いて乾燥した。
そして、溶媒を留去して3,3’’’−ジヘキシル−[2,2’:5’,2’’:5’’,2’’’−クウォーターチオフェン]−5,5’’’−ジイル)ビス(トリブチルスタナン)を含む混合物(1.7g)を得た。
次に、別のフラスコ内に、この得られた混合物1.48gと2−ブロモ−3−ヘキシルチオフェン0.46gを入れて窒素置換した後、トルエン15mL、テトラキス(トリフェニルホスフィン)パラジウム0.05gを順次入れて、還流条件下で4時間撹拌した。
撹拌後、室温まで放冷し、そこへノルマルヘキサン 、トルエンおよびイオン交換水を加えて分液し、得られた有機層を更にイオン交換水で洗浄し、硫酸ナトリウムを用いて乾燥した。
そして、溶媒を留去し、カラムクロマトグラフィーにて精製し、オリゴチオフェン誘導体2を得た(収量:0.38g、収率:53% 2段階通算収率)。
1H−NMR(CDCl3):δ7.16−7.13(m,4H),7.04(d,J=3.9Hz,2H),6.94(s,4H),6.92(d,J=5.4Hz,2H),2.78(m,8H),1.74−1.58(m,8H),1.44−1.31(m,24H),0.95−0.87(m,12H).
そして、フラスコ内に、5,5’−ジブロモ−2,2’−ビチオフェン1.5gとテトラキス(トリフェニルホスフィイン)パラジウム0.27gを入れて窒素置換した後、N,N−ジメチルホルムアミド20mLおよび予め合成したトリブチル(2,3−ジヒドロチエノ[3,4−b][1,4]ジオキシン−5−イル)スタナン6.2gを加え、125℃に昇温し2時間撹拌した。
撹拌後、室温まで放冷し、そこへノルマルヘキサンを加え分液し、得られたN,N−ジメチルホルムアミド層をイオン交換水とメタノールの混合液中に滴下して再沈殿を行った。
そして、沈殿物をろ過によって回収して乾燥し、オリゴチオフェン誘導体3を得た(収量:1.4g、収率:66%)。
1H−NMR(CDCl3):δ7.11(d,J=4.2Hz,2H),7.07(d,J=4.2Hz,2H),6.23(s,2H),4.37−4.33(m,4H),4.28−4.24(m,4H).
撹拌後、イオン交換水およびノルマルヘキサンを加え分液し、得られた有機層を更にイオン交換水で2回洗浄した後、硫酸ナトリウムを用いて乾燥した。
そして、溶媒を留去して(3,3’’’−ジヘキシル−[2,2’:5’,2’’:5’’,2’’’−クウォーターチオフェン]−5,5’’’−ジイル)ビス(トリブチルスタナン)を含む混合物(3.45g)を得た。
次に、別のフラスコ内に、この得られた混合物3.0gと4−ブロモ−N,N−ジフェニルアニリン1.2gを入れて窒素置換した後、トルエン45mL、テトラキス(トリフェニルホスフィン)パラジウム0.10gを順次加え、還流条件下で8時間撹拌した。
撹拌後、室温まで放冷し、そこへクロロホルムおよびイオン交換水を加えて分液し、得られた有機層を更にイオン交換水で洗浄し、硫酸ナトリウムを用いて乾燥した。
そして、溶媒を留去し、カラムクロマトグラフィーにて精製し、オリゴチオフェン誘導体4を得た(収量:0.76g,収率:44% 2段階通算収率)。
1H−NMR(CDCl3):δ7.44(4H,d,J=8.9Hz),7.28−7.23(m,8H),7.12−7.10(m,10H),7.06−7.00(m,12H),2.78(t,J=7.4Hz,4H),1.69(quint,J=7.4Hz,4H),1.44−1.30(m,12H),0.89(m,6H).
その後、再び−78℃に冷却して30分間撹拌した後、トリブチルクロロスタナン8.8mLを滴下して10分撹拌し、次いで0℃に昇温してさらに30分間撹拌した。
撹拌後、反応混合物から減圧下で溶媒を留去し、得られた残渣をトルエンに加え、ろ過によって不溶物を除去し、得られたろ液から減圧下で溶媒を留去し、ターチオフェンのビススタニル体を含むオイル状物12.88g(当該ビススタニル体の純度51.91%)得た。
次いで、窒素雰囲気下で、別のフラスコ内に、このターチオフェンビススタニル体を含むオイル状物6.44g、2−ブロモ−3−ノルマルヘキシルチオフェン2.41g、トルエン24mLおよびテトラキス(トリフェニルホスフィン)パラジウム0.23gを順次入れて、還流条件下4.5時間撹拌した。
室温まで放冷し、溶媒を減圧留去した後、ろ過にて不溶物を除去した。得られたろ液を濃縮し、シリカゲルカラムクロマトグラフィーにて精製し、オリゴチオフェン誘導体5を得た(収量:1.29g、収率:55%、2段階通算収率)。
1H−NMR(CDCl3):7.17(d,J=5.1Hz,2H),7.12(d,J=3.9Hz,2H),7.09(s,2H),7.01(d,J=3.9Hz,2H),6.93(d,J=5.1Hz,2H),2.78(t,J=7.7Hz,4H),1.54−1.70(m,4H),1.28−1.41(m,12H),0.89(t,J=7.0Hz,6H).
[実施例1−1]
式(a−10)で表されるオリゴチオフェン誘導体(Sigma−Aldrich Co.LLC.製)(以下、TP1ともいう。)0.124gと、リンタングステン酸(関東化学(株)製)0.247gとを、窒素雰囲気下で1,3−ジメチル−2−イミダゾリジノン4.0gに溶解させた。得られた溶液に、シクロヘキサノール6.0gおよびプロピレングリコール2.0gを加えて撹拌し、電荷輸送性ワニスを調製した。
TP1の使用量およびリンタングステン酸の使用量を、それぞれ、0.093gおよび0.278g(実施例1−2)、0.074gおよび0.297g(実施例1−3)、0.062gおよび0.309g(実施例1−4)、0.053gおよび0.318g(実施例1−5)とした以外は、実施例1−1と同様の方法で電荷輸送性ワニスを調製した。
TP1 0.124gの代わりにTP3 0.062gを用い、リンタングステン酸の使用量を0.309gとした以外は、実施例1−1と同様の方法で電荷輸送性ワニスを調製した。
TP3の使用量およびリンタングステン酸の使用量を、それぞれ0.034gおよび0.337g(実施例1−7)、0.018gおよび0.353g(実施例1−8)とした以外は、実施例1−6と同様の方法で電荷輸送性ワニスを調製した。
TP5 0.116gと、リンタングステン酸0.348gとを、窒素雰囲気下で1,3−ジメチル−2−イミダゾリジノン10.5gに溶解させた。得られた溶液に2,3−ブタンジオール3g、プロピレングリコールモノメチルエーテル1.5gを順次加えて撹拌し、電荷輸送性ワニスを調製した。
[実施例2−1〜2−5]
実施例1−1〜1−5で得られたワニスを、スピンコーターを用いて石英基板に塗布した後、大気中、50℃で5分間乾燥し、さらに230℃で15分間焼成し、石英基板上に膜厚30nmの均一な薄膜を形成した。そして、形成した薄膜の透過率を測定した。透過率は可視領域である波長400〜800nmをスキャンした。400〜800nmの平均透過率を表1に示す。
なお、石英基板は、プラズマ洗浄装置(150W、30秒間)を用いて表面上の不純物を除却してから使用した。
[実施例3−1]
実施例1−1で得られたワニスを、スピンコーターを用いてITO基板に塗布した後、50℃で5分間乾燥し、さらに、大気雰囲気下、230℃で10分間焼成し、ITO基板上に30nmの均一な薄膜を形成した。ITO基板としては、インジウム錫酸化物(ITO)が表面上に膜厚150nmでパターニングされた25mm×25mm×0.7tのガラス基板を用い、使用前にO2プラズマ洗浄装置(150W、30秒間)によって表面上の不純物を除却した。
次いで、薄膜を形成したITO基板に対し、蒸着装置(真空度1.0×10-5Pa)を用いてα−NPD、Alq3、フッ化リチウム、およびアルミニウムの薄膜を順次積層し、有機EL素子を得た。この際、蒸着レートは、α−NPD,Alq3およびアルミニウムについては0.2nm/秒、フッ化リチウムについては0.02nm/秒の条件でそれぞれ行い、膜厚は、それぞれ30nm、40nm、0.5nmおよび120nmとした。
なお、空気中の酸素、水等の影響による特性劣化を防止するため、有機EL素子は封止基板により封止した後、その特性を評価した。封止は、以下の手順で行った。
酸素濃度2ppm以下、露点−85℃以下の窒素雰囲気中で、有機EL素子を封止基板の間に収め、封止基板を接着材(ナガセケムテックス(株)製,XNR5516Z−B1)により貼り合わせた。この際、捕水剤(ダイニック(株)製,HD−071010W−40)を有機EL素子と共に封止基板内に収めた。貼り合わせた封止基板に対し、UV光を照射(波長:365nm、照射量:6000mJ/cm2)した後、80℃で1時間、アニーリング処理して接着材を硬化させた。
実施例1−1で得られたワニスの代わりに、それぞれ、実施例1−2〜1−9で得られたワニスを用いた以外は、実施例3−1と同様の方法で有機EL素子を作製した。
実施例1−1で得られたワニスの代わりにPEDOT/PSS(H.C.Starck社製AI4083)を用いた以外は、実施例3−1と同様の方法で素子を作製した。
Claims (8)
- 式(2)で表されるオリゴチオフェン誘導体からなる電荷輸送性物質と、ヘテロポリ酸からなるドーパント物質と、有機溶媒とを含むことを特徴とする電荷輸送性ワニス。
Y1〜Y6は、互いに独立して、Z1で置換されていてもよい炭素数1〜20のアルキル基、Z1で置換されていてもよい炭素数2〜20のアルケニル基、Z1で置換されていてもよい炭素数2〜20のアルキニル基、Z2で置換されていてもよい炭素数6〜20のアリール基、またはZ2で置換されていてもよい炭素数2〜20のヘテロアリール基を表し、
Z1は、炭素数6〜20のアリール基または炭素数2〜20のヘテロアリール基を表し、
Z2は、炭素数1〜20のアルキル基、炭素数2〜20のアルケニル基または炭素数2〜20のアルキニル基を表し、
n1〜n3は、互いに独立して、自然数を示し、かつ、4≦n1+n2+n3≦20を満たす。〕 - 前記R 1 およびR 2 が、互いに独立して、水素原子(ただし、R 1 およびR 2 が、同時に水素原子になる場合を除く。)、またはZ 1 で置換されていてもよい炭素数6〜20のアルキル基である、または、いずれも−OY 1 基(ただし、Y 1 は炭素数1〜20のアルキル基である。)であり、かつこれらが互いに結合したものである請求項1記載の電荷輸送性ワニス。
- 請求項1または2記載の電荷輸送性ワニスを用いて作製される電荷輸送性薄膜。
- 請求項3記載の電荷輸送性薄膜を有する電子デバイス。
- 請求項3記載の電荷輸送性薄膜を有する有機エレクトロルミネッセンス素子。
- 前記電荷輸送性薄膜が、正孔注入層または正孔輸送層である請求項5記載の有機エレクトロルミネッセンス素子。
- 請求項1または2記載の電荷輸送性ワニスを基材上に塗布して焼成することを特徴とする電荷輸送性薄膜の製造方法。
- 請求項3記載の電荷輸送性薄膜を用いることを特徴とする有機エレクトロルミネッセンス素子の製造方法。
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2013104776 | 2013-05-17 | ||
| JP2013104776 | 2013-05-17 | ||
| PCT/JP2014/060823 WO2014185208A1 (ja) | 2013-05-17 | 2014-04-16 | 電荷輸送性ワニス |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JPWO2014185208A1 JPWO2014185208A1 (ja) | 2017-02-23 |
| JP6132016B2 true JP6132016B2 (ja) | 2017-05-24 |
Family
ID=51898189
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2015517001A Active JP6132016B2 (ja) | 2013-05-17 | 2014-04-16 | 電荷輸送性ワニス |
Country Status (5)
| Country | Link |
|---|---|
| JP (1) | JP6132016B2 (ja) |
| KR (1) | KR102219003B1 (ja) |
| CN (1) | CN105210207A (ja) |
| TW (1) | TWI650385B (ja) |
| WO (1) | WO2014185208A1 (ja) |
Family Cites Families (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2008112904A (ja) * | 2006-10-31 | 2008-05-15 | Idemitsu Kosan Co Ltd | 有機エレクトロルミネッセンス素子 |
| JP2008306170A (ja) | 2007-05-09 | 2008-12-18 | Toray Ind Inc | 発光素子 |
| JP5617640B2 (ja) * | 2008-11-19 | 2014-11-05 | 日産化学工業株式会社 | 正孔または電子輸送性薄膜形成用ワニス |
| JP5488473B2 (ja) * | 2008-11-19 | 2014-05-14 | 日産化学工業株式会社 | 電荷輸送性ワニス |
| WO2013042623A1 (ja) * | 2011-09-21 | 2013-03-28 | 日産化学工業株式会社 | 電荷輸送性ワニス |
-
2014
- 2014-04-16 WO PCT/JP2014/060823 patent/WO2014185208A1/ja active Application Filing
- 2014-04-16 CN CN201480028599.8A patent/CN105210207A/zh active Pending
- 2014-04-16 TW TW103113865A patent/TWI650385B/zh active
- 2014-04-16 JP JP2015517001A patent/JP6132016B2/ja active Active
- 2014-04-16 KR KR1020157034504A patent/KR102219003B1/ko active IP Right Grant
Also Published As
| Publication number | Publication date |
|---|---|
| KR102219003B1 (ko) | 2021-02-23 |
| WO2014185208A1 (ja) | 2014-11-20 |
| CN105210207A (zh) | 2015-12-30 |
| TWI650385B (zh) | 2019-02-11 |
| JPWO2014185208A1 (ja) | 2017-02-23 |
| KR20160010488A (ko) | 2016-01-27 |
| TW201506098A (zh) | 2015-02-16 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP6414213B2 (ja) | 有機エレクトロルミネッセンス素子の正孔注入層形成用ワニス | |
| JP6597597B2 (ja) | アニリン誘導体およびその利用 | |
| JP6459350B2 (ja) | 電荷輸送性ワニス、電荷輸送性薄膜及び有機エレクトロルミネッセンス素子 | |
| WO2016190326A1 (ja) | 電荷輸送性ワニス及び有機エレクトロルミネッセンス素子 | |
| JP2019135774A (ja) | 正孔注入層形成用電荷輸送性ワニス | |
| JP6760455B2 (ja) | アニリン誘導体およびその製造方法 | |
| JP6601390B2 (ja) | アニリン誘導体およびその利用 | |
| JPWO2017164158A1 (ja) | アリールアミン誘導体とその利用 | |
| JP6011723B2 (ja) | トリフェニルアミン誘導体およびその利用 | |
| JP6551693B2 (ja) | 電荷輸送性ワニス、電荷輸送性薄膜及びその製造方法、並びに有機エレクトロルミネッセンス素子及びその製造方法 | |
| JP6061034B2 (ja) | アニリン誘導体、電荷輸送性ワニス及び有機エレクトロルミネッセンス素子 | |
| WO2016204079A1 (ja) | 電荷輸送性ワニス及び有機エレクトロルミネッセンス素子 | |
| JPWO2015137391A1 (ja) | アニリン誘導体およびその利用 | |
| JP2015092559A (ja) | 電荷輸送性ワニス、電荷輸送性薄膜及び有機エレクトロルミネッセンス素子 | |
| JP6558373B2 (ja) | 電荷輸送性ワニス | |
| JP6132016B2 (ja) | 電荷輸送性ワニス | |
| JP6601405B2 (ja) | 電荷輸送性ワニス | |
| JPWO2016006673A1 (ja) | 電荷輸送性ワニス |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20170321 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20170403 |
|
| R151 | Written notification of patent or utility model registration |
Ref document number: 6132016 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R151 |
|
| S531 | Written request for registration of change of domicile |
Free format text: JAPANESE INTERMEDIATE CODE: R313531 |
|
| S533 | Written request for registration of change of name |
Free format text: JAPANESE INTERMEDIATE CODE: R313533 |
|
| R350 | Written notification of registration of transfer |
Free format text: JAPANESE INTERMEDIATE CODE: R350 |