JP5951618B2 - 気相水素化からアニリンを精製するための方法 - Google Patents
気相水素化からアニリンを精製するための方法 Download PDFInfo
- Publication number
- JP5951618B2 JP5951618B2 JP2013534280A JP2013534280A JP5951618B2 JP 5951618 B2 JP5951618 B2 JP 5951618B2 JP 2013534280 A JP2013534280 A JP 2013534280A JP 2013534280 A JP2013534280 A JP 2013534280A JP 5951618 B2 JP5951618 B2 JP 5951618B2
- Authority
- JP
- Japan
- Prior art keywords
- stream
- aniline
- phase
- water
- aqueous
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
- PAYRUJLWNCNPSJ-UHFFFAOYSA-N Aniline Chemical compound NC1=CC=CC=C1 PAYRUJLWNCNPSJ-UHFFFAOYSA-N 0.000 title claims description 182
- 238000000034 method Methods 0.000 title claims description 119
- 238000005984 hydrogenation reaction Methods 0.000 title claims description 10
- 239000000047 product Substances 0.000 claims description 98
- 238000004821 distillation Methods 0.000 claims description 65
- 239000012071 phase Substances 0.000 claims description 36
- 239000012074 organic phase Substances 0.000 claims description 33
- 239000008346 aqueous phase Substances 0.000 claims description 31
- 238000009833 condensation Methods 0.000 claims description 26
- 230000005494 condensation Effects 0.000 claims description 26
- 238000005191 phase separation Methods 0.000 claims description 26
- LQNUZADURLCDLV-UHFFFAOYSA-N nitrobenzene Chemical compound [O-][N+](=O)C1=CC=CC=C1 LQNUZADURLCDLV-UHFFFAOYSA-N 0.000 claims description 24
- 238000002156 mixing Methods 0.000 claims description 19
- 230000015572 biosynthetic process Effects 0.000 claims description 15
- 239000012535 impurity Substances 0.000 claims description 9
- 239000007795 chemical reaction product Substances 0.000 claims description 8
- 238000000746 purification Methods 0.000 claims description 7
- 230000002378 acidificating effect Effects 0.000 claims description 5
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 66
- 239000002585 base Substances 0.000 description 56
- 239000007789 gas Substances 0.000 description 41
- 239000000243 solution Substances 0.000 description 28
- HEMHJVSKTPXQMS-UHFFFAOYSA-M Sodium hydroxide Chemical compound [OH-].[Na+] HEMHJVSKTPXQMS-UHFFFAOYSA-M 0.000 description 21
- 239000007788 liquid Substances 0.000 description 19
- 150000001875 compounds Chemical class 0.000 description 14
- ISWSIDIOOBJBQZ-UHFFFAOYSA-N Phenol Chemical compound OC1=CC=CC=C1 ISWSIDIOOBJBQZ-UHFFFAOYSA-N 0.000 description 10
- 238000004519 manufacturing process Methods 0.000 description 8
- 239000000203 mixture Substances 0.000 description 8
- 238000005406 washing Methods 0.000 description 8
- 150000003839 salts Chemical class 0.000 description 7
- 238000004088 simulation Methods 0.000 description 7
- 150000008044 alkali metal hydroxides Chemical class 0.000 description 5
- 238000009835 boiling Methods 0.000 description 5
- 238000000926 separation method Methods 0.000 description 5
- QGZKDVFQNNGYKY-UHFFFAOYSA-N Ammonia Chemical compound N QGZKDVFQNNGYKY-UHFFFAOYSA-N 0.000 description 4
- 241000183024 Populus tremula Species 0.000 description 4
- CYGKLLHTPPFPHH-UHFFFAOYSA-N aniline;hydrate Chemical compound O.NC1=CC=CC=C1 CYGKLLHTPPFPHH-UHFFFAOYSA-N 0.000 description 4
- 238000006243 chemical reaction Methods 0.000 description 4
- 238000002485 combustion reaction Methods 0.000 description 4
- 230000000052 comparative effect Effects 0.000 description 4
- DMBHHRLKUKUOEG-UHFFFAOYSA-N diphenylamine Chemical compound C=1C=CC=CC=1NC1=CC=CC=C1 DMBHHRLKUKUOEG-UHFFFAOYSA-N 0.000 description 4
- 238000005265 energy consumption Methods 0.000 description 4
- 230000008929 regeneration Effects 0.000 description 4
- 238000011069 regeneration method Methods 0.000 description 4
- UHOVQNZJYSORNB-UHFFFAOYSA-N Benzene Chemical compound C1=CC=CC=C1 UHOVQNZJYSORNB-UHFFFAOYSA-N 0.000 description 3
- UFHFLCQGNIYNRP-UHFFFAOYSA-N Hydrogen Chemical compound [H][H] UFHFLCQGNIYNRP-UHFFFAOYSA-N 0.000 description 3
- 150000004982 aromatic amines Chemical class 0.000 description 3
- 239000006227 byproduct Substances 0.000 description 3
- 239000001257 hydrogen Substances 0.000 description 3
- 229910052739 hydrogen Inorganic materials 0.000 description 3
- 239000007791 liquid phase Substances 0.000 description 3
- 150000004707 phenolate Chemical class 0.000 description 3
- 239000002351 wastewater Substances 0.000 description 3
- 238000004065 wastewater treatment Methods 0.000 description 3
- IJGRMHOSHXDMSA-UHFFFAOYSA-N Atomic nitrogen Chemical compound N#N IJGRMHOSHXDMSA-UHFFFAOYSA-N 0.000 description 2
- 239000003513 alkali Substances 0.000 description 2
- 229910001860 alkaline earth metal hydroxide Inorganic materials 0.000 description 2
- 229910021529 ammonia Inorganic materials 0.000 description 2
- 238000004458 analytical method Methods 0.000 description 2
- 239000007864 aqueous solution Substances 0.000 description 2
- 239000003054 catalyst Substances 0.000 description 2
- 239000012043 crude product Substances 0.000 description 2
- 238000006481 deamination reaction Methods 0.000 description 2
- 238000001035 drying Methods 0.000 description 2
- 238000001704 evaporation Methods 0.000 description 2
- 238000000605 extraction Methods 0.000 description 2
- XLYOFNOQVPJJNP-UHFFFAOYSA-M hydroxide Chemical compound [OH-] XLYOFNOQVPJJNP-UHFFFAOYSA-M 0.000 description 2
- 125000002887 hydroxy group Chemical group [H]O* 0.000 description 2
- 239000011261 inert gas Substances 0.000 description 2
- 239000000543 intermediate Substances 0.000 description 2
- 239000000463 material Substances 0.000 description 2
- VNWKTOKETHGBQD-UHFFFAOYSA-N methane Chemical compound C VNWKTOKETHGBQD-UHFFFAOYSA-N 0.000 description 2
- 230000007935 neutral effect Effects 0.000 description 2
- ISWSIDIOOBJBQZ-UHFFFAOYSA-M phenolate Chemical compound [O-]C1=CC=CC=C1 ISWSIDIOOBJBQZ-UHFFFAOYSA-M 0.000 description 2
- 229940031826 phenolate Drugs 0.000 description 2
- 238000001556 precipitation Methods 0.000 description 2
- 230000008646 thermal stress Effects 0.000 description 2
- 238000011144 upstream manufacturing Methods 0.000 description 2
- CDAWCLOXVUBKRW-UHFFFAOYSA-N 2-aminophenol Chemical class NC1=CC=CC=C1O CDAWCLOXVUBKRW-UHFFFAOYSA-N 0.000 description 1
- OKTJSMMVPCPJKN-UHFFFAOYSA-N Carbon Chemical compound [C] OKTJSMMVPCPJKN-UHFFFAOYSA-N 0.000 description 1
- CURLTUGMZLYLDI-UHFFFAOYSA-N Carbon dioxide Chemical compound O=C=O CURLTUGMZLYLDI-UHFFFAOYSA-N 0.000 description 1
- 230000004931 aggregating effect Effects 0.000 description 1
- 229910001854 alkali hydroxide Inorganic materials 0.000 description 1
- 229910000272 alkali metal oxide Inorganic materials 0.000 description 1
- 150000001340 alkali metals Chemical class 0.000 description 1
- 239000012223 aqueous fraction Substances 0.000 description 1
- -1 aromatic nitro compound Chemical class 0.000 description 1
- 125000003118 aryl group Chemical group 0.000 description 1
- 230000009286 beneficial effect Effects 0.000 description 1
- 229910052799 carbon Inorganic materials 0.000 description 1
- 229910002090 carbon oxide Inorganic materials 0.000 description 1
- BVKZGUZCCUSVTD-UHFFFAOYSA-N carbonic acid Chemical class OC(O)=O BVKZGUZCCUSVTD-UHFFFAOYSA-N 0.000 description 1
- 150000004649 carbonic acid derivatives Chemical class 0.000 description 1
- 238000009903 catalytic hydrogenation reaction Methods 0.000 description 1
- 238000011109 contamination Methods 0.000 description 1
- 230000018044 dehydration Effects 0.000 description 1
- 238000006297 dehydration reaction Methods 0.000 description 1
- CZZYITDELCSZES-UHFFFAOYSA-N diphenylmethane Chemical class C=1C=CC=CC=1CC1=CC=CC=C1 CZZYITDELCSZES-UHFFFAOYSA-N 0.000 description 1
- 230000000694 effects Effects 0.000 description 1
- 238000005516 engineering process Methods 0.000 description 1
- 238000004817 gas chromatography Methods 0.000 description 1
- 238000006386 neutralization reaction Methods 0.000 description 1
- 229910052757 nitrogen Inorganic materials 0.000 description 1
- TWNQGVIAIRXVLR-UHFFFAOYSA-N oxo(oxoalumanyloxy)alumane Chemical compound O=[Al]O[Al]=O TWNQGVIAIRXVLR-UHFFFAOYSA-N 0.000 description 1
- 150000002989 phenols Chemical class 0.000 description 1
- 229920001228 polyisocyanate Polymers 0.000 description 1
- 239000005056 polyisocyanate Substances 0.000 description 1
- 238000002360 preparation method Methods 0.000 description 1
- 238000010992 reflux Methods 0.000 description 1
- 239000007787 solid Substances 0.000 description 1
- 238000001228 spectrum Methods 0.000 description 1
- 239000012808 vapor phase Substances 0.000 description 1
- 239000003039 volatile agent Substances 0.000 description 1
- 239000002912 waste gas Substances 0.000 description 1
- 239000002699 waste material Substances 0.000 description 1
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C209/00—Preparation of compounds containing amino groups bound to a carbon skeleton
- C07C209/82—Purification; Separation; Stabilisation; Use of additives
- C07C209/86—Separation
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C209/00—Preparation of compounds containing amino groups bound to a carbon skeleton
- C07C209/82—Purification; Separation; Stabilisation; Use of additives
- C07C209/84—Purification
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C211/00—Compounds containing amino groups bound to a carbon skeleton
- C07C211/43—Compounds containing amino groups bound to a carbon skeleton having amino groups bound to carbon atoms of six-membered aromatic rings of the carbon skeleton
- C07C211/44—Compounds containing amino groups bound to a carbon skeleton having amino groups bound to carbon atoms of six-membered aromatic rings of the carbon skeleton having amino groups bound to only one six-membered aromatic ring
- C07C211/45—Monoamines
- C07C211/46—Aniline
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Organic Low-Molecular-Weight Compounds And Preparation Thereof (AREA)
Description
・アニリン、
・プロセス水(すなわち、反応に形成された水および出発ガス流へ必要に応じて添加した水に合計)、
・非凝集性ガス(過剰の水素(任意に、ガス状不純物、例えばメタン、酸化炭素等を含有)、および任意に、例えば添加窒素の選択性を向上させるための添加不活性ガス、EP−A−1882681参照、および任意にガス状副生成物、例えば脱アミノ化反応からのアンモニアを含有))
・低ボイラー、および
・高ボイラー(任意に未反応ニトロベンゼンの量を含有してもよい)
PKの形成を生じさせる凝縮を、TKの形成を生じさせる凝縮より高い温度において行い、PKは、高ボイラーの大部分を含むが、TKは、低ボイラーの大部分およびアニリンの大部分およびプロセス水の大部分を含み、
PK由来の生成物流およびTK由来の生成物流を、少なくとも2つの区域、すなわち、1つのストリッピング区域(AT)および少なくとも1つの精留区域(VT)を含む蒸留塔中へ通過させ、
PK由来の生成物流を、蒸留塔のより低い区域中へ最下部のストリッピング区域および該最下部ストリッピング区域に続く精留区域の間で導入し、TK由来の生成物流を、最上部の精留区域の上にある蒸留塔の上部中へ導入し、
蒸留アニリンを、蒸留塔の最下部区域の蒸留区域および最上部の精留区域の間の側留において取出すこと
を特徴とする方法により達成された。
(本明細書では、物質流の参照数の最初の番号は、関連する図を示す。本発明の異なった実施態様からの同じまたは同等の物質流の場合には、当該参照数の最初の番号に続く数が同じである。)
CC6の下流のガス(流れ538)の温度: 60℃
T2の上部精留区域の理論プレートの数: 10
T2の中部精留区域の理論プレートの数: 9
T2の下部精留区域の理論プレートの数: 12
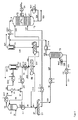
このシミュレーションは、より詳細に図2において上で既に説明した変法に基づいて行った。CC1において凝縮した液体の45%を、流れ5としてワッシャーT1へ通過させた。以下の条件を適用した:
CC1(流れ24)の下流のガスの温度: 118℃
T1における理論プレートの数: 6
T2の上部精留区域の理論プレートの数: 10
T2の中部精留区域の理論プレートの数: 10
T2の下部精留区域の理論プレートの数: 12
CC2における温度: 60℃
このシミュレーションは、図3において上で既に説明した変法に基づいて行った。他の条件は、実施例2と同じである。結果を表9に集約する。
このシミュレーションは、図3において記載の方法に基づいて行った。この実施例では、塔T2は、より少ないプレートを有する。
T2の上部精留区域の理論プレートの数: 9
T2の中部精留区域の理論プレートの数: 6
T2の下部精留区域の理論プレートの数: 2
残りのパラメーターは、実施例3と同じである。
本発明の好ましい態様は、以下を包含する。
[1]ニトロベンゼンの気相水素化および引き続きのアニリンの精製によるアニリンの製造方法であって、
気体粗製反応生成物(11/21/31/41)を得、これを分別凝縮して少なくとも2つの液体プロセス生成物、少なくとも1つの部分凝縮物(PK)(12/22/32/42)および全凝縮物(TK)(111/211/311/411)、を得、
PK(12/22/32/42)の形成を生じさせる凝縮を、TK(111/211/311/411)の形成を生じさせる凝縮より高い温度において行い、
PK由来の生成物流およびTK由来の生成物流を、少なくとも2つの区域、すなわち少なくとも1つのストリッピング区域および少なくとも1つの精留区域を含む蒸留塔(T2)中へ通過させ、
PK由来の生成物流を、蒸留塔の下部区域中へ最下部ストリッピング区域および引き続きの区域の間で導入し、およびTK由来の生成物流を、最上部精留区域より上にある蒸留塔の上部へ導入し、および
蒸留アニリン(122/222/322/422)を、蒸留塔の最下部ストリッピング区域および最上部精留区域の間での側流中において取り出す
ことを特徴とする、方法。
[2]PK(12/22/32/42)の形成を生じさせる凝縮を、60℃〜160℃の温度にて行い、および
TK(111/211/311/411)の形成を生じさせる凝縮を、25℃〜90℃の温度にて行う、[1]に記載の方法。
[3]PK由来の生成物流は、分別凝縮において得られる部分凝縮物(42)であり、および
TK由来の生成物流は、TK(411)またはTKを含むプロセス生成物(4111/41111)の水性相および有機相への相分離により得られる有機相(414)である、
[1]または[2]に記載の方法。
[4]PK由来の生成物流は、PK(12/22/32)またはPKを含むプロセス生成物(161/261/361)と塩基水溶液(17/27/37)との混合および引き続きの水性相および有機相への相分離後に得られる有機相(117/217/317)であり、および
TK由来の生成物流は、TK(111/211/311)またはTKを含むプロセス生成物(2111/3111)と水性相(112/212/312)との混合および引き続きの水性相および有機相への相分離後に得られる有機相(116/214/316)である、
[1]または[2]に記載の方法。
[5]PK(12/22/32)またはPKを含むプロセス生成物(161/261/361)を、塩基水溶液(17/27/37)との混合前、混合中または混合後に、単一段階法または多段階法において、水または流れAの全質量を基準として少なくとも50質量%の水を含む流れAと混合する、
[4]に記載の方法。
[6]少なくとも50質量%の水を含む流れAは、TK(111/211/311)またはTKを含むプロセス生成物(2111/3111)と塩基水溶液(112/212/312)との混合および引き続きの水性相および有機相への相分離後に得られる水性相(113/213/313)である、
[5]に記載の方法。
[7]TK(111/311)またはTK(3111)を含むプロセス生成物と塩基水溶液(112/312)との混合および引き続きの相分離後に得られる有機相(114/314)を、単一段階法または多段階法において、水または流れBの全質量を基準として少なくとも50質量%の水を含む流れBで洗浄する、
[4]〜[6]のいずれか1つに記載の方法。
[8]少なくとも50質量%の水を含む流れBは、蒸留塔(T2)の上部において取出した気相(118)の液体凝縮物流(120)または蒸留塔(T2)の上部において取出した気相(318)の液体凝縮物流を含むプロセス生成物(320)である、
[7]に記載の方法。
[9]TK(211)またはTKを含むプロセス生成物(2111)を、塩基水溶液(212)との混合前、混合中または混合後に、単一段階法または多段階法において、水または流れBの全質量を基準として少なくとも50質量%の水を含む流れBと混合する、
[4]〜[6]のいずれか1つに記載の方法。
[10]少なくとも50質量%の水を含む流れBは、蒸留塔(T2)の上部において取出した気相(218)の液体凝縮物流を含むプロセス生成物(220)である、
[9]に記載の方法。
[11]蒸留塔(T2)の上部において取出した気相の液体凝縮物流を含むプロセス生成物(320)を、
水ストリッパー(T3)中へ、PK(32)またはPKを含むプロセス生成物(313)と塩基水溶液(37)との混合後に相分離により得られる水性相(326)を導入することにより得られるアニリン−水共沸性混合物(328)を、蒸留塔(T2)の上部において取出した気相(318)の全凝縮物(319)へ添加することにより得る、
[8]に記載の方法。
[12]蒸留塔(T2)の上部において取出した気相の液体凝縮物流を含むプロセス生成物(220)を、
水ストリッパー(T3)中へ、PK(22)またはPKを含むプロセス生成物(213)と塩基水溶液(27)との混合後に相分離により得られる水性相(226)を導入することにより得られるアニリン−水共沸性混合物(228)を、蒸留塔(T2)の上部において取出した気相(218)の全凝縮物(219)へ添加することにより得る、
[10]に記載の方法。
[13]蒸留塔(T2)から側流において取出したアニリン(422)を、塩基水溶液(432)と混合し、および酸性不純物を除去したアニリン(434)を、相分離により得る、[3]に記載の方法。
[14]アルカリ金属水酸化物またはアルカリ土類金属水酸化物の溶液を、塩基水溶液(17/27/37−112/212/312−432)として用いる、[4]〜[11]のいずれか1つに記載の方法。
Claims (4)
- ニトロベンゼンの気相水素化および引き続きのアニリンの精製によるアニリンの製造方法であって、
気体粗製反応生成物(11/21/31/41)を得、これを分別凝縮して少なくとも1つの部分凝縮物(PK)(12/22/32/42)および全凝縮物(TK)(111/211/311/411)、を得、
PK(12/22/32/42)の形成を生じさせる凝縮を、TK(111/211/311/411)の形成を生じさせる凝縮より高い温度において行い、
PK由来の生成物流およびTK由来の生成物流を、少なくとも2つの区域、すなわち少なくとも1つのストリッピング区域および少なくとも1つの精留区域を含む蒸留塔(T2)中へ通過させ、
PK由来の生成物流を、蒸留塔の下部区域中へ最下部ストリッピング区域および前記最下部ストリッピング区域に続く精留区域の間で導入し、およびTK由来の生成物流を、最上部精留区域より上にある蒸留塔の上部へ導入し、および
蒸留アニリン(122/222/322/422)を、蒸留塔の最下部ストリッピング区域および最上部精留区域の間での側留中において取り出すことを特徴とする、方法。 - PK由来の生成物流は、分別凝縮において得られる部分凝縮物(42)であり、および
TK由来の生成物流は、TK(411)またはTKを含むプロセス生成物(4111/41111)の水性相および有機相への相分離により得られる有機相(414)である、請求項1に記載の方法。 - PK由来の生成物流は、PK(12/22/32)またはPKを含むプロセス生成物(161/261/361)と塩基水溶液(17/27/37)との混合および引き続きの水性相および有機相への相分離後に得られる有機相(117/217/317)であり、および
TK由来の生成物流は、TK(111/211/311)またはTKを含むプロセス生成物(2111/3111)と水性相(112/212/312)との混合および引き続きの水性相および有機相への相分離後に得られる有機相(116/214/316)である、請求項1に記載の方法。 - 蒸留塔(T2)から側留において取出したアニリン(422)を、塩基水溶液(432)と混合し、および酸性不純物を除去したアニリン(434)を、相分離により得る、請求項2に記載の方法。
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| DE102010042731A DE102010042731A1 (de) | 2010-10-21 | 2010-10-21 | Verfahren zur Reinigung von Anilin aus Gasphasenhydrierungen |
| DE102010042731.4 | 2010-10-21 | ||
| PCT/EP2011/068122 WO2012052407A1 (de) | 2010-10-21 | 2011-10-17 | Verfahren zur reinigung von anilin aus gasphasenhydrierungen |
Publications (3)
| Publication Number | Publication Date |
|---|---|
| JP2013543517A JP2013543517A (ja) | 2013-12-05 |
| JP2013543517A5 JP2013543517A5 (ja) | 2014-12-04 |
| JP5951618B2 true JP5951618B2 (ja) | 2016-07-13 |
Family
ID=44860336
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2013534280A Active JP5951618B2 (ja) | 2010-10-21 | 2011-10-17 | 気相水素化からアニリンを精製するための方法 |
Country Status (9)
| Country | Link |
|---|---|
| US (1) | US9233910B2 (ja) |
| EP (1) | EP2630117B1 (ja) |
| JP (1) | JP5951618B2 (ja) |
| KR (1) | KR101869996B1 (ja) |
| CN (1) | CN103201253B (ja) |
| DE (1) | DE102010042731A1 (ja) |
| PL (1) | PL2630117T3 (ja) |
| PT (1) | PT2630117E (ja) |
| WO (1) | WO2012052407A1 (ja) |
Families Citing this family (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP2641892A1 (de) * | 2012-03-23 | 2013-09-25 | Bayer MaterialScience AG | Verfahren zur Reinigung von Anilin aus Gasphasenhydrierungen |
| CN104718185B (zh) * | 2012-10-11 | 2017-01-18 | 巴斯夫欧洲公司 | 获得纯苯胺的方法 |
| US9115049B2 (en) | 2012-10-11 | 2015-08-25 | Basf Se | Process for obtaining pure aniline |
| CN110627651B (zh) * | 2018-06-25 | 2022-06-14 | 中国石油化工股份有限公司 | 一种降低苯胺中苯酚含量的方法 |
Family Cites Families (17)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US2174008A (en) * | 1938-01-29 | 1939-09-26 | Nat Aniline & Chem Co Inc | Distillation of amines from reduction masses |
| JPS4935341A (ja) | 1972-07-31 | 1974-04-01 | ||
| DE4428017A1 (de) | 1994-08-08 | 1996-02-15 | Bayer Ag | Verfahren zur Herstellung von aromatischen Aminen |
| DE4428018A1 (de) | 1994-08-08 | 1996-02-15 | Bayer Ag | Verfahren zur Herstellung von aromatischen Aminen |
| JP3804082B2 (ja) | 1995-04-27 | 2006-08-02 | 住友化学株式会社 | アニリンの精製方法 |
| JPH0935341A (ja) | 1995-07-18 | 1997-02-07 | Masayuki Matsuda | X線による情報の記録・読み出し方法 |
| JP2001226320A (ja) * | 2000-02-14 | 2001-08-21 | Nippon Shokubai Co Ltd | アクリル酸の捕集方法およびアクリル酸の精製方法 |
| US7049471B2 (en) | 2003-10-10 | 2006-05-23 | E. I. Du Pont De Nemours And Company | Separation of amine from a phenolic compound |
| DE102004026626A1 (de) * | 2004-06-01 | 2005-12-29 | Bayer Materialscience Ag | Verfahren zur destillativen Trennung von wässrigen Aminlösungen |
| JP2005350388A (ja) | 2004-06-10 | 2005-12-22 | Sumitomo Chemical Co Ltd | アニリンの製造方法 |
| JP4552941B2 (ja) | 2006-01-17 | 2010-09-29 | 住友化学株式会社 | アニリンの精製方法および製造方法 |
| DE102006007620A1 (de) | 2006-02-18 | 2007-08-23 | Bayer Materialscience Ag | Verfahren zur Herstellung von Anilin |
| DE102006007619A1 (de) | 2006-02-18 | 2007-08-23 | Bayer Materialscience Ag | Verfahren zur Herstellung von Anilin |
| DE102006035203A1 (de) | 2006-07-29 | 2008-01-31 | Bayer Materialscience Ag | Verfahren zur Herstellung von aromatischen Aminen |
| JP2008184409A (ja) * | 2007-01-29 | 2008-08-14 | Mitsubishi Rayon Co Ltd | アルキルアミン含有混合物の蒸留法及びアルキルアミン類の製造方法 |
| DE102007039091A1 (de) | 2007-08-18 | 2009-02-19 | Bayer Materialscience Ag | Verfahren zur Reinigung von aromatischen Aminen |
| EP2629869A1 (de) * | 2010-10-21 | 2013-08-28 | Bayer Intellectual Property GmbH | Verfahren zur vereinfachten abtrennung eines reaktionsprodukts aus reaktionsgasgemischen mittels mindestens zweimaliger teilweiser kondensation |
-
2010
- 2010-10-21 DE DE102010042731A patent/DE102010042731A1/de not_active Withdrawn
-
2011
- 2011-10-17 JP JP2013534280A patent/JP5951618B2/ja active Active
- 2011-10-17 KR KR1020137012854A patent/KR101869996B1/ko active IP Right Grant
- 2011-10-17 PT PT117732362T patent/PT2630117E/pt unknown
- 2011-10-17 WO PCT/EP2011/068122 patent/WO2012052407A1/de active Application Filing
- 2011-10-17 PL PL11773236T patent/PL2630117T3/pl unknown
- 2011-10-17 EP EP11773236.2A patent/EP2630117B1/de active Active
- 2011-10-17 US US13/878,190 patent/US9233910B2/en active Active
- 2011-10-17 CN CN201180050920.9A patent/CN103201253B/zh active Active
Also Published As
| Publication number | Publication date |
|---|---|
| KR101869996B1 (ko) | 2018-06-22 |
| CN103201253A (zh) | 2013-07-10 |
| EP2630117B1 (de) | 2014-10-15 |
| JP2013543517A (ja) | 2013-12-05 |
| EP2630117A1 (de) | 2013-08-28 |
| DE102010042731A1 (de) | 2012-04-26 |
| WO2012052407A1 (de) | 2012-04-26 |
| US9233910B2 (en) | 2016-01-12 |
| KR20130127983A (ko) | 2013-11-25 |
| PL2630117T3 (pl) | 2015-03-31 |
| CN103201253B (zh) | 2014-12-03 |
| PT2630117E (pt) | 2015-02-17 |
| US20140046096A1 (en) | 2014-02-13 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP5204413B2 (ja) | アニリンの製造方法 | |
| JP4773138B2 (ja) | アミン水溶液の蒸留分離法 | |
| KR101376940B1 (ko) | 아닐린의 제조 방법 | |
| JP2018016628A (ja) | 低沸点成分の分離、ならびに部分凝縮によるイソホロンジアミンにおけるアンモニア含分の低下 | |
| JP5951618B2 (ja) | 気相水素化からアニリンを精製するための方法 | |
| JP2013535478A (ja) | ニトロベンゼンの連続製造方法 | |
| JP5886284B2 (ja) | 断熱ニトロ化によるニトロベンゼンの製造方法 | |
| JP6250662B2 (ja) | 断熱的ニトロ化によりニトロベンゼンを製造する方法 | |
| JP6062527B2 (ja) | 気相水素化からのアニリンの精製方法 | |
| JP6165844B2 (ja) | 芳香族アミンを含む物質混合物、特に粗製アニリンの物質混合物の処理方法 | |
| JP5530516B2 (ja) | 化学装置 | |
| JP2016522803A (ja) | ニトロベンゼン製造からの廃水の後処理方法 | |
| JP2008184409A (ja) | アルキルアミン含有混合物の蒸留法及びアルキルアミン類の製造方法 | |
| JP2007063159A (ja) | メチルアミン類の製造方法 | |
| CN114096512B (zh) | 提纯苯胺的方法 | |
| RU2612799C1 (ru) | Способ выделения осушенного анилина из продукта газофазного каталитического гидрирования нитробензола | |
| RU2167145C1 (ru) | Способ очистки технического нитробензола от серосодержащих, азот- и кислородсодержащих побочных продуктов | |
| TW202237560A (zh) | 乙腈的分離方法 | |
| KR101200218B1 (ko) | 아민 수용액 증류적 분리 방법 | |
| KR101863126B1 (ko) | 공비증류에 의한 2,6-디메틸페놀의 정제방법 | |
| JP2004002346A (ja) | フェノールの精製方法 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20141016 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20141016 |
|
| RD03 | Notification of appointment of power of attorney |
Free format text: JAPANESE INTERMEDIATE CODE: A7423 Effective date: 20150217 |
|
| RD04 | Notification of resignation of power of attorney |
Free format text: JAPANESE INTERMEDIATE CODE: A7424 Effective date: 20150513 |
|
| A977 | Report on retrieval |
Free format text: JAPANESE INTERMEDIATE CODE: A971007 Effective date: 20150601 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20150619 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20150918 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20160115 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20160408 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20160513 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20160608 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 5951618 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |