JP5883785B2 - 改善した白色度特性を有する酸化銀製剤 - Google Patents
改善した白色度特性を有する酸化銀製剤 Download PDFInfo
- Publication number
- JP5883785B2 JP5883785B2 JP2012521116A JP2012521116A JP5883785B2 JP 5883785 B2 JP5883785 B2 JP 5883785B2 JP 2012521116 A JP2012521116 A JP 2012521116A JP 2012521116 A JP2012521116 A JP 2012521116A JP 5883785 B2 JP5883785 B2 JP 5883785B2
- Authority
- JP
- Japan
- Prior art keywords
- oxide
- silver
- zinc oxide
- formulation
- less
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
- NDVLTYZPCACLMA-UHFFFAOYSA-N silver oxide Chemical compound [O-2].[Ag+].[Ag+] NDVLTYZPCACLMA-UHFFFAOYSA-N 0.000 title claims description 175
- 239000000203 mixture Substances 0.000 title claims description 132
- 238000009472 formulation Methods 0.000 title claims description 120
- 229910001923 silver oxide Inorganic materials 0.000 title claims description 88
- XLOMVQKBTHCTTD-UHFFFAOYSA-N Zinc monoxide Chemical compound [Zn]=O XLOMVQKBTHCTTD-UHFFFAOYSA-N 0.000 claims description 268
- 239000011787 zinc oxide Substances 0.000 claims description 136
- ANQVKHGDALCPFZ-UHFFFAOYSA-N ethyl 2-[6-(4-methylpiperazin-1-yl)-1h-benzimidazol-2-yl]acetate Chemical compound C1=C2NC(CC(=O)OCC)=NC2=CC=C1N1CCN(C)CC1 ANQVKHGDALCPFZ-UHFFFAOYSA-N 0.000 claims description 61
- 239000012049 topical pharmaceutical composition Substances 0.000 claims description 16
- 239000007788 liquid Substances 0.000 claims description 7
- 239000004164 Wax ester Substances 0.000 claims description 6
- 235000019386 wax ester Nutrition 0.000 claims description 6
- 235000014692 zinc oxide Nutrition 0.000 description 118
- 239000000523 sample Substances 0.000 description 38
- 238000000034 method Methods 0.000 description 30
- 238000011282 treatment Methods 0.000 description 23
- 208000025865 Ulcer Diseases 0.000 description 18
- 238000012360 testing method Methods 0.000 description 18
- 231100000397 ulcer Toxicity 0.000 description 16
- 229940119170 jojoba wax Drugs 0.000 description 15
- 239000002674 ointment Substances 0.000 description 14
- 229920001817 Agar Polymers 0.000 description 13
- BQCADISMDOOEFD-UHFFFAOYSA-N Silver Chemical compound [Ag] BQCADISMDOOEFD-UHFFFAOYSA-N 0.000 description 13
- 239000008272 agar Substances 0.000 description 13
- WXWBZQPPTQBZLZ-UHFFFAOYSA-N [O-2].[Zn+2].[Ag]=O Chemical compound [O-2].[Zn+2].[Ag]=O WXWBZQPPTQBZLZ-UHFFFAOYSA-N 0.000 description 11
- 239000000463 material Substances 0.000 description 11
- 239000004332 silver Substances 0.000 description 11
- 229910052709 silver Inorganic materials 0.000 description 11
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 11
- 230000000844 anti-bacterial effect Effects 0.000 description 9
- 230000000845 anti-microbial effect Effects 0.000 description 9
- 210000004027 cell Anatomy 0.000 description 9
- 239000004744 fabric Substances 0.000 description 9
- 239000000835 fiber Substances 0.000 description 9
- 238000002156 mixing Methods 0.000 description 9
- 235000013871 bee wax Nutrition 0.000 description 8
- 239000012166 beeswax Substances 0.000 description 8
- 238000004140 cleaning Methods 0.000 description 8
- 238000004043 dyeing Methods 0.000 description 8
- 230000006870 function Effects 0.000 description 8
- 239000002245 particle Substances 0.000 description 8
- 239000000047 product Substances 0.000 description 8
- 238000005406 washing Methods 0.000 description 8
- 208000027418 Wounds and injury Diseases 0.000 description 7
- 238000002360 preparation method Methods 0.000 description 7
- 239000003921 oil Substances 0.000 description 6
- 239000000440 bentonite Substances 0.000 description 5
- 229910000278 bentonite Inorganic materials 0.000 description 5
- SVPXDRXYRYOSEX-UHFFFAOYSA-N bentoquatam Chemical compound O.O=[Si]=O.O=[Al]O[Al]=O SVPXDRXYRYOSEX-UHFFFAOYSA-N 0.000 description 5
- 230000004087 circulation Effects 0.000 description 5
- 239000006071 cream Substances 0.000 description 5
- 244000005700 microbiome Species 0.000 description 5
- 230000002792 vascular Effects 0.000 description 5
- 241000894006 Bacteria Species 0.000 description 4
- 239000013011 aqueous formulation Substances 0.000 description 4
- 230000001580 bacterial effect Effects 0.000 description 4
- 238000007906 compression Methods 0.000 description 4
- 230000006835 compression Effects 0.000 description 4
- 238000001816 cooling Methods 0.000 description 4
- LOKCTEFSRHRXRJ-UHFFFAOYSA-I dipotassium trisodium dihydrogen phosphate hydrogen phosphate dichloride Chemical compound P(=O)(O)(O)[O-].[K+].P(=O)(O)([O-])[O-].[Na+].[Na+].[Cl-].[K+].[Cl-].[Na+] LOKCTEFSRHRXRJ-UHFFFAOYSA-I 0.000 description 4
- 230000005764 inhibitory process Effects 0.000 description 4
- 238000007726 management method Methods 0.000 description 4
- 239000002953 phosphate buffered saline Substances 0.000 description 4
- 239000001993 wax Substances 0.000 description 4
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 3
- 239000007864 aqueous solution Substances 0.000 description 3
- 238000004113 cell culture Methods 0.000 description 3
- 239000003795 chemical substances by application Substances 0.000 description 3
- 239000011248 coating agent Substances 0.000 description 3
- 238000000576 coating method Methods 0.000 description 3
- 239000000839 emulsion Substances 0.000 description 3
- 230000004907 flux Effects 0.000 description 3
- 239000002054 inoculum Substances 0.000 description 3
- 230000000813 microbial effect Effects 0.000 description 3
- 239000007787 solid Substances 0.000 description 3
- 239000004094 surface-active agent Substances 0.000 description 3
- 230000000007 visual effect Effects 0.000 description 3
- 229920000742 Cotton Polymers 0.000 description 2
- 206010056340 Diabetic ulcer Diseases 0.000 description 2
- 241000194032 Enterococcus faecalis Species 0.000 description 2
- PEDCQBHIVMGVHV-UHFFFAOYSA-N Glycerine Chemical compound OCC(O)CO PEDCQBHIVMGVHV-UHFFFAOYSA-N 0.000 description 2
- 206010040943 Skin Ulcer Diseases 0.000 description 2
- 239000003463 adsorbent Substances 0.000 description 2
- QVGXLLKOCUKJST-UHFFFAOYSA-N atomic oxygen Chemical compound [O] QVGXLLKOCUKJST-UHFFFAOYSA-N 0.000 description 2
- 239000013068 control sample Substances 0.000 description 2
- 230000002596 correlated effect Effects 0.000 description 2
- 239000001939 cymbopogon martini roxb. stapf. oil Substances 0.000 description 2
- GUJOJGAPFQRJSV-UHFFFAOYSA-N dialuminum;dioxosilane;oxygen(2-);hydrate Chemical compound O.[O-2].[O-2].[O-2].[Al+3].[Al+3].O=[Si]=O.O=[Si]=O.O=[Si]=O.O=[Si]=O GUJOJGAPFQRJSV-UHFFFAOYSA-N 0.000 description 2
- 238000010790 dilution Methods 0.000 description 2
- 239000012895 dilution Substances 0.000 description 2
- 239000002270 dispersing agent Substances 0.000 description 2
- 239000006185 dispersion Substances 0.000 description 2
- 238000005516 engineering process Methods 0.000 description 2
- 239000006260 foam Substances 0.000 description 2
- 239000011521 glass Substances 0.000 description 2
- 239000004615 ingredient Substances 0.000 description 2
- 239000006210 lotion Substances 0.000 description 2
- 238000005259 measurement Methods 0.000 description 2
- 206010062198 microangiopathy Diseases 0.000 description 2
- 230000004089 microcirculation Effects 0.000 description 2
- 238000012986 modification Methods 0.000 description 2
- 230000004048 modification Effects 0.000 description 2
- 230000017074 necrotic cell death Effects 0.000 description 2
- 230000007935 neutral effect Effects 0.000 description 2
- 235000015097 nutrients Nutrition 0.000 description 2
- 239000001301 oxygen Substances 0.000 description 2
- 229910052760 oxygen Inorganic materials 0.000 description 2
- 230000010412 perfusion Effects 0.000 description 2
- 239000000843 powder Substances 0.000 description 2
- 238000004321 preservation Methods 0.000 description 2
- 150000003378 silver Chemical class 0.000 description 2
- SQGYOTSLMSWVJD-UHFFFAOYSA-N silver(1+) nitrate Chemical compound [Ag+].[O-]N(=O)=O SQGYOTSLMSWVJD-UHFFFAOYSA-N 0.000 description 2
- VFWRGKJLLYDFBY-UHFFFAOYSA-N silver;hydrate Chemical compound O.[Ag].[Ag] VFWRGKJLLYDFBY-UHFFFAOYSA-N 0.000 description 2
- 239000002884 skin cream Substances 0.000 description 2
- 231100000019 skin ulcer Toxicity 0.000 description 2
- 239000000243 solution Substances 0.000 description 2
- 239000011550 stock solution Substances 0.000 description 2
- 239000000725 suspension Substances 0.000 description 2
- 230000036269 ulceration Effects 0.000 description 2
- 230000002087 whitening effect Effects 0.000 description 2
- 200000000007 Arterial disease Diseases 0.000 description 1
- 206010054044 Diabetic microangiopathy Diseases 0.000 description 1
- 244000068988 Glycine max Species 0.000 description 1
- 235000010469 Glycine max Nutrition 0.000 description 1
- 208000001688 Herpes Genitalis Diseases 0.000 description 1
- 238000002768 Kirby-Bauer method Methods 0.000 description 1
- 235000006679 Mentha X verticillata Nutrition 0.000 description 1
- 235000002899 Mentha suaveolens Nutrition 0.000 description 1
- 235000001636 Mentha x rotundifolia Nutrition 0.000 description 1
- 206010067152 Oral herpes Diseases 0.000 description 1
- BPQQTUXANYXVAA-UHFFFAOYSA-N Orthosilicate Chemical compound [O-][Si]([O-])([O-])[O-] BPQQTUXANYXVAA-UHFFFAOYSA-N 0.000 description 1
- FAPWRFPIFSIZLT-UHFFFAOYSA-M Sodium chloride Chemical compound [Na+].[Cl-] FAPWRFPIFSIZLT-UHFFFAOYSA-M 0.000 description 1
- 239000005708 Sodium hypochlorite Substances 0.000 description 1
- 229920002125 Sokalan® Polymers 0.000 description 1
- 241001085768 Stereolepis gigas Species 0.000 description 1
- 206010046914 Vaginal infection Diseases 0.000 description 1
- 201000008100 Vaginitis Diseases 0.000 description 1
- 208000000558 Varicose Ulcer Diseases 0.000 description 1
- 206010047249 Venous thrombosis Diseases 0.000 description 1
- 239000004480 active ingredient Substances 0.000 description 1
- 239000000853 adhesive Substances 0.000 description 1
- 230000001070 adhesive effect Effects 0.000 description 1
- 208000007502 anemia Diseases 0.000 description 1
- 239000004599 antimicrobial Substances 0.000 description 1
- 239000008346 aqueous phase Substances 0.000 description 1
- 230000004872 arterial blood pressure Effects 0.000 description 1
- 210000002565 arteriole Anatomy 0.000 description 1
- 230000009286 beneficial effect Effects 0.000 description 1
- 230000005540 biological transmission Effects 0.000 description 1
- 238000009835 boiling Methods 0.000 description 1
- 239000003610 charcoal Substances 0.000 description 1
- 239000004927 clay Substances 0.000 description 1
- 230000001332 colony forming effect Effects 0.000 description 1
- 238000011109 contamination Methods 0.000 description 1
- 230000000875 corresponding effect Effects 0.000 description 1
- 239000002537 cosmetic Substances 0.000 description 1
- 230000003247 decreasing effect Effects 0.000 description 1
- 239000008367 deionised water Substances 0.000 description 1
- 229910021641 deionized water Inorganic materials 0.000 description 1
- 239000000645 desinfectant Substances 0.000 description 1
- 206010012601 diabetes mellitus Diseases 0.000 description 1
- 201000009101 diabetic angiopathy Diseases 0.000 description 1
- 230000000694 effects Effects 0.000 description 1
- 230000003628 erosive effect Effects 0.000 description 1
- 239000012467 final product Substances 0.000 description 1
- 239000000499 gel Substances 0.000 description 1
- 201000004946 genital herpes Diseases 0.000 description 1
- 235000011187 glycerol Nutrition 0.000 description 1
- 230000009931 harmful effect Effects 0.000 description 1
- 238000003306 harvesting Methods 0.000 description 1
- 230000035876 healing Effects 0.000 description 1
- 210000003000 inclusion body Anatomy 0.000 description 1
- 238000011534 incubation Methods 0.000 description 1
- 208000015181 infectious disease Diseases 0.000 description 1
- 238000011081 inoculation Methods 0.000 description 1
- 238000004519 manufacturing process Methods 0.000 description 1
- 229910052901 montmorillonite Inorganic materials 0.000 description 1
- 238000000465 moulding Methods 0.000 description 1
- 230000009965 odorless effect Effects 0.000 description 1
- 230000003647 oxidation Effects 0.000 description 1
- 238000007254 oxidation reaction Methods 0.000 description 1
- OTCVAHKKMMUFAY-UHFFFAOYSA-N oxosilver Chemical group [Ag]=O OTCVAHKKMMUFAY-UHFFFAOYSA-N 0.000 description 1
- 230000008447 perception Effects 0.000 description 1
- 208000028169 periodontal disease Diseases 0.000 description 1
- 229920003023 plastic Polymers 0.000 description 1
- 239000004033 plastic Substances 0.000 description 1
- 229920000642 polymer Polymers 0.000 description 1
- 230000035935 pregnancy Effects 0.000 description 1
- 238000012545 processing Methods 0.000 description 1
- 230000004044 response Effects 0.000 description 1
- 150000003839 salts Chemical class 0.000 description 1
- 238000013207 serial dilution Methods 0.000 description 1
- 238000007493 shaping process Methods 0.000 description 1
- CQLFBEKRDQMJLZ-UHFFFAOYSA-M silver acetate Chemical compound [Ag+].CC([O-])=O CQLFBEKRDQMJLZ-UHFFFAOYSA-M 0.000 description 1
- 229940071536 silver acetate Drugs 0.000 description 1
- 229910001961 silver nitrate Inorganic materials 0.000 description 1
- -1 silver oxide compound Chemical class 0.000 description 1
- 206010040872 skin infection Diseases 0.000 description 1
- 229910021647 smectite Inorganic materials 0.000 description 1
- 230000000391 smoking effect Effects 0.000 description 1
- 239000011780 sodium chloride Substances 0.000 description 1
- SUKJFIGYRHOWBL-UHFFFAOYSA-N sodium hypochlorite Chemical compound [Na+].Cl[O-] SUKJFIGYRHOWBL-UHFFFAOYSA-N 0.000 description 1
- 238000010186 staining Methods 0.000 description 1
- 238000003860 storage Methods 0.000 description 1
- 239000000126 substance Substances 0.000 description 1
- 239000008399 tap water Substances 0.000 description 1
- 235000020679 tap water Nutrition 0.000 description 1
- 238000002560 therapeutic procedure Methods 0.000 description 1
- 239000002562 thickening agent Substances 0.000 description 1
- 210000004906 toe nail Anatomy 0.000 description 1
- 238000012546 transfer Methods 0.000 description 1
- 239000000341 volatile oil Substances 0.000 description 1
- 230000037303 wrinkles Effects 0.000 description 1
- RNWHGQJWIACOKP-UHFFFAOYSA-N zinc;oxygen(2-) Chemical compound [O-2].[Zn+2] RNWHGQJWIACOKP-UHFFFAOYSA-N 0.000 description 1
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/0012—Galenical forms characterised by the site of application
- A61K9/0014—Skin, i.e. galenical aspects of topical compositions
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K33/00—Medicinal preparations containing inorganic active ingredients
- A61K33/24—Heavy metals; Compounds thereof
- A61K33/30—Zinc; Compounds thereof
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K33/00—Medicinal preparations containing inorganic active ingredients
- A61K33/24—Heavy metals; Compounds thereof
- A61K33/38—Silver; Compounds thereof
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/06—Ointments; Bases therefor; Other semi-solid forms, e.g. creams, sticks, gels
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P17/00—Drugs for dermatological disorders
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P17/00—Drugs for dermatological disorders
- A61P17/02—Drugs for dermatological disorders for treating wounds, ulcers, burns, scars, keloids, or the like
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
- A61P31/02—Local antiseptics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
- A61P31/04—Antibacterial agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
- A61P31/10—Antimycotics
Landscapes
- Health & Medical Sciences (AREA)
- General Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Medicinal Chemistry (AREA)
- Veterinary Medicine (AREA)
- Public Health (AREA)
- Pharmacology & Pharmacy (AREA)
- Life Sciences & Earth Sciences (AREA)
- Animal Behavior & Ethology (AREA)
- Epidemiology (AREA)
- Inorganic Chemistry (AREA)
- Dermatology (AREA)
- General Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Oncology (AREA)
- Communicable Diseases (AREA)
- Engineering & Computer Science (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Medicinal Preparation (AREA)
- Cosmetics (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
Description
≧(L0 *)+
2を満たし、Lo *は、酸化亜鉛抜きの製剤の基準白色度値であり、L*は酸化亜鉛を含む製剤の白色度値である。
酸化銀(II)などの酸化銀; (ii)酸化亜鉛、および、(iii)担体媒質、前記製剤は少なくとも0.05重量%の酸化銀と、25%未満、20重量%未満、15重量%未満、12重量%未満、10重量%未満または8重量%未満の酸化亜鉛とを含み、前記酸化銀および前記酸化亜鉛は、担体媒質内で親密に分散する、そして、(b)皮膚組織に製剤を付与することにより、皮膚組織の治療を遂行する。
酸化銀−酸化亜鉛製剤は25重量%以上の酸化亜鉛を含む酸化亜鉛製剤は乏しい展延性を示し、抗菌の見地からも効果的ではないことも分かった。幾つかの製剤において、20重量%以上の酸化亜鉛含有量は、この種の有害特性を呈し得る。
Internationale d’EclairageまたはCIE)によって指定され、L*成分は明るさの人間の知覚と密接に整合するために決定された。L*の尺度に関して、発光輝度は百分率として表され、L*
= 0は黒を表し、L* = 100は散乱性の白を表す。
布見本を生産するために、ホワイトコットンTシャツから繊維の7×7cm片を切りとる;
1.布見本の重さを量る;
2.清潔な紙タオル上に布見本を置き、染色手順からあらゆる外来の油を吸収する;
3.染色サンプル400mgをスパチュラ背面に付与する;
4.スパチュラを使用して布表面の90%上にサンプルを均一に広げる、注意することは
a. 縁は染色せず、そして、
b. 全ての染色サンプルを使用する;
5.布見本の重量を再度量り、サンプル(概して、〜400mgの付加重量)の完全移送を確実にする;
6.室温(65〜75°F)にて戸外環境で布にサンプルを24時間吸収させる;
7.布を650−700mlの温かい界面活性剤/水溶液(正規水道水およびLestoil、登録商標、の界面活性剤/しみ除去剤または同等品)に漬ける;
a. 水溶液は水1リットルごとに10mlの界面活性剤を使用して調合される;
b. 水溶液は、各サンプル用に新たに原液から取り出される;
c. 原液を130°Fまで暖める;
8.毎分300回転で作動しているミキサーを使用して布を含む水溶液を10分間混ぜる;
9.清浄水のビーカーに布を入れて濯ぐ。布を除去し、毎回新規な清浄水を使用してリンス手順を繰り返し、合計3回濯ぐ;
10.布見本を一様に平面壁にピンで留める;
a. 無染色の縁だけをピンで留める;
b. 布見本を戸外環境に置く;
c. 布見本を室温(65−75°F)にて維持する;そして、
11.比色分析計での測定準備がでるまで布見本を遮光性のポーチに保管する。
理論による制限を望まずに、これを酸化亜鉛粒子が繊維に付着する傾向、酸化銀(II)粒子が付着する傾向との組み合わせ、または酸化亜鉛粒子と関連する傾向に帰することとしたい。例えそうでも、酸化亜鉛は酸化銀(II)の抗菌性効力を減少するように見えないかまたは特段に減らすことはない。
以下の一般的手順によって、酸化銀‐酸化亜鉛実施例製剤を調合した:80℃までホホバ油を加熱した。蜜蝋のようなワックスを次いで導入してもよい。前記材料を約55℃まで冷やしつつ、完全に混ぜ合せる。パルマローザ油を加え、続いて酸化銀(II)および酸化亜鉛を加える。混合は一貫して、ならびに35℃〜40℃に混合物を冷却する間、維持し得る。
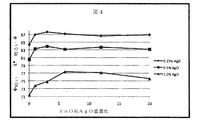
実施例1において提供された一般の手順を使用して、様々な酸化銀‐酸化亜鉛製剤を調合した。表5にて幾つかの具体的な製剤を下記に提供し、例示した。下記で提供されなかった製剤は、質的に同様の結果を生成した。酸化銀および酸化亜鉛の百分率は最終生産物の全体の重量に基づいた重量基準である。視覚の白色度価値判断は、表6にて提供した尺度を用いて各サンプルに対して実行された。
以下の一般的手順によって、酸化銀‐酸化亜鉛実施例製剤を調合した:水を含む容器に粘性成形剤、代表的にはスメクタイト、を添加した(例えば、テキサス州GonzalesのSouthern
Clay Products, Inc.製Gelwhite Hのようなベントナイトまたはモンモリロナイト粉末)。他の粘性成形粘土、特に珪酸塩層が挟まれた構造で配置されている粘土、もまた使用され得る。他の粘性成形剤および増粘剤、例えばグリセリンおよびカルボマー、が使用され得る。好ましくは、この種の選択された材料は、反応性の高い酸化銀(II)による良好な耐性を酸化または化学的侵食に対して示し得る。
実施例14において提供された一般の手順を使用して、水系酸化銀(II)‐酸化亜鉛製剤を調合した。前記製剤は以下を含んだ:
水: 600グラム(87.1%)
ベントナイト: 25グラム(3.6%)
ホホバ油: 15グラム(2.2%)
酸化亜鉛: 40グラム(5.8%)
酸化銀(II): 9グラム(1.3%)
実施例14において提供された一般の手順を使用して、エマルジョン系酸化銀(II)‐酸化亜鉛製剤を調合した。前記製剤は以下を含んだ:
水: 600グラム(63.1%)
ベントナイト: 60グラム(6.3%)
ホホバ油: 240グラム(25.2%)
酸化亜鉛: 50グラム(5.3%)
酸化銀(II): 0.9グラム(0.1%)
30人の患者のコントロールグループを、従来のクリーニングおよび圧縮管理方法を使用して、Irvine3 Circulation/Vascular
Labs(Chieti−Pescara大学、Pescara、イタリア)にて治療した。患者の潰瘍形成は減少動脈圧(平均的皮膚を有する上記のネクローシス限界。かん流圧>50
mmHg)および糖尿病患者細小血管症からの結果として診断され、そして、局所感染によって特徴づけられた。カラー二重鎖走査を静脈血せん、厳しい動脈障害、を除外するために用いた、そして、ドップラー技術は、苛酷局所貧血およびネクローシスをもつ患者を除外するために、脛骨パルスの存在を評価するために用いた。
潰瘍を囲む皮膚上へ付与される銀四酸化物(AgO)を含む軟膏の効力を、29人の患者の治療グループ上のIrvine3 Circulation/Vascular
Labsで試験し、実施例17のコントロールグループのそれらに、同等の潰瘍形成を施した。
Group、イタリア)で潰瘍および周囲の面積を40℃にて2分間洗浄して後、前記クリームを付与した。中性の吸着紙包帯‐皮膚と接触‐を皮膚保護/保存気泡層下に付与した。観察期間の間、潰瘍面積をカバーするために絆創膏または弾性のストッキングを用いた。
銀四酸化物−酸化亜鉛(酸化銀-酸化亜鉛)軟膏の皮膚潰瘍に対する効力を、Irvine3
Circulation/Vascular Labsにおける18人の患者の治療グループ対23人の同等患者を有するコントロールグループで試験した。全ての患者は、従来のクリーニングおよび圧縮管理方法を含む基本的創傷ケア治療を体験した。
銀四酸化物−酸化亜鉛(酸化銀-酸化亜鉛)軟膏の静脈皮膚潰瘍に対する効力、をIrvine3
Circulation/Vascular Labsにおける44人の患者の治療グループ対38人の同等患者を有するコントロールグループで試験した。全ての患者は、従来のクリーニングおよび圧縮管理方法を含む基本的創傷ケア治療を体験した。
実施例20の酸化銀−酸化亜鉛軟膏の糖尿病患者潰瘍に対する効力をIrvine3 Circulation/Vascular
Labsにおける34人の患者の治療グループ対32人の同等患者を有するコントロールグループで試験した。全ての患者は、従来のクリーニングおよび圧縮管理方法を含む基本的創傷ケア治療を体験した。
加えて、治療グループにおいて、潰瘍の完全終了は、コントロールグループの16%と比較して被験者の39%で観察された。
以下のコロニー計数法を使用して様々な製剤の抗菌効力を試験し、比較した:
新たに開けたMuller−Hinton栄養ブイヨン(液体培地)を、バクテリア(ほぼ100,000−150,000カウント)が充満した係蹄を使って接種した。サンプルは、37℃にてインキュベータ内で24時間滞留した。前記ブイヨンが一旦濁ると、充満した他の係蹄は栄養ブイヨンの幾つかのチューブに添加され、前記ブイヨンは10分間放置する。
寒天板上で縞状となる。標準係蹄の使用は、同量の栽培が各プレートに分配されることを確実にする。前記プレートは、37℃にて24時間、インキュベータにおいて熟成される。
・コントロールサンプルに100の数が割り当てられるマニュアル技術、そして、
他のサンプルのコロニー密度に基づいて、相対的な数が、視覚の価値判断に基づいて割り当てられる。
・自動のコロニー計数器(WU−14025−00 Flash & Growコロニー計数器、Cole−Palmer、登録商標、
Vernon Hills、イリノイ州)はコロニーを計数して、99%まで正確である。
様々な製剤の抗菌性効力を、フェカリス菌(ATCC 29212)と水、ベントナイトおよびホホバ油を含む水性製剤とを用いて実施例22で詳述される手順で試験し、比較した。結果は下記の表7において提供する:
様々な製剤の抗菌性効力を、フェカリス菌(ATCC 29212)と蜜蝋およびホホバ油を含む油性製剤とを用いて実施例22で詳述される手順で試験し、比較した。結果は下記の表8において提供する:
改質混釈平板法を使用して様々な製剤の抗菌効力を試験し、比較した。各テスト有機体の懸濁液の微生物集団を調合し、次のように判定した:
各指定された微生物の最近復活した保存種から、固形寒天培地の適切な体積の表面に接種する。
逆さにし、37℃にて、24−48時間、培養する。
Standard番号1.0に相当する。懸濁液濃度を分光光度計で測定し、必要に応じて濃度を調整する。
9mlの無菌PBSを無菌ピペットおよび球根を使用する8本の無菌試験管に添加する。汚染を防ぐため、使用中でないときに試験管は閉鎖しておく。
1ml(1000マイクロリットル)を原型の栽培から取り戻し、バクテリアが完全にその中に懸濁されるように混ぜて、第1(10−1)試験管に添加する。1mlを第1試験管から取り戻し、第2(10−2)試験管に添加し、上記同様に混合する。1mlを第2試験管から取り戻し、第3(10−3)試験管に添加し、上記同様に混合する。1mlを第3試験管から取り戻し、第4(10−4)試験管に添加し、上記同様に混合する。1mlを第4試験管から取り戻し、第5(10−5)試験管に添加し、上記同様に混合する。1mlを第5試験管から取り戻し、第6(10−6)試験管に添加し、上記同様に混合する。1mlを第6試験管から取り戻し、第7(10−7)試験管に添加し、上記同様に混合する。1mlを第7試験管から取り戻し、第8(10−8)試験管に添加し、上記同様に混合する。
寒天の表面上へ第4試験管から1mlを調剤し、サンプルを無菌のセル延展器(L形のガラス棒)を使用して全表面に拡げる。セル延展器を殺菌するため、プレートをエタノールに浸してアルコールを燃焼するため炎焼する。それぞれのプレートに各第6試験管および第8試験管から1mlを調剤することによって、2枚の付加プレート用にこの手順を繰り返す。37℃にて24〜48時間の培養のために倒置する前に、プレートを5分間乾燥する。
30および300の間のコロニーを有する同一希釈の2枚のプレートを識別する。そのプレート上のバクテリアコロニー(サイズに関係なく)の数を計数し、結果を記録する、そして、平均計数を算出する。選択された希釈プレートの平均計数を使用した原型の栽培の有機体の近似数を算出する。
mm)に注入する。適切なフラスコまたは瓶において、脱水寒天の所望量の重さを量り、脱イオン水を使用して、製造業者により推薦される濃度を達成する。撹拌機を有するホットプレートの上に配置して、瓶を沸騰させる。沸騰後、瓶を予め45℃に設定した水槽へ移す。温度が45℃にて安定するまで、寒天の温度を監視する。無菌のサンプルコップに、1Ogのテスト生成物を無菌計量する。酸化銀のかなり異なる濃度を含む製剤が比較されるときに、テスト生成物の重量は全てのサンプル用の酸化銀定数の総量を保つように調整され得る。
テスト生成物の微生物の最終濃度が1グラムにつきほぼ1×10−6cfuであるように、植菌物(概して約0.1ml)を試料コップのテスト生成物に添加する。無菌のガラス棒を用いて完全に混合し、均質サンプルを得る。
ブイヨンを添加し、良く混合する。
実施例33の改良混釈平板法を用いて、フェカリス菌のようなテスト有機体および水を含む水性製剤、ベントナイトおよびホホバ油の効力を評価した。結果は下記の表9において提供する:
実施例33の改良混釈平板法を用いて、フェカリス菌のようなテスト有機体および油性製剤の効力を評価した。結果は下記の表10において提供する:
Kirby−Bauer式検査を使用して次のように様々な製剤の抗菌効力を試験し、比較した:既製のMuller−Hilton寒天に、無菌アプリケータを用いた細菌性植菌物で縞をつけた。サンプルを5分間放置し、バクテリアを寒天表面に確実に付着させた。その後、抗菌性の無菌ブランクディスクを、既知数の被験製剤に対して押圧した。各ディスクへの付与量は測定しなかったものの、各ディスク上の材料の一貫した量を得ることに留意した。データを検証するために多重の複製ディスクを用いた。前記ディスクは寒天の表面に対して押圧され、ディスクまたは寒天に傷害を与えぬよう確かめた。各寒天板は、次いで逆さにされ、37℃にて24時間、インキュベータにおいて放置した。前記寒天板は次にインキュベータから除去され、阻害帯域は定規を用いて測定された。
フェカリス菌および黄色ブドウ球菌(ATCC番号25923)などのバクテリアの様々な個体菌株を用い、実施例44で詳述した手順を使用して様々な油性ならびに水性製剤の抗菌効力を試験し、比較した。
酸化銀の低い合計含有量にもかかわらず、サンプル46によって達成される比較的広い阻害帯域は、サンプル45に関して改良された抗菌効力を示す。
Internationale d’EclairageまたはCIE)によって指定され、百分率として表され、L* = 0は黒を表す、そして、L*
= 100は散乱性の白を表す。
Claims (8)
- 露出した身体組織への塗布用局所製剤であって、前記製剤は酸化銀(II)および酸化亜鉛を含み、前記酸化銀(II)および前記酸化亜鉛は担体媒質内で親密に分散し、
前記酸化銀(II)に対する前記酸化亜鉛の比は、重量比で0.5:1〜14:1である、局所製剤。 - 前記製剤は少なくとも0.05重量%の酸化銀(II)および、少なくとも0.05重量%の酸化亜鉛を含む、請求項1に記載の局所製剤。
- 前記製剤は25重量%未満、20重量%未満、15重量%未満、12重量%未満、または10重量%未満の酸化亜鉛を含む、請求項1または2に記載の局所製剤。
- 前記酸化銀(II)に対する前記酸化亜鉛の前記重量比が12:1未満、10:1未満または8:1未満である、請求項1〜3のいずれか1項に記載の局所製剤。
- 前記担体媒質が、液体蝋エステルをさらに含む、請求項1から4のいずれか1項に記載の局所製剤。
- 前記酸化銀(II)および酸化亜鉛は選択され、前記酸化銀(II)および酸化亜鉛は前記担体媒質内に分散し、そこで前記製剤の白色度は式:
L* ≧(L0 *)+ 2
を満たし、Lo *は、前記酸化亜鉛抜きの前記製剤の基準白色度値であり、L*は前記酸化亜鉛を含む前記製剤の白色度値である、請求項1〜5のいずれか1項に記載の局所製剤。 - 前記酸化銀(II)、前記酸化亜鉛および前記担体媒質は選択され、前記酸化銀(II)および前記酸化亜鉛は前記担体媒質内に分散し、前記製剤の前記白色度値L*は少なくとも75、少なくとも78、少なくとも80、または少なくとも82または少なくとも84である、請求項6に記載の局所製剤。
- 前記酸化銀(II)の含有量は少なくとも0.5重量%であり、前記酸化銀(II)、前記酸化亜鉛および前記担体媒質は選択され、前記酸化銀(II)および前記酸化亜鉛は前記担体媒質内に分散し、そこで、前記製剤の白色度値L*は少なくとも80、少なくとも82または少なくとも84である、請求項1〜5のいずれか1項に記載の局所製剤。
Applications Claiming Priority (5)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US22729709P | 2009-07-21 | 2009-07-21 | |
| US61/227,297 | 2009-07-21 | ||
| GB1003870.1 | 2010-03-09 | ||
| GB1003870A GB2472126B (en) | 2009-07-21 | 2010-03-09 | Topical Formulations Containing Silver (II) Oxide and Zinc Oxide |
| PCT/IB2010/002024 WO2011010221A1 (en) | 2009-07-21 | 2010-07-21 | Silver oxide formulations having improved whiteness characteristics |
Publications (3)
| Publication Number | Publication Date |
|---|---|
| JP2012533614A JP2012533614A (ja) | 2012-12-27 |
| JP2012533614A5 JP2012533614A5 (ja) | 2013-08-22 |
| JP5883785B2 true JP5883785B2 (ja) | 2016-03-15 |
Family
ID=42136680
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2012521116A Active JP5883785B2 (ja) | 2009-07-21 | 2010-07-21 | 改善した白色度特性を有する酸化銀製剤 |
Country Status (11)
| Country | Link |
|---|---|
| US (1) | US8647647B2 (ja) |
| EP (1) | EP2456447B1 (ja) |
| JP (1) | JP5883785B2 (ja) |
| KR (1) | KR101807885B1 (ja) |
| CN (1) | CN102470148B (ja) |
| AU (1) | AU2010274654B2 (ja) |
| CA (1) | CA2806198C (ja) |
| GB (1) | GB2472126B (ja) |
| IL (1) | IL217660A (ja) |
| WO (1) | WO2011010221A1 (ja) |
| ZA (1) | ZA201200963B (ja) |
Families Citing this family (9)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| GB2487438B8 (en) * | 2011-01-24 | 2014-08-06 | Aidance Skincare & Topical Solutions Llc | Stable silver oxide formulations |
| US9687509B2 (en) * | 2009-11-06 | 2017-06-27 | Aidance Skincare And Topical Solutions, Llc | Silver oxide formulations |
| WO2011097546A2 (en) * | 2010-02-06 | 2011-08-11 | Aidance Skincare And Topical Solutions, Llc | Topical antibiotic formulations |
| AU2015208739B2 (en) * | 2014-01-27 | 2020-04-16 | Aidance Skincare & Topical Solutions Llc | Topical antibiotic formulations |
| TWI754608B (zh) * | 2015-02-08 | 2022-02-11 | 以色列商阿爾賈曼技術有限公司 | 包含金屬氧化物之協同組合的皮膚再生材料 |
| TW201630994A (zh) * | 2015-02-08 | 2016-09-01 | 阿爾賈曼技術有限公司 | 使用於安全面罩及個人防護衣物的抗微生物織物材料 |
| US11224227B2 (en) | 2015-02-08 | 2022-01-18 | Argaman Technologies Ltd. | Antimicrobial material comprising synergistic combinations of metal oxides |
| CN107207771B (zh) | 2015-02-08 | 2019-12-06 | 阿尔贾曼技术有限公司 | 包含金属氧化物的协同组合的抗微生物材料 |
| CZ308301B6 (cs) * | 2018-09-17 | 2020-04-29 | Ĺ KODA AUTO a.s. | Soustava pro upevnění prosvětlené masky chladiče |
Family Cites Families (23)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US2521713A (en) * | 1945-07-23 | 1950-09-12 | Sunshine Mining Company | Method for producing a microbicidal composition of matter |
| US4489223A (en) * | 1982-07-28 | 1984-12-18 | Smart Start Corporation | Battery jump cable apparatus |
| EP0190504B1 (en) * | 1984-12-28 | 1993-04-21 | Johnson Matthey Public Limited Company | Antimicrobial compositions |
| WO1990009736A1 (en) * | 1989-02-28 | 1990-09-07 | Kanebo Ltd. | Antibacterial or conductive composition and applications thereof |
| JPH02268104A (ja) * | 1989-04-07 | 1990-11-01 | Kanebo Ltd | 抗菌性組成物 |
| JPH02265605A (ja) * | 1989-04-06 | 1990-10-30 | Tetsuo Nishida | 固液分離装置 |
| US5336499A (en) * | 1992-01-10 | 1994-08-09 | Antelman Technologies, Ltd. | Molecular crystal device for pharmaceuticals |
| US6258385B1 (en) * | 1999-04-22 | 2001-07-10 | Marantech Holding, Llc | Tetrasilver tetroxide treatment for skin conditions |
| JP2003519189A (ja) * | 2000-01-06 | 2003-06-17 | マランテック ホールディング リミテッド ライアビリティ カンパニー | 多価電子活性組成物、その製造方法及び使用方法 |
| US6669966B1 (en) * | 2000-01-06 | 2003-12-30 | Marantech Holding Llc | Compositions for facilitating skin growth and methods and articles using same |
| US6485755B1 (en) * | 2000-01-06 | 2002-11-26 | Marantech Holding | Methods of using electron active compounds for managing cancer |
| US6645531B1 (en) * | 2000-01-06 | 2003-11-11 | Marantech Holding Llc | Multivalent electron active compositions and methods of making and using same |
| US20060105057A1 (en) * | 2000-01-06 | 2006-05-18 | Marantech Holding, Llc | Compositions using tetrasilver tetroxide and methods for management of skin conditions using same |
| US20040247696A1 (en) * | 2001-07-05 | 2004-12-09 | Antelman Marvin S. | Methods of using electron active compounds for managing conditions afflicting mammals |
| BRPI0409420A (pt) * | 2003-04-18 | 2006-04-25 | Merck Patent Gmbh | pigmentos antimicrobianos |
| US20060017197A1 (en) * | 2004-07-20 | 2006-01-26 | Christensen Donald J | Coring of compression-molded phenolic |
| CN100394986C (zh) * | 2004-11-09 | 2008-06-18 | 深圳市源兴生物医药科技有限公司 | 一种含银锌组合物的创伤敷料 |
| CN1778313A (zh) * | 2004-11-22 | 2006-05-31 | 深圳市清华源兴生物医药科技有限公司 | 一种防治皮肤浅部真菌感染和妇女生殖道感染的药物 |
| US20060171971A1 (en) * | 2005-02-01 | 2006-08-03 | The Procter & Gamble Company | Composition for wet wipes containing a non-irritating skin health benefit ingredient and the process for making |
| JP5388575B2 (ja) * | 2005-06-27 | 2014-01-15 | スミス アンド ネフュー ピーエルシー | 抗微生物材料 |
| EP2043611A2 (en) * | 2006-06-30 | 2009-04-08 | Nucryst Pharmaceuticals Corp. | Metal-containing formulations and methods of use |
| WO2008089822A2 (en) * | 2007-01-23 | 2008-07-31 | Merck Patent Gmbh | Antimicrobial composition comprising zinc oxide, barium sulphate and silver ions |
| US8894980B2 (en) * | 2007-11-19 | 2014-11-25 | U.S. Cosmetics Corporation | Wet cake composition for cosmetic products and methods of use |
-
2010
- 2010-03-09 GB GB1003870A patent/GB2472126B/en not_active Expired - Fee Related
- 2010-07-21 WO PCT/IB2010/002024 patent/WO2011010221A1/en active Application Filing
- 2010-07-21 JP JP2012521116A patent/JP5883785B2/ja active Active
- 2010-07-21 KR KR1020127004440A patent/KR101807885B1/ko active IP Right Grant
- 2010-07-21 US US12/841,031 patent/US8647647B2/en active Active
- 2010-07-21 CN CN201080032704.7A patent/CN102470148B/zh active Active
- 2010-07-21 AU AU2010274654A patent/AU2010274654B2/en active Active
- 2010-07-21 CA CA2806198A patent/CA2806198C/en active Active
- 2010-07-21 EP EP10802014.0A patent/EP2456447B1/en active Active
-
2012
- 2012-01-19 IL IL217660A patent/IL217660A/en active IP Right Grant
- 2012-02-09 ZA ZA2012/00963A patent/ZA201200963B/en unknown
Also Published As
| Publication number | Publication date |
|---|---|
| GB2472126A (en) | 2011-01-26 |
| EP2456447A4 (en) | 2013-01-02 |
| AU2010274654A1 (en) | 2012-02-23 |
| EP2456447B1 (en) | 2016-08-24 |
| EP2456447A1 (en) | 2012-05-30 |
| WO2011010221A1 (en) | 2011-01-27 |
| CA2806198C (en) | 2018-02-13 |
| ZA201200963B (en) | 2013-05-29 |
| CN102470148A (zh) | 2012-05-23 |
| IL217660A (en) | 2016-02-29 |
| KR20120037017A (ko) | 2012-04-18 |
| AU2010274654B2 (en) | 2016-04-28 |
| CN102470148B (zh) | 2015-04-01 |
| KR101807885B1 (ko) | 2017-12-11 |
| CA2806198A1 (en) | 2011-01-27 |
| GB2472126B (en) | 2011-08-03 |
| US20110020468A1 (en) | 2011-01-27 |
| JP2012533614A (ja) | 2012-12-27 |
| GB201003870D0 (en) | 2010-04-21 |
| US8647647B2 (en) | 2014-02-11 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP5883785B2 (ja) | 改善した白色度特性を有する酸化銀製剤 | |
| CN105209049B (zh) | 抗微生物组合物及其制造方法 | |
| JP4176227B2 (ja) | 抗微生物組成物 | |
| CN101766552B (zh) | 一种免洗抗菌洗手液及其制备方法 | |
| CN111096912B (zh) | 一种双连续相型眼唇卸妆液及其制备方法 | |
| CN102138872B (zh) | 壳聚糖护肤液及其制备方法 | |
| CN107019686A (zh) | 抗微生物组合物 | |
| CN101588715A (zh) | 包含具有抗微生物性质的组合物的材料、物品和产品 | |
| CN105078793A (zh) | 一种抗菌凝胶洗手露及其制备方法 | |
| CN110420257A (zh) | 一种复合奶牛乳头药浴液及其制备方法 | |
| CN113440441A (zh) | 一种含精油的口腔抑菌组合物及其制备方法 | |
| CA2990627A1 (en) | Topical antiseptic system | |
| JP2004107667A (ja) | 手消毒洗浄剤 | |
| US9629913B2 (en) | Silver oxide formulations | |
| CN109847019A (zh) | 一种用于卫生用品的抑菌组合物及其制备方法 | |
| CN108992462A (zh) | 一种复方聚维酮碘组合物及其制备方法 | |
| JP2022522992A (ja) | 爪甲真菌症のためのワセリンベースphmb組成物及び治療方法 | |
| KR101095789B1 (ko) | 비수계 화장품용 유용성 방부 대체제 조성물 | |
| US10391124B2 (en) | Silver oxide formulations | |
| JPH03157311A (ja) | にきび用化粧料 | |
| KR20230135304A (ko) | 1,2-데칸다이올을 유효 성분으로 포함하는 보존제 조성물 및 이의 제조 방법 | |
| JP2023086964A (ja) | バイオフィルム除去剤 | |
| Unachukwu et al. | Antimicrobial spectrum of honey for aerobic organisms as seen at the National Orthopaedic Hospital, Enugu | |
| KR20110058260A (ko) | 화장료 조성물 | |
| TW202128124A (zh) | 葉黃素之藍光截止能力增強劑及化妝品組成物 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20130705 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20130705 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20140805 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20141031 |
|
| A602 | Written permission of extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A602 Effective date: 20141110 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20141203 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20150507 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20150803 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20160112 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20160208 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 5883785 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |