JP5521999B2 - 化学増幅型フォトレジスト組成物及びレジストパターンの製造方法 - Google Patents
化学増幅型フォトレジスト組成物及びレジストパターンの製造方法 Download PDFInfo
- Publication number
- JP5521999B2 JP5521999B2 JP2010259844A JP2010259844A JP5521999B2 JP 5521999 B2 JP5521999 B2 JP 5521999B2 JP 2010259844 A JP2010259844 A JP 2010259844A JP 2010259844 A JP2010259844 A JP 2010259844A JP 5521999 B2 JP5521999 B2 JP 5521999B2
- Authority
- JP
- Japan
- Prior art keywords
- group
- formula
- hydrocarbon group
- substituent
- acid
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
- 239000000203 mixture Substances 0.000 title claims description 103
- 229920002120 photoresistant polymer Polymers 0.000 title claims description 29
- 238000004519 manufacturing process Methods 0.000 title claims description 6
- -1 triarylsulfonium cation Chemical class 0.000 claims description 294
- 239000002253 acid Substances 0.000 claims description 144
- 229920005989 resin Polymers 0.000 claims description 87
- 239000011347 resin Substances 0.000 claims description 87
- 125000001931 aliphatic group Chemical group 0.000 claims description 74
- 125000000753 cycloalkyl group Chemical group 0.000 claims description 69
- 125000001424 substituent group Chemical group 0.000 claims description 62
- 150000001875 compounds Chemical class 0.000 claims description 41
- 125000004435 hydrogen atom Chemical group [H]* 0.000 claims description 32
- 125000003118 aryl group Chemical group 0.000 claims description 25
- 238000010438 heat treatment Methods 0.000 claims description 22
- 125000005073 adamantyl group Chemical group C12(CC3CC(CC(C1)C3)C2)* 0.000 claims description 16
- 229910052731 fluorine Inorganic materials 0.000 claims description 16
- 125000001153 fluoro group Chemical group F* 0.000 claims description 15
- 229930195734 saturated hydrocarbon Natural products 0.000 claims description 15
- 125000003277 amino group Chemical group 0.000 claims description 14
- WKBALTUBRZPIPZ-UHFFFAOYSA-N 2,6-di(propan-2-yl)aniline Chemical compound CC(C)C1=CC=CC(C(C)C)=C1N WKBALTUBRZPIPZ-UHFFFAOYSA-N 0.000 claims description 8
- 238000001035 drying Methods 0.000 claims description 7
- 239000000758 substrate Substances 0.000 claims description 6
- 150000003839 salts Chemical group 0.000 claims description 5
- 125000006663 (C1-C6) perfluoroalkyl group Chemical group 0.000 claims description 4
- 150000002892 organic cations Chemical class 0.000 claims description 4
- 125000006672 (C1-C18) aliphatic hydrocarbon group Chemical group 0.000 claims description 3
- 150000001338 aliphatic hydrocarbons Chemical class 0.000 claims description 3
- 239000011737 fluorine Substances 0.000 claims description 3
- 125000001183 hydrocarbyl group Chemical group 0.000 claims 2
- 239000000178 monomer Substances 0.000 description 120
- 125000002887 hydroxy group Chemical group [H]O* 0.000 description 50
- 125000002029 aromatic hydrocarbon group Chemical group 0.000 description 31
- 238000011161 development Methods 0.000 description 31
- 239000007864 aqueous solution Substances 0.000 description 28
- 150000002430 hydrocarbons Chemical group 0.000 description 25
- 239000002904 solvent Substances 0.000 description 25
- 125000002496 methyl group Chemical group [H]C([H])([H])* 0.000 description 23
- 239000000243 solution Substances 0.000 description 22
- SNOOUWRIMMFWNE-UHFFFAOYSA-M sodium;6-[(3,4,5-trimethoxybenzoyl)amino]hexanoate Chemical compound [Na+].COC1=CC(C(=O)NCCCCCC([O-])=O)=CC(OC)=C1OC SNOOUWRIMMFWNE-UHFFFAOYSA-M 0.000 description 21
- WGTYBPLFGIVFAS-UHFFFAOYSA-M tetramethylammonium hydroxide Chemical compound [OH-].C[N+](C)(C)C WGTYBPLFGIVFAS-UHFFFAOYSA-M 0.000 description 20
- YEJRWHAVMIAJKC-UHFFFAOYSA-N 4-Butyrolactone Chemical group O=C1CCCO1 YEJRWHAVMIAJKC-UHFFFAOYSA-N 0.000 description 19
- 150000001768 cations Chemical class 0.000 description 18
- 125000005843 halogen group Chemical group 0.000 description 18
- 125000000217 alkyl group Chemical group 0.000 description 15
- 150000002596 lactones Chemical group 0.000 description 14
- 229910052710 silicon Inorganic materials 0.000 description 14
- 239000010703 silicon Substances 0.000 description 14
- XUIMIQQOPSSXEZ-UHFFFAOYSA-N Silicon Chemical compound [Si] XUIMIQQOPSSXEZ-UHFFFAOYSA-N 0.000 description 13
- 229920001577 copolymer Polymers 0.000 description 13
- 239000010410 layer Substances 0.000 description 13
- OKKJLVBELUTLKV-UHFFFAOYSA-N Methanol Chemical compound OC OKKJLVBELUTLKV-UHFFFAOYSA-N 0.000 description 12
- 239000003513 alkali Substances 0.000 description 12
- 125000003545 alkoxy group Chemical group 0.000 description 12
- 229910052799 carbon Inorganic materials 0.000 description 12
- 125000002723 alicyclic group Chemical group 0.000 description 11
- 230000015572 biosynthetic process Effects 0.000 description 11
- 125000001495 ethyl group Chemical group [H]C([H])([H])C([H])([H])* 0.000 description 11
- 238000003786 synthesis reaction Methods 0.000 description 11
- NIXOWILDQLNWCW-UHFFFAOYSA-M Acrylate Chemical compound [O-]C(=O)C=C NIXOWILDQLNWCW-UHFFFAOYSA-M 0.000 description 10
- 125000004122 cyclic group Chemical group 0.000 description 10
- 125000000113 cyclohexyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])(*)C([H])([H])C1([H])[H] 0.000 description 10
- 125000002947 alkylene group Chemical group 0.000 description 9
- 238000007654 immersion Methods 0.000 description 9
- 125000001436 propyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])[H] 0.000 description 9
- 125000004642 (C1-C12) alkoxy group Chemical group 0.000 description 8
- 125000004191 (C1-C6) alkoxy group Chemical group 0.000 description 8
- OZAIFHULBGXAKX-UHFFFAOYSA-N 2-(2-cyanopropan-2-yldiazenyl)-2-methylpropanenitrile Chemical compound N#CC(C)(C)N=NC(C)(C)C#N OZAIFHULBGXAKX-UHFFFAOYSA-N 0.000 description 8
- PAYRUJLWNCNPSJ-UHFFFAOYSA-N Aniline Chemical compound NC1=CC=CC=C1 PAYRUJLWNCNPSJ-UHFFFAOYSA-N 0.000 description 8
- 125000003178 carboxy group Chemical group [H]OC(*)=O 0.000 description 8
- CATSNJVOTSVZJV-UHFFFAOYSA-N heptan-2-one Chemical compound CCCCCC(C)=O CATSNJVOTSVZJV-UHFFFAOYSA-N 0.000 description 8
- 238000000034 method Methods 0.000 description 8
- 125000004043 oxo group Chemical group O=* 0.000 description 8
- 230000035945 sensitivity Effects 0.000 description 8
- 125000006671 (C6-C18) aromatic hydrocarbon group Chemical group 0.000 description 7
- 150000001450 anions Chemical class 0.000 description 7
- 125000000999 tert-butyl group Chemical group [H]C([H])([H])C(*)(C([H])([H])[H])C([H])([H])[H] 0.000 description 7
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 7
- 125000006673 (C1-C12) aliphatic hydrocarbon group Chemical group 0.000 description 6
- 125000004169 (C1-C6) alkyl group Chemical group 0.000 description 6
- OKTJSMMVPCPJKN-UHFFFAOYSA-N Carbon Chemical group [C] OKTJSMMVPCPJKN-UHFFFAOYSA-N 0.000 description 6
- ZMXDDKWLCZADIW-UHFFFAOYSA-N N,N-Dimethylformamide Chemical compound CN(C)C=O ZMXDDKWLCZADIW-UHFFFAOYSA-N 0.000 description 6
- 150000001721 carbon Chemical group 0.000 description 6
- 238000006243 chemical reaction Methods 0.000 description 6
- 125000001449 isopropyl group Chemical group [H]C([H])([H])C([H])(*)C([H])([H])[H] 0.000 description 6
- 125000002950 monocyclic group Chemical group 0.000 description 6
- 125000002914 sec-butyl group Chemical group [H]C([H])([H])C([H])([H])C([H])(*)C([H])([H])[H] 0.000 description 6
- 125000001544 thienyl group Chemical group 0.000 description 6
- 125000004178 (C1-C4) alkyl group Chemical group 0.000 description 5
- 150000004982 aromatic amines Chemical class 0.000 description 5
- 125000004093 cyano group Chemical group *C#N 0.000 description 5
- 238000001459 lithography Methods 0.000 description 5
- 238000005259 measurement Methods 0.000 description 5
- 125000004108 n-butyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 5
- UMRZSTCPUPJPOJ-KNVOCYPGSA-N norbornane Chemical group C1C[C@H]2CC[C@@H]1C2 UMRZSTCPUPJPOJ-KNVOCYPGSA-N 0.000 description 5
- 125000002023 trifluoromethyl group Chemical group FC(F)(F)* 0.000 description 5
- 125000006674 (C1-C36) aliphatic hydrocarbon group Chemical group 0.000 description 4
- RYHBNJHYFVUHQT-UHFFFAOYSA-N 1,4-Dioxane Chemical compound C1COCCO1 RYHBNJHYFVUHQT-UHFFFAOYSA-N 0.000 description 4
- ARXJGSRGQADJSQ-UHFFFAOYSA-N 1-methoxypropan-2-ol Chemical compound COCC(C)O ARXJGSRGQADJSQ-UHFFFAOYSA-N 0.000 description 4
- GQHTUMJGOHRCHB-UHFFFAOYSA-N 2,3,4,6,7,8,9,10-octahydropyrimido[1,2-a]azepine Chemical compound C1CCCCN2CCCN=C21 GQHTUMJGOHRCHB-UHFFFAOYSA-N 0.000 description 4
- WYGWHHGCAGTUCH-UHFFFAOYSA-N 2-[(2-cyano-4-methylpentan-2-yl)diazenyl]-2,4-dimethylpentanenitrile Chemical compound CC(C)CC(C)(C#N)N=NC(C)(C#N)CC(C)C WYGWHHGCAGTUCH-UHFFFAOYSA-N 0.000 description 4
- HEDRZPFGACZZDS-UHFFFAOYSA-N Chloroform Chemical compound ClC(Cl)Cl HEDRZPFGACZZDS-UHFFFAOYSA-N 0.000 description 4
- JUJWROOIHBZHMG-UHFFFAOYSA-N Pyridine Chemical compound C1=CC=NC=C1 JUJWROOIHBZHMG-UHFFFAOYSA-N 0.000 description 4
- PPBRXRYQALVLMV-UHFFFAOYSA-N Styrene Chemical compound C=CC1=CC=CC=C1 PPBRXRYQALVLMV-UHFFFAOYSA-N 0.000 description 4
- WYURNTSHIVDZCO-UHFFFAOYSA-N Tetrahydrofuran Chemical compound C1CCOC1 WYURNTSHIVDZCO-UHFFFAOYSA-N 0.000 description 4
- 125000004453 alkoxycarbonyl group Chemical group 0.000 description 4
- 125000003710 aryl alkyl group Chemical group 0.000 description 4
- 239000003999 initiator Substances 0.000 description 4
- ZXEKIIBDNHEJCQ-UHFFFAOYSA-N isobutanol Chemical compound CC(C)CO ZXEKIIBDNHEJCQ-UHFFFAOYSA-N 0.000 description 4
- 125000000956 methoxy group Chemical group [H]C([H])([H])O* 0.000 description 4
- 125000003518 norbornenyl group Chemical group C12(C=CC(CC1)C2)* 0.000 description 4
- ISWSIDIOOBJBQZ-UHFFFAOYSA-N phenol group Chemical group C1(=CC=CC=C1)O ISWSIDIOOBJBQZ-UHFFFAOYSA-N 0.000 description 4
- LLHKCFNBLRBOGN-UHFFFAOYSA-N propylene glycol methyl ether acetate Chemical compound COCC(C)OC(C)=O LLHKCFNBLRBOGN-UHFFFAOYSA-N 0.000 description 4
- 239000007787 solid Substances 0.000 description 4
- VDZOOKBUILJEDG-UHFFFAOYSA-M tetrabutylammonium hydroxide Chemical compound [OH-].CCCC[N+](CCCC)(CCCC)CCCC VDZOOKBUILJEDG-UHFFFAOYSA-M 0.000 description 4
- 239000012953 triphenylsulfonium Substances 0.000 description 4
- 125000006662 (C2-C4) acyloxy group Chemical group 0.000 description 3
- IMNFDUFMRHMDMM-UHFFFAOYSA-N N-Heptane Chemical compound CCCCCCC IMNFDUFMRHMDMM-UHFFFAOYSA-N 0.000 description 3
- HEMHJVSKTPXQMS-UHFFFAOYSA-M Sodium hydroxide Chemical compound [OH-].[Na+] HEMHJVSKTPXQMS-UHFFFAOYSA-M 0.000 description 3
- ZMANZCXQSJIPKH-UHFFFAOYSA-N Triethylamine Chemical compound CCN(CC)CC ZMANZCXQSJIPKH-UHFFFAOYSA-N 0.000 description 3
- NIXOWILDQLNWCW-UHFFFAOYSA-N acrylic acid group Chemical group C(C=C)(=O)O NIXOWILDQLNWCW-UHFFFAOYSA-N 0.000 description 3
- 239000000908 ammonium hydroxide Substances 0.000 description 3
- FYGUSUBEMUKACF-UHFFFAOYSA-N bicyclo[2.2.1]hept-2-ene-5-carboxylic acid Chemical compound C1C2C(C(=O)O)CC1C=C2 FYGUSUBEMUKACF-UHFFFAOYSA-N 0.000 description 3
- 125000004432 carbon atom Chemical group C* 0.000 description 3
- 239000011203 carbon fibre reinforced carbon Substances 0.000 description 3
- OEYIOHPDSNJKLS-UHFFFAOYSA-N choline Chemical compound C[N+](C)(C)CCO OEYIOHPDSNJKLS-UHFFFAOYSA-N 0.000 description 3
- 229960001231 choline Drugs 0.000 description 3
- 230000000052 comparative effect Effects 0.000 description 3
- 150000004292 cyclic ethers Chemical group 0.000 description 3
- 125000000582 cycloheptyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])([H])C([H])(*)C([H])([H])C1([H])[H] 0.000 description 3
- JHIVVAPYMSGYDF-UHFFFAOYSA-N cyclohexanone Chemical group O=C1CCCCC1 JHIVVAPYMSGYDF-UHFFFAOYSA-N 0.000 description 3
- 230000006837 decompression Effects 0.000 description 3
- 125000004663 dialkyl amino group Chemical group 0.000 description 3
- 238000001704 evaporation Methods 0.000 description 3
- 125000004051 hexyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 3
- 125000004029 hydroxymethyl group Chemical group [H]OC([H])([H])* 0.000 description 3
- RAXXELZNTBOGNW-UHFFFAOYSA-N imidazole Natural products C1=CNC=N1 RAXXELZNTBOGNW-UHFFFAOYSA-N 0.000 description 3
- 125000000959 isobutyl group Chemical group [H]C([H])([H])C([H])(C([H])([H])[H])C([H])([H])* 0.000 description 3
- 239000012046 mixed solvent Substances 0.000 description 3
- 125000001624 naphthyl group Chemical group 0.000 description 3
- 125000001147 pentyl group Chemical group C(CCCC)* 0.000 description 3
- 125000005010 perfluoroalkyl group Chemical group 0.000 description 3
- 125000005003 perfluorobutyl group Chemical group FC(F)(F)C(F)(F)C(F)(F)C(F)(F)* 0.000 description 3
- 125000005004 perfluoroethyl group Chemical group FC(F)(F)C(F)(F)* 0.000 description 3
- 125000005008 perfluoropentyl group Chemical group FC(C(C(C(C(F)(F)F)(F)F)(F)F)(F)F)(F)* 0.000 description 3
- 125000005009 perfluoropropyl group Chemical group FC(C(C(F)(F)F)(F)F)(F)* 0.000 description 3
- 125000001997 phenyl group Chemical group [H]C1=C([H])C([H])=C(*)C([H])=C1[H] 0.000 description 3
- 230000000379 polymerizing effect Effects 0.000 description 3
- 239000011148 porous material Substances 0.000 description 3
- 238000003756 stirring Methods 0.000 description 3
- 238000013519 translation Methods 0.000 description 3
- 230000014616 translation Effects 0.000 description 3
- 229930195735 unsaturated hydrocarbon Natural products 0.000 description 3
- DTGKSKDOIYIVQL-WEDXCCLWSA-N (+)-borneol Chemical group C1C[C@@]2(C)[C@@H](O)C[C@@H]1C2(C)C DTGKSKDOIYIVQL-WEDXCCLWSA-N 0.000 description 2
- 125000006676 (C1-C4) aliphatic hydrocarbon group Chemical group 0.000 description 2
- JGTNAGYHADQMCM-UHFFFAOYSA-M 1,1,2,2,3,3,4,4,4-nonafluorobutane-1-sulfonate Chemical compound [O-]S(=O)(=O)C(F)(F)C(F)(F)C(F)(F)C(F)(F)F JGTNAGYHADQMCM-UHFFFAOYSA-M 0.000 description 2
- MMTQYTFKDNOQOV-UHFFFAOYSA-M 1,1-difluoro-2-[(3-hydroxy-1-adamantyl)methoxy]-2-oxoethanesulfonate;triphenylsulfanium Chemical compound C1=CC=CC=C1[S+](C=1C=CC=CC=1)C1=CC=CC=C1.C1C(C2)CC3CC1(O)CC2(COC(=O)C(F)(F)S([O-])(=O)=O)C3 MMTQYTFKDNOQOV-UHFFFAOYSA-M 0.000 description 2
- OQZAQBGJENJMHT-UHFFFAOYSA-N 1,3-dibromo-5-methoxybenzene Chemical compound COC1=CC(Br)=CC(Br)=C1 OQZAQBGJENJMHT-UHFFFAOYSA-N 0.000 description 2
- SGUVLZREKBPKCE-UHFFFAOYSA-N 1,5-diazabicyclo[4.3.0]-non-5-ene Chemical compound C1CCN=C2CCCN21 SGUVLZREKBPKCE-UHFFFAOYSA-N 0.000 description 2
- DQYLOECNFGCJJO-UHFFFAOYSA-N 1-[(2-chlorophenyl)methyl]-3,4,6,7,8,8a-hexahydro-2h-pyrrolo[1,2-a]pyrimidine Chemical compound ClC1=CC=CC=C1CN1C2CCCN2CCC1 DQYLOECNFGCJJO-UHFFFAOYSA-N 0.000 description 2
- LLTYSYWKRVZEDT-UHFFFAOYSA-N 1-[(2-chlorophenyl)methyl]-3,4,6,7,8,9,10,10a-octahydro-2h-pyrimido[1,2-a]azepine Chemical compound ClC1=CC=CC=C1CN1C2CCCCCN2CCC1 LLTYSYWKRVZEDT-UHFFFAOYSA-N 0.000 description 2
- WJCDJUMRNUMRLR-UHFFFAOYSA-N 1-[(4-methylphenyl)methyl]-3,4,6,7,8,8a-hexahydro-2h-pyrrolo[1,2-a]pyrimidine Chemical compound C1=CC(C)=CC=C1CN1C2CCCN2CCC1 WJCDJUMRNUMRLR-UHFFFAOYSA-N 0.000 description 2
- HYQWHUCTTYCIAU-UHFFFAOYSA-N 1-benzyl-3,4,6,7,8,8a-hexahydro-2h-pyrrolo[1,2-a]pyrimidine Chemical compound C1CCN2CCCC2N1CC1=CC=CC=C1 HYQWHUCTTYCIAU-UHFFFAOYSA-N 0.000 description 2
- AMDNICFZCMZSPD-UHFFFAOYSA-N 1-benzyl-3,4,6,7,8,9,10,10a-octahydro-2h-pyrimido[1,2-a]azepine Chemical compound C1CCN2CCCCCC2N1CC1=CC=CC=C1 AMDNICFZCMZSPD-UHFFFAOYSA-N 0.000 description 2
- RUFPHBVGCFYCNW-UHFFFAOYSA-N 1-naphthylamine Chemical compound C1=CC=C2C(N)=CC=CC2=C1 RUFPHBVGCFYCNW-UHFFFAOYSA-N 0.000 description 2
- 125000000954 2-hydroxyethyl group Chemical group [H]C([*])([H])C([H])([H])O[H] 0.000 description 2
- KIZQNNOULOCVDM-UHFFFAOYSA-M 2-hydroxyethyl(trimethyl)azanium;hydroxide Chemical compound [OH-].C[N+](C)(C)CCO KIZQNNOULOCVDM-UHFFFAOYSA-M 0.000 description 2
- XLLIQLLCWZCATF-UHFFFAOYSA-N 2-methoxyethyl acetate Chemical compound COCCOC(C)=O XLLIQLLCWZCATF-UHFFFAOYSA-N 0.000 description 2
- FUGYGGDSWSUORM-UHFFFAOYSA-N 4-hydroxystyrene Chemical compound OC1=CC=C(C=C)C=C1 FUGYGGDSWSUORM-UHFFFAOYSA-N 0.000 description 2
- 125000004172 4-methoxyphenyl group Chemical group [H]C1=C([H])C(OC([H])([H])[H])=C([H])C([H])=C1* 0.000 description 2
- XLSZMDLNRCVEIJ-UHFFFAOYSA-N 4-methylimidazole Chemical compound CC1=CNC=N1 XLSZMDLNRCVEIJ-UHFFFAOYSA-N 0.000 description 2
- 125000000590 4-methylphenyl group Chemical group [H]C1=C([H])C(=C([H])C([H])=C1*)C([H])([H])[H] 0.000 description 2
- FKNQCJSGGFJEIZ-UHFFFAOYSA-N 4-methylpyridine Chemical compound CC1=CC=NC=C1 FKNQCJSGGFJEIZ-UHFFFAOYSA-N 0.000 description 2
- ZUCMQTPLDXFQTG-UHFFFAOYSA-N 9-[(2-nitrophenyl)methyl]-1,2,3,4,6,7,8,9,10,10a-decahydropyrimido[1,2-a]azepine Chemical compound [O-][N+](=O)C1=CC=CC=C1CC1CC2NCCCN2CCC1 ZUCMQTPLDXFQTG-UHFFFAOYSA-N 0.000 description 2
- CSCPPACGZOOCGX-UHFFFAOYSA-N Acetone Chemical compound CC(C)=O CSCPPACGZOOCGX-UHFFFAOYSA-N 0.000 description 2
- VEXZGXHMUGYJMC-UHFFFAOYSA-N Hydrochloric acid Chemical compound Cl VEXZGXHMUGYJMC-UHFFFAOYSA-N 0.000 description 2
- CERQOIWHTDAKMF-UHFFFAOYSA-M Methacrylate Chemical compound CC(=C)C([O-])=O CERQOIWHTDAKMF-UHFFFAOYSA-M 0.000 description 2
- CERQOIWHTDAKMF-UHFFFAOYSA-N Methacrylic acid Chemical compound CC(=C)C(O)=O CERQOIWHTDAKMF-UHFFFAOYSA-N 0.000 description 2
- YNAVUWVOSKDBBP-UHFFFAOYSA-N Morpholine Chemical compound C1COCCN1 YNAVUWVOSKDBBP-UHFFFAOYSA-N 0.000 description 2
- JLTDJTHDQAWBAV-UHFFFAOYSA-N N,N-dimethylaniline Chemical compound CN(C)C1=CC=CC=C1 JLTDJTHDQAWBAV-UHFFFAOYSA-N 0.000 description 2
- AFBPFSWMIHJQDM-UHFFFAOYSA-N N-methylaniline Chemical compound CNC1=CC=CC=C1 AFBPFSWMIHJQDM-UHFFFAOYSA-N 0.000 description 2
- DMBHHRLKUKUOEG-UHFFFAOYSA-N N-phenyl aniline Natural products C=1C=CC=CC=1NC1=CC=CC=C1 DMBHHRLKUKUOEG-UHFFFAOYSA-N 0.000 description 2
- GLUUGHFHXGJENI-UHFFFAOYSA-N Piperazine Chemical compound C1CNCCN1 GLUUGHFHXGJENI-UHFFFAOYSA-N 0.000 description 2
- NQRYJNQNLNOLGT-UHFFFAOYSA-N Piperidine Chemical compound C1CCNCC1 NQRYJNQNLNOLGT-UHFFFAOYSA-N 0.000 description 2
- 239000004793 Polystyrene Substances 0.000 description 2
- 125000003647 acryloyl group Chemical group O=C([*])C([H])=C([H])[H] 0.000 description 2
- 125000002252 acyl group Chemical group 0.000 description 2
- 125000003282 alkyl amino group Chemical group 0.000 description 2
- 125000005196 alkyl carbonyloxy group Chemical group 0.000 description 2
- 150000001412 amines Chemical class 0.000 description 2
- 125000005428 anthryl group Chemical group [H]C1=C([H])C([H])=C2C([H])=C3C(*)=C([H])C([H])=C([H])C3=C([H])C2=C1[H] 0.000 description 2
- 125000006615 aromatic heterocyclic group Chemical group 0.000 description 2
- 125000001797 benzyl group Chemical group [H]C1=C([H])C([H])=C(C([H])=C1[H])C([H])([H])* 0.000 description 2
- 125000002915 carbonyl group Chemical group [*:2]C([*:1])=O 0.000 description 2
- PFKFTWBEEFSNDU-UHFFFAOYSA-N carbonyldiimidazole Chemical compound C1=CN=CN1C(=O)N1C=CN=C1 PFKFTWBEEFSNDU-UHFFFAOYSA-N 0.000 description 2
- 125000001511 cyclopentyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])(*)C1([H])[H] 0.000 description 2
- NNBZCPXTIHJBJL-UHFFFAOYSA-N decalin Chemical group C1CCCC2CCCCC21 NNBZCPXTIHJBJL-UHFFFAOYSA-N 0.000 description 2
- JQVDAXLFBXTEQA-UHFFFAOYSA-N dibutylamine Chemical compound CCCCNCCCC JQVDAXLFBXTEQA-UHFFFAOYSA-N 0.000 description 2
- ZBCBWPMODOFKDW-UHFFFAOYSA-N diethanolamine Chemical compound OCCNCCO ZBCBWPMODOFKDW-UHFFFAOYSA-N 0.000 description 2
- 125000001664 diethylamino group Chemical group [H]C([H])([H])C([H])([H])N(*)C([H])([H])C([H])([H])[H] 0.000 description 2
- 125000002147 dimethylamino group Chemical group [H]C([H])([H])N(*)C([H])([H])[H] 0.000 description 2
- 238000001312 dry etching Methods 0.000 description 2
- 239000000975 dye Substances 0.000 description 2
- 239000003480 eluent Substances 0.000 description 2
- LZCLXQDLBQLTDK-UHFFFAOYSA-N ethyl 2-hydroxypropanoate Chemical compound CCOC(=O)C(C)O LZCLXQDLBQLTDK-UHFFFAOYSA-N 0.000 description 2
- 238000005227 gel permeation chromatography Methods 0.000 description 2
- 229940035429 isobutyl alcohol Drugs 0.000 description 2
- 239000012528 membrane Substances 0.000 description 2
- LTXRZOZLUURSKO-UHFFFAOYSA-N methyl 4-(3,4,6,7,8,8a-hexahydro-2h-pyrrolo[1,2-a]pyrimidin-1-ylmethyl)benzoate Chemical compound C1=CC(C(=O)OC)=CC=C1CN1C2CCCN2CCC1 LTXRZOZLUURSKO-UHFFFAOYSA-N 0.000 description 2
- 125000002868 norbornyl group Chemical group C12(CCC(CC1)C2)* 0.000 description 2
- 125000002347 octyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 description 2
- 239000012044 organic layer Substances 0.000 description 2
- RNVCVTLRINQCPJ-UHFFFAOYSA-N ortho-methyl aniline Natural products CC1=CC=CC=C1N RNVCVTLRINQCPJ-UHFFFAOYSA-N 0.000 description 2
- RZXMPPFPUUCRFN-UHFFFAOYSA-N p-toluidine Chemical compound CC1=CC=C(N)C=C1 RZXMPPFPUUCRFN-UHFFFAOYSA-N 0.000 description 2
- 125000005005 perfluorohexyl group Chemical group FC(F)(F)C(F)(F)C(F)(F)C(F)(F)C(F)(F)C(F)(F)* 0.000 description 2
- 125000005561 phenanthryl group Chemical group 0.000 description 2
- 125000003386 piperidinyl group Chemical group 0.000 description 2
- 125000003367 polycyclic group Chemical group 0.000 description 2
- 238000006116 polymerization reaction Methods 0.000 description 2
- 229920002223 polystyrene Polymers 0.000 description 2
- KIDHWZJUCRJVML-UHFFFAOYSA-N putrescine Chemical compound NCCCCN KIDHWZJUCRJVML-UHFFFAOYSA-N 0.000 description 2
- UMJSCPRVCHMLSP-UHFFFAOYSA-N pyridine Natural products COC1=CC=CN=C1 UMJSCPRVCHMLSP-UHFFFAOYSA-N 0.000 description 2
- 125000001453 quaternary ammonium group Chemical group 0.000 description 2
- 230000005855 radiation Effects 0.000 description 2
- 239000004065 semiconductor Substances 0.000 description 2
- XSQIGJCTPAJWQT-UHFFFAOYSA-M sodium;1,1-difluoro-2-hydroxy-2-oxoethanesulfonate Chemical compound [Na+].OS(=O)(=O)C(F)(F)C([O-])=O XSQIGJCTPAJWQT-UHFFFAOYSA-M 0.000 description 2
- BDHFUVZGWQCTTF-UHFFFAOYSA-M sulfonate Chemical compound [O-]S(=O)=O BDHFUVZGWQCTTF-UHFFFAOYSA-M 0.000 description 2
- 150000003457 sulfones Chemical class 0.000 description 2
- 150000008053 sultones Chemical class 0.000 description 2
- YLQBMQCUIZJEEH-UHFFFAOYSA-N tetrahydrofuran Natural products C=1C=COC=1 YLQBMQCUIZJEEH-UHFFFAOYSA-N 0.000 description 2
- DCFYRBLFVWYBIJ-UHFFFAOYSA-M tetraoctylazanium;hydroxide Chemical compound [OH-].CCCCCCCC[N+](CCCCCCCC)(CCCCCCCC)CCCCCCCC DCFYRBLFVWYBIJ-UHFFFAOYSA-M 0.000 description 2
- ITMCEJHCFYSIIV-UHFFFAOYSA-N triflic acid Chemical compound OS(=O)(=O)C(F)(F)F ITMCEJHCFYSIIV-UHFFFAOYSA-N 0.000 description 2
- BFPOZPZYPNVMHU-UHFFFAOYSA-M trimethyl-[3-(trifluoromethyl)phenyl]azanium;hydroxide Chemical compound [OH-].C[N+](C)(C)C1=CC=CC(C(F)(F)F)=C1 BFPOZPZYPNVMHU-UHFFFAOYSA-M 0.000 description 2
- GETQZCLCWQTVFV-UHFFFAOYSA-N trimethylamine Chemical compound CN(C)C GETQZCLCWQTVFV-UHFFFAOYSA-N 0.000 description 2
- HADKRTWCOYPCPH-UHFFFAOYSA-M trimethylphenylammonium hydroxide Chemical compound [OH-].C[N+](C)(C)C1=CC=CC=C1 HADKRTWCOYPCPH-UHFFFAOYSA-M 0.000 description 2
- WLOQLWBIJZDHET-UHFFFAOYSA-N triphenylsulfonium Chemical compound C1=CC=CC=C1[S+](C=1C=CC=CC=1)C1=CC=CC=C1 WLOQLWBIJZDHET-UHFFFAOYSA-N 0.000 description 2
- 125000005023 xylyl group Chemical group 0.000 description 2
- ABUIKOPEGIZINI-UHFFFAOYSA-N (1-ethylcyclohexyl) 2-methylprop-2-enoate Chemical compound CC(=C)C(=O)OC1(CC)CCCCC1 ABUIKOPEGIZINI-UHFFFAOYSA-N 0.000 description 1
- WDKWRJUAIFFOII-UHFFFAOYSA-N (2-ethyl-2-adamantyl) bicyclo[2.2.1]hept-2-ene-5-carboxylate Chemical compound C1C(C2)CC3CC1C(CC)(OC(=O)C1C4CC(C=C4)C1)C2C3 WDKWRJUAIFFOII-UHFFFAOYSA-N 0.000 description 1
- OJGSGTWNQWAFBE-UHFFFAOYSA-N (2-methyl-2-adamantyl) bicyclo[2.2.1]hept-2-ene-5-carboxylate Chemical compound C1C(C2)CC3CC1C(C)(OC(=O)C1C4CC(C=C4)C1)C2C3 OJGSGTWNQWAFBE-UHFFFAOYSA-N 0.000 description 1
- HFLCKUMNXPOLSN-UHFFFAOYSA-N (3,5-dihydroxy-1-adamantyl) 2-methylprop-2-enoate Chemical compound C1C(C2)CC3(O)CC2(O)CC1(OC(=O)C(=C)C)C3 HFLCKUMNXPOLSN-UHFFFAOYSA-N 0.000 description 1
- OOIBFPKQHULHSQ-UHFFFAOYSA-N (3-hydroxy-1-adamantyl) 2-methylprop-2-enoate Chemical compound C1C(C2)CC3CC2(O)CC1(OC(=O)C(=C)C)C3 OOIBFPKQHULHSQ-UHFFFAOYSA-N 0.000 description 1
- 125000006668 (C1-C30) aliphatic hydrocarbon group Chemical group 0.000 description 1
- 125000000204 (C2-C4) acyl group Chemical group 0.000 description 1
- AZCPJRSLLFDOJD-UHFFFAOYSA-N 1,2-diazacyclododecane Chemical group C1CCCCCNNCCCC1 AZCPJRSLLFDOJD-UHFFFAOYSA-N 0.000 description 1
- 125000005657 1,3-cyclobutylene group Chemical group [H]C1([H])C([H])([*:1])C([H])([H])C1([H])[*:2] 0.000 description 1
- 125000005838 1,3-cyclopentylene group Chemical group [H]C1([H])C([H])([H])C([H])([*:2])C([H])([H])C1([H])[*:1] 0.000 description 1
- BOMXISRSUVYDJA-UHFFFAOYSA-N 1,3-diazacyclopentadecane Chemical group C1CCCCCCNCNCCCCC1 BOMXISRSUVYDJA-UHFFFAOYSA-N 0.000 description 1
- BESOZAIPOVNPNF-UHFFFAOYSA-N 1,3-diazacyclotetradecane Chemical group C1CCCCCNCNCCCCC1 BESOZAIPOVNPNF-UHFFFAOYSA-N 0.000 description 1
- CMCJOOKSIHPCFE-UHFFFAOYSA-N 1,3-diazacyclotridecane Chemical group C1CCCCCNCNCCCC1 CMCJOOKSIHPCFE-UHFFFAOYSA-N 0.000 description 1
- GQFOMGKNJRERKX-UHFFFAOYSA-N 1,3-diazacycloundecane Chemical group C1CCCCNCNCCC1 GQFOMGKNJRERKX-UHFFFAOYSA-N 0.000 description 1
- VENLCCIIGHXFJN-UHFFFAOYSA-N 1,3-diazecane Chemical group C1CCCNCNCCC1 VENLCCIIGHXFJN-UHFFFAOYSA-N 0.000 description 1
- ZBOWKDHBOFMERX-UHFFFAOYSA-N 1,3-diazepane Chemical group C1CCNCNC1 ZBOWKDHBOFMERX-UHFFFAOYSA-N 0.000 description 1
- MFVFDTCSVFBOTL-UHFFFAOYSA-N 1,3-diazetidine Chemical group C1NCN1 MFVFDTCSVFBOTL-UHFFFAOYSA-N 0.000 description 1
- DKYBVKMIZODYKL-UHFFFAOYSA-N 1,3-diazinane Chemical group C1CNCNC1 DKYBVKMIZODYKL-UHFFFAOYSA-N 0.000 description 1
- VPPMWVKTJWIMOY-UHFFFAOYSA-N 1,3-diazocane Chemical group C1CCNCNCC1 VPPMWVKTJWIMOY-UHFFFAOYSA-N 0.000 description 1
- XDFPXACLQFPFNE-UHFFFAOYSA-N 1,3-diazonane Chemical group C1CCCNCNCC1 XDFPXACLQFPFNE-UHFFFAOYSA-N 0.000 description 1
- 125000004955 1,4-cyclohexylene group Chemical group [H]C1([H])C([H])([H])C([H])([*:1])C([H])([H])C([H])([H])C1([H])[*:2] 0.000 description 1
- JBYHSSAVUBIJMK-UHFFFAOYSA-N 1,4-oxathiane Chemical group C1CSCCO1 JBYHSSAVUBIJMK-UHFFFAOYSA-N 0.000 description 1
- YBFHILNBYXCJKD-UHFFFAOYSA-N 1-(6-methylpyridin-3-yl)-2-(4-methylsulfonylphenyl)ethanone Chemical compound C1=NC(C)=CC=C1C(=O)CC1=CC=C(S(C)(=O)=O)C=C1 YBFHILNBYXCJKD-UHFFFAOYSA-N 0.000 description 1
- BMVXCPBXGZKUPN-UHFFFAOYSA-N 1-hexanamine Chemical compound CCCCCCN BMVXCPBXGZKUPN-UHFFFAOYSA-N 0.000 description 1
- 125000001637 1-naphthyl group Chemical group [H]C1=C([H])C([H])=C2C(*)=C([H])C([H])=C([H])C2=C1[H] 0.000 description 1
- GMCZKAWLACTKCF-UHFFFAOYSA-M 1-phenyl-2-(thiolan-1-ium-1-yl)ethanone;trifluoromethanesulfonate Chemical compound [O-]S(=O)(=O)C(F)(F)F.C=1C=CC=CC=1C(=O)C[S+]1CCCC1 GMCZKAWLACTKCF-UHFFFAOYSA-M 0.000 description 1
- KXZQYLBVMZGIKC-UHFFFAOYSA-N 1-pyridin-2-yl-n-(pyridin-2-ylmethyl)methanamine Chemical compound C=1C=CC=NC=1CNCC1=CC=CC=N1 KXZQYLBVMZGIKC-UHFFFAOYSA-N 0.000 description 1
- OLPZCIDHOZATMA-UHFFFAOYSA-N 2,2-dioxooxathiiran-3-one Chemical compound O=C1OS1(=O)=O OLPZCIDHOZATMA-UHFFFAOYSA-N 0.000 description 1
- 125000005808 2,4,6-trimethoxyphenyl group Chemical group [H][#6]-1=[#6](-[#8]C([H])([H])[H])-[#6](-*)=[#6](-[#8]C([H])([H])[H])-[#6]([H])=[#6]-1-[#8]C([H])([H])[H] 0.000 description 1
- XGLVDUUYFKXKPL-UHFFFAOYSA-N 2-(2-methoxyethoxy)-n,n-bis[2-(2-methoxyethoxy)ethyl]ethanamine Chemical compound COCCOCCN(CCOCCOC)CCOCCOC XGLVDUUYFKXKPL-UHFFFAOYSA-N 0.000 description 1
- WBIBUCGCVLAPQG-UHFFFAOYSA-N 2-(2-pyridin-2-ylethyl)pyridine Chemical compound C=1C=CC=NC=1CCC1=CC=CC=N1 WBIBUCGCVLAPQG-UHFFFAOYSA-N 0.000 description 1
- OHKOAJUTRVTYSW-UHFFFAOYSA-N 2-[(2-aminophenyl)methyl]aniline Chemical compound NC1=CC=CC=C1CC1=CC=CC=C1N OHKOAJUTRVTYSW-UHFFFAOYSA-N 0.000 description 1
- 125000004974 2-butenyl group Chemical group C(C=CC)* 0.000 description 1
- 125000000069 2-butynyl group Chemical group [H]C([H])([H])C#CC([H])([H])* 0.000 description 1
- 125000004182 2-chlorophenyl group Chemical group [H]C1=C([H])C(Cl)=C(*)C([H])=C1[H] 0.000 description 1
- SVONRAPFKPVNKG-UHFFFAOYSA-N 2-ethoxyethyl acetate Chemical compound CCOCCOC(C)=O SVONRAPFKPVNKG-UHFFFAOYSA-N 0.000 description 1
- 125000006176 2-ethylbutyl group Chemical group [H]C([H])([H])C([H])([H])C([H])(C([H])([H])*)C([H])([H])C([H])([H])[H] 0.000 description 1
- 125000003229 2-methylhexyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])(C([H])([H])[H])C([H])([H])* 0.000 description 1
- 125000001622 2-naphthyl group Chemical group [H]C1=C([H])C([H])=C2C([H])=C(*)C([H])=C([H])C2=C1[H] 0.000 description 1
- JBIJLHTVPXGSAM-UHFFFAOYSA-N 2-naphthylamine Chemical compound C1=CC=CC2=CC(N)=CC=C21 JBIJLHTVPXGSAM-UHFFFAOYSA-N 0.000 description 1
- XLLXMBCBJGATSP-UHFFFAOYSA-N 2-phenylethenol Chemical compound OC=CC1=CC=CC=C1 XLLXMBCBJGATSP-UHFFFAOYSA-N 0.000 description 1
- FMFHUEMLVAIBFI-UHFFFAOYSA-N 2-phenylethenyl acetate Chemical compound CC(=O)OC=CC1=CC=CC=C1 FMFHUEMLVAIBFI-UHFFFAOYSA-N 0.000 description 1
- 125000000094 2-phenylethyl group Chemical group [H]C1=C([H])C([H])=C(C([H])=C1[H])C([H])([H])C([H])([H])* 0.000 description 1
- 125000000389 2-pyrrolyl group Chemical group [H]N1C([*])=C([H])C([H])=C1[H] 0.000 description 1
- 125000005809 3,4,5-trimethoxyphenyl group Chemical group [H]C1=C(OC([H])([H])[H])C(OC([H])([H])[H])=C(OC([H])([H])[H])C([H])=C1* 0.000 description 1
- FORAJDRXEYKDFJ-UHFFFAOYSA-N 3-(hydroxymethyl)adamantan-1-ol Chemical compound C1C(C2)CC3CC2(O)CC1(CO)C3 FORAJDRXEYKDFJ-UHFFFAOYSA-N 0.000 description 1
- 125000004975 3-butenyl group Chemical group C(CC=C)* 0.000 description 1
- 125000000474 3-butynyl group Chemical group [H]C#CC([H])([H])C([H])([H])* 0.000 description 1
- YNGIFMKMDRDNBQ-UHFFFAOYSA-N 3-ethenylphenol Chemical compound OC1=CC=CC(C=C)=C1 YNGIFMKMDRDNBQ-UHFFFAOYSA-N 0.000 description 1
- 125000004207 3-methoxyphenyl group Chemical group [H]C1=C([H])C(*)=C([H])C(OC([H])([H])[H])=C1[H] 0.000 description 1
- FRKPCXYPIHAOFI-UHFFFAOYSA-N 3-methylaniline Chemical compound [CH2]C1=CC=CC(N)=C1 FRKPCXYPIHAOFI-UHFFFAOYSA-N 0.000 description 1
- OFNISBHGPNMTMS-UHFFFAOYSA-N 3-methylideneoxolane-2,5-dione Chemical compound C=C1CC(=O)OC1=O OFNISBHGPNMTMS-UHFFFAOYSA-N 0.000 description 1
- 125000001397 3-pyrrolyl group Chemical group [H]N1C([H])=C([*])C([H])=C1[H] 0.000 description 1
- WECDUOXQLAIPQW-UHFFFAOYSA-N 4,4'-Methylene bis(2-methylaniline) Chemical compound C1=C(N)C(C)=CC(CC=2C=C(C)C(N)=CC=2)=C1 WECDUOXQLAIPQW-UHFFFAOYSA-N 0.000 description 1
- UHBAPGWWRFVTFS-UHFFFAOYSA-N 4,4'-dipyridyl disulfide Chemical compound C=1C=NC=CC=1SSC1=CC=NC=C1 UHBAPGWWRFVTFS-UHFFFAOYSA-N 0.000 description 1
- DQRKTVIJNCVZAX-UHFFFAOYSA-N 4-(2-pyridin-4-ylethyl)pyridine Chemical compound C=1C=NC=CC=1CCC1=CC=NC=C1 DQRKTVIJNCVZAX-UHFFFAOYSA-N 0.000 description 1
- RRCWJXNJBQORGX-UHFFFAOYSA-N 4-(2-pyridin-4-yloxyethoxy)pyridine Chemical compound C=1C=NC=CC=1OCCOC1=CC=NC=C1 RRCWJXNJBQORGX-UHFFFAOYSA-N 0.000 description 1
- OGNCVVRIKNGJHQ-UHFFFAOYSA-N 4-(3-pyridin-4-ylpropyl)pyridine Chemical compound C=1C=NC=CC=1CCCC1=CC=NC=C1 OGNCVVRIKNGJHQ-UHFFFAOYSA-N 0.000 description 1
- CBEVWPCAHIAUOD-UHFFFAOYSA-N 4-[(4-amino-3-ethylphenyl)methyl]-2-ethylaniline Chemical compound C1=C(N)C(CC)=CC(CC=2C=C(CC)C(N)=CC=2)=C1 CBEVWPCAHIAUOD-UHFFFAOYSA-N 0.000 description 1
- UHNUHZHQLCGZDA-UHFFFAOYSA-N 4-[2-(4-aminophenyl)ethyl]aniline Chemical compound C1=CC(N)=CC=C1CCC1=CC=C(N)C=C1 UHNUHZHQLCGZDA-UHFFFAOYSA-N 0.000 description 1
- 125000004801 4-cyanophenyl group Chemical group [H]C1=C([H])C(C#N)=C([H])C([H])=C1* 0.000 description 1
- 125000004860 4-ethylphenyl group Chemical group [H]C1=C([H])C(=C([H])C([H])=C1*)C([H])([H])C([H])([H])[H] 0.000 description 1
- 125000004203 4-hydroxyphenyl group Chemical group [H]OC1=C([H])C([H])=C(*)C([H])=C1[H] 0.000 description 1
- TYMLOMAKGOJONV-UHFFFAOYSA-N 4-nitroaniline Chemical compound NC1=CC=C([N+]([O-])=O)C=C1 TYMLOMAKGOJONV-UHFFFAOYSA-N 0.000 description 1
- JAGRUUPXPPLSRX-UHFFFAOYSA-N 4-prop-1-en-2-ylphenol Chemical compound CC(=C)C1=CC=C(O)C=C1 JAGRUUPXPPLSRX-UHFFFAOYSA-N 0.000 description 1
- XGJOFCCBFCHEHK-UHFFFAOYSA-N 4-pyridin-4-ylsulfanylpyridine Chemical compound C=1C=NC=CC=1SC1=CC=NC=C1 XGJOFCCBFCHEHK-UHFFFAOYSA-N 0.000 description 1
- LUMNWCHHXDUKFI-UHFFFAOYSA-N 5-bicyclo[2.2.1]hept-2-enylmethanol Chemical compound C1C2C(CO)CC1C=C2 LUMNWCHHXDUKFI-UHFFFAOYSA-N 0.000 description 1
- OZJPLYNZGCXSJM-UHFFFAOYSA-N 5-valerolactone Chemical group O=C1CCCCO1 OZJPLYNZGCXSJM-UHFFFAOYSA-N 0.000 description 1
- KNDQHSIWLOJIGP-UHFFFAOYSA-N 826-62-0 Chemical compound C1C2C3C(=O)OC(=O)C3C1C=C2 KNDQHSIWLOJIGP-UHFFFAOYSA-N 0.000 description 1
- QGZKDVFQNNGYKY-UHFFFAOYSA-O Ammonium Chemical compound [NH4+] QGZKDVFQNNGYKY-UHFFFAOYSA-O 0.000 description 1
- VHUUQVKOLVNVRT-UHFFFAOYSA-N Ammonium hydroxide Chemical compound [NH4+].[OH-] VHUUQVKOLVNVRT-UHFFFAOYSA-N 0.000 description 1
- NOWKCMXCCJGMRR-UHFFFAOYSA-N Aziridine Chemical group C1CN1 NOWKCMXCCJGMRR-UHFFFAOYSA-N 0.000 description 1
- ROFVEXUMMXZLPA-UHFFFAOYSA-N Bipyridyl Chemical compound N1=CC=CC=C1C1=CC=CC=N1 ROFVEXUMMXZLPA-UHFFFAOYSA-N 0.000 description 1
- DKPFZGUDAPQIHT-UHFFFAOYSA-N Butyl acetate Natural products CCCCOC(C)=O DKPFZGUDAPQIHT-UHFFFAOYSA-N 0.000 description 1
- 125000006539 C12 alkyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 1
- XDTMQSROBMDMFD-UHFFFAOYSA-N Cyclohexane Chemical group C1CCCCC1 XDTMQSROBMDMFD-UHFFFAOYSA-N 0.000 description 1
- MHZGKXUYDGKKIU-UHFFFAOYSA-N Decylamine Chemical compound CCCCCCCCCCN MHZGKXUYDGKKIU-UHFFFAOYSA-N 0.000 description 1
- RWSOTUBLDIXVET-UHFFFAOYSA-N Dihydrogen sulfide Chemical class S RWSOTUBLDIXVET-UHFFFAOYSA-N 0.000 description 1
- XXRCUYVCPSWGCC-UHFFFAOYSA-N Ethyl pyruvate Chemical compound CCOC(=O)C(C)=O XXRCUYVCPSWGCC-UHFFFAOYSA-N 0.000 description 1
- PIICEJLVQHRZGT-UHFFFAOYSA-N Ethylenediamine Chemical compound NCCN PIICEJLVQHRZGT-UHFFFAOYSA-N 0.000 description 1
- YCKRFDGAMUMZLT-UHFFFAOYSA-N Fluorine atom Chemical compound [F] YCKRFDGAMUMZLT-UHFFFAOYSA-N 0.000 description 1
- WJYIASZWHGOTOU-UHFFFAOYSA-N Heptylamine Chemical compound CCCCCCCN WJYIASZWHGOTOU-UHFFFAOYSA-N 0.000 description 1
- WRYCSMQKUKOKBP-UHFFFAOYSA-N Imidazolidine Chemical group C1CNCN1 WRYCSMQKUKOKBP-UHFFFAOYSA-N 0.000 description 1
- NTIZESTWPVYFNL-UHFFFAOYSA-N Methyl isobutyl ketone Chemical compound CC(C)CC(C)=O NTIZESTWPVYFNL-UHFFFAOYSA-N 0.000 description 1
- UIHCLUNTQKBZGK-UHFFFAOYSA-N Methyl isobutyl ketone Natural products CCC(C)C(C)=O UIHCLUNTQKBZGK-UHFFFAOYSA-N 0.000 description 1
- BZLVMXJERCGZMT-UHFFFAOYSA-N Methyl tert-butyl ether Chemical compound COC(C)(C)C BZLVMXJERCGZMT-UHFFFAOYSA-N 0.000 description 1
- GSCCALZHGUWNJW-UHFFFAOYSA-N N-Cyclohexyl-N-methylcyclohexanamine Chemical compound C1CCCCC1N(C)C1CCCCC1 GSCCALZHGUWNJW-UHFFFAOYSA-N 0.000 description 1
- YJLYANLCNIKXMG-UHFFFAOYSA-N N-Methyldioctylamine Chemical compound CCCCCCCCN(C)CCCCCCCC YJLYANLCNIKXMG-UHFFFAOYSA-N 0.000 description 1
- YZCKVEUIGOORGS-IGMARMGPSA-N Protium Chemical compound [1H] YZCKVEUIGOORGS-IGMARMGPSA-N 0.000 description 1
- RWRDLPDLKQPQOW-UHFFFAOYSA-N Pyrrolidine Chemical group C1CCNC1 RWRDLPDLKQPQOW-UHFFFAOYSA-N 0.000 description 1
- KEAYESYHFKHZAL-UHFFFAOYSA-N Sodium Chemical compound [Na] KEAYESYHFKHZAL-UHFFFAOYSA-N 0.000 description 1
- YPWFISCTZQNZAU-UHFFFAOYSA-N Thiane Chemical group C1CCSCC1 YPWFISCTZQNZAU-UHFFFAOYSA-N 0.000 description 1
- SLINHMUFWFWBMU-UHFFFAOYSA-N Triisopropanolamine Chemical compound CC(O)CN(CC(C)O)CC(C)O SLINHMUFWFWBMU-UHFFFAOYSA-N 0.000 description 1
- 125000002777 acetyl group Chemical group [H]C([H])([H])C(*)=O 0.000 description 1
- 230000002378 acidificating effect Effects 0.000 description 1
- 150000007513 acids Chemical class 0.000 description 1
- 125000000641 acridinyl group Chemical group C1(=CC=CC2=NC3=CC=CC=C3C=C12)* 0.000 description 1
- 125000004423 acyloxy group Chemical group 0.000 description 1
- 239000000654 additive Substances 0.000 description 1
- 230000000996 additive effect Effects 0.000 description 1
- 239000012670 alkaline solution Substances 0.000 description 1
- 229940072049 amyl acetate Drugs 0.000 description 1
- 238000004458 analytical method Methods 0.000 description 1
- PGMYKACGEOXYJE-UHFFFAOYSA-N anhydrous amyl acetate Natural products CCCCCOC(C)=O PGMYKACGEOXYJE-UHFFFAOYSA-N 0.000 description 1
- 125000002490 anilino group Chemical group [H]N(*)C1=C([H])C([H])=C([H])C([H])=C1[H] 0.000 description 1
- 125000002078 anthracen-1-yl group Chemical group [H]C1=C([H])C([H])=C2C([H])=C3C([*])=C([H])C([H])=C([H])C3=C([H])C2=C1[H] 0.000 description 1
- 125000000748 anthracen-2-yl group Chemical group [H]C1=C([H])C([H])=C2C([H])=C3C([H])=C([*])C([H])=C([H])C3=C([H])C2=C1[H] 0.000 description 1
- 125000005427 anthranyl group Chemical group 0.000 description 1
- 239000006117 anti-reflective coating Substances 0.000 description 1
- 150000004945 aromatic hydrocarbons Chemical class 0.000 description 1
- 125000001769 aryl amino group Chemical group 0.000 description 1
- KFAUAWMNLGGWLP-UHFFFAOYSA-N azacyclododecane Chemical group C1CCCCCNCCCCC1 KFAUAWMNLGGWLP-UHFFFAOYSA-N 0.000 description 1
- OPIYXDLVKKNYRB-UHFFFAOYSA-N azacyclotetradecane Chemical group C1CCCCCCNCCCCCC1 OPIYXDLVKKNYRB-UHFFFAOYSA-N 0.000 description 1
- UFADJPZTTUWZMP-UHFFFAOYSA-N azacyclotridecane Chemical group C1CCCCCCNCCCCC1 UFADJPZTTUWZMP-UHFFFAOYSA-N 0.000 description 1
- UOIGOLSKSFDTHJ-UHFFFAOYSA-N azacycloundecane Chemical group C1CCCCCNCCCC1 UOIGOLSKSFDTHJ-UHFFFAOYSA-N 0.000 description 1
- ZSIQJIWKELUFRJ-UHFFFAOYSA-N azepane Chemical group C1CCCNCC1 ZSIQJIWKELUFRJ-UHFFFAOYSA-N 0.000 description 1
- HONIICLYMWZJFZ-UHFFFAOYSA-N azetidine Chemical group C1CNC1 HONIICLYMWZJFZ-UHFFFAOYSA-N 0.000 description 1
- QXNDZONIWRINJR-UHFFFAOYSA-N azocane Chemical group C1CCCNCCC1 QXNDZONIWRINJR-UHFFFAOYSA-N 0.000 description 1
- NRHDCQLCSOWVTF-UHFFFAOYSA-N azonane Chemical group C1CCCCNCCC1 NRHDCQLCSOWVTF-UHFFFAOYSA-N 0.000 description 1
- 125000005605 benzo group Chemical group 0.000 description 1
- 125000004618 benzofuryl group Chemical group O1C(=CC2=C1C=CC=C2)* 0.000 description 1
- VEZXCJBBBCKRPI-UHFFFAOYSA-N beta-propiolactone Chemical group O=C1CCO1 VEZXCJBBBCKRPI-UHFFFAOYSA-N 0.000 description 1
- MKOSBHNWXFSHSW-UHFFFAOYSA-N bicyclo[2.2.1]hept-2-en-5-ol Chemical compound C1C2C(O)CC1C=C2 MKOSBHNWXFSHSW-UHFFFAOYSA-N 0.000 description 1
- 125000006267 biphenyl group Chemical group 0.000 description 1
- 125000004799 bromophenyl group Chemical group 0.000 description 1
- 229940043232 butyl acetate Drugs 0.000 description 1
- 125000006309 butyl amino group Chemical group 0.000 description 1
- 125000000484 butyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 description 1
- 125000004063 butyryl group Chemical group O=C([*])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 description 1
- 125000000609 carbazolyl group Chemical group C1(=CC=CC=2C3=CC=CC=C3NC12)* 0.000 description 1
- 239000003795 chemical substances by application Substances 0.000 description 1
- 125000004230 chromenyl group Chemical group O1C(C=CC2=CC=CC=C12)* 0.000 description 1
- 229920006026 co-polymeric resin Polymers 0.000 description 1
- 238000004581 coalescence Methods 0.000 description 1
- 239000011248 coating agent Substances 0.000 description 1
- 238000000576 coating method Methods 0.000 description 1
- 239000012141 concentrate Substances 0.000 description 1
- 238000007334 copolymerization reaction Methods 0.000 description 1
- 125000002592 cumenyl group Chemical group C1(=C(C=CC=C1)*)C(C)C 0.000 description 1
- 125000002993 cycloalkylene group Chemical group 0.000 description 1
- 125000001995 cyclobutyl group Chemical group [H]C1([H])C([H])([H])C([H])(*)C1([H])[H] 0.000 description 1
- 125000000640 cyclooctyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])([H])C([H])(*)C([H])([H])C([H])([H])C1([H])[H] 0.000 description 1
- 125000001559 cyclopropyl group Chemical group [H]C1([H])C([H])([H])C1([H])* 0.000 description 1
- DIOQZVSQGTUSAI-NJFSPNSNSA-N decane Chemical group CCCCCCCCC[14CH3] DIOQZVSQGTUSAI-NJFSPNSNSA-N 0.000 description 1
- 125000002704 decyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 1
- 230000002950 deficient Effects 0.000 description 1
- 238000010511 deprotection reaction Methods 0.000 description 1
- CSYSRRCOBYEGPI-UHFFFAOYSA-N diazo(sulfonyl)methane Chemical compound [N-]=[N+]=C=S(=O)=O CSYSRRCOBYEGPI-UHFFFAOYSA-N 0.000 description 1
- 239000012954 diazonium Substances 0.000 description 1
- 150000001989 diazonium salts Chemical class 0.000 description 1
- 125000004987 dibenzofuryl group Chemical group C1(=CC=CC=2OC3=C(C21)C=CC=C3)* 0.000 description 1
- QVQGTNFYPJQJNM-UHFFFAOYSA-N dicyclohexylmethanamine Chemical compound C1CCCCC1C(N)C1CCCCC1 QVQGTNFYPJQJNM-UHFFFAOYSA-N 0.000 description 1
- MTHSVFCYNBDYFN-UHFFFAOYSA-N diethylene glycol Chemical class OCCOCCO MTHSVFCYNBDYFN-UHFFFAOYSA-N 0.000 description 1
- LAWOZCWGWDVVSG-UHFFFAOYSA-N dioctylamine Chemical compound CCCCCCCCNCCCCCCCC LAWOZCWGWDVVSG-UHFFFAOYSA-N 0.000 description 1
- 125000004914 dipropylamino group Chemical group C(CC)N(CCC)* 0.000 description 1
- QPOWUYJWCJRLEE-UHFFFAOYSA-N dipyridin-2-ylmethanone Chemical compound C=1C=CC=NC=1C(=O)C1=CC=CC=N1 QPOWUYJWCJRLEE-UHFFFAOYSA-N 0.000 description 1
- 238000004090 dissolution Methods 0.000 description 1
- 125000004119 disulfanediyl group Chemical group *SS* 0.000 description 1
- 125000003438 dodecyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 1
- 238000010894 electron beam technology Methods 0.000 description 1
- 150000002148 esters Chemical class 0.000 description 1
- 125000001301 ethoxy group Chemical group [H]C([H])([H])C([H])([H])O* 0.000 description 1
- 125000003754 ethoxycarbonyl group Chemical group C(=O)(OCC)* 0.000 description 1
- 229940116333 ethyl lactate Drugs 0.000 description 1
- 229940117360 ethyl pyruvate Drugs 0.000 description 1
- 125000000031 ethylamino group Chemical group [H]C([H])([H])C([H])([H])N([H])[*] 0.000 description 1
- 125000000816 ethylene group Chemical group [H]C([H])([*:1])C([H])([H])[*:2] 0.000 description 1
- 125000000219 ethylidene group Chemical group [H]C(=[*])C([H])([H])[H] 0.000 description 1
- 125000002534 ethynyl group Chemical group [H]C#C* 0.000 description 1
- 238000001914 filtration Methods 0.000 description 1
- 125000003983 fluorenyl group Chemical group C1(=CC=CC=2C3=CC=CC=C3CC12)* 0.000 description 1
- 125000002541 furyl group Chemical group 0.000 description 1
- 238000004817 gas chromatography Methods 0.000 description 1
- 150000004820 halides Chemical class 0.000 description 1
- MNWFXJYAOYHMED-UHFFFAOYSA-M heptanoate Chemical compound CCCCCCC([O-])=O MNWFXJYAOYHMED-UHFFFAOYSA-M 0.000 description 1
- 125000005842 heteroatom Chemical group 0.000 description 1
- FUZZWVXGSFPDMH-UHFFFAOYSA-M hexanoate Chemical compound CCCCCC([O-])=O FUZZWVXGSFPDMH-UHFFFAOYSA-M 0.000 description 1
- 125000001245 hexylamino group Chemical group [H]N([*])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C(C([H])([H])[H])([H])[H] 0.000 description 1
- XLYOFNOQVPJJNP-UHFFFAOYSA-M hydroxide Chemical compound [OH-] XLYOFNOQVPJJNP-UHFFFAOYSA-M 0.000 description 1
- 238000003384 imaging method Methods 0.000 description 1
- 125000002883 imidazolyl group Chemical group 0.000 description 1
- 125000003453 indazolyl group Chemical group N1N=C(C2=C1C=CC=C2)* 0.000 description 1
- 125000003406 indolizinyl group Chemical group C=1(C=CN2C=CC=CC12)* 0.000 description 1
- 125000001041 indolyl group Chemical group 0.000 description 1
- 239000003112 inhibitor Substances 0.000 description 1
- 238000002347 injection Methods 0.000 description 1
- 239000007924 injection Substances 0.000 description 1
- 229910017053 inorganic salt Inorganic materials 0.000 description 1
- 238000005342 ion exchange Methods 0.000 description 1
- 125000000904 isoindolyl group Chemical group C=1(NC=C2C=CC=CC12)* 0.000 description 1
- 125000001972 isopentyl group Chemical group [H]C([H])([H])C([H])(C([H])([H])[H])C([H])([H])C([H])([H])* 0.000 description 1
- 125000003253 isopropoxy group Chemical group [H]C([H])([H])C([H])(O*)C([H])([H])[H] 0.000 description 1
- 125000005956 isoquinolyl group Chemical group 0.000 description 1
- 150000002576 ketones Chemical class 0.000 description 1
- 125000000686 lactone group Chemical group 0.000 description 1
- 239000007788 liquid Substances 0.000 description 1
- 238000004811 liquid chromatography Methods 0.000 description 1
- FPYJFEHAWHCUMM-UHFFFAOYSA-N maleic anhydride Chemical compound O=C1OC(=O)C=C1 FPYJFEHAWHCUMM-UHFFFAOYSA-N 0.000 description 1
- 125000002960 margaryl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 description 1
- 238000004949 mass spectrometry Methods 0.000 description 1
- JJYPMNFTHPTTDI-UHFFFAOYSA-N meta-toluidine Natural products CC1=CC=CC(N)=C1 JJYPMNFTHPTTDI-UHFFFAOYSA-N 0.000 description 1
- RTWNYYOXLSILQN-UHFFFAOYSA-N methanediamine Chemical compound NCN RTWNYYOXLSILQN-UHFFFAOYSA-N 0.000 description 1
- 125000001160 methoxycarbonyl group Chemical group [H]C([H])([H])OC(*)=O 0.000 description 1
- GQJCAQADCPTHKN-UHFFFAOYSA-N methyl 2,2-difluoro-2-fluorosulfonylacetate Chemical compound COC(=O)C(F)(F)S(F)(=O)=O GQJCAQADCPTHKN-UHFFFAOYSA-N 0.000 description 1
- RMAZRAQKPTXZNL-UHFFFAOYSA-N methyl bicyclo[2.2.1]hept-2-ene-5-carboxylate Chemical compound C1C2C(C(=O)OC)CC1C=C2 RMAZRAQKPTXZNL-UHFFFAOYSA-N 0.000 description 1
- 125000000250 methylamino group Chemical group [H]N(*)C([H])([H])[H] 0.000 description 1
- 125000001570 methylene group Chemical group [H]C([H])([*:1])[*:2] 0.000 description 1
- 125000000325 methylidene group Chemical group [H]C([H])=* 0.000 description 1
- 238000012986 modification Methods 0.000 description 1
- 230000004048 modification Effects 0.000 description 1
- JESXATFQYMPTNL-UHFFFAOYSA-N mono-hydroxyphenyl-ethylene Natural products OC1=CC=CC=C1C=C JESXATFQYMPTNL-UHFFFAOYSA-N 0.000 description 1
- 125000001421 myristyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 description 1
- ZQJAONQEOXOVNR-UHFFFAOYSA-N n,n-di(nonyl)nonan-1-amine Chemical compound CCCCCCCCCN(CCCCCCCCC)CCCCCCCCC ZQJAONQEOXOVNR-UHFFFAOYSA-N 0.000 description 1
- CLZGJKHEVKJLLS-UHFFFAOYSA-N n,n-diheptylheptan-1-amine Chemical compound CCCCCCCN(CCCCCCC)CCCCCCC CLZGJKHEVKJLLS-UHFFFAOYSA-N 0.000 description 1
- DIAIBWNEUYXDNL-UHFFFAOYSA-N n,n-dihexylhexan-1-amine Chemical compound CCCCCCN(CCCCCC)CCCCCC DIAIBWNEUYXDNL-UHFFFAOYSA-N 0.000 description 1
- XTAZYLNFDRKIHJ-UHFFFAOYSA-N n,n-dioctyloctan-1-amine Chemical compound CCCCCCCCN(CCCCCCCC)CCCCCCCC XTAZYLNFDRKIHJ-UHFFFAOYSA-N 0.000 description 1
- OOHAUGDGCWURIT-UHFFFAOYSA-N n,n-dipentylpentan-1-amine Chemical compound CCCCCN(CCCCC)CCCCC OOHAUGDGCWURIT-UHFFFAOYSA-N 0.000 description 1
- 125000006606 n-butoxy group Chemical group 0.000 description 1
- BBDGYADAMYMJNO-UHFFFAOYSA-N n-butyl-n-ethylbutan-1-amine Chemical compound CCCCN(CC)CCCC BBDGYADAMYMJNO-UHFFFAOYSA-N 0.000 description 1
- MTHFROHDIWGWFD-UHFFFAOYSA-N n-butyl-n-methylbutan-1-amine Chemical compound CCCCN(C)CCCC MTHFROHDIWGWFD-UHFFFAOYSA-N 0.000 description 1
- YGNSGUIRANPPSW-UHFFFAOYSA-N n-decyl-n-ethyldecan-1-amine Chemical compound CCCCCCCCCCN(CC)CCCCCCCCCC YGNSGUIRANPPSW-UHFFFAOYSA-N 0.000 description 1
- ATBNMWWDBWBAHM-UHFFFAOYSA-N n-decyl-n-methyldecan-1-amine Chemical compound CCCCCCCCCCN(C)CCCCCCCCCC ATBNMWWDBWBAHM-UHFFFAOYSA-N 0.000 description 1
- GMTCPFCMAHMEMT-UHFFFAOYSA-N n-decyldecan-1-amine Chemical compound CCCCCCCCCCNCCCCCCCCCC GMTCPFCMAHMEMT-UHFFFAOYSA-N 0.000 description 1
- PZAHTXZMBSBSFM-UHFFFAOYSA-N n-ethyl-n-heptylheptan-1-amine Chemical compound CCCCCCCN(CC)CCCCCCC PZAHTXZMBSBSFM-UHFFFAOYSA-N 0.000 description 1
- ZBZSKMOKRUBBGC-UHFFFAOYSA-N n-ethyl-n-hexylhexan-1-amine Chemical compound CCCCCCN(CC)CCCCCC ZBZSKMOKRUBBGC-UHFFFAOYSA-N 0.000 description 1
- GESMBXUFPAHBOJ-UHFFFAOYSA-N n-ethyl-n-nonylnonan-1-amine Chemical compound CCCCCCCCCN(CC)CCCCCCCCC GESMBXUFPAHBOJ-UHFFFAOYSA-N 0.000 description 1
- KYSDFVPIAZIJAW-UHFFFAOYSA-N n-ethyl-n-octyloctan-1-amine Chemical compound CCCCCCCCN(CC)CCCCCCCC KYSDFVPIAZIJAW-UHFFFAOYSA-N 0.000 description 1
- PXAVTVNEDPAYJP-UHFFFAOYSA-N n-ethyl-n-pentylpentan-1-amine Chemical compound CCCCCN(CC)CCCCC PXAVTVNEDPAYJP-UHFFFAOYSA-N 0.000 description 1
- 125000003136 n-heptyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 1
- BXYHQXUPLKMYDE-UHFFFAOYSA-N n-heptyl-n-methylheptan-1-amine Chemical compound CCCCCCCN(C)CCCCCCC BXYHQXUPLKMYDE-UHFFFAOYSA-N 0.000 description 1
- NJWMENBYMFZACG-UHFFFAOYSA-N n-heptylheptan-1-amine Chemical compound CCCCCCCNCCCCCCC NJWMENBYMFZACG-UHFFFAOYSA-N 0.000 description 1
- 125000001298 n-hexoxy group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])O* 0.000 description 1
- 125000001280 n-hexyl group Chemical group C(CCCCC)* 0.000 description 1
- POMGZMHIXYRARC-UHFFFAOYSA-N n-hexyl-n-methylhexan-1-amine Chemical compound CCCCCCN(C)CCCCCC POMGZMHIXYRARC-UHFFFAOYSA-N 0.000 description 1
- PXSXRABJBXYMFT-UHFFFAOYSA-N n-hexylhexan-1-amine Chemical compound CCCCCCNCCCCCC PXSXRABJBXYMFT-UHFFFAOYSA-N 0.000 description 1
- IITLRKXIQJEWFI-UHFFFAOYSA-N n-methyl-n-nonylnonan-1-amine Chemical compound CCCCCCCCCN(C)CCCCCCCCC IITLRKXIQJEWFI-UHFFFAOYSA-N 0.000 description 1
- JJRDPNRWFSHHKJ-UHFFFAOYSA-N n-methyl-n-pentylpentan-1-amine Chemical compound CCCCCN(C)CCCCC JJRDPNRWFSHHKJ-UHFFFAOYSA-N 0.000 description 1
- MFHKEJIIHDNPQE-UHFFFAOYSA-N n-nonylnonan-1-amine Chemical compound CCCCCCCCCNCCCCCCCCC MFHKEJIIHDNPQE-UHFFFAOYSA-N 0.000 description 1
- 125000003935 n-pentoxy group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])O* 0.000 description 1
- 125000000740 n-pentyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 1
- JACMPVXHEARCBO-UHFFFAOYSA-N n-pentylpentan-1-amine Chemical compound CCCCCNCCCCC JACMPVXHEARCBO-UHFFFAOYSA-N 0.000 description 1
- 125000003506 n-propoxy group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])O* 0.000 description 1
- 125000004123 n-propyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])* 0.000 description 1
- HMMPCBAWTWYFLR-UHFFFAOYSA-N n-pyridin-2-ylpyridin-2-amine Chemical compound C=1C=CC=NC=1NC1=CC=CC=N1 HMMPCBAWTWYFLR-UHFFFAOYSA-N 0.000 description 1
- 125000004998 naphthylethyl group Chemical group C1(=CC=CC2=CC=CC=C12)CC* 0.000 description 1
- 125000004923 naphthylmethyl group Chemical group C1(=CC=CC2=CC=CC=C12)C* 0.000 description 1
- 125000004593 naphthyridinyl group Chemical group N1=C(C=CC2=CC=CN=C12)* 0.000 description 1
- 125000000449 nitro group Chemical group [O-][N+](*)=O 0.000 description 1
- 229910052757 nitrogen Inorganic materials 0.000 description 1
- 125000004433 nitrogen atom Chemical group N* 0.000 description 1
- 125000006501 nitrophenyl group Chemical group 0.000 description 1
- KPADFPAILITQBG-UHFFFAOYSA-N non-4-ene Chemical compound CCCCC=CCCC KPADFPAILITQBG-UHFFFAOYSA-N 0.000 description 1
- 125000006574 non-aromatic ring group Chemical group 0.000 description 1
- FJDUDHYHRVPMJZ-UHFFFAOYSA-N nonan-1-amine Chemical compound CCCCCCCCCN FJDUDHYHRVPMJZ-UHFFFAOYSA-N 0.000 description 1
- 125000001400 nonyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 description 1
- JFNLZVQOOSMTJK-KNVOCYPGSA-N norbornene Chemical compound C1[C@@H]2CC[C@H]1C=C2 JFNLZVQOOSMTJK-KNVOCYPGSA-N 0.000 description 1
- IOQPZZOEVPZRBK-UHFFFAOYSA-N octan-1-amine Chemical compound CCCCCCCCN IOQPZZOEVPZRBK-UHFFFAOYSA-N 0.000 description 1
- 125000001117 oleyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])/C([H])=C([H])\C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 description 1
- 125000004894 pentylamino group Chemical group C(CCCC)N* 0.000 description 1
- 125000005327 perimidinyl group Chemical group N1C(=NC2=CC=CC3=CC=CC1=C23)* 0.000 description 1
- 125000004934 phenanthridinyl group Chemical group C1(=CC=CC2=NC=C3C=CC=CC3=C12)* 0.000 description 1
- 125000004625 phenanthrolinyl group Chemical group N1=C(C=CC2=CC=C3C=CC=NC3=C12)* 0.000 description 1
- 125000001791 phenazinyl group Chemical group C1(=CC=CC2=NC3=CC=CC=C3N=C12)* 0.000 description 1
- 125000004344 phenylpropyl group Chemical group 0.000 description 1
- XYFCBTPGUUZFHI-UHFFFAOYSA-O phosphonium Chemical compound [PH4+] XYFCBTPGUUZFHI-UHFFFAOYSA-O 0.000 description 1
- 150000004714 phosphonium salts Chemical class 0.000 description 1
- 125000004592 phthalazinyl group Chemical group C1(=NN=CC2=CC=CC=C12)* 0.000 description 1
- 229920000642 polymer Polymers 0.000 description 1
- 230000001376 precipitating effect Effects 0.000 description 1
- 125000001844 prenyl group Chemical group [H]C([*])([H])C([H])=C(C([H])([H])[H])C([H])([H])[H] 0.000 description 1
- 150000003141 primary amines Chemical class 0.000 description 1
- 238000012545 processing Methods 0.000 description 1
- 230000001737 promoting effect Effects 0.000 description 1
- 125000004368 propenyl group Chemical group C(=CC)* 0.000 description 1
- 125000001501 propionyl group Chemical group O=C([*])C([H])([H])C([H])([H])[H] 0.000 description 1
- 125000006308 propyl amino group Chemical group 0.000 description 1
- 125000004805 propylene group Chemical group [H]C([H])([H])C([H])([*:1])C([H])([H])[*:2] 0.000 description 1
- 125000002568 propynyl group Chemical group [*]C#CC([H])([H])[H] 0.000 description 1
- 125000001042 pteridinyl group Chemical group N1=C(N=CC2=NC=CN=C12)* 0.000 description 1
- 125000000561 purinyl group Chemical group N1=C(N=C2N=CNC2=C1)* 0.000 description 1
- 125000004307 pyrazin-2-yl group Chemical group [H]C1=C([H])N=C(*)C([H])=N1 0.000 description 1
- 125000003373 pyrazinyl group Chemical group 0.000 description 1
- 125000003226 pyrazolyl group Chemical group 0.000 description 1
- 125000001725 pyrenyl group Chemical group 0.000 description 1
- 125000002098 pyridazinyl group Chemical group 0.000 description 1
- 125000004076 pyridyl group Chemical group 0.000 description 1
- 125000000714 pyrimidinyl group Chemical group 0.000 description 1
- 125000000168 pyrrolyl group Chemical group 0.000 description 1
- 125000002294 quinazolinyl group Chemical group N1=C(N=CC2=CC=CC=C12)* 0.000 description 1
- 125000005493 quinolyl group Chemical group 0.000 description 1
- 125000001567 quinoxalinyl group Chemical group N1=C(C=NC2=CC=CC=C12)* 0.000 description 1
- 238000010526 radical polymerization reaction Methods 0.000 description 1
- 125000005920 sec-butoxy group Chemical group 0.000 description 1
- 150000003376 silicon Chemical class 0.000 description 1
- 239000012312 sodium hydride Substances 0.000 description 1
- 229910000104 sodium hydride Inorganic materials 0.000 description 1
- 159000000000 sodium salts Chemical class 0.000 description 1
- CVERWORUNNIQBM-UHFFFAOYSA-M sodium;1,1-difluoro-2-[(3-hydroxy-1-adamantyl)methoxy]-2-oxoethanesulfonate Chemical compound [Na+].C1C(C2)CC3CC1(O)CC2(COC(=O)C(F)(F)S([O-])(=O)=O)C3 CVERWORUNNIQBM-UHFFFAOYSA-M 0.000 description 1
- 239000003381 stabilizer Substances 0.000 description 1
- 125000004079 stearyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 description 1
- 239000000126 substance Substances 0.000 description 1
- 238000006467 substitution reaction Methods 0.000 description 1
- 125000000446 sulfanediyl group Chemical group *S* 0.000 description 1
- 150000003871 sulfonates Chemical class 0.000 description 1
- 125000000542 sulfonic acid group Chemical group 0.000 description 1
- 239000004094 surface-active agent Substances 0.000 description 1
- 125000004213 tert-butoxy group Chemical group [H]C([H])([H])C(O*)(C([H])([H])[H])C([H])([H])[H] 0.000 description 1
- 125000005931 tert-butyloxycarbonyl group Chemical group [H]C([H])([H])C(OC(*)=O)(C([H])([H])[H])C([H])([H])[H] 0.000 description 1
- 150000003509 tertiary alcohols Chemical group 0.000 description 1
- 150000003512 tertiary amines Chemical class 0.000 description 1
- CPOUUWYFNYIYLQ-UHFFFAOYSA-M tetra(propan-2-yl)azanium;hydroxide Chemical compound [OH-].CC(C)[N+](C(C)C)(C(C)C)C(C)C CPOUUWYFNYIYLQ-UHFFFAOYSA-M 0.000 description 1
- JCJNUSDBRRKQPC-UHFFFAOYSA-M tetrahexylazanium;hydroxide Chemical compound [OH-].CCCCCC[N+](CCCCCC)(CCCCCC)CCCCCC JCJNUSDBRRKQPC-UHFFFAOYSA-M 0.000 description 1
- RAOIDOHSFRTOEL-UHFFFAOYSA-N tetrahydrothiophene Chemical group C1CCSC1 RAOIDOHSFRTOEL-UHFFFAOYSA-N 0.000 description 1
- 125000000383 tetramethylene group Chemical group [H]C([H])([*:1])C([H])([H])C([H])([H])C([H])([H])[*:2] 0.000 description 1
- CHYBTAZWINMGHA-UHFFFAOYSA-N tetraoctylazanium Chemical compound CCCCCCCC[N+](CCCCCCCC)(CCCCCCCC)CCCCCCCC CHYBTAZWINMGHA-UHFFFAOYSA-N 0.000 description 1
- RAOIDOHSFRTOEL-UHFFFAOYSA-O thiolan-1-ium Chemical group C1CC[SH+]C1 RAOIDOHSFRTOEL-UHFFFAOYSA-O 0.000 description 1
- 125000005425 toluyl group Chemical group 0.000 description 1
- 125000003944 tolyl group Chemical group 0.000 description 1
- IMFACGCPASFAPR-UHFFFAOYSA-N tributylamine Chemical compound CCCCN(CCCC)CCCC IMFACGCPASFAPR-UHFFFAOYSA-N 0.000 description 1
- ABVVEAHYODGCLZ-UHFFFAOYSA-N tridecan-1-amine Chemical compound CCCCCCCCCCCCCN ABVVEAHYODGCLZ-UHFFFAOYSA-N 0.000 description 1
- 125000002889 tridecyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 description 1
- 125000003258 trimethylene group Chemical group [H]C([H])([*:2])C([H])([H])C([H])([H])[*:1] 0.000 description 1
- ZFEAYIKULRXTAR-UHFFFAOYSA-M triphenylsulfanium;chloride Chemical compound [Cl-].C1=CC=CC=C1[S+](C=1C=CC=CC=1)C1=CC=CC=C1 ZFEAYIKULRXTAR-UHFFFAOYSA-M 0.000 description 1
- YFTHZRPMJXBUME-UHFFFAOYSA-N tripropylamine Chemical compound CCCN(CCC)CCC YFTHZRPMJXBUME-UHFFFAOYSA-N 0.000 description 1
- 125000002221 trityl group Chemical group [H]C1=C([H])C([H])=C([H])C([H])=C1C([*])(C1=C(C(=C(C(=C1[H])[H])[H])[H])[H])C1=C([H])C([H])=C([H])C([H])=C1[H] 0.000 description 1
- 229910021642 ultra pure water Inorganic materials 0.000 description 1
- 239000012498 ultrapure water Substances 0.000 description 1
- 125000002948 undecyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 description 1
- 125000000391 vinyl group Chemical group [H]C([*])=C([H])[H] 0.000 description 1
- 125000001834 xanthenyl group Chemical group C1=CC=CC=2OC3=CC=CC=C3C(C12)* 0.000 description 1
- 125000004933 β-carbolinyl group Chemical group C1(=NC=CC=2C3=CC=CC=C3NC12)* 0.000 description 1
Classifications
-
- G—PHYSICS
- G03—PHOTOGRAPHY; CINEMATOGRAPHY; ANALOGOUS TECHNIQUES USING WAVES OTHER THAN OPTICAL WAVES; ELECTROGRAPHY; HOLOGRAPHY
- G03F—PHOTOMECHANICAL PRODUCTION OF TEXTURED OR PATTERNED SURFACES, e.g. FOR PRINTING, FOR PROCESSING OF SEMICONDUCTOR DEVICES; MATERIALS THEREFOR; ORIGINALS THEREFOR; APPARATUS SPECIALLY ADAPTED THEREFOR
- G03F7/00—Photomechanical, e.g. photolithographic, production of textured or patterned surfaces, e.g. printing surfaces; Materials therefor, e.g. comprising photoresists; Apparatus specially adapted therefor
- G03F7/004—Photosensitive materials
- G03F7/0045—Photosensitive materials with organic non-macromolecular light-sensitive compounds not otherwise provided for, e.g. dissolution inhibitors
-
- G—PHYSICS
- G03—PHOTOGRAPHY; CINEMATOGRAPHY; ANALOGOUS TECHNIQUES USING WAVES OTHER THAN OPTICAL WAVES; ELECTROGRAPHY; HOLOGRAPHY
- G03F—PHOTOMECHANICAL PRODUCTION OF TEXTURED OR PATTERNED SURFACES, e.g. FOR PRINTING, FOR PROCESSING OF SEMICONDUCTOR DEVICES; MATERIALS THEREFOR; ORIGINALS THEREFOR; APPARATUS SPECIALLY ADAPTED THEREFOR
- G03F7/00—Photomechanical, e.g. photolithographic, production of textured or patterned surfaces, e.g. printing surfaces; Materials therefor, e.g. comprising photoresists; Apparatus specially adapted therefor
- G03F7/004—Photosensitive materials
- G03F7/0046—Photosensitive materials with perfluoro compounds, e.g. for dry lithography
-
- G—PHYSICS
- G03—PHOTOGRAPHY; CINEMATOGRAPHY; ANALOGOUS TECHNIQUES USING WAVES OTHER THAN OPTICAL WAVES; ELECTROGRAPHY; HOLOGRAPHY
- G03F—PHOTOMECHANICAL PRODUCTION OF TEXTURED OR PATTERNED SURFACES, e.g. FOR PRINTING, FOR PROCESSING OF SEMICONDUCTOR DEVICES; MATERIALS THEREFOR; ORIGINALS THEREFOR; APPARATUS SPECIALLY ADAPTED THEREFOR
- G03F7/00—Photomechanical, e.g. photolithographic, production of textured or patterned surfaces, e.g. printing surfaces; Materials therefor, e.g. comprising photoresists; Apparatus specially adapted therefor
- G03F7/004—Photosensitive materials
- G03F7/0047—Photosensitive materials characterised by additives for obtaining a metallic or ceramic pattern, e.g. by firing
-
- G—PHYSICS
- G03—PHOTOGRAPHY; CINEMATOGRAPHY; ANALOGOUS TECHNIQUES USING WAVES OTHER THAN OPTICAL WAVES; ELECTROGRAPHY; HOLOGRAPHY
- G03F—PHOTOMECHANICAL PRODUCTION OF TEXTURED OR PATTERNED SURFACES, e.g. FOR PRINTING, FOR PROCESSING OF SEMICONDUCTOR DEVICES; MATERIALS THEREFOR; ORIGINALS THEREFOR; APPARATUS SPECIALLY ADAPTED THEREFOR
- G03F7/00—Photomechanical, e.g. photolithographic, production of textured or patterned surfaces, e.g. printing surfaces; Materials therefor, e.g. comprising photoresists; Apparatus specially adapted therefor
- G03F7/004—Photosensitive materials
- G03F7/038—Macromolecular compounds which are rendered insoluble or differentially wettable
- G03F7/0382—Macromolecular compounds which are rendered insoluble or differentially wettable the macromolecular compound being present in a chemically amplified negative photoresist composition
-
- G—PHYSICS
- G03—PHOTOGRAPHY; CINEMATOGRAPHY; ANALOGOUS TECHNIQUES USING WAVES OTHER THAN OPTICAL WAVES; ELECTROGRAPHY; HOLOGRAPHY
- G03F—PHOTOMECHANICAL PRODUCTION OF TEXTURED OR PATTERNED SURFACES, e.g. FOR PRINTING, FOR PROCESSING OF SEMICONDUCTOR DEVICES; MATERIALS THEREFOR; ORIGINALS THEREFOR; APPARATUS SPECIALLY ADAPTED THEREFOR
- G03F7/00—Photomechanical, e.g. photolithographic, production of textured or patterned surfaces, e.g. printing surfaces; Materials therefor, e.g. comprising photoresists; Apparatus specially adapted therefor
- G03F7/004—Photosensitive materials
- G03F7/039—Macromolecular compounds which are photodegradable, e.g. positive electron resists
- G03F7/0392—Macromolecular compounds which are photodegradable, e.g. positive electron resists the macromolecular compound being present in a chemically amplified positive photoresist composition
-
- G—PHYSICS
- G03—PHOTOGRAPHY; CINEMATOGRAPHY; ANALOGOUS TECHNIQUES USING WAVES OTHER THAN OPTICAL WAVES; ELECTROGRAPHY; HOLOGRAPHY
- G03F—PHOTOMECHANICAL PRODUCTION OF TEXTURED OR PATTERNED SURFACES, e.g. FOR PRINTING, FOR PROCESSING OF SEMICONDUCTOR DEVICES; MATERIALS THEREFOR; ORIGINALS THEREFOR; APPARATUS SPECIALLY ADAPTED THEREFOR
- G03F7/00—Photomechanical, e.g. photolithographic, production of textured or patterned surfaces, e.g. printing surfaces; Materials therefor, e.g. comprising photoresists; Apparatus specially adapted therefor
- G03F7/004—Photosensitive materials
- G03F7/039—Macromolecular compounds which are photodegradable, e.g. positive electron resists
- G03F7/0392—Macromolecular compounds which are photodegradable, e.g. positive electron resists the macromolecular compound being present in a chemically amplified positive photoresist composition
- G03F7/0397—Macromolecular compounds which are photodegradable, e.g. positive electron resists the macromolecular compound being present in a chemically amplified positive photoresist composition the macromolecular compound having an alicyclic moiety in a side chain
-
- G—PHYSICS
- G03—PHOTOGRAPHY; CINEMATOGRAPHY; ANALOGOUS TECHNIQUES USING WAVES OTHER THAN OPTICAL WAVES; ELECTROGRAPHY; HOLOGRAPHY
- G03F—PHOTOMECHANICAL PRODUCTION OF TEXTURED OR PATTERNED SURFACES, e.g. FOR PRINTING, FOR PROCESSING OF SEMICONDUCTOR DEVICES; MATERIALS THEREFOR; ORIGINALS THEREFOR; APPARATUS SPECIALLY ADAPTED THEREFOR
- G03F7/00—Photomechanical, e.g. photolithographic, production of textured or patterned surfaces, e.g. printing surfaces; Materials therefor, e.g. comprising photoresists; Apparatus specially adapted therefor
- G03F7/20—Exposure; Apparatus therefor
- G03F7/2041—Exposure; Apparatus therefor in the presence of a fluid, e.g. immersion; using fluid cooling means
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01L—SEMICONDUCTOR DEVICES NOT COVERED BY CLASS H10
- H01L21/00—Processes or apparatus adapted for the manufacture or treatment of semiconductor or solid state devices or of parts thereof
- H01L21/02—Manufacture or treatment of semiconductor devices or of parts thereof
- H01L21/027—Making masks on semiconductor bodies for further photolithographic processing not provided for in group H01L21/18 or H01L21/34
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01L—SEMICONDUCTOR DEVICES NOT COVERED BY CLASS H10
- H01L21/00—Processes or apparatus adapted for the manufacture or treatment of semiconductor or solid state devices or of parts thereof
- H01L21/02—Manufacture or treatment of semiconductor devices or of parts thereof
- H01L21/027—Making masks on semiconductor bodies for further photolithographic processing not provided for in group H01L21/18 or H01L21/34
- H01L21/0271—Making masks on semiconductor bodies for further photolithographic processing not provided for in group H01L21/18 or H01L21/34 comprising organic layers
Description
[1] 樹脂、酸発生剤及び式(C1)で表される化合物を含有することを特徴とする化学増幅型フォトレジスト組成物。
[式(C1)中、Rc1は、置換基を有していてもよい芳香族基を表す。Rc2及びRc3は、それぞれ独立して、水素原子、置換基を有していてもよい脂肪族炭化水素基、又は置換基を有していてもよい芳香族基を表す。Rc4及びRc6は、それぞれ独立して、水素原子、又は置換基を有していてもよい脂肪族炭化水素基を表すか、Rc4及びRc6が互いに結合して環を形成する。Rc5は、置換基を有していてもよい脂肪族炭化水素基、又は置換基を有していてもよいアミノ基を表し、Rc7は、水素原子、又は置換基を有していてもよい脂肪族炭化水素基を表すか、Rc5及びRc7が互いに結合して環を形成する。]
[式(C1−1)中、Rc8及びRc9は、それぞれ独立して、置換基を有していてもよいC1-18アルカンジイル基を表す。Rc1は前記と同じ意味を表す。]
[式(C1−1−1)及び式(C1−1−2)中、Rc1は前記と同じ意味を表す。]
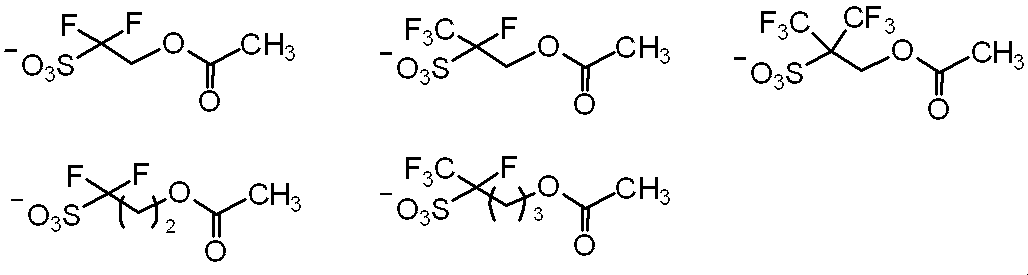
[式(B1)中、
Q1及びQ2は、それぞれ独立に、フッ素原子又はC1〜C6ペルフルオロアルキル基を表す。
Lb1は、単結合又は2価のC1〜C17飽和炭化水素基を表し、前記2価の飽和炭化水素基に含まれる−CH2−は、−O−又は−CO−で置き換わっていてもよい。
Yは、置換基を有していてもよいC1〜C18脂肪族炭化水素基又は置換基を有していてもよいC3〜C18飽和環状炭化水素基を表し、前記脂肪族炭化水素基及び前記飽和環状炭化水素基に含まれる−CH2−は、−O−、−SO2−又は−CO−で置き換わっていてもよい。
Z+は、有機カチオンを表す。]
塗布後の組成物を乾燥させて組成物層を形成する工程、
組成物層に露光機を用いて露光する工程、
露光後の組成物層を加熱する工程、
加熱後の組成物層を、現像装置を用いて現像する工程、
を含むレジストパターンの製造方法。
樹脂(A)は、酸の作用によりアルカリ可溶となる樹脂である。酸の作用によりアルカリ可溶となる樹脂は、酸に不安定な基を有するモノマー(以下「酸に不安定な基を有するモノマー(a1)」という場合がある)を重合することによって製造でき、酸の作用によりアルカリ可溶となる。「酸の作用によりアルカリ可溶となる」とは、「酸との接触前ではアルカリ水溶液に不溶又は難溶であるが、酸との接触後にはアルカリ水溶液に可溶となる」ことを意味する。酸に不安定な基を有するモノマー(a1)は、1種を単独で使用してもよく、2種以上を併用してもよい。
「酸に不安定な基」とは、酸と接触すると脱離基が開裂して、親水性基(例えば、ヒドロキシ基又はカルボキシ基)を形成する基を意味する。酸に不安定な基としては、例えば、−O−が3級炭素原子(但し橋かけ環状炭化水素基の橋頭炭素原子を除く)と結合した式(1)で表されるアルコキシカルボニル基(即ち、3級アルコール残基を有するエステル結合)が挙げられる。なお以下では、式(1)で表される基を「酸に不安定な基(1)」という場合がある。
式(1)では、飽和環状炭化水素基は、好ましくはC3〜C20であり、より好ましくはC3〜C12である。
La1及びLa2は、それぞれ独立に、−O−又は−O−(CH2)k1−CO−O−を表し、k1は1〜7の整数を表す。但しLa1及びLa2で列挙した−O−等は、それぞれ、左側で式(a1−1)及び式(a1−2)の−CO−と結合し、右側でアダマンチル基又はシクロへキシル基と結合することを意味する。
Ra4及びRa5は、それぞれ独立に、水素原子又はメチル基を表す。
Ra6及びRa7は、それぞれ独立に、C1〜C8脂肪族炭化水素基又はC3〜C10飽和環状炭化水素基を表す。
m1は0〜14の整数を表す。
n1は0〜10の整数を表す。
Ra4及びRa5は、好ましくはメチル基である。
Ra6及びRa7の脂肪族炭化水素基は、好ましくはC6以下である。飽和環状炭化水素基は、好ましくはC8以下、より好ましくはC6以下である。
m1は、好ましくは0〜3の整数、より好ましくは0又は1である。
n1は、好ましくは0〜3の整数、より好ましくは0又は1である。
k1は、好ましくは1〜4の整数、より好ましくは1である。
Ra9は、水素原子、置換基(例えば、ヒドロキシ基)を有していてもよいC1〜C3脂肪族炭化水素基、カルボキシ基、シアノ基又はアルコキシカルボニル基(−COORa13)を表し、Ra13は、C1〜C8脂肪族炭化水素基又はC3〜C8飽和環状炭化水素基を表し、前記脂肪族炭化水素基及び前記飽和環状炭化水素基の水素原子はヒドロキシ基で置換されていてもよく、前記脂肪族炭化水素基及び前記飽和環状炭化水素基の−CH2−は−O−又は−CO−で置き換わっていてもよい。
Ra10〜Ra12は、それぞれ独立に、C1〜C12脂肪族炭化水素基又はC3〜C12飽和環状炭化水素基を表すか、或いはRa10及びRa11は互いに結合して炭素原子とともに環を形成していてもよく、前記脂肪族炭化水素基及び前記飽和環状炭化水素基の水素原子はヒドロキシ基等で置換されていてもよく、前記脂肪族炭化水素基及び前記飽和環状炭化水素基の−CH2−は−O−又は−CO−で置き換わっていてもよい。
Ra13としては、例えば、メチル基、エチル基、プロピル基、2−オキソ−オキソラン−3−イル基、又は2−オキソ−オキソラン−4−イル基などが挙げられる。
Ra10〜Ra12としては、例えば、メチル基、エチル基、シクロへキシル基、メチルシクロへキシル基、ヒドロキシシクロへキシル基、オキソシクロへキシル基、アダマンチル基などが挙げられる。
Ra10、Ra11及びこれらが結合する炭素が形成する環としては、例えば、飽和環状炭化水素基が挙げられ、具体的には、シクロへキシル基、アダマンチル基などが挙げられる。
[式(a1−4)中、
R10は、水素原子、ハロゲン原子又はハロゲン原子を有してもよいC1〜C6アルキル基を表す。
R11は、それぞれ独立に、ハロゲン原子、ヒドロキシ基、C1〜C6アルキル基、C1〜C6アルコキシ基、C2〜C4アシル基、C2〜C4アシルオキシ基、アクリロイル基又はメタクリロイル基を表す。
laは0〜4の整数を表す。laが2以上の整数である場合、複数のR11は同一であっても異なってもよい。
R12及びR13はそれぞれ独立に、水素原子又はC1〜C12炭化水素基を表す。
Xa2は、単結合又は置換基を有していてもよい2価のC1〜C17飽和炭化水素基を表し、該飽和炭化水素基に含まれる−CH2−は−CO−、−O−、−S−、−SO2−又は−N(Rc)−で置き換わっていてもよい。Rcは、水素原子又はC1〜C6アルキル基を表す。
Ya3は、C1〜C12脂肪族炭化水素基、C3〜C18飽和環状炭化水素基又はC6〜C18芳香族炭化水素基であり、該脂肪族炭化水素基、飽和環状炭化水素基及び芳香族炭化水素基は、置換基を有していてもよい。]
アルコキシ基としては、例えば、メトキシ基、エトキシ基、n−プロピポキシ基、イソプロポキシ基、n−ブトキシ基、sec−ブトキシ基、tert−ブトキシ基、n−ペントキシ基、n−ヘキトキシ基等が挙げられる。
アシル基としては、例えば、アセチル、プロピオニル、ブチリル等が挙げられる。
アシルオキシ基としては、例えば、アセチルオキシ、プロピオニルオキシ、ブチリルオキシ等が挙げられる。
炭化水素基としては、例えば、脂肪族炭化水素基、飽和環状炭化水素基、芳香族炭化水素基等が挙げられる。
芳香族炭化水素基としては、フェニル基、ナフチル基、アントラニル基、p−メチルフェニル基、p−tert−ブチルフェニル基、p−アダマンチルフェニル基、トリル基、キシリル基、クメニル基、メシチル基、ビフェニル基、アントリル基、フェナントリル基、2,6−ジエチルフェニル基、2−メチル−6−エチルフェニル等のアリール基等が挙げられる。
R11のアルコキシ基としては、C1〜C2がより好ましく、メトキシ基が特に好ましい。
R12及びR13の炭化水素基としては、イソプロピル基、n−ブチル基、sec−ブチル基、tert−ブチル基、ペンチル基、ヘキシル基、オクチル基、2−エチルヘキシル基、シクロヘキシル基、アダマンチル基、2−アルキル−2−アダマンチル基、1−(1−アダマンチル)−1−アルキル基、イソボルニル基等が好ましい。
Xa2及びYa3の基に置換されていてもよい基としては、ハロゲン原子、ヒドロキシ基、C1〜C6アルキル基、C1〜C6アルコキシ基、C2〜C4アシル基、C2〜C4アシルオキシ基等が挙げられる。なかでも、好ましくはヒドロキシ基である。
樹脂(A)が酸に不安定な基を有するモノマー(a1)と酸安定モノマーとの共重合体である場合、酸に不安定な基を有するモノマー(a1)に由来する構造単位は、全構造単位100モル%に対して、好ましくは10〜80モル%、より好ましくは20〜60モル%である。また、アダマンチル基を有するモノマー(特に酸に不安定な基を有するモノマー(a1−1))に由来する構造単位を、酸に不安定な基を有するモノマー(a1)100モル%に対して15モル%以上とすることが好ましい。アダマンチル基を有するモノマーの比率が増えると、レジストのドライエッチング耐性が向上する。
レジスト組成物をKrFエキシマレーザ露光(248nm)、電子線あるいはEUV光などの高エネルギー線露光に用いる場合、ヒドロキシ基を有する酸安定モノマー(a2)として、ヒドロキシスチレン類であるフェノール性水酸基を有する酸安定モノマー(a2−0)を使用することが好ましい。短波長のArFエキシマレーザ露光(193nm)などを用いる場合は、ヒドロキシ基を有する酸安定モノマー(a2)として、式(a2−1)で表されるヒドロキシアダマンチル基を有する酸安定モノマーを使用することが好ましい。ヒドロキシ基を有する酸安定モノマー(a2)は、1種を単独で使用してもよく、2種以上を併用してもよい。
R8は、水素原子、ハロゲン原子又はハロゲン原子を有してもよいC1〜C6アルキル基を表す。
R9は、ハロゲン原子、ヒドロキシ基、C1〜C6アルキル基、C1〜C6アルコキシ基、C2〜C4アシル基、C2〜C4アシルオキシ基、アクリロイル基又はメタクリロイル基を表す。
maは0〜4の整数を表す。maが2以上の整数である場合、複数のR9は同一であっても異なってもよい。]
また、アルコキシ基としては、C1〜C4アルコキシ基が好ましく、C1〜C2アルコキシ基がより好ましく、メトキシ基が特に好ましい。
maは0〜2が好ましく、0又は1がより好ましく、0が特に好ましい。
フェノール性水酸基を有するモノマーとしては、例えば、以下のモノマーが挙げられる。
La3は、−O−又は−O−(CH2)k2−CO−O−を表し、
k2は1〜7の整数を表す。
Ra14は、水素原子又はメチル基を表す。
Ra15及びRa16は、それぞれ独立に、水素原子、メチル基又はヒドロキシ基を表す。
o1は、0〜10の整数を表す。
Ra14は、好ましくはメチル基である。
Ra15は、好ましくは水素原子である。
Ra16は、好ましくは水素原子又はヒドロキシ基である。
o1は、好ましくは0〜3の整数、より好ましくは0又は1である。
酸安定モノマー(a3)が有するラクトン環は、例えば、β−プロピオラクトン環、γ−ブチロラクトン環、δ−バレロラクトン環のような単環でもよく又は単環式のラクトン環と他の環との縮合環でもよい。これらラクトン環の中で、γ−ブチロラクトン環及びγ−ブチロラクトン環と他の環との縮合環が好ましい。
La4〜La6は、それぞれ独立に、−O−又は−O−(CH2)k3−CO−O−を表す。
k3は1〜7の整数を表す。
Ra18〜Ra20は、それぞれ独立に、水素原子又はメチル基を表す。
Ra21は、C1〜C4脂肪族炭化水素基を表す。
p1は0〜5の整数を表す。
Ra22及びRa23は、それぞれ独立に、カルボキシ基、シアノ基又はC1〜C4脂肪族炭化水素基を表す。
q1及びr1は、それぞれ独立に0〜3の整数を表す。p1、q1又はr1が2以上のとき、それぞれ、複数のRa21、Ra22又はRa23は、互いに同一でも異なってもよい。
La4〜La6は、それぞれ独立に、−O−、−O−(CH2)d1−CO−O−であることが好ましく(前記d1は、1〜4の整数である)、より好ましくは−O−である。但しLa4〜La6で列挙した−O−等は、それぞれ、左側で式(a3−1)〜式(a3−3)の−CO−と結合し、右側でラクトン環と結合することを意味する。
Ra18〜Ra21は、好ましくはメチル基である。
Ra22及びRa23は、それぞれ独立に、好ましくはカルボキシ基、シアノ基又はメチル基である。
p1〜r1は、それぞれ独立に、好ましくは0〜2、より好ましくは0又は1である。
その他の酸安定モノマー(a4)としては、例えば、式(a4−1)で表される無水マレイン酸、式(a4−2)で表される無水イタコン酸又は式(a4−3)で表されるノルボルネン環を有する酸安定モノマーなどが挙げられる。
Ra25及びRa26は、それぞれ独立に、水素原子、置換基(例えば、ヒドロキシ基)を有していてもよいC1〜C3脂肪族炭化水素基、シアノ基、カルボキシ基又はアルコキシカルボニル基(−COORa27)を表すか、或いはRa25及びRa26は互いに結合して−CO−O−CO−を形成し、
Ra27は、C1〜C36脂肪族炭化水素基又はC3〜C36飽和環状炭化水素基を表し、脂肪族炭化水素基及び飽和環状炭化水素基の−CH2−は、−O−又は−CO−で置き換わっていてもよい。但し−COORa27が酸不安定基となるものは除く(即ちRa27は、3級炭素原子が−O−と結合するものを含まない)。
Ra27の脂肪族炭化水素基は、好ましくはC1〜C8、より好ましくはC1〜C6である。飽和環状炭化水素基は、好ましくはC4〜C36、より好ましくはC4〜C12である。
Ra27としては、例えば、メチル基、エチル基、プロピル基、2−オキソ−オキソラン−3−イル基、2−オキソ−オキソラン−4−イル基などが挙げられる。
樹脂(A)の含有量は、組成物の固形分中80質量%以上であることが好ましい。
なお本明細書において「組成物中の固形分」とは、後述する溶剤(E)を除いたレジスト組成物成分の合計を意味する。組成物中の固形分及びこれに対する樹脂(A)の含有量は、例えば、液体クロマトグラフィー又はガスクロマトグラフィーなどの公知の分析手段で測定することができる。
酸発生剤(B)は、非イオン系とイオン系とに分類される。非イオン系酸発生剤には、有機ハロゲン化物、スルホネートエステル類(例えば2−ニトロベンジルエステル、芳香族スルホネート、オキシムスルホネート、N−スルホニルオキシイミド、N−スルホニルオキシイミド、スルホニルオキシケトン、DNQ 4−スルホネート)、スルホン類(例えばジスルホン、ケトスルホン、スルホニルジアゾメタン)等が含まれる。イオン系酸発生剤は、オニウムカチオンを含むオニウム塩(例えばジアゾニウム塩、ホスホニウム塩、スルホニウム塩、ヨードニウム塩)が代表的である。オニウム塩のアニオンとしては、スルホン酸アニオン、スルホニルイミドアニオン、スルホニルメチドアニオン等がある。
Q1及びQ2は、それぞれ独立に、フッ素原子又はC1〜C6ペルフルオロアルキル基を表す。
Lb1は、単結合又は2価のC1〜C17飽和炭化水素基を表し、前記2価の飽和炭化水素基に含まれる−CH2−は、−O−又は−CO−で置き換わっていてもよい。
Yは、置換基を有していてもよいC1〜C18脂肪族炭化水素基又は置換基を有していてもよいC3〜C18飽和環状炭化水素基を表し、前記脂肪族炭化水素基及び前記飽和環状炭化水素基に含まれる−CH2−は、−O−、−SO2−又は−CO−で置き換わっていてもよい。
Z+は、有機カチオンを表す。]
式(B1)では、Q1及びQ2は、それぞれ独立に、好ましくはペルフルオロメチル基又はフッ素原子であり、より好ましくはフッ素原子である。
具体的には、メチレン基、エチレン基、プロパン−1,3−ジイル基、プロパン−1,2−ジイル基、ブタン−1,4−ジイル基、ペンタン−1,5−ジイル基、ヘキサン−1,6−ジイル基、ヘプタン−1,7−ジイル基、オクタン−1,8−ジイル基、ノナン−1,9−ジイル基、デカン−1,10−ジイル基、ウンデカン−1,11−ジイル基、ドデカン−1,12−ジイル基、トリデカン−1,13−ジイル基、テトラデカン−1,14−ジイル基、ペンタデカン−1,15−ジイル基、ヘキサデカン−1,16−ジイル基、ヘプタデカン−1,17−ジイル基、メチリデン基、エチリデン基、プロピリデン基、2−プロピリデン基等の直鎖状アルキレン基;
直鎖状アルキレンに、アルキル基(特に、C1〜C4アルキル基、例えば、メチル基、エチル基、プロピル基、イソプロピル基、ブチル基、sec−ブチル基、tert−ブチル基等)の側鎖を有したもの、例えば、1−メチル−1,3−プロピレン基、2−メチル−1,3−プロピレン基、2−メチル−1,2−プロピレン基、1−メチル−1,4−ブチレン基、2−メチル−1,4−ブチレン基等の分岐状アルキレン;
1,3−シクロブチレン基、1,3−シクロペンチレン基、1,4−シクロヘキシレン基、1,5−シクロオクチレン基等のシクロアルキレン基である単環式の飽和環状炭化水素基;
1,4−ノルボルニレン基、2,5−ノルボルニレン基、1,5−アダマンチレン基、2,6−アダマンチレン基等の多環式の飽和環状炭化水素基等が挙げられる。
Lb2は、単結合又はC1〜C15アルキレン基を表す。
Lb3は、単結合又はC1〜C12アルキレン基を表す。
Lb4は、C1〜C13アルキレン基を表す。但しLb3及びLb4の炭素数上限は13である。
Lb5は、C1〜C15アルキレン基を表す。
Lb6及びLb7は、それぞれ独立に、C1〜C15アルキレン基を表す。但しLb6及びLb7の炭素数上限は16である。
Lb8は、C1〜C14アルキレン基を表す。
Lb9及びLb10は、それぞれ独立に、C1〜C11アルキレン基を表す。但しLb9及びLb10の炭素数上限は12である。
中でも、式(b1−1)で表される2価の基が好ましく、Lb2が単結合又は−CH2−である式(b1−1)で表される2価の基がより好ましい。
アラルキル基としては、例えば、ベンジル、フェネチル、フェニルプロピル、トリチル、ナフチルメチル基、ナフチルエチル基等が挙げられる。
脂肪族炭化水素基及び飽和環状炭化水素基の置換基としては、例えば、ハロゲン原子(但しフッ素原子を除く)、ヒドロキシ基、オキソ基、C1〜C12脂肪族炭化水素基、ヒドロキシ基含有C1〜C12脂肪族炭化水素基、C3〜C16飽和環状炭化水素基、C1〜C12アルコキシ基、C6〜C18芳香族炭化水素基、C7〜C21アラルキル基、C2〜C4アシル基、グリシジルオキシ基又は−(CH2)j2−O−CO−Rb1基(式中、Rb1は、C1〜C16脂肪族炭化水素基、C3〜C16飽和環状炭化水素基或いはC6〜C18芳香族炭化水素基を表す。j2は、0〜4の整数を表す。)などが挙げられる。Yの置換基である脂肪族炭化水素基、飽和環状炭化水素基、芳香族炭化水素基及びアラルキル基等は、さらに置換基を有していてもよい。ここでの置換基は、例えば、アルキル基、ハロゲン原子、ヒドロキシ基、オキソ基等が挙げられる。
ヒドロキシ基含有脂肪族炭化水素基としては、例えば、ヒドロキシメチル基、ヒドロキシエチル基などが挙げられる。
Yの脂肪族炭化水素基及び飽和環状炭化水素基における−CH2−が−O−、−SO2−又は−CO−で置き換わった基としては、例えば、環状エーテル基(−CH2−が−O−で置き換わった基)、オキソ基を有する飽和環状炭化水素基(−CH2−が−CO−で置き換わった基)、スルトン環基(隣り合う2つの−CH2−が、それぞれ、−O−又は−SO2−で置き換わった基)又はラクトン環基(隣り合う2つの−CH2−が、それぞれ、−O−又は−CO−で置き換わった基)等が挙げられる。
Rb4〜Rb6は、それぞれ独立に、C1〜C30脂肪族炭化水素基、C3〜C36飽和環状炭化水素基又はC6〜C18芳香族炭化水素基を表す。前記脂肪族炭化水素基は、ヒドロキシ基、C1〜C12アルコキシ基又はC6〜C18芳香族炭化水素基で置換されていてもよく、前記飽和環状炭化水素基は、ハロゲン原子、C2〜C4アシル基又はグリシジルオキシ基で置換されていてもよく、前記芳香族炭化水素基は、ハロゲン原子、ヒドロキシ基、C1〜C36脂肪族炭化水素基、C3〜C36飽和環状炭化水素基又はC1〜C12アルコキシ基で置換されていてもよい。
m2及びn2は、それぞれ独立に0〜5の整数を表す。
Rb11は、水素原子、C1〜C36脂肪族炭化水素基、C3〜C36飽和環状炭化水素基或いはC6〜C18芳香族炭化水素基を表す。
Rb9〜Rb11の脂肪族炭化水素基は、好ましくはC1〜C12であり、飽和環状炭化水素基は、好ましくはC3〜C36、より好ましくはC4〜C12である。
Rb12は、C1〜C12脂肪族炭化水素基、C3〜C18飽和環状炭化水素基或いはC6〜C18芳香族炭化水素基を表す。前記芳香族炭化水素基は、C1〜C12脂肪族炭化水素基、C1〜C12アルコキシ基、C3〜C18飽和環状炭化水素基又はアルキルカルボニルオキシ基で置換されていてもよい。
Rb9とRb10と、及びRb11とRb12とは、それぞれ独立に、互いに結合して3員環〜12員環(好ましくは3員環〜7員環)を形成していてもよく、これらの環の−CH2−は、−O−、−S−又は−CO−で置き換わっていてもよい。
Lb11は、−S−又は−O−を表す。
o2、p2、s2、及びt2は、それぞれ独立に、0〜5の整数を表す。
q2及びr2は、それぞれ独立に、0〜4の整数を表す。
u2は0又は1を表す。
o2〜t2のいずれかが2であるとき、それぞれ、複数のRb13〜Rb18のいずれかは互いに同一でも異なってもよい。
好ましい飽和環状炭化水素基は、シクロプロピル基、シクロブチル基、シクロペンチル基、シクロヘキシル基、シクロヘプチル基、シクロデシル基、2−アルキル−2−アダマンチル基、1−(1−アダマンチル)−1−アルキル基、及びイソボルニル基である。
好ましい芳香族炭化水素基は、フェニル基、4−メチルフェニル基、4−エチルフェニル基、4−tert−ブチルフェニル基、4−シクロへキシルフェニル基、4−メトキシフェニル基、ビフェニリル基、ナフチル基である。
置換基が芳香族炭化水素基である脂肪族炭化水素基(アラルキル基)としては、ベンジル基などが挙げられる。
Rb9及びRb10が形成する環としては、例えば、チオラン−1−イウム環(テトラヒドロチオフェニウム環)、チアン−1−イウム環、1,4−オキサチアン−4−イウム環などが挙げられる。
Rb11及びRb12が形成する環としては、例えば、オキソシクロヘプタン環、オキソシクロヘキサン環、オキソノルボルナン環、オキソアダマンタン環などが挙げられる。
Rb19〜Rb21は、それぞれ独立に、ハロゲン原子(より好ましくはフッ素原子)、ヒドロキシ基、C1〜C36脂肪族炭化水素基、C3〜C36飽和環状炭化水素基又はC1〜C12アルコキシ基を表す。
脂肪族炭化水素基は、好ましくはC1〜C12であり、飽和環状炭化水素基は、好ましくはC4〜C36である。
前記脂肪族炭化水素基は、ヒドロキシ基、C1〜C12アルコキシ基又はC6〜C18芳香族炭化水素基で置換されていてもよい。
前記飽和環状炭化水素基は、ハロゲン原子、C2〜C4アシル基又はグリシジルオキシ基で置換されていてもよい。
v2〜x2は、それぞれ独立に0〜5の整数(好ましくは0又は1)を表す。v2〜x2のいずれかが2以上のとき、それぞれ、複数のRb19〜Rb21のいずれかは、互いに同一でも異なってもよい。
なかでも、Rb19〜Rb21は、それぞれ独立に、好ましくは、ハロゲン原子(より好ましくはフッ素原子)、ヒドロキシ基、C1〜C12アルキル基、又はC1〜C12アルコキシ基である。
化合物(C1)を含むレジスト組成物を使用すると、現像後のレジストパターンの断面形状をさらに矩形に近づけることができる。化合物(C1)は、レジスト組成物用のクエンチャーとして用いることができる。
0.2≦(ΔDa−ΔDb)/(ΔDc−ΔDd)≦0.9 (I)
[式(I)中、
ΔDaは、d1及びdaの差の絶対値を表し、
ΔDbは、d1及びdbの差の絶対値を表し、
ΔDcは、d1及びdcの差の絶対値を表し、
ΔDdは、d1及びddの差の絶対値を表す。
d1、da、db、dc及びddは、(1)〜(3)に記載する方法で測定する。
(1)酸に不安定な基を有し、かつアルカリ水溶液に不溶又は難溶であり、酸と作用してアルカリ水溶液で溶解しえる樹脂と、化合物(C1)と、からなる第1の膜を形成し、第1の膜の膜厚d1を測定する。
(2)第1の膜の上に、アルカリ可溶性樹脂と、−C(Q3)(Q4)−SO3H基(Q3及びQ4は、それぞれ独立に、フッ素原子又はC1〜C6ペルフルオロアルキル基を表す。)を有する酸と、からなる第2の膜を形成する。
(3)
(3−a)第2の膜を形成した後、第1の膜及び第2の膜を40mJ/cm2の露光量で露光し、熱処理し、アルカリ水溶液で現像し、現像後の第1の膜の膜厚daを測定する。
(3−b)第2の膜を形成した後、第1の膜及び第2の膜を40mJ/cm2の露光量で露光し、アルカリ水溶液で現像し、現像後の第1の膜の膜厚dbを測定する。
(3−c)第2の膜を形成した後、第1の膜及び第2の膜を熱処理し、アルカリ水溶液で現像し、現像後の第1の膜の膜厚dcを測定する。
(3−d)第2の膜を形成した後、第1の膜及び第2の膜をアルカリ水溶液で現像し、現像後の第1の膜の膜厚ddを測定する。]
膜厚d1、da、db、dc、dd、de及びdfは、大日本スクリーン製の非接触式膜厚測定装置「ラムダエース」等を用いて、測定することができる。
酸に不安定な基を有し、かつアルカリ水溶液に不溶又は難溶であり、酸と作用してアルカリ水溶液で溶解しえる樹脂とは、酸の作用により分解し、アルカリ現像液に対する溶解度が増大する樹脂であり、酸の作用により分解し、アルカリ可溶性基を生じる基を有する樹脂である。アルカリ可溶性基としては、カルボキシル基、水酸基、スルホン酸基などが挙げられる。酸の作用で分解し得る基としては、−COOH基の水素原子を酸で脱離する基で置換した基が挙げられる。
溶剤の除去は、例えばホットプレート等の加熱装置を用いて溶剤を蒸発させることにより行うか、又は減圧装置を用いて行う。この場合の温度は、例えば50〜200℃である。また、圧力は、1〜1.0×105Paである。
溶剤としては、レジスト組成物に用いられる公知の溶媒が挙げられ、例えば特開2006−257078号公報に記載された溶媒等が挙げられ、例えばプロピレングリコールモノメチルエーテルアセテート、 2−ヘプタノン、プロピレングリコールモノメチルエーテル及びγ−ブチロラクトン等が挙げられる。溶剤は、1種を単独で使用してもよく、2種以上を併用してもよい。
アルカリ可溶性樹脂とは、酸性基を含有する樹脂であり、アルカリ現像液に接触すると溶解する特性を有する樹脂である。
アルカリ可溶性樹脂としては、レジスト組成物に用いられる公知のアルカリ可溶性樹脂が挙げられ、例えば式(III)で表される構造単位からなる樹脂等が挙げられる。
Q1及びQ2は、ペルフルオロメチル基又はフッ素原子であることが好ましく、フッ素原子であることがより好ましい。
溶剤の除去は、例えばホットプレート等の加熱装置を用いて溶剤を蒸発させることにより行うか、又は減圧装置を用いて行う。この場合の温度は、例えば50〜200℃である。また、圧力は、1〜1.0×105Paである。
溶剤としては、レジスト組成物に用いられる公知の溶媒が挙げられ、例えば特開2006−257078号公報に記載された溶剤等が挙げられ、例えばイソブチルアルコール等が挙げられる。
露光は露光機を用いて行う。露光機は、液浸露光機であってもよい。露光光源としては、KrFエキシマレーザ(波長248nm)、ArFエキシマレーザ(波長193nm)、F2レーザ(波長157nm)のような紫外域のレーザ光を放射するもの、固体レーザ光源(YAG又は半導体レーザ等)からのレーザ光を波長変換して遠紫外域又は真空紫外域の高調波レーザ光を放射するもの等、種々のものを用いることができる。
熱処理の加熱温度としては、通常50〜200℃程度、好ましくは70〜150℃程度である。
現像は、現像装置を用いて行われ、通常、アルカリ現像液を利用して現像する。
ここで用いられるアルカリ現像液は、この分野で用いられる各種のアルカリ性水溶液であればよい。例えばテトラメチルアンモニウムヒドロキシドや(2−ヒドロキシエチル)トリメチルアンモニウムヒドロキシド(通称コリン)の水溶液等が挙げられる。
その後、第2の膜に含まれる−C(Q1)(Q2)−SO3H基を有する酸は、熱処理により動く。
露光及び熱処理により−C(Q1)(Q2)−SO3H基を有する酸が動き、第1の膜に含まれる酸に不安定な基を有し、かつアルカリ水溶液に不溶又は難溶であり、酸と作用してアルカリ水溶液で溶解しえる樹脂に作用して該樹脂の一部がアルカリ可溶になり、現像時にアルカリ現像液に溶けるので、膜厚daは、膜厚d1よりも小さくなる。
現像時に、第2の膜はすべてアルカリ現像液に溶ける。
ΔDaは、d1及びdaの差の絶対値を表す。
つまり、ΔDaは、第1の膜及び第2の膜を40mJ/cm2の露光量で露光したときの、露光及び熱処理による第1の膜厚の減少量を示す。
(3−b)における露光及び現像は、(3−a)と同じ条件で行われる。
露光により−C(Q1)(Q2)−SO3H基を有する酸が動き、第1の膜に含まれる酸に不安定な基を有し、かつアルカリ水溶液に不溶又は難溶であり、酸と作用してアルカリ水溶液で溶解しえる樹脂に作用して該樹脂の一部がアルカリ可溶になり、現像時にアルカリ現像液に溶けるので、膜厚dbは、膜厚d1よりも小さくなる。
現像時に、第2の膜はすべてアルカリ現像液に溶ける。
ΔDbは、d1及びdbの差の絶対値を表す。
つまり、ΔDbは、第1の膜及び第2の膜を40mJ/cm2の露光量で露光したときの、露光による第1の膜厚の減少量を示す。
ΔDa−ΔDbは、第1の膜及び第2の膜を40mJ/cm2の露光量で露光したときの、熱処理による第1の膜厚の減少量を示す。
(3−c)における熱処理及び現像は、(3−a)と同じ条件で行われる。
熱処理により−C(Q1)(Q2)−SO3H基を有する酸が動き、第1の膜に含まれる酸に不安定な基を有し、かつアルカリ水溶液に不溶又は難溶であり、酸と作用してアルカリ水溶液で溶解しえる樹脂に作用して該樹脂の一部がアルカリ可溶になり、現像時にアルカリ現像液に溶けるので、膜厚dcは、膜厚d1よりも小さくなる。
現像時に、第2の膜はすべてアルカリ現像液に溶ける。
ΔDcは、d1及びdcの差の絶対値を表す。
つまり、ΔDcは、第1の膜及び第2の膜を露光しなかったときの、熱処理による第1の膜厚の減少量を示す。
(3−d)における現像は、(3−a)と同じ条件で行われる。
現像時に、第2の膜はすべてアルカリ現像液に溶ける。
ΔDdは、d1及びddの差の絶対値を表す。
つまり、ΔDdは、第1の膜及び第2の膜を現像したときの第1の膜厚の減少量を示す。
ΔDc−ΔDdは、第1の膜及び第2の膜を露光しなかったときの、熱処理による第1の膜厚の減少量を示す。
「第1の膜及び第2の膜を露光しなかったときの、熱処理により受けたエネルギーによる第1の膜厚の減少量」に対する「第1の膜及び第2の膜を40mJ/cm2の露光量で露光したときの、熱処理により受けたエネルギーによる第1の膜厚の減少量」の割合が、0.2〜0.9であるとは、40mJ/cm2の露光量で露光すると、露光しないときに比べて、クエンチャーが酸を捕捉する機能が向上し、酸がより動きにくくなるということを表す。
化合物(C1)を含むレジスト組成物を用いれば、レジスト組成物塗膜をマスクを介して露光する際、露光部においては、クエンチャーが酸を捕捉する機能が向上し、酸がより動きにくくなるため、得られるパターンの解像度及びラインエッジラフネスが良好になる。
(ΔDa−ΔDb)/(ΔDc−ΔDd)が0.2未満である場合は、露光部においてクエンチャーが酸を捕捉する機能が向上し過ぎて、酸が動かなくなるため、パターンを解像することができない。
(ΔDa−ΔDb)/(ΔDc−ΔDd)が0.9を超える場合は、露光部及び未露光部において、クエンチャーの機能に差がないため、得られるパターンの解像度及びラインエッジラフネスが十分ではない。
フェニル基、ビフェニリル基、テルフェニリル基、スチルベニル基などの非縮合環式(単環式、環集合式など)の基;
ナフチル基、フェナントリル基、アントリル基、ピレニル基などの芳香族環同士が縮合した全芳香族環−縮合環式の基;
5,6,7,8−テトラヒドロナフチル基(5,6,7,8−テトラヒドロ−2−ナフチル基、5,6,7,8−テトラヒドロ−1−ナフチル基)、9,10−ジヒドロアントラセニル基(9,10−ジヒドロ−1−アントラセニル基、9,10−ジヒドロ−2−アントラセニル基)、フルオレニル基(1−フルオレニル基など)などの芳香族環と非芳香族環とが縮合した部分芳香族環−縮合環式の基;
などが挙げられる。
メチルチオフェニル基など;
1−ナフチル基、2−ナフチル基、1−フェニルアミノ−4−ナフチル基、1−メチルナフチル基、2−メチルナフチル基、1−メトキシ−2−ナフチル基、2−メトキシ−1−ナフチル基、1−ジメチルアミノ−2−ナフチル基、1,2−ジメチル−4−ナフチル基、1,2−ジメチル−6−ナフチル基、1,2−ジメチル−7−ナフチル基、1,3−ジメチル−6−ナフチル基、1,4−ジメチル−6−ナフチル基、1,5−ジメチル−2−ナフチル基、1,6−ジメチル−2−ナフチル基、1−ヒドロキシ−2−ナフチル基、2−ヒドロキシ−1−ナフチル基、1,4−ジヒドロキシ−2−ナフチル基など;
7−フェナントリル基など;
1−アントリル基、2−アントリル基、9−アントリル基など;アントラキノン−2−イル基(=9,10−ジオキソ−9,10−ジヒドロアントラセン−2−イル基)など; 3−ベンゾ〔b〕チエニル基、5−ベンゾ〔b〕チエニル基、2−ベンゾ〔b〕チエニル基など;
4−ジベンゾフリル基、4−メチル−7−ジベンゾフリル基など;
2−キサンテニル基、3−キサンテニル基、8−メチル−2−キサンテニル基など;
2−フェノキサチイニル基、2,7−フェノキサチイニル基など;2−ピロリル基、3−ピロリル基、5−メチル−3−ピロリル基など;
2−イミダゾリル基、4−イミダゾリル基、5−イミダゾリル基、2−メチル−4−イミダゾリル基、2−エチル−4−イミダゾリル基、2−エチル−5−イミダゾリル基など;
3−ピラゾリル基、1−メチル−3−ピラゾリル基、1−プロピル−4−ピラゾリル基など;
2−ピラジニル基、5,6−ジメチル−2−ピラジニル基など;
2−インドリジニル基など;
2−メチル−3−イソインドリル基、2−メチル−1−イソインドリル基など;
1−メチル−2−インドリル基、1−メチル−3−インドリル基、1,5−ジメチル−2−インドリル基など;
1−メチル−3−インダゾリル基など;
2,7−ジメチル−8−プリニル基、2−メトキシ−7−メチル−8−プリニル基など;
2−キノリジニル基など;
3−イソキノリル基、6−イソキノリル基、7−イソキノリル基、3−メトキシ−6−イソキノリル基など;
2−キノリル基、6−キノリル基、7−キノリル基、2−メトキシ−3−キノリル基、2−メトキシ−6−キノリル基など;
6−フタラジニル基、7−フタラジニル基、1−メトキシ−6−フタラジニル基、1,4−ジメトキシ−6−フタラジニル基など;
1,8−ナフチリジン−2−イル基など;
2−キノキサリニル基、6−キノキサリニル基、2,3−ジメチル−6−キノキサリニル基、2,3−ジメトキシ−6−キノキサリニル基など;
2−キナゾリニル基、7−キナゾリニル基、2−ジメチルアミノ−6−キナゾリニル基など;
3−シンノリニル基、6−シンノリニル基、7−シンノリニル基、3−メトキシ−7−シンノリニル基など;
2−プテリジニル基、6−プテリジニル基、7−プテリジニル基、6,7−ジメトキシ−プテリジニル基など;
2−カルバゾリル基、3−カルバゾリル基、9−メチル−2−カルバゾリル基、9−メチル−3−カルバゾリル基など;
β−カルボリン−3−イル基、1−メチル−β−カルボリン−3−イル基、1−メチル−β−カルボリン−6−イル基など;
3−フェナントリジニル基など;
2−アクリジニル基、3−アクリジニル基など;
2−ペリミジニル基、1−メチル−5−ペリミジニル基、5−フェナントロリニル基、6−フェナントロリニル基など;
1−フェナジニル基、2−フェナジニル基など;
3−イソチアゾリル基、4−イソチアゾリル基、5−イソチアゾリル基など;
2−フェノチアジニル基、3−フェノチアジニル基、10−メチル−3−フェノチアジニル基など;
3−イソキサゾリル基、4−イソキサゾリル基、5−イソキサゾリル基など;
4−メチル−フラザニル基など;
2−フェノキサジニル基、10−メチル−2−フェノキサジニル基など;
などが挙げられる。
ジアルキルアミノ基は、例えば、ジメチルアミノ基;メチルエチルアミノ基;ジエチルアミノ基、メチル−n−プロピルアミノ基、メチルイソプロピルアミノ基;メチル−n−ブチルアミノ基、メチルイソブチルアミノ基、エチルイソプロピルアミノ基;ジプロピルアミノ基、ジイソプロピルアミノ基、エチル−n−ブチルアミノ基、エチルイソブチルアミノ基、エチル−tert−ブチルアミノ基;イソプロピル−n−ブチルアミノ基、イソプロピルイソブチルアミノ基;ジ−n−ブチルアミノ基、ジ−イソブチルアミノ基;ジペンチルアミノ基;ジヘキシルアミノ基;ジオクタデシルアミノ基などの炭素数2〜36(好ましくは炭素数2〜12、さらに好ましくは炭素数2〜8)のジアルキルアミノ基が挙げられる。
本発明のレジスト組成物は、化合物(C1)以外のクエンチャー(Q)を含有していてもよい。クエンチャー(Q)には、アミン及びアンモニウムヒドロキシドが含まれる。アミンは、脂肪族アミンでも、芳香族アミンでもよい。脂肪族アミンは、1級アミン〜3級アミンのいずれも使用できる。芳香族アミンは、アニリンのような芳香族環にアミノ基が結合したものや、ピリジンのような複素芳香族アミンのいずれでもよい。
Rq7は、C1-6脂肪族炭化水素基、又はC5-10脂環式炭化水素基を表す。但し脂肪族炭化水素基及び芳香族炭化水素基は、式(Q1)で説明した置換基を有していてもよい。
溶剤(D)としては、例えば、エチルセロソルブアセテート、メチルセロソルブアセテート及びプロピレングリコールモノメチルエーテルアセテートのようなグリコールエーテルエステル類;乳酸エチル、酢酸ブチル、酢酸アミル及びピルビン酸エチルのようなエステル類;アセトン、メチルイソブチルケトン、2−ヘプタノン及びシクロヘキサノンのようなケトン類;γ−ブチロラクトンのような環状エステル類;プロピレングリコールモノメチルエーテルなどを挙げることができる。
レジスト組成物は、必要に応じて、該分野で公知の添加剤、例えば増感剤、溶解抑止剤、界面活性剤、安定剤、染料などを含んでいてもよい。
本発明のレジストパターンの製造方法は、
上述した本発明のレジスト組成物を基板上に塗布する工程、
塗布後の組成物を乾燥させて組成物層を形成する工程、
組成物層に露光機を用いて露光する工程、
露光後の組成物層を加熱する工程、
加熱後の組成物層を、現像装置を用いて現像する工程を含む。
加熱後の組成物層を、現像装置を用いて、通常、アルカリ現像液を利用して現像する。
ここで用いられるアルカリ現像液は、この分野で用いられる各種のアルカリ性水溶液であればよい。例えば、テトラメチルアンモニウムヒドロキシドや(2−ヒドロキシエチル)トリメチルアンモニウムヒドロキシド(通称コリン)の水溶液等が挙げられる。
現像後、超純水でリンスし、基板及びパターン上に残った水を除去することが好ましい。
本発明のレジスト組成物は、KrFエキシマレーザ露光用のレジスト組成物、ArFエキシマレーザ露光用のレジスト組成物、EB用のレジスト組成物又はEUV露光機用のレジスト組成物として好適である。
カラム:「TSKgel Multipore HXL−M」3本+guardcolumn(東ソー社製)
溶離液:テトラヒドロフラン
流量:1.0mL/min
検出器:RI検出器
カラム温度:40℃
注入量:100μL
分子量標準:標準ポリスチレン(東ソー社製)
下記モノマーを用いて樹脂A−1〜樹脂A−4を合成し、これらを実施例、比較例及び参考例に使用した。表1に、樹脂A−1〜樹脂A−4のモノマーのモル比及びMw示す。
モノマー(a1−1−1)、モノマー(a1−2−1)、モノマー(a2−1−2)、モノマー(a3−2−1)をモル比40:10:10:40で仕込み、全モノマー量の1.2質量倍のジオキサンを加えて溶液とした。そこに開始剤としてアゾビスイソブチロニトリル及びアゾビス(2,4−ジメチルバレロニトリル)を全モノマー量に対してそれぞれ1mol%及び3mol%で添加し、75℃で約5時間加熱した。その後、反応液を、大量のメタノール及び水の混合溶媒に注いで沈殿させる操作を3回行って精製し、Mwが7402の共重合体を収率74%で得た。この共重合体は、各モノマーに対応する構造単位を有するものであり、これを樹脂A−1とする。
モノマー(a1−1−2)、モノマー(a2−1−1)、モノマー(a3−1−1)をモル比50:25:25で仕込み、全モノマー量の1.5質量倍のジオキサンを加えて溶液とした。そこに開始剤としてアゾビスイソブチロニトリル及びアゾビス(2,4−ジメチルバレロニトリル)を全モノマー量に対してそれぞれ1mol%及び3mol%添加し、77℃で約5時間加熱した。その後、反応液を、大量のメタノール及び水の混合溶媒に注いで沈殿させる操作を3回行って精製し、Mwが8112の共重合体を収率55%で得た。この共重合体は、各モノマーに対応する構造単位を有するものであり、これを樹脂A−2とする。
モノマー(a1−1−2)、モノマー(a3−1−1)をモル比55:45で仕込み、特許文献2・段落[0236]の「<樹脂の合成例> 合成例(1) 樹脂(1)の合成(側鎖型)」に記載されている方法と同様にして、共重合体を合成した。この共重合体は、各モノマーに対応する構造単位を有するものであり、これを樹脂A−3とする。樹脂A−3の上記GPC条件で測定したMwは11000であった。
モノマー(a1−1−1)、モノマー(a1−2−1)、モノマー(a2−1−1)、モノマー(a3−1−1)及びモノマー(a3−2−1)を、モル比30:14:6:30:20の割合で仕込んだ。次いで、全モノマーの合計質量に対して、1.5質量倍のジオキサンを加えた。得られた混合物に、開始剤としてアゾビスイソブチロニトリルとアゾビス(2,4−ジメチルバレロニトリル)とを全モノマーの合計モル数に対して、それぞれ、1.00mol%と3.00mol%との割合で添加し、これを73℃で約5時間加熱した。その後、反応液を、大量のメタノールと水との混合溶媒(4:1)に注いで沈殿させる操作を3回行うことにより精製し、Mwが8100である共重合体を収率65%で得た。得られた共重合体は、次式の各モノマーから導かれる構造単位を有するものであり、これを樹脂A−4とした。
(1)使用した酸発生剤
B−1:トリフェニルスルホニウム1−((3−ヒドロキシ−1−アダマンチル)メトキシカルボニル)ジフルオロメタンスルホナート{即ち酸発生剤(B1−2)}
B−2:トリフェニルスルホニウム パーフルオロブタンスルホナート
B−3:フェナシルテトラヒドロチオフェニウム パーフルオロメタンスルホナート
ジフルオロ(フルオロスルホニル)酢酸メチルエステル100部、イオン交換水150部に、氷浴下、30%水酸化ナトリウム水溶液230部を滴下した。100℃で3時間還流し、冷却後、濃塩酸88部で中和した。得られた溶液を濃縮することによりジフルオロスルホ酢酸ナトリウム塩164.4部を得た(無機塩含有、純度62.7%)。得られたジフルオロスルホ酢酸ナトリウム塩1.9部(純度62.7%)、N,N−ジメチルホルムアミド9.5部に、1,1’−カルボニルジイミダゾール1.0部を添加し2時間撹拌した。この溶液を、3−ヒドロキシ−1−アダマンチルメタノール1.1部、N,N−ジメチルホルムアミド5.5部に、水素化ナトリウム0.2部を添加し、2時間撹拌した溶液に添加した。15時間撹拌後、生成したジフルオロスルホ酢酸3−ヒドロキシ−1−アダマンチルメチルエステルナトリウム塩をそのまま次の反応に用いた。
C−1:5−ベンジル−1,5−ジアザビシクロ[4.3.0]ノナン(特表2005−511536号公報・実施例1)
C−2:5−(2’−クロロベンジル)−1,5−ジアザビシクロ[4.3.0]ノナン(特表2005−511536号公報・実施例7)
C−3:5−(4’−メチルベンジル)−1,5−ジアザビシクロ[4.3.0]ノナン(特表2005−511536号公報・実施例8)
C−4:8−ベンジル−1,8−ジアザビシクロ[5.4.0]ウンデカン(特表2005−511536号公報・実施例15)
C−5:8−(2’−クロロベンジル)−1,8−ジアザビシクロ[5.4.0]ウンデカン(特表2005−511536号公報・実施例16)
C−6:5−(2’−ニトロベンジル)−1,8−ジアザビシクロ[5.4.0]ウンデカン(特表2005−511536号公報・実施例3)
C−7:5−(4’−メトキシカルボニルベンジル)−1,5−ジアザビシクロ[4.3.0]ノナン(WO2008/119688号パンフレット・Example1)
Q−1:2,6−ジイソプロピルアニリン
Q−2:1,5−ジアザビシクロ[4.3.0]ノン−5−エン(DBN)
Q−3:1,8−ジアザビシクロ[5.4.0]ウンデカ−7−エン(DBU)
〔アルカリ可溶性樹脂(樹脂(S1))の合成〕
モノマー(S)を仕込み、次いで、全モノマーの合計質量に対して、2.0質量倍のジオキサンを加えた。得られた混合物に、開始剤としてアゾビスイソブチロニトリルとアゾビス(2,4−ジメチルバレロニトリル)とを全モノマーの合計モル数に対して、それぞれ、1mol%と3mol%との割合で添加し、これを73℃で約5時間加熱した。その後、反応液を、大量のn−ヘプタンに注いで沈殿させる操作を行うことにより精製した。更に、大量のメタノールに注いで沈殿させる操作を3回行うことにより精製し、重量平均分子量が約2.2×104である共重合体を収率95%で得た。この共重合体は、次式の各モノマーから導かれる構造単位を有するものであり、これを樹脂S1とした。
まず、組成物(1)及び組成物(2)を調整した。
樹脂(A−4) 10質量部、化合物(C−6) 0.05質量部、プロピレングリコールモノメチルエーテルアセテート42質量部、2−ヘプタノン10質量部、プロピレングリコールモノメチルエーテル30質量部及びγ−ブチロラクトン1.5部を混合して溶解し、得られた溶液を孔径0.2μmのフッ素樹脂製フィルターで濾過して、組成物(1)を得た。
樹脂(S1)10質量部、酸(1)0.5質量部及びイソブチルアルコール200質量部を混合して溶解し、さらに孔径0.2μmのフッ素樹脂製フィルターで濾過して、組成物(2)を得た。
12インチのシリコンウエハ上に、組成物(1)を乾燥後の膜厚が300nmとなるようにスピンコートした。組成物(1)を塗布後、得られたシリコンウエハをダイレクトホットプレート上にて、85℃で60秒間プリベーク(PB)して第1の膜を形成した。第1の膜の膜厚d1を大日本スクリーン製の非接触式膜厚測定装置「ラムダエース」によって測定した。
第1の膜の上に、組成物(2)をスピンコートした。組成物(2)を塗布後、得られたシリコンウエハをダイレクトホットプレート上にて、85℃で60秒間プリベーク(PB)して、第2の膜を形成した。
第2の膜を形成した後、液浸露光用ArFエキシマステッパー[XT:1900Gi;ASML社製、NA=1.35、3/4Annular X−Y偏光]を用いて、露光量40mJ/cm2で露光した。
その後、シリコンウエハをホットプレート上にて、85℃で60秒間熱処理(PEB)を行い、さらに2.38質量%テトラメチルアンモニウムヒドロキシド水溶液で60秒間のパドル現像を行った。
現像後の第1の膜の膜厚daをd1と同様の方法で測定した。
第2の膜を形成した後、液浸露光用ArFエキシマステッパー[XT:1900Gi;ASML社製、NA=1.35、3/4Annular X−Y偏光]を用いて、露光量40mJ/cm2で露光した。
その後、2.38質量%テトラメチルアンモニウムヒドロキシド水溶液で60秒間のパドル現像を行った。
現像後の第1の膜の膜厚dbをd1と同様の方法で測定した。
第2の膜を形成した後、シリコンウエハをホットプレート上にて、85℃で60秒間熱処理(PEB)を行い、さらに2.38質量%テトラメチルアンモニウムヒドロキシド水溶液で60秒間のパドル現像を行った。
現像後の第1の膜の膜厚dcをd1と同様の方法で測定した。
第2の膜を形成した後、2.38質量%テトラメチルアンモニウムヒドロキシド水溶液で60秒間のパドル現像を行った。
現像後の第1の膜の膜厚ddをd1と同様の方法で測定した。
クエンチャー(Q−1):2,6−ジイソプロピルアニリン
表5に記載の各成分を混合して溶解し、さらに孔径0.2μmのフッ素樹脂製フィルターで濾過して、液状のレジスト組成物を調製した。
D1:
プロピレングリコールモノメチルエーテルアセテート:265部
2−ヘプタノン:20.0部
プロピレングリコールモノメチルエーテル:20.0部
γ−ブチロラクトン:3.5部
実効感度において、ホール径70nmのマスクで形成したパターンのホール径を、一つのホールにつき24回測定し、その平均値を一つのホールの平均ホール径とした。同一ウエハ内の、ホール径70nmのマスクで形成したパターンの平均ホール径を400箇所測定したものを母集団として標準偏差を求め、標準偏差が1.80nm以上2.00nm以下を基準(△と表記)とし、標準偏差が1.80nm未満の場合CDUが良好(○)と、標準偏差が2.00nmより大きい場合CDUが不良(×)と判断した。
実効感度において、ホール径が52.2nm以上57.7nm以下を保持するフォーカス範囲をDOFとし、DOFが0.16μm以上0.20μm以下を基準(△で表記)とし、DOFが0.20μmより大きい場合を良好(○)と、DOFが0.16μm未満の場合を不良(×)と判断した。
ホール径がそれぞれ72nm、71nm、70nm、69nm、68nm、67nmのマスクを用い、これらマスクホール径を横軸に、実効感度でこれらマスクを用いて形成したパターンのホール径を縦軸にプロットして、その直線の傾きをMEFとして算出した。
傾きが2.8以上3.1以下を基準(△で表記)とし、傾きが2.8未満のものを良好(○)と、3.1より大きいものを不良(×)と判断した。
実効感度において、パターンの断面形状が矩形であるものを良好(○)と、下部が広がったテーパー形状であるか、又はトップが張ったT字形状であるものを不良(×)と判断した。
レジスト組成物塗布後、得られたシリコンウエハをダイレクトホットプレート上にて、表5の「TPB」欄に記載された温度で60秒間プリベーク(PB)した。こうしてレジスト組成物膜を形成したウエハに、液浸露光用ArFエキシマステッパー[XT:1900Gi;ASML社製、NA=1.35、3/4Annular X−Y偏光]を用いて、露光量を段階的に変化させてラインアンドスペースパターンを液浸露光した。
露光後、ホットプレート上にて、表5の「TPEB」欄に記載された温度で60秒間ポストエキスポジャーベーク(PEB)を行い、さらに2.38質量%テトラメチルアンモニウムヒドロキシド水溶液で60秒間のパドル現像を行った。
実効感度において、レジストパターンを走査型電子顕微鏡で観察し、45nmを解像しているものを○、45nmを解像していないものを×とした。
リソグラフィプロセス後のレジストパターンの壁面を走査型電子顕微鏡で観察し、レジストパターンの側壁の凹凸の触れ幅が5nm以下であるものを○、5nmを超えるものを×とした。
また実施例6の結果から、化合物(C1)はクエンチャー(Q)と併用しても、パターン形状を良好に維持することができる。さらに実施例のCDU、DOF及びMEFは、いずれも良好(○)である。
Claims (12)
- 樹脂、酸発生剤及び式(C1)で表される化合物を含有することを特徴とする化学増幅型フォトレジスト組成物。
[式(C1)中、Rc1は、置換基を有していてもよい芳香族基を表す。Rc2及びRc3は、それぞれ独立して、水素原子、置換基を有していてもよい脂肪族炭化水素基、又は置換基を有していてもよい芳香族基を表す。Rc4及びRc6は、それぞれ独立して、水素原子、又は置換基を有していてもよい脂肪族炭化水素基を表すか、Rc4及びRc6が互いに結合して環を形成する。Rc5は、置換基を有していてもよい脂肪族炭化水素基、又は置換基を有していてもよいアミノ基を表し、Rc7は、水素原子、又は置換基を有していてもよい脂肪族炭化水素基を表すか、Rc5及びRc7が互いに結合して環を形成する。] - 式(C1)で表される化合物の含有量が、樹脂100質量部に対して0.01〜5質量部である請求項1〜3のいずれかに記載の化学増幅型フォトレジスト組成物。
- 酸発生剤が、フッ素含有酸発生剤である請求項1〜4のいずれかに記載の化学増幅型フォトレジスト組成物。
- 酸発生剤が、式(B1)で表される塩である請求項1〜5のいずれかに記載の化学増幅型フォトレジスト組成物。
[式(B1)中、
Q1及びQ2は、それぞれ独立に、フッ素原子又はC1〜C6ペルフルオロアルキル基を表す。
Lb1は、単結合又は2価のC1〜C17飽和炭化水素基を表し、前記2価の飽和炭化水素基に含まれる−CH2−は、−O−又は−CO−で置き換わっていてもよい。
Yは、置換基を有していてもよいC1〜C18脂肪族炭化水素基又は置換基を有していてもよいC3〜C18飽和環状炭化水素基を表し、前記脂肪族炭化水素基及び前記飽和環状炭化水素基に含まれる−CH2−は、−O−、−SO2−又は−CO−で置き換わっていてもよい。
Z+は、有機カチオンを表す。] - Z+が、トリアリールスルホニウムカチオンである請求項6に記載の化学増幅型フォトレジスト組成物。
- Yが、置換基を有していてもよいアダマンチル基又は置換基を有していてもよいオキソアダマンチル基である請求項6又は7に記載の化学増幅型フォトレジスト組成物。
- 酸発生剤の含有量が、樹脂100質量部に対して、1〜20質量部である請求項1〜8のいずれかに記載の化学増幅型フォトレジスト組成物。
- 樹脂が、酸の作用によりアルカリ可溶となる樹脂である請求項1〜9のいずれかに記載の化学増幅型フォトレジスト組成物。
- ジイソプロピルアニリンをさらに含有する請求項1〜10のいずれかに記載の化学増幅型フォトレジスト組成物。
- 請求項1〜11のいずれかに記載の化学増幅型フォトレジスト組成物を基板上に塗布する工程、
塗布後の組成物を乾燥させて組成物層を形成する工程、
組成物層に露光機を用いて露光する工程、
露光後の組成物層を加熱する工程、
加熱後の組成物層を、現像装置を用いて現像する工程、
を含むレジストパターンの製造方法。
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2010259844A JP5521999B2 (ja) | 2009-11-26 | 2010-11-22 | 化学増幅型フォトレジスト組成物及びレジストパターンの製造方法 |
Applications Claiming Priority (5)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2009269036 | 2009-11-26 | ||
| JP2009269036 | 2009-11-26 | ||
| JP2010015145 | 2010-01-27 | ||
| JP2010015145 | 2010-01-27 | ||
| JP2010259844A JP5521999B2 (ja) | 2009-11-26 | 2010-11-22 | 化学増幅型フォトレジスト組成物及びレジストパターンの製造方法 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2011175237A JP2011175237A (ja) | 2011-09-08 |
| JP5521999B2 true JP5521999B2 (ja) | 2014-06-18 |
Family
ID=44062342
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2010259844A Active JP5521999B2 (ja) | 2009-11-26 | 2010-11-22 | 化学増幅型フォトレジスト組成物及びレジストパターンの製造方法 |
Country Status (5)
| Country | Link |
|---|---|
| US (1) | US8546059B2 (ja) |
| JP (1) | JP5521999B2 (ja) |
| KR (1) | KR101771397B1 (ja) |
| CN (1) | CN102081303A (ja) |
| TW (1) | TWI495952B (ja) |
Families Citing this family (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN103454857B (zh) * | 2012-05-31 | 2020-01-03 | 住友化学株式会社 | 光致抗蚀剂组合物 |
| TWI649620B (zh) * | 2015-02-18 | 2019-02-01 | 日商住友電木股份有限公司 | 含有光產鹼劑的光可成像組成物 |
Family Cites Families (8)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US6858370B2 (en) * | 2001-02-23 | 2005-02-22 | Fuji Photo Film Co., Ltd. | Positive photosensitive composition |
| DE60219812T8 (de) * | 2001-10-17 | 2008-05-21 | Ciba Specialty Chemicals Holding Inc. | Photoaktivierbare stickstoffbasen |
| RU2381835C2 (ru) * | 2004-07-21 | 2010-02-20 | Циба Спешиалти Кемикэлз Холдинг Инк. | Способ фотоактивации и применение катализатора посредством обращенной двустадийной процедуры |
| US7304175B2 (en) * | 2005-02-16 | 2007-12-04 | Sumitomo Chemical Company, Limited | Salt suitable for an acid generator and a chemically amplified resist composition containing the same |
| CN1971421B (zh) * | 2005-11-21 | 2012-05-30 | 住友化学株式会社 | 适合于酸生成剂的盐和含有该盐的化学放大型抗蚀剂组合物 |
| JP5070814B2 (ja) * | 2005-11-21 | 2012-11-14 | 住友化学株式会社 | 化学増幅型レジスト組成物の酸発生剤用の塩 |
| JP2009126974A (ja) * | 2007-11-26 | 2009-06-11 | Three Bond Co Ltd | 樹脂組成物 |
| WO2009069428A1 (ja) * | 2007-11-28 | 2009-06-04 | Sumitomo Seika Chemicals Co., Ltd. | 光酸発生剤および光反応性組成物 |
-
2010
- 2010-11-22 JP JP2010259844A patent/JP5521999B2/ja active Active
- 2010-11-23 KR KR1020100116801A patent/KR101771397B1/ko active IP Right Grant
- 2010-11-23 CN CN2010105590416A patent/CN102081303A/zh active Pending
- 2010-11-24 US US12/953,606 patent/US8546059B2/en active Active
- 2010-11-24 TW TW099140508A patent/TWI495952B/zh active
Also Published As
| Publication number | Publication date |
|---|---|
| TW201129859A (en) | 2011-09-01 |
| KR20110058694A (ko) | 2011-06-01 |
| CN102081303A (zh) | 2011-06-01 |
| JP2011175237A (ja) | 2011-09-08 |
| TWI495952B (zh) | 2015-08-11 |
| KR101771397B1 (ko) | 2017-08-25 |
| US20110123926A1 (en) | 2011-05-26 |
| US8546059B2 (en) | 2013-10-01 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP5691585B2 (ja) | レジスト組成物 | |
| JP5664328B2 (ja) | 塩及びレジスト組成物 | |
| JP5565231B2 (ja) | レジスト組成物 | |
| JP5605029B2 (ja) | 化合物、樹脂及びレジスト組成物 | |
| JP2011148967A (ja) | 樹脂、レジスト組成物及びパターン形成方法 | |
| JP5703646B2 (ja) | レジスト組成物 | |
| JP5677669B2 (ja) | 樹脂、フォトレジスト組成物及びレジストパターンの製造方法 | |
| KR20110030359A (ko) | 포토레지스트 조성물 | |
| JP5821543B2 (ja) | 塩及びレジスト組成物 | |
| JP5664312B2 (ja) | 塩及びレジスト組成物 | |
| JP5521999B2 (ja) | 化学増幅型フォトレジスト組成物及びレジストパターンの製造方法 | |
| JP2019202991A (ja) | 塩、酸発生剤、レジスト組成物及びレジストパターンの製造方法 | |
| JP2019142858A (ja) | カルボン酸塩、カルボン酸発生剤、樹脂、レジスト組成物及びレジストパターンの製造方法 | |
| JP5677670B2 (ja) | 樹脂、フォトレジスト組成物及びレジストパターンの製造方法 | |
| JP6039223B2 (ja) | レジスト組成物及びレジストパターンの製造方法 | |
| JP2011170151A (ja) | レジスト組成物 | |
| JP2011148984A (ja) | 樹脂、フォトレジスト組成物及びレジストパターンの製造方法 | |
| JP2012008526A (ja) | レジスト組成物 | |
| JP2011248177A (ja) | レジスト組成物 | |
| JP6083462B2 (ja) | 塩及びレジスト組成物 | |
| JP2019199464A (ja) | 塩、酸発生剤、レジスト組成物及びレジストパターンの製造方法 | |
| JP6252154B2 (ja) | レジスト組成物及びレジストパターンの製造方法 | |
| JP5635890B2 (ja) | 樹脂、フォトレジスト組成物及びレジストパターンの製造方法 | |
| JP5810550B2 (ja) | 塩及びレジスト組成物 | |
| JP5516341B2 (ja) | フォトレジスト組成物及びパターン形成方法 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20130621 |
|
| A977 | Report on retrieval |
Free format text: JAPANESE INTERMEDIATE CODE: A971007 Effective date: 20140226 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20140311 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20140324 |
|
| R151 | Written notification of patent or utility model registration |
Ref document number: 5521999 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R151 |
|
| S531 | Written request for registration of change of domicile |
Free format text: JAPANESE INTERMEDIATE CODE: R313531 |
|
| R350 | Written notification of registration of transfer |
Free format text: JAPANESE INTERMEDIATE CODE: R350 |