JP5456802B2 - 細胞遊走促進剤及び創傷治療用の経皮吸収剤 - Google Patents
細胞遊走促進剤及び創傷治療用の経皮吸収剤 Download PDFInfo
- Publication number
- JP5456802B2 JP5456802B2 JP2012011342A JP2012011342A JP5456802B2 JP 5456802 B2 JP5456802 B2 JP 5456802B2 JP 2012011342 A JP2012011342 A JP 2012011342A JP 2012011342 A JP2012011342 A JP 2012011342A JP 5456802 B2 JP5456802 B2 JP 5456802B2
- Authority
- JP
- Japan
- Prior art keywords
- glucose
- pharmaceutical composition
- cell
- steroid
- hmgb1
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
- 230000012292 cell migration Effects 0.000 title claims description 17
- 208000027418 Wounds and injury Diseases 0.000 title claims description 6
- 239000002250 absorbent Substances 0.000 title claims description 6
- 230000002745 absorbent Effects 0.000 title claims description 6
- 206010052428 Wound Diseases 0.000 title claims description 5
- 150000003431 steroids Chemical class 0.000 claims description 57
- WQZGKKKJIJFFOK-GASJEMHNSA-N Glucose Natural products OC[C@H]1OC(O)[C@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-GASJEMHNSA-N 0.000 claims description 55
- 239000008103 glucose Substances 0.000 claims description 55
- 239000003795 chemical substances by application Substances 0.000 claims description 37
- 238000010521 absorption reaction Methods 0.000 claims 1
- 239000008194 pharmaceutical composition Substances 0.000 description 50
- 210000004027 cell Anatomy 0.000 description 33
- 102100037907 High mobility group protein B1 Human genes 0.000 description 32
- 101001025337 Homo sapiens High mobility group protein B1 Proteins 0.000 description 32
- 210000002510 keratinocyte Anatomy 0.000 description 20
- 230000004663 cell proliferation Effects 0.000 description 18
- 239000002537 cosmetic Substances 0.000 description 18
- 210000001519 tissue Anatomy 0.000 description 18
- 230000005779 cell damage Effects 0.000 description 17
- 230000017423 tissue regeneration Effects 0.000 description 17
- 208000037887 cell injury Diseases 0.000 description 16
- 230000000052 comparative effect Effects 0.000 description 16
- 239000002609 medium Substances 0.000 description 15
- 230000003110 anti-inflammatory effect Effects 0.000 description 14
- 230000010261 cell growth Effects 0.000 description 12
- 239000012228 culture supernatant Substances 0.000 description 12
- 229960003957 dexamethasone Drugs 0.000 description 12
- UREBDLICKHMUKA-CXSFZGCWSA-N dexamethasone Chemical compound C1CC2=CC(=O)C=C[C@]2(C)[C@]2(F)[C@@H]1[C@@H]1C[C@@H](C)[C@@](C(=O)CO)(O)[C@@]1(C)C[C@@H]2O UREBDLICKHMUKA-CXSFZGCWSA-N 0.000 description 12
- 239000003814 drug Substances 0.000 description 12
- 230000008439 repair process Effects 0.000 description 12
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 description 11
- 239000006144 Dulbecco’s modified Eagle's medium Substances 0.000 description 10
- -1 inorganic acid salts Chemical class 0.000 description 10
- 201000010099 disease Diseases 0.000 description 9
- JYGXADMDTFJGBT-VWUMJDOOSA-N hydrocortisone Chemical compound O=C1CC[C@]2(C)[C@H]3[C@@H](O)C[C@](C)([C@@](CC4)(O)C(=O)CO)[C@@H]4[C@@H]3CCC2=C1 JYGXADMDTFJGBT-VWUMJDOOSA-N 0.000 description 9
- 238000013508 migration Methods 0.000 description 9
- 210000001626 skin fibroblast Anatomy 0.000 description 9
- 239000000725 suspension Substances 0.000 description 9
- 230000000694 effects Effects 0.000 description 8
- 230000012010 growth Effects 0.000 description 8
- 238000004519 manufacturing process Methods 0.000 description 8
- 230000005012 migration Effects 0.000 description 8
- 230000035755 proliferation Effects 0.000 description 8
- 210000004877 mucosa Anatomy 0.000 description 7
- 150000003839 salts Chemical class 0.000 description 7
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 7
- OKKJLVBELUTLKV-UHFFFAOYSA-N Methanol Chemical compound OC OKKJLVBELUTLKV-UHFFFAOYSA-N 0.000 description 6
- 230000002401 inhibitory effect Effects 0.000 description 6
- 238000000034 method Methods 0.000 description 6
- 230000002829 reductive effect Effects 0.000 description 6
- 239000000523 sample Substances 0.000 description 6
- 239000002552 dosage form Substances 0.000 description 5
- 229960000890 hydrocortisone Drugs 0.000 description 5
- 239000007924 injection Substances 0.000 description 5
- 238000002347 injection Methods 0.000 description 5
- 239000000546 pharmaceutical excipient Substances 0.000 description 5
- 229960005205 prednisolone Drugs 0.000 description 5
- OIGNJSKKLXVSLS-VWUMJDOOSA-N prednisolone Chemical compound O=C1C=C[C@]2(C)[C@H]3[C@@H](O)C[C@](C)([C@@](CC4)(O)C(=O)CO)[C@@H]4[C@@H]3CCC2=C1 OIGNJSKKLXVSLS-VWUMJDOOSA-N 0.000 description 5
- 239000000047 product Substances 0.000 description 5
- 210000003491 skin Anatomy 0.000 description 5
- 239000006228 supernatant Substances 0.000 description 5
- PEDCQBHIVMGVHV-UHFFFAOYSA-N Glycerine Chemical compound OCC(O)CO PEDCQBHIVMGVHV-UHFFFAOYSA-N 0.000 description 4
- 206010061218 Inflammation Diseases 0.000 description 4
- 229940124599 anti-inflammatory drug Drugs 0.000 description 4
- 229940079593 drug Drugs 0.000 description 4
- 230000004054 inflammatory process Effects 0.000 description 4
- 210000004940 nucleus Anatomy 0.000 description 4
- 108090000623 proteins and genes Proteins 0.000 description 4
- 230000009467 reduction Effects 0.000 description 4
- 210000002966 serum Anatomy 0.000 description 4
- 239000002562 thickening agent Substances 0.000 description 4
- 102000003826 Chemokine CCL17 Human genes 0.000 description 3
- 108010082169 Chemokine CCL17 Proteins 0.000 description 3
- 206010012438 Dermatitis atopic Diseases 0.000 description 3
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 3
- 102000007665 Extracellular Signal-Regulated MAP Kinases Human genes 0.000 description 3
- 108010007457 Extracellular Signal-Regulated MAP Kinases Proteins 0.000 description 3
- DNIAPMSPPWPWGF-UHFFFAOYSA-N Propylene glycol Chemical compound CC(O)CO DNIAPMSPPWPWGF-UHFFFAOYSA-N 0.000 description 3
- 201000008937 atopic dermatitis Diseases 0.000 description 3
- 229960002537 betamethasone Drugs 0.000 description 3
- UREBDLICKHMUKA-DVTGEIKXSA-N betamethasone Chemical compound C1CC2=CC(=O)C=C[C@]2(C)[C@]2(F)[C@@H]1[C@@H]1C[C@H](C)[C@@](C(=O)CO)(O)[C@@]1(C)C[C@@H]2O UREBDLICKHMUKA-DVTGEIKXSA-N 0.000 description 3
- 230000006378 damage Effects 0.000 description 3
- 230000009422 growth inhibiting effect Effects 0.000 description 3
- BXWNKGSJHAJOGX-UHFFFAOYSA-N hexadecan-1-ol Chemical compound CCCCCCCCCCCCCCCCO BXWNKGSJHAJOGX-UHFFFAOYSA-N 0.000 description 3
- 230000007246 mechanism Effects 0.000 description 3
- 150000003180 prostaglandins Chemical class 0.000 description 3
- 239000012488 sample solution Substances 0.000 description 3
- 239000000243 solution Substances 0.000 description 3
- 235000000346 sugar Nutrition 0.000 description 3
- QTBSBXVTEAMEQO-UHFFFAOYSA-M Acetate Chemical compound CC([O-])=O QTBSBXVTEAMEQO-UHFFFAOYSA-M 0.000 description 2
- 208000035285 Allergic Seasonal Rhinitis Diseases 0.000 description 2
- 102000000412 Annexin Human genes 0.000 description 2
- 108050008874 Annexin Proteins 0.000 description 2
- 206010009900 Colitis ulcerative Diseases 0.000 description 2
- 208000027932 Collagen disease Diseases 0.000 description 2
- 208000034656 Contusions Diseases 0.000 description 2
- 108010037462 Cyclooxygenase 2 Proteins 0.000 description 2
- 102000010907 Cyclooxygenase 2 Human genes 0.000 description 2
- IAZDPXIOMUYVGZ-UHFFFAOYSA-N Dimethylsulphoxide Chemical compound CS(C)=O IAZDPXIOMUYVGZ-UHFFFAOYSA-N 0.000 description 2
- LYCAIKOWRPUZTN-UHFFFAOYSA-N Ethylene glycol Chemical compound OCCO LYCAIKOWRPUZTN-UHFFFAOYSA-N 0.000 description 2
- WZUVPPKBWHMQCE-UHFFFAOYSA-N Haematoxylin Chemical compound C12=CC(O)=C(O)C=C2CC2(O)C1C1=CC=C(O)C(O)=C1OC2 WZUVPPKBWHMQCE-UHFFFAOYSA-N 0.000 description 2
- 206010020751 Hypersensitivity Diseases 0.000 description 2
- 206010024438 Lichenification Diseases 0.000 description 2
- FQISKWAFAHGMGT-SGJOWKDISA-M Methylprednisolone sodium succinate Chemical compound [Na+].C([C@@]12C)=CC(=O)C=C1[C@@H](C)C[C@@H]1[C@@H]2[C@@H](O)C[C@]2(C)[C@@](O)(C(=O)COC(=O)CCC([O-])=O)CC[C@H]21 FQISKWAFAHGMGT-SGJOWKDISA-M 0.000 description 2
- 206010029164 Nephrotic syndrome Diseases 0.000 description 2
- 108091000080 Phosphotransferase Proteins 0.000 description 2
- 208000012641 Pigmentation disease Diseases 0.000 description 2
- 206010072170 Skin wound Diseases 0.000 description 2
- 201000006704 Ulcerative Colitis Diseases 0.000 description 2
- 238000002835 absorbance Methods 0.000 description 2
- 239000002253 acid Substances 0.000 description 2
- 230000009471 action Effects 0.000 description 2
- 230000004913 activation Effects 0.000 description 2
- 208000030961 allergic reaction Diseases 0.000 description 2
- 208000006673 asthma Diseases 0.000 description 2
- WQZGKKKJIJFFOK-VFUOTHLCSA-N beta-D-glucose Chemical compound OC[C@H]1O[C@@H](O)[C@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-VFUOTHLCSA-N 0.000 description 2
- 230000015572 biosynthetic process Effects 0.000 description 2
- 229960000541 cetyl alcohol Drugs 0.000 description 2
- 150000001875 compounds Chemical class 0.000 description 2
- 239000013068 control sample Substances 0.000 description 2
- 239000003246 corticosteroid Substances 0.000 description 2
- 239000006071 cream Substances 0.000 description 2
- 230000003247 decreasing effect Effects 0.000 description 2
- 206010012601 diabetes mellitus Diseases 0.000 description 2
- 208000035475 disorder Diseases 0.000 description 2
- 239000000839 emulsion Substances 0.000 description 2
- 210000002919 epithelial cell Anatomy 0.000 description 2
- 210000000981 epithelium Anatomy 0.000 description 2
- 239000003205 fragrance Substances 0.000 description 2
- 210000001156 gastric mucosa Anatomy 0.000 description 2
- 150000004676 glycans Chemical class 0.000 description 2
- 235000011187 glycerol Nutrition 0.000 description 2
- 239000008187 granular material Substances 0.000 description 2
- 230000035876 healing Effects 0.000 description 2
- IPCSVZSSVZVIGE-UHFFFAOYSA-N hexadecanoic acid Chemical compound CCCCCCCCCCCCCCCC(O)=O IPCSVZSSVZVIGE-UHFFFAOYSA-N 0.000 description 2
- 230000006872 improvement Effects 0.000 description 2
- 208000015181 infectious disease Diseases 0.000 description 2
- 210000004969 inflammatory cell Anatomy 0.000 description 2
- 239000004615 ingredient Substances 0.000 description 2
- 208000030603 inherited susceptibility to asthma Diseases 0.000 description 2
- 150000002617 leukotrienes Chemical class 0.000 description 2
- 239000006210 lotion Substances 0.000 description 2
- 239000000203 mixture Substances 0.000 description 2
- 210000004400 mucous membrane Anatomy 0.000 description 2
- 230000037311 normal skin Effects 0.000 description 2
- GLDOVTGHNKAZLK-UHFFFAOYSA-N octadecan-1-ol Chemical compound CCCCCCCCCCCCCCCCCCO GLDOVTGHNKAZLK-UHFFFAOYSA-N 0.000 description 2
- 239000002674 ointment Substances 0.000 description 2
- 229920001542 oligosaccharide Polymers 0.000 description 2
- 150000002482 oligosaccharides Chemical class 0.000 description 2
- 210000000056 organ Anatomy 0.000 description 2
- 229940094443 oxytocics prostaglandins Drugs 0.000 description 2
- 102000020233 phosphotransferase Human genes 0.000 description 2
- 239000000049 pigment Substances 0.000 description 2
- 230000019612 pigmentation Effects 0.000 description 2
- 229920001282 polysaccharide Polymers 0.000 description 2
- 239000005017 polysaccharide Substances 0.000 description 2
- 238000002360 preparation method Methods 0.000 description 2
- 230000001737 promoting effect Effects 0.000 description 2
- 230000008929 regeneration Effects 0.000 description 2
- 238000011069 regeneration method Methods 0.000 description 2
- 206010039073 rheumatoid arthritis Diseases 0.000 description 2
- 239000000126 substance Substances 0.000 description 2
- 230000009469 supplementation Effects 0.000 description 2
- 229940124597 therapeutic agent Drugs 0.000 description 2
- 230000000699 topical effect Effects 0.000 description 2
- KIUKXJAPPMFGSW-DNGZLQJQSA-N (2S,3S,4S,5R,6R)-6-[(2S,3R,4R,5S,6R)-3-Acetamido-2-[(2S,3S,4R,5R,6R)-6-[(2R,3R,4R,5S,6R)-3-acetamido-2,5-dihydroxy-6-(hydroxymethyl)oxan-4-yl]oxy-2-carboxy-4,5-dihydroxyoxan-3-yl]oxy-5-hydroxy-6-(hydroxymethyl)oxan-4-yl]oxy-3,4,5-trihydroxyoxane-2-carboxylic acid Chemical compound CC(=O)N[C@H]1[C@H](O)O[C@H](CO)[C@@H](O)[C@@H]1O[C@H]1[C@H](O)[C@@H](O)[C@H](O[C@H]2[C@@H]([C@@H](O[C@H]3[C@@H]([C@@H](O)[C@H](O)[C@H](O3)C(O)=O)O)[C@H](O)[C@@H](CO)O2)NC(C)=O)[C@@H](C(O)=O)O1 KIUKXJAPPMFGSW-DNGZLQJQSA-N 0.000 description 1
- DSEKYWAQQVUQTP-XEWMWGOFSA-N (2r,4r,4as,6as,6as,6br,8ar,12ar,14as,14bs)-2-hydroxy-4,4a,6a,6b,8a,11,11,14a-octamethyl-2,4,5,6,6a,7,8,9,10,12,12a,13,14,14b-tetradecahydro-1h-picen-3-one Chemical compound C([C@H]1[C@]2(C)CC[C@@]34C)C(C)(C)CC[C@]1(C)CC[C@]2(C)[C@H]4CC[C@@]1(C)[C@H]3C[C@@H](O)C(=O)[C@@H]1C DSEKYWAQQVUQTP-XEWMWGOFSA-N 0.000 description 1
- YYGNTYWPHWGJRM-UHFFFAOYSA-N (6E,10E,14E,18E)-2,6,10,15,19,23-hexamethyltetracosa-2,6,10,14,18,22-hexaene Chemical compound CC(C)=CCCC(C)=CCCC(C)=CCCC=C(C)CCC=C(C)CCC=C(C)C YYGNTYWPHWGJRM-UHFFFAOYSA-N 0.000 description 1
- NBWRJAOOMGASJP-UHFFFAOYSA-N 2-(3,5-diphenyl-1h-tetrazol-1-ium-2-yl)-4,5-dimethyl-1,3-thiazole;bromide Chemical compound [Br-].S1C(C)=C(C)N=C1N1N(C=2C=CC=CC=2)N=C(C=2C=CC=CC=2)[NH2+]1 NBWRJAOOMGASJP-UHFFFAOYSA-N 0.000 description 1
- BSKHPKMHTQYZBB-UHFFFAOYSA-N 2-methylpyridine Chemical class CC1=CC=CC=N1 BSKHPKMHTQYZBB-UHFFFAOYSA-N 0.000 description 1
- HVCOBJNICQPDBP-UHFFFAOYSA-N 3-[3-[3,5-dihydroxy-6-methyl-4-(3,4,5-trihydroxy-6-methyloxan-2-yl)oxyoxan-2-yl]oxydecanoyloxy]decanoic acid;hydrate Chemical compound O.OC1C(OC(CC(=O)OC(CCCCCCC)CC(O)=O)CCCCCCC)OC(C)C(O)C1OC1C(O)C(O)C(O)C(C)O1 HVCOBJNICQPDBP-UHFFFAOYSA-N 0.000 description 1
- QTQGHKVYLQBJLO-UHFFFAOYSA-N 4-methylbenzenesulfonate;(4-methyl-1-oxo-1-phenylmethoxypentan-2-yl)azanium Chemical compound CC1=CC=C(S(O)(=O)=O)C=C1.CC(C)CC(N)C(=O)OCC1=CC=CC=C1 QTQGHKVYLQBJLO-UHFFFAOYSA-N 0.000 description 1
- 208000002874 Acne Vulgaris Diseases 0.000 description 1
- 208000023275 Autoimmune disease Diseases 0.000 description 1
- 241000894006 Bacteria Species 0.000 description 1
- 208000035143 Bacterial infection Diseases 0.000 description 1
- 108010077544 Chromatin Proteins 0.000 description 1
- 206010009192 Circulatory collapse Diseases 0.000 description 1
- KRKNYBCHXYNGOX-UHFFFAOYSA-K Citrate Chemical compound [O-]C(=O)CC(O)(CC([O-])=O)C([O-])=O KRKNYBCHXYNGOX-UHFFFAOYSA-K 0.000 description 1
- 102000008186 Collagen Human genes 0.000 description 1
- 108010035532 Collagen Proteins 0.000 description 1
- ITRJWOMZKQRYTA-RFZYENFJSA-N Cortisone acetate Chemical compound C1CC2=CC(=O)CC[C@]2(C)[C@@H]2[C@@H]1[C@@H]1CC[C@@](C(=O)COC(=O)C)(O)[C@@]1(C)CC2=O ITRJWOMZKQRYTA-RFZYENFJSA-N 0.000 description 1
- 229920000742 Cotton Polymers 0.000 description 1
- 108090000695 Cytokines Proteins 0.000 description 1
- FBPFZTCFMRRESA-FSIIMWSLSA-N D-Glucitol Natural products OC[C@H](O)[C@H](O)[C@@H](O)[C@H](O)CO FBPFZTCFMRRESA-FSIIMWSLSA-N 0.000 description 1
- FBPFZTCFMRRESA-JGWLITMVSA-N D-glucitol Chemical compound OC[C@H](O)[C@@H](O)[C@H](O)[C@H](O)CO FBPFZTCFMRRESA-JGWLITMVSA-N 0.000 description 1
- 230000005778 DNA damage Effects 0.000 description 1
- 231100000277 DNA damage Toxicity 0.000 description 1
- 229920001353 Dextrin Polymers 0.000 description 1
- 239000004375 Dextrin Substances 0.000 description 1
- FEWJPZIEWOKRBE-JCYAYHJZSA-N Dextrotartaric acid Chemical compound OC(=O)[C@H](O)[C@@H](O)C(O)=O FEWJPZIEWOKRBE-JCYAYHJZSA-N 0.000 description 1
- 238000008157 ELISA kit Methods 0.000 description 1
- PXGOKWXKJXAPGV-UHFFFAOYSA-N Fluorine Chemical compound FF PXGOKWXKJXAPGV-UHFFFAOYSA-N 0.000 description 1
- VZCYOOQTPOCHFL-OWOJBTEDSA-N Fumaric acid Chemical compound OC(=O)\C=C\C(O)=O VZCYOOQTPOCHFL-OWOJBTEDSA-N 0.000 description 1
- 241000287828 Gallus gallus Species 0.000 description 1
- 108010010803 Gelatin Proteins 0.000 description 1
- PVNIQBQSYATKKL-UHFFFAOYSA-N Glycerol trihexadecanoate Natural products CCCCCCCCCCCCCCCC(=O)OCC(OC(=O)CCCCCCCCCCCCCCC)COC(=O)CCCCCCCCCCCCCCC PVNIQBQSYATKKL-UHFFFAOYSA-N 0.000 description 1
- 229930186217 Glycolipid Natural products 0.000 description 1
- 102000003886 Glycoproteins Human genes 0.000 description 1
- 108090000288 Glycoproteins Proteins 0.000 description 1
- YCISZOVUHXIOFY-HKXOFBAYSA-N Halopredone acetate Chemical compound C1([C@H](F)C2)=CC(=O)C(Br)=C[C@]1(C)[C@]1(F)[C@@H]2[C@@H]2CC[C@](OC(C)=O)(C(=O)COC(=O)C)[C@@]2(C)C[C@@H]1O YCISZOVUHXIOFY-HKXOFBAYSA-N 0.000 description 1
- 102100039869 Histone H2B type F-S Human genes 0.000 description 1
- 101001035372 Homo sapiens Histone H2B type F-S Proteins 0.000 description 1
- VEXZGXHMUGYJMC-UHFFFAOYSA-N Hydrochloric acid Chemical compound Cl VEXZGXHMUGYJMC-UHFFFAOYSA-N 0.000 description 1
- 208000002682 Hyperkalemia Diseases 0.000 description 1
- 208000013016 Hypoglycemia Diseases 0.000 description 1
- QNAYBMKLOCPYGJ-REOHCLBHSA-N L-alanine Chemical compound C[C@H](N)C(O)=O QNAYBMKLOCPYGJ-REOHCLBHSA-N 0.000 description 1
- WQZGKKKJIJFFOK-ZZWDRFIYSA-N L-glucose Chemical compound OC[C@@H]1OC(O)[C@@H](O)[C@H](O)[C@H]1O WQZGKKKJIJFFOK-ZZWDRFIYSA-N 0.000 description 1
- WHUUTDBJXJRKMK-VKHMYHEASA-N L-glutamic acid Chemical compound OC(=O)[C@@H](N)CCC(O)=O WHUUTDBJXJRKMK-VKHMYHEASA-N 0.000 description 1
- ROHFNLRQFUQHCH-YFKPBYRVSA-N L-leucine Chemical compound CC(C)C[C@H](N)C(O)=O ROHFNLRQFUQHCH-YFKPBYRVSA-N 0.000 description 1
- GUBGYTABKSRVRQ-QKKXKWKRSA-N Lactose Natural products OC[C@H]1O[C@@H](O[C@H]2[C@H](O)[C@@H](O)C(O)O[C@@H]2CO)[C@H](O)[C@@H](O)[C@H]1O GUBGYTABKSRVRQ-QKKXKWKRSA-N 0.000 description 1
- 239000004166 Lanolin Substances 0.000 description 1
- ROHFNLRQFUQHCH-UHFFFAOYSA-N Leucine Natural products CC(C)CC(N)C(O)=O ROHFNLRQFUQHCH-UHFFFAOYSA-N 0.000 description 1
- 102100037611 Lysophospholipase Human genes 0.000 description 1
- 241000124008 Mammalia Species 0.000 description 1
- AFVFQIVMOAPDHO-UHFFFAOYSA-N Methanesulfonic acid Chemical compound CS(O)(=O)=O AFVFQIVMOAPDHO-UHFFFAOYSA-N 0.000 description 1
- 229910002651 NO3 Inorganic materials 0.000 description 1
- NHNBFGGVMKEFGY-UHFFFAOYSA-N Nitrate Chemical compound [O-][N+]([O-])=O NHNBFGGVMKEFGY-UHFFFAOYSA-N 0.000 description 1
- 235000021314 Palmitic acid Nutrition 0.000 description 1
- 206010033645 Pancreatitis Diseases 0.000 description 1
- 239000004264 Petrolatum Substances 0.000 description 1
- 108010058864 Phospholipases A2 Proteins 0.000 description 1
- 239000002202 Polyethylene glycol Substances 0.000 description 1
- 208000004210 Pressure Ulcer Diseases 0.000 description 1
- 208000003251 Pruritus Diseases 0.000 description 1
- 206010039085 Rhinitis allergic Diseases 0.000 description 1
- 206010039101 Rhinorrhoea Diseases 0.000 description 1
- 206010040880 Skin irritation Diseases 0.000 description 1
- 229920002472 Starch Polymers 0.000 description 1
- 235000021355 Stearic acid Nutrition 0.000 description 1
- 229930006000 Sucrose Natural products 0.000 description 1
- CZMRCDWAGMRECN-UGDNZRGBSA-N Sucrose Chemical compound O[C@H]1[C@H](O)[C@@H](CO)O[C@@]1(CO)O[C@@H]1[C@H](O)[C@@H](O)[C@H](O)[C@@H](CO)O1 CZMRCDWAGMRECN-UGDNZRGBSA-N 0.000 description 1
- 206010061373 Sudden Hearing Loss Diseases 0.000 description 1
- QAOWNCQODCNURD-UHFFFAOYSA-L Sulfate Chemical compound [O-]S([O-])(=O)=O QAOWNCQODCNURD-UHFFFAOYSA-L 0.000 description 1
- BHEOSNUKNHRBNM-UHFFFAOYSA-N Tetramethylsqualene Natural products CC(=C)C(C)CCC(=C)C(C)CCC(C)=CCCC=C(C)CCC(C)C(=C)CCC(C)C(C)=C BHEOSNUKNHRBNM-UHFFFAOYSA-N 0.000 description 1
- GSEJCLTVZPLZKY-UHFFFAOYSA-N Triethanolamine Chemical class OCCN(CCO)CCO GSEJCLTVZPLZKY-UHFFFAOYSA-N 0.000 description 1
- ZMANZCXQSJIPKH-UHFFFAOYSA-N Triethylamine Chemical class CCN(CC)CC ZMANZCXQSJIPKH-UHFFFAOYSA-N 0.000 description 1
- 208000036142 Viral infection Diseases 0.000 description 1
- 241000700605 Viruses Species 0.000 description 1
- 240000008042 Zea mays Species 0.000 description 1
- 235000005824 Zea mays ssp. parviglumis Nutrition 0.000 description 1
- 235000002017 Zea mays subsp mays Nutrition 0.000 description 1
- XKMYWNHZAQUEPY-YZGJEOKZSA-N [(3s,8s,9s,10r,13r,14s,17r)-10,13-dimethyl-17-[(2r)-6-methylheptan-2-yl]-2,3,4,7,8,9,11,12,14,15,16,17-dodecahydro-1h-cyclopenta[a]phenanthren-3-yl] 12-hydroxyoctadecanoate Chemical compound C([C@@H]12)C[C@]3(C)[C@@H]([C@H](C)CCCC(C)C)CC[C@H]3[C@@H]1CC=C1[C@]2(C)CC[C@H](OC(=O)CCCCCCCCCCC(O)CCCCCC)C1 XKMYWNHZAQUEPY-YZGJEOKZSA-N 0.000 description 1
- 230000002159 abnormal effect Effects 0.000 description 1
- 238000005299 abrasion Methods 0.000 description 1
- 239000006096 absorbing agent Substances 0.000 description 1
- 229940022663 acetate Drugs 0.000 description 1
- 206010000496 acne Diseases 0.000 description 1
- 230000003213 activating effect Effects 0.000 description 1
- 239000000443 aerosol Substances 0.000 description 1
- 235000004279 alanine Nutrition 0.000 description 1
- 150000001298 alcohols Chemical class 0.000 description 1
- 229910052783 alkali metal Inorganic materials 0.000 description 1
- 229910052784 alkaline earth metal Inorganic materials 0.000 description 1
- 239000013566 allergen Substances 0.000 description 1
- 208000026935 allergic disease Diseases 0.000 description 1
- 201000010105 allergic rhinitis Diseases 0.000 description 1
- 235000001014 amino acid Nutrition 0.000 description 1
- 230000003266 anti-allergic effect Effects 0.000 description 1
- 239000002260 anti-inflammatory agent Substances 0.000 description 1
- 239000003963 antioxidant agent Substances 0.000 description 1
- 230000001640 apoptogenic effect Effects 0.000 description 1
- 239000007864 aqueous solution Substances 0.000 description 1
- 230000001580 bacterial effect Effects 0.000 description 1
- 208000022362 bacterial infectious disease Diseases 0.000 description 1
- 230000004888 barrier function Effects 0.000 description 1
- 239000002585 base Substances 0.000 description 1
- 235000013871 bee wax Nutrition 0.000 description 1
- 239000012166 beeswax Substances 0.000 description 1
- JUHORIMYRDESRB-UHFFFAOYSA-N benzathine Chemical class C=1C=CC=CC=1CNCCNCC1=CC=CC=C1 JUHORIMYRDESRB-UHFFFAOYSA-N 0.000 description 1
- 159000000007 calcium salts Chemical class 0.000 description 1
- 244000309466 calf Species 0.000 description 1
- 239000002775 capsule Substances 0.000 description 1
- 150000001720 carbohydrates Chemical class 0.000 description 1
- 235000014633 carbohydrates Nutrition 0.000 description 1
- 125000004432 carbon atom Chemical group C* 0.000 description 1
- 210000004413 cardiac myocyte Anatomy 0.000 description 1
- 239000000679 carrageenan Substances 0.000 description 1
- 235000010418 carrageenan Nutrition 0.000 description 1
- 229920001525 carrageenan Polymers 0.000 description 1
- 229940113118 carrageenan Drugs 0.000 description 1
- 239000000969 carrier Substances 0.000 description 1
- 210000003855 cell nucleus Anatomy 0.000 description 1
- 229940072104 cholesteryl hydroxystearate Drugs 0.000 description 1
- 210000003483 chromatin Anatomy 0.000 description 1
- 229920001436 collagen Polymers 0.000 description 1
- 239000000470 constituent Substances 0.000 description 1
- 235000005822 corn Nutrition 0.000 description 1
- 150000001886 cortisols Chemical class 0.000 description 1
- 229960003290 cortisone acetate Drugs 0.000 description 1
- 238000002425 crystallisation Methods 0.000 description 1
- 230000008025 crystallization Effects 0.000 description 1
- 230000001086 cytosolic effect Effects 0.000 description 1
- 230000007423 decrease Effects 0.000 description 1
- PLCQGRYPOISRTQ-FCJDYXGNSA-L dexamethasone sodium phosphate Chemical compound [Na+].[Na+].C1CC2=CC(=O)C=C[C@]2(C)[C@]2(F)[C@@H]1[C@@H]1C[C@@H](C)[C@@](C(=O)COP([O-])([O-])=O)(O)[C@@]1(C)C[C@@H]2O PLCQGRYPOISRTQ-FCJDYXGNSA-L 0.000 description 1
- 229960002344 dexamethasone sodium phosphate Drugs 0.000 description 1
- 235000019425 dextrin Nutrition 0.000 description 1
- KPUWHANPEXNPJT-UHFFFAOYSA-N disiloxane Chemical class [SiH3]O[SiH3] KPUWHANPEXNPJT-UHFFFAOYSA-N 0.000 description 1
- 239000012153 distilled water Substances 0.000 description 1
- PRAKJMSDJKAYCZ-UHFFFAOYSA-N dodecahydrosqualene Natural products CC(C)CCCC(C)CCCC(C)CCCCC(C)CCCC(C)CCCC(C)C PRAKJMSDJKAYCZ-UHFFFAOYSA-N 0.000 description 1
- LQZZUXJYWNFBMV-UHFFFAOYSA-N dodecan-1-ol Chemical compound CCCCCCCCCCCCO LQZZUXJYWNFBMV-UHFFFAOYSA-N 0.000 description 1
- 238000002651 drug therapy Methods 0.000 description 1
- 239000003995 emulsifying agent Substances 0.000 description 1
- 238000005516 engineering process Methods 0.000 description 1
- 150000002169 ethanolamines Chemical class 0.000 description 1
- 230000001747 exhibiting effect Effects 0.000 description 1
- 239000003889 eye drop Substances 0.000 description 1
- 229940012356 eye drops Drugs 0.000 description 1
- 210000002950 fibroblast Anatomy 0.000 description 1
- 238000011049 filling Methods 0.000 description 1
- SYWHXTATXSMDSB-GSLJADNHSA-N fludrocortisone acetate Chemical compound C1CC2=CC(=O)CC[C@]2(C)[C@]2(F)[C@@H]1[C@@H]1CC[C@@](C(=O)COC(=O)C)(O)[C@@]1(C)C[C@@H]2O SYWHXTATXSMDSB-GSLJADNHSA-N 0.000 description 1
- 229910052731 fluorine Inorganic materials 0.000 description 1
- 239000011737 fluorine Substances 0.000 description 1
- 229960003336 fluorocortisol acetate Drugs 0.000 description 1
- 238000004108 freeze drying Methods 0.000 description 1
- 210000001035 gastrointestinal tract Anatomy 0.000 description 1
- 229920000159 gelatin Polymers 0.000 description 1
- 239000008273 gelatin Substances 0.000 description 1
- 229940014259 gelatin Drugs 0.000 description 1
- 235000019322 gelatine Nutrition 0.000 description 1
- 235000011852 gelatine desserts Nutrition 0.000 description 1
- 239000003862 glucocorticoid Substances 0.000 description 1
- 229930195712 glutamate Natural products 0.000 description 1
- 229950004611 halopredone acetate Drugs 0.000 description 1
- 208000006454 hepatitis Diseases 0.000 description 1
- 231100000283 hepatitis Toxicity 0.000 description 1
- 239000003906 humectant Substances 0.000 description 1
- 229920002674 hyaluronan Polymers 0.000 description 1
- 229960003160 hyaluronic acid Drugs 0.000 description 1
- 229960001401 hydrocortisone sodium succinate Drugs 0.000 description 1
- WGCNASOHLSPBMP-UHFFFAOYSA-N hydroxyacetaldehyde Natural products OCC=O WGCNASOHLSPBMP-UHFFFAOYSA-N 0.000 description 1
- 230000002218 hypoglycaemic effect Effects 0.000 description 1
- 230000001506 immunosuppresive effect Effects 0.000 description 1
- 230000001771 impaired effect Effects 0.000 description 1
- 230000000415 inactivating effect Effects 0.000 description 1
- 230000002779 inactivation Effects 0.000 description 1
- 230000002757 inflammatory effect Effects 0.000 description 1
- 208000014674 injury Diseases 0.000 description 1
- 230000015788 innate immune response Effects 0.000 description 1
- 230000009545 invasion Effects 0.000 description 1
- 229940119170 jojoba wax Drugs 0.000 description 1
- 239000008101 lactose Substances 0.000 description 1
- 229940039717 lanolin Drugs 0.000 description 1
- 235000019388 lanolin Nutrition 0.000 description 1
- 239000007788 liquid Substances 0.000 description 1
- 229940057995 liquid paraffin Drugs 0.000 description 1
- 239000007937 lozenge Substances 0.000 description 1
- 159000000003 magnesium salts Chemical class 0.000 description 1
- 230000007721 medicinal effect Effects 0.000 description 1
- 230000003340 mental effect Effects 0.000 description 1
- 125000002496 methyl group Chemical group [H]C([H])([H])* 0.000 description 1
- 229960004584 methylprednisolone Drugs 0.000 description 1
- 229960000334 methylprednisolone sodium succinate Drugs 0.000 description 1
- 230000001617 migratory effect Effects 0.000 description 1
- 150000002772 monosaccharides Chemical class 0.000 description 1
- 210000000214 mouth Anatomy 0.000 description 1
- WQEPLUUGTLDZJY-UHFFFAOYSA-N n-Pentadecanoic acid Natural products CCCCCCCCCCCCCCC(O)=O WQEPLUUGTLDZJY-UHFFFAOYSA-N 0.000 description 1
- GOQYKNQRPGWPLP-UHFFFAOYSA-N n-heptadecyl alcohol Natural products CCCCCCCCCCCCCCCCCO GOQYKNQRPGWPLP-UHFFFAOYSA-N 0.000 description 1
- 208000010753 nasal discharge Diseases 0.000 description 1
- 230000001338 necrotic effect Effects 0.000 description 1
- 230000012666 negative regulation of transcription by glucose Effects 0.000 description 1
- 231100000252 nontoxic Toxicity 0.000 description 1
- 230000003000 nontoxic effect Effects 0.000 description 1
- 230000009701 normal cell proliferation Effects 0.000 description 1
- 238000010606 normalization Methods 0.000 description 1
- QIQXTHQIDYTFRH-UHFFFAOYSA-N octadecanoic acid Chemical compound CCCCCCCCCCCCCCCCCC(O)=O QIQXTHQIDYTFRH-UHFFFAOYSA-N 0.000 description 1
- OQCDKBAXFALNLD-UHFFFAOYSA-N octadecanoic acid Natural products CCCCCCCC(C)CCCCCCCCC(O)=O OQCDKBAXFALNLD-UHFFFAOYSA-N 0.000 description 1
- 238000010979 pH adjustment Methods 0.000 description 1
- 229940098695 palmitic acid Drugs 0.000 description 1
- 229940066842 petrolatum Drugs 0.000 description 1
- 235000019271 petrolatum Nutrition 0.000 description 1
- 230000001766 physiological effect Effects 0.000 description 1
- 239000002504 physiological saline solution Substances 0.000 description 1
- 239000006187 pill Substances 0.000 description 1
- 229920001223 polyethylene glycol Polymers 0.000 description 1
- 239000011148 porous material Substances 0.000 description 1
- 159000000001 potassium salts Chemical class 0.000 description 1
- 239000000843 powder Substances 0.000 description 1
- 230000002265 prevention Effects 0.000 description 1
- BDERNNFJNOPAEC-UHFFFAOYSA-N propan-1-ol Chemical compound CCCO BDERNNFJNOPAEC-UHFFFAOYSA-N 0.000 description 1
- 230000000069 prophylactic effect Effects 0.000 description 1
- 235000018102 proteins Nutrition 0.000 description 1
- 102000004169 proteins and genes Human genes 0.000 description 1
- 150000003222 pyridines Chemical class 0.000 description 1
- 210000002345 respiratory system Anatomy 0.000 description 1
- 230000028327 secretion Effects 0.000 description 1
- 206010040560 shock Diseases 0.000 description 1
- 210000002363 skeletal muscle cell Anatomy 0.000 description 1
- 208000017520 skin disease Diseases 0.000 description 1
- 230000036556 skin irritation Effects 0.000 description 1
- 231100000475 skin irritation Toxicity 0.000 description 1
- 159000000000 sodium salts Chemical class 0.000 description 1
- 239000012439 solid excipient Substances 0.000 description 1
- 239000000600 sorbitol Substances 0.000 description 1
- 229940031439 squalene Drugs 0.000 description 1
- TUHBEKDERLKLEC-UHFFFAOYSA-N squalene Natural products CC(=CCCC(=CCCC(=CCCC=C(/C)CCC=C(/C)CC=C(C)C)C)C)C TUHBEKDERLKLEC-UHFFFAOYSA-N 0.000 description 1
- 235000019698 starch Nutrition 0.000 description 1
- 239000008107 starch Substances 0.000 description 1
- 239000008117 stearic acid Substances 0.000 description 1
- 229960004274 stearic acid Drugs 0.000 description 1
- 210000000130 stem cell Anatomy 0.000 description 1
- 239000005720 sucrose Substances 0.000 description 1
- 150000008163 sugars Chemical class 0.000 description 1
- 150000003871 sulfonates Chemical class 0.000 description 1
- 239000000829 suppository Substances 0.000 description 1
- 239000004094 surface-active agent Substances 0.000 description 1
- 238000003786 synthesis reaction Methods 0.000 description 1
- 239000006188 syrup Substances 0.000 description 1
- 235000020357 syrup Nutrition 0.000 description 1
- 239000003826 tablet Substances 0.000 description 1
- 229940095064 tartrate Drugs 0.000 description 1
- 206010043778 thyroiditis Diseases 0.000 description 1
- JOXIMZWYDAKGHI-UHFFFAOYSA-N toluene-4-sulfonic acid Chemical compound CC1=CC=C(S(O)(=O)=O)C=C1 JOXIMZWYDAKGHI-UHFFFAOYSA-N 0.000 description 1
- VZCYOOQTPOCHFL-UHFFFAOYSA-N trans-butenedioic acid Natural products OC(=O)C=CC(O)=O VZCYOOQTPOCHFL-UHFFFAOYSA-N 0.000 description 1
- 238000013518 transcription Methods 0.000 description 1
- 230000035897 transcription Effects 0.000 description 1
- 229960005294 triamcinolone Drugs 0.000 description 1
- GFNANZIMVAIWHM-OBYCQNJPSA-N triamcinolone Chemical compound O=C1C=C[C@]2(C)[C@@]3(F)[C@@H](O)C[C@](C)([C@@]([C@H](O)C4)(O)C(=O)CO)[C@@H]4[C@@H]3CCC2=C1 GFNANZIMVAIWHM-OBYCQNJPSA-N 0.000 description 1
- 229960002117 triamcinolone acetonide Drugs 0.000 description 1
- YNDXUCZADRHECN-JNQJZLCISA-N triamcinolone acetonide Chemical compound C1CC2=CC(=O)C=C[C@]2(C)[C@]2(F)[C@@H]1[C@@H]1C[C@H]3OC(C)(C)O[C@@]3(C(=O)CO)[C@@]1(C)C[C@@H]2O YNDXUCZADRHECN-JNQJZLCISA-N 0.000 description 1
- 210000003556 vascular endothelial cell Anatomy 0.000 description 1
- 230000009385 viral infection Effects 0.000 description 1
- 230000029663 wound healing Effects 0.000 description 1
- 229920001285 xanthan gum Polymers 0.000 description 1
- 239000000230 xanthan gum Substances 0.000 description 1
- 235000010493 xanthan gum Nutrition 0.000 description 1
- 229940082509 xanthan gum Drugs 0.000 description 1
- UHVMMEOXYDMDKI-JKYCWFKZSA-L zinc;1-(5-cyanopyridin-2-yl)-3-[(1s,2s)-2-(6-fluoro-2-hydroxy-3-propanoylphenyl)cyclopropyl]urea;diacetate Chemical compound [Zn+2].CC([O-])=O.CC([O-])=O.CCC(=O)C1=CC=C(F)C([C@H]2[C@H](C2)NC(=O)NC=2N=CC(=CC=2)C#N)=C1O UHVMMEOXYDMDKI-JKYCWFKZSA-L 0.000 description 1
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K8/00—Cosmetics or similar toiletry preparations
- A61K8/18—Cosmetics or similar toiletry preparations characterised by the composition
- A61K8/30—Cosmetics or similar toiletry preparations characterised by the composition containing organic compounds
- A61K8/60—Sugars; Derivatives thereof
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/56—Compounds containing cyclopenta[a]hydrophenanthrene ring systems; Derivatives thereof, e.g. steroids
- A61K31/57—Compounds containing cyclopenta[a]hydrophenanthrene ring systems; Derivatives thereof, e.g. steroids substituted in position 17 beta by a chain of two carbon atoms, e.g. pregnane or progesterone
- A61K31/573—Compounds containing cyclopenta[a]hydrophenanthrene ring systems; Derivatives thereof, e.g. steroids substituted in position 17 beta by a chain of two carbon atoms, e.g. pregnane or progesterone substituted in position 21, e.g. cortisone, dexamethasone, prednisone or aldosterone
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/70—Carbohydrates; Sugars; Derivatives thereof
- A61K31/7004—Monosaccharides having only carbon, hydrogen and oxygen atoms
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K8/00—Cosmetics or similar toiletry preparations
- A61K8/18—Cosmetics or similar toiletry preparations characterised by the composition
- A61K8/30—Cosmetics or similar toiletry preparations characterised by the composition containing organic compounds
- A61K8/63—Steroids; Derivatives thereof
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P1/00—Drugs for disorders of the alimentary tract or the digestive system
- A61P1/04—Drugs for disorders of the alimentary tract or the digestive system for ulcers, gastritis or reflux esophagitis, e.g. antacids, inhibitors of acid secretion, mucosal protectants
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P1/00—Drugs for disorders of the alimentary tract or the digestive system
- A61P1/16—Drugs for disorders of the alimentary tract or the digestive system for liver or gallbladder disorders, e.g. hepatoprotective agents, cholagogues, litholytics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P1/00—Drugs for disorders of the alimentary tract or the digestive system
- A61P1/18—Drugs for disorders of the alimentary tract or the digestive system for pancreatic disorders, e.g. pancreatic enzymes
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P11/00—Drugs for disorders of the respiratory system
- A61P11/06—Antiasthmatics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P13/00—Drugs for disorders of the urinary system
- A61P13/12—Drugs for disorders of the urinary system of the kidneys
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P17/00—Drugs for dermatological disorders
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P17/00—Drugs for dermatological disorders
- A61P17/02—Drugs for dermatological disorders for treating wounds, ulcers, burns, scars, keloids, or the like
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P17/00—Drugs for dermatological disorders
- A61P17/10—Anti-acne agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P19/00—Drugs for skeletal disorders
- A61P19/02—Drugs for skeletal disorders for joint disorders, e.g. arthritis, arthrosis
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P29/00—Non-central analgesic, antipyretic or antiinflammatory agents, e.g. antirheumatic agents; Non-steroidal antiinflammatory drugs [NSAID]
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P37/00—Drugs for immunological or allergic disorders
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P37/00—Drugs for immunological or allergic disorders
- A61P37/02—Immunomodulators
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P37/00—Drugs for immunological or allergic disorders
- A61P37/02—Immunomodulators
- A61P37/06—Immunosuppressants, e.g. drugs for graft rejection
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P37/00—Drugs for immunological or allergic disorders
- A61P37/08—Antiallergic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P43/00—Drugs for specific purposes, not provided for in groups A61P1/00-A61P41/00
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P5/00—Drugs for disorders of the endocrine system
- A61P5/14—Drugs for disorders of the endocrine system of the thyroid hormones, e.g. T3, T4
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61Q—SPECIFIC USE OF COSMETICS OR SIMILAR TOILETRY PREPARATIONS
- A61Q19/00—Preparations for care of the skin
- A61Q19/08—Anti-ageing preparations
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/0012—Galenical forms characterised by the site of application
- A61K9/0019—Injectable compositions; Intramuscular, intravenous, arterial, subcutaneous administration; Compositions to be administered through the skin in an invasive manner
Description
細胞障害の治療に用いる医薬組成物として、生体組織(以下、単に組織ということがある)に対し修復作用を有する多糖類やオリゴ糖を含有するものが提案されている。例えば、哺乳動物に対して生理活性を有し且つ糖タンパク質糖鎖及び糖脂質糖鎖を構成する単糖を一種以上構成糖として含む多糖類及び/又はそのオリゴ糖を配合・混合してなる組織・細胞障害のための予防・修復剤が提案されている(例えば、特許文献1)。
一方、循環虚脱、低血糖時の糖質補給、高カリウム血症、非経口的なエネルギー及び水補給を目的とした注射剤に含有されるグルコースは、組織の修復を遅延させると報告されている(例えば、非特許文献1)。
ステロイド剤は、元々、生体内の臓器で産生される化合物であり、一般に、副腎皮質ステロイドを指す。ステロイド剤は、その適用範囲が広く、適応症が最も多い薬剤の一つとして知られている。ステロイド剤の適用対象となる疾患としては、例えば、気管支喘息、アトピー性皮膚炎、花粉症、アレルギー性鼻炎、突発性難聴、関節リュウマチ、膠原病、ネフローゼ症候群、潰瘍性大腸炎等が挙げられる。
そこで、本発明は、細胞障害を効果的に予防でき、各種障害を受けた組織の修復を促進できる医薬組成物を目的とする。
本発明者らは、鋭意検討した結果、意外にもグルコースがHMGB1の産生を促進し、HMGB1の細胞外への放出を誘導し、正常細胞の増殖や遊走を高め、組織の修復を促進できるとの知見を得て、本発明に至った。
さらに、ステロイド剤を含有してもよく、前記グルコース/前記ステロイド剤で表されるモル比が10〜105であることが好ましい。
本発明の医薬組成物は、組織修復促進剤としてグルコースを含有するものである。
医薬組成物としては、例えば、アトピー性皮膚炎、気管支喘息、関節リウマチや膠原病等の自己免疫疾患の治療薬;ネフローゼ症候群、潰瘍性大腸炎、肝炎、膵炎、甲状腺炎、感冒等の臓器炎症等の疾患の治療薬等の抗炎症薬;やけど、傷、床ずれ、にきび、あせも、しもやけ等の創傷の治療薬(創傷治療薬)等が挙げられ、特に抗炎症薬、創傷治療薬において、本発明の効果が顕著である。
本発明の医薬組成物は、組織修復促進剤としてグルコースを含有することで、細胞でのHMGB1の産生を促進し、細胞からのHMGB1の放出を誘導して、組織の修復を促進できる。
組織修復促進剤は、細胞の増殖を促進し、障害細胞を含む組織の自己修復を図るものである。
医薬組成物中のグルコースの含有量は、医薬組成物の剤形、用途、用法等を勘案して決定でき、例えば、経皮吸収剤であれば、0.1〜5mol/Lが好ましく、1〜3mol/Lが好ましい。上記下限値以上であれば、経皮吸収されたグルコースによって、HMGB1の産出と放出とをより促進して、細胞障害をより良好に予防し、組織の修復を促進できる。上記上限値以下であれば、グルコースが医薬組成物中に均一に分散して、細胞障害をより良好に予防し、組織の修復を十分に促進できる。
また、例えば、注射剤であれば、1〜1000mM/Lが好ましく、10〜100mM/Lがより好ましい。上記範囲内であれば、HMGB1の産生と放出とをより促進して、細胞障害をより良好に予防し、組織の修復をより促進できる。
医薬組成物は、ステロイド剤を含有してもよい。医薬組成物は、ステロイド剤を含有することで、抗炎症作用等の優れた作用を発揮できる。加えて、ステロイド剤を含有する医薬組成物において、本発明の効果がより顕著に発揮される。特に、ステロイド剤の抗炎症作用等の薬効が期待される抗炎症薬等の医薬組成物において、ステロイド剤の増殖抑制作用はグルコースにより顕著に軽減される。
プレドニゾロンは経口投与剤として汎用されており、ヒドロコルチゾンのステロイド骨格の1,2位に二重結合を有し、ヒドロコルチゾンよりも強力な抗炎症作用を持つ。
デキサメサゾンは、プレドニゾロンの9位にフッ素、16位にメチル基が導入された合成グルココルチコイドであり、プレドニゾロンよりも強力な抗炎症作用、抗アレルギー作用を発揮する。ベタメタゾンは、デキサメサゾンの異性体であり、長時間作用する強力なステロイド剤として知られている。
医薬組成物は、グルコース及びステロイド剤に加え、必要に応じて、任意成分(特に医薬任意成分ということがある)を含有できる。医薬任意成分としては、例えば、薬理学的に許容される塩、賦形剤、増粘剤、担体、香料、色素等が挙げられる。これらの医薬任意成分は、1種単独で用いられてもよいし、2種以上が組み合わされて用いられてもよい。
例えば、疾患がアトピー性皮膚炎、切り傷や擦り傷等の皮膚の創傷等である場合、経皮吸収剤である医薬組成物を直接患部に塗布する方法等が挙げられる。
また、疾患が口腔内や胃腸である場合、医薬組成物を経口剤として経口投与する方法、医薬組成物を注射剤として患部組織に注入する方法等が挙げられる。もしくは、例えば、上部内視鏡下で患部を医薬組成物で洗浄したり、患部に医薬組成物を塗布することにより、粘膜再生を促してもよい。これにより、健全な粘膜を形成でき、自然治癒を漸増させ、粘膜侵襲を防ぐことができる。さらに、医薬組成物を胃粘膜に塗布することで、胃粘膜の再生を促し、上皮組織を修復できる。上皮細胞の修復、即ち、正常細胞の活性化を促すことで、癌化細胞等の異常細胞の増殖を抑え、組織の正常化を誘導できる。
また、疾患が花粉症等、鼻・眼粘膜部の疾患である場合、医薬組成物を患部に塗布する方法が挙げられる。医薬組成物を鼻・眼粘膜部に塗布すると、鼻・眼粘膜部は、修復され、かつ粘膜層に強固なバリアを形成する。このため、鼻・眼粘膜部にアレルゲンが多数付着してもアレルギー反応を押さえ、鼻詰まりが生じたり、鼻汁又は涙が多量に分泌されたりするのを解消できる。
また、あるいは、疾患が風邪等のウィルスや細菌の感染による上気道粘膜の炎症(感冒)である場合、医薬組成物を点鼻したり吸入させたりする方法が挙げられる。これにより、上気道粘膜の炎症を抑え、上気道粘膜を修復して再生して感染進行を抑制でき、かつ自然免疫応答の賦活化を促進できる。
本発明の薬用化粧品は、本発明の医薬組成物を含有するものである。本発明の薬用化粧品は、例えば、ローション、クリーム、乳液、ファンデーション等であって、皮膚疾患の予防を目的とするものである。なお、薬用化粧品は、日本国の薬事法に定められた医薬部外品に分類されるものである。
薬用化粧品がステロイド剤を含む場合、薬用化粧品中のグルコース/ステロイド比は、10〜105が好ましく、102〜104がより好ましく、102〜103がさらに好ましい。上記範囲内であれば、ステロイド剤の増殖抑制作用がより軽減されて、組織の修復がより促進されやすくなる。加えて、上記範囲内であれば、ステロイド剤の抗炎症作用等の作用が十分に発揮されやすい。
化粧品任意成分としては、例えば、流動パラフィン、セレシン、じろう、ラノリン、ワセリン、セタノール、スクワレン、ホホバ油、ステアリン酸、パルミチン酸、ラウリルアルコール、ステアリルアルコール、セチルアルコール、ミツロウ、メチルポリシロキサン、ジメチルシクロポリシロキサン等の油剤;プロパノール、グリコール、プロピレングリコール、ヒアルロン酸、コラーゲン、ポリエチレングリコール、ヒドロキシステアリン酸コレステリル、グリセリン、ソルビトール等の保湿剤;各種界面活性剤;乳化剤;賦形剤:増粘剤;PH調整剤;酸化防止剤;色素;香料;紫外線吸収剤等が挙げられる。これらの化粧品任意成分は、1種単独で用いられてもよいし、2種以上が組み合わされて用いられてもよい。
さらに、グルコース/ステロイド比を特定の範囲とすることで、ステロイド剤の抗炎症作用等の作用をより高度に維持したまま、ステロイド剤の増殖抑制作用を軽減して、細胞障害をより効果的に予防でき、各種障害を受けた組織の修復をより促進できる。
本発明の薬用化粧品は、本発明の医薬組成物を含有するため、細胞障害を効果的に予防でき、各種障害を受けた組織の修復を促進できる。
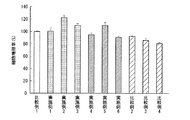
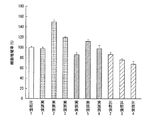
1質量%仔牛血清(FBS)含有ダルベッコ変性イーグル培地(1%FBS−DMEM、ライフテクノロジーズジャパン株式会社製)に、表1の濃度となるようにL−グルコースとデキサメサゾン(製品番号:D4902、シグマ−アルドリッチ(Sigma−Aldorich)社製)とを添加し、医薬組成物を含有する培地(以下、試験用培地という)を調製した。各例の試験用培地を用いて、細胞増殖試験を行い、その結果を表1、図1〜2に示す。
1%FBS−DMEMを用い、正常ヒト皮膚角化細胞(単一ドナー由来の初代培養の正常皮膚角化細胞、タカラバイオ株式会社製)を96穴(well)マイクロプレートに20000cells/wellとなるように播種し、37℃で24時間培養した(前培養)。前培養後、各例の試験用培地を前培養に用いた培地と置換し、37℃で24時間培養した(本培養)。本培養後、3−(4,5−Dimethyl−2−thiazolyl)−2,5−diphenyltetrazolium Bromide(MTT)を0.4mg/mL含有する1%FBS−DMEMを試験用培地と置換し、37℃で4時間培養した(後培養)。後培養後、培地を除去し、Dimethyl sulfoxide100μL/wellを添加混合して試料液とし、この試料液の吸光度(550nm)を測定してMTTの還元量(α)を求めた。また、本培養を行わない以外は上述の方法と同様にして試料液(コントロール試料液)を調製し、このコントロール試料液の吸光度(550nm)を測定してMTTの還元量(β)を求め、下記(1)式により細胞増殖率を算出した。
細胞増殖率(%)=還元量(α)÷還元量(β)×100 ・・・(1)
正常ヒト皮膚角化細胞を正常ヒト皮膚線維芽細胞(単一ドナー由来の初代培養の正常皮膚線維芽細胞、タカラバイオ株式会社製)に換えた以外は、「<細胞増殖試験A>」と同様にして、細胞増殖率を求めた。
表1、図1〜2に示すように、本発明を適用した実施例1〜3は、細胞増殖率が100%と略同等又は100%超となっていた。特に、グルコースを10〜100mM/L含有する実施例2、3において、細胞増殖率の向上が顕著であった。
一方、グルコース及びデキサメサゾンを含まない比較例1は、細胞増殖試験A及びBにおいて、細胞増殖率が100%であった。
実施例1〜3、比較例1の結果から、グルコースを添加することにより、細胞の増殖を促進できることが判った。
比較例2〜4の結果に示すように、デキサメサゾンの含有量の増加に伴い、細胞増殖率が低下していた。この結果から、デキサメサゾンによって正常細胞の増殖が抑制されていることが判った。
細胞増殖試験A及びBにおいて、グルコース及びデキサメサゾンを含有する実施例4〜6は、実施例4〜6と同量のデキサメサゾンを含有し、かつグルコースを含有しない比較例3に比べて高い細胞増殖率であった。実施例4〜6、比較例3の結果から、正常細胞に対するデキサメサゾンの増殖抑制効果が、グルコースによって軽減されることが判った。
以上の結果から、本発明を適用することで、正常細胞の増殖を促進して、細胞障害を予防したり、各種障害を受けた組織の修復を促進したりできることが判った。
グルコース及び正常ヒト皮膚角化細胞を1%FBS−DMEMに添加し、グルコース濃度が10mM/L、正常ヒト皮膚角化細胞の含有量が100000cells/mLの試料懸濁液を調製した。この試料懸濁液100μLをCO2インキュベーター(37℃)内で24時間培養した。培養開始前(0時間)、培養開始3時間後、6時間後、18時間後、24時間後に上清を回収し、回収した上清中のHMGB1濃度をHMGB1 ELISA Kit II(株式会社シノテスト製)で測定した。その結果を図3に示す。
グルコースを含有しない試料懸濁液を用いた以外は、実施例7と同様にして上清中のHMGB1濃度を測定した。その結果を図3に示す。
グルコース濃度10mM/Lの1%FBS−DMEMを調製し、これを試験用培地とした。前培養をしないこと、及びマイクロプレートに10000cells/wellの正常ヒト皮膚角化細胞を播種した以外は、「<細胞増殖試験A>」と同様にして細胞増殖率を求め、その結果を図4に示す。
グルコース及び正常ヒト皮膚線維芽細胞を1%FBS−DMEMに添加し、グルコース濃度が10mM/L、正常ヒト皮膚線維芽細胞の含有量が100000cells/mLの試料懸濁液を調製した。この試料懸濁液を37℃で、24時間培養した後、上清(培養上清)を採取した。採取した培養上清100μLを正常ヒト皮膚角化細胞10000cellsに加え、37℃で24時間培養した。培養後、実施例8と同様にして細胞増殖率を求め、その結果を図4に示す。
さらにニワトリ抗HMGB1ポリクローナル抗体(IgYフラクション)を10μg/mLとなるように試験用培地に添加した以外は、実施例9と同様にして細胞増殖率を求め、その結果を図4に示す。
グルコースを添加しない以外は、実施例8と同様にして細胞増殖率を求め、その結果を図4に示す。
一方、グルコース及び培養上清を添加しなかった比較例6は、細胞増殖率が100%であった。
さらに、抗HMGB1抗体を添加した参考例1は、細胞増殖率が106%であり、実施例9に比べ細胞増殖率が低かった。即ち、HMGB1を不活化させることで、正常ヒト皮膚角化細胞の増殖が抑制された。実施例8〜9、参考例1の結果から、培養上清にはグルコースの存在により放出されたHMGB1が含まれ、このHMGB1によって正常ヒト皮膚角化細胞の増殖が促進されることが判った。
図3、4の結果から、グルコースは正常ヒト皮膚線維芽細胞からのHMGB1の放出を誘導し、放出されたHMGB1は正常ヒト皮膚角化細胞の増殖を促進することが判った。
そして、本発明を適用することで、正常細胞の増殖を促進し、組織の修復を促進できることが判った。
グルコース濃度10mM/Lの1%FBS−DMEMを試験用培地とし、この試験用培地を細胞遊走チャンバー(Becton Dickinson社製)の下層に添加した。100000個の正常ヒト皮膚角化細胞をフィルター(8μmポアサイズ、Becton Dickinson社製)付きインサートに播種した。播種されたインサートを24ウェルプレートに載置し、37℃、5体積%CO2環境下で2時間培養した。フィルター上層の細胞を綿棒で擦り取り、下層の細胞をメタノールで固定後、ヘマトキシリン染色を行った。無作為に選んだ5視野(倍率×200)の細胞数の平均を本例の遊走細胞数とした。後述する比較例7で測定された遊走細胞数を基準細胞遊走数とし、下記(2)式により細胞遊走能を求め、その結果を図5に示す。
グルコース及び正常ヒト皮膚線維芽細胞を1%FBS−DMEMに添加し、グルコース濃度が10mM/L、正常ヒト皮膚線維芽細胞の含有量が100000cells/mLの懸濁液を調製した。この懸濁液を37℃で、24時間培養した後、上清(培養上清)を採取した。この培養上清500μLとグルコース濃度10mM/Lの1%FBS−DMEM500μLとを混合して試験用培地とした以外は、実施例10と同様にして細胞遊走能を求めた。その結果を図5に示す。
さらに抗HMGB1抗体を10μg/mLとなるように試験用培地に添加した以外は、実施例11と同様にして細胞遊走能を求め、その結果を図5に示す。
グルコースを添加しない以外は、実施例10と同様にして細胞遊走能を求め、その結果を図5に示す。
一方、グルコース及び培養上清を添加しなかった比較例7は、細胞遊走能が100%であった。
さらに、抗HMGB1抗体を添加した参考例2は、細胞遊走能が116%であり、実施例11に比べ細胞遊走能が低かった。即ち、HMGB1を不活化させることで、正常ヒト皮膚角化細胞の遊走がより促進された。実施例10〜11、参考例2の結果から、培養上清にはグルコースの存在により放出されたHMGB1が含まれ、このHMGB1によって正常ヒト皮膚角化細胞の遊走が促進されることが判った。
図3、5の結果から、グルコースは正常ヒト皮膚線維芽細胞からのHMGB1の放出を誘導し、放出されたHMGB1は正常ヒト皮膚角化細胞の遊走を促進することが判った。
そして、本発明を適用することで、正常細胞の遊走を促進し、組織の修復を促進できることが判った。
グルコース含有量1.9mol/L、ステロイド(リン酸デキサメタゾンナトリウム)含有量0.096mol/Lを含有する水溶液を調製し、これを外用薬とした。
皮膚全体(顔部、上半身、下半身、指(手・足))に皮膚掻痒、色素沈着、苔癬化が見られる患者(20歳代男性)に対し、前記外用薬を患部に1回/1日塗布した。その結果、外用薬の塗布を開始した翌日には皮膚掻痒感がなくなり、外用薬の塗布を開始した3か月後には色素沈着、皮膚苔癬化が消失した。
外用薬の塗布を開始する前において、患者の血清中IgE濃度は5500、患者のthymus and activation−regulated chemokine(TARC)は5300であった。外用薬の塗布開始3ヶ月後には、患者の血清中IgE濃が2700〜2800、TARCが170と低値となり、アレルギー反応の顕著な改善が認められた。なお、血清中IgE濃度、TRACは共にアレルギー疾患の重症度の指標となるものである。
Claims (3)
- グルコースを含有する細胞遊走促進剤。
- 請求項1に記載の細胞遊走促進剤を含有し、前記グルコースの含有量が1〜5mol/Lである創傷治療用の経皮吸収剤。
- ステロイド剤を含有し、前記グルコース/前記ステロイド剤で表されるモル比が10〜105である請求項2に記載の創傷治療用の経皮吸収剤。
Priority Applications (6)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2012011342A JP5456802B2 (ja) | 2012-01-23 | 2012-01-23 | 細胞遊走促進剤及び創傷治療用の経皮吸収剤 |
| KR1020147020143A KR101514257B1 (ko) | 2012-01-23 | 2013-01-22 | 의약 조성물 및 이를 이용한 약용 화장품 |
| PCT/JP2013/051159 WO2013111729A1 (ja) | 2012-01-23 | 2013-01-22 | 医薬組成物及びこれを用いた薬用化粧品 |
| EP13740840.7A EP2808025B1 (en) | 2012-01-23 | 2013-01-22 | Pharmaceutical composition and quasi-drug cosmetic using same |
| TW102102452A TWI468184B (zh) | 2012-01-23 | 2013-01-23 | 藥學組成物及使用其之藥用化妝品 |
| HK15105077.8A HK1204556A1 (zh) | 2012-01-23 | 2015-05-28 | 藥物組合物及使用該藥物組合物的準藥物化妝品 |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2012011342A JP5456802B2 (ja) | 2012-01-23 | 2012-01-23 | 細胞遊走促進剤及び創傷治療用の経皮吸収剤 |
Publications (3)
| Publication Number | Publication Date |
|---|---|
| JP2013147480A JP2013147480A (ja) | 2013-08-01 |
| JP2013147480A5 JP2013147480A5 (ja) | 2013-09-26 |
| JP5456802B2 true JP5456802B2 (ja) | 2014-04-02 |
Family
ID=48873449
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2012011342A Active JP5456802B2 (ja) | 2012-01-23 | 2012-01-23 | 細胞遊走促進剤及び創傷治療用の経皮吸収剤 |
Country Status (6)
| Country | Link |
|---|---|
| EP (1) | EP2808025B1 (ja) |
| JP (1) | JP5456802B2 (ja) |
| KR (1) | KR101514257B1 (ja) |
| HK (1) | HK1204556A1 (ja) |
| TW (1) | TWI468184B (ja) |
| WO (1) | WO2013111729A1 (ja) |
Families Citing this family (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP6313118B2 (ja) * | 2014-05-16 | 2018-04-18 | 株式会社Cac | IgE抑制剤 |
| JP6584494B2 (ja) * | 2014-09-12 | 2019-10-02 | ザ プロクター アンド ギャンブル カンパニーThe Procter & Gamble Company | メラニン産生細胞のhmgb1活性化を阻害する方法、そのような阻害に好適な薬剤を特定する方法 |
| JP2018172328A (ja) | 2017-03-31 | 2018-11-08 | 株式会社Cac | 皮膚バリア増強剤、医薬組成物、薬用化粧品、及び美容方法 |
Family Cites Families (15)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPS62138432A (ja) * | 1985-12-12 | 1987-06-22 | Shionogi & Co Ltd | 抗炎症ステロイドを含有する安定な錠剤 |
| US5145679A (en) * | 1989-10-05 | 1992-09-08 | Hinson Joan B | Topical emollient for prevention and treatment of circulatory induced lesions |
| CN1116095A (zh) * | 1994-08-03 | 1996-02-07 | 鞍山钢铁公司 | 一种用于治疗烧伤的胶浆剂 |
| JP2920611B2 (ja) * | 1995-12-11 | 1999-07-19 | 株式会社シーエーシー | 皮膚炎の治療外用剤 |
| JP2005281315A (ja) * | 1997-07-02 | 2005-10-13 | Aventis Pharmaceuticals Holdings Inc | 水性薬理組成物 |
| SE9704833D0 (sv) * | 1997-12-22 | 1997-12-22 | Astra Ab | New formulation |
| ATE446096T1 (de) * | 2002-06-03 | 2009-11-15 | Cac Corp | Topische präparate zur behandlung von dermatitis |
| EP1596822A2 (en) * | 2003-02-17 | 2005-11-23 | Sun Pharmaceuticals Industries Ltd. | A low dose corticosteroid composition |
| CN1255184C (zh) * | 2004-03-22 | 2006-05-10 | 中国人民解放军第四军医大学 | 葡萄糖-胰岛素-钾极化液在制备外敷治疗创伤、烧伤的药物中的应用 |
| JP4854194B2 (ja) * | 2004-07-05 | 2012-01-18 | 株式会社ファンケル | ラメラ構造再生剤及び皮膚外用剤 |
| CN101043875B (zh) * | 2004-09-09 | 2014-05-07 | 耶路撒冷希伯来大学伊萨姆研发公司 | 糖皮质激素和糖皮质激素衍生物的脂质体组合物 |
| JP2007182384A (ja) | 2004-09-22 | 2007-07-19 | New Industry Research Organization | 抗炎症治療薬 |
| CA2607912A1 (en) * | 2005-05-13 | 2006-11-16 | Netech Inc. | Medical composition for promotion of skin regeneration |
| JP2008273919A (ja) | 2007-05-07 | 2008-11-13 | Lilac:Kk | 組織・細胞障害のための予防・修復剤 |
| PL3354276T3 (pl) * | 2007-11-13 | 2020-09-21 | Meritage Pharma, Inc. | Kompozycje do leczenia zapalenia przewodu pokarmowego |
-
2012
- 2012-01-23 JP JP2012011342A patent/JP5456802B2/ja active Active
-
2013
- 2013-01-22 WO PCT/JP2013/051159 patent/WO2013111729A1/ja active Application Filing
- 2013-01-22 EP EP13740840.7A patent/EP2808025B1/en not_active Not-in-force
- 2013-01-22 KR KR1020147020143A patent/KR101514257B1/ko active IP Right Grant
- 2013-01-23 TW TW102102452A patent/TWI468184B/zh active
-
2015
- 2015-05-28 HK HK15105077.8A patent/HK1204556A1/zh unknown
Also Published As
| Publication number | Publication date |
|---|---|
| TWI468184B (zh) | 2015-01-11 |
| EP2808025B1 (en) | 2016-07-13 |
| EP2808025A4 (en) | 2014-12-17 |
| KR101514257B1 (ko) | 2015-04-24 |
| EP2808025A1 (en) | 2014-12-03 |
| HK1204556A1 (zh) | 2015-11-27 |
| KR20140097584A (ko) | 2014-08-06 |
| TW201332580A (zh) | 2013-08-16 |
| JP2013147480A (ja) | 2013-08-01 |
| WO2013111729A1 (ja) | 2013-08-01 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| TWI784261B (zh) | 神經活性類固醇,其組合物及其用途 | |
| US20110288134A1 (en) | Composition and method for treating fibrosis | |
| JP2014528474A5 (ja) | ||
| KR20190073365A (ko) | 사이토카인 과분비 및 바이러스성 감염의 치료를 위한 비만 세포 안정화제 | |
| AU2014249534A1 (en) | Use of levocetirizine and montelukast in the treatment of vasculitis | |
| AU2011334617A1 (en) | Folic acid - Ramipril combination: cellprotective, neuroprotective and retinoprotective ophtalmologic compositions | |
| JP5456802B2 (ja) | 細胞遊走促進剤及び創傷治療用の経皮吸収剤 | |
| WO2021025988A1 (en) | Dosing protocols and regimens for aminosterol treatment | |
| WO2020244507A1 (zh) | 一种烟酰胺单核苷酸和/或烟酰胺单核苷酸盐的应用 | |
| DE102017215154A1 (de) | Zusammensetzung zur topischen Behandlung von nicht-Mikroorganismus-verursachten entzündlichen Haut- und Schleimhauterkrankungen | |
| CN104367547B (zh) | 一种适用于口腔给药的缓控释替硝唑软膏 | |
| EP3964215A1 (en) | Pharmaceutical composition, comprising 6-diazo-5-oxo-l-norleucine, for treatment of inflammatory skin disease | |
| AU2018371606B2 (en) | Composition for treating atopy or pruritus comprising N-acetyl or N-acyl amino acid | |
| WO2020244508A1 (zh) | Nadh和/或nadph抗过敏药物和/或抗过敏保健食品中的应用 | |
| CN106924271A (zh) | 人参皂苷c-k用于制备治疗银屑病药物 | |
| JP7396585B2 (ja) | Tslp遺伝子発現抑制用、il-33遺伝子発現抑制用、又はフィラグリン産生促進用組成物 | |
| JP6294773B2 (ja) | 口腔粘膜疾患の予防または治療用経口製剤 | |
| WO1998051313A1 (fr) | Remedes contre les yeux secs | |
| US11819508B2 (en) | Miltefosine for the treatment of viral infections including covid-19 | |
| WO2019135363A1 (ja) | 腱滑膜病変を主体とした疾患の治療薬 | |
| AU2022346513A1 (en) | Gel composition for prevention or treatment of atopic dermatitis | |
| JP2023525662A (ja) | トレハロース又はトレハロースの誘導体を含有する医薬及び経鼻スプレー | |
| WO2006121209A1 (ja) | 湿疹・皮膚炎群治療剤 | |
| CN111511359A (zh) | 非甾体选择性糖皮质激素受体激动调节剂(segram)及其用途 | |
| CN116139140A (zh) | 一种化合物在治疗糖皮质激素不良反应中的用途 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20130704 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20130704 |
|
| A871 | Explanation of circumstances concerning accelerated examination |
Free format text: JAPANESE INTERMEDIATE CODE: A871 Effective date: 20130704 |
|
| A975 | Report on accelerated examination |
Free format text: JAPANESE INTERMEDIATE CODE: A971005 Effective date: 20130731 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20130813 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20131015 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20131210 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20140108 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 5456802 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |