JP5259056B2 - ビウレット化合物、その製造及び使用、ならびにその製造のための中間体 - Google Patents
ビウレット化合物、その製造及び使用、ならびにその製造のための中間体 Download PDFInfo
- Publication number
- JP5259056B2 JP5259056B2 JP2006105620A JP2006105620A JP5259056B2 JP 5259056 B2 JP5259056 B2 JP 5259056B2 JP 2006105620 A JP2006105620 A JP 2006105620A JP 2006105620 A JP2006105620 A JP 2006105620A JP 5259056 B2 JP5259056 B2 JP 5259056B2
- Authority
- JP
- Japan
- Prior art keywords
- alkyl
- uretdione
- general formula
- alkylene
- aralkylene
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Expired - Lifetime
Links
Classifications
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08G—MACROMOLECULAR COMPOUNDS OBTAINED OTHERWISE THAN BY REACTIONS ONLY INVOLVING UNSATURATED CARBON-TO-CARBON BONDS
- C08G18/00—Polymeric products of isocyanates or isothiocyanates
- C08G18/06—Polymeric products of isocyanates or isothiocyanates with compounds having active hydrogen
- C08G18/70—Polymeric products of isocyanates or isothiocyanates with compounds having active hydrogen characterised by the isocyanates or isothiocyanates used
- C08G18/72—Polyisocyanates or polyisothiocyanates
- C08G18/77—Polyisocyanates or polyisothiocyanates having heteroatoms in addition to the isocyanate or isothiocyanate nitrogen and oxygen or sulfur
- C08G18/78—Nitrogen
- C08G18/79—Nitrogen characterised by the polyisocyanates used, these having groups formed by oligomerisation of isocyanates or isothiocyanates
- C08G18/798—Nitrogen characterised by the polyisocyanates used, these having groups formed by oligomerisation of isocyanates or isothiocyanates containing urethdione groups
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08G—MACROMOLECULAR COMPOUNDS OBTAINED OTHERWISE THAN BY REACTIONS ONLY INVOLVING UNSATURATED CARBON-TO-CARBON BONDS
- C08G18/00—Polymeric products of isocyanates or isothiocyanates
- C08G18/06—Polymeric products of isocyanates or isothiocyanates with compounds having active hydrogen
- C08G18/28—Polymeric products of isocyanates or isothiocyanates with compounds having active hydrogen characterised by the compounds used containing active hydrogen
- C08G18/40—High-molecular-weight compounds
- C08G18/48—Polyethers
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C275/00—Derivatives of urea, i.e. compounds containing any of the groups, the nitrogen atoms not being part of nitro or nitroso groups
- C07C275/46—Derivatives of urea, i.e. compounds containing any of the groups, the nitrogen atoms not being part of nitro or nitroso groups containing any of the groups, X being a hetero atom, Y being any atom, e.g. acylureas
- C07C275/58—Y being a hetero atom
- C07C275/62—Y being a nitrogen atom, e.g. biuret
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D229/00—Heterocyclic compounds containing rings of less than five members having two nitrogen atoms as the only ring hetero atoms
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08G—MACROMOLECULAR COMPOUNDS OBTAINED OTHERWISE THAN BY REACTIONS ONLY INVOLVING UNSATURATED CARBON-TO-CARBON BONDS
- C08G18/00—Polymeric products of isocyanates or isothiocyanates
- C08G18/06—Polymeric products of isocyanates or isothiocyanates with compounds having active hydrogen
- C08G18/08—Processes
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08G—MACROMOLECULAR COMPOUNDS OBTAINED OTHERWISE THAN BY REACTIONS ONLY INVOLVING UNSATURATED CARBON-TO-CARBON BONDS
- C08G18/00—Polymeric products of isocyanates or isothiocyanates
- C08G18/06—Polymeric products of isocyanates or isothiocyanates with compounds having active hydrogen
- C08G18/28—Polymeric products of isocyanates or isothiocyanates with compounds having active hydrogen characterised by the compounds used containing active hydrogen
- C08G18/2805—Compounds having only one group containing active hydrogen
- C08G18/2815—Monohydroxy compounds
- C08G18/282—Alkanols, cycloalkanols or arylalkanols including terpenealcohols
- C08G18/2825—Alkanols, cycloalkanols or arylalkanols including terpenealcohols having at least 6 carbon atoms
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08G—MACROMOLECULAR COMPOUNDS OBTAINED OTHERWISE THAN BY REACTIONS ONLY INVOLVING UNSATURATED CARBON-TO-CARBON BONDS
- C08G18/00—Polymeric products of isocyanates or isothiocyanates
- C08G18/06—Polymeric products of isocyanates or isothiocyanates with compounds having active hydrogen
- C08G18/28—Polymeric products of isocyanates or isothiocyanates with compounds having active hydrogen characterised by the compounds used containing active hydrogen
- C08G18/2805—Compounds having only one group containing active hydrogen
- C08G18/2815—Monohydroxy compounds
- C08G18/283—Compounds containing ether groups, e.g. oxyalkylated monohydroxy compounds
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08G—MACROMOLECULAR COMPOUNDS OBTAINED OTHERWISE THAN BY REACTIONS ONLY INVOLVING UNSATURATED CARBON-TO-CARBON BONDS
- C08G18/00—Polymeric products of isocyanates or isothiocyanates
- C08G18/06—Polymeric products of isocyanates or isothiocyanates with compounds having active hydrogen
- C08G18/28—Polymeric products of isocyanates or isothiocyanates with compounds having active hydrogen characterised by the compounds used containing active hydrogen
- C08G18/2805—Compounds having only one group containing active hydrogen
- C08G18/285—Nitrogen containing compounds
- C08G18/2865—Compounds having only one primary or secondary amino group; Ammonia
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08G—MACROMOLECULAR COMPOUNDS OBTAINED OTHERWISE THAN BY REACTIONS ONLY INVOLVING UNSATURATED CARBON-TO-CARBON BONDS
- C08G18/00—Polymeric products of isocyanates or isothiocyanates
- C08G18/06—Polymeric products of isocyanates or isothiocyanates with compounds having active hydrogen
- C08G18/28—Polymeric products of isocyanates or isothiocyanates with compounds having active hydrogen characterised by the compounds used containing active hydrogen
- C08G18/30—Low-molecular-weight compounds
- C08G18/32—Polyhydroxy compounds; Polyamines; Hydroxyamines
- C08G18/3225—Polyamines
- C08G18/3228—Polyamines acyclic
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08G—MACROMOLECULAR COMPOUNDS OBTAINED OTHERWISE THAN BY REACTIONS ONLY INVOLVING UNSATURATED CARBON-TO-CARBON BONDS
- C08G18/00—Polymeric products of isocyanates or isothiocyanates
- C08G18/06—Polymeric products of isocyanates or isothiocyanates with compounds having active hydrogen
- C08G18/28—Polymeric products of isocyanates or isothiocyanates with compounds having active hydrogen characterised by the compounds used containing active hydrogen
- C08G18/30—Low-molecular-weight compounds
- C08G18/32—Polyhydroxy compounds; Polyamines; Hydroxyamines
- C08G18/3225—Polyamines
- C08G18/3237—Polyamines aromatic
- C08G18/324—Polyamines aromatic containing only one aromatic ring
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08G—MACROMOLECULAR COMPOUNDS OBTAINED OTHERWISE THAN BY REACTIONS ONLY INVOLVING UNSATURATED CARBON-TO-CARBON BONDS
- C08G18/00—Polymeric products of isocyanates or isothiocyanates
- C08G18/06—Polymeric products of isocyanates or isothiocyanates with compounds having active hydrogen
- C08G18/28—Polymeric products of isocyanates or isothiocyanates with compounds having active hydrogen characterised by the compounds used containing active hydrogen
- C08G18/40—High-molecular-weight compounds
- C08G18/48—Polyethers
- C08G18/50—Polyethers having heteroatoms other than oxygen
- C08G18/5021—Polyethers having heteroatoms other than oxygen having nitrogen
- C08G18/5024—Polyethers having heteroatoms other than oxygen having nitrogen containing primary and/or secondary amino groups
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08G—MACROMOLECULAR COMPOUNDS OBTAINED OTHERWISE THAN BY REACTIONS ONLY INVOLVING UNSATURATED CARBON-TO-CARBON BONDS
- C08G18/00—Polymeric products of isocyanates or isothiocyanates
- C08G18/06—Polymeric products of isocyanates or isothiocyanates with compounds having active hydrogen
- C08G18/70—Polymeric products of isocyanates or isothiocyanates with compounds having active hydrogen characterised by the isocyanates or isothiocyanates used
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09D—COATING COMPOSITIONS, e.g. PAINTS, VARNISHES OR LACQUERS; FILLING PASTES; CHEMICAL PAINT OR INK REMOVERS; INKS; CORRECTING FLUIDS; WOODSTAINS; PASTES OR SOLIDS FOR COLOURING OR PRINTING; USE OF MATERIALS THEREFOR
- C09D5/00—Coating compositions, e.g. paints, varnishes or lacquers, characterised by their physical nature or the effects produced; Filling pastes
- C09D5/04—Thixotropic paints
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09D—COATING COMPOSITIONS, e.g. PAINTS, VARNISHES OR LACQUERS; FILLING PASTES; CHEMICAL PAINT OR INK REMOVERS; INKS; CORRECTING FLUIDS; WOODSTAINS; PASTES OR SOLIDS FOR COLOURING OR PRINTING; USE OF MATERIALS THEREFOR
- C09D7/00—Features of coating compositions, not provided for in group C09D5/00; Processes for incorporating ingredients in coating compositions
- C09D7/40—Additives
- C09D7/43—Thickening agents
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08K—Use of inorganic or non-macromolecular organic substances as compounding ingredients
- C08K5/00—Use of organic ingredients
- C08K5/16—Nitrogen-containing compounds
- C08K5/21—Urea; Derivatives thereof, e.g. biuret
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Health & Medical Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Medicinal Chemistry (AREA)
- Polymers & Plastics (AREA)
- Life Sciences & Earth Sciences (AREA)
- Engineering & Computer Science (AREA)
- Materials Engineering (AREA)
- Wood Science & Technology (AREA)
- Organic Low-Molecular-Weight Compounds And Preparation Thereof (AREA)
- Polyurethanes Or Polyureas (AREA)
- Paints Or Removers (AREA)
Description
本発明のビウレット化合物は、溶媒系(solvent−borne)、無溶媒系及び水系の塗料、PVCプラスチゾル、エポシキ系コーティング及び不飽和ポリエステル樹脂系のコーティングのようなコーティングシステムのためのチキソトロピー剤としての使用に適している。
ここで、R3、R4及びR5はC2〜C18アルキレン、シクロアルキレン、アリーレン又はアラルキレンであり、それぞれ同一でも異なっていても良く、Zは−COO−、NHCO−、NHCOO−、NHCONH−及び/又はこれらの混合物であり、aは1〜20である。
これらのウレトジオンは本発明のビウレット化合物を製造するための中間体として新規で有用なものである。これらの中間体の製造は既に詳細に上述した。
実施例 1
攪拌機、還流コンデンサ及び温度計を付けた1リッターの三口フラスコに、室温でヘキサメチレンジイシシアネートウレトジオン(Beyer社のDesmodur N3400)の79.6g(0.2モル)、メトキシポリエチレングリコール750の300g(0.4モル)の順に入れた後、80℃に加熱する。イソシアネートが検知できなくなるまで反応させる。次いで、反応混合物を50℃まで冷却する。
実施例 2
攪拌機、水分離器及び温度計を付けた1リッターの三口フラスコに、ダイマー酸の168g(0.3モル)、ヘキサメチレンジアミンの46.4g(0.4モル)、Shellsol A (Shell社の高芳香族炭化水素溶媒)の92gの順に入れた後に、ゆっくりと160℃に加熱する。反応の間に除々に遊離してくる水を共沸させて水分離器で分離する。酸価が3未満になると反応が終る。続いて、反応混合物を50℃に冷却する。
実施例 3
攪拌機、還流コンデンサ及び温度計を付けた1リッターの三口フラスコに、実施例1の反応生成物の103.6g(0.1モル)、実施例2の反応生成物の153.1g(0.05モル)の順に入れた後に、80℃に加熱する。反応混合物をアミン数が3未満になるまで、さらに3時間攪拌する。次いで、生成物をイソブタノールで希釈して固形分50%とする。
本発明の生成物のゲル生成能力を二成分エポキシシステムでテストした。加えて、バインダ中で到達できるフィルムの厚みを確認した。用いた二成分系(2K)バインダシステムは次の通りであった。
1.Epikote 1001/Epikote 834、 ビスフェノールA系ポリエポキシド、Ancamide 700−X−75、高分子量ジアミン
2.Epikote 828、ビスフェノールA系ポリエポキシド、Ancamide 700−X−75、高分子量ジアミン
Epikote 1001 (キシレン中75%) 34.5g
Epikote 834 (キシレン中80%) 7.6g
Byk 052(消泡剤) 0.3g
Bayferrox 130M(酸化鉄顔料) 5.0g
Micro talc At−1(CaCO3) 12.0g
燐酸亜鉛 12.0g
EWO (BaSO4) 5.6g
メチルイソブチルケトン 19.2g
イソブタノール 3.8g
Ancamide 700X75
Epikote 1001:ビスフェノールA型のポリエポキシド(Shell社製)
Epikote 834:ビスフェノールA型のポリエポキシド(Shell社製)
Bye 410:尿素ウレタンで、N−メチルピロリドンで希釈
Jeffamine M 600:アルキルポリエーテルアミン MW 600(Huntsman社製)
Jeffamine M 2070:アルキルポリエーテルアミン MW 2000(Huntsman社製)
Jeffamine ED 900:アルキルポリエーテルジアミン MW 900(Huntsman社製)
Jeffamine ED 2003:アルキルポリエーテルジアミン MW 2000(Huntsman社製)
Ancamide 700−X−75:ポリアミド/エポキシド付加物(Air Products社製)
Claims (8)
- 下記一般式で表されるビウレット化合物。
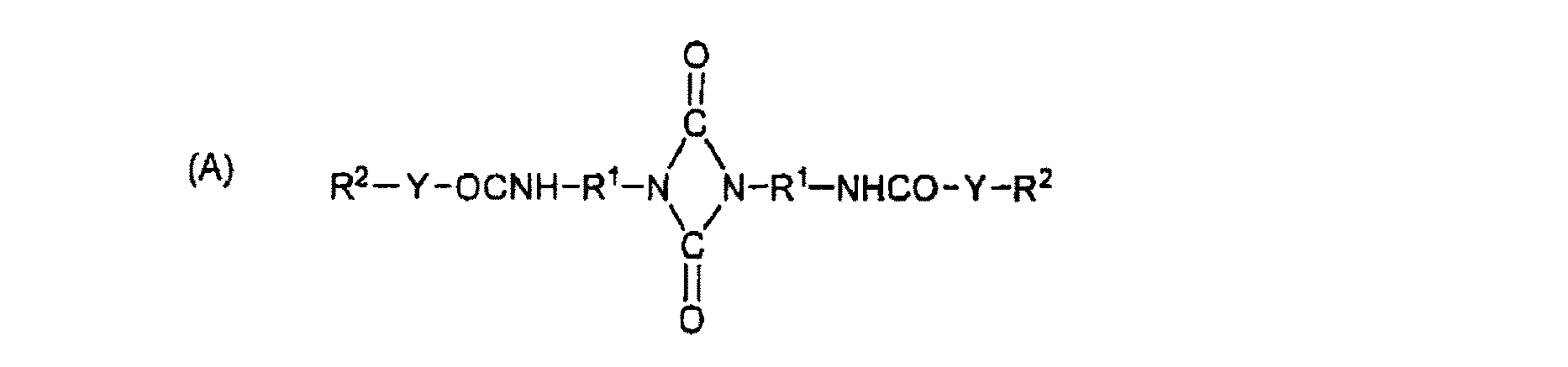
- 下記一般式(A)で表されるウレトジオンを下記一般式(B)で表されるジアミンと反応させることを特徴とする請求項1に記載のビウレット化合物を製造する方法。
(B) H2N−R3−[Z−R4−Z−R5]a−NH2
[式中、R3、R4及びR5はC2〜C18アルキレン、シクロアルキレン、アリーレン又はアラルキレンであり、それぞれ同一でも異なっていても良く、Zは−COO−、NHCO−、NHCOO−、NHCONH−及び/又はこれらの組み合わせであり、aは1〜20である。] - 前記一般式(A)及び(B)の化合物を60〜120℃の間の反応温度で反応させることを特徴とする請求項2に記載のビウレット化合物を製造する方法。
- 一般式(B)で表されるジアミンに対する一般式(A)で表されるウレトジオンのモル比が1:0.3〜1:0.7の間であることを特徴とする請求項2又は3に記載のビウレット化合物を製造する方法。
- 下記一般式で表されるビウレット化合物のレオロジー調節剤としての使用。
- 垂れ防止剤及び/又は沈降防止剤としてのチキソトロピーコーティングシステム用の請求項1に記載のビウレット化合物の使用。
- 前記ウレトジオンがヘキサメチレンジイソシアネートウレトジオンである請求項2に記載のビウレット化合物を製造する方法。
- R1がヘキサメチレン、R3及びR5がヘキサメチレンまたはm−キシリレンであり、R4がテトラメチレンである請求項1に記載のビウレット化合物。
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| DE102005015966A DE102005015966A1 (de) | 2005-04-07 | 2005-04-07 | Biuretverbindungen, ihre Herstellung und Verwendung sowie Zwischenprodukte zu ihrer Herstellung |
| DE102005015966.4 | 2005-04-07 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2006306869A JP2006306869A (ja) | 2006-11-09 |
| JP5259056B2 true JP5259056B2 (ja) | 2013-08-07 |
Family
ID=36616865
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2006105620A Expired - Lifetime JP5259056B2 (ja) | 2005-04-07 | 2006-04-06 | ビウレット化合物、その製造及び使用、ならびにその製造のための中間体 |
Country Status (10)
| Country | Link |
|---|---|
| US (1) | US7652166B2 (ja) |
| EP (1) | EP1710228B1 (ja) |
| JP (1) | JP5259056B2 (ja) |
| KR (1) | KR101275836B1 (ja) |
| CN (1) | CN1847220B (ja) |
| AT (1) | ATE512131T1 (ja) |
| CA (1) | CA2541881C (ja) |
| DE (1) | DE102005015966A1 (ja) |
| DK (1) | DK1710228T3 (ja) |
| TW (1) | TWI405783B (ja) |
Families Citing this family (19)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| DE102004022753B3 (de) | 2004-05-07 | 2006-02-16 | Byk-Chemie Gmbh | Als Dispergiermittel und Dispersionsstabilisatoren geeignete Additionsverbindungen |
| DE102006010721B4 (de) | 2006-03-08 | 2010-04-15 | Byk-Chemie Gmbh | Biuretverbindungen zur Rheologiesteuerung |
| DE102006012999A1 (de) * | 2006-03-22 | 2007-09-27 | Byk-Chemie Gmbh | Additionsverbindungen als Dispergiermittel und Dispersionsstabilisatoren |
| DE102008029858A1 (de) * | 2008-04-23 | 2009-10-29 | Byk-Chemie Gmbh | Stabile Dispersionen von anorganischen Nanopartikeln |
| DE102009017277A1 (de) * | 2009-04-11 | 2010-10-28 | Byk-Chemie Gmbh | Nagellack enthaltend polyamidhaltige Blockpolymere, Verwendung von polyamidhaltigen Blockpolymeren sowie Pigmentpräparation und ihre Verwendung |
| EP2678364B1 (de) * | 2011-02-22 | 2015-04-08 | Basf Se | Rheologiemittel für strahlungshärtbare beschichtungsmassen |
| US9255173B2 (en) | 2013-03-15 | 2016-02-09 | Lake Region Manufacturing, Inc. | Oxirane (ethylene oxide) polyurethane coatings |
| US9714361B2 (en) | 2013-03-15 | 2017-07-25 | Lake Region Manfacturing, Inc. | Oxirane (ethylene oxide) polyurethane coatings |
| KR102555666B1 (ko) * | 2015-07-27 | 2023-07-18 | 비와이케이-케미 게엠베하 | 리올로지 제어용 우레아우레탄 |
| JP6732913B2 (ja) * | 2016-07-15 | 2020-07-29 | 関西ペイント株式会社 | 塗料組成物 |
| JP6975792B2 (ja) * | 2017-01-30 | 2021-12-01 | ベーイプシロンカー ヘミー ゲゼルシャフト ミット ベシュレンクター ハフトゥング | レオロジーコントロール剤としての、及び、レオロジーコントロール剤における尿素基−及び/又はウレタン基−含有アミド、その製造及びその使用 |
| CN107226788A (zh) * | 2017-05-04 | 2017-10-03 | 明光市飞洲新材料有限公司 | 一种铸造涂料专用防流挂剂生产工艺 |
| KR20200050954A (ko) | 2017-09-07 | 2020-05-12 | 쓰리엠 이노베이티브 프로퍼티즈 캄파니 | 우레트다이온-함유 물질을 포함하는 중합체 재료, 2-파트 조성물, 및 방법 |
| EP3733797B1 (en) * | 2017-12-28 | 2022-10-12 | Kansai Paint Co., Ltd | Coating material composition |
| CN112689650A (zh) | 2018-09-20 | 2021-04-20 | 3M创新有限公司 | 包含含脲二酮的材料和环氧组分的聚合物材料、两部分组合物以及方法 |
| US10899944B2 (en) | 2018-10-29 | 2021-01-26 | Lake Region Manufacturing, Inc. | Polyurethane urea-containing adipic acid dihydrazide where active hydrogens react with the epoxy group found on glycidol to form a diol |
| WO2020166197A1 (ja) * | 2019-02-15 | 2020-08-20 | 関西ペイント株式会社 | 粘性調整剤及び塗料組成物 |
| CN111217972B (zh) * | 2020-01-13 | 2022-02-15 | 万华化学集团股份有限公司 | 一种储存稳定的缩二脲多异氰酸酯的制备方法 |
| WO2026027417A1 (en) | 2024-07-30 | 2026-02-05 | Byk-Chemie Gmbh | Rheology control agent |
Family Cites Families (14)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| DE2822908C2 (de) | 1978-05-26 | 1980-03-20 | Byk-Mallinckrodt Chemische Produkte Gmbh, 4230 Wesel | Thixotropiemittel für Überzugsmittel |
| DE3502683A1 (de) * | 1985-01-26 | 1986-08-07 | Hüls AG, 4370 Marl | Polyurethane mit urethan- und biuretstruktur |
| NL8500475A (nl) * | 1985-02-20 | 1986-09-16 | Akzo Nv | Thixotrope bekledingssamenstelling. |
| NL8500476A (nl) * | 1985-02-20 | 1986-09-16 | Akzo Nv | Thixotrope bekledingssamenstelling. |
| GB2190388A (en) | 1986-03-27 | 1987-11-18 | Coates Brothers Plc | Polyamides and thixotropic compositions containing them |
| DE3724555A1 (de) | 1987-07-24 | 1989-02-02 | Basf Ag | Viskositaetsregulierende stoffe fuer einkomponentige polyurethansysteme |
| US5164433A (en) | 1991-04-17 | 1992-11-17 | Rheox, Inc. | Rheological agents and thickeners |
| NZ243136A (en) | 1991-08-16 | 1995-06-27 | Rheox Int | Rheological additive comprising the reaction product of a polycarboxylic acid, two different active hydrogen containing compounds and a monocarboxylic capping agent |
| US5510452A (en) | 1994-07-11 | 1996-04-23 | Rheox, Inc. | Pourable liquid polyesteramide rheological additives and the use thererof |
| DE19606030A1 (de) | 1996-02-19 | 1997-08-21 | Huels Chemische Werke Ag | Isocyanurat-und uretdiongruppenhaltige Polyadditionsprodukte sowie ein Verfahren zu ihrer Herstellung |
| US5939475A (en) | 1996-09-03 | 1999-08-17 | Rheox, Inc. | Organic fluid systems containing clay/polyamide compositions |
| DE19919482C2 (de) * | 1999-04-29 | 2001-04-26 | Byk Chemie Gmbh | Verfahren zur Herstellung eines Thixotropie-Mittels und dessen Verwendung |
| DE10241853B3 (de) * | 2002-09-09 | 2004-01-22 | Byk-Chemie Gmbh | Polymeres Harnstoffurethan als Rheologiesteuerungsmittel und Verfahren zur Herstellung |
| DE102004022753B3 (de) | 2004-05-07 | 2006-02-16 | Byk-Chemie Gmbh | Als Dispergiermittel und Dispersionsstabilisatoren geeignete Additionsverbindungen |
-
2005
- 2005-04-07 DE DE102005015966A patent/DE102005015966A1/de not_active Ceased
-
2006
- 2006-03-28 TW TW095110728A patent/TWI405783B/zh active
- 2006-04-03 AT AT06007037T patent/ATE512131T1/de active
- 2006-04-03 EP EP06007037A patent/EP1710228B1/de not_active Expired - Lifetime
- 2006-04-03 DK DK06007037.2T patent/DK1710228T3/da active
- 2006-04-03 CA CA2541881A patent/CA2541881C/en not_active Expired - Lifetime
- 2006-04-06 JP JP2006105620A patent/JP5259056B2/ja not_active Expired - Lifetime
- 2006-04-07 US US11/400,721 patent/US7652166B2/en active Active
- 2006-04-07 CN CN2006100725694A patent/CN1847220B/zh active Active
- 2006-04-07 KR KR1020060032071A patent/KR101275836B1/ko active Active
Also Published As
| Publication number | Publication date |
|---|---|
| EP1710228B1 (de) | 2011-06-08 |
| DK1710228T3 (da) | 2011-09-19 |
| EP1710228A3 (de) | 2007-12-12 |
| TW200640973A (en) | 2006-12-01 |
| JP2006306869A (ja) | 2006-11-09 |
| TWI405783B (zh) | 2013-08-21 |
| ATE512131T1 (de) | 2011-06-15 |
| US7652166B2 (en) | 2010-01-26 |
| KR20060107417A (ko) | 2006-10-13 |
| CA2541881A1 (en) | 2006-10-07 |
| US20060276675A1 (en) | 2006-12-07 |
| DE102005015966A1 (de) | 2006-10-19 |
| CA2541881C (en) | 2013-07-09 |
| EP1710228A2 (de) | 2006-10-11 |
| CN1847220B (zh) | 2012-01-11 |
| CN1847220A (zh) | 2006-10-18 |
| KR101275836B1 (ko) | 2013-06-18 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP5259056B2 (ja) | ビウレット化合物、その製造及び使用、ならびにその製造のための中間体 | |
| KR101423747B1 (ko) | 유동학적 조절을 위한 비우렛 화합물 | |
| JP5981844B2 (ja) | レオロジー調節剤としてのポリ尿素 | |
| JP4498539B2 (ja) | チキソトロープ剤の製造方法及びその用途 | |
| EP2861684B1 (en) | Curable polyurea forming composition, method of making, and composite article | |
| CN100457837C (zh) | 碳取代甲基胺衍生物及其作为流变控制剂的用途 | |
| DE102005047562A1 (de) | Zweitkomponenten-Systeme für die Herstellung flexibler Beschichtungen | |
| US20100029847A1 (en) | Composition for producing polyurea coatings | |
| JP7440500B2 (ja) | アスパラギン酸エステル官能性ポリシロキサン、それらの調製およびそれらの使用 | |
| WO2000037520A1 (en) | Thixotropic amino formaldehyde resin | |
| WO2012010528A1 (de) | Bindemittelkombinationen für konstruktive trinkwasserrohrbeschichtungen | |
| DE102006002153A1 (de) | Polyasparaginsäureester-haltige Bindemittel | |
| CN111491969B (zh) | 含脲基的抗流挂流变控制剂 | |
| EP4479455B1 (en) | Aspartic acid ester-functional polysiloxanes, their preparation and use thereof | |
| JP5490975B2 (ja) | レオロジー特性を調節するためのアミド含有ポリマー | |
| US20070004894A1 (en) | Silicon-free polyisocyanate or polyurethanes having monoamide-containing hydrophilic groups |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20090225 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20120228 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20120523 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20121016 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20130109 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20130402 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20130424 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20160502 Year of fee payment: 3 |
|
| R150 | Certificate of patent or registration of utility model |
Free format text: JAPANESE INTERMEDIATE CODE: R150 Ref document number: 5259056 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |