本発明の化学品の製造方法は、微生物もしくは培養細胞の発酵培養液を分離膜で濾過し、濾液から生産物を回収すると共に未濾過液を発酵培養液に保持または還流し、かつ、発酵原料を発酵培養液に追加する連続発酵であって、前記の濾過が間欠的に行われ、かつ、分離膜として平均細孔径が0.01μm以上1μm未満の細孔を有する多孔性膜を用い、その膜間差圧を0.1から20kPaの範囲にして濾過処理することを特徴とするものである。
本発明において分離膜として用いられる多孔性膜は、発酵に使用される微生物や培養細胞による目詰まりが起こりにくく、そして、濾過性能が長期間安定に継続する性能を有するものである。そのため、本発明で使用される多孔性膜は、平均細孔径が、0.01μm以上1μm未満であることが重要である。
本発明において分離膜として用いられる多孔性膜について説明する。まず、多孔性膜の構成について説明する。本発明で用いられる多孔性膜は、好ましくは、被処理水の水質や用途に応じた分離性能と透水性能を有するものである。多孔性膜は、阻止性能および透水性能や分離性能、例えば、耐汚れ性の点から、多孔質樹脂層を含む多孔性膜であることが好ましい。多孔質樹脂層を含む多孔性膜は、好ましくは、多孔質基材の表面に、分離機能層として作用とする多孔質樹脂層を有している。多孔質基材は、多孔質樹脂層を支持して分離膜に強度を与える。
本発明で用いられる多孔性膜が、多孔質基材の表面に多孔質樹脂層を有している場合、多孔質基材に多孔質樹脂層が浸透していても、多孔質基材に多孔質樹脂層が浸透していなくてもどちらでも良く、用途に応じて選択される。
多孔質基材の平均厚みは、好ましくは50μm以上3000μm以下である。多孔質基材の材質は、有機材料および/または無機材料等からなり、有機繊維が望ましく用いられる。好ましい多孔質基材は、セルロース繊維、セルローストリアセテート繊維、ポリエステル繊維、ポリプロピレン繊維およびポリエチレン繊維などの有機繊維なる織布や不織布であり、より好ましくは、密度の制御が比較的容易であり製造も容易で安価な不織布が用いられる。
また、多孔質樹脂層は、上述したように分離機能層として作用するものであり、有機高分子膜を好適に使用することができる。有機高分子膜の材質としては、例えば、ポリエチレン系樹脂、ポリプロピレン系樹脂、ポリ塩化ビニル系樹脂、ポリフッ化ビニリデン系樹脂、ポリスルホン系樹脂、ポリエーテルスルホン系樹脂、ポリアクリロニトリル系樹脂、セルロース系樹脂およびセルローストリアセテート系樹脂などが挙げられる。有機高分子膜は、これらの樹脂を主成分とする樹脂の混合物であってもよい。ここで主成分とは、その成分が50重量%以上、好ましくは60重量%以上含有することをいう。
有機高分子膜の材質は、溶液による製膜が容易で物理的耐久性や耐薬品性にも優れているポリ塩化ビニル系樹脂、ポリフッ化ビニリデン系樹脂、ポリスルホン系樹脂、ポリエーテルスルホン系樹脂、ポリアクリロニトリル系樹脂またはポリオレフィン系樹脂が好ましく、ポリフッ化ビニリデン系樹脂またはポリオレフィン系樹脂が好ましく、ポリフッ化ビニリデン系樹脂またはポリオレフィン系樹脂がより好ましく、ポリフッ化ビニリデン系樹脂またはそれを主成分とする樹脂、およびポリオレフィン系樹脂であればポリエチレン系樹脂が最も好ましく用いられる。これら本発明に用いることができる有機高分子膜の材質として選択される樹脂は必要に応じて分子修飾(例えば塩素化等)された樹脂も含まれる。
ここで、ポリフッ化ビニリデン系樹脂としては、フッ化ビニリデンの単独重合体が好ましく用いられる。さらに、ポリフッ化ビニリデン系樹脂は、フッ化ビニリデンと共重合可能なビニル系単量体との共重合体も好ましく用いられる。フッ化ビニリデンと共重合可能なビニル系単量体としては、テトラフルオロエチレン、ヘキサフルオロプロピレンおよび三塩化フッ化エチレンなどが例示される。
本発明で分離膜として使用される多孔性膜は、その平均細孔径が、0.01μm以上1μm未満であることが重要である。多孔性膜の平均細孔径が、0.01μm以上1μm未満であると、発酵に使用される微生物もしくは培養細胞による目詰まりが起こりにくく、かつ、濾過性能が長期間安定に継続する性能を有する。また、多孔性膜の平均細孔径が、0.01μm以上1μm未満であると、微生物もしくは培養細胞がリークすることのない高い排除率と、高い透水性を両立させることができ、透水性を長時間保持することが、より高い精度と再現性を持って実施することができる。
多孔性膜の平均細孔径が、微生物もしくは培養細胞の大きさに近いと、これらが直接孔を塞いでしまう場合があるので、多孔性膜の平均細孔径は1μm未満である。多孔性膜の平均細孔径は、微生物もしくは培養細胞の漏出、すなわち排除率が低下する不具合の発生を防止するため、微生物もしくは培養細胞の大きさと比較して大きすぎないことが好ましい。微生物もしくは培養細胞のうち、細胞の小さい細菌などを用いる場合には、平均細孔径として0.4μm以下が好ましく、0.2μm未満であればより好適に実施することができる。
また、微生物もしくは培養細胞が所望の生産物である化学品以外の物質、例えば、タンパク質や多糖類など凝集しやすい物質を生産する場合があり、更に、発酵培養液中の微生物もしくは培養細胞の一部が死滅することにより細胞の破砕物が生成する場合があり、これらの物質による多孔性膜の閉塞を回避するために、平均細孔径は0.1μm以下であることが好適である。
多孔性膜の平均細孔径は、0.4μm以下であることが好ましく、より好ましくは0.2μm未満あるいは0.1μm以下である。
一方、平均細孔径が小さすぎると多孔性膜の透水性能が低下し、膜が汚れていなくても効率的な運転ができなくなるため、本発明における多孔性膜の平均細孔径は、0.01μm以上である。多孔性膜の平均細孔径は、好ましくは0.02μm以上であり、より好ましくは0.04μm以上である。
ここで、平均細孔径は、倍率10,000倍の走査型電子顕微鏡観察における、9.2μm×10.4μmの範囲内で観察できる細孔すべての直径を測定し、平均することにより求めることができる。
本発明で用いられる多孔性膜の平均細孔径の標準偏差σは、0.1μm以下であることが好ましい。平均細孔径の標準偏差σは小さければ小さい方が望ましい。平均細孔径の標準偏差σは、上述の9.2μm×10.4μmの範囲内で観察できる細孔数をNとして、測定した各々の直径をXkとし、細孔直径の平均をX(ave)とした下記の(式1)により算出される。
本発明で用いられる多孔性膜においては、発酵培養液の透過性が重要な性能の一つである。多孔性膜の透過性の指標として、使用前の多孔性膜の純水透過係数を用いることができる。本発明において、多孔性膜の純水透過係数は、逆浸透膜による25℃の温度の精製水を用い、ヘッド高さ1mで透水量を測定し算出したとき、2×10−9m3/m2/s/pa以上であることが好ましく、純水透過係数が、2×10−9m3/m2/s/pa以上6×10−7m3/m2/s/pa以下であれば、実用的に十分な透過水量が得られる。
本発明で用いられる多孔性膜において、表面粗さとは、表面に対して垂直方向の高さの平均値である。膜表面粗さは、分離膜表面に付着した微生物もしくは培養細胞が、撹拌や循環ポンプによる液流による膜面洗浄効果で剥離しやすくするための因子の一つである。多孔性膜の表面粗さは、0.1μm以下であることが好ましい。表面粗さが0.1μm以下であると、膜に付着した微生物もしくは培養細胞、ならびにその他の固形物が剥がれやすくなる。
さらに好ましくは、多孔性膜の膜表面粗さが0.1μm以下であり、平均細孔径が0.01μm以上1μm未満であり、多孔性膜の純水透過係数が2×10−9m3/m2/s/pa以上の多孔性膜を使用することにより、膜面洗浄に必要な動力を過度に必要としない運転が、より容易に可能であることがわかった。多孔性膜の表面粗さを、0.1μm以下とすることにより、微生物もしくは培養細胞の濾過において、膜表面で発生する剪断力を低下させることができ、微生物の破壊が抑制され、多孔性膜の目詰まりも抑制されることにより、長期間安定な濾過が、より容易に可能になる。また、多孔性膜の表面粗さを、0.1μm以下とすることにより、より低い膜間差圧で連続発酵が実施可能であり、多孔性膜が目詰まりした場合でも高い膜間差圧で運転した場合に比べて、洗浄回復性が良好である。多孔性膜の目詰まりを抑えることにより、安定した連続発酵が可能になることから、多孔性膜の表面粗さは小さければ小さいほど好ましい。
ここで、多孔性膜の膜表面粗さは、下記の原子間力顕微鏡装置(AFM)を使用して、下記の条件で測定したものである。
・装置 原子間力顕微鏡装置(Digital Instruments(株)製Nanoscope IIIa)
・条件 探針 SiNカンチレバー(Digital Instruments(株)製)
走査モード コンタクトモード(気中測定)
水中タッピングモード(水中測定)
走査範囲 10μm、25μm四方(気中測定)
5μm、10μm四方(水中測定)
走査解像度 512×512
・試料調製 測定に際し膜サンプルは、常温でエタノールに15分浸漬後、RO水中に24時間浸漬し洗浄した後、風乾し用いた。RO水とは、ろ過膜の一種である逆浸透膜(RO膜)を用いてろ過し、イオンや塩類などの不純物を排除した水を指す。RO膜の孔の大きさは、概ね2nm以下である。
膜表面粗さdroughは、上記の原子間力顕微鏡装置(AFM)により各ポイントのZ軸方向の高さから、下記の(式2)により算出した。
本発明で用いられる多孔性膜の形状は、好ましくは平膜である。多孔性膜の形状が平膜の場合、その平均厚みは用途に応じて選択される。多孔性膜の形状が平膜の場合の平均厚みは、好ましくは20μm以上5000μm以下であり、より好ましくは50μm以上2000μm以下である。
また、本発明で用いられる多孔性膜の形状は、好ましくは中空糸膜である。多孔性膜が中空糸膜の場合、中空糸の内径は、好ましくは200μm以上5000μm以下であり、膜厚は、好ましくは20μm以上2000μm以下である。また、有機繊維または無機繊維を筒状にした織物や編物を中空糸の内部に含んでいても良い。
次に、本発明で用いられる多孔性膜の作成法の概要を例示して説明する。まず、多孔性膜のうち、平膜の作成法の概要について説明する。
多孔質基材の表面に、樹脂と溶媒とを含む原液の被膜を形成すると共に、その原液を多孔質基材に含浸させる。その後、被膜を有する多孔質基材の被膜側表面のみを、非溶媒を含む凝固浴と接触させて樹脂を凝固させると共に、多孔質基材の表面に多孔質樹脂層を形成する。
原液は、樹脂を溶媒に溶解させて調整する。原液の温度は、製膜性の観点から、通常、5〜120℃の範囲内で選定することが好ましい。溶媒は、樹脂を溶解するものであり、樹脂に作用してそれらが多孔質樹脂層を形成するのを促すものである。溶媒としては、N−メチルピロリジノン(NMP)、N,N−ジメチルアセトアミド(DMAc)、N,N−ジメチルホルムアミド(DMF)、ジメチルスルホキシド(DMSO)、N − メチル− 2 − ピロリドン、メチルエチルケトン、テトラヒドロフラン、テトラメチル尿素、リン酸トリメチル、シクロヘキサノン、イソホロン、γ − ブチロラクトン、メチルイソアミルケトン、フタル酸ジメチル、プロピレングリコールメチルエーテール、プロピレンカーボネート、ジアセトンアルコール、グリセロールトリアセテート、アセトンおよびメチルエチルケトンなどを用いることができる。なかでも、樹脂の溶解性の高いN−メチルピロリジノン(NMP)、N,N−ジメチルアセトアミド(DMAc)、N,N−ジメチルホルムアミド(DMF)およびジメチルスルホキシド(DMSO)が好ましく用いられる。これらの溶媒は、単独で用いても良いし2種類以上を混合して用いても良い。原液は、先述の樹脂を好ましくは5重量%以上60重量%以下の濃度で溶媒に溶解させることにより調製することができる。
また、例えば、ポリエチレングリコール、ポリビニルアルコール、ポリビニルピロリドンおよびグリセリンなどの溶媒以外の成分を溶媒に添加しても良い。溶媒に非溶媒を添加することもできる。非溶媒は、樹脂を溶解しない液体である。非溶媒は、樹脂の凝固の速度を制御して細孔の大きさを制御するように作用する。非溶媒としては、水や、メタノールおよびエタノールなどのアルコール類を用いることができる。なかでも、非溶媒として、価格の点から水やメタノールが好ましく用いられる。溶媒以外の成分および非溶媒は、混合物であってもよい。
原液には、開孔剤を添加することもできる。開孔剤は、凝固浴に浸漬された際に抽出されて、樹脂層を多孔質にする作用を持つものである。開孔剤を添加することにより、平均細孔径の大きさを制御することができる。開孔剤は、凝固浴への溶解性の高いものであることが好ましい。開孔剤としては、例えば、塩化カルシウムや炭酸カルシウムなどの無機塩を用いることができる。また、開孔剤として、ポリエチレングリコールやポリプロピレングリコールなどのポリオキシアルキレン類や、ポリビニルアルコール、ポリビニルブチラールおよびポリアクリル酸などの水溶性高分子化合物や、グリセリンを用いることができる。
次に、多孔性膜のうち、中空糸膜の作成法の概要について説明する。
中空糸膜は、樹脂と溶媒からなる原液を二重管式口金の外側の管から吐出すると共に、中空部形成用流体を二重管式口金の内側の管から吐出して、冷却浴中で冷却固化して作製することができる。
原液は、上述の平膜の作成法で述べた樹脂を好ましくは20重量%以上60重量%以下の濃度で、上述の平膜の生成法で述べた溶媒に溶解させることにより調製することができる。また、中空部形成用流体には、通常気体もしくは液体を用いることができる。また、得られた中空糸膜の外表面に、新たな多孔性樹脂層をコーティング(積層)することもできる。積層は中空糸膜の性質、例えば、親水・疎水性あるいは細孔径等を所望の性質に変化させるために行うことができる。積層される新たな多孔性樹脂層は、樹脂を溶媒に溶解させた原液を、非溶媒を含む凝固浴と接触させて樹脂を凝固させることによって作製することができる。その樹脂の材質は、例えば、上述有機高分子膜の材質と同様のものが好ましく用いられる。また、積層方法としては、原液に中空糸膜を浸漬してもよいし、中空糸膜の表面に原液を塗布してもよく、積層後、付着した原液の一部を掻き取ったり、エアナイフを用いて吹き飛ばしすることにより積層量を調製することもできる。
本発明で用いられる多孔性膜は、樹脂などの部材を用いて中空糸膜の中空部を接着・封止し、支持体に設置することによって分離膜エレメントとすることができる。すなわち、本発明で用いられる多孔性膜は、支持体と組み合わせることによって分離膜エレメントとすることができる。支持体として支持板を用い、その支持板の少なくとも片面に、本発明で用いられる多孔性膜を配した分離膜エレメントは、本発明で用いられる多孔性膜を有する分離膜エレメントの好適な形態の一つである。透水量を大きくするために、支持板の両面に多孔性膜を配することも分離膜エレメントの好ましい態様である。
本発明の化学品の製造方法においては、膜間差圧を0.1から20kPaの範囲で濾過処理することが重要である。発酵培養液を濾過するために、20kPaより高い膜間差圧で濾過処理すると、圧力を加えるための動力が必要であり、化学品を製造するときの経済効果が低下する。また、20kPaより高い膜間差圧を加えることによって微生物もしくは培養細胞が破砕される場合があり、化学品を生産する能力が低下する。本発明の化学品の製造方法は、濾過圧力である膜間差圧が0.1から20kPaの範囲であり、水頭差により膜間差圧を得られることから、特別に発酵反応槽内を加圧状態に保つ必要がなく、化学品を生産する能力が低下しない。また、特別に発酵反応槽内を加圧状態に保つ必要がないことから、多孔性膜を発酵反応槽内部に設置する様態も可能となり、発酵装置がコンパクト化できる利点も挙げられる。本発明の化学品の製造方法では、膜間差圧を、好ましくは0.1から5kPaの範囲で濾過処理する。
本発明で使用される微生物や培養細胞の発酵原料は、発酵培養する微生物や培養細胞の生育を促し、目的とする発酵生産物である化学品を良好に生産させ得るものであればよい。発酵原料としては、例えば、炭素源、窒素源、無機塩類、および必要に応じてアミノ酸、およびビタミンなどの有機微量栄養素を適宜含有する通常の液体培地等が好ましく用いられる。
上記の炭素源としては、例えば、グルコース、シュークロース、フラクトース、ガラクトースおよびラクトース等の糖類、これら糖類を含有する澱粉糖化液、甘藷糖蜜、甜菜糖蜜、ハイテストモラセス、サトウキビ搾汁、更には酢酸やフマル酸等の有機酸、エタノールなどのアルコール類、およびグリセリンなどが使用される。ここで糖類とは、多価アルコールの最初の酸化生成物であり、アルデヒド基またはケトン基をひとつ持ち、アルデヒド基を持つ糖をアルドース、ケトン基を持つ糖をケトースと分類される炭水化物のことを指す。
また、上記の窒素源としては、例えば、アンモニアガス、アンモニア水、アンモニウム塩類、尿素、硝酸塩類、その他補助的に使用される有機窒素源、例えば、油粕類、大豆加水分解液、カゼイン分解物、その他のアミノ酸、ビタミン類、コーンスティープリカー、酵母または酵母エキス、肉エキス、ペプトン等のペプチド類、各種発酵菌体およびその加水分解物などが使用される。
また、上記の無機塩類としては、例えば、リン酸塩、マグネシウム塩、カルシウム塩、鉄塩およびマンガン塩等を適宜添加使用することができる。
本発明で使用される微生物や培養細胞が生育のために特定の栄養素を必要とする場合には、その栄養物を標品もしくはそれを含有する天然物として添加することができる。また、消泡剤も必要に応じて添加使用することができる。
本発明において、発酵培養液とは、発酵原料に微生物または培養細胞が増殖した結果得られる液のことを言う。追加する発酵原料の組成は、目的とする化学品の生産性が高くなるように、培養開始時の発酵原料組成から適宜変更することができる。
本発明では、発酵培養液中の糖類濃度は5g/l以下に保持されるようにすることが好ましい。その理由は、発酵培養液の引き抜きによる糖類の流失を最小限にするためである。そのため、糖類の濃度は可能な限り小さいことが望ましい。
微生物の発酵培養は、通常、pHが4〜8で温度が20〜45℃の範囲で行われることが多い。発酵培養液のpHは、無機の酸あるいは有機の酸、アルカリ性物質、さらには尿素、水酸化カルシウム、炭酸カルシウムおよびアンモニアガスなどによって、上記範囲内のあらかじめ定められた値に調節される。
培養において、酸素の供給速度を上げる必要があれば、空気に酸素を加えて酸素濃度を好適には21%以上に保つ、発酵培養液を加圧する、攪拌速度を上げる、あるいは通気量を上げるなどの手段を用いることができる。逆に、酸素の供給速度を下げる必要があれば、炭酸ガス、窒素およびアルゴンなど酸素を含まないガスを空気に混合して供給することも可能である。
本発明においては、培養初期にBatch培養またはFed−Batch培養を行って微生物濃度を高くした後に連続培養(引き抜き)を開始しても良いし、高濃度の菌体をシードし、培養開始とともに連続培養を行っても良い。適当な時期から、原料培養液の供給および培養物の引き抜きを行うことが可能である。原料培養液供給と培養物の引き抜きの開始時期は、必ずしも同じである必要はない。また、原料培養液の供給と培養物の引き抜きは連続的であってもよいし、間欠的であってもよい。原料培養液には、上記に示したような菌体増殖に必要な栄養素を添加し、菌体増殖が連続的に行われるようにすればよい。
発酵培養液中の微生物または培養細胞の濃度は、発酵培養液の環境が微生物または培養細胞の増殖にとって不適切となって死滅する比率が高くならない範囲で、高い状態で維持することが効率的でよい生産性を得る上で好ましい態様である。一例として、濃度を、乾燥重量として5g/L以上に維持することにより良好な生産効率が得られる。連続発酵装置の運転上の不具合や生産効率の低下を招かなければ、発酵培養液中の微生物または培養細胞の濃度の上限は特に限定されない。
発酵生産能力のあるフレッシュな菌体を増殖させつつ行う連続培養操作は、培養管理上、通常、単一の発酵反応槽で行うことが好ましい。しかしながら、菌体を増殖しつつ生産物を生成する連続発酵培養法であれば、発酵反応槽の数は問わない。発酵反応槽の容量が小さい等の理由から、複数の発酵反応槽を用いることもあり得る。その場合、複数の発酵反応槽を配管で並列または直列に接続して連続培養を行っても、発酵生産物の高生産性は得られる。
本発明においては、微生物や培養細胞を発酵反応槽に維持したままで、発酵反応槽からの発酵培養液の連続的かつ効率的な抜き出しが可能である。そのため、微生物や細胞を連続的に発酵培養し、十分な増殖を確保した後に発酵原料液組成を変更し、目的とする化学品を効率よく製造することも可能である。
本発明で使用される微生物や培養細胞としては、真核細胞、および原核細胞をともに用いることができ、例えば、発酵工業においてよく使用されるパン酵母などの酵母、大腸菌、コリネ型細菌などのバクテリア、糸状菌、放線菌、動物細胞および昆虫細胞などが挙げられる。使用する微生物や細胞は、自然環境から単離されたものでもよく、また、突然変異や遺伝子組換えによって一部性質が改変されたものであってもよい。
本発明で用いられる真核細胞の最も際立った特徴は、細胞内に細胞核(核)と呼ばれる構造を持ち。細胞核(核)を有さない原核生物とは明確に区別される。本発明では、その真核細胞のうちで更に好ましくは酵母を好ましく用いることができる。
本発明において好適な酵母としては、例えば、サッカロミセス属(Genus Saccharomyces)に属する酵母とサッカロミセス・セレビセ(Saccharomyces cerevisiae)に属する酵母が挙げられる。
本発明で用いられる原核細胞の最も際立った特徴は、細胞内に細胞核(核)と呼ばれる構造をもたないことであり、細胞核(核)を有する真核生物とは明確に区別される。
本発明の製造方法で得られる化学品は、上記の微生物や培養細胞が発酵培養液中に生産する物質である。化学品としては、例えば、アルコール、有機酸、アミノ酸、核酸およびビタミンなど発酵工業において大量生産されている物質を挙げることができる。また、本発明は、酵素、抗生物質および組換えタンパク質のような物質の生産に適用することも可能である。例えば、アルコールとしては、エタノール、1,3−プロパンジオール、1,4−ブタンジオールおよびグリセロール等が挙げられる、また、有機酸としては、酢酸、乳酸、ピルビン酸、コハク酸、リンゴ酸、イタコン酸およびクエン酸等を挙げることができ、アミノ酸であれば、グルタミン酸、リジン、スレオニン、アラニン、アルギニン、ヒスチジン、グルタミン等を挙げることができ、アミノ酸の誘導体も本発明の化学品に含まれる。アミノ酸の誘導体として、カダベリンを挙げることができる。また、核酸であればイノシン、グアノシンおよびシチジン等を挙げることができる。
本発明で乳酸を製造する場合、真核細胞であれば酵母、原核細胞であれば乳酸菌を用いることが好ましい。このうち酵母は、乳酸脱水素酵素をコードする遺伝子を細胞に導入した酵母が好ましい。このうち乳酸菌は、消費したグルコースに対して対糖収率として50%以上の乳酸を産生する乳酸菌を用いることが好ましく、更に好ましくは対等収率として80%以上の乳酸菌であることが好適である。それら乳酸菌のうち、ラクトバチラス属(Lactobacillus)、バチラス属(Bacillus)属、ペディオコッカス(Pediococcus)、テトラゲノコッカス属(Genus Tetragenococcus)、カルノバクテリウム属(Genus Carnobacterium)、カルノバクテリウム属(Genus Carnobacterium)、カルノバクテリウム属(Genus Carnobacterium)、カルノバクテリウム属(Genus Carnobacterium)、バゴコッカス属(Genus Vagococcus)、ロイコノストック属(Genus Leuconostoc)、オエノコッカス属(Genus Oenococcus)、アトポビウム属(Genus Atopobium)、ストレプトコッカス属(Genus Streptococcus)、エンテロコッカス属(Genus Enterococcus)、ラクトコッカス属(Genus Lactococcus)およびスポロラクトバチルス属(Genus Sporolactobacillus)に属する乳酸菌を用いることができ、更に好ましくは、スポロラクトバチルス・ラエボラクティカス(Sporolactobacillus laevolacticus)が使用できる。
本発明における連続発酵とは、微生物もしくは培養細胞の発酵培養液を分離膜で濾過処理する様態として間欠的に濾過処理を行いながら、濾液から生産物を回収すると共に未濾過液を前記の発酵培養液に保持または還流し、かつ、発酵原料を発酵培養液に追加することによって化学品を連続的に発酵生産することである。
本発明において、微生物や培養細胞の発酵培養液を分離膜で濾過処理する際の膜間差圧は、微生物や培養細胞および培地成分が容易に目詰まりしない条件であればよいが、上述のように、膜間差圧を0.1kPa以上20kPa以下の範囲にして濾過処理することが重要である。膜間差圧は、好ましくは0.1kPa以上10kPa以下の範囲であり、さらに好ましくは0.1kPa以上5kPaの範囲である。上記膜間差圧の範囲を外れた場合、原核微生物および培地成分の目詰まりが急速に発生し、透過水量の低下を招き、連続発酵運転に不具合を生じることがある。
本発明において、発酵培養液は、後で詳述するように好ましくは分離膜を設置している発酵反応槽内、あるいは膜分離槽内で撹拌状態あるいは発酵培養液が流れている状態である。上記の非濾過処理操作を行うことにより、発酵培養液側の分離膜表面に付着した微生物もしくは培養細胞ならびにその他の固形物が撹拌状態である発酵培養液によって脱落、洗浄されやすくなることから、分離膜の閉塞が発生しにくくなるため、0.1から20kPaの範囲の低い膜間差圧を維持しながら長期間安定した化学品の連続発酵が可能になる。
濾過の駆動力としては、発酵培養液と多孔性膜処理水の液位差(水頭差)を利用したサイホンにより多孔性膜に膜間差圧を発生させることができる。また、濾過の駆動力として多孔性膜処理水側に吸引ポンプを設置してもよいし、多孔性膜の発酵培養液側に加圧ポンプを設置することも可能である。上記の範囲に膜間差圧を制御する手段としては、発酵培養液と多孔性膜処理水の液位差を変化させることにより制御することができる、また、膜間差圧を発生させるためにポンプを使用する場合には、吸引圧力により膜間差圧を制御することができる。更に、発酵培養液側の圧力を導入する気体または液体の圧力によっても膜間差圧を制御することができる。これら圧力制御を行う場合には、発酵培養液側の圧力と多孔性膜処理水側の圧力差をもって膜間差圧とし、膜間差圧の制御に用いることができる。
本発明における間欠的な濾過処理とは、濾過処理操作と非濾過処理操作を交互に繰り返して行うことを言う。このうち、濾過処理操作は、発酵培養液を濾過し発酵濾液を発酵反応槽内から抜き出す操作を指す。また、非濾過処理操作は、発酵培養液の濾過を行わない操作のことを指す。上述のように、分離膜が設置されている槽では培養液が攪拌、あるいは培養液が流れている状態であり、分離膜の微小な表面に於いては培養液が流れている状態である。この培養液が流れている状態にあると発酵培養液中の微生物など固形分等を常に分離膜表面から剥離させる効果がある。ここでろ過処理操作を行うと分離膜上に微生物など固形分等を堆積させる効果がある。固形分が堆積すると分離膜のろ過能力の低下を招く。したがって、本発明の間欠的なろ過処理を行うことによって、ろ過処理操作時に分離膜上に堆積した固形分を非ろ過処理操作時に剥離させ、長期間、分離膜のろ過能力を維持させることが可能となり、その結果、長期間安定した化学品の製造を実現することができる。
次に、濾過処理操作と非濾過処理操作の操作時間と交互繰り返し頻度について説明する。濾過処理操作と非濾過処理操作の操作時間と交互繰り返し頻度については、膜間差圧として0.1から20kPaの範囲を維持した濾過を行うことができる範囲で任意に設定することができる。
例えば、膜間差圧を測定しながら濾過処理操作を継続し、膜間差圧が20kPaにまで上昇したら、非濾過処理操作を行うことにより、膜間差圧を0.1から20kPaの範囲で調節しながら、間欠的な濾過処理を行うことができる。また、規則的に濾過処理操作と非濾過処理操作を繰り返し、膜間差圧を0.1から20kPaの範囲で調節しながら、間欠的な濾過処理を行うことも可能である。
一方、濾過処理操作は発酵培養液から生産物を含む濾液を得る上で重要な操作である。それに対して、非濾過処理操作は、分離膜の閉塞を発生しにくくするために分離膜表面に付着した固形物を洗浄する上で重要な操作である。このことから、高い発酵生産効率を得るためには、非濾過処理操作時間としては、膜間差圧として0.1から20kPaの範囲を維持し、かつ、必要十分な分離膜表面の洗浄効果が得られる時間を確保することが望ましい。そして、可能な限り濾過処理操作時間を長くとって、濾過処理操作と非濾過処理操作の交互繰り返し操作を行うことが好ましい。
具体的には、濾過処理時間と非濾過処理時間の相対比として(濾過処理時間)/(非濾過処理時間)として1から100で操作することができる。好ましくは5から20が好ましく、相対比10で操作することが最も好ましい。また、上記相対比の範囲で、濾過処理時間を1分から1時間の間で操作することが可能である。そのうち5分から20分で操作することが好ましい。これら、上述の濾過処理時間と非濾過処理時間の相対比と濾過処理時間の範囲で濾過処理と非濾過処理を繰り返すことで化学品を連続的に製造することができる。膜間差圧を0.1から20kPaの範囲を維持できれば、上述の濾過処理時間と非濾過処理時間の相対比と濾過処理時間の範囲で、その都度繰り返しの間隔を設定することが可能である。また、規則的に繰り返すこともできる。
このように、間欠的に濾過処理を行うことで、長期間安定した化学品を製造することができる。
次に、本発明で用いられる連続発酵装置の構成および特徴について説明する。本発明で用いられる連続発酵装置は、微生物もしくは培養細胞の発酵培養液を分離膜で濾過し、濾液から生産物を回収するとともに未濾過液を前記の発酵培養液に保持または還流し、かつ、発酵原料を前記の発酵培養液に追加する連続発酵による化学品を製造するための装置である。
本発明で用いられる連続発酵装置は、微生物もしくは培養細胞を発酵培養させるための発酵反応槽を有するものである。
本発明で用いられる連続発酵装置のひとつの形態は、発酵反応槽と、その発酵反応槽内部に配設され分離膜を備えた発酵培養液を濾過するための分離膜エレメントと、その分離膜エレメントに接続され濾過された発酵生産物を排出するための手段と、該分離膜の膜間差圧を0.1から20kPaの範囲に制御するための手段とからなり、その該分離膜として平均細孔径0.01μm以上1μm未満の細孔を有する多孔性膜が用いられる。
本発明で用いられる連続発酵装置の別の形態は、発酵反応槽と、その発酵反応槽に発酵培養液循環手段を介して接続され内部に分離膜を備えた発酵培養液を濾過するための膜分離槽と、その分離膜の膜間差圧を0.1から20kPaの範囲に制御する手段とからなり、その分離膜として平均細孔径0.01μm以上1μm未満の多孔性膜が用いられる。
次に、本発明の化学品の製造方法で用いられる連続発酵装置について、図面を用いて説明する。
本発明の化学品の製造方法で用いられる連続発酵装置のうち、分離膜エレメントが発酵反応槽の外部に設置された代表的な一例を図1の概要図に示す。図1は、本発明の化学品の製造方法で用いられる連続発酵装置の例を説明するための概略側面図である。
図1において、連続発酵装置は、発酵反応槽1と、分離膜エレメント2を備えた膜分離槽12と、水頭差制御装置3とで基本的に構成されている。ここで、分離膜エレメント2には、多孔性膜が組み込まれている。この多孔性と膜分離膜エレメントとしては、例えば、国際公開第2002/064240号パンフレットに開示されている分離膜および分離膜エレメントを使用することが好適である。また、膜分離槽12は、発酵培養液循環ポンプ11を介して発酵反応槽1に接続されている。
図1において、培地供給ポンプ7によって培地を発酵反応槽1に投入し、必要に応じて、攪拌機5で発酵反応槽1内の発酵培養液を攪拌し、また必要に応じて、気体供給装置4によって必要とする気体を供給することができる。このとき、供給された気体を回収リサイクルして再び気体供給装置4で供給することができる。また必要に応じて、pHセンサ・制御装置9およびよびpH調整溶液供給ポンプ8によって発酵培養液のpHを調整し、また必要に応じて、温度調節器10によって発酵培養液の温度を調節することにより、生産性の高い発酵生産を行うことができる。さらに、装置内の発酵培養液は、発酵培養液循環ポンプ11によって発酵反応槽1と膜分離槽12の間を循環する。発酵生産物を含む発酵培養液は、分離膜エレメント2によって微生物と発酵生産物に濾過・分離され、発酵生産物を装置系から取り出すことができる。また、濾過・分離された微生物は、装置系内にとどまることにより装置系内の微生物濃度を高く維持することができ、生産性の高い発酵生産を可能としている。
ここでは、計装・制御装置による発酵培養液の物理化学的条件の調節に、pHおよび温度を例示したが、必要に応じて、溶存酸素やORPの制御、オンラインケミカルセンサーなどの分析装置により、発酵培養液中の化学品の濃度を測定し、発酵培養液中の化学品の濃度を指標とした物理化学的条件の制御を行うことができる。また、培地の連続的もしくは断続的投入は、好ましくは、上記計装装置による発酵培養液の物理化学的環境の測定値を指標として、培地投入量および速度を適宜調節することができる。
ここで、分離膜エレメント2による間欠的な濾過・分離は、膜分離槽12の水面との水頭差圧によって行うことができ、特別な動力を必要としない。必要に応じて、レベルセンサ6および水頭差圧制御装置3によって、分離膜エレメント2の濾過・分離速度および装置系内の発酵培養液量を適当に調節することができる。必要に応じて、気体供給装置4によって必要とする気体を膜分離槽12内に供給することができる。このとき、供給された気体を回収リサイクルして再び気体供給装置4で膜分離槽12内に供給することができる。
分離膜エレメント2による濾過・分離は、必要に応じて、ポンプ等による吸引濾過あるいは装置系内を加圧することにより、濾過・分離することもできる。また、別の培養槽(図示せず)で連続発酵に微生物または培養細胞を培養し、それを必要に応じて発酵反応槽内に供給することができる。別の培養槽で連続発酵に微生物または培養細胞を培養し、得られた発酵培養液を必要に応じて発酵反応槽1内に供給することにより、常にフレッシュで化学品の生産能力の高い微生物または培養細胞による連続発酵が可能となり、高い生産性能を長期間維持した連続発酵が可能となる。
次に、本発明の化学品の製造方法で用いられる連続発酵装置のうち、分離膜エレメントが発酵反応槽の内部に設置された代表的な一例を図2の概要図に示す。図2は、本発明で用いられる他の連続発酵装置の例を説明するための概略側面図である。
図2において、連続発酵装置は、内部に分離膜エレメント2を備えた発酵反応槽1と水頭差制御装置3で基本的に構成されている。発酵反応槽1内の分離膜エレメント2には、多孔性膜が組み込まれている。この多孔性膜と分離膜エレメントとしては、例えば、国際公開第2002/064240号パンフレットに開示されている分離膜および分離膜エレメントを使用することができる。分離膜エレメントに関しては、追って詳述する。
次に、図2の連続発酵装置による連続発酵の形態について説明する。培地供給ポンプ7によって、培地を発酵反応槽1に連続的もしくは断続的に投入する。培地は、発酵反応槽1内に投入される前に必要に応じて、加熱殺菌、加熱滅菌あるいはフィルターを用いた滅菌処理を行うことができる。発酵生産時には、必要に応じて、発酵反応槽1内の攪拌機5で発酵反応槽1内の発酵培養液を攪拌することができる。発酵生産時には、必要に応じて、気体供給装置4によって必要とする気体を発酵反応槽1内に供給することができる。発酵生産時は、必要に応じて、pHセンサ・制御装置9およびpH調整溶液供給ポンプ8によって発酵反応槽1内の発酵培養液のpHを調整し、必要に応じて、温度調節器10によって発酵反応槽1内の発酵培養液の温度を調節することにより、生産性の高い発酵生産を行うことができる。
ここでは、計装・制御装置による発酵培養液の物理化学的条件の調節に、pHおよび温度を例示したが、必要に応じて、溶存酸素やORPの制御、オンラインケミカルセンサーなどの分析装置により、発酵培養液中の化学品の濃度を測定し、発酵培養液中の化学品の濃度を指標とした物理化学的条件の制御を行うことができる。また、培地の連続的もしくは断続的投入は、好ましくは、上記計装装置による発酵培養液の物理化学的環境の測定値を指標として、培地投入量および速度を適宜調節することができる。
図2において、発酵培養液は、発酵反応槽1内に設置された分離膜エレメント2によって、微生物と発酵生産物が濾過・分離され、発酵生産物が装置系から取り出される。また、濾過・分離された微生物が装置系内に留まることにより装置系内の微生物濃度を高く維持することができ、生産性の高い発酵生産を可能としている。ここで、分離膜エレメント2による間欠的な濾過・分離は発酵反応槽1の水面との水頭差圧によって行い、特別な動力を必要としない。また、必要に応じて、レベルセンサ6および水頭差圧制御装置3によって、分離膜エレメント2の濾過・分離速度およびよび発酵反応槽1内の発酵培養液量を適当に調節することができる。上記の分離膜エレメントによる濾過・分離には、必要に応じて、ポンプ等による吸引濾過あるいは装置系内を加圧することにより、濾過・分離することもできる。また、別の培養槽(図示せず)で連続発酵により微生物または培養細胞を培養し、それを必要に応じて発酵反応槽1内に供給することができる。別の培養槽で連続発酵により微生物または培養細胞を培養し、その培養液を必要に応じて発酵反応槽1内に供給することにより、常にフレッシュで化学品の生産能力の高い微生物または培養細胞による連続発酵が可能となり、高い生産性能を長期間維持した連続発酵が可能となる。
次に、本発明の化学品の製造方法で用いられる連続発酵装置で、好ましく用いられる分離膜エレメントについて説明する。
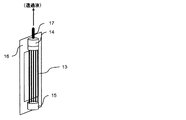
図3に示す分離膜エレメントについて説明する。図3は、本発明で用いられる分離膜エレメントを例示説明するための概略斜視図である。本発明の化学品の製造方法で用いられる連続発酵装置では、好ましくは、国際公開第2002/064240号パンフレットに開示されている分離膜および分離膜エレメントを用いることができる。分離膜エレメントは、図3に示されるように、剛性を有する支持板13の両面に、流路材14と前記の分離膜15(多孔性膜)をこの順序で配し構成されている。支持板13は、両面に凹部16を有している。分離膜15は、発酵培養液を濾過する。流路材14は、分離膜15で濾過された濾液を効率よく支持板13に流すためのものである。支持板13に流れた濾液は、支持板13の凹部16を通り、集水パイプ17を介して連続発酵装置外部に取り出される。濾液を取り出すための動力として、水頭差圧、ポンプ、液体や気体等による吸引濾過、あるいは装置系内を加圧するなどの方法を用いることができる。
図4に示す分離膜エレメントについて説明する。図4は、本発明で用いられる別の分離膜エレメントを例示説明するための概略斜視図である。分離膜エレメントは、図4に示すように、中空糸膜(多孔性膜)で構成された分離膜束18と上部樹脂封止層19と下部樹脂封止層20によって主に構成される。分離膜束18は、上部樹脂封止層19および下部樹脂封止層20よって束状に接着・固定化されている。下部樹脂封止層20による接着・固定化は、分離膜束18の中空糸膜(多孔性膜)の中空部を封止しており、発酵培養液の漏出を防ぐ構造になっている。一方、上部樹脂封止層19は、分離膜束18の中空糸膜(多孔性膜)の内孔を封止しておらず、集水パイプ22に濾液が流れる構造となっている。この分離膜エレメントは、支持フレーム21を介して連続発酵装置内に設置することが可能である。分離膜束18によって濾過された濾液は、中空糸膜の中空部を通り、集水パイプ22を介して連続発酵装置外部に取り出される。濾液を取り出すための動力として、水頭差圧、ポンプ、液体や気体等による吸引濾過、あるいは装置系内を加圧するなどの方法を用いることができる。
本発明の化学品の製造方法で用いられる連続発酵装置の分離膜エレメントを構成する部材は、高圧蒸気滅菌操作に耐性の部材であることが好ましい。連続発酵装置内が滅菌可能であれば、連続発酵時に好ましくない微生物による汚染の危険を回避することができ、より安定した連続発酵が可能となる。分離膜エレメントを構成する部材は、高圧蒸気滅菌操作の条件である、121℃で15分間に耐性であることが好ましい。分離膜エレメント部材は、例えば、ステンレスやアルミニウムなどの金属、ポリアミド系樹脂、フッ素系樹脂、ポリカーボネート系樹脂、ポリアセタール系樹脂、ポリブチレンテレフタレート系樹脂、PVDF、変性ポリフェニレンエーテル系樹脂およびポリサルホン系樹脂等の樹脂を好ましく選定できる。
本発明の化学品の製造方法で用いられる連続発酵装置では、分離膜エレメントは、図1のように発酵反応槽内に設置しても良いし、図2のように発酵反応槽外に設置しても良い。分離膜エレメントを発酵反応槽外に設置する場合には、別途、膜分離槽を設けてその内部に分離膜エレメントを設置することができ、発酵反応槽と膜分離槽の間を発酵培養液を循環させながら、分離膜エレメントにより発酵培養液を連続的に濾過することができる。
本発明の化学品の製造方法で用いられる連続発酵装置では、膜分離槽は、高圧蒸気滅菌可能であることが望ましい。膜分離槽が高圧蒸気滅菌可能であると、雑菌による汚染回避が容易である。
本発明に従って連続発酵を行った場合、高い体積生産速度が得られるとともに、その体積生産速度を長期間維持した極めて効率のよい連続発酵生産が可能となる。ここで、連続発酵培養における生産速度は、次の式(3)で計算される。
・発酵生産速度(g/L/hr)=抜き取り液中の生産物濃度(g/L)×発酵培養液抜き取り速度(L/hr)÷装置の運転液量(L)・・・・(式3)
また、バッチ培養での発酵生産速度は、原料炭素源をすべて消費した時点の生産物量(g)を、炭素源の消費に要した時間(h)とその時点の発酵培養液量(L)で除して求められる。
以下、本発明の連続発酵による化学品の製造方法をさらに詳細に説明するために、上記の発酵生産物として乳酸を選定し、図1ならびに図2に示す連続発酵装置を用いて連続的な乳酸の発酵生産について実施例を挙げて説明する。
ここで、L−乳酸を生産させる微生物には、酵母サッカロミセス・セレビセ(Saccharomyces cerevisae)を用いた。サッカロミセス・セレビセは、本来L−乳酸発酵を持たないが、L−乳酸脱水素酵素をコードする遺伝子をサッカロミセス・セレビセに導入することによりL−乳酸発酵能力をもつサッカロミセス・セレビセ株を造成し実施した。具体的には、ヒト由来LDH遺伝子を酵母ゲノム上のPDC1プロモーターの下流に連結することにより、L−乳酸発酵能力を持つ酵母株を造成して使用した。またD−乳酸を生産させる微生物には、スポロラクトバチルス・ラエボラクティカス(Sporolactobacillus laevolacticus)を用いた。
[参考例1]乳酸生産能力を持つ酵母株の作製
乳酸生産能力を持つ酵母株を、下記のように造成した。具体的には、ヒト由来LDH遺伝子を酵母ゲノム上のPDC1プロモーターの下流に連結することにより、L−乳酸生産能力を持つ酵母株を造成する。ポリメラーゼ・チェーン・リアクション(PCR)には、La−Taq(宝酒造社製)あるいはKOD−Plus−polymerase(東洋紡社製)を用い、付属の取扱説明に従って行った。
ヒト乳ガン株化細胞(MCF−7)を培養回収後、TRIZOL Reagent(Invitrogen)を用いてtotal RNAを抽出し、得られたtotal RNAを鋳型としてSuperScript Choice System(Invitrogen)を用いた逆転写反応によりcDNAの合成を行った。これらの操作の詳細は、それぞれ付属のプロトコールに従った。得られたcDNAを、続くPCRの増幅鋳型とした。
上記の操作で得られたcDNAを増幅鋳型とし、配列番号1および配列番号2で表されるオリゴヌクレオチドをプライマーセットとしたKOD−Plus−polymeraseによるPCRにより、L−ldh遺伝子のクローニングを行った。各PCR増幅断片を精製し末端をT4 Polynucleotide Kinase(TAKARA社製)によりリン酸化後、pUC118ベクター(制限酵素HincIIで切断し、切断面を脱リン酸化処理したもの)にライゲーションした。ライゲーションは、DNA Ligation Kit Ver.2(TAKARA社製)を用いて行った。
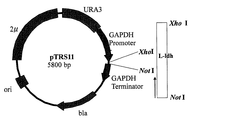
ライゲーションプラスミド産物で大腸菌DH5αを形質転換し、プラスミドDNAを回収することにより、各種L−ldh遺伝子(配列番号3)がサブクローニングされたプラスミドを得た。得られたL−ldh遺伝子が挿入されたpUC118プラスミドを制限酵素XhoIおよびNotIで消化し、得られた各DNA断片を酵母発現用ベクターpTRS11(図5)のXhoI/NotI切断部位に挿入した。このようにして、ヒト由来L−ldh遺伝子発現プラスミドpL−ldh5(L−ldh遺伝子)を得た。ヒト由来のL−ldh遺伝子発現ベクターである上記pL−ldh5は、プラスミド単独で独立行政法人産業技術総合研究所 特許生物寄託センター(茨城県つくば市東1−1−1中央第6)にFERMAP−20421として寄託した(寄託日:平成17年2月21日)。
ヒト由来LDH遺伝子を含むプラスミドpL−ldh5を増幅鋳型とし、配列番号4および配列番号5で表されるオリゴヌクレオチドをプライマーセットとしたPCRにより、1.3kbのヒト由来LDH遺伝子およびサッカロミセス・セレビセ由来のTDH3遺伝子のターミネーター配列含むDNA断片を増幅した。また、プラスミドpRS424を増幅鋳型として、配列番号6および配列番号7で表されるオリゴヌクレオチドをプライマーセットとしたPCRにより、1.2kbのサッカロミセス・セレビセ由来のTRP1遺伝子を含むDNA断片を増幅した。それぞれのDNA断片を、1.5%アガロースゲル電気泳動により分離し、常法に従い精製した。
ここで得られた1.3kb断片と1.2kb断片を混合したものを増幅鋳型とし、配列番号4および配列番号7で表されるオリゴヌクレオチドをプライマーセットとしたPCR法によって得られた産物を1.5%アガロースゲル電気泳動して、ヒト由来LDH遺伝子およびTRP1遺伝子が連結された2.5kbのDNA断片を、常法に従い調整した。この2.5kbのDNA断片で、出芽酵母NBRC10505株を常法に従いトリプトファン非要求性に形質転換した。
得られた形質転換細胞が、ヒト由来LDH遺伝子を酵母ゲノム上のPDC1プロモーターの下流に連結されている細胞であることの確認は、下記のようにして行った。まず、形質転換細胞のゲノムDNAを常法に従って調製し、これを増幅鋳型とした配列番号8および配列番号9で表されるオリゴヌクレオチドをプライマーセットとしたPCRにより、0.7kbの増幅DNA断片が得られることにより確認した。
また、形質転換細胞が乳酸生産能力を持つかどうかは、表1に示すSC培地(METHODS IN YEAST GENETICS 2000 EDITION、 CSHL PRESS)で形質転換細胞を培養した培養上澄に乳酸が含まれていることを、下記に示す条件でHPLC法により乳酸量を測定することにより確認した。
・カラム:Shim−Pack SPR−H(島津社製)
・移動相:5mM p−トルエンスルホン酸(流速0.8mL/min)
・反応液:5mM p−トルエンスルホン酸、20mM ビストリス、0.1mM EDTA・2Na(流速0.8mL/min)
・検出方法:電気伝導度
・温度:45℃。
また、L−乳酸の光学純度測定は、下記の条件でHPLC法により測定した。
・カラム:TSK−gel Enantio L1(東ソー社製)
・移動相 :1mM 硫酸銅水溶液
・流速:1.0ml/min
・検出方法 :UV254nm
・温度 :30℃。
また、L−乳酸の光学純度は、次式で計算される。
・光学純度(%)=100×(L−D)/(L+D)
ここで、LはL−乳酸の濃度であり、DはD−乳酸の濃度を表す。
HPLC分析の結果、4g/LのL−乳酸が検出され、D−乳酸は検出限界以下であった。以上の検討により、この形質転換体がL−乳酸生産能力を持つことが確認された。得られた形質転換細胞を、酵母SW−1株として、後の実施例で用いた。
[参考例2]多孔性膜の作製(その1)
樹脂としてポリフッ化ビニリデン(PVDF)樹脂を、また溶媒としてN,N−ジメチルアセトアミド(DMAc)をそれぞれ用い、これらを90℃の温度下に十分に攪拌し、次の組成を有する原液を得た。
[原液]
・PVDF:13.0重量%
・DMAc:87.0重量%。
次に、上記原液を25℃の温度に冷却した後、あらかじめガラス板上に貼り付けて置いた、密度が0.48g/cm3で、厚みが220μmのポリエステル繊維製不織布(多孔質基材)に塗布し、直ちに次の組成を有する25℃の温度の凝固浴中に5分間浸漬して、多孔質基材に多孔質樹脂層が形成された多孔性膜を得た。
[凝固浴]
・水 :30.0重量%
・DMAc:70.0重量%。
この多孔性膜をガラス板から剥がした後、80℃の温度の熱水に3回浸漬してDMAcを洗い出し、分離膜を得た。多孔質樹脂層表面の9.2μm×10.4μmの範囲内を、倍率10,000倍で走査型電子顕微鏡観察を行ったところ、観察できる細孔すべての直径の平均は0.1μmであった。次に、上記分離膜について純水透水透過係数を評価したところ、50×10-9m3/m2/s/Paであった。純水透水量の測定は、逆浸透膜による25℃の温度の精製水を用い、ヘッド高さ1mで行った。また、平均細孔径の標準偏差は0.035μmで、膜表面粗さは0.06μmであった。
[参考例3]多孔性膜の作製(その2)
重量平均分子量41.7万のフッ化ビニリデンホモポリマーとγ−ブチロラクトンとを、それぞれ38重量%と62重量%の割合で170℃の温度で溶解し原液を作製した。この原液をγ−ブチロラクトンを中空部形成液体として随拌させながら口金から吐出し、温度20℃のγ−ブチロラクトン80重量%水溶液からなる冷却浴中で固化して中空糸膜を作製した。
次いで、重量平均分子量28.4万のフッ化ビニリデンホモポリマーを14重量%、セルロースアセテートプロピオネート(イーストマンケミカル社、CAP482−0.5)を1重量%、N-メチル-2-ピロリドンを77重量%、ポリオキシエチレンヤシ油脂肪酸ソルビタン(三洋化成株式会社、商品名“イオネットT−20C”(登録商標))を5重量%、および水を3重量%の割合で95℃の温度で混合溶解して原液を調整した。この原液を、上記で得られた中空糸膜の表面に均一に塗布し、すぐに水浴中で凝固させた本発明で用いる中空糸多孔性膜を製作した。得られた中空糸多孔性膜の被処理水側表面の平均細孔径は、0.05μmであった。次に、上記の分離膜である中空糸多孔性膜について純水透水量を評価したところ、5.5×10-9m3/m2・s・Paであった。透水量の測定は、逆浸透膜による25℃の温度の精製水を用い、ヘッド高さ1mで行った。また、平均細孔径の標準偏差 は0.006μmであった。
[実施例1]連続発酵によるL−乳酸の製造(その1)
図1に示す連続発酵装置を稼働させることにより、L−乳酸連続発酵系が得られるかどうかを調べるため、表2に示す組成の乳酸発酵培地を用い、この装置の連続発酵試験を行った。該乳酸発酵培地は、121℃の温度で15分間、高圧蒸気滅菌して用いた。分離膜には、前記の参考例2で作製した多孔性膜を用いた。実施例1における運転条件は、特に断らない限り下記のとおりである。
[運転条件]
・発酵反応槽容量:1.5(L)
・膜分離槽容量:0.5(L)
・使用分離膜:PVDF濾過膜
・膜分離エレメント有効濾過面積:120平方cm
・温度調整:30(℃)
・発酵反応槽通気量:0.02(L/min)
・膜分離槽通気量:0.3(L/min)
・発酵反応槽攪拌速度:800(rpm)
・pH調整:1N NaOHによりpH5に調整
・発酵培養液循環装置による循環液量:0.1(L/min)
・膜透過水量制御:膜分離槽水頭差により流量を制御(膜間差圧として20kPa以下に制御した。)
・間欠的な濾過処理:濾過処理(9分間)−非濾過処理(1分間)の周期運転。
微生物もしくは培養細胞として前記の参考例1で造成した酵母SW−1株を用い、培地として表2に示す組成の乳酸発酵培地を用いた。生産物であるL−乳酸の濃度の評価には、前記の参考例1に示したHPLCを用い、グルコース濃度の測定には“グルコーステストワコーC”(登録商標)(和光純薬社製)を用いた。
まず、試験管中で5mlの乳酸発酵培地を用いSW−1株を一晩振とう培養した(前々々培養)。得られた培養液を新鮮な乳酸発酵培地100mlに植菌し、500ml容坂口フラスコ中で24時間、30℃の温度で振とう培養した(前々培養)。前々培養液を、図1に示した連続発酵装置の1.5Lの乳酸発酵培地に植菌し、発酵反応槽1を付属の攪拌機5によって800rpmで攪拌し、発酵反応槽1の通気量の調整、温度調整およびpH調整を行った。発酵培養液循環ポンプ11を稼働させることなく、24時間培養を行った(前培養)。前培養完了後、直ちに、発酵培養液循環ポンプ11を稼働させた。前培養時の運転条件に加え、膜分離槽2を通気し、乳酸発酵培地の連続供給を行い、連続発酵装置の発酵培養液量を2Lとなるように膜透過水量の制御を行いながら間欠的に発酵培養液を濾過・分離し連続培養することにより、連続発酵によるL−乳酸の製造を行った。連続発酵試験を行うときの膜透過水量の制御は、水頭差制御装置3により、膜間差圧が0.1〜20kPa以内となるように適宜水頭差を変化させることによって行い、かつ、間欠的な濾過処理を、9分間の濾過処理操作と1分間の非濾過処理操作を繰り返すことによって行った。適宜、濾液中の生産されたL−乳酸濃度および残存グルコース濃度を測定した。連続発酵開始から550時間の間、膜間差圧が0.1〜20kPa以内で安定してL−乳酸を発酵生産することができた。表3に、培養発酵の条件と結果を示す。
[比較例1]連続発酵によるL−乳酸の製造(その1)
実施例1の比較対照として、濾過処理を連続的に行いL−乳酸の連続発酵を行った結果、連続発酵開始後300時間で膜間差圧が20kPaを超えた。表3に、培養発酵の条件と結果を示す。
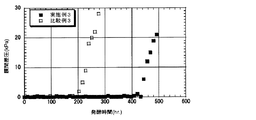
図6は、実施例1と比較例1の発酵時間と膜間差圧を比較したグラフである。この図から、本発明の化学品の製造方法により、長期間安定して化学品を製造できることが明らかになった。
[実施例2]連続発酵によるL−乳酸の製造(その2)
分離膜として参考例3で作成した多孔性膜を用い、その他は実施例1と同様にL−乳酸の連続発酵を行った。その結果、連続発酵開始から500時間の間、膜間差圧が0.1〜20kPa以内で安定してL−乳酸を発酵生産することができた。表3に、培養発酵の条件と結果を示す。
[比較例2]連続発酵によるL−乳酸の製造(その2)
実施例2の比較対照として、濾過処理を連続的に行いL−乳酸の連続発酵を行った結果、連続発酵開始後300時間で膜間差圧が20kPaを超えた。表3に、培養発酵の条件と結果を示す。
図7は、実施例2と比較例2の発酵時間と膜間差圧を比較したグラフである。この図から、本発明の化学品の製造方法により、長期間安定して化学品を製造できることが明らかになった
[実施例3]連続発酵によるL−乳酸の製造(その3)
図2に示す連続発酵装置を稼働させることにより、L−乳酸連続発酵系が得られるかどうかを調べるため、表2に示す組成の乳酸発酵培地を用い、この装置の連続発酵試験を行った。該乳酸発酵培地は、121℃の温度で15分間、高圧蒸気滅菌して用いた。分離膜には、前記の参考例1で作製した多孔性膜を用いた。実施例1における運転条件は、特に断らない限り下記のとおりである。
[運転条件]
・発酵反応槽容量:1.5(L)
・使用分離膜:PVDF濾過膜
・膜分離エレメント有効濾過面積:120平方cm
・温度調整:30(℃)
・発酵反応槽通気量:0.02(L/min)
・発酵反応槽攪拌速度:800(rpm)
・pH調整:1N NaOHによりpH5に調整
・膜透過水量制御:膜分離槽水頭差により流量を制御(膜間差圧として20kPa以下に制御した。)
・間欠的な濾過処理:濾過処理(9分間)−非濾過処理(1分間)の周期運転。
微生物として前記の参考例1で造成した酵母SW−1株を用い、培地として表1に示す組成の乳酸発酵培地を用いた。生産物であるL−乳酸の濃度の評価には、前記の参考例1に示したHPLCを用い、グルコース濃度の測定には“グルコーステストワコーC”(登録商標)(和光純薬社製)を用いた。
まず、試験管中で5mlの乳酸発酵培地を用いSW−1株を一晩振とう培養した(前々々培養)。得られた培養液を新鮮な乳酸発酵培地100mlに植菌し、500ml容坂口フラスコ中で24時間、30℃の温度で振とう培養した(前々培養)。前々培養液を、図1に示した膜分離型の連続発酵装置の1.5Lの乳酸発酵培地に植菌し、発酵反応槽1を付属の攪拌機5によって500rpmで攪拌し、発酵反応槽1の通気量の調整、温度調整およびpH調整を行った。発酵培養液循環ポンプ11を稼働させることなく、24時間培養を行った(前培養)。前培養完了後、直ちに、乳酸発酵培地の連続供給を行い、連続発酵装置の発酵培養液量を1.5Lとなるよう膜透過水量の制御を行いながら間欠的に発酵培養液を濾過・分離し連続培養することで、連続発酵によるL−乳酸の製造を行った。連続発酵試験を行うときの膜透過水量の制御は、水頭差制御装置3により、膜間差圧が0.1〜20kPa以内となるように適宜水頭差を変化させることによって行い、かつ、間欠的な濾過処理を、9分間の濾過処理操作と1分間の非濾過処理操作を繰り返すことによって行った。適宜、濾液中の生産されたL−乳酸濃度および残存グルコース濃度を測定した。連続発酵開始から480時間の間、膜間差圧が0.1〜20kPa以内で安定してL−乳酸を発酵生産することができた。表3に、培養発酵の条件と結果を示す。
[比較例3]連続発酵によるL−乳酸の製造(その3)
実施例3の比較対照として、濾過処理を連続的に行いL−乳酸の連続発酵を行った結果、連続発酵開始後250時間で膜間差圧が20kPaを超えた。表3に、培養発酵の条件と結果を示す。
図8は、実施例3と比較例3の発酵時間と膜間差圧を比較したグラフである。この図から、本発明の化学品の製造方法により、長期間安定して化学品を製造できることが明らかになった
[実施例4]連続発酵によるL−乳酸の製造(その4)
分離膜として参考例3で作成した多孔性膜を用い、その他は実施例1と同様にL−乳酸の連続発酵を行った。その結果、連続発酵開始から450時間の間、膜間差圧が0.1〜20kPa以内で安定してL−乳酸を発酵生産することができた。表3に、培養発酵の条件と結果を示す。
[比較例4]連続発酵によるL−乳酸の製造(その4)
実施例4の比較対照として、濾過処理を連続的に行いL−乳酸の連続発酵を行った結果、連続発酵開始後240時間で膜間差圧が20kPaを超えた。表3に、培養発酵の条件と結果を示す。
図9は、実施例4と比較例4の発酵時間と膜間差圧を比較したグラフである。この図から、本発明の化学品の製造方法により、長期間安定して化学品を製造できることが明らかになった。
[実施例5]連続発酵によるD−乳酸の製造(その1)
微生物としてスポロラクトバチルス・ラエボラクティカス ATCC23492株を用い、培地にグルコース80g/Lと酵母エキス3g/Lを含む乳酸発酵培地を用いて、図1の連続発酵装置でD−乳酸連続発酵を行った。該乳酸発酵培地は、121℃の温度で15分間、高圧蒸気滅菌して用いた。分離膜には、前記の参考例2で作製した多孔性膜を用いた。運転条件は下記のとおりである。
[運転条件]
・発酵反応槽容量:1.5(L)
・使用分離膜:PVDF濾過膜
・分離膜エレメント有効濾過面積:120平方cm
・温度調整:37(℃)
・発酵反応槽通気量:窒素ガス0.2(L/min)
・発酵反応槽攪拌速度:800(rpm)
・pH調整:8N Ca(OH)2によりpH6.0に調整
・膜透過水量制御:膜分離槽水頭差により流量を制御(膜間差圧として20kPa以下に制御した。)
・間欠的な濾過処理:濾過処理(9分間)−非濾過処理(1分間)の周期運転。
生産物であるD−乳酸の濃度の評価には、前記の参考例1に示したHPLCを用いた。まず、試験管中で10mlの乳酸発酵培地を用い、ATCC 23492株を嫌気条件下で一晩培養した(前々々培養)。得られた培養液を新鮮な乳酸発酵培地100mlに植菌し、嫌気条件下、500ml容坂口フラスコ中で24時間、37℃の温度で培養した(前々培養)。前々培養液を、図1に示した連続発酵装置の発酵反応槽中1の1.5Lの乳酸発酵培地に植菌し、攪拌、通気量の調整、温度調整およびpH調整を行った(前培養)。前培養開始24時間後に、乳酸発酵培地の連続供給を行い、連続発酵装置の発酵培養液量を1.5Lとなるよう膜透過水量の制御を行いながら間欠的に発酵培養液を濾過・分離し連続培養することで、連続発酵によるD−乳酸の製造を行った。連続発酵試験を行うときの膜透過水量の制御は、水頭差制御装置3により、膜間差圧が0.1〜20kPa以内となるように適宜水頭差を変化させることによって行い、かつ、間欠的な濾過処理を、9分間の濾過処理操作と1分間の非濾過処理操作を繰り返すことによって行った。適宜、濾液中の生産されたD−乳酸濃度および残存グルコース濃度を測定した。連続発酵開始から400時間の間、膜間差圧が0.1〜20kPa以内で安定してD−乳酸を発酵生産することができた。表4に、培養発酵の条件と結果を示す。
[比較例5]連続発酵によるD−乳酸の製造(その1)
実施例5の比較対照として、濾過処理を連続的に行いL−乳酸の連続発酵を行った結果、連続発酵開始後240時間で膜間差圧が20kPaを超えた。表4に、培養発酵の条件と結果を示す。
図10は、実施例5と比較例5の発酵時間と膜間差圧を比較したグラフである。この図から、本発明の化学品の製造方法により、長期間安定して化学品を製造できることが明らかになった。
[実施例6]連続発酵によるD−乳酸の製造(その2)
微生物としてスポロラクトバチルス・ラエボラクティカス ATCC 23492株を用い、培地にグルコース80g/Lと酵母エキス3g/Lを含む乳酸発酵培地を用いて、図2の連続発酵装置でD−乳酸連続発酵を行った。該乳酸発酵培地は、121℃の温度で15分間、高圧蒸気滅菌して用いた。分離膜には、前記の参考例4で作製した多孔性膜を用いた。運転条件は下記のとおりである。
[運転条件]
・発酵反応槽容量:1.5(L)
・膜分離槽容量:0.5(L)
・使用分離膜:PVDF濾過膜
・分離膜エレメント有効濾過面積:120平方cm
・温度調整:37(℃)
・発酵反応槽通気量:窒素ガス0.2(L/min)
・発酵反応槽攪拌速度:800(rpm)
・pH調整:8N Ca(OH)2によりpH6.0に調整
・培養液循環速度:100ml/min
・膜透過水量制御:膜分離槽水頭差により流量を制御(膜間差圧として20kPa以下に制御した。)
・間欠的な濾過処理:濾過処理(9分間)−非濾過処理(1分間)の周期運転。
生産物であるD−乳酸の濃度の評価には、前記の参考例1に示したHPLCを用いた。分離膜の目詰まりにより濾過液が出てこなくなる時間を測定することにより、連続発酵の安定運転の比較を行った。
まず、試験管中で10mlの乳酸発酵培地を用い、ATCC23492株を嫌気条件下で一晩培養した(前々々培養)。得られた培養液を新鮮な乳酸発酵培地100mlに植菌し、500ml容坂口フラスコで24時間、37℃で培養した(前々培養)。前々培養液を、図2に示した連続発酵装置の発酵反応槽中1の2.0LのL−乳酸発酵培地に植菌し、発酵反応槽1を付属の攪拌機5によって800rpmで攪拌し、発酵反応槽1の通気量の調整、温度調整、pH調整および培養液循環速度調整を行い、24時間培養を行った(前培養)。前培養完了後直ちに、乳酸発酵培地の連続供給を行い、連続発酵装置の発酵反応槽中1の発酵培養液量を2.0Lとなるように膜透過水量の制御を行いながら連続培養し、連続発酵によるD−乳酸の製造を行った。連続発酵試験を行うときの膜透過水量の制御は、水頭差制御装置3により、膜間差圧が0.1〜20kPa以内となるように適宜水頭差を変化させることによって行い、かつ、間欠的な濾過処理を、9分間の濾過処理操作と1分間の非濾過処理操作を繰り返すことによって行った。適宜、濾液中の生産されたD−乳酸濃度および残存グルコース濃度を測定した。連続発酵開始から400時間の間、膜間差圧が0.1〜20kPa以内で安定してD−乳酸を発酵生産することができた。表4に、培養発酵の条件と結果を示す。
[比較例6]連続発酵によるD−乳酸の製造(その2)
実施例6の比較対照として、濾過処理を連続的に行いL−乳酸の連続発酵を行った結果、連続発酵開始後230時間で膜間差圧が20kPaを超えた。表3に、培養発酵の条件と結果を示す。
図11は、実施例6と比較例6の発酵時間と膜間差圧を比較したグラフである。この図から、本発明の化学品の製造方法により、長期間安定して化学品を製造できることが明らかになった。