JP5073777B2 - 雲南苦丁茶成分を含有する組成物 - Google Patents
雲南苦丁茶成分を含有する組成物 Download PDFInfo
- Publication number
- JP5073777B2 JP5073777B2 JP2010103708A JP2010103708A JP5073777B2 JP 5073777 B2 JP5073777 B2 JP 5073777B2 JP 2010103708 A JP2010103708 A JP 2010103708A JP 2010103708 A JP2010103708 A JP 2010103708A JP 5073777 B2 JP5073777 B2 JP 5073777B2
- Authority
- JP
- Japan
- Prior art keywords
- bitter tea
- yunnan bitter
- extract
- yunnan
- tea extract
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Expired - Fee Related
Links
- 0 C[C@@](*)(C(C(C1O)OC)O)OC1OC(C(C(OCCc(cc1)ccc1O)OC1CO)O)*1OC(C=Cc(cc1)ccc1O)=O Chemical compound C[C@@](*)(C(C(C1O)OC)O)OC1OC(C(C(OCCc(cc1)ccc1O)OC1CO)O)*1OC(C=Cc(cc1)ccc1O)=O 0.000 description 1
Images
Landscapes
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Medicines Containing Plant Substances (AREA)
- Acyclic And Carbocyclic Compounds In Medicinal Compositions (AREA)
Description
中国では古くから苦丁茶と呼ばれる茶が飲用されている。苦丁茶は中国長江以南地方、雲南省等で一般に生産されて、モチノキ科(Aquifoliaceae)やモクセイ科(Oleaceae)の植物を起源とし、その葉を乾燥し蒸して茶としたものである。通常の茶と同様、葉に湯を注いで主に食後に飲用するが、その名の通り極めて強い苦みがある。原料として用いられる植物は産地によって変動があり、これまでに前記モチノキ科やモクセイ科植物を含む下記に示す5科5属10種が知られている。
(2)序梗女貞(学名:Ligustrum pedunculare Rehd.,科名:モクセイ科(Oleaceae),産地:四川)
(3)日本毛女貞(学名:L.japonicum var.pubescens Koidz.,科名:モクセイ科(Oleaceae),産地:貴州)
(4)粗壮女貞(学名:L.robustum (Roxb.) Bl.,科名:モクセイ科(Oleaceae),産地:貴州)
(5)枸骨(学名:Ilex cornuta Lindl. ex Paxt.,科名:モチノキ科(Aquifoliaceae),産地:浙江)
(6)苦丁茶冬青(学名:Ilex kudincha C.J.Tseng.,科名:モチノキ科(Aquifoliaceae),産地:広西)
(7)大葉冬青(学名:Ilex latifolia Thunb.,科名:モチノキ科(Aquifoliaceae),産地:浙江・湖南)
(8)毛葉牛黄木(学名:Cratoxylum prunifolium(Kurz)Dyer,科名:オトギリソウ科(Guttiferae),産地:広西)
(9)厚売樹(学名:Ehretia thysiflora(S.etZ.)Nakai,科名:ムラサキ科(Boraginaceae),産地:広西)
(10)石南(学名:Photinia serrulata Lindl.,科名:バラ科(Rosaceae),産地:浙江)
しかし、これまで雲南苦丁茶中の有効成分を特定し、その成分の生理活性作用に着目した利用例についての報告はない。
1.雲南苦丁茶を、水または有機溶剤単独、またはそれらの混合物で抽出処理して得られるポリフェノール成分を主要成分とする雲南苦丁茶成分含有抽出物であって、抗酸化活性及び/またはアルドース還元酵素阻害活性を有する成分を有効成分とする組成物。
2.雲南苦丁茶としてモクセイ科リグストルム(Ligustrum)属植物を使用する前項1記載の組成物。
3.モクセイ科リグストルム(Ligustrum)属植物が紫茎女貞(リグストルム・プルプラセンス;Ligustrum purpurascens Y.C.Yang)である前項2記載の組成物。
4.生活習慣病の治療及び/または予防用の医薬組成物である前項1乃至3のいずれかに記載の組成物。
5.生体に対する過酸化脂質抑制、コレステロール低下、中性脂質低下、高脂血症改善、糖尿病改善、学習機能改善、脳機能改善、または痴呆症予防の作用を有する前項4記載の医薬品組成物。
6.生活習慣病が、糖尿病及びその合併症である前項5記載の医薬品組成物。
7.生活習慣病の改善及び/また予防用の健康食品組成物である前項1乃至3のいずれかに記載の組成物。
8.生体に対する過酸化脂質抑制、コレステロール低下、中性脂質低下、高脂血症改善、糖尿病改善、学習機能改善、脳機能改善、または痴呆症予防の作用を有する前項7記載の健康食品組成物。
9.生活習慣病が、糖尿病及びその合併症である前項8記載の健康食品組成物。
本発明における雲南苦丁茶成分含有抽出物は、雲南苦丁茶を水または有機溶媒単独、またはこれらの混合物で抽出し、ろ過、濃縮等の処理を経て得られたエキス(抽出物)、またはこれを吸着、分離、溶出などの処理をしたものである。
抽出は通常、常圧または加圧下で常温ないし60℃程度で1〜3時間行われるが、必要により抽出温度を70〜90℃に上げてもよく、抽出時間も1時間以下の短時間、あるいは3時間以上で行ってもよい。抽出処理後、ろ過あるいは遠心分離等の適宜の手段で抽出液を回収し、必要により溶媒除去、エキス分の濃縮、乾燥、粉末化等の処理を行う。
従って本発明の組成物は医薬組成物及び健康食品組成物として利用することができる。
健康食品組成物としては、いわゆる生活習慣病、例えば高コレステロール血症、高脂血症、動脈硬化症、虚血性心疾患その他の心疾患及び各種臓器障害、各種脳疾患例えば脳卒中、痴呆症、アルツハイマー症、脳梗塞、脳血管障害、記憶障害等の予防・改善等の健康維持の効果が期待される。
本発明の組成物は、経口または非経口で用いられるが、経口的に使用される場合の投与量は、年齢、体重、症状、目的とする治療あるいは改善効果、投与方法等により異なるが、通常、成人一人当たり、一回につき、100から2000mgの範囲である。本発明組成物を投与する際には、経口投与として一般に錠剤、丸剤、カプセル剤、散剤、顆粒剤、シロップ剤等として用いられる。造粒、錠剤化あるいはシロップ剤とする際に、必要により適宜の補助資材(澱粉類、デキストリン、甘味剤類、色素、香料等)を使用することもできる。
(1-1) 雲南苦丁茶エキスの抽出
雲南苦丁茶は中国雲南省産の「雲南苦丁茶(Ligustrum purpurascens Y.C.Yang.)」の乾燥葉を粉砕し、その100kgについて60℃の温水1500Lで60分間の抽出を行い、不溶物を遠心分離し抽出液とした。抽出液を減圧濃縮し凍結乾燥粉末として雲南苦丁茶エキスとした。
得られた抽出液の性状は以下の通り:
pH5.2、Brix 2.4、比重1.006、固形分1.85%(上記製造例で27.75kg)、ポリフェノール濃度25.6%(固形分当たり)。
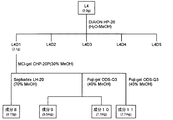
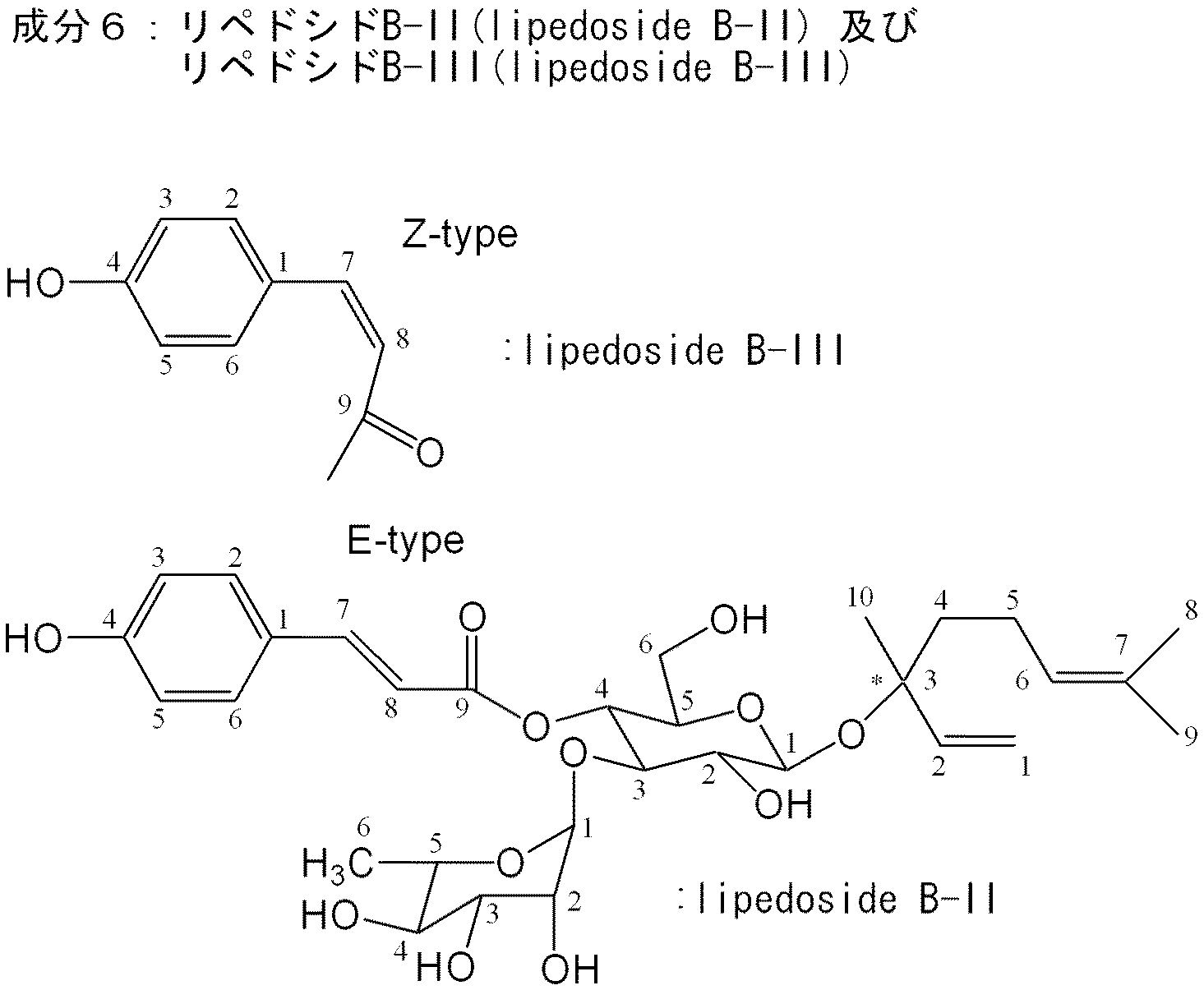
上記雲南苦丁茶エキス20gについて、分画精製操作を行った。分画精製操作の概要のフローを図1及び図2に示す。図1及び2中の分画精製物である、コーヒー酸(caffeic acid)、p−クマル酸(p-coumaric acid)及び精製成分1〜10の構造を以下に示す。
(1-1)背景
蛍光性のタンパク質であるアロフィコシアニン(allophycocyanin)はフリーラジカルによる攻撃を受けると蛍光性を失う。この性質を利用してアロフィコシアニンをフリーラジカル発生物質と試験物質の共存下でインキュベートし蛍光を測定しフリーラジカルの除去作用を調べた。
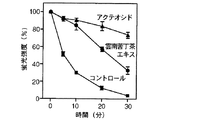
75mMリン酸バッファー(pH7.0)に37.5nM アロフィコシアニンを加えて3mM 2,2’−アゾビス(2−アミノプロパン)ジヒドロクロリド)(AAPH)をフリーラジカル発生試薬として加え、試験試料として雲南苦丁茶エキス、アクテオシド(acteoside)、及びイオン交換水をそれぞれ1μg/mL加えて37℃で反応させ、反応開始から0、5、10、20、30分後のEm 651nm、Ex598nmにおける蛍光強度を測定した。
図3に示すように雲南苦丁茶エキスは強いラジカル消去作用を示し、雲南苦丁茶エキスに含まれる成分であるアクテオシドにも強い活性が認められた。
(2-1)背景
ストレプトゾトシンは酸化剤として臓器に作用して様々な障害を起こす。特に膵臓を障害することで動物は糖尿病の容態を呈するので、ストレプトゾトシン投与動物は糖尿病のモデル動物として用いられる。腎臓を3/4摘出後にストレプトゾトシンを低容量投与することにより糖尿病性腎症モデルを作成することができる。
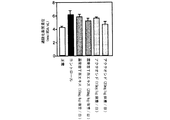
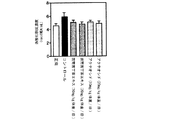
糖尿病の動物モデルは、雄性ウィスターラットの左腎を半分摘出し、1週間術後の回復を待って右腎を全摘出し、3/4腎摘状態にする。さらに1週間術後の回復を待ってストレプトゾトシンを25mg/kg体重、腹腔内投与し4週間後に血糖値(Serum Glucose)、血清中過酸化脂質(Serum MDA)、肝臓ミトコンドリア中過酸化脂質(Liver mitochondria MDA)及び腎臓ミトコンドリア中過酸化脂質濃度(Kidney mitochondria MDA)を測定した。雲南苦丁茶エキス(100mg/kg体重/日及び200mg/kg体重/日)、アクテオシド(100mg/kg体重/日及び200mg/kg体重/日)を経口投与し、コントロールには蒸留水を投与した。
図4に示すように血糖値は雲南苦丁茶群で低下傾向でありアクテオシド投与群ではコントロール群に対して有意に血糖値が低下した。図5〜7に示すようにストレプトゾトシンによる臓器の酸化障害を示す過酸化脂質濃度では雲南苦丁茶エキス及びアクテオシドの200mg/kg体重/日の高用量投与群でコントロール群にくらべ有意に低い値を示し、酸化障害による臓器障害が抑えられることが示された。
(3-1)背景
アルドース還元酵素(aldose reductase)は水晶体、網膜、末梢神経、腎臓及び血管といった糖尿病の合併症が出現する種々の組織に存在し、病体発症において重要な役割を演じている。通常、グルコースはヘキソキナーゼにより解糖系へと代謝されるが、糖尿病時にはアルドース還元酵素活性が亢進しポリオール経路での代謝が促進される。その際に産生されるD−ソルビトールやフルクトースは比較的安定であるため、細胞内に蓄積し、浸透圧上昇、水分貯留を招き細胞障害を引き起こす。
糖尿病の発症にはアルドース還元酵素を介した機構が関与していると考えられており、アルドース還元酵素阻害剤は糖尿病の治療薬としての開発も行われている。
豚の目から水晶体を取出し、PBS(phosphate buffered saline)で洗浄した。水晶体一つに対し1mLのイオン交換水を加えて氷冷下でホモジナイズし、11000×gで20分間遠心分離し上清を得た。得られた上清に40%飽和になるように硫酸アンモニウムを加え、よく撹拌し、4℃で30分間静置して不溶物を沈澱させた。4℃で11000×gで20分間遠心分離し、上清を0.05M NaClで透析した。透析後の溶液を、アルドース還元酵素溶液(タンパク質量を測定しておいた)とした。
雲南苦丁茶エキスの分画物について同様な試験を行った。雲南苦丁茶エキス及びその分画物、それぞれ10μg/mLによるアルドース還元酵素活性抑制率及びIC50を雲南苦丁茶エキス粉末20g中の各成分の分画収量と共に表1に示す。
雲南苦丁茶エキスのアルドース還元酵素阻害におけるIC50は8.4μg/mLであり、低い濃度でアルドース還元酵素を阻害する作用があることが分かった。
この結果から雲南苦丁茶エキスには強いアルドース還元酵素阻害活性があり、その活性はアクテオシド及びその類縁体において強いことが分かった。その含有量比から考えて雲南苦丁茶におけるアルドース還元酵素阻害活性はアクテオシド及びその類縁体のみによるものではなくその他の未知の成分による相乗作用であることが明らかとなった。
(4-1)背景
雲南苦丁茶エキスより分画して得られた物質の構造活性相関を得るために、1,1−ジフェニル−2−ピクリルヒドラジル(1,1-diphenyl-2-picrylhydrazyl)(DPPH)ラジカルの消去作用を測定した。
96穴のマイクロプレートに100μLのDPPH溶液(60μMエタノール溶液)を入れ、試験試料のエタノール溶液100μLまたはコントロールとしてエタノールを100μLそれぞれ加え、静かに混合し室温で30分間放置した後、520nmの吸光度を測定した。抑制率を下記の式で算出し、段階的に希釈した試験試料の抑制率と濃度から50%阻害濃度(IC50)を算出した。
実験結果を表2に示す。
粉末にした雲南苦丁茶を熱水または温水で抽出し、不要物を除去してエキスを得る。エキスは通常行われる方法で粉末化することができ、必要に応じて賦形剤や添加物を添加しても良い。エキスをカラムクロマトグラフィーにより分画し効果試験に供することによりその中のコーヒー酸、コーヒー酸誘導体、アクテオシド及びそれらの類縁体が有効成分の一部であることが判明した。しかし、それらの活性の総和はエキスそのものの活性を表わしていないことから、それら成分の混在による相乗作用あるいは未知の有効性分の存在の可能性が示唆された。
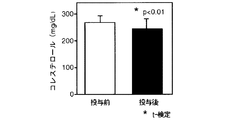
予め血液の採取を行ったボランティア21名(男性12名、女性9名)に対して、上記抽出エキス250mg入りカプセルを8カプセル/日(2.0g/日)(無水物換算)を14日間経口投与した。投与開始から15日目に血液を採取し、抽出エキス投与前の血液と投与後の血液について、過酸化脂質量、SOD(スーパーオキシドディスムターゼ)活性、コレステロール量及び中性脂肪量を測定した。
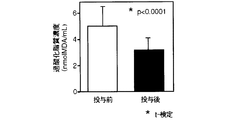
雲南苦丁茶抽出エキス投与前後の過酸化脂質量の測定結果(nmolMDA/ml)を図8に示す。
図8から明らかなように、雲南苦丁茶抽出エキスを投与することにより抽出エキス投与前に比較し過酸化脂質量の生成が抑制された。
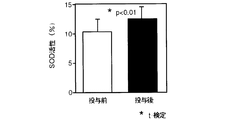
雲南苦丁茶抽出エキス投与前後のSOD活性の測定結果(%)を図9に示す。
図9から明らかなように、雲南苦丁茶抽出エキスを投与することにより抽出エキス投与前に比較しSOD活性が上昇した。
(6-1)背景
痴呆の原因ともなる脳血管性障害の予防及び治療の目的で、in vitroの脳虚血モデルを用いて雲南苦丁茶エキスの抗酸化ストレス作用を検討した。ラット海馬初代培養細胞にグルタミン酸、AMPA受容体作用薬であるカイニン酸、ラジカル誘発剤である過酸化水素、アルツハイマー病の原因物質であるβアミロイドを用い、これらによる神経細胞毒性に対する雲南苦丁茶エキスの保護作用を調べた。
ウィスター系雌性ラット(胎児17日齢)から摘出した海馬より神経細胞を取出し、無血清培地で7日間、96穴のプレートにて2.5×105細胞/穴の密度で培養し、これを海馬初代培養細胞として実験に供した。グルタミン酸、カイニン酸、過酸化水素及びβアミロイドにより誘発される細胞毒性を培養液中のLDH(乳酸脱水素酵素)を和光純薬社製の測定キット(LDH-Cytotoxic Test Wako)を用いて560nmの吸光度により測定し、細胞障害の指標とした。細胞障害率は下記の式により算出した。
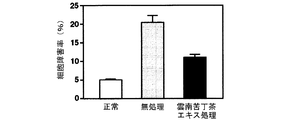
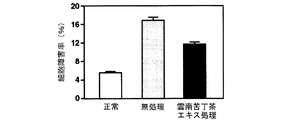
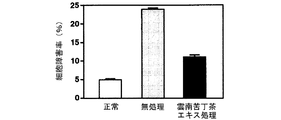
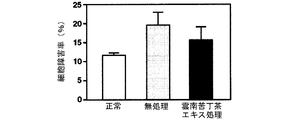
海馬初代培養細胞に対するグルタミン酸毒性、カイニン酸毒性、βアミロイド毒性及び過酸化水素毒性による細胞障害率及びその細胞障害率に及ぼす雲南苦丁茶エキスの影響を調べた結果を図12(グルタミン酸毒性)、図13(カイニン酸毒性)、図14(βアミロイド毒性)及び図15(過酸化水素毒性)に示す。
雲南苦丁茶エキスは海馬初代培養細胞におけるグルタミン酸、カイニン酸、βアミロイド及び過酸化水素による細胞障害を抑制した。このことから雲南苦丁茶エキスにはラジカルの消去による脳細胞の保護効果があることが明らかとなり、酸化ストレスによる脳細胞の障害、痴呆の予防・治療に効果があることが示された。
(7-1)背景
試験例7と同様の目的で、in vivoの脳虚血モデルを用いて雲南苦丁茶エキスの抗酸化ストレス作用を検討した。学習・記憶障害を誘発させることが知られている抗コリン剤であるスコポラミンを用いて、スコポラミンによる空間認知記憶障害ラットモデルにおける雲南苦丁茶エキスの効果について調べた。
食餌制限下のウィスター系雄性ラット(7週齢、体重200−250g)を八方放射状迷路(アーム長48cm、幅10cm、地上高40cm)の中央に置き、アーム先端部分に置いた餌を効率良く摂取できるようになるまで訓練を行い、ラットが初めて訪れたアームの選択数(正選択数)、二回以上訪れたアームの選択数(誤選択数)及び試行終了までの走行時間を最大10分まで測定した。初期選択数7以上で誤選択数が1以下の成績を3試行以上連続して示すように訓練されたラットを空間認知記憶が完成したラットとした。空間認知記憶が完成したラットにスコポラミン(0.5mg/kg体重)を腹腔内投与し、その30分後に発現する空間認知記憶障害に対する雲南苦丁茶エキスの効果を調べた。雲南苦丁茶エキス(100mg/kg体重)は試行60分前に経口投与した。
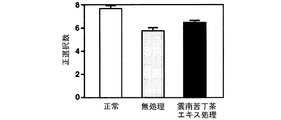
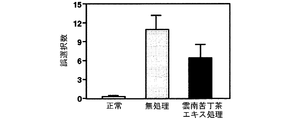
スコポラミンにより誘発される八方放射状迷路における空間認知障害に対する雲南苦丁茶エキスの効果を図16(正選択数)及び図17(誤選択数)に示す。
雲南苦丁茶エキスはスコポラミンにより空間認知障害を誘発されたラットを八方放射状迷路に試行した際の正選択数を増加させ、誤選択数を減少させた。このことから、雲南苦丁茶エキスには学習・記憶能力改善効果があることが示された。
(8-1)実験方法
ナイロン糸の先端を加工した塞栓(約11mm)をddY系マウス(5週齢、体重20−25g)の左内頸動脈内に4時間挿入した。挿入1週間後に、大脳皮質を含む脳の前額断スライスを作成し、TTC(トリフェニルテトラゾリウムクロリド)染色により梗塞巣の体積を測定した。雲南苦丁茶エキス(100mg/kg体重)は2週間経口投与した。
実験結果を表3に示す。
Claims (2)
- 紫茎女貞(リグストルム・プルプラセンス;Ligustrum purpurascens Y.C.Yang)の葉を、水または有機溶剤単独、またはそれらの混合物で抽出処理して得られるポリフェノール成分を主要成分とする抽出物であって、抗酸化活性及び/またはアルドース還元酵素阻害活性を有する成分を有効成分とする脳機能改善組成物。
- 学習機能、脳卒中、痴呆症、アルツハイマー症、脳梗塞、脳血管障害または記憶障害の改善用である請求項1に記載の脳機能改善組成物。
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2010103708A JP5073777B2 (ja) | 2010-04-28 | 2010-04-28 | 雲南苦丁茶成分を含有する組成物 |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2010103708A JP5073777B2 (ja) | 2010-04-28 | 2010-04-28 | 雲南苦丁茶成分を含有する組成物 |
Related Parent Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2003110234A Division JP4544503B2 (ja) | 2003-04-15 | 2003-04-15 | 雲南苦丁茶成分を含有する組成物 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2010163460A JP2010163460A (ja) | 2010-07-29 |
| JP5073777B2 true JP5073777B2 (ja) | 2012-11-14 |
Family
ID=42579897
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2010103708A Expired - Fee Related JP5073777B2 (ja) | 2010-04-28 | 2010-04-28 | 雲南苦丁茶成分を含有する組成物 |
Country Status (1)
| Country | Link |
|---|---|
| JP (1) | JP5073777B2 (ja) |
Families Citing this family (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2014141437A (ja) * | 2013-01-24 | 2014-08-07 | Oriza Yuka Kk | 学習記憶改善剤 |
| US20200113854A1 (en) | 2017-05-30 | 2020-04-16 | Morinaga Milk Industry Co., Ltd. | Composition for Improving Brain Function |
Family Cites Families (7)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP3183754B2 (ja) * | 1993-07-20 | 2001-07-09 | ポーラ化成工業株式会社 | 動脈硬化抑制剤及びこれを含有する組成物 |
| JPH0977676A (ja) * | 1995-09-14 | 1997-03-25 | Pola Chem Ind Inc | アシルコエンザイムaコレステロールアシルトランスフェラーゼ活性阻害剤及びそれを配合した組成物 |
| JPH0977678A (ja) * | 1995-09-14 | 1997-03-25 | Pola Chem Ind Inc | フォスファチジルコリンステロールアシルトランスフェラーゼ活性促進剤及びそれを含有する組成物 |
| JP4071835B2 (ja) * | 1995-09-18 | 2008-04-02 | ポーラ化成工業株式会社 | アシルコエンザイムaコレステロールアシルトランスフェラーゼ活性阻害剤及びそれを配合した組成物 |
| JP3839082B2 (ja) * | 1995-10-11 | 2006-11-01 | ポーラ化成工業株式会社 | 新規テルペノイド化合物 |
| JP4001395B2 (ja) * | 1995-10-11 | 2007-10-31 | ポーラ化成工業株式会社 | コレステロールアシルトランスフェラーゼ活性阻害剤及び組成物 |
| CN102670453A (zh) * | 2001-10-09 | 2012-09-19 | 株式会社芳凯尔 | 一种组合物a在制备美白用组合物中的应用 |
-
2010
- 2010-04-28 JP JP2010103708A patent/JP5073777B2/ja not_active Expired - Fee Related
Also Published As
| Publication number | Publication date |
|---|---|
| JP2010163460A (ja) | 2010-07-29 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| Mohagheghi et al. | The neuroprotective effect of olive leaf extract is related to improved blood–brain barrier permeability and brain edema in rat with experimental focal cerebral ischemia | |
| CN102274244B (zh) | 一种肉桂多酚提取物、其制备方法及其用途 | |
| WO2019155337A1 (en) | Compositions comprising a cannabinoid and punicalagin and methods of use thereof | |
| Asanka Sanjeewa et al. | Exploiting biological activities of brown seaweed Ishige okamurae Yendo for potential industrial applications: A review | |
| JP7652789B2 (ja) | アベナンスラミドおよびβ-グルカンを含む組成物またはエンバク抽出物 | |
| JP4544503B2 (ja) | 雲南苦丁茶成分を含有する組成物 | |
| CN100382798C (zh) | 一种含有咖啡酰奎宁酸的药物组合物 | |
| WO2009093255A2 (en) | A new nutraceutical composition from garcinia mangostana | |
| CN101637492B (zh) | 柿叶总黄酮的制备方法 | |
| HK1210597A1 (en) | Novel extracts of cynara scolymus, coffea spp. and olea europaea for the treatment of metabolic syndrome | |
| CN100420440C (zh) | 抗变态反应剂、含有它的药品、食品或化妆品及它们的制备方法 | |
| JP5751981B2 (ja) | 新規フェニルエタノイド配糖体及び皮膚化粧料 | |
| KR101384423B1 (ko) | 자소엽 추출물을 포함하는 뇌신경질환 예방 또는 치료용 의약 조성물 | |
| KR101965061B1 (ko) | 땅콩 새싹 추출물 또는 이의 분획물을 포함하는 대사성 질환의 예방 또는 치료용 조성물 | |
| US11141449B2 (en) | Method of extracting flavonoids and/or polyphenols from dried and powdered citrus peels, compositions therefrom, and methods of treatment of diseases associated with chronic inflammation | |
| CN106798762A (zh) | 一种植物提取物及其制备方法和应用 | |
| JP7303582B2 (ja) | インディアングーズベリー抽出物と大麦若葉抽出物との複合物(ib複合物)を有効成分として含む肥満及び/または糖尿を伴うメタボリックシンドロームの予防、改善治療用組成物 | |
| TWI708609B (zh) | 用於預防改善或治療身心俱疲症候群之組合物 | |
| KR102566546B1 (ko) | 실리빈 함유 약학 조성물 | |
| KR101330411B1 (ko) | 증숙 처리된 녹차 추출물을 유효성분으로 함유하는 아토피 피부염 개선용 조성물 | |
| JP5073777B2 (ja) | 雲南苦丁茶成分を含有する組成物 | |
| KR102588130B1 (ko) | 쑥 및 삼백초 혼합 추출물을 포함하는 미세먼지로 인한 염증성 호흡기 질환 예방 또는 치료용 조성물 | |
| CN102091088A (zh) | 米邦塔仙人掌多糖在防治慢性神经退行性疾病中的应用 | |
| US20160375076A1 (en) | Herbal Combinations for Treating Eczema | |
| CN100571708C (zh) | 一种具有协同作用的药物组合物 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20100428 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20120821 |
|
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20120822 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 5073777 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20150831 Year of fee payment: 3 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| S533 | Written request for registration of change of name |
Free format text: JAPANESE INTERMEDIATE CODE: R313533 |
|
| R350 | Written notification of registration of transfer |
Free format text: JAPANESE INTERMEDIATE CODE: R350 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| LAPS | Cancellation because of no payment of annual fees |