JP2023516632A - 多能性幹細胞からナチュラルキラー細胞を産生するための方法 - Google Patents
多能性幹細胞からナチュラルキラー細胞を産生するための方法 Download PDFInfo
- Publication number
- JP2023516632A JP2023516632A JP2022552125A JP2022552125A JP2023516632A JP 2023516632 A JP2023516632 A JP 2023516632A JP 2022552125 A JP2022552125 A JP 2022552125A JP 2022552125 A JP2022552125 A JP 2022552125A JP 2023516632 A JP2023516632 A JP 2023516632A
- Authority
- JP
- Japan
- Prior art keywords
- cells
- cell
- concentration
- bulk
- induction medium
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Granted
Links
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N5/00—Undifferentiated human, animal or plant cells, e.g. cell lines; Tissues; Cultivation or maintenance thereof; Culture media therefor
- C12N5/06—Animal cells or tissues; Human cells or tissues
- C12N5/0602—Vertebrate cells
- C12N5/0634—Cells from the blood or the immune system
- C12N5/0647—Haematopoietic stem cells; Uncommitted or multipotent progenitors
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N5/00—Undifferentiated human, animal or plant cells, e.g. cell lines; Tissues; Cultivation or maintenance thereof; Culture media therefor
- C12N5/06—Animal cells or tissues; Human cells or tissues
- C12N5/0602—Vertebrate cells
- C12N5/0634—Cells from the blood or the immune system
- C12N5/0646—Natural killers cells [NK], NKT cells
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K40/00—Cellular immunotherapy
- A61K40/10—Cellular immunotherapy characterised by the cell type used
- A61K40/15—Natural-killer [NK] cells; Natural-killer T [NKT] cells
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K40/00—Cellular immunotherapy
- A61K40/30—Cellular immunotherapy characterised by the recombinant expression of specific molecules in the cells of the immune system
- A61K40/31—Chimeric antigen receptors [CAR]
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K40/00—Cellular immunotherapy
- A61K40/30—Cellular immunotherapy characterised by the recombinant expression of specific molecules in the cells of the immune system
- A61K40/35—Cytokines
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K40/00—Cellular immunotherapy
- A61K40/40—Cellular immunotherapy characterised by antigens that are targeted or presented by cells of the immune system
- A61K40/41—Vertebrate antigens
- A61K40/42—Cancer antigens
- A61K40/4202—Receptors, cell surface antigens or cell surface determinants
- A61K40/421—Immunoglobulin superfamily
- A61K40/4211—CD19 or B4
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P37/00—Drugs for immunological or allergic disorders
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K14/00—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- C07K14/435—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
- C07K14/52—Cytokines; Lymphokines; Interferons
- C07K14/54—Interleukins [IL]
- C07K14/5443—IL-15
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K14/00—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- C07K14/435—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
- C07K14/705—Receptors; Cell surface antigens; Cell surface determinants
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K14/00—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- C07K14/435—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
- C07K14/705—Receptors; Cell surface antigens; Cell surface determinants
- C07K14/70503—Immunoglobulin superfamily
- C07K14/7051—T-cell receptor (TcR)-CD3 complex
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K14/00—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- C07K14/435—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
- C07K14/705—Receptors; Cell surface antigens; Cell surface determinants
- C07K14/70503—Immunoglobulin superfamily
- C07K14/70517—CD8
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K14/00—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- C07K14/435—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
- C07K14/705—Receptors; Cell surface antigens; Cell surface determinants
- C07K14/70578—NGF-receptor/TNF-receptor superfamily, e.g. CD27, CD30, CD40, CD95
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K14/00—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- C07K14/435—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
- C07K14/705—Receptors; Cell surface antigens; Cell surface determinants
- C07K14/715—Receptors; Cell surface antigens; Cell surface determinants for cytokines; for lymphokines; for interferons
- C07K14/7155—Receptors; Cell surface antigens; Cell surface determinants for cytokines; for lymphokines; for interferons for interleukins [IL]
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies
- C07K16/18—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies against material from animals or humans
- C07K16/28—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants
- C07K16/2803—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants against the immunoglobulin superfamily
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K2121/00—Preparations for use in therapy
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K2239/00—Indexing codes associated with cellular immunotherapy of group A61K40/00
- A61K2239/31—Indexing codes associated with cellular immunotherapy of group A61K40/00 characterized by the route of administration
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K2239/00—Indexing codes associated with cellular immunotherapy of group A61K40/00
- A61K2239/38—Indexing codes associated with cellular immunotherapy of group A61K40/00 characterised by the dose, timing or administration schedule
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K2239/00—Indexing codes associated with cellular immunotherapy of group A61K40/00
- A61K2239/46—Indexing codes associated with cellular immunotherapy of group A61K40/00 characterised by the cancer treated
- A61K2239/48—Blood cells, e.g. leukemia or lymphoma
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K2300/00—Mixtures or combinations of active ingredients, wherein at least one active ingredient is fully defined in groups A61K31/00 - A61K41/00
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2319/00—Fusion polypeptide
- C07K2319/01—Fusion polypeptide containing a localisation/targetting motif
- C07K2319/03—Fusion polypeptide containing a localisation/targetting motif containing a transmembrane segment
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2500/00—Specific components of cell culture medium
- C12N2500/02—Atmosphere, e.g. low oxygen conditions
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2500/00—Specific components of cell culture medium
- C12N2500/30—Organic components
- C12N2500/38—Vitamins
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2501/00—Active agents used in cell culture processes, e.g. differentation
- C12N2501/10—Growth factors
- C12N2501/115—Basic fibroblast growth factor (bFGF, FGF-2)
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2501/00—Active agents used in cell culture processes, e.g. differentation
- C12N2501/10—Growth factors
- C12N2501/125—Stem cell factor [SCF], c-kit ligand [KL]
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2501/00—Active agents used in cell culture processes, e.g. differentation
- C12N2501/10—Growth factors
- C12N2501/145—Thrombopoietin [TPO]
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2501/00—Active agents used in cell culture processes, e.g. differentation
- C12N2501/10—Growth factors
- C12N2501/15—Transforming growth factor beta (TGF-β)
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2501/00—Active agents used in cell culture processes, e.g. differentation
- C12N2501/10—Growth factors
- C12N2501/155—Bone morphogenic proteins [BMP]; Osteogenins; Osteogenic factor; Bone inducing factor
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2501/00—Active agents used in cell culture processes, e.g. differentation
- C12N2501/10—Growth factors
- C12N2501/165—Vascular endothelial growth factor [VEGF]
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2501/00—Active agents used in cell culture processes, e.g. differentation
- C12N2501/20—Cytokines; Chemokines
- C12N2501/23—Interleukins [IL]
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2501/00—Active agents used in cell culture processes, e.g. differentation
- C12N2501/20—Cytokines; Chemokines
- C12N2501/23—Interleukins [IL]
- C12N2501/2302—Interleukin-2 (IL-2)
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2501/00—Active agents used in cell culture processes, e.g. differentation
- C12N2501/20—Cytokines; Chemokines
- C12N2501/23—Interleukins [IL]
- C12N2501/2307—Interleukin-7 (IL-7)
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2501/00—Active agents used in cell culture processes, e.g. differentation
- C12N2501/20—Cytokines; Chemokines
- C12N2501/26—Flt-3 ligand (CD135L, flk-2 ligand)
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2501/00—Active agents used in cell culture processes, e.g. differentation
- C12N2501/50—Cell markers; Cell surface determinants
- C12N2501/515—CD3, T-cell receptor complex
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2501/00—Active agents used in cell culture processes, e.g. differentation
- C12N2501/998—Proteins not provided for elsewhere
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2501/00—Active agents used in cell culture processes, e.g. differentation
- C12N2501/999—Small molecules not provided for elsewhere
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2506/00—Differentiation of animal cells from one lineage to another; Differentiation of pluripotent cells
- C12N2506/45—Differentiation of animal cells from one lineage to another; Differentiation of pluripotent cells from artificially induced pluripotent stem cells
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2510/00—Genetically modified cells
Landscapes
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- General Health & Medical Sciences (AREA)
- Immunology (AREA)
- Genetics & Genomics (AREA)
- Zoology (AREA)
- Engineering & Computer Science (AREA)
- Biochemistry (AREA)
- Medicinal Chemistry (AREA)
- Biomedical Technology (AREA)
- Public Health (AREA)
- Veterinary Medicine (AREA)
- Animal Behavior & Ethology (AREA)
- Cell Biology (AREA)
- Biophysics (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Molecular Biology (AREA)
- Toxicology (AREA)
- Gastroenterology & Hepatology (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Biotechnology (AREA)
- Wood Science & Technology (AREA)
- Epidemiology (AREA)
- Hematology (AREA)
- General Engineering & Computer Science (AREA)
- Microbiology (AREA)
- Pharmacology & Pharmacy (AREA)
- Chemical Kinetics & Catalysis (AREA)
- General Chemical & Material Sciences (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Developmental Biology & Embryology (AREA)
- Oncology (AREA)
- Communicable Diseases (AREA)
- Micro-Organisms Or Cultivation Processes Thereof (AREA)
- Medicines Containing Material From Animals Or Micro-Organisms (AREA)
- Measuring Or Testing Involving Enzymes Or Micro-Organisms (AREA)
- Peptides Or Proteins (AREA)
- Virology (AREA)
Abstract
Description
本出願は、2021年2月28日に出願された米国仮出願番号62/983,511の優先権を主張し、その開示は参照により本明細書に組み込まれる。
ナチュラルキラー(NK)細胞は、免疫系の細胞傷害性リンパ球である。NK細胞は、がん細胞、病原体感染細胞、その他の損傷を受けた細胞に対して細胞傷害性である。NK細胞は、自然リンパ球(ILC)であり、特に免疫応答の自然アームと適応アームとを架橋する細胞傷害性の大型顆粒リンパ球である。それらは、末梢血中の循環リンパ球の10~15%を構成する。NK細胞はまた、免疫系内で最高レベルの細胞傷害性活性を呈する。したがって、NK細胞の機能及び数の変化は、感染及びがんに対する免疫系の機能に影響を与える。
いくつかの実施形態では、ステップ(A)は、約10日間継続する。別の実施形態では、ステップ(A)は、約10~18日間継続する。
定義
投与:本明細書で使用される場合、「投与する」、「投与すること」、「投与」、「導入すること」または「導入」という用語は、治療用細胞、例えば、iPSCまたはHPC由来CD56+/CD3-免疫細胞を、このような細胞の送達をもたらす方法または経路によって対象に送達する文脈において、互換的に使用される。例えば、静脈内、局所、経口、筋肉内、腹腔内、髄腔内、皮下または経皮など、細胞を投与するための様々な方法が当技術分野で知られている。細胞は、担体の有無にかかわらず投与させ得る。
いくつかの実施形態では、NK細胞またはiPS由来NK細胞を産生する方法が提供され、この方法では、単離ステップを必要としない。
本明細書で提供される方法は、いかなる単離ステップも介在させずに、CD56+/CD3-細胞の産生が可能である。いくつかの実施形態では、本方法は、造血細胞(HPC)(HP細胞バルク)を含む細胞の集団を得るために、HPC誘導培地において、iPSCなどの多能性幹細胞を培養することを含む。HP細胞バルク集団は、その後、CD4/CD8二重陽性細胞を含む細胞集団を得るために、単離ステップを実施することなく、CD4/CD8誘導培地において培養される。いくつかの実施形態では、CD4/CD8二重陽性細胞を含む細胞集団はまた、CD4+/CD8-細胞、CD4-/CD8-細胞、及びCD4-/CD8+細胞を含む。その後、培養期間において、CD56+/CD3-免疫細胞が豊富な集団を得るために、単離ステップを実施することなく、細胞をNK誘導培地で培養する。したがって、いくつかの実施形態では、CD56+/CD3-細胞を産生する方法は、1)造血細胞を含む集団(HP細胞バルク)を得るために、HPC誘導培地で多能性細胞を培養することと;2)CD4+/CD8-細胞、CD4-/CD8-細胞、及びCD4-/CD8+細胞を含む細胞の集団を得るためのCD4/CD8誘導培地において、HP細胞バルクを培養することと;及び3)一定期間、NK誘導において、CD4+/CD8-細胞、CD4-/CD8-細胞、及びCD4-/CD8+細胞を含む細胞の集団を培養して、CD56+/CD3-細胞を得ることと、を含む。
いくつかの実施形態では、iPSCなどの多能性細胞をHPC誘導培地で培養して、HP細胞バルクを含む集団を産生する。いくつかの実施形態では、HPC細胞バルクを得るためにHPC誘導培地においてiPSCを培養することは、HPC誘導培地においてiPSCを培養することを含む。HPC誘導培地は、HP細胞バルクの生産が可能になる様々な成分を含むことができる。いくつかの実施形態では、HPC誘導培地は、骨形成タンパク質-4(BMP4)、血管内皮成長因子(VEGF)、塩基性線維芽細胞成長因子(bFGF)、アスコルビン酸、ROCK阻害剤、GSK3阻害剤、幹細胞因子(SCF)、トロンボポエチン(TPO)、Flt3L、及びTGFβ阻害剤から選択される少なくとも1つ以上の化合物を含む。したがって、いくつかの実施形態では、iPSCからHPCを誘導するためのHPC誘導培地は、BMP4を含む。いくつかの実施形態では、iPSCからHPCを誘導するための培養培地は、VEGFを含む。いくつかの実施形態では、iPSCからHPCを誘導するための培養培地は、bFGFを含む。いくつかの実施形態では、iPSCからHPCを誘導するための培養培地は、TGFβを含む。
いくつかの実施形態では、HPC細胞バルク、または他の方法で得られたHPC、例えば、ヒトドナーから単離された一次HPCまたは胚性幹細胞由来など他の幹細胞源/種から分化したHPCは、培地中で任意の単離ステップを介在させることなくさらに培養し、CD4/CD8二重陽性(DP)細胞を含む細胞の集団を得る。いくつかの実施形態では、HPC細胞バルク、または他の方法で得られたHPC、例えば、ヒトドナーから単離された一次HPCまたは胚性幹細胞由来など他の幹細胞源/種から分化したHPCは、培地中で任意の単離ステップを介在させることなくさらに培養し、CD4+/CD8細胞を含む細胞集団を得る。いくつかの実施形態では、HPC細胞バルク、または他の方法で得られたHPC、例えば、ヒトドナーから単離された一次HPCまたは胚性幹細胞由来など他の幹細胞源/種から分化したHPCは、培地中で任意の単離ステップを介在させることなくさらに培養し、CD4-/CD8-細胞を含む細胞集団を得る。いくつかの実施形態では、HPC細胞バルク、または他の方法で得られたHPC、例えば、ヒトドナーから単離された一次HPCまたは胚性幹細胞由来など他の幹細胞源/型から分化したHPCは、培地中で任意の単離ステップを介在させることなくさらに培養し、CD4-/CD8+細胞を含む細胞集団を得る。この方法によって得られる細胞集団としては、CD4-/CD8-細胞、CD4-/CD8+細胞、CD4+/CD8+細胞、及びCD4+/CD8-細胞が含まれることを理解されたい。細胞集団には、例えば、リンパ球が含まれる。いくつかの実施形態では、HPC細胞バルクは、アスコルビン酸、幹細胞因子(SCF)、IL-7、Flt3L、TPO、フィブロネクチンまたはそのバリアント、Notchリガンド(例えば、Jag-1、Jag-2、DLL-1、DLL-3、DLL-4)、p38阻害剤及びSDF-1からなる群から選択される少なくとも1つの化合物を有するCD4/CD8誘導培地で培養させ、CD4-/CD8-細胞、CD4-/CD8+細胞、CD4+/CD8+細胞、及びCD4+/CD8-細胞を含む集団を得る。したがって、いくつかの実施形態では、HPC細胞バルクは、アスコルビン酸を含むCD4/CD8誘導培地で培養させ、CD4-/CD8-細胞、CD4-/CD8+細胞、CD4+/CD8+細胞、及びCD4+/CD8-細胞を含む集団を得る。いくつかの実施形態では、HPC細胞バルクは、SCFを含むCD4/CD8誘導培地で培養させ、CD4-/CD8-細胞、CD4-/CD8+細胞、CD4+/CD8+細胞、及びCD4+/CD8-細胞を含む集団を得る。いくつかの実施形態では、HPC細胞バルクは、IL-7を含むCD4/CD8誘導培地で培養させ、CD4-/CD8-細胞、CD4-/CD8+細胞、CD4+/CD8+細胞、及びCD4+/CD8-細胞を含む集団を得る。いくつかの実施形態では、HPC細胞バルクは、Flt3Lを含むCD4/CD8誘導培地で培養させ、CD4-/CD8-細胞、CD4-/CD8+細胞、CD4+/CD8+細胞、及びCD4+/CD8-細胞を含む集団を得る。いくつかの実施形態では、HPC細胞バルクは、p38阻害剤を含むCD4/CD8誘導培地で培養させ、CD4-/CD8-細胞、CD4-/CD8+細胞、CD4+/CD8+細胞、及びCD4+/CD8-細胞を含む集団を得る。いくつかの実施形態では、HPC細胞バルクは、SDF-1を含むCD4/CD8誘導培地で培養させ、CD4-/CD8-細胞、CD4-/CD8+細胞、CD4+/CD8+細胞、及びCD4+/CD8-細胞を含む集団を得る。
CD56+/CD3-細胞の集団を得るために、上記のように、CD4-/CD8-細胞、CD4-/CD8+細胞、CD4+/CD8+細胞、及びCD4+/CD8-細胞を含む細胞の集団は、細胞培養培地でさらに培養することができる。いくつかの実施形態では、培養培地は、NK誘導培地である。いくつかの実施形態では、NK誘導培地は、IL-7、IL-2及び抗CD3抗体のうちの1つ以上を含む。
いくつかの実施形態では、任意の多能性、多分化能、または患者由来のHPCを、本明細書に記載の方法で使用することができる。例えば、いくつかの実施形態では、細胞は、胚性幹細胞である。いくつかの実施形態では、細胞は、成体幹細胞である。様々な成体幹細胞が当技術分野で知られており、例えば、間葉系幹細胞、造血幹細胞、臍帯由来細胞、骨髄幹細胞、脂肪幹細胞などが挙げられる。いくつかの実施形態では、細胞は、人工多能性幹細胞(iPSC)である。したがって、本明細書に記載の方法に従って産生されるNK細胞は、ドナーに直接由来する一次HPCなどの任意の多能性、多分化能、または患者由来のHPCから作製することができる。
いくつかの実施形態では、iPSCから造血前駆細胞を産生するための培地(すなわち、HPC誘導培地)は、動物細胞の培養に使用される基礎培地にビタミンCを添加することによって調製され得る。基礎培地の例としては、イスコーブ改変ダルベッコ培地(IMDM)、培地199、イーグル最小必須培地(EMEM)、αMEM培地、ダルベッコ改変イーグル培地(DMEM)、ハムF12培地、RPMI 1640培地、フィッシャー培地、及び神経基礎培地(Life Technologies)、及びこれらの培地の2つ以上の混合物が挙げられる。いくつかの実施形態では、培地は、血清を含む。いくつかの実施形態では、培地は、無血清である。
いくつかの実施形態では、CD4/CD8誘導培地は、CD4+/CD8+、CD4-/CD8-細胞、CD4-/CD8+細胞、及びCD4+/CD8-細胞を含む細胞集団をもたらす。「CD4/CD8二重陽性細胞」(DP細胞)とは、CD4及びCD8の両方を発現する細胞を意味する。CD4/CD8二重陽性細胞は、CD4、CD8、CD3、及びCD45陽性の細胞として同定できる。「CD4/CD8二重陰性細胞」(DN細胞)とは、CD4-及びCD8-の両方を発現しない細胞を意味する。「CD4-/CD8+細胞」とは、CD4-を発現しないが、CD8+を発現する細胞を意味する。「CD4+/CD8-細胞」とは、CD4を発現するが、CD8を発現しない細胞を意味する。
いくつかの実施形態では、NK細胞は、CD56+/CD3-免疫細胞である。
いくつかの実施形態では、NK細胞は、1つ以上の導入遺伝子を含むように操作される。例えば、NK細胞は、腫瘍指向性キメラ抗原受容体(CAR)を発現するように遺伝子操作することができ、それによって抗腫瘍エフェクター細胞を産生する。一例では、NK細胞またはiPS NK細胞は、CARを発現するように操作することができる。いくつかの実施形態では、NK細胞に対する細胞前駆体は、CARを発現するように操作される。例えば、いくつかの実施形態では、iPS細胞は、CARを発現するように操作される。いくつかの実施形態では、HP細胞バルク中の細胞は、CARを発現するように操作される。いくつかの実施形態では、NK細胞は、CARを発現するように操作される。さらに、いくつかの実施形態では、これらのトランスジェニック受容体は、タンパク質由来ではない腫瘍関連抗原に配向させ得る。特定の実施形態では、NK細胞またはiPS NK細胞は、少なくとも1つのCARを含むように改変される。いくつかの実施形態では、単一のCARは、2つ以上の抗原を標的とする。
本発明による細胞は、それを必要とする患者において、がん、ウイルス感染または自己免疫障害を治療するために使用することができる。別の実施形態では、本発明による単離された細胞は、それを必要とする患者における、がん、自己免疫障害のウイルス感染の治療のための医薬品の製造において使用され得る。
いくつかの実施形態では、細胞は、多種多様な方法で、宿主生物、例えば、哺乳動物に導入され得る。細胞は、特定の実施形態では、腫瘍の部位に導入され得るが、代替の実施形態では、細胞はがんに進行するか、またはがんに進行するように改変される。使用される細胞の数は、複数の状況、導入の目的、細胞の寿命、使用されるプロトコル、例えば、投与回数、細胞が増殖する能力、組換え構築物などの安定性に依存する。細胞は、分散液として適用してもよく、一般に、目的の部位またはその近くに注入される。細胞は、生理学的に許容される培地中にあり得る。一例では、本発明のNK細胞またはiPS NK細胞は、1つ以上のCAR、TCR、または高親和性CD16など、任意の他の操作されたタンパク質もしくはポリペプチドドメインを発現し得る。いくつかの実施形態では、細胞は、免疫認識を阻害するために内包化され、腫瘍の部位に配置される。
いくつかの実施形態では、本発明のNK細胞またはiPS NK細胞は、1つ以上のCAR、TCR、または高親和性CD16またはCD19などの任意の他の操作されたタンパク質またはポリペプチドドメインを発現するように操作される。これらのポリペプチドを含む発現ベクターを生成するための組換え技術は、当技術分野で周知であり、以下に一般的に記載されている。
「ベクター」という用語は、複製することができる細胞に導入するために核酸配列を挿入することができる担体核酸分子を指すために使用される。核酸配列は「外因性」であり得、これは、ベクターが導入されている細胞にとって外来性であるか、または配列が細胞内の配列と相同であるが、通常、配列が発見されない宿主細胞の核酸内の任意の位置にあることを意味する。ベクターとしては、プラスミド、コスミド、及びウイルス(例えば、バクテリオファージ、動物ウイルス、及び植物ウイルス)、ならびに人工染色体(例えば、YAC)を挙げることができる。当技術分野の技術のうちの1つは、標準的な組換え技術を介してベクターを構築するために十分に装備されている(例えば、Maniatis et al.、1988及びAusubel et al.,1994を参照、これらは、両方とも参照により本明細書に組み込まれる)。
「プロモーター」は、その場所で転写の開始及び速度が制御される核酸配列の領域である制御配列である。この配列は、RNAポリメラーゼ及び他の転写因子などの調節タンパク質及び分子が結合して、核酸配列の特定の転写を開始し得る遺伝子エレメントを含み得る。「操作可能に位置付られた」、「操作可能に連結された」、「制御下にある」、及び「転写制御下にある」という句は、プロモーターが正しい機能的場所、及び/または転写開始及び/またはその配列の発現を制御するために、核酸配列に関連する配向にあることを意味する。
特定の実施形態では、プラスミドベクターは、宿主細胞を形質転換するための使用が企図される。一般に、宿主細胞と適合性のある種由来のレプリコン及び制御配列を含有するプラスミドベクターが、これらの宿主に関連して使用される。このベクターは、通常、複製部位、及び形質転換細胞において表現型選択を提供することができるマーキング配列を有する。非限定的な例では、E.coliは、多くの場合、E.coli種に由来するプラスミドであるpBR322の誘導体を使用して形質転換される。pBR322には、アンピシリン及びテトラサイクリンの耐性遺伝子が含まれているため、形質転換細胞を容易に同定する手段をもたらす。pBRプラスミド、または他の微生物プラスミドまたはファージもまた、例えば、微生物がそれ自体のタンパク質の発現のために使用することができるプロモーターを含むか、または含むように改変される必要がある。
特定のウイルスが受容体媒介エンドサイトーシスを介して細胞に感染するかまたは細胞に侵入し、宿主細胞のゲノムに組み込まれて、ウイルス遺伝子を安定的かつ効率的に発現する能力により、外来核酸を細胞(例えば、哺乳動物細胞)に移すための魅力的な候補となっている。本発明の成分は、1つ以上のCAR、TCR、または本発明の高親和性CD16などの他の任意の操作されたタンパク質またはポリペプチドドメインをコードするウイルスベクターであり得る。本発明の核酸を送達するために使用され得るウイルスベクターの非限定的な例を以下に記載する。
核酸を送達するための特定の方法は、アデノウイルス発現ベクターを使用することを含む。アデノウイルスベクターは、ゲノムDNAに組み込むには、能力が低いことが知られているが、この特徴は、これらのベクターによってもたらされる高効率の遺伝子導入によって相殺される。「アデノウイルス発現ベクター」は、(a)構築物のパッケージングをサポートする、及び(b)クローン化された組織または細胞特異的構築物を最終的に発現するのに十分なアデノウイルス配列を含む構築物を含むものを意味する。遺伝子構成またはアデノウイルス、36kb、直鎖、二本鎖DNAウイルスに関する知識により、大きな片のアデノウイルスDNAを最大7kbの外来配列に置換できる(Grunhaus and Horwitz,1992)。
核酸は、アデノウイルス支援トランスフェクションを用いて、細胞に導入させ得る。アデノウイルス連結系を使用した細胞系では、トランスフェクション効率の向上が報告されている(Kelleher and Vos,1994;Cotten et al.,1992;Curiel,1994)。アデノ関連ウイルス(AAV)は、高い組み込み頻度を有し、非分裂細胞に感染し得るため、本発明の細胞内で使用するための魅力的なベクター系であり、したがって、例えば、組織培養(Muzyczka,1992)またはin vivoにおいて、哺乳動物細胞への遺伝子の送達に有用である。AAVは、感染性について広い宿主範囲を有する(Tratschin et al.,1984;Laughlin et al.,1986;Lebkowski et al.,1988;McLaughlin et al.,1988)。rAAVベクターの生成及び使用に関する詳細は、例えば、米国特許第5,139,941号及び同第4,797,368号に記載されており、これらは各々、参照により本明細書に組み込まれる。
レトロウイルスは、遺伝子を宿主ゲノムに組み込み、大量の外来遺伝物質を移し、広範囲の種及び細胞種に感染させ、特殊な細胞株にパッケージングするその能力により、送達ベクターとして有用である(Miller,1992)。
本発明の特定の実施形態では、臨床的態様のための本発明の方法は、抗がん剤など、過剰増殖性疾患の治療において有効な他の剤と組み合わされる。「抗がん剤」剤は、例えば、がん細胞を死滅させること、がん細胞にアポトーシスを誘導すること、がん細胞の成長速度を低下させること、転移の発生率または数を減少させること、腫瘍サイズを減少させること、腫瘍成長を阻害すること、腫瘍またはがん細胞への血液供給を減少させること、がん細胞または腫瘍に対する免疫応答を促進すること、がんの進行を予防することもしくは阻害すること、またはがんを有する対象の寿命を延長させることにより、対象において、がんに悪影響を与え得る。より一般的には、これらの他の組成物は、細胞を死滅させるまたは細胞の増殖を阻害するのに有効な組み合わせ量で提供されるであろう。このプロセスは、がん細胞を発現構築物及び剤(複数可)または複数の因子と同時に接触させることを含み得る。これは、細胞を単一の組成物または両方の剤を含む薬理学的製剤と接触させることによって、または細胞を2つの別個の組成物もしくは製剤と同時に接触させることによって達成することができ、ここで、一方の組成物は、発現構築物を含み、他方の組成物は、第2の剤(複数可)を含む。
がん治療には、化学療法剤及び放射線治療の両方をベースにした治療との様々な組み合わせ療法も含む。組み合わせ化学療法としては、例えば、アブラキサン、アルトレタミン、ドセタキセル、ハーセプチン、メトトレキサート、ノバントロン、ゾラデックス、シスプラチン(CDDP)、カルボプラチン、プロカルバジン、メクロレタミン、シクロホスファミド、カンプトテシン、イホスファミド、メルファラン、クロラムブシル、ブスルファン、ニトロソウレア、ダクチノマイシン、ダウノルビシン、ドキソルビシン、ブレオマイシン、プリコマイシン(plicomycin)、マイトマイシン、エトポシド(VP16)、タモキシフェン、ラロキシフェン、エストロゲン受容体結合剤、タキソール、ゲムシタビエン、ナベルビン、ファルネシルタンパク質タンスフェラーゼ阻害剤、トランスプラチナ、5-フルオロウラシル、ビンクリスチン、ビンブラスチン及びメトトレキサート、またはそれらの任意の類似物または誘導バリアント及びそれらの組み合わせが挙げられる。
DNA損傷を引き起こし、かつ広く使用されている他の因子としては、一般に、ガンマ線、X線、及び/または腫瘍細胞への放射性同位元素の直接送達である。マイクロ波及び紫外線照射など、他の形態のDNA損傷因子も考えられる。これらの因子はすべて、DNA、DNAの前駆体、DNAの複製及び修復、ならびに染色体のアセンブリング及び維持に対して、広範囲の損傷を与える可能性が最も高い。X線の線量範囲は、長期間(3~4週間)では1日線量50~200レントゲン、単回線量では2000~6000レントゲンの範囲である。放射性同位元素の線量範囲は、幅広く異なり、同位体の半減期、放出される放射線の強度及び種類、ならびに新生物細胞による取り込みに依存する。
免疫療法は、一般に、がん細胞を標的にして破壊させるために、免疫エフェクター細胞及び分子を使用することに依存する。免疫エフェクターは、例えば、腫瘍細胞の表面上にあるいくつかのマーカーに特異的な抗体であり得る。抗体のみが治療のエフェクターとして作用し得る、または他の細胞を動員させて、実際に細胞を死滅させ得る。抗体はまた、薬物または毒素(化学療法剤、放射性核種、リシンA鎖、コレラ毒素、百日咳毒素など)に結合させて、単に標的剤として作用し得る。あるいは、エフェクターは、腫瘍細胞標的と直接的または間接的に相互作用する表面分子を担持するリンパ球であり得る。様々なエフェクター細胞には、細胞傷害性T細胞及びNK細胞が含まれる。
さらに別の実施形態では、二次治療は、治療用ポリヌクレオチドが、本発明の臨床実施形態の前、後、または同時に投与される遺伝子療法である。細胞増殖の誘導物質、細胞増殖の阻害剤、またはプログラム細胞死の調節因子など、様々な発現産物が本発明に含まれる。
がん患者の約60%は、予防的、診断的または病期分類、治癒的及び姑息的手術など、ある種の外科手術を受ける。治癒的手術は、本発明の治療、化学療法、放射線療法、ホルモン療法、遺伝子療法、免疫療法及び/または代替療法などの他の療法と併用して使用され得るがん治療である。
iPS細胞株であるFfI-01s04株は、健康な個体の末梢血単核細胞から得た。StemFit完全培地に分散したFfI-01s04細胞を、6x105細胞/ウェル、低酸素(5%O2)条件下(「0日目」)で、超低接着処理6ウェルプレートに播種した。StemFit完全培地には、10μM CHIR99021及び50μM Y-27632を含めた。翌日(すなわち、1日目)、FfI-01s04細胞をBMP4(50ng/ml)、VEGF(50ng/ml)、bFGF(50ng/ml)、及びアスコルビン酸2-ホスフェート(50μg/ml)を含む造血前駆細胞(HPC)分化培地に分散した。HPC誘導培養培地には、ヒトインスリン(10μg/ml)、ヒトトランスフェリン(5.5μg/ml)、亜セレン酸ナトリウム(6.7ng/ml)、L-グルタミン(2mM)及びα-モノチオグリセロール(0.4mM)を添加したStemPro34を含めた。2日目に、SB431542(培地中6μM)を培養培地(すなわち、細胞を含むHPC分化培地)に添加し、細胞を2日間培養した。4日目に、細胞をVEGF(50ng/ml)、bFGF(50ng/ml)、SCF(50ng/ml)、及びアスコルビン酸2-ホスフェート(50μg/ml)を含む別の培地に再分散させ、さらに3日間培養した。7日目に、細胞をVEGF(50ng/ml)、bFGF(50ng/ml)、SCF(50ng/ml)、アスコルビン酸2-ホスフェート(50μg/ml)、TPO(30ng/ml)及びFlt3L(10ng/ml)を含む別の培地に曝露し、この培地を使用してさらに7日間培養した。この7日間の培養期間中、培地は、2~3日ごとに交換した。
14日目に、いかなる細胞単離も受けずに、実施例1から得られた細胞集団(「HP細胞バルク」)を15cmディッシュに3.12x106細胞/ディッシュで播種し、37℃、5%O2で培養した。様々な播種密度を使用してよく、該播種密度は、一実施形態であることに留意されたい。各15cmディッシュは、rh-DLL4/Fc キメラ(Sino Biological)及びRetroNectin(Takara Bio Inc)でコーティングした。この培養期間中、培地は2~3日ごとに交換した。15%FBS、4mML-グルタミン、100U/mlペニシリン、100μg/mlストレプトマイシン、55μM2-メルカプトエタノール、50μg/mlアスコルビン酸2-ホスフェート、10μg/mlヒトインスリン、5.5μg/mlヒトトランスフェリン、6.7ng/ml亜セレン酸ナトリウム、50ng/mlSCF、50ng/mlIL-7、50ng/mlFlt3L、100ng/mlTPO、15μM SB203580、30nM SDF-1αを添加したMEMα(ThermoFisherScientific(Gibco))を、これらの細胞を培養するための培地として使用した。21日目に、新たにhDLL4/RetroNectinをコーティングした新しい15cmディッシュに細胞を継代させた。28日目に、新たにhDLL4/RetroNectinをコーティングした新しい15cmディッシュに細胞をさらに継代させた。35日目に、CD4/CD8細胞などのすべての細胞(「DP細胞バルク」)を回収した。
35日目に、DP細胞バルク、すなわち、細胞単離を受けることなく実施例2で得られた細胞を、1x106細胞/ウェルで、48ウェルプレートに播種し、5%CO2、37℃で3日間培養した。15%FBS、4mM L-グルタミン、100U/mlペニシリン、100ng/mlストレプトマイシン、50μg/mlアスコルビン酸2-ホスフェート、10μg/mlヒトインスリン、5.5μg/mlヒトトランスフェリン、6.7ng/ml亜セレン酸ナトリウム、500ng/m1 抗CD3抗体(UCHT1)、10ng/ml IL-2、及び10ng/ml IL-7を添加したMEMα培地を、培養培地として使用した。38日目に、15%FBS、4mL-グルタミン、100U/mlペニシリン、100ng/mlストレプトマイシン、50μg/mlアスコルビン酸2-ホスフェート、10μg/mlヒトインスリン、5.5μg/mlヒトトランスフェリン、6.7ng/ml亜セレン酸ナトリウム、10ng/ml IL-2、及び10ng/ml IL-7を添加した別のMEMα培地に細胞を分散させ、培養培地として使用した。42日目に、NK細胞を含むすべての細胞(「NK細胞バルク」)を回収した。
次に、NK細胞バルクを表1に記載の抗体のセットで染色し、フローサイトメトリーにより分析した。図1に示すとおり、CD3陰性NK細胞バルクの一部は、CD56(「CD56陽性免疫細胞」)を発現した。図1CD56陽性免疫細胞及びCD3陰性免疫細胞は、ナチュラルキラー細胞(NK細胞)である。したがって、CD56陽性免疫細胞及びCD3陰性免疫細胞は、iPS細胞(FfI-01s04株)由来のHP細胞バルクから調製した。上記のプロセスで得られたCD56を発現する細胞は、iPS NK細胞と呼ばれることもある。フローサイトメトリーに使用した抗体を表1に示す。
NK細胞バルク集団(すなわち、実施例3で得られた細胞)中の異なる細胞種を同定するために、非線形次元圧縮法(単一細胞RNA-seq(scRNAseq)をベースにしたUMAP(uniform manifold approximation and projection))を適用した。
NK細胞は、1つ以上のCARを発現するようにさらに改変させた。NK細胞の改変には、(1)抗CD19CAR遺伝子及びIL-15Rα/IL-15遺伝子を合成するステップと;(2)抗CD19CAR遺伝子及びIL-15Rα/IL-15遺伝子を含むレトロウイルスベクターを調製するステップと;(3)抗CD19CAR遺伝子及びIL-15Rα/IL-15遺伝子を含むレトロウイルスベクターでNK細胞を形質導入するステップと、を含む。
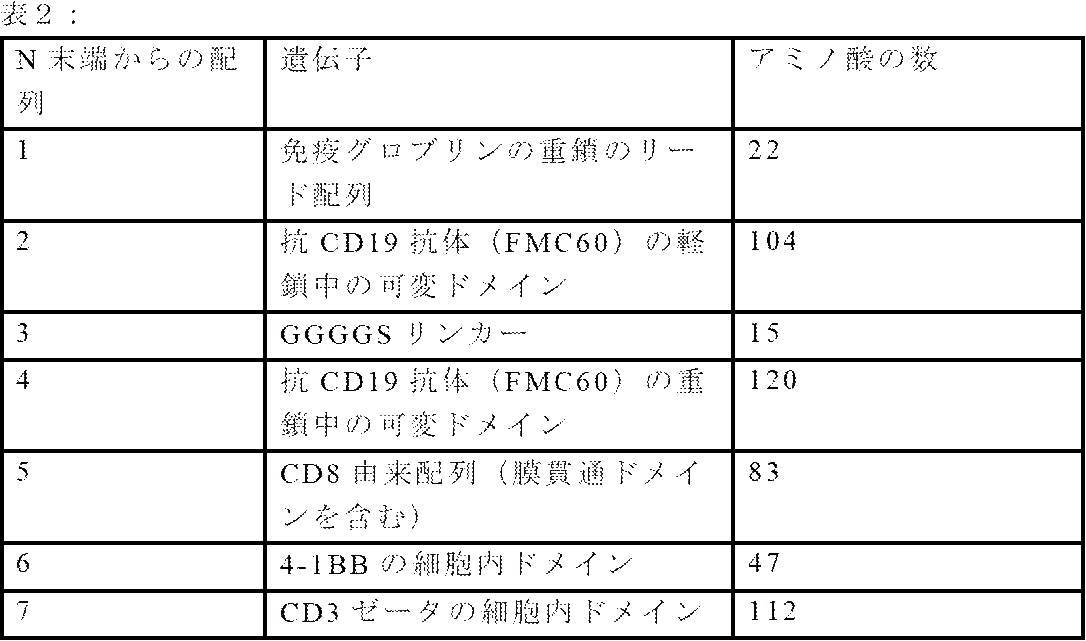
抗CD19CAR遺伝子は、表2に示すとおり、N末端から配置されるように設計されたオリゴペプチドを合成することによって調製した。
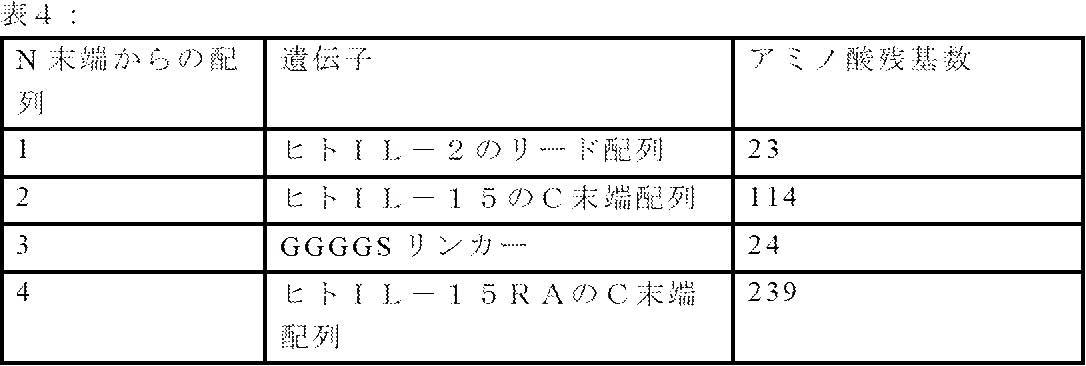
IL-15Rα/IL-15遺伝子は、N末端から配置されるように設計されたオリゴペプチドを合成することによって調製した。IL-15Rα/IL-15は、Mortier et al.,2006,The Journal of Biological Chemistry,Vol 281,No 3,pages 1612-1619,January 20,2006;Chertova et al.,The Journal of Biological Chemistry,Vol.288,No.25,Pages 18093-18103,June 21,2013;及びRowley et al.,Eur J Immunol,2009 February;39(2):491-506に従って構築した(それぞれ、その全体が、参照によって、組み込まれる)。
抗CD19CAR遺伝子は、pMYレトロウイルスベクターのマルチクローニング部位に組み込ませた。レトロウイルスベクターは、レトロウイルスベクターを産生するために、FRY-RD18細胞を使用して生成した。
IL-15Rα/IL-15遺伝子は、別のpMYレトロウイルスベクターのマルチクローニング部位に組み込ませた。レトロウイルスベクターは、レトロウイルスベクターを生産するために、FRY-RD18細胞を使用して生成した。
iPS NK細胞は、抗CD19CAR遺伝子を含むレトロウイルスベクター、及びIL-15Rα/IL-15遺伝子を含むレトロウイルスベクターで形質導入させて、抗CD19CAR発現iPSNK細胞(「iNK-CAR19」)を生成した。
ルシフェラーゼ発現Nalm6細胞(ATCC;がん細胞)(5x105細胞)を、尾静脈を介して、NOD/Shi-scidIL-2Rガンマヌルマウス(「NSGマウス」)に移植した。NSGマウス(雄、4~5週齢)は、Jackson Laboratoryから入手した。Nalm6細胞移植の4日後、0.2mlのPBSまたは細胞を含まないわずか0.2mlのPBSに分散させたiNK-CAR19(1x107細胞)を、尾静脈を介してNalm6移植NSGマウスに投与した。iNK-CAR19細胞またはPBSを投与後、尾静脈を介してルシフェリンをマウスに投与した。ルシフェラーゼ活性は、IVISイメージングシステム(PerkinElmer)を使用して、70日以上測定した。
当業者は、日常的な実験のみを用いて、本明細書に記載される本発明の特定の実施形態に対する多くの添加均等物を認識する、または確認することができるだろう。本発明の特許請求の範囲は、上記説明に限定されることを意図するものではなく、むしろ以下の特許請求の範囲に記載される通りである。
Claims (73)
- 多能性幹細胞由来NK細胞を産生する方法であって、
(A)多能性幹細胞に由来する造血前駆細胞(HPC)(HP細胞バルク)を含むバルク細胞集団を提供することと、
(B)前記HP細胞バルクを1つ以上の培養培地で培養して、CD56+/CD3-細胞を産生することと、を含み、
細胞単離ステップを含まない、方法。 - 前記方法が、ステップ(A)及び(B)において、細胞単離ステップを含まない、請求項1に記載の方法。
- (A)の前記HP細胞バルクが、CD34+細胞を含む、請求項1または2に記載の方法。
- 前記HP細胞バルク中の前記細胞の20%以上が、CD34+細胞である、請求項3に記載の方法。
- 前記HP細胞バルクの20%~90%が、CD34+細胞である、請求項4に記載の方法。
- ステップ(B)が、
(i)CD4/CD8誘導培地中で前記HP細胞バルクを培養して、CD4-/CD8-細胞、CD4-/CD8+細胞、CD4+/CD8-、及びCD4+/CD8+細胞を含む中間の異種細胞集団を生成することと、
(ii)NK誘導培地で前記中間の異種細胞集団を培養して、前記CD56+/CD3-細胞を産生することと、を含む、前記請求項のいずれか1項に記載の方法。 - 前記方法が、CD4+/CD8+細胞を単離するステップを含まない、前記請求項のいずれか1項に記載の方法。
- ステップ(A)が、HPC誘導培地において多能性幹細胞を培養して、HP細胞バルクを産生することを含む、前記請求項のいずれか1項に記載の方法。
- 前記多能性幹細胞が、人工多能性幹細胞(iPSC)である、前記請求項のいずれか1項に記載の方法。
- 前記HPC誘導培地が、骨形成タンパク質-4(BMP4)、血管内皮成長因子(VEGF)、塩基性線維芽細胞成長因子(bFGF)、アスコルビン酸、Flt3リガンド(Flt3L)、トロンボポエチン(TPO)及びTGFβ阻害剤から選択される少なくとも1つの化合物を含む、請求項8または9に記載の方法。
- 前記HPC誘導培地が、5ng/mL~500ng/mlの濃度で、BMP4を含む、請求項10に記載の方法。
- 前記BMP4が、濃度50ng/mlである、請求項11に記載の方法。
- バルク細胞培地が、5ng/mL~500ng/mlの濃度で、VEGFを含む、請求項10~12のいずれか1項に記載の方法。
- 前記VEGFが、濃度約50ng/mlである、請求項13に記載の方法。
- 前記HPC誘導培地が、5ng/mL~500ng/mlの濃度で、bFGFを含む、請求項10~14のいずれか1項に記載の方法。
- 前記bFGFが、濃度50ng/mlである、請求項15に記載の方法。
- 前記バルク細胞培地が、5μg/mL~500μg/mlの濃度でアスコルビン酸を含む、請求項10~16のいずれか1項に記載の方法。
- 前記アスコルビン酸が、濃度50μg/mlである、請求項17に記載の方法。
- 前記HPC誘導培地が、1ng/mL~100ng/mlの濃度で、Flt3Lを含む、請求項10~18のいずれか1項に記載の方法。
- 前記Flt3Lが、濃度50ng/mlである、請求項19に記載の方法。
- 前記HPC誘導培地が、1ng/mL~200ng/mlの濃度で、TPOを含む、請求項10~20のいずれか1項に記載の方法。
- 前記TPOが、濃度100ng/mlである、請求項21に記載の方法。
- 前記CD4/CD8誘導培地が、アスコルビン酸、幹細胞因子(SCF)、IL-7、Flt3L、トロンボポエチン(TPO)、p38阻害剤及びSDF-1からなる群から選択される少なくとも1つの化合物を含む、請求項6~22のいずれか1項に記載の方法。
- 前記CD4/CD8誘導培地が、5μg/ml~約500μg/mlの濃度のアスコルビン酸を含む、請求項23に記載の方法。
- 前記アスコルビン酸が、濃度50μg/mlである、請求項24に記載の方法。
- 前記CD4/CD8誘導培地が、5ng/mL~100ng/mlの濃度で、SCFを含む、請求項23~25のいずれか1項に記載の方法。
- 前記SCFが、濃度50ng/mlである、請求項26に記載の方法。
- 前記CD4/CD8誘導培地が、1ng/mL~100ng/mlの濃度で、IL-7を含む、請求項23~27のいずれか1項に記載の方法。
- 前記IL-7が、濃度50ng/mlである、請求項28に記載の方法。
- 前記CD4/CD8誘導培地が、1ng/mL~100ng/mlの濃度で、Flt3Lを含む、請求項23~29のいずれか1項に記載の方法。
- 前記Flt3Lが、濃度50ng/mlのFlt3Lである、請求項30に記載の方法。
- 前記CD4/CD8誘導培地が、1ng/mL~200ng/mlの濃度で、TPOを含む、請求項23~31のいずれか1項に記載の方法。
- 前記TPOが、濃度100ng/mlである、請求項32に記載の方法。
- 前記CD4/CD8誘導培地が、0.5μM~100μMの濃度で、p38阻害剤を含む、請求項23~33のいずれか1項に記載の方法。
- 前記p38阻害剤が、SB203580である、請求項34に記載の方法。
- 前記SB203580が、濃度15μMである、請求項35に記載の方法。
- 前記CD4/CD8誘導培地が、10ng/mL~約100ng/mlの濃度で、SDF-1阻害剤を含む、請求項23~36のいずれか1項に記載の方法。
- 前記SDF-1阻害剤が、濃度30nMである、請求項37に記載の方法。
- 前記NK誘導培地が、CD3活性化因子、IL-2及びIL7からなる群から選択される少なくとも1つの化合物を含む、請求項6~38のいずれか1項に記載の方法。
- 前記NK誘導培地が、1ng/mL~100ng/mlの濃度で、IL-2を含む、請求項39に記載の方法。
- 前記IL-2が、濃度10ng/mlである、請求項40に記載の方法。
- 前記第2の誘導培地が、1ng/mL~100ng/mlの濃度で、IL-7を含む、請求項39~41のいずれか1項に記載の方法。
- 前記IL-7が、濃度10ng/mlである、請求項42に記載の方法。
- 前記培養ステップのそれぞれが、約5%酸素で実施される、前記請求項のいずれか1項に記載の方法。
- 前記培養ステップのそれぞれが、14%を超える酸素で実施される、請求項1~43のいずれか1項に記載の方法。
- 前記培養ステップのそれぞれが、大気中酸素で実施される、請求項1~43のいずれか1項に記載の方法。
- 前記培養ステップのそれぞれが、5%未満の酸素で実施される、請求項1~43のいずれか1項に記載の方法。
- 前記バルク細胞培地中で多能性幹細胞を培養して、10日を超えて持続して、HP細胞バルクを得る、請求項8~47のいずれか1項に記載の方法。
- 前記バルク細胞培地中で多能性幹細胞を培養して、11~15日の間持続して、HP細胞バルクを得る、請求項48に記載の方法。
- 前記バルク細胞培地中で多能性幹細胞を培養して、14日間持続して、HP細胞バルクを得る、請求項49に記載の方法。
- 前記iPSCが、末梢血単核細胞から得られる、請求項9~50のいずれか1項に記載の方法。
- 濃縮ステップなく、産生された細胞の少なくとも約50%、55%、60%、75%、80%、85%、90%、95%、97%またはそれ以上が、CD56+/CD3-細胞である、前記請求項のいずれか1項に記載の方法。
- 産生された細胞の約25%未満が、CD3+細胞である、請求項52に記載の方法。
- 産生された細胞のパーセンテージが、フローサイトメトリーによって決定される、請求項52または53に記載の方法。
- 産生された細胞のパーセンテージが、単一細胞RNAシーケンス(scRNAseq)によって決定される、請求項52または53に記載の方法。
- CD56+/CD3-細胞を単離するステップをさらに含む、前記請求項のいずれか1項に記載の方法。
- CD56+/CD3-細胞が、蛍光活性化セルソーティング(FACS)または磁気ソーティングによって単離される、請求項56に記載の方法。
- 前記CD56+/CD3-免疫細胞が、NK細胞である、前記請求項のいずれか1項に記載の方法。
- 前記CD56+/CD3-細胞が、1つ以上のキメラ抗原受容体(CAR)を発現するように遺伝子改変されている、前記請求項のいずれか1項に記載の方法。
- 前記単離されたCD56+/CD3-細胞が、1つ以上のキメラ抗原受容体(CAR)を発現するように遺伝子改変されている、請求項59に記載の方法。
- 前記抗原が、CD19である、請求項60記載の方法。
- 前記細胞が、IL-15Rα/IL-15複合体を発現するように、さらに遺伝子改変されている、請求項59~61のいずれか1項に記載の方法。
- (1)血管内皮成長因子(VEGF)、塩基性線維芽細胞成長因子(bFGF)、及びアスコルビン酸から選択される少なくとも1つの化合物を含むHPC誘導培地においてiPSCを培養し、造血前駆細胞(HPC)を含む異種細胞集団(HP細胞バルク)得るステップと;
(2)アスコルビン酸、p38阻害剤及びSDF-1のうちの1つ以上を含むCD4/CD8誘導培地において、(1)で得られた前記HP細胞バルクを培養し、中間の異種細胞集団を得るステップと;
(3)CD3活性化因子、IL-2及びIL-7からなる群から選択される少なくとも1つの化合物を含むNK誘導培地において、(2)の前記中間の異種細胞集団を培養するステップと、を含む、人工多能性幹細胞(iPSC)由来のCD56+/CD3-免疫細胞を産生する方法。 - 前記請求項のいずれか1項に記載の方法を使用して産生されたNK細胞集団。
- 多能性幹細胞由来CD56+免疫細胞全体の60%以上の比率で、多能性幹細胞由来CD56+/CD3-細胞を含む、選別されていない細胞集団。
- 細胞の25%未満が、CD3+細胞である、請求項65に記載の選別されていない細胞集団。
- 5%未満の細胞が、単球である、請求項65または66に記載の選別されていない細胞集団。
- 5%未満の細胞が、B細胞である、請求項65または66に記載の選別されていない細胞集団。
- 細胞のパーセンテージが、フローサイトメトリーによって決定される、請求項65~68のいずれか1項に記載の選別されていない集団。
- 細胞のパーセンテージが、単一細胞RNAシーケンス(scRNAseq)によって決定される、請求項65~68のいずれか1項に記載の選別されていない集団。
- 細胞療法を必要とする対象を治療する方法であって、前記請求項のいずれか1項に記載のNK細胞を前記対象に投与することを含む、方法。
- 前記対象が、がんを有する、請求項68に記載の方法。
- 前記がんが、白血病またはリンパ腫である、請求項69に記載の方法。
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US202062983511P | 2020-02-28 | 2020-02-28 | |
| US62/983,511 | 2020-02-28 | ||
| PCT/US2021/019917 WO2021174004A1 (en) | 2020-02-28 | 2021-02-26 | Method for producing natural killer cells from pluripotent stem cells |
Publications (3)
| Publication Number | Publication Date |
|---|---|
| JP2023516632A true JP2023516632A (ja) | 2023-04-20 |
| JPWO2021174004A5 JPWO2021174004A5 (ja) | 2024-03-05 |
| JP7778708B2 JP7778708B2 (ja) | 2025-12-02 |
Family
ID=75108897
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2022552125A Active JP7778708B2 (ja) | 2020-02-28 | 2021-02-26 | 多能性幹細胞からナチュラルキラー細胞を産生するための方法 |
Country Status (14)
| Country | Link |
|---|---|
| US (1) | US12351824B2 (ja) |
| EP (1) | EP4110904A1 (ja) |
| JP (1) | JP7778708B2 (ja) |
| KR (1) | KR20220148174A (ja) |
| CN (1) | CN115427555A (ja) |
| AR (1) | AR121455A1 (ja) |
| AU (1) | AU2021225952A1 (ja) |
| BR (1) | BR112022017216A2 (ja) |
| CA (1) | CA3169617A1 (ja) |
| CO (1) | CO2022011682A2 (ja) |
| IL (1) | IL295964A (ja) |
| MX (1) | MX2022010521A (ja) |
| TW (1) | TWI886220B (ja) |
| WO (1) | WO2021174004A1 (ja) |
Families Citing this family (14)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| TW202237826A (zh) | 2020-11-30 | 2022-10-01 | 瑞士商克里斯珀醫療股份公司 | 基因編輯的自然殺手細胞 |
| WO2022144632A1 (en) | 2020-12-30 | 2022-07-07 | Crispr Therapeutics Ag | Compositions and methods for differentiating stem cells into nk cells |
| CN113801846B (zh) * | 2021-09-22 | 2024-06-04 | 南京艾尔普再生医学科技有限公司 | 一种从人诱导多能干细胞分化为自然杀伤细胞的方法 |
| CN114350608B (zh) * | 2022-01-27 | 2024-05-28 | 昭泰英基生物医药(香港)有限公司 | 一种诱导t细胞重编程为类nk细胞的组合物及其应用 |
| CN114517176B (zh) * | 2022-01-27 | 2022-12-02 | 广东普罗凯融生物医药科技有限公司 | 一种将ips细胞诱导成nk细胞的试剂盒及其应用方法 |
| US20250382574A1 (en) | 2022-06-27 | 2025-12-18 | Takeda Pharmaceutical Company Limited | Cell culture method |
| WO2024101862A1 (ko) * | 2022-11-07 | 2024-05-16 | 마루테라퓨틱스 주식회사 | Nk 세포의 분화 효율 및 기능성 증가를 위한 배양 방법 |
| WO2024107010A1 (ko) * | 2022-11-17 | 2024-05-23 | 주식회사 씨티셀즈 | 미분화 줄기세포로부터 자연 살해 세포로의 분화 방법 및 이의 용도 |
| CN115537397B (zh) * | 2022-12-02 | 2023-03-24 | 广东先康达细胞库有限公司 | Nk细胞诱导培养基及其培养方法 |
| CN118667760A (zh) * | 2023-03-17 | 2024-09-20 | 深圳市三启生物技术有限公司 | 诱导多能干细胞分化为cd34+造血干/祖细胞的培养基组合 |
| TW202506996A (zh) * | 2023-04-27 | 2025-02-16 | 日商武田藥品工業股份有限公司 | 擴增cd56+/cd3-細胞之方法 |
| CN116410336B (zh) * | 2023-06-02 | 2023-09-22 | 云南赛元生物技术有限公司 | 一种嵌合抗原受体的编码核苷酸、car-nk细胞及其构建方法和应用 |
| CN117050940B (zh) * | 2023-10-11 | 2024-01-26 | 苏州艾凯利元生物科技有限公司 | 一种制备自然杀伤细胞的方法 |
| CN117050941B (zh) * | 2023-10-11 | 2024-01-26 | 苏州艾凯利元生物科技有限公司 | 一种制备自然杀伤细胞的方法 |
Citations (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2017078807A1 (en) * | 2015-11-04 | 2017-05-11 | Fate Therapeutics, Inc. | Methods and compositions for inducing hematopoietic cell differentiation |
Family Cites Families (44)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US4797368A (en) | 1985-03-15 | 1989-01-10 | The United States Of America As Represented By The Department Of Health And Human Services | Adeno-associated virus as eukaryotic expression vector |
| US4683202A (en) | 1985-03-28 | 1987-07-28 | Cetus Corporation | Process for amplifying nucleic acid sequences |
| US5139941A (en) | 1985-10-31 | 1992-08-18 | University Of Florida Research Foundation, Inc. | AAV transduction vectors |
| US6013516A (en) | 1995-10-06 | 2000-01-11 | The Salk Institute For Biological Studies | Vector and method of use for nucleic acid delivery to non-dividing cells |
| US5928906A (en) | 1996-05-09 | 1999-07-27 | Sequenom, Inc. | Process for direct sequencing during template amplification |
| US5994136A (en) | 1997-12-12 | 1999-11-30 | Cell Genesys, Inc. | Method and means for producing high titer, safe, recombinant lentivirus vectors |
| US9453219B2 (en) | 2003-05-15 | 2016-09-27 | Mello Biotech Taiwan Co., Ltd. | Cosmetic designs and products using intronic RNA |
| CN103773804A (zh) | 2005-12-13 | 2014-05-07 | 国立大学法人京都大学 | 核重新编程因子 |
| JP5813321B2 (ja) | 2007-03-23 | 2015-11-17 | ウィスコンシン アラムニ リサーチ ファンデーション | 体細胞の再プログラム化 |
| JP2008307007A (ja) | 2007-06-15 | 2008-12-25 | Bayer Schering Pharma Ag | 出生後のヒト組織由来未分化幹細胞から誘導したヒト多能性幹細胞 |
| ES2589122T3 (es) | 2007-08-31 | 2016-11-10 | Whitehead Institute For Biomedical Research | Estimulación de la ruta de la Wnt en la reprogramación de células somáticas |
| CN101617043B (zh) | 2007-10-31 | 2014-03-12 | 国立大学法人京都大学 | 核重编程方法 |
| JP5558097B2 (ja) | 2007-12-10 | 2014-07-23 | 国立大学法人京都大学 | 効率的な核初期化方法 |
| EP2242838A1 (en) | 2007-12-17 | 2010-10-27 | GliaMed, Inc. | Stem-like cells and method for reprogramming adult mammalian somatic cells |
| WO2009091659A2 (en) | 2008-01-16 | 2009-07-23 | Shi-Lung Lin | Generation of tumor-free embryonic stem-like pluripotent cells using inducible recombinant rna agents |
| US20100330677A1 (en) | 2008-02-11 | 2010-12-30 | Cambridge Enterprise Limited | Improved Reprogramming of Mammalian Cells, and Cells Obtained |
| EP2090649A1 (en) | 2008-02-13 | 2009-08-19 | Fondazione Telethon | Method for reprogramming differentiated cells |
| WO2009102983A2 (en) | 2008-02-15 | 2009-08-20 | President And Fellows Of Harvard College | Efficient induction of pluripotent stem cells using small molecule compounds |
| EP2955222B1 (en) | 2008-03-17 | 2018-09-12 | The Scripps Research Institute | Combined chemical and genetic approaches for generation of induced pluripotent stem cells |
| WO2009114949A1 (en) | 2008-03-20 | 2009-09-24 | UNIVERSITé LAVAL | Methods for deprogramming somatic cells and uses thereof |
| KR20110007607A (ko) | 2008-04-07 | 2011-01-24 | 뉴포텐셜, 인크. | 소분자 조절제의 사용을 통한 다능 유전자의 유도에 의한 세포 재프로그래밍 |
| US8530238B2 (en) | 2008-06-27 | 2013-09-10 | Kyoto University | Method of efficiently establishing induced pluripotent stem cells |
| WO2010009015A2 (en) | 2008-07-14 | 2010-01-21 | Oklahoma Medical Research Foundation | Production of pluripotent cells through inhibition of bright/arid3a function |
| WO2010147612A1 (en) | 2009-06-18 | 2010-12-23 | Lixte Biotechnology, Inc. | Methods of modulating cell regulation by inhibiting p53 |
| US20120021519A1 (en) | 2008-09-19 | 2012-01-26 | Presidents And Fellows Of Harvard College | Efficient induction of pluripotent stem cells using small molecule compounds |
| WO2010033920A2 (en) | 2008-09-19 | 2010-03-25 | Whitehead Institute For Biomedical Research | Compositions and methods for enhancing cell reprogramming |
| WO2010042800A1 (en) | 2008-10-10 | 2010-04-15 | Nevada Cancer Institute | Methods of reprogramming somatic cells and methods of use for such cells |
| EP2342333A4 (en) | 2008-10-30 | 2013-05-08 | Univ Kyoto | Method for producing induced pluripotent stem cells |
| WO2010056831A2 (en) | 2008-11-12 | 2010-05-20 | Nupotential, Inc. | Reprogramming a cell by inducing a pluripotent gene through use of an hdac modulator |
| US9045737B2 (en) | 2008-12-13 | 2015-06-02 | Dnamicroarray, Inc. | Artificial three-dimensional microenvironment niche culture |
| KR101764100B1 (ko) | 2009-02-27 | 2017-08-02 | 고쿠리츠 다이가쿠 호진 교토 다이가쿠 | 신규한 핵 재프로그래밍 물질 |
| WO2010102267A2 (en) | 2009-03-06 | 2010-09-10 | Ipierian, Inc. | Tgf-beta pathway inhibitors for enhancement of cellular reprogramming of human cells |
| WO2010111409A2 (en) | 2009-03-25 | 2010-09-30 | The Salk Institute For Biological Studies | Pluripotent stem cells |
| WO2010111422A2 (en) | 2009-03-25 | 2010-09-30 | The Salk Institute For Biological Studies | Induced pluripotent stem cell generation using two factors and p53 inactivation |
| US8852940B2 (en) | 2009-04-01 | 2014-10-07 | The Regents Of The University Of California | Embryonic stem cell specific microRNAs promote induced pluripotency |
| WO2010124290A2 (en) | 2009-04-24 | 2010-10-28 | Whitehead Institute For Biomedical Research | Compositions and methods for deriving or culturing pluripotent cells |
| WO2010147395A2 (en) | 2009-06-16 | 2010-12-23 | Korea Research Institute Of Bioscience And Biotechnology | Medium composition comprising neuropeptide y for the generation, maintenance, prologned undifferentiated growth of pluripotent stem cells and method of culturing pluripotent stem cell using the same |
| CA2785627C (en) | 2009-12-29 | 2020-02-18 | Gamida-Cell Ltd. | Methods for enhancing natural killer cell proliferation and activity |
| UY35468A (es) | 2013-03-16 | 2014-10-31 | Novartis Ag | Tratamiento de cáncer utilizando un receptor quimérico de antígeno anti-cd19 |
| SG11201706041XA (en) | 2015-01-26 | 2017-08-30 | Fate Therapeutics Inc | Methods and compositions for inducing hematopoietic cell differentiation |
| JP6980534B2 (ja) * | 2015-06-25 | 2021-12-15 | ザ チルドレンズ メディカル センター コーポレーション | 造血幹細胞の増大、富化、および維持に関する方法および組成物 |
| AU2016342179B2 (en) | 2015-10-20 | 2022-08-18 | FUJIFILM Cellular Dynamics, Inc. | Multi-lineage hematopoietic precursor cell production by genetic programming |
| CN109415699B (zh) * | 2016-06-23 | 2024-08-27 | 国立大学法人京都大学 | Cd4cd8双阳性t细胞的制备方法 |
| IL269716B2 (en) | 2017-04-18 | 2025-07-01 | Fujifilm Cellular Dynamics Inc | Antigen-specific immune effector cells |
-
2021
- 2021-02-26 MX MX2022010521A patent/MX2022010521A/es unknown
- 2021-02-26 US US17/186,877 patent/US12351824B2/en active Active
- 2021-02-26 EP EP21713302.4A patent/EP4110904A1/en active Pending
- 2021-02-26 JP JP2022552125A patent/JP7778708B2/ja active Active
- 2021-02-26 CN CN202180017317.4A patent/CN115427555A/zh active Pending
- 2021-02-26 KR KR1020227028995A patent/KR20220148174A/ko active Pending
- 2021-02-26 BR BR112022017216A patent/BR112022017216A2/pt unknown
- 2021-02-26 AR ARP210100517A patent/AR121455A1/es unknown
- 2021-02-26 AU AU2021225952A patent/AU2021225952A1/en active Pending
- 2021-02-26 IL IL295964A patent/IL295964A/en unknown
- 2021-02-26 TW TW110107162A patent/TWI886220B/zh active
- 2021-02-26 WO PCT/US2021/019917 patent/WO2021174004A1/en not_active Ceased
- 2021-02-26 CA CA3169617A patent/CA3169617A1/en active Pending
-
2022
- 2022-08-19 CO CONC2022/0011682A patent/CO2022011682A2/es unknown
Patent Citations (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2017078807A1 (en) * | 2015-11-04 | 2017-05-11 | Fate Therapeutics, Inc. | Methods and compositions for inducing hematopoietic cell differentiation |
Non-Patent Citations (4)
| Title |
|---|
| CELL STEM CELL, vol. 23, no. 2, JPN6025004624, 2018, pages 181 - 192, ISSN: 0005645743 * |
| EXPERIMENTAL HEMATOLOGY, vol. 71, JPN6025004636, 2019, pages 13 - 23, ISSN: 0005645745 * |
| FRONTIERS IN IMMUNOLOGY, vol. 5, JPN6025004635, 2014, pages 439 - 1, ISSN: 0005645746 * |
| STEM CELL REPORTS, vol. 9, no. 6, JPN6025004632, 2017, pages 1796 - 1812, ISSN: 0005645744 * |
Also Published As
| Publication number | Publication date |
|---|---|
| IL295964A (en) | 2022-10-01 |
| KR20220148174A (ko) | 2022-11-04 |
| AU2021225952A1 (en) | 2022-10-20 |
| MX2022010521A (es) | 2022-09-19 |
| TWI886220B (zh) | 2025-06-11 |
| JP7778708B2 (ja) | 2025-12-02 |
| TW202146646A (zh) | 2021-12-16 |
| AR121455A1 (es) | 2022-06-08 |
| CA3169617A1 (en) | 2021-09-02 |
| US12351824B2 (en) | 2025-07-08 |
| WO2021174004A1 (en) | 2021-09-02 |
| CO2022011682A2 (es) | 2022-08-30 |
| BR112022017216A2 (pt) | 2022-10-11 |
| US20210292713A1 (en) | 2021-09-23 |
| EP4110904A1 (en) | 2023-01-04 |
| CN115427555A (zh) | 2022-12-02 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP7778708B2 (ja) | 多能性幹細胞からナチュラルキラー細胞を産生するための方法 | |
| JPWO2017221975A1 (ja) | Cd4cd8両陽性t細胞の製造方法 | |
| KR20190057387A (ko) | 만능 줄기 세포를 hla 동형 접합 면역 세포로 직접 분화시키기 위한 방법 | |
| KR20220130158A (ko) | 인간 만능 줄기 세포로부터의 무-간질 t 세포 분화 | |
| WO2022059780A1 (ja) | iPS細胞を介する再生T細胞の製造方法 | |
| TW202421780A (zh) | T細胞的製造方法 | |
| US20250177524A1 (en) | Cell bank composed of ips cells for introducing t cell receptor gene | |
| JP2024541859A (ja) | 幹細胞の遺伝子改変による複数のt細胞受容体を有するt細胞 | |
| US20240108656A1 (en) | Method for producing natural killer cells from pluripotent stem cells | |
| TW202235094A (zh) | 經回春的t細胞之製造方法、包含彼之組成物、及彼之使用方法 | |
| US20250368955A1 (en) | B cell lineages derived from pluripotent cells | |
| JP2024517966A (ja) | 同種異系car t細胞療法のために幹細胞を操作すること | |
| JP2024517968A (ja) | 幹細胞からの操作されたt細胞の産生 | |
| EA050899B1 (ru) | Способ получения естественных клеток-киллеров из плюрипотентных стволовых клеток | |
| WO2025076134A1 (en) | Nk cells or t cells expressing chimeric hematopoietic growth factor receptors and methods of use | |
| CN116615209A (zh) | 制备再生t细胞的方法、包含再生t细胞的组合物及使用再生t细胞的方法 | |
| CN120265300A (zh) | 来源于多能细胞的自然杀伤细胞谱系 | |
| CN119301255A (zh) | 用于基因修饰的免疫细胞疗法的选择性调节基因(srg)系统 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20240222 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20240222 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20250204 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20250403 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20250722 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20250918 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20251028 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20251119 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 7778708 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |