JP2022518906A - サルカルディン塩 - Google Patents
サルカルディン塩 Download PDFInfo
- Publication number
- JP2022518906A JP2022518906A JP2021542541A JP2021542541A JP2022518906A JP 2022518906 A JP2022518906 A JP 2022518906A JP 2021542541 A JP2021542541 A JP 2021542541A JP 2021542541 A JP2021542541 A JP 2021542541A JP 2022518906 A JP2022518906 A JP 2022518906A
- Authority
- JP
- Japan
- Prior art keywords
- solid form
- xrpd pattern
- sarcardin
- peaks
- salt
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
- 150000003839 salts Chemical class 0.000 title claims abstract description 323
- 238000000034 method Methods 0.000 claims abstract description 29
- 206010003119 arrhythmia Diseases 0.000 claims abstract description 16
- 230000006793 arrhythmia Effects 0.000 claims abstract description 16
- 239000008194 pharmaceutical composition Substances 0.000 claims abstract description 13
- 238000000634 powder X-ray diffraction Methods 0.000 claims description 340
- 239000007787 solid Substances 0.000 claims description 302
- SJJCQDRGABAVBB-UHFFFAOYSA-N 1-hydroxy-2-naphthoic acid Chemical compound C1=CC=CC2=C(O)C(C(=O)O)=CC=C21 SJJCQDRGABAVBB-UHFFFAOYSA-N 0.000 claims description 103
- VEXZGXHMUGYJMC-UHFFFAOYSA-N Hydrochloric acid Chemical compound Cl VEXZGXHMUGYJMC-UHFFFAOYSA-N 0.000 claims description 87
- XTEGVFVZDVNBPF-UHFFFAOYSA-N naphthalene-1,5-disulfonic acid Chemical compound C1=CC=C2C(S(=O)(=O)O)=CC=CC2=C1S(O)(=O)=O XTEGVFVZDVNBPF-UHFFFAOYSA-N 0.000 claims description 70
- KVBGVZZKJNLNJU-UHFFFAOYSA-N naphthalene-2-sulfonic acid Chemical compound C1=CC=CC2=CC(S(=O)(=O)O)=CC=C21 KVBGVZZKJNLNJU-UHFFFAOYSA-N 0.000 claims description 49
- AFAXGSQYZLGZPG-UHFFFAOYSA-N ethanedisulfonic acid Chemical compound OS(=O)(=O)CCS(O)(=O)=O AFAXGSQYZLGZPG-UHFFFAOYSA-N 0.000 claims description 41
- AFAXGSQYZLGZPG-UHFFFAOYSA-L ethane-1,2-disulfonate Chemical compound [O-]S(=O)(=O)CCS([O-])(=O)=O AFAXGSQYZLGZPG-UHFFFAOYSA-L 0.000 claims description 40
- 239000002253 acid Substances 0.000 claims description 38
- 238000001157 Fourier transform infrared spectrum Methods 0.000 claims description 36
- BMYNFMYTOJXKLE-UHFFFAOYSA-N 3-azaniumyl-2-hydroxypropanoate Chemical compound NCC(O)C(O)=O BMYNFMYTOJXKLE-UHFFFAOYSA-N 0.000 claims description 20
- CPELXLSAUQHCOX-UHFFFAOYSA-N Hydrogen bromide Chemical compound Br CPELXLSAUQHCOX-UHFFFAOYSA-N 0.000 claims description 18
- XTEGVFVZDVNBPF-UHFFFAOYSA-L naphthalene-1,5-disulfonate(2-) Chemical compound C1=CC=C2C(S(=O)(=O)[O-])=CC=CC2=C1S([O-])(=O)=O XTEGVFVZDVNBPF-UHFFFAOYSA-L 0.000 claims description 14
- SYZGIWXQGIBJGN-UHFFFAOYSA-N hbi-3000 Chemical compound C1=CC(OC)=CC=C1S(=O)(=O)NCC1=CC(CN2CCCC2)=C(O)C(CN2CCCC2)=C1 SYZGIWXQGIBJGN-UHFFFAOYSA-N 0.000 claims description 9
- 206010003658 Atrial Fibrillation Diseases 0.000 claims description 8
- 208000003663 ventricular fibrillation Diseases 0.000 claims description 7
- 206010047302 ventricular tachycardia Diseases 0.000 claims description 7
- 238000005033 Fourier transform infrared spectroscopy Methods 0.000 claims description 6
- 208000009729 Ventricular Premature Complexes Diseases 0.000 claims description 6
- 150000004682 monohydrates Chemical class 0.000 claims description 6
- 150000004683 dihydrates Chemical class 0.000 claims description 5
- 239000000546 pharmaceutical excipient Substances 0.000 claims description 5
- 208000003734 Supraventricular Tachycardia Diseases 0.000 claims description 2
- QAOWNCQODCNURD-UHFFFAOYSA-L Sulfate Chemical compound [O-]S([O-])(=O)=O QAOWNCQODCNURD-UHFFFAOYSA-L 0.000 abstract description 13
- 238000010586 diagram Methods 0.000 abstract 1
- 238000004455 differential thermal analysis Methods 0.000 description 67
- 238000001757 thermogravimetry curve Methods 0.000 description 56
- 239000000463 material Substances 0.000 description 47
- 230000008018 melting Effects 0.000 description 41
- 238000002844 melting Methods 0.000 description 41
- 239000012458 free base Substances 0.000 description 38
- YXFVVABEGXRONW-UHFFFAOYSA-N Toluene Chemical compound CC1=CC=CC=C1 YXFVVABEGXRONW-UHFFFAOYSA-N 0.000 description 36
- 239000002904 solvent Substances 0.000 description 34
- 239000000243 solution Substances 0.000 description 32
- 239000000203 mixture Substances 0.000 description 30
- 239000003795 chemical substances by application Substances 0.000 description 28
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 28
- IMNFDUFMRHMDMM-UHFFFAOYSA-N N-Heptane Chemical compound CCCCCCC IMNFDUFMRHMDMM-UHFFFAOYSA-N 0.000 description 26
- 238000002411 thermogravimetry Methods 0.000 description 23
- 238000002360 preparation method Methods 0.000 description 22
- KFZMGEQAYNKOFK-UHFFFAOYSA-N Isopropanol Chemical compound CC(C)O KFZMGEQAYNKOFK-UHFFFAOYSA-N 0.000 description 21
- 238000002474 experimental method Methods 0.000 description 20
- 239000007853 buffer solution Substances 0.000 description 17
- 230000004580 weight loss Effects 0.000 description 17
- XEKOWRVHYACXOJ-UHFFFAOYSA-N Ethyl acetate Chemical compound CCOC(C)=O XEKOWRVHYACXOJ-UHFFFAOYSA-N 0.000 description 15
- 238000000354 decomposition reaction Methods 0.000 description 14
- 125000001624 naphthyl group Chemical group 0.000 description 14
- 238000000425 proton nuclear magnetic resonance spectrum Methods 0.000 description 14
- 125000000542 sulfonic acid group Chemical group 0.000 description 14
- 238000005160 1H NMR spectroscopy Methods 0.000 description 13
- 239000013078 crystal Substances 0.000 description 12
- 230000005855 radiation Effects 0.000 description 12
- 230000008859 change Effects 0.000 description 11
- 239000002002 slurry Substances 0.000 description 11
- 241001465754 Metazoa Species 0.000 description 10
- QAOWNCQODCNURD-UHFFFAOYSA-N Sulfuric acid Chemical compound OS(O)(=O)=O QAOWNCQODCNURD-UHFFFAOYSA-N 0.000 description 10
- 238000004458 analytical method Methods 0.000 description 10
- 239000000872 buffer Substances 0.000 description 10
- CSCPPACGZOOCGX-UHFFFAOYSA-N Acetone Chemical compound CC(C)=O CSCPPACGZOOCGX-UHFFFAOYSA-N 0.000 description 9
- 238000004128 high performance liquid chromatography Methods 0.000 description 9
- 238000001990 intravenous administration Methods 0.000 description 9
- 238000005259 measurement Methods 0.000 description 9
- 238000003860 storage Methods 0.000 description 9
- 210000004027 cell Anatomy 0.000 description 8
- 239000007858 starting material Substances 0.000 description 8
- 239000002585 base Substances 0.000 description 7
- 125000002887 hydroxy group Chemical group [H]O* 0.000 description 7
- 239000000843 powder Substances 0.000 description 7
- LSNNMFCWUKXFEE-UHFFFAOYSA-M Bisulfite Chemical compound OS([O-])=O LSNNMFCWUKXFEE-UHFFFAOYSA-M 0.000 description 6
- 150000001732 carboxylic acid derivatives Chemical class 0.000 description 6
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 description 6
- 238000010438 heat treatment Methods 0.000 description 6
- 150000007524 organic acids Chemical class 0.000 description 6
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 5
- 238000002441 X-ray diffraction Methods 0.000 description 5
- 125000003118 aryl group Chemical group 0.000 description 5
- 201000010099 disease Diseases 0.000 description 5
- 238000001802 infusion Methods 0.000 description 5
- 238000013341 scale-up Methods 0.000 description 5
- 238000012216 screening Methods 0.000 description 5
- -1 (pyrrolidin-1-ylmethyl) benzyl Chemical group 0.000 description 4
- DHMQDGOQFOQNFH-UHFFFAOYSA-N Glycine Chemical compound NCC(O)=O DHMQDGOQFOQNFH-UHFFFAOYSA-N 0.000 description 4
- 238000012512 characterization method Methods 0.000 description 4
- 230000000977 initiatory effect Effects 0.000 description 4
- 239000006069 physical mixture Substances 0.000 description 4
- 230000008569 process Effects 0.000 description 4
- 239000012453 solvate Substances 0.000 description 4
- 125000001424 substituent group Chemical group 0.000 description 4
- 238000012360 testing method Methods 0.000 description 4
- LNETULKMXZVUST-UHFFFAOYSA-N 1-naphthoic acid Chemical group C1=CC=C2C(C(=O)O)=CC=CC2=C1 LNETULKMXZVUST-UHFFFAOYSA-N 0.000 description 3
- HEMHJVSKTPXQMS-UHFFFAOYSA-M Sodium hydroxide Chemical compound [OH-].[Na+] HEMHJVSKTPXQMS-UHFFFAOYSA-M 0.000 description 3
- 206010065342 Supraventricular tachyarrhythmia Diseases 0.000 description 3
- 150000007513 acids Chemical class 0.000 description 3
- 230000001154 acute effect Effects 0.000 description 3
- 230000008901 benefit Effects 0.000 description 3
- 239000008280 blood Substances 0.000 description 3
- 210000004369 blood Anatomy 0.000 description 3
- 239000002775 capsule Substances 0.000 description 3
- 150000001875 compounds Chemical class 0.000 description 3
- 230000007423 decrease Effects 0.000 description 3
- DSGUSEBCDAKBCM-UHFFFAOYSA-N ethane-1,2-disulfonic acid;dihydrate Chemical compound O.O.OS(=O)(=O)CCS(O)(=O)=O DSGUSEBCDAKBCM-UHFFFAOYSA-N 0.000 description 3
- 238000001914 filtration Methods 0.000 description 3
- 150000004820 halides Chemical class 0.000 description 3
- 150000004677 hydrates Chemical class 0.000 description 3
- 150000007522 mineralic acids Chemical class 0.000 description 3
- 238000001179 sorption measurement Methods 0.000 description 3
- 238000013112 stability test Methods 0.000 description 3
- 238000003756 stirring Methods 0.000 description 3
- TXKRWVMEUQBFSO-UHFFFAOYSA-N sulfuric acid;trihydrate Chemical compound O.O.O.OS(O)(=O)=O TXKRWVMEUQBFSO-UHFFFAOYSA-N 0.000 description 3
- 230000001225 therapeutic effect Effects 0.000 description 3
- 125000003944 tolyl group Chemical group 0.000 description 3
- QCQCHGYLTSGIGX-GHXANHINSA-N 4-[[(3ar,5ar,5br,7ar,9s,11ar,11br,13as)-5a,5b,8,8,11a-pentamethyl-3a-[(5-methylpyridine-3-carbonyl)amino]-2-oxo-1-propan-2-yl-4,5,6,7,7a,9,10,11,11b,12,13,13a-dodecahydro-3h-cyclopenta[a]chrysen-9-yl]oxy]-2,2-dimethyl-4-oxobutanoic acid Chemical compound N([C@@]12CC[C@@]3(C)[C@]4(C)CC[C@H]5C(C)(C)[C@@H](OC(=O)CC(C)(C)C(O)=O)CC[C@]5(C)[C@H]4CC[C@@H]3C1=C(C(C2)=O)C(C)C)C(=O)C1=CN=CC(C)=C1 QCQCHGYLTSGIGX-GHXANHINSA-N 0.000 description 2
- IJGRMHOSHXDMSA-UHFFFAOYSA-N Atomic nitrogen Chemical compound N#N IJGRMHOSHXDMSA-UHFFFAOYSA-N 0.000 description 2
- 241000282472 Canis lupus familiaris Species 0.000 description 2
- IAZDPXIOMUYVGZ-WFGJKAKNSA-N Dimethyl sulfoxide Chemical compound [2H]C([2H])([2H])S(=O)C([2H])([2H])[2H] IAZDPXIOMUYVGZ-WFGJKAKNSA-N 0.000 description 2
- 239000004471 Glycine Substances 0.000 description 2
- 238000004566 IR spectroscopy Methods 0.000 description 2
- 238000003109 Karl Fischer titration Methods 0.000 description 2
- 241000283973 Oryctolagus cuniculus Species 0.000 description 2
- PMZURENOXWZQFD-UHFFFAOYSA-L Sodium Sulfate Chemical compound [Na+].[Na+].[O-]S([O-])(=O)=O PMZURENOXWZQFD-UHFFFAOYSA-L 0.000 description 2
- FAPWRFPIFSIZLT-UHFFFAOYSA-M Sodium chloride Chemical compound [Na+].[Cl-] FAPWRFPIFSIZLT-UHFFFAOYSA-M 0.000 description 2
- 206010047289 Ventricular extrasystoles Diseases 0.000 description 2
- 230000002378 acidificating effect Effects 0.000 description 2
- 125000001931 aliphatic group Chemical group 0.000 description 2
- 230000003288 anthiarrhythmic effect Effects 0.000 description 2
- 230000000903 blocking effect Effects 0.000 description 2
- 230000000052 comparative effect Effects 0.000 description 2
- 238000011833 dog model Methods 0.000 description 2
- 239000003814 drug Substances 0.000 description 2
- 230000000694 effects Effects 0.000 description 2
- 238000009472 formulation Methods 0.000 description 2
- 239000000499 gel Substances 0.000 description 2
- 229910000042 hydrogen bromide Inorganic materials 0.000 description 2
- 150000002500 ions Chemical class 0.000 description 2
- 239000007788 liquid Substances 0.000 description 2
- 238000012986 modification Methods 0.000 description 2
- 230000004048 modification Effects 0.000 description 2
- 208000010125 myocardial infarction Diseases 0.000 description 2
- 230000036470 plasma concentration Effects 0.000 description 2
- 238000004611 spectroscopical analysis Methods 0.000 description 2
- 238000001228 spectrum Methods 0.000 description 2
- LWIHDJKSTIGBAC-UHFFFAOYSA-K tripotassium phosphate Chemical compound [K+].[K+].[K+].[O-]P([O-])([O-])=O LWIHDJKSTIGBAC-UHFFFAOYSA-K 0.000 description 2
- HNSDLXPSAYFUHK-UHFFFAOYSA-N 1,4-bis(2-ethylhexyl) sulfosuccinate Chemical compound CCCCC(CC)COC(=O)CC(S(O)(=O)=O)C(=O)OCC(CC)CCCC HNSDLXPSAYFUHK-UHFFFAOYSA-N 0.000 description 1
- XMTQQYYKAHVGBJ-UHFFFAOYSA-N 3-(3,4-DICHLOROPHENYL)-1,1-DIMETHYLUREA Chemical compound CN(C)C(=O)NC1=CC=C(Cl)C(Cl)=C1 XMTQQYYKAHVGBJ-UHFFFAOYSA-N 0.000 description 1
- 229920002799 BoPET Polymers 0.000 description 1
- WUVNUFSCTADJFL-UHFFFAOYSA-N C1(=CC=CC=2C(=CC=CC12)S(=O)(=O)O)S(=O)(=O)O.C1(=CC=CC=2C(=CC=CC12)S(=O)(=O)O)S(=O)(=O)O Chemical compound C1(=CC=CC=2C(=CC=CC12)S(=O)(=O)O)S(=O)(=O)O.C1(=CC=CC=2C(=CC=CC12)S(=O)(=O)O)S(=O)(=O)O WUVNUFSCTADJFL-UHFFFAOYSA-N 0.000 description 1
- 241000282693 Cercopithecidae Species 0.000 description 1
- FBPFZTCFMRRESA-KVTDHHQDSA-N D-Mannitol Chemical compound OC[C@@H](O)[C@@H](O)[C@H](O)[C@H](O)CO FBPFZTCFMRRESA-KVTDHHQDSA-N 0.000 description 1
- DJBNUMBKLMJRSA-UHFFFAOYSA-N Flecainide Chemical compound FC(F)(F)COC1=CC=C(OCC(F)(F)F)C(C(=O)NCC2NCCCC2)=C1 DJBNUMBKLMJRSA-UHFFFAOYSA-N 0.000 description 1
- WQZGKKKJIJFFOK-GASJEMHNSA-N Glucose Natural products OC[C@H]1OC(O)[C@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-GASJEMHNSA-N 0.000 description 1
- 102000004310 Ion Channels Human genes 0.000 description 1
- 241000124008 Mammalia Species 0.000 description 1
- 229930195725 Mannitol Natural products 0.000 description 1
- 241000699670 Mus sp. Species 0.000 description 1
- 239000005041 Mylar™ Substances 0.000 description 1
- 238000012565 NMR experiment Methods 0.000 description 1
- 238000005481 NMR spectroscopy Methods 0.000 description 1
- 239000002033 PVDF binder Substances 0.000 description 1
- UIIMBOGNXHQVGW-UHFFFAOYSA-M Sodium bicarbonate Chemical class [Na+].OC([O-])=O UIIMBOGNXHQVGW-UHFFFAOYSA-M 0.000 description 1
- 206010042434 Sudden death Diseases 0.000 description 1
- 206010047281 Ventricular arrhythmia Diseases 0.000 description 1
- 230000002159 abnormal effect Effects 0.000 description 1
- 238000009825 accumulation Methods 0.000 description 1
- 239000004480 active ingredient Substances 0.000 description 1
- XAGFODPZIPBFFR-UHFFFAOYSA-N aluminium Chemical compound [Al] XAGFODPZIPBFFR-UHFFFAOYSA-N 0.000 description 1
- 229910052782 aluminium Inorganic materials 0.000 description 1
- 238000010171 animal model Methods 0.000 description 1
- 239000003416 antiarrhythmic agent Substances 0.000 description 1
- 230000001746 atrial effect Effects 0.000 description 1
- 230000009286 beneficial effect Effects 0.000 description 1
- 230000005540 biological transmission Effects 0.000 description 1
- 230000015572 biosynthetic process Effects 0.000 description 1
- 230000002051 biphasic effect Effects 0.000 description 1
- 239000013590 bulk material Substances 0.000 description 1
- 210000004413 cardiac myocyte Anatomy 0.000 description 1
- 238000005119 centrifugation Methods 0.000 description 1
- 230000001684 chronic effect Effects 0.000 description 1
- 229940069078 citric acid / sodium citrate Drugs 0.000 description 1
- 239000000470 constituent Substances 0.000 description 1
- 239000002178 crystalline material Substances 0.000 description 1
- 238000013480 data collection Methods 0.000 description 1
- 230000018044 dehydration Effects 0.000 description 1
- 238000006297 dehydration reaction Methods 0.000 description 1
- 239000008121 dextrose Substances 0.000 description 1
- 208000035475 disorder Diseases 0.000 description 1
- 238000006073 displacement reaction Methods 0.000 description 1
- 229940079593 drug Drugs 0.000 description 1
- 239000005293 duran Substances 0.000 description 1
- 229950008913 edisilate Drugs 0.000 description 1
- 230000008029 eradication Effects 0.000 description 1
- 210000003527 eukaryotic cell Anatomy 0.000 description 1
- 238000011156 evaluation Methods 0.000 description 1
- 230000001747 exhibiting effect Effects 0.000 description 1
- 229960000449 flecainide Drugs 0.000 description 1
- 238000004108 freeze drying Methods 0.000 description 1
- 239000007789 gas Substances 0.000 description 1
- 239000007903 gelatin capsule Substances 0.000 description 1
- 239000011521 glass Substances 0.000 description 1
- 125000001475 halogen functional group Chemical group 0.000 description 1
- 208000019622 heart disease Diseases 0.000 description 1
- 230000036571 hydration Effects 0.000 description 1
- 238000006703 hydration reaction Methods 0.000 description 1
- 150000003840 hydrochlorides Chemical class 0.000 description 1
- 125000004435 hydrogen atom Chemical group [H]* 0.000 description 1
- 239000012729 immediate-release (IR) formulation Substances 0.000 description 1
- 238000000338 in vitro Methods 0.000 description 1
- 230000001939 inductive effect Effects 0.000 description 1
- 238000012844 infrared spectroscopy analysis Methods 0.000 description 1
- 238000002329 infrared spectrum Methods 0.000 description 1
- 230000002401 inhibitory effect Effects 0.000 description 1
- 230000005764 inhibitory process Effects 0.000 description 1
- 239000010410 layer Substances 0.000 description 1
- 244000144972 livestock Species 0.000 description 1
- 230000007774 longterm Effects 0.000 description 1
- 239000000594 mannitol Substances 0.000 description 1
- 235000010355 mannitol Nutrition 0.000 description 1
- 230000007246 mechanism Effects 0.000 description 1
- 230000004660 morphological change Effects 0.000 description 1
- 239000012452 mother liquor Substances 0.000 description 1
- 150000002790 naphthalenes Chemical class 0.000 description 1
- 230000007935 neutral effect Effects 0.000 description 1
- 229910052757 nitrogen Inorganic materials 0.000 description 1
- 229940100691 oral capsule Drugs 0.000 description 1
- 239000012044 organic layer Substances 0.000 description 1
- 239000002245 particle Substances 0.000 description 1
- 238000005220 pharmaceutical analysis Methods 0.000 description 1
- 239000000825 pharmaceutical preparation Substances 0.000 description 1
- 229940127557 pharmaceutical product Drugs 0.000 description 1
- 229920006254 polymer film Polymers 0.000 description 1
- 229920002981 polyvinylidene fluoride Polymers 0.000 description 1
- 229910000160 potassium phosphate Inorganic materials 0.000 description 1
- 235000011009 potassium phosphates Nutrition 0.000 description 1
- 210000001236 prokaryotic cell Anatomy 0.000 description 1
- 238000010926 purge Methods 0.000 description 1
- 238000011555 rabbit model Methods 0.000 description 1
- 238000002390 rotary evaporation Methods 0.000 description 1
- 238000000926 separation method Methods 0.000 description 1
- CBXWGGFGZDVPNV-UHFFFAOYSA-N so4-so4 Chemical compound OS(O)(=O)=O.OS(O)(=O)=O CBXWGGFGZDVPNV-UHFFFAOYSA-N 0.000 description 1
- 239000011780 sodium chloride Substances 0.000 description 1
- 229910052938 sodium sulfate Inorganic materials 0.000 description 1
- 235000011152 sodium sulphate Nutrition 0.000 description 1
- 238000002336 sorption--desorption measurement Methods 0.000 description 1
- 230000003595 spectral effect Effects 0.000 description 1
- 239000008227 sterile water for injection Substances 0.000 description 1
- 239000000126 substance Substances 0.000 description 1
- 238000006467 substitution reaction Methods 0.000 description 1
- 229940124530 sulfonamide Drugs 0.000 description 1
- 150000003456 sulfonamides Chemical class 0.000 description 1
- BDHFUVZGWQCTTF-UHFFFAOYSA-M sulfonate Chemical compound [O-]S(=O)=O BDHFUVZGWQCTTF-UHFFFAOYSA-M 0.000 description 1
- 150000003460 sulfonic acids Chemical class 0.000 description 1
- 229910021653 sulphate ion Inorganic materials 0.000 description 1
- 238000013268 sustained release Methods 0.000 description 1
- 239000012730 sustained-release form Substances 0.000 description 1
- 208000024891 symptom Diseases 0.000 description 1
- 208000011580 syndromic disease Diseases 0.000 description 1
- 210000001519 tissue Anatomy 0.000 description 1
- 238000004448 titration Methods 0.000 description 1
- 230000000699 topical effect Effects 0.000 description 1
- 150000004684 trihydrates Chemical group 0.000 description 1
- 230000002861 ventricular Effects 0.000 description 1
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/40—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having five-membered rings with one nitrogen as the only ring hetero atom, e.g. sulpiride, succinimide, tolmetin, buflomedil
- A61K31/4025—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having five-membered rings with one nitrogen as the only ring hetero atom, e.g. sulpiride, succinimide, tolmetin, buflomedil not condensed and containing further heterocyclic rings, e.g. cromakalim
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P9/00—Drugs for disorders of the cardiovascular system
- A61P9/06—Antiarrhythmics
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C303/00—Preparation of esters or amides of sulfuric acids; Preparation of sulfonic acids or of their esters, halides, anhydrides or amides
- C07C303/32—Preparation of esters or amides of sulfuric acids; Preparation of sulfonic acids or of their esters, halides, anhydrides or amides of salts of sulfonic acids
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C303/00—Preparation of esters or amides of sulfuric acids; Preparation of sulfonic acids or of their esters, halides, anhydrides or amides
- C07C303/42—Separation; Purification; Stabilisation; Use of additives
- C07C303/44—Separation; Purification
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C309/00—Sulfonic acids; Halides, esters, or anhydrides thereof
- C07C309/01—Sulfonic acids
- C07C309/02—Sulfonic acids having sulfo groups bound to acyclic carbon atoms
- C07C309/03—Sulfonic acids having sulfo groups bound to acyclic carbon atoms of an acyclic saturated carbon skeleton
- C07C309/05—Sulfonic acids having sulfo groups bound to acyclic carbon atoms of an acyclic saturated carbon skeleton containing at least two sulfo groups bound to the carbon skeleton
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D295/00—Heterocyclic compounds containing polymethylene-imine rings with at least five ring members, 3-azabicyclo [3.2.2] nonane, piperazine, morpholine or thiomorpholine rings, having only hydrogen atoms directly attached to the ring carbon atoms
- C07D295/04—Heterocyclic compounds containing polymethylene-imine rings with at least five ring members, 3-azabicyclo [3.2.2] nonane, piperazine, morpholine or thiomorpholine rings, having only hydrogen atoms directly attached to the ring carbon atoms with substituted hydrocarbon radicals attached to ring nitrogen atoms
- C07D295/12—Heterocyclic compounds containing polymethylene-imine rings with at least five ring members, 3-azabicyclo [3.2.2] nonane, piperazine, morpholine or thiomorpholine rings, having only hydrogen atoms directly attached to the ring carbon atoms with substituted hydrocarbon radicals attached to ring nitrogen atoms substituted by singly or doubly bound nitrogen atoms
- C07D295/135—Heterocyclic compounds containing polymethylene-imine rings with at least five ring members, 3-azabicyclo [3.2.2] nonane, piperazine, morpholine or thiomorpholine rings, having only hydrogen atoms directly attached to the ring carbon atoms with substituted hydrocarbon radicals attached to ring nitrogen atoms substituted by singly or doubly bound nitrogen atoms with the ring nitrogen atoms and the substituent nitrogen atoms separated by carbocyclic rings or by carbon chains interrupted by carbocyclic rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D403/00—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00
- C07D403/02—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00 containing two hetero rings
- C07D403/10—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00 containing two hetero rings linked by a carbon chain containing aromatic rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07B—GENERAL METHODS OF ORGANIC CHEMISTRY; APPARATUS THEREFOR
- C07B2200/00—Indexing scheme relating to specific properties of organic compounds
- C07B2200/13—Crystalline forms, e.g. polymorphs
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Health & Medical Sciences (AREA)
- Medicinal Chemistry (AREA)
- Veterinary Medicine (AREA)
- Public Health (AREA)
- Animal Behavior & Ethology (AREA)
- General Health & Medical Sciences (AREA)
- Pharmacology & Pharmacy (AREA)
- Life Sciences & Earth Sciences (AREA)
- Epidemiology (AREA)
- Engineering & Computer Science (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Heart & Thoracic Surgery (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- General Chemical & Material Sciences (AREA)
- Cardiology (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Acyclic And Carbocyclic Compounds In Medicinal Compositions (AREA)
- Materials Engineering (AREA)
- Polymers & Plastics (AREA)
- Organic Low-Molecular-Weight Compounds And Preparation Thereof (AREA)
- Inorganic Chemistry (AREA)
Abstract
Description
本出願は、2019年1月29日出願の米国仮出願第62/798,467号、および2020年1月10日出願の米国仮出願第62/959,687号に基づく優先権を主張するものであり、これら仮出願の全体は参照により本明細書に引用される。
本明細書では、結晶性サルカルディン(sulcardine)塩を含むがサルカルディンの硫酸塩を除くサルカルディン塩が提供される。加えて、サルカルディン塩を含む医薬組成物、およびサルカルディン塩を有効量で投与する工程を含む不整脈を処置する方法も提供される。
ある実施形態では、本明細書にはサルカルディンのナフタレン-1,5-ジスルホン酸塩が提供される。いくつかの実施形態では、前記塩は結晶性である。
ある実施形態では、本明細書にはサルカルディンの1-ヒドロキシ-2-ナフトエ酸塩の形態Iが提供される。いくつかの実施形態では、前記塩は結晶性である。
ある実施形態では、本明細書にはサルカルディンの1-ヒドロキシ-2-ナフトエ酸塩の形態IIが提供される。いくつかの実施形態では、前記塩は結晶性である。
ある実施形態では、本明細書にはサルカルディンのナフタレン-2-スルホン酸塩が提供される。いくつかの実施形態では、前記塩は結晶性である。
ある実施形態では、本明細書にはサルカルディン塩酸塩の形態Iが提供される。いくつかの実施形態では、前記塩は結晶性である。
ある実施形態では、本明細書にはサルカルディン塩酸塩の形態IIが提供される。いくつかの実施形態では、前記塩は結晶性である。
ある実施形態では、本明細書にはサルカルディンのエタン-1,2-ジスルホン酸塩が提供される。いくつかの実施形態では、前記塩は結晶性である。
ある実施形態では、本明細書にはサルカルディンのエタン-1,2-ジスルホン酸塩が提供される。いくつかの実施形態では、前記塩は結晶性である。
ある実施形態では、本明細書にはサルカルディンのエタン-1,2-ジスルホン酸塩が提供される。いくつかの実施形態では、前記塩は結晶性である。
ある実施形態では、本明細書にはサルカルディン臭化水素酸塩が提供される。いくつかの実施形態では、前記塩は結晶性である。
Pixcel検出器(128チャネル)を備えたPANalytical X’pert proの上でXRPD解析を実施し、試料を3~35°2Θで走査した。Mylarのポリマーフィルムを備えたマルチウェルプレート上に材料を載せ、試料を支持した。その後、マルチウェルプレートを回折計に入れ、Cu K放射(α1λ=1.54060Å、α2=1.54443Å、β=1.39225Å、α1:α2比=0.5)を用いて解析し、40kV/40mAの発電機設定を使用して伝達モード(ステップサイズ0.0130°2°Θ、ステップ時間18.87s)で作動させた。HighScore Plus4.7のデスクトップアプリケーション(PANalytical,2017)を使用してデータを可視化し、画像を生成した。
サルカルディン硫酸塩三水和物を酢酸エチル(16vol.)と飽和重炭酸ナトリウム溶液(16vol.)に溶かした。この二相性溶液を分離漏斗に移し、層を分離した。有機質層を硫酸ナトリウムで乾燥させ、次いで溶剤を回転蒸発により取り除き、結果生じた油を周囲温度で約3時間、真空下で乾燥させた。図4は、結果として生じた非晶質サルカルディン遊離塩基のXRPDパターンである。全例に対し、以下に詳述する最初のスクリーニング作業をサルカルディン遊離塩基10mg上で行った。全XRPDディフラクトグラムをサルカルディン硫酸塩三水和物、サルカルディン遊離塩基、および関連するカウンターイオンと比較すると、明確に異なることが分かった。
緩衝液20mMをpH1.2(HCl/KCl)、pH3.0(HCl/グリシン)、pH4.0(クエン酸/クエン酸ナトリウム)、およびpH7.4(一塩基性リン酸カリウム/NaOH)に調製した。各緩衝液0.5mLに適切な塩を加え、スラリーを形成した。スラリーのpHを測定し、必要に応じて0.2M緩衝液成分(例えば0.2M HCl(aq))を用いて所望のpH(緩衝液の初期pH)に戻した。試料を周囲温度で約72時間かけてスラリー状にした。
サルカルディン遊離塩基にナフタレン-1,5-ジスルホン酸(1.05eq.)とアセトン(20vol.)を加えた。4時間周期で約72時間かけて試料を周囲温度と40℃との間の温度サイクルにかけると、白色と橙色の固体が残った。
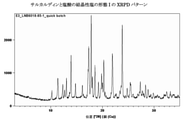
サルカルディン遊離塩基(200mg)にアセトン2mLとナフタレン-1,5-ジスルホン酸169.8mg(1.05eq.)を加えた。この試料を実施例16に従い温度サイクルにかけた。結果として得た固体をBuchner漏斗により濾過し、フィルタを約15分間乾燥させた。図1は本実施例のXRPDパターンを示す。図1はこの塩のXRPDパターンであり、塩が結晶性であることを示している。ピークの表は表2に示す。分解が生じるまでTGに重量損失はなく、244℃の開始温度でDTAに融解事象を認めた(図2)。ナフタレン-1,5-ジスルホン酸を1H-NMRに1:1で認めたが、顕著な溶剤を認めなかった(図3)。溶解度を測定すると、pH1.2の緩衝液では1.6mg・mL-1、pH3.0の緩衝液では0.7mg・mL-1、pH4.0の緩衝液では1.0mg・mL-1、およびpH7.4の緩衝液では6.9mg・mL-1であった(表3)。
1Mの1-ヒドロキシ-2-ナフトエ酸貯蔵液をTHF(1.05eq.)と酢酸エチル(20vol.)に溶かしたものをサルカルディン遊離塩基に加えた。4時間周期で約72時間かけて試料を周囲温度と40℃との間の温度サイクルにかけ、次いで冷蔵庫に約24時間置くと、茶色の固体が残った。
1Mの1-ヒドロキシ-2-ナフトエ酸貯蔵液をTHF(1.05eq.)とトルエン(20vol.)に溶かしたものをサルカルディン遊離塩基に加えた。4時間周期で約72時間かけて試料を周囲温度と40℃との間の温度サイクルにかけ、次いで冷蔵庫に約24時間置いた。試料を包含するバイアルを開封し、溶剤を蒸発させると、白色と茶色の固体が残った。
トルエン2mLと1Mの1-ヒドロキシ-2-ナフト酸溶液457μLをTHFに溶かしたものを、サルカルディン遊離塩基200mgに加えた。この試料を実施例16に従い温度サイクルにかけた。固体をBuchner漏斗により濾過し、フィルタを約15分間乾燥させた。
1Mのナフタレン-2-スルホン酸貯蔵液をTHF(1.05eq.)と酢酸エチル(20vol.)に溶かしたものをサルカルディン遊離塩基に加えた。4時間周期で約72時間かけて試料を周囲温度と40℃との間の温度サイクルにかけた。ヘプタン(10vol.)を加え、試料を冷凍庫に約24時間置いた。試料を包含するバイアルを開封し、溶剤を蒸発させると、白色と橙色の固体が残った。
トルエン2mLと1Mのナフタレン-2-スルホン酸溶液457μLをTHFに溶かしたものを、サルカルディン遊離塩基200mgに加えた。この試料を実施例16に従い温度サイクルにかけた。固体をBuchner漏斗により濾過し、フィルタを乾燥して白色固体を得た。
1MのHCl貯蔵液をTHF(1.05eq.)、2-プロパノール(20vol.)、およびヘプタン(10vol.)に溶かしたものを、サルカルディン遊離塩基に加えた。4時間周期で約72時間かけて試料を周囲温度と40℃との間の温度サイクルにかけた。追加のヘプタン(20vol.)を加え、試料を冷凍庫に約24時間置くと、白色固体が残った。この材料はXRPDにより結晶性であった(図17A)。
2mLのTHFと1Mの塩酸溶液457μLをTHFに溶かしたものを、サルカルディン遊離塩基200mgに加えた。この試料を実施例16に従い温度サイクルにかけた。固体をBuchner漏斗により濾過し、フィルタを乾燥して白色固体を得た。
1Mのエタン-1,2-ジスルホン酸貯蔵液をTHF(1.05eq.)、トルエン(20vol.)、およびヘプタン(10vol.)に溶かしたものを、サルカルディン遊離塩基に加えた。4時間周期で約72時間かけて試料を周囲温度と40℃との間の温度サイクルにかけた。追加のヘプタン(20vol.)を加え、試料を冷凍庫に約24時間置くと、白色固体が残った。
トルエン2mLおよび1Mのエタン-1,2-ジスルホン酸溶液218μlをTHF(0.55eq.)に溶かしたものを、サルカルディン遊離塩基200mgに加えた。この試料を実施例16に従い温度サイクルにかけた。固体をBuchner漏斗により濾過して乾燥して、白色固体を得た。
1MのHBr貯蔵液をTHF(1.05eq.)、2-プロパノール(20vol.)、およびヘプタン(10vol.)に溶かしたものを、サルカルディン遊離塩基に加えた。4時間周期で約72時間かけて試料を周囲温度と40℃との間の温度サイクルにかけた。さらにヘプタン(20vol.)を加え、試料を冷凍庫に約24時間置いた。試料を包含するバイアルを開封し、溶剤を蒸発させると、橙色の固体が残った。
以下の方法を用いて撹拌しながら温度サイクルを行った。
1. 25℃で1時間保持
2. 0.1℃/分で5℃に冷却
3. 5℃で1時間保持
4. 0.1℃/分で25℃に加熱
5. 上記を計72時間繰り返し、5℃でサンプルを取り除く
サルカルディン遊離塩基約3gを包含する溶液にトルエン45mLを加え、溶液を形成した。この溶液に、1Mのエタン-1,2-ジスルホン酸貯蔵液(エタン-1,2-ジスルホン酸二水和物をTHFに使用したもの)約6.85mL(1.05eq.)を加え、ガム状の固体を形成した。4時間周期で約24時間、この溶液を周囲温度と40℃との間の温度サイクルにかけた。24時間後、フラスコ内に少量の白色の自由流動固体を認め、フラスコ内にガム状の白色材料からなる大きな塊を認めた。両材料は、XRPD(図32における回折パターンLNB15318-53-1-SlurryおよびLNB15318-53-1-Bulk)により主に非晶質で現れた。次いで、この材料をさらに24時間温度サイクルにかけた。48時間後、自由流動オフホワイト粉末とオフホワイト固体凝集物との混合物をフラスコ内に認めた。自由流動材料のアリコートを集めてXRPD解析を行い、このパターンを図33に認めることができる(回折パターンLNB15318-53-1-48h)。材料をBuchner濾過により濾過し、周囲温度で約24時間、真空下で乾燥させた。乾燥材料を集めて秤量し、XRPD(図26と33の回折パターンLNB15318-53-1-Dry)により解析した。この回折パターンLNB15318-53-1-Dryを使用して形態Iのピークリストを作成した。
サルカルディン遊離塩基約4gを包含する溶液にトルエン60mLを加え、溶液を形成した。この溶液に、1Mのエタン-1,2-ジスルホン酸貯蔵液(エタン-1,2-ジスルホン酸二水和物をTHFに使用したもの)9.34mL(1.05eq.)を加え、ガム状の固体を形成した。4時間周期で約96時間撹拌しながら、この試料を周囲温度と40℃との間の温度サイクルにかけた。自由流動性のオフホワイト粉末を認めた。湿った固体試料をXRPDにより解析した。この材料は、モノエジシル酸塩の形態Iと、ここで形態IIと称するものとの混合物として生じた(図34の回折パターンLNB1919-44-1)。固体をBuchner濾過により分離し、周囲温度で一晩、真空下で乾燥させた。乾燥した材料を集めて100mL Duranフラスコに移した。EtOH/水(0.4aw)40mLを加え、移動性のスラリーを形成した。次いで、このスラリーを周囲温度で約120時間、撹拌バーを用いて撹拌した。材料のアリコートを採取し、XRPDにより解析した(図28と図35の回折パターンLNB1919-44-3)。この材料をモノエジシル酸塩形態IIと同定した。バルク材料をBuchner濾過により分離し、周囲温度で約24時間、真空下で乾燥させた。乾燥した材料をXRPDにより解析し(図35の回折パターンLNB1919-44-3-Dry)、この材料が形態IIであることを認めた。この回折パターンLNB1919-44-3-Dryを使用して形態IIのピークリストを作成した。
サルカルディン遊離塩基約100mgをトルエン2mLに溶かした。これに1Mのエタン-1,2-ジスルホン酸貯蔵液(エタン-1,2-ジスルホン酸二水和物をTHFに使用したもの)229μlを加えた。試料を4時間サイクルで、周囲温度と40℃との間の温度サイクルにかけた。この材料のアリコートを約24時間後に集め、さらに24時間温度サイクルにかけた。材料のアリコートを採取し、XRPDにより解析した。独特の結晶パターンを認めた。このパターンは図32のLNB15318-51-1 48hrであり、モノエジシル酸塩の形態Iと表記した。
形態IのGVS特徴化中に初めて形態IIを認めた。形態IのGVS解析後に集めた材料をXRPDにより解析した。より高値の水和物の形成を示す新たなパターン(形態II)を認めた。XRPD対照は図34の「LNB15318-53-1-PostGVS」である。
形態I約26mgをメッシュ蒸気吸着天秤皿に載せ、Hiden AnalyticalのIGASorp Moisture Sorption Analyser balanceに装填した。試料を40~90%相対湿度(RH)から増分10%でランピングプロファイルにかけ、25℃で安定重量を達成する(98%工程完了、最短工程時間30分、最長工程時間60分)まで各工程で試料を維持した。収着サイクル完了後、同じ手順を用いて試料を0%RHまで乾燥させ、最終的に40%RHの出発点に戻した。2つのサイクルを行った。収着/脱着サイクル中の重量変化をプロットし、試料の吸湿性を求めた。GVS解析後に集めた材料をXRPDにより解析した。
KF解析のため材料約30mgを秤量し、予め秤量したガラスバイアルに入れた。次いで、この材料を、ヒドラナール溶液を包含するKF電量計の滴定セルに加えた。空のバイアルを固体の添加後に逆秤量して、細胞に加えた材料の質量を求めた。次いで試料を滴定した。解析を二通り行い、結果の平均を算出した。
Agilent Supernova単結晶x線回折計を用いて密閉管により生成されるMo Kα放射(λ=0.71073Å)を使用して、サルカルディンの1-ヒドロキシ-2-ナフトエ酸塩の形態IIの単結晶X線解析を120Kで行った。単斜空間群P21/n(a=10.2443(2)Å、b=29.9171(6)Å、c=10.8406(3)Å、β=103.375(2)°、容量=3232.31(13)Å3、Z=4、Z’=1)を対象に、全データを縮尺し、解決し、洗練させた。5.79%のR1(I>(2σI))値に戻る2Θ範囲5.622~65.972°の123397(11798固有)の反射を使用して、最終モデルを構築し、サルカルディンの予測構造を確認した。非対称単位(図36)は、1つの関連する1-ヒドロキシ-2-ナフトエ酸カウンターイオン(1:1のサルカルディン:カウンターイオン比)とともに1つの完全なサルカルディン分子を包含することを認めた。塩の形態IIと一致した120Kで集めたデータを使用し、特徴的な実験XRPD2Θディフラクトグラムを算出した。結晶データを表13に示す。
赤外分光法をBruker ALPHA P分光計上で行った。十分な材料を分光計のプレートの中心に置き、以下のパラメータを用いてスペクトルを得た。
解像度:4cm-1
バックグラウンドスキャン時間:16スキャン
試料スキャン時間:16スキャン
データ収集:4000~400cm-1
結果スペクトル:透過率
ソフトウェア:OPUSバージョン6
サルカルディン硫酸塩三水和物、ナフトエ酸塩形態II(1-ヒドロキシ-2-ナフトエ酸塩の形態II)、およびモノエジシル酸塩の形態IIにおける熱力学的溶解度は、0.9%塩化ナトリウム溶液と水中5%デキストロースからなる培地において求めた。
本試験の薬物動態学的な目的は、薬物動態試験中に雄イヌにサルカルディン硫酸塩、サルカルディンナフトエ酸塩、またはサルカルディンモノエジシル酸塩(形態II)を経口カプセル投与または静脈内(IV)注入した後のサルカルディンへの曝露を評価することであった。
サルカルディンの単回経口投与後のCmax値は、硫酸塩製剤群では2820ng/mL(図38A)、モノエジシル酸塩製剤群では4570ng/mL(図38B)であった。各群すべての動物のデータを使用し、平均薬物動態パラメータを算出した。経口モノエジシル酸基の値は動物2001を含んでおり(図38B)、これは異常値であると考えられ、投薬の誤りを反映する場合がある。動物2001のデータがなければ、モノエジシル酸塩製剤群のCmax値はおそらく4570ng/mlより高い。サルカルディンの中央ピーク血漿中濃度を、サルカルディン硫酸塩製剤群では投与後2時間(Tmax 2hr)で、モノエジシル酸塩製剤群では投与後0.5時間(Tmax 0.5hr)で認めた。
Claims (64)
- サルカルディンの酸塩を含む固体形態であって、酸はエタン-1,2-ジスルホン酸、ナフタレン-1,5-ジスルホン酸、1-ヒドロキシ-2-ナフトエ酸、ナフタレン-2-スルホン酸、塩酸、または臭化水素酸である、固体形態。
- 前記固体形態が結晶性である、請求項1に記載の固体形態。
- サルカルディンのエタン-1,2-ジスルホン酸塩を含む、請求項1に記載の固体形態。
- 約18.8、20.2、および21.2°2Θのピークを含むXRPDパターンを特徴とする、請求項3に記載の固体形態。
- 前記XRPDパターンは約9.2、10.4、および13.8°2Θのピークをさらに含む、請求項4に記載の固体形態。
- 前記XRPDパターンは約9.6、14.2、および14.9°2Θのピークをさらに含む、請求項5に記載の固体形態。
- 図26に提示されるXRPDパターンと一致するXRPDパターンを特徴とする、請求項4に記載の固体形態。
- 約14.2°2ΘのXRPDピーク、および約3500cm-1超のピークを含むFT-IRスペクトルを特徴とする、請求項3に記載の固体形態。
- 約5.2°2Θのピークが存在しない場合の約14.2°2ΘのXRPDピーク、および約3500cm-1超のピークを含むFT-IRスペクトルを特徴とし、かつ、場合により約1206cm-1と約814cm-1の1つ以上のFT-IRピークをさらに含む、請求項8に記載の固体形態。
- 2つのピークが約9.0°2Θと約9.8°2Θとの間にあるXRPDパターンであって、場合により2つのピーク間の差が約0.4°2ΘであるXRPDパターン、および約3500cm-1超のピークを含むFT-IRスペクトルを特徴とし、かつ、場合により約1206cm-1と約814cm-1の1つ以上のFT-IRピークをさらに含む、請求項3に記載の固体形態。
- 約9.2°2Θ、約9.6°2Θ、約10.4°2Θ、約13.8°2Θ、約14.2°2Θ、および約14.9°2Θの1つ以上のピークを含むXRPDパターン、ならびに約3500cm-1超のピークを含むFT-IRスペクトルを特徴とし、かつ、場合により約1206cm-1と約814cm-1の1つ以上のFT-IRピークをさらに含む、請求項3に記載の固体形態。
- 約3500cm-1超のピークが約3556cm-1である、請求項8から11のいずれか1つに記載の固体形態。
- サルカルディンのモノエタン-1,2-ジスルホン酸塩である、請求項4から12のいずれか1つに記載の固体形態。
- サルカルディンのモノエタン-1,2-ジスルホン酸塩の一水和物である、請求項13に記載の固体形態。
- 約15.7、16.9、および23.6°2Θのピークを含むXRPDパターンを特徴とする、請求項3に記載の固体形態。
- 前記XRPDパターンは約5.2、9.1、および11.3°2Θのピークをさらに含む、請求項15に記載の固体形態。
- 前記XRPDパターンは約17.6および19.2°2Θのピークをさらに含む、請求項16に記載の固体形態。
- 図28に提示されるXRPDパターンと一致するXRPDパターンを特徴とする、請求項15に記載の固体形態。
- ピークが約5.2°2ΘであるXRPDパターン、および約3500cm-1より上でピークを含まないFT-IRスペクトルを特徴とし、かつ、場合により約3374cm-1と約826cm-1の1つ以上のピークをさらに含む、請求項3に記載の固体形態。
- 約5.2°2Θ、約9.1°2Θ、約10.2°2Θ、約10.8°2Θ、約11.3°2Θ、約13.6°2Θ、および約15.7°2Θの1つ以上のピークを含むXRPDパターン、ならびに約3500cm-1より上でピークを含まないFT-IRスペクトルを特徴とし、かつ、場合により約3374cm-1と約826cm-1の1つ以上のピークをさらに含む、請求項3に記載の固体形態。
- サルカルディンのモノエタン-1,2-ジスルホン酸塩である、請求項15から20のいずれか1つに記載の固体形態。
- サルカルディンのモノエタン-1,2-ジスルホン酸塩の二水和物である、請求項21に記載の固体形態。
- 約14.1、17.8、および23.7°2Θのピークを含むXRPDパターンを特徴とする、請求項3に記載の固体形態。
- 前記XRPDパターンは約5.6および14.9°2Θのピークをさらに含む、請求項23に記載の固体形態。
- 前記XRPDパターンは約11.0および13.0°2Θのピークをさらに含む、請求項24に記載の固体形態。
- 図19に提示されるXRPDパターンと一致するXRPDパターンを特徴とする、請求項23に記載の固体形態。
- サルカルディンのヘミ-エタン-1,2-ジスルホン酸塩である、請求項23から26のいずれか1つに記載の固体形態。
- サルカルディンのナフタレン-1,5-ジスルホン酸塩を含む、請求項1に記載の固体形態。
- 約14.9、15.9、および23.6°2Θのピークを含むXRPDパターンを特徴とする、請求項28に記載の固体形態。
- 前記XRPDパターンは約4.9および10.4°2Θのピークをさらに含む、請求項29に記載の固体形態。
- 前記XRPDパターンは約11.3、12.3、および19.0°2Θのピークをさらに含む、請求項30に記載の固体形態。
- 図1に提示されるXRPDパターンと一致するXRPDパターンを特徴とする、請求項29に記載の固体形態。
- サルカルディンの1-ヒドロキシ-2-ナフトエ酸塩を含む、請求項1に記載の固体形態。
- 約16.8、18.6、および18.9°2Θのピークを含むXRPDパターンを特徴とする、請求項33に記載の固体形態。
- 前記XRPDパターンは約6.7および6.9°2Θのピークをさらに含む、請求項34に記載の固体形態。
- 前記XRPDパターンは約13.8、20.3、および20.8°2Θのピークをさらに含む、請求項35に記載の固体形態。
- 図6に提示されるXRPDパターンと一致するXRPDパターンを特徴とする、請求項34に記載の固体形態。
- 約5.8、18.6、および19.9°2Θのピークを含むXRPDパターンを特徴とする、請求項33に記載の固体形態。
- 前記XRPDパターンは約10.6、17.8、および21.4°2Θのピークをさらに含む、請求項38に記載の固体形態。
- 前記XRPDパターンは約20.6および25.3°2Θのピークをさらに含む、請求項39に記載の固体形態。
- 図9に提示されるXRPDパターンと一致するXRPDパターンを特徴とする、請求項38に記載の固体形態。
- およそa=10.2Å、b=29.9Å、c=10.8Å、α=90°、β=103.4°、γ=90°の単位セル寸法を有する、請求項38から41のいずれか1つに記載の固体形態。
- サルカルディンのナフタレン-2-スルホン酸塩を含む、請求項1に記載の固体形態。
- 約17.2、17.8、および21.3°2Θのピークを含むXRPDパターンを特徴とする、請求項43に記載の固体形態。
- 前記XRPDパターンは約13.3、13.5、16.6、および16.9°2Θのピークをさらに含む、請求項44に記載の固体形態。
- 前記XRPDパターンは約9.4および10.6°2Θのピークをさらに含む、請求項45に記載の固体形態。
- 図13に提示されるXRPDパターンと一致するXRPDパターンを特徴とする、請求項44に記載の固体形態。
- サルカルディン塩酸塩を含む、請求項1に記載の固体形態。
- 約12.3、13.0、および17.8°2Θのピークを含むXRPDパターンを特徴とする、請求項48に記載の固体形態。
- 前記XRPDパターンは約13.9、17.4、および23.9°2Θのピークをさらに含む、請求項49に記載の固体形態。
- 前記XRPDパターンは約20.3および21.9°2Θのピークをさらに含む、請求項50に記載の固体形態。
- 図17に提示されるXRPDパターンと一致するXRPDパターンを特徴とする、請求項49に記載の固体形態。
- 約13.5、19.6、および20.6°2Θのピークを含むXRPDパターンを特徴とする、請求項48に記載の固体形態。
- 前記XRPDパターンは約10.1、11.8、および16.4°2Θのピークをさらに含む、請求項53に記載の固体形態。
- 前記XRPDパターンは約17.8、19.4、および25.5°2Θのピークをさらに含む、請求項54に記載の固体形態。
- 図17Aに提示されるXRPDパターンと一致するXRPDパターンを特徴とする、請求項53に記載の固体形態。
- サルカルディン臭化水素酸塩を含む、請求項1に記載の固体形態。
- 約17.9、19.7、および24.0°2Θのピークを含むXRPDパターンを特徴とする、請求項57に記載の固体形態。
- 前記XRPDパターンは約14.1および14.9°2Θのピークをさらに含む、請求項58に記載の固体形態。
- 前記XRPDパターンは約5.7、13.0、および16.2°2Θのピークをさらに含む、請求項59に記載の固体形態。
- 図23に提示されるXRPDパターンと一致するXRPDパターンを特徴とする、請求項58に記載の固体形態。
- 請求項1から61のいずれか1つに記載の固体形態と、1つ以上の薬学的に許容可能な賦形剤とを含む、医薬組成物。
- 不整脈を処置する方法であって、請求項1から61のいずれか1つに記載の固体形態または請求項62に記載の医薬組成物を治療上有効な量で対象に投与する工程を含む、方法。
- 前記不整脈は、心房細動、上室性頻脈性不整脈、心室性期外収縮、心室頻拍、または心室細動である、請求項63に記載の方法。
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2023188791A JP2024039020A (ja) | 2019-01-29 | 2023-11-02 | サルカルディン塩 |
Applications Claiming Priority (5)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US201962798467P | 2019-01-29 | 2019-01-29 | |
| US62/798,467 | 2019-01-29 | ||
| US202062959687P | 2020-01-10 | 2020-01-10 | |
| US62/959,687 | 2020-01-10 | ||
| PCT/US2020/015370 WO2020159959A1 (en) | 2019-01-29 | 2020-01-28 | Sulcardine salts |
Related Child Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2023188791A Division JP2024039020A (ja) | 2019-01-29 | 2023-11-02 | サルカルディン塩 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2022518906A true JP2022518906A (ja) | 2022-03-17 |
| JPWO2020159959A5 JPWO2020159959A5 (ja) | 2022-10-31 |
Family
ID=69724142
Family Applications (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2021542541A Pending JP2022518906A (ja) | 2019-01-29 | 2020-01-28 | サルカルディン塩 |
| JP2023188791A Pending JP2024039020A (ja) | 2019-01-29 | 2023-11-02 | サルカルディン塩 |
Family Applications After (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2023188791A Pending JP2024039020A (ja) | 2019-01-29 | 2023-11-02 | サルカルディン塩 |
Country Status (15)
| Country | Link |
|---|---|
| US (3) | US11426382B2 (ja) |
| EP (1) | EP3917921A1 (ja) |
| JP (2) | JP2022518906A (ja) |
| KR (2) | KR102697726B1 (ja) |
| CN (2) | CN112638903B (ja) |
| AU (1) | AU2020216925B2 (ja) |
| BR (1) | BR112021014640A8 (ja) |
| CA (1) | CA3128152A1 (ja) |
| CL (1) | CL2021001968A1 (ja) |
| CO (1) | CO2021011042A2 (ja) |
| IL (1) | IL285184B2 (ja) |
| MX (2) | MX2021009033A (ja) |
| SG (1) | SG11202108160YA (ja) |
| WO (1) | WO2020159959A1 (ja) |
| ZA (2) | ZA202105344B (ja) |
Families Citing this family (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2020123824A1 (en) | 2018-12-13 | 2020-06-18 | Huya Bioscience International, Llc | Sulcardine administration for treatment of acute atrial fibrillation |
| CA3128152A1 (en) | 2019-01-29 | 2020-08-06 | Huya Bioscience International, Llc | Sulcardine salts |
| AU2021288056A1 (en) | 2020-06-12 | 2023-02-09 | Huyabio International, Llc | Sulcardine administration for treatment of acute atrial fibrillation |
Citations (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2013511473A (ja) * | 2009-11-17 | 2013-04-04 | フヤ バイオサイエンス インターナショナル エルエルシー | 心房細動の治療 |
| JP2013511472A (ja) * | 2009-11-17 | 2013-04-04 | フヤ バイオサイエンス インターナショナル エルエルシー | サルカルディン及びその塩の緩速点滴 |
| JP2018506562A (ja) * | 2015-02-26 | 2018-03-08 | ジェネンテック, インコーポレイテッド | ピロロピリジン化合物の結晶形態 |
| WO2018156895A1 (en) * | 2017-02-24 | 2018-08-30 | Gilead Sciences, Inc. | Inhibitors of bruton's tyrosine kinase |
Family Cites Families (8)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN1172908C (zh) * | 1999-12-10 | 2004-10-27 | 中国科学院上海药物研究所 | N-取代苄基或苯基芳香磺酰胺化合物及其用途 |
| CN1299813C (zh) | 2004-12-28 | 2007-02-14 | 华南理工大学 | 自动撕膜落料及多样性搅拌的机构和控制装置 |
| CN1939298A (zh) * | 2005-09-29 | 2007-04-04 | 中国科学院上海药物研究所 | 硫酸舒欣啶固体和靶向制剂及其制备方法 |
| AU2016272089B2 (en) | 2015-06-03 | 2021-02-18 | Triastek, Inc. | Dosage forms and use thereof |
| EP3452003A4 (en) | 2016-05-05 | 2019-06-26 | Triastek, Inc. | PHARMACEUTICAL FORM WITH CONTROLLED RELEASE |
| EP3573602A4 (en) | 2017-01-26 | 2020-09-16 | Triastek, Inc. | DOSAGE FORMS OF CONTROLLED RELEASE AT SPECIFIC GASTROINTESTINAL SITES |
| WO2020123824A1 (en) | 2018-12-13 | 2020-06-18 | Huya Bioscience International, Llc | Sulcardine administration for treatment of acute atrial fibrillation |
| CA3128152A1 (en) | 2019-01-29 | 2020-08-06 | Huya Bioscience International, Llc | Sulcardine salts |
-
2020
- 2020-01-28 CA CA3128152A patent/CA3128152A1/en active Pending
- 2020-01-28 CN CN202080004796.1A patent/CN112638903B/zh active Active
- 2020-01-28 AU AU2020216925A patent/AU2020216925B2/en active Active
- 2020-01-28 KR KR1020227017874A patent/KR102697726B1/ko active IP Right Grant
- 2020-01-28 KR KR1020217027357A patent/KR102405199B1/ko active IP Right Grant
- 2020-01-28 SG SG11202108160YA patent/SG11202108160YA/en unknown
- 2020-01-28 JP JP2021542541A patent/JP2022518906A/ja active Pending
- 2020-01-28 EP EP20707973.2A patent/EP3917921A1/en active Pending
- 2020-01-28 MX MX2021009033A patent/MX2021009033A/es unknown
- 2020-01-28 CN CN202211089980.8A patent/CN115385871A/zh active Pending
- 2020-01-28 WO PCT/US2020/015370 patent/WO2020159959A1/en unknown
- 2020-01-28 BR BR112021014640A patent/BR112021014640A8/pt unknown
- 2020-01-28 US US16/775,142 patent/US11426382B2/en active Active
- 2020-01-28 IL IL285184A patent/IL285184B2/en unknown
- 2020-10-23 US US17/079,347 patent/US11020374B2/en active Active
-
2021
- 2021-07-27 MX MX2023014776A patent/MX2023014776A/es unknown
- 2021-07-27 CL CL2021001968A patent/CL2021001968A1/es unknown
- 2021-07-28 ZA ZA2021/05344A patent/ZA202105344B/en unknown
- 2021-08-23 CO CONC2021/0011042A patent/CO2021011042A2/es unknown
- 2021-10-05 ZA ZA2021/07474A patent/ZA202107474B/en unknown
-
2022
- 2022-07-11 US US17/862,117 patent/US20220356319A1/en active Pending
-
2023
- 2023-11-02 JP JP2023188791A patent/JP2024039020A/ja active Pending
Patent Citations (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2013511473A (ja) * | 2009-11-17 | 2013-04-04 | フヤ バイオサイエンス インターナショナル エルエルシー | 心房細動の治療 |
| JP2013511472A (ja) * | 2009-11-17 | 2013-04-04 | フヤ バイオサイエンス インターナショナル エルエルシー | サルカルディン及びその塩の緩速点滴 |
| JP2018506562A (ja) * | 2015-02-26 | 2018-03-08 | ジェネンテック, インコーポレイテッド | ピロロピリジン化合物の結晶形態 |
| WO2018156895A1 (en) * | 2017-02-24 | 2018-08-30 | Gilead Sciences, Inc. | Inhibitors of bruton's tyrosine kinase |
Also Published As
| Publication number | Publication date |
|---|---|
| US11020374B2 (en) | 2021-06-01 |
| IL285184A (en) | 2021-09-30 |
| MX2021009033A (es) | 2021-10-13 |
| JP2024039020A (ja) | 2024-03-21 |
| CN112638903B (zh) | 2022-08-26 |
| ZA202105344B (en) | 2023-01-25 |
| KR20210130157A (ko) | 2021-10-29 |
| MX2023014776A (es) | 2024-01-15 |
| US20210038568A1 (en) | 2021-02-11 |
| US20220356319A1 (en) | 2022-11-10 |
| CL2021001968A1 (es) | 2022-01-28 |
| CN115385871A (zh) | 2022-11-25 |
| SG11202108160YA (en) | 2021-08-30 |
| CN112638903A (zh) | 2021-04-09 |
| KR102697726B1 (ko) | 2024-08-21 |
| ZA202107474B (en) | 2022-06-29 |
| BR112021014640A8 (pt) | 2022-12-20 |
| IL285184B1 (en) | 2023-08-01 |
| BR112021014640A2 (pt) | 2021-09-21 |
| US11426382B2 (en) | 2022-08-30 |
| AU2020216925B2 (en) | 2022-09-15 |
| IL285184B2 (en) | 2023-12-01 |
| WO2020159959A1 (en) | 2020-08-06 |
| CO2021011042A2 (es) | 2022-01-17 |
| AU2020216925A1 (en) | 2021-09-02 |
| KR102405199B1 (ko) | 2022-06-02 |
| CA3128152A1 (en) | 2020-08-06 |
| KR20220079688A (ko) | 2022-06-13 |
| US20200316024A1 (en) | 2020-10-08 |
| EP3917921A1 (en) | 2021-12-08 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP2022518906A (ja) | サルカルディン塩 | |
| JP2022176961A (ja) | {[5-(3-クロロフェニル)-3-ヒドロキシピリジン-2-カルボニル]アミノ}酢酸の固体形態、組成物、及びその使用 | |
| TWI657826B (zh) | Complex of angiotensin II receptor antagonist metabolite and NEP inhibitor and preparation method thereof | |
| BR112020022738A2 (pt) | formas cristalinas de um inibidor tlr7/tlr8 | |
| JP2017193561A (ja) | 3−(4−ニトロ−1−オキソイソインドリン−2−イル)ピペリジン−2,6−ジオンの固体形態 | |
| JP2022503890A (ja) | 2-(1-アシルオキシ-n-ペンチル)安息香酸と塩基性アミノ酸またはアミノグアニジンによって形成される塩と、その製造方法及び用途 | |
| JP2023550428A (ja) | インテグリン阻害剤およびその使用 | |
| KR20240000540A (ko) | (s)-n-(3-(2-(((r)-1-하이드록시프로판-2-일)아미노)-6-모르폴리노피리딘-4-일)-4-메틸페닐)-3-(2,2,2-트리플루오로에틸)피롤리딘-1-카르복스아미드 및 이의 염의 고체 상태 형태 | |
| BR112019015487A2 (pt) | Formas cristalinas de tebipenem pivoxil, composições incluindo as mesmas, métodos de fabricação e métodos de uso | |
| TWI762770B (zh) | 脂化肽的水溶性鹽以及製備與使用其的方法 | |
| ES2651689T3 (es) | Forma salina de alfa-6-mPEG6-O-hidroxicodona sólida como antagonista opioide y usos de la misma | |
| CN104768927B (zh) | (3s,3s’)‑4,4’‑二硫烷二基双(3‑氨基丁烷‑1‑磺酸)合l‑赖氨酸的新的结晶相 | |
| EA043571B1 (ru) | Соли сулькардина | |
| CN105367622B (zh) | 一种阿加曲班化合物 | |
| JP2019530719A (ja) | 4−(2−((1r,2r)−2−ヒドロキシシクロヘキシルアミノ)ベンゾチアゾール−6−イルオキシ)−n−メチルピコリンアミドの結晶形 | |
| BR112021002200A2 (pt) | sal erbumina de trepostinila | |
| WO2024169765A1 (zh) | 一种二肽类化合物的盐、其制备方法和用途 | |
| Corrigan | Salt forms: pharmaceutical aspects | |
| WO2022238389A2 (en) | Novel forms of entinostat | |
| EA043230B1 (ru) | Эрбуминовая соль трепростинила | |
| BRPI0707997A2 (pt) | forma cristalizada i de besipiridina.hcl, processo para sua obtenção, uso desta e composição terapêutica | |
| NZ759132B2 (en) | Solid forms of {[5-(3-chlorophenyl)-3-hydroxypyridine-2-carbonyl]amino}acetic acid, compositions, and uses thereof |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20211110 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20221021 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20221021 |
|
| A871 | Explanation of circumstances concerning accelerated examination |
Free format text: JAPANESE INTERMEDIATE CODE: A871 Effective date: 20221028 |
|
| RD12 | Notification of acceptance of power of sub attorney |
Free format text: JAPANESE INTERMEDIATE CODE: A7432 Effective date: 20221110 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A821 Effective date: 20221110 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20230105 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20230404 |
|
| A02 | Decision of refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A02 Effective date: 20230704 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20240221 |