JP2020193301A - ポリカーボネート樹脂及びそれを含む光学部材 - Google Patents
ポリカーボネート樹脂及びそれを含む光学部材 Download PDFInfo
- Publication number
- JP2020193301A JP2020193301A JP2019101277A JP2019101277A JP2020193301A JP 2020193301 A JP2020193301 A JP 2020193301A JP 2019101277 A JP2019101277 A JP 2019101277A JP 2019101277 A JP2019101277 A JP 2019101277A JP 2020193301 A JP2020193301 A JP 2020193301A
- Authority
- JP
- Japan
- Prior art keywords
- mol
- polycarbonate resin
- less
- repeating unit
- above formula
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
- 229920005668 polycarbonate resin Polymers 0.000 title claims abstract description 66
- 239000004431 polycarbonate resin Substances 0.000 title claims abstract description 66
- 230000003287 optical effect Effects 0.000 title claims description 26
- 125000002887 hydroxy group Chemical group [H]O* 0.000 claims description 34
- ISWSIDIOOBJBQZ-UHFFFAOYSA-N phenol group Chemical group C1(=CC=CC=C1)O ISWSIDIOOBJBQZ-UHFFFAOYSA-N 0.000 claims description 31
- 229920000642 polymer Polymers 0.000 claims description 28
- UMPGNGRIGSEMTC-UHFFFAOYSA-N 4-[1-(4-hydroxyphenyl)-3,3,5-trimethylcyclohexyl]phenol Chemical compound C1C(C)CC(C)(C)CC1(C=1C=CC(O)=CC=1)C1=CC=C(O)C=C1 UMPGNGRIGSEMTC-UHFFFAOYSA-N 0.000 claims description 13
- 125000000217 alkyl group Chemical group 0.000 claims description 8
- 125000004432 carbon atom Chemical group C* 0.000 claims description 7
- 238000003384 imaging method Methods 0.000 claims description 6
- 239000012788 optical film Substances 0.000 claims description 4
- GYLZMVYMSPSPDA-UHFFFAOYSA-N 4-[1-(4-hydroxyphenyl)-3-methylcyclohexyl]phenol Chemical compound C1C(C)CCCC1(C=1C=CC(O)=CC=1)C1=CC=C(O)C=C1 GYLZMVYMSPSPDA-UHFFFAOYSA-N 0.000 claims description 3
- IISBACLAFKSPIT-UHFFFAOYSA-N bisphenol A Chemical compound C=1C=C(O)C=CC=1C(C)(C)C1=CC=C(O)C=C1 IISBACLAFKSPIT-UHFFFAOYSA-N 0.000 abstract description 13
- OTLDLKLSNZMTTA-UHFFFAOYSA-N octahydro-1h-4,7-methanoindene-1,5-diyldimethanol Chemical compound C1C2C3C(CO)CCC3C1C(CO)C2 OTLDLKLSNZMTTA-UHFFFAOYSA-N 0.000 abstract description 10
- 239000002994 raw material Substances 0.000 abstract description 10
- 229930185605 Bisphenol Natural products 0.000 abstract description 3
- SDDLEVPIDBLVHC-UHFFFAOYSA-N Bisphenol Z Chemical compound C1=CC(O)=CC=C1C1(C=2C=CC(O)=CC=2)CCCCC1 SDDLEVPIDBLVHC-UHFFFAOYSA-N 0.000 abstract description 3
- 229920005989 resin Polymers 0.000 description 19
- 239000011347 resin Substances 0.000 description 19
- YMWUJEATGCHHMB-UHFFFAOYSA-N Dichloromethane Chemical compound ClCCl YMWUJEATGCHHMB-UHFFFAOYSA-N 0.000 description 15
- 238000005481 NMR spectroscopy Methods 0.000 description 10
- 238000011156 evaluation Methods 0.000 description 9
- 239000000203 mixture Substances 0.000 description 9
- 239000000178 monomer Substances 0.000 description 8
- 150000001875 compounds Chemical class 0.000 description 7
- 238000000034 method Methods 0.000 description 7
- 239000000243 solution Substances 0.000 description 7
- 230000002087 whitening effect Effects 0.000 description 7
- 238000006243 chemical reaction Methods 0.000 description 6
- -1 cyclohexylidene group Chemical class 0.000 description 6
- 239000010408 film Substances 0.000 description 6
- 150000004650 carbonic acid diesters Chemical class 0.000 description 5
- 125000002496 methyl group Chemical group [H]C([H])([H])* 0.000 description 5
- 238000006116 polymerization reaction Methods 0.000 description 5
- 238000012360 testing method Methods 0.000 description 5
- UIIMBOGNXHQVGW-UHFFFAOYSA-M Sodium bicarbonate Chemical compound [Na+].OC([O-])=O UIIMBOGNXHQVGW-UHFFFAOYSA-M 0.000 description 4
- 238000001746 injection moulding Methods 0.000 description 4
- 238000005259 measurement Methods 0.000 description 4
- 125000001997 phenyl group Chemical group [H]C1=C([H])C([H])=C(*)C([H])=C1[H] 0.000 description 4
- WGTYBPLFGIVFAS-UHFFFAOYSA-M tetramethylammonium hydroxide Chemical compound [OH-].C[N+](C)(C)C WGTYBPLFGIVFAS-UHFFFAOYSA-M 0.000 description 4
- UHOVQNZJYSORNB-UHFFFAOYSA-N Benzene Chemical compound C1=CC=CC=C1 UHOVQNZJYSORNB-UHFFFAOYSA-N 0.000 description 3
- LYCAIKOWRPUZTN-UHFFFAOYSA-N Ethylene glycol Chemical compound OCCO LYCAIKOWRPUZTN-UHFFFAOYSA-N 0.000 description 3
- 125000003118 aryl group Chemical group 0.000 description 3
- 230000000052 comparative effect Effects 0.000 description 3
- 150000001925 cycloalkenes Chemical class 0.000 description 3
- ROORDVPLFPIABK-UHFFFAOYSA-N diphenyl carbonate Chemical compound C=1C=CC=CC=1OC(=O)OC1=CC=CC=C1 ROORDVPLFPIABK-UHFFFAOYSA-N 0.000 description 3
- 238000002347 injection Methods 0.000 description 3
- 239000007924 injection Substances 0.000 description 3
- 238000004519 manufacturing process Methods 0.000 description 3
- 238000000465 moulding Methods 0.000 description 3
- 239000012488 sample solution Substances 0.000 description 3
- 239000000126 substance Substances 0.000 description 3
- 125000001424 substituent group Chemical group 0.000 description 3
- KLDXJTOLSGUMSJ-UNTFVMJOSA-N (3s,3ar,6s,6ar)-2,3,3a,5,6,6a-hexahydrofuro[3,2-b]furan-3,6-diol Chemical compound O[C@H]1CO[C@@H]2[C@@H](O)CO[C@@H]21 KLDXJTOLSGUMSJ-UNTFVMJOSA-N 0.000 description 2
- SICLLPHPVFCNTJ-UHFFFAOYSA-N 1,1,1',1'-tetramethyl-3,3'-spirobi[2h-indene]-5,5'-diol Chemical compound C12=CC(O)=CC=C2C(C)(C)CC11C2=CC(O)=CC=C2C(C)(C)C1 SICLLPHPVFCNTJ-UHFFFAOYSA-N 0.000 description 2
- WFNXYMSIAASORV-UHFFFAOYSA-N 2-[1-(2-hydroxyphenyl)cyclohexyl]phenol Chemical group OC1=CC=CC=C1C1(C=2C(=CC=CC=2)O)CCCCC1 WFNXYMSIAASORV-UHFFFAOYSA-N 0.000 description 2
- BVKZGUZCCUSVTD-UHFFFAOYSA-L Carbonate Chemical compound [O-]C([O-])=O BVKZGUZCCUSVTD-UHFFFAOYSA-L 0.000 description 2
- QIGBRXMKCJKVMJ-UHFFFAOYSA-N Hydroquinone Chemical compound OC1=CC=C(O)C=C1 QIGBRXMKCJKVMJ-UHFFFAOYSA-N 0.000 description 2
- RTAQQCXQSZGOHL-UHFFFAOYSA-N Titanium Chemical compound [Ti] RTAQQCXQSZGOHL-UHFFFAOYSA-N 0.000 description 2
- 238000002835 absorbance Methods 0.000 description 2
- 230000004075 alteration Effects 0.000 description 2
- 239000007864 aqueous solution Substances 0.000 description 2
- 229910052799 carbon Inorganic materials 0.000 description 2
- 238000004040 coloring Methods 0.000 description 2
- 238000000748 compression moulding Methods 0.000 description 2
- 238000012937 correction Methods 0.000 description 2
- 125000001495 ethyl group Chemical group [H]C([H])([H])C([H])([H])* 0.000 description 2
- RMBPEFMHABBEKP-UHFFFAOYSA-N fluorene Chemical compound C1=CC=C2C3=C[CH]C=CC3=CC2=C1 RMBPEFMHABBEKP-UHFFFAOYSA-N 0.000 description 2
- 238000010438 heat treatment Methods 0.000 description 2
- NIHNNTQXNPWCJQ-UHFFFAOYSA-N o-biphenylenemethane Natural products C1=CC=C2CC3=CC=CC=C3C2=C1 NIHNNTQXNPWCJQ-UHFFFAOYSA-N 0.000 description 2
- 239000013307 optical fiber Substances 0.000 description 2
- 125000004430 oxygen atom Chemical group O* 0.000 description 2
- 230000000704 physical effect Effects 0.000 description 2
- 229920000515 polycarbonate Polymers 0.000 description 2
- 239000004417 polycarbonate Substances 0.000 description 2
- 230000009257 reactivity Effects 0.000 description 2
- 239000011342 resin composition Substances 0.000 description 2
- GHMLBKRAJCXXBS-UHFFFAOYSA-N resorcinol Chemical compound OC1=CC=CC(O)=C1 GHMLBKRAJCXXBS-UHFFFAOYSA-N 0.000 description 2
- 229910000030 sodium bicarbonate Inorganic materials 0.000 description 2
- 235000017557 sodium bicarbonate Nutrition 0.000 description 2
- 239000000758 substrate Substances 0.000 description 2
- 239000010936 titanium Substances 0.000 description 2
- 229910052719 titanium Inorganic materials 0.000 description 2
- YBHWVDKCKDWQBX-UHFFFAOYSA-N 2-[2-cyclohexyl-4-[9-[3-cyclohexyl-4-(2-hydroxyethoxy)phenyl]fluoren-9-yl]phenoxy]ethanol Chemical compound OCCOC1=CC=C(C2(C3=CC=CC=C3C3=CC=CC=C32)C=2C=C(C(OCCO)=CC=2)C2CCCCC2)C=C1C1CCCCC1 YBHWVDKCKDWQBX-UHFFFAOYSA-N 0.000 description 1
- JTLKXEMTIVAKJG-UHFFFAOYSA-N 2-[2-tert-butyl-4-[9-[5-tert-butyl-4-(2-hydroxyethoxy)-2-methylphenyl]fluoren-9-yl]-5-methylphenoxy]ethanol Chemical compound CC1=CC(OCCO)=C(C(C)(C)C)C=C1C1(C=2C(=CC(OCCO)=C(C=2)C(C)(C)C)C)C2=CC=CC=C2C2=CC=CC=C21 JTLKXEMTIVAKJG-UHFFFAOYSA-N 0.000 description 1
- IRTFFZWZLVOXMG-UHFFFAOYSA-N 2-[4-[9-[4-(2-hydroxyethoxy)-3,5-dimethylphenyl]fluoren-9-yl]-2,6-dimethylphenoxy]ethanol Chemical compound CC1=C(OCCO)C(C)=CC(C2(C3=CC=CC=C3C3=CC=CC=C32)C=2C=C(C)C(OCCO)=C(C)C=2)=C1 IRTFFZWZLVOXMG-UHFFFAOYSA-N 0.000 description 1
- LUXQHIIWBDDUDE-UHFFFAOYSA-N 2-[4-[9-[4-(2-hydroxyethoxy)-3-methylphenyl]fluoren-9-yl]-2-methylphenoxy]ethanol Chemical compound C1=C(OCCO)C(C)=CC(C2(C3=CC=CC=C3C3=CC=CC=C32)C=2C=C(C)C(OCCO)=CC=2)=C1 LUXQHIIWBDDUDE-UHFFFAOYSA-N 0.000 description 1
- WXNRFPMJYZGKSS-UHFFFAOYSA-N 2-[4-[9-[4-(2-hydroxyethoxy)-3-propan-2-ylphenyl]fluoren-9-yl]-2-propan-2-ylphenoxy]ethanol Chemical compound C1=C(OCCO)C(C(C)C)=CC(C2(C3=CC=CC=C3C3=CC=CC=C32)C=2C=C(C(OCCO)=CC=2)C(C)C)=C1 WXNRFPMJYZGKSS-UHFFFAOYSA-N 0.000 description 1
- NQXNYVAALXGLQT-UHFFFAOYSA-N 2-[4-[9-[4-(2-hydroxyethoxy)phenyl]fluoren-9-yl]phenoxy]ethanol Chemical compound C1=CC(OCCO)=CC=C1C1(C=2C=CC(OCCO)=CC=2)C2=CC=CC=C2C2=CC=CC=C21 NQXNYVAALXGLQT-UHFFFAOYSA-N 0.000 description 1
- UQFAPXHGDUABRM-UHFFFAOYSA-N 2-cyclohexyl-4-[9-(3-cyclohexyl-4-hydroxyphenyl)fluoren-9-yl]phenol Chemical compound OC1=CC=C(C2(C3=CC=CC=C3C3=CC=CC=C32)C=2C=C(C(O)=CC=2)C2CCCCC2)C=C1C1CCCCC1 UQFAPXHGDUABRM-UHFFFAOYSA-N 0.000 description 1
- BHEUHZKBYVNFKH-UHFFFAOYSA-N 2-tert-butyl-4-[9-(3-tert-butyl-4-hydroxyphenyl)fluoren-9-yl]phenol Chemical compound C1=C(O)C(C(C)(C)C)=CC(C2(C3=CC=CC=C3C3=CC=CC=C32)C=2C=C(C(O)=CC=2)C(C)(C)C)=C1 BHEUHZKBYVNFKH-UHFFFAOYSA-N 0.000 description 1
- YMTYZTXUZLQUSF-UHFFFAOYSA-N 3,3'-Dimethylbisphenol A Chemical compound C1=C(O)C(C)=CC(C(C)(C)C=2C=C(C)C(O)=CC=2)=C1 YMTYZTXUZLQUSF-UHFFFAOYSA-N 0.000 description 1
- OPELWUSJOIBVJS-UHFFFAOYSA-N 3,3'-spirobi[1,2-dihydroindene] Chemical compound C12=CC=CC=C2CCC11C2=CC=CC=C2CC1 OPELWUSJOIBVJS-UHFFFAOYSA-N 0.000 description 1
- VPWNQTHUCYMVMZ-UHFFFAOYSA-N 4,4'-sulfonyldiphenol Chemical compound C1=CC(O)=CC=C1S(=O)(=O)C1=CC=C(O)C=C1 VPWNQTHUCYMVMZ-UHFFFAOYSA-N 0.000 description 1
- VWGKEVWFBOUAND-UHFFFAOYSA-N 4,4'-thiodiphenol Chemical compound C1=CC(O)=CC=C1SC1=CC=C(O)C=C1 VWGKEVWFBOUAND-UHFFFAOYSA-N 0.000 description 1
- BATCUENAARTUKW-UHFFFAOYSA-N 4-[(4-hydroxyphenyl)-diphenylmethyl]phenol Chemical compound C1=CC(O)=CC=C1C(C=1C=CC(O)=CC=1)(C=1C=CC=CC=1)C1=CC=CC=C1 BATCUENAARTUKW-UHFFFAOYSA-N 0.000 description 1
- NUDSREQIJYWLRA-UHFFFAOYSA-N 4-[9-(4-hydroxy-3-methylphenyl)fluoren-9-yl]-2-methylphenol Chemical compound C1=C(O)C(C)=CC(C2(C3=CC=CC=C3C3=CC=CC=C32)C=2C=C(C)C(O)=CC=2)=C1 NUDSREQIJYWLRA-UHFFFAOYSA-N 0.000 description 1
- FLMZHPQIDVOWEJ-UHFFFAOYSA-N 4-[9-(4-hydroxy-3-phenylphenyl)fluoren-9-yl]-2-phenylphenol Chemical compound OC1=CC=C(C2(C3=CC=CC=C3C3=CC=CC=C32)C=2C=C(C(O)=CC=2)C=2C=CC=CC=2)C=C1C1=CC=CC=C1 FLMZHPQIDVOWEJ-UHFFFAOYSA-N 0.000 description 1
- PSLSQHVPMSZQGS-UHFFFAOYSA-N 4-[9-(4-hydroxy-3-propan-2-ylphenyl)fluoren-9-yl]-2-propan-2-ylphenol Chemical compound C1=C(O)C(C(C)C)=CC(C2(C3=CC=CC=C3C3=CC=CC=C32)C=2C=C(C(O)=CC=2)C(C)C)=C1 PSLSQHVPMSZQGS-UHFFFAOYSA-N 0.000 description 1
- YWFPGFJLYRKYJZ-UHFFFAOYSA-N 9,9-bis(4-hydroxyphenyl)fluorene Chemical compound C1=CC(O)=CC=C1C1(C=2C=CC(O)=CC=2)C2=CC=CC=C2C2=CC=CC=C21 YWFPGFJLYRKYJZ-UHFFFAOYSA-N 0.000 description 1
- VOWWYDCFAISREI-UHFFFAOYSA-N Bisphenol AP Chemical compound C=1C=C(O)C=CC=1C(C=1C=CC(O)=CC=1)(C)C1=CC=CC=C1 VOWWYDCFAISREI-UHFFFAOYSA-N 0.000 description 1
- OKTJSMMVPCPJKN-UHFFFAOYSA-N Carbon Chemical group [C] OKTJSMMVPCPJKN-UHFFFAOYSA-N 0.000 description 1
- KLDXJTOLSGUMSJ-JGWLITMVSA-N Isosorbide Chemical compound O[C@@H]1CO[C@@H]2[C@@H](O)CO[C@@H]21 KLDXJTOLSGUMSJ-JGWLITMVSA-N 0.000 description 1
- JMMSLMMJRMCXPW-UHFFFAOYSA-N OC.OC.C1CC2CCC1C2 Chemical compound OC.OC.C1CC2CCC1C2 JMMSLMMJRMCXPW-UHFFFAOYSA-N 0.000 description 1
- AYVGBNGTBQLJBG-UHFFFAOYSA-N [3-(hydroxymethyl)cyclopentyl]methanol Chemical compound OCC1CCC(CO)C1 AYVGBNGTBQLJBG-UHFFFAOYSA-N 0.000 description 1
- YIMQCDZDWXUDCA-UHFFFAOYSA-N [4-(hydroxymethyl)cyclohexyl]methanol Chemical compound OCC1CCC(CO)CC1 YIMQCDZDWXUDCA-UHFFFAOYSA-N 0.000 description 1
- 239000006096 absorbing agent Substances 0.000 description 1
- 238000010521 absorption reaction Methods 0.000 description 1
- 239000000654 additive Substances 0.000 description 1
- 230000001476 alcoholic effect Effects 0.000 description 1
- 239000003242 anti bacterial agent Substances 0.000 description 1
- 239000002216 antistatic agent Substances 0.000 description 1
- 125000003710 aryl alkyl group Chemical group 0.000 description 1
- MUCRFDZUHPMASM-UHFFFAOYSA-N bis(2-chlorophenyl) carbonate Chemical compound ClC1=CC=CC=C1OC(=O)OC1=CC=CC=C1Cl MUCRFDZUHPMASM-UHFFFAOYSA-N 0.000 description 1
- CDQSJQSWAWPGKG-UHFFFAOYSA-N butane-1,1-diol Chemical compound CCCC(O)O CDQSJQSWAWPGKG-UHFFFAOYSA-N 0.000 description 1
- 150000001721 carbon Chemical group 0.000 description 1
- BVKZGUZCCUSVTD-UHFFFAOYSA-N carbonic acid Chemical compound OC(O)=O BVKZGUZCCUSVTD-UHFFFAOYSA-N 0.000 description 1
- 238000005266 casting Methods 0.000 description 1
- 239000003054 catalyst Substances 0.000 description 1
- 125000004122 cyclic group Chemical group 0.000 description 1
- 125000000113 cyclohexyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])(*)C([H])([H])C1([H])[H] 0.000 description 1
- 230000006837 decompression Effects 0.000 description 1
- 238000013461 design Methods 0.000 description 1
- 230000000694 effects Effects 0.000 description 1
- 230000007613 environmental effect Effects 0.000 description 1
- 238000001125 extrusion Methods 0.000 description 1
- 239000003063 flame retardant Substances 0.000 description 1
- 239000011521 glass Substances 0.000 description 1
- 230000009477 glass transition Effects 0.000 description 1
- 239000012760 heat stabilizer Substances 0.000 description 1
- MHIBEGOZTWERHF-UHFFFAOYSA-N heptane-1,1-diol Chemical compound CCCCCCC(O)O MHIBEGOZTWERHF-UHFFFAOYSA-N 0.000 description 1
- ACCCMOQWYVYDOT-UHFFFAOYSA-N hexane-1,1-diol Chemical compound CCCCCC(O)O ACCCMOQWYVYDOT-UHFFFAOYSA-N 0.000 description 1
- 229960002479 isosorbide Drugs 0.000 description 1
- 239000004611 light stabiliser Substances 0.000 description 1
- 239000000314 lubricant Substances 0.000 description 1
- 239000006078 metal deactivator Substances 0.000 description 1
- 239000006082 mold release agent Substances 0.000 description 1
- 239000012299 nitrogen atmosphere Substances 0.000 description 1
- FVXBCDWMKCEPCL-UHFFFAOYSA-N nonane-1,1-diol Chemical compound CCCCCCCCC(O)O FVXBCDWMKCEPCL-UHFFFAOYSA-N 0.000 description 1
- OEIJHBUUFURJLI-UHFFFAOYSA-N octane-1,8-diol Chemical compound OCCCCCCCCO OEIJHBUUFURJLI-UHFFFAOYSA-N 0.000 description 1
- UWJJYHHHVWZFEP-UHFFFAOYSA-N pentane-1,1-diol Chemical compound CCCCC(O)O UWJJYHHHVWZFEP-UHFFFAOYSA-N 0.000 description 1
- 239000004033 plastic Substances 0.000 description 1
- 239000004014 plasticizer Substances 0.000 description 1
- 238000005498 polishing Methods 0.000 description 1
- 239000012985 polymerization agent Substances 0.000 description 1
- 239000002243 precursor Substances 0.000 description 1
- 238000012545 processing Methods 0.000 description 1
- ULWHHBHJGPPBCO-UHFFFAOYSA-N propane-1,1-diol Chemical compound CCC(O)O ULWHHBHJGPPBCO-UHFFFAOYSA-N 0.000 description 1
- 230000000717 retained effect Effects 0.000 description 1
- 239000000523 sample Substances 0.000 description 1
- 238000007789 sealing Methods 0.000 description 1
- 230000003595 spectral effect Effects 0.000 description 1
- 125000003003 spiro group Chemical group 0.000 description 1
- 238000003756 stirring Methods 0.000 description 1
- 239000004094 surface-active agent Substances 0.000 description 1
- 238000002834 transmittance Methods 0.000 description 1
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 1
Landscapes
- Polyesters Or Polycarbonates (AREA)
Abstract
【課題】ビスフェノールAを原料として使用せず、かつ高温耐湿性が高いポリカーボネート樹脂の提供。【解決手段】繰返し単位(1)がトリシクロデカンジメタノール、繰返し単位(2)が4,4’−シクロヘキシリデンビスフェノール及び、繰返し単位(3)が4,4’−(3,3,5−トリシクロヘキシリデン)ビスフェノールに代表される単位、または式(4)の繰返し単位を含み、繰返し単位(3)または式(4)の繰返し単位が3mol%以上60mol%以下であり、かつ波長589nmにおける屈折率が1.550〜1.580である、ポリカーボネート樹脂:【選択図】なし
Description
本発明は、ポリカーボネート及びそれを含む光学部材、特に撮像レンズに関する。
スマートフォン等の機器で用いられるプラスチック製の撮像レンズには、低複屈折化及び収差補正能力の向上が強く求められている。従来、このような撮像レンズでは、互いに異なる光学特性(屈折率、アッベ数)を有する複数のレンズの組み合わせ、及びレンズ形状の組み合わせによって、収差補正を行っている。
近年では、ビスフェノールAを原料とする高屈折率、低アッベ数の樹脂やシクロオレフィン系からなる低屈折率、高アッベ数の樹脂を組み合わせてレンズユニットを作成することが多くなってきた。さらに、中屈折率、中アッベ数の樹脂を組み合わせることにより、レンズ設計の幅が拡がり、より高度な性能を持たせるための微調整を行うことが可能になった。このため、中屈折率、中アッベ数の樹脂の需要が増えてきた。
特許文献1には、芳香族ジヒドロキシ化合物と、トリシクロデカンジメタノール(以下、TCDDMと略す)を原料に用いた中屈折率、中アッベ数の樹脂が開示されている。
特許文献1に記載の樹脂は、ビスフェノールAを原料とする樹脂と、シクロオレフィン系樹脂との中間の屈折率、アッベ数を持ち、バランスの良い優れた光学特性を持つが、高温での耐湿性に課題があることが分かった。そこで、本発明は、高温耐湿性が高く、屈折率が1.550〜1.580であり、中アッベ数を有するポリカーボネート樹脂及びそれを含む光学部材を提供することを目的とする。
本発明者らは、以下の態様を有する本発明により、上記課題を解決できることを見出した。
《態様1》
式(1)、式(2)及び、式(3)または式(4)の繰返し単位を含み、式(3)または式(4)の繰返し単位が3mol%以上60mol%以下であり、かつ波長589nmにおける屈折率が1.550〜1.580である、ポリカーボネート樹脂:
{式(3)中、nは1〜8の整数であり、R1は、それぞれ炭素原子数1〜3のアルキル基から選択される。}
{式(4)中、l、mは同じまたは異なって0〜3の整数であり、R2、R3は、それぞれ独立に、炭素原子数1〜3のアルキル基から選択される。}
《態様1》
式(1)、式(2)及び、式(3)または式(4)の繰返し単位を含み、式(3)または式(4)の繰返し単位が3mol%以上60mol%以下であり、かつ波長589nmにおける屈折率が1.550〜1.580である、ポリカーボネート樹脂:
《態様2》
上記式(3)または上記式(4)の繰返し単位が、5mol%以上50mol%以下である、態様1に記載のポリカーボネート樹脂。
《態様3》
上記式(1)の繰返し単位が、10mol%以上55mol%以下である、態様1または2に記載のポリカーボネート樹脂。
《態様4》
上記式(2)の繰返し単位が、3mol%以上65mol%以下である、態様1〜3のいずれか一項に記載のポリカーボネート樹脂。
《態様5》
上記式(3)中、nが1〜3の整数である態様1〜4のいずれか一項に記載のポリカーボネート樹脂。
《態様6》
上記式(3)の繰り返し単位が、4,4’−(3,3,5−トリメチルシクロヘキシリデン)ビスフェノール、または4,4’−(3−メチルシクロヘキシリデン)ビスフェノールに由来する構造である、態様1〜5のいずれか一項に記載のポリカーボネート樹脂。
上記式(3)または上記式(4)の繰返し単位が、5mol%以上50mol%以下である、態様1に記載のポリカーボネート樹脂。
《態様3》
上記式(1)の繰返し単位が、10mol%以上55mol%以下である、態様1または2に記載のポリカーボネート樹脂。
《態様4》
上記式(2)の繰返し単位が、3mol%以上65mol%以下である、態様1〜3のいずれか一項に記載のポリカーボネート樹脂。
《態様5》
上記式(3)中、nが1〜3の整数である態様1〜4のいずれか一項に記載のポリカーボネート樹脂。
《態様6》
上記式(3)の繰り返し単位が、4,4’−(3,3,5−トリメチルシクロヘキシリデン)ビスフェノール、または4,4’−(3−メチルシクロヘキシリデン)ビスフェノールに由来する構造である、態様1〜5のいずれか一項に記載のポリカーボネート樹脂。
《態様8》
全ポリマー末端に対する末端フェノール性水酸基比率が60%以下である、態様1〜7のいずれか一項に記載のポリカーボネート樹脂。
《態様9》
アッベ数が33.0〜40.5である、態様1〜8のいずれか一項に記載のポリカーボネート樹脂。
《態様10》
態様1〜9のいずれか一項に記載のポリカーボネート樹脂を含む、光学部材。
《態様11》
レンズである、態様10に記載の光学部材。
《態様12》
光学フィルムである、態様10に記載の光学部材。
《態様13》
携帯電話、スマートフォン、タブレット端末、パソコン、デジタルカメラ、ビデオカメラ、車載カメラ、または監視カメラのいずれかに用いるための撮像レンズである、態様11に記載の光学部材。
全ポリマー末端に対する末端フェノール性水酸基比率が60%以下である、態様1〜7のいずれか一項に記載のポリカーボネート樹脂。
《態様9》
アッベ数が33.0〜40.5である、態様1〜8のいずれか一項に記載のポリカーボネート樹脂。
《態様10》
態様1〜9のいずれか一項に記載のポリカーボネート樹脂を含む、光学部材。
《態様11》
レンズである、態様10に記載の光学部材。
《態様12》
光学フィルムである、態様10に記載の光学部材。
《態様13》
携帯電話、スマートフォン、タブレット端末、パソコン、デジタルカメラ、ビデオカメラ、車載カメラ、または監視カメラのいずれかに用いるための撮像レンズである、態様11に記載の光学部材。
《ポリカーボネート樹脂》
本発明のポリカーボネート樹脂は、上記の式(1)のトリシクロデカン系単位および上記の式(2)のシクロヘキシリデンビスフェノール単位と、上記式(3)の置換基を持つシクロヘキシリデンビスフェノール系単位または上記式(4)のスピロビインダン系単位のいずれか一つを含み、上記式(3)または(4)の繰返し単位が、3mol%以上60mol%以下である。また、本発明の樹脂は、波長589nmにおける屈折率が1.550〜1.580である。
本発明のポリカーボネート樹脂は、上記の式(1)のトリシクロデカン系単位および上記の式(2)のシクロヘキシリデンビスフェノール単位と、上記式(3)の置換基を持つシクロヘキシリデンビスフェノール系単位または上記式(4)のスピロビインダン系単位のいずれか一つを含み、上記式(3)または(4)の繰返し単位が、3mol%以上60mol%以下である。また、本発明の樹脂は、波長589nmにおける屈折率が1.550〜1.580である。
特許文献1に記載の樹脂は、ビスフェノールAを原料とする樹脂と、シクロオレフィン系樹脂との中間の屈折率、アッベ数を持ち、バランスの良い優れた光学特性を持つが、高温での耐湿性に課題があることが分かった。すなわち、特許文献1記載の樹脂は、高温高湿に長期間さらされることで非常に大きく変形し、白化することを見出した。
そして、本発明者らは、特許文献1に記載の樹脂において、上記式(3)または(4)の繰返し単位を一定程度導入することによって、特許文献1に記載の撮像レンズの変形や白化を実質的に防止できることを見出した。
上記の式(3)または(4)の繰返し単位であれば、特許文献1に記載の樹脂から高温耐湿性を向上させながら、屈折率及びアッベ数を大きく変えることなく、所望の屈折率(1.550〜1.580)に調節することができ、レンズの成形も比較的容易であることが分かった。光学用途のポリカーボネート樹脂において、モノマーの組成を変更しながら、屈折率及びアッベ数を大きく変えることなく、他の特性を向上させるという点は非常に困難であり、上記式(3)または(4)の繰返し単位の導入によって、上記のような特性が得られたことは予想外であった。
理論に拘束されないが、上記式(3)の繰返し単位の導入によって上記の結果が得られた理由としては、上記式(3)の繰返し単位中の2つのベンゼン環と、その間に位置するシクロヘキシリデン基との存在が挙げられる。このシクロヘキシリデン基は、2つのベンゼン環と結合する炭素が4級炭素原子であるため、3つの環状構造は、同一平面には存在しない。また、シクロヘキシリデン基にアルキル置換基が存在することにより、ポリマー主鎖の動きが制限され、高温耐湿性が向上したものと考えられる。
理論に拘束されないが、上記式(4)の繰返し単位の導入によって上記の結果が得られた理由としては、上記式(4)の繰り返し単位は分子のねじれが起こりにくい強直な構造であり、脂肪族であるスピロ環部分にメチル基があることにより、上記式(1)の構造と親和性が高く、ポリマー主鎖の動きが制限され、高温耐湿性が向上したものと考えられる。
〈ポリマー構造〉
本発明のポリカーボネート樹脂は、上記式(1)および(2)の繰り返し単位と、(3)または(4)いずれか一つの繰返し単位を含む。
本発明のポリカーボネート樹脂は、上記式(1)および(2)の繰り返し単位と、(3)または(4)いずれか一つの繰返し単位を含む。
本発明のポリカーボネート樹脂は、上記式(1)の繰返し単位を、10mol%以上、15mol%以上、20mol%以上、25mol%以上、30mol%以上、35mol%以上、40mol%以上、45mol%以上、50mol%以上で含んでいてもよく、60mol%以下、55mol%以下、50mol%以下、45mol%以下、40mol%以下、または35mol%以下で含んでいてもよい。本発明の樹脂は、上記式(1)の繰返し単位を、好ましくは10mol%以上55mol%以下、より好ましくは20mol%以上50mol%以下で含むことができる。
上記式(1)の繰返し単位が下限より少ない場合は、屈折率が高くなり、流動性、成形性が悪化する。また、上限より多い場合は、屈折率および高温耐湿性が小さくなる。
本発明のポリカーボネート樹脂は、上記式(2)の繰返し単位を、3mol%以上、5mol%以上、10mol%以上、20mol%以上、25mol%以上、30mol%以上、35mol%、40mol%以上、45mol%以上、50mol%以上、60mol%以上で含んでいてもよく、65mol%以下、55mol%以下、50mol%以下、45mol%以下、40mol%以下、35mol%以下、30mol%以下、25mol%以下、または20mol%以下で含んでいてもよい。例えば、本発明の樹脂は、上記式(2)の繰返し単位を、3mol%以上65mol%以下、10mol%以上60mol%以下、または20mol%以上55mol%以下で含むことができる。
上記式(2)の繰返し単位が上限より多い場合は、屈折率が高くなる。
本発明のポリカーボネート樹脂は、上記式(3)の繰返し単位を、3mol%以上、5mol%以上、10mol%以上、15mol%以上、20mol%以上、25mol%以上、または30mol%以上で含んでいてもよく、60mol%以下、55mol%以下、50mol%以下、45mol%以下、40mol%以下で含んでいてもよい。本発明のポリカーボネート樹脂は、上記式(3)の繰返し単位を好ましくは5〜50mol%、より好ましくは15〜50mol%、特に好ましくは25〜45mol%で含む。
上記式(3)の繰返し単位を含むことで、高温状態で製品を使用したときの白化や変形を抑制することができる。また、上限より多い場合は、流動性、成形性が悪化する。
上記式(3)中、nは、1〜8の範囲であり、好ましくは1〜5、より好ましくは1〜3、さらに好ましくは1または3、特に好ましくは3である。また、R1は、それぞれ炭素原子数1〜3のアルキル基から選択され、好ましくはメチル基またはエチル基、特に好ましくはメチル基である。また、特に上記式(3)の繰返し単位が、4,4’−(3,3,5−トリメチルシクロヘキシリデン)ビスフェノール(いわゆる、ビスフェノールTMC、以下BPTMCと略す)、4,4’−(3−メチルシクロヘキシリデン)ビスフェノール(いわゆる、ビスフェノール3MZ)であることが好ましく、なかでもBPTMCが特に好ましい。
本発明のポリカーボネート樹脂は、上記式(4)の繰返し単位を、3mol%以上、5mol%以上、10mol%以上、15mol%以上、20mol%以上、25mol%以上、または30mol%以上で含んでいてもよく、60mol%以下、55mol%以下、50mol%以下、45mol%以下、40mol%以下で含んでいてもよい。本発明のポリカーボネート樹脂は、上記式(4)の繰返し単位を好ましくは5〜50mol%、より好ましくは15〜50mol%、特に好ましくは20〜45mol%で含む。
上記式(4)の繰返し単位を含むことで、高温状態で製品を使用したときの白化や変形を抑制することができる。また、上限より多い場合は、流動性、成形性が悪化する。
上記式(4)中、l、mは同じまたは異なって0〜3の整数であり、好ましくはl=m=0〜2であり、特に好ましくはl=m=0である。R2、R3はそれぞれ炭素原子数1〜3のアルキル基から選択され、好ましくはメチル基またはエチル基、特に好ましくはメチル基である。また、特に上記式(4)の繰り返し単位が、3,3,3’,3’−テトラメチル−1,1’−スピロビインダン−6,6’−ジオール(以下、SBIと略す)、3,3,3’,3’,5,5’−ヘキサメチル−1,1’−スピロビインダン−6,6’−ジオール(以下ジメチルSBIと略す)、3,3,3’,3’,5,5’,7,7’−オクタメチル−1,1’−スピロビインダン−6,6’−ジオール(以下、テトラメチルSBIと略す)から選ばれる化合物が好ましく、なかでもSBIが特に好ましい。
上記式(3)は、反応に関与する部分である芳香族ヒドロキシ基周辺の立体障害が上記式(4)より少ないため、反応性が良く、製造時間が短縮されるのでより好ましい。また、上記式(4)で置換基が付くとさらにヒドロキシ基周辺の立体障害が大きくなるため、反応性は悪くなるが、必要な物性を得るために置換基のついた化合物を使用することは、場合によっては好ましいことである。
本発明のポリカーボネート樹脂は、上記の本発明の有利な効果が得られる範囲で、上記式(1)、(2)、(3)、(4)の繰返し単位以外の繰返し単位を含んでいてもよい。そのような繰返し単位をもたらすジヒドロキシ化合物としては、エチレングリコール、プロパンジオール、ブタンジオール、ペンタンジオール、ヘキサンジオール、ヘプタンジオール、オクタンジオール、ノナンジオール、シクロヘキサン−1,4−ジメタノール、デカリン−2,6−ジメタノール、ノルボルナンジメタノール、ペンタシクロペンタデカンジメタノール、シクロペンタン−1,3−ジメタノール、イソソルビド、イソマンニド、イソイジド、ヒドロキノン、レゾルシノール、2,2−ビス(4−ヒドロキシフェニル)プロパン、2,2−ビス(3−メチル−4−ヒドロキシフェニル)プロパン、1,1−ビス(4−ヒドロキシフェニル)−1−フェニルエタン、ビス(4−ヒドロキシフェニル)ジフェニルメタン、1,3−ビス(2−(4−ヒドロキシフェニル)−2−プロピル)ベンゼン、ビス(4−ヒドロキシフェニル)スルホン、ビス(4−ヒドロキシフェニル)スルフィド、ビフェノール、9,9−ビス(4−ヒドロキシフェニル)フルオレン、9,9−ビス(4−ヒドロキシ−3−メチルフェニル)フルオレン、9,9−ビス(4−ヒドロキシ−3−イソプロピルフェニル)フルオレン、9,9−ビス(4−ヒドロキシ−3−tert−ブチルフェニル)フルオレン、9,9−ビス(4−ヒドロキシ−3−シクロヘキシルフェニル)フルオレン、9,9−ビス(4−ヒドロキシ−3−フェニルフェニル)フルオレン、9,9−ビス(4−(2−ヒドロキシエトキシ)フェニル)フルオレン、9,9−ビス(4−(2−ヒドロキシエトキシ)−3−メチルフェニル)フルオレン、9,9−ビス(4−(2−ヒドロキシエトキシ)−3−イソプロピルフェニル)フルオレン、9,9−ビス(4−(2−ヒドロキシエトキシ)−3−tert−ブチルフェニル)フルオレン、9,9−ビス(4−(2−ヒドロキシエトキシ)−3−シクロヘキシルフェニル)フルオレン、9,9−ビス(4−(2−ヒドロキシエトキシ)−3−フェニルフェニル)フルオレン、9,9−ビス(4−(2−ヒドロキシエトキシ)−3,5−ジメチルフェニル)フルオレン、9,9−ビス(4−(2−ヒドロキシエトキシ)−3−tert−ブチル−6−メチルフェニル)フルオレン等が挙げられる。このような繰返し単位は、全繰返し単位中に10mol%以下であってもよい。
本発明のポリカーボネート樹脂は、ポリマー末端のフェノール性水酸基が全ポリマー末端の60%以下であることが好ましい。
すなわち、上記式(2)、(3)、(4)の繰返し単位をもたらすモノマーがポリマーの末端に存在すると、末端基がフェノール性水酸基になる。そこで、例えば原料であるジヒドロキシ化合物よりも過剰な量で炭酸ジエステルを重合時に使用し、末端をフェニル基にすることによって、ポリマーの末端フェノール性水酸基の量を減らすことが好ましい。
末端フェノール性水酸基の比率は
末端フェノール性水酸基比率=(末端フェノール性水酸基量/全ポリマー末端量)×100
として求めることができる。なお、全ポリマー末端は、末端フェノール性水酸基、末端アルコール性水酸基および末端フェニル基からなる。
末端フェノール性水酸基比率=(末端フェノール性水酸基量/全ポリマー末端量)×100
として求めることができる。なお、全ポリマー末端は、末端フェノール性水酸基、末端アルコール性水酸基および末端フェニル基からなる。
この例に限定するものではないが、具体的には以下のような手法で末端フェノール性水酸基比率を求めることができる。
(1)末端フェノール性水酸基のオルト位のプロトンを、ポリマーの1H NMR測定で観測し、6.58〜6.83ppm該当ピークの積分を取りこの強度を1とする。これは、水酸基1つに対し、プロトン2個分である。この時、同時に上記式(1)に由来するTCDDMの酸素原子の隣のアルキル基プロトン4個分である3.8〜4.2ppmピークの積分強度を求め、(A)とする。当然ながら、末端フェノール性水酸基のピークが観測されないときは(A)は求められず、末端フェノール性水酸基比率は0である。
(1)末端フェノール性水酸基のオルト位のプロトンを、ポリマーの1H NMR測定で観測し、6.58〜6.83ppm該当ピークの積分を取りこの強度を1とする。これは、水酸基1つに対し、プロトン2個分である。この時、同時に上記式(1)に由来するTCDDMの酸素原子の隣のアルキル基プロトン4個分である3.8〜4.2ppmピークの積分強度を求め、(A)とする。当然ながら、末端フェノール性水酸基のピークが観測されないときは(A)は求められず、末端フェノール性水酸基比率は0である。
(2)ポリマーのGPC測定で得られる数平均分子量と各繰返し単位の分子量とmol比からポリマーの平均重合度(B)を求める。
(3)末端フェノール性水酸基比率(%)は、[上記式(1)のmol%]×(B)/(A)として計算される。
式(4)のモノマーを使用した場合には、末端フェノール性水酸基のオルト位のプロトンの位置が違う、あるいは存在しないため上記の方法が使えない。この場合には、Makromolekulare Chem. 88(1965) 215−231の記載をもとに、チタン発色法を用いて、480nm, 520nmにおけるモノマーの吸光度を測定して、連立方程式を解くことにより末端フェノール性水酸基量を求め、GPC測定で得られる平均重合度から全末端量を算出し、末端フェノール性水酸基比率(%)=(末端フェノール性水酸基量/全ポリマー末端量)×100として求める。
本発明のポリカーボネート樹脂の全ポリマー末端に対する、末端フェノール性水酸基比率は、好ましくは60%以下、より好ましくは55%以下、さらに好ましくは50%以下特に好ましくは45%以下、最も好ましくは40%以下である。
末端フェノール性水酸基比率が上限より大きい場合は、高温耐湿性が悪化し、樹脂の変色が起こりやすくなり、レンズ等に成形した場合、像の色が変化することがある。
末端フェノール性水酸基を封止するための炭酸ジエステルとしては、置換されていてもよい炭素原子数6〜12のアリール基、アラルキル基等の炭酸ジエステルが挙げられる。具体的には、ジフェニルカーボネート、ジトリールカーボネート、ビス(クロロフェニル)カーボネートおよびビス(m−クレジル)カーボネート等が例示される。このなかでも特に、ジフェニルカーボネートが好ましい。炭酸ジエステルの使用量は、上記式(1)、(2)、(3)または、(1)、(2)、(4)の繰返し単位をもたらすためのジヒドロキシ化合物の全モノマーに対して、好ましくは95〜110mol%、より好ましくは98〜104mol%、さらに好ましくは100〜104mol%、特に好ましくは100〜103mol%である。
〈ポリマー物性〉
本発明のポリカーボネート樹脂の屈折率は、温度:25℃、波長:589nmで測定した場合に、1.550以上であり、1.555以上、又は1.560以上であってもよく、1.580以下であり、1.575以下、または1.570以下であってもよい。
本発明のポリカーボネート樹脂の屈折率は、温度:25℃、波長:589nmで測定した場合に、1.550以上であり、1.555以上、又は1.560以上であってもよく、1.580以下であり、1.575以下、または1.570以下であってもよい。
本発明のポリカーボネート樹脂のアッベ数は、34.0以上、34.5以上、35.0以上、35.5以上、36.0以上、36.5以上、又は37.0以上であってもよく、42.0以下、41.5以下、41.0以下、40.5以下、40.0以下、又は39.5以下であってもよい。
ここで、アッベ数は、温度:25℃、波長:486.13nm、587.56nm、656.27nmの屈折率から、下記式を用いて算出する:
νd=(nd−1)/(nF−nC)
nd:波長587.56nmにおける屈折率、
nF:波長486.13nmにおける屈折率、
nC:波長656.27nmにおける屈折率を意味する。
νd=(nd−1)/(nF−nC)
nd:波長587.56nmにおける屈折率、
nF:波長486.13nmにおける屈折率、
nC:波長656.27nmにおける屈折率を意味する。
本発明のポリカーボネート樹脂の比粘度は、0.12〜0.32の範囲にあることが好ましく、0.18〜0.30の範囲にあることがより好ましい。比粘度が0.12〜0.32であると成形性と強度とのバランスに優れる。
比粘度の測定方法は、ポリカーボネート樹脂0.7gを塩化メチレン100mlに溶解した溶液の20℃における比粘度(ηSP)を、オストワルド粘度計にて測定し、以下の式から算出する。
比粘度(ηSP)=(t−t0)/t0
[t0は、塩化メチレンの落下秒数、tは、試料溶液の落下秒数]
比粘度(ηSP)=(t−t0)/t0
[t0は、塩化メチレンの落下秒数、tは、試料溶液の落下秒数]
本発明のポリカーボネート樹脂の配向複屈折(Δn)の絶対値は、10.0×10−3以下であることが好ましく、9.0×10−3以下より好ましく、8.0×10−3以下がさらに好ましく、7.0×10−3以下であることが特に好ましい。配向複屈折(Δn)は、そのポリカーボネート樹脂から得られる厚さ100μmのフィルムをガラス転移温度(Tg)+10℃で2倍延伸した後に、波長589nmにおいて測定する。
本発明のポリカーボネート樹脂は、1mm厚の全光線透過率が、好ましくは80%以上、より好ましくは85%以上、さらに好ましくは88%以上である。
本発明のポリカーボネート樹脂は、23℃、24時間浸漬後の吸水率が0.20%以下であると好ましく、0.18%以下であるとより好ましい。
本発明のポリカーボネート樹脂のTgは、130℃以上、135℃以上、140℃以上、145℃以上、または150℃以上であってもよく、165℃以下、160℃以下、155℃以下、150℃以下、145℃以下、140℃以下であってもよい。
本発明のポリカーボネート樹脂は、湿熱2000hΔbが、好ましくは10以下、より好ましくは5以下、さらに好ましくは3以下、特に好ましくは2以下、最も好ましくは1.5以下である。
湿熱2000hΔbが上限より高い場合は、高温状態で製品を使用したときの色変化が大きくなり、特にレンズ等に成形した場合、像の色が変化することがある。
本発明のポリカーボネート樹脂は、PCT処理前後のΔb値が、好ましくは2以下、より好ましくは1以下、さらに好ましくは0.6以下、特に好ましくは0.5以下、最も好ましくは0.4以下である。
PCT処理前後のΔb値が上限より高い場合は、高温状態で製品を使用したときの色変化が大きくなり、特にレンズ等に成形した場合、像の色が変化することがある。
〈製造方法〉
本発明のポリカーボネート樹脂は、通常のポリカーボネート樹脂を製造するそれ自体公知の反応手段、例えばジヒドロキシ化合物に炭酸ジエステルなどのカーボネート前駆物質を反応させる方法により製造される。
本発明のポリカーボネート樹脂は、通常のポリカーボネート樹脂を製造するそれ自体公知の反応手段、例えばジヒドロキシ化合物に炭酸ジエステルなどのカーボネート前駆物質を反応させる方法により製造される。
《光学部材》
本発明の光学部材は、上記のポリカーボネート樹脂を含む。そのような光学部材としては、上記のポリカーボネート樹脂が有用となる光学用途であれば、特に限定されないが、光ディスク、透明導電性基板、光カード、シート、フィルム、光ファイバー、レンズ、プリズム、光学膜、基盤、光学フィルター、ハードコート膜等を挙げることができる。フィルムとしては、特に光学フィルムを挙げることができる。
本発明の光学部材は、上記のポリカーボネート樹脂を含む。そのような光学部材としては、上記のポリカーボネート樹脂が有用となる光学用途であれば、特に限定されないが、光ディスク、透明導電性基板、光カード、シート、フィルム、光ファイバー、レンズ、プリズム、光学膜、基盤、光学フィルター、ハードコート膜等を挙げることができる。フィルムとしては、特に光学フィルムを挙げることができる。
また、本発明の光学部材には、上記のポリカーボネート樹脂を含む樹脂組成物から構成されていてもよく、その樹脂組成物には、必要に応じて熱安定剤、可塑剤、光安定剤、重合金属不活性化剤、難燃剤、滑剤、帯電防止剤、界面活性剤、抗菌剤、紫外線吸収剤、離型剤等の添加剤を配合することができる。
〈撮像レンズ〉
本発明の光学部材として、特に撮像レンズを挙げることができる。このような撮像レンズとしては、携帯電話、スマートフォン、タブレット端末、パソコン、デジタルカメラ、ビデオカメラ、車載カメラ、監視カメラ等のための撮像レンズを挙げることができる。
本発明の光学部材として、特に撮像レンズを挙げることができる。このような撮像レンズとしては、携帯電話、スマートフォン、タブレット端末、パソコン、デジタルカメラ、ビデオカメラ、車載カメラ、監視カメラ等のための撮像レンズを挙げることができる。
本発明の撮像レンズは、射出成形、圧縮成形、射出圧縮成形、溶融押出成形、キャスティング等の任意の方法により成形、加工することができるが、射出成形が特に好適である。
射出成形の成形条件は特に限定されないが、成形機のシリンダー温度は180〜320℃が好ましく、220〜300℃がより好ましく、240〜280℃が特に好ましい。また、金型温度は70〜130℃が好ましく、80〜125℃がより好ましく、90〜120℃が特に好ましい。射出圧力は5〜170MPaが好ましく、50〜160MPaがより好ましく、100〜150MPaが特に好ましい。
本発明を以下の実施例でさらに具体的に説明をするが、本発明はこれによって限定されるものではない。
《製造例》
〈実施例1〉
39.26g(0.20mol)のトリシクロデカンジメタノール(TCDDM)、40.25g(0.15mol)の4,4’−シクロヘキシリデンビスフェノール(ビスフェノールZ、以下BPZと略す)、46.57g(0.15mol)の4,4’−(3,3,5−トリメチルシクロヘキシリデン)ビスフェノール(BPTMC)、110.32g(0.515mol)のジフェニルカーボネート(以下DPCと略す)、及び触媒として濃度60mmol/Lの炭酸水素ナトリウム水溶液0.033mL(炭酸水素ナトリウム 2.0μmol)と、濃度274mmol/Lのテトラメチルアンモニウムヒドロキシド水溶液0.547mL(テトラメチルアンモニウムヒドロキシド150μmol)を、窒素雰囲気下180℃に加熱し溶融させた。その後、10分間かけて減圧度を20kPaに調整した。60℃/hの速度で250℃まで昇温を行い、フェノールの留出量が、DPCが全部反応したときの理論フェノール発生量の70%になった後、1時間かけて反応器内圧を133Pa以下とした。撹拌して反応を行い、反応終了後フラスコから樹脂を取り出した。反応終了までの時間は3.5時間であった。得られたポリカーボネート樹脂の組成比をNMRによって測定し、原料仕込み量の比率であることを確認した。末端フェノール性水酸基比率は得られたポリカーボネート樹脂の数平均分子量とNMR測定結果から算出した。
〈実施例1〉
39.26g(0.20mol)のトリシクロデカンジメタノール(TCDDM)、40.25g(0.15mol)の4,4’−シクロヘキシリデンビスフェノール(ビスフェノールZ、以下BPZと略す)、46.57g(0.15mol)の4,4’−(3,3,5−トリメチルシクロヘキシリデン)ビスフェノール(BPTMC)、110.32g(0.515mol)のジフェニルカーボネート(以下DPCと略す)、及び触媒として濃度60mmol/Lの炭酸水素ナトリウム水溶液0.033mL(炭酸水素ナトリウム 2.0μmol)と、濃度274mmol/Lのテトラメチルアンモニウムヒドロキシド水溶液0.547mL(テトラメチルアンモニウムヒドロキシド150μmol)を、窒素雰囲気下180℃に加熱し溶融させた。その後、10分間かけて減圧度を20kPaに調整した。60℃/hの速度で250℃まで昇温を行い、フェノールの留出量が、DPCが全部反応したときの理論フェノール発生量の70%になった後、1時間かけて反応器内圧を133Pa以下とした。撹拌して反応を行い、反応終了後フラスコから樹脂を取り出した。反応終了までの時間は3.5時間であった。得られたポリカーボネート樹脂の組成比をNMRによって測定し、原料仕込み量の比率であることを確認した。末端フェノール性水酸基比率は得られたポリカーボネート樹脂の数平均分子量とNMR測定結果から算出した。
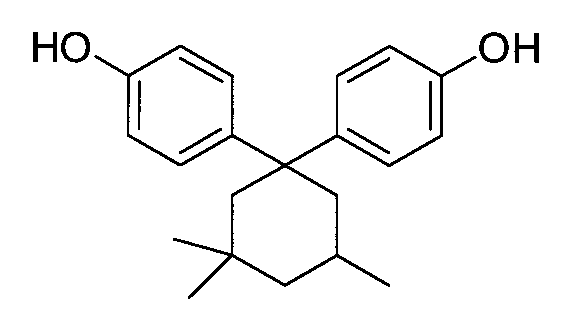
なお、TCDDMは、上記式(1)の繰返し単位を導入するために用いられており、BPZは、上記式(2)の繰返し単位を導入するために用いられている。また、BPTMCは、上記式(3)の繰返し単位を導入するために用いられており、以下の化学構造を有する:
〈実施例2〜6〉
TCDDM、BPZ、及びBPTMCを表1に記載の量に変更したこと以外は実施例1と同様にして、ポリカーボネート樹脂を製造した。なお、得られたポリカーボネート樹脂の組成比をNMRによって測定し、原料使用量の比率であることを確認した。
TCDDM、BPZ、及びBPTMCを表1に記載の量に変更したこと以外は実施例1と同様にして、ポリカーボネート樹脂を製造した。なお、得られたポリカーボネート樹脂の組成比をNMRによって測定し、原料使用量の比率であることを確認した。
〈実施例7〜9〉
BPTMCの代わりに4,4’−(3−メチルシクロヘキシリデン)ビスフェノール(以下BP3MZと略す)を使用したこと、及び各モノマーの量を表1に記載の量に変更したこと以外は実施例1と同様にして、ポリカーボネート樹脂を製造した。なお、得られたポリカーボネート樹脂の組成比をNMRによって測定し、原料使用量の比率であることを確認した。BP3MZは、上記式(3)の繰返し単位を導入するために用いられており、以下の化学構造を有する:
BPTMCの代わりに4,4’−(3−メチルシクロヘキシリデン)ビスフェノール(以下BP3MZと略す)を使用したこと、及び各モノマーの量を表1に記載の量に変更したこと以外は実施例1と同様にして、ポリカーボネート樹脂を製造した。なお、得られたポリカーボネート樹脂の組成比をNMRによって測定し、原料使用量の比率であることを確認した。BP3MZは、上記式(3)の繰返し単位を導入するために用いられており、以下の化学構造を有する:
〈実施例10〉
BPTMCの代わりに、3,3,3’,3’−テトラメチル−1,1’−スピロビインダン−6,6’−ジオール(以下、SBIと略す)を使用したこと、及び各モノマーの量を表1に記載の量に変更したことと反応終了までの時間が4.5時間であったこと以外は実施例1と同様にして、ポリカーボネート樹脂を製造した。なお、得られたポリカーボネート樹脂の組成比をNMRによって測定し、原料使用量の比率であることを確認した。SBIは上記式(4)の繰返し単位を導入するために用いられており、以下の化学構造を有する:
BPTMCの代わりに、3,3,3’,3’−テトラメチル−1,1’−スピロビインダン−6,6’−ジオール(以下、SBIと略す)を使用したこと、及び各モノマーの量を表1に記載の量に変更したことと反応終了までの時間が4.5時間であったこと以外は実施例1と同様にして、ポリカーボネート樹脂を製造した。なお、得られたポリカーボネート樹脂の組成比をNMRによって測定し、原料使用量の比率であることを確認した。SBIは上記式(4)の繰返し単位を導入するために用いられており、以下の化学構造を有する:
(実施例11、12)
DPCの使用量を変更したこと以外は実施例1と同様の方法でポリカーボネート樹脂を製造した。なお、得られたポリカーボネート樹脂の組成比をNMRによって測定し、原料使用量の比率であることを確認した。
DPCの使用量を変更したこと以外は実施例1と同様の方法でポリカーボネート樹脂を製造した。なお、得られたポリカーボネート樹脂の組成比をNMRによって測定し、原料使用量の比率であることを確認した。
〈比較例1〜3〉
TCDDM、BPZ、及びBPTMCを表1に記載の量に変更したこと以外は実施例1と同様にして、ポリカーボネート樹脂を製造した。なお、得られたポリカーボネート樹脂の組成比をNMRによって測定し、原料使用量の比率であることを確認した。
TCDDM、BPZ、及びBPTMCを表1に記載の量に変更したこと以外は実施例1と同様にして、ポリカーボネート樹脂を製造した。なお、得られたポリカーボネート樹脂の組成比をNMRによって測定し、原料使用量の比率であることを確認した。
《評価方法》
〈ポリマー組成および末端フェノール性水酸基比率〉
日本電子株式会社製JNM−ECZ400Sにて1H NMRを測定することによって、各ポリマーの組成比を算出した。また、GPC測定で得られる数平均分子量とこのスペクトルデータを使用して、各ポリマーの末端フェノール性水酸基比率(%)を定量化した。
〈ポリマー組成および末端フェノール性水酸基比率〉
日本電子株式会社製JNM−ECZ400Sにて1H NMRを測定することによって、各ポリマーの組成比を算出した。また、GPC測定で得られる数平均分子量とこのスペクトルデータを使用して、各ポリマーの末端フェノール性水酸基比率(%)を定量化した。
(1)末端フェノール性水酸基のオルト位のプロトンを、ポリマーの1H NMR測定で観測し、6.58〜6.83ppm該当ピークの積分を取りこの強度を1とする。これは、水酸基1つに対し、プロトン2個分である。この時、同時に上記式(1)に由来するTCDDMの酸素原子の隣のアルキル基プロトン4個分である3.8〜4.2ppmピークの積分強度を求め、(A)とする。
(2)ポリマーのGPC測定で得られる数平均分子量と各繰返し単位の分子量とmol比からポリマーの平均重合度(B)を求める。
(3)末端フェノール性水酸基比率(%)は、[上記式(1)のmol%]×(B)/(A)として計算した。
実施例10については、Makromolekulare Chem. 88(1965) 215−231の記載をもとに、チタン発色法を用いて、480nm, 520nmにおけるモノマーの吸光度を測定して、連立方程式を解くことにより末端フェノール性水酸基量を求め、GPC測定で得られる平均重合度から全末端量を算出し、末端フェノール性水酸基比率(%)=(末端フェノール性水酸基量/全ポリマー末端量)×100 として求めた。
〈光学特性〉
(屈折率)
各ポリマーの3mm厚試験片を作製し研磨した後、島津製作所製のカルニュー精密屈折計KPR−2000を使用して、屈折率nd(589nm)を測定した。
(屈折率)
各ポリマーの3mm厚試験片を作製し研磨した後、島津製作所製のカルニュー精密屈折計KPR−2000を使用して、屈折率nd(589nm)を測定した。
(アッベ数)
また、同様にして、アッベ数を算出した。
アッベ数の測定波長は、486.13nm、587.56nm、656.27nmの屈折率から下記の式を用いて算出した。
νd=(nd−1)/(nF−nC)
nd:波長587.56nmにおける屈折率、
nF:波長486.13nmにおける屈折率、
nC:波長656.27nmにおける屈折率を意味する。
また、同様にして、アッベ数を算出した。
アッベ数の測定波長は、486.13nm、587.56nm、656.27nmの屈折率から下記の式を用いて算出した。
νd=(nd−1)/(nF−nC)
nd:波長587.56nmにおける屈折率、
nF:波長486.13nmにおける屈折率、
nC:波長656.27nmにおける屈折率を意味する。
(配向複屈折の絶対値)
ポリカーボネート樹脂を塩化メチレンに溶解した後、ガラスシャーレ上にキャストし、十分乾燥することで厚さ100μmのキャストフィルムを作製した。該フィルムをTg+10℃で2倍延伸し、日本分光(株)製エリプソメーターM−220を用いて589nmにおける位相差(Re)を測定し、下記式より配向複屈折の絶対値(|Δn|)を求めた。
|Δn|=|Re/d|
Δn:配向複屈折
Re:位相差(nm)
d:厚さ(nm)
ポリカーボネート樹脂を塩化メチレンに溶解した後、ガラスシャーレ上にキャストし、十分乾燥することで厚さ100μmのキャストフィルムを作製した。該フィルムをTg+10℃で2倍延伸し、日本分光(株)製エリプソメーターM−220を用いて589nmにおける位相差(Re)を測定し、下記式より配向複屈折の絶対値(|Δn|)を求めた。
|Δn|=|Re/d|
Δn:配向複屈折
Re:位相差(nm)
d:厚さ(nm)
〈湿熱2000hΔb〉
各ポリマーの2mmの厚さの成形板を作製しエスペック株式会社の小型環境試験器SH−241の湿熱処理機を使用して、温度85℃、相対湿度85%、処理時間2000時間の条件下で湿熱処理を行った。そして、サンプル1gを5mLの塩化メチレンに溶解し、その溶液色相のb値を日立製U−3310形分光光度計で測定することで、試験前後のサンプルの溶液のΔb(湿熱2000h処理後の溶液b値−湿熱2000h処理前の溶液b値)を得た。
各ポリマーの2mmの厚さの成形板を作製しエスペック株式会社の小型環境試験器SH−241の湿熱処理機を使用して、温度85℃、相対湿度85%、処理時間2000時間の条件下で湿熱処理を行った。そして、サンプル1gを5mLの塩化メチレンに溶解し、その溶液色相のb値を日立製U−3310形分光光度計で測定することで、試験前後のサンプルの溶液のΔb(湿熱2000h処理後の溶液b値−湿熱2000h処理前の溶液b値)を得た。
〈高温耐湿性:PCT〉
(PCT処理前後のΔb値)
各ポリマーの2mmの厚さの成形板を作製し、ヤマト科学製蒸気滅菌器SN−510を使用して、120℃、2気圧の条件下で11時間蒸気処理を行った(いわゆる、プレッシャークッカー試験(Pressure Cooker Test):「PCT」と略す)。
PCT処理前後のポリマーを1g/5mLの濃度で塩化メチレンに溶解させ、その溶液色相のb値を日立製U−3310形分光光度計で測定することで、PCT処理前後のサンプルの溶液のΔb(PCT処理後の溶液b値−PCT処理前の溶液b値)を得た。
また、PCT処理前後の成形板の白化及び変形の有無を目視にて評価した。評価は以下の基準で行った。
(PCT処理後の成形片の白化)
○:不透明な部分が全くなく透明である。
△:若干不透明な部分が見られる。
×:全体が不透明である。
(PCT処理後の成形片の変形)
○:全く変形なし。
△:ほぼ元の形を保っているがやや変形が見られる。
×:元の形を保持していない。
(PCT処理後の成形片の総合評価)
○:上記白化、変形の評価おいて、共に○の場合。
△:上記白化、変形の評価おいて、それぞれ△○、○△、△△の場合。
×:上記白化、変形の評価おいて、少なくとも一つが×の場合。
(PCT処理前後のΔb値)
各ポリマーの2mmの厚さの成形板を作製し、ヤマト科学製蒸気滅菌器SN−510を使用して、120℃、2気圧の条件下で11時間蒸気処理を行った(いわゆる、プレッシャークッカー試験(Pressure Cooker Test):「PCT」と略す)。
PCT処理前後のポリマーを1g/5mLの濃度で塩化メチレンに溶解させ、その溶液色相のb値を日立製U−3310形分光光度計で測定することで、PCT処理前後のサンプルの溶液のΔb(PCT処理後の溶液b値−PCT処理前の溶液b値)を得た。
また、PCT処理前後の成形板の白化及び変形の有無を目視にて評価した。評価は以下の基準で行った。
(PCT処理後の成形片の白化)
○:不透明な部分が全くなく透明である。
△:若干不透明な部分が見られる。
×:全体が不透明である。
(PCT処理後の成形片の変形)
○:全く変形なし。
△:ほぼ元の形を保っているがやや変形が見られる。
×:元の形を保持していない。
(PCT処理後の成形片の総合評価)
○:上記白化、変形の評価おいて、共に○の場合。
△:上記白化、変形の評価おいて、それぞれ△○、○△、△△の場合。
×:上記白化、変形の評価おいて、少なくとも一つが×の場合。
〈レンズの光学歪み評価〉
シリンダー温度280℃、金型温度120℃で、住友重機(株)製SE30DU射出成形機を用いて厚さ0.2mm、凸面曲率半径5mm、凹面曲率半径4mm、Φ5mmの非球面レンズを射出成形した。非球面レンズを二枚の偏光板の間に挟み直交ニコル法で光漏れを目視することにより光学歪みを評価した。評価は以下の基準で行った。
◎:殆ど光漏れがない。
〇:僅かに光漏れが認められる。
△:光漏れがある。
×:光漏れが顕著である。
シリンダー温度280℃、金型温度120℃で、住友重機(株)製SE30DU射出成形機を用いて厚さ0.2mm、凸面曲率半径5mm、凹面曲率半径4mm、Φ5mmの非球面レンズを射出成形した。非球面レンズを二枚の偏光板の間に挟み直交ニコル法で光漏れを目視することにより光学歪みを評価した。評価は以下の基準で行った。
◎:殆ど光漏れがない。
〇:僅かに光漏れが認められる。
△:光漏れがある。
×:光漏れが顕著である。
《結果》
各実施例及び比較例の構成並びにその評価結果を、以下の表1にまとめた。
各実施例及び比較例の構成並びにその評価結果を、以下の表1にまとめた。
実施例1〜12は、従来技術(特許文献1)に対応する比較例1と、屈折率及びアッベ数において同等であり、複屈折の上昇も許容範囲でありながら、高温耐湿性試験の結果が良好であった。
Claims (13)
- 上記式(3)または上記式(4)の繰返し単位が、5mol%以上50mol%以下である、請求項1に記載のポリカーボネート樹脂。
- 上記式(1)の繰返し単位が、10mol%以上55mol%以下である、請求項1または2に記載のポリカーボネート樹脂。
- 上記式(2)の繰返し単位が、3mol%以上65mol%以下である、請求項1〜3のいずれか一項に記載のポリカーボネート樹脂。
- 上記式(3)中、nが1〜3の整数である請求項1〜4のいずれか一項に記載のポリカーボネート樹脂。
- 上記式(3)の繰り返し単位が、4,4’−(3,3,5−トリメチルシクロヘキシリデン)ビスフェノール、または4,4’−(3−メチルシクロヘキシリデン)ビスフェノールに由来する構造である、請求項1〜5のいずれか一項に記載のポリカーボネート樹脂。
- 全ポリマー末端に対する末端フェノール性水酸基比率が60%以下である、請求項1〜7のいずれか一項に記載のポリカーボネート樹脂。
- アッベ数が33.0〜40.5である、請求項1〜8のいずれか一項に記載のポリカーボネート樹脂。
- 請求項1〜9のいずれか一項に記載のポリカーボネート樹脂を含む、光学部材。
- レンズである、請求項10に記載の光学部材。
- 光学フィルムである、請求項10に記載の光学部材。
- 携帯電話、スマートフォン、タブレット端末、パソコン、デジタルカメラ、ビデオカメラ、車載カメラ、または監視カメラのいずれかに用いるための撮像レンズである、請求項11に記載の光学部材。
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2019101277A JP2020193301A (ja) | 2019-05-30 | 2019-05-30 | ポリカーボネート樹脂及びそれを含む光学部材 |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2019101277A JP2020193301A (ja) | 2019-05-30 | 2019-05-30 | ポリカーボネート樹脂及びそれを含む光学部材 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| JP2020193301A true JP2020193301A (ja) | 2020-12-03 |
Family
ID=73545599
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2019101277A Pending JP2020193301A (ja) | 2019-05-30 | 2019-05-30 | ポリカーボネート樹脂及びそれを含む光学部材 |
Country Status (1)
| Country | Link |
|---|---|
| JP (1) | JP2020193301A (ja) |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2023054665A1 (ja) * | 2021-09-30 | 2023-04-06 | 三菱ケミカル株式会社 | 熱可塑性樹脂組成物、通信機器部材、並びにマイクロ波及び/又はミリ波用通信機器 |
Citations (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2000063506A (ja) * | 1998-06-12 | 2000-02-29 | Mitsubishi Gas Chem Co Inc | 芳香族―脂肪族共重合ポリカ―ボネ―ト |
| JP2002539310A (ja) * | 1999-03-18 | 2002-11-19 | ゼネラル・エレクトリック・カンパニイ | 光学製品での使用に適したポリカーボネート |
| JP2003034718A (ja) * | 2001-07-24 | 2003-02-07 | Mitsui Chemicals Inc | ポリカーボネート共重合体およびその用途 |
| JP2015183026A (ja) * | 2014-03-20 | 2015-10-22 | 帝人株式会社 | 芳香族−脂肪族ポリカーボネートおよび、それらからなるプラスチックレンズ |
-
2019
- 2019-05-30 JP JP2019101277A patent/JP2020193301A/ja active Pending
Patent Citations (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2000063506A (ja) * | 1998-06-12 | 2000-02-29 | Mitsubishi Gas Chem Co Inc | 芳香族―脂肪族共重合ポリカ―ボネ―ト |
| JP2002539310A (ja) * | 1999-03-18 | 2002-11-19 | ゼネラル・エレクトリック・カンパニイ | 光学製品での使用に適したポリカーボネート |
| JP2003034718A (ja) * | 2001-07-24 | 2003-02-07 | Mitsui Chemicals Inc | ポリカーボネート共重合体およびその用途 |
| JP2015183026A (ja) * | 2014-03-20 | 2015-10-22 | 帝人株式会社 | 芳香族−脂肪族ポリカーボネートおよび、それらからなるプラスチックレンズ |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2023054665A1 (ja) * | 2021-09-30 | 2023-04-06 | 三菱ケミカル株式会社 | 熱可塑性樹脂組成物、通信機器部材、並びにマイクロ波及び/又はミリ波用通信機器 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP7072637B2 (ja) | ポリカーボネート樹脂及びそれを含む光学部材 | |
| KR101455889B1 (ko) | 폴리카보네이트 수지 및 그의 제조방법 | |
| JP6727200B2 (ja) | 撮像レンズ | |
| WO2021220811A1 (ja) | 熱可塑性樹脂および光学部材 | |
| JP2020193301A (ja) | ポリカーボネート樹脂及びそれを含む光学部材 | |
| CN104781306B (zh) | 聚缩甲醛树脂共聚物及制造方法 | |
| JP2017210569A (ja) | 光学用ポリカーボネート樹脂 | |
| JP2024026220A (ja) | 熱可塑性樹脂及びそれを含む光学部材 | |
| KR20240053002A (ko) | 열가소성 수지 및 광학 부재 | |
| JP2022011687A (ja) | 熱可塑性樹脂および光学部材 | |
| TWI851561B (zh) | 聚碳酸酯樹脂及含其之光學零件 | |
| WO2011007427A1 (ja) | 溶解性、親和性に優れるポリカーボネート材料の製造方法ならびにそれらからなるコンタクトレンズ材料 | |
| WO2020189409A1 (ja) | ポリエステルカーボネート樹脂、及び当該樹脂を含む樹脂組成物を成形してなる成形体 | |
| KR20200045771A (ko) | 폴리에스테르계 수지 및 이를 포함하는 광학 부재 | |
| JP2024055310A (ja) | 熱可塑性樹脂組成物及びそれを含む光学部材 | |
| US20110077372A1 (en) | Ether-containing cyclic structure-containing polymer, polymer composition for optical material, and molded article thereof, optical component and lens | |
| JP2023067738A (ja) | 熱可塑性樹脂および光学部材 | |
| TW202214548A (zh) | 樹脂組成物 | |
| JP2024016426A (ja) | 熱可塑性樹脂および光学部材 | |
| WO2022158123A1 (ja) | 熱可塑性樹脂およびそれからなる光学部材 | |
| JP2024118588A (ja) | 熱可塑性樹脂組成物及びそれを含む光学部材 | |
| CN115160551A (zh) | 一种聚碳酸酯树脂及其制备方法,一种光学树脂 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20220222 |
|
| A977 | Report on retrieval |
Free format text: JAPANESE INTERMEDIATE CODE: A971007 Effective date: 20221215 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20230110 |
|
| A02 | Decision of refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A02 Effective date: 20230530 |