JP2017514522A - ヒト化可変性リンパ球受容体(vlr)および組成物ならびにそれに関連する使用 - Google Patents
ヒト化可変性リンパ球受容体(vlr)および組成物ならびにそれに関連する使用 Download PDFInfo
- Publication number
- JP2017514522A JP2017514522A JP2017510445A JP2017510445A JP2017514522A JP 2017514522 A JP2017514522 A JP 2017514522A JP 2017510445 A JP2017510445 A JP 2017510445A JP 2017510445 A JP2017510445 A JP 2017510445A JP 2017514522 A JP2017514522 A JP 2017514522A
- Authority
- JP
- Japan
- Prior art keywords
- amino acid
- certain embodiments
- acid sequence
- seq
- sequence
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K14/00—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- C07K14/435—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
- C07K14/705—Receptors; Cell surface antigens; Cell surface determinants
- C07K14/70503—Immunoglobulin superfamily
- C07K14/7051—T-cell receptor (TcR)-CD3 complex
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K14/00—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- C07K14/435—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
- C07K14/46—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans from vertebrates
- C07K14/461—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans from vertebrates from fish
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2319/00—Fusion polypeptide
- C07K2319/30—Non-immunoglobulin-derived peptide or protein having an immunoglobulin constant or Fc region, or a fragment thereof, attached thereto
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N15/00—Mutation or genetic engineering; DNA or RNA concerning genetic engineering, vectors, e.g. plasmids, or their isolation, preparation or purification; Use of hosts therefor
Abstract
Description
本発明は、国立衛生研究所(National Institutes of Health)によって授与された助成金5R01A1072435の下で政府の支援を受けてなされた。政府は、本発明における特定の権利を有する。
本願は、2014年5月2日に出願された米国仮特許出願第61/987,566号明細書(本明細書でその全体が参照により援用される)に対して優先権を主張する。
特定の実施形態では、本開示は、分子に対する特異的結合剤を作製する方法であって、可変性リンパ球受容体(VLR)を有する細胞が分子に結合し、かつ無顎類の形質細胞が分子に結合する可変性リンパ球受容体(VLR)を生成するような条件下で、分子を無顎類に投与するステップを含む、方法に関する。標的分子に結合する可変性リンパ球受容体(VLR)のアミノ酸配列の提供は、種々の方法によって達成され得る。Yuらは、ヒトT細胞で免疫されたヤツメウナギ幼生由来のモノクローナルVLR抗体パネルの作製、ならびに抗原精製および質量分析同定のための組換えモノクローナルVLR抗体の使用について報告している。J Immunol Methods,2012,386(1−2):43−9、表題「Purification and identification of cell surface antigens using lamprey monoclonal antibodies」を参照のこと。
特定の実施形態では、本開示は、分子に結合する無顎類の可変性リンパ球受容体(VLR)のアミノ酸配列を提供するステップと;可変性リンパ球受容体中のどのアミノ酸が、結合分子に空間的に最も近い状態であるか、および/または結合分子に対してイオン相互作用をもたらすか、および/または水素結合するか、および/またはファンデルワールス力をもたらすかを評価し、可変性リンパ球受容体における標的アミノ酸を提供するステップと;可変性リンパ球受容体(VLR)アミノ酸配列に対して20%超、25%超、もしくは30%超またはそれより大きい配列同一性を有する既知のヒトアミノ酸配列を提供するステップと;分子に特異的に結合するように形成された修飾ヒトアミノ酸配列を提供するため、標的アミノ酸および可変性リンパ球受容体中の標的アミノ酸を囲む十分な数のアミノ酸を既知のヒトアミノ酸配列内部で置換するステップと;組換え核酸から修飾ヒトアミノ酸配列を発現させるステップと、を含む方法によって作成される、分子に特異的に結合する単離された修飾ヒトアミノ酸配列に関する。
特定の実施形態では、本開示は、(配列番号10)
(式中、各位置のXは個別かつ独立に任意のアミノ酸であり、nは5〜20の間であるかまたはnは10〜18の間であり、またはnは14、15、もしくは16であり、但しポリペプチドは、(配列番号11)IVDCRG、(配列番号12)EIRLEQ、(配列番号13)RIDLSN、(配列番号14)SLVLYG、(配列番号15)LLLLNA、(配列番号16)LLSLYD、および(配列番号17)TMHLAQから選択される野生型Slit2−D2配列の少なくとも1つ、2つ、3つ、4つ、5つ 6つ、もしくは全部を有しない)を含む単離された組換えポリペプチドまたはその変異体を検討する。特定の実施形態では、変異体は、1つ、2つ、または3つのアミノ酸の置換を有し、但しアミノ酸の置換はXアミノ酸でない。特定の実施形態では、置換は保存的置換である。
(式中、各位置のXは個別かつ独立に任意のアミノ酸であり、nは5〜20の間であるかまたはnは10〜18の間であり、またはnは14、15、もしくは16であり、但し任意選択的に、ポリペプチドは、(配列番号11)IVDCRG、(配列番号12)EIRLEQ、(配列番号13)RIDLSN、(配列番号14)SLVLYG、(配列番号15)LLLLNA、(配列番号16)LLSLYD、および(配列番号17)TMHLAQから選択される野生型Slit2−D2配列の少なくとも1つ、2つ、3つ、4つ、5つ、6つ、もしくは全部を有しない)を含む単離された組換えポリペプチドまたはその変異体を検討する。
(式中、各位置のXは個別かつ独立に任意のアミノ酸であり、nは5〜20の間であるかまたはnは10〜18の間であり、またはnは14、15、もしくは16であり、但し任意選択的に、ポリペプチドは、(配列番号12)EIRLEQ、(配列番号13)RIDLSN、(配列番号14)SLVLYG、(配列番号15)LLLLNA、(配列番号16)LLSLYD、および(配列番号17)TMHLAQから選択される野生型Slit2−D2配列の少なくとも1つ、2つ、3つ、4つ、5つ、もしくは全部を有しない)を含む単離された組換えポリペプチドまたはその変異体を検討する。特定の実施形態では、変異体は、1つ、2つ、もしくは3つのアミノ酸の置換、欠失または挿入を有し、但しアミノ酸の置換、欠失または挿入はXアミノ酸でない。特定の実施形態では、置換は保存的置換である。
(式中、各位置のXは個別かつ独立に任意のアミノ酸であり、nは5〜20の間であるかまたはnは10〜18の間であり、またはnは14、15、もしくは16であり、但し任意選択的に、ポリペプチドは、(配列番号13)RIDLSN、(配列番号14)SLVLYG、(配列番号15)LLLLNA、(配列番号16)LLSLYD、および(配列番号17)TMHLAQから選択される野生型Slit2−D2配列の少なくとも1つ、2つ、3つ、4つ、もしくは全部を有しない)を含む単離された組換えポリペプチドまたはその変異体を検討する。特定の実施形態では、変異体は、1つ、2つ、もしくは3つのアミノ酸の置換、欠失または挿入を有し、但しアミノ酸の置換、欠失または挿入はXアミノ酸でない。特定の実施形態では、置換は保存的置換である。
(式中、各位置のXは個別かつ独立に任意のアミノ酸であり、nは5〜20の間であるかまたはnは10〜18の間であり、またはnは14、15、もしくは16であり、但し任意選択的に、ポリペプチドは、(配列番号14)SLVLYG、(配列番号15)LLLLNA、(配列番号16)LLSLYD、および(配列番号17)TMHLAQから選択される野生型Slit2−D2配列の少なくとも1つ、2つ、3つ、4つ、もしくは全部を有しない)を含む単離された組換えポリペプチドまたはその変異体を検討する。特定の実施形態では、変異体は、1つ、2つ、もしくは3つのアミノ酸の置換、欠失または挿入を有し、但しアミノ酸の置換、欠失または挿入はXアミノ酸でない。特定の実施形態では、置換は保存的置換である。
(式中、各位置のXは個別かつ独立に任意のアミノ酸であり、nは5〜20の間であるかまたはnは10〜18の間であり、またはnは14、15、もしくは16であり、但し任意選択的に、ポリペプチドは、(配列番号14)SLVLYG、(配列番号15)LLLLNA、(配列番号16)LLSLYD、および(配列番号17)TMHLAQから選択される野生型Slit2−D2配列の少なくとも1つ、2つ、3つ、4つ、もしくは全部を有しない)を含む単離された組換えポリペプチドまたはその変異体を検討する。特定の実施形態では、変異体は、1つ、2つ、もしくは3つのアミノ酸の置換、欠失または挿入を有し、但しアミノ酸の置換、欠失または挿入はXアミノ酸でない。特定の実施形態では、置換は保存的置換である。
(式中、各位置のXは個別かつ独立に任意のアミノ酸であり、nは5〜20の間であるかまたはnは10〜18の間であり、またはnは14、15、もしくは16であり、但し任意選択的に、ポリペプチドは、(配列番号15)LLLLNA、(配列番号16)LLSLYD、および(配列番号17)TMHLAQから選択される野生型Slit2−D2配列の少なくとも1つ、2つ、3つ、4つ、もしくは全部を有しない)を含む単離された組換えポリペプチドまたはその変異体を検討する。特定の実施形態では、変異体は、1つ、2つ、もしくは3つのアミノ酸の置換、欠失または挿入を有し、但し、アミノ酸の置換、欠失または挿入はXアミノ酸でない。特定の実施形態では、置換は保存的置換である。
(式中、各位置のXは個別かつ独立に任意のアミノ酸であり、nは5〜20の間であるかまたはnは10〜18の間であり、またはnは14、15、もしくは16であり、但し任意選択的に、ポリペプチドは、(配列番号16)LLSLYDおよび(配列番号17)TMHLAQから選択される野生型Slit2−D2配列の少なくとも1つ、2つ、3つ、4つ、もしくは全部を有しない)を含む単離された組換えポリペプチドまたはその変異体を検討する。特定の実施形態では、変異体は、1つ、2つ、もしくは3つのアミノ酸の置換、欠失または挿入を有し、但しアミノ酸の置換、欠失または挿入はXアミノ酸でない。特定の実施形態では、置換は保存的置換である。
(式中、各位置のXは個別かつ独立に任意のアミノ酸であり、nは5〜20の間であるかまたはnは10〜18の間であり、またはnは14、15、もしくは16であり、但し任意選択的に、ポリペプチドは、(配列番号12)EIRLEQ、(配列番号13)RIDLSN、(配列番号14)SLVLYG、(配列番号15)LLLLNA、(配列番号16)LLSLYD、および(配列番号17)TMHLAQから選択される野生型Slit2−D2配列の少なくとも1つ、2つ、3つ、4つ、5つ、もしくは全部を有しない)を含む単離された組換えポリペプチドまたはその変異体を検討する。特定の実施形態では、変異体は、1つ、2つ、もしくは3つのアミノ酸の置換、欠失または挿入を有し、但しアミノ酸の置換、欠失または挿入はXアミノ酸でない。特定の実施形態では、置換は保存的置換である。
(式中、各位置のXは個別かつ独立に任意のアミノ酸であり、nは5〜20の間であるかまたはnは10〜18の間であり、またはnは14、15、もしくは16であり、但し任意選択的に、ポリペプチドは、(配列番号13)RIDLSN、(配列番号14)SLVLYG、(配列番号15)LLLLNA、(配列番号16)LLSLYD、および(配列番号17)TMHLAQから選択される野生型Slit2−D2配列の少なくとも1つ、2つ、3つ、4つ、もしくは全部を有しない)を含む単離された組換えポリペプチドまたはその変異体を検討する。特定の実施形態では、変異体は、1つ、2つ、もしくは3つのアミノ酸の置換、欠失または挿入を有し、但しアミノ酸の置換、欠失または挿入はXアミノ酸でない。特定の実施形態では、置換は保存的置換である。
(式中、各位置のXは個別かつ独立に任意のアミノ酸であり、nは5〜20の間であるかまたはnは10〜18の間であり、またはnは14、15、もしくは16であり、但し任意選択的に、ポリペプチドは、(配列番号14)SLVLYG、(配列番号15)LLLLNA、(配列番号16)LLSLYD、および(配列番号17)TMHLAQから選択される野生型Slit2−D2配列の少なくとも1つ、2つ、3つ、4つ、もしくは全部を有しない)を含む単離された組換えポリペプチドまたはその変異体を検討する。特定の実施形態では、変異体は、1つ、2つ、もしくは3つのアミノ酸の置換、欠失または挿入を有し、但しアミノ酸の置換、欠失または挿入はXアミノ酸でない。特定の実施形態では、置換は保存的置換である。
(式中、各位置のXは個別かつ独立に任意のアミノ酸であり、nは5〜20の間であるかまたはnは10〜18の間であり、またはnは14、15、もしくは16であり、但し任意選択的に、ポリペプチドは、(配列番号14)SLVLYG、(配列番号15)LLLLNA、(配列番号16)LLSLYD、および(配列番号17)TMHLAQから選択される野生型Slit2−D2配列の少なくとも1つ、2つ、3つ、もしくは全部を有しない)を含む単離された組換えポリペプチドまたはその変異体を検討する。特定の実施形態では、変異体は、1つ、2つ、もしくは3つのアミノ酸の置換、欠失または挿入を有し、但しアミノ酸の置換、欠失または挿入はXアミノ酸でない。特定の実施形態では、置換は保存的置換である。
(式中、各位置のXは個別かつ独立に任意のアミノ酸であり、nは5〜20の間であるかまたはnは10〜18の間であり、またはnは14、15、もしくは16であり、但し任意選択的に、ポリペプチドは、(配列番号15)LLLLNA、(配列番号16)LLSLYD、および(配列番号17)TMHLAQから選択される野生型Slit2−D2配列の少なくとも1つ、2つ、もしくは全部を有しない)を含む単離された組換えポリペプチドまたはその変異体を検討する。特定の実施形態では、変異体は、1つ、2つ、もしくは3つのアミノ酸の置換、欠失または挿入を有し、但しアミノ酸の置換、欠失または挿入はXアミノ酸でない。特定の実施形態では、置換は保存的置換である。
(式中、各位置のXは個別かつ独立に任意のアミノ酸であり、nは5〜20の間であるかまたはnは10〜18の間であり、またはnは14、15、もしくは16であり、但し任意選択的に、ポリペプチドは、(配列番号16)LLSLYDおよび(配列番号17)TMHLAQから選択される野生型Slit2−D2配列の少なくとも1つもしくは全部を有しない)を含む単離された組換えポリペプチドまたはその変異体を検討する。特定の実施形態では、変異体は、1つ、2つ、もしくは3つのアミノ酸の置換、欠失または挿入を有し、但しアミノ酸の置換、欠失または挿入はXアミノ酸でない。
(式中、各位置のXは個別かつ独立に任意のアミノ酸であり、但し、ポリペプチドは、(配列番号16)LLSLYDおよび(配列番号17)TMHLAQから選択される野生型Slit2−D2配列の少なくとも1つを有しない)を含む単離された組換えポリペプチドまたはその変異体を検討する。特定の実施形態では、変異体は、1つ、2つ、もしくは3つのアミノ酸の置換、欠失または挿入を有し、但しアミノ酸の置換はXアミノ酸でない。特定の実施形態では、置換は保存的置換である。
(式中、各位置のXは個別かつ独立に任意のアミノ酸であり、但しポリペプチドは、(配列番号15)LLLLNA、(配列番号16)LLSLYD、および(配列番号17)TMHLAQから選択される野生型Slit2−D2配列の少なくとも1つ、2つ、もしくは全部を有しない)を含む単離された組換えポリペプチドまたはその変異体を検討する。特定の実施形態では、変異体は、1つ、2つ、もしくは3つのアミノ酸の置換を有し、但しアミノ酸の置換はXアミノ酸でない。特定の実施形態では、置換は保存的置換である。
特定の実施形態では、本開示は、(配列番号39)
(式中、各位置のXは個別かつ独立に任意のアミノ酸であり、nは5〜20の間であるかまたはnは10〜18の間であり、またはnは14、15、もしくは16である)を含む単離された組換えポリペプチドまたはその変異体を検討する。特定の実施形態では、本明細書に開示される配列のいずれにおいても、[X]nは[X]m−[VLRまたはMM3のループ配列]または[X]m−[VLRまたはMM3のループ配列]Aである(式中、[X]mは、任意選択的にX1、X1X2、X1X2X3、X1X2X3X4である(式中、X1はH、X2はT、X3はN、およびX4はPである))。
(式中、各位置のXは個別かつ独立に任意のアミノ酸であり、nは5〜20の間であるかまたはnは10〜18の間であり、またはnは14、15、もしくは16である)を含む単離された組換えポリペプチドまたはその変異体を検討する。特定の実施形態では、変異体は、1つ、2つ、もしくは3つのアミノ酸の置換、欠失または挿入を有し、但しアミノ酸の置換、欠失または挿入はXアミノ酸でない。特定の実施形態では、置換は保存的置換である。
(式中、各位置のXは個別かつ独立に任意のアミノ酸であり、nは5〜20の間であるかまたはnは10〜18の間であり、またはnは14、15、もしくは16である)を含む単離された組換えポリペプチドまたはその変異体を検討する。特定の実施形態では、変異体は、1つ、2つ、もしくは3つのアミノ酸の置換、欠失または挿入を有し、但しアミノ酸の置換、欠失または挿入はXアミノ酸でない。特定の実施形態では、置換は保存的置換である。
(式中、各位置のXは個別かつ独立に任意のアミノ酸であり、nは5〜20の間であるかまたはnは10〜18の間であり、またはnは14、15、もしくは16である)を含む単離された組換えポリペプチドまたはその変異体を検討する。特定の実施形態では、変異体は、1つ、2つ、もしくは3つのアミノ酸の置換、欠失または挿入を有し、但しアミノ酸の置換、欠失または挿入はXアミノ酸でない。特定の実施形態では、置換は保存的置換である。
(式中、各位置のXは個別かつ独立に任意のアミノ酸であり、nは5〜20の間であるかまたはnは10〜18の間であり、またはnは14、15、もしくは16である)を含む単離された組換えポリペプチドまたはその変異体を検討する。特定の実施形態では、変異体は、1つ、2つ、もしくは3つのアミノ酸の置換、欠失または挿入を有し、但しアミノ酸の置換、欠失または挿入はXアミノ酸でない。特定の実施形態では、置換は保存的置換である。
(式中、各位置のXは個別かつ独立に任意のアミノ酸であり、nは5〜20の間であるかまたはnは10〜18の間であり、またはnは14、15、もしくは16である)を含む単離された組換えポリペプチドまたはその変異体を検討する。特定の実施形態では、変異体は、1つ、2つ、もしくは3つのアミノ酸の置換、欠失または挿入を有し、但しアミノ酸の置換、欠失または挿入はXアミノ酸でない。特定の実施形態では、置換は保存的置換である。
(式中、各位置のXは個別かつ独立に任意のアミノ酸であり、nは5〜20の間であるかまたはnは10〜18の間であり、またはnは14、15、もしくは16である)を含む単離された組換えポリペプチドまたはその変異体を検討する。特定の実施形態では、変異体は、1つ、2つ、もしくは3つのアミノ酸の置換、欠失または挿入を有し、但しアミノ酸の置換、欠失または挿入はXアミノ酸でない。特定の実施形態では、置換は保存的置換である。
(式中、各位置のXは個別かつ独立に任意のアミノ酸であり、nは5〜20の間であるかまたはnは10〜18の間であり、またはnは14、15、もしくは16である)を含む単離された組換えポリペプチドまたはその変異体を検討する。特定の実施形態では、変異体は、1つ、2つ、もしくは3つのアミノ酸の置換、欠失または挿入を有し、但しアミノ酸の置換、欠失または挿入はXアミノ酸でない。特定の実施形態では、置換は保存的置換である。
(式中、各位置のXは個別かつ独立に任意のアミノ酸であり、nは5〜20の間であるかまたはnは10〜18の間であり、またはnは14、15、もしくは16である)を含む単離された組換えポリペプチドまたはその変異体を検討する。特定の実施形態では、変異体は、1つ、2つ、もしくは3つのアミノ酸の置換、欠失または挿入を有し、但しアミノ酸の置換、欠失または挿入はXアミノ酸でない。特定の実施形態では、置換は保存的置換である。
(式中、各位置のXは個別かつ独立に任意のアミノ酸であり、nは5〜20の間であるかまたはnは10〜18の間であり、またはnは14、15、もしくは16である)を含む単離された組換えポリペプチドまたはその変異体を検討する。特定の実施形態では、変異体は、1つ、2つ、もしくは3つのアミノ酸の置換、欠失または挿入を有し、但しアミノ酸の置換、欠失または挿入はXアミノ酸でない。特定の実施形態では、置換は保存的置換である。
(式中、各位置のXは個別かつ独立に任意のアミノ酸である)を含む単離された組換えポリペプチドまたはその変異体を検討する。特定の実施形態では、変異体は、1つ、2つ、もしくは3つのアミノ酸の置換、欠失または挿入を有し、但しアミノ酸の置換、欠失または挿入はXアミノ酸でない。特定の実施形態では、置換は保存的置換である。
(式中、各位置のXは個別かつ独立に任意のアミノ酸である)を含む単離された組換えポリペプチドまたはその変異体を検討する。特定の実施形態では、変異体は、1つ、2つ、もしくは3つのアミノ酸の置換、欠失または挿入を有し、但しアミノ酸の置換、欠失または挿入はXアミノ酸でない。特定の実施形態では、置換は保存的置換である。
(式中、各位置のXは個別かつ独立に任意のアミノ酸である)を含む単離された組換えポリペプチドまたはその変異体を検討する。特定の実施形態では、変異体は、1つ、2つ、もしくは3つのアミノ酸の置換、欠失または挿入を有し、但しアミノ酸の置換、欠失または挿入はXアミノ酸でない。特定の実施形態では、置換は保存的置換である。
ヒト化された特異的結合剤は、タンパク質ディスプレイ技術、例えばファージディスプレイ、酵母表面ディスプレイ、細菌ディスプレイ、または無細胞系を用いて、変異タンパク質のコンビナトリアルライブラリーから単離してもよい。Finlay et al.,Methods Mol.Biol.,2011,681:87−101;Daugherty,Curr.Opin.Struct.Biol.,2007,17:474−480;Gai&Wittrup,Curr.Opin.Struct.Biol.,2007,17:467−473;Zhou et al.,MAbs.,2010,2:508−518;Shen et al.,Proc.Nat.Acad.Sci.USA,2005,102:5969−5974を参照のこと。典型的には、固有の変異タンパク質の集団が、対応する突然変異核酸からの発現により、ディスプレイプラットフォームを介して連結される。ディスプレイプラットフォーム上で発現される変異タンパク質を標的分子に曝露するかまたは標的分子と混合してから、分子と結合された変異体は、分析用に同定および/または分離される。典型的には、タンパク質配列は、ディスプレイプラットフォーム内の関連核酸を配列決定することにより決定される。例えば、酵母表面ディスプレイでは、組換え酵母細胞が変異タンパク質を発現し、ここで酵母細胞は細胞壁タンパク質に抱合された変異タンパク質を発現する。酵母細胞は、酵母細胞の表面上に発現される変異タンパク質をコードするプラスミドDNAを有することができ、プラスミドDNAの配列決定することにより、変異タンパク質のタンパク質配列が提供される。Gera et al.,Protein selection using yeast surface display,Methods,2013,60(1):15−26を参照のこと。ファージディスプレイでは、変異タンパク質が典型的にはバクテリオファージコートタンパク質に抱合される。細胞に基づく系はまた、典型的には、例えば、細菌,酵母、および哺乳類細胞における細胞表面タンパク質に抱合された変異タンパク質の発現に依存し、宿主細胞は変異タンパク質をコードするプラスミドベクターを保有する。無細胞系もまた開発されており、変異タンパク質は、リボソームディスプレイまたはmRNAディスプレイと称されるそのコードmRNAに直接的に抱合される。
a)標的分子に特異的に結合するヤツメウナギ抗体配列を提供するステップ;
b)1)比較ウインドウにわたり、ヤツメウナギ抗体配列をヒトロイシンリッチリピート配列と比較し、重複アミノ酸位置、保存的置換を有する非重複アミノ酸位置、および非保存的置換を有する非重複アミノ酸位置を同定するステップと;
2)重複アミノ酸位置をそれら各々の位置におけるアミノ酸として割り当てるステップと;
3)ヒトリッチリピート配列のアミノ酸を、それら各々の位置における保存的置換を有する非重複アミノ酸位置に割り当てるステップと;
4)ヒトロイシンリッチリピート配列またはヤツメウナギのアミノ酸配列でのアミノ酸間にランダム選択を割り当て、それら各々の位置に変異ロイシンリッチリピート配列のライブラリーを提供するステップと;
を含む方法によって作成される、ロイシンリッチリピート配列のライブラリーを同定するステップ;
b)各々の位置に割り当てられたアミノ酸を有する変異ロイシンリッチリピート配列のディスプレイライブラリーを調製し、標的分子と混合して結合するステップ;
c)標的分子に結合する変異ロイシンリッチリピート配列の1つ以上を同定し、ヒト化された特異的結合剤を提供するステップ;
d)ヒト化された特異的結合剤をコードする組換えベクターを含む発現系においてヒト化された特異的結合剤を発現させるステップ
のうちの1つ以上を含む、方法を検討する。
特定の実施形態では、本開示は、任意選択的に、ヒト免疫系のエフェクター機能にとって十分なFc受容体および補体によって認識されるヒト抗体定常領域に抱合された、本明細書に開示されるようなヒト化アミノ酸配列を含むように修飾された可変性リンパ球受容体に関する。特定の実施形態では、本開示は、エフェクター機能を提供する、例えば、インビボまたはインビトロでの抗体依存細胞傷害性、また任意選択的には野生型ヒト抗体に匹敵する半減期を誘発することが可能な、本明細書に開示される修飾ヒトアミノ酸配列とFc配列またはその断片を含む融合タンパク質に関する。治療抗体では、典型的にはインタクトなIgG分子を用いている。IgG1 Fcは、エフェクター機能を引き起こすFcγ受容体と相互作用することができる。Fcは補体アクチベーターC1qに対する結合部位を有する。新生児Fc受容体(FcRn)における結合部位は半減期に効果を及ぼす。
または断片もしくは変異体の中に存在し、例えば、1、2、もしくは3つのアミノ酸の欠失、付加、または置換変異体、あるいはそれに対して50%超、60%超、70%超、80%超、90%超、95%超またはそれより大きい同一性を有する配列を有する。
その断片もしくは変異体の変異体、あるいはそれに対して50%超、60%超、70%超、80%超、90%超、95%超またはそれより大きい同一性を有する配列を有する、免疫受容体チロシンに基づく活性化モチーフ(下線)を有するペプチドである。
B細胞は、典型的にはB細胞を未熟および成熟形質細胞などのより特殊化した細胞に分化するように刺激するT細胞に抗原を提示する。形質細胞は大量の抗体を産生する。多発性骨髄腫は、形質細胞内で形成するがんである。B細胞悪性腫瘍は、正常および悪性B細胞の枯渇をもたらす、CD20表面抗原に特異的な治療抗体によって効果的に治療される。B細胞リンパ腫および白血病の治療が奏効するにもかかわらず、成熟B細胞が形質細胞に分化するときCD20表面発現が失われることから、抗CD20抗体は多発性骨髄腫を治療する場合に有効でない。多発性骨髄腫形質細胞を標的化するために現在研究中の他の形質細胞表面抗原もまた、多数の他の細胞型および組織によって発現されるが、形質細胞の標的化は許容できない副作用の可能性があるために複雑である。現在、モノクローナル抗体に基づく治療として、多発性骨髄腫を有する患者に対して利用可能なものはない。化学療法剤および自家造血幹細胞移植による治療は、全生存を延長するものの、被験者を治癒しない場合がある。したがって、改善された治療方法を同定する必要がある。
固有の結合特異性を有するモノクローナルVLR抗体
大きい進化的距離を組み合わせた基本的に異なるタンパク質構造は、VLR抗体が、構造的または免疫寛容原性的な理由(すなわち、「自己」を認識し、ひいては自己免疫性合併症を引き起こす抗体の産生を宿主が阻止する必要性)で従来の抗体により検出できない抗原を検出し得ることを示唆する。ヤツメウナギの進化的距離および根本的に異なるVLR抗体のタンパク質構造により、VLR抗体は、構造的または免疫寛容原性的な理由で従来の抗体を用いて検出できないバイオマーカーの発見にとって理想的な試薬になる。VLR抗体MM3の結合特性は、任意の既知の細胞表面抗原に対応しないことから、VLR抗体の固有の抗原認識特性が支持される。特定のヒト造血細胞集団に結合するモノクローナルヤツメウナギVLR抗体は同定されている。これらVLR抗体のいくつかに対する結合特異性の分析によると、対象として従来の哺乳動物モノクローナル抗体が全く産生されていないような抗原構造をVLR抗体が認識することが示される。
Hanらは、我々のヤツメウナギVLR2913結晶構造を用いて、1.67Åの解像度での分子置換によりヒト血液型O赤血球のH抗原由来のH−三糖と複合体を形成したVLR RBC36外部ドメイン(ECD)の結晶構造を報告している(2008,Science 321:1834−183)。II型H抗原三糖は、α−l−Fucp−(1→2)−β−d−Galp−(1→4)−β−d−GlcNacp−OHである。
Slit−M4では、214中195のアミノ酸位置はヒトである(91%)。
を含む(式中、太字はαヘリックス、[X]mは任意選択的にX1、X1X2、X1X2X3、X1X2X3X4である(式中X1はH、X2はT、X3はN、X4はP、X5はRまたはKである))。
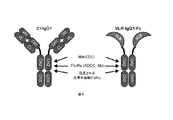
多数の治療抗体によるインビボでの腫瘍細胞の排除は、抗体の定常領域(Fc)によって媒介される。ヒトIgG1の定常領域は、CH2ドメインを介して補体およびFcγ受容体(FcγR)に結合し、補体依存性細胞傷害性(CDC)、抗体依存細胞傷害性(ADCC)、およびFcγR担持マクロファージによる抗体オプソニン化細胞の食細胞による貪食を介して標的細胞の死滅を促進する。VLRの抗原結合ドメインおよびヒト抗体、例えばIgG1の定常領域からなる融合タンパク質は、VLR抗体の固有の抗原検出をヒトの免疫クリアランス機構と共役させることになる。ヒトIgG抗体の定常領域はまた、ヒト血漿中の抗体の半減期を延長する。FcRnが、IgG定常領域のCH2およびCH3ドメインに結合し、エンドサイトーシス区画からの抗体のリサイクルを促進することで、循環中のその存在が延長され、治療薬としてのその有効性が増強される。
またはその断片もしくは変異体(例えば、1つ、2つ、もしくは3つのアミノ酸の欠失、付加、または置換変異体を有する)、またはそれに対して50%超、60%超、70%超、80%超、90%超、95%超もしくはそれより大きい同一性を有する配列の中に存在する。
その断片もしくは変異体の変異体、またはそれに対して50%超、60%超、70%超、80%超、90%超、95%超もしくはそれより大きい同一性を有する配列を有する免疫受容体チロシンに基づく活性化モチーフ(下線)を有するペプチドである。
Slit2−D2突然変異体は、IgG1−Fcを有するレンチウイルス発現ベクターにクローン化し、一過性トランスフェクションによりHEK−293T細胞内で発現させた。Slit2−D2突然変異体の発現は、上清を抗−IgG−HRP結合二次抗体を用いてウエスタンブロットすることにより確認した。上清は、CHO−H細胞株を染色するために用いて、結合性を、抗−IgG−PE結合二次抗体を用いてフローサイトメトリーにより検出した。正の対照として、CHO−H細胞をまた、野生型RBC36−IgG−Fc融合タンパク質で染色した。Slit−M4−IgG−Fcタンパク質で染色したCHO−H細胞の場合、H−三糖の特異性をSlit2−D2スキャフォールドに移せることが示された(図6)。
形質細胞に特異的なVLR mAb(MM3)を、ヤツメウナギをヒト多発性骨髄腫細胞で免疫することにより作製した。ヒト形質細胞抗原に対するマウス抗体は予め作成しているが、形質細胞に特異的なものはない。MM3 VLR mAbは、正常(25中25のドナー試験試料)および悪性ヒト形質細胞(32中27の骨髄腫患者)の双方に結合するが、他のB細胞または造血系細胞に結合しない(図9)。MM3はまた、非ヒト霊長類(アカゲザルおよびスーティーマンガベイ)における形質細胞を認識するが、マウス形質細胞に結合しない。アカゲザル骨髄由来のMM3+細胞が形質細胞であったことを確認するため、MM3+細胞をフローサイトメトリーにより選別し、透過型電子顕微鏡により分析した。MM3+細胞は、形質細胞に特有の特徴である、小さくて密な偏心性の核および大きい細胞質量を有し、大幅に拡大した粗面小胞体およびゴルジを伴っていた。非ヒト霊長類における形質細胞上でのMM3抗原の保存により、VLR抗体がインビボで形質細胞を標的化し、枯渇させる能力の評価用のモデル系が提供される。CD19およびCD138の発現に基づき、健常ヒトドナー由来のヒト骨髄由来形質細胞サブセット上でのMM3の発現を分析するため、多重パラメータフローサイトメトリーを用いた(図10)。MM3 VLR mAbで長寿命形質細胞集団(CD19−、CD27+、CD138+、CD38hi)を含む、4つすべてのCD38hi形質細胞サブセットを染色した。それでまた、最も広範に用いられる形質細胞マーカーであるCD138を発現しないヒト骨髄における抗体分泌細胞の亜集団を染色した。
シグナルペプチドおよびストーク(下線)を含むMM3完全配列(配列番号57)
特定の実施形態では、本開示は、
(配列番号64)
またはその変異体;
(配列番号74)
またはその変異体;
(配列番号75)
またはその変異体;
(配列番号76)
またはその変異体;または
(配列番号77)
またはその変異体、を含むSlit2−MM3ポリペプチドを検討する。
Claims (21)
- 分子に特異的に結合する単離された修飾ヒトアミノ酸配列において、
分子に結合する無顎類の可変性リンパ球受容体(VLR)のアミノ酸配列を提供するステップと;
前記可変性リンパ球受容体中のどのアミノ酸が、前記結合分子に空間的に最も近い状態であるか、および/または前記結合分子に対してイオン相互作用をもたらすか、および/または水素結合するか、および/またはファンデルワールス力をもたらすかを評価し、前記可変性リンパ球受容体における標的アミノ酸を提供するステップと;
前記可変性リンパ球受容体(VLR)アミノ酸配列に対して20%超もしくはそれより大きい配列同一性を有する既知のヒトアミノ酸配列を提供するステップと;
前記分子に特異的に結合するように形成された修飾ヒトアミノ酸配列を提供するため、前記可変性リンパ球受容体中の前記標的アミノ酸および前記標的アミノ酸を囲む十分な数のアミノ酸を前記既知のヒトアミノ酸配列内部で置換するステップと;
組換え核酸から前記修飾ヒトアミノ酸配列を発現させるステップと、
を含む方法によって作成されることを特徴とする、分子に特異的に結合する単離された修飾ヒトアミノ酸配列。 - 請求項1に記載の単離された修飾ヒトアミノ酸配列において、前記可変性リンパ球受容体がヤツメウナギ可変性リンパ球受容体B(VLRB)であることを特徴とする、単離された修飾ヒトアミノ酸配列。
- 請求項1に記載の単離された修飾ヒトアミノ酸配列において、前記既知のヒトアミノ酸配列がヒトロイシンリッチリピート受容体であることを特徴とする、単離された修飾ヒトアミノ酸配列。
- 請求項1に記載の単離された修飾ヒトアミノ酸配列において、前記既知のヒトアミノ酸配列が、Slitファミリータンパク質(Slit1、2、および3)、CD42b、またはNogo−66であることを特徴とする、単離された修飾ヒトアミノ酸配列。
- 請求項1に記載の単離された修飾ヒトアミノ酸配列において、前記分子がウイルスまたは微生物抗原であることを特徴とする、単離された修飾ヒトアミノ酸配列。
- 請求項5に記載の単離された修飾ヒトアミノ酸配列において、前記ウイルスまたは微生物抗原が、炭疽菌(Bacillus anthracis)、インフルエンザ(Influenza)、またはHIV−1抗原であることを特徴とする、単離された修飾ヒトアミノ酸配列。
- 請求項1に記載の単離された修飾ヒトアミノ酸配列において、前記分子が腫瘍関連抗原であることを特徴とする、単離された修飾ヒトアミノ酸配列。
- 請求項1に記載の単離された修飾ヒトアミノ酸配列において、前記分子が、特に正常または悪性ヒト細胞に関連することを特徴とする、単離された修飾ヒトアミノ酸配列。
- 請求項8に記載の単離された修飾ヒトアミノ酸配列において、前記正常または悪性ヒト細胞が、血液型O赤血球、B細胞白血病細胞、またはBリンパ腫細胞株であることを特徴とする、単離された修飾ヒトアミノ酸配列。
- 請求項1に記載の単離された修飾ヒトアミノ酸配列を含む組換えベクター。
- 請求項12に記載のベクターを含む発現系。
- 請求項1に記載の修飾ヒトアミノ酸配列およびFc配列を含む融合タンパク質。
- 請求項13に記載の融合タンパク質を含む組換えベクター。
- 請求項14に記載のベクターを含む発現系。
- 請求項16に記載の組換えポリペプチドにおいて、ヒトFc配列をさらに含むことを特徴とする、組換えポリペプチド。
- 請求項16に記載の組換えポリペプチドにおいて、配列
YLDLNNNKLQTIAKGTFGTFSPLRAIQHMWLY(配列番号66)、
YLDLNNNKLQTIAKGTFGTFSPLRAIQHMWLYQ(配列番号67)、または
YLDLNNNKLQTIAKGTFGTFSPLRAIQHMWLYG(配列番号68)
を有することを特徴とする、組換えポリペプチド。 - 請求項16に記載の組換えポリペプチドにおいて、B細胞ではなく、形質細胞に特異的に結合する能力があることを特徴とする、組換えポリペプチド。
- 配列番号56を含む組換えポリペプチド、その変異体。
- 請求項20に記載の組換えポリペプチドをコードする核酸を含む組換えベクター。
- 請求項21に記載のベクターを含む発現系。
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US201461987566P | 2014-05-02 | 2014-05-02 | |
| US61/987,566 | 2014-05-02 | ||
| PCT/US2015/028645 WO2015168469A1 (en) | 2014-05-02 | 2015-04-30 | Humanized variable lymphocyte receptors (vlr) and compositions and uses related thereto |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2017514522A true JP2017514522A (ja) | 2017-06-08 |
| JP2017514522A5 JP2017514522A5 (ja) | 2018-06-14 |
Family
ID=54359347
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2017510445A Pending JP2017514522A (ja) | 2014-05-02 | 2015-04-30 | ヒト化可変性リンパ球受容体(vlr)および組成物ならびにそれに関連する使用 |
Country Status (8)
| Country | Link |
|---|---|
| US (3) | US10167330B2 (ja) |
| EP (1) | EP3137496A4 (ja) |
| JP (1) | JP2017514522A (ja) |
| KR (1) | KR20160147787A (ja) |
| CN (1) | CN106459173A (ja) |
| CA (1) | CA2947429A1 (ja) |
| IL (1) | IL248327A0 (ja) |
| WO (1) | WO2015168469A1 (ja) |
Families Citing this family (11)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CA2947429A1 (en) | 2014-05-02 | 2015-11-05 | Emory University | Humanized variable lymphocyte receptors (vlr) and compositions and uses related thereto |
| SE1500434A1 (en) * | 2015-10-29 | 2017-04-30 | Theravac Pharmaceuticals Ab | A novel fusion partner for highly efficient and safe vaccines |
| CN107365387B (zh) | 2016-05-12 | 2022-03-15 | 阿思科力(苏州)生物科技有限公司 | 一种双特异性抗原结合构建体及其制备方法和应用 |
| US11339225B2 (en) * | 2016-05-12 | 2022-05-24 | Asclepius (Suzhou) Technology Company Group, Co., Ltd. | Bispecific antigen-binding construct and preparation method and use thereof |
| CN106543278B (zh) * | 2016-12-06 | 2019-04-12 | 阿思科力(苏州)生物科技有限公司 | 融合蛋白Slit2D2(C386S)-HSA及其在治疗纤维化疾病中的应用 |
| WO2018140857A2 (en) * | 2017-01-27 | 2018-08-02 | Board Of Supervisors Of Louisiana State University And Agricultural And Mechanical College | Bifunctional small peptide for autoimmune diabetes |
| EP3600378A4 (en) * | 2017-03-24 | 2020-12-23 | Orpheus Bioscience Inc. | PANTIDS FOR THE TREATMENT OF AUTOIMMUNE DISORDERS |
| JP7164544B2 (ja) * | 2017-04-11 | 2022-11-01 | インヒブルクス インコーポレイテッド | 制約されたcd3結合を有する多重特異性ポリペプチド構築物およびそれを使用する方法 |
| KR101972894B1 (ko) * | 2017-05-18 | 2019-04-29 | 경상대학교산학협력단 | 소수성 테일 도메인이 제거된 먹장어 유래 vlrb 단백질에 칠성장어 유래 vlrb 단백질의 c 말단 서열이 연결된 융합 단백질 및 이의 용도 |
| US20220041659A1 (en) * | 2018-12-21 | 2022-02-10 | Wisconsin Alumni Research Foundation | Variable lymphocyte receptors that target the brain extracellular matrix and methods of use |
| WO2023010060A2 (en) * | 2021-07-27 | 2023-02-02 | Novab, Inc. | Engineered vlrb antibodies with immune effector functions |
Citations (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2008500064A (ja) * | 2004-05-21 | 2008-01-10 | ザ ユーエービー リサーチ ファウンデーション | 可変性リンパ球受容体、その関連ポリペプチドおよび核酸、ならびにその使用 |
Family Cites Families (8)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPH1118777A (ja) | 1997-07-09 | 1999-01-26 | Asahi Chem Ind Co Ltd | 新規スリット様ポリペプチド |
| WO2008016854A2 (en) | 2006-08-02 | 2008-02-07 | The Uab Research Foundation | Methods and compositions related to soluble monoclonal variable lymphocyte receptors of defined antigen specificity |
| WO2010065407A2 (en) | 2008-12-01 | 2010-06-10 | University Of Maryland Biotechnology Institute | High affinity recombinant sea lamprey antibodies selected by a yeast surface display platform |
| SG10201510092QA (en) | 2010-12-09 | 2016-01-28 | Univ Pennsylvania | Use of chimeric antigen receptor-modified t cells to treat cancer |
| WO2013078425A1 (en) | 2011-11-22 | 2013-05-30 | University Of Maryland, Baltimore | Lambodies with high affinity and selectivity for glycans and uses therefor |
| CN103033617B (zh) * | 2012-11-30 | 2014-12-03 | 辽宁师范大学 | 基于可变淋巴细胞受体的肿瘤标志物检测试剂盒及其制备方法 |
| UY35468A (es) | 2013-03-16 | 2014-10-31 | Novartis Ag | Tratamiento de cáncer utilizando un receptor quimérico de antígeno anti-cd19 |
| CA2947429A1 (en) | 2014-05-02 | 2015-11-05 | Emory University | Humanized variable lymphocyte receptors (vlr) and compositions and uses related thereto |
-
2015
- 2015-04-30 CA CA2947429A patent/CA2947429A1/en not_active Abandoned
- 2015-04-30 US US15/308,535 patent/US10167330B2/en active Active
- 2015-04-30 KR KR1020167030600A patent/KR20160147787A/ko not_active Application Discontinuation
- 2015-04-30 JP JP2017510445A patent/JP2017514522A/ja active Pending
- 2015-04-30 EP EP15786773.0A patent/EP3137496A4/en not_active Withdrawn
- 2015-04-30 WO PCT/US2015/028645 patent/WO2015168469A1/en active Application Filing
- 2015-04-30 CN CN201580021759.0A patent/CN106459173A/zh active Pending
-
2016
- 2016-10-13 IL IL248327A patent/IL248327A0/en unknown
-
2018
- 2018-11-07 US US16/183,340 patent/US20190202887A1/en not_active Abandoned
-
2020
- 2020-04-23 US US16/857,130 patent/US11384134B2/en active Active
Patent Citations (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2008500064A (ja) * | 2004-05-21 | 2008-01-10 | ザ ユーエービー リサーチ ファウンデーション | 可変性リンパ球受容体、その関連ポリペプチドおよび核酸、ならびにその使用 |
Non-Patent Citations (3)
| Title |
|---|
| DRUG DESIGN REVIEWS ONLINE, 2005, VOL.2, P.305-322, JPN6019008815 * |
| PNAS, 2012, VOL.109, P.3299-3304, JPN6019008817 * |
| SCIENCE, 2008, VOL.321, P.1834-1837, JPN6019008810 * |
Also Published As
| Publication number | Publication date |
|---|---|
| US10167330B2 (en) | 2019-01-01 |
| US20190202887A1 (en) | 2019-07-04 |
| CA2947429A1 (en) | 2015-11-05 |
| WO2015168469A1 (en) | 2015-11-05 |
| EP3137496A1 (en) | 2017-03-08 |
| EP3137496A4 (en) | 2017-10-11 |
| US20200308247A1 (en) | 2020-10-01 |
| CN106459173A (zh) | 2017-02-22 |
| US20170081385A1 (en) | 2017-03-23 |
| KR20160147787A (ko) | 2016-12-23 |
| IL248327A0 (en) | 2016-11-30 |
| US11384134B2 (en) | 2022-07-12 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| US11384134B2 (en) | Recombinant vector and expression system comprising a nucleic acid encoding a variable lymphocyte receptor (VLR) | |
| US11136369B2 (en) | Expression of chimeric polypeptide with variable lymphocyte receptors on immune cells and uses for treating cancer | |
| CN108884136A (zh) | 用于癌症免疫治疗的转染t细胞和t细胞受体 | |
| CN110857322A (zh) | 抗人claudin 18.2单克隆抗体及其应用 | |
| AU2015313268B2 (en) | Cancer-cell-specific antibody, anticancer agent, and cancer testing method | |
| WO2014058389A1 (en) | Optimised heavy chain and light chain signal peptides for the production of recombinant antibody therapeutics | |
| EP3165535A1 (en) | Screening and engineering method of super-stable immunoglobulin variable domains and their uses | |
| JP7264381B2 (ja) | 血中半減期の向上のための抗体Fc変異体 | |
| US20210163923A1 (en) | Selecting for developability of polypeptide drugs in eukaryotic cell display systems | |
| JP2019193652A (ja) | 前立腺特異幹細胞抗原に対する抗体およびその使用 | |
| CN111247429A (zh) | 用于新颖抗原结合模块的特异性测试的通用报告细胞测定法 | |
| JP2021514648A (ja) | 新規の標的抗原結合部分のための特異性アッセイ | |
| JP2021508246A (ja) | 新規抗原結合部分の特異性試験のためのcar−t細胞アッセイ | |
| CN117616053A (zh) | 一种三特异性抗体的设计、制备及用途 | |
| US20220348654A1 (en) | AGLYCOSYLATED ANTIBODY Fc REGION FOR TREATING CANCER | |
| EP3775902A1 (en) | Diagnostic assays to detect tumor antigens in cancer patients | |
| US20240124575A1 (en) | Human cd33 antibody and use thereof | |
| CN117279937A (zh) | Epcam结合分子及其用途 | |
| CN116888154A (zh) | Cea6结合分子及其用途 | |
| CN116829161A (zh) | 嵌合抗原受体t细胞及方法 | |
| CN116916956A (zh) | Fap结合分子及其用途 | |
| CN110461878A (zh) | 用于在癌症疗法中靶向坏死的人源化抗核抗体 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20180427 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20180427 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20190319 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20190619 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20190808 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20191001 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20191204 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20200401 |
|
| A02 | Decision of refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A02 Effective date: 20200526 |