JP2017501976A - コバルト触媒並びにヒドロシリル化及び脱水素シリル化のためのその使用 - Google Patents
コバルト触媒並びにヒドロシリル化及び脱水素シリル化のためのその使用 Download PDFInfo
- Publication number
- JP2017501976A JP2017501976A JP2016532098A JP2016532098A JP2017501976A JP 2017501976 A JP2017501976 A JP 2017501976A JP 2016532098 A JP2016532098 A JP 2016532098A JP 2016532098 A JP2016532098 A JP 2016532098A JP 2017501976 A JP2017501976 A JP 2017501976A
- Authority
- JP
- Japan
- Prior art keywords
- unsaturated
- group
- alkyl
- complex
- substituted
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Granted
Links
- 239000003054 catalyst Substances 0.000 title claims abstract description 66
- 238000006459 hydrosilylation reaction Methods 0.000 title claims abstract description 58
- 238000006884 silylation reaction Methods 0.000 title claims abstract description 42
- 238000006356 dehydrogenation reaction Methods 0.000 title abstract description 22
- 229910017052 cobalt Inorganic materials 0.000 title description 9
- 239000010941 cobalt Substances 0.000 title description 9
- GUTLYIVDDKVIGB-UHFFFAOYSA-N cobalt atom Chemical compound [Co] GUTLYIVDDKVIGB-UHFFFAOYSA-N 0.000 title description 8
- 238000000034 method Methods 0.000 claims description 62
- 230000008569 process Effects 0.000 claims description 54
- BLRPTPMANUNPDV-UHFFFAOYSA-N Silane Chemical compound [SiH4] BLRPTPMANUNPDV-UHFFFAOYSA-N 0.000 claims description 38
- 229910052739 hydrogen Inorganic materials 0.000 claims description 35
- 239000000203 mixture Substances 0.000 claims description 35
- 150000001875 compounds Chemical class 0.000 claims description 34
- 239000001257 hydrogen Substances 0.000 claims description 33
- 238000006243 chemical reaction Methods 0.000 claims description 31
- 125000003118 aryl group Chemical group 0.000 claims description 30
- 125000003107 substituted aryl group Chemical group 0.000 claims description 25
- -1 polyethylene Polymers 0.000 claims description 24
- 150000001336 alkenes Chemical class 0.000 claims description 21
- 150000002431 hydrogen Chemical class 0.000 claims description 21
- 125000005842 heteroatom Chemical group 0.000 claims description 20
- 125000000547 substituted alkyl group Chemical group 0.000 claims description 19
- 229920002554 vinyl polymer Polymers 0.000 claims description 19
- 229920001296 polysiloxane Polymers 0.000 claims description 18
- 125000000391 vinyl group Chemical group [H]C([*])=C([H])[H] 0.000 claims description 18
- 125000006702 (C1-C18) alkyl group Chemical group 0.000 claims description 17
- 239000002904 solvent Substances 0.000 claims description 16
- 125000000524 functional group Chemical group 0.000 claims description 15
- 125000003903 2-propenyl group Chemical group [H]C([*])([H])C([H])=C([H])[H] 0.000 claims description 14
- HEDRZPFGACZZDS-UHFFFAOYSA-N Chloroform Chemical compound ClC(Cl)Cl HEDRZPFGACZZDS-UHFFFAOYSA-N 0.000 claims description 14
- 125000001997 phenyl group Chemical group [H]C1=C([H])C([H])=C(*)C([H])=C1[H] 0.000 claims description 14
- 125000001424 substituent group Chemical group 0.000 claims description 14
- XEEYBQQBJWHFJM-UHFFFAOYSA-N Iron Chemical compound [Fe] XEEYBQQBJWHFJM-UHFFFAOYSA-N 0.000 claims description 13
- VYPSYNLAJGMNEJ-UHFFFAOYSA-N Silicium dioxide Chemical compound O=[Si]=O VYPSYNLAJGMNEJ-UHFFFAOYSA-N 0.000 claims description 13
- 125000002496 methyl group Chemical group [H]C([H])([H])* 0.000 claims description 13
- 229920000570 polyether Polymers 0.000 claims description 13
- UFHFLCQGNIYNRP-UHFFFAOYSA-N Hydrogen Chemical compound [H][H] UFHFLCQGNIYNRP-UHFFFAOYSA-N 0.000 claims description 12
- 125000000217 alkyl group Chemical group 0.000 claims description 11
- JRZJOMJEPLMPRA-UHFFFAOYSA-N olefin Natural products CCCCCCCC=C JRZJOMJEPLMPRA-UHFFFAOYSA-N 0.000 claims description 11
- 239000000758 substrate Substances 0.000 claims description 10
- 239000004721 Polyphenylene oxide Substances 0.000 claims description 9
- 125000000753 cycloalkyl group Chemical group 0.000 claims description 9
- 229920000642 polymer Polymers 0.000 claims description 9
- 239000000376 reactant Substances 0.000 claims description 9
- 125000002877 alkyl aryl group Chemical group 0.000 claims description 8
- 239000012530 fluid Substances 0.000 claims description 8
- 125000001183 hydrocarbyl group Chemical group 0.000 claims description 8
- 229920006395 saturated elastomer Polymers 0.000 claims description 8
- 125000001931 aliphatic group Chemical group 0.000 claims description 7
- 125000003342 alkenyl group Chemical group 0.000 claims description 7
- 125000003710 aryl alkyl group Chemical group 0.000 claims description 7
- 229910052799 carbon Inorganic materials 0.000 claims description 7
- 229910000077 silane Inorganic materials 0.000 claims description 7
- 125000003808 silyl group Chemical group [H][Si]([H])([H])[*] 0.000 claims description 7
- 125000005346 substituted cycloalkyl group Chemical group 0.000 claims description 7
- MCMNRKCIXSYSNV-UHFFFAOYSA-N Zirconium dioxide Chemical compound O=[Zr]=O MCMNRKCIXSYSNV-UHFFFAOYSA-N 0.000 claims description 6
- 239000012298 atmosphere Substances 0.000 claims description 6
- 150000004756 silanes Chemical class 0.000 claims description 6
- 229910052710 silicon Inorganic materials 0.000 claims description 6
- 239000010703 silicon Substances 0.000 claims description 6
- 125000005915 C6-C14 aryl group Chemical group 0.000 claims description 5
- OKTJSMMVPCPJKN-UHFFFAOYSA-N Carbon Chemical compound [C] OKTJSMMVPCPJKN-UHFFFAOYSA-N 0.000 claims description 5
- 150000001252 acrylic acid derivatives Chemical group 0.000 claims description 5
- 150000001345 alkine derivatives Chemical class 0.000 claims description 5
- 150000001412 amines Chemical class 0.000 claims description 5
- 150000004945 aromatic hydrocarbons Chemical class 0.000 claims description 5
- KPUWHANPEXNPJT-UHFFFAOYSA-N disiloxane Chemical class [SiH3]O[SiH3] KPUWHANPEXNPJT-UHFFFAOYSA-N 0.000 claims description 5
- 150000004678 hydrides Chemical class 0.000 claims description 5
- 241000257303 Hymenoptera Species 0.000 claims description 4
- 239000004793 Polystyrene Substances 0.000 claims description 4
- 150000008378 aryl ethers Chemical class 0.000 claims description 4
- 125000005394 methallyl group Chemical group 0.000 claims description 4
- 229920002223 polystyrene Polymers 0.000 claims description 4
- 235000021122 unsaturated fatty acids Nutrition 0.000 claims description 4
- UWRZIZXBOLBCON-UHFFFAOYSA-N 2-phenylethenamine Chemical compound NC=CC1=CC=CC=C1 UWRZIZXBOLBCON-UHFFFAOYSA-N 0.000 claims description 3
- BAPJBEWLBFYGME-UHFFFAOYSA-N Methyl acrylate Chemical group COC(=O)C=C BAPJBEWLBFYGME-UHFFFAOYSA-N 0.000 claims description 3
- 239000004698 Polyethylene Substances 0.000 claims description 3
- 239000004743 Polypropylene Substances 0.000 claims description 3
- 229910004298 SiO 2 Inorganic materials 0.000 claims description 3
- 229910004283 SiO 4 Inorganic materials 0.000 claims description 3
- 125000004423 acyloxy group Chemical group 0.000 claims description 3
- 125000003545 alkoxy group Chemical group 0.000 claims description 3
- PNEYBMLMFCGWSK-UHFFFAOYSA-N aluminium oxide Inorganic materials [O-2].[O-2].[O-2].[Al+3].[Al+3] PNEYBMLMFCGWSK-UHFFFAOYSA-N 0.000 claims description 3
- 150000001924 cycloalkanes Chemical class 0.000 claims description 3
- 150000002118 epoxides Chemical class 0.000 claims description 3
- 150000002170 ethers Chemical class 0.000 claims description 3
- 229910052736 halogen Inorganic materials 0.000 claims description 3
- 229920000573 polyethylene Polymers 0.000 claims description 3
- 229920001155 polypropylene Polymers 0.000 claims description 3
- 230000000717 retained effect Effects 0.000 claims description 3
- 239000000377 silicon dioxide Substances 0.000 claims description 3
- 150000004670 unsaturated fatty acids Chemical class 0.000 claims description 3
- 150000001925 cycloalkenes Chemical class 0.000 claims description 2
- 150000002148 esters Chemical class 0.000 claims description 2
- 150000008282 halocarbons Chemical class 0.000 claims description 2
- 125000005843 halogen group Chemical group 0.000 claims description 2
- 229930195733 hydrocarbon Natural products 0.000 claims description 2
- 150000002430 hydrocarbons Chemical class 0.000 claims description 2
- 229920001467 poly(styrenesulfonates) Polymers 0.000 claims description 2
- ABJSOROVZZKJGI-OCYUSGCXSA-N (1r,2r,4r)-2-(4-bromophenyl)-n-[(4-chlorophenyl)-(2-fluoropyridin-4-yl)methyl]-4-morpholin-4-ylcyclohexane-1-carboxamide Chemical compound C1=NC(F)=CC(C(NC(=O)[C@H]2[C@@H](C[C@@H](CC2)N2CCOCC2)C=2C=CC(Br)=CC=2)C=2C=CC(Cl)=CC=2)=C1 ABJSOROVZZKJGI-OCYUSGCXSA-N 0.000 claims 1
- CERQOIWHTDAKMF-UHFFFAOYSA-M Methacrylate Chemical group CC(=C)C([O-])=O CERQOIWHTDAKMF-UHFFFAOYSA-M 0.000 claims 1
- 239000003446 ligand Substances 0.000 abstract description 16
- 150000004700 cobalt complex Chemical class 0.000 abstract description 13
- 150000001868 cobalt Chemical class 0.000 abstract description 8
- JFJNVIPVOCESGZ-UHFFFAOYSA-N 2,3-dipyridin-2-ylpyridine Chemical compound N1=CC=CC=C1C1=CC=CN=C1C1=CC=CC=N1 JFJNVIPVOCESGZ-UHFFFAOYSA-N 0.000 abstract description 7
- 125000001181 organosilyl group Chemical group [SiH3]* 0.000 abstract description 5
- 238000004132 cross linking Methods 0.000 abstract description 3
- 239000000047 product Substances 0.000 description 52
- KWKAKUADMBZCLK-UHFFFAOYSA-N 1-octene Chemical compound CCCCCCC=C KWKAKUADMBZCLK-UHFFFAOYSA-N 0.000 description 20
- DRGAZIDRYFYHIJ-UHFFFAOYSA-N 2,2':6',2''-terpyridine Chemical compound N1=CC=CC=C1C1=CC=CC(C=2N=CC=CC=2)=N1 DRGAZIDRYFYHIJ-UHFFFAOYSA-N 0.000 description 17
- YXFVVABEGXRONW-UHFFFAOYSA-N Toluene Chemical compound CC1=CC=CC=C1 YXFVVABEGXRONW-UHFFFAOYSA-N 0.000 description 15
- 230000015572 biosynthetic process Effects 0.000 description 13
- OFBQJSOFQDEBGM-UHFFFAOYSA-N Pentane Chemical compound CCCCC OFBQJSOFQDEBGM-UHFFFAOYSA-N 0.000 description 12
- TVMXDCGIABBOFY-UHFFFAOYSA-N n-Octanol Natural products CCCCCCCC TVMXDCGIABBOFY-UHFFFAOYSA-N 0.000 description 11
- 239000011541 reaction mixture Substances 0.000 description 10
- 238000003786 synthesis reaction Methods 0.000 description 10
- 150000004696 coordination complex Chemical class 0.000 description 9
- 229910052751 metal Inorganic materials 0.000 description 8
- 239000002184 metal Substances 0.000 description 8
- 238000003756 stirring Methods 0.000 description 8
- QQQSFSZALRVCSZ-UHFFFAOYSA-N triethoxysilane Chemical compound CCO[SiH](OCC)OCC QQQSFSZALRVCSZ-UHFFFAOYSA-N 0.000 description 8
- 238000005481 NMR spectroscopy Methods 0.000 description 7
- IJGRMHOSHXDMSA-UHFFFAOYSA-N Atomic nitrogen Chemical compound N#N IJGRMHOSHXDMSA-UHFFFAOYSA-N 0.000 description 6
- ZMANZCXQSJIPKH-UHFFFAOYSA-N Triethylamine Chemical compound CCN(CC)CC ZMANZCXQSJIPKH-UHFFFAOYSA-N 0.000 description 6
- XXROGKLTLUQVRX-UHFFFAOYSA-N allyl alcohol Chemical compound OCC=C XXROGKLTLUQVRX-UHFFFAOYSA-N 0.000 description 6
- UHOVQNZJYSORNB-MZWXYZOWSA-N benzene-d6 Chemical compound [2H]C1=C([2H])C([2H])=C([2H])C([2H])=C1[2H] UHOVQNZJYSORNB-MZWXYZOWSA-N 0.000 description 6
- 239000011203 carbon fibre reinforced carbon Substances 0.000 description 6
- 229910052742 iron Inorganic materials 0.000 description 6
- 239000000463 material Substances 0.000 description 6
- VLKZOEOYAKHREP-UHFFFAOYSA-N n-Hexane Chemical compound CCCCCC VLKZOEOYAKHREP-UHFFFAOYSA-N 0.000 description 6
- 239000007795 chemical reaction product Substances 0.000 description 5
- 238000005160 1H NMR spectroscopy Methods 0.000 description 4
- 239000012230 colorless oil Substances 0.000 description 4
- 125000004122 cyclic group Chemical group 0.000 description 4
- 125000001495 ethyl group Chemical group [H]C([H])([H])C([H])([H])* 0.000 description 4
- 238000001914 filtration Methods 0.000 description 4
- 229910000510 noble metal Inorganic materials 0.000 description 4
- BASFCYQUMIYNBI-UHFFFAOYSA-N platinum Chemical compound [Pt] BASFCYQUMIYNBI-UHFFFAOYSA-N 0.000 description 4
- 238000006467 substitution reaction Methods 0.000 description 4
- UHOVQNZJYSORNB-UHFFFAOYSA-N Benzene Chemical compound C1=CC=CC=C1 UHOVQNZJYSORNB-UHFFFAOYSA-N 0.000 description 3
- RTZKZFJDLAIYFH-UHFFFAOYSA-N Diethyl ether Chemical compound CCOCC RTZKZFJDLAIYFH-UHFFFAOYSA-N 0.000 description 3
- JUJWROOIHBZHMG-UHFFFAOYSA-N Pyridine Chemical group C1=CC=NC=C1 JUJWROOIHBZHMG-UHFFFAOYSA-N 0.000 description 3
- 230000008901 benefit Effects 0.000 description 3
- 125000004432 carbon atom Chemical group C* 0.000 description 3
- 238000000576 coating method Methods 0.000 description 3
- 239000013078 crystal Substances 0.000 description 3
- 125000000113 cyclohexyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])(*)C([H])([H])C1([H])[H] 0.000 description 3
- 125000000743 hydrocarbylene group Chemical group 0.000 description 3
- 125000001624 naphthyl group Chemical group 0.000 description 3
- 229910052757 nitrogen Inorganic materials 0.000 description 3
- 239000002244 precipitate Substances 0.000 description 3
- 239000007787 solid Substances 0.000 description 3
- LIKMAJRDDDTEIG-UHFFFAOYSA-N 1-hexene Chemical compound CCCCC=C LIKMAJRDDDTEIG-UHFFFAOYSA-N 0.000 description 2
- STMDPCBYJCIZOD-UHFFFAOYSA-N 2-(2,4-dinitroanilino)-4-methylpentanoic acid Chemical compound CC(C)CC(C(O)=O)NC1=CC=C([N+]([O-])=O)C=C1[N+]([O-])=O STMDPCBYJCIZOD-UHFFFAOYSA-N 0.000 description 2
- VVJKKWFAADXIJK-UHFFFAOYSA-N Allylamine Chemical compound NCC=C VVJKKWFAADXIJK-UHFFFAOYSA-N 0.000 description 2
- PAYRUJLWNCNPSJ-UHFFFAOYSA-N Aniline Chemical compound NC1=CC=CC=C1 PAYRUJLWNCNPSJ-UHFFFAOYSA-N 0.000 description 2
- XKRFYHLGVUSROY-UHFFFAOYSA-N Argon Chemical compound [Ar] XKRFYHLGVUSROY-UHFFFAOYSA-N 0.000 description 2
- UEXCJVNBTNXOEH-UHFFFAOYSA-N Ethynylbenzene Chemical group C#CC1=CC=CC=C1 UEXCJVNBTNXOEH-UHFFFAOYSA-N 0.000 description 2
- UFWIBTONFRDIAS-UHFFFAOYSA-N Naphthalene Chemical compound C1=CC=CC2=CC=CC=C21 UFWIBTONFRDIAS-UHFFFAOYSA-N 0.000 description 2
- PPBRXRYQALVLMV-UHFFFAOYSA-N Styrene Chemical compound C=CC1=CC=CC=C1 PPBRXRYQALVLMV-UHFFFAOYSA-N 0.000 description 2
- 239000000853 adhesive Substances 0.000 description 2
- 230000001070 adhesive effect Effects 0.000 description 2
- 125000002947 alkylene group Chemical group 0.000 description 2
- 125000000304 alkynyl group Chemical group 0.000 description 2
- 125000000129 anionic group Chemical group 0.000 description 2
- 125000000732 arylene group Chemical group 0.000 description 2
- 150000001721 carbon Chemical group 0.000 description 2
- 230000003197 catalytic effect Effects 0.000 description 2
- 125000002993 cycloalkylene group Chemical group 0.000 description 2
- LPIQUOYDBNQMRZ-UHFFFAOYSA-N cyclopentene Chemical compound C1CC=CC1 LPIQUOYDBNQMRZ-UHFFFAOYSA-N 0.000 description 2
- 239000000706 filtrate Substances 0.000 description 2
- 229910052731 fluorine Inorganic materials 0.000 description 2
- 239000011737 fluorine Substances 0.000 description 2
- 239000011521 glass Substances 0.000 description 2
- 125000001072 heteroaryl group Chemical group 0.000 description 2
- 150000002391 heterocyclic compounds Chemical class 0.000 description 2
- 239000002815 homogeneous catalyst Substances 0.000 description 2
- 125000001449 isopropyl group Chemical group [H]C([H])([H])C([H])(*)C([H])([H])[H] 0.000 description 2
- 239000002808 molecular sieve Substances 0.000 description 2
- CCCMONHAUSKTEQ-UHFFFAOYSA-N octadec-1-ene Chemical compound CCCCCCCCCCCCCCCCC=C CCCMONHAUSKTEQ-UHFFFAOYSA-N 0.000 description 2
- 125000000962 organic group Chemical group 0.000 description 2
- 230000003647 oxidation Effects 0.000 description 2
- 238000007254 oxidation reaction Methods 0.000 description 2
- 239000002245 particle Substances 0.000 description 2
- 229910052697 platinum Inorganic materials 0.000 description 2
- 125000001436 propyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])[H] 0.000 description 2
- KEFOZNJTQPJEOB-UHFFFAOYSA-N pyridine-2,3-diimine Chemical compound N=C1C=CC=NC1=N KEFOZNJTQPJEOB-UHFFFAOYSA-N 0.000 description 2
- 239000000565 sealant Substances 0.000 description 2
- 239000000741 silica gel Substances 0.000 description 2
- 229910002027 silica gel Inorganic materials 0.000 description 2
- 229940024463 silicone emollient and protective product Drugs 0.000 description 2
- URGAHOPLAPQHLN-UHFFFAOYSA-N sodium aluminosilicate Chemical compound [Na+].[Al+3].[O-][Si]([O-])=O.[O-][Si]([O-])=O URGAHOPLAPQHLN-UHFFFAOYSA-N 0.000 description 2
- 239000004094 surface-active agent Substances 0.000 description 2
- 125000003944 tolyl group Chemical group 0.000 description 2
- 229910052723 transition metal Inorganic materials 0.000 description 2
- 150000003624 transition metals Chemical class 0.000 description 2
- 125000005023 xylyl group Chemical group 0.000 description 2
- 125000003837 (C1-C20) alkyl group Chemical group 0.000 description 1
- PRBHEGAFLDMLAL-UHFFFAOYSA-N 1,5-Hexadiene Natural products CC=CCC=C PRBHEGAFLDMLAL-UHFFFAOYSA-N 0.000 description 1
- SDRZFSPCVYEJTP-UHFFFAOYSA-N 1-ethenylcyclohexene Chemical compound C=CC1=CCCCC1 SDRZFSPCVYEJTP-UHFFFAOYSA-N 0.000 description 1
- 238000001644 13C nuclear magnetic resonance spectroscopy Methods 0.000 description 1
- VXDHQYLFEYUMFY-UHFFFAOYSA-N 2-methylprop-2-en-1-amine Chemical compound CC(=C)CN VXDHQYLFEYUMFY-UHFFFAOYSA-N 0.000 description 1
- 125000001494 2-propynyl group Chemical group [H]C#CC([H])([H])* 0.000 description 1
- XAYDWGMOPRHLEP-UHFFFAOYSA-N 6-ethenyl-7-oxabicyclo[4.1.0]heptane Chemical compound C1CCCC2OC21C=C XAYDWGMOPRHLEP-UHFFFAOYSA-N 0.000 description 1
- ZCYVEMRRCGMTRW-UHFFFAOYSA-N 7553-56-2 Chemical compound [I] ZCYVEMRRCGMTRW-UHFFFAOYSA-N 0.000 description 1
- NIXOWILDQLNWCW-UHFFFAOYSA-M Acrylate Chemical compound [O-]C(=O)C=C NIXOWILDQLNWCW-UHFFFAOYSA-M 0.000 description 1
- CPELXLSAUQHCOX-UHFFFAOYSA-M Bromide Chemical compound [Br-] CPELXLSAUQHCOX-UHFFFAOYSA-M 0.000 description 1
- WKBOTKDWSSQWDR-UHFFFAOYSA-N Bromine atom Chemical compound [Br] WKBOTKDWSSQWDR-UHFFFAOYSA-N 0.000 description 1
- VEXZGXHMUGYJMC-UHFFFAOYSA-M Chloride anion Chemical compound [Cl-] VEXZGXHMUGYJMC-UHFFFAOYSA-M 0.000 description 1
- ZAMOUSCENKQFHK-UHFFFAOYSA-N Chlorine atom Chemical compound [Cl] ZAMOUSCENKQFHK-UHFFFAOYSA-N 0.000 description 1
- SNRUBQQJIBEYMU-UHFFFAOYSA-N Dodecane Natural products CCCCCCCCCCCC SNRUBQQJIBEYMU-UHFFFAOYSA-N 0.000 description 1
- PXGOKWXKJXAPGV-UHFFFAOYSA-N Fluorine Chemical compound FF PXGOKWXKJXAPGV-UHFFFAOYSA-N 0.000 description 1
- DGAQECJNVWCQMB-PUAWFVPOSA-M Ilexoside XXIX Chemical compound C[C@@H]1CC[C@@]2(CC[C@@]3(C(=CC[C@H]4[C@]3(CC[C@@H]5[C@@]4(CC[C@@H](C5(C)C)OS(=O)(=O)[O-])C)C)[C@@H]2[C@]1(C)O)C)C(=O)O[C@H]6[C@@H]([C@H]([C@@H]([C@H](O6)CO)O)O)O.[Na+] DGAQECJNVWCQMB-PUAWFVPOSA-M 0.000 description 1
- 229910010082 LiAlH Inorganic materials 0.000 description 1
- OAICVXFJPJFONN-UHFFFAOYSA-N Phosphorus Chemical compound [P] OAICVXFJPJFONN-UHFFFAOYSA-N 0.000 description 1
- 239000005062 Polybutadiene Substances 0.000 description 1
- 239000002202 Polyethylene glycol Substances 0.000 description 1
- 229920005830 Polyurethane Foam Polymers 0.000 description 1
- 238000004639 Schlenk technique Methods 0.000 description 1
- XUIMIQQOPSSXEZ-UHFFFAOYSA-N Silicon Chemical compound [Si] XUIMIQQOPSSXEZ-UHFFFAOYSA-N 0.000 description 1
- NINIDFKCEFEMDL-UHFFFAOYSA-N Sulfur Chemical compound [S] NINIDFKCEFEMDL-UHFFFAOYSA-N 0.000 description 1
- HEDRZPFGACZZDS-MICDWDOJSA-N Trichloro(2H)methane Chemical compound [2H]C(Cl)(Cl)Cl HEDRZPFGACZZDS-MICDWDOJSA-N 0.000 description 1
- 125000002252 acyl group Chemical group 0.000 description 1
- 238000013006 addition curing Methods 0.000 description 1
- 150000001338 aliphatic hydrocarbons Chemical class 0.000 description 1
- 125000005037 alkyl phenyl group Chemical group 0.000 description 1
- XYLMUPLGERFSHI-UHFFFAOYSA-N alpha-Methylstyrene Chemical compound CC(=C)C1=CC=CC=C1 XYLMUPLGERFSHI-UHFFFAOYSA-N 0.000 description 1
- HSFWRNGVRCDJHI-UHFFFAOYSA-N alpha-acetylene Natural products C#C HSFWRNGVRCDJHI-UHFFFAOYSA-N 0.000 description 1
- 150000001450 anions Chemical class 0.000 description 1
- 229910052786 argon Inorganic materials 0.000 description 1
- 125000004429 atom Chemical group 0.000 description 1
- QVGXLLKOCUKJST-UHFFFAOYSA-N atomic oxygen Chemical compound [O] QVGXLLKOCUKJST-UHFFFAOYSA-N 0.000 description 1
- 238000010923 batch production Methods 0.000 description 1
- 125000001797 benzyl group Chemical group [H]C1=C([H])C([H])=C(C([H])=C1[H])C([H])([H])* 0.000 description 1
- 230000001588 bifunctional effect Effects 0.000 description 1
- 230000000903 blocking effect Effects 0.000 description 1
- GDTBXPJZTBHREO-UHFFFAOYSA-N bromine Substances BrBr GDTBXPJZTBHREO-UHFFFAOYSA-N 0.000 description 1
- 229910052794 bromium Inorganic materials 0.000 description 1
- 125000001246 bromo group Chemical group Br* 0.000 description 1
- 125000000484 butyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 description 1
- CREMABGTGYGIQB-UHFFFAOYSA-N carbon carbon Chemical compound C.C CREMABGTGYGIQB-UHFFFAOYSA-N 0.000 description 1
- 239000012018 catalyst precursor Substances 0.000 description 1
- 238000006555 catalytic reaction Methods 0.000 description 1
- 230000008859 change Effects 0.000 description 1
- 239000003795 chemical substances by application Substances 0.000 description 1
- 239000000460 chlorine Substances 0.000 description 1
- 229910052801 chlorine Inorganic materials 0.000 description 1
- 125000001309 chloro group Chemical group Cl* 0.000 description 1
- YCITZMJNBYYMJO-UHFFFAOYSA-N chloro(diphenyl)silicon Chemical compound C=1C=CC=CC=1[Si](Cl)C1=CC=CC=C1 YCITZMJNBYYMJO-UHFFFAOYSA-N 0.000 description 1
- YGHUUVGIRWMJGE-UHFFFAOYSA-N chlorodimethylsilane Chemical compound C[SiH](C)Cl YGHUUVGIRWMJGE-UHFFFAOYSA-N 0.000 description 1
- 239000003426 co-catalyst Substances 0.000 description 1
- 150000001869 cobalt compounds Chemical class 0.000 description 1
- UOPTZAYKABCBRQ-UHFFFAOYSA-N cobalt pyridine Chemical compound [Co].c1ccncc1.c1ccncc1 UOPTZAYKABCBRQ-UHFFFAOYSA-N 0.000 description 1
- 238000010924 continuous production Methods 0.000 description 1
- 238000007796 conventional method Methods 0.000 description 1
- 125000006165 cyclic alkyl group Chemical group 0.000 description 1
- 125000004956 cyclohexylene group Chemical group 0.000 description 1
- 125000000640 cyclooctyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])([H])C([H])(*)C([H])([H])C([H])([H])C1([H])[H] 0.000 description 1
- 239000000412 dendrimer Substances 0.000 description 1
- 229920000736 dendritic polymer Polymers 0.000 description 1
- 230000001627 detrimental effect Effects 0.000 description 1
- RAABOESOVLLHRU-UHFFFAOYSA-N diazene Chemical compound N=N RAABOESOVLLHRU-UHFFFAOYSA-N 0.000 description 1
- 229910000071 diazene Inorganic materials 0.000 description 1
- 238000007865 diluting Methods 0.000 description 1
- 230000003292 diminished effect Effects 0.000 description 1
- 125000003438 dodecyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 1
- 230000000694 effects Effects 0.000 description 1
- 239000013536 elastomeric material Substances 0.000 description 1
- 125000004185 ester group Chemical group 0.000 description 1
- 125000005677 ethinylene group Chemical group [*:2]C#C[*:1] 0.000 description 1
- 238000003818 flash chromatography Methods 0.000 description 1
- 125000001153 fluoro group Chemical group F* 0.000 description 1
- 239000000499 gel Substances 0.000 description 1
- 238000007429 general method Methods 0.000 description 1
- 150000002367 halogens Chemical group 0.000 description 1
- 125000000623 heterocyclic group Chemical group 0.000 description 1
- 239000002638 heterogeneous catalyst Substances 0.000 description 1
- PYGSKMBEVAICCR-UHFFFAOYSA-N hexa-1,5-diene Chemical compound C=CCCC=C PYGSKMBEVAICCR-UHFFFAOYSA-N 0.000 description 1
- 125000001145 hydrido group Chemical group *[H] 0.000 description 1
- 125000004435 hydrogen atom Chemical group [H]* 0.000 description 1
- 238000005984 hydrogenation reaction Methods 0.000 description 1
- 125000002887 hydroxy group Chemical group [H]O* 0.000 description 1
- 125000004464 hydroxyphenyl group Chemical group 0.000 description 1
- 125000001841 imino group Chemical group [H]N=* 0.000 description 1
- 239000004615 ingredient Substances 0.000 description 1
- 229910052500 inorganic mineral Inorganic materials 0.000 description 1
- 229910052740 iodine Inorganic materials 0.000 description 1
- 239000011630 iodine Substances 0.000 description 1
- 125000002346 iodo group Chemical group I* 0.000 description 1
- 150000002503 iridium Chemical class 0.000 description 1
- 125000000959 isobutyl group Chemical group [H]C([H])([H])C([H])(C([H])([H])[H])C([H])([H])* 0.000 description 1
- 239000012948 isocyanate Substances 0.000 description 1
- 150000002513 isocyanates Chemical class 0.000 description 1
- 238000006317 isomerization reaction Methods 0.000 description 1
- 239000007788 liquid Substances 0.000 description 1
- 238000007885 magnetic separation Methods 0.000 description 1
- 229910052748 manganese Inorganic materials 0.000 description 1
- 238000004519 manufacturing process Methods 0.000 description 1
- 150000002734 metacrylic acid derivatives Chemical class 0.000 description 1
- 239000011707 mineral Substances 0.000 description 1
- 125000000896 monocarboxylic acid group Chemical group 0.000 description 1
- 229910052759 nickel Inorganic materials 0.000 description 1
- 239000012299 nitrogen atmosphere Substances 0.000 description 1
- QJGQUHMNIGDVPM-UHFFFAOYSA-N nitrogen group Chemical group [N] QJGQUHMNIGDVPM-UHFFFAOYSA-N 0.000 description 1
- SJYNFBVQFBRSIB-UHFFFAOYSA-N norbornadiene Chemical compound C1=CC2C=CC1C2 SJYNFBVQFBRSIB-UHFFFAOYSA-N 0.000 description 1
- JFNLZVQOOSMTJK-KNVOCYPGSA-N norbornene Chemical compound C1[C@@H]2CC[C@H]1C=C2 JFNLZVQOOSMTJK-KNVOCYPGSA-N 0.000 description 1
- 125000002868 norbornyl group Chemical group C12(CCC(CC1)C2)* 0.000 description 1
- 238000000655 nuclear magnetic resonance spectrum Methods 0.000 description 1
- MSRJTTSHWYDFIU-UHFFFAOYSA-N octyltriethoxysilane Chemical compound CCCCCCCC[Si](OCC)(OCC)OCC MSRJTTSHWYDFIU-UHFFFAOYSA-N 0.000 description 1
- 238000006384 oligomerization reaction Methods 0.000 description 1
- 229920000620 organic polymer Polymers 0.000 description 1
- 125000002524 organometallic group Chemical group 0.000 description 1
- 229910052760 oxygen Inorganic materials 0.000 description 1
- 239000001301 oxygen Substances 0.000 description 1
- 150000002940 palladium Chemical class 0.000 description 1
- RGSFGYAAUTVSQA-UHFFFAOYSA-N pentamethylene Natural products C1CCCC1 RGSFGYAAUTVSQA-UHFFFAOYSA-N 0.000 description 1
- 125000000843 phenylene group Chemical group C1(=C(C=CC=C1)*)* 0.000 description 1
- 125000000286 phenylethyl group Chemical group [H]C1=C([H])C([H])=C(C([H])=C1[H])C([H])([H])C([H])([H])* 0.000 description 1
- 229910052698 phosphorus Inorganic materials 0.000 description 1
- 239000011574 phosphorus Substances 0.000 description 1
- 150000003057 platinum Chemical class 0.000 description 1
- 229920002857 polybutadiene Polymers 0.000 description 1
- 229920001223 polyethylene glycol Polymers 0.000 description 1
- 238000006116 polymerization reaction Methods 0.000 description 1
- 229920000098 polyolefin Polymers 0.000 description 1
- 239000011496 polyurethane foam Substances 0.000 description 1
- 239000011148 porous material Substances 0.000 description 1
- 239000010970 precious metal Substances 0.000 description 1
- 238000002360 preparation method Methods 0.000 description 1
- FBCQUCJYYPMKRO-UHFFFAOYSA-N prop-2-enyl 2-methylprop-2-enoate Chemical compound CC(=C)C(=O)OCC=C FBCQUCJYYPMKRO-UHFFFAOYSA-N 0.000 description 1
- QTECDUFMBMSHKR-UHFFFAOYSA-N prop-2-enyl prop-2-enoate Chemical compound C=CCOC(=O)C=C QTECDUFMBMSHKR-UHFFFAOYSA-N 0.000 description 1
- DNAJDTIOMGISDS-UHFFFAOYSA-N prop-2-enylsilane Chemical compound [SiH3]CC=C DNAJDTIOMGISDS-UHFFFAOYSA-N 0.000 description 1
- 125000004368 propenyl group Chemical group C(=CC)* 0.000 description 1
- 238000000425 proton nuclear magnetic resonance spectrum Methods 0.000 description 1
- UMJSCPRVCHMLSP-UHFFFAOYSA-N pyridine Natural products COC1=CC=CN=C1 UMJSCPRVCHMLSP-UHFFFAOYSA-N 0.000 description 1
- 125000002112 pyrrolidino group Chemical group [*]N1C([H])([H])C([H])([H])C([H])([H])C1([H])[H] 0.000 description 1
- 150000003254 radicals Chemical class 0.000 description 1
- 239000002994 raw material Substances 0.000 description 1
- 230000009467 reduction Effects 0.000 description 1
- 239000013557 residual solvent Substances 0.000 description 1
- 229920005989 resin Polymers 0.000 description 1
- 239000011347 resin Substances 0.000 description 1
- 150000003283 rhodium Chemical class 0.000 description 1
- 238000004062 sedimentation Methods 0.000 description 1
- 229920002379 silicone rubber Polymers 0.000 description 1
- 239000011734 sodium Substances 0.000 description 1
- 229910052708 sodium Inorganic materials 0.000 description 1
- 239000011949 solid catalyst Substances 0.000 description 1
- 230000000087 stabilizing effect Effects 0.000 description 1
- 125000004079 stearyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 description 1
- 239000000126 substance Substances 0.000 description 1
- 229910052717 sulfur Inorganic materials 0.000 description 1
- 239000011593 sulfur Substances 0.000 description 1
- 230000007704 transition Effects 0.000 description 1
- 125000004665 trialkylsilyl group Chemical group 0.000 description 1
- DAVGYCGZLQMNSH-UHFFFAOYSA-N triethoxy(octan-2-yl)silane Chemical compound CCCCCCC(C)[Si](OCC)(OCC)OCC DAVGYCGZLQMNSH-UHFFFAOYSA-N 0.000 description 1
- 125000000026 trimethylsilyl group Chemical group [H]C([H])([H])[Si]([*])(C([H])([H])[H])C([H])([H])[H] 0.000 description 1
- 229920006305 unsaturated polyester Polymers 0.000 description 1
- 239000004711 α-olefin Substances 0.000 description 1
Classifications
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J31/00—Catalysts comprising hydrides, coordination complexes or organic compounds
- B01J31/16—Catalysts comprising hydrides, coordination complexes or organic compounds containing coordination complexes
- B01J31/22—Organic complexes
- B01J31/2282—Unsaturated compounds used as ligands
- B01J31/2295—Cyclic compounds, e.g. cyclopentadienyls
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07F—ACYCLIC, CARBOCYCLIC OR HETEROCYCLIC COMPOUNDS CONTAINING ELEMENTS OTHER THAN CARBON, HYDROGEN, HALOGEN, OXYGEN, NITROGEN, SULFUR, SELENIUM OR TELLURIUM
- C07F15/00—Compounds containing elements of Groups 8, 9, 10 or 18 of the Periodic Table
- C07F15/06—Cobalt compounds
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07F—ACYCLIC, CARBOCYCLIC OR HETEROCYCLIC COMPOUNDS CONTAINING ELEMENTS OTHER THAN CARBON, HYDROGEN, HALOGEN, OXYGEN, NITROGEN, SULFUR, SELENIUM OR TELLURIUM
- C07F15/00—Compounds containing elements of Groups 8, 9, 10 or 18 of the Periodic Table
- C07F15/06—Cobalt compounds
- C07F15/065—Cobalt compounds without a metal-carbon linkage
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07F—ACYCLIC, CARBOCYCLIC OR HETEROCYCLIC COMPOUNDS CONTAINING ELEMENTS OTHER THAN CARBON, HYDROGEN, HALOGEN, OXYGEN, NITROGEN, SULFUR, SELENIUM OR TELLURIUM
- C07F7/00—Compounds containing elements of Groups 4 or 14 of the Periodic Table
- C07F7/02—Silicon compounds
- C07F7/08—Compounds having one or more C—Si linkages
- C07F7/0834—Compounds having one or more O-Si linkage
- C07F7/0838—Compounds with one or more Si-O-Si sequences
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07F—ACYCLIC, CARBOCYCLIC OR HETEROCYCLIC COMPOUNDS CONTAINING ELEMENTS OTHER THAN CARBON, HYDROGEN, HALOGEN, OXYGEN, NITROGEN, SULFUR, SELENIUM OR TELLURIUM
- C07F7/00—Compounds containing elements of Groups 4 or 14 of the Periodic Table
- C07F7/02—Silicon compounds
- C07F7/08—Compounds having one or more C—Si linkages
- C07F7/0834—Compounds having one or more O-Si linkage
- C07F7/0838—Compounds with one or more Si-O-Si sequences
- C07F7/0872—Preparation and treatment thereof
- C07F7/0876—Reactions involving the formation of bonds to a Si atom of a Si-O-Si sequence other than a bond of the Si-O-Si linkage
- C07F7/0878—Si-C bond
- C07F7/0879—Hydrosilylation reactions
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07F—ACYCLIC, CARBOCYCLIC OR HETEROCYCLIC COMPOUNDS CONTAINING ELEMENTS OTHER THAN CARBON, HYDROGEN, HALOGEN, OXYGEN, NITROGEN, SULFUR, SELENIUM OR TELLURIUM
- C07F7/00—Compounds containing elements of Groups 4 or 14 of the Periodic Table
- C07F7/02—Silicon compounds
- C07F7/08—Compounds having one or more C—Si linkages
- C07F7/18—Compounds having one or more C—Si linkages as well as one or more C—O—Si linkages
- C07F7/1804—Compounds having Si-O-C linkages
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07F—ACYCLIC, CARBOCYCLIC OR HETEROCYCLIC COMPOUNDS CONTAINING ELEMENTS OTHER THAN CARBON, HYDROGEN, HALOGEN, OXYGEN, NITROGEN, SULFUR, SELENIUM OR TELLURIUM
- C07F7/00—Compounds containing elements of Groups 4 or 14 of the Periodic Table
- C07F7/02—Silicon compounds
- C07F7/08—Compounds having one or more C—Si linkages
- C07F7/18—Compounds having one or more C—Si linkages as well as one or more C—O—Si linkages
- C07F7/1804—Compounds having Si-O-C linkages
- C07F7/1872—Preparation; Treatments not provided for in C07F7/20
- C07F7/1876—Preparation; Treatments not provided for in C07F7/20 by reactions involving the formation of Si-C linkages
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08J—WORKING-UP; GENERAL PROCESSES OF COMPOUNDING; AFTER-TREATMENT NOT COVERED BY SUBCLASSES C08B, C08C, C08F, C08G or C08H
- C08J3/00—Processes of treating or compounding macromolecular substances
- C08J3/24—Crosslinking, e.g. vulcanising, of macromolecules
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J2231/00—Catalytic reactions performed with catalysts classified in B01J31/00
- B01J2231/30—Addition reactions at carbon centres, i.e. to either C-C or C-X multiple bonds
- B01J2231/32—Addition reactions to C=C or C-C triple bonds
- B01J2231/323—Hydrometalation, e.g. bor-, alumin-, silyl-, zirconation or analoguous reactions like carbometalation, hydrocarbation
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J2531/00—Additional information regarding catalytic systems classified in B01J31/00
- B01J2531/80—Complexes comprising metals of Group VIII as the central metal
- B01J2531/84—Metals of the iron group
- B01J2531/845—Cobalt
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08J—WORKING-UP; GENERAL PROCESSES OF COMPOUNDING; AFTER-TREATMENT NOT COVERED BY SUBCLASSES C08B, C08C, C08F, C08G or C08H
- C08J2383/00—Characterised by the use of macromolecular compounds obtained by reactions forming in the main chain of the macromolecule a linkage containing silicon with or without sulfur, nitrogen, oxygen, or carbon only; Derivatives of such polymers
- C08J2383/04—Polysiloxanes
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Health & Medical Sciences (AREA)
- Medicinal Chemistry (AREA)
- Polymers & Plastics (AREA)
- Inorganic Chemistry (AREA)
- Engineering & Computer Science (AREA)
- Materials Engineering (AREA)
- Low-Molecular Organic Synthesis Reactions Using Catalysts (AREA)
- Catalysts (AREA)
- Organic Low-Molecular-Weight Compounds And Preparation Thereof (AREA)
Abstract
Description
本出願は、「コバルト触媒並びにヒドロシリル化及び脱水素シリル化のためのその使用」と題する2013年11月19日出願の米国仮出願第61/906,204号の優先権及び利益を主張し、その仮出願の全開示はすべて、ここでの参照によって本明細書に取り入れるものとする。
本発明は全般に、遷移金属含有化合物に関し、より具体的にはターピリジン配位子を含むコバルト錯体、並びにヒドロシリル化及び脱水素シリル化反応のための触媒としてのそれらの使用に関する。
ヒドロシリル化の化学は、典型的にはシリルヒドリドと不飽和有機基の間の反応を伴い、シリコーン界面活性剤、シリコーン流体、及びシランのような市販のシリコーン系製品、並びにシーラント、接着剤、及びコーティングのような多くの付加硬化型の製品を製造するための合成経路の基礎をなしている。典型的なヒドロシリル化反応は、オレフィンのような不飽和基に対するシリルヒドリド(Si−H)の付加を触媒するために、貴金属触媒を用いる。こうした反応で結果として得られる生成物は、シリル置換された飽和化合物である。これらの殆どの場合に、シリル基の付加は逆マルコフニコフ的に、即ち不飽和基のより置換されていない炭素原子に対して進行する。貴金属で触媒されたヒドロシリル化の殆どは、末端不飽和オレフィンについてのみ上首尾に作用する。というのは、内部不飽和部分は一般に非反応性であるか、又は僅かしか反応しないからである。現在のところ、Si−H基の付加後にまだ原料基質に不飽和が残存するようなオレフィンの一般的なシリル化のために、商業的に実行可能な方法は限られている。脱水素シリル化と呼ばれるこの反応は、新たなシリコーン材料、例えばシラン、シリコーン流体、架橋シリコーンエラストマー、及びシリル化又はシリコーン架橋された有機ポリマー、例えばポリオレフィン、不飽和ポリエステルなどの合成に対する、潜在的な用途を有している。
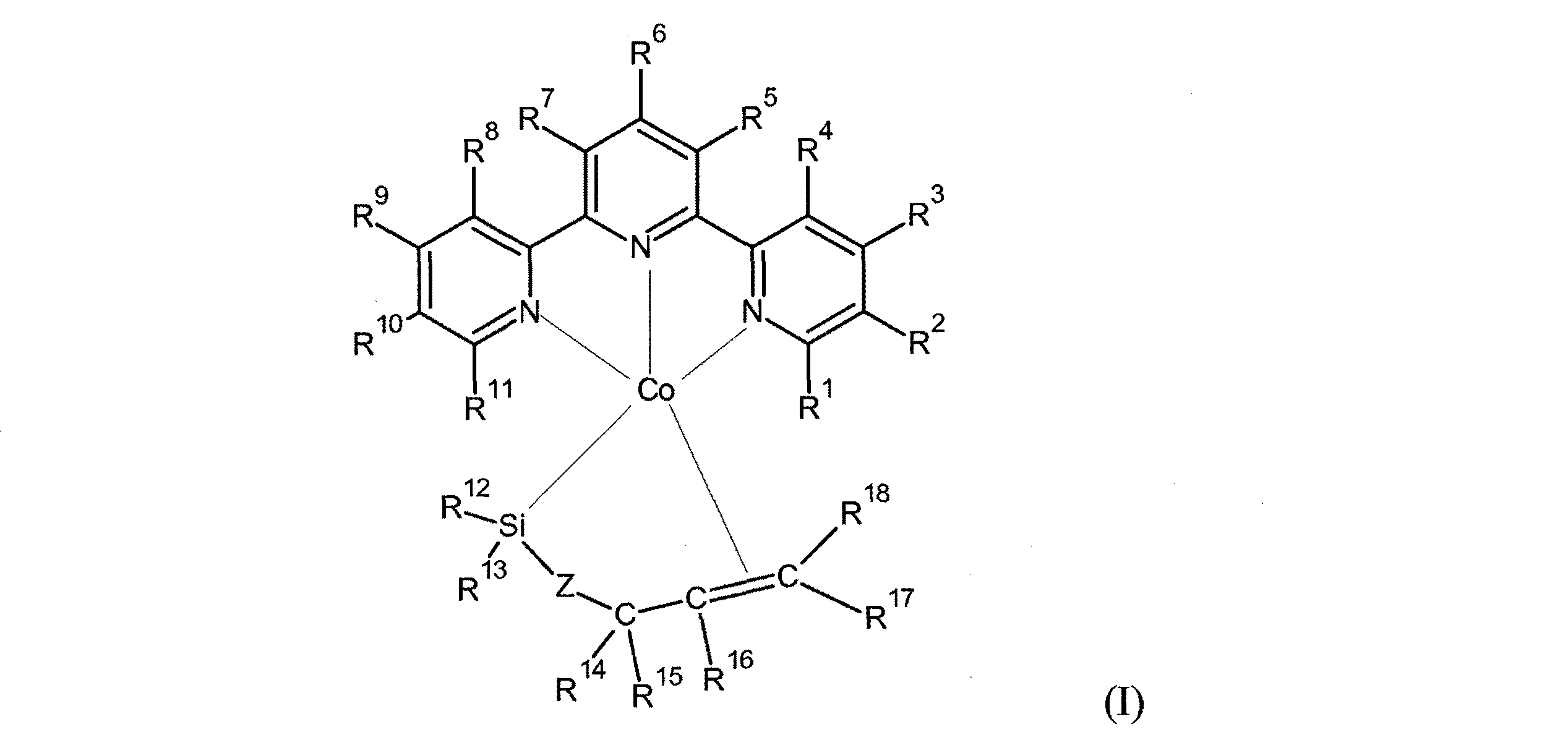
のコバルト錯体を提供し、式中、R1〜R18の各々は独立して、水素、C1〜C18アルキル、C1〜C18置換アルキル、C5〜C18シクロアルキル、C5〜C18置換シクロアルキル、C6〜C18アリール、C6〜C18置換アリール、又は不活性置換基であり、式中、1又はより多くのR1〜R18は、水素以外の場合、任意選択で少なくとも1つのヘテロ原子を含み;任意選択でR1〜R11の相互に隣接するいずれか2つ、R4−R5、及び/又はR7−R8は一緒になって置換又は未置換の、飽和又は不飽和の環構造の環を形成してもよく;またZはO、NR19、又はCR20R21であって、R19、R20、及びR21は、独立して、水素、C1〜C18アルキル、C1〜C18置換アルキル、C6〜C18アリール、C6〜C18置換アリール基、アルカリール基、アラルキル基であり、1又はより多くのR19、R20、及びR21は任意選択で少なくとも1つのヘテロ原子を含む。
1つの実施形では、R12及びR13は独立してC1〜C8の直鎖、分岐、若しくは環状アルキル、又はC6〜C18アリールから選択される。
1つの実施形では、R12及びR13はメチルであり、R14〜R18は水素である。
1つの実施形では、R12及びR13はフェニルであり、R14〜R18は水素である。
1つの実施形態では、R1、R2、R3、R4、R5、R6、R7、R8、R9、R10及び/又はR11の少なくとも1つは支持体と共有結合する官能基を含む。
であり、式中、R1〜R18の各々は独立して、水素、C1〜C18アルキル、C1〜C18置換アルキル、C5〜C18シクロアルキル、C5〜C18置換シクロアルキル、C6〜C18アリール、C6〜C18置換アリール、又は不活性置換基であり、式中、1又はより多くのR1〜R18は、水素以外の場合、任意選択で少なくとも1つのヘテロ原子を含み;任意選択でR1〜R11の相互に隣接するいずれか2つ、R4−R5、及び/又はR7−R8は一緒になって置換又は未置換の、飽和又は不飽和の環構造の環を形成してもよく;またZはO、NR19、又はCR20R21であって、R19、R20、及びR21は、独立して、水素、C1〜C18アルキル、C1〜C18置換アルキル、C6〜C18アリール、C6〜C18置換アリール基、アルカリール基、アラルキル基であり、1又はより多くのR19、R20、及びR21は任意選択で少なくとも1つのヘテロ原子を含む。
1つの実施形では、R12及びR13は独立してC1〜C8の直鎖、分岐、若しくは環状アルキル、又はC6〜C18アリールから選択される。
1つの実施形では、R12及びR13はメチルであり、R14〜R18は水素である。
1つの実施形では、R12及びR13はフェニルであり、R14〜R18は水素である。
の錯体と接触させることを含み、式中、R1〜R18の各々は独立して、水素、C1〜C18アルキル、C1〜C18置換アルキル、C5〜C18シクロアルキル、C5〜C18置換シクロアルキル、C6〜C18アリール、C6〜C18置換アリール、又は不活性置換基であり、式中、1又はより多くのR1〜R18は、水素以外の場合、任意選択で少なくとも1つのヘテロ原子を含み;任意選択でR1〜R11の相互に隣接するいずれか2つ、R4−R5、及び/又はR7−R8は一緒になって置換又は未置換の、飽和又は不飽和の環構造の環を形成してもよく;またZはO、NR19、又はCR20R21であって、R19、R20、及びR21は、独立して、水素、C1〜C18アルキル、C1〜C18置換アルキル、C6〜C18アリール、C6〜C18置換アリール基、アルカリール基、アラルキル基であり、1又はより多くのR19、R20、及びR21は任意選択で少なくとも1つのヘテロ原子を含む。
R22 mSiHpX4−(m+p);
MaMH bDcDH dTeTH fQg;
R28 3Si(CHR28)xSiOSiR28 2(OSiR28 2)yOSiR28 2H;
R28 3Si(CHR28)xSiR28 2H
の化合物の1又は組み合わせ、或いはこれらの2又はより多くの組み合わせから選択され、式中、R22の各々は独立して、置換又は未置換の脂肪族又は芳香族ヒドロカルビル基;Xはハロゲン、アルコキシ、アシロキシ、又はシラザン;mは0〜3;pは1〜3、但しm+p≦4であり、4価のケイ素は保持され;Mは式R23 3SiO1/2の単官能基を表し;Dは式R23 2SiO2/2の2官能基を表し;Tは式R23SiO3/2の3官能基を表し;Qは式SiO4/2の4官能基を表し;MHはHR23 2SiO1/2を表し、THはHSiO3/2を表し、そしてDH基はR23HSiO2/2を表し;R24の各々は独立して、C1〜C18アルキル、C1〜C18置換アルキル、C6〜C14アリール又は置換アリールであり、R23は任意選択で少なくとも1つのヘテロ原子を含み;下付文字a、b、c、d、e、f、及びgはその化合物のモル質量が100と100,000ダルトンの間となる値;R28の各々は独立して、C1〜C18アルキル、C1〜C18置換アルキル、C6〜C14アリール又は置換アリール;xは1〜8、そしてyは0〜10である。
本発明は、1つの側面においてコバルト錯体を提供し、この錯体はヒドロシリル化又は脱水素シリル化反応において、触媒として使用可能である。触媒組成物は、ターピリジン配位子と、キレートしたアルケン置換シリル配位子とを有するコバルト錯体を含み、アルケニル置換はケイ素に対してベータ位にあることが好ましい。1つの実施形態では、触媒は式(I)の錯体又はその付加物:
であり、式中、R1〜R18の各々は独立して、水素、C1〜C18アルキル、C1〜C18置換アルキル、C5〜C18シクロアルキル、C5〜C18置換シクロアルキル、C6〜C18アリール、C6〜C18置換アリール、又は不活性置換基であり、式中、1又はより多くのR1〜R18は、水素以外の場合、任意選択で少なくとも1つのヘテロ原子を含み;任意選択でR1〜R11の相互に隣接するいずれか2つ、R4−R5、及び/又はR7−R8は一緒になって置換又は未置換の、飽和又は不飽和の環構造の環を形成してもよく;またZはO、NR19、又はCR20R21であって、R19、R20、及びR21は、独立して、水素、C1〜C18アルキル、C1〜C18置換アルキル、C6〜C18アリール、C6〜C18置換アリール基、アルカリール基、アラルキル基であり、1又はより多くのR19、R20、及びR21は任意選択で少なくとも1つのヘテロ原子を含む。この触媒錯体において、Coはどのような価数又は酸化状態(例えば、+1、+2、又は+3)にあることもできる。
本発明によれば、式(I)のコバルト錯体は、ヒドロシリル化プロセス、及び/又は脱水素シリル化プロセスのための触媒として使用可能である。各々のプロセスは一般に、(a)シリルヒドリド化合物を、(b)少なくとも1つの不飽和官能基を有する不飽和化合物と反応させることを含む。
R24(OCH2CH2)z(OCH2CHR26)w−OR25;及び/又は
R25O(CHR26CH2O)w(CH2CH2O)z−CR27 2−C≡C−CR27 2(OCH2CH2)z(OCH2CHR26)wR25
を有するポリオキシアルキレンを含み、式中、R24は2から10の炭素原子を含む不飽和有機基、例えばアリル、メチルアリル、プロパルギル又は3−ペンチニルである。不飽和がオレフィン的である場合、それは望ましくは末端にあって、円滑なヒドロシリル化を容易にする。しかしながら、不飽和が三重結合である場合には、それは内部にあってよい。R25の各々は独立して、水素、ビニル、アリル、メタリル、又は1から8炭素原子のポリエーテル封鎖基、例えばアルキル基:CH3、n−C4H9、t−C4H9又はi−C8H17、CH3COO、t−C4H9COOのようなアシル基、CH3C(O)CH2C(O)Oのようなベータケトエステル基、又はトリアルキルシリル基である。R26及びR27はC1〜C20アルキル基のような1価の炭化水素基、例えばメチル、エチル、イソプロピル、2−エチルヘキシル、ドデシル及びステアリル、又はアリール基、例えばフェニル及びナフチル、又はアルカリール基、例えばベンジル、フェニルエチル及びノニルフェニル、又はシクロアルキル基、例えばシクロヘキシル及びシクロオクチルである。R27はまた水素であってよい。メチルは、R26及びR27基に特に適している。zの各々は0から100以下であり、wの各々は0から100以下である。1つの実施形態では、z及びwの値は1から50以下である。
空気及び水分の影響を受けやすい全ての操作は、標準的なシュレンク技術を用いて、又は精製窒素雰囲気を含んでいるMBraun社の不活性雰囲気ドライボックスを用いて行った。空気及び水分の影響を受けやすい操作のための溶媒は、溶媒用のシステムカラムを通過させることによって乾燥及び脱酸素し、ドライボックス中に4Åのモレキュラーシーブと共に格納した。ベンゼン-d6はCambridge IsotopeLaboratoriesから購入し、ナトリウムで乾燥し、ドライボックス中に4Åのモレキュラーシーブと共に格納した。2,2’;6’,2”-ターピリジン (terpy)配位子は、Strem社から入手し、高真空下で一夜乾燥し、ドライボックスに持ち込んだ。液体基質はLiAlH4又はCaH2で乾燥し、使用前に高真空で脱ガスした。
NMRスペクトルは、Varian社製INOVA-500又はBruker社製-500MHz分光計を用いて取得した。1HNMRスペクトルの化学シフト(δ)は1000000分の1(ppm)単位で与えられ、ベンゼン−d6の残留溶媒(7.16ppm)を参照とした。
アロキシジフェニルシランの合成は、Bergens, S. H.;Noheda, P.;Whelan, J.;Bosnich, B. J. Am. Chem. Soc. 1992, 114, 2121-2128記載の修正された文献手順に従い、空気中で行った。Et2O(250mL)中のアリルアルコール(2.9g,50mmol)とトリエチルアミン(5.1g,50mmol)の溶液をアイスバスで冷却した。迅速に撹拌しながら、この溶液にクロロジフェニルシラン(11g,50mmol)を滴下して処理した。大量のふわふわした白色の沈殿物(Et3NHCl)が直ちに観察された。この混合物を室温まで加温し、1時間にわたって撹拌した。得られた溶液をCelite(セライト)で濾過し、Et2Oで洗浄した。濾液を濃縮すると無色の油が生じ、これを蒸留すると(84-85℃, 65mmTorr)所望の生成物が無色の油として、80%の収率で得られた。1H NMR(400MHz, ベンゼン-d6)δ 7.74-7.62(m, 4H), 7.27-7.06(m, 6H), 5.81(ddt, J=17.1, 10.6, 4.6Hz,1H), 5.69(s, 1H), 5.31(dq, J=17.1, 1.8Hz, 1H), 5.00(dq, J=10.6, 1.8Hz, 1H),4.16(dt, J=4.6, 1.8Hz, 2H)。13C NMR(126MHz, C6D6)δ 136.73, 135.11, 134.31, 130.66, 128.39, 128.25, 128.06, 127.87,114.77, 65.60。
アロキシジメチルシラン、アロキシジフェニルシランと同様の方法で合成した。Et2O(250mL)中のアリルアルコール(2.9g,50mmol)とトリエチルアミン(5.1g,50mmol)の溶液をアイスバスで冷却した。迅速に撹拌しながら、この溶液にクロロジメチルシランを(4.7g,50mmol)を滴下添加した。大量のふわふわした白色の沈殿物(Et3NHCl)が直ちに観察された。この混合物を室温まで加温し、1時間にわたって撹拌した。得られた溶液をCelite(セライト)で濾過し、Et2Oで洗浄した。濾液を濃縮すると無色の油が生じ、これを分別蒸留すると(79-83℃)生成物が無色の油として、50%の収率で得られた。1H NMR(400MHz, クロロホルム-d)δ 5.93(ddt, J=17.2, 10.1, 5.0Hz, 1H),5.26(dq, J=17.2, 1.8Hz, 1H), 5.12(dq, J=10.4, 1.6Hz, 1H), 4.68-4.55(m, 1H),4.18(dt, J=5.0, 1.7Hz, 2H), 0.23(s, 3H), 0.23(s, 3H)。
ペンタン(20mL)中のpy2Co(CH2TMS)2(390mg,1mmol)の溶液を下記文献手順に従い調製し、−35℃で冷却した。Zhu, D.; Janssen, F. F. B. J.; Budzelaar, P. H. M. Organometallics2010, 29, 1897. ターピリジン配位子(233mg、1当量)を溶解し、コバルト化合物を含む溶液に添加した。直ちに緑から紫への色の変化が観察された。溶液は室温で0.5時間撹拌し、次いで減圧下で揮発成分を除去した。残存物をペンタンに溶解し、Celite(セライト)で濾過して(terpy)Co(CH2TMS)2を得た。Et2O中の(terpy)Co(CH2TMS)2の溶液をモノシリル錯体を生成するために4時間撹拌し、次いで−35℃で、トルエン/ペンタンから再結晶を行い、紫色の結晶を得られた。1H NMR (400 MHz, ベンゼン-d6) δ12.23 (d, J = 6.2 Hz, 3H), 8.64 (t, J = 7.6 Hz, 2H), 8.01 (t, J = 6.8 Hz, 2H),7.55 (d, J = 8.2 Hz, 2H), 7.02 (d, J = 7.5 Hz, 3H), 1.15 (s, 2H), -0.13 (d, J =5.0 Hz, 9H)
グローブボックスで、トルエン中の(terpy)Co(CH2TMS)(38mg,0.1mmol)の紫色溶液をアリルオキシジフェニルシラン(24mg,0.1mmol)と共に処理し、4時間撹拌した。紫色の溶液が添加に伴い観察された。溶液はCelite(セライト)で濾過して減圧下で濃縮した。得られた溶液にペンタンを積層させ、−35℃で2日間保存し、所望の生成物として同定された紫色の結晶が得られた。1H NMR (300 MHz, ベンゼン-d6) δ7.85 (dd, J = 7.7, 1.0 Hz, 1H), 7.75 - 7.57 (m, 3H), 7.34-6.74 (m, 11H),6.67-6.60 (m, 3H), 6.54 - 6.43 (m, 2H), 6.36 (td, J = 6.7, 1.5 Hz, 1H), 6.25(td, J = 6.5, 1.2 Hz, 1H), 5.47 (dd, J= 10.2, 6.8 Hz, 1H) (s, 1H), 4.43(t, J = 9.2 Hz, 1H), 3.95-4.12 (m, 1H) 3.24 - 3.12 (m, 1H), 2.77 (d, J = 12.5Hz, 1H). 13C NMR (126 MHz, C6D6) δ 149.65,148.17, 147.88, 145.19, 144.92, 144.51, 143.10, 139.71, 132.46, 132.11, 129.33,128.0, 127.8, 127.6, 127.14, 126.68, 125.94, 125.54, 119.82, 119.62, 119.40,119.01, 118.99, 117.81, 115.69, 74.94, 68.85, 56.32.
この化合物は、(terpy)Co(Ph2SiOC3H5)と同様の方法で調製された。グローブボックスで、トルエン中の(terpy)Co(CH2TMS)(38mg,0.1mmol)の紫色溶液をアリルオキシジメチルシラン(16mg,0.12mmol)と共に処理し、6時間撹拌した。紫色溶液と沈殿物の形成が観察された。固形物を濾過により分離し、トルエンに溶かしCelite(セライト)を通過させることにより精製した。得られた溶液にペンタンを積層させ、−35℃で1日間保存し、所望の生成物として同定された紫色の結晶が得られた。1H NMR (300 MHz, ベンゼン-d6) δ7.97 (dd, J = 8.0, 0.9 Hz, 1H), 7.86 (dd, J = 7.8, 0.9 Hz, 1H) 7.75 (d, J = 8.2Hz, 1H), 7.68 (d, J = 6.6 Hz, 1H), 7.64 (d, J = 8.3, 1H), 7.25 (t, J = 7.6 Hz,2H), 7.02 (d, J = 6.4 Hz, 1H), 6.93 - 6.75 (m, 2H), 5.27 (dd, J = 10.5, 6.2 Hz,1H), 4.25 (t, J = 10.4 Hz, 1H), 3.89-3.72 (m, 1H), 3.39 (dd, J = 9.2, 2.0 Hz,1H), 2.96 (dd, J = 12.4, 1.9 Hz, 1H), -0.37 (s, 3H), -1.11 (s, 3H).
グローブボックス中で、1−オクテン(112mg,1mmol)とトリエトキシシラン(164mg,1mmol)を、撹拌棒を備えたバイアル中に秤量した。固形のCo触媒(2−3mg,0.5mol%)を別のバイアル中に秤量し、次いで基質中に添加した。バイアルをキャップでシールし、撹拌した。1時間後、空気に曝露することによって反応を急冷した。生成混合物を、シリカゲルを介して濾過し、ヘキサンで溶出させた。生成混合物は、濾過より先にGCにより分析した。続いて、それを、一般的にフラッシュクロマトグラフィー用に使用されるシリカゲルのプラグ(Fluka(登録商標)高純度グレード、孔径60、粒径230−400メッシュ、粒径40−63μm)を通して濾過し、ヘキサンで溶出させた。得られた溶出液を真空下で乾燥し、1Hび13CNMR分光法によって分析した。収量は1−オクテンの添加に基づくものとする。
反応生成物は、上記と同じに同定した。n−オクチルトリエトキシシラン(生成物A)は、逆マルコフニコフヒドロシリル化生成物である。2−トリエトキシシリルオクタン(生成物B)は、マルコフニコフヒドロシリル化生成物である。生成物Cは、脱水素シリル化を経て生成されたアリルシラン(2−オクテニルトリエトキシシラン)である。オクタンは、生成物Cと等モル量生成される。
グローブボックス中で、1−オクテン(112mg,1mmol)とトリエトキシシラン(164mg,1mmol)を、撹拌棒を備えたバイアル中に秤量した。紫色の(terpy)Co(Ph2SiOC3H5)(2mg,0.5mol%)を別のバイアル中に秤量し、次いで基質と合わせた。バイアルを室温で1時間撹拌した。空気に曝露することによって反応を急冷した。反応混合物は上記の一般的な手順により処理した。GC及び1HNMR分光法は、逆マルコフニコフヒドロシリル化生成物の収率が>95%、及び脱水素シリル化生成物の収率が約2%であることを示した。
グローブボックス中で、1−オクテン(112mg,1mmol)とトリエトキシシラン(164mg,1mmol)を、撹拌棒を備えたバイアル中に秤量した。紫色の(terpy)Co(Me2SiOC3H5)(2mg,0.5mol%)を別のバイアル中に秤量し、次いで基質と合わせた。バイアルの内容物を室温で1時間撹拌した。空気に曝露することによって反応を急冷した。反応混合物は上記の一般的な手順により処理した。GC及び1HNMR分光法は、逆マルコフニコフヒドロシリル化生成物の収率が90%、及び脱水素シリル化生成物の収率が9%であることを示した。
撹拌棒を備えた50mLのシュレンクフラスコに、1−オクテン(112mg,1mmol)とトリエトキシシラン(164mg,1mmol)をグローブボックス中で入れた。このフラスコをガラスストッパーで封し、ボックスから取り出した。(terpy)Co(Ph2SiOC3H5)(2mg,0.5mol%)をバイアル中に充填し、ボックスから取り出して10分間空気に曝露した。アルゴン流下に、この固体触媒をシュレンクフラスコに添加した。フラスコをガラスストッパーで封し、1時間撹拌した。反応は空気に曝露することによって急冷した。反応混合物はGC及び1HNMR分光法によって分析し、逆マルコフニコフヒドロシリル化生成物の収率が>98%、及び脱水素シリル化生成物が痕跡量であることを確定した。
グローブボックス中、Momentiv社SL6100(1g)及びMomentiv社SL6020 D1(44mg)を、撹拌棒を備えたバイアル中に秤量した。紫色固体の(terpy)Co(Ph2SiOC3H5)(5mg,1mol%)(実施例9)又は(terpy)Co(Me2SiOC3H5)(4mg,1mol%)(実施例10)を別のバイアルに秤量し、次いで基質と合わせた。1時間、ゲルの生成が観察された。
Claims (41)
- 式:
を有し、式中、R1〜R18の各々は独立して、水素、C1〜C18アルキル、C1〜C18置換アルキル、C5〜C18シクロアルキル、C5〜C18置換シクロアルキル、C6〜C18アリール、C6〜C18置換アリール、又は不活性置換基であり、式中、1又はより多くのR1〜R18は、水素以外の場合、任意選択で少なくとも1つのヘテロ原子を含み;任意選択でR1〜R11の相互に隣接するいずれか2つ、R4−R5、及び/又はR7−R8は一緒になって置換又は未置換の、飽和又は不飽和の環構造の環を形成してもよく;またZはO、NR19、又はCR20R21であって、R19、R20、及びR21は、独立して、水素、C1〜C18アルキル、C1〜C18置換アルキル、C6〜C18アリール、C6〜C18置換アリール基、アルカリール基、アラルキル基であり、1又はより多くのR19、R20、及びR21は任意選択で少なくとも1つのヘテロ原子を含む、錯体。 - ZがOである、請求項1の錯体。
- R12及びR13が独立してC1〜C8の直鎖、分岐、若しくは環状アルキル、又はC6〜C18アリールから選択される、請求項2の錯体。
- R12及びR13がメチルであり、R14〜R18が水素である、請求項2の錯体。
- R12及びR13がフェニルであり、R14〜R18が水素である、請求項2の錯体。
- 錯体が支持体上に固定されている、請求項1〜7のいずれかの錯体。
- 支持体が、カーボン、シリカ、アルミナ、MgCl2、ジルコニア、ポリエチレン、ポリプロピレン、ポリスチレン、ポリ(アミノスチレン)、スルホン化ポリスチレン、又はこれらの2又はより多くの組み合わせから選択される、請求項8の錯体。
- R1、R2、R3、R4、R5、R6、R7、R8、R9、R10及び/又はR11の少なくとも1つが支持体と共有結合する官能基を含む、請求項8又は9の錯体。
- (a)少なくとも1つの不飽和官能基を有する不飽和化合物、(b)少なくとも1つのシリルヒドリド官能基を有するシリルヒドリド、及び(c)触媒を含む混合物を、任意選択的に溶媒の存在下で反応させて、シリル化生成物を生成することを含み、ここで触媒が式(I)の錯体又はその付加物:
であり、式中、R1〜R18の各々は独立して、水素、C1〜C18アルキル、C1〜C18置換アルキル、C5〜C18シクロアルキル、C5〜C18置換シクロアルキル、C6〜C18アリール、C6〜C18置換アリール、又は不活性置換基であり、式中、1又はより多くのR1〜R18は、水素以外の場合、任意選択で少なくとも1つのヘテロ原子を含み;任意選択でR1〜R11の相互に隣接するいずれか2つ、R4−R5、及び/又はR7−R8は一緒になって置換又は未置換の、飽和又は不飽和の環構造の環を形成してもよく;またZはO、NR19、又はCR20R21であって、R19、R20、及びR21は、独立して、水素、C1〜C18アルキル、C1〜C18置換アルキル、C6〜C18アリール、C6〜C18置換アリール基、アルカリール基、アラルキル基であり、1又はより多くのR19、R20、及びR21は任意選択で少なくとも1つのヘテロ原子を含む、シリル化生成物を生成するためのプロセス。 - ZがOである、請求項11のプロセス。
- R12及びR13が独立してC1〜C8の直鎖、分岐、若しくは環状アルキル、又はC6〜C18アリールから選択される、請求項12のプロセス。
- R12及びR13がメチルであり、R14〜R18が水素である、請求項12のプロセス。
- R12及びR13がフェニルであり、R14〜R18が水素である、請求項12のプロセス。
- シリル化生成物から錯体及び/又はその誘導体を除去することをさらに含む、請求項11〜17のいずれかのプロセス。
- シリル化生成物が、ヒドロシリル化生成物を含む、請求項11〜18のいずれかのプロセス。
- シリル化生成物が、脱水素シリル化生成物を含む、請求項11〜18のいずれかのプロセス。
- シリル化生成物が、(d)ヒドロシリル化生成物と、(e)脱水素シリル化生成物の混合物を含む、請求項11のプロセス。
- ヒドロシリル化生成物が、シリル化生成物の50.1%〜99.9%を占める、請求項21のプロセス。
- 脱水素シリル化生成物が、シリル基及び不飽和基を有するシラン又はシロキサンを含有し、不飽和基がシリル基に対してα位又はβ位にある、請求項20のプロセス。
- 不飽和化合物(a)が、直鎖又は分岐オレフィン;シクロアルケン;アルキル封鎖アリルポリエーテル;ビニル官能性アルキル封鎖アリル又はメタリルポリエーテル;アルキル封鎖末端不飽和アミン;アルキン;末端不飽和アクリレート又はメタクリレート;不飽和アリールエーテル;ビニル官能化ポリマー又はオリゴマー;ビニル官能化及び/又は末端不飽和アルケニル官能化シラン及び/又はシリコーン;不飽和脂肪酸;不飽和エステル;或いはこれらの2又はより多くの組み合わせから選択される、請求項11〜23のいずれかのプロセス。
- 錯体が支持体上に固定されている、請求項11〜24のいずれかのプロセス。
- 反応が不活性雰囲気下に行われる、請求項11〜25のいずれかのプロセス。
- 反応が、炭化水素、ハロゲン化炭化水素、エーテル、及びこれらの組み合わせからなる群より選択される溶媒の存在下に行われる、請求項11〜26のいずれかのプロセス。
- 反応が、−10℃から300℃の温度において行われる、請求項11〜27のいずれかのプロセス。
- 請求項11のプロセスによって生成される組成物であって、触媒又はその誘導体を含有する、組成物。
- シラン、シリコーン流体、架橋シリコーン、或いはこれらの2又はより多くの組み合わせから選択される少なくとも1つの成分を含む、請求項29の組成物。
- (a)少なくとも1つの不飽和官能基を有する不飽和化合物、(b)少なくとも1つのシリルヒドリド官能基を有するシリルヒドリドのヒドロシリル化反応物質を含有する組成物をヒドロシリル化するためのプロセスであって、ヒドロシリル化反応物質を含有する組成物を式:
の錯体と接触させることを含み、式中、R1〜R18の各々は独立して、水素、C1〜C18アルキル、C1〜C18置換アルキル、C5〜C18シクロアルキル、C5〜C18置換シクロアルキル、C6〜C18アリール、C6〜C18置換アリール、又は不活性置換基であり、式中、1又はより多くのR1〜R18は、水素以外の場合、任意選択で少なくとも1つのヘテロ原子を含み;任意選択でR1〜R11の相互に隣接するいずれか2つ、R4−R5、及び/又はR7−R8は一緒になって置換又は未置換の、飽和又は不飽和の環構造の環を形成してもよく;またZはO、NR19、又はCR20R21であって、R19、R20、及びR21は、独立して、水素、C1〜C18アルキル、C1〜C18置換アルキル、C6〜C18アリール、C6〜C18置換アリール基、アルカリール基、アラルキル基であり、1又はより多くのR19、R20、及びR21は任意選択で少なくとも1つのヘテロ原子を含む、プロセス。 - ZがOであり、R12及びR13が独立してC1〜C8の直鎖、分岐、又は環状アルキル、及びC6〜C18アリールから選択される、請求項31のプロセス。
- ZがOであり、R12及びR13が独立してメチル又はフェニルから選択される、請求項31のプロセス。
- ヒドロシリル化反応物質が、シラン又はシリコーンヒドリド流体、及び不飽和基質を含む、請求項31〜33のいずれかのプロセス。
- ヒドリド流体が、式:
R22 mSiHpX4−(m+p);
MaMH bDcDH dTeTH fQg;
R28 3Si(CHR28)xSiOSiR28 2(OSiR28 2)yOSiR28 2H;
R28 3Si(CHR28)xSiR28 2H
の化合物の1又は組み合わせ、或いはこれらの2又はより多くの組み合わせから選択され、式中、R22の各々は独立して、置換又は未置換の脂肪族又は芳香族ヒドロカルビル基;Xはハロゲン、アルコキシ、アシロキシ、又はシラザン;mは0〜3;pは1〜3、但しm+p≦4であり、4価のケイ素は保持され;Mは式R23 3SiO1/2の単官能基を表し;Dは式R23 2SiO2/2の2官能基を表し;Tは式R23SiO3/2の3官能基を表し;Qは式SiO4/2の4官能基を表し;MHはHR23 2SiO1/2を表し、THはHSiO3/2を表し、そしてDH基はR23HSiO2/2を表し;R24の各々は独立して、C1〜C18アルキル、C1〜C18置換アルキル、C6〜C14アリール又は置換アリールであり、R23は任意選択で少なくとも1つのヘテロ原子を含み;下付文字a、b、c、d、e、f、及びgはその化合物のモル質量が100と100,000ダルトンの間となる値;R28の各々は独立して、C1〜C18アルキル、C1〜C18置換アルキル、C6〜C14アリール又は置換アリール;xは1〜8、そしてyは0〜10である、請求項34のプロセス。 - 不飽和化合物が、不飽和ポリエーテル;ビニル官能化アルキル封鎖アリル又はメチルアリルポリエーテル;末端不飽和アミン;アルキン;C2〜C45オレフィン;不飽和エポキシド;末端不飽和アクリレート又はメチルアクリレート;不飽和アリールエーテル;不飽和芳香族炭化水素;不飽和シクロアルカン;ビニル官能化ポリマー又はオリゴマー;ビニル官能化及び/又末端不飽和アルケニル官能化シラン及び/又はシリコーン、或いはこれらの2又はより多くの組み合わせから選択される、請求項34又は35のプロセス。
- 反応が約−10℃から約200℃の温度で行われる、請求項31〜36のいずれかのプロセス。
- 反応が減圧下で行われる、請求項31〜37のいずれかのプロセス。
- 反応が過圧下で行われる、請求項31〜38のいずれかのプロセス。
- 錯体が支持体上に固定されている、請求項31〜39のいずれかのプロセス。
- 脱水素シリル化生成物が、成分(b)に由来する1又はより多くの末端シリル基を有する、請求項20のプロセス。
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US201361906204P | 2013-11-19 | 2013-11-19 | |
| US61/906,204 | 2013-11-19 | ||
| PCT/US2014/066348 WO2015077304A1 (en) | 2013-11-19 | 2014-11-19 | Cobalt catalysts and their use for hydrosilylation and dehydrogenative silylation |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2017501976A true JP2017501976A (ja) | 2017-01-19 |
| JP6486924B2 JP6486924B2 (ja) | 2019-03-20 |
Family
ID=52130810
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2016532098A Active JP6486924B2 (ja) | 2013-11-19 | 2014-11-19 | コバルト触媒並びにヒドロシリル化及び脱水素シリル化のためのその使用 |
Country Status (6)
| Country | Link |
|---|---|
| US (1) | US9381505B2 (ja) |
| EP (1) | EP3071585B1 (ja) |
| JP (1) | JP6486924B2 (ja) |
| CN (1) | CN105916869B (ja) |
| TW (1) | TW201524603A (ja) |
| WO (1) | WO2015077304A1 (ja) |
Families Citing this family (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US10717752B2 (en) * | 2015-07-24 | 2020-07-21 | Momentive Performance Materials Inc. | Dehydrogenative silylation, hydrosilylation and crosslinking using pyridinediimine cobalt carboxylate catalysts |
| FR3061183B1 (fr) * | 2016-12-23 | 2020-09-11 | Bluestar Silicones France | Compose du cobalt utile comme catalyseur d'hydrosilylation, de silylation deshydrogenante et de reticulation de compositions silicones |
| CN110465330B (zh) * | 2019-08-09 | 2022-06-10 | 杭州师范大学 | 一种利用钴催化剂的硅氢加成反应的方法 |
| TWI802750B (zh) * | 2019-09-16 | 2023-05-21 | 國立臺灣科技大學 | 矽化合物、其製備方法與鋰電池 |
| CN114409669B (zh) * | 2022-01-24 | 2023-06-23 | 云南民族大学 | 一种氧杂降冰片烯环上c-5位炔基取代的斑蝥素衍生物及其制备方法与应用 |
Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2012532885A (ja) * | 2009-07-10 | 2012-12-20 | モメンティブ パフォーマンス マテリアルズ インコーポレイテッド | ヒドロシリル化触媒 |
| JP2012532884A (ja) * | 2009-07-10 | 2012-12-20 | モメンティブ パフォーマンス マテリアルズ インコーポレイテッド | ヒドロシリル化触媒 |
| JP2013544824A (ja) * | 2010-11-24 | 2013-12-19 | モメンティブ パフォーマンス マテリアルズ インコーポレイテッド | ヒドロシリル化触媒として使用される三座窒素配位子を有する金属錯体のin−situ活性化 |
Family Cites Families (64)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US3296291A (en) | 1962-07-02 | 1967-01-03 | Gen Electric | Reaction of silanes with unsaturated olefinic compounds |
| US3159601A (en) | 1962-07-02 | 1964-12-01 | Gen Electric | Platinum-olefin complex catalyzed addition of hydrogen- and alkenyl-substituted siloxanes |
| US3220972A (en) | 1962-07-02 | 1965-11-30 | Gen Electric | Organosilicon process using a chloroplatinic acid reaction product as the catalyst |
| US3775452A (en) | 1971-04-28 | 1973-11-27 | Gen Electric | Platinum complexes of unsaturated siloxanes and platinum containing organopolysiloxanes |
| GB1476314A (en) | 1973-06-23 | 1977-06-10 | Dow Corning Ltd | Coating process |
| GB2013207B (en) | 1977-11-14 | 1982-10-27 | Spencer J L | Hydrosilylation catalysts |
| US4572971A (en) | 1983-03-25 | 1986-02-25 | Fairchild Camera And Instrument Corporation | Tri-state driver circuit for automatic test equipment |
| US4550152A (en) | 1983-10-28 | 1985-10-29 | General Electric Company | Nickel complex catalyst for hydrosilation reactions |
| US4578497A (en) | 1984-11-30 | 1986-03-25 | Gulf Research & Development Company | Tetraalkylsilane synthetic fluids |
| US4729821A (en) | 1986-11-03 | 1988-03-08 | Board Of Regents, The University Of Texas System | In situ activation of catalysts by applied electrical potentials |
| US4788312A (en) | 1988-03-16 | 1988-11-29 | Technolube Division Lubricating Specialties Co. | Trisilahydrocarbon lubricants |
| FR2641785B1 (fr) | 1989-01-19 | 1992-07-31 | Essilor Int | Composition de polymeres transparents pour lentilles de contact de type rigide, permeables a l'oxygene |
| US5026893A (en) | 1990-06-11 | 1991-06-25 | Lubricating Specialties Company | Polysilahydrocarbon lubricants |
| KR930703402A (ko) | 1990-12-13 | 1993-11-30 | 게리 리 그리스울드 | 방사선-활성화된 하이드로실릴화 반응 |
| JPH05295269A (ja) | 1991-11-29 | 1993-11-09 | General Electric Co <Ge> | 熱硬化性オルガノポリシロキサン組成物、予備生成済み潜伏性白金触媒およびそれの調製方法 |
| CA2080153A1 (en) | 1991-11-29 | 1993-05-30 | Chris A. Sumpter | Heat curable organopolysiloxane compositions, preformed latent platinum catalysts, and methods for making |
| US5880241A (en) | 1995-01-24 | 1999-03-09 | E. I. Du Pont De Nemours And Company | Olefin polymers |
| US5691435A (en) | 1996-01-25 | 1997-11-25 | Wacker-Chemie Gmbh | Crosslinkable compositions |
| US6417305B2 (en) | 1996-12-17 | 2002-07-09 | E. I. Du Pont De Nemours And Company | Oligomerization of ethylene |
| US6423848B2 (en) | 1996-12-17 | 2002-07-23 | E. I. Du Pont De Nemours And Company | Tridentate ligand |
| IL129929A0 (en) | 1996-12-17 | 2000-02-29 | Du Pont | Polymerization of ethylene with specific iron or cobalt complexes novel pyridinebis (imines) and novel complexes of pyridinebis(imines) with iron and cobalt |
| US6214761B1 (en) | 1996-12-17 | 2001-04-10 | E. I. Du Pont De Nemours And Company | Iron catalyst for the polymerization of olefins |
| US6432862B1 (en) | 1996-12-17 | 2002-08-13 | E. I. Du Pont De Nemours And Company | Cobalt catalysts for the polymerization of olefins |
| US6103946A (en) | 1997-07-15 | 2000-08-15 | E. I. Du Pont De Nemours And Company | Manufacture of α-olefins |
| KR100516336B1 (ko) | 1997-09-05 | 2005-09-22 | 비피 케미칼즈 리미티드 | 중합 촉매 |
| ID27209A (id) | 1998-03-12 | 2001-03-08 | Bp Chem Int Ltd | Katalis-katalis polimerisasi |
| JP2002506095A (ja) | 1998-03-12 | 2002-02-26 | ビーピー ケミカルズ リミテッド | エチレンのホモポリマー |
| CA2323477C (en) | 1998-03-12 | 2007-09-25 | Bp Chemicals Limited | Polymerization catalyst comprising a pyridine-bis(imine)complex |
| CA2323476A1 (en) | 1998-03-12 | 1999-09-16 | Bp Chemicals Limited | Polymerization catalyst comprising a pyridine-bis(imine) complex |
| US6297338B1 (en) | 1998-03-30 | 2001-10-02 | E. I. Du Pont De Nemours And Company | Polymerization of olefins |
| US7906451B2 (en) | 1998-03-30 | 2011-03-15 | E.I. Du Pont De Nemours And Company | Mixed polymerization catalyst component for polymerizing olefins |
| GB9819847D0 (en) | 1998-09-12 | 1998-11-04 | Bp Chem Int Ltd | Novel compounds |
| DE19856115A1 (de) | 1998-12-04 | 2000-06-21 | Wacker Chemie Gmbh | Alkenylgruppen aufweisende Siloxancopolymere |
| US6620895B1 (en) | 1999-03-22 | 2003-09-16 | E. I. Du Pont De Nemours And Company | Processing polyethylenes |
| US6281303B1 (en) | 1999-07-27 | 2001-08-28 | Eastman Chemical Company | Olefin oligomerization and polymerization catalysts |
| US6458905B1 (en) | 1999-08-16 | 2002-10-01 | Phillips Petroleum Company | Complexes of pyridldiimines with vanadium and other transition metals, and their use as olefin oligomerization and polymerization catalysts |
| US6278011B1 (en) | 1999-08-30 | 2001-08-21 | The University Of Dayton | Polysilahydrocarbons as lubricants for aerospace application |
| ES2265041T3 (es) | 2001-04-30 | 2007-02-01 | Ciba Specialty Chemicals Holding Inc. | Uso de compuestos de complejos metalicos como catalizadores de oxidacion. |
| WO2003042131A1 (en) | 2001-11-15 | 2003-05-22 | Stichting Voor De Technische Wetenschappen | Hydrogenation catalyst and catalysed hydrogenation process |
| EP1521758B1 (en) | 2002-07-17 | 2006-05-24 | Exxonmobil Chemical Patents Inc. | Late transition metal catalysts for olefin polymerization and oligomerization |
| DE60305715T2 (de) | 2002-09-25 | 2007-05-31 | Shell Internationale Research Maatschappij B.V. | Katalysatorsysteme für die ethylen-oligomerisierung zu linearen alpha-olefinen |
| EP1773895B1 (en) | 2004-07-09 | 2011-12-28 | E.I. Du Pont De Nemours And Company | Catalysts for olefin polymerization or oligomerization |
| US8062552B2 (en) | 2005-05-19 | 2011-11-22 | Brookhaven Science Associates, Llc | Electrocatalyst for oxygen reduction with reduced platinum oxidation and dissolution rates |
| CN100378111C (zh) | 2005-07-01 | 2008-04-02 | 中国科学院上海有机化学研究所 | 含碳氧醚键有机硅化合物、合成方法及其应用 |
| US7268096B2 (en) | 2005-07-21 | 2007-09-11 | Chevron Phillips Chemical Company Lp | Diimine metal complexes, methods of synthesis, and methods of using in oligomerization and polymerization |
| US7507775B2 (en) | 2005-10-13 | 2009-03-24 | Momentive Performance Materials Inc. | Hydrolysis resistant organomodified disiloxane surfactants |
| US8456733B2 (en) | 2005-10-26 | 2013-06-04 | Basf Se | Coloured particles for electrophoretic displays |
| DE102005057460A1 (de) | 2005-12-01 | 2007-06-06 | Wacker Chemie Ag | Zu hochfesten Elastomeren vernetzbare ionisch und/oder organometallisch funktionalisierte Siliconpolymere |
| US7429672B2 (en) | 2006-06-09 | 2008-09-30 | Momentive Performance Materials Inc. | Process for the direct synthesis of trialkoxysilane |
| US7259220B1 (en) | 2006-07-13 | 2007-08-21 | General Electric Company | Selective hydrosilylation method |
| US7696269B2 (en) | 2006-12-28 | 2010-04-13 | Momentive Performance Materials Inc. | Silated core polysulfides, their preparation and use in filled elastomer compositions |
| EP2643330B1 (en) * | 2010-11-24 | 2017-01-04 | Momentive Performance Materials Inc. | Metal-catalyzed mono-hydrosilylation of polyunsaturated compounds |
| US8637626B2 (en) | 2010-11-24 | 2014-01-28 | Momentive Performance Materials Inc. | Non-precious metal-containing 2,8-bis(imino)quinoline complexes and their use as hydrosilylation catalysts |
| US9394325B2 (en) * | 2011-08-19 | 2016-07-19 | The Trustees Of Princeton University | Enantiopure base-metal catalysts for asymmetric catalysis and bis(imino)pyridine iron alkyl complexes for catalysis |
| JP2014531446A (ja) | 2011-09-20 | 2014-11-27 | ダウ コーニング コーポレーションDow Corning Corporation | コバルト含有ヒドロシリル化触媒及びその触媒を含有する組成物 |
| EP2758408A1 (en) | 2011-09-20 | 2014-07-30 | Dow Corning Corporation | Metal containing hydrosilylation catalysts and compositions containing the catalysts |
| US9782763B2 (en) | 2011-12-14 | 2017-10-10 | Momentive Performance Materials Inc. | Non-precious metal-based hyrdosilylation catalysts exhibiting improved selectivity |
| US9447125B2 (en) | 2012-08-16 | 2016-09-20 | Momentive Performance Materials Inc. | Reusable homogeneous cobalt pyridine diimine catalysts for dehydrogenative silylation and tandem dehydrogenative-silylation-hydrogenation |
| US8927674B2 (en) | 2012-08-16 | 2015-01-06 | Princeton University | Dehydrogenative silylation and crosslinking using cobalt catalysts |
| US9371340B2 (en) | 2012-08-16 | 2016-06-21 | Momentive Performance Materials Inc. | Dehydrogenative silylation, hydrosilylation and crosslinking using cobalt catalysts |
| US9890182B2 (en) | 2013-05-06 | 2018-02-13 | Momentive Performance Materials Inc. | Selective 1,2-hydrosilylation of terminally unsaturated 1,3-dienes using iron catalysts |
| US9371339B2 (en) | 2013-05-06 | 2016-06-21 | Momentive Performance Materials Inc. | Saturated and unsaturated silahydrocarbons via iron and cobalt pyridine diimine catalyzed olefin silylation |
| EP2996804B1 (en) | 2013-05-15 | 2020-12-30 | Momentive Performance Materials Inc. | Activation of metal salts with silylhydrides and their use in hydrosilylation reactions |
| WO2015077302A1 (en) | 2013-11-19 | 2015-05-28 | Momentive Performance Materials Inc. | Cobalt catalysts and their use for hydrosilylation and dehydrogenative silylation |
-
2014
- 2014-11-19 WO PCT/US2014/066348 patent/WO2015077304A1/en active Application Filing
- 2014-11-19 EP EP14815500.5A patent/EP3071585B1/en active Active
- 2014-11-19 CN CN201480073587.7A patent/CN105916869B/zh active Active
- 2014-11-19 TW TW103140142A patent/TW201524603A/zh unknown
- 2014-11-19 US US14/547,661 patent/US9381505B2/en active Active
- 2014-11-19 JP JP2016532098A patent/JP6486924B2/ja active Active
Patent Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2012532885A (ja) * | 2009-07-10 | 2012-12-20 | モメンティブ パフォーマンス マテリアルズ インコーポレイテッド | ヒドロシリル化触媒 |
| JP2012532884A (ja) * | 2009-07-10 | 2012-12-20 | モメンティブ パフォーマンス マテリアルズ インコーポレイテッド | ヒドロシリル化触媒 |
| JP2013544824A (ja) * | 2010-11-24 | 2013-12-19 | モメンティブ パフォーマンス マテリアルズ インコーポレイテッド | ヒドロシリル化触媒として使用される三座窒素配位子を有する金属錯体のin−situ活性化 |
Non-Patent Citations (6)
| Title |
|---|
| BART, SUZANNE C. , ET AL., JOURNAL OF THE AMERICAN CHEMICAL SOCIETY, vol. 126(42), JPN6018022681, 2004, pages 13794 - 13807, ISSN: 0003818563 * |
| BLEEKE, JOHN R. , ET AL., ORGANOMETALLICS, vol. 26(16), JPN6018022686, 2007, pages 3904 - 3907, ISSN: 0003818568 * |
| LYONS, THOMAS W. , ET AL., CHEMISTRY A EUROPEAN JOURNAL, vol. 19(31), JPN6018022683, 2013, pages 10124 - 10127, ISSN: 0003818565 * |
| SISAK, ATTILA, JOURNAL OF ORGANOMETALLIC CHEMISTRY, vol. 586(1), JPN6018022684, 1999, pages 48 - 53, ISSN: 0003818566 * |
| WATANABE, TAKAHITO, ET AL., JOURNAL OF THE AMERICAN CHEMICAL SOCIETY, vol. 129(37), JPN6018022685, 2007, pages 11338 - 11339, ISSN: 0003818567 * |
| WHITE, ROSEMARY E. , ET AL., INORGANIC CHEMISTRY, vol. 45(17), JPN6018022682, 2006, pages 7004 - 7009, ISSN: 0003818564 * |
Also Published As
| Publication number | Publication date |
|---|---|
| CN105916869B (zh) | 2019-11-22 |
| WO2015077304A1 (en) | 2015-05-28 |
| EP3071585B1 (en) | 2018-11-07 |
| CN105916869A (zh) | 2016-08-31 |
| TW201524603A (zh) | 2015-07-01 |
| US20150141647A1 (en) | 2015-05-21 |
| EP3071585A1 (en) | 2016-09-28 |
| US9381505B2 (en) | 2016-07-05 |
| JP6486924B2 (ja) | 2019-03-20 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP6486925B2 (ja) | コバルト触媒並びにヒドロシリル化及び脱水素シリル化のためのその使用 | |
| US9381506B2 (en) | Cobalt catalysts and their use for hydrosilylation and dehydrogenative silylation | |
| KR101450080B1 (ko) | 하이드로실릴화 촉매 | |
| US9371340B2 (en) | Dehydrogenative silylation, hydrosilylation and crosslinking using cobalt catalysts | |
| JP6486924B2 (ja) | コバルト触媒並びにヒドロシリル化及び脱水素シリル化のためのその使用 | |
| US9447125B2 (en) | Reusable homogeneous cobalt pyridine diimine catalysts for dehydrogenative silylation and tandem dehydrogenative-silylation-hydrogenation | |
| JP6327426B2 (ja) | ヒドロシリル化反応触媒 | |
| WO2017126562A1 (ja) | 新規イソシアニド化合物及びヒドロシリル化反応触媒 | |
| EP3590596B1 (en) | Catalyst for hydrosilylation reaction, hydrogenation reaction, and hydrosilane reduction reaction | |
| US20180334470A1 (en) | Dialkyl cobalt catalysts and their use for hydrosilylation and dehydrogenative silylation | |
| WO2015192029A1 (en) | Platinum catalyzed hydrosilylation reactions utilizing cyclodiene additives | |
| JP6389297B2 (ja) | コバルト触媒を用いる脱水素シリル化および架橋 | |
| EP3071583B1 (en) | Dehydrogenative silylation, hydrosilylation and crosslinking using cobalt catalysts |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20171010 |
|
| A977 | Report on retrieval |
Free format text: JAPANESE INTERMEDIATE CODE: A971007 Effective date: 20180614 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20180619 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20180914 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20181116 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20190205 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20190220 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 6486924 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |