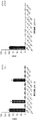JP2016523973A - 疾患の処置のためのキナーゼ阻害物質 - Google Patents
疾患の処置のためのキナーゼ阻害物質 Download PDFInfo
- Publication number
- JP2016523973A JP2016523973A JP2016525463A JP2016525463A JP2016523973A JP 2016523973 A JP2016523973 A JP 2016523973A JP 2016525463 A JP2016525463 A JP 2016525463A JP 2016525463 A JP2016525463 A JP 2016525463A JP 2016523973 A JP2016523973 A JP 2016523973A
- Authority
- JP
- Japan
- Prior art keywords
- cancer
- alkyl
- substituted
- compound according
- disease
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
- 0 CC(N(*)C(*=C(**)*=C(*)*)=C)=O Chemical compound CC(N(*)C(*=C(**)*=C(*)*)=C)=O 0.000 description 8
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D239/00—Heterocyclic compounds containing 1,3-diazine or hydrogenated 1,3-diazine rings
- C07D239/02—Heterocyclic compounds containing 1,3-diazine or hydrogenated 1,3-diazine rings not condensed with other rings
- C07D239/24—Heterocyclic compounds containing 1,3-diazine or hydrogenated 1,3-diazine rings not condensed with other rings having three or more double bonds between ring members or between ring members and non-ring members
- C07D239/28—Heterocyclic compounds containing 1,3-diazine or hydrogenated 1,3-diazine rings not condensed with other rings having three or more double bonds between ring members or between ring members and non-ring members with hetero atoms or with carbon atoms having three bonds to hetero atoms with at the most one bond to halogen, directly attached to ring carbon atoms
- C07D239/46—Two or more oxygen, sulphur or nitrogen atoms
- C07D239/48—Two nitrogen atoms
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/495—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with two or more nitrogen atoms as the only ring heteroatoms, e.g. piperazine or tetrazines
- A61K31/505—Pyrimidines; Hydrogenated pyrimidines, e.g. trimethoprim
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/495—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with two or more nitrogen atoms as the only ring heteroatoms, e.g. piperazine or tetrazines
- A61K31/505—Pyrimidines; Hydrogenated pyrimidines, e.g. trimethoprim
- A61K31/506—Pyrimidines; Hydrogenated pyrimidines, e.g. trimethoprim not condensed and containing further heterocyclic rings
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/495—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with two or more nitrogen atoms as the only ring heteroatoms, e.g. piperazine or tetrazines
- A61K31/505—Pyrimidines; Hydrogenated pyrimidines, e.g. trimethoprim
- A61K31/517—Pyrimidines; Hydrogenated pyrimidines, e.g. trimethoprim ortho- or peri-condensed with carbocyclic ring systems, e.g. quinazoline, perimidine
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/495—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with two or more nitrogen atoms as the only ring heteroatoms, e.g. piperazine or tetrazines
- A61K31/505—Pyrimidines; Hydrogenated pyrimidines, e.g. trimethoprim
- A61K31/519—Pyrimidines; Hydrogenated pyrimidines, e.g. trimethoprim ortho- or peri-condensed with heterocyclic rings
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/535—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with at least one nitrogen and one oxygen as the ring hetero atoms, e.g. 1,2-oxazines
- A61K31/5375—1,4-Oxazines, e.g. morpholine
- A61K31/5377—1,4-Oxazines, e.g. morpholine not condensed and containing further heterocyclic rings, e.g. timolol
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K45/00—Medicinal preparations containing active ingredients not provided for in groups A61K31/00 - A61K41/00
- A61K45/06—Mixtures of active ingredients without chemical characterisation, e.g. antiphlogistics and cardiaca
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P1/00—Drugs for disorders of the alimentary tract or the digestive system
- A61P1/04—Drugs for disorders of the alimentary tract or the digestive system for ulcers, gastritis or reflux esophagitis, e.g. antacids, inhibitors of acid secretion, mucosal protectants
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P1/00—Drugs for disorders of the alimentary tract or the digestive system
- A61P1/16—Drugs for disorders of the alimentary tract or the digestive system for liver or gallbladder disorders, e.g. hepatoprotective agents, cholagogues, litholytics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P11/00—Drugs for disorders of the respiratory system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P11/00—Drugs for disorders of the respiratory system
- A61P11/06—Antiasthmatics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P13/00—Drugs for disorders of the urinary system
- A61P13/12—Drugs for disorders of the urinary system of the kidneys
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P17/00—Drugs for dermatological disorders
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P17/00—Drugs for dermatological disorders
- A61P17/02—Drugs for dermatological disorders for treating wounds, ulcers, burns, scars, keloids, or the like
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P17/00—Drugs for dermatological disorders
- A61P17/06—Antipsoriatics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P19/00—Drugs for skeletal disorders
- A61P19/02—Drugs for skeletal disorders for joint disorders, e.g. arthritis, arthrosis
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P19/00—Drugs for skeletal disorders
- A61P19/08—Drugs for skeletal disorders for bone diseases, e.g. rachitism, Paget's disease
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P19/00—Drugs for skeletal disorders
- A61P19/08—Drugs for skeletal disorders for bone diseases, e.g. rachitism, Paget's disease
- A61P19/10—Drugs for skeletal disorders for bone diseases, e.g. rachitism, Paget's disease for osteoporosis
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P21/00—Drugs for disorders of the muscular or neuromuscular system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/02—Drugs for disorders of the nervous system for peripheral neuropathies
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/04—Centrally acting analgesics, e.g. opioids
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/14—Drugs for disorders of the nervous system for treating abnormal movements, e.g. chorea, dyskinesia
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/14—Drugs for disorders of the nervous system for treating abnormal movements, e.g. chorea, dyskinesia
- A61P25/16—Anti-Parkinson drugs
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/28—Drugs for disorders of the nervous system for treating neurodegenerative disorders of the central nervous system, e.g. nootropic agents, cognition enhancers, drugs for treating Alzheimer's disease or other forms of dementia
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P29/00—Non-central analgesic, antipyretic or antiinflammatory agents, e.g. antirheumatic agents; Non-steroidal antiinflammatory drugs [NSAID]
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
- A61P31/04—Antibacterial agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
- A61P31/12—Antivirals
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
- A61P31/12—Antivirals
- A61P31/14—Antivirals for RNA viruses
- A61P31/16—Antivirals for RNA viruses for influenza or rhinoviruses
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
- A61P31/12—Antivirals
- A61P31/14—Antivirals for RNA viruses
- A61P31/18—Antivirals for RNA viruses for HIV
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
- A61P31/12—Antivirals
- A61P31/20—Antivirals for DNA viruses
- A61P31/22—Antivirals for DNA viruses for herpes viruses
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P33/00—Antiparasitic agents
- A61P33/02—Antiprotozoals, e.g. for leishmaniasis, trichomoniasis, toxoplasmosis
- A61P33/06—Antimalarials
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
- A61P35/02—Antineoplastic agents specific for leukemia
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
- A61P35/04—Antineoplastic agents specific for metastasis
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P37/00—Drugs for immunological or allergic disorders
- A61P37/02—Immunomodulators
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P37/00—Drugs for immunological or allergic disorders
- A61P37/08—Antiallergic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P43/00—Drugs for specific purposes, not provided for in groups A61P1/00-A61P41/00
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P7/00—Drugs for disorders of the blood or the extracellular fluid
- A61P7/02—Antithrombotic agents; Anticoagulants; Platelet aggregation inhibitors
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P9/00—Drugs for disorders of the cardiovascular system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P9/00—Drugs for disorders of the cardiovascular system
- A61P9/04—Inotropic agents, i.e. stimulants of cardiac contraction; Drugs for heart failure
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P9/00—Drugs for disorders of the cardiovascular system
- A61P9/10—Drugs for disorders of the cardiovascular system for treating ischaemic or atherosclerotic diseases, e.g. antianginal drugs, coronary vasodilators, drugs for myocardial infarction, retinopathy, cerebrovascula insufficiency, renal arteriosclerosis
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P9/00—Drugs for disorders of the cardiovascular system
- A61P9/12—Antihypertensives
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D401/00—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom
- C07D401/02—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom containing two hetero rings
- C07D401/12—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom containing two hetero rings linked by a chain containing hetero atoms as chain links
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D403/00—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00
- C07D403/02—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00 containing two hetero rings
- C07D403/12—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00 containing two hetero rings linked by a chain containing hetero atoms as chain links
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D405/00—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom
- C07D405/02—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom containing two hetero rings
- C07D405/12—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom containing two hetero rings linked by a chain containing hetero atoms as chain links
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D405/00—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom
- C07D405/14—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom containing three or more hetero rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D409/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having sulfur atoms as the only ring hetero atoms
- C07D409/02—Heterocyclic compounds containing two or more hetero rings, at least one ring having sulfur atoms as the only ring hetero atoms containing two hetero rings
- C07D409/12—Heterocyclic compounds containing two or more hetero rings, at least one ring having sulfur atoms as the only ring hetero atoms containing two hetero rings linked by a chain containing hetero atoms as chain links
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D409/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having sulfur atoms as the only ring hetero atoms
- C07D409/14—Heterocyclic compounds containing two or more hetero rings, at least one ring having sulfur atoms as the only ring hetero atoms containing three or more hetero rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D471/00—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, at least one ring being a six-membered ring with one nitrogen atom, not provided for by groups C07D451/00 - C07D463/00
- C07D471/02—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, at least one ring being a six-membered ring with one nitrogen atom, not provided for by groups C07D451/00 - C07D463/00 in which the condensed system contains two hetero rings
- C07D471/04—Ortho-condensed systems
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D487/00—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, not provided for by groups C07D451/00 - C07D477/00
- C07D487/02—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, not provided for by groups C07D451/00 - C07D477/00 in which the condensed system contains two hetero rings
- C07D487/04—Ortho-condensed systems
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y02—TECHNOLOGIES OR APPLICATIONS FOR MITIGATION OR ADAPTATION AGAINST CLIMATE CHANGE
- Y02A—TECHNOLOGIES FOR ADAPTATION TO CLIMATE CHANGE
- Y02A50/00—TECHNOLOGIES FOR ADAPTATION TO CLIMATE CHANGE in human health protection, e.g. against extreme weather
- Y02A50/30—Against vector-borne diseases, e.g. mosquito-borne, fly-borne, tick-borne or waterborne diseases whose impact is exacerbated by climate change
Abstract
Description
本出願は2013年7月9日出願の米国特許仮出願第61/844,304号および2013年11月8日出願の米国特許仮出願第61/901,808号の優先権および恩典を主張し、いずれもその内容が全体として参照により本明細書に組み入れられる。
肺がんは、米国内の男性および女性の両方におけるがん関連死の最も一般的な原因である(Jemal, A., Cancer Statistics, 2007, CA Cancer J. Clin. 2007; 57: 43-66(非特許文献1))。患者の大部分(80%)は、非小細胞肺がん(NSCLC)を有し、現在利用可能な治療法では治癒不可能な進行期肺がんを呈する。進行期NSCLC患者では化学療法が処置の頼みの綱であり、化学療法は生存期間中央値8〜10ヶ月を伴う。これらの数字は過去25年間ほとんど変わっていない。
式中、X1、X2、X3a、X3b、X4、X5、Y、Z1、Z2、Z3、Q、およびnはそれぞれ、本明細書において定義または説明される化学部分の様々な群より選択される。
定義
本発明においては以下の定義を使用する(別途明示されない限り)。
本発明は、新規化合物およびそれらの使用に関する。本発明は、本発明の化合物の合成に関する。
式中、
Z1はNまたはCR1であり;
Z2はNまたはCR2であり;
Z3はNまたはCR3であるが、但し、YがNR4である場合、Z1、Z2、またはZ3のうち2つはNであり;
R1はH、C1〜C8アルキル、ハロゲン、またはハロ(C1〜C8アルキル)であり;
R2はH、C1〜C8アルキル、ハロゲン、またはハロ(C1〜C8アルキル)であり;
X2はOまたはNR10であり;
R10は水素またはC1〜C8アルキルであるか、
あるいは、Z2がCR2でありかつX2がNR10である場合、R2およびR10は一緒になって6員複素環を形成することができ、ここで該複素環は1個または複数のR28で置換されていてもよく;
R3はH、C1〜C8アルキル、ハロゲン、またはハロ(C1〜C8アルキル)であり;
YはNR4であるか、
あるいは、Y-X4およびR3は一緒になって非置換もしくは置換C6アリールまたは非置換もしくは置換の5員もしくは6員ヘテロアリールを形成し、ここで該置換アリールまたは該置換ヘテロアリールは1個または複数のR5で置換されており;
R4はHまたはC1〜C8アルキルであり;
各R5は独立して、ハロゲン、OR6、NR7R8、NR7C(O)R8、SR9、C1〜C8アルキル、5員複素環もしくは6員複素環で置換されていてもよいC2〜C8アルキニル、またはハロ(C1〜C8アルキル)であり;
各R6は独立して水素またはC1〜C8アルキルであり;
各R7およびR8は独立して、水素、C1〜C8アルキル、または非置換もしくは置換の5員もしくは6員複素環であり、ここで該置換複素環は1個または複数のR16で置換されており;
各R9は独立して水素またはC1〜C8アルキルであり;
X1はH、C1〜C8アルキル、またはハロゲンであり;
各X3aおよびX3bは独立して水素、C1〜C8アルキル、または非存在(nが0である場合)であり;
QはC1〜C8アルキル、非置換もしくは置換C6〜C10アリール、非置換もしくは置換の5員もしくは6員ヘテロアリール、非置換もしくは置換3員〜8員シクロアルキル、または非置換もしくは置換3員〜8員複素環であり、ここで該置換アリール、該置換ヘテロアリール、該置換シクロアルキル、または該置換複素環は1個または複数のR11で置換されており;
各R11は独立して、ハロゲン、OR12、NR13R14、SR15、C1〜C8アルキル、またはハロ(C1〜C8アルキル)であり;
各R12は独立して水素またはC1〜C8アルキルであり;
各R13およびR14は独立して水素またはC1〜C8アルキルであり;
各R15は独立して水素またはC1〜C8アルキルであり;
nは0、1、2、3、または4であり;
X4は非置換もしくは置換C6〜C10アリール、非置換もしくは置換の5員もしくは6員ヘテロアリール、非置換もしくは置換C1〜C8アルキル、または非置換もしくは置換(CH2)1〜3-C6〜C10アリールであり、
ここで該置換アリール、該置換ヘテロアリール、または該置換アルキルは1個または複数のR16で置換されており;
各R16は独立して、ハロゲン、OR17、NR18R19、SR20、非置換もしくは置換C1〜C8アルキル、ハロ(C1〜C8アルキル)、C(O)(C1〜C8アルキル)、C(O)(ハロ(C1〜C8アルキル))、C(O)(C2〜C8アルケニル)、非置換もしくは置換複素環、またはC(O)-非置換もしくはC(O)-置換複素環であり、ここで該置換アルキルまたは該置換複素環は1個または複数のR21で置換されており;
各R17は独立して水素またはC1〜C8アルキルであり;
各R18およびR19は独立して、水素、C1〜C8アルキル、C(O)(C1〜C8アルキル)、C(O)(C2〜C8アルケニル)、またはC(O)-非置換もしくはC(O)-置換複素環であり、ここで該アルキルまたは該アルケニルは、1個または複数のOH、CN、ハロゲン、C3〜C8シクロアルキル、O(C1〜C8アルキル)、NH2、NH(C1〜C8アルキル)、またはN(C1〜C8アルキル)2で置換されていてもよく、かつここで該置換複素環は1個または複数のR21で置換されており;
各R20は独立して水素またはC1〜C8アルキルであり;
各R21はC1〜C8アルキル、C(O)(C1〜C8アルキル)、C(O)(C2〜C8アルケニル)、または複素環であり;
X5は、非置換もしくは置換C6〜C10アリール、非置換もしくは置換5員〜8員ヘテロアリール、または非置換もしくは置換C1〜C8アルキルであり、ここで該置換アリール、該置換ヘテロアリール、または該置換アルキルは1個または複数のR22で置換されており;
各R22は独立して、ハロゲン、OR23、NR24R25、SR26、C1〜C8アルキル、ハロ(C1〜C8アルキル)、C(O)(C1〜C8アルキル)、C(O)(C2〜C8アルケニル)、非置換もしくは置換複素環、非置換もしくは置換C6〜C10アリール、またはC(O)-非置換もしくはC(O)-置換複素環であり、ここで該置換複素環または該置換アリールは1個または複数のR27で置換されているか、
あるいは、2個またはそれ以上のR22は、それらが結合している原子と一緒になって、非置換もしくは置換3員〜8員シクロアルキル、または非置換もしくは置換5員〜6員複素環を形成し、ここで該シクロアルキルまたは該複素環は1個または複数のR27で置換されており;
各R23は独立して水素またはC1〜C8アルキルであり;
各R24およびR25は独立して、水素、C1〜C8アルキル、C(O)(C1〜C8アルキル)、またはC(O)(C2〜C8アルケニル)であり、ここで該アルキルまたは該アルケニルは、1個または複数のOH、CN、ハロゲン、C3〜C8シクロアルキル、O(C1〜C8アルキル)、NH2、NH(C1〜C8アルキル)、またはN(C1〜C8アルキル)2で置換されていてもよく;
各R26は独立して水素またはC1〜C8アルキルであり;
各R27はハロゲン、C1〜C8アルキル、C(O)(C1〜C8アルキル)、C(O)(C2〜C8アルケニル)、NR29C(O)(C1〜C8アルキル)、またはNR29C(O)(C2〜C8アルケニル)であり;
各R28はハロゲン、C1〜C8アルキル、またはハロ(C1〜C8アルキル)であるか、
あるいは、2個のR28およびそれらが結合している炭素が一緒になってC=Oを形成し; かつ
各R29は水素またはC1〜C8アルキルである。
式中、sは1、2、3、または4であり、かつtは0、1、または2であり、かつR4、R5、R28、X1、Y、X2、X3a、X3b、Q、n、X4、およびX5は、式Iについて定義の通りである。
式中、uは0、1、2、3、4、または5であり、かつR16、X1、X2、X3a、X3b、Q、n、およびX5は、式Iについて定義の通りである。
式中、R16、R17、X1、X2、X3a、X3b、Q、n、およびX5は、式Iについて定義の通りである。
式中、R16、R17、X1、X2、X3a、X3b、Q、n、X5、およびR17は式Iについて定義の通りである。
式中、wは0、1、または2であり、かつR22、X1、X2、X3a、X3b、Q、n、およびX4は式Iについて定義の通りである。
本発明は、本発明の化合物の使用のための方法に関する。本発明の化合物は有用な薬理活性スペクトルを有し、したがって疾患の予防および/または処置に特に好適である。
本発明は、本発明の化合物または薬学的に許容されるその塩を薬学的に許容される担体と共に含む、薬学的組成物を提供する。
一般
尿素形成をBiotage(登録商標)Initiator+マイクロ波合成装置を使用して行った。すべての反応を、0.25mm E. Merckプレコーティングシリカゲルプレート(60 F254)を用いる薄層クロマトグラフィー(TLC)、ならびにSunFire(商標)C18カラム(4.6×50mm、粒径5μm)を使用するWaters LCMSシステム(Waters 2489紫外/可視検出器、Waters 3100質量検出器、Waters 515 HPLCポンプ、Waters 2545バイナリーグラジエントモジュール、Waters試薬マネージャー、およびWaters 2767試料マネージャー)によってモニタリングした: 溶媒勾配 = 0分で100% A、5分で1% A; 溶媒A = 水中0.035% TFA; 溶媒B = MeOH中0.035% TFA; 流量: 2.5mL/分。反応生成物の精製を、Teledyne Isco RediSep(登録商標)Rf高性能ゴールドカラムまたはSilicycle SiliaSep(商標)高性能カラム(4g、12g、24g、40g、または80g)付きCombiFlash(登録商標)Rfを使用するフラッシュクロマトグラフィー、およびSunFire(商標)分取C18カラム(19×50mm、粒径5μm)を使用するWaters LCMSシステムによって行った: 溶媒勾配 = 0分で80% A、8分で10% A; 溶媒A = 水中0.035% TFA; 溶媒B = MeOH中0.035% TFA; 流量: 25mL/分。すべての化合物の純度は95%超であり、Waters LCMSシステムによって分析された。1H NMRおよび13C NMRスペクトルをVarian Inova-600(1Hで600MHz、13Cで125MHz)分光計を使用して得た。1H NMRでのクロロホルム(δ = 7.24)に対する化学シフト、または1H NMRでのジメチルスルホキシド(δ = 2.50)に対する化学シフト、および13C NMRでのジメチルスルホキシド(δ = 39.51)に対する化学シフトが報告される。データは(br = ブロード、s = 一重項、d = 二重項、t = 三重項、q = 四重項、m = 多重項)として報告される。
A. 6-クロロ-N-(3-ニトロフェニル)ピリミジン-4-アミン
4,6-ジクロロピリミジン(2.0g、13.52mmol)の2-プロパノール(34mL)溶液に3-ニトロアニリン(1.86g、13.52mmol)およびジオキサン中4N HCl(3.38ml、13.52mmol)を加えた。反応混合物を80℃で24時間攪拌し、溶媒の当初量の半分に減圧濃縮した。反応混合物に水(150mL)を加え、得られた析出物を濾取した。固体を窒素ガスを使用して送風により乾燥させて6-クロロ-N-(3-ニトロフェニル)ピリミジン-4-アミン(2.3g、収率68%)を明黄色固体として得た。保持時間 = 4.15分;
。
6-クロロ-N-(3-ニトロフェニル)ピリミジン-4-アミン(1.0g、4.00mmol)の2-ブタノール(10mL)およびトリフルオロ酢酸(0.3mL)溶液に2-メトキシ-4-(4-メチルピペラジン-1-イル)アニリン(606mg、4.39mmol)を加えた。反応混合物を120℃で10時間攪拌し、溶媒を減圧濃縮した。反応混合物をジクロロメタンで希釈し、飽和炭酸カリウム水溶液およびブラインで洗浄した。有機層をMgSO4で乾燥させ、セライトパッドを通じて濾過し、減圧濃縮した。残渣をシリカゲル上でのカラムクロマトグラフィー(1:99〜3:97、アンモニアのメタノール中7.0N溶液/ジクロロメタン)で精製してN4-(2-メトキシ-4-(4-メチルピペラジン-1-イル)フェニル)-N6-(3-ニトロフェニル)ピリミジン-4,6-ジアミン(1.3g、収率75%)を固体として得た。保持時間 = 2.73分;
。
5mLマイクロ波バイアルにN4-(2-メトキシ-4-(4-メチルピペラジン-1-イル)フェニル)-N6-(3-ニトロフェニル)ピリミジン-4,6-ジアミン(200mg、0.46mmol)、フェニルイソシアネート(164mg、1.38mmol)、およびトルエン(2mL)を添加した。反応バイアルを密封し、130℃で1時間加熱した。反応バイアルにフェニルイソシアネート(109mg、2.35mmol)をさらに加え、130℃で1時間加熱した。反応混合物を減圧濃縮した。残渣をシリカゲル上でのカラムクロマトグラフィー(1:99〜7:93、メタノール/ジクロロメタン)で精製し、HPLCを使用してさらに精製して保持時間 = 3.78分; MS m/z: 555.41 [M+1]の帯黄白色固体としての1-(6-((2-メトキシ-4-(4-メチルピペラジン-1-イル)フェニル)アミノ)ピリミジン-4-イル)-1-(3-ニトロフェニル)-3-フェニル尿素(90mg、収率35%)および保持時間 = 4.17分; MS m/z: 555.41 [M+1]の帯黄白色固体としての1-(2-メトキシ-4-(4-メチルピペラジン-1-イル)フェニル)-1-(6-((3-ニトロフェニル)アミノ)ピリミジン-4-イル)-3-フェニル尿素(70mg、収率27%)を得た。
1-(6-((2-メトキシ-4-(4-メチルピペラジン-1-イル)フェニル)アミノ)ピリミジン-4-イル)-1-(3-ニトロフェニル)-3-フェニル尿素(80mg、0.14mmol)の酢酸エチル(1mL)および濃HCl(0.1mL)溶液に塩化スズ(II)二水和物(162mg、0.76mmol)を加えた。反応混合物を60℃で6時間攪拌した。反応混合物を酢酸エチルで希釈し、飽和NaHCO3溶液で中和した。有機層をMgSO4で乾燥させ、セライトパッドを通じて濾過し、減圧濃縮した。粗生成物をさらに精製せずに次の反応に使用した。保持時間 = 3.45分; MS m/z: 525.55 [M+1]。
1-(3-アミノフェニル)-1-(6-((2-メトキシ-4-(4-メチルピペラジン-1-イル)フェニル)アミノ)ピリミジン-4-イル)-3-フェニル尿素(60mg、0.11mmol)のTHF(1mL)および飽和NaHCO3溶液(1mL)中溶液に塩化アクリロイル(10μl、0.13mmol)を0℃で加えた。反応混合物を0℃で30分間攪拌した。反応混合物を酢酸エチルと水との間で分配した。水層を酢酸エチルで抽出し、一緒にした有機層をブラインで洗浄した。有機層をMgSO4で乾燥させ、セライトパッドを通じて濾過し、減圧濃縮した。残渣をシリカゲル上でのカラムクロマトグラフィー(1:99〜10:90、メタノール/ジクロロメタン)で精製してN-(3-(1-(6-((2-メトキシ-4-(4-メチルピペラジン-1-イル)フェニル)アミノ)ピリミジン-4-イル)-3-フェニルウレイド)フェニル)アクリルアミド(42mg、収率63%)を帯黄白色固体として得た。保持時間 = 3.73分;
。
1-(2-メトキシ-4-(4-メチルピペラジン-1-イル)フェニル)-1-(6-((3-ニトロフェニル)アミノ)ピリミジン-4-イル)-3-フェニル尿素から出発して実施例1 DおよびEに関して記載のようにN-(3-((6-(1-(2-メトキシ-4-(4-メチルピペラジン-1-イル)フェニル)-3-フェニルウレイド)ピリミジン-4-イル)アミノ)フェニル)アクリルアミドを調製した。保持時間 = 3.96分;
。
A. tert-ブチル (2-メトキシ-4-(4-メチルピペラジン-1-イル)フェニル)カルバメート
2-メトキシ-4-(4-メチルピペラジン-1-イル)アニリン(10g、45.2mmol)のトルエン(230mL)溶液に二炭酸ジ-tert-ブチル(9.87g、45.2mmol)を加えた。反応混合物を120℃で6時間攪拌し、減圧濃縮した。残渣をシリカゲル上でのカラムクロマトグラフィー(3:97〜10:90、アンモニアのメタノール中7.0N溶液/ジクロロメタン)で精製して標記化合物(12.5g、収率86%)を得た。保持時間 = 3.23分;
。
tert-ブチル (2-メトキシ-4-(4-メチルピペラジン-1-イル)フェニル)カルバメート(10g、31.1mmol)の無水THF(160mL)溶液にNaH(1.9g、46.7mmol)を0℃で加えた。30分後、4,6-ジクロロピリミジン(6.9g、46.7mmol)を反応混合物に0℃で加えた。反応混合物を60℃に6時間加熱した後、それを室温に冷却し、水で反応停止させた。残留THFを減圧濃縮した後、水(200mL)を反応混合物に加えた。残渣をEtOH(15mL)で2時間摩砕した。生成された固体を濾過し、水で洗浄した。生成物を乾燥させて褐色固体(10.2g、収率76%)を得た。保持時間 = 3.65分;
。
tert-ブチル (6-クロロピリミジン-4-イル)(2-メトキシ-4-(4-メチルピペラジン-1-イル)フェニル)カルバメート(10.0g、23.08mmol)、3-ニトロアニリン(6.37g、46.17mmol)、K2CO3(9.6g、69.25mmol)の2-ブタノール(230mL)中混合物を10分間脱気した。反応混合物にPd2(dba)3(1.26g、1.39mmol)およびX-phos(990mg、2.08mmol)を加え、120℃で6時間加熱した後、それをセライトパッドで濾過し、減圧濃縮した。残渣をシリカゲル上でのカラムクロマトグラフィー(3:97〜10:90、アンモニアのメタノール中7.0N溶液/ジクロロメタン)で精製して標記化合物(10.3g、収率83%)を得た。保持時間 = 3.70分;
。
tert-ブチル (2-メトキシ-4-(4-メチルピペラジン-1-イル)フェニル)(6-((3-ニトロフェニル)アミノ)ピリミジン-4-イル)カルバメート(1000mg、1.87mmol)のジクロロメタン(19mL)溶液にDMAP(342mg、2.80mmol)およびクロロギ酸4-ニトロフェニル(375mg、1.87mmol)を加えた。1時間後、DMAP(342mg、2.80mmol)およびクロロギ酸4-ニトロフェニル(375mg、1.87mmol)を反応混合物に加え、8時間攪拌した。反応が完了した時点で、反応混合物をジクロロメタン(100mL)で希釈し、ブラインで2回洗浄した。有機層をMgSO4で乾燥させ、濾過し、減圧濃縮した。
。
tert-ブチル (6-(3-ベンジル-1-(3-ニトロフェニル)ウレイド)ピリミジン-4-イル)(2-メトキシ-4-(4-メチルピペラジン-1-イル)フェニル)カルバメート(500mg、0.75mmol)の酢酸エチル(10mL)溶液に塩化スズ(II)二水和物(844mg、3.74mmol)および濃HCl(1mL)を加えた。反応混合物を60℃で6時間攪拌した後、それを室温に冷却した。pHが約5に到達するまで水酸化アンモニウム溶液(28〜30% NH3)を反応混合物に加え、pHが7になるまでNa2CO3を反応混合物に加えた。反応混合物をセライトパッドを通じて濾過し、減圧濃縮した。粗生成物をさらに精製せずに次の反応に使用した。保持時間 = 3.05分;
。
1-(3-アミノフェニル)-3-ベンジル-1-(6-((2-メトキシ-4-(4-メチルピペラジン-1-イル)フェニル)アミノ)ピリミジン-4-イル)尿素から出発して実施例1Eに関して記載のようにN-(3-(3-ベンジル-1-(6-((2-メトキシ-4-(4-メチルピペラジン-1-イル)フェニル)アミノ)ピリミジン-4-イル)ウレイド)フェニル)アクリルアミドを調製した。保持時間 = 3.13分;
。
A. 2-クロロ-N-(3-ニトロフェニル)ピリミジン-4-アミン
2,4-ジクロロピリミジンから出発して実施例1Aに関して記載のように2-クロロ-N-(3-ニトロフェニル)ピリミジン-4-アミンを調製した。保持時間 = 2.83分; MS m/z: 250.81 [M+1]。
2-クロロ-N-(3-ニトロフェニル)ピリミジン-4-アミン(160mg、0.64mmol)のTHF(3mL)溶液にDIEA(0.22mL、1.28mmol)およびクロロギ酸ベンジル(0.91μL、0.64mmol)を加えた。反応混合物を24時間攪拌した後、それを酢酸エチルと水との間で分配した。有機層を分離し、水層を酢酸エチルで抽出した。一緒にした有機抽出物をブラインで洗浄し、MgSO4で乾燥させ、濾過し、減圧濃縮した。粗生成物をシリカゲル上でのカラムクロマトグラフィー(0:100〜1:99、メタノール/ジクロロメタン)で精製して標記化合物(190mg、収率77%)を得た。保持時間 = 3.65分; MS m/z: 385.21 [M+1]。
ベンジル (2-クロロピリミジン-4-イル)(3-ニトロフェニル)カルバメートから出発して実施例1Bに関して記載のようにベンジル (2-((2-メトキシ-4-(4-メチルピペラジン-1-イル)フェニル)アミノ)ピリミジン-4-イル)(3-ニトロフェニル)カルバメートを調製した。
ベンジル (2-((2-メトキシ-4-(4-メチルピペラジン-1-イル)フェニル)アミノ)ピリミジン-4-イル)(3-ニトロフェニル)カルバメートから出発して実施例3EおよびFに関して記載のようにベンジル (3-アクリルアミドフェニル)(2-((2-メトキシ-4-(4-メチルピペラジン-1-イル)フェニル)アミノ)ピリミジン-4-イル)カルバメートを調製した。保持時間 = 3.30分, MS m/z: 594.39 [M+1],
。
A. 7-メトキシ-N-メチル-6-ニトロキナゾリン-4-アミン
4-クロロ-7-メトキシ-6-ニトロキナゾリン(1.0g、4.18mmol)の無水THF(10mL)溶液にメチルアミンのTHF中2.0M溶液(4.4mL)を0℃で加えた。反応混合物を室温で4時間攪拌し、溶媒の当初量の半分に減圧濃縮した。反応混合物に水(100mL)を加え、得られた析出物を濾取した。固体を窒素ガスを使用して送風により乾燥させて7-メトキシ-N-メチル-6-ニトロキナゾリン-4-アミン(870mg、収率89%)を明黄色固体として得た。
7-メトキシ-N-メチル-6-ニトロキナゾリン-4-アミン(800mg、3.42mmol)のメタノール(8mL)溶液にパラジウム10重量%(乾燥ベース)担持湿潤活性炭であるDegussaタイプE101 NE/Wを窒素雰囲気下で加えた。反応混合物をバルーン圧下で6時間水素化した。得られた懸濁液をセライトパッドを通じて濾過した後、濾液を濃縮して7-メトキシ-N4-メチルキナゾリン-4,6-ジアミン(670mg、収率96%)を白色固体として得た。
7-メトキシ-N4-メチルキナゾリン-4,6-ジアミン(600mg、2.94mmol)および(S)-1-(tert-ブトキシカルボニル)ピロリジン-2-カルボン酸(632mg、2.94mmol)のDMF(12mL)溶液にHATU(3.3g、8.82mmol)およびDIEA(2.56mL、14.70mmol)を加えた。反応混合物を室温で終夜攪拌した後、それを酢酸エチルと飽和NH4Cl溶液との間で分配した。水層を酢酸エチルで抽出した。一緒にした有機層をブラインで洗浄し、MgSO4で乾燥させ、セライトパッドで濾過し、減圧濃縮した。粗化合物を(0:100〜3:97、メタノール/ジクロロメタン)を溶媒とするフラッシュシリカクロマトグラフィーで精製して(S)-tert-ブチル 2-((7-メトキシ-4-(メチルアミノ)キナゾリン-6-イル)カルバモイル)ピロリジン-1-カルボキシレート(910mg、収率77%)を白色固体として得た。
5mL密封バイアルに(S)-tert-ブチル 2-((7-メトキシ-4-(メチルアミノ)キナゾリン-6-イル)カルバモイル)ピロリジン-1-カルボキシレート(200mg、0.50mmol)、ベンジルイソシアネート(92μL、0.75mmol)、およびトルエン(2mL)を添加した。反応バイアルを密封し、100℃で4時間加熱した。反応混合物を減圧濃縮し、残渣をシリカゲル上でのカラムクロマトグラフィー(1:99〜5:95、メタノール/ジクロロメタン)で精製して(S)-tert-ブチル 2-((4-(3-ベンジル-1-メチルウレイド)-7-メトキシキナゾリン-6-イル)カルバモイル)ピロリジン-1-カルボキシレート(190mg、収率71%)を帯黄白色固体として得た。
2-((4-(3-ベンジル-1-メチルウレイド)-7-メトキシキナゾリン-6-イル)カルバモイル)ピロリジン-1-カルボキシレート(100mg、0.19mmol)のジクロロメタン(1mL)溶液にTFA(1mL)を加えた。反応混合物を4時間攪拌し、減圧濃縮した。粗混合物をジクロロメタンと飽和NaHCO3溶液との間で分配した。水層をジクロロメタンで抽出した。一緒にした有機層をブラインで洗浄し、MgSO4で乾燥させ、セライトパッドで濾過し、減圧濃縮した。粗生成物をさらに精製せずに次の反応に使用した。
(S)-N-(4-(3-ベンジル-1-メチルウレイド)-7-メトキシキナゾリン-6-イル)ピロリジン-2-カルボキサミド(50mg、0.12mmol)の無水DMF(1mL)およびDIEA(40μL、0.23mmol)溶液に塩化アクリロイル(10μl、0.12mmol)を0℃で加えた。反応混合物を0℃で2時間攪拌した。反応混合物を酢酸エチルと水との間で分配した。水層を酢酸エチルで抽出し、一緒にした有機層をブラインで洗浄した。有機層をMgSO4で乾燥させ、セライトパッドを通じて濾過し、減圧濃縮した。残渣をシリカゲル上でのカラムクロマトグラフィー(1:99〜10:90、メタノール/ジクロロメタン)で精製して(S)-1-アクリロイル-N-(4-(3-ベンジル-1-メチルウレイド)-7-メトキシキナゾリン-6-イル)ピロリジン-2-カルボキサミド(38mg、収率68%)を帯黄白色固体として得た。保持時間 = 3.13分,
。
A. エチル2-(メチルチオ)-4-((3-ニトロフェニル)アミノ)ピリミジン-5-カルボキシレート
エチル4-クロロ-2-(メチルチオ)ピリミジン-5-カルボキシレートから出発して実施例1Aに関して記載のようにエチル2-(メチルチオ)-4-((3-ニトロフェニル)アミノ)ピリミジン-5-カルボキシレートを調製した。
エチル2-(メチルチオ)-4-((3-ニトロフェニル)アミノ)ピリミジン-5-カルボキシレート(1.0g、2.99mmol)のTHF(5mL)およびMeOH(5mL)溶液に水(5mL)中LiOH・H2O(628mg、14.97mmol)を加えた。反応混合物を室温で終夜攪拌した。有機溶媒を減圧除去し、水(4mL)を反応混合物に加えた。反応混合物に1N HCl溶液を加えて固体を生成した。固体生成物を濾過し、窒素ガス流で乾燥させた。標記生成物(720mg、収率79%)をさらに精製せずに次の反応に使用した。
2-(メチルチオ)-4-((3-ニトロフェニル)アミノ)ピリミジン-5-カルボン酸(600mg、1.96mmol)およびアニリン(268μL、2.94mmol)のDMF(6mL)溶液にEDCI(563mg、2.94mmol)、HOBt水和物(450mg、3.33mmol)、およびTEA(409μL、2.94mmol)を加えた。反応混合物を室温で終夜攪拌した後、それを酢酸エチルと飽和NH4Cl溶液との間で分配した。水層を酢酸エチルで抽出した。一緒にした有機層をブラインで洗浄し、MgSO4で乾燥させ、セライトパッドで濾過し、減圧濃縮した。粗化合物を(0:100〜3:97、メタノール/ジクロロメタン)を溶媒とするフラッシュシリカクロマトグラフィーで精製して2-(メチルチオ)-4-((3-ニトロフェニル)アミノ)-N-フェニルピリミジン-5-カルボキサミド(620mg、収率83%)を得た。
25mL密封バイアルに2-(メチルチオ)-4-((3-ニトロフェニル)アミノ)-N-フェニルピリミジン-5-カルボキサミド(620mg、1.63mmol)、CDI(2.6g、16.27mmol)、およびキシレン(6mL)を添加した。反応バイアルを密封し、160℃で24時間加熱した。反応混合物を減圧濃縮し、残渣をシリカゲル上でのカラムクロマトグラフィー(1:99〜7:95、メタノール/ジクロロメタン)で精製して7-(1H-イミダゾール-1-イル)-1-(3-ニトロフェニル)-3-フェニルピリミド[4,5-d]ピリミジン-2,4(1H,3H)-ジオン(240 mg、収率35%)を得た。
7-(1H-イミダゾール-1-イル)-1-(3-ニトロフェニル)-3-フェニルピリミド[4,5-d]ピリミジン-2,4(1H,3H)-ジオンから出発して実施例1Bに関して記載のように7-((2-メトキシ-4-(4-メチルピペラジン-1-イル)フェニル)アミノ)-1-(3-ニトロフェニル)-3-フェニルピリミド[4,5-d]ピリミジン-2,4(1H,3H)-ジオンを調製した。
7-((2-メトキシ-4-(4-メチルピペラジン-1-イル)フェニル)アミノ)-1-(3-ニトロフェニル)-3-フェニルピリミド[4,5-d]ピリミジン-2,4(1H,3H)-ジオンから出発して実施例3EおよびFに関して記載のようにN-(3-(7-((2-メトキシ-4-(4-メチルピペラジン-1-イル)フェニル)アミノ)-2,4-ジオキソ-3-フェニル-3,4-ジヒドロピリミド[4,5-d]ピリミジン-1(2H)-イル)フェニル)アクリルアミドカルバメートを調製した。保持時間 = 2.93分,
。
A. エチル4-(メチルアミノ)-2-(メチルチオ)ピリミジン-5-カルボキシレート
エチル4-クロロ-2-(メチルチオ)ピリミジン-5-カルボキシレート(2.0g、8.6mmol)のTHF(20mL)溶液にメチルアミンのTHF中2.0M溶液(11.34mL、21.4mmol)を0℃で加えた。反応混合物を室温で1時間攪拌し、溶媒の当初量の半分に減圧濃縮した。反応混合物に水(2000mL)を加え、得られた析出物を濾取した。固体を窒素ガスを使用して送風により乾燥させてエチル4-(メチルアミノ)-2-(メチルチオ)ピリミジン-5-カルボキシレート(1.75g、収率89%)を白色固体として得た。
。
4-(メチルアミノ)-2-(メチルチオ)ピリミジン-5-カルボキシレート(300mg、1.32mmol)のTHF(6.6mL)溶液に水素化アルミニウムリチウムのTHF中2.0M溶液(0.79mL、1.58mmol)を0℃で加えた。反応混合物を室温で2時間攪拌し、飽和NH4Cl溶液(2mL)で処理した。室温で30分間攪拌した後、反応混合物をセライトパッドを通じて濾過した。濾液を酢酸エチル(30mL)と水(20mL)との間で分配した。有機層をブラインで洗浄し、MgSO4で乾燥させ、セライトパッドを通じて濾過し、減圧濃縮した。得られた白色固体(210mg、収率86%)をさらに精製せずに次の工程に使用した。
。
4-(メチルアミノ)-2-(メチルチオ)ピリミジン-5-カルボアルデヒド(190mg、1.04mmol)のメタノール(5mL)溶液に酢酸(0.12mL、2.06mmol)、アニリン9(106mg、1.14mmol)、およびNa(CN)BH3(325mg、5.18mmol)を加え、得られた溶液を室温で終夜攪拌した。反応混合物を酢酸エチル(30mL)と飽和NaHCO3(20mL)との間で分配した後、水層を酢酸エチル(10mL×3)で抽出した。一緒にした有機層をブラインで洗浄し、MgSO4で乾燥させ、セライトパッドを通じて濾過し、減圧濃縮した。得られた粗生成物を酢酸エチル/ヘキサン(1/4〜2/3)によるシリカゲルクロマトグラフィーで精製して標記生成物N-メチル-2-(メチルチオ)-5-((フェニルアミノ)メチル)ピリミジン-4-アミン(180mg、収率67%)を白色固体として得た。
N-メチル-2-(メチルチオ)-5-((フェニルアミノ)メチル)ピリミジン-4-アミン(180mg、0.69mmol)の1,4-ジオキサン(3.60mL)溶液にDIEA(0.36mL、2.08mmol)およびトリホスゲン(82mg、0.28mmol)を0℃で加え、室温で1時間攪拌した。析出物を濾去し、濾液を110℃で3時間攪拌した。反応混合物を室温に冷却し、酢酸エチル(20mL)と飽和NaHCO3(20mL)溶液との間で分配した。有機層をブラインで洗浄し、MgSO4で乾燥させ、セライトパッドを通じて濾過し、減圧濃縮した。得られた粗生成物をシリカゲル上でのカラムクロマトグラフィー(0:100〜3:97、メタノール/ジクロロメタン)で精製して標記生成物1-メチル-7-(メチルスルホニル)-3-フェニル-3,4-ジヒドロピリミド[4,5-d]ピリミジン-2(1H)-オン(140mg、収率71%)を白色固体として得た。
1-メチル-7-(メチルスルホニル)-3-フェニル-3,4-ジヒドロピリミド[4,5-d]ピリミジン-2(1H)-オン(140mg、0.49mmol)のジクロロメタン(2mL)溶液にm-クロロ過安息香酸(361mg、1.47mmol)を0℃で加えた。反応混合物を0℃で30分間攪拌した後、室温でさらに3時間攪拌した。反応混合物をジクロロメタン(20mL)と飽和NaHCO3(20mL)との間で分配した。有機層をブラインで洗浄し、MgSO4で乾燥させ、セライトパッドを通じて濾過し、減圧濃縮した。得られた白色固体をさらに精製せずに次の工程に使用した。
1-メチル-7-(メチルスルホニル)-3-フェニル-3,4-ジヒドロピリミド[4,5-d]ピリミジン-2(1H)-オン(130mg、0.41mmol)の2-ブタノール(1.0mL)溶液に2-メトキシ-5-ニトロアニリン(137mg、0.82mmol)およびTFA(0.1mL)を加えた。密封反応容器中で反応混合物を120℃で24時間攪拌した。反応混合物を室温に冷却し、減圧濃縮した。粗反応混合物を酢酸エチル(10mL)と飽和NaHCO3溶液との間で分配した。水層を酢酸エチルで抽出した。一緒にした有機層をブラインで洗浄し、MgSO4で乾燥させ、セライトパッドを通じて濾過し、減圧濃縮した。得られた粗生成物をシリカゲル上でのカラムクロマトグラフィー(0:100〜5:95、メタノール/ジクロロメタン)で精製して7-((2-メトキシ-5-ニトロフェニル)アミノ)-1-メチル-3-フェニル-3,4-ジヒドロピリミド[4,5-d]ピリミジン-2(1H)-オン(120mg、収率72%)を得た。
7-((2-メトキシ-5-ニトロフェニル)アミノ)-1-メチル-3-フェニル-3,4-ジヒドロピリミド[4,5-d]ピリミジン-2(1H)-オン(120mg、0.30mmol)のメタノール(2mL)溶液にパラジウム10重量%(乾燥ベース)担持湿潤活性炭であるDegussaタイプE101 NE/Wを窒素雰囲気下で加えた。反応混合物をバルーン圧下で6時間水素化した。得られた懸濁液をセライトパッドを通じて濾過し、濾液を濃縮して7-((5-アミノ-2-メトキシフェニル)アミノ)-1-メチル-3-フェニル-3,4-ジヒドロピリミド[4,5-d]ピリミジン-2(1H)-オン(105mg、収率94%)を得た。
Ba/F3細胞の生成
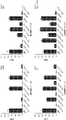
発がん性変化物をコードする特異的cDNA(EGFR: Del 19、L858R、L718Q、L844V、Del/T790M、L858R/T790M、Del 19/L718Q、Del 19/L844V、Del 19/T790M/L718QおよびL858R/T790M/L718Q; FGFR: TEL-FGFR1、TEL-FGFR2、TEL-FGFR1 V561M、TEL-FGFR2 V561M; ALK: EML4-ALK; ROS1: CD74-ROS1)を標準的分子生物学技術を使用してpDNA-Dual(BD Biosciences)ベクターにクローニングした。変異体特異的プライマーによる部位特異的変異誘発(Agilent)を製造者の説明書に従って使用して変異を導入した。すべての構築物をDNA配列決定によって確かめた。構築物をレトロウイルス感染を使用してBa/F3細胞に導入した。ポリクローナル細胞株をピューロマイシン選択によって樹立し、続いてインターロイキン3(IL-3)の非存在下で培養した。緑色蛍光タンパク質(GFP)を発現する非感染Ba/F3細胞または細胞株を対照として使用した。
増殖および増殖阻害をMTSアッセイ法によって評価した。このアッセイ法は、生細胞の数を決定するための比色法であり、細胞が3-(4,5-ジメチルチアゾール-2-イル)-5-(3-カルボキシメトキシフェニル)-2-(4-スルホフェニル)-2H-テトラゾリウム(MTS)を細胞培地に可溶性でかつ分光測定で検出可能なホルマザン生成物に生物還元することに基づいており、製造者の推奨条件に従って行った。Ba/F3細胞を72時間の処理に供し、実験1回当たりで使用する細胞の数を、その期間にわたる線形増殖動態を確保するために経験的に決定した。すべての実験点を6〜12個のウェル中で設定し、すべての実験を少なくとも3回繰り返した。データをWindows用GraphPad Prismバージョン5.0(GraphPad Software; http://www.graphpad.com)を使用して図表で表示した。非線形回帰モデルを使用して曲線をS字型用量反応にフィッティングした。結果を以下の表に示す。
BTKキナーゼアッセイ法を、LanthaScreen(登録商標)キナーゼアッセイ法を使用して行った。
1. ATP Km,appを決定するために必要なキナーゼ濃度の最適化。最初に、最小TR-FRET発光比と最大TR-FRET発光比との間での約80%変化を誘発するために必要なキナーゼの量(EC80値)を決定するために、アッセイ法をキナーゼの希釈系列に対して高いATP濃度(1mM)で行った。
2. ATP Km,appの決定。次に、最小TR-FRET発光比と最大TR-FRET発光比との間での50%変化を誘発するために必要なATPの量(EC50値)を決定するために、段階1において決定された酵素の濃度を使用して、アッセイ法をATPの希釈系列に対して行った。このATP濃度をATPの「見かけの」Km値、またはATP Km,appと呼んだ。
3. ATP Km,appでのアッセイ法に必要なキナーゼ濃度の最適化。ATPのATP Km,app濃度での最小TR-FRET発光比と最大TR-FRET発光比との間での約80%変化を誘発するために必要なキナーゼの濃度(EC80値)を決定するために、段階2において決定されたATPのATP Km,app濃度を使用してキナーゼ力価測定を繰り返した。これを、本発明の化合物のIC50値を決定するためのアッセイ法において使用するキナーゼ濃度とした。
Claims (89)
- 式Iの化合物、または薬学的に許容されるその塩:
式中、
Z1はNまたはCR1であり;
Z2はNまたはCR2であり;
Z3はNまたはCR3であるが、但し、YがNR4である場合、Z1、Z2、またはZ3のうち2つはNであり;
R1はH、C1〜C8アルキル、ハロゲン、またはハロ(C1〜C8アルキル)であり;
R2はH、C1〜C8アルキル、ハロゲン、またはハロ(C1〜C8アルキル)であり;
X2はOまたはNR10であり;
R10は水素またはC1〜C8アルキルであるか、
あるいは、Z2がCR2でありかつX2がNR10である場合、R2およびR10は一緒になって6員複素環を形成することができ、ここで該複素環は1個または複数のR28で置換されていてもよく;
R3はH、C1〜C8アルキル、ハロゲン、またはハロ(C1〜C8アルキル)であり;
YはNR4であるか、
あるいは、Y-X4およびR3は一緒になって非置換もしくは置換C6アリールまたは非置換もしくは置換の5員もしくは6員ヘテロアリールを形成し、ここで該置換アリールまたは該置換ヘテロアリールは1個または複数のR5で置換されており;
R4はHまたはC1〜C8アルキルであり;
各R5は独立して、ハロゲン、OR6、NR7R8、NR7C(O)R8、SR9、C1〜C8アルキル、5員複素環もしくは6員複素環で置換されていてもよいC2〜C8アルキニル、またはハロ(C1〜C8アルキル)であり;
各R6は独立して水素またはC1〜C8アルキルであり;
各R7およびR8は独立して、水素、C1〜C8アルキル、または非置換もしくは置換の5員もしくは6員複素環であり、ここで該置換複素環は1個または複数のR16で置換されており;
各R9は独立して水素またはC1〜C8アルキルであり;
X1はH、C1〜C8アルキル、またはハロゲンであり;
各X3aおよびX3bは独立して水素、C1〜C8アルキル、または非存在(nが0である場合)であり;
QはC1〜C8アルキル、非置換もしくは置換C6〜C10アリール、非置換もしくは置換の5員もしくは6員ヘテロアリール、非置換もしくは置換3員〜8員シクロアルキル、または非置換もしくは置換3員〜8員複素環であり、ここで該置換アリール、該置換ヘテロアリール、該置換シクロアルキル、または該置換複素環は1個または複数のR11で置換されており;
各R11は独立して、ハロゲン、OR12、NR13R14、SR15、C1〜C8アルキル、またはハロ(C1〜C8アルキル)であり;
各R12は独立して水素またはC1〜C8アルキルであり;
各R13およびR14は独立して水素またはC1〜C8アルキルであり;
各R15は独立して水素またはC1〜C8アルキルであり;
nは0、1、2、3、または4であり;
X4は、非置換もしくは置換C6〜C10アリール、非置換もしくは置換の5員もしくは6員ヘテロアリール、非置換もしくは置換C1〜C8アルキル、または非置換もしくは置換(CH2)1〜3-C6〜C10アリールであり、
ここで該置換アリール、該置換ヘテロアリール、または該置換アルキルは1個または複数のR16で置換されており;
各R16は独立して、ハロゲン、OR17、NR18R19、SR20、非置換もしくは置換C1〜C8アルキル、ハロ(C1〜C8アルキル)、C(O)(C1〜C8アルキル)、C(O)(ハロ(C1〜C8アルキル))、C(O)(C2〜C8アルケニル)、非置換もしくは置換複素環、またはC(O)-非置換もしくはC(O)-置換複素環であり、ここで該置換アルキルまたは該置換複素環は1個または複数のR21で置換されており;
各R17は独立して水素またはC1〜C8アルキルであり;
各R18およびR19は独立して、水素、C1〜C8アルキル、C(O)(C1〜C8アルキル)、C(O)(C2〜C8アルケニル)、またはC(O)-非置換もしくはC(O)-置換複素環であり、ここで該アルキルまたは該アルケニルは、1個または複数のOH、CN、ハロゲン、C3〜C8シクロアルキル、O(C1〜C8アルキル)、NH2、NH(C1〜C8アルキル)、またはN(C1〜C8アルキル)2で置換されていてもよく、かつここで、該置換複素環は1個または複数のR21で置換されており;
各R20は独立して水素またはC1〜C8アルキルであり;
各R21はC1〜C8アルキル、C(O)(C1〜C8アルキル)、C(O)(C2〜C8アルケニル)、または複素環であり;
X5は、非置換もしくは置換C6〜C10アリール、非置換もしくは置換5員〜8員ヘテロアリール、または非置換もしくは置換C1〜C8アルキルであり、ここで該置換アリール、該置換ヘテロアリール、または該置換アルキルは1個または複数のR22で置換されており;
各R22は独立して、ハロゲン、OR23、NR24R25、SR26、C1〜C8アルキル、ハロ(C1〜C8アルキル)、C(O)(C1〜C8アルキル)、C(O)(C2〜C8アルケニル)、非置換もしくは置換複素環、非置換もしくは置換C6〜C10アリール、またはC(O)-非置換もしくはC(O)-置換複素環であり、ここで該置換複素環または該置換アリールは1個または複数のR27で置換されているか、
あるいは、2個またはそれ以上のR22は、それらが結合している原子と一緒になって、非置換もしくは置換3員〜8員シクロアルキル、または非置換もしくは置換5員〜6員複素環を形成し、ここで該シクロアルキルまたは該複素環は1個または複数のR27で置換されており;
各R23は独立して水素またはC1〜C8アルキルであり;
各R24およびR25は独立して、水素、C1〜C8アルキル、C(O)(C1〜C8アルキル)、またはC(O)(C2〜C8アルケニル)であり、ここで該アルキルまたは該アルケニルは、1個または複数のOH、CN、ハロゲン、C3〜C8シクロアルキル、O(C1〜C8アルキル)、NH2、NH(C1〜C8アルキル)、またはN(C1〜C8アルキル)2で置換されていてもよく;
各R26は独立して水素またはC1〜C8アルキルであり;
各R27はハロゲン、C1〜C8アルキル、C(O)(C1〜C8アルキル)、C(O)(C2〜C8アルケニル)、NR29C(O)(C1〜C8アルキル)、またはNR29C(O)(C2〜C8アルケニル)であり;
各R28はハロゲン、C1〜C8アルキル、またはハロ(C1〜C8アルキル)であるか、
あるいは、2個のR28およびそれらが結合している炭素が一緒になってC=Oを形成し; かつ
各R29は水素またはC1〜C8アルキルである。 - X1が水素またはハロゲンである、請求項1〜9のいずれか一項に記載の化合物。
- X1が水素である、請求項10に記載の化合物。
- X1がハロゲンである、請求項10に記載の化合物。
- X1が塩素である、請求項12に記載の化合物。
- nが0、1、または2である、請求項1〜13のいずれか一項に記載の化合物。
- nが0または1である、請求項14に記載の化合物。
- nが0である、請求項15に記載の化合物。
- nが1である、請求項15に記載の化合物。
- X3aおよびX3bがそれぞれ水素であるか、または、X3aもしくはX3bの一方がメチルであり、かつ残りのX3aもしくはX3bが水素である、請求項1〜15および17のいずれか一項に記載の化合物。
- X3aおよびX3bがそれぞれ水素である、請求項18に記載の化合物。
- X3aまたはX3bの一方がメチルであり、かつ残りのX3aまたはX3bが水素である、請求項18に記載の化合物。
- X3aおよびX3bが結合している炭素原子の立体配置がS配置である、請求項20に記載の化合物。
- Qが、非置換もしくは置換フェニル、または非置換もしくは置換の5員もしくは6員ヘテロアリールである、請求項1〜21のいずれか一項に記載の化合物。
- Qが、非置換フェニル、または非置換の5員もしくは6員ヘテロアリールである、請求項22に記載の化合物。
- Qが非置換フェニルである、請求項23に記載の化合物。
- 前記ヘテロアリールがピリジルまたはチエニルである、請求項22または23に記載の化合物。
- Qが、1個、2個、3個、または4個のR11で置換されている、請求項22または25に記載の化合物。
- 各R11が独立して、メチル、エチル、プロピル、イソプロピル、クロロ、フルオロ、メトキシ、エトキシ、プロポキシ、またはイソプロポキシである、請求項26に記載の化合物。
- 各R11が独立してメチル、クロロ、またはメトキシである、請求項27に記載の化合物。
- X4が、置換フェニル、またはメチルである、請求項1〜3および7〜28のいずれか一項に記載の化合物。
- X4が、1個または2個のR16で置換されたフェニルである、請求項29に記載の化合物。
- 少なくとも1個のR16がOCH3である、請求項30に記載の化合物。
- X4がメチルである、請求項29に記載の化合物。
- X5が、置換フェニル、またはメチルである、請求項1〜6および10〜28のいずれか一項に記載の化合物。
- X5がメチルである、請求項33に記載の化合物。
- X5が、1個のR22で置換されたフェニルである、請求項33に記載の化合物。
- R22がNR24R25である、請求項35に記載の化合物。
- R24またはR25の一方がC(O)(C2〜C8アルケニル)であり、かつ残りのR24またはR25が水素である、請求項36に記載の化合物。
- uが1または2である、請求項4に記載の化合物。
- 少なくとも1個のR16がOCH3である、請求項38に記載の化合物。
- R17がメチルである、請求項1〜28のいずれか一項に記載の化合物。
- R16が、置換複素環、またはNR18R19である、請求項40に記載の化合物。
- R16がメチルピペラジンである、請求項41に記載の化合物。
- R16が、NH2で置換されていてもよいNHC(O)(C2〜C4アルケニル)、NH(C1〜C3アルキル)で置換されていてもよいNHC(O)(C2〜C4アルケニル)、またはN(C1〜C3アルキル)2で置換されていてもよいNHC(O)(C2〜C4アルケニル)である、請求項41に記載の化合物。
- R22がNR24R25である、請求項1〜6および8〜28のいずれか一項に記載の化合物。
- R24およびR25の一方がC(O)(C2〜C8アルケニル)であり、かつ残りのR24およびR25が水素である、請求項44に記載の化合物。
- 表1より選択される化合物。
- 請求項1〜46のいずれか一項に記載の化合物または薬学的に許容されるその塩と薬学的な担体、希釈剤、または賦形剤とを含む、薬学的組成物。
- それを必要とする対象に請求項1〜46のいずれか一項に記載の化合物または薬学的に許容されるその塩を投与する段階を含む、該対象においてキナーゼを阻害する方法。
- 対象に請求項1〜46のいずれか一項に記載の化合物または薬学的に許容されるその塩を投与する段階を含む、該対象において上皮増殖因子受容体(EGFR)を阻害する方法。
- 前記EGFRがHerキナーゼである、請求項49に記載の方法。
- 対象に請求項1〜46のいずれか一項に記載の化合物または薬学的に許容されるその塩を投与する段階を含む、該対象において線維芽細胞増殖因子受容体(FGFR)を阻害する方法。
- 対象に請求項1〜46のいずれか一項に記載の化合物または薬学的に許容されるその塩を投与する段階を含む、該対象において線維芽細胞増殖因子受容体(FGFR)および上皮増殖因子受容体(EGFR)を阻害する方法。
- それを必要とする対象に請求項1〜46のいずれか一項に記載の化合物または薬学的に許容されるその塩を投与する段階を含む、該対象において疾患を処置および/または予防する方法。
- 前記疾患がキナーゼによって媒介される、請求項53に記載の方法。
- 前記疾患がEGFRおよび/またはFGFRによって媒介される、請求項53に記載の方法。
- 前記疾患ががんまたは増殖性疾患である、請求項53に記載の方法。
- 前記疾患が、肺がん、結腸がん、乳がん、前立腺がん、肝がん、膵がん(pancreas cancer)、脳がん、腎がん、卵巣がん、胃がん(stomach cancer)、皮膚がん、骨がん、胃部のがん (gastric cancer)、乳がん、膵臓がん(pancreatic cancer)、神経膠腫、神経膠芽腫、肝細胞がん、乳頭状腎がん、頭頸部扁平上皮がん、白血病、リンパ腫、骨髄腫、または固形腫瘍である、請求項56に記載の方法。
- 前記疾患が肺がんである、請求項57に記載の方法。
- 前記肺がんが非小細胞肺がん(NSCLC)である、請求項58に記載の方法。
- 前記疾患が、炎症、関節炎、関節リウマチ、脊椎関節症、痛風関節炎、変形性関節症、若年性関節炎、および他の関節炎状態、全身性エリテマトーデス(SLE)、皮膚関連の病気、乾癬、湿疹、熱傷、皮膚炎、神経炎症、アレルギー、疼痛、神経障害性疼痛、発熱、肺障害、肺炎症、成人呼吸促迫症候群、肺サルコイドーシス、喘息、珪肺症、慢性肺炎症性疾患、および慢性閉塞性肺疾患(COPD)、心血管疾患、動脈硬化症、心筋梗塞(心筋梗塞後徴候を含む)、血栓症、うっ血性心不全、心臓再灌流障害、ならびに、脈管器管障害、再狭窄、心筋症、虚血性脳卒中および出血性脳卒中を含む脳卒中などの高血圧および/または心不全に関連する合併症、再灌流障害、腎臓再灌流障害、脳卒中および脳虚血を含む虚血、ならびに心臓/冠動脈バイパス術による虚血、神経変性障害、肝疾患および腎炎、胃腸病、炎症性腸疾患、クローン病、胃炎、過敏性腸症候群、潰瘍性大腸炎、潰瘍性疾患、胃潰瘍、ウイルス感染症および細菌感染症、敗血症、敗血症性ショック、グラム陰性敗血症、マラリア、髄膜炎、HIV感染症、日和見感染症、感染症もしくは悪性腫瘍に続発する悪液質、後天性免疫不全症候群(AIDS)に続発する悪液質、AIDS、ARC(AIDS関連症候群)、肺炎、ヘルペスウイルス、感染症による筋肉痛、インフルエンザ、自己免疫疾患、移植片対宿主反応および同種移植片拒絶、骨吸収疾患の処置、骨粗鬆症、多発性硬化症、がん、白血病、リンパ腫、結腸直腸がん、脳がん、骨がん、上皮細胞由来新生物(上皮がん)、基底細胞がん、腺がん、胃腸がん、口唇がん、口腔がん、食道がん、小腸がん、胃がん、結腸がん、肝がん、膀胱がん、膵がん、卵巣がん、子宮頸がん、肺がん、乳がん、皮膚がん、扁平上皮がんおよび/もしくは基底細胞がん、前立腺がん、腎細胞がん、ならびに全身の上皮細胞を冒す他の公知のがん、慢性骨髄性白血病(CML)、急性骨髄性白血病(AML)および急性前骨髄球性白血病(APL)、新生物を含む血管新生、転移、中枢神経系障害、炎症性成分もしくはアポトーシス性成分を有する中枢神経系障害、アルツハイマー病、パーキンソン病、ハンチントン病、筋萎縮性側索硬化症、脊髄損傷、ならびに末梢神経障害、またはB細胞リンパ腫である、請求項53に記載の方法。
- 前記疾患が、炎症、関節炎、関節リウマチ、脊椎関節症、痛風関節炎、変形性関節症、若年性関節炎、および他の関節炎状態、全身性エリテマトーデス(SLE)、皮膚関連の病気、乾癬、湿疹、皮膚炎、疼痛、肺障害、肺炎症、成人呼吸促迫症候群、肺サルコイドーシス、喘息、慢性肺炎症性疾患、および慢性閉塞性肺疾患(COPD)、心血管疾患、動脈硬化症、心筋梗塞(心筋梗塞後徴候を含む)、うっ血性心不全、心臓再灌流障害、炎症性腸疾患、クローン病、胃炎、過敏性腸症候群、白血病、またはリンパ腫である、請求項53に記載の方法。
- それを必要とする対象に請求項1〜46のいずれか一項に記載の化合物または薬学的に許容されるその塩を投与する段階を含む、該対象においてキナーゼ媒介障害を処置する方法。
- 前記化合物が、ALKチロシンキナーゼ、ROS1チロシンキナーゼ、EGFRチロシンキナーゼ、およびFGFRチロシンキナーゼのうち1つまたは複数を共有結合的に修飾する、請求項62に記載の方法。
- 前記対象にさらなる治療用物質が投与される、請求項62に記載の方法。
- 前記化合物および前記さらなる治療用物質が同時投与または連続投与される、請求項64に記載の方法。
- それを必要とする対象に請求項1〜46のいずれか一項に記載の化合物または薬学的に許容されるその塩を投与する段階を含む、対象においてEGFR標的療法に耐性のある疾患を処置する方法。
- 前記EGFR標的療法が、ゲフィチニブ、エルロチニブ、ラパチニブ、XL-647、HKI-272、BIBW2992、AV-412、CI-1033、PF00299804、BMS 690514、セツキシマブ、パニツムマブ、またはマツズマブによる処置を含む、請求項66に記載の方法。
- 前記疾患がEGFR変異を含む、請求項66に記載の方法。
- 前記EGFR変異が、EGFRのT790M耐性変異、T854A耐性変異、D761 Y耐性変異、またはL718Q耐性変異である、請求項68に記載の方法。
- EGFR L718Qが化合物WZ4002に対する耐性変異である、請求項69に記載の方法。
- 前記L718Q耐性変異が、活性化変異単独と共に、または、活性化変異および前記T790M変異と共に存在する、請求項68または70に記載の方法。
- 前記L718Q耐性変異が、活性化変異L858R単独と共に存在する、請求項71に記載の方法。
- 前記L718Q耐性変異が、活性化変異L858Rおよび前記TM790変異と共に存在する、請求項71に記載の方法。
- 前記疾患ががんである、請求項66に記載の方法。
- 前記疾患が、肺がん、結腸がん、乳がん、前立腺がん、肝がん、膵がん、脳がん、腎がん、卵巣がん、胃がん、皮膚がん、骨がん、胃部のがん、乳がん、膵臓がん、神経膠腫、神経膠芽腫、肝細胞がん、乳頭状腎がん、頭頸部扁平上皮がん、白血病、リンパ腫、骨髄腫、または固形腫瘍である、請求項74に記載の方法。
- 前記疾患が肺がんである、請求項75に記載の方法。
- 前記肺がんが非小細胞肺がん(NSCLC)である、請求項76に記載の方法。
- それを必要とする対象に請求項1〜46のいずれか一項に記載の化合物または薬学的に許容されるその塩を投与する段階を含む、該対象においてEGFR活性化腫瘍を含むがんを処置する方法。
- EGFR活性化が、EGFRの変異、EGFRの増幅、EGFRの発現、およびEGFRのリガンド媒介活性化より選択される、請求項78に記載の方法。
- 前記EGFRの変異が、G719S、G719C、G719A、L858R、L861Q、エキソン19欠失変異、またはエキソン20挿入変異に位置する、請求項78に記載の方法。
- 前記疾患が、肺がん、結腸がん、乳がん、前立腺がん、肝がん、膵がん、脳がん、腎がん、卵巣がん、胃がん、皮膚がん、骨がん、胃部のがん、乳がん、膵臓がん、神経膠腫、神経膠芽腫、肝細胞がん、乳頭状腎がん、頭頸部扁平上皮がん、白血病、リンパ腫、骨髄腫、または固形腫瘍である、請求項78に記載の方法。
- 前記疾患が肺がんである、請求項81に記載の方法。
- 前記肺がんが非小細胞肺がん(NSCLC)である、請求項82に記載の方法。
- それを必要とする対象に請求項1〜46のいずれか一項に記載の化合物または薬学的に許容されるその塩を投与する段階を含む、対象において疾患の状態でのゲフィチニブまたはエルロチニブに対する耐性を予防する方法。
- 前記疾患が、肺がん、結腸がん、乳がん、前立腺がん、肝がん、膵がん、脳がん、腎がん、卵巣がん、胃がん、皮膚がん、骨がん、胃部のがん、乳がん、膵臓がん、神経膠腫、神経膠芽腫、肝細胞がん、乳頭状腎がん、頭頸部扁平上皮がん、白血病、リンパ腫、骨髄腫、または固形腫瘍である、請求項84に記載の方法。
- 前記疾患が肺がんである、請求項85に記載の方法。
- 前記肺がんが非小細胞肺がん(NSCLC)である、請求項86に記載の方法。
- 前記対象がヒトである、請求項48〜87のいずれか一項に記載の方法。
- 請求項1〜46のいずれか一項に記載の化合物または薬学的に許容されるその塩を合成する方法。
Applications Claiming Priority (5)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US201361844304P | 2013-07-09 | 2013-07-09 | |
| US61/844,304 | 2013-07-09 | ||
| US201361901808P | 2013-11-08 | 2013-11-08 | |
| US61/901,808 | 2013-11-08 | ||
| PCT/US2014/046022 WO2015006492A1 (en) | 2013-07-09 | 2014-07-09 | Kinase inhibitors for the treatment of disease |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2016523973A true JP2016523973A (ja) | 2016-08-12 |
| JP2016523973A5 JP2016523973A5 (ja) | 2017-07-27 |
Family
ID=52280579
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2016525463A Pending JP2016523973A (ja) | 2013-07-09 | 2014-07-09 | 疾患の処置のためのキナーゼ阻害物質 |
Country Status (6)
| Country | Link |
|---|---|
| US (3) | US9783504B2 (ja) |
| EP (1) | EP3019491A4 (ja) |
| JP (1) | JP2016523973A (ja) |
| AU (1) | AU2014287209B2 (ja) |
| CA (1) | CA2917667A1 (ja) |
| WO (1) | WO2015006492A1 (ja) |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2020121994A (ja) * | 2015-02-20 | 2020-08-13 | インサイト・コーポレイションIncyte Corporation | Fgfr阻害剤としての二環式複素環 |
Families Citing this family (62)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US8754114B2 (en) | 2010-12-22 | 2014-06-17 | Incyte Corporation | Substituted imidazopyridazines and benzimidazoles as inhibitors of FGFR3 |
| GB201204384D0 (en) | 2012-03-13 | 2012-04-25 | Univ Dundee | Anti-flammatory agents |
| EP3822273B1 (en) | 2012-06-13 | 2024-04-10 | Incyte Holdings Corporation | Substituted tricyclic compounds as fgfr inhibitors |
| WO2014026125A1 (en) | 2012-08-10 | 2014-02-13 | Incyte Corporation | Pyrazine derivatives as fgfr inhibitors |
| US9266892B2 (en) | 2012-12-19 | 2016-02-23 | Incyte Holdings Corporation | Fused pyrazoles as FGFR inhibitors |
| CN105307657B (zh) | 2013-03-15 | 2020-07-10 | 西建卡尔有限责任公司 | 杂芳基化合物和其用途 |
| TWI647220B (zh) | 2013-03-15 | 2019-01-11 | 美商西建卡爾有限責任公司 | 雜芳基化合物及其用途 |
| UA120248C2 (uk) | 2013-03-15 | 2019-11-11 | Селджен Кар Ллс | Гетероарильні сполуки та їх застосування |
| SG10201708520YA (en) | 2013-04-19 | 2017-12-28 | Incyte Corp | Bicyclic heterocycles as fgfr inhibitors |
| US9783504B2 (en) * | 2013-07-09 | 2017-10-10 | Dana-Farber Cancer Institute, Inc. | Kinase inhibitors for the treatment of disease |
| DK3057943T3 (en) | 2013-10-18 | 2018-07-30 | Eisai R&D Man Co Ltd | PYRIMIDINE-FGFR4 INHIBITORS |
| BR112016008276B1 (pt) | 2013-10-25 | 2021-03-02 | Novartis Ag | derivados bicíclicos de piridila fundidos ao anel, seus usos e seu intermediário, e composição farmacêutica |
| CN116942629A (zh) | 2013-12-13 | 2023-10-27 | 诺华股份有限公司 | 药物剂型 |
| CN104860891B (zh) * | 2014-02-25 | 2017-06-30 | 上海海雁医药科技有限公司 | 芳氨基嘧啶类化合物及其应用以及由其制备的药物组合物和药用组合物 |
| AU2015292818B2 (en) | 2014-07-21 | 2020-01-16 | Dana-Farber Cancer Institute, Inc. | Imidazolyl kinase inhibitors and uses thereof |
| US10457691B2 (en) | 2014-07-21 | 2019-10-29 | Dana-Farber Cancer Institute, Inc. | Macrocyclic kinase inhibitors and uses thereof |
| EP3536323A1 (en) | 2014-08-08 | 2019-09-11 | Dana Farber Cancer Institute, Inc. | Uses of salt-inducible kinase (sik) inhibitors |
| US20180185341A1 (en) | 2014-10-03 | 2018-07-05 | Novartis Ag | Use of ring-fused bicyclic pyridyl derivatives as fgfr4 inhibitors |
| US10851105B2 (en) | 2014-10-22 | 2020-12-01 | Incyte Corporation | Bicyclic heterocycles as FGFR4 inhibitors |
| CA2974958A1 (en) * | 2015-01-26 | 2016-08-04 | Yale University | Compositions and methods of using tyrosine kinase inhibitors |
| CN105985342B (zh) * | 2015-02-06 | 2018-07-24 | 华东理工大学 | 作为egfr抑制剂的嘧啶并嘧啶二酮衍生物及其应用 |
| CN105884695B (zh) * | 2015-02-13 | 2019-02-26 | 山东轩竹医药科技有限公司 | 杂环衍生物类酪氨酸激酶抑制剂 |
| MA41551A (fr) | 2015-02-20 | 2017-12-26 | Incyte Corp | Hétérocycles bicycliques utilisés en tant qu'inhibiteurs de fgfr4 |
| WO2016134294A1 (en) | 2015-02-20 | 2016-08-25 | Incyte Corporation | Bicyclic heterocycles as fgfr4 inhibitors |
| US9802917B2 (en) | 2015-03-25 | 2017-10-31 | Novartis Ag | Particles of N-(5-cyano-4-((2-methoxyethyl)amino)pyridin-2-yl)-7-formyl-6-((4-methyl-2-oxopiperazin-1-yl)methyl)-3,4-dihydro-1,8-naphthyridine-1(2H)-carboxamide |
| ES2864712T3 (es) | 2015-04-14 | 2021-10-14 | Eisai R&D Man Co Ltd | Compuesto inhibidor de FGFR4 cristalino y usos del mismo |
| CN104860890B (zh) * | 2015-04-29 | 2018-03-13 | 上海泓博智源医药股份有限公司 | T790m突变型egfr的抑制剂及其在制备抗肿瘤药物中的应用 |
| WO2017012647A1 (en) * | 2015-07-20 | 2017-01-26 | Galapagos Nv | Novel compounds and pharmaceutical compositions thereof for the treatment of inflammatory disorders |
| AU2016296877B2 (en) * | 2015-07-20 | 2020-09-17 | Dana-Farber Cancer Institute, Inc. | Novel pyrimidines as EGFR inhibitors and methods of treating disorders |
| CN106892922B (zh) * | 2015-12-18 | 2019-04-19 | 华东理工大学 | 作为egfr抑制剂的5,8-二氢蝶啶-6,7-二酮衍生物及其应用 |
| US11357769B2 (en) | 2016-05-10 | 2022-06-14 | Eisai R&D Management Co., Ltd. | Drug combinations for reducing cell viability and/or cell proliferation |
| CN110225914A (zh) | 2016-07-05 | 2019-09-10 | 布罗德研究所股份有限公司 | 双环脲激酶抑制剂及其用途 |
| WO2018053373A1 (en) | 2016-09-16 | 2018-03-22 | The General Hospital Corporation | Uses of satl-inducible kinase (sik) inhibitors for treating osteoporosis |
| US11285158B2 (en) | 2017-02-28 | 2022-03-29 | The General Hospital Corporation | Uses of pyrimidopyrimidinones as SIK inhibitors |
| KR102583737B1 (ko) * | 2017-03-03 | 2023-09-26 | 오클랜드 유니서비시즈 리미티드 | Fgfr 키나제 저해제 및 약학적 용도 |
| CN108727382B (zh) * | 2017-04-19 | 2022-07-19 | 华东理工大学 | 作为btk抑制剂的杂环化合物及其应用 |
| DK3391907T3 (da) | 2017-04-20 | 2020-03-09 | Iomx Therapeutics Ag | Intracellulær kinase sik3, der er associeret med resistens over for antitumorimmunresponser, og anvendelser deraf |
| AR111960A1 (es) | 2017-05-26 | 2019-09-04 | Incyte Corp | Formas cristalinas de un inhibidor de fgfr y procesos para su preparación |
| WO2019029541A1 (zh) * | 2017-08-08 | 2019-02-14 | 南京药捷安康生物科技有限公司 | 成纤维细胞生长因子受体抑制剂及其用途 |
| WO2019075386A1 (en) | 2017-10-13 | 2019-04-18 | The Regents Of The University Of California | MODULATORS OF MTORC1 |
| CN112867716A (zh) | 2018-05-04 | 2021-05-28 | 因赛特公司 | Fgfr抑制剂的固体形式和其制备方法 |
| CN112566912A (zh) | 2018-05-04 | 2021-03-26 | 因赛特公司 | Fgfr抑制剂的盐 |
| CN112601742A (zh) * | 2018-06-30 | 2021-04-02 | 北京生命科学研究所 | 组织蛋白酶c抑制剂 |
| EP3876930A4 (en) * | 2018-11-07 | 2022-07-20 | Dana-Farber Cancer Institute, Inc. | BENZIMIDAZOLE DERIVATIVES AND AZA-BENZIMIDAZOLE DERIVATIVES AS JANUS KINASE 2 INHIBITORS AND THEIR USES |
| WO2020097400A1 (en) * | 2018-11-07 | 2020-05-14 | Dana-Farber Cancer Institute, Inc. | Imidazopyridine derivatives and aza-imidazopyridine derivatives as janus kinase 2 inhibitors and uses thereof |
| WO2020185532A1 (en) | 2019-03-08 | 2020-09-17 | Incyte Corporation | Methods of treating cancer with an fgfr inhibitor |
| ES2962852T3 (es) | 2019-05-10 | 2024-03-21 | Deciphera Pharmaceuticals Llc | Inhibidores de la autofagia de heteroarilaminopirimidina amida y métodos de uso de los mismos |
| FI3966207T3 (fi) | 2019-05-10 | 2023-11-30 | Deciphera Pharmaceuticals Llc | Autofagian fenyyliaminopyrimidiiniamidi-inhibiittoreita ja menetelmiä niiden käyttämiseksi |
| CN114258318A (zh) | 2019-06-17 | 2022-03-29 | 德西费拉制药有限责任公司 | 氨基嘧啶酰胺自噬抑制剂及其使用方法 |
| CN110563657B (zh) * | 2019-07-05 | 2024-05-03 | 温州医科大学 | 一种1-(2,6-二氯苯基)-3-取代脲类结肠癌抑制剂及其制备和应用 |
| CN110283130B (zh) * | 2019-07-05 | 2023-12-19 | 温州医科大学 | 一种1-(2,5-二甲氧基苯基)-3-取代脲类结肠癌抑制剂及其制备和应用 |
| WO2021007269A1 (en) | 2019-07-09 | 2021-01-14 | Incyte Corporation | Bicyclic heterocycles as fgfr inhibitors |
| AU2020366006A1 (en) | 2019-10-14 | 2022-04-21 | Incyte Corporation | Bicyclic heterocycles as FGFR inhibitors |
| US11566028B2 (en) | 2019-10-16 | 2023-01-31 | Incyte Corporation | Bicyclic heterocycles as FGFR inhibitors |
| EP4069696A1 (en) | 2019-12-04 | 2022-10-12 | Incyte Corporation | Tricyclic heterocycles as fgfr inhibitors |
| KR20220131900A (ko) | 2019-12-04 | 2022-09-29 | 인사이트 코포레이션 | Fgfr 억제제의 유도체 |
| WO2021219731A2 (en) | 2020-04-28 | 2021-11-04 | Iomx Therapeutics Ag | Bicyclic kinase inhibitors and uses thereof |
| TW202204350A (zh) | 2020-05-06 | 2022-02-01 | 美商雅捷可斯治療公司 | 作為jak2抑制劑之6-雜芳基氧基苯并咪唑及氮雜苯并咪唑 |
| US20240100172A1 (en) | 2020-12-21 | 2024-03-28 | Hangzhou Jijing Pharmaceutical Technology Limited | Methods and compounds for targeted autophagy |
| US11939331B2 (en) | 2021-06-09 | 2024-03-26 | Incyte Corporation | Tricyclic heterocycles as FGFR inhibitors |
| AU2022321449A1 (en) * | 2021-08-02 | 2023-12-21 | Abbisko Therapeutics Co., Ltd. | Pyrimidine-4,6-diamine derivative, a preparation method therefor, and a pharmaceutical application thereof |
| WO2023086319A1 (en) | 2021-11-09 | 2023-05-19 | Ajax Therapeutics, Inc. | 6-he tero aryloxy benzimidazoles and azabenzimidazoles as jak2 inhibitors |
Citations (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2006000420A1 (en) * | 2004-06-24 | 2006-01-05 | Novartis Ag | Pyrimidine urea derivatives as kinase inhibitors |
| JP2009520768A (ja) * | 2005-12-21 | 2009-05-28 | ノバルティス アクチエンゲゼルシャフト | Fgf阻害剤であるピリミジニルアリールウレア誘導体 |
| JP2013512956A (ja) * | 2009-12-07 | 2013-04-18 | ノバルティス アーゲー | 3−(2,6−ジクロロ−3,5−ジメトキシ−フェニル)−1−{6−[4−(4−エチル−ピペラジン−1−イル)−フェニルアミノ]−ピリミジン−4−イル}−1−メチル−尿素の結晶形態およびその塩 |
| WO2014007951A2 (en) * | 2012-06-13 | 2014-01-09 | Incyte Corporation | Substituted tricyclic compounds as fgfr inhibitors |
Family Cites Families (18)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP1801112A1 (en) | 1998-05-26 | 2007-06-27 | Warner-Lambert Company LLC | Bicyclic pyrimidines and bicyclic 3,4-dihydropyrimidines as inhibitors of cellular proliferation |
| CN1138778C (zh) * | 1998-05-26 | 2004-02-18 | 沃尼尔·朗伯公司 | 用作细胞增殖抑制剂的二环嘧啶及二环3,4-二氢嘧啶化合物及用途 |
| JP2003525897A (ja) * | 2000-03-06 | 2003-09-02 | アストラゼネカ アクチボラグ | 治 療 |
| US20030158188A1 (en) | 2002-02-20 | 2003-08-21 | Chih-Hung Lee | Fused azabicyclic compounds that inhibit vanilloid receptor subtype 1 (VR1) receptor |
| US7129351B2 (en) * | 2002-11-04 | 2006-10-31 | Hoffmann-La Roche Inc. | Pyrimido compounds having antiproliferative activity |
| US7504396B2 (en) * | 2003-06-24 | 2009-03-17 | Amgen Inc. | Substituted heterocyclic compounds and methods of use |
| AU2004260689B8 (en) * | 2003-07-29 | 2008-05-15 | Irm Llc | Compounds and compositions as protein kinase inhibitors |
| KR101347613B1 (ko) | 2004-03-31 | 2014-01-06 | 다나-파버 캔서 인스티튜트 인크. | 암에 걸린 인간 환자의 표피성장인자 수용체 표적 치료의 유효 가능성 결정 방법, 키트, 핵산 프로브 및 프라이머쌍 |
| US20090023723A1 (en) | 2005-09-21 | 2009-01-22 | Pharmacopeia Drug Discovery, Inc. | Purinone derivatives for treating neurodegenerative diseases |
| US20090312321A1 (en) * | 2006-05-15 | 2009-12-17 | Irm Llc | Compositions and methods for fgf receptor kinases inhibitors |
| WO2010129053A2 (en) | 2009-05-05 | 2010-11-11 | Dana Farber Cancer Institute | Egfr inhibitors and methods of treating disorders |
| US20120258940A1 (en) * | 2009-12-18 | 2012-10-11 | Giordano Caponigro | Method for treating haematological cancers |
| KR101301533B1 (ko) | 2010-02-09 | 2013-09-04 | 한미사이언스 주식회사 | 암세포 성장 억제 효과를 갖는 신규 피리미딘 유도체 |
| CN102816162B (zh) * | 2011-06-10 | 2016-04-27 | 中国科学院广州生物医药与健康研究院 | 嘧啶并嘧啶酮类化合物及其药用组合物和应用 |
| WO2013088191A1 (en) * | 2011-12-12 | 2013-06-20 | Institut National De La Sante Et De La Recherche Medicale (Inserm) | Antagonist of the fibroblast growth factor receptor 3 (fgfr3) for use in the treatment or the prevention of skeletal disorders linked with abnormal activation of fgfr3 |
| GB201204384D0 (en) | 2012-03-13 | 2012-04-25 | Univ Dundee | Anti-flammatory agents |
| RS62233B1 (sr) * | 2012-07-11 | 2021-09-30 | Blueprint Medicines Corp | Inhibitori receptora fibroblast faktora rasta |
| US9783504B2 (en) * | 2013-07-09 | 2017-10-10 | Dana-Farber Cancer Institute, Inc. | Kinase inhibitors for the treatment of disease |
-
2014
- 2014-07-09 US US14/903,650 patent/US9783504B2/en active Active
- 2014-07-09 EP EP14822373.8A patent/EP3019491A4/en not_active Withdrawn
- 2014-07-09 WO PCT/US2014/046022 patent/WO2015006492A1/en active Application Filing
- 2014-07-09 JP JP2016525463A patent/JP2016523973A/ja active Pending
- 2014-07-09 AU AU2014287209A patent/AU2014287209B2/en not_active Ceased
- 2014-07-09 CA CA2917667A patent/CA2917667A1/en not_active Abandoned
-
2017
- 2017-09-06 US US15/696,309 patent/US10316002B2/en not_active Expired - Fee Related
-
2019
- 2019-05-06 US US16/403,793 patent/US10906878B2/en active Active
Patent Citations (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2006000420A1 (en) * | 2004-06-24 | 2006-01-05 | Novartis Ag | Pyrimidine urea derivatives as kinase inhibitors |
| JP2009520768A (ja) * | 2005-12-21 | 2009-05-28 | ノバルティス アクチエンゲゼルシャフト | Fgf阻害剤であるピリミジニルアリールウレア誘導体 |
| JP2013512956A (ja) * | 2009-12-07 | 2013-04-18 | ノバルティス アーゲー | 3−(2,6−ジクロロ−3,5−ジメトキシ−フェニル)−1−{6−[4−(4−エチル−ピペラジン−1−イル)−フェニルアミノ]−ピリミジン−4−イル}−1−メチル−尿素の結晶形態およびその塩 |
| WO2014007951A2 (en) * | 2012-06-13 | 2014-01-09 | Incyte Corporation | Substituted tricyclic compounds as fgfr inhibitors |
Non-Patent Citations (1)
| Title |
|---|
| ZHOU, W. ET AL., CHEMISTRY & BIOLOGY, vol. 17, JPN7018001156, 2010, pages 285 - 295, ISSN: 0003908391 * |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2020121994A (ja) * | 2015-02-20 | 2020-08-13 | インサイト・コーポレイションIncyte Corporation | Fgfr阻害剤としての二環式複素環 |
Also Published As
| Publication number | Publication date |
|---|---|
| US20190256475A1 (en) | 2019-08-22 |
| US10906878B2 (en) | 2021-02-02 |
| EP3019491A4 (en) | 2016-12-21 |
| US10316002B2 (en) | 2019-06-11 |
| EP3019491A1 (en) | 2016-05-18 |
| WO2015006492A1 (en) | 2015-01-15 |
| AU2014287209B2 (en) | 2019-01-24 |
| US9783504B2 (en) | 2017-10-10 |
| CA2917667A1 (en) | 2015-01-15 |
| AU2014287209A1 (en) | 2016-01-28 |
| US20170369449A1 (en) | 2017-12-28 |
| US20160176825A1 (en) | 2016-06-23 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP2016523973A (ja) | 疾患の処置のためのキナーゼ阻害物質 | |
| EP3207035B1 (en) | Compounds and compositions for modulating egfr mutant kinase activities | |
| US11136326B2 (en) | Pyrrolopyrimidine derivatives as TAM inhibitors | |
| JP5918693B2 (ja) | Egfr阻害剤及び疾患の治療方法 | |
| JP6945015B2 (ja) | N2,n4−ジフェニルピリミジン−2,4−ジアミン誘導体、その製造方法、およびこれを有効成分として含む癌の予防または治療用の薬学的組成物 | |
| US11566028B2 (en) | Bicyclic heterocycles as FGFR inhibitors | |
| US20210094935A1 (en) | Bicyclic heterocycles as fgfr inhibitors | |
| AU2007284562A1 (en) | Using PI3K and MEK modulators in treatments of cancer | |
| KR20090103897A (ko) | 피라졸로피리미딘 화합물 | |
| KR20150104089A (ko) | 치환된 인돌-5-올 유도체와 그들의 치료적 용도 | |
| TW200934763A (en) | Peptide deformylase inhibitors | |
| TW201336847A (zh) | 喹啉基吡咯并嘧啶化合物或其鹽 | |
| WO2022047093A1 (en) | Vinyl imidazole compounds as inhibitors of kras | |
| TW201605805A (zh) | 喹唑啉酮及異喹啉酮衍生物 | |
| CA2991645A1 (en) | Novel pyrimidines as egfr inhibitors and methods of treating disorders | |
| TW201922709A (zh) | 表皮生長因子受體抑制劑 | |
| CA2974335C (en) | Novel salt of fused pyrimidine compound and crystal thereof | |
| CN101346371B (zh) | 癌症治疗中用作酪氨酸激酶抑制剂的4-(3-氨基吡唑)嘧啶衍生物 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20160328 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20170612 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20170612 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20180416 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20180713 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20180831 |
|
| A02 | Decision of refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A02 Effective date: 20181031 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20190222 |
|
| C60 | Trial request (containing other claim documents, opposition documents) |
Free format text: JAPANESE INTERMEDIATE CODE: C60 Effective date: 20190222 |
|
| A911 | Transfer to examiner for re-examination before appeal (zenchi) |
Free format text: JAPANESE INTERMEDIATE CODE: A911 Effective date: 20190301 |
|
| C21 | Notice of transfer of a case for reconsideration by examiners before appeal proceedings |
Free format text: JAPANESE INTERMEDIATE CODE: C21 Effective date: 20190304 |
|
| A912 | Re-examination (zenchi) completed and case transferred to appeal board |
Free format text: JAPANESE INTERMEDIATE CODE: A912 Effective date: 20190510 |
|
| C211 | Notice of termination of reconsideration by examiners before appeal proceedings |
Free format text: JAPANESE INTERMEDIATE CODE: C211 Effective date: 20190515 |
|
| C22 | Notice of designation (change) of administrative judge |
Free format text: JAPANESE INTERMEDIATE CODE: C22 Effective date: 20190918 |
|
| C13 | Notice of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: C13 Effective date: 20200312 |
|
| C22 | Notice of designation (change) of administrative judge |
Free format text: JAPANESE INTERMEDIATE CODE: C22 Effective date: 20200406 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20200611 |
|
| C23 | Notice of termination of proceedings |
Free format text: JAPANESE INTERMEDIATE CODE: C23 Effective date: 20201014 |
|
| C03 | Trial/appeal decision taken |
Free format text: JAPANESE INTERMEDIATE CODE: C03 Effective date: 20201111 |
|
| C30A | Notification sent |
Free format text: JAPANESE INTERMEDIATE CODE: C3012 Effective date: 20201111 |