JP2013216632A - 医薬組成物 - Google Patents
医薬組成物 Download PDFInfo
- Publication number
- JP2013216632A JP2013216632A JP2012090158A JP2012090158A JP2013216632A JP 2013216632 A JP2013216632 A JP 2013216632A JP 2012090158 A JP2012090158 A JP 2012090158A JP 2012090158 A JP2012090158 A JP 2012090158A JP 2013216632 A JP2013216632 A JP 2013216632A
- Authority
- JP
- Japan
- Prior art keywords
- pharmaceutical composition
- scopolamine
- component
- salt
- antihistamine
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Granted
Links
Images
Landscapes
- Medicinal Preparation (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Acyclic And Carbocyclic Compounds In Medicinal Compositions (AREA)
Abstract
【解決手段】本発明は、スコポラミン類に炭酸マグネシウム等の制酸剤、適宜メクリジン等の抗ヒスタミン剤を含有する医薬組成物である。
【選択図】なし
Description
一方、スコポラミンや種々の抗ヒスタミン剤は不快な味を有するため、経口固形製剤として使用するためには、コーティングを施したりカプセル剤とする等の製剤設計に基づく方法(特許文献1など)や、甘味剤を配合する方法(特許文献2、特許文献3など)など、苦味成分を物理的にマスキングすることが多い。しかしながら、コーティングやカプセル化などは煩雑な工程が必要でコストもかかり、また、スコポラミン等に糖アルコール、多価アルコール等甘味剤を配合してもその効果は十分とは言えなかった。
[項1](a)スコポラミン、メチルスコポラミン及びそれらの塩からなる群から選ばれる1種又は2種以上、及び(b)炭酸マグネシウムを含有する医薬組成物。
[項4](b)制酸剤が炭酸マグネシウムである[項2]の医薬組成物。
[項6](c)抗ヒスタミン剤がメクリジン又はその塩である[項2]〜[項4]のいずれかの医薬組成物。
[項9](a)成分1重量部に対し、(c)成分が1重量部〜500重量部で含有する[項2]〜[項8]のいずれかの医薬組成物。
[項10]成人 1日あたりの配合量が、(a)成分 0.01〜0.50mg、(b)成分 0.01〜1500mg、(c)成分 0.01〜250mgである[項2]〜[項9]のいずれかの医薬組成物。
[項12]固形剤である[項11]の鎮暈剤。
[項13]チュアブル錠である[項12]の鎮暈剤。
[項15]さらに抗ヒスタミン剤を含有する、項14の苦味緩和剤。
[項16]抗ヒスタミン剤がメグリジン又はその塩である、項15の苦味緩和剤。
[項18]スコポラミンもしくはその塩またはメチルスコポラミンもしくはその塩の苦味を緩和するための炭酸マグネシウム及び抗ヒスタミン剤の組み合わせの使用。
[項19]抗ヒスタミン剤がメグリジン又はその塩である、項18の使用。
スコポラミン類のヒトへの投与量としては、成人の場合、0.01〜0.5mg/1日で、1日1〜3回に分けて投与され得る。スコポラミン類を鎮暈剤として用いる場合、1投与単位あたりのスコポラミン類の含有量は0.01〜0.25mg、好ましくは0.1〜0.25mgである。
本発明における(a)成分の1製剤単位あたりの濃度は、通常、0.0015W/W%〜1.0W/W%であり、好ましくは、0.01W/W%〜0.6W/W%である。(a)成分を2種以上組み合わせる場合は、その総量の含有量である。
本発明における(b)成分:制酸剤の含有量は、(a)成分 1重量部に対し、1重量部〜3000重量部であり、好ましくは、1重量部〜1000重量部である。
(a)成分もしくは(b)成分を2種以上組み合わせる場合は、(a)成分の総量 1重量部に対し、(b)成分の総量は1重量部〜3000重量部であり、好ましくは、1重量部〜1000重量部である。
本発明における制酸剤の含有量は、(a)成分 0.01〜0.50mgに対し、0.01〜1500mgであり、好ましくは0.01〜1000mgである。
(a)成分もしくは(b)成分を2種以上組み合わせる場合は、(a)成分の総量 0.01〜0.50mgに対し、(b)成分の総量は0.01〜1500mgであり、好ましくは0.01〜1000mgである。
本発明における(b)成分の1製剤単位あたりの濃度は、通常、0.0015W/W%〜82.5W/W%であり、好ましくは、0.005W/W%〜60W/W%である。(b)成分を2種以上組み合わせる場合は、その総量の含有量である。
本発明における(c)成分:抗ヒスタミン剤の含有量は、スコポラミン類1重量部に対し、1重量部〜500重量部であり、好ましくは、10重量部〜350重量部である。
(a)成分もしくは(c)成分を2種以上組み合わせる場合は、(a)成分の総量 1重量部に対し、(c)成分の総量は1重量部〜500重量部であり、好ましくは、10重量部〜350重量部である。
本発明における(c)成分の含有量は、(a)成分:スコポラミン類 0.01〜0.50mgに対し、0.01〜250mgであり、好ましくは0.01〜180mgである。
(a)成分もしくは(c)成分を2種以上組み合わせる場合は、(a)成分の総量 0.01〜0.50mgに対し、(c)成分の総量は0.01〜250mgであり、好ましくは0.01〜180mgである。
本発明における(c)成分の1製剤単位あたりの濃度は、通常、0.0015W/W%〜90W/W%であり、好ましくは、0.05W/W%〜90W/W%である。(c)成分を2種以上組み合わせる場合は、その総量の含有量である。
スコポラミン以外の副交感神経遮断薬:例えば、塩酸オキシフェンサイクリミン、塩酸ジサイクロミン、塩酸メチキセン、臭化メチルアトロピン、臭化メチルアニソトロピン、臭化メチル−1−ヒヨスチアミン、臭化メチルベナクチジウム、ベラドンナエキス、ヨウ化イソプロパミド、ヨウ化ジフェニルピペリジノメチルジオキソラン、ロートエキスなど。
鎮痙薬:例えば、塩酸パパリンなど。
鎮吐薬:例えば、アミノ安息香酸エチル、シュウ酸セリウム、ピペリジルアセチルアミノ安息香エチルなど。
鎮静薬:例えば、アリルイソプロピルアセチル尿素、ブロムワレリル尿素など
強心利尿薬:例えば、カフェイン、クエン酸カフェイン、無水カフェイン、アミノフィリン、ジプロフィリン、テオフィリンなど。
これらの薬効成分で苦味が更に強くなった場合でも、本発明によりその苦味を緩和され得る。
また、本発明の医薬組成物は、更に常法によりコーティング等を施してもよい。
以下に任意に配合できる慣用成分を具体的に例示するが、本発明に用いられる成分はこれらに限定されるものではない。
抗酸化剤:ジブチルヒドロキシトルエン(BHT)、没食子酸プロピル、ブチルヒドロキシアニソール(BHA)、トコフェロール、クエン酸など。
矯味剤:アスパルテーム、アスコルビン酸、ステビア、メントール、カンゾウ粗エキス、単シロップなど。
甘味剤:ショ糖、アスパルテームなどの天然又は合成甘味剤。
香料:カンフル、ボルネオール、シンナムアルデヒドなど。
懸濁化剤:カオリン、カルメロースナトリウム、キサンタンガム、メチルセルロース、トラガントなど。
消泡剤:ジメチルポリシロキサン、シリコン消泡剤など。
粘稠剤:キサンタンガム、トラガント、メチルセルロース、デキストリンなど。
溶解補助剤:エタノール、ショ糖脂肪酸エステル、マクロゴールなど。
本発明の医薬組成物は、通常の医薬組成物と同様の方法で投与することができる。
本発明の医薬組成物の投与量は、その形態、投与方法、投与目的及び当該組成物の投与対象者の年齢、体重、症状によって適宜設定される。また、本発明の医薬組成物の経口投与は、所望の投与量範囲内において、1日あたり単回で、又は数回に分けて行ってもよく、食前、食間、食後、又は食事と同時に投与されてもよい。なお、本明細書中の用語「投与」は、「服用」を包含することを意図して用いられる。なお、本明細書中の用語は「経口投与」、「内服」と互換的に用いられ得る。
炭酸マグネシウムによるスコポラミンの苦味の緩和効果を確認するために、下記の表1に従い、各成分を秤量し、常法に従い混合したものを、試料として調製した。なお、各成分の効果を確認する際に調製した個々の成分を除いた混合試料では、除いた成分の代わりに乳糖またはバレイショデンプンを用いた。
ビジュアルアナログスケール(VAS)法を用いて、各試料の苦味の強さを評価した。具体的には、調査シートに10cmの直線を引き、この直線の左端(0cm)を0点(全く苦味がない)、右端(10cm)を10点(非常に強い苦味)とし、上記試料(混合粉)を1回あたり0.4g服用した時に感じられる「苦味」について、パネラーが感じた程度を調査シートに記載した。なおパネラーは、比較例1Aを服用するとき、苦味の強さ(スコア値)4.0点以上の苦味を感ずるものとした。また、苦味の評価は、4人のパネラーのスコア平均値及び苦味抑制率を算出することにより行った。苦味抑制率は、下記の式1により算出した。
式1:苦味抑制率(%)=
[1−(実施例の苦味の強さ:スコア値平均)/(比較例の苦味の強さ:スコア値平均)]
×100
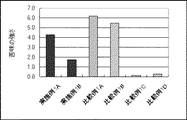
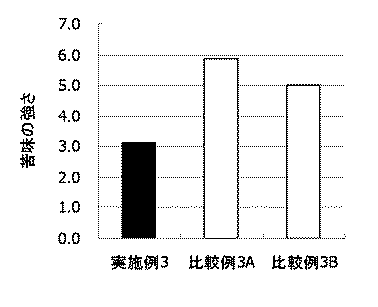
結果を表1に示し、各試料の苦味の強さをグラフにまとめた(図1および図2)。
臭化水素酸スコポラミン(比較例1A)では、いずれのパネラーも強い苦味を感じた。この苦味は、炭酸マグネシウムが加わることにより軽減した(実施例1A)。さらにメクリジン塩酸塩が加わることにより、さらに苦味は軽減され(実施例1B)、臭化水素酸スコポラミに炭酸マグネシウム及びメクリジン塩酸塩が加わることにより、より高い苦味緩和作用を得ることが出来た。
なお、乳糖に代えてバレイショデンプンで倍散とした場合も、臭化水素酸スコポラミン苦味は軽減されず(比較例1Aと比較例2との比較)、乳糖、バレイショデンプン共に苦味の緩和作用がないことを確認した。
各種制酸剤によるスコポラミンの苦味の緩和効果を確認するために、下記の表2−1及び表2−2に従い、各成分を秤量し、常法に従い混合したものを、試料として調製した。
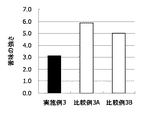
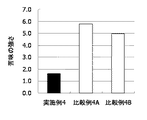
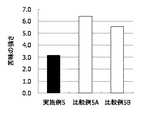
試験1と同様の方法で行った。結果を表2−1及び表2−2に示し、各試料の苦味の強さをグラフにまとめた(図2〜図5)。なお、実施例2と比較例2の結果は、試験1の結果を用いた。
炭酸マグネシウムに代えて、種々の制酸剤を臭化水素酸スコポラミン及びメクリジン塩酸塩に配合し、苦味を評価した。いずれの制酸剤の場合にも、臭化水素酸スコポラミンの苦味が低減した。炭酸マグネシウムの場合に、最も顕著な苦味緩和作用がみられた。
Claims (19)
- (a)スコポラミン、メチルスコポラミン及びそれらの塩からなる群から選ばれる1種又は2種以上、及び(b)炭酸マグネシウムを含有する医薬組成物。
- (a)スコポラミン、メチルスコポラミン及びそれらの塩からなる群より選ばれる1種又は2種以上、(b)制酸剤、及び(c)抗ヒスタミン剤を含有する医薬組成物。
- (b)制酸剤が無機系制酸剤のマグネシウム、アルミニウム、ナトリウム、カルシウムの塩、並びに、合成ヒドロタルサイトからなる群より選ばれる1種又は2種以上である請求項2の医薬組成物。
- (b)制酸剤が炭酸マグネシウムである請求項2の医薬組成物。
- (c)抗ヒスタミン剤が、メクリジン、クロルフェニラミン、ジフェンヒドラミン、ジフェニルピラリン、ジメンヒドリナート、フェネタジン、プロメタジン、ジフェニドール、フェニラミン、ジフェニルピラリン及びそれらの塩からなる群より選ばれる1種又は2種以上である請求項2〜4のいずれかの医薬組成物。
- (c)抗ヒスタミン剤がメクリジン又はその塩である請求項2〜4のいずれかの医薬組成物。
- (a)成分が臭化水素酸スコポラミンである請求項1〜6のいずれかの医薬組成物。
- (a)成分1重量部に対し、(b)成分が1重量部〜3000重量部で含有する請求項1〜7のいずれかの医薬組成物。
- (a)成分1重量部に対し、(c)成分が1重量部〜500重量部で含有する請求項2〜8のいずれかの医薬組成物。
- 成人 1日あたりの配合量が、(a)成分 0.01〜0.50mg、(b)成分 0.01〜1500mg、(c)成分 0.01〜250mgである請求項2〜9のいずれかの医薬組成物。
- 請求項1〜10のいずれかの医薬組成物を含む鎮暈剤。
- 固形剤である請求項11の鎮暈剤。
- チュアブル錠である請求項12の鎮暈剤。
- 炭酸マグネシウムを含有する、スコポラミンもしくはその塩またはメチルスコポラミンもしくはその塩の苦味緩和剤。
- さらに抗ヒスタミン剤を含有する、請求項14の苦味緩和剤。
- 抗ヒスタミン剤がメクリジン又はその塩である、請求項15の苦味緩和剤。
- スコポラミンもしくはその塩またはメチルスコポラミンもしくはその塩の苦味を緩和するための炭酸マグネシウムの使用。
- スコポラミンもしくはその塩またはメチルスコポラミンもしくはその塩の苦味を緩和するための炭酸マグネシウム及び抗ヒスタミン剤の組み合わせの使用。
- 抗ヒスタミン剤がメクリジン又はその塩である、請求項18の使用。
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2012090158A JP6088151B2 (ja) | 2012-04-11 | 2012-04-11 | 医薬組成物 |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2012090158A JP6088151B2 (ja) | 2012-04-11 | 2012-04-11 | 医薬組成物 |
Related Child Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2016207660A Division JP2017014292A (ja) | 2016-10-24 | 2016-10-24 | 医薬組成物 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2013216632A true JP2013216632A (ja) | 2013-10-24 |
| JP6088151B2 JP6088151B2 (ja) | 2017-03-01 |
Family
ID=49589204
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2012090158A Active JP6088151B2 (ja) | 2012-04-11 | 2012-04-11 | 医薬組成物 |
Country Status (1)
| Country | Link |
|---|---|
| JP (1) | JP6088151B2 (ja) |
Cited By (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2016008208A (ja) * | 2014-06-26 | 2016-01-18 | ロート製薬株式会社 | メクリジン含有医薬組成物の安定化方法 |
| CN105326803A (zh) * | 2015-12-05 | 2016-02-17 | 翔宇药业股份有限公司 | 一种用于治疗晕动症的盐酸地芬尼多片及其制备方法 |
| JP2017186313A (ja) * | 2016-03-30 | 2017-10-12 | エスエス製薬株式会社 | 経口用医薬組成物 |
| CN107334747A (zh) * | 2017-07-25 | 2017-11-10 | 东莞云森生物医药科技有限公司 | 一种预防晕动症的口香糖 |
Families Citing this family (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2017014292A (ja) * | 2016-10-24 | 2017-01-19 | ロート製薬株式会社 | 医薬組成物 |
Citations (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPH04327526A (ja) * | 1991-04-26 | 1992-11-17 | Lion Corp | 経口用固形製剤 |
| JPH0920653A (ja) * | 1995-05-02 | 1997-01-21 | Taisho Pharmaceut Co Ltd | 鎮暈剤 |
| JPH0952838A (ja) * | 1995-06-09 | 1997-02-25 | Taisho Pharmaceut Co Ltd | 経口用組成物 |
| JP2002255797A (ja) * | 2000-12-28 | 2002-09-11 | Eisai Co Ltd | 鋳型錠 |
| JP2002363105A (ja) * | 2001-05-31 | 2002-12-18 | Taiho Yakuhin Kogyo Kk | 不快な味のマスキング方法及び内服用液剤 |
| JP2009263298A (ja) * | 2008-04-28 | 2009-11-12 | Ss Pharmaceut Co Ltd | 不快な味を隠ぺいした経口組成物 |
-
2012
- 2012-04-11 JP JP2012090158A patent/JP6088151B2/ja active Active
Patent Citations (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPH04327526A (ja) * | 1991-04-26 | 1992-11-17 | Lion Corp | 経口用固形製剤 |
| JPH0920653A (ja) * | 1995-05-02 | 1997-01-21 | Taisho Pharmaceut Co Ltd | 鎮暈剤 |
| JPH0952838A (ja) * | 1995-06-09 | 1997-02-25 | Taisho Pharmaceut Co Ltd | 経口用組成物 |
| JP2002255797A (ja) * | 2000-12-28 | 2002-09-11 | Eisai Co Ltd | 鋳型錠 |
| JP2002363105A (ja) * | 2001-05-31 | 2002-12-18 | Taiho Yakuhin Kogyo Kk | 不快な味のマスキング方法及び内服用液剤 |
| JP2009263298A (ja) * | 2008-04-28 | 2009-11-12 | Ss Pharmaceut Co Ltd | 不快な味を隠ぺいした経口組成物 |
Non-Patent Citations (1)
| Title |
|---|
| JPN6016003705; 薬学雑誌 Vol.104, No.2, 1984, p.199-203 * |
Cited By (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2016008208A (ja) * | 2014-06-26 | 2016-01-18 | ロート製薬株式会社 | メクリジン含有医薬組成物の安定化方法 |
| CN105326803A (zh) * | 2015-12-05 | 2016-02-17 | 翔宇药业股份有限公司 | 一种用于治疗晕动症的盐酸地芬尼多片及其制备方法 |
| JP2017186313A (ja) * | 2016-03-30 | 2017-10-12 | エスエス製薬株式会社 | 経口用医薬組成物 |
| CN107334747A (zh) * | 2017-07-25 | 2017-11-10 | 东莞云森生物医药科技有限公司 | 一种预防晕动症的口香糖 |
Also Published As
| Publication number | Publication date |
|---|---|
| JP6088151B2 (ja) | 2017-03-01 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| US5629013A (en) | Chewable calcium carbonate antacid tablet compositions | |
| US5244670A (en) | Ingestible pharmaceutical compositions for treating upper gastrointestinal tract distress | |
| JP5979931B2 (ja) | 医薬組成物 | |
| JP6088151B2 (ja) | 医薬組成物 | |
| EP0578768A1 (en) | EDIBLE PHARMACEUTICAL COMPOSITIONS FOR TREATING DIGESTIVE PAIN PAIN. | |
| JP2023164934A (ja) | 固形医薬品 | |
| JP7397563B2 (ja) | 固形製剤 | |
| WO2014010656A1 (ja) | 優れた血中アルコール濃度低下促進剤 | |
| JP2014114253A (ja) | 生薬を含有する鎮痛抗炎症用組成物 | |
| WO2010023874A1 (ja) | ロペラミド塩酸塩含有フィルム製剤 | |
| JP2020186221A (ja) | パーキンソン病治療薬の安定化方法 | |
| JP2010241760A (ja) | 不快な味の軽減された口腔内速崩壊錠及びその製造方法 | |
| JPWO2014010658A1 (ja) | ヒハツ配合製剤 | |
| CN115666516A (zh) | 包括卡培他滨的快速分散药物组合物 | |
| CN118284415B (zh) | 一种达罗他胺药物组合物及其制备方法和用途 | |
| CN112912070A (zh) | 夜间多尿的治疗或预防剂 | |
| JP2017014292A (ja) | 医薬組成物 | |
| JP2015229664A (ja) | メクリジン含有医薬組成物 | |
| JP4131747B2 (ja) | マンニトール含有シロスタゾール口腔内崩壊散剤 | |
| JP2003095981A (ja) | 医薬組成物 | |
| JP2015229665A (ja) | メクリジン含有医薬組成物 | |
| KR101458670B1 (ko) | 분지쇄아미노산을 함유하는 약제학적 조성물 및 그 제조방법 | |
| JP5896806B2 (ja) | 内服組成物 | |
| JP6940109B2 (ja) | 認知症における認知機能改善用組成物 | |
| JP2016008208A (ja) | メクリジン含有医薬組成物の安定化方法 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20150327 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20160209 |
|
| RD04 | Notification of resignation of power of attorney |
Free format text: JAPANESE INTERMEDIATE CODE: A7424 Effective date: 20160219 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20160318 |
|
| A02 | Decision of refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A02 Effective date: 20160726 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20161025 |
|
| A911 | Transfer to examiner for re-examination before appeal (zenchi) |
Free format text: JAPANESE INTERMEDIATE CODE: A911 Effective date: 20161101 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20170110 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20170203 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 6088151 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |