JP2012252995A - 金属空気二次電池 - Google Patents
金属空気二次電池 Download PDFInfo
- Publication number
- JP2012252995A JP2012252995A JP2011178515A JP2011178515A JP2012252995A JP 2012252995 A JP2012252995 A JP 2012252995A JP 2011178515 A JP2011178515 A JP 2011178515A JP 2011178515 A JP2011178515 A JP 2011178515A JP 2012252995 A JP2012252995 A JP 2012252995A
- Authority
- JP
- Japan
- Prior art keywords
- metal
- secondary battery
- air secondary
- electrode material
- positive electrode
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Withdrawn
Links
- 229910052751 metal Inorganic materials 0.000 title claims abstract description 15
- 239000002184 metal Substances 0.000 title claims abstract description 15
- 239000011148 porous material Substances 0.000 claims abstract description 70
- 239000002245 particle Substances 0.000 claims abstract description 64
- 239000003575 carbonaceous material Substances 0.000 claims abstract description 47
- 239000007774 positive electrode material Substances 0.000 claims abstract description 40
- 239000003054 catalyst Substances 0.000 claims abstract description 39
- 229910052760 oxygen Inorganic materials 0.000 claims abstract description 25
- 239000001301 oxygen Substances 0.000 claims abstract description 25
- QVGXLLKOCUKJST-UHFFFAOYSA-N atomic oxygen Chemical compound [O] QVGXLLKOCUKJST-UHFFFAOYSA-N 0.000 claims abstract description 24
- 238000009826 distribution Methods 0.000 claims abstract description 14
- 239000007773 negative electrode material Substances 0.000 claims abstract description 14
- 229910044991 metal oxide Inorganic materials 0.000 claims abstract description 12
- 150000004706 metal oxides Chemical class 0.000 claims abstract description 12
- 239000002923 metal particle Substances 0.000 claims abstract description 11
- 239000003792 electrolyte Substances 0.000 claims abstract description 9
- 230000009467 reduction Effects 0.000 claims abstract description 9
- 229910021645 metal ion Inorganic materials 0.000 claims abstract description 7
- 239000011149 active material Substances 0.000 claims abstract description 6
- 239000012528 membrane Substances 0.000 claims abstract description 6
- BASFCYQUMIYNBI-UHFFFAOYSA-N platinum Chemical compound [Pt] BASFCYQUMIYNBI-UHFFFAOYSA-N 0.000 claims description 39
- 229910052697 platinum Inorganic materials 0.000 claims description 19
- 239000010419 fine particle Substances 0.000 claims description 11
- 238000000034 method Methods 0.000 claims description 10
- IJGRMHOSHXDMSA-UHFFFAOYSA-N Atomic nitrogen Chemical compound N#N IJGRMHOSHXDMSA-UHFFFAOYSA-N 0.000 claims description 9
- 239000006258 conductive agent Substances 0.000 claims description 8
- 230000001186 cumulative effect Effects 0.000 claims description 7
- 238000002336 sorption--desorption measurement Methods 0.000 claims description 6
- 230000006870 function Effects 0.000 claims description 5
- QSHDDOUJBYECFT-UHFFFAOYSA-N mercury Chemical compound [Hg] QSHDDOUJBYECFT-UHFFFAOYSA-N 0.000 claims description 4
- 229910052753 mercury Inorganic materials 0.000 claims description 4
- 229910052757 nitrogen Inorganic materials 0.000 claims description 3
- OKTJSMMVPCPJKN-UHFFFAOYSA-N Carbon Chemical compound [C] OKTJSMMVPCPJKN-UHFFFAOYSA-N 0.000 description 36
- 229910052799 carbon Inorganic materials 0.000 description 34
- 229910052744 lithium Inorganic materials 0.000 description 15
- 238000006243 chemical reaction Methods 0.000 description 13
- -1 nickel metal hydride Chemical class 0.000 description 11
- NUJOXMJBOLGQSY-UHFFFAOYSA-N manganese dioxide Chemical compound O=[Mn]=O NUJOXMJBOLGQSY-UHFFFAOYSA-N 0.000 description 10
- WHXSMMKQMYFTQS-UHFFFAOYSA-N Lithium Chemical compound [Li] WHXSMMKQMYFTQS-UHFFFAOYSA-N 0.000 description 8
- HBBGRARXTFLTSG-UHFFFAOYSA-N Lithium ion Chemical compound [Li+] HBBGRARXTFLTSG-UHFFFAOYSA-N 0.000 description 8
- 229910001416 lithium ion Inorganic materials 0.000 description 8
- FUJCRWPEOMXPAD-UHFFFAOYSA-N lithium oxide Chemical compound [Li+].[Li+].[O-2] FUJCRWPEOMXPAD-UHFFFAOYSA-N 0.000 description 8
- 229910001947 lithium oxide Inorganic materials 0.000 description 8
- 230000000052 comparative effect Effects 0.000 description 7
- 239000000243 solution Substances 0.000 description 7
- 239000002033 PVDF binder Substances 0.000 description 6
- HEMHJVSKTPXQMS-UHFFFAOYSA-M Sodium hydroxide Chemical compound [OH-].[Na+] HEMHJVSKTPXQMS-UHFFFAOYSA-M 0.000 description 6
- 229920002981 polyvinylidene fluoride Polymers 0.000 description 6
- 229910018071 Li 2 O 2 Inorganic materials 0.000 description 5
- 239000004698 Polyethylene Substances 0.000 description 5
- 230000005540 biological transmission Effects 0.000 description 5
- 239000008151 electrolyte solution Substances 0.000 description 5
- 229920000573 polyethylene Polymers 0.000 description 5
- 238000003860 storage Methods 0.000 description 5
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 5
- UQSXHKLRYXJYBZ-UHFFFAOYSA-N Iron oxide Chemical compound [Fe]=O UQSXHKLRYXJYBZ-UHFFFAOYSA-N 0.000 description 4
- SECXISVLQFMRJM-UHFFFAOYSA-N N-Methylpyrrolidone Chemical compound CN1CCCC1=O SECXISVLQFMRJM-UHFFFAOYSA-N 0.000 description 4
- 239000002253 acid Substances 0.000 description 4
- 239000011230 binding agent Substances 0.000 description 4
- 239000000463 material Substances 0.000 description 4
- 239000011163 secondary particle Substances 0.000 description 4
- OIFBSDVPJOWBCH-UHFFFAOYSA-N Diethyl carbonate Chemical compound CCOC(=O)OCC OIFBSDVPJOWBCH-UHFFFAOYSA-N 0.000 description 3
- RTZKZFJDLAIYFH-UHFFFAOYSA-N Diethyl ether Chemical compound CCOCC RTZKZFJDLAIYFH-UHFFFAOYSA-N 0.000 description 3
- MYMOFIZGZYHOMD-UHFFFAOYSA-N Dioxygen Chemical compound O=O MYMOFIZGZYHOMD-UHFFFAOYSA-N 0.000 description 3
- KMTRUDSVKNLOMY-UHFFFAOYSA-N Ethylene carbonate Chemical compound O=C1OCCO1 KMTRUDSVKNLOMY-UHFFFAOYSA-N 0.000 description 3
- ZMXDDKWLCZADIW-UHFFFAOYSA-N N,N-Dimethylformamide Chemical compound CN(C)C=O ZMXDDKWLCZADIW-UHFFFAOYSA-N 0.000 description 3
- 239000011247 coating layer Substances 0.000 description 3
- 239000004020 conductor Substances 0.000 description 3
- 229910001873 dinitrogen Inorganic materials 0.000 description 3
- 229910001882 dioxygen Inorganic materials 0.000 description 3
- 239000010931 gold Substances 0.000 description 3
- 230000006872 improvement Effects 0.000 description 3
- QSZMZKBZAYQGRS-UHFFFAOYSA-N lithium;bis(trifluoromethylsulfonyl)azanide Chemical compound [Li+].FC(F)(F)S(=O)(=O)[N-]S(=O)(=O)C(F)(F)F QSZMZKBZAYQGRS-UHFFFAOYSA-N 0.000 description 3
- 238000012423 maintenance Methods 0.000 description 3
- 230000014759 maintenance of location Effects 0.000 description 3
- 238000005259 measurement Methods 0.000 description 3
- PXHVJJICTQNCMI-UHFFFAOYSA-N nickel Substances [Ni] PXHVJJICTQNCMI-UHFFFAOYSA-N 0.000 description 3
- 229920001343 polytetrafluoroethylene Polymers 0.000 description 3
- 239000004810 polytetrafluoroethylene Substances 0.000 description 3
- BQCIDUSAKPWEOX-UHFFFAOYSA-N 1,1-Difluoroethene Chemical compound FC(F)=C BQCIDUSAKPWEOX-UHFFFAOYSA-N 0.000 description 2
- WNXJIVFYUVYPPR-UHFFFAOYSA-N 1,3-dioxolane Chemical compound C1COCO1 WNXJIVFYUVYPPR-UHFFFAOYSA-N 0.000 description 2
- YEJRWHAVMIAJKC-UHFFFAOYSA-N 4-Butyrolactone Chemical compound O=C1CCCO1 YEJRWHAVMIAJKC-UHFFFAOYSA-N 0.000 description 2
- NLHHRLWOUZZQLW-UHFFFAOYSA-N Acrylonitrile Chemical compound C=CC#N NLHHRLWOUZZQLW-UHFFFAOYSA-N 0.000 description 2
- XKRFYHLGVUSROY-UHFFFAOYSA-N Argon Chemical compound [Ar] XKRFYHLGVUSROY-UHFFFAOYSA-N 0.000 description 2
- 229920000049 Carbon (fiber) Polymers 0.000 description 2
- XTHFKEDIFFGKHM-UHFFFAOYSA-N Dimethoxyethane Chemical compound COCCOC XTHFKEDIFFGKHM-UHFFFAOYSA-N 0.000 description 2
- IAZDPXIOMUYVGZ-UHFFFAOYSA-N Dimethylsulphoxide Chemical compound CS(C)=O IAZDPXIOMUYVGZ-UHFFFAOYSA-N 0.000 description 2
- IAYPIBMASNFSPL-UHFFFAOYSA-N Ethylene oxide Chemical compound C1CO1 IAYPIBMASNFSPL-UHFFFAOYSA-N 0.000 description 2
- ZHNUHDYFZUAESO-UHFFFAOYSA-N Formamide Chemical compound NC=O ZHNUHDYFZUAESO-UHFFFAOYSA-N 0.000 description 2
- VVQNEPGJFQJSBK-UHFFFAOYSA-N Methyl methacrylate Chemical compound COC(=O)C(C)=C VVQNEPGJFQJSBK-UHFFFAOYSA-N 0.000 description 2
- WYURNTSHIVDZCO-UHFFFAOYSA-N Tetrahydrofuran Chemical compound C1CCOC1 WYURNTSHIVDZCO-UHFFFAOYSA-N 0.000 description 2
- 238000001994 activation Methods 0.000 description 2
- 239000003513 alkali Substances 0.000 description 2
- 239000007864 aqueous solution Substances 0.000 description 2
- 239000006229 carbon black Substances 0.000 description 2
- 239000004917 carbon fiber Substances 0.000 description 2
- 238000011161 development Methods 0.000 description 2
- 238000010586 diagram Methods 0.000 description 2
- 230000000694 effects Effects 0.000 description 2
- 238000007772 electroless plating Methods 0.000 description 2
- FKRCODPIKNYEAC-UHFFFAOYSA-N ethyl propionate Chemical compound CCOC(=O)CC FKRCODPIKNYEAC-UHFFFAOYSA-N 0.000 description 2
- 238000011156 evaluation Methods 0.000 description 2
- PCHJSUWPFVWCPO-UHFFFAOYSA-N gold Chemical compound [Au] PCHJSUWPFVWCPO-UHFFFAOYSA-N 0.000 description 2
- 229910052737 gold Inorganic materials 0.000 description 2
- HCDGVLDPFQMKDK-UHFFFAOYSA-N hexafluoropropylene Chemical group FC(F)=C(F)C(F)(F)F HCDGVLDPFQMKDK-UHFFFAOYSA-N 0.000 description 2
- XEEYBQQBJWHFJM-UHFFFAOYSA-N iron Substances [Fe] XEEYBQQBJWHFJM-UHFFFAOYSA-N 0.000 description 2
- 229910003473 lithium bis(trifluoromethanesulfonyl)imide Inorganic materials 0.000 description 2
- 229910003002 lithium salt Inorganic materials 0.000 description 2
- 238000004519 manufacturing process Methods 0.000 description 2
- VNWKTOKETHGBQD-UHFFFAOYSA-N methane Chemical compound C VNWKTOKETHGBQD-UHFFFAOYSA-N 0.000 description 2
- 239000000203 mixture Substances 0.000 description 2
- 239000004570 mortar (masonry) Substances 0.000 description 2
- 229910052759 nickel Inorganic materials 0.000 description 2
- 239000011255 nonaqueous electrolyte Substances 0.000 description 2
- 229920000642 polymer Polymers 0.000 description 2
- 239000000843 powder Substances 0.000 description 2
- 239000011164 primary particle Substances 0.000 description 2
- 239000002002 slurry Substances 0.000 description 2
- 239000002904 solvent Substances 0.000 description 2
- 238000003756 stirring Methods 0.000 description 2
- 239000000126 substance Substances 0.000 description 2
- 230000007704 transition Effects 0.000 description 2
- PYOKUURKVVELLB-UHFFFAOYSA-N trimethyl orthoformate Chemical compound COC(OC)OC PYOKUURKVVELLB-UHFFFAOYSA-N 0.000 description 2
- ZZXUZKXVROWEIF-UHFFFAOYSA-N 1,2-butylene carbonate Chemical compound CCC1COC(=O)O1 ZZXUZKXVROWEIF-UHFFFAOYSA-N 0.000 description 1
- LZDKZFUFMNSQCJ-UHFFFAOYSA-N 1,2-diethoxyethane Chemical compound CCOCCOCC LZDKZFUFMNSQCJ-UHFFFAOYSA-N 0.000 description 1
- VAYTZRYEBVHVLE-UHFFFAOYSA-N 1,3-dioxol-2-one Chemical compound O=C1OC=CO1 VAYTZRYEBVHVLE-UHFFFAOYSA-N 0.000 description 1
- JWUJQDFVADABEY-UHFFFAOYSA-N 2-methyltetrahydrofuran Chemical compound CC1CCCO1 JWUJQDFVADABEY-UHFFFAOYSA-N 0.000 description 1
- VWIIJDNADIEEDB-UHFFFAOYSA-N 3-methyl-1,3-oxazolidin-2-one Chemical compound CN1CCOC1=O VWIIJDNADIEEDB-UHFFFAOYSA-N 0.000 description 1
- OYOKPDLAMOMTEE-UHFFFAOYSA-N 4-chloro-1,3-dioxolan-2-one Chemical compound ClC1COC(=O)O1 OYOKPDLAMOMTEE-UHFFFAOYSA-N 0.000 description 1
- AETJTBDBQRMLLQ-UHFFFAOYSA-N 4-chloro-5-methyl-1,3-dioxolan-2-one Chemical compound CC1OC(=O)OC1Cl AETJTBDBQRMLLQ-UHFFFAOYSA-N 0.000 description 1
- QPLDLSVMHZLSFG-UHFFFAOYSA-N Copper oxide Chemical compound [Cu]=O QPLDLSVMHZLSFG-UHFFFAOYSA-N 0.000 description 1
- FEWJPZIEWOKRBE-JCYAYHJZSA-N Dextrotartaric acid Chemical compound OC(=O)[C@H](O)[C@@H](O)C(O)=O FEWJPZIEWOKRBE-JCYAYHJZSA-N 0.000 description 1
- YCKRFDGAMUMZLT-UHFFFAOYSA-N Fluorine atom Chemical compound [F] YCKRFDGAMUMZLT-UHFFFAOYSA-N 0.000 description 1
- 229910018068 Li 2 O Inorganic materials 0.000 description 1
- 229910001323 Li2O2 Inorganic materials 0.000 description 1
- 229910015015 LiAsF 6 Inorganic materials 0.000 description 1
- 229910013063 LiBF 4 Inorganic materials 0.000 description 1
- 229910013684 LiClO 4 Inorganic materials 0.000 description 1
- 229910013870 LiPF 6 Inorganic materials 0.000 description 1
- 229910012513 LiSbF 6 Inorganic materials 0.000 description 1
- RJUFJBKOKNCXHH-UHFFFAOYSA-N Methyl propionate Chemical compound CCC(=O)OC RJUFJBKOKNCXHH-UHFFFAOYSA-N 0.000 description 1
- 239000004743 Polypropylene Substances 0.000 description 1
- VYPSYNLAJGMNEJ-UHFFFAOYSA-N Silicium dioxide Chemical compound O=[Si]=O VYPSYNLAJGMNEJ-UHFFFAOYSA-N 0.000 description 1
- BQCADISMDOOEFD-UHFFFAOYSA-N Silver Chemical compound [Ag] BQCADISMDOOEFD-UHFFFAOYSA-N 0.000 description 1
- 230000004913 activation Effects 0.000 description 1
- 229910045601 alloy Inorganic materials 0.000 description 1
- 239000000956 alloy Substances 0.000 description 1
- 229910000147 aluminium phosphate Inorganic materials 0.000 description 1
- 229910003481 amorphous carbon Inorganic materials 0.000 description 1
- 229910052786 argon Inorganic materials 0.000 description 1
- 239000012298 atmosphere Substances 0.000 description 1
- 238000009835 boiling Methods 0.000 description 1
- 239000002134 carbon nanofiber Substances 0.000 description 1
- 239000002041 carbon nanotube Substances 0.000 description 1
- 229910021393 carbon nanotube Inorganic materials 0.000 description 1
- 239000011304 carbon pitch Substances 0.000 description 1
- 239000000969 carrier Substances 0.000 description 1
- 230000003197 catalytic effect Effects 0.000 description 1
- 239000003638 chemical reducing agent Substances 0.000 description 1
- 239000011362 coarse particle Substances 0.000 description 1
- UBEWDCMIDFGDOO-UHFFFAOYSA-N cobalt(2+);cobalt(3+);oxygen(2-) Chemical compound [O-2].[O-2].[O-2].[O-2].[Co+2].[Co+3].[Co+3] UBEWDCMIDFGDOO-UHFFFAOYSA-N 0.000 description 1
- 239000008139 complexing agent Substances 0.000 description 1
- 239000002131 composite material Substances 0.000 description 1
- 150000001875 compounds Chemical class 0.000 description 1
- 239000000470 constituent Substances 0.000 description 1
- 150000001923 cyclic compounds Chemical class 0.000 description 1
- 238000000354 decomposition reaction Methods 0.000 description 1
- 230000003247 decreasing effect Effects 0.000 description 1
- 238000003795 desorption Methods 0.000 description 1
- 238000009792 diffusion process Methods 0.000 description 1
- IEJIGPNLZYLLBP-UHFFFAOYSA-N dimethyl carbonate Chemical compound COC(=O)OC IEJIGPNLZYLLBP-UHFFFAOYSA-N 0.000 description 1
- 230000005611 electricity Effects 0.000 description 1
- 230000007613 environmental effect Effects 0.000 description 1
- JBTWLSYIZRCDFO-UHFFFAOYSA-N ethyl methyl carbonate Chemical compound CCOC(=O)OC JBTWLSYIZRCDFO-UHFFFAOYSA-N 0.000 description 1
- 239000011737 fluorine Substances 0.000 description 1
- 229910052731 fluorine Inorganic materials 0.000 description 1
- 239000007789 gas Substances 0.000 description 1
- 239000011245 gel electrolyte Substances 0.000 description 1
- 239000002241 glass-ceramic Substances 0.000 description 1
- 229910002804 graphite Inorganic materials 0.000 description 1
- 239000010439 graphite Substances 0.000 description 1
- 229910001385 heavy metal Inorganic materials 0.000 description 1
- 239000012212 insulator Substances 0.000 description 1
- 238000005342 ion exchange Methods 0.000 description 1
- 239000002608 ionic liquid Substances 0.000 description 1
- 230000002427 irreversible effect Effects 0.000 description 1
- 159000000002 lithium salts Chemical class 0.000 description 1
- 229910052987 metal hydride Inorganic materials 0.000 description 1
- 239000006262 metallic foam Substances 0.000 description 1
- 229940017219 methyl propionate Drugs 0.000 description 1
- 239000011812 mixed powder Substances 0.000 description 1
- 239000008188 pellet Substances 0.000 description 1
- ACVYVLVWPXVTIT-UHFFFAOYSA-N phosphinic acid Chemical compound O[PH2]=O ACVYVLVWPXVTIT-UHFFFAOYSA-N 0.000 description 1
- NBIIXXVUZAFLBC-UHFFFAOYSA-N phosphoric acid Substances OP(O)(O)=O NBIIXXVUZAFLBC-UHFFFAOYSA-N 0.000 description 1
- 229920002239 polyacrylonitrile Polymers 0.000 description 1
- 229920001155 polypropylene Polymers 0.000 description 1
- 238000002360 preparation method Methods 0.000 description 1
- 238000003825 pressing Methods 0.000 description 1
- RUOJZAUFBMNUDX-UHFFFAOYSA-N propylene carbonate Chemical compound CC1COC(=O)O1 RUOJZAUFBMNUDX-UHFFFAOYSA-N 0.000 description 1
- 238000012827 research and development Methods 0.000 description 1
- 229920005989 resin Polymers 0.000 description 1
- 239000011347 resin Substances 0.000 description 1
- 238000007789 sealing Methods 0.000 description 1
- 229910052709 silver Inorganic materials 0.000 description 1
- 239000004332 silver Substances 0.000 description 1
- VFWRGKJLLYDFBY-UHFFFAOYSA-N silver;hydrate Chemical compound O.[Ag].[Ag] VFWRGKJLLYDFBY-UHFFFAOYSA-N 0.000 description 1
- 239000007784 solid electrolyte Substances 0.000 description 1
- 229910052596 spinel Inorganic materials 0.000 description 1
- 239000011029 spinel Substances 0.000 description 1
- 238000004544 sputter deposition Methods 0.000 description 1
- 239000010935 stainless steel Substances 0.000 description 1
- 229910001220 stainless steel Inorganic materials 0.000 description 1
- 229920003048 styrene butadiene rubber Polymers 0.000 description 1
- HXJUTPCZVOIRIF-UHFFFAOYSA-N sulfolane Chemical compound O=S1(=O)CCCC1 HXJUTPCZVOIRIF-UHFFFAOYSA-N 0.000 description 1
- 238000012360 testing method Methods 0.000 description 1
- YLQBMQCUIZJEEH-UHFFFAOYSA-N tetrahydrofuran Natural products C=1C=COC=1 YLQBMQCUIZJEEH-UHFFFAOYSA-N 0.000 description 1
- 229910052723 transition metal Inorganic materials 0.000 description 1
- 229910000314 transition metal oxide Inorganic materials 0.000 description 1
- 238000007740 vapor deposition Methods 0.000 description 1
- 238000005406 washing Methods 0.000 description 1
- 239000013585 weight reducing agent Substances 0.000 description 1
Images
Classifications
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y02—TECHNOLOGIES OR APPLICATIONS FOR MITIGATION OR ADAPTATION AGAINST CLIMATE CHANGE
- Y02E—REDUCTION OF GREENHOUSE GAS [GHG] EMISSIONS, RELATED TO ENERGY GENERATION, TRANSMISSION OR DISTRIBUTION
- Y02E60/00—Enabling technologies; Technologies with a potential or indirect contribution to GHG emissions mitigation
- Y02E60/10—Energy storage using batteries
Landscapes
- Catalysts (AREA)
- Inert Electrodes (AREA)
- Hybrid Cells (AREA)
Abstract
【課題】良好なサイクル特性を得ることを可能にする金属空気二次電池を提供することを目的とする。
【解決手段】本発明は、金属イオンを吸蔵・放出する負極材と、酸素を活物質とする正極材と、前記負極材と前記正極材の間に設置された電解質膜を有する金属空気二次電池において、正極材の一部に、酸素還元と酸素発生の両機能を備える触媒として、粒径が1nm〜30nmの金属粒子または金属酸化物粒子を用いており、1nm〜1μmの細孔径分布において、2nm〜30nmのみに極大細孔径を有する炭素材料を、金属空気二次電池の正極に用いることにより、上記課題を解決する。
【選択図】図6
【解決手段】本発明は、金属イオンを吸蔵・放出する負極材と、酸素を活物質とする正極材と、前記負極材と前記正極材の間に設置された電解質膜を有する金属空気二次電池において、正極材の一部に、酸素還元と酸素発生の両機能を備える触媒として、粒径が1nm〜30nmの金属粒子または金属酸化物粒子を用いており、1nm〜1μmの細孔径分布において、2nm〜30nmのみに極大細孔径を有する炭素材料を、金属空気二次電池の正極に用いることにより、上記課題を解決する。
【選択図】図6
Description
本発明は負極に金属,正極活物質として空気または酸素を用いた金属空気二次電池に関するものであり、更に詳細にはサイクル特性の向上を目的として、触媒の粒径と、導電剤または触媒担体の炭素材料に関するものである。
近年、環境保護と省エネルギー化の意識の高まりから、自動車業界においては、従来のガソリンを燃料とした自動車に代わって、駆動源としてガソリンエンジンと、電気で駆動するモータを併用するハイブリッド電気自動車(HEV)や、モータのみで動く電気自動車(EV)の開発競争が激化している。電気エネルギーの供給源である蓄電池の特性は、これらの自動車の性能を大きく左右する。鉛電池やニッケル水素二次電池に比べリチウムイオン二次電池は、その軽量,高出力という特徴から、上記の自動車の蓄電池としての利用が、最も期待されている。しかし、その重量エネルギー密度は、250〜300Wh/kgが理論的上限と考えられている。電気自動車の本格的な普及には、約500Wh/kgの重量エネルギー密度が必要であると言われており、現在、蓄電池の研究開発の中心であるリチウムイオン二次電池とは、作動原理が全く異なり、より大きな重量エネルギー密度が期待できる革新型電池の開発が求められている。リチウムイオン二次電池の重量エネルギー密度を制約している要因の一つとして、コバルト酸リチウムに代表される含リチウム遷移金属酸化物の正極材料がある。その構成元素である遷移金属元素は、重金属であるため、蓄電池として組み込むと重量が増加し、結果として重量エネルギー密度が小さくなってしまう。そこで、正極材料に大気中の酸素を利用し、負極材料に金属を利用する金属空気電池が注目されている。さらに、電力貯蔵用途としても、重量低減によるコスト低減を見込めるため、金属空気電池に対する期待が高まっている。例えば、負極活物質として金属リチウムを用いたリチウム空気二次電池では、以下の反応原理により、電池としての機能を発現する。
(放電反応)
(負極側)2Li→2Li++2e- …(1) (正極側)O2+2Li++2e-→Li2O2 …(2) (全反応)2Li+O2→Li2O2 …(3) (充電反応)
(負極側)2Li←2Li++2e- …(4) (正極側)O2+2Li++2e-←Li2O2 …(5) (全反応)2Li+O2←Li2O2 …(6)
(負極側)2Li→2Li++2e- …(1) (正極側)O2+2Li++2e-→Li2O2 …(2) (全反応)2Li+O2→Li2O2 …(3) (充電反応)
(負極側)2Li←2Li++2e- …(4) (正極側)O2+2Li++2e-←Li2O2 …(5) (全反応)2Li+O2←Li2O2 …(6)
金属空気電池においては、これまで補聴器電源の亜鉛空気電池に代表されるように、一次電池としての実用化に留まっており、充放電可能な二次電池としての実用化は未だであった。
一次電池としての性能、すなわち放電特性と、触媒担体である炭素材料の物理的特性の関係は、特許文献1において報告されている。特許文献1では、アルカリ賦活処理を行った炭素材料を用いて、その放電特性の評価を行っている。アルカリ賦活処理により、炭素材料に無数の細孔が生成し、その結果、2400m2/gを超える比表面積をもつ。この大きな比表面積と、細孔容積、さらに全細孔容積に占める一次細孔容積が大きい程、大きな放電容量が得られたと報告している。しかしながら、充電反応についての言及はなく、上記の特性とサイクル特性、すなわち二次電池特性との関連についての報告はされていない。
二次電池化を阻む大きな障害として、充電時において過電圧が大きいことが挙げられる。例えば、非特許文献1では、理論開回路電圧2.96Vに対して、放電電位が2.5〜2.7Vであるものの、充電電位が4.0V以上と高く、充電過電圧が高いことが報告されている。充電過電圧が高いと、不可逆容量も大きくなり、サイクル特性も悪化すると考えられる。
これに対して、非特許文献2において、触媒に白金粒子を、触媒担体にカーボンブラックであるVulcanXC72Rを用いた正極材では、VulcanXC72Rの炭素材料単独正極材に比較して、充電過電圧が約0.7V低減し、充電電位が約3.6Vであったと報告している。しかし、本文献は初期サイクルのみの報告であり、2サイクル目以降のサイクル特性についての報告はない。さらに、触媒担体である炭素材料はVulcanXC72Rのみであり、炭素材料の構造的特徴、例えば比表面積や、細孔径分布,細孔容積の差異による二次電池特性の違いについての言及はない。
さらに、特許文献2では、金属空気二次電池の空気極に用いる触媒として、粒径が2〜500nmのペロブスカイト酸化物を用いており、粒径の規定はあるものの、触媒を担持する炭素材料の細孔または細孔径についての記述はない。
さらに、特許文献2では、金属空気二次電池の空気極に用いる触媒として、粒径が2〜500nmのペロブスカイト酸化物を用いており、粒径の規定はあるものの、触媒を担持する炭素材料の細孔または細孔径についての記述はない。
以上により、触媒粒子と触媒担体がどのような構造的特徴を有すれば、金属空気電池のサイクル特性が向上するかについて、明らかになっていないと言える。
本発明は負極に金属,正極活物質として空気または酸素を用いた金属空気二次電池において、サイクル特性の向上を目的として、触媒の粒径と同時に、導電剤または触媒担体の炭素材料が有する細孔径を規定するものである。
Takeshi Ogasawara et al,"Rechargeable Li2O2 Electrode for Lithium Batteries",Journal of the American Chemical Society 2006, 128, 1390-1393
Yang Shao-Horn et al, "The Influence of Catalysts on Discharge and Charge Voltages of Rechargeable Li-Oxygen Batteries"Electrochemical and Solid-State Letters 2010, 13(6), A69-A72
本発明の目的は負極に金属,正極活物質として空気または酸素を用いた金属空気二次電池において、サイクル特性の向上を実現することである。
本発明では、金属イオンを吸蔵・放出する負極材と、酸素を活物質とする正極材と、前記負極材と前記正極材の間に設置された電解質膜を有する金属空気二次電池において、正極材の一部に、酸素還元と酸素発生の両機能を備える触媒として、粒径が1nm〜30nmの金属粒子または金属酸化物粒子を用いており、1nm〜1μmにおける極大細孔径が少なくとも1乃至2つ存在し、且つ2nm〜30nmの範囲に存在する炭素材料を用いることを特徴とする。
本発明では、正極材として、1nm〜1μmにおける極大細孔径が2nm〜30nmの領域に存在し、それ以外の領域における微分細孔容積が、前記極大細孔径の微分細孔容積の70%以下である炭素材料を用いることを特徴とする。
本発明では、前記炭素材料が、導電剤または触媒の担体であることを特徴とする。
本発明では、窒素吸脱着法と水銀ポロシメータにより求めた細孔径を有する炭素材料を用いることを特徴とする。
本発明では、酸素還元と酸素発生の両機能を備える触媒として白金微粒子を用いることを特徴とする。
本発明では、3.6nm〜200nmにおける累積細孔容積の、3.6nm〜1μmにおける累積細孔容積に対する割合が70%以上である前記炭素材料を用いることを特徴とする。
本発明では、触媒に白金粒子を用いた場合、2.0V〜4.0Vの範囲において、作動させることを特徴とする。
また、本発明では、金属イオンを吸蔵・放出する負極材と、酸素を活物質とする正極材と、前記負極材と前記正極材の間に設置された電解質膜を有する金属空気二次電池において、正極材は、粒子径が1nm〜500nmの金属粒子または金属酸化物粒子と、1nm〜1μmの細孔径分布において2nm〜30nmの範囲に極大細孔径が存在する炭素材料と、を有することを特徴とする。
また、本発明では、金属イオンを吸蔵・放出する負極材と、酸素を活物質とする正極材と、前記負極材と前記正極材の間に設置された電解質膜を有する金属空気二次電池において、正極材は、粒子径が1nm〜500nmの金属粒子または金属酸化物粒子と、1nm〜1μmの細孔径分布において2nm〜30nmの範囲に極大細孔径が存在する炭素材料と、を有することを特徴とする。
本発明によれば、負極に金属,正極活物質として空気または酸素を用いた金属空気二次電池において、導電剤または触媒担体の炭素材料が有する細孔径と、触媒の粒径を規定することでサイクル特性の向上を達成することができる。なお、上記した以外の課題、構成及び効果は、以下の実施形態の説明により明らかにされる。
本発明は、一定範囲内のみに極大細孔径を有する導電剤または触媒担体の炭素材料と、一定範囲内の粒径をもつ触媒粒子を用いることにより、良好なサイクル特性に寄与する金属空気二次電池であることを特徴とする。
本発明では、1nm〜1μmの細孔径分布において、2nm〜30nmのみに極大細孔径を有する炭素材料を、導電剤または触媒担体として用いる。
本発明に用いる金属粒子または金属酸化物粒子は、金属空気二次電池における酸素触媒活性がある物質であればいずれでも構わない。金属では、例えば白金(Pt),金(Au),銀(Ag)などを用いることが可能である。金属酸化物では、二酸化マンガン(MnO2),酸化鉄(FeO,Fe2O3,Fe3O4),酸化コバルト(Co3O4),酸化銀(Ag2O),酸化銅(CuO),ABO3で表わされるペロブスカイト型酸化物,AB2X4で表わされるスピネル型化合物などが可能である。
金属粒子または金属酸化物粒子は、1nm〜500nmの粒子径が望ましく、特に、1nm〜30nmの粒子径が望ましい。粒子径は、透過型電子顕微鏡(TEM)により測定した。本発明に用いる1nm〜30nmの粒子径をもつ金属粒子または金属酸化物粒子を炭素材表面に担持させる方法として、スパッタリング法、蒸着法が挙げられる。特に、白金微粒子については、塩化白金酸(H2PtCl6)を用いた無電解めっき法が有効である。
金属粒子または金属酸化物粒子は、1nm〜500nmの粒子径が望ましく、特に、1nm〜30nmの粒子径が望ましい。粒子径は、透過型電子顕微鏡(TEM)により測定した。本発明に用いる1nm〜30nmの粒子径をもつ金属粒子または金属酸化物粒子を炭素材表面に担持させる方法として、スパッタリング法、蒸着法が挙げられる。特に、白金微粒子については、塩化白金酸(H2PtCl6)を用いた無電解めっき法が有効である。
本発明に用いる触媒粒子は、導電剤または触媒担体の炭素材料の表面上に、担持されている構造が、一般的であるが、触媒粒子と上記炭素材料が混合している構造でも構わない。
本発明に用いる正極材に含まれる導電剤または担体は、一般に黒鉛,メソフェ−ズ炭素,カーボンブラック,活性炭,非結晶性炭素,炭素繊維,気相成長法炭素繊維,カーボンナノチューブ,ピッチ系炭素質材料,ポリアクリロニトリル系炭素繊維などの導電性を伴う炭素材料であればいずれでも構わない。特に、比表面積が大きい炭素材料を用いることが望ましい。比表面積が大きいと、触媒粒子の分散性が向上し、過電圧の低減とサイクル特性の向上に寄与するからである。比表面積は、1m2/g〜1500m2/g、特に100m2/g〜1500m2/gが望ましい。一次粒子径は、1nm〜100nm、特に1nm〜50nmが望ましい。二次粒子径は、1μm以下であることが望ましい。1μm以上になると、二次粒子間の隙間が細孔として存在する可能性があるからである。ただし、導電剤の役割のみを担う炭素材料については、導電性があれば、細孔径、比表面積に関わらず、用いることができる。
比表面積は、窒素ガス吸脱着法で測定し、粒子径は、透過型電子顕微鏡(TEM)により測定した。一次粒子径及び二次粒子径は、それぞれ平均粒子径であり、粉体の粒径分布において,ある粒子径より大きい個数又は体積が,全粉体のそれの50%をしめるときの粒子径で定義される(D50)。粒子の形状が一様でないため、粒径を粒子の輪郭線上の任意の2点間距離のうち、最大の長さとし、平均粒径は30個から求めた平均値とした。
比表面積は、窒素ガス吸脱着法で測定し、粒子径は、透過型電子顕微鏡(TEM)により測定した。一次粒子径及び二次粒子径は、それぞれ平均粒子径であり、粉体の粒径分布において,ある粒子径より大きい個数又は体積が,全粉体のそれの50%をしめるときの粒子径で定義される(D50)。粒子の形状が一様でないため、粒径を粒子の輪郭線上の任意の2点間距離のうち、最大の長さとし、平均粒径は30個から求めた平均値とした。
本発明における負極金属としては、リチウムの他に、リチウムとの合金を用いても良い。また、金属空気二次電池として使われる負極金属であればいずれでも構わない。
本発明に用いる正極材に含まれる導電剤または担体は、バインダと混合後、スラリーを作製してカーボンペーパに塗布するか、または金属性のフォームに含浸しても構わない。
また混合した粉末をペレット成形して正極材として用いても構わない。
また混合した粉末をペレット成形して正極材として用いても構わない。
本発明に用いる電解液としては、一般的にリチウムイオン二次電池などで用いる非水系電解液を用いることができる。例えばプロピレンカーボネート,エチレンカーボネート,ブチレンカーボネート,ビニレンカーボネート,γ−ブチロラクトン,ジメチルカーボネート,ジエチルカーボネート,メチルエチルカーボネート,1,2−ジメトキシエタン,2−メチルテトラヒドロフラン,ジメチルスルフォキシド,1,3−ジオキソラン,ホルムアミド,ジメチルホルムアミド,プロピオン酸メチル,プロピオン酸エチル,リン酸トリエステル,トリメトキシメタン,ジオキソラン,ジエチルエーテル,スルホラン,3−メチル−2−オキサゾリジノン,テトラヒドロフラン,1,2−ジエトキシエタン,クロルエチレンカーボネート,クロルプロピレンカーボネートより選択された一種類の溶媒または複数の混合物でも構わない。望ましくは、高沸点の環状化合物を用いるのが良い。さらに、エチレンオキシド,アクリロニトリル,フッ化ビニリデン,メタクリル酸メチル,ヘキサフルオロプロピレンなどの高分子に保持させた固体電解質や、イオン液体を、非水電解液の代わりに使用しても良い。
本発明に用いる電解質としては、一般的にリチウムイオン二次電池などで用いる電解質を用いることができる。例えば、化学式でLiPF6,LiBF4,LiClO4,LiCF3SO3,LiCF3CO2,LiAsF6,LiSbF6,LiTFSI、あるいはリチウムトリフルオロメタンスルホンイミドで代表されるリチウムのイミド塩などの多種類のリチウム塩などが可能である。
また、エチレンオキシド,アクリロニトリル,フッ化ビニリデン,メタクリル酸メチル,ヘキサフルオロプロピレンの高分子内に、上述した非水電解液を含浸させたゲル電解質を、使用しても良い。
本発明に用いる正極材に含まれる結着材としては、一般的にリチウムイオン二次電池などで用いる結着材を用いることができる。例えばポリフッ化ビニリデン(PVDF),ポリテトラフルオロエチレン(PTFE)などのフッ素系樹脂,スチレンブタジエンゴム(SBR)などを用いることが可能である。
本発明に用いるセパレータとしては、一般的にリチウムイオン二次電池などで用いるセパレータを用いることができる。例えばポリエチレン,ポリプロピレンなどの多孔質セパレータや、金属イオン導電性を有するガラスセラミックスなどを用いることが可能である。
本発明に用いる集電体は、SUSメッシュの他、ニッケルメッシュ,ステンレスメッシュ,金メッシュなど導電性のある金属性のメッシュであればいずれでも構わない。
本発明に用いるセルの形体は、金属空気電池反応が確認できるものであれば、スエジロック型,平板型,円筒型などのいずれでも構わない。すなわち本発明は、セルの形体に依存しない。
図1に本発明の実施例による金属空気二次電池を示す。以下、負極として金属リチウムを用い、電解液として非水溶媒を用いたリチウム空気二次電池について説明する。
以下、本発明の好ましい実施形態を詳細に説明する。実施例に相当する炭素材料の一例として、1nm〜1μmの範囲において、2nm〜30nmのみに極大細孔径を有するカーボンAを用いた。実施例1、2は、担体である炭素材の細孔径のみの規定であり、実施例3は、炭素材の細孔径に加えて、触媒の粒径を規定したものである。
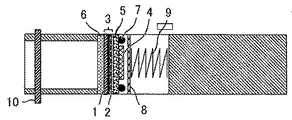
本実施例においては、スエジロック型セルのリチウム空気二次電池を作製した。図1に、スエジロック型セルの模式図を示す。セルの組み立ては、グローブボックス内で行った。
厚さ370μm,直径12mmのカーボンペーパ1には、白金微粒子,カーボンAとバインダであるポリフッ化ビニリデン(PVDF)の複合材(カーボン塗布層2)が塗布してある。これをカーボンペーパ正極材3とした。カーボンペーパ正極材3と負極のリチウム金属4は、ポリエチレン製セパレータ5により絶縁した。負極のリチウム金属4は、直径8mm,厚さ1mmにくり抜いたものを使用した。ポリエチレン製セパレータ5は、直径14mmにくり抜いたものを使用した。リチウム金属4の表面と、カーボン塗布層2の表面に、電解液を数滴滴下し、ポリエチレン製セパレータ5に含浸した。電解液は、電解質である1M LiTFSIを含んだエチレンカーボネート(EC)/ジエチルカーボネート(DEC)=3/7を用いた。カーボンペーパ1の反対側には、厚さ1mmのSUS製メッシュ(100メッシュ)からなる集電体6を配置した。リチウム金属の周りにOリング7を配置し、リチウム金属4の後ろから、押さえ板8をあて、その後ろに絞め付けバネ9をおいた。これにより、リチウム金属4−セパレータ5−カーボンペーパ正極材3が密着される構造となる。次に、集電体6の外部から酸素ガス(99.9%)を流量500ml/分でセル内部に流した。約60分酸素ガスを流し、セルに付けた酸素封入弁10を閉じ、セル内部に酸素ガスを封入した。
次に、正極の作製方法を詳述する。カーボンA50重量部と、白金微粒子(平均粒径5nm)40重量部,ポリフッ化ビニリデン(PVDF)40重量部,少量のN−メチル−2−ピロリドン(NMP)をメノウ乳鉢に添加し、良くかき混ぜた。生成したスラリー液を、φ12mmのPTFE処理済みのカーボンペーパに塗布し、大気中80℃、1時間乾燥後、さらに真空中120℃、3時間乾燥を行い、カーボンペーパ正極材3とした。
上記正極材を組み込んで、作製したセルを端子付きデシケータにいれ、デシケータ内部にアルゴンガスを封入した。デシケータの外側端子を充放電評価装置にとりつけ、セルの充放電評価を実施した。充放電条件は、放電:CC 0.1mA/cm2 2.0Vカットオフ、充電:CC 0.1mA/cm2 4.0Vカットオフ、休止時間は充放電後それぞれ1時間とし、10サイクル試験を行った。
〔比較例1〜4〕
実施例1において、正極材の担体であるカーボンAに替えて、カーボンB,カーボンC,カーボンD,VulcanXC72R、のいずれかを用いた以外は同様である。
実施例1において、正極材の担体であるカーボンAに替えて、カーボンB,カーボンC,カーボンD,VulcanXC72R、のいずれかを用いた以外は同様である。
実施例1において、触媒である白金微粒子に替えて、電解二酸化マンガン粒子(平均粒径3μm)を用いた以外は同様である。
〔比較例5〕
実施例2において、正極材の担体であるカーボンAに替えて、カーボンCを用いた以外は同様である。
実施例2において、正極材の担体であるカーボンAに替えて、カーボンCを用いた以外は同様である。
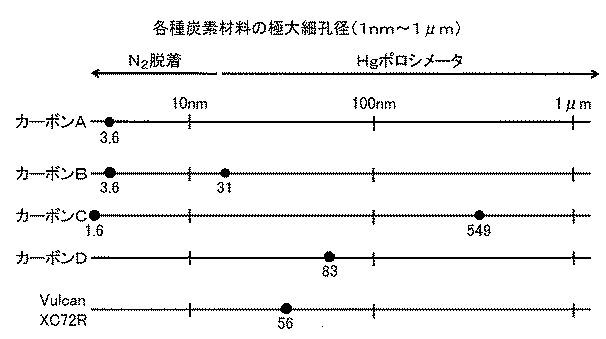
(細孔径分布の測定)
まず、1〜20nmの範囲は窒素ガス吸脱着法を用いて、20nm〜1μmの範囲は水銀ポロシメータを用いることにより、各種担体である炭素材料の細孔径分布を調べた。窒素ガス吸脱着法による測定では、脱着のデータを採用した。表1に、各種炭素材料の比表面積,細孔径分布において極大値を示した細孔径と微分細孔容積,一定の細孔径範囲における累積細孔容積を示す。また、図2に、カーボンAの細孔径分布を示す。二次粒子間の隙間を除くため、1μm以上の細孔径は除外した。この細孔径分布に示すように、カーボンAは3.6nmに極大細孔径を有し、その微分細孔容積は0.81cc/gである。この細孔径以外の領域においては、0.41cc/g以下であり、前記微分細孔容積の70%以下である。このため、カーボンAは、より優先して2〜30nmの領域に細孔が多い材料である。
まず、1〜20nmの範囲は窒素ガス吸脱着法を用いて、20nm〜1μmの範囲は水銀ポロシメータを用いることにより、各種担体である炭素材料の細孔径分布を調べた。窒素ガス吸脱着法による測定では、脱着のデータを採用した。表1に、各種炭素材料の比表面積,細孔径分布において極大値を示した細孔径と微分細孔容積,一定の細孔径範囲における累積細孔容積を示す。また、図2に、カーボンAの細孔径分布を示す。二次粒子間の隙間を除くため、1μm以上の細孔径は除外した。この細孔径分布に示すように、カーボンAは3.6nmに極大細孔径を有し、その微分細孔容積は0.81cc/gである。この細孔径以外の領域においては、0.41cc/g以下であり、前記微分細孔容積の70%以下である。このため、カーボンAは、より優先して2〜30nmの領域に細孔が多い材料である。
図3に、実施例1と比較例1〜4の放電容量維持率の結果を、表2に初回サイクルのR値を示す。ここで、R値とは(充電容量/放電容量)×100(%)で定義される値であり、リチウムイオン二次電池における充放電効率に相当する。
カーボンAを用いると、2サイクル目の放電容量維持率は約80%であり、その後も良好なサイクル特性が得られた。その初期サイクルのR値は65%であった。一方、それ以外の炭素材料を用いた場合には、2サイクル目の放電容量維持率は約20%以下、初期サイクルのR値もVulcanXC72Rを除くと20%以下と低く、カーボンAを用いた時と比較して、サイクル特性が良くないことがわかった。カーボンAは1nm〜1μmの細孔径分布において、2〜30nmのみに極大細孔径を有するため、放電生成物であるリチウム酸化物(Li2O,Li2O2)が細かく分散する。また、3.6nm〜200nmにおける累積細孔容積が、3.6nm〜1μmにおける累積細孔容積の70%以上を占めるため、細かいリチウム酸化物の生成量も多くなる。これらの細かいリチウム酸化物は、充電反応において分解され易いため、サイクル特性が向上したと考えられる。一方、それ以外の炭素材料では、細孔径が30nm以上の大きな細孔を有するため、放電反応において、粗大化したリチウム酸化物が生成する。このリチウム酸化物は絶縁物であるため、充電反応において、これらを分解するために多大なエネルギーを要し、分解されないリチウム酸化物が残存すると考えられる。この原因のため、サイクル特性が悪化したと考えられる。
次に、図4に、実施例2と比較例5の放電容量維持率の結果を示す。触媒である二酸化マンガン粒子の平均粒径は3μmであり、図3の白金微粒子程には粒径が細かくないため、粒子が粗大化していると思われる。しかしながら、二酸化マンガンを用いても、実施例2にあるカーボンAの方が、比較例5にあるカーボンCよりもサイクル特性が良い。尚、二酸化マンガンの粒径を1nm〜30nmにすれば、実施例2よりもさらに良好な結果が得られると期待される。従って、触媒の種類,触媒の粒径に関わらず、カーボンAの有効性が証明された。以上により、2nm〜30nmの範囲にのみに、極大細孔径を有する炭素材料を担体に用いることにより、サイクル特性を向上することができる。なお、極大細孔径の数は、1個に限定されるものではなく、上記範囲内に複数存在してもよい。
実施例1、2において、触媒粒径の規定はなかった。透過型電子顕微鏡により触媒である白金粒子を観察したところ、数ナノメートルの微粒子と同時に、100nm以上の粗大粒子も見つかった。そこで、以下のような無電解めっき法を用いることにより、粒径数nmの白金微粒子のみを炭素材表面に担持させた。
1Lビーカーに、カーボンA 1gと純水(イオン交換水)600ccを混合し、超音波を加えながら約30分撹拌した。その後、撹拌しながら、塩化白金酸(H2PtCl6)溶液3.55gを少しずつ添加し、さらに1時間撹拌した。次に、錯化剤であるL−酒石酸0.077gと還元剤である次亜リン酸(H3PO2)1.35gを添加し、1M NaOH水溶液により、PHを4付近に調整した。その後、純水を加えて、全溶液量を500mlにしてから、90℃のウォーターバスに投入し、溶液の温度を90℃に昇温した。そのまま、溶液の温度を90℃に保ちながら、撹拌を4時間続けた。塩化白金酸(H2PtCl6)の還元に伴い、PHが低下するため、1M NaOH水溶液を添加することにより、溶液のPHを4付近に維持した。塩化白金酸(H2PtCl6)が完全に消滅し、反応が終了したら、溶液をろ過し、純水(200ml/回)による洗浄、ろ過を5回以上繰り返した。洗浄後の作製サンプルは、恒温槽にて大気中、80℃で12時間乾燥させた。乾燥後のサンプルは、乳鉢にて粉砕してから、電極作製用に用いた。透過型電子顕微鏡による観察により、カーボンAに担持された白金微粒子の粒径は1nm〜3nmであった。電極作製方法は、実施例1と同様である。
1Lビーカーに、カーボンA 1gと純水(イオン交換水)600ccを混合し、超音波を加えながら約30分撹拌した。その後、撹拌しながら、塩化白金酸(H2PtCl6)溶液3.55gを少しずつ添加し、さらに1時間撹拌した。次に、錯化剤であるL−酒石酸0.077gと還元剤である次亜リン酸(H3PO2)1.35gを添加し、1M NaOH水溶液により、PHを4付近に調整した。その後、純水を加えて、全溶液量を500mlにしてから、90℃のウォーターバスに投入し、溶液の温度を90℃に昇温した。そのまま、溶液の温度を90℃に保ちながら、撹拌を4時間続けた。塩化白金酸(H2PtCl6)の還元に伴い、PHが低下するため、1M NaOH水溶液を添加することにより、溶液のPHを4付近に維持した。塩化白金酸(H2PtCl6)が完全に消滅し、反応が終了したら、溶液をろ過し、純水(200ml/回)による洗浄、ろ過を5回以上繰り返した。洗浄後の作製サンプルは、恒温槽にて大気中、80℃で12時間乾燥させた。乾燥後のサンプルは、乳鉢にて粉砕してから、電極作製用に用いた。透過型電子顕微鏡による観察により、カーボンAに担持された白金微粒子の粒径は1nm〜3nmであった。電極作製方法は、実施例1と同様である。
〔参考例1〕
実施例1における10サイクルまでのR値を参考例とする。
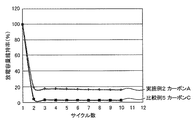
図6に、実施例3と参考例のR値の推移を示す。実施例3では、参考例に比べて、触媒である白金粒子の粒径が、さらに小さくなったことにより、放電反応に伴って白金粒子表面に生成するリチウム酸化物も、微粒子化される。さらに、白金粒子の微粒子化と同時に、2nm〜30nmの範囲内にある炭素材の細孔径のために、サイクル経過に伴う白金粒子の粗大化も抑制されると考えられる。透過型電子顕微鏡による観察の結果、30サイクル経過後の白金粒子の粒径は、最大30nmであった。以上の効果により、充電反応におけるリチウム酸化物の分解が、円滑に進行するようになった結果、充放電効率に相当するR値の向上につながったと推察される。
実施例1における10サイクルまでのR値を参考例とする。
図6に、実施例3と参考例のR値の推移を示す。実施例3では、参考例に比べて、触媒である白金粒子の粒径が、さらに小さくなったことにより、放電反応に伴って白金粒子表面に生成するリチウム酸化物も、微粒子化される。さらに、白金粒子の微粒子化と同時に、2nm〜30nmの範囲内にある炭素材の細孔径のために、サイクル経過に伴う白金粒子の粗大化も抑制されると考えられる。透過型電子顕微鏡による観察の結果、30サイクル経過後の白金粒子の粒径は、最大30nmであった。以上の効果により、充電反応におけるリチウム酸化物の分解が、円滑に進行するようになった結果、充放電効率に相当するR値の向上につながったと推察される。
上述のように、本発明では、金属イオンを吸蔵・放出する負極材と、酸素を活物質とする正極材と、前記負極材と前記正極材の間に設置された電解質膜を有する金属空気二次電池において、正極材は、粒子径が1nm〜500nmの金属粒子または金属酸化物粒子と、1nm〜1μmの細孔径分布において2nm〜30nmの範囲に極大細孔径が存在する炭素材料と、を有することを特徴とする。
本発明によれば、金属粒子又は金属酸化物粒子の粒子径と、炭素材料の細孔径を、上記範囲に規定した正極材を、金属空気二次電池に用いることで、サイクル特性の向上を達成することができる。
なお、炭素材料の極大細孔径は1つに限定されるものではなく、複数存在してもよい。
本発明によれば、金属粒子又は金属酸化物粒子の粒子径と、炭素材料の細孔径を、上記範囲に規定した正極材を、金属空気二次電池に用いることで、サイクル特性の向上を達成することができる。
なお、炭素材料の極大細孔径は1つに限定されるものではなく、複数存在してもよい。
1 カーボンペーパ
2 カーボン塗布層
3 カーボンペーパ正極材
4 負極(リチウム金属)
5 ポリエチレン製セパレータ
6 集電体
7 Oリング
8 押さえ板
9 絞め付けバネ
10 酸素封入弁
2 カーボン塗布層
3 カーボンペーパ正極材
4 負極(リチウム金属)
5 ポリエチレン製セパレータ
6 集電体
7 Oリング
8 押さえ板
9 絞め付けバネ
10 酸素封入弁
Claims (10)
- 金属イオンを吸蔵・放出する負極材と、酸素を活物質とする正極材と、前記負極材と前記正極材の間に設置された電解質膜を有する金属空気二次電池において、正極材の一部に、酸素還元と酸素発生の両機能を備える触媒として、粒径が1nm〜30nmの金属粒子または金属酸化物粒子を用いており、1nm〜1μmにおける極大細孔径が少なくとも1乃至2つ存在し、且つ、2nm〜30nmの範囲に存在する炭素材料を用いることを特徴とする金属空気二次電池。
- 請求項1に記載の金属空気二次電池において、正極材として、1nm〜1μmにおける極大細孔径が2nm〜30nmの領域に存在し、それ以外の領域における微分細孔容積が、前記極大細孔径の微分細孔容積の70%以下である炭素材料を用いることを特徴とする金属空気二次電池。
- 請求項1〜2に記載の金属空気二次電池において、前記炭素材料が、導電剤または触媒の担体であることを特徴とする金属空気二次電池。
- 請求項1〜3に記載の金属空気二次電池において、窒素吸脱着法と水銀ポロシメータにより求めた細孔径を有する炭素材料を用いることを特徴とする金属空気二次電池。
- 請求項1〜4に記載の金属空気二次電池において、酸素還元と酸素発生の両機能を備える触媒として白金微粒子を用いることを特徴とする金属空気二次電池。
- 請求項1〜5に記載の金属空気二次電池において、3.6nm〜200nmにおける累積細孔容積の、3.6nm〜1μmにおける累積細孔容積に対する割合が70%以上である前記炭素材料を用いることを特徴とする金属空気二次電池。
- 請求項1〜6に記載の金属空気二次電池において、触媒に白金粒子を用いた場合、2.0V〜4.0Vの範囲において、作動させることを特徴とする金属空気二次電池。
- 金属イオンを吸蔵・放出する負極材と、酸素を活物質とする正極材と、前記負極材と前記正極材の間に設置された電解質膜を有する金属空気二次電池において、
前記正極材は、
粒子径が1nm〜500nmの金属粒子または金属酸化物粒子と、
1nm〜1μmの細孔径分布において2nm〜30nmの範囲に極大細孔径が存在する炭素材料と、
を有することを特徴とする金属空気二次電池。 - 請求項8に記載の金属空気二次電池において、前記金属粒子又は金属酸化物粒子は、粒子径が1nm以上30nm以下の範囲にあることを特徴とする金属空気二次電池。
- 請求項8又は9に記載の金属空気二次電池において、前記炭素材料は、極大細孔径が少なくとも1乃至複数存在することを特徴とする金属空気二次電池。
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2011178515A JP2012252995A (ja) | 2011-05-10 | 2011-08-17 | 金属空気二次電池 |
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2011104839 | 2011-05-10 | ||
| JP2011104839 | 2011-05-10 | ||
| JP2011178515A JP2012252995A (ja) | 2011-05-10 | 2011-08-17 | 金属空気二次電池 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| JP2012252995A true JP2012252995A (ja) | 2012-12-20 |
Family
ID=47525611
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2011178515A Withdrawn JP2012252995A (ja) | 2011-05-10 | 2011-08-17 | 金属空気二次電池 |
Country Status (1)
| Country | Link |
|---|---|
| JP (1) | JP2012252995A (ja) |
Cited By (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2013206723A (ja) * | 2012-03-28 | 2013-10-07 | Honda Motor Co Ltd | 二次電池 |
| WO2013179807A1 (ja) * | 2012-05-30 | 2013-12-05 | 株式会社 日立製作所 | 金属空気二次電池 |
| JP2017157505A (ja) * | 2016-03-04 | 2017-09-07 | 日本電信電話株式会社 | リチウム空気二次電池 |
| JPWO2020235638A1 (ja) * | 2019-05-23 | 2020-11-26 |
-
2011
- 2011-08-17 JP JP2011178515A patent/JP2012252995A/ja not_active Withdrawn
Cited By (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2013206723A (ja) * | 2012-03-28 | 2013-10-07 | Honda Motor Co Ltd | 二次電池 |
| WO2013179807A1 (ja) * | 2012-05-30 | 2013-12-05 | 株式会社 日立製作所 | 金属空気二次電池 |
| JP2017157505A (ja) * | 2016-03-04 | 2017-09-07 | 日本電信電話株式会社 | リチウム空気二次電池 |
| JPWO2020235638A1 (ja) * | 2019-05-23 | 2020-11-26 | ||
| WO2020235638A1 (ja) * | 2019-05-23 | 2020-11-26 | 国立研究開発法人物質・材料研究機構 | 多孔炭素構造体、その製造方法、それを用いた正極材及びそれを用いた電池 |
| JP7177547B2 (ja) | 2019-05-23 | 2022-11-24 | 国立研究開発法人物質・材料研究機構 | 多孔炭素構造体、その製造方法、それを用いた正極材及びそれを用いた電池 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| US20120115048A1 (en) | Positive electrode for lithium air battery, method of preparing the positive electrode, and lithium air battery including the positive electrode | |
| KR101851317B1 (ko) | 다공성 탄소계 복합재료, 이를 포함하는 양극 및 리튬공기전지, 및 이의 제조방법 | |
| JP5373966B2 (ja) | 空気極および金属空気電池 | |
| JP5625059B2 (ja) | 金属空気二次電池 | |
| US20120115047A1 (en) | Positive electrode for lithium air battery, method of preparing the same, and lithium air battery employing the positive electrode | |
| JP5273256B2 (ja) | 非水電解質および金属空気電池 | |
| JP5580931B2 (ja) | 金属−空気二次電池用正極触媒及び金属−空気二次電池 | |
| JP5427661B2 (ja) | 金属空気二次電池 | |
| KR20150020227A (ko) | 탄소-담지 망간 산화물 촉매의 제조 방법 및 재충전가능한 리튬-에어 배터리에서의 그의 용도 | |
| KR101484503B1 (ko) | 리튬-공기 전지용 양극 촉매, 그의 제조방법 및 그를 포함하는 리튬-공기 전지 | |
| CN101604750A (zh) | 一种锂离子电池负极材料的制备方法 | |
| KR101590678B1 (ko) | 리튬 이차전지용 음극 활물질 및 이를 포함하는 리튬 이차전지 | |
| JPWO2016132932A1 (ja) | 酸素還元反応用触媒及び金属空気二次電池用空気極 | |
| US9318783B2 (en) | Positive electrode for lithium air battery, method of preparing same, and lithium air battery including same | |
| JP2012252995A (ja) | 金属空気二次電池 | |
| KR101512349B1 (ko) | 나트륨 이차전지용 양극 활물질 및 이의 제조방법 | |
| JP2013118145A (ja) | 金属空気二次電池 | |
| KR102231210B1 (ko) | 리튬 공기 전지용 양극, 이의 제조 방법 및 이를 포함하는 리튬 공기 전지 | |
| KR20130117351A (ko) | 이차전지용 전극 및 이를 포함하는 이차전지 | |
| KR102452938B1 (ko) | 리튬 금속 전지용 전해질 및 이를 포함하는 리튬 금속 전지 | |
| JP2014022210A (ja) | 金属空気二次電池用炭素材料並びにこれを用いた金属空気二次電池用正極部材及び金属空気二次電池 | |
| WO2020255489A1 (ja) | 負極材、負極、電池セル | |
| JP5593169B2 (ja) | 金属空気二次電池 | |
| JP2022076603A (ja) | リチウム-硫黄系二次電池用電解液およびリチウム-硫黄系二次電池 | |
| KR101466397B1 (ko) | 리튬이차전지의 음극전극, 이의 제조방법, 및 상기 음극전극을 포함하는 리튬 이차전지 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A300 | Application deemed to be withdrawn because no request for examination was validly filed |
Free format text: JAPANESE INTERMEDIATE CODE: A300 Effective date: 20141104 |