JP2012191874A - 核酸分析デバイス、及び核酸分析装置 - Google Patents
核酸分析デバイス、及び核酸分析装置 Download PDFInfo
- Publication number
- JP2012191874A JP2012191874A JP2011057091A JP2011057091A JP2012191874A JP 2012191874 A JP2012191874 A JP 2012191874A JP 2011057091 A JP2011057091 A JP 2011057091A JP 2011057091 A JP2011057091 A JP 2011057091A JP 2012191874 A JP2012191874 A JP 2012191874A
- Authority
- JP
- Japan
- Prior art keywords
- nucleic acid
- analysis device
- fine particles
- molecule
- bonding pad
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Granted
Links
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12Q—MEASURING OR TESTING PROCESSES INVOLVING ENZYMES, NUCLEIC ACIDS OR MICROORGANISMS; COMPOSITIONS OR TEST PAPERS THEREFOR; PROCESSES OF PREPARING SUCH COMPOSITIONS; CONDITION-RESPONSIVE CONTROL IN MICROBIOLOGICAL OR ENZYMOLOGICAL PROCESSES
- C12Q1/00—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions
- C12Q1/68—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions involving nucleic acids
- C12Q1/6876—Nucleic acid products used in the analysis of nucleic acids, e.g. primers or probes
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N21/00—Investigating or analysing materials by the use of optical means, i.e. using sub-millimetre waves, infrared, visible or ultraviolet light
- G01N21/62—Systems in which the material investigated is excited whereby it emits light or causes a change in wavelength of the incident light
- G01N21/63—Systems in which the material investigated is excited whereby it emits light or causes a change in wavelength of the incident light optically excited
- G01N21/64—Fluorescence; Phosphorescence
- G01N21/645—Specially adapted constructive features of fluorimeters
- G01N21/648—Specially adapted constructive features of fluorimeters using evanescent coupling or surface plasmon coupling for the excitation of fluorescence
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12Q—MEASURING OR TESTING PROCESSES INVOLVING ENZYMES, NUCLEIC ACIDS OR MICROORGANISMS; COMPOSITIONS OR TEST PAPERS THEREFOR; PROCESSES OF PREPARING SUCH COMPOSITIONS; CONDITION-RESPONSIVE CONTROL IN MICROBIOLOGICAL OR ENZYMOLOGICAL PROCESSES
- C12Q1/00—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions
- C12Q1/68—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions involving nucleic acids
- C12Q1/6813—Hybridisation assays
- C12Q1/6834—Enzymatic or biochemical coupling of nucleic acids to a solid phase
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12Q—MEASURING OR TESTING PROCESSES INVOLVING ENZYMES, NUCLEIC ACIDS OR MICROORGANISMS; COMPOSITIONS OR TEST PAPERS THEREFOR; PROCESSES OF PREPARING SUCH COMPOSITIONS; CONDITION-RESPONSIVE CONTROL IN MICROBIOLOGICAL OR ENZYMOLOGICAL PROCESSES
- C12Q1/00—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions
- C12Q1/68—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions involving nucleic acids
- C12Q1/6869—Methods for sequencing
- C12Q1/6874—Methods for sequencing involving nucleic acid arrays, e.g. sequencing by hybridisation
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N21/00—Investigating or analysing materials by the use of optical means, i.e. using sub-millimetre waves, infrared, visible or ultraviolet light
- G01N21/62—Systems in which the material investigated is excited whereby it emits light or causes a change in wavelength of the incident light
- G01N21/63—Systems in which the material investigated is excited whereby it emits light or causes a change in wavelength of the incident light optically excited
- G01N21/64—Fluorescence; Phosphorescence
- G01N21/645—Specially adapted constructive features of fluorimeters
- G01N21/6452—Individual samples arranged in a regular 2D-array, e.g. multiwell plates
-
- C—CHEMISTRY; METALLURGY
- C40—COMBINATORIAL TECHNOLOGY
- C40B—COMBINATORIAL CHEMISTRY; LIBRARIES, e.g. CHEMICAL LIBRARIES
- C40B40/00—Libraries per se, e.g. arrays, mixtures
- C40B40/04—Libraries containing only organic compounds
- C40B40/06—Libraries containing nucleotides or polynucleotides, or derivatives thereof
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N21/00—Investigating or analysing materials by the use of optical means, i.e. using sub-millimetre waves, infrared, visible or ultraviolet light
- G01N21/62—Systems in which the material investigated is excited whereby it emits light or causes a change in wavelength of the incident light
- G01N21/63—Systems in which the material investigated is excited whereby it emits light or causes a change in wavelength of the incident light optically excited
- G01N21/64—Fluorescence; Phosphorescence
- G01N21/6428—Measuring fluorescence of fluorescent products of reactions or of fluorochrome labelled reactive substances, e.g. measuring quenching effects, using measuring "optrodes"
- G01N2021/6439—Measuring fluorescence of fluorescent products of reactions or of fluorochrome labelled reactive substances, e.g. measuring quenching effects, using measuring "optrodes" with indicators, stains, dyes, tags, labels, marks
Landscapes
- Chemical & Material Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Health & Medical Sciences (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Organic Chemistry (AREA)
- Zoology (AREA)
- Wood Science & Technology (AREA)
- Analytical Chemistry (AREA)
- Engineering & Computer Science (AREA)
- Biochemistry (AREA)
- General Health & Medical Sciences (AREA)
- Immunology (AREA)
- Physics & Mathematics (AREA)
- Biotechnology (AREA)
- Microbiology (AREA)
- Molecular Biology (AREA)
- Biophysics (AREA)
- Bioinformatics & Cheminformatics (AREA)
- General Engineering & Computer Science (AREA)
- Genetics & Genomics (AREA)
- Pathology (AREA)
- General Physics & Mathematics (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Apparatus Associated With Microorganisms And Enzymes (AREA)
- Investigating, Analyzing Materials By Fluorescence Or Luminescence (AREA)
- Measuring Or Testing Involving Enzymes Or Micro-Organisms (AREA)
Abstract
【解決手段】本発明は、支持基板の所定位置に微小な金属製の接着用パッドを設け、当該接着用パッドに対し、疎水性を有するリンカーを固着させ、当該リンカーに核酸試料断片一分子を固定した嵩高い微粒子を結合させることにより、短時間かつ安価で、再現性がよい高効率な核酸の一分子固定を可能にした。本発明により、核酸分析装置を用いた核酸分析デバイスにおいて、読み取塩基長を長くでき、かつ多種類の被解析核酸分子を一度に解析可能になる。
【選択図】図1
Description
前記基板上の前記微粒子の固定位置に疎水化処理を行った接着用パッドを備え、
前記接着用パッドに対して前記微粒子が疎水的相互作用により固定されることを特徴とする核酸分析デバイスを開示する。
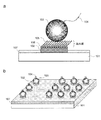
図1aは平滑支持基板101に接着用パッド102が形成され、該接着用パッド上にプローブ分子104が固定された微粒子103が末端に官能基106を有する線状分子105から形成される疎水膜を介して疎水的相互作用により結合している状態を示し、図1bは平滑支持基板101上の接着用パッド102にプローブ分子104が固定された微粒子103が規則正しく多数固定された状態を示す。
アミノ基 Ti、Ni
カルボキシル基 Ti
リン酸基 Ti、Al
アルデヒド基 Ti、Ni
糖のヒドロキシル基 Ti
このため、接着用パッドの直径は微粒子の直径の1/5〜5倍、好ましくは微粒子の直径以下である。
以下に、実際にプローブ分子104が固定された微粒子103を核酸分析デバイスに固定する実施例を示す。本実施例では、厚み0.7mmの石英ガラス基板上に、厚み10nm、直径60nmのチタン製の接着用パッドを1μm間隔で格子状に配列して形成した核酸分析デバイスを作製し使用した。
実施例2では、線状分子105としてアルキルグリコシドの非イオン性界面活性剤であるオクチルグルコシドを用い、微粒子103として半導体製の量子ドットを用いた例を示す。ここでは実施例1で使用した核酸分析デバイスと同等の構成で、チタン製接着用パッド102の直径が20nmである、平滑支持基板101を用いた。オクチルグルコシドを使用する利点として、非特異的吸着防止膜107の作製後でも微粒子接着用の線状分子105を反応させることができること、およびpH変化等で線状分子105が着脱可能であることが挙げられる。アルキルリン酸はPEGに比較的付着しやすいため、非特異的吸着防止膜107を形成させる前に接着用パッド102をアルキルリン酸で処理して、接着用パッド102にアルキルリン酸を結合させる必要がある。一方、オクチルグルコシド等のアルキルグリコシドを用いる場合、アルキルグルコシドは非特異的吸着防止膜107にはほとんど吸着しないためPEGシラン膜製膜により非特異的吸着防止膜107を形成させた後に接着用パッド102上にアルキルグルコシドを結合させることにより疎水性パターニングが可能である。したがって、線状分子105としてアルキルグルコシドを用いる場合、核酸分析デバイスを使用した後にアルキルグルコシドを基板から除去することができ、核酸分析デバイスを繰り返し使用できるという利点がある。
核酸分析デバイスの製造方法の一例を、図3を用いて説明する。平滑支持基板301(図3a)上に接着用パッドを構成する材料、例えば、金、チタン、ニッケル又はアルミをスパッタリングで製膜する(図3b)。これを金属の薄膜(金属デポ膜)308とする。平滑支持基板301として石英ガラス基板やサファイア基板を用い、接着用パッドの材料として金、アルミ又はニッケルを用いる場合には、基板材料と接着用パッドの材料との間に接着を補強するためにチタンやクロムの薄膜を形成させることが好ましい。また、接着用パッドはできる限り薄いほうが好ましい。これは、平滑支持基板301に厚みがあると側面部の面積が増え、接着用パッドの直径が微粒子の直径以下の場合でも、複数の微粒子が固定されてしまう可能性が高まるためである。そのため、金属の薄膜308は成膜の時点でできる限り薄く作製するほうが好ましい。この金属の薄膜308の上にレジスト309でパターンを形成する(図3c)。次にレジストパターン以外の金属の薄膜308をエッチングにより除去する(図3d)。さらにレジスト309を剥離すると接着用パッド302が完成する。レジスト剥離後、接着用パッド302にのみ選択的に吸着する線状分子305を導入し(図3e)、さらに非特異的吸着防止膜307を形成させる(図3f)。
核酸分析デバイスの製造方法の一例を、図4を用いて説明する。実施例3と同様の材料を使用するが、金属薄膜(金属デポ膜)408上に例えばガラスなどを材料とする平滑被覆膜410を形成し、その平滑被覆膜410を加工することでパターニングを行う例を示す。平滑支持基板401上に接着用パッドを構成する材料で製膜する。本実施例の場合、接着用パッドを構成する材料は可視光透過性を有する必要がある。例えば、チタン又はアルミをスパッタリングで製膜する。これを金属の薄膜408とする(図4A a、図4B a)。平滑支持基板401としてガラス基板又はサファイア基板を用いる。また、接着用薄膜層408はできる限り薄いほうが好ましい。さらに接着用薄膜層408は600℃以上でアニール処理することが好ましい。これらは基板下面より照射する励起光の透過率を高めるためである。そのため、金属の薄膜408は成膜の時点でできる限り薄く作製し、アニール処理することが好ましい。
本実施例では、核酸分析デバイスを用いた核酸分析装置の好ましい構成の一例について図5を参照しながら説明する。本実施例の核酸分析装置は、少なくとも核酸分析デバイスと、核酸分析デバイスに対して、蛍光色素を有するヌクレオチド,核酸合成酵素、及び核酸試料を供給する手段と、核酸分析デバイスに光を照射する手段と、核酸分析デバイス上においてヌクレオチド、核酸合成酵素、及び核酸試料が共存することにより起きる核酸伸長反応により核酸鎖中に取り込まれた蛍光色素の蛍光を測定する発光検出手段と、を備える。
102,202,302,402 接着用パッド
103,203 微粒子
104 プローブ分子
105,205,305,405 線状分子
106,206 線状分子末端の官能基
107,207,307,407 非特異的吸着防止膜
204 核酸合成酵素
208 鋳型核酸断片
209 核酸基質
308,408 金属デポ膜
309,409 電子線用レジスト
410 平滑被覆膜
501 カバープレート
502 検出窓
503 注入口
504 排出口
505 デバイス
506 流路
507,508 YAGレーザ光源
509,510 レーザ光
511 λ/4板
512 ダイクロイックミラー
513 レンズ
514 プリズム
515 対物レンズ
516 光学フィルタ
517 結像レンズ
518 2次元CCDカメラ
Claims (14)
- 支持基板及び検出対象の核酸を捕捉できるプローブ分子を有する微粒子を含み、該微粒子を前記支持基板上に一つずつ離して固定されている核酸分析デバイスであって、
前記基板上の前記微粒子の固定位置に疎水化処理を行った接着用パッドを備え、
前記接着用パッドに対して前記微粒子が疎水的相互作用により固定されることを特徴とする核酸分析デバイス。 - 微粒子1個に対して、プローブ分子が一分子固定されていることを特徴とする、請求項1記載の核酸分析デバイス。
- 微粒子が、疎水性を有する材料でできているか、又は表面に疎水性をもたらす修飾がなされていることを特徴とする、請求項1又は2に記載の核酸分析デバイス。
- 微粒子が疎水性部分としてアルキル鎖を有する線状分子を介して疎水的相互作用により接着用パッドに固定されている、請求項1〜3のいずれか1項に記載の核酸分析デバイス。
- 接着用パッドが、金、チタン、ニッケル及びアルミからなる群から選択される材料からなることを特徴とする、請求項1〜4のいずれか1項に記載の核酸分析デバイス。
- 支持基板が、石英、サファイア及びシリコンからなる群から選択される材料からなることを特徴とする、請求項1〜5のいずれか1項に記載の核酸分析デバイス。
- プローブ分子が核酸又は核酸合成酵素であることを特徴とする、請求項1〜6のいずれか1項に記載の核酸分析デバイス。
- (i) 検出対象の核酸を捕捉できるプローブ分子を有する微粒子が、基板上に規則正しく離れて形成されている疎水化処理を行った接着用パッドに、疎水的相互作用により規則的に固定されている核酸分析デバイス、
(ii) 前記核酸分析デバイスに対して、蛍光色素を有するヌクレオチド、核酸合成酵素、及び核酸試料を供給する手段、
(iii) 前記核酸分析デバイスに光を照射する手段、
(iv) 前記核酸分析デバイス上において前記ヌクレオチド、前記核酸合成酵素、及び前記核酸試料が共存することにより起きる核酸伸長反応により核酸鎖中に取り込まれた蛍光色素の蛍光を測定する発光検出手段とを備えた、
核酸試料の塩基配列情報を取得する核酸分析装置。 - プローブ分子が、核酸又は核酸合成酵素であることを特徴とする、請求項8記載の核酸分析装置。
- 微粒子1個に対して、プローブ分子が一分子固定されていることを特徴とする、請求項8又は9に記載の核酸分析装置。
- 記微粒子が、疎水性を有する材料でできているか、又は表面に疎水性をもたらす修飾がなされていることを特徴とする、請求項8〜10のいずれか1項に記載の核酸分析装置。
- 核酸分析デバイスの接着用パッドが、金、チタン、ニッケル及びアルミからなる群から選択される材料からなることを特徴とする、請求項8〜11のいずれか1項に記載の核酸分析装置。
- 核酸分析デバイスの支持基板が、石石英、サファイア及びシリコンからなる群から選択される材料からなることを特徴とする、請求項8〜12のいずれか1項に記載の核酸分析装置。
- 分析デバイスに光を照射する手段として、エバネッセント場を利用することを特徴とする、請求項8〜13のいずれか1項に記載の核酸分析装置。
Priority Applications (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2011057091A JP5587816B2 (ja) | 2011-03-15 | 2011-03-15 | 核酸分析デバイス、及び核酸分析装置 |
| US14/002,125 US9957562B2 (en) | 2011-03-15 | 2012-01-24 | Nucleic acid analysis device and nucleic acid analyzer |
| PCT/JP2012/051388 WO2012124377A1 (ja) | 2011-03-15 | 2012-01-24 | 核酸分析デバイス、及び核酸分析装置 |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2011057091A JP5587816B2 (ja) | 2011-03-15 | 2011-03-15 | 核酸分析デバイス、及び核酸分析装置 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2012191874A true JP2012191874A (ja) | 2012-10-11 |
| JP5587816B2 JP5587816B2 (ja) | 2014-09-10 |
Family
ID=46830458
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2011057091A Expired - Fee Related JP5587816B2 (ja) | 2011-03-15 | 2011-03-15 | 核酸分析デバイス、及び核酸分析装置 |
Country Status (3)
| Country | Link |
|---|---|
| US (1) | US9957562B2 (ja) |
| JP (1) | JP5587816B2 (ja) |
| WO (1) | WO2012124377A1 (ja) |
Cited By (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPWO2017026439A1 (ja) * | 2015-08-11 | 2018-05-31 | 東レ株式会社 | 半導体素子、その製造方法およびそれを用いたセンサ |
| WO2023027184A1 (ja) * | 2021-08-27 | 2023-03-02 | 国立大学法人神戸大学 | 基材上に収率よく空孔を形成する技術のためのコアシェル鋳型分子・粒子 |
| WO2023027183A1 (ja) * | 2021-08-27 | 2023-03-02 | 国立大学法人神戸大学 | 基板上に粒子を凝集なく並べる技術 |
Families Citing this family (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| KR101593545B1 (ko) * | 2014-05-29 | 2016-02-26 | 서울대학교 산학협력단 | 재사용이 가능한 화학적 또는 생물학적 센서 및 그 사용방법 |
| DE102016200324A1 (de) * | 2016-01-14 | 2017-07-20 | MTU Aero Engines AG | Verfahren zum Ermitteln einer Konzentration wenigstens eines Werkstoffs in einem Pulver für ein additives Herstellverfahren |
| JP7011145B2 (ja) * | 2017-03-15 | 2022-02-10 | 国立大学法人群馬大学 | 固定化ポリメラーゼによる修飾ポリヌクレオチド合成法 |
| WO2019059182A1 (ja) * | 2017-09-25 | 2019-03-28 | 旭化成株式会社 | 有機着色微粒子、診断薬キット、及びインビトロ診断方法 |
| CA3144019A1 (en) * | 2019-06-19 | 2020-12-24 | European Molecular Biology Laboratory | Photo-micropatterning for electron microscopy |
Citations (9)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2004294240A (ja) * | 2003-03-26 | 2004-10-21 | Seiko Epson Corp | 核酸固定化方法およびそれを用いるバイオセンサの製造法 |
| JP2005037881A (ja) * | 2003-04-21 | 2005-02-10 | Fuji Photo Film Co Ltd | パターン形成方法、画像形成方法、微粒子吸着パターン形成方法、導電性パターン形成方法、パターン形成材料、及び平版印刷版 |
| JP2005208044A (ja) * | 2003-12-25 | 2005-08-04 | Nippon Sheet Glass Co Ltd | 生体関連物質選択付着性基板 |
| JP2005291952A (ja) * | 2004-03-31 | 2005-10-20 | Kyocera Chemical Corp | 生体関連物質固定用粒子およびマイクロアレイ |
| JP2006250668A (ja) * | 2005-03-10 | 2006-09-21 | Tatsuro Endo | 非標識バイオチップ |
| JP2008190937A (ja) * | 2007-02-02 | 2008-08-21 | Hitachi High-Technologies Corp | 生体分子検出素子、生体分子検出素子の製造方法及び生体分子検出方法 |
| JP2009085607A (ja) * | 2007-09-27 | 2009-04-23 | Hitachi High-Technologies Corp | 生体分子検出素子及び生体分子検出素子の製造方法 |
| JP2010145272A (ja) * | 2008-12-19 | 2010-07-01 | Konica Minolta Holdings Inc | プラズモン励起センサを用いたアッセイ法 |
| JP2010172271A (ja) * | 2009-01-30 | 2010-08-12 | Hitachi High-Technologies Corp | 核酸分析デバイス、及び核酸分析装置 |
Family Cites Families (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2003023401A1 (en) | 2001-09-12 | 2003-03-20 | Eidgenössische Technische Hochschule Zürich | Device with chemical surface patterns |
-
2011
- 2011-03-15 JP JP2011057091A patent/JP5587816B2/ja not_active Expired - Fee Related
-
2012
- 2012-01-24 US US14/002,125 patent/US9957562B2/en not_active Expired - Fee Related
- 2012-01-24 WO PCT/JP2012/051388 patent/WO2012124377A1/ja active Application Filing
Patent Citations (9)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2004294240A (ja) * | 2003-03-26 | 2004-10-21 | Seiko Epson Corp | 核酸固定化方法およびそれを用いるバイオセンサの製造法 |
| JP2005037881A (ja) * | 2003-04-21 | 2005-02-10 | Fuji Photo Film Co Ltd | パターン形成方法、画像形成方法、微粒子吸着パターン形成方法、導電性パターン形成方法、パターン形成材料、及び平版印刷版 |
| JP2005208044A (ja) * | 2003-12-25 | 2005-08-04 | Nippon Sheet Glass Co Ltd | 生体関連物質選択付着性基板 |
| JP2005291952A (ja) * | 2004-03-31 | 2005-10-20 | Kyocera Chemical Corp | 生体関連物質固定用粒子およびマイクロアレイ |
| JP2006250668A (ja) * | 2005-03-10 | 2006-09-21 | Tatsuro Endo | 非標識バイオチップ |
| JP2008190937A (ja) * | 2007-02-02 | 2008-08-21 | Hitachi High-Technologies Corp | 生体分子検出素子、生体分子検出素子の製造方法及び生体分子検出方法 |
| JP2009085607A (ja) * | 2007-09-27 | 2009-04-23 | Hitachi High-Technologies Corp | 生体分子検出素子及び生体分子検出素子の製造方法 |
| JP2010145272A (ja) * | 2008-12-19 | 2010-07-01 | Konica Minolta Holdings Inc | プラズモン励起センサを用いたアッセイ法 |
| JP2010172271A (ja) * | 2009-01-30 | 2010-08-12 | Hitachi High-Technologies Corp | 核酸分析デバイス、及び核酸分析装置 |
Cited By (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPWO2017026439A1 (ja) * | 2015-08-11 | 2018-05-31 | 東レ株式会社 | 半導体素子、その製造方法およびそれを用いたセンサ |
| US11002705B2 (en) | 2015-08-11 | 2021-05-11 | Toray Industries, Inc. | Semiconductor element, method for manufacturing same, and sensor in which same is used |
| WO2023027184A1 (ja) * | 2021-08-27 | 2023-03-02 | 国立大学法人神戸大学 | 基材上に収率よく空孔を形成する技術のためのコアシェル鋳型分子・粒子 |
| WO2023027183A1 (ja) * | 2021-08-27 | 2023-03-02 | 国立大学法人神戸大学 | 基板上に粒子を凝集なく並べる技術 |
| JP7334003B2 (ja) | 2021-08-27 | 2023-08-28 | 国立大学法人神戸大学 | 基板上に粒子を凝集なく並べる技術 |
Also Published As
| Publication number | Publication date |
|---|---|
| WO2012124377A1 (ja) | 2012-09-20 |
| US9957562B2 (en) | 2018-05-01 |
| JP5587816B2 (ja) | 2014-09-10 |
| US20130338041A1 (en) | 2013-12-19 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP5587816B2 (ja) | 核酸分析デバイス、及び核酸分析装置 | |
| JP5260339B2 (ja) | 核酸分析デバイス、及び核酸分析装置 | |
| JP5222599B2 (ja) | 核酸分析デバイス及びそれを用いた核酸分析装置 | |
| JP5816291B2 (ja) | 生体分子分析方法及び生体分子分析装置 | |
| EP2040060B1 (en) | Apparatus and method for detecting a target substance | |
| JP5663008B2 (ja) | 核酸分析デバイスの製造方法 | |
| EP2871464B1 (en) | Analysis device and analysis method | |
| JP2008190937A (ja) | 生体分子検出素子、生体分子検出素子の製造方法及び生体分子検出方法 | |
| JP5822929B2 (ja) | 核酸分析装置 | |
| JP5635130B2 (ja) | 単分子プローブ核酸付き微粒子及びその製造方法、並びに核酸分析方法 | |
| JP5309092B2 (ja) | 核酸分析用デバイス,核酸分析装置、及び核酸分析用デバイスの製造方法 | |
| US9040251B2 (en) | Biomolecule fixing board and method of manufacturing the same | |
| JP5097495B2 (ja) | 生体分子検出素子及び生体分子検出素子の製造方法 | |
| JP5651485B2 (ja) | 核酸分析装置 | |
| JP5026359B2 (ja) | 核酸分析デバイス、核酸分析装置及び核酸分析方法 | |
| WO2014021020A1 (ja) | 免疫分析方法及び免疫分析装置 | |
| WO2011092780A1 (ja) | 核酸分析装置,核酸分析反応デバイス、および核酸分析用反応デバイス用基板 | |
| JP2012058114A (ja) | 核酸分析デバイス,核酸分析装置、及び核酸分析方法 | |
| JP2003329676A (ja) | 生化学検体の検出方法と検出チップ |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20130124 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20140701 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20140724 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 5587816 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| S531 | Written request for registration of change of domicile |
Free format text: JAPANESE INTERMEDIATE CODE: R313531 |
|
| S533 | Written request for registration of change of name |
Free format text: JAPANESE INTERMEDIATE CODE: R313533 |
|
| R350 | Written notification of registration of transfer |
Free format text: JAPANESE INTERMEDIATE CODE: R350 |
|
| LAPS | Cancellation because of no payment of annual fees |