JP2012152154A - シート状細胞培養物の製造方法、シート状細胞培養物形成用基材の製造方法、気泡の除去方法および気体の検出システム - Google Patents
シート状細胞培養物の製造方法、シート状細胞培養物形成用基材の製造方法、気泡の除去方法および気体の検出システム Download PDFInfo
- Publication number
- JP2012152154A JP2012152154A JP2011015083A JP2011015083A JP2012152154A JP 2012152154 A JP2012152154 A JP 2012152154A JP 2011015083 A JP2011015083 A JP 2011015083A JP 2011015083 A JP2011015083 A JP 2011015083A JP 2012152154 A JP2012152154 A JP 2012152154A
- Authority
- JP
- Japan
- Prior art keywords
- substrate
- liquid
- bubbles
- biological material
- sheet
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Granted
Links
- 239000000758 substrate Substances 0.000 title claims abstract description 116
- 238000000034 method Methods 0.000 title claims abstract description 44
- 238000004519 manufacturing process Methods 0.000 title claims abstract description 25
- 239000007788 liquid Substances 0.000 claims abstract description 98
- 239000012620 biological material Substances 0.000 claims abstract description 65
- 238000012258 culturing Methods 0.000 claims abstract description 7
- 238000010899 nucleation Methods 0.000 claims abstract description 7
- 238000004113 cell culture Methods 0.000 claims description 84
- 238000001514 detection method Methods 0.000 claims description 33
- 210000002966 serum Anatomy 0.000 claims description 26
- 238000002834 transmittance Methods 0.000 claims description 13
- 239000000203 mixture Substances 0.000 claims description 10
- 238000011533 pre-incubation Methods 0.000 claims description 8
- 102000004169 proteins and genes Human genes 0.000 claims description 7
- 108090000623 proteins and genes Proteins 0.000 claims description 7
- 230000006378 damage Effects 0.000 claims description 3
- 230000007547 defect Effects 0.000 abstract description 11
- 210000004027 cell Anatomy 0.000 description 77
- 239000000463 material Substances 0.000 description 49
- 238000011084 recovery Methods 0.000 description 12
- 239000000243 solution Substances 0.000 description 11
- 238000003860 storage Methods 0.000 description 11
- 238000005259 measurement Methods 0.000 description 10
- 239000003102 growth factor Substances 0.000 description 7
- 210000004683 skeletal myoblast Anatomy 0.000 description 7
- 239000007787 solid Substances 0.000 description 7
- 239000000126 substance Substances 0.000 description 7
- 239000002609 medium Substances 0.000 description 6
- 210000001519 tissue Anatomy 0.000 description 6
- 239000006144 Dulbecco’s modified Eagle's medium Substances 0.000 description 5
- 239000006143 cell culture medium Substances 0.000 description 5
- 238000005406 washing Methods 0.000 description 5
- 150000003926 acrylamides Chemical class 0.000 description 4
- 239000000654 additive Substances 0.000 description 4
- 230000000735 allogeneic effect Effects 0.000 description 4
- 239000007640 basal medium Substances 0.000 description 4
- 239000011248 coating agent Substances 0.000 description 4
- 238000000576 coating method Methods 0.000 description 4
- 239000001963 growth medium Substances 0.000 description 4
- 239000010410 layer Substances 0.000 description 4
- 230000002107 myocardial effect Effects 0.000 description 4
- 230000000704 physical effect Effects 0.000 description 4
- -1 polyethylene Polymers 0.000 description 4
- HRPVXLWXLXDGHG-UHFFFAOYSA-N Acrylamide Chemical compound NC(=O)C=C HRPVXLWXLXDGHG-UHFFFAOYSA-N 0.000 description 3
- 239000012980 RPMI-1640 medium Substances 0.000 description 3
- 230000015572 biosynthetic process Effects 0.000 description 3
- 230000004069 differentiation Effects 0.000 description 3
- 210000002919 epithelial cell Anatomy 0.000 description 3
- 230000008569 process Effects 0.000 description 3
- 102000010834 Extracellular Matrix Proteins Human genes 0.000 description 2
- 108010037362 Extracellular Matrix Proteins Proteins 0.000 description 2
- 108050007372 Fibroblast Growth Factor Proteins 0.000 description 2
- 102000018233 Fibroblast Growth Factor Human genes 0.000 description 2
- XEEYBQQBJWHFJM-UHFFFAOYSA-N Iron Chemical compound [Fe] XEEYBQQBJWHFJM-UHFFFAOYSA-N 0.000 description 2
- 108010073929 Vascular Endothelial Growth Factor A Proteins 0.000 description 2
- 102000005789 Vascular Endothelial Growth Factors Human genes 0.000 description 2
- 108010019530 Vascular Endothelial Growth Factors Proteins 0.000 description 2
- 210000004369 blood Anatomy 0.000 description 2
- 239000008280 blood Substances 0.000 description 2
- 230000021164 cell adhesion Effects 0.000 description 2
- 230000008859 change Effects 0.000 description 2
- 238000007796 conventional method Methods 0.000 description 2
- 229920001577 copolymer Polymers 0.000 description 2
- 238000010908 decantation Methods 0.000 description 2
- 238000010586 diagram Methods 0.000 description 2
- 238000010790 dilution Methods 0.000 description 2
- 239000012895 dilution Substances 0.000 description 2
- 210000002744 extracellular matrix Anatomy 0.000 description 2
- 229940126864 fibroblast growth factor Drugs 0.000 description 2
- 239000000499 gel Substances 0.000 description 2
- 238000009434 installation Methods 0.000 description 2
- 238000004264 monolayer culture Methods 0.000 description 2
- 210000003098 myoblast Anatomy 0.000 description 2
- 208000010125 myocardial infarction Diseases 0.000 description 2
- QNILTEGFHQSKFF-UHFFFAOYSA-N n-propan-2-ylprop-2-enamide Chemical compound CC(C)NC(=O)C=C QNILTEGFHQSKFF-UHFFFAOYSA-N 0.000 description 2
- 239000002504 physiological saline solution Substances 0.000 description 2
- 229920000642 polymer Polymers 0.000 description 2
- 229920002981 polyvinylidene fluoride Polymers 0.000 description 2
- 230000008439 repair process Effects 0.000 description 2
- 230000004044 response Effects 0.000 description 2
- 241000894007 species Species 0.000 description 2
- 150000003431 steroids Chemical class 0.000 description 2
- 230000000638 stimulation Effects 0.000 description 2
- 239000011782 vitamin Substances 0.000 description 2
- 229940088594 vitamin Drugs 0.000 description 2
- 229930003231 vitamin Natural products 0.000 description 2
- 235000013343 vitamin Nutrition 0.000 description 2
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 2
- XLPJNCYCZORXHG-UHFFFAOYSA-N 1-morpholin-4-ylprop-2-en-1-one Chemical compound C=CC(=O)N1CCOCC1 XLPJNCYCZORXHG-UHFFFAOYSA-N 0.000 description 1
- RESPXSHDJQUNTN-UHFFFAOYSA-N 1-piperidin-1-ylprop-2-en-1-one Chemical compound C=CC(=O)N1CCCCC1 RESPXSHDJQUNTN-UHFFFAOYSA-N 0.000 description 1
- WLPAQAXAZQUXBG-UHFFFAOYSA-N 1-pyrrolidin-1-ylprop-2-en-1-one Chemical compound C=CC(=O)N1CCCC1 WLPAQAXAZQUXBG-UHFFFAOYSA-N 0.000 description 1
- AKVUWTYSNLGBJY-UHFFFAOYSA-N 2-methyl-1-morpholin-4-ylprop-2-en-1-one Chemical compound CC(=C)C(=O)N1CCOCC1 AKVUWTYSNLGBJY-UHFFFAOYSA-N 0.000 description 1
- RASDUGQQSMMINZ-UHFFFAOYSA-N 2-methyl-1-piperidin-1-ylprop-2-en-1-one Chemical compound CC(=C)C(=O)N1CCCCC1 RASDUGQQSMMINZ-UHFFFAOYSA-N 0.000 description 1
- LVCMKNCJDCTPIB-UHFFFAOYSA-N 2-methyl-1-pyrrolidin-1-ylprop-2-en-1-one Chemical compound CC(=C)C(=O)N1CCCC1 LVCMKNCJDCTPIB-UHFFFAOYSA-N 0.000 description 1
- YQIGLEFUZMIVHU-UHFFFAOYSA-N 2-methyl-n-propan-2-ylprop-2-enamide Chemical compound CC(C)NC(=O)C(C)=C YQIGLEFUZMIVHU-UHFFFAOYSA-N 0.000 description 1
- 206010002383 Angina Pectoris Diseases 0.000 description 1
- 241000283690 Bos taurus Species 0.000 description 1
- 108091003079 Bovine Serum Albumin Proteins 0.000 description 1
- 229910001369 Brass Inorganic materials 0.000 description 1
- 241000282472 Canis lupus familiaris Species 0.000 description 1
- 241000283707 Capra Species 0.000 description 1
- QDHHCQZDFGDHMP-UHFFFAOYSA-N Chloramine Chemical compound ClN QDHHCQZDFGDHMP-UHFFFAOYSA-N 0.000 description 1
- 102000008186 Collagen Human genes 0.000 description 1
- 108010035532 Collagen Proteins 0.000 description 1
- 206010056370 Congestive cardiomyopathy Diseases 0.000 description 1
- RYGMFSIKBFXOCR-UHFFFAOYSA-N Copper Chemical compound [Cu] RYGMFSIKBFXOCR-UHFFFAOYSA-N 0.000 description 1
- 208000028006 Corneal injury Diseases 0.000 description 1
- 201000010046 Dilated cardiomyopathy Diseases 0.000 description 1
- 102000004190 Enzymes Human genes 0.000 description 1
- 108090000790 Enzymes Proteins 0.000 description 1
- 241000283086 Equidae Species 0.000 description 1
- 208000000461 Esophageal Neoplasms Diseases 0.000 description 1
- 241000282326 Felis catus Species 0.000 description 1
- 241000282412 Homo Species 0.000 description 1
- 229920002302 Nylon 6,6 Polymers 0.000 description 1
- 206010030155 Oesophageal carcinoma Diseases 0.000 description 1
- 241001494479 Pecora Species 0.000 description 1
- 102000035195 Peptidases Human genes 0.000 description 1
- 108091005804 Peptidases Proteins 0.000 description 1
- 239000004698 Polyethylene Substances 0.000 description 1
- 239000004743 Polypropylene Substances 0.000 description 1
- 239000004793 Polystyrene Substances 0.000 description 1
- 239000004372 Polyvinyl alcohol Substances 0.000 description 1
- BUGBHKTXTAQXES-UHFFFAOYSA-N Selenium Chemical compound [Se] BUGBHKTXTAQXES-UHFFFAOYSA-N 0.000 description 1
- 241000282887 Suidae Species 0.000 description 1
- 239000004809 Teflon Substances 0.000 description 1
- 229920006362 Teflon® Polymers 0.000 description 1
- 102000004142 Trypsin Human genes 0.000 description 1
- 108090000631 Trypsin Proteins 0.000 description 1
- QYKIQEUNHZKYBP-UHFFFAOYSA-N Vinyl ether Chemical class C=COC=C QYKIQEUNHZKYBP-UHFFFAOYSA-N 0.000 description 1
- 206010052428 Wound Diseases 0.000 description 1
- 208000027418 Wounds and injury Diseases 0.000 description 1
- 230000002411 adverse Effects 0.000 description 1
- 229910052782 aluminium Inorganic materials 0.000 description 1
- XAGFODPZIPBFFR-UHFFFAOYSA-N aluminium Chemical compound [Al] XAGFODPZIPBFFR-UHFFFAOYSA-N 0.000 description 1
- 150000001413 amino acids Chemical class 0.000 description 1
- 239000003242 anti bacterial agent Substances 0.000 description 1
- 229940088710 antibiotic agent Drugs 0.000 description 1
- DMLAVOWQYNRWNQ-UHFFFAOYSA-N azobenzene Chemical group C1=CC=CC=C1N=NC1=CC=CC=C1 DMLAVOWQYNRWNQ-UHFFFAOYSA-N 0.000 description 1
- 239000010951 brass Substances 0.000 description 1
- 239000000872 buffer Substances 0.000 description 1
- 239000007853 buffer solution Substances 0.000 description 1
- 244000309466 calf Species 0.000 description 1
- 229910002091 carbon monoxide Inorganic materials 0.000 description 1
- 210000004413 cardiac myocyte Anatomy 0.000 description 1
- 230000024245 cell differentiation Effects 0.000 description 1
- 230000003915 cell function Effects 0.000 description 1
- 230000004663 cell proliferation Effects 0.000 description 1
- 229920002678 cellulose Polymers 0.000 description 1
- 239000001913 cellulose Substances 0.000 description 1
- 229920001436 collagen Polymers 0.000 description 1
- 238000011109 contamination Methods 0.000 description 1
- 229910052802 copper Inorganic materials 0.000 description 1
- 239000010949 copper Substances 0.000 description 1
- 210000004087 cornea Anatomy 0.000 description 1
- 125000004122 cyclic group Chemical group 0.000 description 1
- 230000003247 decreasing effect Effects 0.000 description 1
- 201000010099 disease Diseases 0.000 description 1
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 description 1
- 239000006185 dispersion Substances 0.000 description 1
- 238000004090 dissolution Methods 0.000 description 1
- 239000003792 electrolyte Substances 0.000 description 1
- 238000012143 endoscopic resection Methods 0.000 description 1
- 210000002889 endothelial cell Anatomy 0.000 description 1
- 210000002615 epidermis Anatomy 0.000 description 1
- 201000004101 esophageal cancer Diseases 0.000 description 1
- 210000003238 esophagus Anatomy 0.000 description 1
- 239000012894 fetal calf serum Substances 0.000 description 1
- 230000001605 fetal effect Effects 0.000 description 1
- 210000002950 fibroblast Anatomy 0.000 description 1
- 230000006870 function Effects 0.000 description 1
- 239000011521 glass Substances 0.000 description 1
- 208000019622 heart disease Diseases 0.000 description 1
- 210000003494 hepatocyte Anatomy 0.000 description 1
- 238000003384 imaging method Methods 0.000 description 1
- 230000001771 impaired effect Effects 0.000 description 1
- 239000012535 impurity Substances 0.000 description 1
- 229910052742 iron Inorganic materials 0.000 description 1
- 230000001678 irradiating effect Effects 0.000 description 1
- 238000002955 isolation Methods 0.000 description 1
- 210000004379 membrane Anatomy 0.000 description 1
- 239000012528 membrane Substances 0.000 description 1
- 229910052751 metal Inorganic materials 0.000 description 1
- 239000002184 metal Substances 0.000 description 1
- 210000002200 mouth mucosa Anatomy 0.000 description 1
- 208000031225 myocardial ischemia Diseases 0.000 description 1
- KAKALCZDCFZYRN-UHFFFAOYSA-N n-(2-ethoxyethyl)-2-methylprop-2-enamide Chemical compound CCOCCNC(=O)C(C)=C KAKALCZDCFZYRN-UHFFFAOYSA-N 0.000 description 1
- YLQHOUDDHYMERA-UHFFFAOYSA-N n-(2-ethoxyethyl)prop-2-enamide Chemical compound CCOCCNC(=O)C=C YLQHOUDDHYMERA-UHFFFAOYSA-N 0.000 description 1
- KPEKHIHQXHOSRM-UHFFFAOYSA-N n-(oxolan-2-ylmethyl)prop-2-enamide Chemical compound C=CC(=O)NCC1CCCO1 KPEKHIHQXHOSRM-UHFFFAOYSA-N 0.000 description 1
- FIBUWQFQYAAXHD-UHFFFAOYSA-N n-cyclopropyl-2-methylprop-2-enamide Chemical compound CC(=C)C(=O)NC1CC1 FIBUWQFQYAAXHD-UHFFFAOYSA-N 0.000 description 1
- LCXIFAOALNZGDO-UHFFFAOYSA-N n-cyclopropylprop-2-enamide Chemical compound C=CC(=O)NC1CC1 LCXIFAOALNZGDO-UHFFFAOYSA-N 0.000 description 1
- ZIWDVJPPVMGJGR-UHFFFAOYSA-N n-ethyl-2-methylprop-2-enamide Chemical compound CCNC(=O)C(C)=C ZIWDVJPPVMGJGR-UHFFFAOYSA-N 0.000 description 1
- SWPMNMYLORDLJE-UHFFFAOYSA-N n-ethylprop-2-enamide Chemical compound CCNC(=O)C=C SWPMNMYLORDLJE-UHFFFAOYSA-N 0.000 description 1
- 238000004806 packaging method and process Methods 0.000 description 1
- 210000002379 periodontal ligament Anatomy 0.000 description 1
- 210000002381 plasma Anatomy 0.000 description 1
- 229920003229 poly(methyl methacrylate) Polymers 0.000 description 1
- 229920002432 poly(vinyl methyl ether) polymer Polymers 0.000 description 1
- 229920002401 polyacrylamide Polymers 0.000 description 1
- 229920000573 polyethylene Polymers 0.000 description 1
- 229920000139 polyethylene terephthalate Polymers 0.000 description 1
- 239000005020 polyethylene terephthalate Substances 0.000 description 1
- 239000004926 polymethyl methacrylate Substances 0.000 description 1
- 229920001155 polypropylene Polymers 0.000 description 1
- 229920002223 polystyrene Polymers 0.000 description 1
- 229920002451 polyvinyl alcohol Polymers 0.000 description 1
- 238000012545 processing Methods 0.000 description 1
- 230000002062 proliferating effect Effects 0.000 description 1
- 238000011160 research Methods 0.000 description 1
- 230000006903 response to temperature Effects 0.000 description 1
- 229910052711 selenium Inorganic materials 0.000 description 1
- 239000011669 selenium Substances 0.000 description 1
- 239000010703 silicon Substances 0.000 description 1
- 229910052710 silicon Inorganic materials 0.000 description 1
- 210000003491 skin Anatomy 0.000 description 1
- 210000004927 skin cell Anatomy 0.000 description 1
- 230000037380 skin damage Effects 0.000 description 1
- 229910001220 stainless steel Inorganic materials 0.000 description 1
- 239000010935 stainless steel Substances 0.000 description 1
- 238000010561 standard procedure Methods 0.000 description 1
- 230000004936 stimulating effect Effects 0.000 description 1
- 238000003756 stirring Methods 0.000 description 1
- 239000011550 stock solution Substances 0.000 description 1
- 210000002784 stomach Anatomy 0.000 description 1
- 239000006228 supernatant Substances 0.000 description 1
- 230000004083 survival effect Effects 0.000 description 1
- 210000002437 synoviocyte Anatomy 0.000 description 1
- 210000003437 trachea Anatomy 0.000 description 1
- 230000007704 transition Effects 0.000 description 1
- 238000002054 transplantation Methods 0.000 description 1
- AAAQKTZKLRYKHR-UHFFFAOYSA-N triphenylmethane Chemical compound C1=CC=CC=C1C(C=1C=CC=CC=1)C1=CC=CC=C1 AAAQKTZKLRYKHR-UHFFFAOYSA-N 0.000 description 1
- 239000012588 trypsin Substances 0.000 description 1
- VBEQCZHXXJYVRD-GACYYNSASA-N uroanthelone Chemical compound C([C@@H](C(=O)N[C@H](C(=O)N[C@@H](CS)C(=O)N[C@@H](CC(N)=O)C(=O)N[C@@H](CS)C(=O)N[C@H](C(=O)N[C@@H]([C@@H](C)CC)C(=O)NCC(=O)N[C@@H](CC=1C=CC(O)=CC=1)C(=O)N[C@@H](CO)C(=O)NCC(=O)N[C@@H](CC(O)=O)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CS)C(=O)N[C@@H](CCC(N)=O)C(=O)N[C@@H]([C@@H](C)O)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CC(O)=O)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CC=1C2=CC=CC=C2NC=1)C(=O)N[C@@H](CC=1C2=CC=CC=C2NC=1)C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CCCNC(N)=N)C(O)=O)C(C)C)[C@@H](C)O)NC(=O)[C@H](CO)NC(=O)[C@H](CC(O)=O)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](CO)NC(=O)[C@H](CCC(O)=O)NC(=O)[C@@H](NC(=O)[C@H](CC=1NC=NC=1)NC(=O)[C@H](CCSC)NC(=O)[C@H](CS)NC(=O)[C@@H](NC(=O)CNC(=O)CNC(=O)[C@H](CC(N)=O)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](CS)NC(=O)[C@H](CC=1C=CC(O)=CC=1)NC(=O)CNC(=O)[C@H](CC(O)=O)NC(=O)[C@H](CC=1C=CC(O)=CC=1)NC(=O)[C@H](CO)NC(=O)[C@H](CO)NC(=O)[C@H]1N(CCC1)C(=O)[C@H](CS)NC(=O)CNC(=O)[C@H]1N(CCC1)C(=O)[C@H](CC=1C=CC(O)=CC=1)NC(=O)[C@H](CO)NC(=O)[C@@H](N)CC(N)=O)C(C)C)[C@@H](C)CC)C1=CC=C(O)C=C1 VBEQCZHXXJYVRD-GACYYNSASA-N 0.000 description 1
- 125000000391 vinyl group Chemical group [H]C([*])=C([H])[H] 0.000 description 1
Images
Landscapes
- Apparatus Associated With Microorganisms And Enzymes (AREA)
- Micro-Organisms Or Cultivation Processes Thereof (AREA)
Abstract
【解決手段】 本発明のシート状細胞培養物の製造方法は、生物材料を含む液体を基材上に付与する第1の工程と、基材上の液体における気泡を検出する第2の工程と、生物材料を基材に固定する第3の工程と、基材上に細胞を播種する第4の工程と、細胞を培養してシート状細胞培養物を形成する第5の工程と、を含み、第2の工程において、気泡が検出された場合には、気泡を除去するまたは前記液体を基材から除去して第1の工程を再度行う。
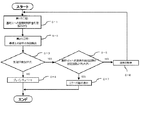
【選択図】 図1
Description
さらに、培養基材を血清で被覆し、当該培養基材上に細胞を播種、培養する、製造工程由来不純物を含まないシート状細胞培養物の製造方法が提供された(特許文献2参照)。
(1) 生物材料を含む液体を基材上に付与する第1の工程と、
基材上の液体における気泡を検出する第2の工程と、
生物材料を基材に固定する第3の工程と、
基材上に細胞を播種する第4の工程と、
細胞を培養してシート状細胞培養物を形成する第5の工程と、を含み、
第2の工程において、気泡が検出された場合には、気泡を除去するまたは前記液体を基材から除去して第1の工程を再度行うシート状細胞培養物の製造方法。
(2) 第4の工程における細胞の播種が、細胞が実質的に増殖することなくシート状細胞培養物を形成し得る密度で行われる、(1)に記載の方法。
(3) 生物材料が、タンパク質を含む組成物であり、かつ、当該組成物のタンパク質の基材への固定をプレインキュベートによって行う、(1)または(2)に記載の方法。
(4) 生物材料は血清である、(1)〜(3)のいずれかに記載の方法。
(5) 気泡の検出を、液体に超音波を照射した際の超音波の透過率を測定することによって行う、(1)〜(4)のいずれかに記載の方法。
(6) シート状細胞培養物形成用基材の製造方法であって、
生物材料を含む液体を基材上に付与する第1の工程と、
基材上の液体における気泡を検出する第2の工程と、
生物材料を基材に固定する第3の工程と、を含み、
第2の工程において、気泡が検出された場合には、気泡を除去するまたは前記液体を基材から除去して第1の工程を再度行う前記方法。
(7) シート状細胞培養物の製造時において、生物材料を含む液体を基材上に付与した後、かつ生物材料を基材に固定する前に、基材上の液体における気泡を検出する工程を含み、
気泡が検出された場合には、当該気泡を吸引または破壊することにより除去するまたは前記液体を基材から除去して新たな生物材料を含む液体を基材上に付与する気泡の除去方法。
(8) (7)に記載の気泡の除去方法を実行するための気体の検出システムであって、
基材上に付与された生物材料を含む液体における気泡を検出するための気泡検出手段と、
気泡検出手段の検出結果に基づいて気泡の有無を判定する判定手段とを含むことを特徴とする、前記システム。
本発明のシート状細胞培養物の製造方法は、生物材料を含む液体を基材(以下、培養基材ともいう)上に付与する第1の工程と、基材上の液体における気泡を検出する第2の工程と、生物材料を基材に固定する第3の工程と、基材上に細胞を播種する第4の工程と、細胞を培養してシート状細胞培養物を形成する第5の工程と、を含み、第2の工程において、気泡が検出された場合には、気泡を除去するまたは前記液体を基材から除去して第1の工程を再度行うものである。
また、本発明のシート状細胞培養物形成用基材の製造方法は、前記第1の工程と、第2の工程と、第3の工程とを含み、第2の工程において、気泡が検出された場合には、気泡を除去するまたは前記液体を基材から除去して第1の工程を再度行うものである。
まず、第1の工程では、生物材料を含む液体を培養基材上に付与する。
容器は、培養液などの液体を透過させない構造・材料が好ましい。かかる材料としては、限定することなく、例えば、ポリエチレン、ポリプロピレン、テフロン(登録商標)、ポリエチレンテレフタレート、ポリメチルメタクリレート、ナイロン6,6、ポリビニルアルコール、セルロース、シリコン、ポリスチレン、ガラス、ポリアクリルアミド、ポリジメチルアクリルアミド、金属(例えば、鉄、ステンレス、アルミニウム、銅、真鍮)等が挙げられ、これらのうち1種または2種以上を組み合わせて用いることができる。
上記培養基材は、種々の形状であってもよいが、少なくとも1つの平坦な面を有することが好ましい。かかる容器の例としては、限定することなく、例えば、細胞培養皿、細胞培養ボトルなどが挙げられる。
また、容器は、平坦であることが好ましい。また、その面積は特に限定されないが、典型的には、1〜200cm2、好ましくは2〜100cm2、より好ましくは3〜50cm2である。
また、容器は、その内部に固形もしくは半固形の表面を有してもよい。固形の表面としては、上記のごとき種々の材料のプレートや容器などが、半固形の表面としては、ゲル、軟質のポリマーマトリクスなどが挙げられ、これらのうち1種または2種以上を組み合わせて用いることができる。
血清としては、異種血清および同種血清を用いることができる。異種血清は、細胞培養物を移植する場合、レシピエントとは異なる種の生物に由来する血清を意味する。例えば、レシピエントがヒトである場合、ウシやウマに由来する血清、例えば、ウシ胎仔血清(FBS、FCS)、仔ウシ血清(CS)、ウマ血清(HS)などが異種血清に該当する。また、「同種血清」は、レシピエントと同一の種の生物に由来する血清を意味する。例えば、レシピエントがヒトである場合、ヒト血清が同種血清に該当する。同種血清は、自己血清、すなわち、レシピエントに由来する血清を含む。
このような血清は、市販されているか、または、所望の生物から採取した血液から定法により調製することができる。具体的には、例えば、採取した血液を室温で20〜60分程度放置して凝固させ、これを1000〜1200×g程度で遠心分離し、上清を採取する方法などが挙げられる。
また、本明細書において、「成長因子」は、細胞の増殖を、それがない場合に比べて促進する任意の物質を意味し、例えば、上皮細胞成長因子(EGF)、血管内皮成長因子(VEGF)、線維芽細胞成長因子(FGF)などを含む。
生物材料の希釈、分散、溶解に用いることの出来る液体としては、任意の媒体、例えば、限定することなく、水、生理食塩水、種々の緩衝液(例えば、PBS、HBSなど)、種々の液体培地(例えば、DMEM、MEM、F12、DME、RPMI1640、MCDB(MCDB102、104、107、131、153、199など)、L15、SkBM、RITC80−7、DMEM/F12など)等が挙げられ、これらのうち1種または2種以上を組み合わせて用いることができる。
また、生物材料が血清である場合、その希釈濃度は、血清成分が培養基材上に付着することができれば特に限定されず、例えば、0.5〜90%(v/v)、好ましくは1〜60%(v/v)、より好ましくは5〜40%(v/v)である。
また、液体中にかかる成分が含まれる場合、その液体中における濃度は、例えば、0.1μg/mL〜100μg/mL、好ましくは0.4μg/mL〜40μg/mL、より好ましくは1μg/mL〜10μg/mLとすることができる。
培養基材上の液体に気泡が存在する場合、後述する第3の工程において、生物材料が培養基材の表面に均一に固定されず、培養基材の一部において生物材料が付着しにくい部分が生じる場合がある。このような場合には、生物材料が十分に付着していない部分には、シート状細胞培養物が形成されず、結果としてシート状細胞培養物に孔等の欠点が生じる場合がある。このため、本発明においては、本工程において上記気泡を検出して、その気泡を除去または液体の入れ替えを行うことにより、上記問題を防止している。
上述した中でも、培養基材上の液体に超音波を照射し、その透過率を測定することによって、気泡を検出することが好ましい。これにより、比較的精度よく、液体中の気泡を検出することができる。なお、気泡が存在すると、超音波の透過率が低下するため、一定以上の値の透過率を示した場合を、気泡がないものとし、それより低い値の透過率を示した場合、気泡が存在するものとして取り扱うことができる。
気泡の除去方法としては、特に限定されず、例えば、超音波等の振動または針等で気泡に刺激を与えることにより気泡を破壊する方法、ピペット等の吸引手段により気泡を吸引する方法、培養基材を振動させて気泡を除去する方法等が挙げられ、これらのうち、1種または2種以上を組み合わせて用いることができる。
また、気泡が検出されない場合には、次の第3の工程を行う(エンド)。
プレインキュベート時間は、生物材料の成分が培養基材上に付着することができれば特に限定されず、例えば、1〜72時間、好ましくは4〜48時間、より好ましくは5〜24時間、さらに好ましくは6〜12時間である。
また、プレインキュベート温度も、生物材料の成分が培養基材上に付着することができれば特に限定されず、例えば、0〜60℃、好ましくは4〜45℃、より好ましくは室温〜40℃である。
洗浄液としては、培養基材に付着した生物材料の成分に悪影響を与えない液体媒体であれば特に限定されず、例えば、限定することなく、水、生理食塩水、種々の緩衝液(例えば、PBS、HBSなど)、種々の液体培地(例えば、DMEM、MEM、F12、DME、RPMI1640、MCDB(MCDB102、104、107、131、153、199など)、L15、SkBM、RITC80−7、DMEM/F12など)等で行うことができる。
洗浄手法としては、慣用の培養基材洗浄手法、例えば、限定することなく、培養基材上に洗浄液を加えて所定時間(例えば、5〜60秒間)攪拌後、廃棄する手法などを用いることができる。
本発明に用いることの出来る細胞としては、細胞培養物、特にシート状の細胞培養物を形成し得る任意の細胞が含まれる。かかる細胞の例としては、限定されずに、筋芽細胞(例えば、骨格筋芽細胞)、心筋細胞、線維芽細胞、滑膜細胞、上皮細胞(例えば、角膜上皮細胞、口腔粘膜上皮細胞)、内皮細胞、肝細胞、膵細胞、歯根膜細胞、皮膚細胞などが含まれる。これらのうち、本発明においては、単層の細胞培養物を形成するもの、例えば、筋芽細胞が好ましい。ここで、単層の細胞培養物とは、細胞から形成される層が1つであることを意味する。そして、このような層は、細胞が垂直方向に1つしかない状態で平面上に広がった状態のみならず、垂直方向に複数個の細胞が存在するような厚みを有するように形成された状態をも含んでいる。
細胞は、細胞培養物による治療が可能な任意の生物に由来し得る。かかる生物には、限定されずに、例えば、ヒト、非ヒト霊長類、イヌ、ネコ、ブタ、ウマ、ヤギ、ヒツジなどが含まれる。
また、本発明の方法に用いる細胞は1種類のみであってもよいが、2種類以上の細胞を用いることもできる。本発明の好ましい態様において、細胞培養物を形成する細胞が2種類以上ある場合、最も多い細胞の比率(純度)は、細胞培養物製造終了時において、65%以上、好ましくは70%以上、より好ましくは75%以上である。
培養に用いる細胞培養液(単に「培養液」もしくは「培地」と呼ぶ場合もある)は、細胞の生存を維持できるものであれば特に限定されないが、典型的には、アミノ酸、ビタミン類、電解質を主成分としたものが利用できる。本発明の一態様において、培養液は、細胞培養用の基礎培地をベースにしたものである。かかる基礎培地には、限定されずに、例えば、DMEM、MEM、F12、DME、RPMI1640、MCDB(MCDB102、104、107、131、153、199など)、L15、SkBM、RITC80−7などが含まれる。これらの基礎培地の多くは市販されており、その組成も公知となっている。
これにより、シート状細胞培養物が得られる。播種された細胞は、培養基材の表面に付着してこれらが連結することにより、シート状細胞培養となる。本発明においては、培養基材の表面は、生物材料が均一に固定されているため、細胞と培養基材との間の親和性がむらなく調節されており、得られるシート状細胞培養物は、孔等の欠点の発生が抑制された均一なものとなる。
また、細胞の培養は、所定の期間内、好ましくは、細胞が分化に移行しない期間内に行われる。したがって、この態様において、細胞は、培養期間中、未分化の状態に維持される。細胞の分化への移行は、当業者に知られた任意の方法で評価することができる。例えば、骨格筋芽細胞の場合は、MHCの発現や、細胞の多核化を分化の指標とすることができる。本発明の好ましい態様において、培養期間は48時間以内、より好ましくは40時間以内、さらに好ましくは24時間以内である。
気泡検出システム1は、キャビネット2と、トレー3と、気泡検出手段4と、制御部5と液体供給回収手段6を有している。
また、キャビネット2は、空間21においてプレインキュベートを実施することが可能なように構成されている。したがって、気泡検出システム1は、気泡の検出、除去、プレインキュベートを当該装置内で、基材101を移動させることなく実施することが可能である。
また、トレー3の中央付近には、基材101の設置部位において、基材101の底面の形状に対応した形状の貫通孔が設けられており、当該貫通孔には、後述する超音波照射手段41が設置される。
超音波照射手段41は、基材101の設置部位に対応して、トレー3の貫通孔に配置されている。超音波照射手段41は、制御部5の指示に応じて超音波を基材101上にある液体100に照射する。
超音波測定手段42は、基材101の超音波照射手段41とは反対側の面側、すなわち、基材101の上側に設置され、基材101および液体100を通過した超音波を検出し、その量を測定するものである。そして、その測定値は、制御部5に送信される。
また、超音波測定手段42は、上下に移動可能であり、例えば、上側に移動した際には、超音波測定手段42と超音波照射手段41との間に形成される空間において、基材101の設置、設置された基材101への液体の供給、回収等が可能となるように構成されている。
制御部5は、判定手段51と、記憶部52とを有している。
判定手段51は、気泡検出手段4の検出結果に基づいて気泡の有無を判定するものであり、超音波照射手段41から照射した超音波の照射量に対する、基材101および液体100を通過した超音波の検出量を計算することにより、基材101および液体100の超音波の透過率を算出する。判定手段51は、透過率が設定値未満である場合には、気泡が検出されたものとして判定し、後述する出力手段54にその旨出力する。一方、判定手段51は、透過率が設定値以上である場合には、気泡が検出されないものとして判定し、後述する出力手段54にその旨出力する。
このような制御部5は、例えば、公知の中央演算処理装置、内部記憶装置、外部記憶装置等を用いて構成されることが出来る。
入力手段53は、例えば、キーボード、マウス、タブレット等であり、使用者が気泡検出システム1の操作を行う際に、制御部5へ指示を入力、送信することが出来る。
出力手段54は、例えば、ディスプレイ、プリンタ等であり、例えば得られた気泡の検出結果や、気泡検出システム1の操作に必要な情報等を表示することが出来る。
貯留部61は、基材101へ供給する液体100(本実施態様では液体培地)を貯留する。
供給手段62は、貯留部61と連通しており、貯留部61にある液体100を基材101上に供給する。
回収手段63は、基材101上にある液体100を吸引することにより回収する。回収された液体100は、図示せぬ排出手段によって、気泡検出システム1の系外へ排出される。
このような供給手段62および回収手段63は、例えば、可撓性を有するチューブと、その先端に接続されかつチューブと反対側に向けて縮経した円筒状の供給部または回収部とをそれぞれ備え、供給部および回収部が上記移動手段により移動可能となることにより、構成される。
供給回数が上記回数を超えていない場合には、液体供給回収手段6の回収手段63により培養液が回収され、培養液は、基材101上から除去されて図示せぬ排出手段を介して判定システム1の系外に排出される(S−6)。さらに、S−1のステップに戻り、基材101へ培養液(液体100)が再度付与される。
一方、供給回数が上記回数を超えた場合には、出力手段54に、エラーの旨の表示を行い(S−7)、終了する(エンド)。
例えば、各構成は、同様の機能を発揮し得る任意のものと置換することができ、あるいは、任意の構成のものを付加することもできる。
2 キャビネット
21 空間
3 トレー
4 気泡検出手段
41 超音波照射手段
42 超音波測定手段
5 制御部
51 判定手段
52 記憶部
53 入力手段
54 出力手段
6 液体供給回収手段
61 貯留部
62 供給手段
63 回収手段
100 液体
101 基材
Claims (8)
- 生物材料を含む液体を基材上に付与する第1の工程と、
基材上の液体における気泡を検出する第2の工程と、
生物材料を基材に固定する第3の工程と、
基材上に細胞を播種する第4の工程と、
細胞を培養してシート状細胞培養物を形成する第5の工程と、を含み、
第2の工程において、気泡が検出された場合には、気泡を除去するまたは前記液体を基材から除去して第1の工程を再度行うシート状細胞培養物の製造方法。 - 第4の工程における細胞の播種が、細胞が実質的に増殖することなくシート状細胞培養物を形成し得る密度で行われる、請求項1に記載の方法。
- 生物材料が、タンパク質を含む組成物であり、かつ、当該組成物のタンパク質の基材への固定をプレインキュベートによって行う、請求項1または2に記載の方法。
- 生物材料は血清である、請求項1〜3のいずれか一項に記載の方法。
- 気泡の検出を、液体に超音波を照射した際の超音波の透過率を測定することによって行う、請求項1〜4のいずれか一項に記載の方法。
- シート状細胞培養物形成用基材の製造方法であって、
生物材料を含む液体を基材上に付与する第1の工程と、
基材上の液体における気泡を検出する第2の工程と、
生物材料を基材に固定する第3の工程と、を含み、
第2の工程において、気泡が検出された場合には、気泡を除去するまたは前記液体を基材から除去して第1の工程を再度行う前記方法。 - シート状細胞培養物の製造時において、生物材料を含む液体を基材上に付与した後、かつ生物材料を基材に固定する前に、基材上の液体における気泡を検出する工程を含み、
気泡が検出された場合には、当該気泡を吸引または破壊することにより除去するまたは前記液体を基材から除去して新たな生物材料を含む液体を基材上に付与する気泡の除去方法。 - 請求項7に記載の気泡の除去方法を実行するための気体の検出システムであって、
基材上に付与された生物材料を含む液体における気泡を検出するための気泡検出手段と、
気泡検出手段の検出結果に基づいて気泡の有無を判定する判定手段とを含むことを特徴とする、前記システム。
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2011015083A JP6055166B2 (ja) | 2011-01-27 | 2011-01-27 | シート状細胞培養物の製造方法、シート状細胞培養物形成用基材の製造方法、気泡の除去方法および気体の検出システム |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2011015083A JP6055166B2 (ja) | 2011-01-27 | 2011-01-27 | シート状細胞培養物の製造方法、シート状細胞培養物形成用基材の製造方法、気泡の除去方法および気体の検出システム |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2012152154A true JP2012152154A (ja) | 2012-08-16 |
| JP6055166B2 JP6055166B2 (ja) | 2016-12-27 |
Family
ID=46834601
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2011015083A Active JP6055166B2 (ja) | 2011-01-27 | 2011-01-27 | シート状細胞培養物の製造方法、シート状細胞培養物形成用基材の製造方法、気泡の除去方法および気体の検出システム |
Country Status (1)
| Country | Link |
|---|---|
| JP (1) | JP6055166B2 (ja) |
Cited By (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2014138556A (ja) * | 2013-01-21 | 2014-07-31 | Terumo Corp | シート状細胞培養物の製造方法 |
| JP2015043750A (ja) * | 2013-08-29 | 2015-03-12 | 大日本印刷株式会社 | 培地充填方法 |
| WO2016104666A1 (ja) * | 2014-12-26 | 2016-06-30 | テルモ株式会社 | 液体移送方法 |
Citations (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPH06178808A (ja) * | 1992-12-14 | 1994-06-28 | Sharp Corp | 輸液装置 |
| JP2007130290A (ja) * | 2005-11-11 | 2007-05-31 | Terumo Corp | 体外循環装置 |
| WO2010023914A1 (ja) * | 2008-08-29 | 2010-03-04 | 株式会社ジェイ・エム・エス | 輸液装置 |
| JP2010521246A (ja) * | 2007-03-15 | 2010-06-24 | ボストン サイエンティフィック リミテッド | 細胞接着性のタンパク質及びペプチドの安定性を改善する方法 |
| JP2010226991A (ja) * | 2009-03-26 | 2010-10-14 | Terumo Corp | シート状細胞培養物の製造方法 |
| JP2010280719A (ja) * | 2009-03-09 | 2010-12-16 | Menicon Co Ltd | 自己組織化ペプチドおよび高強度ペプチドゲル |
-
2011
- 2011-01-27 JP JP2011015083A patent/JP6055166B2/ja active Active
Patent Citations (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPH06178808A (ja) * | 1992-12-14 | 1994-06-28 | Sharp Corp | 輸液装置 |
| JP2007130290A (ja) * | 2005-11-11 | 2007-05-31 | Terumo Corp | 体外循環装置 |
| JP2010521246A (ja) * | 2007-03-15 | 2010-06-24 | ボストン サイエンティフィック リミテッド | 細胞接着性のタンパク質及びペプチドの安定性を改善する方法 |
| WO2010023914A1 (ja) * | 2008-08-29 | 2010-03-04 | 株式会社ジェイ・エム・エス | 輸液装置 |
| JP2010280719A (ja) * | 2009-03-09 | 2010-12-16 | Menicon Co Ltd | 自己組織化ペプチドおよび高強度ペプチドゲル |
| JP2010226991A (ja) * | 2009-03-26 | 2010-10-14 | Terumo Corp | シート状細胞培養物の製造方法 |
Non-Patent Citations (2)
| Title |
|---|
| BD BIOCOAT AND BD FALCON FLUOROBLOK TIPS AND TECHNIQUES [ONLINE], JPN6015004090, 27 April 2010 (2010-04-27), pages 19, ISSN: 0002998214 * |
| 三井洋司監, 動物細胞培養の実際, vol. 初版, JPN6015051661, 1990, pages 36, ISSN: 0003222156 * |
Cited By (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2014138556A (ja) * | 2013-01-21 | 2014-07-31 | Terumo Corp | シート状細胞培養物の製造方法 |
| JP2015043750A (ja) * | 2013-08-29 | 2015-03-12 | 大日本印刷株式会社 | 培地充填方法 |
| WO2016104666A1 (ja) * | 2014-12-26 | 2016-06-30 | テルモ株式会社 | 液体移送方法 |
| JPWO2016104666A1 (ja) * | 2014-12-26 | 2017-10-05 | テルモ株式会社 | 液体移送方法 |
| US10787633B2 (en) | 2014-12-26 | 2020-09-29 | Terumo Kabushiki Kaisha | Liquid transport method |
| US11261412B2 (en) | 2014-12-26 | 2022-03-01 | Terumo Kabushiki Kaisha | Liquid transport method |
Also Published As
| Publication number | Publication date |
|---|---|
| JP6055166B2 (ja) | 2016-12-27 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| Tysoe et al. | Isolation and propagation of primary human cholangiocyte organoids for the generation of bioengineered biliary tissue | |
| Jiao et al. | Thermoresponsive nanofabricated substratum for the engineering of three-dimensional tissues with layer-by-layer architectural control | |
| JP2011172925A (ja) | 医療用積層体 | |
| CA2842023C (en) | Method and cell culture apparatus for long-term cell culture | |
| WO2004011593A1 (ja) | 生体由来の細胞または組織の自動培養装置 | |
| JPWO2015005349A1 (ja) | 細胞培養支持体、細胞培養装置、細胞培養キット、及び細胞シート | |
| JP6055166B2 (ja) | シート状細胞培養物の製造方法、シート状細胞培養物形成用基材の製造方法、気泡の除去方法および気体の検出システム | |
| JP4649224B2 (ja) | 付着性細胞の培養方法および培養装置 | |
| US11697794B2 (en) | Method for producing layered cell sheet and layered cell sheet produced by the same | |
| JP2007508816A5 (ja) | ||
| JP6228723B2 (ja) | シート形成細胞播種システム | |
| JP2012159408A (ja) | 脆弱試料の引張特性測定方法 | |
| WO2021100718A1 (ja) | 細胞集合体、その製造方法、その作製キット、及びそれを用いた化合物の評価方法 | |
| Helfer et al. | Frame-hydrogel methodology for engineering highly functional cardiac tissue constructs | |
| CN109153963B (zh) | 粘附状态的细胞培养物的改变方法 | |
| EP4039701A1 (en) | Method for producing fibrin sheet | |
| JP2011155869A (ja) | シート状細胞培養物剥離システム | |
| US20170121664A1 (en) | Cell separation device and cell separation method | |
| Nagymihaly et al. | Isolation and culture of corneal stromal stem cells | |
| JPWO2016152592A1 (ja) | シート状細胞培養物の評価方法 | |
| JP5917000B2 (ja) | シート形成評価方法 | |
| WO2023145797A1 (ja) | 細胞剥離方法、細胞剥離システム及び情報処理装置 | |
| WO2024117025A1 (ja) | 細胞剥離方法、細胞剥離システム及び情報処理装置 | |
| JP2023111839A (ja) | 細胞剥離方法、細胞剥離システム及び情報処理装置 | |
| CN112852719B (zh) | 一种临床级干细胞无血清培养基 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20131205 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20150210 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20150401 |
|
| A02 | Decision of refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A02 Effective date: 20150813 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20151111 |
|
| A911 | Transfer to examiner for re-examination before appeal (zenchi) |
Free format text: JAPANESE INTERMEDIATE CODE: A911 Effective date: 20151119 |
|
| A912 | Re-examination (zenchi) completed and case transferred to appeal board |
Free format text: JAPANESE INTERMEDIATE CODE: A912 Effective date: 20151225 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20161202 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 6055166 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |