JP2012136641A - 重合性キラル化合物、重合性液晶組成物、液晶性高分子及び光学異方体 - Google Patents
重合性キラル化合物、重合性液晶組成物、液晶性高分子及び光学異方体 Download PDFInfo
- Publication number
- JP2012136641A JP2012136641A JP2010290080A JP2010290080A JP2012136641A JP 2012136641 A JP2012136641 A JP 2012136641A JP 2010290080 A JP2010290080 A JP 2010290080A JP 2010290080 A JP2010290080 A JP 2010290080A JP 2012136641 A JP2012136641 A JP 2012136641A
- Authority
- JP
- Japan
- Prior art keywords
- group
- formula
- independently
- polymerizable
- liquid crystal
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Granted
Links
- VRHGLODXIVTURM-AITUUCJRSA-N CC(C)[C@H](CC[C@@H](C)C1)/C1=N/N Chemical compound CC(C)[C@H](CC[C@@H](C)C1)/C1=N/N VRHGLODXIVTURM-AITUUCJRSA-N 0.000 description 1
- CIIWTVCFBGVXGZ-CWDWHVAESA-N CC(C)[C@H](CC[C@@H](C)C1)/C1=N/N=C/c(cc1)ccc1OCCCCCCOC(C=C)=O Chemical compound CC(C)[C@H](CC[C@@H](C)C1)/C1=N/N=C/c(cc1)ccc1OCCCCCCOC(C=C)=O CIIWTVCFBGVXGZ-CWDWHVAESA-N 0.000 description 1
- NOOLISFMXDJSKH-ZDGBYWQASA-N CC(C)[C@H](CC[C@@H](C)C1)C1O Chemical compound CC(C)[C@H](CC[C@@H](C)C1)C1O NOOLISFMXDJSKH-ZDGBYWQASA-N 0.000 description 1
Abstract
Description
目的に応じた光学異方体を製造するためには、その目的に応じた回転方向の円偏向を分離する必要がある。そのためには左右両螺旋回転方向のコレステリック規則性を得る必要がある。
例えば、特許文献1には、式:(Z11−Y11−A11−O−CO−O−M11−Y12)r1Xa〔式中、A11は橋かけ基、M11はメソゲン基、Y11及びY12は、化学結合、−O−、−S−、−CO−O−、−O−CO−、−O−CO−O−、−CO−N(Ra)−、又は、−N(Ra)−CO−、Raは水素原子又はC1〜C4アルキル基、Xaはr1価のキラル基、r1は2〜6の整数、Z11は、(α1)少なくとも1つは、重付加反応に関与することができる反応性基であり、(α2)少なくとも2つは、重付加反応に関与することができる反応性基を持つ置換基である。(β1)条件(α1)又は(α2)が満足される限り、水素原子又は非反応性基である。〕で示されるキラル化合物が開示されている。
また、特許文献5には、下記化1で示される化合物に代表されるイソソルビト誘導体が、キラルドーパントとして有用である旨が開示されている。
唯一、左螺旋を誘起する重合性キラル化合物が特許文献3に例示されている。しかしながら、この文献に記載されている化合物は螺旋捻れ力(HTP)の記載がないものか、低いHTPしか発現しないものがほとんどである。なかには、HTP=63と高い化合物も例示されているが、使用に際しては、溶解性が低い課題を有しているだけでなく、経済面でも多工程で高コストである問題点を有していた。
(1)下記式(I)
G1は、置換基を有していてもよい、炭素数1〜20の2価の脂肪族基を表す。該脂肪族基には、−O−、−S−、−O−C(=O)−、−C(=O)−O−、−O−C(=O)−O−、−NR2−C(=O)−、−C(=O)−NR2−、−NR2−、又は−C(=O)−が介在していてもよい(ただし、−O−、又は、−S−がそれぞれ2以上隣接して介在する場合を除く。)。ここで、R2は、水素原子又は炭素数1〜6のアルキル基を表す。
A1及びA2はそれぞれ独立して、置換基を有していてもよい炭素数1〜20の2価の脂肪族基、又は、置換基を有していてもよい炭素数6〜20の芳香族基を表し、
Z1は、ハロゲン原子で置換されていてもよい炭素数2〜10のアルケニル基を表す。
Qは、水素原子、置換基を有していてもよい炭素数1〜6のアルキル基、又は下記式(2)
aは0又は1を表し、bは1又は2を表す。〕
で示される左螺旋を誘起する重合性キラル化合物。
(2)前記式(I)中、A1〜A3が、それぞれ独立して、置換基を有していてもよいフェニレン基、置換基を有していてもよいビフェニレン基、又は置換基を有していてもよいナフチレン基である、(1)に記載の左螺旋を誘起する重合性キラル化合物。
(3)前記式(I)中、Z1及びZ2がそれぞれ独立して、CH2=CH−、CH2=C(CH3)−、CH2=C(Cl)−、CH2=CH−CH2−、CH2=C(CH3)−CH2−、CH2=C(CH3)−CH2CH2−、(CH3)2C=CH−CH2−、CH3−CH=CH−、CH3−CH=CH−CH2−、CH2=CH−CH2−CH2−、又は、(CH3)2C=CH−CH2−CH2−である、(1)又は(2)に記載の左螺旋を誘起する重合性キラル化合物。
G1及びG2がそれぞれ独立して、−O−、−C(=O)−O−、−O−C(=O)−、−C(=O)−が介在していてもよい(ただし、−O−が2以上隣接して介在する場合を除く。)、−(CH2)4−、又は−(CH2)6−を表し、Z1及びZ2がそれぞれ独立して、CH2=CH−、CH2=C(CH3)−、又は、CH2=C(Cl)−を表し、
A1〜A3がそれぞれ独立して、下記(a1)、(a2)又は(a3)
(5)前記式(I)中、Y1〜Y5がそれぞれ独立して、−C(=O)−O−、−O−C(=O)−、又は、−O−を表し、
G1及びG2がそれぞれ独立して、−(CH2)4−、又は、−(CH2)6−を表し、
Z1及びZ2がそれぞれ独立して、CH2=CH−、又は、CH2=C(CH3)−を表し、
A1〜A3がそれぞれ独立して、前記(a1)又は(a2)で表される基である、
(1)〜(4)のいずれかに記載の左螺旋を誘起する重合性キラル化合物。
(6)前記式(I)中、Y1〜Y5がそれぞれ独立して、−C(=O)−O−、−O−C(=O)−、又は、−O−を表し、
G1及びG2がそれぞれ独立して、−(CH2)4−、又は、−(CH2)6−を表し、
Z1及びZ2が、CH2=CH−を表し、
Qが、水素原子又はメチル基を表し、
A1が、前記(a1)で表される基であり、
aは0であり、bは1である、(1)〜(5)のいずれかに記載の左螺旋を誘起する重合性キラル化合物。
(7)前記(1)〜(6)のいずれかに記載の重合性化合物、及び、重合可能な液晶化合物を含有する左螺旋性重合性液晶組成物。
(8)前記(1)〜(6)のいずれかに記載の重合性キラル化合物、又は、(7)に記載の左螺旋性重合性液晶組成物を重合して得られる左螺旋性液晶性高分子。
(9)前記(8)に記載の左螺旋性液晶性高分子を構成材料とする光学異方体。
本発明の重合性キラル化合物、又は本発明の重合性液晶組成物を重合することにより、実用的なHTPを有する左螺旋性(左円偏光のみを選択反射する)液晶性高分子を得ることができる。
本発明の左螺旋を誘起する重合性キラル化合物(以下、「本発明の重合性キラル化合物」ということがある。)は、前記式(I)で表される化合物である。ここで、「左螺旋を誘起する」とは、重合性液晶化合物に混合されることで、左螺旋性のコレステリック相を発現させる性質を有することを意味する。
これらの中でも、−O−、−O−C(=O)−、及び、−C(=O)−O−が好ましい。
G1の炭素数1〜20の2価の脂肪族基としては、鎖状構造を有する脂肪族基であっても、脂環式構造を有する脂肪族基であってもよい。これらの中でも、本発明の所望の効果をより良好に発現させる観点から、置換基を有していてもよい、鎖状構造を有する炭素数1〜20の2価の脂肪族基が好ましく、炭素数1〜20のアルキレン基、炭素数2〜20のアルケニレン基等の、鎖状構造を有する炭素数1〜20の2価の脂肪族基がより好ましく、メチレン基、エチレン基、トリメチレン基、プロピレン基、テトラメチレン基、ペンタメチレン基、ヘキサメチレン基、オクタメチレン基等の、炭素数1〜12のアルキレン基がさらに好ましく、ヘキサメチレン基〔−(CH2)6−〕が特に好ましい。
ただし、−O−、又は、−S−がそれぞれ2以上隣接して介在する場合は除かれる。
これらの中でも、−O−、−O−C(=O)−、−C(=O)−O−、及び、−C(=O)−が好ましい。
前記芳香族基としては、1つのベンゼン環を有する、2価の単環芳香族基や、2つ以上、通常、2〜4個のベンゼン環を有する、2価の多環芳香族基が挙げられる。
これらの中でも、A1及びA2が、それぞれ独立して、下記(a1)、(a2)、又は(a3)で表されるいずれかの基であることが好ましく、(a1)又は(a2)で表される基であることがより好ましく、A1及びA2がともに、(a1)で表される基であることが特に好ましい。
R3の、置換基を有していてもよい炭素数1〜10のアルキル基の炭素数1〜10のアルキル基としては、メチル基、エチル基、n−プロピル基、イソプロピル基、n−ブチル基、s−ブチル基、イソブチル基、t−ブチル基、n−ペンチル基、n−ヘキシル基、n−ヘプチル基、n−オクチル基、n−ノニル基、n−デシル基等が挙げられ、好ましくは、メチル基、エチル基、n−プロピル基及びイソプロピル基である。
R4〜R6の炭素数1〜6のアルキル基としては、メチル基、エチル基、n−プロピル基、イソプロピル基、n−ブチル基、s−ブチル基、イソブチル基、t−ブチル基、n−ペンチル基、n−ヘキシル基等が挙げられ、好ましくは、メチル基、エチル基、n−プロピル基及びイソプロピル基である。
また、置換基のハロゲン原子としては、フッ素原子、塩素原子、臭素原子等が挙げられ、塩素原子が好ましい。
式(2)中、Y4及びY5は前記Y1〜Y3と同じ意味を表し、A3は前記A1、A2と同じ意味を表し、G2は前記G1と同じ意味を表し、Z2は前記Z1と同じ意味を表す。
かかる環としては、ベンゼン環;シクロペンタン環、シクロヘキサン環、シクロヘプタン環、シクロオクタン環等のシクロアルキル環;下記式で表されるフルオレン環;等が挙げられる。
(α)前記式(I)中、Y1〜Y5がそれぞれ独立して、−C(=O)−O−、−O−C(=O)−、又は、−O−を表し、
G1及びG2がそれぞれ独立して、−O−、−C(=O)−O−、−O−C(=O)−、−C(=O)−が介在していてもよい(ただし、−O−が2以上隣接して介在する場合を除く。)、−(CH2)4−、又は−(CH2)6−を表し、
Z1及びZ2がそれぞれ独立して、CH2=CH−、CH2=C(CH3)−、又は、CH2=C(Cl)−を表し、
A1〜A3がそれぞれ独立して、前記(a1)、(a2)又は(a3)で表される基である化合物が好ましく、
(β)前記式(I)中、Y1〜Y5がそれぞれ独立して、−C(=O)−O−、−O−C(=O)−、又は、−O−を表し、
G1及びG2がそれぞれ独立して、−(CH2)4−、又は、−(CH2)6−を表し、
Z1及びZ2がそれぞれ独立して、CH2=CH−、又は、CH2=C(CH3)−を表し、
A1〜A3がそれぞれ独立して、前記(a1)又は(a2)で表される基である化合物がより好ましく、
(γ)前記式(I)中、Y1〜Y5がそれぞれ独立して、−C(=O)−O−、−O−C(=O)−、又は、−O−を表し、
G1及びG2がそれぞれ独立して、−(CH2)4−、又は、−(CH2)6−を表し、
Z1及びZ2がCH2=CH−を表し、
Qが水素原子又はメチル基を表し、
A1及びA2が、前記(a1)で表される基である化合物が更に好ましい。
R14は水素原子または炭素数1〜6のアルキル基を表す。
n、mはそれぞれ独立して、1〜20の整数を表す。
Q1は、水素原子、置換基を有していてもよい炭素数1〜6のアルキル基、又は下記式(2A)
Q2は、水素原子、置換基を有していてもよい炭素数1〜6のアルキル基、又は下記(2B)
Q3は、水素原子、置換基を有していてもよい炭素数1〜6のアルキル基、又は下記(2C)
(左螺旋を誘起する重合性キラル化合物の製造方法)
本発明の重合性キラル化合物はいずれも、−O−、−S−、−NH−C(=O)−、−C(=O)−NH−、−NH−C(=O)−NH−、−O−C(=O)−、−C(=O)−O−等の種々の化学結合を形成する公知の方法(例えば、サンドラー・カロ官能基別有機化合物合成法[I]、[II] 廣川書店、1976年発行参照)を組み合わせて製造することができる。
(i)式:D1−hal(halはハロゲン原子を表す。以下にて同じ。)で表される化合物と、式:D2−OMet(Metはアルカリ金属(主にナトリウム)を表す。以下にて同じ。)で表される化合物とを混合して縮合させる。なお、式中、D1及びD2は任意の有機基を表す(以下にて同じ。)。この反応は一般的にウイリアムソン合成と呼ばれる。
(ii)式:D1−halで表される化合物と、式:D2−OHで表される化合物とを水酸化ナトリウム、水酸化カリウム等の塩基存在下、混合して縮合させる。
(iii)式:D1−E(Eはエポキシ基を表す。)で表される化合物と、式:D2−OHで表される化合物とを水酸化ナトリウム、水酸化カリウム等の塩基存在下、混合して縮合させる。
(iv)式:D1−OFN(OFNは不飽和結合を有する基を表す。)で表される化合物と、式:D2−OMetで表される化合物を、水酸化ナトリウム、水酸化カリウム等の塩基存在下、混合して付加反応させる。
(v)式:D1−halで表される化合物と、式:D2−OMetで表される化合物とを、銅あるいは塩化第一銅存在下、混合して縮合させる。この反応は一般的にウルマン縮合と呼ばれる。
(vi)式:D1−COOHで表される化合物と、式:D2−OH又はD2−NH2で表される化合物とを、脱水縮合剤(N,N−ジシクロヘキシルカルボジイミド等)の存在下に脱水縮合させる。
(vii)式:D1−COOHで表される化合物にハロゲン化剤を作用させることにより、式:D1−CO−halで表される化合物を得、このものと式:D2−OH又はD2−NH2で表される化合物とを、塩基の存在下に反応させる。
(viii)式:D1−COOHで表される化合物に酸無水物を作用させることにより、混合酸無水物を得た後、このものに、式:D2−OH又はD2−NH2で表される化合物を反応させる。
(ix)式:D1−COOHで表される化合物と、式:D2−OH又はD2−NH2で表される化合物とを、酸触媒あるいは塩基触媒の存在下に脱水縮合させる。
(x)式:D1−COOHで表される化合物に三塩化リンあるいは五塩化リンを作用させる。
(xi)式:D1−COOHで表される化合物に塩化チオニルを作用させる。
(xii)式:D1−COOHで表される化合物に塩化オキサリルを作用させる。
(xiii)式:D1−COOAg(Ag:銀元素)で表される化合物に塩素を作用させる。
(xiv)式:D1−COOHで表される化合物に赤色酸化第二水銀の四塩化炭素溶液を作用させる。
水酸基を保護する方法としては、公知の方法(例えば、Greene’s Protective Groups in Organic Synthesis 第3版 出版:Wiley−Interscience、1999年発行参照)を利用して製造することができる。
(xv)式:D1D2D3−Si−halで表される化合物と、式:D4−OHで表される化合物とを、イミダゾール、ピリジン等の塩基存在下、混合して反応させる。なお、式中、D3、D4は任意の有機基を表す。
(xvi)3,4−ジヒドロ−2H−ピラン等のビニルエーテルと、式:D2−OHで表される化合物を、パラトルエンスルホン酸、パラトルエンスルホン酸ピリジン塩、塩化水素等の酸存在下、混合して反応させる。
(xvii)式:D1−C(=O)−halで表される化合物と、式:D4−OHで表される化合物とを、トリエチルアミン、ピリジン等の塩基存在下、混合して反応させる。
(xviii)式:D1−C(=O)−O−C(=O)−D2で表される酸無水物と、式:D3−OHで表される化合物とを混合して反応させる、あるいは水酸化ナトリウム、トリエチルアミン等の塩基存在下、混合して反応させる。
(xix)D1−halで表される化合物と式:D2−OHで表される化合物とを、水酸化ナトリウム、トリエチルアミン等の塩基存在下、混合して反応させる。
(xx)式:D1−O−CH2−halで表される化合物と、式:D2−OHで表される化合物とを、水素化ナトリウム、水酸化ナトリウム、トリエチルアミン、ピリジン等の塩基存在下、混合して反応させる。
(xxi)D1−O−CH2−C(=O)−halで表される化合物と、式:D2−OHで表される化合物とを、炭酸カリウム、水酸化ナトリウム等の塩基存在下、混合して反応させる。
(xxii)式:D1−O−C(=O)−halで表される化合物と、式:D2−OHで表される化合物とを、トリエチルアミン、ピリジン等の塩基存在下、混合して反応させる。
(xxiii)テトラブチルアンモニウムフルオライド等フッ素イオンを混合して脱保護させる。
(xxiv)パラトルエンスルホン酸、パラトルエンスルホン酸ピリジン塩、塩化水素、酢酸等の酸存在下、混合して脱保護させる。
(xxv)水素化ナトリウム、水酸化ナトリウム、水酸化カリウム、炭酸ナトリウム、炭酸カリウム、トリエチルアミン、ピリジン等の塩基存在下、混合して脱保護させる。
(xxvi)Pd−C等の触媒存在下、水素添加することにより脱保護させる。
(製造方法1)前記式(I)で表される化合物のうち、Qが、水素原子又は置換基を有していてもよい炭素数1〜6のアルキル基である化合物(IA)は、以下に示す方法により製造することができる。
工程1に用いる塩基触媒としては、トリエチルアミン、ピリジン、ジイソプロピルエチルアミン等が挙げられる。塩基触媒の使用量は、式(III)で表される化合物1モルに対し、通常、0.1〜0.5モルである。
用いる有機溶媒としては、メタノール、エタノール、n−プロパノール、イソプロパノール、n−ブタノール等のアルコール系溶媒;ジエチルエーテル、テトラヒドロフラン、1,2−ジメトキシエタン、1,4−ジオキサン等のエーテル系溶媒;酢酸エチル、酢酸プロピル、プロピオン酸メチル等のエステル系溶媒;ベンゼン、トルエン、キシレン等の芳香族炭化水素系溶媒;n−ペンタン、n−ヘキサン、n−ヘプタン等の脂肪族炭化水素系溶媒;N,N−ジメチルホルムアミド、N−メチルピロリドン、ヘキサメチルリン酸トリアミド等のアミド系溶媒;ジメチルスルホキシド、スルホラン等の含硫黄系溶媒;及びこれらの2種以上からなる混合溶媒;等が挙げられる。
反応時間は、反応規模にもよるが、通常、数分から数時間である。
以上のようにして、式(V)で表される化合物を含む反応液を得る。
用いる有機溶媒としては、ジエチルエーテル、テトラヒドロフラン、1,2−ジメトキシエタン、1,4−ジオキサン等のエーテル系溶媒;酢酸エチル、酢酸プロピル、プロピオン酸メチル等のエステル系溶媒;ベンゼン、トルエン、キシレン等の芳香族炭化水素系溶媒;n−ペンタン、n−ヘキサン、n−ヘプタン等の脂肪族炭化水素系溶媒;N,N−ジメチルホルムアミド、N−メチルピロリドン、ヘキサメチルリン酸トリアミド等のアミド系溶媒;ジメチルスルホキシド、スルホラン等の含硫黄系溶媒;及びこれらの2種以上からなる混合溶媒;等が挙げられる。
例えば、式(V)中、Yが水酸基(OH)である化合物と、式:Z1−COOHで表されるカルボン酸とを、1−エチル−3−(3−ジメチルアミノプロピルカルボジイミド塩酸塩(WSC)等の脱水剤と4−ジメチルアミノピリジンの存在下に、脱水反応を行うことにより、末端に、式:−O−C(=O)−Z1で表される基を有する式(IA)で表される目的物を得ることができる。
すなわち、式(III)で表される化合物に、所望により、トリエチルアミン、ピリジン等の塩基触媒の存在下、式(VII)で表される化合物を反応させて、目的とする式(IB)で表される化合物(本発明の重合性キラル化合物)を得ることができる。
用いる有機溶媒としては、ジエチルエーテル、テトラヒドロフラン、1,2−ジメトキシエタン、1,4−ジオキサン等のエーテル系溶媒;酢酸エチル、酢酸プロピル、プロピオン酸メチル等のエステル系溶媒;ベンゼン、トルエン、キシレン等の芳香族炭化水素系溶媒;n−ペンタン、n−ヘキサン、n−ヘプタン等の脂肪族炭化水素系溶媒;N,N−ジメチルホルムアミド、N−メチルピロリドン、ヘキサメチルリン酸トリアミド等のアミド系溶媒;ジメチルスルホキシド、スルホラン等の含硫黄系溶媒;及びこれらの2種以上からなる混合溶媒;等が挙げられる。
反応は、−10℃から用いる溶媒の沸点までの温度範囲で円滑に進行する。
反応時間は、反応規模にもよるが、通常、数分から数時間である。
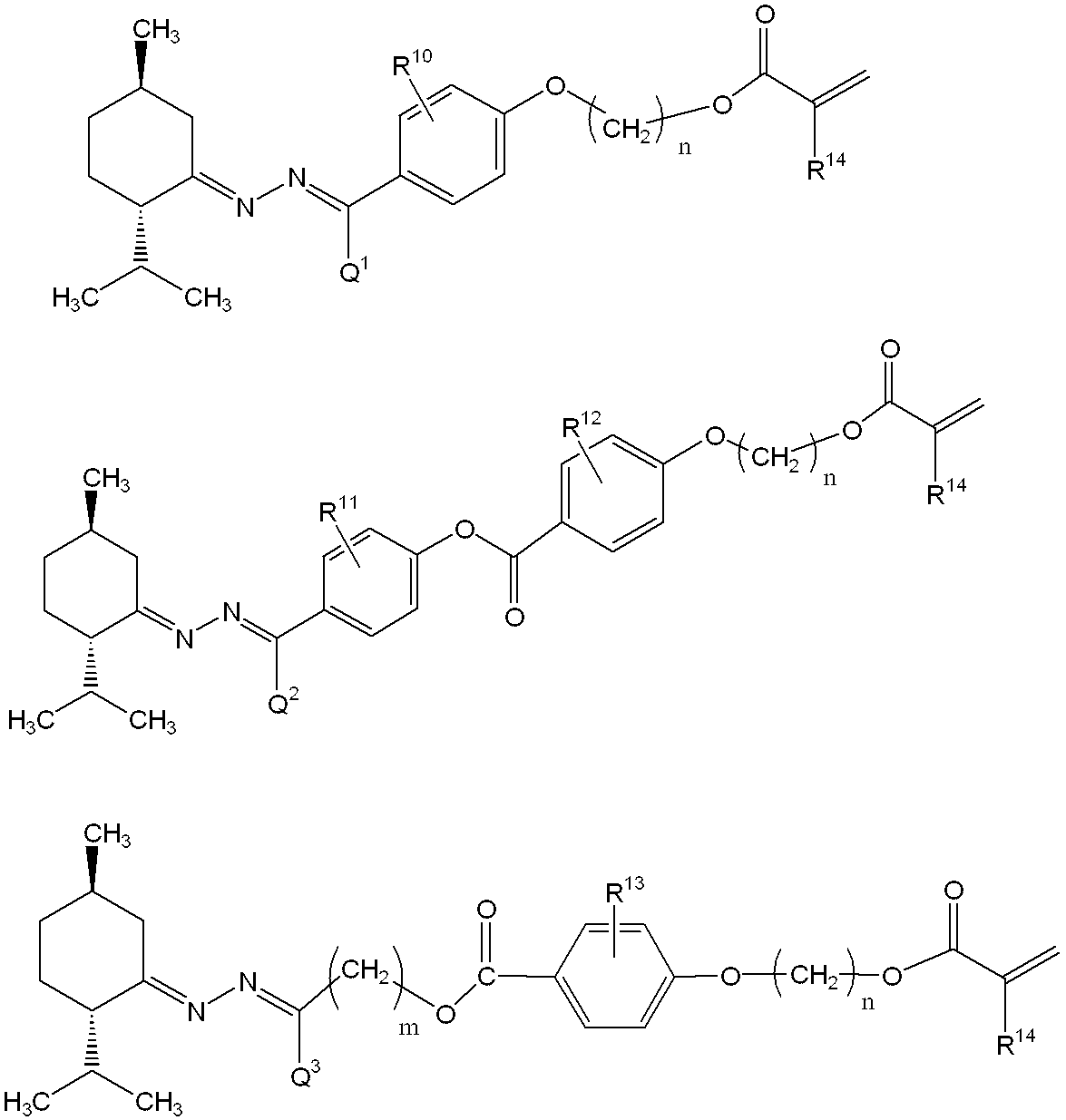
前記式(2)で表される化合物の更に好ましい具体例としては、次のものが挙げられる。
用いる有機溶媒としては、ジエチルエーテル、テトラヒドロフラン、1,2−ジメトキシエタン、1,4−ジオキサン等のエーテル系溶媒;酢酸エチル、酢酸プロピル、プロピオン酸メチル等のエステル系溶媒;ベンゼン、トルエン、キシレン等の芳香族炭化水素系溶媒;n−ペンタン、n−ヘキサン、n−ヘプタン等の脂肪族炭化水素系溶媒;N,N−ジメチルホルムアミド、N−メチルピロリドン、ヘキサメチルリン酸トリアミド等のアミド系溶媒;ジメチルスルホキシド、スルホラン等の含硫黄系溶媒;及びこれらの2種以上からなる混合溶媒;等が挙げられる。
反応は、−10℃から用いる溶媒の沸点までの温度範囲で円滑に進行する。
反応時間は、反応規模にもよるが、通常、数分から数時間である。
目的物の構造は、NMRスペクトル、IRスペクトル、マススペクトル等の測定、元素分析等により、同定することができる。
本発明の左螺旋性重合性液晶組成物(以下、「本発明の重合性液晶組成物」ということがある。)は、本発明の重合性キラル化合物の少なくとも一種、及び重合可能な液晶化合物を含有するものである。
本発明の重合性液晶組成物を構成する重合性液晶化合物は、本発明の重合性キラル化合物を混合することで、左螺旋性のコレステリック相を発現し得る。
本発明において、重合可能な液晶化合物は、一種単独で、或いは二種以上を組み合わせて用いることができる。
重合性非液晶化合物は、得られる左螺旋性液晶高分子の相転移温度を調整する目的で添加される。
重合性非液晶化合物は、一般的には、重合性単量体であって、このもの自体を重合させても液晶性高分子を得ることができないものである。
用いる重合性非液晶化合物としては、特に限定されないが、本発明の目的を達成する観点から、下記式で表される化合物が好ましい。
用いる重合開始剤としては、用いる重合性液晶化合物に存在する重合性基の種類に応じて適宜なものを選択して使用すればよい。例えば、重合性基がラジカル重合性であればラジカル重合開始剤を、アニオン重合性であればアニオン重合開始剤を、カチオン重合性であればカチオン重合開始剤を、それぞれ使用すればよい。
これらの重合開始剤は一種単独で、又は二種以上を組み合わせて用いることができる。
これらの有機溶媒は、一種単独で、或いは二種以上を組み合わせて用いることができる。
本発明の左螺旋性液晶性高分子(以下、「本発明の液晶性高分子」ということがある。)は、本発明の、重合性キラル化合物又は重合性液晶組成物を(共)重合して得られる高分子である。
ここで、「(共)重合」とは、通常の(共)重合反応のほか、(共)架橋反応を含む広い意味での化学反応を意味するものとする。
例えば、インプレーンスイッチング(IPS)方式の液晶表示素子に使用するようなプレチルト角のごく小さな配向膜を支持体上に設ければ、ほとんど水平に配向した重合性液晶層が得られる。
このような加熱処理をすることで、単に塗布するだけの塗工方法と比べて、配向欠陥の少ない均質な液晶性高分子膜を作製することができる。
左螺旋性であることは、例えば、分光光度計測定において、左円偏光を選択反射することから確認される。
HTPは、下記式により求められる。
P:液晶性高分子のヘリカルピッチの長さ(μm)
C:重合性液晶化合物に対するキラル剤の濃度(質量%)
n:重合性液晶化合物の平均屈折率
λ:液晶性高分子の選択反射帯域の中心値(μm)
本発明の第4は、本発明の液晶性高分子を構成材料とする光学異方体である。
本発明の光学異方体としては、位相差板、液晶表示素子用配向膜、偏光板、視野角拡大板、カラーフィルター、ローパスフィルター、光偏光プリズム、各種光フィルター等が挙げられる。
なお、カラムクロマトグラフィーに用いた展開溶媒の比(括弧内に示す溶媒比)は容積比である。
滴下終了後、60℃にて4.5時間攪拌した。反応終了後、室温まで冷却した後、反応液を飽和重曹水100mlに投入し、クロロホルム50mlで3回抽出した。抽出したクロロホルム層を10%の重曹水50mlで洗浄し、無水硫酸ナトリウムで乾燥した。硫酸ナトリウムをろ別した後、ロータリーエバポレーターにてクロロホルムを減圧留去して、白色固体1.6gを得た。構造は1H−NMRで同定した。
構造は1H−NMRで同定した。
次に、その濃縮物にテトラヒドロフラン30mlを加えて溶解させ、前ステップで合成した中間体C 3.0g(4.70mmol)を加え、加熱還流条件下10時間反応させた。反応終了後、反応液に蒸留水200ml、飽和食塩水50mlを加え、クロロホルム300mlで抽出した。有機層を無水硫酸ナトリウムで乾燥させ、硫酸ナトリウムをロ別し、ロ液をロータリーエバポレーターで濃縮した後、濃縮物をシリカゲルカラムクロマトグラフィー(THF:クロロホルム:n−ヘキサン =0.25:4.75:5)により精製することで、重合性キラル化合物2を1.37g、収率37%で得た(Step2b)。構造は1H−NMRで同定した。
次いで、反応液に5−ホルミルサリチル酸メチル1168mg(6.48mmol)を加えてさらに2時間反応させた。反応終了後、反応液に蒸留水50ml、飽和食塩水30mlを加え、酢酸エチル300mlで抽出した。有機層を無水硫酸ナトリウムで乾燥させ、硫酸ナトリムをロ別し、ロ液をロータリーエバポレーターで濃縮した後、濃縮物をシリカゲルカラムクロマトグラフィー(THF:クロロホルム:n−ヘキサン =0.5:3:6.5)により精製することで、中間体Dを1.25g、収率58%で得た(Step1b)。
構造は1H−NMRで同定した。
(1−1:配向膜を有する透明樹脂基材の調製)
脂環式オレフィンポリマーからなるフィルム(株式会社オプテス製、商品名「ゼオノアフィルムZF16−100」)の両面をコロナ放電処理した。5%のポリビニルアルコールの水溶液を当該フィルムの片面に♯2のワイヤーバーを使用して塗布し、塗膜を乾燥し、膜厚0.1μmの配向膜を形成した。次いで当該配向膜をラビング処理し、配向膜を有する透明樹脂基材を作製した。
上記で得た重合性キラル化合物1〜3、下記重合性液晶化合物、下記重合性非液晶化合物、有機溶媒としての、シクロペンタノン及び1,3−ジオキソラン、界面活性剤(AGCセイミケミカル社製、商品名「サーフロンKH−40」)、並びに、光重合開始剤(BASF社製、商品名「イルガキュア1919」)を、表1に示す配合割合で使用材料の各成分を混合し、固形分約40%のコレステリック液晶組成物を調製した。このコレステリック液晶組成物を♯6のワイヤーバーを使用して、上記(1−1)で作製した配向膜を有する透明樹脂基材の、配向膜を有する面に塗布した。塗膜を130℃で2分間配向処理することにより、乾燥膜厚5μmのコレステリック液晶層を形成させた。得られた塗布膜に水銀ランプで2000mJ/cm2に相当する紫外線を照射して厚さ約3μmのコレステリック高分子硬化膜を得た。
分光光度計(大塚電子社製、瞬間マルチ測光システム MCPD−3000)でコレステリック高分子硬化膜の透過スペクトルを測定し、選択反射の中心波長λを調べた。以下の式により、螺旋捻り力HTP(μm−1)を、式:HTP=1/(P×C)=n/(λ×C)により求めた。
なお、Pはコレステリック高分子硬化膜のヘリカルピッチの長さ(μm)、Cは重合性液晶化合物に対するキラル剤の濃度(質量部/100)、nは重合性液晶化合物の平均屈折率、λはコレステリック高分子硬化膜の選択反射帯域の中心値(μm)である。
結果を表2にまとめて示す。
上記(1−3)で透過スペクトルを測定する際に、入射光を右円偏光と左円偏光のそれぞれを使用し、各円偏光に対する選択反射の有無を調べた。螺旋方向は、右円偏光を選択反射するものが右捩れ、左円偏光を選択反射するものは左捩れである。選択反射が確認できたものは○、選択反射を確認できなかったものは×とし、結果を表2にまとめて示す。
Claims (9)
- 下記式(I)
G1は、置換基を有していてもよい、炭素数1〜20の2価の脂肪族基を表す。該脂肪族基には、−O−、−S−、−O−C(=O)−、−C(=O)−O−、−O−C(=O)−O−、−NR2−C(=O)−、−C(=O)−NR2−、−NR2−、又は、−C(=O)−が介在していてもよい(ただし、−O−又は−S−がそれぞれ2以上隣接して介在する場合を除く。)。ここで、R2は水素原子又は炭素数1〜6のアルキル基を表す。
A1及びA2はそれぞれ独立して、置換基を有していてもよい炭素数1〜20の2価の脂肪族基、又は、置換基を有していてもよい炭素数6〜20の芳香族基を表し、
Z1は、ハロゲン原子で置換されていてもよい炭素数2〜10のアルケニル基を表す。
Qは、水素原子、置換基を有していてもよい炭素数1〜6のアルキル基、又は、下記式(2)
aは0又は1を表し、bは1又は2を表す。〕
で示される左螺旋を誘起する重合性キラル化合物。 - 前記式(I)中、A1〜A3がそれぞれ独立して、置換基を有していてもよいフェニレン基、置換基を有していてもよいビフェニレン基、又は、置換基を有していてもよいナフチレン基である
請求項1に記載の左螺旋を誘起する重合性キラル化合物。 - 前記式(I)中、Z1及びZ2がそれぞれ独立して、CH2=CH−、CH2=C(CH3)−、CH2=C(Cl)−、CH2=CH−CH2−、CH2=C(CH3)−CH2−、CH2=C(CH3)−CH2CH2−、(CH3)2C=CH−CH2−、CH3−CH=CH−、CH3−CH=CH−CH2−、CH2=CH−CH2−CH2−、又は、(CH3)2C=CH−CH2−CH2−である
請求項1又は2に記載の左螺旋を誘起する重合性キラル化合物。 - 前記式(I)中、Y1〜Y5がそれぞれ独立して、−C(=O)−O−、−O−C(=O)−、又は、−O−を表し、
G1及びG2がそれぞれ独立して、−O−、−C(=O)−O−、−O−C(=O)−、−C(=O)−が介在していてもよい(ただし、−O−が2以上隣接して介在する場合を除く。)、−(CH2)4−、又は−(CH2)6−を表し、Z1及びZ2がそれぞれ独立して、CH2=CH−、CH2=C(CH3)−、又は、CH2=C(Cl)−を表し、
A1〜A3がそれぞれ独立して、下記(a1)、(a2)又は(a3)
請求項1〜3のいずれかに記載の左螺旋を誘起する重合性キラル化合物。 - 前記式(I)中、Y1〜Y5がそれぞれ独立して、−C(=O)−O−、−O−C(=O)−、又は、−O−を表し、
G1及びG2がそれぞれ独立して、−(CH2)4−、又は、−(CH2)6−を表し、
Z1及びZ2がそれぞれ独立して、CH2=CH−、又は、CH2=C(CH3)−を表し、
A1〜A3がそれぞれ独立して、下記(a1)又は(a2)
請求項1〜4のいずれかに記載の左螺旋を誘起する重合性キラル化合物。 - 前記式(I)中、Y1〜Y5がそれぞれ独立して、−C(=O)−O−、−O−C(=O)−、又は、−O−を表し、
G1及びG2がそれぞれ独立して、−(CH2)4−、又は、−(CH2)6−を表し、
Z1及びZ2が、CH2=CH−を表し、
Qが、水素原子又はメチル基を表し、
A1が、下記(a1)
aは0であり、bは1である
請求項1〜5のいずれかに記載の左螺旋を誘起する重合性キラル化合物。 - 請求項1〜6のいずれかに記載の重合性キラル化合物、及び、重合可能な液晶化合物を含有する左螺旋性重合性液晶組成物。
- 請求項1〜6のいずれかに記載の重合性キラル化合物、又は、請求項7に記載の左螺旋性重合性液晶組成物を重合して得られる左螺旋性液晶性高分子。
- 請求項8に記載の左螺旋性液晶性高分子を構成材料とする光学異方体。
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2010290080A JP5621584B2 (ja) | 2010-12-27 | 2010-12-27 | 重合性キラル化合物、重合性液晶組成物、液晶性高分子及び光学異方体 |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2010290080A JP5621584B2 (ja) | 2010-12-27 | 2010-12-27 | 重合性キラル化合物、重合性液晶組成物、液晶性高分子及び光学異方体 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2012136641A true JP2012136641A (ja) | 2012-07-19 |
| JP5621584B2 JP5621584B2 (ja) | 2014-11-12 |
Family
ID=46674324
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2010290080A Active JP5621584B2 (ja) | 2010-12-27 | 2010-12-27 | 重合性キラル化合物、重合性液晶組成物、液晶性高分子及び光学異方体 |
Country Status (1)
| Country | Link |
|---|---|
| JP (1) | JP5621584B2 (ja) |
Cited By (7)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2013018526A1 (ja) * | 2011-07-29 | 2013-02-07 | 日本ゼオン株式会社 | 光学異方体の波長分散調整方法及び重合性組成物 |
| US20140107247A1 (en) * | 2011-04-15 | 2014-04-17 | Zeon Corporation | Polymerizable compound, polymerizable composition, polymer, and optically anisotropic body |
| CN108349925A (zh) * | 2015-11-09 | 2018-07-31 | Dic株式会社 | 聚合性化合物和光学各向异性体 |
| JP2018161815A (ja) * | 2017-03-27 | 2018-10-18 | 日本ゼオン株式会社 | 操作パネル用積層体及びその製造方法 |
| US11186669B2 (en) | 2015-01-16 | 2021-11-30 | Dic Corporation | Polymerizable composition and optically anisotropic body using same |
| US11261378B2 (en) | 2014-12-25 | 2022-03-01 | Dic Corporation | Polymerizable compound and optically anisotropic object |
| US11697695B2 (en) | 2015-01-16 | 2023-07-11 | Dic Corporation | Polymerizable composition and optically anisotropic body using same |
Citations (7)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPH0920781A (ja) * | 1995-06-09 | 1997-01-21 | Basf Ag | 重合可能なキラル化合物 |
| JPH0931077A (ja) * | 1995-06-09 | 1997-02-04 | Basf Ag | 重合可能なキラル化合物 |
| JPH11193287A (ja) * | 1997-10-08 | 1999-07-21 | Basf Ag | 重合可能なキラルな化合物およびその使用 |
| JP2000309589A (ja) * | 1999-03-25 | 2000-11-07 | Basf Ag | キラルドーパント、コレステリック液晶組成物、組成物の使用および組成物を含有する化粧および医薬製剤 |
| JP2003137887A (ja) * | 2001-07-02 | 2003-05-14 | Merck Patent Gmbh | キラル化合物 |
| JP2010070505A (ja) * | 2008-09-19 | 2010-04-02 | Nippon Zeon Co Ltd | 重合性液晶化合物、重合性液晶組成物、液晶性高分子及び光学異方体 |
| WO2010038591A1 (ja) * | 2008-10-01 | 2010-04-08 | 日本ゼオン株式会社 | 重合性キラル化合物、重合性液晶組成物、液晶性高分子及び光学異方体 |
-
2010
- 2010-12-27 JP JP2010290080A patent/JP5621584B2/ja active Active
Patent Citations (7)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPH0920781A (ja) * | 1995-06-09 | 1997-01-21 | Basf Ag | 重合可能なキラル化合物 |
| JPH0931077A (ja) * | 1995-06-09 | 1997-02-04 | Basf Ag | 重合可能なキラル化合物 |
| JPH11193287A (ja) * | 1997-10-08 | 1999-07-21 | Basf Ag | 重合可能なキラルな化合物およびその使用 |
| JP2000309589A (ja) * | 1999-03-25 | 2000-11-07 | Basf Ag | キラルドーパント、コレステリック液晶組成物、組成物の使用および組成物を含有する化粧および医薬製剤 |
| JP2003137887A (ja) * | 2001-07-02 | 2003-05-14 | Merck Patent Gmbh | キラル化合物 |
| JP2010070505A (ja) * | 2008-09-19 | 2010-04-02 | Nippon Zeon Co Ltd | 重合性液晶化合物、重合性液晶組成物、液晶性高分子及び光学異方体 |
| WO2010038591A1 (ja) * | 2008-10-01 | 2010-04-08 | 日本ゼオン株式会社 | 重合性キラル化合物、重合性液晶組成物、液晶性高分子及び光学異方体 |
Cited By (11)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US20140107247A1 (en) * | 2011-04-15 | 2014-04-17 | Zeon Corporation | Polymerizable compound, polymerizable composition, polymer, and optically anisotropic body |
| US9234056B2 (en) * | 2011-04-15 | 2016-01-12 | Zeon Corporation | Polymerizable compound, polymerizable composition, polymer, and optically anisotropic body |
| WO2013018526A1 (ja) * | 2011-07-29 | 2013-02-07 | 日本ゼオン株式会社 | 光学異方体の波長分散調整方法及び重合性組成物 |
| US11261378B2 (en) | 2014-12-25 | 2022-03-01 | Dic Corporation | Polymerizable compound and optically anisotropic object |
| US11186669B2 (en) | 2015-01-16 | 2021-11-30 | Dic Corporation | Polymerizable composition and optically anisotropic body using same |
| US11697695B2 (en) | 2015-01-16 | 2023-07-11 | Dic Corporation | Polymerizable composition and optically anisotropic body using same |
| CN108349925A (zh) * | 2015-11-09 | 2018-07-31 | Dic株式会社 | 聚合性化合物和光学各向异性体 |
| JP2018145192A (ja) * | 2015-11-09 | 2018-09-20 | Dic株式会社 | 重合性化合物及び光学異方体 |
| US10919870B2 (en) | 2015-11-09 | 2021-02-16 | Dic Corporation | Polymerizable compound and optically anisotropic body |
| CN108349925B (zh) * | 2015-11-09 | 2022-08-16 | Dic株式会社 | 聚合性化合物和光学各向异性体 |
| JP2018161815A (ja) * | 2017-03-27 | 2018-10-18 | 日本ゼオン株式会社 | 操作パネル用積層体及びその製造方法 |
Also Published As
| Publication number | Publication date |
|---|---|
| JP5621584B2 (ja) | 2014-11-12 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP5401822B2 (ja) | 重合性液晶化合物、重合性液晶組成物、液晶性高分子および光学異方体 | |
| JP5510321B2 (ja) | 重合性液晶化合物、重合性液晶組成物、液晶性高分子及び光学異方体 | |
| JP5522047B2 (ja) | 重合性キラル化合物、重合性液晶組成物、液晶性高分子及び光学異方体 | |
| EP2143710B1 (en) | Polymerizable liquid crystal compound, polymerizable liquid crystal composition, liquid crystalline polymer, and optically anisotropic material | |
| JP5621584B2 (ja) | 重合性キラル化合物、重合性液晶組成物、液晶性高分子及び光学異方体 | |
| TWI418613B (zh) | A liquid crystal compound, a liquid crystal composition, an optical film, and an optical laminate | |
| JP5564773B2 (ja) | 重合性液晶化合物、重合性液晶組成物、液晶性高分子及び光学異方体 | |
| TWI523936B (zh) | 共聚物、以及由其硬化物所構成之液晶配向層 | |
| KR20100014882A (ko) | 중합성 액정 화합물, 중합성 액정 조성물, 액정 중합체 및 광학 이방체 | |
| JP5401823B2 (ja) | 重合性液晶化合物、重合性液晶組成物、液晶性高分子および光学異方体 | |
| JP5396815B2 (ja) | 重合性化合物、重合性液晶化合物、重合性液晶組成物、液晶性高分子及び光学異方体 | |
| JP5407870B2 (ja) | 重合性液晶化合物、重合性液晶組成物、液晶性高分子および光学異方体 | |
| JP5737283B2 (ja) | 重合性キラル化合物、重合性液晶組成物、液晶性高分子及び光学異方体 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20130913 |
|
| A977 | Report on retrieval |
Free format text: JAPANESE INTERMEDIATE CODE: A971007 Effective date: 20140210 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20140218 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20140421 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20140826 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20140908 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 5621584 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |