JP2011522835A - 抗cd8抗体は、細胞傷害性エフェクターのプライミングを遮断し、制御性cd8+t細胞の生成を導く - Google Patents
抗cd8抗体は、細胞傷害性エフェクターのプライミングを遮断し、制御性cd8+t細胞の生成を導く Download PDFInfo
- Publication number
- JP2011522835A JP2011522835A JP2011512705A JP2011512705A JP2011522835A JP 2011522835 A JP2011522835 A JP 2011522835A JP 2011512705 A JP2011512705 A JP 2011512705A JP 2011512705 A JP2011512705 A JP 2011512705A JP 2011522835 A JP2011522835 A JP 2011522835A
- Authority
- JP
- Japan
- Prior art keywords
- cells
- antibody
- suppressor
- cell
- peripheral blood
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
- 210000001744 T-lymphocyte Anatomy 0.000 title claims abstract description 253
- 230000037452 priming Effects 0.000 title claims description 23
- 239000012636 effector Substances 0.000 title description 7
- 231100000433 cytotoxic Toxicity 0.000 title description 4
- 230000001472 cytotoxic effect Effects 0.000 title description 4
- 230000001105 regulatory effect Effects 0.000 title description 3
- 238000000034 method Methods 0.000 claims abstract description 69
- 239000000203 mixture Substances 0.000 claims abstract description 21
- 230000001939 inductive effect Effects 0.000 claims abstract description 12
- 210000001821 langerhans cell Anatomy 0.000 claims description 102
- 210000004027 cell Anatomy 0.000 claims description 68
- 210000004443 dendritic cell Anatomy 0.000 claims description 44
- 108091007433 antigens Proteins 0.000 claims description 39
- 102000036639 antigens Human genes 0.000 claims description 39
- 239000000427 antigen Substances 0.000 claims description 36
- 210000003819 peripheral blood mononuclear cell Anatomy 0.000 claims description 33
- 238000012258 culturing Methods 0.000 claims description 26
- 108010017213 Granulocyte-Macrophage Colony-Stimulating Factor Proteins 0.000 claims description 24
- 102100039620 Granulocyte-macrophage colony-stimulating factor Human genes 0.000 claims description 24
- 230000028993 immune response Effects 0.000 claims description 17
- 238000000338 in vitro Methods 0.000 claims description 17
- 239000002243 precursor Substances 0.000 claims description 16
- 108060008682 Tumor Necrosis Factor Proteins 0.000 claims description 15
- 102000000852 Tumor Necrosis Factor-alpha Human genes 0.000 claims description 14
- 102000001398 Granzyme Human genes 0.000 claims description 13
- 108060005986 Granzyme Proteins 0.000 claims description 13
- 230000037453 T cell priming Effects 0.000 claims description 13
- 230000003247 decreasing effect Effects 0.000 claims description 12
- 102000004127 Cytokines Human genes 0.000 claims description 11
- 108090000695 Cytokines Proteins 0.000 claims description 11
- 102000000588 Interleukin-2 Human genes 0.000 claims description 11
- 108010002350 Interleukin-2 Proteins 0.000 claims description 11
- 206010052779 Transplant rejections Diseases 0.000 claims description 11
- 102100031573 Hematopoietic progenitor cell antigen CD34 Human genes 0.000 claims description 10
- 101000777663 Homo sapiens Hematopoietic progenitor cell antigen CD34 Proteins 0.000 claims description 10
- 230000028327 secretion Effects 0.000 claims description 10
- 238000002054 transplantation Methods 0.000 claims description 10
- 102100037850 Interferon gamma Human genes 0.000 claims description 8
- 108010074328 Interferon-gamma Proteins 0.000 claims description 8
- KHGNFPUMBJSZSM-UHFFFAOYSA-N Perforine Natural products COC1=C2CCC(O)C(CCC(C)(C)O)(OC)C2=NC2=C1C=CO2 KHGNFPUMBJSZSM-UHFFFAOYSA-N 0.000 claims description 8
- 230000027455 binding Effects 0.000 claims description 8
- 210000001616 monocyte Anatomy 0.000 claims description 8
- 229930192851 perforin Natural products 0.000 claims description 8
- 102000004388 Interleukin-4 Human genes 0.000 claims description 7
- 108090000978 Interleukin-4 Proteins 0.000 claims description 7
- 108010002616 Interleukin-5 Proteins 0.000 claims description 7
- 241000700605 Viruses Species 0.000 claims description 7
- 230000002401 inhibitory effect Effects 0.000 claims description 7
- 210000001519 tissue Anatomy 0.000 claims description 7
- 108090000176 Interleukin-13 Proteins 0.000 claims description 6
- 230000000779 depleting effect Effects 0.000 claims description 5
- 210000000056 organ Anatomy 0.000 claims description 5
- 230000002093 peripheral effect Effects 0.000 claims description 5
- 230000002829 reductive effect Effects 0.000 claims description 4
- 230000001629 suppression Effects 0.000 claims description 4
- 241000124008 Mammalia Species 0.000 claims description 3
- 230000000903 blocking effect Effects 0.000 claims description 3
- 230000007423 decrease Effects 0.000 claims description 3
- 210000005259 peripheral blood Anatomy 0.000 claims description 3
- 239000011886 peripheral blood Substances 0.000 claims description 3
- 102000000743 Interleukin-5 Human genes 0.000 claims description 2
- 230000003614 tolerogenic effect Effects 0.000 claims 2
- 230000000961 alloantigen Effects 0.000 abstract description 13
- 230000006058 immune tolerance Effects 0.000 abstract description 4
- 101000946843 Homo sapiens T-cell surface glycoprotein CD8 alpha chain Proteins 0.000 description 220
- 102100034922 T-cell surface glycoprotein CD8 alpha chain Human genes 0.000 description 220
- 230000000735 allogeneic effect Effects 0.000 description 40
- 230000004044 response Effects 0.000 description 25
- 102100036011 T-cell surface glycoprotein CD4 Human genes 0.000 description 22
- 108090000765 processed proteins & peptides Proteins 0.000 description 21
- 206010022000 influenza Diseases 0.000 description 17
- 230000005764 inhibitory process Effects 0.000 description 17
- 230000004913 activation Effects 0.000 description 16
- 230000035755 proliferation Effects 0.000 description 16
- 101000578784 Homo sapiens Melanoma antigen recognized by T-cells 1 Proteins 0.000 description 13
- 102100028389 Melanoma antigen recognized by T-cells 1 Human genes 0.000 description 13
- 241000699670 Mus sp. Species 0.000 description 13
- 238000011282 treatment Methods 0.000 description 12
- 230000006052 T cell proliferation Effects 0.000 description 11
- 238000001727 in vivo Methods 0.000 description 11
- 230000037361 pathway Effects 0.000 description 11
- 230000001404 mediated effect Effects 0.000 description 10
- 102100032937 CD40 ligand Human genes 0.000 description 9
- 230000005867 T cell response Effects 0.000 description 9
- IQFYYKKMVGJFEH-XLPZGREQSA-N Thymidine Chemical compound O=C1NC(=O)C(C)=CN1[C@@H]1O[C@H](CO)[C@@H](O)C1 IQFYYKKMVGJFEH-XLPZGREQSA-N 0.000 description 9
- 238000003501 co-culture Methods 0.000 description 9
- 208000024908 graft versus host disease Diseases 0.000 description 8
- 239000002609 medium Substances 0.000 description 8
- 230000001419 dependent effect Effects 0.000 description 7
- 230000006870 function Effects 0.000 description 7
- 230000036039 immunity Effects 0.000 description 7
- 210000003289 regulatory T cell Anatomy 0.000 description 7
- 210000003491 skin Anatomy 0.000 description 7
- 208000009329 Graft vs Host Disease Diseases 0.000 description 6
- 101000946889 Homo sapiens Monocyte differentiation antigen CD14 Proteins 0.000 description 6
- 101000914514 Homo sapiens T-cell-specific surface glycoprotein CD28 Proteins 0.000 description 6
- 102100035877 Monocyte differentiation antigen CD14 Human genes 0.000 description 6
- 102100027213 T-cell-specific surface glycoprotein CD28 Human genes 0.000 description 6
- 210000003958 hematopoietic stem cell Anatomy 0.000 description 6
- 238000010348 incorporation Methods 0.000 description 6
- 230000006698 induction Effects 0.000 description 6
- 230000009467 reduction Effects 0.000 description 6
- 101000868215 Homo sapiens CD40 ligand Proteins 0.000 description 5
- 238000003556 assay Methods 0.000 description 5
- 230000000139 costimulatory effect Effects 0.000 description 5
- 239000012528 membrane Substances 0.000 description 5
- 108090000623 proteins and genes Proteins 0.000 description 5
- 238000010186 staining Methods 0.000 description 5
- 229940104230 thymidine Drugs 0.000 description 5
- 108010029697 CD40 Ligand Proteins 0.000 description 4
- 102100022297 Integrin alpha-X Human genes 0.000 description 4
- 241001465754 Metazoa Species 0.000 description 4
- 210000001185 bone marrow Anatomy 0.000 description 4
- 230000001413 cellular effect Effects 0.000 description 4
- 238000010790 dilution Methods 0.000 description 4
- 239000012895 dilution Substances 0.000 description 4
- 230000002500 effect on skin Effects 0.000 description 4
- 238000011156 evaluation Methods 0.000 description 4
- 238000000684 flow cytometry Methods 0.000 description 4
- UCSJYZPVAKXKNQ-HZYVHMACSA-N streptomycin Chemical compound CN[C@H]1[C@H](O)[C@@H](O)[C@H](CO)O[C@H]1O[C@@H]1[C@](C=O)(O)[C@H](C)O[C@H]1O[C@@H]1[C@@H](NC(N)=N)[C@H](O)[C@@H](NC(N)=N)[C@H](O)[C@H]1O UCSJYZPVAKXKNQ-HZYVHMACSA-N 0.000 description 4
- 208000024891 symptom Diseases 0.000 description 4
- DWRXFEITVBNRMK-UHFFFAOYSA-N Beta-D-1-Arabinofuranosylthymine Natural products O=C1NC(=O)C(C)=CN1C1C(O)C(O)C(CO)O1 DWRXFEITVBNRMK-UHFFFAOYSA-N 0.000 description 3
- 102100036301 C-C chemokine receptor type 7 Human genes 0.000 description 3
- 101000716065 Homo sapiens C-C chemokine receptor type 7 Proteins 0.000 description 3
- 101001057504 Homo sapiens Interferon-stimulated gene 20 kDa protein Proteins 0.000 description 3
- 101001055144 Homo sapiens Interleukin-2 receptor subunit alpha Proteins 0.000 description 3
- 102100027268 Interferon-stimulated gene 20 kDa protein Human genes 0.000 description 3
- 108010002586 Interleukin-7 Proteins 0.000 description 3
- 238000011316 allogeneic transplantation Methods 0.000 description 3
- 238000004458 analytical method Methods 0.000 description 3
- 239000011324 bead Substances 0.000 description 3
- IQFYYKKMVGJFEH-UHFFFAOYSA-N beta-L-thymidine Natural products O=C1NC(=O)C(C)=CN1C1OC(CO)C(O)C1 IQFYYKKMVGJFEH-UHFFFAOYSA-N 0.000 description 3
- 210000004369 blood Anatomy 0.000 description 3
- 239000008280 blood Substances 0.000 description 3
- 238000004113 cell culture Methods 0.000 description 3
- 230000006378 damage Effects 0.000 description 3
- 238000002474 experimental method Methods 0.000 description 3
- 238000011577 humanized mouse model Methods 0.000 description 3
- 230000001506 immunosuppresive effect Effects 0.000 description 3
- 239000003018 immunosuppressive agent Substances 0.000 description 3
- 102000006495 integrins Human genes 0.000 description 3
- 108010044426 integrins Proteins 0.000 description 3
- 230000003389 potentiating effect Effects 0.000 description 3
- 230000002265 prevention Effects 0.000 description 3
- 230000009719 regenerative response Effects 0.000 description 3
- 241000894007 species Species 0.000 description 3
- 230000004083 survival effect Effects 0.000 description 3
- 230000002992 thymic effect Effects 0.000 description 3
- 230000004580 weight loss Effects 0.000 description 3
- 102100024222 B-lymphocyte antigen CD19 Human genes 0.000 description 2
- 108091003079 Bovine Serum Albumin Proteins 0.000 description 2
- 101150013553 CD40 gene Proteins 0.000 description 2
- 108010047041 Complementarity Determining Regions Proteins 0.000 description 2
- PMATZTZNYRCHOR-CGLBZJNRSA-N Cyclosporin A Chemical compound CC[C@@H]1NC(=O)[C@H]([C@H](O)[C@H](C)C\C=C\C)N(C)C(=O)[C@H](C(C)C)N(C)C(=O)[C@H](CC(C)C)N(C)C(=O)[C@H](CC(C)C)N(C)C(=O)[C@@H](C)NC(=O)[C@H](C)NC(=O)[C@H](CC(C)C)N(C)C(=O)[C@H](C(C)C)NC(=O)[C@H](CC(C)C)N(C)C(=O)CN(C)C1=O PMATZTZNYRCHOR-CGLBZJNRSA-N 0.000 description 2
- 108010036949 Cyclosporine Proteins 0.000 description 2
- 102000025850 HLA-A2 Antigen Human genes 0.000 description 2
- 108010074032 HLA-A2 Antigen Proteins 0.000 description 2
- 102000008949 Histocompatibility Antigens Class I Human genes 0.000 description 2
- 101000980825 Homo sapiens B-lymphocyte antigen CD19 Proteins 0.000 description 2
- 101000917858 Homo sapiens Low affinity immunoglobulin gamma Fc region receptor III-A Proteins 0.000 description 2
- 101000917839 Homo sapiens Low affinity immunoglobulin gamma Fc region receptor III-B Proteins 0.000 description 2
- 101000581981 Homo sapiens Neural cell adhesion molecule 1 Proteins 0.000 description 2
- 101000716102 Homo sapiens T-cell surface glycoprotein CD4 Proteins 0.000 description 2
- 101000914484 Homo sapiens T-lymphocyte activation antigen CD80 Proteins 0.000 description 2
- 102100022339 Integrin alpha-L Human genes 0.000 description 2
- 108010064593 Intercellular Adhesion Molecule-1 Proteins 0.000 description 2
- 102100037877 Intercellular adhesion molecule 1 Human genes 0.000 description 2
- 102100029185 Low affinity immunoglobulin gamma Fc region receptor III-B Human genes 0.000 description 2
- 108010064548 Lymphocyte Function-Associated Antigen-1 Proteins 0.000 description 2
- 108091054437 MHC class I family Proteins 0.000 description 2
- 102100027347 Neural cell adhesion molecule 1 Human genes 0.000 description 2
- 229930182555 Penicillin Natural products 0.000 description 2
- JGSARLDLIJGVTE-MBNYWOFBSA-N Penicillin G Chemical compound N([C@H]1[C@H]2SC([C@@H](N2C1=O)C(O)=O)(C)C)C(=O)CC1=CC=CC=C1 JGSARLDLIJGVTE-MBNYWOFBSA-N 0.000 description 2
- 230000006044 T cell activation Effects 0.000 description 2
- 230000024932 T cell mediated immunity Effects 0.000 description 2
- 102100027222 T-lymphocyte activation antigen CD80 Human genes 0.000 description 2
- 102100040247 Tumor necrosis factor Human genes 0.000 description 2
- 102100040245 Tumor necrosis factor receptor superfamily member 5 Human genes 0.000 description 2
- 230000000840 anti-viral effect Effects 0.000 description 2
- 208000017760 chronic graft versus host disease Diseases 0.000 description 2
- 229960001265 ciclosporin Drugs 0.000 description 2
- 230000016396 cytokine production Effects 0.000 description 2
- 210000004207 dermis Anatomy 0.000 description 2
- 238000011161 development Methods 0.000 description 2
- 230000009025 developmental regulation Effects 0.000 description 2
- 201000010099 disease Diseases 0.000 description 2
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 description 2
- 231100000673 dose–response relationship Toxicity 0.000 description 2
- 230000000694 effects Effects 0.000 description 2
- 210000002615 epidermis Anatomy 0.000 description 2
- 210000002919 epithelial cell Anatomy 0.000 description 2
- 239000012091 fetal bovine serum Substances 0.000 description 2
- 239000012737 fresh medium Substances 0.000 description 2
- 230000005745 host immune response Effects 0.000 description 2
- 210000002865 immune cell Anatomy 0.000 description 2
- 229960003444 immunosuppressant agent Drugs 0.000 description 2
- 230000001861 immunosuppressant effect Effects 0.000 description 2
- 230000000968 intestinal effect Effects 0.000 description 2
- 230000000670 limiting effect Effects 0.000 description 2
- 210000004698 lymphocyte Anatomy 0.000 description 2
- 230000035800 maturation Effects 0.000 description 2
- 201000001441 melanoma Diseases 0.000 description 2
- 239000011325 microbead Substances 0.000 description 2
- 238000010172 mouse model Methods 0.000 description 2
- 230000035772 mutation Effects 0.000 description 2
- 229940049954 penicillin Drugs 0.000 description 2
- 102000004196 processed proteins & peptides Human genes 0.000 description 2
- 230000002062 proliferating effect Effects 0.000 description 2
- ZAHRKKWIAAJSAO-UHFFFAOYSA-N rapamycin Natural products COCC(O)C(=C/C(C)C(=O)CC(OC(=O)C1CCCCN1C(=O)C(=O)C2(O)OC(CC(OC)C(=CC=CC=CC(C)CC(C)C(=O)C)C)CCC2C)C(C)CC3CCC(O)C(C3)OC)C ZAHRKKWIAAJSAO-UHFFFAOYSA-N 0.000 description 2
- 210000002966 serum Anatomy 0.000 description 2
- 230000011664 signaling Effects 0.000 description 2
- 229960002930 sirolimus Drugs 0.000 description 2
- QFJCIRLUMZQUOT-HPLJOQBZSA-N sirolimus Chemical compound C1C[C@@H](O)[C@H](OC)C[C@@H]1C[C@@H](C)[C@H]1OC(=O)[C@@H]2CCCCN2C(=O)C(=O)[C@](O)(O2)[C@H](C)CC[C@H]2C[C@H](OC)/C(C)=C/C=C/C=C/[C@@H](C)C[C@@H](C)C(=O)[C@H](OC)[C@H](O)/C(C)=C/[C@@H](C)C(=O)C1 QFJCIRLUMZQUOT-HPLJOQBZSA-N 0.000 description 2
- 230000000638 stimulation Effects 0.000 description 2
- 229960005322 streptomycin Drugs 0.000 description 2
- 239000000758 substrate Substances 0.000 description 2
- 230000008685 targeting Effects 0.000 description 2
- 230000001225 therapeutic effect Effects 0.000 description 2
- 238000002560 therapeutic procedure Methods 0.000 description 2
- 238000002689 xenotransplantation Methods 0.000 description 2
- MZOFCQQQCNRIBI-VMXHOPILSA-N (3s)-4-[[(2s)-1-[[(2s)-1-[[(1s)-1-carboxy-2-hydroxyethyl]amino]-4-methyl-1-oxopentan-2-yl]amino]-5-(diaminomethylideneamino)-1-oxopentan-2-yl]amino]-3-[[2-[[(2s)-2,6-diaminohexanoyl]amino]acetyl]amino]-4-oxobutanoic acid Chemical compound OC[C@@H](C(O)=O)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](CCCN=C(N)N)NC(=O)[C@H](CC(O)=O)NC(=O)CNC(=O)[C@@H](N)CCCCN MZOFCQQQCNRIBI-VMXHOPILSA-N 0.000 description 1
- POVNCJSPYFCWJR-USZUGGBUSA-N (4s)-4-[[(2s)-2-[[(2s)-2-amino-3-(4-hydroxyphenyl)propanoyl]amino]-4-methylpentanoyl]amino]-5-[(2s)-2-[[2-[(2s)-2-[[(2s)-1-[[(2s,3r)-1-[[(1s)-1-carboxy-2-methylpropyl]amino]-3-hydroxy-1-oxobutan-2-yl]amino]-3-methyl-1-oxobutan-2-yl]carbamoyl]pyrrolidin-1- Chemical compound C([C@H](N)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CCC(O)=O)C(=O)N1[C@@H](CCC1)C(=O)NCC(=O)N1[C@@H](CCC1)C(=O)N[C@@H](C(C)C)C(=O)N[C@@H]([C@@H](C)O)C(=O)N[C@@H](C(C)C)C(O)=O)C1=CC=C(O)C=C1 POVNCJSPYFCWJR-USZUGGBUSA-N 0.000 description 1
- 102100034540 Adenomatous polyposis coli protein Human genes 0.000 description 1
- 208000023275 Autoimmune disease Diseases 0.000 description 1
- 101001105315 Bacillus subtilis (strain 168) 50S ribosomal protein L17 Proteins 0.000 description 1
- 208000035143 Bacterial infection Diseases 0.000 description 1
- 102100026596 Bcl-2-like protein 1 Human genes 0.000 description 1
- 102100027207 CD27 antigen Human genes 0.000 description 1
- 229930105110 Cyclosporin A Natural products 0.000 description 1
- 102100039498 Cytotoxic T-lymphocyte protein 4 Human genes 0.000 description 1
- 206010012735 Diarrhoea Diseases 0.000 description 1
- 206010015150 Erythema Diseases 0.000 description 1
- 208000010201 Exanthema Diseases 0.000 description 1
- 102000004269 Granulocyte Colony-Stimulating Factor Human genes 0.000 description 1
- 108010017080 Granulocyte Colony-Stimulating Factor Proteins 0.000 description 1
- 102000006354 HLA-DR Antigens Human genes 0.000 description 1
- 108010058597 HLA-DR Antigens Proteins 0.000 description 1
- 102100022102 Histone-lysine N-methyltransferase 2B Human genes 0.000 description 1
- 241000282412 Homo Species 0.000 description 1
- 101000914511 Homo sapiens CD27 antigen Proteins 0.000 description 1
- 101100220044 Homo sapiens CD34 gene Proteins 0.000 description 1
- 101000889276 Homo sapiens Cytotoxic T-lymphocyte protein 4 Proteins 0.000 description 1
- 101001045848 Homo sapiens Histone-lysine N-methyltransferase 2B Proteins 0.000 description 1
- -1 ICOS Proteins 0.000 description 1
- 108010067060 Immunoglobulin Variable Region Proteins 0.000 description 1
- 102000017727 Immunoglobulin Variable Region Human genes 0.000 description 1
- 206010062016 Immunosuppression Diseases 0.000 description 1
- ZDXPYRJPNDTMRX-VKHMYHEASA-N L-glutamine Chemical compound OC(=O)[C@@H](N)CCC(N)=O ZDXPYRJPNDTMRX-VKHMYHEASA-N 0.000 description 1
- 229930182816 L-glutamine Natural products 0.000 description 1
- OUYCCCASQSFEME-QMMMGPOBSA-N L-tyrosine Chemical compound OC(=O)[C@@H](N)CC1=CC=C(O)C=C1 OUYCCCASQSFEME-QMMMGPOBSA-N 0.000 description 1
- 108700018351 Major Histocompatibility Complex Proteins 0.000 description 1
- 102000012750 Membrane Glycoproteins Human genes 0.000 description 1
- 108010090054 Membrane Glycoproteins Proteins 0.000 description 1
- 241000699666 Mus <mouse, genus> Species 0.000 description 1
- 238000011789 NOD SCID mouse Methods 0.000 description 1
- 101710160107 Outer membrane protein A Proteins 0.000 description 1
- 108091007960 PI3Ks Proteins 0.000 description 1
- 102000035195 Peptidases Human genes 0.000 description 1
- 108091005804 Peptidases Proteins 0.000 description 1
- 102000003993 Phosphatidylinositol 3-kinases Human genes 0.000 description 1
- 108090000430 Phosphatidylinositol 3-kinases Proteins 0.000 description 1
- 101710177166 Phosphoprotein Proteins 0.000 description 1
- 108091000080 Phosphotransferase Proteins 0.000 description 1
- 241000288906 Primates Species 0.000 description 1
- 239000004365 Protease Substances 0.000 description 1
- 102000004022 Protein-Tyrosine Kinases Human genes 0.000 description 1
- 108090000412 Protein-Tyrosine Kinases Proteins 0.000 description 1
- 239000012980 RPMI-1640 medium Substances 0.000 description 1
- 238000011579 SCID mouse model Methods 0.000 description 1
- 229940100514 Syk tyrosine kinase inhibitor Drugs 0.000 description 1
- 108091008874 T cell receptors Proteins 0.000 description 1
- 102000016266 T-Cell Antigen Receptors Human genes 0.000 description 1
- 108700012920 TNF Proteins 0.000 description 1
- 208000036142 Viral infection Diseases 0.000 description 1
- 230000003213 activating effect Effects 0.000 description 1
- 230000001154 acute effect Effects 0.000 description 1
- 229940060587 alpha e Drugs 0.000 description 1
- 230000001857 anti-mycotic effect Effects 0.000 description 1
- 238000009175 antibody therapy Methods 0.000 description 1
- 239000002543 antimycotic Substances 0.000 description 1
- 238000013459 approach Methods 0.000 description 1
- 230000001363 autoimmune Effects 0.000 description 1
- 210000003719 b-lymphocyte Anatomy 0.000 description 1
- 230000001580 bacterial effect Effects 0.000 description 1
- 208000022362 bacterial infectious disease Diseases 0.000 description 1
- 230000009286 beneficial effect Effects 0.000 description 1
- 230000008901 benefit Effects 0.000 description 1
- 230000003115 biocidal effect Effects 0.000 description 1
- 230000015572 biosynthetic process Effects 0.000 description 1
- 210000002798 bone marrow cell Anatomy 0.000 description 1
- 238000010322 bone marrow transplantation Methods 0.000 description 1
- 229940046731 calcineurin inhibitors Drugs 0.000 description 1
- 230000020411 cell activation Effects 0.000 description 1
- 230000004663 cell proliferation Effects 0.000 description 1
- 230000009134 cell regulation Effects 0.000 description 1
- 230000005754 cellular signaling Effects 0.000 description 1
- 239000003153 chemical reaction reagent Substances 0.000 description 1
- 239000003795 chemical substances by application Substances 0.000 description 1
- 230000000295 complement effect Effects 0.000 description 1
- 230000001276 controlling effect Effects 0.000 description 1
- 230000004940 costimulation Effects 0.000 description 1
- 229930182912 cyclosporin Natural products 0.000 description 1
- 230000009089 cytolysis Effects 0.000 description 1
- 230000001461 cytolytic effect Effects 0.000 description 1
- 210000005220 cytoplasmic tail Anatomy 0.000 description 1
- 230000001086 cytosolic effect Effects 0.000 description 1
- 230000003013 cytotoxicity Effects 0.000 description 1
- 231100000135 cytotoxicity Toxicity 0.000 description 1
- 230000007812 deficiency Effects 0.000 description 1
- 230000002950 deficient Effects 0.000 description 1
- 238000013461 design Methods 0.000 description 1
- 206010012601 diabetes mellitus Diseases 0.000 description 1
- 229960005423 diatrizoate Drugs 0.000 description 1
- 230000004069 differentiation Effects 0.000 description 1
- 230000003467 diminishing effect Effects 0.000 description 1
- 108010007093 dispase Proteins 0.000 description 1
- 230000003828 downregulation Effects 0.000 description 1
- 229940079593 drug Drugs 0.000 description 1
- 239000003814 drug Substances 0.000 description 1
- 230000008030 elimination Effects 0.000 description 1
- 238000003379 elimination reaction Methods 0.000 description 1
- 230000002708 enhancing effect Effects 0.000 description 1
- 231100000321 erythema Toxicity 0.000 description 1
- 201000005884 exanthem Diseases 0.000 description 1
- 239000013604 expression vector Substances 0.000 description 1
- 210000004700 fetal blood Anatomy 0.000 description 1
- MHMNJMPURVTYEJ-UHFFFAOYSA-N fluorescein-5-isothiocyanate Chemical compound O1C(=O)C2=CC(N=C=S)=CC=C2C21C1=CC=C(O)C=C1OC1=CC(O)=CC=C21 MHMNJMPURVTYEJ-UHFFFAOYSA-N 0.000 description 1
- 238000010230 functional analysis Methods 0.000 description 1
- 238000002825 functional assay Methods 0.000 description 1
- 230000003394 haemopoietic effect Effects 0.000 description 1
- 230000036074 healthy skin Effects 0.000 description 1
- 239000000833 heterodimer Substances 0.000 description 1
- 239000000710 homodimer Substances 0.000 description 1
- 230000028996 humoral immune response Effects 0.000 description 1
- 230000005934 immune activation Effects 0.000 description 1
- 230000008102 immune modulation Effects 0.000 description 1
- 230000003832 immune regulation Effects 0.000 description 1
- 230000008629 immune suppression Effects 0.000 description 1
- 210000000987 immune system Anatomy 0.000 description 1
- 229940125721 immunosuppressive agent Drugs 0.000 description 1
- 230000000415 inactivating effect Effects 0.000 description 1
- 230000000937 inactivator Effects 0.000 description 1
- 230000008595 infiltration Effects 0.000 description 1
- 238000001764 infiltration Methods 0.000 description 1
- 108010061181 influenza matrix peptide (58-66) Proteins 0.000 description 1
- 239000003112 inhibitor Substances 0.000 description 1
- 238000002347 injection Methods 0.000 description 1
- 239000007924 injection Substances 0.000 description 1
- 230000004073 interleukin-2 production Effects 0.000 description 1
- 230000003834 intracellular effect Effects 0.000 description 1
- 210000004153 islets of langerhan Anatomy 0.000 description 1
- 238000002955 isolation Methods 0.000 description 1
- 238000012933 kinetic analysis Methods 0.000 description 1
- 231100000636 lethal dose Toxicity 0.000 description 1
- 210000000265 leukocyte Anatomy 0.000 description 1
- 239000003446 ligand Substances 0.000 description 1
- 210000004185 liver Anatomy 0.000 description 1
- 230000007774 longterm Effects 0.000 description 1
- 206010025135 lupus erythematosus Diseases 0.000 description 1
- 210000005210 lymphoid organ Anatomy 0.000 description 1
- 238000004519 manufacturing process Methods 0.000 description 1
- 210000003071 memory t lymphocyte Anatomy 0.000 description 1
- 238000002493 microarray Methods 0.000 description 1
- ZAHQPTJLOCWVPG-UHFFFAOYSA-N mitoxantrone dihydrochloride Chemical compound Cl.Cl.O=C1C2=C(O)C=CC(O)=C2C(=O)C2=C1C(NCCNCCO)=CC=C2NCCNCCO ZAHQPTJLOCWVPG-UHFFFAOYSA-N 0.000 description 1
- 238000012986 modification Methods 0.000 description 1
- 230000004048 modification Effects 0.000 description 1
- 230000001717 pathogenic effect Effects 0.000 description 1
- 102000020233 phosphotransferase Human genes 0.000 description 1
- 229920001184 polypeptide Polymers 0.000 description 1
- 210000004986 primary T-cell Anatomy 0.000 description 1
- 230000008569 process Effects 0.000 description 1
- 230000001681 protective effect Effects 0.000 description 1
- 102000004169 proteins and genes Human genes 0.000 description 1
- 238000000746 purification Methods 0.000 description 1
- 239000000700 radioactive tracer Substances 0.000 description 1
- 206010037844 rash Diseases 0.000 description 1
- 210000005212 secondary lymphoid organ Anatomy 0.000 description 1
- 238000000926 separation method Methods 0.000 description 1
- 230000019491 signal transduction Effects 0.000 description 1
- VIDRYROWYFWGSY-UHFFFAOYSA-N sotalol hydrochloride Chemical compound Cl.CC(C)NCC(O)C1=CC=C(NS(C)(=O)=O)C=C1 VIDRYROWYFWGSY-UHFFFAOYSA-N 0.000 description 1
- 235000015096 spirit Nutrition 0.000 description 1
- 230000004936 stimulating effect Effects 0.000 description 1
- 239000006228 supernatant Substances 0.000 description 1
- 230000020382 suppression by virus of host antigen processing and presentation of peptide antigen via MHC class I Effects 0.000 description 1
- 208000015215 susceptibility to respiratory infections associated with CD8alpha chain mutation Diseases 0.000 description 1
- 238000004448 titration Methods 0.000 description 1
- 238000012546 transfer Methods 0.000 description 1
- OUYCCCASQSFEME-UHFFFAOYSA-N tyrosine Natural products OC(=O)C(N)CC1=CC=C(O)C=C1 OUYCCCASQSFEME-UHFFFAOYSA-N 0.000 description 1
- 230000003827 upregulation Effects 0.000 description 1
- 230000009385 viral infection Effects 0.000 description 1
- 230000003612 virological effect Effects 0.000 description 1
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies
- C07K16/18—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans
- C07K16/28—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies
- C07K16/18—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans
- C07K16/28—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants
- C07K16/2803—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants against the immunoglobulin superfamily
- C07K16/2815—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants against the immunoglobulin superfamily against CD8
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K39/0005—Vertebrate antigens
- A61K39/001—Preparations to induce tolerance to non-self, e.g. prior to transplantation
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K39/395—Antibodies; Immunoglobulins; Immune serum, e.g. antilymphocytic serum
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K39/46—Cellular immunotherapy
- A61K39/461—Cellular immunotherapy characterised by the cell type used
- A61K39/4611—T-cells, e.g. tumor infiltrating lymphocytes [TIL], lymphokine-activated killer cells [LAK] or regulatory T cells [Treg]
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K39/46—Cellular immunotherapy
- A61K39/462—Cellular immunotherapy characterized by the effect or the function of the cells
- A61K39/4621—Cellular immunotherapy characterized by the effect or the function of the cells immunosuppressive or immunotolerising
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K39/46—Cellular immunotherapy
- A61K39/464—Cellular immunotherapy characterised by the antigen targeted or presented
- A61K39/4643—Vertebrate antigens
- A61K39/46434—Antigens related to induction of tolerance to non-self
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P37/00—Drugs for immunological or allergic disorders
- A61P37/02—Immunomodulators
- A61P37/06—Immunosuppressants, e.g. drugs for graft rejection
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N5/00—Undifferentiated human, animal or plant cells, e.g. cell lines; Tissues; Cultivation or maintenance thereof; Culture media therefor
- C12N5/06—Animal cells or tissues; Human cells or tissues
- C12N5/0602—Vertebrate cells
- C12N5/0634—Cells from the blood or the immune system
- C12N5/0636—T lymphocytes
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N5/00—Undifferentiated human, animal or plant cells, e.g. cell lines; Tissues; Cultivation or maintenance thereof; Culture media therefor
- C12N5/06—Animal cells or tissues; Human cells or tissues
- C12N5/0602—Vertebrate cells
- C12N5/0634—Cells from the blood or the immune system
- C12N5/0639—Dendritic cells, e.g. Langherhans cells in the epidermis
- C12N5/064—Immunosuppressive dendritic cells
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K35/00—Medicinal preparations containing materials or reaction products thereof with undetermined constitution
- A61K35/12—Materials from mammals; Compositions comprising non-specified tissues or cells; Compositions comprising non-embryonic stem cells; Genetically modified cells
- A61K2035/122—Materials from mammals; Compositions comprising non-specified tissues or cells; Compositions comprising non-embryonic stem cells; Genetically modified cells for inducing tolerance or supression of immune responses
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K2039/505—Medicinal preparations containing antigens or antibodies comprising antibodies
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/70—Immunoglobulins specific features characterized by effect upon binding to a cell or to an antigen
- C07K2317/73—Inducing cell death, e.g. apoptosis, necrosis or inhibition of cell proliferation
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2501/00—Active agents used in cell culture processes, e.g. differentation
- C12N2501/20—Cytokines; Chemokines
- C12N2501/22—Colony stimulating factors (G-CSF, GM-CSF)
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2501/00—Active agents used in cell culture processes, e.g. differentation
- C12N2501/20—Cytokines; Chemokines
- C12N2501/24—Interferons [IFN]
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2501/00—Active agents used in cell culture processes, e.g. differentation
- C12N2501/20—Cytokines; Chemokines
- C12N2501/26—Flt-3 ligand (CD135L, flk-2 ligand)
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2501/00—Active agents used in cell culture processes, e.g. differentation
- C12N2501/50—Cell markers; Cell surface determinants
- C12N2501/505—CD4; CD8
Abstract
本発明は、対象に、同種抗原に対するCD8+T細胞免疫寛容を誘導するのに十分な有効量の抗CD8抗体を提供するステップを含む、必要とする対象において寛容を誘導するための組成物及び方法を含む。
Description
本発明は、全般的に、制御性T細胞の分野、より具体的には、抗CD8抗体を作製し用いるための組成物及び方法に関する。
本発明の範囲を限定することなく、本発明の背景を免疫細胞寛容との関連において記載する。Reichert, et al.に対して発行された米国特許第5593677号明細書は、移植片対宿主疾患の予防のための方法について教示している。この方法は、抗CD8モノクローナル抗体とCD4+細胞失活剤との組合せ使用によるヒトにおける移植片対宿主疾患の治療及び予防を含む。骨髄移植を受ける患者におけるGVHDに対する予防又は防御のための方法は、同種提供者の骨髄がHLA適合性について患者と適合している場合に、提供者の骨髄を、T細胞傷害性/サプレッサー細胞を1%未満まで枯渇させるのに十分な量の1又は複数の抗CD8モノクローナル抗体及び補体で処理するステップと、処理された骨髄を患者に移植するステップと、患者に、CD4+細胞を失活させるのに十分な有効量のシクロスポリンAを投与するステップとを含む。
Tykocinski, et al.に対して発行された米国特許第5601828号明細書は、CD8誘導体と、細胞調節及び細胞生着の増進のための使用方法とに関する。特異的及び非特異的な免疫調節、細胞生着の増進並びに非免疫細胞の調節は、多様な膜結合性及び可溶性のCD8組成物を用いることにより達成される。この特許において、T細胞増殖又は同種抗原若しくはMHC関連抗原に対する細胞傷害性を特異的に低減するための方法は、その表面内又はその表面上でCD8の細胞外ドメイン部分と同種抗原若しくはMHC関連抗原を提示する天然に存在しない膜を提供するステップであって、少なくとも免疫グロブリンVホモログドメインを含むCD8の細胞外ドメイン部分が、細胞表面分子と共有若しくは非共有結合する分子と共有結合しているステップと、膜を、同種抗原又はMHC関連抗原に対して応答できるT細胞に、同種抗原又はMHC関連抗原に対するT細胞の特異的細胞免疫応答を低減するのに十分な時間及び条件下で曝露するステップとを含む。
Sachsに対して発行された米国特許第5876708号明細書は、同種及び異種移植と、受容者に、短い経過の補助低減処置を施すステップ又は短い経過を投与するステップを含む、寛容を誘導するための方法と、短い経過の免疫抑制剤を投与することによる移植片の許容を延長する方法とに関する。この方法は、第1の種の霊長類受容者に、第2の種の哺乳類から得た移植片に対する寛容を、受容者に、第2の種の造血幹細胞を導入し、移植片を受容者に移植することにより誘導するステップと、受容者のT細胞を失活させるステップと、受容者に、短い経過の免疫抑制剤を投与するステップとを含み、この作用剤は抗T細胞抗体ではなく、短い経過は120日以下である。
やはりSachsに対して発行された米国特許第6911220号明細書は、同種及び異種移植に関する。この発明は、提供者の胸腺組織を受容者に導入するステップを含む、免疫能を回復又は誘導するための方法を提供する。この発明も、提供者の胸腺組織を受容者に導入するステップを含む、受容者における寛容を誘導するための方法を提供する。この発明は、さらに、受容者に、短い経過の補助低減処置を施すステップ又は短い経過を投与するステップを含む寛容を誘導する方法と、短い経過の免疫抑制剤を投与することによる移植片の許容を延長する方法とを提供する。
Bushell, et al.により出願された米国特許出願第20070166307号明細書は、移植片拒絶の抑制を対象とする。簡潔に、CD4、CD8、CD154、LFA−1、CD80、CD86及びICAM−1からなる群より選択される細胞表面抗原に対する抗体、好ましくは抗CD4抗体を、非細胞性タンパク質抗原とともに投与して、動物における制御性Tリンパ球の集団を生成し、制御性Tリンパ球の集団を、動物に非細胞性タンパク質抗原をさらに投与することにより再活性化させ、制御性Tリンパ球の集団が活性化されている間に器官又は組織を移植することにより抑制される動物における移植拒絶が教示されている。制御性T細胞は、T細胞を、CD4、CD8、CD154、LFA−1、CD80、CD86及びICAM−1からなる群より選択される細胞表面抗原に対する抗体と、同種抗原又は非細胞性タンパク質抗原のいずれかを提示する細胞の存在下で培養することにより、エクスビボで生成できる。エクスビボで生成されたTリンパ球は、移植拒絶を克服する代替法として、又はインビボ法と組み合わせて用いることができる。類似のアプローチを、自己免疫状態の治療のために採用できる。
アロ拒絶の特異的阻害のための米国特許出願第20050042217号明細書は、Qi, et al.により出願された。この明細書は、同種抗原に対する細胞性免疫応答及び体液性免疫応答をともに特異的に阻害するための方法及び組成物を提供することにより、移植同種移植片の生存の延長及び移植受容者における移植片対宿主疾患の治療における使用を見出している。この方法は、標的細胞特異的抗原に対する宿主免疫応答を、抗原を発現する標的細胞をCD8ポリペプチドとCD8α鎖とともにコードする発現ベクターと接触させることにより阻害することを教示し、ここで、CD8ポリペプチドは、標的細胞により発現され、それにより標的細胞に対する宿主免疫応答が特異的に阻害される。つまり、標的細胞上でのCD8の増加が、免疫応答を特異的に阻害する。
本発明は、必要とする対象において免疫寛容を誘導するための組成物及び方法を含む。ある実施形態において、組成物及び方法は、対象に、抗原に対するCD8+T細胞免疫寛容を誘導するのに十分な有効量の抗CD8抗体を提供することにより、対象における免疫寛容を誘導するために用いてよい。ある態様において、抗CD8抗体はヒト化されている。別の態様において、抗CD8抗体は、非枯渇性である。この方法は、1又は複数の以下の表現型:グランザイムAの減少、グランザイムBの減少、パーフォリンの減少、IL−2、IFN−γ若しくはこれら両方の分泌量の減少、IL−10の分泌又はそれらの組合せを測定又は決定することにより決定されるサプレッサーT細胞の生成も含んでよい。ある態様において、サプレッサーT細胞の生成は、IL−10を分泌するサプレッサーT細胞の増殖である。別の態様において、抗CD8抗体は、cM−T807、T8、RPA−T8、HIT8a、Leu2、T8及びOKT8から選択される。ある例において、抗原は同種である。
別の実施形態において、本発明は、単離CD8+T細胞を、1又は複数の以下の表現型:グランザイムAの減少、グランザイムBの減少、パーフォリンの減少、IL−2、IFN−γ若しくはこれら両方の分泌量の減少、IL−10の分泌又はそれらの組合せを特徴するサプレッサーCD8+T細胞の生成を引き起こすのに有効な量の抗CD8非枯渇性遮断抗体で処理してサプレッサーCD8+T細胞を移植患者に導入することにより、移植患者における移植拒絶を、その他の免疫応答を維持しながら低減する組成物及び方法を含む。ある態様において、CD8+T細胞は、GM−CSF及びIFN−α−2bと培養した単球から得られる単離樹状細胞(IFN−DC)とインキュベートされる。別の態様において、樹状細胞は、CD34+ヒト末梢細胞を、GM−CSF、Flt3−L及びTNFαと9〜10日間培養することによりインビトロで生成されたランゲルハンス細胞(LC,Langerhans cell)である。樹状細胞の別の例は、CD1a+CD14− LCである。別の態様において、抗CD8抗体は、ウイルスに対する免疫応答に影響することなく、生着された器官に対する免疫応答を下方制御する。別の態様において、抗CD8抗体で処理されたCD8+T細胞は、高結合活性の抗原特異的ナイーブT細胞である。ある非限定的な例において、抗CD8抗体は、cM−T807、T8、RPA−T8、HIT8a、Leu2、T8、OKT8及び表1に列挙される抗CD8抗体から選択される。インビトロでのT細胞の処理のある態様において、抗CD8抗体は、0.5〜5,000ng/mlでCD8+T細胞培養物中に提供される。インビボでの使用のために、本発明は、個体の重量に依存して血液中の等価な濃度について同様のレベルを達成するために提供され得る。
別の態様において、本発明は、末梢血単核細胞を単離するステップと、LC前駆体を末梢血単核細胞から単離するステップと、LC前駆体をGM−CSF、Flt3−L及びTNFαと培養してLCを作製するステップと、T細胞を末梢血単核細胞から単離し、LCとT細胞とを、抗CD8抗体の存在下で、サプレッサーT細胞を生成する条件下で共培養するステップと、T細胞、LC又はその両方を、移植の前、移植と同時又は移植の後に患者に再導入するステップも含んでよい。別の態様において、この方法は、移植患者から末梢血単核細胞を単離するステップと、LCを単離し、LC GM−CSF、Flt3−L及びTNFαを培養するステップと、T細胞を移植患者から単離し、LCとT細胞とを、抗CD8抗体の存在下で共培養してサプレッサーT細胞を生成するステップと、T細胞、LCS又はその両方を、移植の前、移植と同時又は移植の後に患者に再導入するステップも含んでよい。ある態様において、サプレッサーCD8+T細胞は、2型サイトカイン(IL−4、IL−5及びIL−13)及びIL−10の増加した発現を有する。
本発明のさらに別の実施形態は、サプレッサーT細胞を作製する方法及びそれにより作製される細胞を含み、該方法は、末梢血単核細胞を単離するステップと、LC前駆体を末梢血単核細胞から単離するステップと、LC前駆体を、GM−CSF、Flt3−L及びTNFαと培養してLCを作製するステップと、T細胞を末梢血単核細胞から単離し、LCとT細胞とを、抗CD8抗体の存在下で、サプレッサーT細胞を生成する条件下で共培養するステップとを含む。ある態様において、抗CD8抗体は、ウイルスに対する免疫応答に影響することなく、生着された器官に対する免疫応答を下方制御する。ある態様において、CD8+T細胞は、高結合活性の抗原特異的ナイーブT細胞である。ある態様において、ランゲルハンス細胞は、CD1a+CD14− LCである。別の態様において、CD1a+CD14−ランゲルハンス細胞は、細胞選別により得られる。さらに別の態様において、ランゲルハンス細胞は、CD34+HPCをGM−CSF、Flt3−L及びTNFαと9〜10日間培養することによりインビトロで生成される。ある態様において、抗CD8抗体は、cM−T807、T8、RPA−T8、HIT8a、Leu2、T8及びOKT8から選択される。抗CD8抗体は、0.5〜5,000ng/mlで培養物中に提供されてもよい。
さらに別の実施形態において、本発明は、末梢血単核細胞を単離し、単球を末梢血単核細胞から単離し、単球を、GM−CSF及びIFN−α−2bと培養して(IFN−DC)を作製し、T細胞を末梢血単核細胞から単離し、IFN−DCとT細胞とを、抗CD8抗体の存在下で、サプレッサーT細胞を生成する条件下で共培養することにより、サプレッサーT細胞を作製する方法及びそれにより作製されるサプレッサーT細胞を含む。
本発明の別の実施形態は、末梢血単核細胞を単離し、LC前駆体を末梢血単核細胞から単離し、LC前駆体をGM−CSF、Flt3−L及びTNFαと培養してLCを作製し、T細胞を末梢血単核細胞から単離し、LCとT細胞とを、抗CD8抗体の存在下で、サプレッサーT細胞を生成する条件下で共培養することにより作製されたサプレッサーT細胞を含む組成物を投与することにより、免疫応答に影響を及ぼすための方法である。
本発明のさらに別の実施形態は、末梢血単核細胞を単離するステップと、LC前駆体を末梢血単核細胞から単離するステップと、LC前駆体をGM−CSF、Flt3−L及びTNFαと培養してLCを作製するステップと、T細胞を末梢血単核細胞から単離し、LCとT細胞とを、抗CD8抗体の存在下で、サプレッサーT細胞を生成する条件下で共培養するステップとを含む方法により作製されたサプレッサーT細胞を導入することにより、哺乳類における移植された組織の拒絶を阻害する方法である。
別の実施形態において、本発明は、移植拒絶を低減する組成物であって、その他の免疫応答を消失させることなく移植拒絶を低減するのに十分な有効量のサプレッサーT細胞を含み、サプレッサーT細胞が、抗CD8抗体の存在下で、サプレッサーT細胞を生成する条件下で成熟LCと共培養された単離末梢血T細胞から生成される組成物である。ある態様において、抗CD8抗体は、cM−T807、T8、RPA−T8、HIT8a、Leu2、T8及びOKT8から選択される。別の態様において、抗CD8抗体は、0.5〜5,000ng/mlで培養物中に提供される。ある態様において、細胞は凍結しており、使用前に注射用の媒体に再懸濁される。
本発明の特徴及び利点をより完全に理解するために、ここで、添付の図面に従って本発明の詳細な説明について言及する。添付の図面においては次のとおりである。
本発明の種々の実施形態を作製して用いることについて以下に詳細に論じるが、本発明は、広い多様性の具体的な状況において具体化できる多くの応用可能な発明の概念を提供することが認識されるべきである。本明細書において論じる具体的な実施形態は、本発明を作製し、用いるための具体的な様式の単なる例示であり、本発明の範囲を限定するものでない。
本発明の理解を促進するために、いくつかの用語を以下において定義する。本明細書において定義される用語は、本発明に関連する領域における当業者により通常理解されるのと同じ意味を有する。「1つの(a)」、「1つの(an)」及び「その(the)」のような用語は、単数形の物体にのみ言及することを意図しないが、全般的なクラスを含むことを意図し、その具体例は、例示のために用いられ得る。本明細書における術語は、本発明の具体的な実施形態を記載するために用いられるが、それらの使用は、特許請求の範囲に概説されることを除いて、本発明を限定しない。
樹状細胞(DC,Dendritic cell)は、Ag特異的免疫の誘導を担う効力のあるAPCである(Banchereau, J. & Steinman, R. M. Dendritic cells and the control of immunity. Nature 392, 245-52 (1998))。異なる組織に存在するDCのいくつかの集団が存在し、異なる機能的属性を有する(Banchereau, J. & Steinman, R. M. Dendritic cells and the control of immunity. Nature 392, 245-52 (1998))。健康な皮膚は、少なくとも2つのDC集団、表皮においてランゲルハンス細胞(LC)及び真皮において間質DCを有する。これらのDCは、不活性化されたときに末梢寛容のために、そして活性化されたときに免疫のために流入領域リンパ器官に遊走する。その他のDCは、2次リンパ器官に存在し、血液中を循環することが見出されている。DC生物学の理解における多くの進歩が、インビトロで生成したDCを用いて行われた研究に由来した。特に、TNFa及びGM−CSFの存在下でのCD34+造血前駆細胞(HPC,hematopoietic progenitor cell)の培養物は、間質DC及びランゲルハンス細胞をともに生じさせる(Caux, C. et al. CD34+ hematopoietic progenitors from human cord blood differentiate along two independent dendritic cell pathways in response to GM-CSF+TNF alpha. J Exp Med 184, 695-706 (1996))。本発明者らは、IntDCではなくLCが、ナイーブCD8+T細胞のプライミングにおいて特に効果的であることを示した。また、これらのサブセットはともに、メモリー応答の誘導において等しく効果的であり、両方のサブセットにより活性化されるCD8+T細胞は、CD8分子の等しい発現を示す。
CD8は、MHCクラスI分子と複合体を形成したペプチド抗原(pMHCI)のTCR認識のための補助受容体として機能する表面糖タンパク質である。これは、ααホモ二量体又はαβヘテロ二量体のいずれかとして発現され(Zamoyska, R. The CD8 coreceptor revisited: one chain good, two chains better. Immunity 1, 243-6 (1994))、両方の鎖は単一細胞外Igスーパーファミリー(IgSF)Vドメイン、膜近位ヒンジ領域、膜貫通ドメイン及び細胞質側末端を発現する(Zamoyska, R. The CD8 coreceptor revisited: one chain good, two chains better. Immunity 1, 243-6 (1994))。CD8は、MHCクラスI分子のβ2m並びにα2及びα3ドメインと、そのβ鎖及び細胞外IgSF Vドメイン内の相補性決定領域(CDR,complementary determining region)を用いて相互作用する。この会合は、そのクラスI標的とのT細胞受容体の接着/結合活性を増加させる。さらに、CD8α鎖会合チロシンプロテインキナーゼp56lckにより媒介される内部シグナル伝達カスケードは(Veillette, A., Bookman, M. A., Horak, E. M. & Bolen, J. B. The CD4 and CD8 T cell surface antigens are associated with the internal membrane tyrosine-protein kinase p56lck. Cell 55, 301-8 (1988)、Chalupny, N. J., Ledbetter, J. A. & Kavathas, P. Association of CD8 with p56lck is required for early T cell signalling events. Embo J 10, 1201-7 (1991))、T細胞活性化を導く。Lckは、ナイーブCD8+T細胞の活性化及び増殖のために必要である。しかし、その発現は、インビボ又はインビトロでの2次抗原刺激に対するメモリーCD8+T細胞の応答のために必須ではない(Bachmann, M. F. et al. Developmental regulation of Lck targeting to the CD8 coreceptor controls signaling in naive and memory T cells. J Exp Med 189, 1521-30 (1999)、Tewari, K., Walent, J., Svaren, J., Zamoyska, R. & Suresh, M. Differential requirement for Lck during primary and memory CD8+ T cell responses. Proc Natl Acad Sci U S A 103, 16388-93 (2006))。CD8α又はCD8β遺伝子標的マウスのいずれかにより示されるように、CD8は、MHCクラスI拘束性Tリンパ球の成熟及び機能において重要な役割を有する(Fung-Leung, W. P. et al. The lack of CD8 alpha cytoplasmic domain resulted in a dramatic decrease in efficiency in thymic maturation but only a moderate reduction in cytotoxic function of CD8+ T lymphocytes. Eur J Immunol 23, 2834-40 (1993)、Nakayama, K. et al. Requirement for CD8 beta chain in positive selection of CD8-lineage T cells. Science 263, 1131-3 (1994))。繰り返し細菌感染に罹患している1名の患者は、CD8α遺伝子における単一変異によるCD8欠損を示すことが見出された。CD8の欠如は、CD8+T細胞分化系列決定又は末梢細胞溶解機能のいずれにとっても必須でないようであった(de la Calle-Martin, O. et al. Familial CD8 deficiency due to a mutation in the CD8 alpha gene. J Clin Invest 108, 117-23 (2001))。
2D2;4D12.1;7B12 1G11;8E−1.7;8G5;14;21Thy;51.1;66.2;109−2D4;138−17;143−44;278F24;302F27;AICD8.1;抗T8;B9.1.1;B9.2.4;B9.3.1;B9.4.1;B9.7.6;B9.8.6;B9.11;B9.11.10;BE48;BL15;BL−TS8;BMAC8;BU88;BW135/80;C1−11G3;C10;C12/D3;CD8−4C9;CLB−T8/1;CTAG−CD8,3B5;F80−1D4D11;F101−87(S−T8a);G10−1;G10−1.1;HI208;HI209;HI212;HIT8a;HIT8b;HIT8d;ICO−31;ICO−122;IP48;ITI−5C2;ITM8−1;JML−H7;JML−H8;L2;L533;Leu−2a;LT8;LY17.2E7;LY19.3B2;M236;M−T122;M−T415;M−T805;M−T806;M−T807;M−T808;M−T809;M−T1014;MCD8;MEM−31;MEM−146;NU−Ts/c;OKT8;OKT8f;P218;RPA−T8;SM4;T8;T8/2T8−19;T8/2T8−2A1;T8/2T8−1B5;T8/2T8−1C1;T8/7Pt3F9;T8/21thy2D3;T8/21thy;T8/TPE3FP;T8b;T41D8;T811;Tu68;Tu102;UCHT4;VIT8;VIT8b;WuT8−1;X107;YTC141.1;及び/又はYTC182.20を含むヒト白血球分化抗原(Human Leucocyte Differentiation Antigens,HLDA)についての国際ワークショップの一部分のもののような、モノクローナル抗体を含むいくつかの公知の抗CD8抗体のいずれも、本発明に関連して用いてよい。
ヒト化抗CD8抗体の限定しない例は、cM−T807(Centocor社、MA)及びTRX2(Oxford Therapeutic Antibody Centre、Oxford University、Oxford、United Kingdom)を含む。
樹状細胞(DC)は、抗原特異的免疫応答を開始して極性化する。ヒト骨髄細胞(mDC,myeloid DC)は、ランゲルハンス細胞及びヒトの皮膚に存在する間質(真皮)DCのような異なるサブセットを含む。我々は、間質DCと比較した場合に、ランゲルハンス細胞が、同種及び自己の抗原に対してナイーブCD8+T細胞をプライミングすることについて特に強力であるが、これらのmDCサブセットはともに、2次応答の誘導においては等しく有効であったことを報告した。本研究は、CD8+T細胞プライミングの誘導におけるLCの優れた機能を説明するであろうパラメータを分析するために行った。LCによりプライミングされたCD8+T細胞は、IntDCによりプライミングされたCD8+T細胞と比較して、より高いレベルのCD8を発現するが、両方のサブセットにより誘導される抗原特異的メモリーCD8+T細胞は、等しいレベルのCD8を提示する。
本明細書において、抗CD8モノクローナル抗体が、自己及び同種抗原CTLのDCにより媒介されるインビトロプライミングを遮断することを示す。抗CD8の存在下でプライミングされるCD8+T細胞は、標的を死滅させることができず、2型(IL−4、IL−5、IL−13)及び制御性(IL−10)のサイトカインを産生した。さらに、抗CD8mAbの存在下でプライミングされたCD8+T細胞は、アロ反応を阻害でき、よって、サプレッサーCD8+T細胞として作用した。しかし、インフルエンザ及びCMVに対するもののような2次CTL応答の誘導は、妨害されなかった。同様に、抗CD8mAbは、CD4+T細胞応答を変化させなかった。ヒト−マウスモデル細胞集団におけるアロ反応性CD8+T細胞のインビボでの活性化のための抗CD8mAbの投与は、同種CD8+T細胞の注射により誘導される移植片対宿主疾患の発生を妨げた。つまり、抗CD8抗体療法は、CD8+T細胞により媒介される移植片拒絶を、抗ウイルス保護応答を混乱させることなく予防し、よって現在の免疫抑制治療を超える著しい進歩を示すかもしれない。本出願は、CD8ライゲーションが、T細胞プライミングの阻害及び制御性T細胞の生成をもたらすことを示した。
本発明者らは、LCが、間質DCと比較してナイーブCD8T細胞のプライミングにおいて非常に効果があるが、これらのmDCサブセットはともに、2次応答の誘導において等しく有効であることを示した。本研究は、CD8+T細胞プライミングの誘導におけるLCの優れた機能を説明するであろうパラメータを分析するために行った。本明細書において、CD8ライゲーションが、T細胞プライミングの阻害をもたらすだけでなく、制御性T細胞の生成も引き起こすことを示す。
DC精製及び培養。CD34由来DCは、G−CSF動員性CD34−HPCを0.5×106/mlにて25cm2フラスコ中で、5%自己血清、50μM 2−β−メルカプトエタノール、1% L−グルタミン、1%ペニシリン/ストレプトマイシン並びにサイトカイン;GM−CSF(50ng/ml;Immunex Corp.社製)、FLT3−L(100 ng/ml;R&D社製)及びTNF−α(10ng/ml;R&D社製)を含有するYssel培地(Irvine Scientific社製、CA又はGemini BioProducts社製)中で培養することにより生成した。培養物は、37℃にて5%CO2を用いて湿潤環境中でインキュベートした。細胞を、サイトカインを補った新鮮な培地に培養第5日に移し、第9又は10日に採集した。CD1a+CD14−−LC及びCD1a−CD14+−intDCを選別した。純度は、日常的に、95〜99%であった。
CD14+単球(純度90%を超える)(1×106細胞/ml)を、1%ペニシリン/ストレプトマイシンを補ったCellgenix培地(Cellgenix社製)並びに100ng/mlのGM−CSF(Berlex社製)及び500U/mlのIFN−α−2b(Schering Corp社製)の中で37℃及び5%CO2にて培養することにより、IFN由来DC(IFN−DC)を生成し、新鮮な培地及びサイトカインを第1日に加え、DCを第3日に採集した。
LC及び真皮IntDCを、正常ヒト皮膚検体から精製した。検体を、細菌プロテアーゼ2型ジスパーゼ(Roche社製)、抗生物質/抗真菌物質(Gibco社製)中で4℃にて18時間、次いで37℃にて2時間インキュベートした。表皮及び真皮のシートを次いで分離し、小片(およそ1〜10mm)に切断し、10%胎児ウシ血清(FBS)を補ったRPMI 1640(Gibco社製)中に入れた。2日後に、培地中に遊走した細胞を回収し、Ficoll-ジアトリゾエート勾配、1.077g/dl(リンパ球分離用培地(LSM,Lymphocyte Separation Medium)、MP Biomedicals社製)を用いてさらに濃縮した。DCを、抗CD1a FITC(OKT6;DAKO社製)mAb及び抗CD14−APC(LeuM3;Invitrogen社製)mAbで染色した後に細胞選別により精製した。
T細胞単離。細胞を、成人ボランティア提供者からの白血球除去により得られた凍結PBMCから単離した。ナイーブCD8T細胞を、CD4−、CD56−、CD16−及びCD19−磁気細胞除去(Miltenyi社製)の後にCD45RA+CCR7+HLA−DR−CD8+細胞として選別した。CD8T細胞を除去し、得られる細胞をCD4+CCR7+CD45RA+CD4−CD16−CD19−CD56−として選別した以外は同様の方法で、ナイーブCD4+T細胞を得た。再生応答のために、CD8+T細胞を、濃縮集団からポジティブ選択した。
DC/CD8T細胞共培養。自己CD8+T細胞−DC共培養。1次応答評価のために、ナイーブCD8+T細胞(1×106細胞/ウェル)を、HLA−A201拘束性MART−1(MART−1M26〜35、ELAGIGILTV)又はgp100(gp100M209〜217、IMDQVPFSV)ペプチド(3μM)と3時間予めインキュベートした自己mDC(5×104細胞/ウェル)で刺激した。細胞を9日間、24ウェルプレートにおいて、10U/mlのIL−7(R&D社製)及び100ng/mlのCD40L(R&D社製)を補ったYssel完全培地中で培養した。IL−2(R&D社製)を10U/mlにて第3日に加えた。抗CD8又はアイソタイプ適合対照は、そうでないと記載しない限り第0日に加えた。
ペプチド特異的CD8+T細胞の増殖は、培養期間の最後にてペプチド/HLA−A201四量体(Beckman Coulter社製)に結合する細胞の数を計数することにより決定した。再生応答の評価のために、全CD8+T細胞(1×106細胞/ml)を、HLA−A201拘束性インフルエンザ−MPペプチド(GILGFVFTL)を負荷した自己(5×105細胞/ml)mDCサブセットで刺激した。抗CD8又はアイソタイプ適合対照の存在下で。インフルエンザ−MP特異的CD8+T細胞の頻度を、インフルエンザ−MP/HLA−A201四量体を用いることにより決定した。
同種CD8T細胞培養。ナイーブCD8+T細胞の同種増殖を、[H3]−チミジン取り込み又はCFSE希釈により評価した。ナイーブT細胞(1×105細胞/ウェル)を、丸底96ウェルプレートにおいて、2.5×104(そうでないと記載しない限り)の同種mDCサブセットを加えた10%熱失活プールABヒト血清を補ったYssel培地(Yssel完全培地)、IL−7及びIL−2(10IU/ml、R&D社製)中で培養した。CD40Lを用いて、DCを活性化した。5日後に、細胞を18時間、1μCi[H3]−チミジンを用いてパルスし、トレーサーの取り込みを、継続中の増殖の指標として決定した。
CFSE希釈による増殖の評価のために、細胞を、0.5μMのCFSEで、製造者の手順に従って標識した。7日後に、細胞を採集し、増殖のレベルをフローサイトメトリーにより分析した。さらに、プライミングされたCD8+T細胞の質を、以下に記載するようにして評価した。
記載する場合、CD8に対する遮断抗体(クローンRPA−T8、OKT6、BD又はT8 Beckman Coulter社製)又はアイソタイプ対照抗体を、共培養物に加えた。
2次同種CD8+T細胞培養のために、5×104のナイーブCD8T細胞を、2.5×103のCD40リガンド活性化DCと、丸底96ウェルプレートにおいて、IL−7及びIL−2を加えて培養した。6日後に、細胞を、1次培養に用いたのと同じ提供者からのDCを用いて再刺激した。抗CD8抗体又はアイソタイプ適合対照を、培養物に3日間加え、その後、細胞増殖を、[3H]チミジンの取り込みにより評価した。
サイトカイン産生。CD8+T細胞サイトカイン産生評価のために、増殖したCD8+T細胞(FSChighCD11c−又はCFSElowCD11c−)を第7日に、1次同種培養物からの細胞選別により単離し、抗CD3及び抗CD28被覆マイクロビーズを用いて1晩再刺激した。上清中のサイトカインを、マルチプレックスビーズベースのサイトカインアッセイにより評価した。
CD8+Tサプレッサーアッセイ。CD8+Tサプレッサー機能アッセイのために、増殖したCD8+T細胞(FSChighCD11c−又はCFSElowCD11c−)を第7日に、1次同種培養物からの細胞選別により単離し、段階的な数で、5×104ナイーブCD8+T細胞とCD40L活性化2.5×103同種DC(LC)との共培養物に加えた。培養5日後に、1μ/Ciの[3H]チミジンをそれぞれのウェルに加え、細胞への取り込みを18時間後に決定した。
T細胞タンパク質及び遺伝子分析。エフェクター分子の染色のために、プライミングされたCD8+T細胞を固定し、透過性にし、PE標識抗グランザイムA、グランザイムB及びパーフォリン(BD Biosciences社製)で染色した。
CD8+T細胞表現型分析のために、細胞を、全てBD biosciences社からのCD25(M−A251)、CD28(CD28.2)、CCR7、CD103(Ber−ACT8)の表面発現について染色した。
マイクロアレイ遺伝子分析のために、1次同種培養物から増殖CD8T細胞(CFSE−)を選別し、抗CD3及び抗CD28被覆マイクロビーズで再刺激した。
インビボでの移植片対宿主疾患に対する抗CD8治療の評価。動員性末梢血(mobilized peripheral blood,MPB)CD34+細胞(動物あたり3〜6×106のMPB CD34+細胞)を、致死量以下で照射した(137Csγ照射による300センチグレイ)NOD/SCIDマウスの別々の実験的コホートに、以前に記載されたようにして、移植の10〜12週間後に静脈内注入し、マウスに、同種提供者からの10Mの選別したナイーブCD8+T細胞を皮下注射した。マウスを、IgG1対照mAb又は抗CD8mAb(RPA−T8、BD biosciences社製、第0日に0.75mg及び第3日に0.25mg)を用いて皮下処置した。2回の実験のうちの一方において、抗CD40モノクローナル抗体(MAB89、Schering-Plough社製)を、同種移植の日に腹腔内注射して、DCを活性化した。
マウスを、生存、並びに下痢、体重減少及びひだ状の皮膚により発現されるGVHDの臨床徴候について毎日観察した。症状が現れた場合に、マウスを採集した。ヒトCD8+T細胞を、フローサイトメトリーにより分析した。
インビトロ生成LCを用いるナイーブCD8+T細胞のインビトロプライミング。HLA−A201+LC及びIntDCを、CD34+HPCを、GM−CSF、Flt3−L及びTNFαの存在下で9〜10日間培養することによりインビトロで生成した。細胞を、CD1a+CD14−LC(LC)とCD1a−CD14+IntDC(IntDC)とに選別した。1次応答のために、3μMのHLA−A201拘束性黒色腫ペプチドMART−1(26〜35)を負荷したDCサブセットを、自己ナイーブCD8+T細胞と9〜10日間培養した。培養の最後での抗原特異的CD8+T細胞の頻度を、特異的ペプチド−MHC四量体を用いて測定した。
図1a及び図1bに示すように、LCによりプライミングされたナイーブCD8+T細胞は、IntDCでプライミングされたCD8+T細胞と比較して、表面CD8発現を上方制御する。メモリー応答のために、DCサブセットに、1μMのHLA−A201拘束性インフルエンザ基質ペプチドM1を負荷した。DCを、選別した自己メモリーCD8+T細胞と培養した。対照的に、両方のサブセットは、ウイルス抗原に対する2次応答の誘導について等しく効果的であり、いずれのサブセットにより活性化されたCD8+T細胞も、等しいレベルの表面CD8を発現する(図1c)。
抗CD8抗体は、抗原特異的CD8+T細胞のプライミングを妨げる。抗CD8mAb RPA−T8を加えることにより、MART−1によりパルスされたLCによるMART−1特異的CD8+T細胞の増殖が効果的に遮断された(図2a)。動態分析は、抗CD8mAbを培養物に加えた場合に、第1日〜第9日に、ほとんど抗原特異的CD8+T細胞増殖が観察されないことを示す(図2b)。CD8+T細胞プライミングの阻害は、0.1μg/mlの抗体が抗原特異的CD8+T細胞の増殖のほぼ完全な阻害をもたらし、50%阻害濃度(IC50,50% Inhibitory Concentration)が50〜500ng/mlの範囲であったので、非常に効果的であった(図2c)。3つの試験した抗CD8抗体(T8、RPA−T8及びOKT8)のうち3つが、T細胞プライミングを阻害した(図2d)。
70時間目まで培養物への抗CD8mAbの添加を遅らせてもまだ、黒色腫特異的CD8+T細胞プライミングの75%が阻害された(図2e)。MART−1ペプチド負荷LCとナイーブCD8+T細胞を低濃度の抗CD8の存在下で培養すると、1次対照培養物と比較して、MART−1特異的CD8+T細胞の数が減少した(図2f)。さらに、抗CD8mAbに曝露したCD8+T細胞は、対照抗体に曝露したものと比較して、より低いMART−1 MHC−四量体強度染色を示した。培養物に加える抗CD8mAbが多いほど、抗原特異的T細胞上で観察される四量体強度結合がより小さかった(図2g)。
抗CD8mAbは、単球をGM−CSF及びIFNと培養することにより生成するDC(IFN−DC)により誘導されるMART−1及びgp100特異的CD8+T細胞のプライミングを遮断できたが(図2h)、このことは、阻害効果が、DCの供給源にもプライミングのために選択された抗原にも依存しないことを示す。さらに、抗CD8mAbは、高濃度のペプチドをDCに負荷した場合又は抗原が培養の間中存在した場合でさえもプライミングを遮断できた(図2i)。これらのデータをまとめると、遮断CD8が、高結合活性抗原特異的ナイーブT細胞のDCにより誘導されるプライミングを妨げることを示す。
抗CD8抗体は、DCにより媒介されるCD8T細胞のアロ増殖を阻害する。抗CD8mAb又はアイソタイプ対照を、ナイーブCD8+T細胞の培養物に、段階的な数のインビトロ生成同種LCとともに加えた。[3H]チミジン取り込みアッセイを用いる図3aに示すように、LCにより誘導される同種ナイーブCD8+T細胞の増殖は、抗CD8mAbにより阻害された。LCと同種ナイーブCD4+及びCD8+T細胞との共培養物に対して行ったCFSE希釈アッセイにより、CD8+T細胞増殖の阻害を確認した(図3b上のパネル)。これはさらに、同種CD4+T細胞の増殖が、抗CD8抗体により影響されなかったことを明らかにした(図3b下のパネル)。実際に、CD8+T細胞増殖が30ng/mlにて阻害されたが(図3c上のパネル)、CD4+T細胞は、用いた抗CD8mAbのいずれの濃度についても(0〜3μg/ml)増殖の低下を示さなかった(図3c下のパネル)。ヒト皮膚から単離された真皮DC又はLCにより誘導される同種T細胞の活発な増殖も、抗CD8mAbにより遮断された(図3d及びe)。抗CD8mAbの存在下では、CD8+T細胞とDCの間でわずかにまばらな小さいクラスタのみが形成された(図3f)。しかし、抗CD8mAbを含まない培養物では、活発な増殖が、DC及びCD8+T細胞の多くの大きいクラスタを伴った(図3g)。つまり、抗CD8抗体は、同種CD8+T細胞のDCにより媒介されるプライミングを阻害できる。
抗CD8は、自己又は同種抗原に対する2次応答を遮断しない。メモリーCD8+T細胞応答が抗CD8mAbによっても阻害されるかを調べるために、免疫優性HLA−A2結合インフルエンザ基質タンパク質M1ペプチド(57〜68)を負荷したHLA−A2+LC又はIntDCを、CD8+T細胞並びに抗CD8mAb及びその適切な対照とともに培養した。両方のDCサブセットについて、四量体染色により測定される抗原特異的CD8+T細胞の数は、抗CD8mAb又はアイソタイプ対照と同等であった(図4a及びc)。抗CD8mAbの濃度が2.5μg/mlほど高くても、阻害は検出されなかった(図4b及びd)。試験した2つの他の抗CD8mAb(T8 Beckman、RPA−T8 BD)は、メモリー細胞のインフルエンザペプチドにより誘導される活性化を阻害しなかった(図4e)。
メモリー同種CD8+T細胞応答が抗CD8mAbにより影響されるかを証明するために、ナイーブCD8+T細胞を、同種LC又はIntDCにより7日間プライミングし、T細胞を3日間再刺激した。図4fに示すように、抗CD8mAbは、LC又はIntDCのいずれを用いても、元来の同種抗原でのCD8+T細胞再刺激を阻害できなかった。つまり、これらのデータは、メモリーCD8+T細胞応答がCD8に依存しないことを証明する。
CD8+T細胞の抗CD8mAbでのプライミングは、低レベルの細胞溶解分子を有する2型T細胞を生じる。図5に示すように、同種DCを用いるプライミングの間に抗CD8mAbに曝露したCD8+T細胞は、低レベルのCD25、ICOS、CD27、CD28と、グランザイムA及びB並びにパーフォリンのより低い細胞内発現とを発現する(図5a)。LC及びアイソタイプ対照で7日間プライミングされたCD8+T細胞は、抗CD3と抗CD28とを用いる24時間の再刺激の後に、IFN−γ(2,000〜6,000pg/ml)及びIL−2(1,000〜6000pg/ml)、並びに低レベルのIL−4、IL−5、IL−13及びIL−10を産生した。LC及び抗CD8でプライミングされたCD8+T細胞は、同量のIFN−γ及びIL−2を分泌したが、高い量のIL−4(100〜600pg/ml)、IL−5(500〜2500pg/ml)、IL−13(1000〜7000pg/ml)及びIL−10(70〜100pg/ml)を分泌した(図5b)。
まとめると、データは、抗CD8mAbが、活性化されたCD8+T細胞の表現型を変更して、2型サイトカインを分泌し、低レベルの細胞傷害性分子を発現する細胞を生じることを示す。
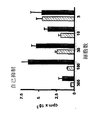
抗CD8の存在下でプライミングされたアロ反応性CD8+T細胞は、ナイーブCD8+T細胞応答を強く抑制する。抗CD8mAbの存在下でプライミングされたCD8+T細胞がサプレッサー機能を示すかを決定するために、CFSE標識ナイーブCD8+T細胞(提供者A)を、同種LC(提供者B)と、抗CD8mAb又はアイソタイプ適合対照とともに7日間培養した。活性化されたCD8+T細胞(CFSE−CD11c−)を選別し、段階的な数(3〜300)にて、50,000の提供者Aからの自己ナイーブCD8+T細胞と2500の提供者Bからの同種LCとの共培養物に加えた。抗CD8mAbを用いてプライミングされたCD8+T細胞は、ナイーブCD8+T細胞の同種LCへの増殖を用量依存的な様式で強く阻害し、100ほどの少ない細胞が80%程度アロ反応を抑制し、10の細胞が50%遮断した。しかし、アイソタイプ対照でプライミングされたCD8+T細胞は、阻害を示さなかった(図6a)。阻害は、抗CD8mAb処理CD8+T細胞にそれらのアロ特異的DCを加えたときに特に著しく、抑制の強さは、提供者CからのDCを用いると、より低かった(図6b)。
抗CD8mAbは、同種CD8+T細胞活性化及び移植片対宿主疾患をインビボで阻害する。抗CD8抗体を用いてインビトロで観察されたCD8IT細胞プライミングの強い阻害に導かれて、我々は、このことが、pDC、mDC及びB細胞に分化するがT細胞に分化しないヒトCD34+HPCを移植された免疫不全NOD−SCIDマウスにおいてインビボでも発生するかを調べた。これらのヒト化マウスに、同種提供者からの20×106の精製CD8+T細胞を、0.75mgの抗CD8mAb又はアイソタイプ適合対照抗体のいずれかとともに、皮下にて養子移入した。さらに0.25mgの抗体を第3日に注射した。2回の実験のうちの一方において、抗CD40抗体(MAB89、Schering Plough社製、100μg)を、DC活性化のために腹腔内注射した。マウスを、疾病の徴候について定期的に調べた。CD8+T細胞の移入の10週間後に、アイソタイプ適合対照抗体を受容したマウスは、目の周囲の発疹、体重減少及び脱力の慢性移植片対宿主疾患の臨床症状を発生した(図7a)。しかし、抗CD8抗体での処置は、病原性T細胞の活性化及び増殖と臨床症状の発生とをともに完全に阻害した(図7)。アイソタイプ対照処置マウスの骨髄からのCD8+T細胞はCD103を上方制御したが、抗CD8mAbで処置したマウスは上方制御しなかった(図7b)。
まとめると、これらのデータは、抗CD8mAb療法が、ヒト免疫系を有する免疫不全マウスにおいて移植片対宿主疾患を媒介するCD8+T細胞の同種1次活性化を妨げることにおいて効果的であることを示す。
本研究は、なぜLCが間質DCよりも、これらのmDCサブセットがともに2次CD8+T細胞応答の誘導において等しく効果的であるのに、ナイーブCD8+T細胞のプライミングにおいて、より効力があるのかを理解するために行った。抗CD8mAbをナイーブCD8+T細胞とDCとの共培養物に加えた結果から、いくつかの結論が導かれた。第1に、ナイーブCD8+T細胞のプライミングは、非常に低い濃度の抗体で著しく阻害されることが見出されたが、メモリー細胞の活性化は、高濃度の抗体にさえ影響されなかった。第2に、残存増殖細胞は、エフェクター経路よりもむしろサプレッサー経路に沿って分化した。
これらのデータは、試験した抗CD8モノクローナル抗体の全体が、非常に低い濃度にて、自己又は同種MHCの状況においてインビトロで提示される抗原に対するCD8+T細胞のDCにより媒介される増殖を遮断することを証明した。しかし、ウイルス又は同種抗原に対する再生応答は、抗CD8mAbにより阻害されなかった。これらのデータは、抗CD8抗体がナイーブCD8+T細胞の増殖を遮断できるが、エフェクター及びメモリー細胞のものは遮断できないことを示す、マウスリンパ球を用いたインビトロ研究についての以前の報告と一致する(Bachmann, M. F. et al. Developmental regulation of Lck targeting to the CD8 coreceptor controls signaling in naive and memory T cells. J Exp Med 189, 1521-30 (1999))。アロ反応性ナイーブCD8+T細胞の活性化も遮断した抗CD8は、ヒト化マウスモデルにおいてインビボでも観察され、移植片対宿主応答の除去をもたらした。おそらく最も著しい観察は、抗CD8抗体を加えることが、応答の型をエフェクター応答からサプレッサー応答へ質的に改変したことである。生成されたサプレッサー細胞は、発現が低下したグランザイムA及びB並びにパーフォリンと、低いCD28との独特の表現型を発現する。さらに、これらの細胞は、発現が増加した2型サイトカイン(IL−4、IL−5及びIL−13)と、発現が増加したIL−10との変更された表現型パターンを発現する。さらに、これらの細胞は、100のこれらの細胞が80%のアロ反応を、特に同族APCにより活性化されたときに遮断できるという効力のある抑制能力を発現する。興味深いことに、この表現型は、我々が他の所で報告するようなCD14+IntDC上で培養されたCD8+T細胞の表現型と同等である。
これらの観察は、臨床的に重要である。なぜなら、T細胞は、同種移植片拒絶の主なメディエーターであるからである(Hall, B. M. Cells mediating allograft rejection. Transplantation 51, 1141-51 (1991)、Rosenberg, A. S. & Singer, A. Cellular basis of skin allograft rejection: an in vivo model of immune-mediated tissue destruction. Annu Rev Immunol 10, 333-58 (1992))。同種移植片受容者におけるT細胞の最初の活性化を特異的に遮断する治療を設計することに対して、多くの努力が向けられてきた。CD4+T細胞依存性経路及びCD8+T細胞依存性経路はともに、同種移植片拒絶を開始することが示されている。ラパマイシン(Slavik, J. M., Lim, D. G., Burakoff, S. J. & Hafler, D. A. Rapamycin-resistant proliferation of CD8+ T cells correlates with p27kip1 down-regulation and bcl-xL induction, and is prevented by an inhibitor of phosphoinositide 3-kinase activity. J Biol Chem 279, 910-9 (2004))、シクロスポリン(Boleslawski, E. et al. Defective inhibition of peripheral CD8+ T cell IL-2 production by anti-calcineurin drugs during acute liver allograft rejection. Transplantation 77, 1815-20 (2004))、抗CD4mAb(Jones, N. D. et al. CD40-CD40 ligand-independent activation of CD8+ T cells can trigger allograft rejection. J Immunol 165, 1111-8 (2000))、抗CD154mAb(Guo, Z. et al. CD8 T cell-mediated rejection of intestinal allografts is resistant to inhibition of the CD40/CD154 costimulatory pathway. Transplantation 71, 1351-4 (2001))及びCTLA4−Ig(Newell, K. A. et al. Cutting edge: blockade of the CD28/B7 costimulatory pathway inhibits intestinal allograft rejection mediated by CD4+ but not CD8+ T cells. J Immunol 163, 2358-62 (1999))のような免疫調節ストラテジーは、CD4依存性免疫活性化の抑制に非常に効果的であるが、拒絶のCD8依存性経路は、研究において、耐性であることが示されている。カルシニューリン阻害剤による抑制に対するCD8+T細胞の耐性は、臨床研究における急性同種移植片拒絶の発生率の増加とも関連している(Zhai, Y., Meng, L., Gao, F., Busuttil, R. W. & Kupiec-Weglinski, J. W. Allograft rejection by primed/memory CD8+ T cells is CD154 blockade resistant: therapeutic implications for sensitized transplant recipients. J Immunol 169, 4667-73 (2002))。このことは、インビボで観察されるCD4+及びCD8+T細胞の異なる共刺激要件と一致する。CD8依存性の同種移植片拒絶は、CD40/CD154共刺激に依存し、CD28/B7共刺激経路から独立している(Newell, K. A. et al. Cutting edge: blockade of the CD28/B7 costimulatory pathway inhibits intestinal allograft rejection mediated by CD4+ but not CD8+ T cells. J Immunol 163, 2358-62 (1999))。
第1世代の抗CD3mAbは、その他のほとんどの免疫抑制治療と同様に、CMVのような重篤なウイルス感染を伴う免疫抑制をもたらす同種移植片受容者におけるT細胞の最初の活性化を遮断する。つまり、抗CD8抗体がウイルス特異的メモリー応答を損なわれないままにしながら、エフェクター細胞プライミングを遮断するとの観察は、抗ウイルス2次応答を損なわれないままにしながら、移植片を攻撃するアロ反応性CD8+T細胞の生成を妨げるのだろう。
移植部位でのCD8+T細胞によるCD103の上方制御は、同種移植片損傷を媒介するCD8+T細胞の能力と密接につながっている(Hadley, G. A., Bartlett, S. T., Via, C. S., Rostapshova, E. A. & Moainie, S. The epithelial cell-specific integrin, CD103 (alpha E integrin), defines a novel subset of alloreactive CD8+ CTL. J Immunol 159, 3748-56 (1997))。上皮細胞特異的インテグリンであるCD103(αEインテグリン)は、アロ反応性CD8+CTLの新規なサブセットを規定する(Feng, Y. et al. CD103 expression is required for destruction of pancreatic islet allografts by CD8(+) T cells. J Exp Med 196, 877-86 (2002))。同種移植片拒絶の(CD4非依存性)CD8依存性経路の活性化は、活発な免疫応答を惹起し、これは、免疫調節に対して非常に耐性が高い。腎臓拒絶中の主にCD8+CTLA4+Tリンパ球の強い局所的な浸潤が、患者において記載されている。このことは、CD8+T細胞が、免疫抑制を逃れて、拒絶プロセスに参加できることを示唆する。CD4及びCD8応答の両方を制御することは、寛容及び長期の生存を促進するために必要であり得る(Cobbold, S. P., Martin, G. & Waldmann, H. The induction of skin graft tolerance in major histocompatibility complex-mismatched or primed recipients: primed T cells can be tolerized in the periphery with anti-CD4 and anti-CD8 antibodies. Eur J Immunol 20, 2747-55 (1990))。
CD8療法は、ループス又は糖尿病のような自己免疫疾患における自己反応性CD8+T細胞のプライミングの予防においても有益であり得る。
本明細書で論じられるいずれの実施形態も、本発明のいずれの方法、キット、試薬又は組成物に関しても実行でき、またその逆も同じであると考えられる。さらに、本発明の組成物は、本発明の方法を達成するために用いることができる。
本明細書に記載される具体的な実施形態は、例示のために示され、本発明の限定として示されるのでないことが理解される。本発明の主な特徴は、本発明の範囲を逸脱することなく、種々の実施形態において用いることができる。当業者は、日常的なものを超える実験を行うことなく、本明細書に記載される特定の手順の多数の等価物を認識するか、又は確認できる。このような等価物は、本発明の範囲内と考えられ、特許請求の範囲によりカバーされる。
本明細書で言及する全ての出版物及び特許出願は、本発明が関する当該技術における当業者のレベルを示す。全ての出版物及び特許出願は、それぞれ個別の出版物又は特許出願が、参照により組み込まれると具体的にかつ個別に記載されているのと同程度で、参照により本明細書に組み込まれる。
特許請求の範囲及び/又は明細書において用語「含む」とともに用いる場合の語句「1つの(a)」又は「1つの(an)」の使用は、「1つ(one)」を意味し得るが、「1又は複数」、「少なくとも1つ」及び「1及び1より多い」の意味とも一致する。特許請求の範囲における用語「又は」の使用は、それが選択肢のみ及び「及び/又は」に言及するという定義を開示が支持しても、選択肢のみに言及すると明記するか、又は選択肢が互いに排他的である場合を除いて、「及び/又は」を意味するために用いられる。本出願をとおして、用語「約」は、値が、値を決定するために用いた装置、方法についての固有の誤差の変動、又は研究対象のうちに存在する変動を含むことを示すために用いられる。本明細書及び特許請求の範囲において用いる場合、語句「含んでいる(comprising)」(並びに「含む(comprise)」及び「含む(comprises)」のような含んでいる(comprising)の任意の形)、「有している(having)」(並びに「有する(have)」及び「有する(has)」のような有している(having)の任意の形)、「含んでいる(including)」(並びに「含む(includes)」及び「含む(include)」のような含んでいる(including)の任意の形)、又は「含有している(containing)」(並びに「含有する(contains)」及び「含有する(contain)のような含有している(containing)の任意の形)は、包括的又は拡張可能であり、追加の明記されていない要素又は方法ステップを排除しない。
本明細書で用いる場合、用語「又はそれらの組合せ」とは、この用語に先行する列挙された項目の全ての順列及び組合せに言及する。例えば、「A、B、C又はそれらの組合せ」は、A、B、C、AB、AC、BC又はABCの少なくとも1つを含むことを意図し、もし特定の文脈において順序が重要である場合、BA、CA、CB、CBA、BCA、ACB、BAC又はCABも含むことを意図する。この例の続きとして、BB、AAA、MB、BBC、AAABCCCC、CBBAAA、CABABBなどのような1若しくは複数の項目又は用語の反復を含む組合せも明確に含まれる。当業者は、文脈から明らかでない限り、典型的には、任意の組合せの項目又は用語の数に制限がないことを理解する。
本明細書に開示され、請求される組成物及び/又は方法の全ては、本発明の開示に照らして、過度の実験を行うことなく作製して実行できる。本発明の組成物及び方法は、好ましい実施形態の点で記載されているが、組成物及び/又は方法並びに本明細書に記載される方法のステップ又はステップの順序を、本発明の概念、精神及び範囲を逸脱することなく、変動し得ることが当業者に明らかである。当業者にとって明らかな全てのこのような類似の置換及び改変は、添付の特許請求の範囲により定義されるような本発明の精神、範囲及び概念内であるとみなされる。
(参考文献)
1. Banchereau, J. & Steinman, R. M. Dendritic cells and the control of immunity. Nature 392, 245-52 (1998)
2. Caux, C. et al. CD34+ hematopoietic progenitors from human cord blood differentiate along two independent dendritic cell pathways in response to GM-CSF+TNF alpha. J Exp Med 184, 695-706 (1996)
3. Zamoyska, R. The CD8 coreceptor revisited: one chain good, two chains better. Immunity 1, 243-6 (1994)
4. Veillette, A., Bookman, M. A., Horak, E. M. & Bolen, J. B. The CD4 and CD8 T cell surface antigens are associated with the internal membrane tyrosine-protein kinase p56lck. Cell 55, 301-8 (1988)
5. Chalupny, N. J., Ledbetter, J. A. & Kavathas, P. Association of CD8 with p56lck is required for early T cell signalling events. Embo J 10, 1201-7 (1991)
6. Bachmann, M. F. et al. Developmental regulation of Lck targeting to the CD8 coreceptor controls signaling in naive and memory T cells. J Exp Med 189, 1521-30 (1999)
7. Tewari, K., Walent, J., Svaren, J., Zamoyska, R. & Suresh, M. Differential requirement for Lck during primary and memory CD8+ T cell responses. Proc Natl Acad Sci U S A 103, 16388-93 (2006)
8. Fung-Leung, W. P. et al. The lack of CD8 alpha cytoplasmic domain resulted in a dramatic decrease in efficiency in thymic maturation but only a moderate reduction in cytotoxic function of CD8+ T lymphocytes. Eur J Immunol 23, 2834-40 (1993)
9. Nakayama, K. et al. Requirement for CD8 beta chain in positive selection of CD8-lineage T cells. Science 263, 1131-3 (1994)
10. de la Calle-Martin, O. et al. Familial CD8 deficiency due to a mutation in the CD8 alpha gene. J Clin Invest 108, 117-23 (2001)
11. Hall, B. M. Cells mediating allograft rejection. Transplantation 51, 1141-51 (1991)
12. Rosenberg, A. S. & Singer, A. Cellular basis of skin allograft rejection: an in vivo model of immune-mediated tissue destruction. Annu Rev Immunol 10, 333-58 (1992)
13. Slavik, J. M., Lim, D. G., Burakoff, S. J. & Hafler, D. A. Rapamycin-resistant proliferation of CD8+ T cells correlates with p27kip1 down-regulation and bcl-xL induction, and is prevented by an inhibitor of phosphoinositide 3-kinase activity. J Biol Chem 279, 910-9 (2004)
14. Boleslawski, E. et al. Defective inhibition of peripheral CD8+ T cell IL-2 production by anti-calcineurin drugs during acute liver allograft rejection. Transplantation 77, 1815-20 (2004)
15. Jones, N. D. et al. CD40-CD40 ligand-independent activation of CD8+ T cells can trigger allograft rejection. J Immunol 165, 1111-8 (2000)
16. Guo, Z. et al. CD8 T cell-mediated rejection of intestinal allografts is resistant to inhibition of the CD40/CD154 costimulatory pathway. Transplantation 71, 1351-4 (2001)
17. Newell, K. A. et al. Cutting edge: blockade of the CD28/B7 costimulatory pathway inhibits intestinal allograft rejection mediated by CD4+ but not CD8+ T cells. J Immunol 163, 2358-62 (1999)
18. Zhai, Y., Meng, L., Gao, F., Busuttil, R. W. & Kupiec-Weglinski, J. W. Allograft rejection by primed/memory CD8+ T cells is CD154 blockade resistant: therapeutic implications for sensitized transplant recipients. J Immunol 169, 4667-73 (2002)
19. Hadley, G. A., Bartlett, S. T., Via, C. S., Rostapshova, E. A. & Moainie, S. The epithelial cell-specific integrin, CD103 (alpha E integrin), defines a novel subset of alloreactive CD8+ CTL. J Immunol 159, 3748-56 (1997)
20. Feng, Y. et al. CD103 expression is required for destruction of pancreatic islet allografts by CD8(+) T cells. J Exp Med 196, 877-86 (2002)
21. Cobbold, S. P., Martin, G. & Waldmann, H. The induction of skin graft tolerance in major histocompatibility complex-mismatched or primed recipients: primed T cells can be tolerized in the periphery with anti-CD4 and anti-CD8 antibodies. Eur J Immunol 20, 2747-55 (1990)
1. Banchereau, J. & Steinman, R. M. Dendritic cells and the control of immunity. Nature 392, 245-52 (1998)
2. Caux, C. et al. CD34+ hematopoietic progenitors from human cord blood differentiate along two independent dendritic cell pathways in response to GM-CSF+TNF alpha. J Exp Med 184, 695-706 (1996)
3. Zamoyska, R. The CD8 coreceptor revisited: one chain good, two chains better. Immunity 1, 243-6 (1994)
4. Veillette, A., Bookman, M. A., Horak, E. M. & Bolen, J. B. The CD4 and CD8 T cell surface antigens are associated with the internal membrane tyrosine-protein kinase p56lck. Cell 55, 301-8 (1988)
5. Chalupny, N. J., Ledbetter, J. A. & Kavathas, P. Association of CD8 with p56lck is required for early T cell signalling events. Embo J 10, 1201-7 (1991)
6. Bachmann, M. F. et al. Developmental regulation of Lck targeting to the CD8 coreceptor controls signaling in naive and memory T cells. J Exp Med 189, 1521-30 (1999)
7. Tewari, K., Walent, J., Svaren, J., Zamoyska, R. & Suresh, M. Differential requirement for Lck during primary and memory CD8+ T cell responses. Proc Natl Acad Sci U S A 103, 16388-93 (2006)
8. Fung-Leung, W. P. et al. The lack of CD8 alpha cytoplasmic domain resulted in a dramatic decrease in efficiency in thymic maturation but only a moderate reduction in cytotoxic function of CD8+ T lymphocytes. Eur J Immunol 23, 2834-40 (1993)
9. Nakayama, K. et al. Requirement for CD8 beta chain in positive selection of CD8-lineage T cells. Science 263, 1131-3 (1994)
10. de la Calle-Martin, O. et al. Familial CD8 deficiency due to a mutation in the CD8 alpha gene. J Clin Invest 108, 117-23 (2001)
11. Hall, B. M. Cells mediating allograft rejection. Transplantation 51, 1141-51 (1991)
12. Rosenberg, A. S. & Singer, A. Cellular basis of skin allograft rejection: an in vivo model of immune-mediated tissue destruction. Annu Rev Immunol 10, 333-58 (1992)
13. Slavik, J. M., Lim, D. G., Burakoff, S. J. & Hafler, D. A. Rapamycin-resistant proliferation of CD8+ T cells correlates with p27kip1 down-regulation and bcl-xL induction, and is prevented by an inhibitor of phosphoinositide 3-kinase activity. J Biol Chem 279, 910-9 (2004)
14. Boleslawski, E. et al. Defective inhibition of peripheral CD8+ T cell IL-2 production by anti-calcineurin drugs during acute liver allograft rejection. Transplantation 77, 1815-20 (2004)
15. Jones, N. D. et al. CD40-CD40 ligand-independent activation of CD8+ T cells can trigger allograft rejection. J Immunol 165, 1111-8 (2000)
16. Guo, Z. et al. CD8 T cell-mediated rejection of intestinal allografts is resistant to inhibition of the CD40/CD154 costimulatory pathway. Transplantation 71, 1351-4 (2001)
17. Newell, K. A. et al. Cutting edge: blockade of the CD28/B7 costimulatory pathway inhibits intestinal allograft rejection mediated by CD4+ but not CD8+ T cells. J Immunol 163, 2358-62 (1999)
18. Zhai, Y., Meng, L., Gao, F., Busuttil, R. W. & Kupiec-Weglinski, J. W. Allograft rejection by primed/memory CD8+ T cells is CD154 blockade resistant: therapeutic implications for sensitized transplant recipients. J Immunol 169, 4667-73 (2002)
19. Hadley, G. A., Bartlett, S. T., Via, C. S., Rostapshova, E. A. & Moainie, S. The epithelial cell-specific integrin, CD103 (alpha E integrin), defines a novel subset of alloreactive CD8+ CTL. J Immunol 159, 3748-56 (1997)
20. Feng, Y. et al. CD103 expression is required for destruction of pancreatic islet allografts by CD8(+) T cells. J Exp Med 196, 877-86 (2002)
21. Cobbold, S. P., Martin, G. & Waldmann, H. The induction of skin graft tolerance in major histocompatibility complex-mismatched or primed recipients: primed T cells can be tolerized in the periphery with anti-CD4 and anti-CD8 antibodies. Eur J Immunol 20, 2747-55 (1990)
Claims (33)
- 必要とする対象において寛容を誘導する方法であって、
単離T細胞を、抗原を用いるT細胞プライミングの間に寛容原性T細胞を誘導するのに有効な量の非枯渇性抗CD8抗体と接触させるステップと、
必要とするか又は寛容にある対象に、前記寛容原性T細胞を提供するステップと
を含む方法。 - 抗CD8抗体がヒト化されている、請求項1に記載の方法。
- 抗CD8抗体が非枯渇性である、請求項1に記載の方法。
- サプレッサーT細胞の生成が、1又は複数の以下の表現型:グランザイムAの減少、グランザイムBの減少、パーフォリンの減少、IL−2、IFN−γ若しくはこれら両方の分泌量の減少、IL−10の分泌又はそれらの組合せを決定することにより決定される、請求項1に記載の方法。
- サプレッサーT細胞の生成が、IL−10を分泌するサプレッサーT細胞の増殖である、請求項1に記載の方法。
- 抗CD8抗体が、cM−T807、T8、RPA−T8、HIT8a、Leu2、T8及びOKT8から選択される、請求項1に記載の方法。
- 抗原が同種である、請求項1に記載の方法。
- 移植患者における移植拒絶を、その他の免疫応答を維持しながら低減する方法であって、
単離CD8+T細胞を、抗原を用いるプライミングの間にサプレッサーCD8+T細胞の生成を引き起こすのに有効な量の抗CD8非枯渇性遮断抗体で処理するステップであって、T細胞の抑制が、1又は複数の以下の表現型:グランザイムAの減少、グランザイムBの減少、パーフォリンの減少、IL−2、IFN−γ若しくはこれら両方の分泌量の減少、IL−10の分泌又はそれらの組合せを特徴とするステップと、
前記サプレッサーCD8+T細胞を、移植患者に導入するステップと
を含む方法。 - CD8+T細胞が、GM−CSF及びIFN−α−2bと培養した単球から得られる単離樹状細胞(IFN−DC)とインキュベートされる、請求項8に記載の方法。
- 樹状細胞が、CD34+ヒト末梢細胞を、GM−CSF、Flt3−L及びTNFαと9〜10日間培養することによりインビトロで生成されたランゲルハンス細胞(LC)である、請求項9に記載の方法。
- 樹状細胞が、CD1a+CD14−ランゲルハンス細胞である、請求項9に記載の方法。
- 抗CD8抗体が、ウイルスに対する免疫応答に影響することなく、生着された器官に対する免疫応答を下方制御する、請求項8に記載の方法。
- 抗CD8抗体で処理されたCD8+T細胞が、高結合活性の抗原特異的ナイーブT細胞である、請求項8に記載の方法。
- 抗CD8抗体が、cM−T807、T8、RPA−T8、HIT8a、Leu2、T8及びOKT8から選択される、請求項8に記載の方法。
- 抗CD8抗体が、0.5〜5,000ng/mlで培養物中に提供される、請求項8に記載の方法。
- 末梢血単核細胞を単離するステップと、LC前駆体を前記末梢血単核細胞から単離するステップと、前記LC前駆体をGM−CSF、Flt3−L及びTNFαと培養してLCを作製するステップと、T細胞を末梢血単核細胞から単離し、前記LCと前記T細胞とを、抗CD8抗体の存在下で、サプレッサーT細胞が生成される条件下で共培養するステップと、前記T細胞、前記LC又はその両方を、移植の前、移植と同時又は移植の後に患者に再導入するステップとをさらに含む、請求項8に記載の方法。
- 移植患者から末梢血単核細胞を単離するステップと、LCを単離し、前記LCをGM−CSF、Flt3−L及びTNFαと培養するステップと、T細胞を移植患者から単離し、前記LCと前記T細胞とを、抗CD8抗体の存在下で共培養してサプレッサーT細胞を生成するステップと、前記T細胞、前記LCS又はその両方を、移植の前、移植と同時又は移植の後に患者に再導入するステップとをさらに含む、請求項8に記載の方法。
- サプレッサーCD8+T細胞が、2型サイトカイン(IL−4、IL−5及びIL−13)及びIL−10の増加した発現を有する、請求項8に記載の方法。
- サプレッサーT細胞を作製する方法であって、
末梢血単核細胞を単離するステップと、ランゲルハンス細胞(LC)前駆体を前記末梢血単核細胞から単離するステップと、前記LC前駆体を、GM−CSF、Flt3−L及びTNFαと培養してLCを作製するステップと、T細胞を末梢血単核細胞から単離し、前記LCと前記T細胞とを、抗CD8抗体の存在下で、サプレッサーT細胞が生成される条件下で共培養するステップとを含む方法。 - 抗CD8抗体が、ウイルスに対する免疫応答に影響することなく、生着された器官に対する免疫応答を下方制御する、請求項19に記載の方法。
- CD8+T細胞が、高結合活性の抗原特異的ナイーブT細胞である、請求項19に記載の方法。
- ランゲルハンス細胞が、CD1a+CD14−ランゲルハンス細胞である、請求項19に記載の方法。
- CD1a+CD14−ランゲルハンス細胞が、細胞選別により得られる、請求項19に記載の方法。
- ランゲルハンス細胞が、CD34+HPCをGM−CSF、Flt3−L及びTNFαと9〜10日間培養することによりインビトロで生成される、請求項19に記載の方法。
- 抗CD8抗体が、cM−T807、T8、RPA−T8、HIT8a、Leu2、T8及びOKT8から選択される、請求項19に記載の方法。
- 抗CD8抗体が、0.5〜5,000ng/mlで培養物中に提供される、請求項19に記載の方法。
- サプレッサーT細胞を作製する方法であって、
末梢血単核細胞を単離するステップと、単球を前記末梢血単核細胞から単離するステップと、前記単球を、GM−CSF及びIFN−α−2bと培養して(IFN−DC)を作製するステップと、T細胞を末梢血単核細胞から単離し、前記IFN−DCと前記T細胞とを、抗CD8抗体の存在下で、グランザイムAの減少、グランザイムBの減少、パーフォリンの減少、IL−2、IFN−γ若しくはこれら両方の分泌量の減少、IL−10の分泌又はそれらの組合せにより測定されるサプレッサーT細胞が生成される条件下で共培養するステップとを含む方法。 - 免疫応答に影響を及ぼすための方法であって、末梢血単核細胞を単離し、LC前駆体を前記末梢血単核細胞から単離し、前記LC前駆体をGM−CSF、Flt3−L及びTNFαと培養してLCを作製し、T細胞を末梢血単核細胞から単離し、前記LCと前記T細胞とを、抗CD8抗体の存在下で、サプレッサーT細胞が生成される条件下で共培養することにより作製されたサプレッサーT細胞を含む組成物を投与するステップを含む方法。
- 哺乳動物における移植された組織の拒絶を阻害する方法であって、末梢血単核細胞を単離するステップと、LC前駆体を前記末梢血単核細胞から単離するステップと、前記LC前駆体をGM−CSF、Flt3−L及びTNFαと培養してLCを作製するステップと、T細胞を末梢血単核細胞から単離し、前記LCと前記T細胞とを、抗CD8抗体の存在下で、サプレッサーT細胞が生成される条件下で共培養するステップとを含む方法により作製されたサプレッサーT細胞を導入するステップを含む方法。
- 移植拒絶を低減する組成物であって、その他の免疫応答を消失させることなく移植拒絶を低減するのに十分な有効量のサプレッサーT細胞を含み、前記サプレッサーT細胞が、抗CD8抗体の存在下で、サプレッサーT細胞が生成される条件下で成熟LCと共培養された単離末梢血T細胞から生成される組成物。
- 抗CD8抗体が、cM−T807、T8、RPA−T8、HIT8a、Leu2、T8及びOKT8から選択される、請求項30に記載の組成物。
- 抗CD8抗体が、0.5〜5,000ng/mlで培養物中に提供される、請求項30に記載の組成物。
- 細胞が、凍結しており、使用前に注射用の媒体に再懸濁される、請求項30に記載の組成物。
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US5964708P | 2008-06-06 | 2008-06-06 | |
| US61/059,647 | 2008-06-06 | ||
| PCT/US2009/046464 WO2009149382A2 (en) | 2008-06-06 | 2009-06-05 | Anti-cd8 antibodies block priming of cytotoxic effectors and lead to generation of regulatory cd8+t cells |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2011522835A true JP2011522835A (ja) | 2011-08-04 |
| JP2011522835A5 JP2011522835A5 (ja) | 2012-07-19 |
Family
ID=41398905
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2011512705A Pending JP2011522835A (ja) | 2008-06-06 | 2009-06-05 | 抗cd8抗体は、細胞傷害性エフェクターのプライミングを遮断し、制御性cd8+t細胞の生成を導く |
Country Status (14)
| Country | Link |
|---|---|
| US (1) | US20090304659A1 (ja) |
| EP (1) | EP2297204A4 (ja) |
| JP (1) | JP2011522835A (ja) |
| KR (1) | KR20110025812A (ja) |
| CN (1) | CN102112491A (ja) |
| AU (1) | AU2009255999A1 (ja) |
| BR (1) | BRPI0915582A2 (ja) |
| CA (1) | CA2728772A1 (ja) |
| IL (1) | IL209798A0 (ja) |
| MX (1) | MX2010013265A (ja) |
| NZ (1) | NZ590197A (ja) |
| TW (1) | TW201000130A (ja) |
| WO (1) | WO2009149382A2 (ja) |
| ZA (1) | ZA201100061B (ja) |
Cited By (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2013081428A (ja) * | 2011-10-11 | 2013-05-09 | Biotherapy Institute Of Japan | Cd56陽性t細胞増強方法 |
| WO2020250940A1 (ja) | 2019-06-11 | 2020-12-17 | 小野薬品工業株式会社 | 免疫抑制剤 |
Families Citing this family (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US10092597B2 (en) | 2014-01-14 | 2018-10-09 | The University Of Hong Kong | Human CD8+ regulatory T cells inhibit GVHD and preserve general immunity in humanized mice |
| WO2018085897A1 (en) * | 2016-11-14 | 2018-05-17 | Murdoch Childrens Research Institute | Transplant rejection assay |
| US10730944B2 (en) * | 2017-07-24 | 2020-08-04 | Regeneron Pharmaceuticals, Inc. | Anti-CD8 antibodies and uses thereof |
| EP4186925A1 (en) * | 2020-07-21 | 2023-05-31 | Suzhou Smartnuclide Biopharmaceutical Co., Ltd. | Cd8 binding polypeptide and use thereof |
| CN112156110B (zh) * | 2020-09-15 | 2022-10-14 | 上海交通大学医学院 | Cd8+抑制性t细胞在免疫调节中的应用及诱导方法 |
Citations (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPH04503405A (ja) * | 1988-12-16 | 1992-06-18 | クールター エレクトロニクス インコーポレイテッド | 選択された特性を現わす集団についての細胞または形成体をスクリーニングする方法および装置 |
| WO2004112835A2 (en) * | 2003-06-20 | 2004-12-29 | Isis Innovation Ltd | Suppression of transplant rejection |
| JP2006500932A (ja) * | 2002-09-27 | 2006-01-12 | バイオイー, インコーポレイテッド | 細胞分離組成物および細胞分離法 |
| WO2008005859A2 (en) * | 2006-06-30 | 2008-01-10 | Baylor Research Institute | Dendritic cells generated using gm-csf and interferon alpha and loaded with heat-treated and killed cancer cells |
Family Cites Families (13)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US5178858A (en) * | 1987-12-02 | 1993-01-12 | Reichert Thomas A | Method for prevention of graft versus host disease |
| US5601828A (en) * | 1989-03-15 | 1997-02-11 | Tkb Associates Limited Partnership | CD8 derivatives and methods of use for cellular modulation and enhancement of cellular engraftment |
| GB8912497D0 (en) * | 1989-05-31 | 1989-07-19 | Cobbold Stephen P | Monoclonal antibodies |
| US5690933A (en) * | 1989-05-31 | 1997-11-25 | Glaxo Wellcome Inc. | Monoclonal antibodies for inducing tolerance |
| AU660003B2 (en) * | 1990-11-23 | 1995-06-08 | Coulter International Corporation | Method and apparatus for screening microscopic cells utilizing light scatter techniques |
| US6911220B1 (en) * | 1992-02-19 | 2005-06-28 | The General Hospital Corporation | Allogeneic and xenogeneic transplantation |
| US5876708A (en) * | 1992-02-19 | 1999-03-02 | The General Hospital Corporation | Allogeneic and xenogeneic transplantation |
| ATE432339T1 (de) * | 1996-04-05 | 2009-06-15 | Univ South Alabama | Verwendung von onkofötal-antigen spezifischen cd4,cd8 zytotoxischen, suppressor t-zellen und interleukin-10 |
| WO1998037917A1 (en) * | 1997-02-28 | 1998-09-03 | Enzo Therapeutics, Inc., A Fully Owned Subsidiary Of Enzo Biochem, Inc. | Novel processes implementing selective immune down regulation (sidr) |
| US6803036B1 (en) * | 1998-03-03 | 2004-10-12 | University Of Southern California | Use of cytokines, cells and mitogens to inhibit graft versus host disease |
| US20040022761A1 (en) * | 2001-05-11 | 2004-02-05 | Banchereau Jacques F | Compositions and methods for producing antigen-presenting cells |
| WO2004083404A2 (en) * | 2003-03-19 | 2004-09-30 | Isogenis, Inc. | Gene therapy vectors having reduced immunogenicity based on cd8 alpha-chain |
| EP1674479A1 (en) * | 2004-12-22 | 2006-06-28 | Memorial Sloan-Kettering Cancer Center | Modulation of Fc Gamma receptors for optimizing immunotherapy |
-
2009
- 2009-06-05 EP EP09759540.9A patent/EP2297204A4/en not_active Withdrawn
- 2009-06-05 WO PCT/US2009/046464 patent/WO2009149382A2/en active Application Filing
- 2009-06-05 US US12/479,349 patent/US20090304659A1/en not_active Abandoned
- 2009-06-05 MX MX2010013265A patent/MX2010013265A/es active IP Right Grant
- 2009-06-05 KR KR1020117000123A patent/KR20110025812A/ko not_active Application Discontinuation
- 2009-06-05 BR BRPI0915582A patent/BRPI0915582A2/pt not_active IP Right Cessation
- 2009-06-05 CN CN2009801301198A patent/CN102112491A/zh active Pending
- 2009-06-05 CA CA2728772A patent/CA2728772A1/en not_active Abandoned
- 2009-06-05 JP JP2011512705A patent/JP2011522835A/ja active Pending
- 2009-06-05 NZ NZ590197A patent/NZ590197A/xx not_active IP Right Cessation
- 2009-06-05 AU AU2009255999A patent/AU2009255999A1/en not_active Abandoned
- 2009-06-06 TW TW098118952A patent/TW201000130A/zh unknown
-
2010
- 2010-12-06 IL IL209798A patent/IL209798A0/en unknown
-
2011
- 2011-01-03 ZA ZA2011/00061A patent/ZA201100061B/en unknown
Patent Citations (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPH04503405A (ja) * | 1988-12-16 | 1992-06-18 | クールター エレクトロニクス インコーポレイテッド | 選択された特性を現わす集団についての細胞または形成体をスクリーニングする方法および装置 |
| JP2006500932A (ja) * | 2002-09-27 | 2006-01-12 | バイオイー, インコーポレイテッド | 細胞分離組成物および細胞分離法 |
| WO2004112835A2 (en) * | 2003-06-20 | 2004-12-29 | Isis Innovation Ltd | Suppression of transplant rejection |
| WO2008005859A2 (en) * | 2006-06-30 | 2008-01-10 | Baylor Research Institute | Dendritic cells generated using gm-csf and interferon alpha and loaded with heat-treated and killed cancer cells |
Non-Patent Citations (3)
| Title |
|---|
| JPN6013057688; 病理と臨床 第24巻,第5号, 2006, p.473-479 * |
| JPN6013057690; 実験医学 第18巻,第15号, 2000, p.2116-2122 * |
| JPN6013057691; American Journal of Transplantation Vol.7, No.5, 2007, p.1055-1061 * |
Cited By (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2013081428A (ja) * | 2011-10-11 | 2013-05-09 | Biotherapy Institute Of Japan | Cd56陽性t細胞増強方法 |
| WO2020250940A1 (ja) | 2019-06-11 | 2020-12-17 | 小野薬品工業株式会社 | 免疫抑制剤 |
Also Published As
| Publication number | Publication date |
|---|---|
| AU2009255999A1 (en) | 2009-12-10 |
| TW201000130A (en) | 2010-01-01 |
| WO2009149382A3 (en) | 2010-04-29 |
| NZ590197A (en) | 2012-10-26 |
| MX2010013265A (es) | 2011-02-24 |
| BRPI0915582A2 (pt) | 2016-01-26 |
| EP2297204A4 (en) | 2013-10-23 |
| KR20110025812A (ko) | 2011-03-11 |
| ZA201100061B (en) | 2011-10-26 |
| WO2009149382A2 (en) | 2009-12-10 |
| CA2728772A1 (en) | 2009-12-10 |
| CN102112491A (zh) | 2011-06-29 |
| US20090304659A1 (en) | 2009-12-10 |
| EP2297204A2 (en) | 2011-03-23 |
| IL209798A0 (en) | 2011-02-28 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| Pêche et al. | Prolongation of heart allograft survival by immature dendritic cells generated from recipient type bone marrow progenitors | |
| EP1730260B1 (en) | Regulatory t cells and their use in immunotherapy and suppression of autoimmune responses | |
| EP3842450A1 (en) | Antibody/t-cell receptor chimeric constructs and uses thereof | |
| JP2019047814A (ja) | B細胞の増加及び評価方法並びに疾患治療のための増加b細胞の使用方法 | |
| CA2413866C (en) | Compositions and methods of monoclonal and polyclonal antibodies specific for t cell subpopulations | |
| EP2399594B1 (en) | Tumour cell-activated Natural Killer cells | |
| US9885016B2 (en) | Compositions and methods for modulating an immune response | |
| US9580684B2 (en) | Methods and compositions for the generation and maintenance of regulatory T cells | |
| US20210147800A1 (en) | Methods for producing regulatory immune cells and uses thereof | |
| JP2011522835A (ja) | 抗cd8抗体は、細胞傷害性エフェクターのプライミングを遮断し、制御性cd8+t細胞の生成を導く | |
| US20090232854A1 (en) | Uses of bispecific antibody coated dendritic cells pulsed with antigens and gm-csf in immune regulation | |
| AU2019310855A2 (en) | Method for treating tumor using immune effector cell | |
| JP2022526856A (ja) | 臨床的に意義のあるegfr変異型タンパク質との交差反応性を有する高親和性キメラ抗原受容体(car)を含む、組成物および方法 | |
| US20150110738A1 (en) | Methods and compositions for generating and using allogeneic suppressor cells | |
| Hartwig et al. | Depletion of alloreactive donor T lymphocytes by CD95-mediated activation-induced cell death retains antileukemic, antiviral, and immunoregulatory T cell immunity | |
| Naderi et al. | High expression of Fas ligand on cord blood dendritic cells: a possible immunoregulatory mechanism after cord blood transplantation | |
| JP2022529947A (ja) | ドナーアポトーシス白血球が誘導する移植免疫寛容のバイオマーカー | |
| Katsumata et al. | Evaluation of the impact of conventional immunosuppressant on the establishment of murine transplantation tolerance–an experimental study | |
| Wekerle | DPPIV inhibition in a murine model of mixed chimerism and transplantation tolerance | |
| SNG | The Role of MHCI Quality and Quantity in Determining CD8 T cell Development, Survival and Function | |
| Jaeckel et al. | Human Donor-Specific Tregs Can Prevent Allograft Rejection in Humanized Immune Reconstituted Mice.: Abstract# 743 | |
| Shiao | Memory T cells and the endothelium in allograft rejection | |
| Prasad | Studies of immune biology of the common marmoset: a novel non-human primate transplant model. | |
| FOWLER et al. | National Institutes of Health, Bethesda, Maryland, USA | |
| Bézie et al. | Advances on CD8 Tregs and their potential in transplantation |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20120531 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20120531 |
|
| A02 | Decision of refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A02 Effective date: 20140421 |