JP2011154031A - 放射線検査装置 - Google Patents
放射線検査装置 Download PDFInfo
- Publication number
- JP2011154031A JP2011154031A JP2011048482A JP2011048482A JP2011154031A JP 2011154031 A JP2011154031 A JP 2011154031A JP 2011048482 A JP2011048482 A JP 2011048482A JP 2011048482 A JP2011048482 A JP 2011048482A JP 2011154031 A JP2011154031 A JP 2011154031A
- Authority
- JP
- Japan
- Prior art keywords
- radiation
- ray
- radiation detector
- rays
- image
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
- 230000005855 radiation Effects 0.000 title claims abstract description 515
- 238000007689 inspection Methods 0.000 title claims abstract description 98
- 238000001514 detection method Methods 0.000 claims abstract description 134
- 238000012937 correction Methods 0.000 claims abstract description 39
- 238000000034 method Methods 0.000 claims abstract description 34
- 238000012545 processing Methods 0.000 claims description 51
- 238000002603 single-photon emission computed tomography Methods 0.000 claims description 38
- 239000004065 semiconductor Substances 0.000 claims description 10
- 238000001727 in vivo Methods 0.000 claims description 6
- 230000008569 process Effects 0.000 abstract description 5
- 230000005251 gamma ray Effects 0.000 description 130
- 238000003384 imaging method Methods 0.000 description 129
- 238000012636 positron electron tomography Methods 0.000 description 79
- 238000003860 storage Methods 0.000 description 35
- 229940079593 drug Drugs 0.000 description 30
- 239000003814 drug Substances 0.000 description 30
- 230000005540 biological transmission Effects 0.000 description 29
- 230000006866 deterioration Effects 0.000 description 20
- 238000005259 measurement Methods 0.000 description 17
- 239000000463 material Substances 0.000 description 11
- 230000002238 attenuated effect Effects 0.000 description 9
- 239000000126 substance Substances 0.000 description 8
- 238000010586 diagram Methods 0.000 description 7
- 206010028980 Neoplasm Diseases 0.000 description 6
- 210000000988 bone and bone Anatomy 0.000 description 6
- RPPBZEBXAAZZJH-UHFFFAOYSA-N cadmium telluride Chemical compound [Te]=[Cd] RPPBZEBXAAZZJH-UHFFFAOYSA-N 0.000 description 6
- 230000000694 effects Effects 0.000 description 6
- 201000011510 cancer Diseases 0.000 description 5
- 230000008054 signal transmission Effects 0.000 description 5
- 210000001835 viscera Anatomy 0.000 description 5
- 230000007423 decrease Effects 0.000 description 4
- 239000000203 mixture Substances 0.000 description 4
- 230000009467 reduction Effects 0.000 description 4
- 230000035945 sensitivity Effects 0.000 description 4
- 238000001228 spectrum Methods 0.000 description 4
- 238000012360 testing method Methods 0.000 description 4
- 238000004364 calculation method Methods 0.000 description 3
- 238000002059 diagnostic imaging Methods 0.000 description 3
- 238000005516 engineering process Methods 0.000 description 3
- 230000007246 mechanism Effects 0.000 description 3
- 238000007493 shaping process Methods 0.000 description 3
- 238000010521 absorption reaction Methods 0.000 description 2
- 230000009471 action Effects 0.000 description 2
- 239000002131 composite material Substances 0.000 description 2
- 238000002591 computed tomography Methods 0.000 description 2
- 239000013078 crystal Substances 0.000 description 2
- 238000002347 injection Methods 0.000 description 2
- 239000007924 injection Substances 0.000 description 2
- 230000001678 irradiating effect Effects 0.000 description 2
- 238000002360 preparation method Methods 0.000 description 2
- 229940121896 radiopharmaceutical Drugs 0.000 description 2
- 239000012217 radiopharmaceutical Substances 0.000 description 2
- 230000002799 radiopharmaceutical effect Effects 0.000 description 2
- 238000004904 shortening Methods 0.000 description 2
- 239000007787 solid Substances 0.000 description 2
- 238000002834 transmittance Methods 0.000 description 2
- 229910052721 tungsten Inorganic materials 0.000 description 2
- JBRZTFJDHDCESZ-UHFFFAOYSA-N AsGa Chemical compound [As]#[Ga] JBRZTFJDHDCESZ-UHFFFAOYSA-N 0.000 description 1
- 230000008901 benefit Effects 0.000 description 1
- 230000015572 biosynthetic process Effects 0.000 description 1
- 229910052792 caesium Inorganic materials 0.000 description 1
- TVFDJXOCXUVLDH-UHFFFAOYSA-N caesium atom Chemical compound [Cs] TVFDJXOCXUVLDH-UHFFFAOYSA-N 0.000 description 1
- 230000015556 catabolic process Effects 0.000 description 1
- 238000007796 conventional method Methods 0.000 description 1
- 238000006731 degradation reaction Methods 0.000 description 1
- 238000009826 distribution Methods 0.000 description 1
- 230000006872 improvement Effects 0.000 description 1
- 230000003902 lesion Effects 0.000 description 1
- 230000004060 metabolic process Effects 0.000 description 1
- 229910052750 molybdenum Inorganic materials 0.000 description 1
- 238000012831 peritoneal equilibrium test Methods 0.000 description 1
- 238000012877 positron emission topography Methods 0.000 description 1
- 230000002285 radioactive effect Effects 0.000 description 1
- 238000004088 simulation Methods 0.000 description 1
- 238000003786 synthesis reaction Methods 0.000 description 1
- 230000002194 synthesizing effect Effects 0.000 description 1
- 230000002123 temporal effect Effects 0.000 description 1
- WFKWXMTUELFFGS-UHFFFAOYSA-N tungsten Chemical compound [W] WFKWXMTUELFFGS-UHFFFAOYSA-N 0.000 description 1
- 239000010937 tungsten Substances 0.000 description 1
- 230000009278 visceral effect Effects 0.000 description 1
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 1
- 238000004846 x-ray emission Methods 0.000 description 1
- 229910052725 zinc Inorganic materials 0.000 description 1
- 239000011701 zinc Substances 0.000 description 1
Images
Landscapes
- Measurement Of Radiation (AREA)
- Apparatus For Radiation Diagnosis (AREA)
- Nuclear Medicine (AREA)
Abstract
【課題】放射線のより正確な到達位置を把握し、作成される画像の精度を向上する。
【解決手段】被検体からの放射線を検出する複数の放射線検出器と、前記一つの放射線検出器に接続され、前記複数の放射線検出器によって検出された複数の放射線検出信号を処理する信号処理装置と、別に設置されたX線CT装置からのX線の検出信号の減衰率を用いて、PET像又はSPECT像に対して放射線が被検体の体内で散乱する現象の補正である体内減衰補正を行い、PET像又はSPECT像の画像再構成を行うコンピュータとを有することを特徴とする放射線検査装置。
【選択図】 図5
【解決手段】被検体からの放射線を検出する複数の放射線検出器と、前記一つの放射線検出器に接続され、前記複数の放射線検出器によって検出された複数の放射線検出信号を処理する信号処理装置と、別に設置されたX線CT装置からのX線の検出信号の減衰率を用いて、PET像又はSPECT像に対して放射線が被検体の体内で散乱する現象の補正である体内減衰補正を行い、PET像又はSPECT像の画像再構成を行うコンピュータとを有することを特徴とする放射線検査装置。
【選択図】 図5
Description
本発明は、放射線検査装置に係り、特にX線CT,陽電子放出型CT(ポジトロン・エミッション・コンピューテッド・トモグラフィ(Positron Emission Computed Tomography)、以下、PETという),単光子放出型CT(シングル・フォトン・エミッション・コンピューテッド・トモグラフィ(Single Photon Emission Computed Tomography))、以下、SPECTという)、及びデジタルX線検査に用いるフラットパネルディテクタ等に適用するのに好適な放射線検査装置に関するものである。
被検体である被検診者の体内の機能,形態を無侵襲で撮像する技術として、放射線を用いた検査がある。放射線検査装置の代表的なものとして、X線CT,デジタルX線検査,PET及びSPECTがある。
PET検査は、放射性核種である陽電子放出核種(15O,13N,11C,18F等)を含む放射性薬剤(PET用薬剤という)を被検診者に投与し、PET用薬剤が体内のどの部位で多く消費されているかを調べる検査、すなわちPET用薬剤に起因して被検診者の体内から放射されるγ線を放射線検出器で検出する行為である。PET用薬剤に含まれた放射性核種から放出された陽電子が、付近の細胞(癌細胞)の電子と結合して陽電子消滅し511keVのエネルギーを持つ、一対のγ線(対γ線という)を放射する。それらのγ線は、互いにほぼ正反対の方向(180°±0.6°)に放射されるので、この対γ線を放射線検出器で検知すれば、どの2つの放射線検出器の間で陽電子が放出されたかがわかる。それらの多数のγ線対を検知することで、PET用薬剤を多く消費する場所がわかる。そして、例えば陽電子放出核種と糖を結合して製造されたPET用薬剤を用いた場合、糖代謝の激しい癌病巣を発見することが可能である。なお、得られたデータは、アイトリプルイー トランザクション オン ニュークリア サイエンス(IEEE Transaction on Nuclear Science)NS−21巻の21頁に記載されているフィルタードバックプロジェクション法(Filtered Back Projection Method )により、各ボクセルのデータに変換する。PET検査に用いられる陽電子放出核種(15O,13N、11C、18F等)の半減期は、2分から110分である。
PET検査では、陽電子消滅の際に発生するγ線が体内で減衰するため、トランスミッションデータを撮影しγ線の体内減衰を補正する。トランスミッションデータ撮影とは、例えば放射線源にセシウムを用いてγ線を入射させ、被検体内を透過した強度を測定することにより被検体内におけるγ線の減衰率を測定する方法である。得られたγ線減衰率を用いて被検体内部でのγ線減衰率を見積もりPET検査で得られたデータを補正することにより、より高精度なPET像を得ることが可能である。
現在、PET検査の精度を向上させる方法の一つとして、メディカル イメージング テクノロジー(MEDICAL IMAGING TECHNOLOGY)第18巻 第1号の15ページに有るように、反射板をクリスタル中に挿入し、深さ位置を検出するDOI(Depth−Of−Interaction)検出器を用いることで深さ位置情報取得し、それを用いて画像を再構成し、画質を向上させる方法がある。この方法を使うためには放射線検出器の奥行き方向の位置情報も知ることのできる放射線検出器を用いる必要がある。
しかし、DOI検出器の問題として、信号伝達物質減少に起因する画像劣化がある。例えば5mm角のBGOシンチレータを用いた場合、信号伝達物質である光子は511keV
のγ線が1つ入射した場合約200個発生する。しかし、上記のDOI検出器のように、反射材により一部の光子を反射させた場合、信号伝達物質が減少する。光電子増倍管に到達する信号伝達物質数をN、入射γ線のエネルギーをEとしたとき、エネルギースペクトルの広がりσは、(1)式で表される。このためNが小さくなるとσが増大し、エネルギ
のγ線が1つ入射した場合約200個発生する。しかし、上記のDOI検出器のように、反射材により一部の光子を反射させた場合、信号伝達物質が減少する。光電子増倍管に到達する信号伝達物質数をN、入射γ線のエネルギーをEとしたとき、エネルギースペクトルの広がりσは、(1)式で表される。このためNが小さくなるとσが増大し、エネルギ
ースペクトルが広がる。エネルギースペクトルが広がった場合には、入射γ線のエネルギーと、DOI検出器で発生する信号との間の相関が悪くなる。その結果、入射γ線のエネルギーを正確に測ることが難しくなる。
入射γ線のエネルギーを正確に測れない場合、入射γ線の中に含まれる散乱線を除去することが困難になる。PETでは散乱線を除去するために放射線検出器から出力された信号をエネルギーフィルターをかけて、あるエネルギー以上のγ線のみを検知する。しかし、エネルギースペクトルが広がった場合、例えば511keVのγ線が放射線検出器から出力する信号と、300keVのγ線が放射線検出器から出力する信号とを区別できない場合、エネルギーフィルターは300keV以下にする必要がある。この場合、300keV以上の散乱線も同時に計測するため、ノイズが増大する。これはPET画像劣化の要因となる。
SPECTは、放射性核種であるシングルフォトン放出核種(99Tc,67Ga,201Tl等)、及び特定の腫瘍または特定の分子に集積する性質を有する物質(例えば糖)を含む放射性薬剤(SPECT用薬剤という)を被検診者に投与し、放射性核種から放出されるγ線を放射線検出器で検出する。SPECTによる検査時によく用いられるシングルフォトン放出核種から放出されるγ線のエネルギーは数100keV前後である。SPECTの場合、単一γ線が放出されるため、放射線検出器に入射したγ線の角度が得られない。そこで、コリメータを用いて特定の角度から入射するγ線のみを放射線検出器で検出することにより角度情報を得ている。SPECTは、SPECT用薬剤に起因して体内で発生するγ線を検知してSPECT用薬剤を多く消費する場所を特定する検査方法である。
SPECTの場合も、得られたデータはフィルタードバックプロジェクションなどの方法により各ボクセルのデータに変換する。なお、SPECTでもトランスミッション像を撮影することがある。SPECTに用いる99Tc,67Ga,201Tlは、PET用の放射性核種の半減期よりも長く6時間から3日である。
SPECTの場合も、得られたデータはフィルタードバックプロジェクションなどの方法により各ボクセルのデータに変換する。なお、SPECTでもトランスミッション像を撮影することがある。SPECTに用いる99Tc,67Ga,201Tlは、PET用の放射性核種の半減期よりも長く6時間から3日である。
X線CTはX線源から放出された放射線を被検診者に照射し、その被検診者の体内における放射線の透過率から体内の形態を撮像する方法である。放射線検出器で測定した体内を透過したX線の強度を用いて、X線源と放射線検出器との間における体内の線減弱係数を求める。この線減弱係数を用い、前述のフィルタードバックプロジェクション法により各ボクセルの線減弱係数を求め、その値をCT値に変換する。
フラットパネルディテクタは、従来のX線レントゲン検査をデジタル化したデジタルX線検査に用いる平面型放射線検出器である。フラットパネルディテクタ撮影装置は、従来のX線フィルムの替りに、その平面型放射線検出器を備えており、体内を透過したX線を検出して体内減衰情報をデジタル情報として扱い、このデジタル情報をモニタ上に表示する。フラットパネルディテクタ撮影装置は、X線フィルムなどが不要であり、また撮像直後に像を見ることが可能である。
アイトリプルイー トランザクション オン ニュークリア サイエンス(IEEE Transaction on Nuclear Science)NS−21巻の21頁
メディカル イメージング テクノロジー(MEDICAL IMAGING TECHNOLOGY)第18巻 第1号の15ページ
これらの放射線検査装置には、検査の精度を保つため、放射線検出器の検出効率の感度補正を例えば3ヶ月に1回以上行う必要があることである。放射線検出器の検出効率は、時間がたつにつれて劣化するが、その劣化特性は検出器による個体差がある。そのため、定期的に各放射線検出器の検出効率を知る必要がある。PET検査やSPECT検査では各放射線検出器に入射した光子数を計測するため、放射線検出器の検出効率にばらつきがある場合は正しい計測ができない。そのため、予め各放射線検出器の検出効率を知り、その効率の逆数を各放射線検出器に乗じて放射線検出器の検出効率差に伴う画像劣化の補正を行う。一方、X線CT検査やフラットパネルディテクタ検査では、X線の強度を放射線検出器で検出するが、強度の測定に関しても同様に検出効率にばらつきがある場合は補正する必要がある。
このように放射線検査装置には、検査精度を保つために各放射線検出器の検出効率のばらつきを調べなければならないという問題があり、多大な時間と労力を必要としていた。
本発明の目的は、放射線のより正確な到達位置を把握でき、作成される画像の精度を向上できる放射線検査装置を提供することにある。
上記目的を達成する本発明の特徴は、被検体からの放射線を検出する複数の放射線検出器と、前記一つの放射線検出器に接続され、前記複数の放射線検出器によって検出された複数の放射線検出信号を処理する信号処理装置と、別に設置されたX線CT装置からのX線の検出信号の減衰率を用いて、PET像又はSPECT像に対して放射線が被検体の体内で散乱する現象の補正である体内減衰補正を行い、PET像又はSPECT像の画像再構成を行うコンピュータとを有することを特徴とする放射線検査装置である。
本発明によれば、被検体に対向する放射線検出器から奥行き方向において放射線が到達した位置をより正確に確認でき、被検体の体内の状態を示す精度のよい画像が得られる。
以下図面を用いて説明する。
本発明の好適な一実施例である放射線検査装置を、図1及び図2を用いて以下に説明する。本実施例の放射線検査装置1は、PET検査に用いられるものである。放射線検査装置は、撮像装置2,信号処理装置7,断層像作成装置10,被検診者保持装置14,較正線源周方向移動装置37及び駆動装置制御装置35を備える。
撮像装置2は、ケーシング3,多数の放射線検出器4及び放射線検出器支持板5を有している。ケーシング3は、被検体である被検診者が挿入される孔部(貫通孔)6を有する。多数の放射線検出器(例えば合計10000個)4が、孔部6の周囲を取囲んで、かつ孔部6の軸方向に配置される。これらの放射線検出器4のうち最も内側に位置する放射線検出器4は、図2に示すように、孔部6の周囲に環状に配置される。他の放射線検出器4は、最も内側に配置された上記放射線検出器4を基点に孔部6の中心から放射状になるように配置される。放射線検出器4は、孔部6の半径方向において異なる位置にも配置される。すなわち、本実施例は、孔部6の半径方向において三層になるように三個の放射線検出器4(例えば、図2に示す放射線検出器4a,4b,4c)を直線状に配置している。各層の放射線検出器4は、それぞれ環状(例えば、同心円状)に配置される。
放射線検出器4は、図3に示すように、放射線検出器支持板5の側面に取付けられる。すなわち、放射線検出器4は、リングを半分にした形状を有する放射線検出器支持板5の側面に放射状に取付けられる。放射線検出器4が取付けられた複数の放射線検出器支持板5が、孔部6の下方で孔部6の軸方向に配置される。これらの放射線検出器支持板5はケーシング3に固定される。図3は図示していないが、放射線検出器4が取付けられた複数の放射線検出器支持板5は、孔部6より上方でも孔部6の軸方向に配置され、ケーシング3に固定される。孔部6より下方に配置された1つの放射線検出器支持板5は、孔部6より上方に配置された1つの放射線検出器支持板5と共に同一面内でリングを形成するように配置される。放射線検出器支持板5は、環状に形成してもよい。
信号処理装置7は、各放射線検出器4毎に設けられたγ線弁別装置8、及び同時計数装置9を備える。γ線弁別装置8は配線13により対応する放射線検出器4に接続される。γ線弁別装置8は放射線検出器4と同じ数だけ設置される。1つの同時計数装置9は、各γ線弁別装置8に接続される。断層像作成装置10は、コンピュータ11,記憶装置12及び表示装置13を備える。コンピュータ11は同時計数装置9に接続され、記憶装置12はコンピュータ11に接続される。表示装置13はコンピュータ11に接続される。被検診者保持装置14は、支持部材15、及び支持部材15の上端部に位置して長手方向に移動可能に支持部材15に設置されたベッド16を備える。撮像装置2は、ベッド16の長手方向と直行する方向に配置される。
代表的な放射線検出器として、半導体放射線検出器及びシンチレータがある。シンチレータは、放射線検出部であるクリスタル(BGO,NaIなど)の後部に光電子増倍管などを配置する必要があるため、積層配置する場合(例えば、前述の三層)には不向きである。半導体放射線検出器は、光電子増倍管などが不要であるため、積層配置に向いている。本実施例では、放射線検出器4は、半導体放射線検出器を用いており、検出部である5mm立方体をカドミウムテルル(CdTe)で構成している。その検出部はガリウムヒ素(GaAs)またはカドミウムテルル亜鉛(CZT)で構成してもよい。
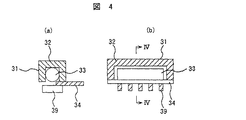
較正線源周方向移動装置37は、ガイドレール28及び較正線源装置29を備える。環状のガイドレール28は、孔部6を取囲むようにケーシングの被検診者保持装置14側の側面に取付けられる。較正線源装置29は較正線源駆動装置30及び較正線源31を有する。較正線源駆動装置30はガイドレール28に移動可能に取付けられる。較正線源駆動装置30は、図示されていないが、ガイドレール28のラックと噛合うピニオンを有し、このピニオンを減速機構を介して回転させるモーターを備える。較正線源31は、較正線源駆動装置30のケーシング(図示せず)に設置されて水平方向に伸縮が可能なアーム38の先端部に取付けられている。較正線源31は、図4に示すように、一方向に開口を有するγ線遮蔽体32内にγ線源33を収納している。躯体となるケーシング(図示せず)が、上記の開口部分を除いてγ線遮蔽体32の外側を覆っている。較正線源31は、γ線遮蔽体32の開口を塞ぐ移動可能なシャッター34を有する。γ線源33には、511keVのγ線を放出するGa−Ge線源を用いる。Ga−Ge線源の替りに662keVのγ線を放出するCs線源を用いてもよい。較正線源31はトランスミッションデータ撮影時に用いられる線源である。γ線遮蔽体32の開口の前面に配置されたコリメータ39が、シャッター34の開閉動作を妨げないようにγ線遮蔽体32に取付けられる。
まず、放射線検査装置1Aを用いたトランスミッションデータ撮影について説明する。トランスミッションデータ撮影は、較正線源を用いて被検診者の体内のγ線透過率を計測する手法である。その計測要する時間は、1〜2分程度かかる。較正線源から放出されたγ線は、被検診者を透過した後、放射線検出器4で計測される。較正線源の放射能強度及び計測されたγ線に基づいて、被検診者の体内でのγ線減衰率を求める。求められたγ線減衰率は、PET検査における体内散乱(放射性薬剤に起因して体内で発生したγ線が体内で散乱,減衰する現象)の補正に用いられる。
トランスミッションデータ撮影を具体的に述べる。被検診者17が横たわっているベッド16が孔部6内に挿入される。トランスミッションデータ撮影を開始するとき、線源制御装置69はシャッター34を開く。γ線源33から放出されたγ線は、γ線遮蔽体32の開口及びコリメータ39を通って被検診者17に照射される。γ線源33からのγ線は、コリメータ39によって指向性が強くなり進行方向が特定される。駆動装置制御装置35は、トランスミッションデータ撮影を開始するとき、駆動開始信号を出力して、較正線源駆動装置30のモーターを回転させる。モーターの回転によって、較正線源駆動装置30はガイドレール28に沿って被検診者17の周囲を移動する。較正線源31は孔部6内で被検診者17の周囲を移動する。このため、較正線源31から放出された高指向性のγ線は、被検診者17に周方向のあらゆる位置から照射される。ベッド16が孔部6の反対側に向かって移動する。被検診者17を透過したそのγ線は放射線検出器4によって計測される。高指向性のγ線が照射されるため、放射線検出器4が計測するγ線は、非散乱のγ線であり、γ線源33より放出された時と同じ511keVのエネルギーを有する。
放射線検出器4は、被検診者17を透過したγ線を計測してγ線撮像信号を出力する。このγ線撮像信号に対して、後述のPET検査時に検出されるγ線撮像信号と同様に、γ線弁別装置8はパルス信号を発生し、同時計数装置9はパルス信号を計数してその計数値、及び対γ線を検出した2つの検出点(孔部6の軸心を中心にしてほぼ180°方向が異なって配置された一対の放射線検出器4の位置)を出力する。コンピュータ11は、その計数値、及び2つの検出点の位置情報を記憶装置12に記憶する。トランスミッションデータ撮影を終了するとき、駆動装置制御装置35は、駆動終了信号を出力して、較正線源駆動装置30のモーターを停止させる。そのとき、線源制御装置69はγ線の外部への放出を遮るために較正線源31のシャッター34を閉じる。
孔部6の半径方向に直線状に三層配置された3つの放射線検出器4(例えば、図1に示す放射線検出器4a,4b,4c)を、1つの放射線検出器グループと称する。本実施例は、複数の放射線検出器グループを有する。放出されたγ線のエネルギーが均一である場合、理論式によりγ線の検出効率が求まる。放射線検出器4は、検出部を5mm厚さのCdTeで構成した半導体放射線検出器であるため、511keVのγ線の検出効率は約20%である。そのため、1つの放射線検出器グループにおいて、一層目の放射線検出器4では入射γ線の約20%が、二層目の放射線検出器4では、一層目の放射線検出器4を透過した80%のγ線うちの約20%、つまり約16%のγ線が減衰する。三層目の放射線検出器4では、二層目の放射線検出器を透過した64%のγ線のうちの約20%、すなわち12.8%のγ線が減衰する。それらの減衰に応じたγ線撮像信号が一層目及び二層目の各放射線検出器4から出力される。そして、そのγ線撮像信号は、該当する信号処理装置7のγ線弁別装置8で散乱γ線を除去されてパルス信号に変えられる。その信号処理装置7の同時計数装置9はパルス信号を計数する。各層の放射線検出器4からのγ線撮像信号を独立に計測した場合、一層から三層の3つの放射線検出器4の検出効率の理論値の比(約20:16:12.8)と大きく異なる(例えば±5%以上異なる)場合は、いずれかの放射線検出器4が劣化して検出効率が低下していることになる。例えば、それらの3つの放射線検出器4のうち、どれか1つの放射線検出器4が劣化し、他の2つの放射線検出器4が正常に動作していた場合、1つの放射線検出器グループでの検出効率の実測値の比は前記の理論値の比に対して大きく異なる。このため、劣化した放射線検出器4を発見することができる。さらに、正常な2つの放射線検出器4の検出効率と前記比から求めた検出効率と、実測の検出効率から、劣化による検出効率の低下パーセンテージを計算できる。例えば、1つの放射線検出器グループにおける3つの放射線検出器4の計測値に基づいて求められた検出効率の実測値の比が、20:4:12.8になったとする。この場合、2層目の放射線検出器4の検出効率の実測値の比が、上記の検出効率の理論値の比と比較して12ポイント(低下パーセンテージ:75%)低下いる。このため。2層目の放射線検出器4は故障していると考えられる。
故障検知方法の概念について説明する。ある時点で、γ線源33から放出されたγ線は、コリメータ39の形状上、1つの放射線検出器グループ内の3つの放射線検出器4(例えば、図2に示す放射線検出器4a,4b,4c)に入射されるが、他の放射線検出器グループ(例えば、1つの放射線検出器グループに隣接した放射線検出器グループ)内の3つの放射線検出器4には入射されない。1つの放射線検出器グループに属する放射線検出器4の検出効率の比を、γ線透過距離及びγ線透過順序を考慮しながら、過去の放射線検出器4の劣化度合いを記したデータを用いて求める。また、1つの放射線検出器グループに属する放射線検出器4の検出効率の理論値の比を、シミュレーションまたは理論計算により求める。その1つの放射線検出器グループ内の各放射線検出器4から出力された各γ線撮像信号に基づいて求めた検出効率の実測値の比と、上記の検出効率の理論値の比とを比較し、その放射線検出器グループ内の各放射線検出器4が劣化していないか(または劣化しているか)を判断する。検出効率の実測値の比と、上記の検出効率の理論値の比との比較は、全放射線検出器グループに対して行う。検出効率の理論値の比は撮像装置2に設置された放射線検出器4が同じ種類であれば、どれか1つの放射線検出器グループで代表して算出すればよい。また、各γ線撮像信号に基づいて求めた検出効率の実測値の比と、過去の放射線検出器4の劣化度合いを記したデータを用いて求めた検出効率の比とを比較し、その放射線検出器グループ内の各放射線検出器4における劣化の進行状況を判断する。放射線検出器4が劣化している場合には、記憶装置12に劣化度合いの情報を記憶し、劣化及び故障をユーザーに知らせる。このような処理を各放射線検出器グループ毎に繰り返すことにより、撮像装置2に設置された各放射線検出器の検出効率の劣化度合いの把握及び故障した放射線検出器の摘出が行える。この故障検知方法の概念を適用した具体的な処理は、図5及び図6を用いて後述する。
次に、放射線検査装置1を用いたPET検査について説明する。被検体である被検診者17に予め注射等によりPET用薬剤を投与する。その後、PET用薬剤が被検診者17の体内に拡散して患部(例えば癌の患部)に集まって撮像可能な状態になるまでの所定時間の間、被検診者17は待機する。PET用薬剤は、検査する患部に応じて選ばれる。その所定時間経過後に、被検診者17はベッド16上に寝かせられ、撮像装置2を用いたPET検査が実施される。PET検査の実施の際には、ベッド16が撮像装置2に向かって移動され、被検診者17はベッド16と共に孔部6内に挿入される。被検診者17の体内の患部より放出された511keVのγ線(PET用薬剤に18Fを含んでいる場合)は、放射線検出器4に入射される。各放射線検出器4は、PET用薬剤に起因して患部から放出されたγ線をそれぞれ検出し、γ線の検出信号(以下、γ線撮像信号という)を出力する。γ線撮像信号は、該当する配線13を介して該当するγ線弁別装置8に入力される。γ線弁別装置8は、波形整形装置(図示せず)を有する。この波形整形装置は、入力したγ線撮像信号を時間的なガウス分布の波形を有するγ線撮像信号に変換する。PET用薬剤から放出された陽電子の陽電子消滅(患部で発生)により生成されるγ線のエネルギーは、511keVである。しかし、体内でγ線が散乱した場合、エネルギーは511keVより低くなる。γ線弁別装置8は、散乱γ線を除去するため、例えばエネルギーが511keVよりも低い400keVをエネルギー設定値として、このエネルギー設定値以上のエネルギーを有するγ線撮像信号を通過させるフィルター(図示せず)を備えている。このフィルターは波形整形装置から出力されたγ線撮像信号を入力する。ここで、例として、400keVをエネルギー設定値としたのは511keVのγ線が放射線検出器4に入射したときに発生するγ線撮像信号のばらつきを考慮したためである。γ線弁別装置8は、そのフィルターを通過したγ線撮像信号に対して、所定のエネルギーを有するパルス信号を発生させる。
同時計数装置9は、全てのγ線弁別装置8から出力されたパルス信号を入力し、各放射線検出器4から出力された各γ線撮像信号に対する計数値を求める。更に、同時計数装置9は、トランスミッションデータ撮影時と同様に、前述の対γ線の各γ線に対するそれぞれのパルス信号を用いて、その対γ線を検出した2つの検出点の位置情報を求める。これらの検出点の位置情報は、コンピュータ11に伝えられ、コンピュータ11によって記憶装置12に記憶される。前述の各γ線撮像信号に対する計数値も、コンピュータ11により記憶装置12に記憶される。
コンピュータ11は、その計数値等を用いて図5及ぶ図6に示す処理手順を実行して被検診者17の断層像を再構成する。その処理手順の内容を詳細に説明する。PET検査時における計数値及び該当する検出点の位置情報、及びトランスミッション撮影時における計数値が、記憶装置12から読み出されて入力される(ステップ40)。放射線検出器グループ内の各放射線検出器に対する検出効率の理論値の比を算出する(ステップ41)。この論理比は、被検診者17から放出されたγ線透過距離(PET用薬剤に含まれる放射性核種に応じて変わる)及びγ線透過順序を用いた理論計算により求められる。18Fを含んでいるPET用薬剤を被検診者17に投与した場合には、放射線検出器グループ内における一層から三層の3つの放射線検出器4に対する検出効率の理論値の比は約20:16:12.8である。本実施例のようにその都度、検出効率の理論値の比を算出するのではなく、含まれる放射性核種の異なる各PET用薬剤に対して、放射線検出器グループ内における全放射線検出器に対する検出効率の理論値の比を予め算出して記憶装置12に記憶させておいてもよい。
次に、劣化した放射線検出器4を抽出する(ステップ42)。ステップ42の処理は、放射線検出器グループ毎に行われ、図6を用いて具体的に説明する。まず、1つの放射線検出器グループを選択する(ステップ50)。選択された放射線検出器グループ内の放射線検出器に対する検出効率の実測値の比を算出する(ステップ51)。すなわち、選択された放射線検出器グループ内の各放射線検出器4から出力されたそれぞれのγ線撮像信号に基づいて得られた各計数値を用いて、それらの放射線検出器に対する検出効率の実測値の比を算出する。検出効率の実測値の比と検出効率の理論値の比との差が設定範囲(理論値の比に対して±5%の範囲)内にあるかを判定する(ステップ52)。その差が設定範囲内にある場合(「Yes」の場合)は、選択された放射線検出器グループ内の各放射線検出器4は、劣化しておらず正常に動作している。その差が設定範囲内にない場合(「No」の場合)は、その放射線検出器グループ内の劣化している放射線検出器(劣化放射線検出器という)4を、記憶装置12に記憶させる(ステップ53)。その差が設定範囲内にない場合は、その放射線検出器グループ内のいずれか(または全て)の放射線検出器4が劣化していることを意味する。放射線検出器グループ内の劣化放射線検出器は、各放射線検出器における検出効率の実測値の比の値とその理論値の比の値とを前述のように比較することによって確認できる。次に、劣化放射線検出器4に関する劣化情報を表示装置13に出力する(ステップ54)。劣化放射線検出器4に関する劣化情報は、記憶装置12に記憶されている過去の放射線検出器4の劣化度合いを記したデータを用いて求めた検出効率の比の情報である。オペレータは、表示装置13に表示された劣化放射線検出器4に関する劣化情報に基づいて劣化放射線検出器4の劣化の進行状況を判断できる。劣化の進行度合いが大きな劣化放射線検出器4は新しい放射線検出器4と交換する必要がある。劣化放射線検出器4の検出効率を補正する(ステップ55)。例えば、1つの放射線検出器グループ内の放射線検出器4a及び4cの実測値の比の値が理論値の比の値と一致しており、放射線検出器4bの実測値の比の値が理論値の比よりかなり低い場合は、放射線検出器4a及び4cの各検出効率の実測値の比、及びに放射線検出器4a,4b及び4cの検出効率の理論値の比に基づいて推測される検出効率を放射線検出器4bの検出効率として補正する。この補正された検出効率に基づいて求められた計数値は、放射線検出器4bの計数値として記憶装置12に記憶される。
ステップ52が「Yes」のときまたはステップ55の処理が終了したとき、「選択されない放射線グループが残っている」かについて判定する(ステップ56)。ステップ56の判定が「Yes」の場合には、ステップ57で次の放射線検出器グループが選択され、ステップ56の判定が「No」になるまで、ステップ51以降の処理が実行される。ステップ56の判定が「No」になったとき、トランスミッション像を作成する(ステップ43)。すなわち、トランスミッションデータ撮影時に得られたγ線撮像信号に対する計数値を用いて、被検診者17の体内の各ボクセルにおけるγ線減衰率を算出する。各ボクセルにおけるこのγ線減衰率は記憶装置12に記憶される。
次に、各放射線検出器間における体内の減衰補正計数を算出する(ステップ44)。PET検査では対γ線が放出されるため、対γ線の体内における動距離の和に基づいて体内の減衰補正計数を算出する。PET検査時に得られた計数値,検出点の位置情報及びステップ43で算出したγ線減衰率を用いて、後述のステップ47で述べる断層像の再構成の手法により、被検診者17の断層像を再構成する。まず、ステップ43で得られた各ボクセルにおけるγ線減衰率を用いて、対γ線を検出するある一対の放射線検出器4(例えば、図7(b)に示す放射線検出器4fと放射線検出器4g)間におけるガンマ線減衰率をフォワードプロジェクション法により求める。求められたそのガンマ線減衰率の逆数が減衰補正計数である。ステップ45において、減衰補正計数を用い体内減衰補正を行う。PET検査時において得られた計数値にその減衰補正計数を掛け合わせることによって、PET検査時において得られた計数値の補正が行われる。被検診者17の患部で発生したγ線は体内を透過する間に吸収・減衰されるが、上記の減衰補正計数を用いた補正をPET検査時において得られた計数値に対して行うことによって、更に高精度な計数値を得ることができる。
更に、ステップ46において、放射線検出器の検出効率差を反映してγ線撮像信号に対する補正を行う。PET検査では対γ線が放出されるため、対γ線のそれぞれのγ線が到達する2つの放射線検出器グループ内の検出効率を用いて計数値を補正する必要がある。つまり、その2つの放射線検出器グループ内でそれぞれγ線を検出した放射線検出器4の検出効率の補正計数を両方かけることにより補正する。これを具体的に説明する。各放射線検出器4における検出効率についての、フォワードプロジェクション撮像時における理論値と実測値との差がステップ42で求められている。放射線検出器グループjにおいて、i番目の放射線検出器4に対する、フォワードプロジェクション撮像時における、検出効率の理論値をXfiij、及びステップ45で補正された計数値をXseijとする。い番目の検出器が故障していると判定され、k番目の検出器が正常である場合、i番目の放射線検出器に対する補正PET計数値Xsiijは(2)式で表される。iは孔部6に近い放射線検出器4から1,2,3…となる。(2)式で求められた補正PET計数値(放射線 Xsiij=Xsekj×Xfiij/Xfikj …(2)
検出器の検出効率差を反映して補正された計数値)は記憶装置12に記憶される。
検出器の検出効率差を反映して補正された計数値)は記憶装置12に記憶される。
患部(例えば癌の患部)を含む、被検診者17の断層像を再構成する(ステップ47)。ステップ47では、ステップ46における補正によって得られた補正PET計数値Xsiij、及び検出点の位置情報を用いて、断層像の再構成が行われる。その断層像の再構成について、具体的に説明する。その断層像再構成の処理は、フィルタードバックプロジェクション法を適用し、上記計数値の情報及び検出点の位置情報を用いてコンピュータ11で行われる。コンピュータ11は、断層像再構成装置である。その断層像は、フィルタードバックプロジェクション法では、前述した文献に記載されているように、距離t及び角度θの2つのパラメータによりソートされたデータを用いて再構成される。距離t及び角度θについて、図2を用いて具体的に説明する。被検診者17の患部から放出された対γ線が放射線検出器4d,4eで検出されたとする。放射線検出器4dと放射線検出器4eとを結ぶ直線18の中点を通り、直線18に垂直に交わる直線が19である。基準軸20(一番内側の放射線検出器4が配置される円の中心点、すなわち孔部6の中心点を通る直線であればどの方向でもよい)と直線19とのなす角度がθであり、孔部6の中心点21と直線18との距離がtである。角度θは、対γ線を検出した放射線検出器4dと放射線検出器4eとを結ぶ直線18が、基準軸20に対してどれだけ回転しているかを表している。
放射線検査装置1は、孔部6の半径方向において複数の放射線検出器4を積層配置しているが、この積層配置によって以下に示す新しい機能を発揮できる。例えば、図7(a)に示すように被検診者17の体内のγ線対発生点22(患部)より発生した2つのγ線23a,23bが放射線検出器4f,4gに入射した場合を考える。検出器の内部のどの位置で減衰したかはわからないため、従来法では一対の放射線検出器4f,4hの先端位置を結ぶ線、つまり図7(b)に示す線24を検出線とした。しかし、放射線検査装置1では、孔部6の半径方向において放射線検出器4を積層配置しているため、その半径方向で外側に位置する放射線検出器4gのγ線撮像信号が得られ、放射線検出器4fと放射線検出器4gとを結ぶ線25を検出線とすることができる。つまり、従来の検出器ではわからなかった検出器の奥行き方向における減衰位置を把握することができる。この結果、検出線25は、γ線対が発生した位置を正確に通るため、画像の精度が向上する。この結果、検出線がより実際のガンマ線対発生点に近くなるため、測定データの精度が向上する。
次に得られた結果をフィルタードバックプロジェクションにより再構成する。コンピュータによって再構成された断層のデータは、記憶装置12に記憶されると共に、表示装置13に表示される。
(1)本実施例は、放射線検出器4を、孔部6の軸方向及び周方向のみならず、半径方向にも複数配置することにより、従来のPET検査に用いられる放射線検出器のように信号伝達物質を減らさずに、孔部6の半径方向において細分した位置でのγ線撮像信号を得ることができる。このため、本実施例は、孔部6の半径方向においてγ線が到達した正確な位置情報(γ線撮像信号を出力した放射線検出器4の位置情報)を得ることができる。なお、従来のPET検査では、孔部6の半径方向には1つの放射線検出器を配置し、この放射線検出器内部に反射材を配置して信号伝達物質が光電子増倍管に到達したパターンにより、孔部6の半径方向においてγ線が到達した位置の情報を求めていた。このとき、反射材により信号伝達物質の一部が放射線検出器内で減衰したり、放射線検出器外へ反射してしまうため、信号伝達物質が減少し、エネルギー分解能の低下が発生した。
(2)本実施例は、孔部6の半径方向において独立した複数の放射線検出器4を配置しているため、それぞれの放射線検出器の信号伝達物質の全てをγ線の検出に使用でき、放射線検出器のエネルギー分解能が向上する。エネルギー分解能の高い放射線検出器をPET検査で用いた場合、散乱によりエネルギーが減衰したγ線と無散乱の511keVのエネルギーのγ線との区別が可能になる。その結果、γ線弁別装置8のフィルターにより散乱線をより多く除去することが可能となる。
(3)本実施例は、放射線検出器内の信号伝達物質数を減らすことなく孔部6の半径方向におけるγ線の正確な到達位置の情報を取得できるため、γ線の正確な到達位置の情報を使用することによる断層像の精度の向上と、放射線検出器の反射材が不要であることにより信号伝達物質の減少が阻止でき、エネルギー分解能が向上して散乱線の断層像再構成への影響を抑えることが可能となった。その結果、本実施例は、断層像の精度、つまりPET検査の精度を向上できる。
(4)本実施例は、放射線検出器4として半導体放射線検出器を用いているため、孔部6の半径方向に複数の放射線検出器4を配置することができ、そのように複数の放射線検出器4を配置しても撮像装置2が大きくならない。
(5)本実施例は、1つの放射線検出器グループ内の各放射線検出器4に対する検出効率の実測値の比とそれらの放射線検出器4に対する理論値の比とを比較することによって、それらの放射線検出器4のうちで劣化している放射線検出器4を簡単に見つけることができる。特に、孔部6の半径方向において、複数の放射線検出器4を直線状に配置した場合には、上記の劣化している放射線検出器4を簡単に見つけられる。
(6)本実施例は、検出効率差によるノイズ及び体内散乱ノイズを一台の撮像装置2を用いた撮像によって補正することができる。
本実施例のステップ47では、ステップ45で補正した計数値をステップ46で検出効率差を反映して補正した補正PET係数値を用いて断層像を再構成しているが、ステップ46での補正を省略してステップ45で補正した計数値を用いてステップ47で断層像を再構成することも可能である。
本実施例では、三個の放射線検出器4を孔部6の半径方向に直線状に配置しているが、三個の放射線検出器をそのように直線状ではなく、内側から二番目の放射線検出器4を孔部6の周方向にずらして(例えば一番内側の2つの放射線検出器の間の空間に面するように)配置してもよい。このように、孔部6の半径方向に複数の放射線検出器4が直線状に配置されていない場合には、撮像装置を組立てた後に、各放射線検出器に到達するまでのγ線の減衰率を試験により測定しなければならない。前述の実施例のように、孔部6の半径方向に複数の放射線検出器4が直線状に配置されている場合には、放射線検出器4のγ線の減衰率が分かっているため、そのような試験を行う必要がない。
なお、本実施例ではトランスミッションの撮影によるγ線の体内吸収補正を行ったが、その補正の替りに一般的に用いられているPETの補正技術を用いてもよい。体内吸収補正の他の方法について説明する。別に設置されたX線CT装置を用いて被検診者17を透過したX線をX線CT装置の放射線検出器で測定する。その放射線検出器から出力されたX線の検出信号の減衰率を用いて被検診者17の断層像を再構成し、体内の各位置でのCT値を求める。得られたCT値から、体内の各位置における物質組成を見積もる。そして物質組成データから511keVにおける各位置での線減弱係数を見積もる。得られた線減弱係数データを用いて、PET検査において一対のγ線を検出した一対の半導体素子部間の線減弱係数をフォワードプロジェクション法により求める。求められたその線減弱係数の逆数をγ線撮像信号の計数値に掛け合わせることにより体内減衰によるデータ差の補正がなされる。
本発明の他の実施例である放射線検査装置を、図8を用いて以下に説明する。本実施例の放射線検査装置1Aは、SPECT検査に用いられるものであり、放射線検査装置1の撮像装置2を撮像装置2Aに、信号処理装置7を信号処理装置7Aに替えた構成を有する。放射線検査装置1Aにおけるそれら以外の構成は放射線検査装置1と同じである。信号処理装置7Aは、γ線弁別装置8A、及びγ線弁別装置8Aに接続された計数装置36を有し、放射線検出器4毎に設けられる。γ線弁別装置8Aは、実施例1におけるγ線弁別装置8のフィルターにおけるエネルギー設定値400keVを120keVに変えた構成を有する。撮像装置2Aは、撮像装置2の構成にコリメータ27を付加し、更に撮像装置2の構成のうち較正線源周方向移動装置37を較正線源周方向移動装置37Aに替えたものである。コリメータ27は、最も内側に配置される放射線検出器4の内側に配置され、放射線検出器支持板5に取付けられる。コリメータ27は、環状をしており、放射線検出器4に対して斜め入射使用とするγ線を吸収する。本実施例も複数の放射線検出器グループを有する。
較正線源周方向移動装置37Aは、ガイドレール28及び較正線源装置29Aを備える。較正線源装置29Aは較正線源駆動装置30,較正線源31A及びアーム38を有する。較正線源31Aは、アーム38に取付けられる。図9に示す較正線源31Aは、較正線源31のγ線源33をγ線源33Aに替えると共に、較正線源31からコリメータ39を取除いた構成を有する。γ線源33Aは、141keV前後のγ線を放出する線源を用いる。例えば120keVの57Coを用いる。
まず、放射線検査装置1Aを用いたトランスミッションデータ撮影は、放射線検査装置1を用いた場合と同様に行われ、被検診者の体内でのγ線減衰率を求める。得られたγ線減衰率は、SPECT検査における体内散乱の補正に用いられる。放射線検出器4は本例では120keVのエネルギーを有する。
放出されたγ線のエネルギーが均一である場合、理論式によりγ線の検出効率が求まる。放射線検出器4は、検出部を5mm厚さのCdTeで構成した半導体放射線検出器であるため、141keVのγ線の検出効率は約80%である。本例では120keVの線源を用いているが、検出効率は大差がないので141keVとして処理しても妥当な結果になる。そのため、1つの放射線検出器グループの三層配置された3つの放射線検出器4において、一層目の放射線検出器4で入射γ線の約80%が、二層目の放射線検出器4では、一層目の放射線検出器4を透過した20%のγ線うちの約80%、つまり約16%のγ線が減衰する。三層目の放射線検出器4では、二層目の放射線検出器を透過した4%のγ線のうちの約80%、すなわち3.2%のγ線が減衰する。それらの減衰に応じたγ線撮像信号が各放射線検出器4から出力される。各層の放射線検出器4からのγ線撮像信号を独立に計測した場合、各層の放射線検出器4の検出効率の実測値の比が理論値の比(80:16:3.2)と大きく異なる(例えば±5%以上異なる)場合は、いずれかの放射線検出器4が劣化している。本実施例も、実施例1と同様にして、1つの放射線検出器グループ内における劣化放射線検出器4を見つけることができ、劣化による検出効率の低下パーセンテージを得ることができる。本実施例における故障検知方法の概念について説明する。
本実施例では、ある時点でγ線源33Aから放出されたγ線は、コリメータ27の形状上、1つの放射線検出器グループ内の3つの放射線検出器4に入射されるが、例えば、その1つの放射線検出器グループに隣接した他の放射線検出器グループ内の3つの放射線検出器4には入射されない。このような本実施例においても、実施例1で述べた故障検知方法の概念が適用され、後述するが図5及び図6に示す処理とほぼ同じ処理が適用される。
放射線検査装置1Aを用いたSPECT検査について説明する。SPECT用薬剤を投与された被検診者が横たわっているベッド16が撮像装置2Aの孔部6内に挿入される。SPECT用薬剤は、被検診者17の患部に集まっている。SPECT用薬剤に起因して被検診者17の体内の患部から放出された141keVのγ線(SPECT用薬剤に99Tcを含んでいる場合)は、実施例1と同様に、各放射線検出器4によって検出される。各放射線検出器4から出力されたγ線撮像信号は、該当するγ線弁別装置8Aに入力される。γ線弁別装置8Aは、フィルターでエネルギー設定値120keV以上のエネルギーを有するγ線撮像信号(散乱γ線を含まない)を通過させ、このγ線撮像信号に対して所定のエネルギーを有するパルス信号を発生させる。計数装置36は、そのパルス信号を用いて計数を行い、γ線撮像信号に対する計数値を求める。計数装置36はその計数値と共に検出点の位置情報(そのγ線撮像信号を出力した放射線検出器4の位置情報)を出力する。コンピュータ11は、その計数値を、検出点の位置情報と関連つけて記憶装置12に記憶する。
コンピュータ11は、その計数値等を用いて図5及ぶ図6に示す処理手順を実行して被検診者17の断層像を再構成する。本実施例では、その処理手順においてステップ40,41,44,46及び47が実施例1と異なっているがその他のステップの処理は同じである。ここでは、本実施例におけるステップ40,41,44,46及び47の処理についてのみ説明する。本実施例のステップ40では、SPECT検査時における計数値及び該当する検出点の位置情報、及びトランスミッション撮影時における計数値が、記憶装置12から読み出されて入力される。ステップ41では、放射線検出器グループ内の各放射線検出器に対する検出効率の理論値の比を算出する。この論理比は、被検診者17から放出されたγ線透過距離(SPECT用薬剤に含まれる放射性核種に応じて変わる)及びγ線透過順序を用いた理論計算により求められる。99Tcを含んでいるSPECT用薬剤を被検診者17に投与した場合には、放射線検出器グループ内における一層から三層の3つの放射線検出器4に対する検出効率の理論値の比は約80:16:3.2である。
本実施例のステップ44では、各放射線検出器間における減衰補正計数が算出される。PET検査では患部から対γ線が放出されるのに対してSPECT検査では単一γ線が放出されるため、本実施例のステップ44では、実施例1と異なり、1つの放射線検出器グループ内での各放射線検出器間における減衰補正計数が算出される。すなわち、SPECT検査では患部からのγ線は1つのSPECT検査時に得られた計数値、及びステップ43で算出したγ線減衰率を用いて、被検診者17の断層像を再構成する。まず、ステップ43で得たトランスミッション像をバックプロジェクションして、体内の各位置におけるγ線減衰率を求める。得られたγ線減衰率を用いて体内の各位置における物質組成を見積もる。見積もった物質組成データを用い、141keVにおける体内の各位置での線減弱係数を見積もる。得られた線減弱係数データを用いて、ある放射線検出器に対し、コリメータ27で入射する方向においてγ線が発生した場合における線減弱係数の平均値をフォワードプロジェクションにより求める。求められたその線減弱係数の逆数が減衰補正計数である。
更に、本実施例のステップ46では、放射線検出器の検出効率差を反映してγ線撮像信号に対する補正を行う。SPECT検査では単一γ線が放出されるため、単一γ線が到達する1つの放射線検出器グループ内の検出効率を用いて計数値を補正する。この補正は、実施例1で示した(2)式を用いて行われる。(2)式のXsiijは補正SPECT計数値であり、(2)式で求められたその補正SPECT計数値は記憶装置12に記憶される。ステップ47では、ステップ46における補正によって得られた補正SPECT計数値Xsiij、及び検出点の位置情報を用いて、断層像の再構成が行われる。
本実施例も実施例1で生じた効果(1)〜(6)を得ることができる。
本発明の他の実施例である放射線検査装置を、図10及び図11に基づいて説明する。本実施例の放射線検査装置1Bは、X線CT検査(X線源60から放射されて被検診者の体内を透過したX線を放射線検出器で検出する行為)及びPET検査に用いられるものであり、放射線検査装置1の撮像装置2を撮像装置2Bに替え、放射線検査装置1の信号処理装置7を信号処理装置7Aに替えた構成を有する。放射線検査装置1Bにおけるそれら以外の構成は放射線検査装置1と同じである。撮像装置2Bは、撮像装置2の構成のうち較正線源周方向移動装置37を較正線源周方向移動装置37Bに替えたものである。較正線源周方向移動装置37Bは、ガイドレール28及び較正線源装置29Bを備える。較正線源装置29Bは較正線源駆動装置30,較正線源31,X線源60及びアーム38を有する。較正線源31及びX線源60は、アーム38の先端部に取付けられる。較正線源31及びX線源60は、孔部6の周方向に並ぶようにアーム38の先端部に取付けてもよい。較正線源周方向移動装置37BはX線源周方向移動装置,X線源装置,較正線源駆動装置30はX線源駆動装置でもある。本実施例は、駆動装置制御装置35及び線源制御装置69を有する。
X線源60は図示されていないが公知のX線管を有する。このX線管は、陽極,陰極,陰極の電流源、及び陽極と陰極との間に電圧を印加する電圧源を外筒内に備える。陰極はタングステン製のフィラメントである。電流源から陰極に電流を流すことによってフィラメントから電子が放出される。この電子は、電圧源から陰極と陽極との間に印加される電圧(数百kV)によって加速され、ターゲットである陽極(W,Mo等)に衝突する。電子の陽極への衝突により80keVのX線が発生する。このX線がX線源60から放出される。
信号処理装置7Aは信号弁別装置61,信号弁別装置61に含まれていないγ線弁別装置8及び同時係数装置9を有する。各放射線検出器グループ内で最も内側に位置する一層目(4X)のそれぞれの放射線検出器4毎に信号弁別装置61が接続される。各信号弁別装置61は、図12に示すように、切替スイッチ62,γ線弁別装置8及びX線信号処理装置66を有する。切替スイッチ62は可動端子63及び固定端子64及び65を有する。一層目(4X)の放射線検出器4は配線13によって切替スイッチ62の可動端子63に接続される。γ線弁別装置8は固定端子64に接続され、X線信号処理装置66は固定端子65に接続される。電源68のマイナス端子は抵抗67を介して配線13に接続され、電源68のプラス端子は放射線検出器4に接続される。各放射線検出器グループ内における内側から二層目(4Y)及び三層目(4Z)に位置するそれぞれの放射線検出器4は、実施例1と同様に、対応するγ線弁別装置8にそれぞれ接続される。信号弁別装置61内のγ線弁別装置8を含む全てのγ線弁別装置8は、1つの同時計数装置9に接続される。実施例1と同様に、幾つかの放射線検出器4毎に1つの同時係数装置9を設けてもよい。同時計数装置9及びX線信号処理装置66はコンピュータ11に接続される。
まず、トランスミッションデータ撮影が、実施例1と同様に較正線源31を用いて行われる。トランスミッションデータ撮影終了後に、放射線検査であるPET検査及びX線CT検査が撮像装置2Bを用いて行われる。
本実施例におけるX線CT検査及びPET検査について説明する。注射などの方法により予めPET用薬剤が、体内投与放射能が370MBqになるように被検体である被検診者17に投与される。所定時間経過後に、被検診者17が横たわったベッド16が撮像装置2Bの孔部6内に被検診者17と共に挿入される。X線CT検査及びPET検査は撮像装置2Bを用いて行われる。
本実施例における放射線検査を具体的に説明する前に、本実施例の放射線検出の原理について説明する。X線CT像(X線CTによって得られた、被検体の、内臓及び骨の画像を含む断層像)のデータは、X線源から放射されたX線を特定の方向に所定時間の間、被検体に照射し、体内を透過したX線を放射線検出器により検出する作業(スキャン)を繰り返し、複数の放射線検出器で検出されたX線の強度に基づいて作成される。精度の良いX線CT像のデータを得るためには、X線CT検査において、X線を検出している放射線検出器に、PET用薬剤に起因して被検体の内部から放出されるγ線が入射しないことが望ましい。1つの放射線検出器においてはγ線の入射率に対応して被検体へのX線の照射時間を短くすればγ線の影響が無視できるので、これにより被検体へのX線の照射時間の短縮を図った。そのX線の照射時間Tを決めるために、まず、1つの放射線検出器へのγ線の入射率を考える。PET検査において被検体に投与するPET用薬剤に基づいた体内の放射能をN(Bq),発生するγ線の体内通過率をA,1つの放射線検出器の立体角から求めた入射率をB,検出素子の感度をCとすると、1つの放射線検出器で検出するγ線の率α(個/sec)は(3)式で与えられる。(3)式において係数の「2」は、1個の陽電子消滅の際に一対(2個)のγ線が放出されることを意味している。照射時間T内に α=2NABC …(3)
1つの検出素子でγ線が検出される確率Wは(4)式で与えられる。(4)式のWの値を小さくするように照射時間Tを決めることによって、X線CT検査時に、1つの放射線
W=1−exp(−Tα) …(4)
検出器に入射されるγ線の影響は無視できる程度になる。
1つの検出素子でγ線が検出される確率Wは(4)式で与えられる。(4)式のWの値を小さくするように照射時間Tを決めることによって、X線CT検査時に、1つの放射線
W=1−exp(−Tα) …(4)
検出器に入射されるγ線の影響は無視できる程度になる。
X線の照射時間Tの一例を以下に述べる。(3)および(4)式に基づいて具体的なX線の照射時間Tを求めた。PET検査において被検体に投与するPET用薬剤に起因する体内での放射線の強度は、最大で370MBq程度であり(N=370MBq)、γ線の体内通過率Aは被検体の体を半径15cmの水と仮定すれば0.6程度(A=0.6)である。例えば一辺5mmの放射線検出器を半径50cmでリング状に配置する場合を考えると、1つの放射線検出器の立体角から求めた入射率Bは8×10-6(B=8×10-6)である。また、放射線検出器の検出感度Cは半導体放射線検出器を使用した場合最大で0.6程度(C=0.6)である。これらの値から1つの放射線検出器のγ線の検出率αは2000(個/sec)程度である。X線の照射時間Tを例えば1.5μsecとすれば、1つの放射線検出器がX線検出中にγ線を検出する確率Wは0.003となり、このγ線はほとんど無視できる。体内投与放射能を360MBq以下とした場合、X線の照射時間を1.5μsec以下にすれば、W<0.003つまりγ線の検出確率は0.3%以下となり無視できる。
上記の原理が適用されて撮像装置2Bを用いた本実施例におけるX線CT検査及びPET検査について具体的に説明する。
駆動装置制御装置35は、X線CT検査を開始するとき、駆動開始信号を出力して、較正線源駆動装置30のモーターに接続された、電源とつながる開閉器(以下、モーター開閉器という)を閉じる。電流の供給によりモーターが回転して、その回転力が減速機構を介してピニオンに伝えられ、較正線源装置29B、すなわちX線源60がガイドレール28に沿って周方向に移動する。X線源60は、孔部6内に挿入された状態で被検診者17の周囲を設定速度で移動する。X線CT検査終了時には、駆動装置制御装置35は駆動停止信号を出力してモーター開閉器を開く。これによって、X線源60の周方向への移動が停止される。本実施例では、周方向に環状に配置された全ての放射線検出器4は、その周方向に移動しなく、かつ孔部6の軸方向にも移動しない。移動しないX線源制御装置及び駆動装置制御装置から移動するX線源装置への制御信号の伝送はX線源装置の移動に支障にならない公知の技術を適用する。
線源制御装置69はX線源60からのX線の放出時間を制御する。すなわち、線源制御装置69は、X線発生信号及びX線停止信号を繰り返して出力する。最初のX線発生信号の出力は、線源制御装置69への上記駆動開始信号の入力に基づいてなされる。X線発生信号の出力によってX線源60におけるX線管の陽極(または陰極)と電源との間に設けられた開閉器(以下、X線源開閉器という、図示せず)が閉じられ、第1設定時間経過した時にX線停止信号が出力されてX線源開閉器が開き、そして第2設定時間経過した時にX線源開閉器を閉じる、という制御が繰り返される。陽極と陰極との間には、第1設定時間の間で電圧が印加され、第2設定時間の間で電圧が印加されない。線源制御装置69によるその制御によって、X線管から80keVのX線がパルス状に放出される。第1設定時間である照射時間Tは、放射線検出器4でのγ線の検出確率を無視できるように例えば1μsecに設定される。第2設定時間は、X線源60が1つの放射線検出器4とこれに周方向において隣接する他の放射線検出器4の間を移動する時間T0であり、ガイドレール28の周方向におけるX線源60の移動速度で定まる。第1及び第2設定時間は線源制御装置69に記憶されている。
X線停止信号及びX線発生信号の繰り返し出力によって、X線源60は、第1設定時間、すなわち1μsecの間にX線を放出し、第2設定時間の間にX線の放出を停止する。このX線の放出及び停止がX線源60の周方向への移動期間中に繰り返されることになる。
X線源60から放出されたそのX線は、ファンビーム状に、被検診者17に照射される。X線源60の周方向の移動によって、被検診者17には周囲よりX線が照射される。被検診者17を透過したX線は、孔部6の軸心を基点にX線源60から180度の位置にある放射線検出器4を中心に周方向に位置する複数個の放射線検出器4によって検出される。これらの放射線検出器4は、そのX線の検出信号(以下、X線撮像信号という)を出力する。このX線撮像信号は、該当する配線13を経て対応するそれぞれの信号弁別装置61に入力される。上記のX線を検出しているそれらの放射線検出器4は、便宜的に第1放射線検出器4と称する。
ベッド16上の被検診者17から、PET用薬剤に起因した511keVのγ線が放出されている。第1放射線検出器4以外の放射線検出器4は、γ線撮像信号を出力する。γ線を検出している放射線検出器4を、便宜的に第2放射線検出器4と称する。第2放射線検出器4のうち、一層目に位置する第2放射線検出器4から出力されたγ線撮像信号は該当する配線13を経て対応するそれぞれの信号弁別装置61に入力され、二層目及び三層目に位置する第2放射線検出器4から出力されたγ線撮像信号は配線13を経て対応するそれぞれのγ線弁別装置8に入力される。信号弁別装置61は一層目に配置された放射線検出器4のみが信号弁別装置61に接続されている。これは、X線のエネルギーが80keVであるため、被検診者17を透過したほとんど(90%以上)のX線が一層目の放射線検出器4で検出されるからである。
信号弁別装置61内で、一層目の第2放射線検出器4から出力されたγ線撮像信号はγ線弁別装置8に伝えられ、第1放射線検出器4から出力されたX線撮像信号はX線信号処理装置66に伝えられる。このような各撮像信号の伝送は、信号弁別装置61の切替スイッチ62の切替操作によって行われる。切替スイッチ62の可動端子63を固定端子64または固定端子65に接続する切替操作は、駆動装置制御装置35の出力である切替制御信号に基づいて行われる。駆動装置制御装置35は、一層目の放射線検出装置4のうち第1放射線検出器4を選択し、この第1放射線検出器4に接続される信号弁別装置61における可動端子63を固定端子65に接続する。1つの放射線検出器グループ内での内側からの各層の放射線検出器4における検出効率の理論値の比は20:16:12.8である。
第1放射線検出器4の選択について説明する。較正線源駆動装置30内のモーターにはエンコーダー(図示せず)が連結される。駆動装置制御装置35は、エンコーダーの検出信号を入力して周方向における較正線源駆動装置30、すなわちX線源60の位置を求め、このX線源60の位置と180°反対側に位置する放射線検出器4を、記憶している各放射線検出器4の位置のデータを用いて選択する。X線源60から放射されるX線はガイドレール28の周方向である幅を有しているため、被検診者17を透過したX線を検出する放射線検出器4は、選択されたその放射線検出器4以外にも周方向に複数個存在することになる。駆動装置制御装置35はその複数の放射線検出器4も選択する。これらの放射線検出器4が、第1放射線検出器である。周方向におけるX線源60の移動に伴って、第1放射線検出器4も違ってくる。X線源60の周方向への移動に伴って、第1放射線検出器4も擬似的に周方向に移動しているように見える。駆動装置制御装置35が、X線源60の周方向への移動に伴って別の放射線検出器4を選択したときには、新たに第1放射線検出器4となる放射線検出器4に接続された可動端子63は固定端子65に接続される。X線源60の周方向への移動に伴って第1放射線検出器4でなくなった放射線検出器4に接続された可動端子63は駆動装置制御装置35によって固定端子64に接続される。第一層目の個々の放射線検出器4は、X線源60の位置との関係で、あるときは第1放射線検出器4となり、別のあるときには第2放射線検出器4となる。このため、第一層目の1つの放射線検出器4は、時間的にずれてX線撮像信号及びγ線撮像信号の両方を出力する。
第1放射線検出器4は、第1設定時間である1μsecの間にX線源60から照射されて被検診者17を透過したX線を検出する。1μsecの間に第1放射線検出器4が被検診者17から放出されるγ線を検出する確率は、前述したように、無視できるほど小さい。PET用薬剤に起因して被検診者17の体内で発生した多数のγ線は、特定の方向に放出されるのではなく、あらゆる方向に放出される。これらのγ線は、前述したように、対となってほぼ正反対の方向(180°±0.6°)に放出され、いずれかの第2放射線検出器4によって検出される。
一層目の放射線検出器4から出力されたX線撮像信号及びγ線撮像信号を入力したときの信号弁別装置61の信号処理について説明する。第1放射線検出器4から出力されたX線撮像信号は、前述したように、切替スイッチ62の作用によってX線信号処理装置66に入力される。X線信号処理装置66は、入力したX線撮像信号を積分装置によって積算し、X線撮像信号の積算値、すなわち計測したX線の強度の情報を出力する。X線撮像信号の強度情報は、コンピュータ11に伝えられ、コンピュータ11によって記憶装置12に記憶される。一層目の第2放射線検出器4から出力されたγ線撮像信号は、切替スイッチ62の作用によってγ線弁別装置8に入力される。信号弁別装置61のγ線弁別装置8は、エネルギー設定値(400keV)以上のエネルギーを有するγ線撮像信号を入力したときに所定のエネルギーを有するパルス信号を発生させる。同時計数装置9は、実施例1と同様に、全てのγ線弁別装置8から出力されたパルス信号を入力して、各γ線撮像信号に対する計数値、及び対γ線を検出した2つの検出点の位置情報を出力する。計数値及び位置情報は、コンピュータ11に伝えられ、コンピュータ11によって記憶装置12に記憶される。
コンピュータ11は、図13に示す処理を実行する。X線撮像信号の強度,PET検査時における計数値及び該当する検出点の位置情報、及びトランスミッションデータ撮影時における計数値が、記憶装置12から読み出されて入力される(ステップ69)。X線撮像信号の強度を用いて、被検診者17の体内の各ボクセルにおけるX線の減衰率を算出する(ステップ70)。この減衰率は記憶装置12に記憶される。被検診者17の横断面の断層像が、該当する位置でのX線撮像信号の減衰率を用いて再構成される(ステップ71)。X線撮像信号の減衰率を用いて再構成した断層像をX線CT像と称する。X線CT像を再構成するために、記憶装置12から読み出されたX線撮像信号の減衰率を用いて、X線源60と第1放射線検出器4の半導体素子部との間における被検診者17の体内での線減弱係数を求める。この線減弱係数を用いて、フィルタードバックプロジェクション法により各ボクセルの線減弱係数を求める。各ボクセルの線減弱係数の値を用いて各ボクセルにおけるCT値を得る。これらのCT値を用いてX線CT像のデータが得られる。このX線CT像のデータは、記憶装置12に記憶される。次に、被検診者17の横断面の断層像が、該当する位置でのγ線撮像信号の計数値、及び検出点の位置情報を用いて再構成される(ステップ72)。γ線撮像信号の計数値を用いて再構成した断層像をPET像と称する。ステップ72では実施例1で述べた図5のステップ41から47の処理が実行されてPET像が得られる。このPET像のデータは、記憶装置12に記憶される。PET像のデータとX線CT像のデータとを合成して、両データを含む合成断層像のデータを求め、記憶装置12に記憶させる(ステップ73)。PET像のデータとX線CT像のデータとの合成は、両方の像データにおける共通の参照点(例えば、孔部6の中心軸の位置)を合わせることによって、簡単にかつ精度良く行うことができる。すなわち、PET像のデータ及びX線CT像のデータは、共有する放射線検出器4から出力された撮像信号に基づいて作成されるので、前述のように位置合せを精度良く行える。合成断層像のデータは、記憶装置12から呼び出されて表示装置13に出力され(ステップ74)、表示装置13に表示される。表示装置13に表示された合成断層像はX線CT像を含んでいるので、PET像における患部の、被検診者35の体内での位置を容易に確認することができる。すなわち、X線CT像は内臓及び骨の像を含んでいるので、医者は、患部(例えば、癌の患部)が存在する位置を、その内臓及び骨との関係で特定することができる。
本実施例によれば、実施例1において生じる効果(1)〜(6)を得ることができ、更に以下に示す効果も得ることができる。
(7)本実施例は、孔部6の周囲に配置されたそれらの放射線検出器4によって、被検体である被検診者17から放出される複数の対γ線を検出できると共に、周方向に移動するX線源60から放出されて被検診者17を透過したX線も検出できる(一層目の放射線検出器4で)。このため、従来技術は撮像装置として透過X線を検出する撮像装置及びγ線を検出する他の撮像装置を必要としていたが、本実施例は、撮像装置は一台あればよく、X線CT検査及びPET検査の両方を実施できる放射線検査装置の構成が単純化できる。
(8)本実施例は、孔部6の周囲に配置された一層目の放射線検出器4のそれぞれがX線撮像信号及びγ線撮像信号の両方を出力する。このような構成も、放射線検査装置の構成の更なる単純化、及び放射線検査装置の小型化に貢献する。
(9)本実施例は、一層目の放射線検出器4の1つの出力信号であるX線撮像信号を用いて、被検診者35の、内臓及び骨の画像を含む第1の断層像(X線CT像)を再構成でき、一層目から三層目の各放射線検出器4の出力であるγ線撮像信号を用いて、その被検診者17の、患部の画像を含む第2の断層像(PET像)を再構成できる。第1断層像のデータ及び第2断層像のデータは、1つの撮像装置2Bの、孔部6の周囲に配置された放射線検出器4の出力信号に基づいて再構成されているので、第1断層像のデータ及び第2断層像のデータを精度良く位置合せして合成することができる。このため、精度のよい、患部,内臓及び骨の画像を含む断層像(合成断層像)を簡単に得ることができる。この合成断層像によれば、内臓及び骨との関係で、患部の位置を正確に知ることができる。例えば、第1断層像のデータ及び第2断層像のデータを、撮像装置2Bの孔部6の軸心を中心に合わせることによって、簡単に両断層像を合成した画像データを得ることができる。
(10)本実施例は、第1の断層像を作成するために必要な撮像信号、及び第2の断層像を作成するために必要な撮像信号を共用する放射線検出器4から得ることができるため、被検診者17の検査に要する時間(検査時間)を著しく短縮できる。換言すれば、短い検査時間で、第1の断層像を作成するために必要な撮像信号、及び第2の断層像を作成するために必要な撮像信号を得ることができる。本実施例は、従来技術のように、被検診者を、透過X線を検出する撮像装置からγ線を検出する他の撮像装置まで移動させる必要がなく、被検診者が動く確率を低減できる。被検診者を、透過X線を検出する撮像装置からγ線を検出する他の撮像装置まで移動させる必要がなくなることも、被検診者の検査時間の短縮に寄与する。
(11)X線信号処理装置66、すなわち第1信号処理装置に入力されるγ線撮像信号が著しく減少するため、精度の良い第1断層像のデータを得ることができる。このため、第1断層像のデータと第2断層像のデータとを合成して得られた画像データを用いることにより、患部の位置をより正確に知ることができる。
(12)本実施例は、配置された放射線検出器群の内側でX線源60が周回するため、孔部6の直径が大きくなり、一層目に配置できる放射線検出器4の個数を多くすることができる。周方向における放射線検出器4の個数の増加は、感度の向上をもたらし、被検診者17の横断面の分解能を向上させる。
(13)本実施例では、X線源60が取付けられるアーム38及びX線源60は放射線検出器4の内側に位置しているため、それらが被検診者17から放出されるγ線を遮って、それらの真後ろに位置する放射線検出器4がそのγ線を検出できなく、PET像の作成に必要な検出データが欠損する可能性がある。しかし、本実施例は、前述のように、較正源駆動装置30によってX線源60及びアーム38が周方向に周回しているので、実質的にはデータの欠損は問題とならない。特に、X線源60及びアーム38の周回速度は約1秒/1スライスであり、最短で数分オーダーのPET検査に要する時間と比較すると十分短い。これによっても、実質的にはそのデータの欠損は問題にならない。
本発明の他の実施例である放射線検査装置を、図14を用いて以下に説明する。本実施例の放射線検査装置75は、フラットパネルディテクタを用いたデジタルX線検査装置である。放射線検査装置75は、支柱77によって支えられるX線源76,複数の放射線検出器(図示せず)が設置されて支柱79で支えられたフラットパネルディテクタ78,X線信号処理装置66及びX線像作成装置80を備える。フラットパネルディテクタ78は、高さ方向及び幅方向に多数の放射線検出器4を配置しており、更に奥行き方向(被検診者17を透過したX線の進行方向81)にも図15に示すように直線状に放射線検出器4i,4j,4kのように三層配置されている。図15における82は、X線源76に対向する面である。X線信号処理装置66は、各放射線検出器4に接続されている。X線像作成装置80はコンピュータ11,記憶装置12及び表示装置13を有する。記憶装置12及び表示装置13は全放射線検出器4が接続されているコンピュータ11に接続される。
放射線検査装置75を用いたX線検査について説明する。被検診者17はX線源76を背にしてX線源76とフラットパネルディテクタ78との間に立っている。X線源76より放出されたX線は、被検診者17を透過してフラットパネルディテクタ78の各放射線検出器40により検出される。放射線検出器4はX線を検出してX線撮像信号を出力する。このX線撮像信号はX線信号処理装置66で積算されてX線強度の情報を出力する。各X線信号処理装置66から出力されたX線強度の情報はコンピュータ11に入力されて記憶装置13に記憶される。コンピュータ11は、記憶装置12からX線強度の情報を取込んで被検診者17に対する体内の各位置におけるX線の減衰率を算出する。
フラットパネルディテクタ78の面82から奥行き方向に直線上に配置された三層配置の3つの放射線検出器4で1つの放射線検出器グループが形成される。本実施例でもX線源76から放出されるX線のエネルギーに応じて放射線検出器グループ内の各放射線検出器4に対する検出効率の比が変化する。例えば、100keVのX線を用い、2mm角のCdTeで構成された検出部を有する放射線検出器4で被検診者17を透過したそのX検を検出した場合は、放射線検出器グループ内での検出効率の理論値の比は約84:13:2.5である。この検出効率の理論値の比は記憶装置12に記憶されている。
コンピュータ11は記憶装置12に記憶されているX線強度の情報を用いて各放射線検出器グループ内の放射線検出器4に対する検出効率の実測値の比を算出する。コンピュータ11は、実施例1のステップ52の処理を実行する。算出された各検出効率の実測値の比と検出効率の理論値の比との差が設定範囲内にある場合には、コンピュータ11が、算出した上記のX線の減衰率を用いて被検診者17に関するX線画像である濃淡画像のデータを作成する。上記の差が設定範囲内にない場合には、コンピュータ11は実施例1のステップ53,54及び55の処理を実行する。ステップ55の処理で劣化放射線検出器の検出効率が補正された場合には、補正された検出効率に基づいてその放射線検出器に対するX線強度を求め、このX線強度を反映して上記のX線減衰率を補正する。コンピュータ11は、補正されたX線減衰率を用いて上記の濃淡画像のデータを作成する。
本実施例は、実施例1で述べた効果(1)〜(5)を得ることができる。但し、効果(3)はX線画像の精度が向上するとなる。
本実施例においても、フラットパネルディテクタ78の奥行き方向に放射線検出器を直線状に配置しなくてもよい。例えば、図15において、二層目の全ての放射線検出器4が一層目に配置された2つの放射線検出器4と重なるように(面82から見て)配置することが可能である。
次に、検出器を直線状に並べない場合の補正法に関して、フラットパネルディテクタを用いたデジタルX線検査を用いた例を示す。フラットパネルディテクタを用いた検査装置は図10と同じであるが、フラットパネルディテクタ70の放射線検出器4は、例えば図15に示す2層目の放射線検出器4が横にずれた状態で1層目,2層目,3層目が非直線状に配置されている。このような放射線検出器4の多層配置においても、一部の放射線検出器4の劣化の確認、及び劣化放射線検出器の計測値に対する補正が可能となる。
本発明の他の実施例である放射線検査装置を、図16を用いて説明する。本実施例の放射線検査装置83はX線CT装置である。放射線検査装置83は、アーム86に設置されたX線源84,アーム86に設置された放射線検出部85,X線処理装置66及び断層像作成装置88を備える。アーム86は支柱87によって支えられる。X線源84と放射線検出部85は、相互間に被検診者17が入れる間隔で離れて配置され、相互に対向している。放射線検出部85には、フラットパネルディテクタ78と同様に、高さ方向及び幅方向に多数の放射線検出器4がされ、かつX線源84に対向する面から奥行き方向にも放射線検出器4が直線状に三層に渡って配置される。アーム86は、詳細な機構が示されていないが、X線源84及び放射線検出部85がベッド16上に横たわっている被検診者17の周囲を旋回するように回転することができる。
放射線検査装置83を用いた検査について説明する。被検診者17はベッド16上に横たわった状態でX線源84と放射線検出部85との間に位置している。X線源84から放出されたX線は、被検診者17に照射されて被検診者17の体内を透過する。この透過したX線は放射線検出部85の各放射線検出器4で検出される。アーム86の回転装置(図示せず)によって、X線源84及び放射線検出部85が被検診者17の周囲を回転する(被検診者17のある1断面に対し180°または360°)。各放射線検出器4から出力されたX線の測定信号は、それぞれのX線信号処理装置66に入力される。X線信号処理装置66はその測定信号に基づいてX線強度を求める。コンピュータ11は、そのX線強度に基づいて、回転するX線源84の位置と回転する放射線検出部85のX線源84に対向する位置との間における、被検診者17の体内でのX線減衰率を算出する。この線減弱係数は記憶装置12に記憶する。
コンピュータ11は、放射線検出部85のX線源84に対向する面から直線状に三層配置された各放射線検出器4について検出効率の実測値の比を実施例1のステップ51と同様に算出し、引続いて実施例1のステップ52,53,54及び55の処理を実行する。ステップ52の処理で、算出された各検出効率の実測値の比と検出効率の理論値の比との差が設定範囲内にあると判定された場合には、コンピュータ11は、記憶装置12に記憶された検出器間と線源の間のX線の減衰率から、先に示したフィルタードバックプロジェクション法(Filtered Back Projection Method)などを用いて各ボクセルの線減弱係数を求め、その値をCT値に変換する。ステップ52の処理で、上記の差が設定範囲内にな
いと判定された場合には、コンピュータ11は、補正された検出効率を用いて記憶装置12に記憶された線源弱係数を補正し、補正された線源弱係数を用いてCT値を算出する。
コンピュータ11は、各ボクセルのCT値を用いてX線CT像を再構成する。
いと判定された場合には、コンピュータ11は、補正された検出効率を用いて記憶装置12に記憶された線源弱係数を補正し、補正された線源弱係数を用いてCT値を算出する。
コンピュータ11は、各ボクセルのCT値を用いてX線CT像を再構成する。
本実施例は、実施例4で得られる効果を得ることができる。
1,1A,1B,75,83…放射線検査装置、2,2A,2B…撮像装置、3…ケーシング、4…放射線検出器、5…放射線検出器支持板、6…孔部、7…信号処理装置、8…γ線弁別装置、9…同時計数装置、10,88…断層像作成装置、11…コンピュータ、14…被検診者保持装置、16…ベッド、27…コリメータ、28…ガイドレール、29,29A,29B…較正線源装置、30…較正線源駆動装置、31,31A…較正線源、33,33A…γ線源、35…駆動装置制御装置、37,37A,37B…較正線源周方向移動装置、38…アーム、60,76,84…X線源、61…信号弁別装置、62…切替スイッチ、66…X線信号処理装置、69…線源制御装置、78…フラットパネルディテクタ、80…X線像作成装置。
Claims (7)
- 被検体からの放射線を検出する複数の放射線検出器と、
前記一つの放射線検出器に接続され、前記複数の放射線検出器によって検出された複数の放射線検出信号を処理する信号処理装置と、
別に設置されたX線CT装置からのX線の検出信号の減衰率を用いて、PET像又はSPECT像に対して放射線が被検体の体内で散乱する現象の補正である体内減衰補正を行い、PET像又はSPECT像の画像再構成を行うコンピュータとを有することを特徴とする放射線検査装置。 - X線を照射する一つのX線源と、
被検体からの放射線を検出する複数の放射線検出器と、
前記一つの放射線検出器に接続され、前記複数の放射線検出器によって検出された複数の放射線検出信号を処理する信号処理装置と、
前記X線源からの複数のX線の検出信号を用いて、PET像又はSPECT像に対して放射線が被検体の体内で散乱する現象の補正である体内減衰補正を行い、PET像又はSPECT像の画像再構成と、X線CT像の画像再構成を行うコンピュータとを有することを特徴とする放射線検査装置。 - 請求項1又は請求項2の放射線検査装置において、
前記コンピュータは、
PET像又はSPECT像と、X線CT像との合成を行い、前記合成は、両方の像データにおける共通の参照点を合わせ、合成した画像を表示装置へ出力することを特徴とする放射線検査装置。 - 請求項1又は請求項2の放射線検査装置において、
前記コンピュータは、
前記体内減衰補正を行う際に、
前記X線源からの複数のX線の検出信号を用いて、体内の複数の位置での線減弱係数を見積もり、得られた線減弱係数データを用いて、放射線が放射線検出器にコリメータで入射する方向においてγ線が発生した場合における線減弱係数の平均値をフォワードプロジェクションにより求め、求められたその線減弱係数の逆数を減衰補正計数としてSPECT検査の放射線の計数値に掛け合わせることにより体内減衰によるデータ差の補正を行うことを特徴とする放射線検査装置。 - 請求項1又は請求項2の放射線検査装置において、
前記コンピュータは、
前記体内減衰補正を行う際に、
PET検査の対γ線の体内における動距離の和に基づいて体内の減衰補正計数を算出し、前記減衰補正計数をPET検査の放射線の計数値に掛け合わせることにより体内減衰の補正を行うことを特徴とする放射線検査装置。 - 請求項1又は請求項2の放射線検査装置において、
前記コンピュータは、
前記体内減衰補正を行う際に、
前記X線源からの複数のX線の検出信号を用いて、体内の複数の位置での線減弱係数を見積もり、得られた線減弱係数データを用いて、PET検査において一対のγ線を検出した一対の半導体素子部間の線減弱係数をフォワードプロジェクション法により求め、求められたその線減弱係数の逆数を減衰補正計数としてPET検査の放射線の計数値に掛け合わせることにより体内減衰の補正を行うことを特徴とする放射線検査装置。 - 請求項1又は請求項2の放射線検査装置において、
前記複数の放射線検出器は、前記X線の進行方向に複数配置されることを特徴とする放射線検査装置。
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2011048482A JP2011154031A (ja) | 2011-03-07 | 2011-03-07 | 放射線検査装置 |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2011048482A JP2011154031A (ja) | 2011-03-07 | 2011-03-07 | 放射線検査装置 |
Related Parent Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2008305840A Division JP2009058528A (ja) | 2008-12-01 | 2008-12-01 | 放射線検査装置 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| JP2011154031A true JP2011154031A (ja) | 2011-08-11 |
Family
ID=44540090
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2011048482A Pending JP2011154031A (ja) | 2011-03-07 | 2011-03-07 | 放射線検査装置 |
Country Status (1)
| Country | Link |
|---|---|
| JP (1) | JP2011154031A (ja) |
Cited By (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| KR101304993B1 (ko) | 2012-08-07 | 2013-09-06 | 서강대학교산학협력단 | Pet 영상 획득 장치 |
| WO2014005049A1 (en) * | 2012-06-28 | 2014-01-03 | Gregerson Eugene A | Method and system for x-ray ct imaging |
| US9980689B2 (en) | 2012-06-12 | 2018-05-29 | Mobius Imaging, Llc | Detector system for imaging device |
Citations (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPS57138077U (ja) * | 1981-02-25 | 1982-08-28 | ||
| JPS6057283A (ja) * | 1983-09-09 | 1985-04-03 | Hitachi Medical Corp | ポジトロンct装置 |
| JPH0720245A (ja) * | 1993-06-30 | 1995-01-24 | Shimadzu Corp | ポジトロンct装置 |
| JPH095441A (ja) * | 1995-06-23 | 1997-01-10 | Toshiba Corp | 放射線診断方法及び放射線診断装置 |
-
2011
- 2011-03-07 JP JP2011048482A patent/JP2011154031A/ja active Pending
Patent Citations (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPS57138077U (ja) * | 1981-02-25 | 1982-08-28 | ||
| JPS6057283A (ja) * | 1983-09-09 | 1985-04-03 | Hitachi Medical Corp | ポジトロンct装置 |
| JPH0720245A (ja) * | 1993-06-30 | 1995-01-24 | Shimadzu Corp | ポジトロンct装置 |
| JPH095441A (ja) * | 1995-06-23 | 1997-01-10 | Toshiba Corp | 放射線診断方法及び放射線診断装置 |
Cited By (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US9980689B2 (en) | 2012-06-12 | 2018-05-29 | Mobius Imaging, Llc | Detector system for imaging device |
| WO2014005049A1 (en) * | 2012-06-28 | 2014-01-03 | Gregerson Eugene A | Method and system for x-ray ct imaging |
| US9111379B2 (en) | 2012-06-28 | 2015-08-18 | Mobius Imaging, Llc | Method and system for X-ray CT imaging |
| US9576378B2 (en) | 2012-06-28 | 2017-02-21 | Mobius Imaging, Llc | Method and system for x-ray CT imaging |
| US9978157B2 (en) | 2012-06-28 | 2018-05-22 | Mobius Imaging, Llc | Method and system for x-ray CT imaging |
| KR101304993B1 (ko) | 2012-08-07 | 2013-09-06 | 서강대학교산학협력단 | Pet 영상 획득 장치 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| US7297958B2 (en) | Radiological imaging apparatus | |
| JP4093013B2 (ja) | 放射線検査装置 | |
| JP3888156B2 (ja) | 放射線検査装置 | |
| US7026622B2 (en) | Radiological imaging apparatus | |
| JP3820972B2 (ja) | Pet装置 | |
| KR100501588B1 (ko) | 방사선 검사 장치 및 그 검사 방법 | |
| KR20030076250A (ko) | 방사선검사장치 및 방사선검사방법 및 방사선검사지원방법 | |
| JP3664121B2 (ja) | 放射線検査装置及び放射線検査方法 | |
| JP4321492B2 (ja) | 放射線検査装置 | |
| JP4604974B2 (ja) | Pet装置 | |
| JP3851575B2 (ja) | Pet検査装置 | |
| JP2011154031A (ja) | 放射線検査装置 | |
| JP2004350942A (ja) | 断層像作成装置及び放射線検査装置 | |
| JP4737201B2 (ja) | 放射線検査装置 | |
| JP3937942B2 (ja) | 放射線検査装置 | |
| JP5532061B2 (ja) | 放射線検査装置 | |
| JP2007181729A (ja) | 放射線検査装置の制御方法および画像情報作成方法 | |
| JP2009058528A (ja) | 放射線検査装置 | |
| JP3938078B2 (ja) | 放射線検査装置 | |
| JP3797379B2 (ja) | 陽電子放出型ct装置 | |
| JP2005164609A (ja) | 陽電子放出型ct装置 | |
| JP4333692B2 (ja) | 放射線検査装置 | |
| JP4400641B2 (ja) | 放射線検査装置及び陽電子放出型ct装置 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20110307 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20130528 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20130729 |
|
| A02 | Decision of refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A02 Effective date: 20140325 |