JP2010083886A - 経口投与用粒子状医薬組成物 - Google Patents
経口投与用粒子状医薬組成物 Download PDFInfo
- Publication number
- JP2010083886A JP2010083886A JP2009222020A JP2009222020A JP2010083886A JP 2010083886 A JP2010083886 A JP 2010083886A JP 2009222020 A JP2009222020 A JP 2009222020A JP 2009222020 A JP2009222020 A JP 2009222020A JP 2010083886 A JP2010083886 A JP 2010083886A
- Authority
- JP
- Japan
- Prior art keywords
- pharmaceutical composition
- oral administration
- particulate pharmaceutical
- water
- drug
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Granted
Links
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/0012—Galenical forms characterised by the site of application
- A61K9/0053—Mouth and digestive tract, i.e. intraoral and peroral administration
- A61K9/0056—Mouth soluble or dispersible forms; Suckable, eatable, chewable coherent forms; Forms rapidly disintegrating in the mouth; Lozenges; Lollipops; Bite capsules; Baked products; Baits or other oral forms for animals
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/48—Preparations in capsules, e.g. of gelatin, of chocolate
- A61K9/50—Microcapsules having a gas, liquid or semi-solid filling; Solid microparticles or pellets surrounded by a distinct coating layer, e.g. coated microspheres, coated drug crystals
- A61K9/5073—Microcapsules having a gas, liquid or semi-solid filling; Solid microparticles or pellets surrounded by a distinct coating layer, e.g. coated microspheres, coated drug crystals having two or more different coatings optionally including drug-containing subcoatings
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P13/00—Drugs for disorders of the urinary system
- A61P13/08—Drugs for disorders of the urinary system of the prostate
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P19/00—Drugs for skeletal disorders
- A61P19/08—Drugs for skeletal disorders for bone diseases, e.g. rachitism, Paget's disease
- A61P19/10—Drugs for skeletal disorders for bone diseases, e.g. rachitism, Paget's disease for osteoporosis
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/28—Drugs for disorders of the nervous system for treating neurodegenerative disorders of the central nervous system, e.g. nootropic agents, cognition enhancers, drugs for treating Alzheimer's disease or other forms of dementia
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P3/00—Drugs for disorders of the metabolism
- A61P3/06—Antihyperlipidemics
Landscapes
- Health & Medical Sciences (AREA)
- Veterinary Medicine (AREA)
- Life Sciences & Earth Sciences (AREA)
- Engineering & Computer Science (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Pharmacology & Pharmacy (AREA)
- Public Health (AREA)
- General Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Animal Behavior & Ethology (AREA)
- Medicinal Chemistry (AREA)
- General Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Epidemiology (AREA)
- Physical Education & Sports Medicine (AREA)
- Biomedical Technology (AREA)
- Physiology (AREA)
- Nutrition Science (AREA)
- Neurology (AREA)
- Neurosurgery (AREA)
- Zoology (AREA)
- Rheumatology (AREA)
- Orthopedic Medicine & Surgery (AREA)
- Diabetes (AREA)
- Urology & Nephrology (AREA)
- Psychiatry (AREA)
- Hospice & Palliative Care (AREA)
- Hematology (AREA)
- Obesity (AREA)
- Medicinal Preparation (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
Abstract
【解決手段】前記経口投与用粒子状医薬組成物は、薬物含有粒子を、メタアクリル酸メチル・メタアクリル酸ブチル・メタアクリル酸ジメチルアミノエチル共重合体、および水溶性高分子物質を含む被膜物質により被覆されてなる。
【選択図】なし
Description
詳細には、本発明は、薬物含有粒子を、メタアクリル酸メチル・メタアクリル酸ブチル・メタアクリル酸ジメチルアミノエチル共重合体、および水溶性高分子物質を含む被膜物質により被覆されてなる、経口投与用粒子状医薬組成物、および該経口投与用粒子状医薬組成物を含有してなる口腔内崩壊錠に関するものである。
また、本発明は、薬物含有粒子に被覆し、圧縮成形後も溶出速度の変化を低減する経口投与用粒子状医薬組成物を製造するためのメタアクリル酸メチル・メタアクリル酸ブチル・メタアクリル酸ジメチルアミノエチル共重合体および水溶性高分子物質の使用に関するものである。
更に、本発明は、薬物含有粒子に被覆し、圧縮成形後も溶出速度の変化を低減する経口投与用粒子状医薬組成物の製造方法に関するものである。
薬物を含有する核と、2種類の水溶性成分である、不溶化促進剤および不溶化物質を含有する中間層と、最外層に内部への水浸入速度を制御する水浸入制御層を含有する経口投与用時限放出型粒子状医薬組成物が知られており、水浸入制御層に用いる素材としてアクリル酸系高分子が例示されている(特許文献4)。しかしながら、選択される薬物または基剤によっては、初期薬物溶出を低減し、かつその後の速やかな薬物放出性を達成するためには更なる改善の余地がある。
また、メチルセルロースとモノマー単位にメタクリル酸エステルおよび/又はアクリル酸エステルを含むアクリル酸系ポリマーとを含むフィルムコートにより固形製剤の苦味などの不快な味を隠蔽し、かつ溶出性に優れるフィルムコーティング剤が開示されている(特許文献6)。
しかしながら、特許文献5又は6のいずれもコーティング顆粒を圧縮成形する際の溶出変化については記載されておらず、圧縮成形による溶出速度の変化が懸念される。
さらに、圧縮による衝撃を吸収する賦形剤とともに圧縮する方法として、薬物含有被膜粒子に、平均粒子径20μm以下の被膜保護剤を物理混合し、圧縮成形した製剤が記載されている。薬物含有被覆粒子の圧縮成形時における被膜の損傷を低減した圧縮成形製剤を提供するため、薬物含有被膜粒子を含み、かつ平均粒子径が約50μm以上で初期溶出速度比が4以上を示す物質の微粒子を被膜保護剤として含む圧縮成形製剤に関する発明が開示されている(特許文献8)。
しかしながら、特許文献7又は8のいずれも、選択された薬物または基剤によっては、初期薬物溶出を低減しても、その後の速やかな薬物放出が達成されない、また、アルコール処理が可能な特別な装置の使用が必要とされる課題が考えられる。
また、本発明は、薬物含有粒子に被覆し、圧縮成形後も溶出速度の変化を低減する経口投与用粒子状医薬組成物を製造するためのメタアクリル酸メチル・メタアクリル酸ブチル・メタアクリル酸ジメチルアミノエチル共重合体および水溶性高分子物質の使用を提供するものである。
更に、本発明は、メタアクリル酸メチル・メタアクリル酸ブチル・メタアクリル酸ジメチルアミノエチル共重合体、および水溶性高分子物質を含む被膜物質により被覆されてなる、経口投与用粒子状医薬組成物の製造方法を提供するものである。
[1]薬物含有粒子が、メタアクリル酸メチル・メタアクリル酸ブチル・メタアクリル酸ジメチルアミノエチル共重合体、および水溶性高分子物質を含む被膜物質により被覆されてなる、経口投与用粒子状医薬組成物、
[2]さらに被膜物質に流動化剤を含有する、[1]に記載の経口投与用粒子状医薬組成物、
[3]水溶性高分子物質が、ヒドロキシプロピルセルロース、ヒドロキシプロピルメチルセルロース、メチルセルロース、ヒドロキシエチルセルロース、ポビドン、コポリビドン、ポリビニルアルコール−ポリエチレングリコールグラフトコポリマー、ポリビニルアルコール、マクロゴール、およびポリエチレンオキサイドからなる群より選択される1種または2種以上である、[1]または[2]に記載の経口投与用粒子状医薬組成物。
[4]水溶性高分子物質が、ヒドロキシプロピルセルロース、ヒドロキシプロピルメチルセルロース、メチルセルロース、およびヒドロキシエチルセルロースからなる群より選択される1種または2種以上である、[1]〜[3]のいずれかに記載の経口投与用粒子状医薬組成物、
[5]水溶性高分子物質の量が、メタアクリル酸メチル・メタアクリル酸ブチル・メタアクリル酸ジメチルアミノエチル共重合体の量に対して1重量%以上30重量%以下である、[1]〜[4]のいずれかに記載の経口投与用粒子状医薬組成物、
[6]流動化剤が、ケイ酸金属類、二酸化ケイ素類、高級脂肪酸金属塩類、金属酸化物類、アルカリ土類金属塩、および金属水酸化物からなる群より選択される1種または2種以上である、[1]〜[5]のいずれかに記載の経口投与用粒子状医薬組成物、
[7]流動化剤が、タルク、カオリン、ケイ酸カルシウム、ケイ酸マグネシウム、軽質無水ケイ酸、ステアリン酸マグネシウム、ステアリン酸カルシウム、酸化鉄、酸化チタン、炭酸カルシウム、リン酸カルシウム、セッコウ、炭酸マグネシウム、水酸化アルミニウム、含水二酸化ケイ素、結晶セルロース、合成ケイ酸アルミニウム、重質無水ケイ酸、水酸化アルミナマグネシウム、ステアリン酸、トウモロコシデンプン、メタケイ酸アルミン酸マグネシウム、リン酸水素カルシウム造粒物、およびグリセリルモノステアレートからなる群より選択される1種または2種以上である、[1]〜[6]のいずれかに記載の経口投与用粒子状医薬組成物、
[8]流動化剤が、タルク、カオリン、ケイ酸カルシウム、ケイ酸マグネシウム、軽質無水ケイ酸、ステアリン酸マグネシウム、およびグリセリルモノステアレートからなる群より選択される1種または2種以上である、[1]〜[7]のいずれかに記載の経口投与用粒子状医薬組成物、
[9]流動化剤の量が、メタアクリル酸メチル・メタアクリル酸ブチル・メタアクリル酸ジメチルアミノエチル共重合体の量に対して1重量%以上500重量%以下である、[1]〜[8]のいずれかに記載の経口投与用粒子状医薬組成物、
[10]水溶性高分子物質がヒドロキシプロピルメチルセルロースであり、かつメタアクリル酸メチル・メタアクリル酸ブチル・メタアクリル酸ジメチルアミノエチル共重合体の量に対して1重量%以上30重量%以下である、[1]〜[9]のいずれかに記載の経口投与用粒子状医薬組成物、
[11]薬物が酸性薬物またはその塩である、[1]〜[10]のいずれかに記載の経口投与用粒子状医薬組成物、
[12]薬物が不快な味を有する、[1]〜[11]のいずれかに記載の経口投与用粒子状医薬組成物、
[13][1]〜[12]のいずれかに記載の経口投与用粒子状医薬組成物において、(1)(i)メタアクリル酸メチル・メタアクリル酸ブチル・メタアクリル酸ジメチルアミノエチル共重合体、および水溶性高分子物質からなる被膜物質による被覆層の内側に、または(ii)メタアクリル酸メチル・メタアクリル酸ブチル・メタアクリル酸ジメチルアミノエチル共重合体、水溶性高分子物質、および流動化剤からなる被膜物質による被覆層の内側に、(2)水溶性の不溶化促進剤及び水溶性の不溶化物質を含有する層を有する、[1]〜[12]のいずれかに記載の経口投与用粒子状医薬組成物、
[14][1]〜[13]のいずれかに記載の経口投与用粒子状医薬組成物を含有してなる口腔内崩壊錠、
[15]薬物含有粒子が、メタアクリル酸メチル・メタアクリル酸ブチル・メタアクリル酸ジメチルアミノエチル共重合体、および水溶性高分子物質を含む被膜物質により被覆することを特徴とする、経口投与用粒子状医薬組成物の製造方法、
[16]さらに被膜物質に流動化剤を含有する、[15]に記載の経口投与用粒子状医薬組成物の製造方法、
[17]水溶性高分子物質が、ヒドロキシプロピルセルロース、ヒドロキシプロピルメチルセルロース、メチルセルロース、ヒドロキシエチルセルロース、ポビドン、コポリビドン、ポリビニルアルコール−ポリエチレングリコールグラフトコポリマー、ポリビニルアルコール、マクロゴール、およびポリエチレンオキサイドからなる群より選択される1種または2種以上である、[15]または[16]に記載の経口投与用粒子状医薬組成物の製造方法、
[18]水溶性高分子物質が、ヒドロキシプロピルセルロース、ヒドロキシプロピルメチルセルロース、メチルセルロース、およびヒドロキシエチルセルロースからなる群より選択される1種または2種以上である、[15]〜[17]のいずれかに記載の経口投与用粒子状医薬組成物の製造方法、
[19]水溶性高分子物質の量が、メタアクリル酸メチル・メタアクリル酸ブチル・メタアクリル酸ジメチルアミノエチル共重合体の量に対して1重量%以上30重量%以下である、[15]〜[18]のいずれかに記載の経口投与用粒子状医薬組成物の製造方法、
[20]流動化剤が、ケイ酸金属類、二酸化ケイ素類、高級脂肪酸金属塩類、金属酸化物類、アルカリ土類金属塩、および金属水酸化物からなる群より選択される1種または2種以上である、[15]〜[19]のいずれかに記載の経口投与用粒子状医薬組成物の製造方法、
[21]流動化剤が、タルク、カオリン、ケイ酸カルシウム、ケイ酸マグネシウム、軽質無水ケイ酸、ステアリン酸マグネシウム、ステアリン酸カルシウム、酸化鉄、酸化チタン、炭酸カルシウム、リン酸カルシウム、セッコウ、炭酸マグネシウム、水酸化アルミニウム、含水二酸化ケイ素、結晶セルロース、合成ケイ酸アルミニウム、重質無水ケイ酸、水酸化アルミナマグネシウム、ステアリン酸、トウモロコシデンプン、メタケイ酸アルミン酸マグネシウム、リン酸水素カルシウム造粒物、およびグリセリルモノステアレートからなる群より選択される1種または2種以上である、[15]〜[20]のいずれかに記載の経口投与用粒子状医薬組成物の製造方法、
[22]流動化剤が、タルク、カオリン、ケイ酸カルシウム、ケイ酸マグネシウム、軽質無水ケイ酸、ステアリン酸マグネシウム、およびグリセリルモノステアレートからなる群より選択される1種または2種以上である、[15]〜[21]のいずれかに記載の経口投与用粒子状医薬組成物の製造方法、
[23]流動化剤の量が、メタアクリル酸メチル・メタアクリル酸ブチル・メタアクリル酸ジメチルアミノエチル共重合体の量に対して1重量%以上500重量%以下である、[15]〜[22]のいずれかに記載の経口投与用粒子状医薬組成物の製造方法、
[24]水溶性高分子物質がヒドロキシプロピルメチルセルロースであり、かつメタアクリル酸メチル・メタアクリル酸ブチル・メタアクリル酸ジメチルアミノエチル共重合体の量に対して1重量%以上30重量%以下である、[15]〜[23]のいずれかに記載の経口投与用粒子状医薬組成物の製造方法、
[25]薬物が酸性薬物またはその塩である、[15]〜[24]のいずれかに記載の経口投与用粒子状医薬組成物の製造方法、
[26]薬物が不快な味を有する、[15]〜[25]のいずれかに記載の経口投与用粒子状医薬組成物の製造方法、
[27][1]〜[12]のいずれかに記載の経口投与用粒子状医薬組成物の製造方法であって、(1)薬物含有粒子の外側に、水溶性の不溶化促進剤及び水溶性の不溶化物質を含有する層を形成する工程、(2)得られた粒子を、(i)メタアクリル酸メチル・メタアクリル酸ブチル・メタアクリル酸ジメチルアミノエチル共重合体、および水溶性高分子物質からなる被膜物質、または(ii)メタアクリル酸メチル・メタアクリル酸ブチル・メタアクリル酸ジメチルアミノエチル共重合体、水溶性高分子物質、および流動化剤からなる被膜物質により被覆する工程を含む、前記製造方法、
[28][1]〜[12]のいずれかに記載の経口投与用粒子状医薬組成物を製剤化する工程を含む、口腔内崩壊錠の製造方法、
[29]メタアクリル酸メチル・メタアクリル酸ブチル・メタアクリル酸ジメチルアミノエチル共重合体とともに、薬物含有粒子を被覆し、圧縮成形後も放出速度の変化を低減する経口投与用粒子状医薬組成物を製造するための水溶性高分子物質の使用
に関する。
本明細書における「粒子状医薬組成物」とは、サイズが下記の一定値より小さく、1種または2種以上の医薬添加剤と共に、種々の形態として経口投与を行う薬物含有粒子状組成物を意味する。粒子状組成物の形状が球に近似できる場合、粒子状医薬組成物のサイズは平均粒子径が2mm以下であると規定する。また、粒子状医薬組成物の形状が球以外の形状の場合、粒子状医薬組成物のサイズは平均最長径が2mm以下であると規定する。
なお、下限数値は製薬学的に許容される範囲であれば特に制限されないが、例えば1μm以上、他の態様として10μm以上、更なる態様として20μm以上が挙げられる。
粒子径の測定法としては、第15改正日本薬局方一般試験法に記載されている顕微鏡法が挙げられる。顕微鏡法は光学顕微鏡を用いて肉眼又は顕微鏡写真によって直接に個々の粒子の外観および形状を観察し、その大きさを測定する方法であり、長軸平均径、三軸平均径や、二軸平均径を粒子径として用いることができる。
また、配合割合は、通常薬物の種類、用途(適応症)、年齢(又は体重)に応じ適宜選択されるが、治療学的に有効な量あるいは予防学的に有効な量であれば特に制限されない。例えば、本発明の「粒子状医薬組成物」又は医薬品製剤当たり0.5重量%以上90重量%以下であり、他の態様としては0.5重量%以上80重量%以下であり、更なる態様としては0.5重量%以上70重量%以下である。
前記高分子物質としては、例えば、アラビアゴム、アルギン酸ナトリウム、α化デンプン、カゼインナトリウム、カラギーナン、カルボキシビニルポリマー、カルボキシメチルスターチナトリウム、カルメロースナトリウム、キサンタンガム、デキストラン、デキストリン、ヒドロキシプロピルセルロース、ヒドロキシプロピルメチルセルロース、メチルセルロース、ヒドロキシエチルセルロース、プルラン、ポビドン、コポリビドン、ポリオキシエチレン−ポリオキシプロピレングリコール、ポリビニルアセタールジエチルアミノアセテート、ポリビニルアルコール−ポリエチレングリコールグラフトコポリマー、ポリビニルアルコール、マクロゴール、ポリエチレンオキサイドが挙げられ、他の態様として、ヒドロキシプロピルセルロース、ヒドロキシプロピルメチルセルロース、メチルセルロース、ヒドロキシエチルセルロース、ポビドン、コポリビドン、ポリビニルアルコール−ポリエチレングリコールグラフトコポリマー、ポリビニルアルコール、マクロゴール、ポリエチレンオキサイド等が挙げられる。更なる態様としてヒドロキシプロピルセルロース、ヒドロキシプロピルメチルセルロース、メチルセルロース、ヒドロキシエチルセルロース等が挙げられる。更に他の態様としてヒドロキシプロピルセルロース、ヒドロキシプロピルメチルセルロース、ヒドロキシエチルセルロース等が挙げられる。ヒドロキシプロピルメチルセルロースとしては、日本薬局方ヒプロメロース(信越化学)の商品名で市販されている高分子物質(表示粘度3mPa・s以上15mPa・s以下)を挙げることができる。
これらの水溶性高分子物質は1種または2種以上を適宜組合せて使用することができる。
また、中間層被覆粒子に対して、例えば1重量%以上500重量%以下である。他の態様として5重量%以上200重量%以下であり、更なる態様として10重量%以上100重量%以下である。粒子状医薬組成物中の被覆量の割合が、例えば1重量%以上200重量%以下である。他の態様として5重量%以上100重量%以下であり、更に他の態様として5重量%以上50重量%以下である。
崩壊剤としては、例えばトウモロコシデンプン、バレイショデンプン、カルメロースカルシウム、カルメロースナトリウムなどが挙げられる。
酸味料としては、例えばクエン酸、酒石酸、リンゴ酸などが挙げられる。
発泡剤としては、例えば重曹などが挙げられる。
人工甘味料としては、例えばサッカリンナトリウム、グリチルリチン二カリウム、アスパルテーム、ステビア、ソーマチンなどが挙げられる。
香料としては、例えばレモン、レモンライム、オレンジ、メントールなどが挙げられる。
滑沢剤としては、例えばステアリン酸マグネシウム、ステアリン酸カルシウム、ショ糖脂肪酸エステル、ポリエチレングリコール、タルク、ステアリン酸などが挙げられる。
着色剤としては、例えば黄色三二酸化鉄、赤色三二酸化鉄、食用黄色4号、5号、食用赤色3号、102号、食用青色3号などが挙げられる。
緩衝剤としては、クエン酸、コハク酸、フマル酸、酒石酸、アスコルビン酸まその塩類、グルタミン酸、グルタミン、グリシン、アスパラギン酸、アラニン、アルギニンまたはその塩類、酸化マグネシウム、酸化亜鉛、水酸化マグネシウム、リン酸、ホウ酸またはその塩類などが挙げられる。
抗酸化剤としては、例えばアスコルビン酸、ジブチルヒドロキシトルエン、没食子酸プロピルなどが挙げられる。
界面活性剤としては、例えばポリソルベート80、ラウリル硫酸ナトリウム、ポリオキシエチレン硬化ヒマシ油などが挙げられる。医薬賦形剤としては、1種または2種以上組合せて適宜適量添加することができる。
これらの各種医薬賦形剤の配合量は、薬物含有粒子に対して、例えば1重量%以上100重量%以下であり、他の態様として、5重量%以上80重量%以下、更なる態様として10重量%以上50重量%以下である。
以下に本発明の粒子状医薬組成物を含有させた口腔内崩壊錠に関して説明するが、本発明の医薬品製剤を限定するものではない。
本発明の粒子状医薬組成物はこのような口腔内崩壊錠に含有させることができ、例えば、国際公開第WO95/20380号パンフレット(米国対応特許第5576014号明細書)、国際公開第WO2002/92057号パンフレット(米国対応特許出願公開第2003/099701号明細書)、米国特許第4305502号明細書、米国特許第4371516号明細書、特許第2807346号(米国対応特許第5466464号明細書)、特開平5-271054号公報(欧州対応特許第553777号明細書)、特開平10-182436号公報(米国対応特許第5958453号明細書)、特許第3412694号(米国対応特許第5223264号明細書)、国際公開第WO98/02185パンフレット(米国対応特許第6287596号明細書)、及び国際公開第WO2008/032767号パンフレット(米国対応特許出願公開第2008/0085309号明細書)に記載の公知の口腔内崩壊錠の薬物として該粒子状医薬組成物を適用し、該公報に記載の口腔内崩壊錠基剤を用い、該公報記載の方法に従い、口腔内崩壊錠とすることができる。このように粒子状医薬組成物を含有する口腔内崩壊錠としては、特許第3412694号明細書(米国対応特許第5223264号明細書)、特開2003-55197号公報に記載された口腔内崩壊錠が挙げられ、本発明の粒子状医薬組成物はこれらの口腔内崩壊錠に含有させることができる。
本発明の粒子状医薬組成物は、例えば、コーティング、乾燥、熱処理、打錠等、自体公知の方法により製造可能である。
本発明の粒子状医薬組成物を得るには、薬物を含有する核に対して本発明における被膜物質を被覆する。薬物を含有する核としては、薬物のみからなる粒子を用いることもできる。また公知の技術を用いて、薬物と1種または2種以上の添加物からなる粒子を製造し、それを用いてもよい。薬物と添加物からなる粒子の製造は、例えば薬物と適当な賦形剤(例えば結晶セルロース、乳糖、トウモロコシデンプン等)とを混合し、必要に応じて結合剤(例えばヒドロキシプロピルセルロース等)を加えて、造粒し、整粒、乾燥してもよい。また適当な核となる添加物粒子(例えば結晶セルロース(粒)(微結晶セルロースとして記載している場合がある)、精製白糖球状顆粒、白糖・デンプン球状顆粒等)に薬物と結合剤を溶解または分散した液を噴霧してもよい。
また、薬物を含有する核の外側に中間層を被覆、あるいは本発明の粒子状医薬組成物に更に医薬賦形剤をコーティング後、本発明における被膜物質を被覆してもよい。
薬物を含有する核に対して、中間層あるいは水浸入量制御層を被覆する際の好ましい品温は15℃以上60℃以下であり、他の態様として15℃以上45℃以下である。
薬物含有粒子に被覆した粒子状医薬組成物は、乾燥、熱処理などを施しても良い。
打錠装置としては、例えばロータリー打錠機、単発打錠機などが挙げられるが、通常製薬学的に圧縮成形物(好適には錠剤)が製造される方法であれば、装置とも特に限定されない。
一例として国際公開第WO95/20380号パンフレット(米国対応特許第5576014号明細書)に記載された口腔内崩壊錠の場合を挙げると、本発明の粒子状医薬組成物と成形性の低い糖類を混合して、かかる混合物を成形性の高い糖類を結合剤として噴霧して被覆及び/または造粒して、該造粒物を圧縮成形する工程を採用することが出来る。さらに調製した成形物の硬度を高めるために、加湿、乾燥の工程を採用することが出来る。「加湿」は、含まれる糖類の見かけの臨界相対湿度により決定されるが、通常その臨界相対湿度以上に加湿する。例えば、湿度として30RH%以上100RH%以下であり、他の態様として50RH%以上90RH%以下である。このときの温度は15℃以上50℃以下であることが好ましく、他の態様として20℃以上40℃以下である。処理時間は1時間以上36時間以下であり、他の態様として12時間以上24時間以下である。「乾燥」は、加湿により吸収した水分を除去する工程であれば特に限定されない。例えば乾燥の温度条件として、10℃以上100℃以下を設定でき、他の態様として20℃以上60℃以下、更なる態様として25℃以上40℃以下を設定することができる。処理時間は、0.5時間以上6時間以下とすることができ、他の態様として1時間以上4時間以下とすることができる。
ラウリル硫酸ナトリウム(SLS)(日光ケミカルズ社製、製品名ニッコールSLS、以下同じ)208.3gおよびヒドロキシプロピルメチルセルロース(HPMC)(信越化学工業社製、製品名TC-5E、以下記載無い場合同じ)83.4gを精製水 2000gに溶解した液に、アトルバスタチンカルシウム三水和物(ファイザー社製、以下同じ)208.3gを攪拌下添加して、分散液を調製した。調製した分散液を流動層造粒装置(Glatt社製、製品名GPCG-1、以下同じ)を用いて、結晶セルロース(粒)(旭化成ケミカルズ社製、製品名CP-102Y、以下同じ)500gに噴霧し、第1層を被覆した粒子を調製した(流動層造粒装置条件:送液量7.0g/min、噴霧空気圧0.20MPa)。
第1層を被覆した粒子950.0gに対し、メチルセルロース(信越化学工業社製、製品名 SM-4、以下同じ)47.5gを精製水 1140.0gに溶解した液を、流動層造粒装置を用いて噴霧し、第2層を被覆した粒子を調製した(流動層造粒装置条件:送液量6.6g/min、噴霧空気圧0.20MPa)。
第2層を被覆した粒子600.0gに対して、クエン酸ナトリウム二水和物(和光純薬社製、以下同じ)170.9gおよびメチルセルロース150.0gを精製水3964.8gに溶解した液を、流動層造粒装置を用いて噴霧し、第3層を被覆した粒子を調製した(流動層造粒装置条件:送液量6.5g/min、噴霧空気圧0.25MPa)。
第3層を被覆した粒子900.0gに対して、メチルセルロース45.0gを精製水1080.0gに溶解した液を流動層造粒装置を用いて噴霧し、第4層を被覆した粒子を調製した(流動層造粒装置条件:送液量6.6g/min、噴霧空気圧0.25MPa)。
HPMC 2.0gを精製水171.0gに溶解した液にメタノール 684.0gを添加・混合し、HPMC液(水・アルコール混液)を調製した。このHPMC液に、続いてメタアクリル酸メチル・メタアクリル酸ブチル・メタアクリル酸ジメチルアミノエチル共重合体(オイドラギットE)(エボニックデグザGmbH社製、製品名オイドラギットE100、以下同じ)27.4gを添加し溶解させ、タルク(松村産業社製、製品名ハイフィラー、以下同じ)15.7gを添加し分散させた。この分散液を、流動層造粒装置を用いて、第4層を被覆した薬物含有粒子300.0gに対して噴霧し、本発明の粒子状医薬組成物を製造した(流動層造粒装置条件:送液量7.0g/min、噴霧空気圧0.2MPa)。
実施例1にて調製した第1層を被覆した粒子300.0gに対し、メチルセルロース 196.1gを精製水 4707.0gに溶解した液を、流動層造粒装置を用いて噴霧し、第2層を被覆した粒子を調製した(流動層造粒装置条件:送液量6.6g/min、噴霧空気圧0.25MPa)。
HPMC 8.1gを精製水456.0gに溶解した液にメタノール1824.0gを添加・混合し、HPMC液(水・アルコール混液)を調製した。このHPMC液に、続いてオイドラギットE 71.2gを溶解させ、タルク40.7gを添加し分散させた。この分散液を、流動層造粒装置を用いて第2層を被覆した薬物含有粒子300.0gに対して噴霧し、本発明の粒子状医薬組成物を製造した(流動層造粒装置条件:送液量7.0g/min、噴霧空気圧0.18MPa)。得られた粒子状医薬組成物の平均粒子径は247μmであった。
ラウリル硫酸ナトリウム180.0gおよびHPMC 120.0gを精製水2400.0gに溶解した液に、アトルバスタチンカルシウム三水和物300.0gを攪拌下添加し、分散液を調製した。調製した分散液を流動層造粒装置を用いて、結晶セルロース(粒)500.0gに噴霧し、第1層を被覆した粒子を調製した(流動層造粒条件:送液量6.0g/min、噴霧空気圧0.20MPa)。
第1層を被覆した粒子670.0gに対し、クエン酸ナトリウム二水和物114.5gおよびメチルセルロース100.5gを精製水2656.4gに溶解した液を、流動層造粒装置を用いて噴霧し、第2層を被覆した粒子を調製した(流動層造粒条件:送液量7.0g/min、噴霧空気圧0.28MPa)。
HPMC 9.28gを精製水432.0gに溶解した液にメタノール 1727.4gを添加・混合し、HPMC液(水・アルコール混液)を調製した。このHPMC液に、続いてオイドラギットE 81.2gを添加し溶解させ、タルク23.2gを添加し分散させた。この分散液を、流動層造粒装置を用いて第2層を被覆した粒子284.2gに対して噴霧し、本発明の粒子状医薬組成物を製造した(流動層造粒条件:送液量7.0g/min、噴霧空気圧0.20MPa)。
マンニトール15.0gを精製水135.0gに溶解した。このマンニトール溶液を、流動層造粒装置を用いて第3層を被覆した粒子300.0gに対して噴霧し、本発明の粒子状医薬組成物(マスキング粒子)を製造した(流動層造粒条件:送液量5.0g/min、噴霧空気圧0.18MPa)。
HPMC 7.8gを精製水440.0gに溶解した液にメタノール1760.2gを添加・混合し、HPMC液(水・アルコール混液)を調製した。このHPMC液に、続いてオイドラギットE 84.0gを添加し溶解させ、タルク24.0gを添加し分散させた。この分散液を、流動層造粒装置を用いて実施例11で調製した第2層を被覆した粒子289.5gに対して噴霧し、本発明の粒子状医薬組成物を製造した(流動層造粒条件:送液量7.0g/min、噴霧空気圧0.20MPa)。
マンニトール15.0gを精製水135.0gに溶解した。このマンニトール溶液を、流動層造粒装置を用いて第3層を被覆した粒子300.0gに対して噴霧し、本発明の粒子状医薬組成物(マスキング粒子)を製造した(流動層造粒条件:送液量5.0g/min、噴霧空気圧0.18MPa)。
ラウリル硫酸ナトリウム3.25kgおよびHPMC 2.17kgを精製水43.36kgに溶解した液に、アトルバスタチンカルシウム三水和物5.42kgを攪拌下添加し、分散液を調製した。調製した分散液を流動層造粒装置を用いて、結晶セルロース(粒)5.42kgに噴霧し、第1層を被覆した粒子を調製した(流動層造粒条件:送液量80g/min、噴霧空気圧0.35MPa)。
第1層を被覆した粒子7.8kgに対し、クエン酸ナトリウム二水和物1.33kgおよびメチルセルロース1.17kgを精製水30.96kgに溶解した液を、流動層造粒装置を用いて噴霧し、第2層を被覆した粒子を調製した(流動層造粒条件:送液量90g/min、噴霧空気圧0.35MPa)。
精製水15.67kg、メタノール 62.67kgからなる混液にHPMC 0.28kg、オイドラギットE 2.45kgさらにタルク1.4kgを添加し分散液を調製した。この分散液を、流動層造粒装置を用いて、第2層を被覆した粒子10.30kgに対して噴霧し、本発明の粒子状医薬組成物を製造した(流動層造粒条件:送液量90g/min、噴霧空気圧0.45MPa)。
マンニトール0.72kgを精製水6.28kgに溶解した。このマンニトール溶液を、流動層造粒装置を用いて第3層を被覆した粒子14.43kgに対して噴霧し、本発明の粒子状医薬組成物(マスキング粒子)を製造した(流動層造粒条件:送液量100g/min、噴霧空気圧0.35MPa)。
実施例13で調製した第1層を被覆した粒子710.0gに対し、クエン酸ナトリウム二水和物121.4gおよびメチルセルロース106.5gを精製水2815gに溶解した液を、流動層造粒装置を用いて噴霧し、第2層を被覆した粒子を調製した(流動層造粒条件:送液量 6.0g/min、噴霧空気圧0.20MPa)。
HPMC(信越化学工業社製、製品名TC-5S)8.1gを精製水456.0gに溶解した液にメタノール1824.0gを添加・混合し、HPMC液(水・アルコール混液)を調製した。このHPMC液に、続いてオイドラギットE 71.2gを添加し溶解させ、タルク40.7gを添加し分散させた。この分散液を、流動層造粒装置を用いて調製した第2層を被覆した粒子300.0gに対して噴霧し、本発明の粒子状医薬組成物を製造した(流動層造粒条件:送液量6.2g/min、噴霧空気圧0.22MPa)。
ヒドロキシプロピルセルロース(日本曹達社製、製品名HPC-SL)8.1gを精製水456.0gに溶解した液にメタノール1824.0gを添加・混合し、HPMC液(水・アルコール混液)を調製した。このHPMC液に、続いてオイドラギットE 71.2gを添加し溶解させ、タルク40.7gを添加し分散させた。この分散液を、流動層造粒装置を用いて実施例14で調製した第2層を被覆した粒子300.0gに対して噴霧し、本発明の粒子状医薬組成物を製造した(流動層造粒条件:送液量7.0g/min、噴霧空気圧0.18MPa)。
ポリビニルアルコール(日本合成化学社製、製品名ゴーセノールEG-05)8.1gを精製水456.0gに溶解した液にメタノール1824.0gを添加・混合し、HPMC液(水・アルコール混液)を調製した。このHPMC液に、続いてオイドラギットE 71.2gを添加し溶解させ、タルク40.7gを添加し分散させた。この分散液を、流動層造粒装置を用いて実施例14で調製した第2層を被覆した粒子300.0gに対して噴霧し、本発明の粒子状医薬組成物を製造した(流動層造粒条件:送液量7.0g/min、噴霧空気圧0.22MPa)。
ポリビニルアルコール―ポリエチレングリコールグラフトコポリマー(BASF製、製品名Kollicoat IR)8.1gを精製水456.0gに溶解した液にメタノール1824.0gを添加・混合し、HPMC液(水・アルコール混液)を調製した。このHPMC液に、続いてオイドラギットE 71.2gを添加し溶解させ、タルク40.7gを添加し分散させた。この分散液を、流動層造粒装置を用いて実施例14で調製した第2層を被覆した粒子300.0gに対して噴霧し、本発明の粒子状医薬組成物を製造した(流動層造粒条件:送液量7.0g/min、噴霧空気圧0.18MPa)。
ポリビニルピロリドン(和光製、製品名 ポリビニルピロリドンK30)8.1gを精製水456.0gに溶解した液にメタノール1824.0gを添加・混合し、HPMC液(水・アルコール混液)を調製した。このHPMC液に、続いてオイドラギットE 71.2gを添加し溶解させ、タルク40.7gを添加し分散させた。この分散液を、流動層造粒装置を用いて実施例14で調製した第2層を被覆した粒子300.0gに対して噴霧し、本発明の粒子状医薬組成物を製造した(流動層造粒条件:送液量7.0g/min、噴霧空気圧0.18MPa)。
ラウリル硫酸ナトリウム180.0gおよびHPMC 120.0gを精製水2400.0gに溶解した液に、フルルビプロフェン300.0gを攪拌下添加し、分散液を調製する。調製した分散液を流動層造粒装置を用いて、結晶セルロース(粒)300.0gに噴霧し、第1層を被覆した粒子を調製する(流動層造粒条件:送液量6.0g/min、噴霧空気圧0.20MPa)。
第1層を被覆した粒子670.0gに対し、クエン酸ナトリウム二水和物114.5gおよびメチルセルロース100.5gを精製水2656.4gに溶解した液を、流動層造粒装置を用いて噴霧し、第2層を被覆した粒子を調製する(流動層造粒条件:送液量7.0g/min、噴霧空気圧0.28MPa)。
HPMC 8.1gを精製水456.0gに溶解した液にメタノール1824.0gを添加・混合し、HPMC液(水・アルコール混液)を調製する。このHPMC液に、続いてオイドラギットE 71.2gを添加し溶解させ、タルク40.7gを添加し分散させる。この分散液を、流動層造粒装置を用いて第2層を被覆した粒子300.0gに対して噴霧し、本発明の粒子状医薬組成物を製造する(流動層造粒条件:送液量7.0g/min、噴霧空気圧0.20MPa)。
ラウリル硫酸ナトリウム180.0gおよびHPMC 120.0gを精製水2400.0gに溶解した液に、イブプロフェン300.0gを攪拌下添加し、分散液を調製する。調製した分散液を流動層造粒装置を用いて、結晶セルロース(粒)300.0gに噴霧し、第1層を被覆した粒子を調製する(流動層造粒条件:送液量6.0g/min、噴霧空気圧0.20MPa)。
第1層を被覆した粒子670.0gに対し、クエン酸ナトリウム二水和物114.5gおよびメチルセルロース100.5gを精製水2656.4gに溶解した液を、流動層造粒装置を用いて噴霧し、第2層を被覆した粒子を調製する(流動層造粒条件:送液量7.0g/min、噴霧空気圧0.28MPa)。
HPMC 8.1gを精製水456.0gに溶解した液にメタノール1824.0gを添加・混合し、HPMC液(水・アルコール混液)を調製する。このHPMC液に、続いてオイドラギットE 71.2gを添加し溶解させ、タルク40.7gを添加し分散させる。この分散液を、流動層造粒装置を用いて第2層を被覆した粒子300.0gに対して噴霧し、本発明の粒子状医薬組成物を製造する(流動層造粒条件:送液量7.0g/min、噴霧空気圧0.20MPa)。
ラウリル硫酸ナトリウム180.0gおよびHPMC 120.0gを精製水2400.0gに溶解した液に、ナプロキセン300.0gを攪拌下添加し、分散液を調製する。調製した分散液を流動層造粒装置を用いて、結晶セルロース(粒)300.0gに噴霧し、第1層を被覆した粒子を調製する(流動層造粒条件:送液量6.0g/min、噴霧空気圧0.20MPa)。
第1層を被覆した粒子670.0gに対し、クエン酸ナトリウム二水和物114.5gおよびメチルセルロース100.5gを精製水2656.4gに溶解した液を、流動層造粒装置を用いて噴霧し、第2層を被覆した粒子を調製する(流動層造粒条件:送液量7.0g/min、噴霧空気圧0.28MPa)。
HPMC 8.1gを精製水456.0gに溶解した液にメタノール1824.0gを添加・混合し、HPMC液(水・アルコール混液)を調製する。このHPMC液に、続いてオイドラギットE 71.2gを添加し溶解させ、タルク40.7gを添加し分散させる。この分散液を、流動層造粒装置を用いて第2層を被覆した粒子300.0gに対して噴霧し、本発明の粒子状医薬組成物を製造する(流動層造粒条件:送液量7.0g/min、噴霧空気圧0.20MPa)。
ラウリル硫酸ナトリウム180.0gおよびHPMC 120.0gを精製水2400.0gに溶解した液に、ケトプロフェン300.0gを攪拌下添加し、分散液を調製する。調製した分散液を流動層造粒装置を用いて、結晶セルロース(粒)300.0gに噴霧し、第1層を被覆した粒子を調製する(流動層造粒条件:送液量6.0g/min、噴霧空気圧0.20MPa)。
第1層を被覆した粒子670.0gに対し、クエン酸ナトリウム二水和物114.5gおよびメチルセルロース100.5gを精製水2656.4gに溶解した液を、流動層造粒装置を用いて噴霧し、第2層を被覆した粒子を調製する(流動層造粒条件:送液量7.0g/min、噴霧空気圧0.28MPa)。
HPMC 8.1gを精製水456.0gに溶解した液にメタノール1824.0gを添加・混合し、HPMC液(水・アルコール混液)を調製する。このHPMC液に、続いてオイドラギットE 71.2gを添加し溶解させ、タルク40.7gを添加し分散させる。この分散液を、流動層造粒装置を用いて第2層を被覆した粒子300.0gに対して噴霧し、本発明の粒子状医薬組成物を製造する(流動層造粒条件:送液量7.0g/min、噴霧空気圧0.20MPa)。
コハク酸ソリフェナシン333.3gおよびマクロゴール6000(三洋化成工業製、以下同じ)111.1gをメタノール 552.6gと精製水552.6gの混合液に溶解し薬物溶液を調製した。調製した薬物溶液を流動層造粒装置を用いて、結晶セルロース(粒)555.6gに噴霧し、第1層を被覆した粒子を調製した(流動層造粒装置条件:送液量6.1g/min、噴霧空気圧0.24MPa)。
第1層を被覆した粒子666.6gに対し、リン酸二水素ナトリウム二水和物(関東化学製)216.7gおよびメチルセルロース166.7gを精製水4378.1に溶解した液を、流動層造粒装置を用いて噴霧し、第1層を被覆した粒子を調製した(流動層造粒装置条件:送液量7.2g/min、噴霧空気圧0.20MPa)。
オイドラギットNE30D 33.3gと精製水356.7gの混合液にタルク10.0gを分散させた。この分実気を、流動層造粒装置を用いて、第2層を被覆した粒子200.0gに対して噴霧し、比較例3の粒子状医薬組成物を製造した(流動層造粒装置条件:送液量7.0g/min、噴霧空気圧0.20MPa)。
ラウリル硫酸ナトリウム135.0gおよびHPMC 90.0gを精製水 1800.0gに溶解した液に、アトルバスタチンカルシウム三水和物225.0gを攪拌下添加して、分散液を調製した。調製した分散液を流動層造粒装置を用いて、結晶セルロース(粒)500gに噴霧し、第1層を被覆した粒子を調製した(流動層造粒装置条件:送液量7.0g/min、噴霧空気圧0.20MPa)。
第1層を被覆した粒子800.0gに対し、メチルセルロース40.0gを精製水960.0gに溶解した液を、流動層造粒装置を用いて噴霧し、第2層を被覆した粒子を調製した(流動層造粒装置条件:送液量5.0g/min、噴霧空気圧0.23MPa)。
第2層を被覆した粒子400gに対して、クエン酸ナトリウム二水和物114.0gおよびメチルセルロース100.0gを精製水2643.2gに溶解した液を、流動層造粒装置を用いて噴霧し、第3層を被覆した粒子を調製した(流動層造粒装置条件:送液量7.0g/min、噴霧空気圧0.25MPa)。
第3層を被覆した粒子600.0gに対して、メチルセルロース30.0gを精製水720.0gに溶解した液を流動層造粒装置を用いて噴霧し、第4層を被覆した粒子を調製した(流動層造粒装置条件:送液量6.6g/min、噴霧空気圧0.25MPa)。
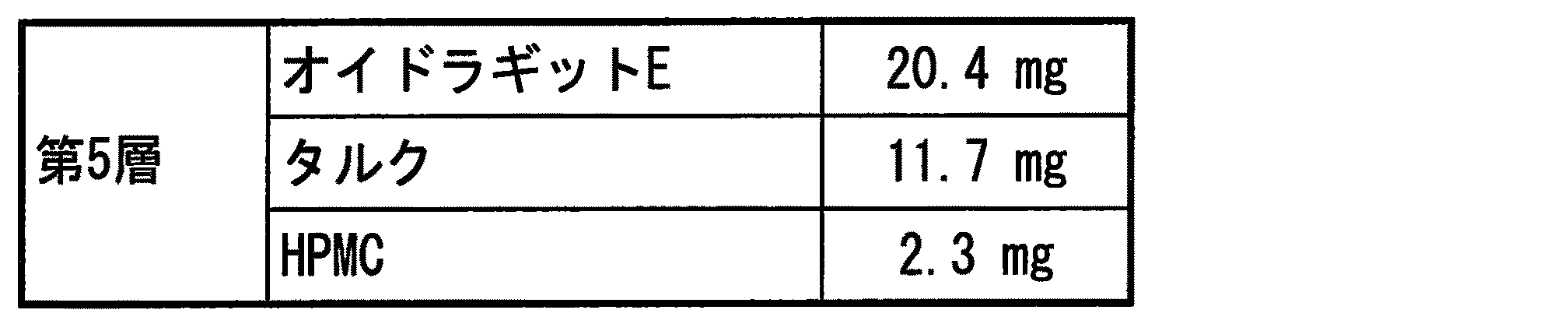
精製水136.8gおよびメタノール1231.2gからなる混液にオイドラギットE 45.8gを添加し溶解させ、タルク26.2gを添加し分散させた。この分散液を、流動層造粒装置を用いて、第4層を被覆した薬物含有粒子300.0gに対して噴霧した(流動層造粒装置条件:送液量5.2g/min、噴霧空気圧0.22MPa)。
HPMC 25.0gを精製水600.0gに添加し溶解させた。このHPMC溶液を、流動層造粒装置を用いて、第5層を被覆した薬物含有粒子250.0gに対して噴霧し比較例4の粒子状医薬組成物を調製した(流動層造粒装置条件:送液量5.0g/min、噴霧空気圧0.20MPa)。
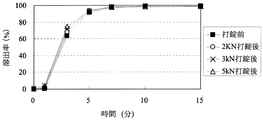
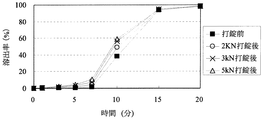
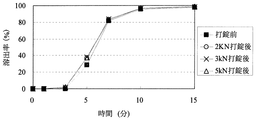
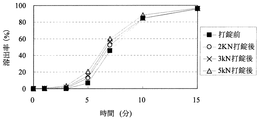
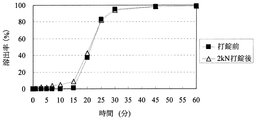
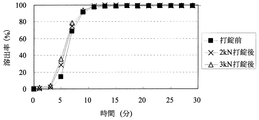
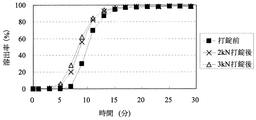
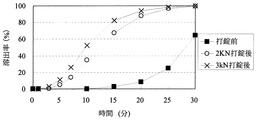
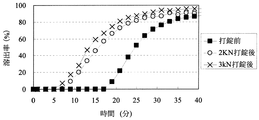
[粒子状医薬組成物の溶出試験]
実施例4〜14、16〜18または比較例1〜3の粒子状医薬組成物(打錠前)及びそれらを含有する口腔内崩壊錠(打錠後)について自動6連溶出試験機を用いて、日本薬局方溶出試験法第2法に従い溶出試験を行った。対照試料として、薬物を10mgを含む粒子を量り取った。試験液は水900mLを用いた。比較例3は日本薬局方崩壊試験第2液(JP2)900mLを用いた。なおパドルの回転数は100回転/分であった。
DT2%溶出変化(%)=DT2%-2(%)
DT50%溶出変化(%)=DT5%-50(%)
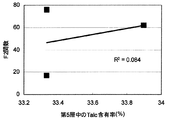
溶出挙動の同等性を評価する指標としてf2関数が知られている。f2関数の値は次の式で表す。
本発明は、不快な味を有する薬物による不快感を軽減し、コンプライアンスを向上させることが出来る。また、圧縮成形による粒子状医薬組成物の核部からの薬物溶出を低減することが出来る。更に、一定時間後に薬物が速やかに放出することによって消化管上部で薬物が放出し薬物が十分な薬効を発現することができる。
本発明は、幅広い物性を有する薬物に適用することが出来る。
以上、本発明を特定の態様に沿って説明したが、当業者に自明の変形や改良は本発明の範囲に含まれる。
Claims (20)
- 薬物含有粒子が、メタアクリル酸メチル・メタアクリル酸ブチル・メタアクリル酸ジメチルアミノエチル共重合体、および水溶性高分子物質を含む被膜物質により被覆されてなる、経口投与用粒子状医薬組成物。
- さらに被膜物質に流動化剤を含有する、請求項1に記載の経口投与用粒子状医薬組成物。
- 水溶性高分子物質が、ヒドロキシプロピルセルロース、ヒドロキシプロピルメチルセルロース、メチルセルロース、ヒドロキシエチルセルロース、ポビドン、コポリビドン、ポリビニルアルコール−ポリエチレングリコールグラフトコポリマー、ポリビニルアルコール、マクロゴール、およびポリエチレンオキサイドからなる群より選択される1種または2種以上である、請求項1または2に記載の経口投与用粒子状医薬組成物。
- 水溶性高分子物質が、ヒドロキシプロピルセルロース、ヒドロキシプロピルメチルセルロース、メチルセルロース、およびヒドロキシエチルセルロースからなる群より選択される1種または2種以上である、請求項1〜3のいずれか一項に記載の経口投与用粒子状医薬組成物。
- 水溶性高分子物質の量が、メタアクリル酸メチル・メタアクリル酸ブチル・メタアクリル酸ジメチルアミノエチル共重合体の量に対して1重量%以上30重量%以下である、請求項1〜4のいずれか一項に記載の経口投与用粒子状医薬組成物。
- 流動化剤が、ケイ酸金属類、二酸化ケイ素類、高級脂肪酸金属塩類、金属酸化物類、アルカリ土類金属塩、および金属水酸化物からなる群より選択される1種または2種以上である、請求項1〜5のいずれか一項に記載の経口投与用粒子状医薬組成物。
- 流動化剤が、タルク、カオリン、ケイ酸カルシウム、ケイ酸マグネシウム、軽質無水ケイ酸、ステアリン酸マグネシウム、ステアリン酸カルシウム、酸化鉄、酸化チタン、炭酸カルシウム、リン酸カルシウム、セッコウ、炭酸マグネシウム、水酸化アルミニウム、含水二酸化ケイ素、結晶セルロース、合成ケイ酸アルミニウム、重質無水ケイ酸、水酸化アルミナマグネシウム、ステアリン酸、トウモロコシデンプン、メタケイ酸アルミン酸マグネシウム、リン酸水素カルシウム造粒物、およびグリセリルモノステアレートからなる群より選択される1種または2種以上である、請求項1〜6のいずれか一項に記載の経口投与用粒子状医薬組成物。
- 流動化剤が、タルク、カオリン、ケイ酸カルシウム、ケイ酸マグネシウム、軽質無水ケイ酸、ステアリン酸マグネシウム、およびグリセリルモノステアレートからなる群より選択される1種または2種以上である、請求項1〜7のいずれか一項に記載の経口投与用粒子状医薬組成物。
- 流動化剤の量が、メタアクリル酸メチル・メタアクリル酸ブチル・メタアクリル酸ジメチルアミノエチル共重合体の量に対して1重量%以上500重量%以下である、請求項1〜8のいずれか一項に記載の経口投与用粒子状医薬組成物。
- 水溶性高分子物質がヒドロキシプロピルメチルセルロースであり、かつメタアクリル酸メチル・メタアクリル酸ブチル・メタアクリル酸ジメチルアミノエチル共重合体の量に対して1重量%以上30重量%以下である、請求項1〜9のいずれか一項に記載の経口投与用粒子状医薬組成物。
- 薬物が酸性薬物またはその塩である、請求項1〜10のいずれか一項に記載の経口投与用粒子状医薬組成物。
- 薬物が不快な味を有する、請求項1〜11のいずれか一項に記載の経口投与用粒子状医薬組成物。
- 請求項1〜12のいずれか一項に記載の経口投与用粒子状医薬組成物において、(1)(i)メタアクリル酸メチル・メタアクリル酸ブチル・メタアクリル酸ジメチルアミノエチル共重合体、および水溶性高分子物質からなる被膜物質による被覆層の内側に、または(ii)メタアクリル酸メチル・メタアクリル酸ブチル・メタアクリル酸ジメチルアミノエチル共重合体、水溶性高分子物質、および流動化剤からなる被膜物質による被覆層の内側に、(2)1種または2種以上の水溶性の不溶化促進剤、及び1種または2種以上の水溶性の不溶化物質を含有する層を有する、請求項1〜12のいずれか一項に記載の経口投与用粒子状医薬組成物。
- 請求項1〜13のいずれか一項に記載の経口投与用粒子状医薬組成物を含有してなる口腔内崩壊錠。
- 薬物含有粒子が、メタアクリル酸メチル・メタアクリル酸ブチル・メタアクリル酸ジメチルアミノエチル共重合体、および水溶性高分子物質を含む被膜物質により被覆することを特徴とする、経口投与用粒子状医薬組成物の製造方法。
- さらに被膜物質に流動化剤を含有する、請求項15に記載の経口投与用粒子状医薬組成物の製造方法。
- 水溶性高分子物質が、ヒドロキシプロピルセルロース、ヒドロキシプロピルメチルセルロース、メチルセルロース、ヒドロキシエチルセルロース、ポビドン、コポリビドン、ポリビニルアルコール−ポリエチレングリコールグラフトコポリマー、ポリビニルアルコール、マクロゴール、およびポリエチレンオキサイドからなる群より選択される1種または2種以上である、請求項15または16に記載の経口投与用粒子状医薬組成物の製造方法。
- 流動化剤が、ケイ酸金属類、二酸化ケイ素類、高級脂肪酸金属塩類、金属酸化物類、アルカリ土類金属塩、および金属水酸化物からなる群より選択される1種または2種以上である、請求項15〜17のいずれか一項に記載の経口投与用粒子状医薬組成物の製造方法。
- 請求項1〜12のいずれか一項に記載の経口投与用粒子状医薬組成物の製造方法であって、(1)薬物含有粒子の外側に、水溶性の不溶化促進剤及び水溶性の不溶化物質を含有する層を形成する工程、(2)得られた粒子を、(i)メタアクリル酸メチル・メタアクリル酸ブチル・メタアクリル酸ジメチルアミノエチル共重合体、および水溶性高分子物質からなる被膜物質、または(ii)メタアクリル酸メチル・メタアクリル酸ブチル・メタアクリル酸ジメチルアミノエチル共重合体、水溶性高分子物質、および流動化剤からなる被膜物質により被覆する工程を含む、前記製造方法。
- メタアクリル酸メチル・メタアクリル酸ブチル・メタアクリル酸ジメチルアミノエチル共重合体とともに、薬物含有粒子を被覆し、圧縮成形後も放出速度の変化を低減する経口投与用粒子状医薬組成物を製造するための水溶性高分子物質の使用。
Applications Claiming Priority (4)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US10137908P | 2008-09-30 | 2008-09-30 | |
| US10139408P | 2008-09-30 | 2008-09-30 | |
| US61/101,394 | 2008-09-30 | ||
| US61/101,379 | 2008-09-30 |
Related Child Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2010188328A Division JP5282772B2 (ja) | 2008-09-30 | 2010-08-25 | 経口投与用粒子状医薬組成物 |
Publications (3)
| Publication Number | Publication Date |
|---|---|
| JP2010083886A true JP2010083886A (ja) | 2010-04-15 |
| JP2010083886A5 JP2010083886A5 (ja) | 2010-10-07 |
| JP4706785B2 JP4706785B2 (ja) | 2011-06-22 |
Family
ID=42073455
Family Applications (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2009222020A Expired - Fee Related JP4706785B2 (ja) | 2008-09-30 | 2009-09-28 | 経口投与用粒子状医薬組成物 |
| JP2010188328A Expired - Fee Related JP5282772B2 (ja) | 2008-09-30 | 2010-08-25 | 経口投与用粒子状医薬組成物 |
Family Applications After (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2010188328A Expired - Fee Related JP5282772B2 (ja) | 2008-09-30 | 2010-08-25 | 経口投与用粒子状医薬組成物 |
Country Status (3)
| Country | Link |
|---|---|
| US (1) | US20100136110A1 (ja) |
| JP (2) | JP4706785B2 (ja) |
| WO (1) | WO2010038691A1 (ja) |
Cited By (7)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2011144120A (ja) * | 2010-01-13 | 2011-07-28 | Towa Yakuhin Kk | HMG−CoAレダクターゼ阻害剤含有経口固形製剤 |
| WO2011121824A1 (ja) * | 2010-03-29 | 2011-10-06 | アステラス製薬株式会社 | 口腔内崩壊錠 |
| WO2011121823A1 (ja) * | 2010-03-29 | 2011-10-06 | アステラス製薬株式会社 | 経口投与用粒子状医薬組成物 |
| JP2014516961A (ja) * | 2011-05-16 | 2014-07-17 | サン・ファーマ・アドバンスド・リサーチ・カンパニー・リミテッド | 多粒子医薬組成物 |
| JP2015067608A (ja) * | 2013-09-27 | 2015-04-13 | キョーリンリメディオ株式会社 | テルミサルタン含有製剤及びその製造方法 |
| JP2018070657A (ja) * | 2012-11-30 | 2018-05-10 | アキュラ・ファーマシューティカルズ・インコーポレーテッド | 活性医薬成分の自己制御放出 |
| JP2022106927A (ja) * | 2016-03-15 | 2022-07-20 | エイサー セラピューティクス インコーポレーテッド | フェニル酪酸ナトリウムを含む口当たりの良い組成物及びその使用 |
Families Citing this family (13)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP6073543B2 (ja) * | 2010-07-08 | 2017-02-01 | 沢井製薬株式会社 | ロラタジン含有口腔内崩壊錠の製造方法 |
| WO2012056509A1 (ja) * | 2010-10-25 | 2012-05-03 | 興和株式会社 | 医薬組成物 |
| EP2500013B1 (en) * | 2011-03-15 | 2019-10-02 | Alfred E. Tiefenbacher (GmbH & Co. KG) | Pharmaceutical composition comprising solifenacin |
| FI126168B (en) | 2012-09-18 | 2016-07-29 | Novaldmedical Ltd Oy | A method for coating pharmaceutical substrates |
| CN104042628B (zh) * | 2013-03-15 | 2017-04-12 | 复旦大学 | 氢氧化铝在制备治疗肝癌药物中的应用 |
| SI3033076T1 (sl) * | 2013-08-14 | 2021-01-29 | Evonik Operations Gmbh | Sestavek za oplaščenje |
| EP3398588A4 (en) * | 2015-12-28 | 2019-10-02 | Nippon Shinyaku Co., Ltd. | COMPRESSION MOLDED PREPARATION |
| US20190054029A1 (en) * | 2016-02-23 | 2019-02-21 | Nipro Corporation | Pharmaceutical composition particles, orally disintegrating preparation including same, and method for producing pharmaceutical composition particles |
| WO2018065826A1 (en) * | 2016-10-06 | 2018-04-12 | Sucampo Ag | Multilayer beads for pharmaceutical use |
| US11696895B2 (en) | 2017-12-28 | 2023-07-11 | Sumitomo Pharma Co., Ltd. | Fine particle coating (drug-containing hollow particle and method for manufacturing same) |
| CN111712235A (zh) | 2018-01-16 | 2020-09-25 | 应用材料公司 | 金属氧化物包封的药物组合物及其制备方法 |
| WO2021041675A1 (en) * | 2019-08-27 | 2021-03-04 | Applied Materials, Inc. | Vapor phase coatings for pharmaceutical solubility control |
| TW202216124A (zh) | 2020-10-02 | 2022-05-01 | 美商應用材料股份有限公司 | 製備氧化矽塗佈藥品的低溫處理 |
Citations (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPS61501150A (ja) * | 1984-02-10 | 1986-06-12 | ベンツォン ファーマ エイ/エス | 拡散被覆された複合単位服用剤 |
| JPH08333242A (ja) * | 1995-06-09 | 1996-12-17 | Tanabe Seiyaku Co Ltd | 圧縮成型製剤 |
| JP2000273037A (ja) * | 1999-03-19 | 2000-10-03 | Kyoto Pharmaceutical Industries Ltd | 解熱・鎮痛チュアブル錠およびその製造法 |
| WO2005105045A1 (ja) * | 2004-04-30 | 2005-11-10 | Astellas Pharma Inc. | 経口投与用時限放出型粒子状医薬組成物及び該組成物を含有する口腔内速崩壊錠 |
| JP2007211006A (ja) * | 2006-01-16 | 2007-08-23 | Ono Pharmaceut Co Ltd | 溶出安定性を有するコーティング固形製剤 |
| WO2007110875A1 (en) * | 2006-03-24 | 2007-10-04 | Panacea Biotec Ltd. | Antibiotic compositions of modified release and process of production thereof |
Family Cites Families (7)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| DK62184D0 (da) * | 1984-02-10 | 1984-02-10 | Benzon As Alfred | Diffusionsovertrukket polydepotpraeparat |
| US4800087A (en) * | 1986-11-24 | 1989-01-24 | Mehta Atul M | Taste-masked pharmaceutical compositions |
| US5576014A (en) * | 1994-01-31 | 1996-11-19 | Yamanouchi Pharmaceutical Co., Ltd | Intrabuccally dissolving compressed moldings and production process thereof |
| TR199901564T2 (xx) * | 1997-01-06 | 1999-09-21 | Pfizer Inc. | H�zl� ��z�lebilen ve tat-maskesi sa�layan dozaj ispen�iyari formu. |
| US6872405B2 (en) * | 2001-05-10 | 2005-03-29 | Yamanouchi Pharmaceutical Co., Ltd. | Quick-disintegrating tablet in buccal cavity and manufacturing method thereof |
| WO2007126136A2 (en) * | 2006-04-27 | 2007-11-08 | Takeda Pharmaceutical Company Limited | Mask- tasting solid preparation of pioglitazone |
| WO2008032767A1 (fr) * | 2006-09-14 | 2008-03-20 | Astellas Pharma Inc. | Comprimé se désintegrant oralement et procédé de fabrication de celui-ci |
-
2009
- 2009-09-28 JP JP2009222020A patent/JP4706785B2/ja not_active Expired - Fee Related
- 2009-09-28 US US12/568,257 patent/US20100136110A1/en not_active Abandoned
- 2009-09-28 WO PCT/JP2009/066743 patent/WO2010038691A1/ja active Application Filing
-
2010
- 2010-08-25 JP JP2010188328A patent/JP5282772B2/ja not_active Expired - Fee Related
Patent Citations (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPS61501150A (ja) * | 1984-02-10 | 1986-06-12 | ベンツォン ファーマ エイ/エス | 拡散被覆された複合単位服用剤 |
| JPH08333242A (ja) * | 1995-06-09 | 1996-12-17 | Tanabe Seiyaku Co Ltd | 圧縮成型製剤 |
| JP2000273037A (ja) * | 1999-03-19 | 2000-10-03 | Kyoto Pharmaceutical Industries Ltd | 解熱・鎮痛チュアブル錠およびその製造法 |
| WO2005105045A1 (ja) * | 2004-04-30 | 2005-11-10 | Astellas Pharma Inc. | 経口投与用時限放出型粒子状医薬組成物及び該組成物を含有する口腔内速崩壊錠 |
| JP2007211006A (ja) * | 2006-01-16 | 2007-08-23 | Ono Pharmaceut Co Ltd | 溶出安定性を有するコーティング固形製剤 |
| WO2007110875A1 (en) * | 2006-03-24 | 2007-10-04 | Panacea Biotec Ltd. | Antibiotic compositions of modified release and process of production thereof |
Cited By (7)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2011144120A (ja) * | 2010-01-13 | 2011-07-28 | Towa Yakuhin Kk | HMG−CoAレダクターゼ阻害剤含有経口固形製剤 |
| WO2011121824A1 (ja) * | 2010-03-29 | 2011-10-06 | アステラス製薬株式会社 | 口腔内崩壊錠 |
| WO2011121823A1 (ja) * | 2010-03-29 | 2011-10-06 | アステラス製薬株式会社 | 経口投与用粒子状医薬組成物 |
| JP2014516961A (ja) * | 2011-05-16 | 2014-07-17 | サン・ファーマ・アドバンスド・リサーチ・カンパニー・リミテッド | 多粒子医薬組成物 |
| JP2018070657A (ja) * | 2012-11-30 | 2018-05-10 | アキュラ・ファーマシューティカルズ・インコーポレーテッド | 活性医薬成分の自己制御放出 |
| JP2015067608A (ja) * | 2013-09-27 | 2015-04-13 | キョーリンリメディオ株式会社 | テルミサルタン含有製剤及びその製造方法 |
| JP2022106927A (ja) * | 2016-03-15 | 2022-07-20 | エイサー セラピューティクス インコーポレーテッド | フェニル酪酸ナトリウムを含む口当たりの良い組成物及びその使用 |
Also Published As
| Publication number | Publication date |
|---|---|
| JP2010265325A (ja) | 2010-11-25 |
| WO2010038691A1 (ja) | 2010-04-08 |
| US20100136110A1 (en) | 2010-06-03 |
| JP5282772B2 (ja) | 2013-09-04 |
| JP4706785B2 (ja) | 2011-06-22 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP4706785B2 (ja) | 経口投与用粒子状医薬組成物 | |
| JP4277904B2 (ja) | 経口投与用時限放出型粒子状医薬組成物及び該組成物を含有する口腔内速崩壊錠 | |
| JP4019374B2 (ja) | 口腔内速崩壊錠用徐放性微粒子含有組成物およびその製造法 | |
| JP6092936B2 (ja) | 口腔内崩壊錠の製造方法 | |
| JP5534004B2 (ja) | 口腔内崩壊錠 | |
| JP5750847B2 (ja) | アトルバスタチン経口投与用粒子状医薬組成物 | |
| JP2009114113A (ja) | 口腔内崩壊錠及びその製造方法 | |
| JP6098634B2 (ja) | 速崩壊性錠剤 | |
| WO2019151405A1 (ja) | 錠剤及びその製造方法 | |
| JP5824524B2 (ja) | ヒドロキシアルキルセルロース微粒子を含有する口腔内崩壊錠 | |
| US20050175689A1 (en) | Coated fine particles containing drug for intrabuccally fast disintegrating tablet | |
| JP5614445B2 (ja) | 経口投与用粒子状医薬組成物 | |
| JP4965096B2 (ja) | 圧縮成型製剤 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20100825 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20100825 |
|
| A871 | Explanation of circumstances concerning accelerated examination |
Free format text: JAPANESE INTERMEDIATE CODE: A871 Effective date: 20100825 |
|
| A975 | Report on accelerated examination |
Free format text: JAPANESE INTERMEDIATE CODE: A971005 Effective date: 20100915 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20100928 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20101129 |
|
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20110215 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20110228 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20140325 Year of fee payment: 3 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20140325 Year of fee payment: 3 |
|
| S531 | Written request for registration of change of domicile |
Free format text: JAPANESE INTERMEDIATE CODE: R313531 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20140325 Year of fee payment: 3 |
|
| R350 | Written notification of registration of transfer |
Free format text: JAPANESE INTERMEDIATE CODE: R350 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| LAPS | Cancellation because of no payment of annual fees |