JP2010046068A - トランスポーター阻害物質スクリーニング方法 - Google Patents
トランスポーター阻害物質スクリーニング方法 Download PDFInfo
- Publication number
- JP2010046068A JP2010046068A JP2009220017A JP2009220017A JP2010046068A JP 2010046068 A JP2010046068 A JP 2010046068A JP 2009220017 A JP2009220017 A JP 2009220017A JP 2009220017 A JP2009220017 A JP 2009220017A JP 2010046068 A JP2010046068 A JP 2010046068A
- Authority
- JP
- Japan
- Prior art keywords
- transporter
- virus
- activity
- membrane
- expressing
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Granted
Links
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N15/00—Mutation or genetic engineering; DNA or RNA concerning genetic engineering, vectors, e.g. plasmids, or their isolation, preparation or purification; Use of hosts therefor
- C12N15/09—Recombinant DNA-technology
- C12N15/63—Introduction of foreign genetic material using vectors; Vectors; Use of hosts therefor; Regulation of expression
- C12N15/79—Vectors or expression systems specially adapted for eukaryotic hosts
- C12N15/85—Vectors or expression systems specially adapted for eukaryotic hosts for animal cells
- C12N15/86—Viral vectors
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K14/00—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- C07K14/435—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
- C07K14/705—Receptors; Cell surface antigens; Cell surface determinants
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N7/00—Viruses; Bacteriophages; Compositions thereof; Preparation or purification thereof
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K38/00—Medicinal preparations containing peptides
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2710/00—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA dsDNA viruses
- C12N2710/00011—Details
- C12N2710/14011—Baculoviridae
- C12N2710/14111—Nucleopolyhedrovirus, e.g. autographa californica nucleopolyhedrovirus
- C12N2710/14121—Viruses as such, e.g. new isolates, mutants or their genomic sequences
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2710/00—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA dsDNA viruses
- C12N2710/00011—Details
- C12N2710/14011—Baculoviridae
- C12N2710/14111—Nucleopolyhedrovirus, e.g. autographa californica nucleopolyhedrovirus
- C12N2710/14141—Use of virus, viral particle or viral elements as a vector
- C12N2710/14143—Use of virus, viral particle or viral elements as a vector viral genome or elements thereof as genetic vector
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N2333/00—Assays involving biological materials from specific organisms or of a specific nature
- G01N2333/005—Assays involving biological materials from specific organisms or of a specific nature from viruses
- G01N2333/01—DNA viruses
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N2500/00—Screening for compounds of potential therapeutic value
- G01N2500/10—Screening for compounds of potential therapeutic value involving cells
Landscapes
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Genetics & Genomics (AREA)
- Organic Chemistry (AREA)
- Zoology (AREA)
- Engineering & Computer Science (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Wood Science & Technology (AREA)
- Biochemistry (AREA)
- General Engineering & Computer Science (AREA)
- Biotechnology (AREA)
- Biomedical Technology (AREA)
- General Health & Medical Sciences (AREA)
- Molecular Biology (AREA)
- Biophysics (AREA)
- Virology (AREA)
- Immunology (AREA)
- Medicinal Chemistry (AREA)
- Microbiology (AREA)
- Cell Biology (AREA)
- Gastroenterology & Hepatology (AREA)
- Toxicology (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Physics & Mathematics (AREA)
- Plant Pathology (AREA)
- Measuring Or Testing Involving Enzymes Or Micro-Organisms (AREA)
- Micro-Organisms Or Cultivation Processes Thereof (AREA)
Abstract
【解決手段】トランスポーターをコードする遺伝子を含む組換えウイルスを感染させた宿主を培養し、該宿主から放出される出芽ウイルス膜上にトランスポーターを発現させる方法。および、膜上に内因性トランスポーターを発現していない、出芽バキュロウイルスを用いたトランスポーター活性の測定方法。
【選択図】なし
Description
[1]トランスポーターをコードする遺伝子を含む組換えウイルスを感染させた宿主を培養し、該宿主から放出される出芽ウイルス膜上にトランスポーターを発現させることを特徴とする、トランスポーター活性を有するトランスポーターを発現させる方法、
[2]ウイルスがバキュロウイルスである[1]記載の方法、
[3]トランスポーターが非ウイルス由来である[1]または[2]いずれか記載の方法、
[4]トランスポーターがペプチドトランスポーターまたは有機アニオントランスポーターである[1]〜[3]いずれか記載の方法、
[5]トランスポーターがPepT1、PepT2又はOATP-Cである[4]記載の方法、
[6]トランスポーター活性を有するトランスポーターを発現しているウイルス、
[7]トランスポーターが非ウイルス由来である[6]記載のウイルス、
[8]ウイルスがバキュロウイルスである[7]記載のウイルス、
[9]ウイルスが出芽ウイルスである[6]〜[8]いずれか記載のウイルス、
[10]トランスポーターがペプチドトランスポーターまたは有機アニオントランスポーターである[6]〜[9]いずれか記載のウイルス、
[11]トランスポーターがPepT1、PepT2又はOATP-Cである[10]記載のウイルス、
[12]ウイルス膜上でトランスポーターを発現させることを特徴とする、トランスポーターの活性測定方法、
[13]ウイルスが出芽バキュロウイルスである[12]記載の方法、
[14]トランスポーターがペプチドトランスポーターまたは有機アニオントランスポーターである[12]または[13]記載の方法、
[15]トランスポーターがPepT1、PepT2又はOATP-Cである[14]記載の方法、
[16]以下の工程を含むトランスポーターのトランスポート活性を阻害又は促進する物質のスクリーニング方法、
(a)ウイルス膜上にトランスポーターを発現させる工程、
(b)該トランスポーターに被験物質を接触させる工程、及び
(c)トランスポート活性を阻害又は促進する物質を選択する工程
[17]ウイルスがバキュロウイルスである[16]記載の方法、
[18]ウイルスが出芽ウイルスである[16]又は[17]記載の方法、
[19]トランスポーターが非ウイルス由来である[16]〜[18]いずれか記載の方法、
[20]トランスポーターがペプチドトランスポーターまたは有機アニオントランスポーターである、[16]〜[19]いずれか記載の方法、
[21]トランスポーターがPepT1、PepT2又はOATP-Cである、[20]記載の方法、
[22]ウイルスが担体に固定されていることを特徴とする[16]〜[21]いずれか記載の方法、及び
[23]ウイルスの担体への固定が、ウイルス膜上に発現している膜タンパク質に対する抗体を介して行われていることを特徴とする[22]記載の方法、
[24]ウイルスの担体への固定が、ウイルス膜上に発現しているタンパク質をビオチン化することでビオチン・ストレプトアビジン反応を介して行われることを特徴とする請求項22記載の方法、
を提供するものである。
1. PepT1発現出芽バキュロウイルスの調製
ヒト腎臓ライブラリーからPCRを用いて完全長のPepT1遺伝子を単離した。完全長のヒトPepT1遺伝子をpBlueBacHis2A (Invitrogen) に挿入することでトランスファーベクターpBlueBacHis-PepT1を作製した後、Bac-N-Blue transfection kit (Invitrogen) を用いてBac-N-Blue DNAと共にトランスファーベクターをSf9細胞に導入することでヒトPepT1発現用組換えウイルスを調製した。即ち、4μgのpBlueBacHis-PepT1をBac-N-Blue DNAに加え、さらに1mLのGrace's培地(GIBCO)20μLのCell FECTIN試薬を加え、混和し、室温で15分間静置した後、Grace's培地で1回洗浄した2×106個のSf9細胞に滴下した。室温で4時間静置した後、さらに2mLの完全培地(10%ウシ胎児血清(Sigma社製)、100units/mLのペニシリン、及び100μg/mLストレプトマイシン(GIBCO-BRL社製)を含むGrace's培地)を加え、27℃で培養した。相同組換えにより作製されたヒトPepT1発現用組換えウイルスはキット添付の指示書に従い二度の純化を行った後、組換えウイルスのウイルスストックを得た。
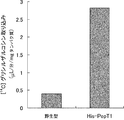
[14C]グリシルザルコシンを終濃度50μMになるようにHBSS(pH6.0)で希釈し、基質溶液とした。ウイルス溶液40μL(100μg蛋白)を37℃で30分間プレインキュベートし、あらかじめ37℃で加温していた基質溶液を160μL添加し、反応を開始した。1分後、氷冷していたHBSS(pH7.4)(以下、「反応停止液」と略す)を1mL添加して、反応を停止させた。直ちにウイルスを含む反応液を混合セルロース膜フィルターを用いて吸引濾過し、5mLの反応停止液で2回洗浄した。膜フィルターを液体シンチレーターバイアルに移し、クリアゾルIを5mL添加してフィルターを溶解した。溶解後、液体シンチレーションカウンターでフィルター上の放射能を計測した。ウイルス溶液に基質溶液を添加する前に反応停止液を添加した系についても同様にフィルターへの非特異的吸着を計測し、得られた値を各実験の数値から差し引いた。
N末端にHis-tagを付加したPepT1発現ウイルスでのPepT1活性を図1に示した。PepT1を発現していない野生型ウイルスに比べて、約7倍の活性比でPepT1活性を検出することができた。
1. PepT2発現出芽バキュロウイルスの調製
ヒト腎臓ライブラリーから完全長PepT2遺伝子を単離した。完全長のヒトPepT2をコードする遺伝子は、PCRを用いてpBlueBacHis2A (Invitrogen) に組み込むことで完全長のPepT2トランスファーベクター(pBlueBac)を作製し、ウイルスDNAと共にSf-9細胞に導入した。相同組換えにより作製された組換えウイルスを純化した後、組換えウイルス高活性ストックを作製した。ストックウイルスをSf-9細胞に感染させ、一定期間培養後にウイルスならびにSf-9細胞膜上へのPepT2の発現を行った。ウイルスならびにSf-9細胞膜上でのPepT2発現は抗His抗体を用いたウエスタン解析で確認した。より詳細には、PepT2遺伝子を用いた以外は、実施例1に記載の方法に従って操作を行った。
[3H]グリシルザルコシンを終濃度0.8μMになるようにHBSS(pH6.0)で希釈し、基質溶液とした。ウイルス溶液40μL(100μg蛋白)を37℃で30分間プレインキュベートし、予め37℃で加温していた基質溶液を160μL添加し、反応を開始させた。1分後、反応停止液1mLを添加して、反応を停止させた。直ちにウイルスを含む反応液を混合セルロース膜フィルターを用いて吸引濾過し、5mLの反応停止液で2回洗浄した。膜フィルターを液体シンチレーションバイアルに移し、クリアゾルIを5mL添加してフィルターを溶解させた。溶解後、液体シンチレーションカウンターでフィルター上の放射能を計測した。ウイルス溶液に基質溶液を添加する前に反応停止液を添加して同様の操作を行い、フィルターへの非特異的吸着を計測し値を各実験の数値から差し引いた。
N末端にHis-tagを付加したPepT2発現ウイルスでのPepT2活性を図2に示した。PepT2を発現していない野生型ウイルスに比べて、約9倍の活性比でPepT2活性を検出することができた。
1. OATP-C発現出芽バキュロウイルスの調製
野生型ヒトOATP-C(OATP-C WT)をコードするcDNAは以下のようにしてクローニングした。すなわち、ヒト成体肝臓由来cDNAを鋳型とし、以下のプライマーの組み合わせによるPCRによりOATP-C WT cDNAを2つの断片に分け増幅した。
5’側
OAHC17プライマー:5' gat ggt acc aaa ctg agc atc aac aac aaa aac 3' (配列番号:1)
OAHC18プライマー:5' gat ggt acc cat cga gaa tca gta gga gtt atc 3' (配列番号:2)
3’側
OAHC21プライマー:5' gat ggt acc tac cct ggg atc tct gtt ttc taa 3' (配列番号:3)
OAHC22プライマー:5' gat ggt acc gtt tgg aaa cac aga agc aga agt 3' (配列番号:4)
これらの断片をそれぞれpT7Blue-Tベクター(Novagen社)にサブクローニングし、PCRエラーのないクローンを選択した。重なり合う領域に存在するBgl IIサイトで両者を連結した後、両端に存在するKpn Iサイトで切断し、pcDNA3ベクター(Invitrogen社)のKpn Iサイトに組み込み、pcDNA3/OATP-C WTを得た。
OATP-C N130D用プライマー:5’ gaa act aat atc gat tca tca gaa aat 3’(配列番号:5)
OATP-C V174A用プライマー:5’ atg tgg ata tat gcg ttc atg ggt aat 3’(配列番号:6)
C45プライマー:5' gat gtc gac tta aca atg tgt ttc act 3'(配列番号:7)
C58プライマー:5' gat gtc gac tat gga cca aaa tca aca t 3'(配列番号:8)
これらをSal Iにより切断し、pBlueBac His2Aベクター(Invitrogen社)のSal Iサイトに組み込むことにより、N末端にHis-tagが付加された各OATP-Cタンパクをコードするトランスファーベクター(pBlueBac His2A/OATP-C WT、pBlueBac His2A/OATP-C N130D、pBlueBac His2A/OATP-C V174A)を作製した。
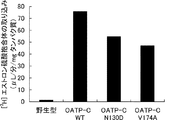
[3H]エストロン硫酸抱合体を終濃度10nMになるようにHBSS(pH7.4)で希釈し、基質溶液とした。ウイルス溶液20μL(50μg蛋白)を37℃で30分間プレインキュベートし、予め37℃で加温していた基質溶液を180μL添加し、反応を開始させた。1分後、氷冷していたHBSS(pH7.4)(以下、反応停止液と略す)を1mL添加して、反応を停止させた。直ちにウイルスを含む反応液を混合セルロース膜フィルターを用いて吸引濾過し、5mLの反応停止液で2回洗浄した。膜フィルターを液体シンチレーターバイアルに移し、クリアゾルIを5mL添加してフィルターを溶解させた。溶解後、液体シンチレーションカウンターでフィルター上の放射能を計測した。基質溶液を添加する前に反応停止液を添加して同様の操作を行い、フィルターへの非特異的吸着を計測し、各実験の数値から差し引いた。
[14C]グリシルザルコシンを終濃度50μMになるようにHBSS(pH6.0)で希釈し、基質溶液とした。また、ヒトPepT1の細胞外領域を認識するマウス型モノクローナル抗体を終濃度200μg/mLになるようにPBSで希釈し、抗体溶液とした。N末端にHis-tagを付加したPepT1発現出芽バキュロウイルス溶液20μL(50μg蛋白)と抗体溶液20μLを混合し、37℃で1時間プレインキュベートした。予め、37℃で加温していた基質溶液160μLをウイルス溶液に添加し、反応を開始させた。1分後、氷冷していたHBSS(pH7.4)(以下、「反応停止液」と略す)を1mL添加し、反応を停止させた。直ちにウイルスを含む反応液を混合セルロース膜フィルターを用いて吸引濾過し、5 mLの反応停止液で2回洗浄した。膜フィルターを液体シンチレーションバイアルに移し、クリアゾルIを5 mL添加してフィルターを溶解させた。溶解後、液体シンチレーションカウンターでフィルター上の放射能を計測した。基質溶液を添加する前に反応停止液を添加して同様の操作を行い、フィルターへの非特異的吸着を計測し、各実験の数値から差し引いた。
Claims (24)
- トランスポーターをコードする遺伝子を含む組換えウイルスを感染させた宿主を培養し、該宿主から放出される出芽ウイルス膜上にトランスポーターを発現させることを特徴とする、トランスポーター活性を有するトランスポーターを発現させる方法。
- ウイルスがバキュロウイルスである請求項1記載の方法。
- トランスポーターが非ウイルス由来である請求項1または2いずれか記載の方法。
- トランスポーターがペプチドトランスポーターまたは有機アニオントランスポーターである請求項1〜3いずれか記載の方法。
- トランスポーターがPepT1、PepT2又は OATP-Cである請求項4記載の方法。
- トランスポーター活性を有するトランスポーターを発現しているウイルス。
- トランスポーターが非ウイルス由来である請求項6記載のウイルス。
- ウイルスがバキュロウイルスである請求項7記載のウイルス。
- ウイルスが出芽ウイルスである、請求項6〜8いずれか記載のウイルス。
- トランスポーターがペプチドトランスポーターまたは有機アニオントランスポーターである請求項6〜9いずれか記載のウイルス。
- トランスポーターがPepT1、PepT2又は OATP-Cである請求項10記載のウイルス。
- ウイルス膜上でトランスポーターを発現させることを特徴とする、トランスポーターの活性測定方法。
- ウイルスが出芽バキュロウイルスである請求項12記載の方法。
- トランスポーターがペプチドトランスポーターまたは有機アニオントランスポーターである請求項12または13記載の方法。
- トランスポーターがPepT1、PepT2又は OATP-Cである請求項14記載の方法。
- 以下の工程を含むトランスポーターのトランスポート活性を阻害又は促進する物質のスクリーニング方法。
(a)ウイルス膜上にトランスポーターを発現させる工程、
(b)該トランスポーターに被験物質を接触させる工程、及び
(c)トランスポート活性を阻害又は促進する物質を選択する工程 - ウイルスがバキュロウイルスである請求項16記載の方法。
- ウイルスが出芽ウイルスである請求項16又は17記載の方法。
- トランスポーターが非ウイルス由来である請求項16〜18いずれか記載の方法。
- トランスポーターがペプチドトランスポーターまたは有機アニオントランスポーターである、請求項16〜19いずれか記載の方法。
- トランスポーターがPepT1、PepT2又は OATP-Cである、請求項20記載の方法。
- ウイルスが担体に固定されていることを特徴とする請求項16〜21いずれか記載の方法。
- ウイルスの担体への固定が、ウイルス膜上に発現している膜タンパク質に対する抗体を介して行われていることを特徴とする請求項22記載の方法。
- ウイルスの担体への固定が、ウイルス膜上に発現しているタンパク質をビオチン化することでビオチン・ストレプトアビジン反応を介して行われることを特徴とする請求項22記載の方法。
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2009220017A JP5258112B2 (ja) | 2002-03-29 | 2009-09-25 | トランスポーター阻害物質スクリーニング方法 |
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2002096038 | 2002-03-29 | ||
| JP2002096038 | 2002-03-29 | ||
| JP2009220017A JP5258112B2 (ja) | 2002-03-29 | 2009-09-25 | トランスポーター阻害物質スクリーニング方法 |
Related Parent Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2003580549A Division JPWO2003083116A1 (ja) | 2002-03-29 | 2003-03-28 | トランスポーター阻害物質スクリーニング方法 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2010046068A true JP2010046068A (ja) | 2010-03-04 |
| JP5258112B2 JP5258112B2 (ja) | 2013-08-07 |
Family
ID=28671820
Family Applications (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2003580549A Withdrawn JPWO2003083116A1 (ja) | 2002-03-29 | 2003-03-28 | トランスポーター阻害物質スクリーニング方法 |
| JP2009220017A Expired - Fee Related JP5258112B2 (ja) | 2002-03-29 | 2009-09-25 | トランスポーター阻害物質スクリーニング方法 |
Family Applications Before (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2003580549A Withdrawn JPWO2003083116A1 (ja) | 2002-03-29 | 2003-03-28 | トランスポーター阻害物質スクリーニング方法 |
Country Status (5)
| Country | Link |
|---|---|
| US (1) | US7666610B2 (ja) |
| EP (1) | EP1491631B1 (ja) |
| JP (2) | JPWO2003083116A1 (ja) |
| AU (1) | AU2003220930A1 (ja) |
| WO (1) | WO2003083116A1 (ja) |
Families Citing this family (9)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2003033024A1 (fr) * | 2001-10-16 | 2003-04-24 | Chugai Seiyaku Kabushiki Kaisha | Inhibiteur de proliferation cellulaire |
| DE60235499D1 (de) | 2001-12-04 | 2010-04-08 | Chugai Pharmaceutical Co Ltd | ZELLWACHSTUMSHEMMER MIT ANTI-PepT-ANTIKÖRPER |
| EP1491631B1 (en) | 2002-03-29 | 2013-05-08 | Chugai Seiyaku Kabushiki Kaisha | Methods of screening for transporter inhibitors |
| WO2003104453A1 (ja) | 2002-06-05 | 2003-12-18 | 中外製薬株式会社 | 抗体作製方法 |
| EP1621553A4 (en) | 2003-03-28 | 2006-08-23 | Chugai Pharmaceutical Co Ltd | ANTIBODIES INHIBITING TRANSPORT ACTIVITY OF PEPTIDE TRANSPORTERS |
| WO2005054861A1 (en) * | 2003-11-22 | 2005-06-16 | Bayer Healthcare Ag | Diagnostics and therapeutics for diseases associated with potassium channel subfamily k, member 10 (kcnk10) |
| EP1731032B1 (en) | 2004-03-31 | 2016-10-19 | Chugai Seiyaku Kabushiki Kaisha | Transgenic mice carrying gene for soluble form of membrane protein useful for antibody production against a target antigen, and methods using thereof |
| DE102004048391B4 (de) * | 2004-10-01 | 2007-08-16 | Iongate Biosciences Gmbh | Typ-PepT1-Protein-Assay |
| MX2014014086A (es) * | 2012-05-23 | 2015-01-26 | Genentech Inc | Metodo de seleccion para agentes terapeuticos. |
Citations (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO1998046777A1 (fr) * | 1997-04-11 | 1998-10-22 | Centre National De La Recherche Scientifique (Cnrs) | Preparation de recepteurs membranaires a partir de baculovirus extracellulaires |
Family Cites Families (23)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| DE69127627T2 (de) | 1990-08-29 | 1998-02-19 | Genpharm Int | Produktion und Nützung nicht-menschliche transgentiere zur Produktion heterologe Antikörper |
| WO1993002227A1 (en) | 1991-07-15 | 1993-02-04 | Eco-Tec Limited | Process and apparatus for treating fluoride containing acid solutions |
| EP0652950B1 (en) | 1992-07-24 | 2007-12-19 | Amgen Fremont Inc. | Generation of xenogeneic antibodies |
| US5285485A (en) | 1993-02-01 | 1994-02-08 | General Electric Company | Composite nuclear fuel container and method for producing same |
| IL108499A (en) | 1993-02-04 | 2000-02-29 | Lilly Co Eli | Mammalian influx peptide transporter |
| EP0754225A4 (en) | 1993-04-26 | 2001-01-31 | Genpharm Int | HETEROLOGIC ANTIBODY-PRODUCING TRANSGENIC NON-HUMAN ANIMALS |
| US5500346A (en) | 1993-06-29 | 1996-03-19 | Eli Lilly And Company | Monoclonal antibodies to human influx peptide transporter |
| US5849525A (en) | 1994-03-09 | 1998-12-15 | Brigham And Women's Hospital, Inc. | Compositions corresponding to a proton-coupled peptide transporter and methods of making and using same |
| JPH08134100A (ja) | 1994-11-09 | 1996-05-28 | Unitika Ltd | 糖鎖特異的抗体の製造方法 |
| KR100654645B1 (ko) | 1995-04-27 | 2007-04-04 | 아브게닉스, 인크. | 면역화된 제노마우스 유래의 인간 항체 |
| AU2466895A (en) | 1995-04-28 | 1996-11-18 | Abgenix, Inc. | Human antibodies derived from immunized xenomice |
| JP2843532B2 (ja) | 1995-07-25 | 1999-01-06 | 建設基礎エンジニアリング株式会社 | 仕上げプレート付き網状型枠 |
| KR19990071666A (ko) | 1995-11-30 | 1999-09-27 | 이경하 | 술파미드 유도체 |
| JPH11172A (ja) | 1997-06-11 | 1999-01-06 | Snow Brand Milk Prod Co Ltd | ペプチド輸送タンパク質遺伝子を含むdna、ベクター及び微生物 |
| AU776865B2 (en) | 1998-11-10 | 2004-09-23 | University Of Rochester | T cells specific for target antigens and methods and vaccines based thereon |
| JP4552056B2 (ja) | 1999-11-15 | 2010-09-29 | 独立行政法人科学技術振興機構 | 後天的免疫寛容の獲得方法 |
| JP2001197846A (ja) | 2000-01-18 | 2001-07-24 | Ys New Technology Kenkyusho:Kk | 免疫寛容動物の作製方法 |
| WO2003033024A1 (fr) | 2001-10-16 | 2003-04-24 | Chugai Seiyaku Kabushiki Kaisha | Inhibiteur de proliferation cellulaire |
| DE60235499D1 (de) | 2001-12-04 | 2010-04-08 | Chugai Pharmaceutical Co Ltd | ZELLWACHSTUMSHEMMER MIT ANTI-PepT-ANTIKÖRPER |
| EP1491631B1 (en) | 2002-03-29 | 2013-05-08 | Chugai Seiyaku Kabushiki Kaisha | Methods of screening for transporter inhibitors |
| WO2003104453A1 (ja) | 2002-06-05 | 2003-12-18 | 中外製薬株式会社 | 抗体作製方法 |
| EP1621553A4 (en) * | 2003-03-28 | 2006-08-23 | Chugai Pharmaceutical Co Ltd | ANTIBODIES INHIBITING TRANSPORT ACTIVITY OF PEPTIDE TRANSPORTERS |
| EP1731032B1 (en) | 2004-03-31 | 2016-10-19 | Chugai Seiyaku Kabushiki Kaisha | Transgenic mice carrying gene for soluble form of membrane protein useful for antibody production against a target antigen, and methods using thereof |
-
2003
- 2003-03-28 EP EP03715597.5A patent/EP1491631B1/en not_active Expired - Lifetime
- 2003-03-28 AU AU2003220930A patent/AU2003220930A1/en not_active Abandoned
- 2003-03-28 US US10/509,343 patent/US7666610B2/en not_active Expired - Fee Related
- 2003-03-28 WO PCT/JP2003/003975 patent/WO2003083116A1/ja not_active Ceased
- 2003-03-28 JP JP2003580549A patent/JPWO2003083116A1/ja not_active Withdrawn
-
2009
- 2009-09-25 JP JP2009220017A patent/JP5258112B2/ja not_active Expired - Fee Related
Patent Citations (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO1998046777A1 (fr) * | 1997-04-11 | 1998-10-22 | Centre National De La Recherche Scientifique (Cnrs) | Preparation de recepteurs membranaires a partir de baculovirus extracellulaires |
Non-Patent Citations (6)
| Title |
|---|
| JPN5004004708; GERGELY S.: BIOCHEMICAL AND BIOPHYSICAL RESEARCH COMMUNICATIONS V288 N5, 2001, P1258-1264 * |
| JPN5004004709; NOE J.: HEPATOLOGY V33 N5, 2001, P1223-1231 * |
| JPN6012015144; Hum Gene Ther. Vol.8, 1997, p.2011-2018 * |
| JPN6012015145; J Biotechnol. Vol.95, 20020323, p.269-275 * |
| JPN6012015146; Biochem J. Vol.283, 1992, p.643-646 * |
| JPN6012015147; Biochem Biophys Res Commun. Vol.273, 2000, p.251-260 * |
Also Published As
| Publication number | Publication date |
|---|---|
| AU2003220930A1 (en) | 2003-10-13 |
| EP1491631B1 (en) | 2013-05-08 |
| JP5258112B2 (ja) | 2013-08-07 |
| US20060084119A1 (en) | 2006-04-20 |
| WO2003083116A1 (en) | 2003-10-09 |
| EP1491631A1 (en) | 2004-12-29 |
| EP1491631A4 (en) | 2005-07-20 |
| JPWO2003083116A1 (ja) | 2005-08-04 |
| US7666610B2 (en) | 2010-02-23 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP5258112B2 (ja) | トランスポーター阻害物質スクリーニング方法 | |
| US7732149B2 (en) | Methods of screening agonistic antibodies | |
| TWI831365B (zh) | 抗gpc3抗體 | |
| Kartner et al. | Mislocalization of ΔF508 CFTR in cystic fibrosis sweat gland | |
| US20110003971A1 (en) | Modulators and modulation of the interaction between rgm and neogenin | |
| EA032728B1 (ru) | Антитела для выявления комплексов интегрина в ffpe материале | |
| EP0722088B1 (en) | Method and reagent for detecting human disorders | |
| JP2009050269A (ja) | ヒトhmg−1に特異的に結合する抗体及びその製造方法 | |
| RU2155345C2 (ru) | Способ скрининга невропатологии | |
| WO1999060025A1 (fr) | Anticorps recombines de gene | |
| US5773293A (en) | Anti-ICAM-4 antibodies and hybridomas | |
| CN113912713B (zh) | 一种抗α-突触核蛋白的单克隆抗体及其应用 | |
| JP2006524489A (ja) | Spex組成物および使用方法 | |
| US20090275082A1 (en) | Mast Cell-Derived Membrane Proteins | |
| US20230393144A1 (en) | Methods for mitigating interference by therapeutic anti-cd47 antibodies in pre-transfusion assays | |
| JPH11326328A (ja) | Xiapとの結合を阻害する物質のスクリーニング方法 | |
| RU2208230C2 (ru) | Icam-4 и его диагностическое использование | |
| JP4541613B2 (ja) | 新規サイトカイン | |
| WO2005110433A1 (ja) | Bach2の発現が人為的に抑制されている非ヒト動物とその利用 | |
| US5852170A (en) | ICAM-4 materials and methods | |
| WO2007037245A1 (ja) | 血管新生抑制作用を有するポリペプチド | |
| CN120623352A (zh) | 抗human IgG的抗体、其制备方法及用途 | |
| CN120665199A (zh) | 抗human IgG的抗体、其制备方法及用途 | |
| WO2025209940A1 (en) | Ebv vaccine and antibodies | |
| US5700658A (en) | ICAM-4 materials and methods |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20120322 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20120725 |
|
| A521 | Written amendment |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20120924 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20130417 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20130422 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20160502 Year of fee payment: 3 |
|
| R150 | Certificate of patent or registration of utility model |
Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| LAPS | Cancellation because of no payment of annual fees |