JP2008507955A - チトクロムp450−2c19をコードする遺伝子における突然変異を検出する方法 - Google Patents
チトクロムp450−2c19をコードする遺伝子における突然変異を検出する方法 Download PDFInfo
- Publication number
- JP2008507955A JP2008507955A JP2007522887A JP2007522887A JP2008507955A JP 2008507955 A JP2008507955 A JP 2008507955A JP 2007522887 A JP2007522887 A JP 2007522887A JP 2007522887 A JP2007522887 A JP 2007522887A JP 2008507955 A JP2008507955 A JP 2008507955A
- Authority
- JP
- Japan
- Prior art keywords
- seq
- cyp2c19
- nucleotide
- primer
- group
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
- 102100029363 Cytochrome P450 2C19 Human genes 0.000 title claims abstract description 45
- 238000000034 method Methods 0.000 title claims abstract description 43
- 108090000623 proteins and genes Proteins 0.000 title claims abstract description 30
- 101710142428 Cytochrome P450 2C19 Proteins 0.000 title claims abstract description 7
- 230000035772 mutation Effects 0.000 title abstract description 30
- 108700028369 Alleles Proteins 0.000 claims abstract description 52
- 239000000523 sample Substances 0.000 claims abstract description 42
- 125000003729 nucleotide group Chemical group 0.000 claims description 53
- 239000002773 nucleotide Substances 0.000 claims description 50
- 230000000295 complement effect Effects 0.000 claims description 42
- 108010026925 Cytochrome P-450 CYP2C19 Proteins 0.000 claims description 38
- 239000011324 bead Substances 0.000 claims description 18
- 238000002493 microarray Methods 0.000 claims description 14
- 239000007787 solid Substances 0.000 claims description 13
- FWMNVWWHGCHHJJ-SKKKGAJSSA-N 4-amino-1-[(2r)-6-amino-2-[[(2r)-2-[[(2r)-2-[[(2r)-2-amino-3-phenylpropanoyl]amino]-3-phenylpropanoyl]amino]-4-methylpentanoyl]amino]hexanoyl]piperidine-4-carboxylic acid Chemical compound C([C@H](C(=O)N[C@H](CC(C)C)C(=O)N[C@H](CCCCN)C(=O)N1CCC(N)(CC1)C(O)=O)NC(=O)[C@H](N)CC=1C=CC=CC=1)C1=CC=CC=C1 FWMNVWWHGCHHJJ-SKKKGAJSSA-N 0.000 claims description 7
- 238000012408 PCR amplification Methods 0.000 claims description 5
- 238000001514 detection method Methods 0.000 abstract description 22
- 238000009396 hybridization Methods 0.000 abstract description 9
- 108020004414 DNA Proteins 0.000 description 24
- 238000006243 chemical reaction Methods 0.000 description 21
- 239000004005 microsphere Substances 0.000 description 12
- 108091034117 Oligonucleotide Proteins 0.000 description 10
- 238000004458 analytical method Methods 0.000 description 8
- BASFCYQUMIYNBI-UHFFFAOYSA-N platinum Chemical compound [Pt] BASFCYQUMIYNBI-UHFFFAOYSA-N 0.000 description 8
- 102000004190 Enzymes Human genes 0.000 description 7
- 108090000790 Enzymes Proteins 0.000 description 7
- FAPWRFPIFSIZLT-UHFFFAOYSA-M Sodium chloride Chemical compound [Na+].[Cl-] FAPWRFPIFSIZLT-UHFFFAOYSA-M 0.000 description 6
- 108091028043 Nucleic acid sequence Proteins 0.000 description 5
- 230000000694 effects Effects 0.000 description 5
- 238000005516 engineering process Methods 0.000 description 5
- 239000000203 mixture Substances 0.000 description 5
- 239000011541 reaction mixture Substances 0.000 description 5
- LMDZBCPBFSXMTL-UHFFFAOYSA-N 1-Ethyl-3-(3-dimethylaminopropyl)carbodiimide Substances CCN=C=NCCCN(C)C LMDZBCPBFSXMTL-UHFFFAOYSA-N 0.000 description 4
- 108010007577 Exodeoxyribonuclease I Proteins 0.000 description 4
- 102100029075 Exonuclease 1 Human genes 0.000 description 4
- 239000007983 Tris buffer Substances 0.000 description 4
- 230000002806 hypometabolic effect Effects 0.000 description 4
- 229910052697 platinum Inorganic materials 0.000 description 4
- LENZDBCJOHFCAS-UHFFFAOYSA-N tris Chemical compound OCC(N)(CO)CO LENZDBCJOHFCAS-UHFFFAOYSA-N 0.000 description 4
- 102000003992 Peroxidases Human genes 0.000 description 3
- 239000013504 Triton X-100 Substances 0.000 description 3
- 229920004890 Triton X-100 Polymers 0.000 description 3
- JLCPHMBAVCMARE-UHFFFAOYSA-N [3-[[3-[[3-[[3-[[3-[[3-[[3-[[3-[[3-[[3-[[3-[[5-(2-amino-6-oxo-1H-purin-9-yl)-3-[[3-[[3-[[3-[[3-[[3-[[5-(2-amino-6-oxo-1H-purin-9-yl)-3-[[5-(2-amino-6-oxo-1H-purin-9-yl)-3-hydroxyoxolan-2-yl]methoxy-hydroxyphosphoryl]oxyoxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(5-methyl-2,4-dioxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(6-aminopurin-9-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(6-aminopurin-9-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(6-aminopurin-9-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(6-aminopurin-9-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxyoxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(5-methyl-2,4-dioxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(4-amino-2-oxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(5-methyl-2,4-dioxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(5-methyl-2,4-dioxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(6-aminopurin-9-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(6-aminopurin-9-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(4-amino-2-oxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(4-amino-2-oxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(4-amino-2-oxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(6-aminopurin-9-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(4-amino-2-oxopyrimidin-1-yl)oxolan-2-yl]methyl [5-(6-aminopurin-9-yl)-2-(hydroxymethyl)oxolan-3-yl] hydrogen phosphate Polymers Cc1cn(C2CC(OP(O)(=O)OCC3OC(CC3OP(O)(=O)OCC3OC(CC3O)n3cnc4c3nc(N)[nH]c4=O)n3cnc4c3nc(N)[nH]c4=O)C(COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3CO)n3cnc4c(N)ncnc34)n3ccc(N)nc3=O)n3cnc4c(N)ncnc34)n3ccc(N)nc3=O)n3ccc(N)nc3=O)n3ccc(N)nc3=O)n3cnc4c(N)ncnc34)n3cnc4c(N)ncnc34)n3cc(C)c(=O)[nH]c3=O)n3cc(C)c(=O)[nH]c3=O)n3ccc(N)nc3=O)n3cc(C)c(=O)[nH]c3=O)n3cnc4c3nc(N)[nH]c4=O)n3cnc4c(N)ncnc34)n3cnc4c(N)ncnc34)n3cnc4c(N)ncnc34)n3cnc4c(N)ncnc34)O2)c(=O)[nH]c1=O JLCPHMBAVCMARE-UHFFFAOYSA-N 0.000 description 3
- 230000003321 amplification Effects 0.000 description 3
- 239000000872 buffer Substances 0.000 description 3
- 210000004027 cell Anatomy 0.000 description 3
- 239000003153 chemical reaction reagent Substances 0.000 description 3
- 229940079593 drug Drugs 0.000 description 3
- 239000003814 drug Substances 0.000 description 3
- 238000003205 genotyping method Methods 0.000 description 3
- 238000011534 incubation Methods 0.000 description 3
- 238000007403 mPCR Methods 0.000 description 3
- 230000002503 metabolic effect Effects 0.000 description 3
- 238000003199 nucleic acid amplification method Methods 0.000 description 3
- 108040007629 peroxidase activity proteins Proteins 0.000 description 3
- 238000011160 research Methods 0.000 description 3
- 239000011780 sodium chloride Substances 0.000 description 3
- QKNYBSVHEMOAJP-UHFFFAOYSA-N 2-amino-2-(hydroxymethyl)propane-1,3-diol;hydron;chloride Chemical compound Cl.OCC(N)(CO)CO QKNYBSVHEMOAJP-UHFFFAOYSA-N 0.000 description 2
- 102000002260 Alkaline Phosphatase Human genes 0.000 description 2
- 108020004774 Alkaline Phosphatase Proteins 0.000 description 2
- 101150003340 CYP2C19 gene Proteins 0.000 description 2
- 108010004729 Phycoerythrin Proteins 0.000 description 2
- 229920001213 Polysorbate 20 Polymers 0.000 description 2
- 108010090804 Streptavidin Proteins 0.000 description 2
- 239000007984 Tris EDTA buffer Substances 0.000 description 2
- 238000003556 assay Methods 0.000 description 2
- 230000003993 interaction Effects 0.000 description 2
- 238000002372 labelling Methods 0.000 description 2
- 239000000463 material Substances 0.000 description 2
- 239000000256 polyoxyethylene sorbitan monolaurate Substances 0.000 description 2
- 235000010486 polyoxyethylene sorbitan monolaurate Nutrition 0.000 description 2
- 238000002360 preparation method Methods 0.000 description 2
- 230000002194 synthesizing effect Effects 0.000 description 2
- 238000012360 testing method Methods 0.000 description 2
- SXGZJKUKBWWHRA-UHFFFAOYSA-N 2-(N-morpholiniumyl)ethanesulfonate Chemical compound [O-]S(=O)(=O)CC[NH+]1CCOCC1 SXGZJKUKBWWHRA-UHFFFAOYSA-N 0.000 description 1
- FPQQSJJWHUJYPU-UHFFFAOYSA-N 3-(dimethylamino)propyliminomethylidene-ethylazanium;chloride Chemical compound Cl.CCN=C=NCCCN(C)C FPQQSJJWHUJYPU-UHFFFAOYSA-N 0.000 description 1
- 206010067484 Adverse reaction Diseases 0.000 description 1
- 241000143060 Americamysis bahia Species 0.000 description 1
- 239000004971 Cross linker Substances 0.000 description 1
- 108010000561 Cytochrome P-450 CYP2C8 Proteins 0.000 description 1
- 108010000543 Cytochrome P-450 CYP2C9 Proteins 0.000 description 1
- 108010001237 Cytochrome P-450 CYP2D6 Proteins 0.000 description 1
- 102100029368 Cytochrome P450 2C18 Human genes 0.000 description 1
- 102100029359 Cytochrome P450 2C8 Human genes 0.000 description 1
- 102100029358 Cytochrome P450 2C9 Human genes 0.000 description 1
- 102100021704 Cytochrome P450 2D6 Human genes 0.000 description 1
- IGXWBGJHJZYPQS-SSDOTTSWSA-N D-Luciferin Chemical compound OC(=O)[C@H]1CSC(C=2SC3=CC=C(O)C=C3N=2)=N1 IGXWBGJHJZYPQS-SSDOTTSWSA-N 0.000 description 1
- 102000053602 DNA Human genes 0.000 description 1
- 238000000018 DNA microarray Methods 0.000 description 1
- 230000006820 DNA synthesis Effects 0.000 description 1
- 102000016928 DNA-directed DNA polymerase Human genes 0.000 description 1
- 108010014303 DNA-directed DNA polymerase Proteins 0.000 description 1
- 241000238557 Decapoda Species 0.000 description 1
- CYCGRDQQIOGCKX-UHFFFAOYSA-N Dehydro-luciferin Natural products OC(=O)C1=CSC(C=2SC3=CC(O)=CC=C3N=2)=N1 CYCGRDQQIOGCKX-UHFFFAOYSA-N 0.000 description 1
- 208000030453 Drug-Related Side Effects and Adverse reaction Diseases 0.000 description 1
- KCXVZYZYPLLWCC-UHFFFAOYSA-N EDTA Chemical compound OC(=O)CN(CC(O)=O)CCN(CC(O)=O)CC(O)=O KCXVZYZYPLLWCC-UHFFFAOYSA-N 0.000 description 1
- 108700024394 Exon Proteins 0.000 description 1
- 108060002716 Exonuclease Proteins 0.000 description 1
- BJGNCJDXODQBOB-UHFFFAOYSA-N Fivefly Luciferin Natural products OC(=O)C1CSC(C=2SC3=CC(O)=CC=C3N=2)=N1 BJGNCJDXODQBOB-UHFFFAOYSA-N 0.000 description 1
- 101000919360 Homo sapiens Cytochrome P450 2C18 Proteins 0.000 description 1
- DDWFXDSYGUXRAY-UHFFFAOYSA-N Luciferin Natural products CCc1c(C)c(CC2NC(=O)C(=C2C=C)C)[nH]c1Cc3[nH]c4C(=C5/NC(CC(=O)O)C(C)C5CC(=O)O)CC(=O)c4c3C DDWFXDSYGUXRAY-UHFFFAOYSA-N 0.000 description 1
- 238000005481 NMR spectroscopy Methods 0.000 description 1
- 102000004160 Phosphoric Monoester Hydrolases Human genes 0.000 description 1
- 108090000608 Phosphoric Monoester Hydrolases Proteins 0.000 description 1
- DBMJMQXJHONAFJ-UHFFFAOYSA-M Sodium laurylsulphate Chemical compound [Na+].CCCCCCCCCCCCOS([O-])(=O)=O DBMJMQXJHONAFJ-UHFFFAOYSA-M 0.000 description 1
- 230000005856 abnormality Effects 0.000 description 1
- 238000002835 absorbance Methods 0.000 description 1
- 230000006838 adverse reaction Effects 0.000 description 1
- 238000000137 annealing Methods 0.000 description 1
- 239000000935 antidepressant agent Substances 0.000 description 1
- 229940005513 antidepressants Drugs 0.000 description 1
- 239000003430 antimalarial agent Substances 0.000 description 1
- 229940033495 antimalarials Drugs 0.000 description 1
- 239000002249 anxiolytic agent Substances 0.000 description 1
- 230000000949 anxiolytic effect Effects 0.000 description 1
- 229940005530 anxiolytics Drugs 0.000 description 1
- 238000003491 array Methods 0.000 description 1
- 230000008033 biological extinction Effects 0.000 description 1
- 239000008280 blood Substances 0.000 description 1
- 210000004369 blood Anatomy 0.000 description 1
- 150000001718 carbodiimides Chemical class 0.000 description 1
- 210000000349 chromosome Anatomy 0.000 description 1
- 230000009260 cross reactivity Effects 0.000 description 1
- SUYVUBYJARFZHO-RRKCRQDMSA-N dATP Chemical compound C1=NC=2C(N)=NC=NC=2N1[C@H]1C[C@H](O)[C@@H](COP(O)(=O)OP(O)(=O)OP(O)(O)=O)O1 SUYVUBYJARFZHO-RRKCRQDMSA-N 0.000 description 1
- SUYVUBYJARFZHO-UHFFFAOYSA-N dATP Natural products C1=NC=2C(N)=NC=NC=2N1C1CC(O)C(COP(O)(=O)OP(O)(=O)OP(O)(O)=O)O1 SUYVUBYJARFZHO-UHFFFAOYSA-N 0.000 description 1
- RGWHQCVHVJXOKC-SHYZEUOFSA-J dCTP(4-) Chemical compound O=C1N=C(N)C=CN1[C@@H]1O[C@H](COP([O-])(=O)OP([O-])(=O)OP([O-])([O-])=O)[C@@H](O)C1 RGWHQCVHVJXOKC-SHYZEUOFSA-J 0.000 description 1
- HAAZLUGHYHWQIW-KVQBGUIXSA-N dGTP Chemical compound C1=NC=2C(=O)NC(N)=NC=2N1[C@H]1C[C@H](O)[C@@H](COP(O)(=O)OP(O)(=O)OP(O)(O)=O)O1 HAAZLUGHYHWQIW-KVQBGUIXSA-N 0.000 description 1
- NHVNXKFIZYSCEB-XLPZGREQSA-N dTTP Chemical compound O=C1NC(=O)C(C)=CN1[C@@H]1O[C@H](COP(O)(=O)OP(O)(=O)OP(O)(O)=O)[C@@H](O)C1 NHVNXKFIZYSCEB-XLPZGREQSA-N 0.000 description 1
- 230000002950 deficient Effects 0.000 description 1
- 238000012217 deletion Methods 0.000 description 1
- 230000037430 deletion Effects 0.000 description 1
- 230000036425 denaturation Effects 0.000 description 1
- 238000004925 denaturation Methods 0.000 description 1
- 239000005547 deoxyribonucleotide Substances 0.000 description 1
- 125000002637 deoxyribonucleotide group Chemical group 0.000 description 1
- 230000001419 dependent effect Effects 0.000 description 1
- 238000011033 desalting Methods 0.000 description 1
- 238000013461 design Methods 0.000 description 1
- 238000002405 diagnostic procedure Methods 0.000 description 1
- 230000036267 drug metabolism Effects 0.000 description 1
- 238000001952 enzyme assay Methods 0.000 description 1
- 102000013165 exonuclease Human genes 0.000 description 1
- GNBHRKFJIUUOQI-UHFFFAOYSA-N fluorescein Chemical compound O1C(=O)C2=CC=CC=C2C21C1=CC=C(O)C=C1OC1=CC(O)=CC=C21 GNBHRKFJIUUOQI-UHFFFAOYSA-N 0.000 description 1
- 239000007850 fluorescent dye Substances 0.000 description 1
- 230000002068 genetic effect Effects 0.000 description 1
- 102000054766 genetic haplotypes Human genes 0.000 description 1
- 239000011521 glass Substances 0.000 description 1
- 230000001771 impaired effect Effects 0.000 description 1
- 238000000338 in vitro Methods 0.000 description 1
- 238000001727 in vivo Methods 0.000 description 1
- 238000010348 incorporation Methods 0.000 description 1
- 238000004519 manufacturing process Methods 0.000 description 1
- 239000012528 membrane Substances 0.000 description 1
- 230000004060 metabolic process Effects 0.000 description 1
- 238000012986 modification Methods 0.000 description 1
- 230000004048 modification Effects 0.000 description 1
- 239000003068 molecular probe Substances 0.000 description 1
- 239000013642 negative control Substances 0.000 description 1
- 108020004707 nucleic acids Proteins 0.000 description 1
- 102000039446 nucleic acids Human genes 0.000 description 1
- 150000007523 nucleic acids Chemical class 0.000 description 1
- 239000002245 particle Substances 0.000 description 1
- 239000013610 patient sample Substances 0.000 description 1
- 238000002264 polyacrylamide gel electrophoresis Methods 0.000 description 1
- 238000003752 polymerase chain reaction Methods 0.000 description 1
- 108091033319 polynucleotide Proteins 0.000 description 1
- 102000040430 polynucleotide Human genes 0.000 description 1
- 239000002157 polynucleotide Substances 0.000 description 1
- 238000002600 positron emission tomography Methods 0.000 description 1
- 125000002924 primary amino group Chemical group [H]N([H])* 0.000 description 1
- 229940126409 proton pump inhibitor Drugs 0.000 description 1
- 239000000612 proton pump inhibitor Substances 0.000 description 1
- 238000004007 reversed phase HPLC Methods 0.000 description 1
- PYWVYCXTNDRMGF-UHFFFAOYSA-N rhodamine B Chemical compound [Cl-].C=12C=CC(=[N+](CC)CC)C=C2OC2=CC(N(CC)CC)=CC=C2C=1C1=CC=CC=C1C(O)=O PYWVYCXTNDRMGF-UHFFFAOYSA-N 0.000 description 1
- 239000000243 solution Substances 0.000 description 1
- 230000003595 spectral effect Effects 0.000 description 1
- 239000000758 substrate Substances 0.000 description 1
- 238000011144 upstream manufacturing Methods 0.000 description 1
- 239000011534 wash buffer Substances 0.000 description 1
- 238000005406 washing Methods 0.000 description 1
- 239000012224 working solution Substances 0.000 description 1
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12Q—MEASURING OR TESTING PROCESSES INVOLVING ENZYMES, NUCLEIC ACIDS OR MICROORGANISMS; COMPOSITIONS OR TEST PAPERS THEREFOR; PROCESSES OF PREPARING SUCH COMPOSITIONS; CONDITION-RESPONSIVE CONTROL IN MICROBIOLOGICAL OR ENZYMOLOGICAL PROCESSES
- C12Q1/00—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions
- C12Q1/68—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions involving nucleic acids
- C12Q1/6813—Hybridisation assays
- C12Q1/6834—Enzymatic or biochemical coupling of nucleic acids to a solid phase
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Life Sciences & Earth Sciences (AREA)
- Zoology (AREA)
- Wood Science & Technology (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Health & Medical Sciences (AREA)
- Engineering & Computer Science (AREA)
- Microbiology (AREA)
- Immunology (AREA)
- Physics & Mathematics (AREA)
- Molecular Biology (AREA)
- Biotechnology (AREA)
- Biophysics (AREA)
- Analytical Chemistry (AREA)
- Biochemistry (AREA)
- Bioinformatics & Cheminformatics (AREA)
- General Engineering & Computer Science (AREA)
- General Health & Medical Sciences (AREA)
- Genetics & Genomics (AREA)
- Measuring Or Testing Involving Enzymes Or Micro-Organisms (AREA)
Abstract
Description
本発明は、チトクロムP450-2C19をコードする遺伝子の中に位置する突然変異の検出のための方法およびキットに関する。
P450-2C19は、様々な臨床的に重要な薬物の代謝に関与する代謝酵素である。P450-2C19よって代謝されられる薬物は、抗鬱薬、抗不安薬、抗マラリア薬、およびプロトンポンプ阻害剤を含む。P450の他のメンバーと同様に、個体は、2C19酵素活性のレベルに基づいて、高代謝群または低代謝群として分類することができる。
CYP2C19遺伝子は、CYP2C8、CYP2C9、およびCYP2C18、ならびにより離れて関連するCYPファミリーのメンバーを含む多くのCYP遺伝子のクラスター中の染色体10q23上に位置する。遺伝子は、約50 Kbpの領域にわたる9つのエキソンからなる。
多重対立遺伝子プライマー伸長、および伸長されたプライマーの固体支持体へのハイブリダイゼーションは、先行技術の中に一般的に記述されている。ASPE技術は、米国特許第4,851,331号(特許文献1)に概説されている。本技術は、ゲノム中の特異的な多型部位の有無を同定するよう設計される。
(1)多重化PCRを利用して、多型遺伝子座を含むDNAの領域を増幅する工程。
(2)DNAの増幅領域が対立遺伝子特異的伸長のための標的配列として働く、プライマーの対立遺伝子特異的伸長。標的配列と完全マッチを形成する3'末端ヌクレオチドを有する伸長プライマーを伸長して、伸長産物を形成する。改変ヌクレオチドは伸長産物に組み入れらて、このようなヌクレオチドは検出目的で伸長産物を効率的に標識する。あるいは、伸長プライマーは、標的配列とミスマッチを形成する3'末端ヌクレオチドを代わりに含み得る。この場合、プライマー伸長は起こらない。
(3)マイクロアレイなどの固体支持体上の、伸長産物の5'端に相補的であるプローブに、伸長産物をハイブリダイズする工程。
ひとつの態様において、本発明は、表1に認められる突然変異の群より選択される試料中の変異体の有無を検出する方法であって、以下の工程を含む方法を提供する:
SEQ ID NO:2 およびSEQ ID NO:3、SEQ ID NO:4および SEQ ID NO:5、SEQ ID NO:6およびSEQ ID NO:7、SEQ ID NO:8 およびSEQ ID NO:9、ならびにSEQ ID NO:10およびSEQ ID NO:11からなるPCRプライマー対の群より選択される、少なくとも二つのPCRプライマー対を用いて、上述の突然変異を含み得るDNAの領域を増幅する工程。
SEQ ID NO:12〜SEQ ID NO:25からなる群より選択されるタグ付き対立遺伝子特異的伸長プライマーを、増幅DNAの相補的領域にハイブリダイズする工程であって、各タグ付き対立遺伝子特異的プライマーは、増幅DNAの領域に相補的な3'部分、上述の変異体部位のひとつの1つの対立遺伝子(野生型または突然変異型)に相補的な3'末端ヌクレオチド、およびプローブ(アンチタグ)配列に相補的な5'部分を有する、工程。
プライマーの3'末端ヌクレオチドが標的配列中の対応するヌクレオチドに相補的である場合に、タグ付きASPEプライマーを伸長させ、これによりプライマーの標識伸長産物が合成される工程;プライマーの末端ヌクレオチドが標的配列中の対応するヌクレオチドに相補的でない場合には、伸長産物は合成されない。
伸長産物をプローブにハイブリダイズする工程、および標識された伸長産物の検出。標識された伸長産物の検出は、ASPEプライマーの3'末端ヌクレオチドに相補的な対立遺伝子の存在を示している。標識された伸長産物が存在しない場合、ASPEプライマーの3'端に相補的な対立遺伝子が試料中に存在しないと判定される。
本出願において用いられる次の用語は、以下に定義された意味を有すると理解される。
上述の変異体を含み得るDNAの領域を増幅する工程。
少なくとも二つのタグ付き対立遺伝子特異的伸長プライマーを増幅DNAの相補的領域にハイブリダイズする工程であって、各タグ付き対立遺伝子特異的プライマーが、増幅DNAの領域に相補的な3'部分、上述の突然変異部位のひとつの1つの対立遺伝子(野生型または突然変異型)に相補的な3'末端ヌクレオチド、およびプローブ配列に相補的な5'部分を有する、工程。
プライマーの3'末端ヌクレオチドが標的配列中の対応するヌクレオチドに相補的である場合に、タグ付きASPEプライマーを伸長させ、これによりプライマーの標識伸長産物が合成される工程;プライマーの末端ヌクレオチドが標的配列中の対応するヌクレオチドに相補的でない場合には、伸長産物は合成されない。
以下の方法において使用するための核酸(最も好ましくはゲノムDNA)を提供するため、当技術分野において公知の様々な方法を用いて患者試料を抽出することができる。好ましい態様において、DNA試料は全血から抽出される。
最初の工程において、変異体部位を含むCYP2C19をコードする遺伝子由来のDNAの少なくとも二つの領域が増幅される。
本発明の方法のASPE工程は、SEQ ID NO:12〜SEQ ID NO:25からなるASPEプライマーの群より選択されるタグ付きASPEプライマーを用いて実施される。
本発明の対立遺伝子特異的プライマーのタグ付き5'部分はプローブ配列に相補的である。対立遺伝子特異的プライマーを、対応するプローブ配列にハイブリダイズすると、伸長産物の存在を検出できる。
さらなる態様において、本発明はCYP2C19をコードする遺伝子中の突然変異の多重検出のためのキットを提供する。
1) オリゴヌクレオチド
全てのオリゴヌクレオチドは、Integrated DNA Technologies(Coralville, IA)によって合成された。PCRプライマーは無修飾であり、標準的な脱塩手順により精製した。カルボキシル化ミクロスフェアと連結するために、汎用アンチタグ(プローブ)を3'-C7アミノ修飾した。全てのアンチタグを逆相HPLC精製した。対立遺伝子特異的配列に対して5'側の24merの汎用タグ配列からなるキメラASPEプライマーもまた無修飾であったが、ポリアクリルアミドゲル電気泳動により精製した。再構成の後、供給業者により提供された吸光係数を用いて、正確なオリゴヌクレオチド濃度を分光測定で決定した。再構成されたオリゴヌクレオチドを200 nmから800 nmの間でスキャンし、260 nmにおいて吸光度を測定してオリゴヌクレオチド濃度を計算した。
Platinum Taq、Platinum Tsp、個々のdNTP、およびビオチン-dCTPは、Invitrogen Corporation(Carlsbad, CA)から購入した。シュリンプアルカリフォスファターゼおよびエキソヌクレアーゼIは、USB Corporation(Cleveland, OH)から購入した。カルボキシル化蛍光ミクロスフェアは、Luminex Corporation(Austin, TX)により提供された。EDCクロスリンカー(1-エチル-3-(3-ジメチルアミノプロピル)カルボジイミドハイドロクロリド)は、Pierce(Rockford, IL)から購入した。MES(2-(N-モルフォリノ)エタンスルホン酸)、10% SDS、NaCl、Tris、Triton X-100、Tween-20、およびTE緩衝液を含むOmniPur試薬は、EM Science(Darmstadt, Germany)から購入した。ストレプトアビジン-接合フィコエリスリンは、Molecular Probes Inc.(Eugene, OR)から入手した。
a) 多重PCR(5重):
最終容積25uL中でゲノムDNA 25 ngを用いて多重PCRを実行した。「無標的」PCRネガティブ対照を各アッセイの実行に含んだ。反応は、20 mmol/LのTris-HCl、pH8.4、50 mmol/LのKCl、2.5 mmol/LのMgCl2、それぞれ200 umol/LのdNTP、5ユニットのPlatinum Taq 、および150 nmol/Lのプライマーからなった。MJ Research PTC-200サーモサイクラー(Waterdown MA)中で、95℃で5分間に続いて、95℃で30秒間、58℃で30秒間、および72℃で30秒間を30サイクルというサイクルパラメータ設定を用いて、試料のサイクルを行った。その後、試料を72℃で5分間保持し、使用まで4℃で保管した。
ASPE反応に先立って、プライマー伸長反応の間にビオチン-dCTPを効率的に取り込むことができるように、各PCR反応物をシュリンプアルカリフォスファターゼ(SAP)で処理し、いかなる残存ヌクレオチド(特にdCTP)も不活性化した。また、タグ付きASPEプライマーおよび伸長反応自体へのいかなる干渉も回避するために、各PCR反応物をエキソヌクレアーゼI(EXO)で処理し、残存PCRプライマーを分解した。各PCR反応物 25 uLに対して、SAP 2.0 uL(2.0ユニット)およびEXO 0.5 uL(5ユニット)を直接加え、試料をボルテックスし、短時間遠心分離した。その後、試料を37℃で30分間インキュベートし、続いて酵素を不活性化するため99℃で15分間インキュベートした。その後、試料を直接ASPE反応に加えた。
Luminex's 1工程カルボジイミド連結手順の後、アミノ修飾アンチタグ配列をカルボキシル化ミクロスフェアに連結した。簡潔に述べると、最終容量50 uL の0.1 mol/L MES, pH4.5中で、5×106個のミクロスフェアを1 nmol NH2-オリゴに結合させた。使用直前に10 mg/mL EDC作業溶液を調製し、2.5 uLをビーズ混合物に添加し30分間インキュベートした。新たに調製されたEDCの第二の2.5 uL分割量を添加し、その後さらに30分間インキュベートした。0.02%(v/v)Tween-20および0.1%(w/v)SDS中で洗浄後、アンチタグ連結ビーズをTE緩衝液(10 mmol/LのTris, pH8.0、1 mmol/LのEDTA)100uL中に再懸濁した。ビーズ濃度を、Beckman Coulter Z2 粒子計算およびサイズ解析装置(Coulter Corp, Miami FL)を用いて決定した。
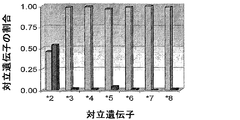
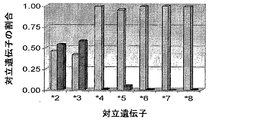
10アンチタグを有するビーズ集団のそれぞれ約2500ビーズを用いて、各ハイブリダイゼーション反応を実行した。ビーズをハイブリダイゼーション緩衝液(0.22 mol/LのNaCl、0.11 mol/LのTris, pH 8.0、および0.088%(v/v)Triton X-100)に混合し、混合物の45 uLをMJ Research 96-ウェルプレート(Reno, NV)の各ウェルに添加した。その後、各ASPE反応物の5 uL分割量を各ウェルに直接添加した。その後、MJ Research PTC-100中で試料を96℃で2分間熱し、次に37℃で1時間インキュベートした。このインキュベーションの後、試料を1.2 umのDurapore膜(Millipore Corp, Bedford, MA)を通して濾過し、洗浄緩衝液(0.2 mol/LのNaCl、0.1 mol/LのTris, pH8.0、および0.08%(v/v)Triton X-100)を用いて1回洗浄した。その後、ビーズをレポーター溶液(洗浄緩衝液中に1 ug/mL ストレプトアビジン接合フィコエリスリン)150 uL中に再懸濁し、室温で15分間インキュベートした。反応物をLuminex xMAPで読み取った。ビーズ集団および100 uL試料容量当たり100事象を測定するように取得パラメータを設定した。ゲート設定を、試料を流す前に確立し、研究経過中の全期間を通じて維持した。
Claims (15)
- チトクロームP450-2C19をコードしている遺伝子中の多型部位において、CYP2C19*2、CYP2C19*3、CYP2C19*4、CYP2C19*5、CYP2C19*6、CYP2C19*7、およびCYP2C19*8からなる群より選択されるヌクレオチド変異体の有無を検出するための方法であって、以下の工程を含む方法:
(a)前記変異体を含むDNAの領域を増幅して、増幅DNA産物を形成する工程;
(b)少なくとも二つのタグ付き対立遺伝子特異的伸長プライマーを、増幅DNA産物中の相補的標的配列にハイブリダイズする工程であって、各タグ付き対立遺伝子特異的伸長プライマーが、増幅DNAにハイブリダイズすることが可能な3'端ハイブリダイズ部分を有し、かつ少なくとも二つのタグ付き対立遺伝子特異的伸長プライマーの3'端ハイブリダイズ部分がSEQ ID NO:12〜SEQ ID NO:25の塩基25以上からなる群より選択される配列、および対応するプローブ配列に相補的な5'端タグ部分を含み、3'端ハイブリダイズ部分の末端ヌクレオチドが、疑わしい変異体ヌクレオチドまたはその部位の対応する野生型ヌクレオチドのいずれかに相補的である工程;
(c)3'端ハイブリダイズ部分の末端ヌクレオチドが増幅DNA産物中の多型部位の一つの対立遺伝子に完全マッチしている場合、標識ヌクレオチドを用いて少なくとも二つのタグ付き対立遺伝子特異的伸長プライマーを伸長させる工程;
(d)少なくとも二つのタグ付き対立遺伝子特異的伸長プライマーを、対応するプローブ配列にハイブリダイズし、標識された伸長産物の存在を検出する工程。 - 少なくとも二つのタグ付き対立遺伝子特異的プライマーの5'端タグ部分が、SEQ ID NO:12〜SEQ ID NO:25の塩基1〜24からなる群より選択される配列を含む、請求項2記載の方法。
- プローブ配列が固体支持体に連結している、請求項1記載の方法。
- 固体支持体が、ビーズ、スペクトル的にコード化されたビーズ、およびチップに基づくマイクロアレイからなる群より選択される、請求項3記載の方法。
- 増幅する工程が、以下からなる対の群より選択されるPCRプライマーの少なくとも二つの対を含むPCR増幅プライマーセットを用いて、PCRにより実施される、請求項1記載の方法:
SEQ ID NO:2およびSEQ ID NO:3、SEQ ID NO:4およびSEQ ID NO:5、SEQ ID NO:6およびSEQ ID NO:7、SEQ ID NO:8およびSEQ ID NO:9、ならびにSEQ ID NO:10およびSEQ ID NO:11。 - チトクロームP450-2C19をコードしている遺伝子中の多型部位において、CYP2C19*2、CYP2C19*3、CYP2C19*4、CYP2C19*5、CYP2C19*6、CYP2C19*7、およびCYP2C19*8からなる群より選択されるヌクレオチド変異体の有無を検出するための方法であって、以下の工程を含む方法:
(a)前記変異体を含むDNAの領域を増幅して、増幅DNA産物を形成する工程;
(b)SEQ ID NO:12〜SEQ ID NO:25からなる群より選択される少なくとも二つのタグ付き対立遺伝子特異的伸長プライマーを、増幅DNA産物中の相補的標的配列にハイブリダイズする工程であって、各タグ付き対立遺伝子特異的伸長プライマーが、増幅DNAにハイブリダイズすることが可能な3'端ハイブリダイズ部分および対応するプローブ配列に相補的な5'端タグ部分を有し、3'端ハイブリダイズ部分の末端ヌクレオチドが、疑わしい変異体ヌクレオチドまたはその部位の対応する野生型ヌクレオチドのいずれかに相補的である工程;
(c)3'端ハイブリダイズ部分の末端ヌクレオチドが増幅DNA産物中の多型部位の一つの対立遺伝子に完全マッチしている場合、標識ヌクレオチドを用いて少なくとも二つのタグ付き対立遺伝子特異的伸長プライマーを伸長させる工程;
(d)少なくとも二つのタグ付き対立遺伝子特異的伸長プライマーを対応するプローブ配列にハイブリダイズし、標識された伸長産物の存在を検出する工程。 - プローブ配列が固体支持体に連結している、請求項6記載の方法。
- 固体支持体が、ビーズ、スペクトル的にコード化されたビーズ、およびチップに基づくマイクロアレイからなる群より選択される、請求項7記載の方法。
- 増幅する工程が、以下からなる対の群より選択されるPCRプライマーの少なくとも二つの対を含むPCR増幅プライマーセットを用いて、PCRにより実施される、請求項6記載の方法:
SEQ ID NO:2およびSEQ ID NO:3、SEQ ID NO:4およびSEQ ID NO:5、SEQ ID NO:6およびSEQ ID NO:7、SEQ ID NO:8およびSEQ ID NO:9、ならびにSEQ ID NO:10およびSEQ ID NO:11。 - チトクロムP450-2C19をコードする遺伝子中の多型部位において、CYP2C19*2、CYP2C19*3、CYP2C19*4、CYP2C19*5、CYP2C19*6、CYP2C19*7、およびCYP2C19*8からなる群より選択されるヌクレオチド変異体の有無を検出するためのキットであって、少なくとも二つのタグ付き対立遺伝子特異的伸長プライマーのセット含み、各タグ付き対立遺伝子特異的伸長プライマーは、疑わしい変異体ヌクレオチドまたは多型部位の一つの対応する野生型ヌクレオチドのいずれかに相補的な3'末端ヌクレオチドを含む3'端ハイブリダイズ部分、および対応するプローブ配列に相補的な5'端タグ付き部分を有し、かつ少なくとも二つのタグ付き対立遺伝子特異的伸長プライマーはSEQ ID NO:12〜SEQ ID NO:25からなる群より選択される、キット。
- 多型部位を含むDNAの領域を増幅するための、以下からなる対の群より選択されるPCRプライマーの少なくとも二つの対を含むPCR増幅プライマーセットをさらに含む、請求項10記載のキット:
SEQ ID NO:2およびSEQ ID NO:3、SEQ ID NO:4およびSEQ ID NO:5、SEQ ID NO:6およびSEQ ID NO:7、SEQ ID NO:8およびSEQ ID NO:9、ならびにSEQ ID NO:10およびSEQ ID NO:11。 - プローブのセットをさらに含む、請求項10記載のキット。
- プローブのセットが支持体に連結している、請求項12記載のキット。
- チトクロムP450-2C19をコードする遺伝子中の少なくとも二つの多型部位において、CYP2C19*2、CYP2C19*3、CYP2C19*4、CYP2C19*5、CYP2C19*6、CYP2C19*7、およびCYP2C19*8からなる群より選択される変異体ヌクレオチドの有無の検出に使用するためのキットであって、少なくとも二つの多型部位を含むDNAの領域を増幅するための、以下からなる対の群より選択されるPCRプライマーの少なくとも二つの対を含むPCR増幅プライマーセットを含む、キット:SEQ ID NO:2およびSEQ ID NO:3、SEQ ID NO:4およびSEQ ID NO:5、SEQ ID NO:6およびSEQ ID NO:7、SEQ ID NO:8およびSEQ ID NO:9、ならびにSEQ ID NO:10およびSEQ ID NO:11。
- 少なくとも二つのタグ付き対立遺伝子特異的伸長プライマーのセットをさらに含むキットであって、各タグ付き対立遺伝子特異的伸長プライマーは、増幅DNAにハイブリダイズすることが可能な3'端ハイブリダイズ部分、対応するプローブ配列に相補的な5'端タグ部分を有し、3'端ハイブリダイズ部分の末端ヌクレオチドは、疑わしい変異体ヌクレオチドまたは多型部位の対応する野生型ヌクレオチドのいずれかに相補的である、請求項14記載のキット。
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US59212404P | 2004-07-30 | 2004-07-30 | |
| PCT/CA2005/001180 WO2006010266A1 (en) | 2004-07-30 | 2005-07-29 | Method of detecting mutations in the gene encoding cytochrome p450-2c19 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2008507955A true JP2008507955A (ja) | 2008-03-21 |
| JP2008507955A5 JP2008507955A5 (ja) | 2008-09-11 |
Family
ID=35785879
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2007522887A Pending JP2008507955A (ja) | 2004-07-30 | 2005-07-29 | チトクロムp450−2c19をコードする遺伝子における突然変異を検出する方法 |
Country Status (6)
| Country | Link |
|---|---|
| US (1) | US20080248466A1 (ja) |
| EP (1) | EP1778868A4 (ja) |
| JP (1) | JP2008507955A (ja) |
| AU (1) | AU2005266805B2 (ja) |
| CA (1) | CA2575422A1 (ja) |
| WO (1) | WO2006010266A1 (ja) |
Families Citing this family (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US20090215637A1 (en) * | 2004-06-30 | 2009-08-27 | Frank Merante | Method of detecting mutations in the gene encoding cytochrome P450-2D6 |
| CA2571817A1 (en) * | 2004-06-30 | 2006-01-12 | Tm Bioscience Pgx, Inc. | Method of detecting mutations in the gene encoding cytochrome p450-2c9 |
| AU2009236729B2 (en) * | 2008-01-25 | 2012-12-06 | Theranostics Laboratory | Methods and compositions for the assessment of drug response |
| US20120035060A1 (en) * | 2010-08-03 | 2012-02-09 | Bioarray Solutions, Ltd. | Highly multiplexed genotyping using leukoreduced blood samples |
Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2000004766A1 (en) * | 1998-07-24 | 2000-02-03 | Delaval Holding Ab | An apparatus for automatically milking an animal |
| US20030059774A1 (en) * | 2000-08-30 | 2003-03-27 | Carl Risinger | Detection of CYP2C19 polymorphisms |
Family Cites Families (13)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US4851331A (en) * | 1986-05-16 | 1989-07-25 | Allied Corporation | Method and kit for polynucleotide assay including primer-dependant DNA polymerase |
| US5474796A (en) * | 1991-09-04 | 1995-12-12 | Protogene Laboratories, Inc. | Method and apparatus for conducting an array of chemical reactions on a support surface |
| US5605662A (en) * | 1993-11-01 | 1997-02-25 | Nanogen, Inc. | Active programmable electronic devices for molecular biological analysis and diagnostics |
| JPH0856695A (ja) * | 1993-07-20 | 1996-03-05 | Sumitomo Chem Co Ltd | 安全性評価方法 |
| US6620593B1 (en) * | 1993-07-20 | 2003-09-16 | Sumitomo Chemical Company, Limited | Method for safety evaluation of chemical compound using recombinant yeast expressing human cytochrome P450 |
| AU5890899A (en) * | 1998-08-28 | 2000-03-21 | Sangtec Molecular Diagnostics Ab | A method for measuring a patient's ability to metabolise certain drugs |
| GB9902971D0 (en) * | 1999-02-11 | 1999-03-31 | Zeneca Ltd | Assay |
| US6287778B1 (en) * | 1999-10-19 | 2001-09-11 | Affymetrix, Inc. | Allele detection using primer extension with sequence-coded identity tags |
| BRPI0206747B1 (pt) * | 2001-01-25 | 2017-03-21 | Luminex Molecular Diagnostics Inc | polinucleotídeos para uso como etiquetas e complementos de etiquetas, fabricação e uso dos mesmos |
| AU2002314734B2 (en) * | 2001-03-30 | 2007-08-30 | Ge Healthcare Bio-Sciences Ab | P450 single nucleotide polymorphism biochip analysis |
| US7195877B2 (en) * | 2001-07-20 | 2007-03-27 | Bioventures, Inc. | Cytochrome P450 genetic variations |
| DE10237691B4 (de) * | 2002-08-15 | 2010-01-28 | Biotez Berlin-Buch Gmbh Biochemisch-Technologisches Zentrum | Verfahren zum Nachweis von Einzelnukleotid-Polymorphismen (SNP) in Genen des Arzneimittelmetabolismus und Testkit zur Durchführung des Verfahrens |
| CA2571817A1 (en) * | 2004-06-30 | 2006-01-12 | Tm Bioscience Pgx, Inc. | Method of detecting mutations in the gene encoding cytochrome p450-2c9 |
-
2005
- 2005-07-29 US US11/658,798 patent/US20080248466A1/en not_active Abandoned
- 2005-07-29 CA CA002575422A patent/CA2575422A1/en not_active Abandoned
- 2005-07-29 WO PCT/CA2005/001180 patent/WO2006010266A1/en active Application Filing
- 2005-07-29 AU AU2005266805A patent/AU2005266805B2/en not_active Ceased
- 2005-07-29 JP JP2007522887A patent/JP2008507955A/ja active Pending
- 2005-07-29 EP EP05770386A patent/EP1778868A4/en not_active Withdrawn
Patent Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2000004766A1 (en) * | 1998-07-24 | 2000-02-03 | Delaval Holding Ab | An apparatus for automatically milking an animal |
| US20030059774A1 (en) * | 2000-08-30 | 2003-03-27 | Carl Risinger | Detection of CYP2C19 polymorphisms |
Also Published As
| Publication number | Publication date |
|---|---|
| AU2005266805B2 (en) | 2010-10-28 |
| EP1778868A1 (en) | 2007-05-02 |
| US20080248466A1 (en) | 2008-10-09 |
| EP1778868A4 (en) | 2007-12-12 |
| AU2005266805A1 (en) | 2006-02-02 |
| WO2006010266A1 (en) | 2006-02-02 |
| CA2575422A1 (en) | 2006-02-02 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| US7879543B2 (en) | Method of detecting mutations associated with thrombosis | |
| JP3937136B2 (ja) | 塩基多型の検出方法 | |
| EP1231281B1 (en) | Method of detecting variation or polymorphism | |
| US20060199183A1 (en) | Probe biochips and methods for use thereof | |
| JP2007525998A (ja) | 脆弱x症候群などのstrpの検出 | |
| US20070238113A1 (en) | Method for detecting mutations and/or polymorphisms | |
| AU2005259786B2 (en) | Method of detecting mutations in the gene encoding cytochrome P450-2C9 | |
| JPWO2008066162A1 (ja) | Cyp2c19遺伝子増幅用プライマーセット、それを含むcyp2c19遺伝子増幅用試薬およびその用途 | |
| US20070003938A1 (en) | Hybridization of genomic nucleic acid without complexity reduction | |
| Voisey et al. | SNP technologies for drug discovery: a current review | |
| AU2005266805B2 (en) | Method of detecting mutations in the gene encoding Cytochrome P450-2C19 | |
| AU2005259787B2 (en) | Method of detecting mutations in the gene encoding cytochrome P450-2D6 | |
| KR101249635B1 (ko) | 양극성 장애 진단용 egr2 유전자 snp, 그를 포함하는 마이크로어레이 및 키트 | |
| JP2013074824A (ja) | Mdr1遺伝子の多型を検出するためのプローブ | |
| JP2010246400A (ja) | 多型の識別方法 | |
| JP2009022191A (ja) | ヒトチトクロームp450(cyp)2d6遺伝子変異の検出方法 | |
| JP2005245273A (ja) | アルデヒド脱水素酵素遺伝子多型の簡易検出方法および検出用試薬 | |
| JP2005027519A (ja) | ヒトチトクロームp4502a6遺伝子多型の簡易検出方法および検出用試薬 | |
| JP2005198525A (ja) | グルタチオンs−トランスフェラーゼ遺伝子多型の検出方法および検出用キット |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20080724 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20080724 |
|
| A711 | Notification of change in applicant |
Free format text: JAPANESE INTERMEDIATE CODE: A712 Effective date: 20090701 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20100312 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A821 Effective date: 20100312 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20110317 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20110617 |
|
| A02 | Decision of refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A02 Effective date: 20111205 |