JP2007520480A - 少なくとも一つの脂肪酸を含むジヒドロピリジンタイプのカルシウムアンタゴニスト用の経皮的デリバリー器具 - Google Patents
少なくとも一つの脂肪酸を含むジヒドロピリジンタイプのカルシウムアンタゴニスト用の経皮的デリバリー器具 Download PDFInfo
- Publication number
- JP2007520480A JP2007520480A JP2006549643A JP2006549643A JP2007520480A JP 2007520480 A JP2007520480 A JP 2007520480A JP 2006549643 A JP2006549643 A JP 2006549643A JP 2006549643 A JP2006549643 A JP 2006549643A JP 2007520480 A JP2007520480 A JP 2007520480A
- Authority
- JP
- Japan
- Prior art keywords
- transdermal delivery
- drug
- delivery device
- type calcium
- fatty acid
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/70—Web, sheet or filament bases ; Films; Fibres of the matrix type containing drug
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/70—Web, sheet or filament bases ; Films; Fibres of the matrix type containing drug
- A61K9/7023—Transdermal patches and similar drug-containing composite devices, e.g. cataplasms
- A61K9/703—Transdermal patches and similar drug-containing composite devices, e.g. cataplasms characterised by shape or structure; Details concerning release liner or backing; Refillable patches; User-activated patches
- A61K9/7038—Transdermal patches of the drug-in-adhesive type, i.e. comprising drug in the skin-adhesive layer
- A61K9/7046—Transdermal patches of the drug-in-adhesive type, i.e. comprising drug in the skin-adhesive layer the adhesive comprising macromolecular compounds
- A61K9/7053—Transdermal patches of the drug-in-adhesive type, i.e. comprising drug in the skin-adhesive layer the adhesive comprising macromolecular compounds obtained by reactions only involving carbon to carbon unsaturated bonds, e.g. polyvinyl, polyisobutylene, polystyrene
- A61K9/7061—Polyacrylates
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/435—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom
- A61K31/44—Non condensed pyridines; Hydrogenated derivatives thereof
- A61K31/455—Nicotinic acids, e.g. niacin; Derivatives thereof, e.g. esters, amides
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/06—Organic compounds, e.g. natural or synthetic hydrocarbons, polyolefins, mineral oil, petrolatum or ozokerite
- A61K47/08—Organic compounds, e.g. natural or synthetic hydrocarbons, polyolefins, mineral oil, petrolatum or ozokerite containing oxygen, e.g. ethers, acetals, ketones, quinones, aldehydes, peroxides
- A61K47/12—Carboxylic acids; Salts or anhydrides thereof
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P9/00—Drugs for disorders of the cardiovascular system
- A61P9/12—Antihypertensives
Abstract
高血圧の治療のための、皮膚を通じたジヒドロピリジンタイプのカルシウムアンタゴニストのデリバリー用の経皮的デリバリー器具が提供される。前記器具は、裏張り層と接着性マトリックス貯蔵庫とを含んで良い。前記接着性マトリックス貯蔵庫は、裏張り層の一面に固着されており、少なくとも一つの脂肪酸浸透促進剤と、ジヒドロピリジンタイプのカルシウムアンタゴニストを含んで良い。
Description
本発明は、一週間までの継続時間の高血圧の治療のための十分な時間で、皮膚を介してジヒドロピリジンタイプのカルシウムアンタゴニストをデリバリーするための製剤に関する。
一つの実施態様では、本発明は、裏張り層と接着性マトリックス貯蔵庫とを含む経皮的デリバリー器具に関する。裏張り層は不透明であっても良い。接着性マトリックス貯蔵庫は、裏張り層の一面に固着されており、ジヒドロピリジンタイプのカルシウムアンタゴニストと、少なくとも一つの脂肪酸浸透促進剤とを含む。ある実施態様では、接着性マトリックス貯蔵庫は、本質的に溶媒を含まない。本発明は、感光性薬剤について適している。
脂肪酸浸透促進剤は、24時間に亘り5%まで増大した凝集物の経皮的デリバリーを生ずる。ある好ましい実施態様では、浸透促進剤は、24時間に亘り少なくとも20%まで凝集物の経皮的デリバリーを増大する。ある実施態様では、接着性マトリックス貯蔵庫は、二つ以上の別個の脂肪酸浸透促進剤を含んで良い。二つの別個の脂肪酸浸透促進剤は、分子の不飽和の度合いまたは鎖の長さが異なって良い。
ジヒドロピリジンタイプのカルシウムアンタゴニストは、接着性マトリックス貯蔵庫の少なくとも20重量%、または少なくとも50重量%以上を含んでも良い。
本発明の別の特徴点では、前記製剤は安定化剤を含んでも良く、それはジヒドロピリジンタイプのカルシウムアンタゴニストの分解を防止する。適切な安定化剤は、BHTまたはBHAのような抗酸化剤を含むがこれらに制限されない。
用語解説
以下の定義は、ここで頻繁に使用される特定の用語の理解を容易にするために提供される。
以下の定義は、ここで頻繁に使用される特定の用語の理解を容易にするために提供される。
用語「投与期間」は、デリバリー器具が被験者に活性剤または活性剤の組合せを放出する時間的な期間を意味する。
ここで互換的に使用される用語「薬剤」及び「薬剤組成物」は、ジヒドロピリジンタイプのカルシウムアンタゴニストを指す。
用語「薬剤貯蔵庫」は、経皮的デリバリー用の薬剤を保持して放出される、薬剤とマトリックス材料を組み合わせることによって生産される組成物を意味する。薬剤貯蔵庫は、薬剤貯蔵庫組成物、固体薬剤貯蔵庫層、固体薬剤貯蔵庫接着層、または液体薬剤貯蔵庫層であることができる。ある実施態様では、薬剤貯蔵庫は、マルチラミネートの経皮的薬剤デリバリー医療器具における固体薬剤貯蔵庫層であることができる。接着剤と組み合わされると、薬剤貯蔵庫は、固体薬剤貯蔵庫接着層であることもでき、それは例えばモノリスの経皮的薬剤デリバリー医療器具において使用できる。薬剤貯蔵庫は、他に記載がなければ、浸透促進剤、可塑剤、及びいずれかの他の適切な添加剤を含むこともできる。
用語「薬剤の移動に有効な関係」は、薬剤の経皮的投与に適応された器具が、薬剤の経皮的侵入を可能にするために被験者の皮膚と十分に接触を維持することを意味する。
用語「有効量」及び「治療上の有効量」は、所望の局所的または全身的な治療効果を提供するための化合物の非毒性だが十分な量を意味する。
用語「流動」は、32℃でヒトの死体の皮膚の領域を通じた単位領域辺りの薬剤のデリバリーの速度を意味する。
用語「モノリス」は、薬剤貯蔵庫層が、経皮的投与のための薬剤と、皮膚との接触を可能にする経皮的薬剤投与において医療器具を維持する接着剤組成物とを含む経皮的医療器具を意味する。ある実施態様では、モノリスは、薬剤組成物、接着剤組成物、及びマトリックス組成物を含む薬剤貯蔵庫接着層である。
用語「マルチラミネート」は、薬剤貯蔵庫層を含む少なくとも二つの層を含む経皮的医療器具を指す。ある実施態様では、マルチラミネートの経皮的医療器具は、固体薬剤貯蔵庫層、速度制御膜層、裏張り層、及び接着層を含むことができる。
用語「固体薬剤貯蔵庫」は、薬剤貯蔵庫組成物を生産するのに使用されるいずれかの溶媒を1%w/w未満、好ましくは1000ppm未満含む薬剤貯蔵庫を意味する。例えばある実施態様では、ヘプタンとイソプロピルアルコールを使用して生産された固体薬剤貯蔵庫は、固体薬剤貯蔵庫中に1000ppm未満のヘプタンと1000ppm未満のアルコールとを含む。
用語「浸透促進剤」は、組織を通じた所定の活性剤または活性剤の組み合わせの吸収を容易にする天然または合成の分子を意味する。
用語「感圧性接着剤」は、圧力の適用で基体に接着し、永久的に粘着性を維持する粘弾性物質を指す。
用語「被験者」は、動物、好ましくは哺乳類、より好ましくはヒトを意味する。
用語「持続放出」は、一定に期間に亘る活性剤または活性剤の組み合わせの連続的な放出を意味する。
「厚み」は、他に記載がなければ、ミル(1ミルは1インチの千分の一)単位で測定され、本発明の経皮的デリバリー医療器具を二つの顕微鏡スライドの間に配置した際の空間を測定することによって決定できる。
「経皮的」または「皮膚を通じての」デリバリーは、薬剤の局所的適用による薬剤の投与のための入り口として、皮膚及び/または他の身体表面の内部またはそれを通じた通過による薬剤のデリバリーを意味する。
用語「溶媒含量」は、カールフィッシャー法(水について)または適切な分析法(ガスクロマトグラフィー等)で測定され、本発明のデリバリー器具の百万当たりの部または重量パーセントとして表される、単位投与量辺りの残余の工程溶媒(例えば水、ヘプタン、イソプロピルアルコール)のパーセントである。
「凝集物の経皮的デリバリー」の増大は、死体の皮膚で測定され、凝集物の量は直接測定されるか、一連の流動測定の曲線の下部の領域を集積することによって測定される。
本発明に関する「ジヒドロピリジンタイプのカルシウムアンタゴニスト」は、ジヒドロピリジン環の2位と6位がメチルで置換され、3位と5位がプロピル、アセチル、メトキシカルボニル、エトキシカルボニル、またはメトキシメトキシカルボニル(CH3OCH3OOC-)で置換され、4位がニトロまたはクロロから選択される1から2の電子吸引基で置換されているシクロペンチルまたはシクロヘキシルで置換されているものである。用語「ジヒドロピリジンタイプのカルシウムアンタゴニスト」は、製薬学的に許容可能なその塩、並びに薬剤の塩基形態を包含する。ある実施態様では、ジヒドロピリジンタイプのカルシウムアンタゴニストは、フェロジピンまたはイスラジピンである。重量パーセンテージはここで、非塩形態に標準化された化合物を指す。
「脂肪酸浸透促進剤」は、各ジヒドロピリジンタイプのカルシウムアンタゴニストの凝集物の経皮的デリバリーを増大するのに有効である、C4-C30、好ましくはC1-C24の脂肪酸である。
「溶媒」は、ニート形態で25℃で液体である化合物である。それは製剤成分を可溶化または懸濁するのに有効である。典型的に好ましい溶媒は、穏やかな加熱により1%未満、好ましくは1000ppm未満に残余の溶媒濃度が容易に減少するため揮発性でもある。
本発明は、以下の発明の詳細な説明を通じて更に記載され、詳細な説明は本発明の好ましい実施態様を説明し、添付の特許請求の範囲に示された本発明の範囲を制限することを企図しない。以下の詳細な説明は、薬剤としてジヒドロピリジンタイプのカルシウムアンタゴニスト及び鎮痛薬的に有効なその誘導体を利用する本発明の実施態様を参考にして本発明を記載しているが、他の薬剤も本発明の技術で使用するのに適していることが理解されるべきである。
本発明の一つの実施態様では、接着性マトリックス材料を含む組成物が提供される。適切な接着性材料は、アクリレート、PIB、シリコーン、及び/またはポリイソブチレンを含むがこれらに制限されない。接着性マトリックスはまた、ポリジメチルシロキサンを任意に含んで良い。
裏張り材料は当該技術分野で周知であり、ポリエチレン、酢酸ビニル樹脂、エチレン/酢酸ビニルコポリマー、ポリビニルクロリド、ポリウレタン等のプラスチックフィルム、金属ホイル、不職布、布、市販のラミネートを含むことができる。裏張り材料は一般的に、2から1000ミクロメートルの範囲の厚みを有する。好ましい実施態様では、裏張り材料は、薬剤貯蔵層に含まれる薬剤、並びに薬剤貯蔵層の他の含有物に対して実質的に浸透可能でない。裏張りは、アルミニウムの相を含む複層ポリマーフィルムであっても良い。例えば裏張り材料は、ポリエチレンテレフタレート(PET)とポリエチレン−(酢酸ビニル)コポリマーのマルチラミネートを含むことができる。適切な裏張り材料の数多くの例が当該技術分野で認識されている。ある実施態様では、裏張りは不透明である。裏張り材料のある非制限的な特定の例は、(1)一面に被覆されたEVA(例えば12%酢酸ビニル、VA)のシール可能な層を有するPET裏張り材料;(2)低密度PET、ナイロン(登録商標)、EVA、及びエチレンビニルアルコールの層を含むフィルム;(3)低密度ポリエチレン、ナイロン(登録商標)、及びEVAの相を含むフィルム;(4)低密度ポリエチレンとナイロン(登録商標)を含む二層フィルム;(5)ポリエチレンの単一層;または(6)PETの単一層を含む。
各種の適切な切断可能な放出裏地が当該技術分野で周知であり、約3ミルの公称厚みで生産されたフルオロポリマー(例えばフルオロカーボンジアクリレート)またはシリコーン(ポリシロキサンポリマー)被覆ポリエステルフィルムを含む。適切な市販の放出裏地の例は、SCOTCHPAK(登録商標)9742として市販されている3M(Minneota, MN)によって製造される5見るのフルオロポリマー被覆ポリエステルフィルムを含む。フルオロポリマーコーティングを有する、ポリエステルまたはポリエチレンテレフタレート(PET)以外の材料で製造されたフィルムを使用することも可能である。例えば前記フィルムは、ポリスチレンまたはポリプロピレンからも製造できる。同じ材料は、シリコーンのような各種のコーティングでも使用できる。ポリシロキサンが複数ポリマー状接着システムの一部である好ましい実施態様として、放出裏地はシリコーン接着剤と適合可能でなければならない。本発明の特定の好ましい実施態様では、適切な市販の裏地は、約3ミルの厚みで生産されたフルオロポリマー被覆ポリエステルフィルムである3M社のSCOTCH PAK(登録商標)1022である。
好ましくは本発明の医療器具は、末端の少なくとも一部、好ましくは全部が密封されていない固体薬剤貯蔵庫を含む。用語、薬剤貯蔵庫と裏張り層の「末端」は、液体またはゲルベースの薬剤貯蔵庫を規定するために共に密封されているであろう端部の周囲の領域を指す。液体またはゲル薬剤貯蔵庫を含む医療器具とは異なり、本発明の特定の実施態様の医療器具の固体薬剤貯蔵庫は、末端の周囲を密封する必要がない。液体またはゲルの薬剤貯蔵庫層の末端は、裏張り層と膜の間のシールを通じて貯蔵庫からの薬剤の遺漏を防止するために実質的に流体を封じ込めるはずである。好ましい実施態様では、固体貯蔵庫層を含む本発明の医療器具は、パッチが剥がれても薬剤の遺漏の汚染が存在せず、遺漏に対して保存するための密封が必要ない。薬剤貯蔵庫層の密封の必要を避けることは、一つ以上の更なる工業生産工程を避けることによって生産コストを下げることが潜在的に可能である。
ある実施態様では、本発明の医療器具は、更に速度制御膜を含むことができる。速度制御膜は好ましくは、0.5から10ミルの厚み、好ましくは1-5ミルの厚みであり、例えば低密度ポリエチレン(LDPE)、EVAコポリマー(例えば40%w/wまで、好ましくは約5から19%w/wの間のVA)、熱密封可能なポリエステル、エラストマー性ポリエステルブロックコポリマー、PVC等からなることができる。
ある実施態様では、速度制御膜は、微小孔または多孔性材料を含むことができる。微小孔材料は、約0.08から0.5ミクロン、好ましくは約0.1から0.4ミクロン、より好ましくは約0.2から0.4ミクロンの直径範囲の孔を有する別個の孔の構造を有する。適切な微小孔膜の例は、ポリエチレンとポリプロピレンのフィルム、ナイロン(登録商標)、及びニトロセルロースフィルムを含む。本発明の他の実施態様は、Hoechst-Celanese, Charlotte, N.C.社から入手可能なCelgard K-256のような微小孔ポリエチレン膜を利用するであろう。そのような材料は、織布及び不職布として入手可能である。これらの材料は、ナイロン(登録商標)、ポリプロピレン、ポリエチレン、ポリオレフィン等から製造できる。
本発明の経皮的デリバリーシステムの形状は、必要なまたは所望のようにいずれの形態またはサイズであっても良い。パッチの好ましいサイズは、5から60cm2である。所定の継続時間で必要な速度で薬剤をデリバリーするために、パッチ中の薬剤の荷重量は、薬剤の飽和を維持するのに十分であるべきである。説明として、単一の投与量単位は、一日当たり約0.5mgの薬剤をデリバリーするために、3.5cm2の範囲で表面領域を有して良い。7日間の継続時間を維持するために、前記パッチは、薬剤でパッチを飽和するのに必要とされる量を超えて、約3.5mgの薬剤(7日間×0.5mg/日)を含むべきである。本発明では、マトリックス中の薬剤の溶解性は、20-30%の間と測定されている。本発明の接着剤/薬剤層についての許容可能なコーティング重量は5-10mg/cm2である。説明の目的のため、3.5cm2のパッチは、5mg/cm2のコーティング重量で飽和のために4.4mgの薬剤を必要とし、システム中で必要とされる約7.9mg(45%)の薬剤を生ずる。別の説明例では、3.5cm2のパッチは、25%の推定溶解度で、10mg/cm2のコーティング重量で飽和のために8.8mgの薬剤を必要とし、システム中で必要とされる12.3mg(35%)の薬剤の全量を有する。同様に、6.6mgの薬剤が、7.5mg/cm2のコーティング重量で飽和のために必要とされ、システム中で必要とされる10.1mg(39%)の薬剤の全量を有する。この目的のために使用されるアクリレート接着性マトリックス中の薬剤の高い溶解度の結果として、比較的高濃度の薬剤が、システム中の薬剤の飽和と、一週間までの継続期間に亘る定常速度の薬剤デリバリーを維持するために必要とされる。
ある実施態様では、経皮的薬剤デリバリーシステムのマトリックス組成物は、皮膚を通じた薬剤のデリバリーを加速するために既知の試薬を任意に含むことができる。これらの試薬は、皮膚浸透促進剤、アクセレラント、アジュバント、及び吸収促進剤として称されており、ここで集合的に「浸透促進剤」と称される。このクラスの試薬は、複数のポリマーの内部で薬剤の溶解性と拡散性を改良する機能を有するもの、例えば湿度を維持する角質層の能力を変更する、皮膚を軟化する、皮膚の浸透性を改良する、浸透助剤若しくは毛胞開口剤として作用する、または境界層を含む皮膚の状態を変更することにより、皮膚を介して吸収を改良するものを含む、多様な作用メカニズムを有するものを含む。これらの試薬のあるものは、一つより多い作用メカニズムを有するが、本質的にそれらは薬剤のデリバリーを促進するように機能する。
浸透促進剤は、24時間に亘り5%まで増大した凝集物の経皮的デリバリーを生ずるべきである。ある実施態様では、浸透促進剤は、24時間に亘り少なくとも20%まで凝集物の経皮的デリバリーを増大する。ある実施態様では、接着性マトリックス貯蔵庫は、二つ以上の別個の脂肪酸浸透促進剤を含んで良い。二つの別個の脂肪酸浸透促進剤は、不飽和の度合いが異なっても良い。
本発明での使用に適した浸透促進剤は、皮膚を通じた活性剤の吸収を容易にする天然または合成の分子を含むがそれらに制限されない。ある例の浸透促進剤は、薬剤の可溶性を促進する多価アルコール、例えばジプロピレングリコール、プロピレングリコール、及びポリエチレングリコール;オリーブオイル、スクアラン、及びラノリンのようなオイル;セチルエーテル及びオレイルエーテルのような脂肪エーテル;薬剤の拡散性を促進するイソプロピルミリステートのような脂肪酸エステル;水分を維持するケラチンの能力に影響するウレア及びアラントインのようなウレア誘導体;ケラチンの浸透性に影響する極性溶媒、例えばジメチルデシルホスホキシド、メチルオクチル-スルホキシド、ジメチルラウリルアミド、ドデシルピロリドン、イソソルビトール、ジメチル-アセトニド、ジメチルスルホキシド、デシルメチル-スルホキシド、及びジメチルホルムアミド;ケラチンを軟化するサリチル酸;浸透助剤であるアミノ酸;毛胞開口剤であるベンジルニコチネート;並びに皮膚と投与される薬剤の表面状態を変化するラウリルスルフェート塩のような高分子量脂肪族界面活性剤である。他の試薬は、オレイン酸及びリノレン酸、アスコルビン酸、パンテノール、ブチル化ヒドロキシトルエン、トコフェロール、トコフェリルアセタート、トコフェリルリノールエート、プロピルオレエート、イソプロピルパルミテート、及びグリセリルモノオレエートを含む。各促進剤の濃度は、0.5から20%の間であるべきである。
本発明の医療器具は、更に各種の増粘剤、フィラー、及び皮膚組成物での使用が既知である他の添加剤と共に提供されても良い。前記組成物が水を吸収する傾向を有する場合、例えばレシチンが共溶媒として使用されている場合、親水性フィラーが特に有用である。本発明は特に、感光性薬剤に良く適している。本発明の方法は、活性成分の分解を更に最小化するための黄色光の下で容易に実施されて良い。
本発明のある好ましい器具の特徴が上述されている一方で、本発明は、図面に説明され、以下に提供される特定の選ばれた実施態様に関して更に説明できる。以下に議論される選ばれた実施態様は説明の目的で含まれているものであり、一般的に記載される本発明の範囲を制限することを企図せず、いずれの態様でもそのように解釈されるべきではない。
図1におけるデータは、本発明のための敵で綱ベースポリマー、薬剤範囲、ポリマー範囲、及び促進剤を示す。本発明に適した各種のベースポリマー(接着剤)が、薬剤とベースポリマーについての適切な濃度の範囲と共に表に示されている。各ベースポリマーについて、適切な促進剤のリストが示されている。アクリレート接着剤は、最も広い範囲の促進剤と適合可能であり、アクリレート接着剤で使用されて良い促進剤のリストが、表内で別個に示されている。架橋剤と共に及びなしで各種の官能基を有するアクリレート接着剤が入手可能である。本発明については、化学的に反応性の官能基または架橋剤なしのアクリレート接着剤が最も適している。これらのアクリレート接着剤の範囲内では、オレイン酸とリノレン酸が、ジヒドロピリジン薬剤での最も有効な促進剤である。いくつかの適切な溶媒も表に掲載されている。
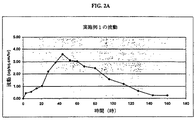
図2は、経皮的医療器具からのジヒドロピリジンタイプのカルシウムアンタゴニストフェロジピンの浸透プロフィールの一連のグラフを示す。特に図2は、アワリー単位の時間の関数としての、μg/cm2単位の医療器具からのジヒドロピリジンタイプのカルシウムアンタゴニストの流動速度を表すグラフを示す。
図2Aは、浸透促進剤を含まないプロトタイプの製剤から測定されたin vitro流動データを含む。前記製剤は、裏張りに結合した接着性貯蔵庫からなり、接着性貯蔵庫は、アクリレート接着剤、フェロジピン、及び安定化剤からなり、促進剤が添加されていない。この製剤から、一週間に亘り測定されたin vitroの流動は、約3日目で約3.5μg/cm2-hrのピークに増大し、継続時間に亘り減少した。図2Aに関する詳細は、実施例1に示されている。
図2Bは、接着性貯蔵庫が浸透促進剤として3%リノレン酸と6%オレイン酸を含む点を除いて、図2Aに示されたプロトタイプと同じプロトタイプの製剤から測定されたin vitro流動データを含む。この製剤からは、一週間に亘り測定されたin vitroの流動は、約2.5日目で約4.5μg/cm2-hrのピークに増大し、継続時間に亘り減少した。
図2Cは、接着性貯蔵庫が浸透促進剤として4%リノレン酸と8%オレイン酸を含む点を除いて、図2Aに示されたプロトタイプと同じプロトタイプの製剤から測定されたin vitro流動データを含む。この製剤からは、一週間に亘り測定されたin vitroの流動は、約1日未満で約5.5μg/cm2-hrのピークに増大し、継続時間に亘り減少した。図2における一連のグラフは、リノレン酸とオレイン酸という浸透促進剤の製剤への添加が、in vitro流動速度を増大し、最大の流動速度に到達するラグタイムを減少することを示す。
本発明の好ましい実施態様の多くが、ジヒドロピリジンタイプのカルシウムアンタゴニストを含む経皮的デリバリーパッチに関するものであるが、本発明はパッチ器具に制限されるものではない。当業者に予測できるように、各種のジヒドロピリジンタイプのカルシウムアンタゴニストを含む経皮的デリバリー器具が、本発明に従って調製できて使用できる。そのような経皮的デリバリー器具は物品の形態に制限はなく、テープ、パッチ、シート、包帯、または当業者に既知のいずれかの他の形態のような物品を含み、それらに制限されない。一般的に前記器具は、ジヒドロピリジンタイプのカルシウムアンタゴニスト、または他の薬剤の事前に選択された量を皮膚を通じてデリバリーするのに適したサイズのパッチの形態であろう。
本発明の各種の医療器具における固体薬剤貯蔵庫層または薬剤貯蔵庫接着層のための組成物の上述の記載を与えられた当業者は、各種の既知の加工法を使用して当該器具を生産できるであろう。好ましくは、本発明の固体薬剤貯蔵庫層及び薬剤貯蔵庫接着層を調製するための組成物は、以下に記載される工程を使用して生産される。
好ましい実施態様では本発明は、哺乳動物の皮膚、好ましくはヒトの皮膚の領域との接着を可能にする、皮膚を介した薬剤流動にジヒドロピリジンタイプのカルシウムアンタゴニストを含む医療器具を配置することにより、疾患を治療する方法を提供する。本発明に係るジヒドロピリジンタイプのカルシウムアンタゴニストを含む器具は、例えば慢性及び急性の高血圧といった、ジヒドロピリジンタイプのカルシウムアンタゴニストで治療が可能ないずれかの疾患を治療するために使用されて良い。前記器具は皮膚上に配置でき、企図される治療効果を達成または維持するのに十分な投与期間持続可能である。十分な投与期間を構成する時間は、本発明の器具の流動速度と治療される疾患を考慮して、当業者により選択できる。好ましい実施態様では、本発明の医療器具は、医学的に適切な投与期間に亘り哺乳動物の皮膚の領域と接触を可能にする薬剤流動を維持する。
薬剤の経皮的デリバリーは、従来の薬剤デリバリー手段に関連する過剰投与量及び投与量不足の問題を迂回する手段を与える。薬剤が静脈内または経口で投与される場合、血中の薬剤の初期濃度は迅速に最大値に達し、それは一般的に治療上の有効濃度の薬剤のものよりずっと高い。血中で最大濃度に到達した後、薬剤が分配、代謝、排出、または分解するため、次いで前記濃度はゆっくりと下降する。次第に薬剤の血中濃度は、治療上の有効濃度未満に下降する(即ち「投与量不足」)。この時点で、有効性を達成するために、薬剤を再投与する必要が生じる。薬剤の血中濃度を最小の治療上の有効濃度と毒性濃度の間に維持することが重要である。これを達成する一つの方法は、より低い薬剤投与量をより頻繁に患者に投与することである。しかしながらこれは、患者のコンプライアンスの問題のため、ほとんどの場合に許容し難い代替案である。薬剤の経皮的デリバリーは、薬剤のデリバリーの速度を患者からの薬剤のクリアランスの速度に従わせるようにデザインでき、かくして血中の薬剤濃度を一定に維持でき、薬剤の無駄と過剰投与の問題を減少できる。
薬剤のデリバリー速度を制御できるという利点に加えて、経皮的薬剤デリバリーは、快適で簡便な非侵襲性の薬剤投与方法を提供する。経口薬剤デリバリーに関する胃腸の刺激と他の副作用は減少または除去されて良く、針のような非侵襲性の方法に関する患者の不安の軽減もまた除去される。
以下の実施例は、本発明を更に説明するが、もちろん如何なる態様でも本発明の範囲を制限するとは解釈されるべきではない。
この明細書で引用される、特許及び特許出願を含むがそれらに制限されない印刷物及び参考文献は、書くここの印刷物または参考文献が、十分に示されているようにここに参考として特定的且つ個々的に取り込まれることが示されているように、引用される全範囲において完全に参考としてここに取り込まれる。本願が優先権を主張しているいずれの特許出願も、印刷物及び参考文献について上述したのと同じ態様で、ここに参考として取り込まれる。
本発明は好ましい実施態様について強調して記載されているが、好ましい器具及び方法における変形例が使用されて良いこと、本発明は特にここに記載されているもの以外でも実施されて良いことは当業者に明らかであろう。従って本発明は、添付の特許請求の範囲に規定される本発明の精神及び範囲内に包含される全ての変形例を含む。
実施例1
表1に示されたような湿潤基準で成分を混合することにより薬剤-接着剤溶液を調製し、30.0%w/wのフェロジピン、69.5%w/wのアクリレート接着剤(Gelva Multipolymer Solution 3071、ポリアクリレート、架橋剤なし、反応基なし)、及び0.5%w/wのBHTの乾燥組成を有する製剤を生産した。フェロジピンは35℃で30分間ソニケートすることにより、酢酸エチルに分散した。アクリレート接着剤溶液を添加し、混合物を35℃で30分間ソニケートした。BHTを添加し、混合物を約24時間ローラーミルで回転させ、均一な分散物を得た。このコーティング溶液を、非常に低速でコーターを使用し、適切なゲージを使用して、放出裏地(Medirelease 2249、シリコーン処理ポリエステルフィルム)にキャストし、約2ミルの乾燥厚みを得た。キャストフィルムを90℃の乾燥オーブンで20分間乾燥し、溶媒を除去した。裏張りフィルム(Scotchpak 1109、アルミニウム層を有する複層ポリマーフィルム)を、放出裏地の上の乾いたキャスト接着剤の露出表面にラミネートした。
表1に示されたような湿潤基準で成分を混合することにより薬剤-接着剤溶液を調製し、30.0%w/wのフェロジピン、69.5%w/wのアクリレート接着剤(Gelva Multipolymer Solution 3071、ポリアクリレート、架橋剤なし、反応基なし)、及び0.5%w/wのBHTの乾燥組成を有する製剤を生産した。フェロジピンは35℃で30分間ソニケートすることにより、酢酸エチルに分散した。アクリレート接着剤溶液を添加し、混合物を35℃で30分間ソニケートした。BHTを添加し、混合物を約24時間ローラーミルで回転させ、均一な分散物を得た。このコーティング溶液を、非常に低速でコーターを使用し、適切なゲージを使用して、放出裏地(Medirelease 2249、シリコーン処理ポリエステルフィルム)にキャストし、約2ミルの乾燥厚みを得た。キャストフィルムを90℃の乾燥オーブンで20分間乾燥し、溶媒を除去した。裏張りフィルム(Scotchpak 1109、アルミニウム層を有する複層ポリマーフィルム)を、放出裏地の上の乾いたキャスト接着剤の露出表面にラミネートした。
浸透試験:ヒトの死体の皮膚を通じたフェロジピンの流動を、In-Line Auto Sampling Equipmentを使用して測定した。受容溶液として32±0.5℃に維持した40%エタノール水溶液を使用して、実験を7日間稼動させた。0.62-cm2の領域の円形のパッチをラミネートから切断した;放出裏地を取り出し、皮膚を含む乾いた薬剤接着層と皮膚(角質層側)の断面に製剤を載せた。薬剤接着層と受容溶液の間に存在する皮膚層を有する細胞に、パッチと共に皮膚の断片を配置した。規則的な時間間隔で、皮膚の下部の細胞を通じて流動する受容溶液を回収し、HPLCによりフェロジピン含量について分析した。実施例1の浸透の結果が表2Aに示されており、アワリー単位の時間に対するμg/cm2/hr単位の流動を表している。
実施例2
表2に示されたような湿潤基準で成分を混合することにより薬剤-接着剤溶液を調製し、30.0%w/wのフェロジピン、60.5%w/wのアクリレート接着剤(Gelva Multipolymer Solution 3071、ポリアクリレート、架橋剤なし、反応基なし)、3.0%のリノレン酸(Crossential L98、浸透促進剤)、6.0%のオレイン酸(Super Refined Oleic Acid、浸透助剤)、及び0.5%w/wのBHTの乾燥組成を有する製剤を生産した。フェロジピンは35℃で30分間ソニケートすることにより、酢酸エチルに分散した。アクリレート接着剤溶液を添加し、混合物を35℃で30分間ソニケートした。リノレン酸、オレイン酸、及びBHTを添加し、混合物を約24時間ローラーミルで回転させ、均一な分散物を得た。このコーティング溶液を、非常に低速でコーターを使用し、適切なゲージを使用して、放出裏地(Medirelease 2249、シリコーン処理ポリエステルフィルム)にキャストし、約2ミルの乾燥厚みを得た。キャストフィルムを90℃の乾燥オーブンで20分間乾燥し、溶媒を除去した。裏張りフィルム(Scotchpak 1109、アルミニウム層を有する複層ポリマーフィルム)を、放出裏地の上の乾いたキャスト接着剤の露出表面にラミネートした。
表2に示されたような湿潤基準で成分を混合することにより薬剤-接着剤溶液を調製し、30.0%w/wのフェロジピン、60.5%w/wのアクリレート接着剤(Gelva Multipolymer Solution 3071、ポリアクリレート、架橋剤なし、反応基なし)、3.0%のリノレン酸(Crossential L98、浸透促進剤)、6.0%のオレイン酸(Super Refined Oleic Acid、浸透助剤)、及び0.5%w/wのBHTの乾燥組成を有する製剤を生産した。フェロジピンは35℃で30分間ソニケートすることにより、酢酸エチルに分散した。アクリレート接着剤溶液を添加し、混合物を35℃で30分間ソニケートした。リノレン酸、オレイン酸、及びBHTを添加し、混合物を約24時間ローラーミルで回転させ、均一な分散物を得た。このコーティング溶液を、非常に低速でコーターを使用し、適切なゲージを使用して、放出裏地(Medirelease 2249、シリコーン処理ポリエステルフィルム)にキャストし、約2ミルの乾燥厚みを得た。キャストフィルムを90℃の乾燥オーブンで20分間乾燥し、溶媒を除去した。裏張りフィルム(Scotchpak 1109、アルミニウム層を有する複層ポリマーフィルム)を、放出裏地の上の乾いたキャスト接着剤の露出表面にラミネートした。
浸透試験:浸透実験の方法は、実施例1に記載されたものであった。実施例2の浸透の結果が表2Bに示されており、アワリー単位の時間に対するμg/cm2/hr単位の流動を表している。
実施例3
表3に示されたような湿潤基準で成分を混合することにより薬剤-接着剤溶液を調製し、30.0%w/wのフェロジピン、57.5%w/wのアクリレート接着剤(Gelva Multipolymer Solution 3071、ポリアクリレート、架橋剤なし、反応基なし)、4.0%のリノレン酸(Crossential L98、浸透促進剤)、8.0%のオレイン酸(Super Refined Oleic Acid、浸透助剤)、及び0.5%w/wのBHTの乾燥組成を有する製剤を生産した。製造方法は、実施例2に記載のものと同一であった。
表3に示されたような湿潤基準で成分を混合することにより薬剤-接着剤溶液を調製し、30.0%w/wのフェロジピン、57.5%w/wのアクリレート接着剤(Gelva Multipolymer Solution 3071、ポリアクリレート、架橋剤なし、反応基なし)、4.0%のリノレン酸(Crossential L98、浸透促進剤)、8.0%のオレイン酸(Super Refined Oleic Acid、浸透助剤)、及び0.5%w/wのBHTの乾燥組成を有する製剤を生産した。製造方法は、実施例2に記載のものと同一であった。
浸透試験:浸透実験の方法は、実施例1に記載されたものであった。実施例3の浸透の結果が表2Cに示されており、アワリー単位の時間に対するμg/cm2/hr単位の流動を表している。
実施例4
表4に示されたような湿潤基準で成分を混合することにより薬剤-接着剤溶液を調製し、35.0%w/wのフェロジピン及び65.0%w/wのアクリレート接着剤(Duro-Tak(登録商標)87-7098、ポリアクリレート-酢酸ビニル、架橋剤済み、ヒドロキシル基)の乾燥組成を有する製剤を生産した。フェロジピンをアクリレート接着剤溶液に添加し、混合物を約24時間ローラーミルで回転させ、均一な分散物を得た。このコーティング溶液を、非常に低速でコーターを使用し、適切なゲージを使用して、放出裏地(Medirelease 2249、シリコーン処理ポリエステルフィルム)にキャストし、約2ミルの乾燥厚みを得た。キャストフィルムを65℃の乾燥オーブンで20分間乾燥し、溶媒を除去した。裏張りフィルム(Scotchpak 9733、ポリエステルフィルムラミネート)を、放出裏地の上の乾いたキャスト接着剤の露出表面にラミネートした。
表4に示されたような湿潤基準で成分を混合することにより薬剤-接着剤溶液を調製し、35.0%w/wのフェロジピン及び65.0%w/wのアクリレート接着剤(Duro-Tak(登録商標)87-7098、ポリアクリレート-酢酸ビニル、架橋剤済み、ヒドロキシル基)の乾燥組成を有する製剤を生産した。フェロジピンをアクリレート接着剤溶液に添加し、混合物を約24時間ローラーミルで回転させ、均一な分散物を得た。このコーティング溶液を、非常に低速でコーターを使用し、適切なゲージを使用して、放出裏地(Medirelease 2249、シリコーン処理ポリエステルフィルム)にキャストし、約2ミルの乾燥厚みを得た。キャストフィルムを65℃の乾燥オーブンで20分間乾燥し、溶媒を除去した。裏張りフィルム(Scotchpak 9733、ポリエステルフィルムラミネート)を、放出裏地の上の乾いたキャスト接着剤の露出表面にラミネートした。
フェロジピンの分析
前記製剤を、フェロジピンと分解産物の存在のアッセイのためHPLCにより分析した。時間ゼロの分析は、フェロジピンの分解産物、即ちフェロジピン関連化合物Aの存在を示した。前記製剤を40℃/75%RHで10日間貯蔵し、分解の量に対する効果を評価した。分解産物の量の増加が、40℃/75%RHでの10日間の貯蔵の後に観察された。この結果は表4Aに記載されている
前記製剤を、フェロジピンと分解産物の存在のアッセイのためHPLCにより分析した。時間ゼロの分析は、フェロジピンの分解産物、即ちフェロジピン関連化合物Aの存在を示した。前記製剤を40℃/75%RHで10日間貯蔵し、分解の量に対する効果を評価した。分解産物の量の増加が、40℃/75%RHでの10日間の貯蔵の後に観察された。この結果は表4Aに記載されている
実施例5
表5に示されたような湿潤基準で成分を混合することにより薬剤-接着剤溶液を調製し、30.0%w/wのフェロジピン、63.5%w/wのアクリレート接着剤(Gelva Multipolymer Solution 3071、ポリアクリレート、架橋剤なし、反応基なし)、2.0%のリノレン酸(Crossential L98、浸透促進剤)、4.0%のオレイン酸(Super Refined Oleic Acid、浸透助剤)、及び0.5%w/wのBHTの乾燥組成を有する製剤を生産した。製造方法は、実施例2に記載のものと同一であった。
表5に示されたような湿潤基準で成分を混合することにより薬剤-接着剤溶液を調製し、30.0%w/wのフェロジピン、63.5%w/wのアクリレート接着剤(Gelva Multipolymer Solution 3071、ポリアクリレート、架橋剤なし、反応基なし)、2.0%のリノレン酸(Crossential L98、浸透促進剤)、4.0%のオレイン酸(Super Refined Oleic Acid、浸透助剤)、及び0.5%w/wのBHTの乾燥組成を有する製剤を生産した。製造方法は、実施例2に記載のものと同一であった。
フェロジピンの分析
前記製剤を、フェロジピンと分解産物の存在のアッセイのためHPLCにより分析した。時間ゼロの分析は、フェロジピンの分解産物、即ちフェロジピン関連化合物Aの存在を示した。前記製剤を40℃/75%RHで12週日間貯蔵し、周期的に分析して、分解の量に対する効果を評価した。分解産物は、40℃/75%RHでの12週間の貯蔵の後に観察されなかった。これらのデータは、フェロジピンのフェロジピン関連化合物Aへの分解を防止するのに、BHTが有効であることを示す。
前記製剤を、フェロジピンと分解産物の存在のアッセイのためHPLCにより分析した。時間ゼロの分析は、フェロジピンの分解産物、即ちフェロジピン関連化合物Aの存在を示した。前記製剤を40℃/75%RHで12週日間貯蔵し、周期的に分析して、分解の量に対する効果を評価した。分解産物は、40℃/75%RHでの12週間の貯蔵の後に観察されなかった。これらのデータは、フェロジピンのフェロジピン関連化合物Aへの分解を防止するのに、BHTが有効であることを示す。
実施例6、7、8、及び9
アクリレート接着剤(低Tgを有するMultipolymer Solution、ポリアクリレート、架橋剤なし、反応基なし)について、実施例6から9として35%の薬剤と各種の割合の促進剤を含む4種の製剤を調製した。表6から9に示されたような湿潤基準で成分を混合することにより薬剤-接着剤溶液を調製し、それぞれ表6から9に特定される乾燥製剤を生産した。フェロジピンは低速でプロペラブレードを使用して30分間混合することにより、酢酸エチルに分散した。アクリレート接着剤溶液を添加し、混合物を再び低速で30分間混合した。リノレン酸(Crossential L98、浸透促進剤)、オレイン酸(Super Refined Oleic Acid、浸透助剤)、及びBHT(抗酸化剤)を添加(製剤ごとに必要量で)し、混合物を再び低速で30分間混合した。次いで混合物を約24時間ローラーミルで回転させ、均一な分散物を得た。このコーティング溶液を、非常に低速でコーターを使用し、適切なゲージを使用して、放出裏地(Medirelease 2249、シリコーン処理ポリエステルフィルム)にキャストし、約3ミルの乾燥厚みを得た。キャストフィルムを90℃の乾燥オーブンで20分間乾燥し、溶媒を除去した。裏張りフィルム(Scotchpak 1109、アルミニウム層を有する複層ポリマーフィルム)を、放出裏地の上の乾いたキャスト接着剤の露出表面にラミネートした。
アクリレート接着剤(低Tgを有するMultipolymer Solution、ポリアクリレート、架橋剤なし、反応基なし)について、実施例6から9として35%の薬剤と各種の割合の促進剤を含む4種の製剤を調製した。表6から9に示されたような湿潤基準で成分を混合することにより薬剤-接着剤溶液を調製し、それぞれ表6から9に特定される乾燥製剤を生産した。フェロジピンは低速でプロペラブレードを使用して30分間混合することにより、酢酸エチルに分散した。アクリレート接着剤溶液を添加し、混合物を再び低速で30分間混合した。リノレン酸(Crossential L98、浸透促進剤)、オレイン酸(Super Refined Oleic Acid、浸透助剤)、及びBHT(抗酸化剤)を添加(製剤ごとに必要量で)し、混合物を再び低速で30分間混合した。次いで混合物を約24時間ローラーミルで回転させ、均一な分散物を得た。このコーティング溶液を、非常に低速でコーターを使用し、適切なゲージを使用して、放出裏地(Medirelease 2249、シリコーン処理ポリエステルフィルム)にキャストし、約3ミルの乾燥厚みを得た。キャストフィルムを90℃の乾燥オーブンで20分間乾燥し、溶媒を除去した。裏張りフィルム(Scotchpak 1109、アルミニウム層を有する複層ポリマーフィルム)を、放出裏地の上の乾いたキャスト接着剤の露出表面にラミネートした。
浸透試験:ヒトの死体の皮膚を通じたフェロジピンの流動を、In-Line Auto Sampling Equipmentを使用して測定した。受容溶液として32±0.5℃に維持した40%エタノール水溶液を使用して、実験を7日間稼動させた。0.62-cm2の領域の円形のパッチをラミネートから切断した;放出裏地を取り出し、皮膚を含む乾いた薬剤接着層と皮膚(角質層側)の断面に製剤を載せた。薬剤接着層と受容溶液の間に存在する皮膚層を有する細胞に、パッチと共に皮膚の断片を配置した。規則的な時間間隔で、皮膚の下部の細胞を通じて流動する受容溶液を回収し、HPLCによりフェロジピン含量について分析した。
実施例6から9の浸透の結果が表3A、3B、3C、及び3Dに示されており、アワリー単位の時間に対するμg/cm2/hr単位の流動を表している。
実施例10、11、12、及び13
アクリレート接着剤(高Tgを有するMultipolymer Solution、ポリアクリレート、架橋剤なし、反応基なし)について、実施例10から13として35%の薬剤と各種の割合の促進剤を含む4種の製剤を調製した。表10から13に示されたような湿潤基準で成分を混合することにより薬剤-接着剤溶液を調製し、それぞれ表10から13に特定される乾燥製剤を生産した。製造方法は、実施例6、7、8、及び9に記載されたものに従った。
アクリレート接着剤(高Tgを有するMultipolymer Solution、ポリアクリレート、架橋剤なし、反応基なし)について、実施例10から13として35%の薬剤と各種の割合の促進剤を含む4種の製剤を調製した。表10から13に示されたような湿潤基準で成分を混合することにより薬剤-接着剤溶液を調製し、それぞれ表10から13に特定される乾燥製剤を生産した。製造方法は、実施例6、7、8、及び9に記載されたものに従った。
浸透試験:浸透実験についての方法は、実施例6、7、8、及び9に記載されたものに従った。
実施例10から13の浸透の結果が表4A、4B、4C、及び4Dに示されており、アワリー単位の時間に対するμg/cm2/hr単位の流動を表している。
実施例14、15、16、17、及び18
アクリレート接着剤(中Tgを有するMultipolymer Solution、ポリアクリレート、架橋剤なし、反応基なし)について、実施例14から18として35%の薬剤と各種の割合の促進剤を含む5種の製剤を調製した。表14から18に示されたような湿潤基準で成分を混合することにより薬剤-接着剤溶液を調製し、それぞれ表14から18に特定される乾燥製剤を生産した。製造方法は、実施例6、7、8、及び9に記載されたものに従った。
アクリレート接着剤(中Tgを有するMultipolymer Solution、ポリアクリレート、架橋剤なし、反応基なし)について、実施例14から18として35%の薬剤と各種の割合の促進剤を含む5種の製剤を調製した。表14から18に示されたような湿潤基準で成分を混合することにより薬剤-接着剤溶液を調製し、それぞれ表14から18に特定される乾燥製剤を生産した。製造方法は、実施例6、7、8、及び9に記載されたものに従った。
浸透試験:浸透実験についての方法は、実施例6、7、8、及び9に記載されたものに従った。
実施例14から18の浸透の結果が表5A、5B、5C、5D、及び5Eに示されており、アワリー単位の時間に対するμg/cm2/hr単位の流動を表している。
本発明は、特定の例示的なその実施態様を参考にして記載されているが、本発明の範囲から離れることなく、本発明の記載された実施態様に対して、当業者は各種の変更を施しても良い。ここで使用される用語及び記載は、説明のためのみに示されたものであり、制限的なものとして意味するものではない。特に、本発明は実施例によって記載されてはいるが、各種の組成物及び方法が、ここに記載された発明の概念を実施できるであろう。本発明は各種の用語及び特定の実施態様において記載され開示されているが、本発明の範囲は、それによって制限されることを企図されるものではなく、且つ制限されると考慮されるべきでもない。そのような他の変更または実施態様は、特にここに添付されている特許請求の範囲の幅と範囲内に存在するものであるため、ここでの教示によって示唆されており、特に保存されているものであるはずである。これらの及び他の変形例が、添付の特許請求の範囲及びその均等物に定義されている本発明の範囲内で可能であることは、当業者により認識されているであろう。
Claims (15)
- 裏張り層;及び
ジヒドロピリジンタイプのカルシウムアンタゴニストと脂肪酸浸透促進剤とを含む、裏張り層の一面に固着された接着性マトリックス貯蔵庫
を含む、経皮的デリバリー器具。 - 前記脂肪酸浸透促進剤が、24時間に亘り5%まで凝集物の経皮的デリバーを増大するのに有効である、請求項1に記載の経皮的デリバリー器具。
- 前記脂肪酸浸透促進剤が、24時間に亘り少なくとも20%まで凝集物の経皮的デリバーを増大するのに有効である、請求項2に記載の経皮的デリバリー器具。
- 前記接着性マトリックス貯蔵庫が、溶媒を実質的に含まない、請求項1に記載の経皮的デリバリー器具。
- 前記接着性マトリックス貯蔵庫が、二つ以上の別個の脂肪酸浸透促進剤を含む、請求項1に記載の経皮的デリバリー器具。
- 前記二つの別個の脂肪酸浸透促進剤が、不飽和の度合いが異なる、請求項5に記載の経皮的デリバリー器具。
- 前記ジヒドロピリジンタイプのカルシウムアンタゴニストが、前記接着性マトリックス貯蔵庫の20重量%以上を含む、請求項1に記載の経皮的デリバリー器具。
- 前記ジヒドロピリジンタイプのカルシウムアンタゴニストが、前記接着性マトリックス貯蔵庫の20重量%より多くを含む、請求項1に記載の経皮的デリバリー器具。
- 前記ジヒドロピリジンタイプのカルシウムアンタゴニストが、前記接着性マトリックス貯蔵庫の25重量%以上を含む、請求項1に記載の経皮的デリバリー器具。
- アクリレートポリマーが、前記接着性マトリックス貯蔵庫中のポリマーの50重量%以上を含む、請求項1に記載の経皮的デリバリー器具。
- 前記製剤が更に安定化剤を含み、前記安定化剤がジヒドロピリジンタイプのカルシウムアンタゴニストの分解を防止する、請求項1に記載の経皮的デリバリー器具。
- 前記安定化剤がBHTである、請求項11に記載の経皮的デリバリー器具。
- 前記裏張り層が不透明である、請求項1に記載の経皮的デリバリー器具。
- 前記ジヒドロピリジンタイプのカルシウムアンタゴニストがフェロジピンである、請求項1に記載の経皮的デリバリー器具。
- 前記ジヒドロピリジンタイプのカルシウムアンタゴニストがイスラジピンである、請求項1に記載の経皮的デリバリー器具。
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US53634404P | 2004-01-14 | 2004-01-14 | |
| PCT/US2005/001302 WO2005067897A1 (en) | 2004-01-14 | 2005-01-14 | Transdermal delivery device for dihydropyridine type calcium antagonists containing at least one fatty acid |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2007520480A true JP2007520480A (ja) | 2007-07-26 |
| JP2007520480A5 JP2007520480A5 (ja) | 2011-06-30 |
Family
ID=34794398
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2006549643A Pending JP2007520480A (ja) | 2004-01-14 | 2005-01-14 | 少なくとも一つの脂肪酸を含むジヒドロピリジンタイプのカルシウムアンタゴニスト用の経皮的デリバリー器具 |
Country Status (13)
| Country | Link |
|---|---|
| US (1) | US20050186262A1 (ja) |
| EP (1) | EP1711170B1 (ja) |
| JP (1) | JP2007520480A (ja) |
| KR (1) | KR20060123551A (ja) |
| CN (1) | CN1929827A (ja) |
| AT (1) | ATE437634T1 (ja) |
| AU (1) | AU2005204391A1 (ja) |
| BR (1) | BRPI0506851A (ja) |
| CA (1) | CA2552887A1 (ja) |
| DE (1) | DE602005015679D1 (ja) |
| ES (1) | ES2330653T3 (ja) |
| IL (1) | IL176802A0 (ja) |
| WO (1) | WO2005067897A1 (ja) |
Families Citing this family (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US8080560B2 (en) | 2004-12-17 | 2011-12-20 | 3M Innovative Properties Company | Immune response modifier formulations containing oleic acid and methods |
| US8889154B2 (en) | 2005-09-15 | 2014-11-18 | Medicis Pharmaceutical Corporation | Packaging for 1-(2-methylpropyl)-1H-imidazo[4,5-c] quinolin-4-amine-containing formulation |
| CN102370625A (zh) * | 2010-08-20 | 2012-03-14 | 江苏联环药业股份有限公司 | 非洛地平片 |
| EP2583645A1 (en) * | 2011-10-21 | 2013-04-24 | Josek Berek Apolet | Skin lesion protector |
| CN114569730A (zh) * | 2022-01-25 | 2022-06-03 | 鑫稳生物医药科技(嘉善)有限公司 | 非洛地平促透剂组合、非洛地平经皮给药制剂及经皮递送装置 |
Citations (14)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPH01156919A (ja) * | 1987-06-24 | 1989-06-20 | Fujisawa Pharmaceut Co Ltd | 経皮吸収用製剤 |
| JPH01172322A (ja) * | 1987-12-09 | 1989-07-07 | L'oreal Sa | ピリミジン誘導体及びカルシウム拮抗体の組み合わせ物 |
| JPH03261722A (ja) * | 1990-03-12 | 1991-11-21 | Sekisui Chem Co Ltd | 経皮吸収製剤 |
| JPH07145061A (ja) * | 1993-11-25 | 1995-06-06 | Sekisui Chem Co Ltd | 経皮吸収製剤 |
| EP0680759A1 (en) * | 1994-03-09 | 1995-11-08 | The Board Of Governors For Higher Education State Of Rhode Island And Providence Plantations | Transdermal delivery of calcium channel blockers, such as nifedipine |
| WO1996015793A1 (fr) * | 1994-11-17 | 1996-05-30 | Toray Industries, Inc. | Preparation absorbable par voie percutanee |
| WO1997030987A1 (fr) * | 1996-02-23 | 1997-08-28 | Mercian Corporation | Derives de 1,4-dihydropyridine actifs au plan optique et procede de fabrication |
| JPH11116469A (ja) * | 1997-10-08 | 1999-04-27 | Kyukyu Yakuhin Kogyo Kk | 速溶性フィルム製剤 |
| JP2000136128A (ja) * | 1998-10-29 | 2000-05-16 | Hisamitsu Pharmaceut Co Inc | エストラジオール含有貼付剤 |
| JP2001342130A (ja) * | 2000-06-01 | 2001-12-11 | Teikoku Seiyaku Co Ltd | 4−ビフェニル酢酸含有貼付剤 |
| US20020028234A1 (en) * | 1998-08-03 | 2002-03-07 | Easterling W. Jerry | Noninvasive method for treating hemangiomas through transdermal delivery of calcium channel blocker agents and medicament for use in such method |
| WO2002034206A2 (en) * | 2000-10-23 | 2002-05-02 | Euro-Celtique, S.A. | Felodipine transdermal device and methods |
| JP2002526409A (ja) * | 1998-10-02 | 2002-08-20 | スカンポ・アクチェンゲゼルシャフト | 光障害性網膜変性疾患処置用組成物 |
| JP2004083523A (ja) * | 2002-08-28 | 2004-03-18 | Hisamitsu Pharmaceut Co Inc | 貼付剤 |
Family Cites Families (9)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| DE3315272C2 (de) * | 1983-04-27 | 1986-03-27 | Lohmann Gmbh & Co Kg, 5450 Neuwied | Pharmazeutisches Produkt und Verfahren zu seiner Herstellung |
| GB9022788D0 (en) * | 1990-10-19 | 1990-12-05 | Cortecs Ltd | Pharmaceutical formulations |
| IL104192A (en) * | 1992-02-17 | 1998-01-04 | Siegfried Ag Pharma | Pharmaceutical dosage forms having prolonged release rate of zero order of the active ingredient |
| GR1002079B (en) * | 1994-07-26 | 1995-12-05 | Lavipharm A E | System of a special structure and composition for the rapid transdermal administration of oestrogens. |
| US20020160995A1 (en) * | 1998-08-03 | 2002-10-31 | Easterling W. Jerry | Medication and method for remediating existing scars through transdermal, topical delivery of calcium channel blockers |
| US6772223B1 (en) * | 2000-04-10 | 2004-08-03 | International Business Machines Corporation | Configurable classification interface for networking devices supporting multiple action packet handling rules |
| US20020126672A1 (en) * | 2001-01-10 | 2002-09-12 | Nelson Chow | Method and apparatus for a flexible and reconfigurable packet classifier using content addressable memory |
| US6813690B1 (en) * | 2001-06-12 | 2004-11-02 | Network Appliance, Inc. | Caching media data using content-sensitive identifiers |
| US7126907B2 (en) * | 2001-08-31 | 2006-10-24 | Tropic Networks Inc. | Label switched communication network, a method of conditioning the network and a method of data transmission |
-
2005
- 2005-01-14 US US11/034,857 patent/US20050186262A1/en not_active Abandoned
- 2005-01-14 AT AT05705748T patent/ATE437634T1/de not_active IP Right Cessation
- 2005-01-14 AU AU2005204391A patent/AU2005204391A1/en not_active Abandoned
- 2005-01-14 JP JP2006549643A patent/JP2007520480A/ja active Pending
- 2005-01-14 DE DE602005015679T patent/DE602005015679D1/de active Active
- 2005-01-14 EP EP05705748A patent/EP1711170B1/en not_active Not-in-force
- 2005-01-14 KR KR1020067016343A patent/KR20060123551A/ko not_active Application Discontinuation
- 2005-01-14 ES ES05705748T patent/ES2330653T3/es active Active
- 2005-01-14 BR BRPI0506851-7A patent/BRPI0506851A/pt not_active Application Discontinuation
- 2005-01-14 CN CNA2005800081277A patent/CN1929827A/zh active Pending
- 2005-01-14 WO PCT/US2005/001302 patent/WO2005067897A1/en active Application Filing
- 2005-01-14 CA CA002552887A patent/CA2552887A1/en not_active Abandoned
-
2006
- 2006-07-12 IL IL176802A patent/IL176802A0/en unknown
Patent Citations (14)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPH01156919A (ja) * | 1987-06-24 | 1989-06-20 | Fujisawa Pharmaceut Co Ltd | 経皮吸収用製剤 |
| JPH01172322A (ja) * | 1987-12-09 | 1989-07-07 | L'oreal Sa | ピリミジン誘導体及びカルシウム拮抗体の組み合わせ物 |
| JPH03261722A (ja) * | 1990-03-12 | 1991-11-21 | Sekisui Chem Co Ltd | 経皮吸収製剤 |
| JPH07145061A (ja) * | 1993-11-25 | 1995-06-06 | Sekisui Chem Co Ltd | 経皮吸収製剤 |
| EP0680759A1 (en) * | 1994-03-09 | 1995-11-08 | The Board Of Governors For Higher Education State Of Rhode Island And Providence Plantations | Transdermal delivery of calcium channel blockers, such as nifedipine |
| WO1996015793A1 (fr) * | 1994-11-17 | 1996-05-30 | Toray Industries, Inc. | Preparation absorbable par voie percutanee |
| WO1997030987A1 (fr) * | 1996-02-23 | 1997-08-28 | Mercian Corporation | Derives de 1,4-dihydropyridine actifs au plan optique et procede de fabrication |
| JPH11116469A (ja) * | 1997-10-08 | 1999-04-27 | Kyukyu Yakuhin Kogyo Kk | 速溶性フィルム製剤 |
| US20020028234A1 (en) * | 1998-08-03 | 2002-03-07 | Easterling W. Jerry | Noninvasive method for treating hemangiomas through transdermal delivery of calcium channel blocker agents and medicament for use in such method |
| JP2002526409A (ja) * | 1998-10-02 | 2002-08-20 | スカンポ・アクチェンゲゼルシャフト | 光障害性網膜変性疾患処置用組成物 |
| JP2000136128A (ja) * | 1998-10-29 | 2000-05-16 | Hisamitsu Pharmaceut Co Inc | エストラジオール含有貼付剤 |
| JP2001342130A (ja) * | 2000-06-01 | 2001-12-11 | Teikoku Seiyaku Co Ltd | 4−ビフェニル酢酸含有貼付剤 |
| WO2002034206A2 (en) * | 2000-10-23 | 2002-05-02 | Euro-Celtique, S.A. | Felodipine transdermal device and methods |
| JP2004083523A (ja) * | 2002-08-28 | 2004-03-18 | Hisamitsu Pharmaceut Co Inc | 貼付剤 |
Also Published As
| Publication number | Publication date |
|---|---|
| BRPI0506851A (pt) | 2007-06-12 |
| WO2005067897A1 (en) | 2005-07-28 |
| EP1711170A1 (en) | 2006-10-18 |
| DE602005015679D1 (de) | 2009-09-10 |
| KR20060123551A (ko) | 2006-12-01 |
| ES2330653T3 (es) | 2009-12-14 |
| CA2552887A1 (en) | 2005-07-28 |
| EP1711170B1 (en) | 2009-07-29 |
| CN1929827A (zh) | 2007-03-14 |
| US20050186262A1 (en) | 2005-08-25 |
| AU2005204391A1 (en) | 2005-07-28 |
| IL176802A0 (en) | 2006-10-31 |
| ATE437634T1 (de) | 2009-08-15 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| US8153151B2 (en) | Composition and method for controlling drug delivery from silicone adhesive blends | |
| JP4511691B2 (ja) | 経皮的投与のためのマトリックスパッチ | |
| US7247315B2 (en) | Compositions and medical device for transdermal delivery of a drug and methods of making and using same | |
| JP6336476B2 (ja) | ホルモン及びその他の薬剤を経皮送達するための組成物及び方法 | |
| JPH041127A (ja) | 医療用貼付剤 | |
| JP2005023088A (ja) | 室温で液体である低分子量薬を含む経皮組成物 | |
| CA2896336C (en) | Compositions and methods for transdermal delivery of non-steroidal anti-inflammatory agents | |
| AU2002329763A1 (en) | Composition and transdermal drug delivery device | |
| US20180256562A1 (en) | Transdermal Delivery System | |
| KR102307852B1 (ko) | 약물의 경피 흡수 촉진용 조성물 및 패치 제제 | |
| US8940326B2 (en) | Transdermal patch and method for delivery of vitamin B12 | |
| FI118885B (fi) | Skopolamiinilaastari | |
| JP2007520480A (ja) | 少なくとも一つの脂肪酸を含むジヒドロピリジンタイプのカルシウムアンタゴニスト用の経皮的デリバリー器具 | |
| WO2020092990A1 (en) | Pharmaceutical compositions and methods of making a patch formulation for transdermal delivery | |
| MX2007011681A (es) | Parche transdermico. | |
| JP2007520480A5 (ja) | ||
| KR101353478B1 (ko) | 펜타닐을 함유하는 경피투여용 패취 제제 | |
| WO2005046653A1 (en) | Antiphlogistic and analgesic plaster comprising felbinac compound | |
| KR102537845B1 (ko) | 그라니세트론을 함유하는 경피흡수제제 | |
| KR20050077426A (ko) | 비스테로이드성 소염진통제 함유 플라스터 | |
| JPH06279288A (ja) | パップ剤 | |
| KR20220158748A (ko) | 첩부제 | |
| CN116056689A (zh) | 艾司氯胺酮-混悬剂-tts | |
| JP2019034905A (ja) | デヒドロ酢酸含有経皮吸収製剤 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20071012 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20110215 |
|
| A524 | Written submission of copy of amendment under article 19 pct |
Free format text: JAPANESE INTERMEDIATE CODE: A524 Effective date: 20110512 |
|
| A02 | Decision of refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A02 Effective date: 20120221 |