JP2007238564A - カロチノイド−コラーゲンペプチド縮合体 - Google Patents
カロチノイド−コラーゲンペプチド縮合体 Download PDFInfo
- Publication number
- JP2007238564A JP2007238564A JP2006066564A JP2006066564A JP2007238564A JP 2007238564 A JP2007238564 A JP 2007238564A JP 2006066564 A JP2006066564 A JP 2006066564A JP 2006066564 A JP2006066564 A JP 2006066564A JP 2007238564 A JP2007238564 A JP 2007238564A
- Authority
- JP
- Japan
- Prior art keywords
- general formula
- carotenoid
- formula
- collagen peptide
- group
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
- 0 **C(CCC(N*)=O)=O Chemical compound **C(CCC(N*)=O)=O 0.000 description 2
Landscapes
- Peptides Or Proteins (AREA)
- Cosmetics (AREA)
- Indole Compounds (AREA)
- Organic Low-Molecular-Weight Compounds And Preparation Thereof (AREA)
Abstract
Description
本発明は外用に適した組成物に関し、更に詳細には、カロチノイド-コラーゲンペプチド縮合体を有効成分として含有する化粧品、外用医薬品等外用に適する組成物に関する。
従来より、乳液、クリーム、化粧水、パック、分散液、洗浄料等の化粧品や、軟膏剤、クリーム剤、外用液剤等の外用医薬品には、これらに所定の薬効を付与することを目的として薬効成分が加えられている。カロチノイドは細胞賦活性や抗酸化性に優れ、これらに広く用いられている。
しかしながら、カロチノイドを配合した化粧品、外用医薬品等の外用に適する組成物(以下、「外用剤」ということがある)では、カロチノイドが製剤中で変質するなどして所期の薬効が得られない場合が多く、また、カロチノイドは親水性に欠けるため製剤の安定性に問題があり、その改善が望まれていた。
本発明者らは、外用剤に配合されるカロチノイドの効果を向上させるべく鋭意検討を行った結果、カロチノイド−コラーゲンペプチド縮合体が、カロチノイドが本来有する作用を維持しつつ、かつ、高い安定性を有することを見出し、本発明を完成した。
すなわち、本発明は、下記一般式(1)で表されるカロチノイド−コラーゲンペプチド縮合体を提供するものである。
一般式(1)
一般式(1)
式中、Calはカロチノイド残基を表し、Colはコラーゲンペプチド鎖を表す。
本発明によれば、皮膚外用剤などに有用な安定性、特に空気酸化と光照射への安定性に優れたカロチノイド誘導体を提供できる。さらには、該カロチノイド誘導体により、皮膚への安全性に優れ、抗酸化性能に優れ、且つ、製剤注で安定な皮膚用外用剤を提供できる。
本発明において有用なカロチノイドは、水酸基を有するカロチノイドであり、複数の水酸基を有する場合、その水酸基は置換されていなくても、置換されていてもよい。このようなカロチノイドとしては、アスタキサンチン、カプサンチン、フコキサンチン、ヘテロキサンチン、ロロキサンチン、ルテオキサンチン、リコフィル、リコキサンチン、ネオクロム、ネオキサンチン、ロドピン、ロドピナール、ロドピノール、ロドビブリン、トロリキサンチン、キサントフィル、ゼアキサンチンが挙げられる。
本発明においてはアスタキサンチン類が特に好ましい。本発明に用いられるアスタキサンチン類は、既に酸化防止効果、抗炎症効果(特開平2−49091号)、皮膚老化防止効果(特開平5−155736号)、美白効果(日本香粧品科学会第19回学術大会講演
要旨集、p.66,1994年)を有することが知られたものである。
要旨集、p.66,1994年)を有することが知られたものである。
このアスタキサンチン類は、化学合成品でも、オキアミ、サケ、マス、福寿草、赤色酵母等の天然物から抽出されたものでもよく、それらの天然抽出物から種々の方法で精製されたものでもよい。
すなわち、ヘマトコッカス藻に抽出溶媒を加え抽出し、この抽出液を濾別して得られるアスタキサンチン類抽出エキスや、この抽出エキスから更に抽出溶媒を留去し、必要に応じて水素添加や加水分解等の化学反応を行った後、分子蒸留、あるいはカラムクロマトグラフィーや高速液体クロマトグラフィー(HPLC)等の手段を用いて脱臭、精製を行った精製アスタキサンチン類を用いることができる。
上記抽出溶媒としては、アセトン、エーテル、クロロホルム及びアルコール(エタノール、メタノール等)等の有機溶媒を用いることができ、また、これらの混合溶液を用いることもできる。あるいは、超臨界状態の二酸化炭素を用いてもよい。
本明細書において、「アスタキサンチン類」とは、アスタキサンチンおよびその誘導体の両者を包含するものである。
アスタキサンチンは、下記一般式(8)で示されるカロチノイドである。
一般式(8)
一般式(8)
式中、R1は、水素原子、アシル基、燐酸エステル基またはグルコシド基を表す。該アシル基、燐酸エステル基およびグルコシド基は、置換基を有していてもよい。
以下、一般式(8)においてエステル基を有する場合、本明細書において、アスタキサンチンエステルと言う。アスタキサンチンエステルとしては、例えば、グリシン、アラニン等のアミノ酸エステル類、酢酸エステル、クエン酸エステル等のカルボン酸エステル及びその塩類、リン酸エステル、グルコシド等の配糖体類、またはエイコサペンタエン酸やドコサヘキサエン酸等の高度不飽和脂肪酸、オレイン酸やリノール酸等の不飽和脂肪酸またはパルミチン酸やステアリン酸等の飽和脂肪酸から選択される脂肪酸エステル類等から選択されるモノエステル体及び同種または異種のジエステル体等が挙げられる。これらの誘導体のうち、脂肪酸酸エステル類が望ましく、オレイン酸やパルミチン酸のような炭素数12以上の不飽和脂肪酸エステルが特に望ましい。
本発明において有用なコラーゲンペプチドは、特に限定されず何れのものも使用することができる。コラーゲン自体でも人工的に変性させたものでもよく、天然由来抽出コラーゲンでも、また、それに化学処理や酵素処理をして得られたコラーゲンペプチドであってもよく、遺伝子組み換えコラーゲンでもよい。
分子量は600から50万が好ましく、1000から15万がさらに好ましい。
天然由来の多重鎖コラーゲンペプチドでも、それが解けた単鎖コラーゲンペプチドでもよい。一般にゼラチンと呼ばれるコラーゲン由来ペプチドを利用してもよい。天然コラーゲンの原料として、魚類、牛やブタなどの哺乳類、鯛などの魚類、クロレラなどの藻類などが知られているが、特に限定されることは無い。これらコラーゲンペプチドについては、コラーゲン実験法(永井裕、藤本大三郎/編、講談社)及びコラーゲン(藤本大三郎/著、共立出版)を参照出来る。
分子量は600から50万が好ましく、1000から15万がさらに好ましい。
天然由来の多重鎖コラーゲンペプチドでも、それが解けた単鎖コラーゲンペプチドでもよい。一般にゼラチンと呼ばれるコラーゲン由来ペプチドを利用してもよい。天然コラーゲンの原料として、魚類、牛やブタなどの哺乳類、鯛などの魚類、クロレラなどの藻類などが知られているが、特に限定されることは無い。これらコラーゲンペプチドについては、コラーゲン実験法(永井裕、藤本大三郎/編、講談社)及びコラーゲン(藤本大三郎/著、共立出版)を参照出来る。
本発明のカロチノイド−コラーゲンペプチド縮合体は、下記一般式(1)で表されるも
のである。
一般式(1)
のである。
一般式(1)
式中、Calはカロチノイド残基を表し、Colはコラーゲンペプチド鎖を表す。
前記一般式(1)で表されるカロチノイド−コラーゲンペプチド縮合体としては、下記一般式(2)で表されるアスタキサンチン−コラーゲンペプチド縮合体が好ましい。
一般式(2)
一般式(2)
式中、R1は、水素原子、アシル基、燐酸エステル基またはグルコシド基を表し、Colはコラーゲンペプチド鎖を表す。
尚、カロチノイド残基とは、本発明において有用な、水酸基を有するカロチノイドにおいて、縮合反応に用いられる水酸基を除いた基を言う。
前記一般式(1)で表されるカロチノイド−コラーゲンペプチド縮合体は、下記合成ルートによって製造することができる。下記合成ルートにおいて、Calはカロチノイド残基を表し、Colはコラーゲンペプチド鎖を表す。
まず、水酸基を有するカロチノイド(7)と、無水コハク酸とを縮合してカロチノイドエステルカルボン酸化合物(3)とする。この化合物(3)とN−ヒドロキシフタルイミドとを縮合させてカロチノイドエステル−フタルイミド化合物(4)を得る。さらにこの化合物(4)とコラーゲンペプチドとを反応させてカロチノイド−コラーゲンペプチド縮合体(1)を得ることができる。
本発明の製造方法に関し、さらに詳細に説明する。
カロチノイド(7)と無水コハク酸との縮合では、両者を有機溶剤中で縮合させる。その際、塩基を用いても用いなくてもよいが、塩基を用いることが好ましい。この塩基としては有機塩基でも無機塩基でもよい。有機塩基としては、ピリジン、メチルピリジン、ジメチルピリジン、トリメチルピリジンなどのピリジン類やイミダゾールなどのアゾール類、トリエチルアミンやトリブチルアミンのようなトリアルキルアミン類が好ましく、無機塩基としては、炭酸ナトリウムや炭酸水素ナトリウム、炭酸カリウムなどの炭酸塩が好ましい。
カロチノイド(7)と無水コハク酸との縮合では、両者を有機溶剤中で縮合させる。その際、塩基を用いても用いなくてもよいが、塩基を用いることが好ましい。この塩基としては有機塩基でも無機塩基でもよい。有機塩基としては、ピリジン、メチルピリジン、ジメチルピリジン、トリメチルピリジンなどのピリジン類やイミダゾールなどのアゾール類、トリエチルアミンやトリブチルアミンのようなトリアルキルアミン類が好ましく、無機塩基としては、炭酸ナトリウムや炭酸水素ナトリウム、炭酸カリウムなどの炭酸塩が好ましい。
カロチノイド(7)と無水コハク酸との縮合に用いられる有機溶媒としては、ジメチルスルホキシド(DMSO)やアルコール類などの無水コハク酸と反応する溶媒を除けば特に限定は無いが、塩化メチレンなどの有機塩素溶媒、酢酸エステル、アセトニトリル、エーテル、テトラヒドロフラン(THF)、ジメチルホルムアミド(DMF)、ジメチルアセトアミド(DMAc)、N−メチルピロリドン、N,N−ジメチルイミダゾリジノンが好ましい。
カロチノイド(7)と無水コハク酸との縮合における反応温度は20℃から70℃が好ましく、20℃から50℃がさらに好ましい。
カロチノイド(7)と無水コハク酸のモル比は1倍から5倍が好ましく、1倍から2倍が好ましく、1.05倍から1.2倍が特に好ましい。
カロチノイドエステルカルボン酸化合物(3)とN−ヒドロキシフタルイミドとの縮合においては、カルボン酸とN−ヒドロキシフタルイミドの縮合法として既知の方法を用いることができる。すなわち、カルボジイミドなどの脱水縮合剤を用いる方法や、カルボン酸を塩化チオニルやオキシ塩化リンなどの塩素化剤を用いていったん三塩化物に変えた後、塩基存在下、N−ヒドロキシフタルイミドと反応させる方法等を用いることができる。それらの中では、カルボジイミドを用いる方法が特に好ましい。
カロチノイドエステルカルボン酸化合物(3)とN−ヒドロキシフタルイミドとの縮合に用いられる溶媒は、カルボジイミドを用いる場合は、エーテル、THF、アセトニトリル、酢酸エチル、DMF、DMAc、N−メチルピロリドン、N,N−ジメチルイミダゾリジノンが好ましい。
カロチノイドエステルカルボン酸化合物(3)とN−ヒドロキシフタルイミドとの縮合における反応温度は、カルボジイミドを用いる場合は、20℃から70℃が好ましく、20℃から50℃がさらに好ましい。
カロチノイドエステルカルボン酸化合物(3)とN−ヒドロキシフタルイミドのモル比は1倍から5倍が好ましく、1倍から2倍が好ましく、1.05倍から1.2倍が特に好ましい。
カロチノイドエステルカルボン酸化合物(3)とN−ヒドロキシフタルイミドとの縮合に用いられるカルボジイミドは、ジシクロヘキシルカルボジイミド(DCC)が特に好ましく、その量は、モル比で、カロチノイドエステルカルボン酸化合物(3)に対して、1倍から2倍が好ましく、1.05倍から1.2倍が特に好ましい。
カロチノイドエステル−フタルイミド化合物(4)とコラーゲンペプチドとの縮合では、カロチノイドエステル−フタルイミド化合物(4)を非水溶性の溶剤に、コラーゲンペプチドを水に溶解し、二層系で反応させる方法や、カロチノイドエステル−フタルイミド化合物(4)をDMFなどの水溶性の溶剤に溶解し、コラーゲンペプチドの水溶液と混合して単層系で反応させる方法のいずれも用いることができるが、単層系の反応が好ましい。このとき用いられる溶剤はDMF、DMAc、N−メチルピロリドン、N,N−ジメチルイミダゾリジノンが特に好ましい。
カロチノイドエステル−フタルイミド化合物(4)とコラーゲンペプチドとの縮合における温度は、単層系の場合、25℃から95℃が好ましく、30℃から70℃がさらに好ましく、40℃から60℃がもっとも好ましい。
カロチノイドエステル−フタルイミド化合物(4)とコラーゲンペプチドの比はコラーゲンペプチド中のリジン比に依存する。カロチノイドエステル−フタルイミド化合物(4)はコラーゲンペプチド中のリジン残基に対し、0.1から5当量が好ましく、0.2から3当量がさらに好ましく、0.2から2当量が特に好ましい。
前記一般式(2)で表されるアスタキサンチン−コラーゲンペプチド縮合体は、下記合成ルートによって製造することができる。下記合成ルートにおいて、R1は、水素原子、アシル基、燐酸エステル基またはグルコシド基を表し、Colはコラーゲンペプチド鎖を表す。
まず、水酸基を有するアスタキサンチン(8)と、無水コハク酸とを縮合してアスタキサンチンエステルカルボン酸化合物(5)とする。この化合物(5)とN−ヒドロキシフタルイミドとを縮合させてカロチノイドエステル−フタルイミド化合物(6)を得る。さらにこの化合物(6)とコラーゲンペプチドとを反応させてカロチノイド−コラーゲンペプチド縮合体(2)を得ることができる。
カロチノイド−コラーゲンペプチド縮合体(2)の製造方法の詳細は、前記カロチノイド−コラーゲンペプチド縮合体(1)の製造方法と同様であり、各縮合反応における好ましい縮合法、有機溶媒、反応温度、等も同様である。
次に実施例を挙げて本発明を更に詳細に説明するが、本発明はこれらになんら制限されるものではない。
参考例1:アスタキサンチンの精製
(1)前吸着
ヘマトコッカス抽出物(武田紙器製 79g)を酢酸エチル800mLに溶解させ、シリカゲル(和光純薬 C-200 165g)を添加し減圧濃縮した。濃縮後は窒素でブローした。
(1)前吸着
ヘマトコッカス抽出物(武田紙器製 79g)を酢酸エチル800mLに溶解させ、シリカゲル(和光純薬 C-200 165g)を添加し減圧濃縮した。濃縮後は窒素でブローした。
(2)カラム充填
シリカゲル(和光純薬 C-200 2342g 3900mL)をヘキサン/酢酸エチル9:1で懸濁し、太さ16cm 長さ60cmのカラムに充填した。
シリカゲル(和光純薬 C-200 2342g 3900mL)をヘキサン/酢酸エチル9:1で懸濁し、太さ16cm 長さ60cmのカラムに充填した。
(3)展開
カラムの上部に展開溶媒を張り、前吸着させたシリカゲルを添加した。ヘキサン/酢酸エチル=9:1の溶離液を12L流した。ついで、ヘキサン/酢酸エチル=5:1の溶離液を6L流した。さらにヘキサン/酢酸エチル=5:1の溶離液を7L流した。
展開液をTLCで分析し、モノエステル分画部を減圧溜去しモノエステル体14gを得た。このモノエステル体はカルボン酸部が炭素数18の不飽和脂肪酸の混合物(R1=C17H29-33CO)であった。
カラムの上部に展開溶媒を張り、前吸着させたシリカゲルを添加した。ヘキサン/酢酸エチル=9:1の溶離液を12L流した。ついで、ヘキサン/酢酸エチル=5:1の溶離液を6L流した。さらにヘキサン/酢酸エチル=5:1の溶離液を7L流した。
展開液をTLCで分析し、モノエステル分画部を減圧溜去しモノエステル体14gを得た。このモノエステル体はカルボン酸部が炭素数18の不飽和脂肪酸の混合物(R1=C17H29-33CO)であった。
実施例1:アスタキサンチンエステルカルボン酸化合物(5A : R1=C17H31CO)の合成
アスタキサンチンモノエステル(8A : R1=C17H31CO)3.0g(3.5mmol)と無水コハク酸0.41g(4.1mmol)を塩化メチレン20mlに溶解しトリエチルアミン0.42g(4.1mmol)を添加し室温で16時間反応させた。反応液に1モル/L HCl 10mlを添加し分液しさらに水で有機層を洗浄した。有機層を硫酸ナトリウムで乾燥した後で濃縮し、3.1g(収率 93%)でアスタキサンチンエステルカルボン酸化合物(5A)を得た。
(1HNMR(CDCl3 6.1-6.7(14H,m), 5.5-5.6(2H,m), 5.3-5.4(4H,m),1.99(12H,s), 1.90(6H,s), 1.33(6H,s), 1.23(6H,s). MS m/z =990.7(R1=C17H33), 988.7(R1=C17H31) . mp 72℃分解
アスタキサンチンモノエステル(8A : R1=C17H31CO)3.0g(3.5mmol)と無水コハク酸0.41g(4.1mmol)を塩化メチレン20mlに溶解しトリエチルアミン0.42g(4.1mmol)を添加し室温で16時間反応させた。反応液に1モル/L HCl 10mlを添加し分液しさらに水で有機層を洗浄した。有機層を硫酸ナトリウムで乾燥した後で濃縮し、3.1g(収率 93%)でアスタキサンチンエステルカルボン酸化合物(5A)を得た。
(1HNMR(CDCl3 6.1-6.7(14H,m), 5.5-5.6(2H,m), 5.3-5.4(4H,m),1.99(12H,s), 1.90(6H,s), 1.33(6H,s), 1.23(6H,s). MS m/z =990.7(R1=C17H33), 988.7(R1=C17H31) . mp 72℃分解
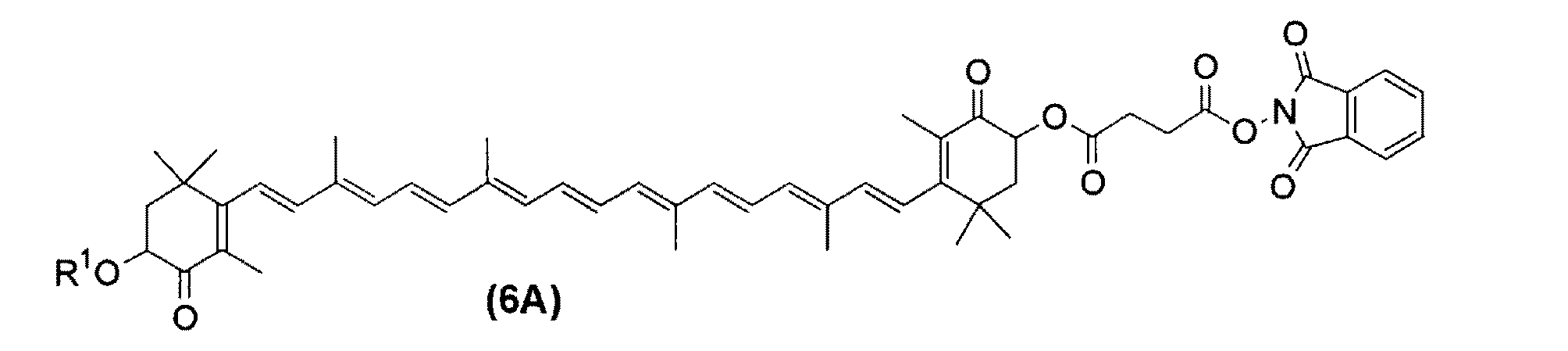
実施例2:アスタキサンチンエステル−フタルイミド化合物(6A : R1=C17H31CO)の合成
アスタキサンチンエステルカルボン酸化合物(5A)2.8g(2.9mmol)とN−ヒドロキシフタルイミド0.57g(3.5mmol)をTHF 20mlに溶解し、DCC 0.72g(3.5mmol)
を添加し室温で16時間反応させた。析出したジシクロヘキシル尿素(DCU)を濾別し、DCUをTHFで洗浄した。有機層を濃縮し、アスタキサンチンエステル−フタルイミド化合物(6A : R1=C17H31CO)濃縮物3.1gを得た。
(1HNMR(CDCl3 6.1-6.7(14H,m), 5.5-5.6(2H,m), 5.3-5.4(4H,m),2.02(12H,s), 1.90(6H,s), 1.32(6H,s), 1.22(6H,s). MS m/z =1015.6(R1=C17H33), 1013.6(R1=C17H31) . mp 46℃ 分解
得られた濃縮物はこのまま次の反応に用いた。
アスタキサンチンエステルカルボン酸化合物(5A)2.8g(2.9mmol)とN−ヒドロキシフタルイミド0.57g(3.5mmol)をTHF 20mlに溶解し、DCC 0.72g(3.5mmol)
を添加し室温で16時間反応させた。析出したジシクロヘキシル尿素(DCU)を濾別し、DCUをTHFで洗浄した。有機層を濃縮し、アスタキサンチンエステル−フタルイミド化合物(6A : R1=C17H31CO)濃縮物3.1gを得た。
(1HNMR(CDCl3 6.1-6.7(14H,m), 5.5-5.6(2H,m), 5.3-5.4(4H,m),2.02(12H,s), 1.90(6H,s), 1.32(6H,s), 1.22(6H,s). MS m/z =1015.6(R1=C17H33), 1013.6(R1=C17H31) . mp 46℃ 分解
得られた濃縮物はこのまま次の反応に用いた。
実施例3:アスタキサンチン-コラーゲンペプチド縮合体(2A : R1=C17H31CO)の合成
実施例3で得られたアスタキサンチンエステル−フタルイミド化合物(6A)濃縮物3.1gをDMAc 20gで溶解した。コラーゲンペプチド(ニッピ製 FCP-A 平均分子量:1万、Lys比率2.6%)15gをDMAcと水に50℃で溶解させた。このコラーゲンペプチド溶液に、窒素気流下で上記アスタキサンチンエステル−フタルイミド化合物(6A)のDMAc溶液を添加し、60℃で5時間反応させた。さらに室温で16時間反応させた。反応液をアセトニトリルに添加し窒素気流下で室温で終夜撹拌した。析出したアスタキサンチン-コラーゲンペプチド縮合体(2A : R1=C17H31CO)を濾取し、30℃で減圧乾燥した。収量9.8g。スペクトル分析から、アスタキサンチン部の重量比は25%であった。1HNMR CDCl3 6.1-6.7の積分を14Hとして、計算値から求めた。
実施例3で得られたアスタキサンチンエステル−フタルイミド化合物(6A)濃縮物3.1gをDMAc 20gで溶解した。コラーゲンペプチド(ニッピ製 FCP-A 平均分子量:1万、Lys比率2.6%)15gをDMAcと水に50℃で溶解させた。このコラーゲンペプチド溶液に、窒素気流下で上記アスタキサンチンエステル−フタルイミド化合物(6A)のDMAc溶液を添加し、60℃で5時間反応させた。さらに室温で16時間反応させた。反応液をアセトニトリルに添加し窒素気流下で室温で終夜撹拌した。析出したアスタキサンチン-コラーゲンペプチド縮合体(2A : R1=C17H31CO)を濾取し、30℃で減圧乾燥した。収量9.8g。スペクトル分析から、アスタキサンチン部の重量比は25%であった。1HNMR CDCl3 6.1-6.7の積分を14Hとして、計算値から求めた。
実施例4:アスタキサンチン−コラーゲンペプチド縮合体(2A)の固体分散液
前記で得られたアスタキサンチン−コラーゲンペプチド縮合体(2A)を下記(1)の方法により分散固体とした。
(1) 蒸留水21.4gおよびリン脂質コポリマー界面活性剤(日本油脂 Lipidure-PMB)の溶液2.65gとを60mlネジブタ瓶に入れた。アスタキサンチン−コラーゲンペプチド縮合体(2A)1.0gをこの溶液に添加した。酸化ジルコニウム(ZrO)のビーズ40ml(2mm径)を添加し、ふたをしっかりしめたのちミルに置き回転数4800r.p.m.にて粒子サイズ1μm以下の化合物の微粉体分散物を得た。
前記で得られたアスタキサンチン−コラーゲンペプチド縮合体(2A)を下記(1)の方法により分散固体とした。
(1) 蒸留水21.4gおよびリン脂質コポリマー界面活性剤(日本油脂 Lipidure-PMB)の溶液2.65gとを60mlネジブタ瓶に入れた。アスタキサンチン−コラーゲンペプチド縮合体(2A)1.0gをこの溶液に添加した。酸化ジルコニウム(ZrO)のビーズ40ml(2mm径)を添加し、ふたをしっかりしめたのちミルに置き回転数4800r.p.m.にて粒子サイズ1μm以下の化合物の微粉体分散物を得た。
試料液の調整
上記のようにして調製した微粉体分散物を、表1に示す重量濃度になるように蒸留水で希釈して試料液を調製した。
上記のようにして調製した微粉体分散物を、表1に示す重量濃度になるように蒸留水で希釈して試料液を調製した。
比較例1
蒸留水21.3gおよびリン脂質コポリマー界面活性剤(日本油脂 Lipidure-PMB)の溶液2.65gとを60mlネジブタ瓶に入れた。前記参考例によって精製したアスタキサンチンモノエステル0.10gとTHF 1mlの溶液をこの溶液に添加した。酸化ジルコニウム(ZrO)のビーズ40ml(2mm径)を添加し、ふたをしっかりしめたのちミルに置き回転数4800r.p.m.にて分散液を得た。
蒸留水21.3gおよびリン脂質コポリマー界面活性剤(日本油脂 Lipidure-PMB)の溶液2.65gとを60mlネジブタ瓶に入れた。前記参考例によって精製したアスタキサンチンモノエステル0.10gとTHF 1mlの溶液をこの溶液に添加した。酸化ジルコニウム(ZrO)のビーズ40ml(2mm径)を添加し、ふたをしっかりしめたのちミルに置き回転数4800r.p.m.にて分散液を得た。
試料液の調整
上記のようにして調製した分散液を、表1に示す重量濃度になるように蒸留水で希釈して比較試料液とした。
上記のようにして調製した分散液を、表1に示す重量濃度になるように蒸留水で希釈して比較試料液とした。
〔分散物の評価〕
{空気酸化に対する安定性}
評価用の試料は、50mlのナス型フラスコに試料15ml入れて25℃、空気雰囲気下攪拌して試験を行った。評価は、窒素雰囲気下の470nmの吸収(アスタキサンチンの吸収極大)を100として空気雰囲気下の残存率を算出した。結果を表1に示す。
{空気酸化に対する安定性}
評価用の試料は、50mlのナス型フラスコに試料15ml入れて25℃、空気雰囲気下攪拌して試験を行った。評価は、窒素雰囲気下の470nmの吸収(アスタキサンチンの吸収極大)を100として空気雰囲気下の残存率を算出した。結果を表1に示す。
{光照射に対する安定性}
メリーゴーランド型キセノン退色試験機を用いて、光照射実験を行った。キセノン光原は、500Wのランプを使用した。評価用の試料は、4面透明な蓋付の10mm石英セルに試料3ml入れて25℃、無攪拌で試験を行った。評価は、光照射なしの470nmの吸収(アスタキサンチンの吸収極大)を100として光照射後の残存率を算出した。結果を表1に示す。
メリーゴーランド型キセノン退色試験機を用いて、光照射実験を行った。キセノン光原は、500Wのランプを使用した。評価用の試料は、4面透明な蓋付の10mm石英セルに試料3ml入れて25℃、無攪拌で試験を行った。評価は、光照射なしの470nmの吸収(アスタキサンチンの吸収極大)を100として光照射後の残存率を算出した。結果を表1に示す。
表1に示したように、本発明のアスタキサンチン−コラーゲンペプチド縮合体は、比較例のアスタキサンチンより高い安定性を示した。
実施例5:抗酸化活性[スーパーオキサイド除去活性]
実施例4で得られた試料を下記測定方法によりスーパーオキサイド除去活性を測定した。すなわち、0.05M炭酸ナトリウム緩衝液(pH10.2)2.4mlに基質溶液[3.0mM キサンチン(0.05M炭酸ナトリウム緩衝液に溶解)]0.1ml、3.0mM EDTA 0.1ml、0.15%(W/V)ウシ血清アルブミン0.1ml、0.75mM ニトロブル−テトラゾリウム 0.1ml及び各被験試料0.1mlを混合し、25℃で10分間放置した。次いで、酵素溶液[キサンチンオキシダーゼ溶液(精製水にて約0.04units/ml希釈)]0.1mlを加えて反応を開始し、25℃で20分間インキュベートした後、6mM CaCl2 0.1mlを加えて反応を停止した。次いで560nmにおける吸光度(A)を測定した。
実施例4で得られた試料を下記測定方法によりスーパーオキサイド除去活性を測定した。すなわち、0.05M炭酸ナトリウム緩衝液(pH10.2)2.4mlに基質溶液[3.0mM キサンチン(0.05M炭酸ナトリウム緩衝液に溶解)]0.1ml、3.0mM EDTA 0.1ml、0.15%(W/V)ウシ血清アルブミン0.1ml、0.75mM ニトロブル−テトラゾリウム 0.1ml及び各被験試料0.1mlを混合し、25℃で10分間放置した。次いで、酵素溶液[キサンチンオキシダーゼ溶液(精製水にて約0.04units/ml希釈)]0.1mlを加えて反応を開始し、25℃で20分間インキュベートした後、6mM CaCl2 0.1mlを加えて反応を停止した。次いで560nmにおける吸光度(A)を測定した。
対照には被験試料のかわりに蒸留水を加えた試料の吸光度(B)、また各試料のブランクには、6mM CaCl2 0.1mlを加えて反応停止後に、キサンチンオキシダーゼ0.1mlを添加した試料の吸光度(C)を測定し、次式より、スーパーオキサイド除去率を算出した。その結果を表2に示す。
除去率=((B−(A−C))/B)×100
A:試料の酵素反応による吸光度
B:対照の酵素反応による吸光度
C:試料の無酵素反応による吸光度
A:試料の酵素反応による吸光度
B:対照の酵素反応による吸光度
C:試料の無酵素反応による吸光度
表2に示したように本発明のアスタキサンチン-コラーゲンペプチド縮合体はアスタキサンチンモノエステルと同等以上の抗酸化活性を示した。さらに、抗酸化性が知られているビタミンC、ビタミンEとの併用により、特に低濃度領域で抗酸化性が強くなることが示された。
このことは、本発明のアスタキサンチン−コラーゲンペプチド縮合体は活性酸素除去剤を併用することにより、皮膚中での活性酸素生成に起因する過酸化脂質の生成、炎症、黒化、老化に対し、極めて高い予防効果を有することを示すものと言える。
実施例6:アスタキサンチンステアリン酸エステル(R1=C17H35)
アスタキサンチン(和光純薬、生化学用)0.60g(1.0mmol)とステアリン酸塩化物(アルドリッチ)0.33g(1.1mmol)をアセトニトリル10mlに溶解し、4℃で、トリエチルアミ
ン1mlを加えた。その後、22℃に温度を上げ、その温度で、4時間攪拌した。反応液を40mlの水に投じ、20mlの酢酸エチルで3回抽出した。酢酸エチル抽出液を1規定塩酸液で洗浄し、飽和重曹水と飽和食塩水で洗浄した。酢酸エチル溶液を無水硫酸ナトリウムで乾燥後、溶媒溜去し、シリカゲル(和光純薬 C-200) 40gを用い、ヘキサン/酢酸エチルで溶出させ精製した。収量0.32g(融点79-83℃)。
実施例1〜5と同様にして、固体分散液を得た後、同様の評価を行ったところ、同様の結果が得られた。
アスタキサンチン(和光純薬、生化学用)0.60g(1.0mmol)とステアリン酸塩化物(アルドリッチ)0.33g(1.1mmol)をアセトニトリル10mlに溶解し、4℃で、トリエチルアミ
ン1mlを加えた。その後、22℃に温度を上げ、その温度で、4時間攪拌した。反応液を40mlの水に投じ、20mlの酢酸エチルで3回抽出した。酢酸エチル抽出液を1規定塩酸液で洗浄し、飽和重曹水と飽和食塩水で洗浄した。酢酸エチル溶液を無水硫酸ナトリウムで乾燥後、溶媒溜去し、シリカゲル(和光純薬 C-200) 40gを用い、ヘキサン/酢酸エチルで溶出させ精製した。収量0.32g(融点79-83℃)。
実施例1〜5と同様にして、固体分散液を得た後、同様の評価を行ったところ、同様の結果が得られた。
実施例7:アスタキサンチン酢酸エステル
実施例6のステアリン酸塩化物を酢酸塩化物に変えた以外は同様にして酢酸エステル(R1=CH3、融点141℃分解)を合成した。
実施例1〜5と同様にして、固体分散液を得た後、同様の評価を行ったところ、同様の結果が得られた。
実施例6のステアリン酸塩化物を酢酸塩化物に変えた以外は同様にして酢酸エステル(R1=CH3、融点141℃分解)を合成した。
実施例1〜5と同様にして、固体分散液を得た後、同様の評価を行ったところ、同様の結果が得られた。
Claims (12)
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2006066564A JP2007238564A (ja) | 2006-03-10 | 2006-03-10 | カロチノイド−コラーゲンペプチド縮合体 |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2006066564A JP2007238564A (ja) | 2006-03-10 | 2006-03-10 | カロチノイド−コラーゲンペプチド縮合体 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| JP2007238564A true JP2007238564A (ja) | 2007-09-20 |
Family
ID=38584440
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2006066564A Pending JP2007238564A (ja) | 2006-03-10 | 2006-03-10 | カロチノイド−コラーゲンペプチド縮合体 |
Country Status (1)
| Country | Link |
|---|---|
| JP (1) | JP2007238564A (ja) |
Cited By (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US10125104B2 (en) | 2014-05-20 | 2018-11-13 | Asta Pharmaceuticals Co., Ltd. | Carotenoid derivative, pharmaceutically acceptable salt thereof, or pharmaceutically acceptable ester or amide thereof |
| CN109689610A (zh) * | 2016-09-16 | 2019-04-26 | 巴斯夫欧洲公司 | 制备作为类胡萝卜素的结构单元的12’-阿朴胡萝卜素醛酯的方法 |
| WO2023273206A1 (zh) * | 2021-07-01 | 2023-01-05 | 海南三元星生物科技股份有限公司 | 虾青素-胶原蛋白肤口服液及其制备方法 |
-
2006
- 2006-03-10 JP JP2006066564A patent/JP2007238564A/ja active Pending
Cited By (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US10125104B2 (en) | 2014-05-20 | 2018-11-13 | Asta Pharmaceuticals Co., Ltd. | Carotenoid derivative, pharmaceutically acceptable salt thereof, or pharmaceutically acceptable ester or amide thereof |
| CN109689610A (zh) * | 2016-09-16 | 2019-04-26 | 巴斯夫欧洲公司 | 制备作为类胡萝卜素的结构单元的12’-阿朴胡萝卜素醛酯的方法 |
| WO2023273206A1 (zh) * | 2021-07-01 | 2023-01-05 | 海南三元星生物科技股份有限公司 | 虾青素-胶原蛋白肤口服液及其制备方法 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| US4039559A (en) | Aliphatic carboxylic acid esters of Vitamin E and process for preparation thereof | |
| DE69532760T2 (de) | Mittel zur verabreichung von antigenen | |
| EP0703954B1 (fr) | Compositions de derives de polyphenols et leur preparation | |
| JP5470037B2 (ja) | マトリックスの官能化のためのアスコルビン酸誘導体の使用 | |
| JP3576927B2 (ja) | レチニルカルボネート誘導体、調製方法及び使用 | |
| JPWO1997014705A1 (ja) | 高純度トコフェロールリン酸エステル類、その製造方法、その分析方法並びに化粧料 | |
| EP0587499B1 (fr) | Composés benzopyraniques, leur procédé de préparation et leur utilisation comme protecteurs cellulaires | |
| CN1906149A (zh) | 适用作自由基清除剂的高级富勒烯 | |
| JP2021525803A (ja) | カンナビノイド及びそれらの使用 | |
| PL196944B1 (pl) | Sposób wytwarzania estrów delta-9-tetrahydrokanabinolu | |
| JP2007238564A (ja) | カロチノイド−コラーゲンペプチド縮合体 | |
| JPH07118134A (ja) | 皮膚外用剤 | |
| JP4168170B2 (ja) | アルブチンエステル化合物及びその製造方法 | |
| JP4759413B2 (ja) | 皮膚外用剤 | |
| FR2510583A1 (fr) | Derives nouveaux d'acide ursodesoxycholique, leur procede de preparation et leur application en therapeutique | |
| JP2002332210A (ja) | 化粧品に使用するための古細菌からの抽出画分 | |
| JP2004523525A (ja) | レチノール誘導体およびその製造方法 | |
| EP1284145A1 (de) | 2-(3,4-Dihydroxyphenyl)ethyl-substituierte Kohlensäurederivate und deren Verwendung | |
| FR2510558A1 (fr) | Derives nouveaux d'acide chenodesoxycholique | |
| US11718576B2 (en) | Compositions and methods comprising resveratrol | |
| KR101451401B1 (ko) | 비타민 c와 비타민 e의 컨쥬게이트 및 그를 포함하는 항산화제 | |
| US20070281991A1 (en) | Preparation Of Phenol-Amide Compounds With Anti-Oxidizing Properties | |
| JP2000239245A (ja) | フェノールアミンのヒドロキシマンデル酸アミド | |
| JP3878095B2 (ja) | 日焼け予防用の皮膚外用剤 | |
| CN118561728A (zh) | 一种视黄醇衍生物及其制备方法和应用 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| RD04 | Notification of resignation of power of attorney |
Free format text: JAPANESE INTERMEDIATE CODE: A7424 Effective date: 20071109 |
|
| RD04 | Notification of resignation of power of attorney |
Free format text: JAPANESE INTERMEDIATE CODE: A7424 Effective date: 20071116 |
|
| RD04 | Notification of resignation of power of attorney |
Free format text: JAPANESE INTERMEDIATE CODE: A7424 Effective date: 20071126 |