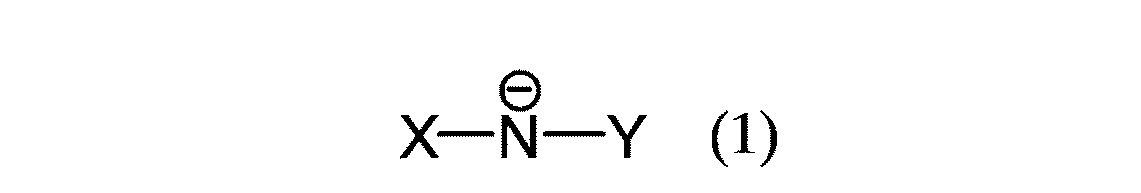JP2005298375A - 常温溶融塩の精製方法 - Google Patents
常温溶融塩の精製方法 Download PDFInfo
- Publication number
- JP2005298375A JP2005298375A JP2004114327A JP2004114327A JP2005298375A JP 2005298375 A JP2005298375 A JP 2005298375A JP 2004114327 A JP2004114327 A JP 2004114327A JP 2004114327 A JP2004114327 A JP 2004114327A JP 2005298375 A JP2005298375 A JP 2005298375A
- Authority
- JP
- Japan
- Prior art keywords
- room temperature
- molten salt
- temperature molten
- group
- purifying
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
Classifications
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y02—TECHNOLOGIES OR APPLICATIONS FOR MITIGATION OR ADAPTATION AGAINST CLIMATE CHANGE
- Y02E—REDUCTION OF GREENHOUSE GAS [GHG] EMISSIONS, RELATED TO ENERGY GENERATION, TRANSMISSION OR DISTRIBUTION
- Y02E60/00—Enabling technologies; Technologies with a potential or indirect contribution to GHG emissions mitigation
- Y02E60/10—Energy storage using batteries
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y02—TECHNOLOGIES OR APPLICATIONS FOR MITIGATION OR ADAPTATION AGAINST CLIMATE CHANGE
- Y02E—REDUCTION OF GREENHOUSE GAS [GHG] EMISSIONS, RELATED TO ENERGY GENERATION, TRANSMISSION OR DISTRIBUTION
- Y02E60/00—Enabling technologies; Technologies with a potential or indirect contribution to GHG emissions mitigation
- Y02E60/13—Energy storage using capacitors
Landscapes
- Pyrrole Compounds (AREA)
- Organic Low-Molecular-Weight Compounds And Preparation Thereof (AREA)
- Secondary Cells (AREA)
Abstract
【課題】 常温溶融塩から、該溶融塩中に不純物として含まれる、アルカリ金属等の金属、及びハロゲンを、簡便、かつ効率的に除去する精製方法を提供する。
【解決手段】 常温溶融塩中に不純物として含まれるアルカリ金属等の金属及びハロゲンを、酸水溶液又はアルカリ水溶液で洗浄することにより、高純度の常温溶融塩を得る。
【選択図】 なし
【解決手段】 常温溶融塩中に不純物として含まれるアルカリ金属等の金属及びハロゲンを、酸水溶液又はアルカリ水溶液で洗浄することにより、高純度の常温溶融塩を得る。
【選択図】 なし
Description
本発明は、常温溶融塩の精製方法に関する。
常温溶融塩はイオン性液体とも呼ばれ、室温付近で液状を呈し広い温度範囲で蒸気圧が低く、また常温固体の塩に比較して有機溶媒等他物質との相溶性が高く、さらに、イオンのみで構成され高いイオン伝導性を示すことから、電気化学デバイスの電解質、電解液、又は有機合成用の溶媒として展開が図られている。
常温溶融塩としては、例えば、1−エチル−3−メチルイミダゾリウム(EMI)カチオン又は1−ブチルピリジニウムカチオンと、テトラフルオロボレートアニオン又はヘキサフルオロホスフェートアニオンとの組合せによる親水性を示す塩が広く知られている。
また、EMIカチオンとビス(トリフルオロメタンスルホニル)イミドアニオンの組合せ等で疎水性を示す常温溶融塩が見出されており、それらは水洗によりアルカリ金属、ハロゲン等の不純物除去が可能なため、高純度の塩が得られることから、電気化学デバイスへの適用検討(例えば、特許文献1参照)が盛んになっている。
さらに、塩の融点、粘度を下げる目的で、4級アンモニウムカチオン、4級ホスホニウムカチオンにアルコキシアルキル基を導入し、常温溶融塩としたものが各種考案されており(例えば、特許文献2参照)、これらも電気化学デバイスへの適用が検討されている。
常温溶融塩を電気化学デバイスに適用するに際しては、不純物としてアルカリ金属等の金属やハロゲンを含有しない、高純度の常温溶融塩が望まれている。ハロゲンの存在は装置の腐食、電極の劣化を招き、また、アルカリ金属の存在はサイクル特性等に影響を与えるという指摘がある。
EMI又は1−ブチルピリジニウム等を含めた4級アンモニウム型常温溶融塩は、通常、3級アミン化合物をハロゲン化アルキルにより4級ハロゲン塩化し、その後、ハロゲンアニオンを所望のアニオンを含むアルカリ金属塩等により変換する方法により製造されており、製造工程でハロゲン、アルカリ金属を含む原料を用いるため、これらの混入が避けられない。特にEMIのテトラフルオロボレート塩のような水溶性の常温溶融塩の場合、アルカリ金属、ハロゲン等の不純物を水洗により除去することができず、数百〜数千ppm以上残留してしまい、特に微量のアルカリ金属、ハロゲンを嫌う電気化学デバイス用材料に適用する際には問題となっている。
一方、EMIのビス(トリフルオロメタンスルホニル)イミド塩のような塩の場合は、例えば、ハロゲン塩からイミドのアルカリ金属塩を用いてイオン交換することにより、疎水性の常温溶融塩とすることができるため、水洗を繰り返せば、最終的には製造時に混在するアルカリ金属やハロゲンを数ppmレベルまで低減することができる。
しかしながら、例えば、アルコキシアルキル基が結合したような、ヘテロ原子含有4級アンモニウムカチオンの場合には、同様にEMIのビス(トリフルオロメタンスルホニル)イミドアニオンとの常温溶融塩としても、アルカリ金属、ハロゲンは除去しにくく、特に数ppmレベルへの低減は困難となる。
そのため、水洗以外に吸着剤の適用、イオン交換樹脂の適用によるアルカリ金属や、ハロゲンの除去等が考えられるが、操作が煩雑になる、効果が得られにくい、コストがかかる、常温溶融塩のロスが大きくなる等の問題があり、工業的な方法とはいい難い。
本発明は上記の問題に対して鑑みられたものであり、その目的は、不純物であるアルカリ金属等の金属及びハロゲンの含有量が少ない高純度の常温溶融塩とすることのできる、簡便かつ効率的な精製方法を提供することである。
本発明者らは上記したような課題に対し鋭意検討を行った結果、常温溶融塩を酸水溶液又はアルカリ水溶液で洗浄することにより、不純物であるアルカリ金属等の金属及びハロゲンを、簡便かつ効率的に低減することができることを見出し、本発明を完成させるに至った。
すなわち本発明は、以下に示すとおりの、常温溶融塩の精製方法である。
(1)常温溶融塩を酸水溶液又はアルカリ水溶液で洗浄することを特徴とする常温溶融塩の精製方法。
(2)アルカリ水溶液がアンモニア水溶液であることを特徴とする上記(1)に記載の常温溶融塩の精製方法。
(3)アンモニア水溶液中のアンモニアの濃度が0.02〜0.5wt%であることを特徴とする上記(2)に記載の常温溶融塩の精製方法。
(4)常温溶融塩が、アンモニウム、イミダゾリウム、ピリジニウム、ホスホニウム、及びスルホニウムからなる群より選ばれる1種又は2種以上のカチオンと、下記一般式(1)
で示されるイミドアニオンからなる常温溶融塩であることを特徴とする上記(1)乃至(3)のいずれかに記載の常温溶融塩の精製方法。
(5)カチオンが、カチオン中心以外にヘテロ原子を有する官能基を含む、アンモニウム、イミダゾリウム、ピリジニウム、ホスホニウム、及びスルホニウムからなる群より選ばれる1種又は2種以上のカチオンであることを特徴とする上記(4)に記載の常温溶融塩の精製方法。
(6)カチオン中心以外にヘテロ原子を有する官能基がアルコキシアルキル基であることを特徴とする上記(5)に記載の常温溶融塩の精製方法。
以下、本発明について詳細に説明する。
本発明において、常温溶融塩を洗浄するために用いられる酸又はアルカリとしては、特に限定するものではなく、種々の酸、アルカリを用いることができるが、除去対象であるアルカリ金属や、ハロゲンを含まず、常温溶融塩に溶解しにくいものが好ましい。具体的には、酸としては、例えば、硝酸、硫酸等が挙げられ、アルカリとしては、例えば、アンモニア、ヒドラジン等が挙げられる。これらの中でも、アンモニアが、常温溶融塩の回収率、品質、精製コスト面で特に優れている。
本発明において、酸水溶液又はアルカリ水溶液のpHは特に限定するものではないが、酸水溶液の場合、pHが1〜4の範囲、アルカリ水溶液の場合、pHが10〜13の範囲とすることが、常温溶融塩からの金属及びハロゲンの除去性能、常温溶融塩の回収率の面から好ましい。アンモニア水溶液の場合には、その濃度は0.02〜0.5wt%の範囲であることが好ましく、0.02wt%未満ではアルカリ金属及びハロゲン成分の除去性能が十分でなく、0.5wt%を越えると、作業時の臭気が著しく、常温溶融塩の回収率も低下する場合がある。
本発明において、酸水溶液又はアルカリの使用量については、不純物を除去できる程度使用すれば良く、特に限定するものではないが、不純物である金属及びハロゲン成分の除去効率の面から、常温溶融塩に対して10〜1000wt%の範囲、特に30〜300wt%の範囲が好ましい。常温溶融塩を洗浄する際の処理温度については、通常、室温で行えば良く、特に限定するものではないが、条件によっては0〜60℃の範囲で実施することも可能である。さらに詳細な洗浄条件について、特に限定するものではないが、攪拌羽根や、マグネチックスターラー、振とう等により、激しく攪拌することにより、常温溶融塩と酸又はアルカリの接触面をできるだけ増やした方が、直ちに(数分程度の内に)不純物除去が行うことができる。
本発明の、酸水溶液又はアルカリ水溶液による常温溶融塩の洗浄後、さらに水洗を実施することにより、洗浄で用いた酸又はアルカリ源を常温溶融塩から除去することができ、より高純度の常温溶融塩とすることができる。
本発明の精製方法は、疎水性を示す常温溶融塩に対して適用することが好ましい。ここで、疎水性を示す常温溶融塩としては、常温溶融塩と本発明で用いられる酸又はアルカリとが完全に均一にならなければ良く、特に限定するものではないが、本発明の精製方法は、水への溶解度がおおよそ10wt%以下の常温溶融塩に対して適用することが収率等の面で好ましい。
本発明の精製方法は、従来公知のEMI、トリメチルブチルアンモニウム等のビス(トリフルオロメタンスルホニル)イミド塩にも適用できる。これらのカチオン中心以外が炭化水素のみで構成されるカチオン種のイミド塩の場合は、上記したとおり、単純な水洗を繰り返し実施すれば、不純物であるアルカリ金属及びハロゲンを数ppmのレベルまで低減することは可能であるが、本発明の方法を用いれば、使用水量の低減を図ることができ、より効率的に不純物の除去が可能となる。
本発明の精製方法は、アルコキシアルキル基を含有するような、カチオン中心以外に酸素、窒素、硫黄等のヘテロ原子を含むようなカチオン種からなる常温溶融塩に対して、特に有効である。このようなカチオン中心以外にヘテロ原子を含有するカチオンからなる常温溶融塩は、アルカリ金属や、ハロゲンを溶解しやすい傾向があるため、これら不純物の除去が難しくなり、単純な水洗を繰り返しても数百〜数十ppmのレベルに止まる。これらカチオンを含む常温溶融塩に対し、本発明の精製方法を施すことにより、アルカリ金属及びハロゲン成分をそれぞれ数ppmのレベルまで低減することが可能となる。
カチオン中心以外にヘテロ原子を含有するカチオンとしては、例えば、(2−メトキシエチル)トリエチルアンモニウム、(2−メトキシエチル)ジエチルメチルアンモニウム、(2−エトキシエチル)トリエチルアンモニウム、(2−エトキシエチル)トリメチルアンモニウム、(2−エトキシエチル)ジエチルメチルアンモニウム、(3−メトキシプロピル)トリメチルアンモニウム、(3−メトキシブチル)トリメチルアンモニウム、(6−メトキシヘキシル)トリメチルアンモニウム、{2’−メトキシ(2−エトキシエチル)}トリメチルアンモニウム、{2’−エトキシ(2−エトキシエチル)}エチルジメチルアンモニウム、(2−ヒドロキシエチル)トリメチルアンモニウム、(3−ヒドロキシプロピル)トリメチルアンモニウム、(6−ヒドロキシヘキシル)トリメチルアンモニウム、(2−ジメチルアミノエチル)トリメチルアンモニウム、(2−ジメチルアミノエチル)エチルジメチルアンモニウム、(2−ジエチルアミノエチル)トリエチルアンモニウム、(2−ジエチルアミノエチル)メチルジエチルアンモニウム、(3−ジメチルアミノプロピル)トリメチルアンモニウム、(4−ジメチルアミノブチル)トリメチルアンモニウム、(6−ジメチルアミノヘキシル)トリメチルアンモニウム等が挙げられる。
一方、アニオン種に関しても、カチオンと組合せた場合に疎水性を示す常温溶融塩に対して、本発明の精製方法を適用することが好ましく、具体的には、上記一般式(1)で示されるイミドアニオン等が例示される。
上記一般式(1)で示されるイミドアニオンとしては、特に限定するものではないが、例えば、ビス(トリフルオロメチルスルホニル)イミド、ビス(ペンタフルオロエチルスルホニル)イミド、ビス(フルオロスルホニル)イミド、ビス(トリフルオロメチルカルボニル)イミド、(トリフルオロメチルスルホニル)(トリフルオロメチルカルボニル)イミド等が好適なものとして挙げられる。
本発明によれば、簡便な方法により、効率的に常温溶融塩に含まれるアルカリ金属等の金属やハロゲン等の不純物を除去することができる。
本発明の精製方法により得られる常温溶融塩は、不純物であるアルカリ金属等の金属及びハロゲンをほとんど含まないことから、二次電池、電気二重層キャパシタ、燃料電池、色素増感太陽電池等の電気化学デバイス材料として特に好適である。
以下、参考例、実施例、比較例に基づいて具体的に説明するが、本発明はこれらの実施例のみに限定されるものではない。
[参考例1] 疎水性アルコキシアルキル基含有アンモニウム常温溶融塩[(2−メトキシエチル)ジエチルメチルアンモニウム・ビス(トリフルオロメチルスルホニル)イミド]の製造
攪拌機、冷却管、滴下ロート、温度計、並びに固形物の投入が可能な投入口を附した200mlフラスコに、2−ジエチルアミノエタノール11.7g(100mmol)及びテトラヒドロフラン100mlを仕込み、攪拌下、水素化ナトリウム(60%、油性)4.2g(105mmol)を少量ずつ添加し、ヒドロキシル基のナトリウムアルコラート化を行った。反応により水素が発生、発熱するので、水冷により温度を40℃以下に保ちながら行った。水素化ナトリウム添加終了後、投入口を閉め、25〜40℃の間で30分間攪拌を行った後、続いて、ヨードメタン31.2g(220mmol)を滴下ロートより60分にわたり滴下した。アルコラート化反応時と同様水冷により温度を40℃以下に保ちながら行い、滴下終了後40℃で6時間反応を行った。生成した(2−メトキシエチル)ジエチルメチルアンモニウム・ヨーダイド、及び副生するヨウ化ナトリウムは析出し、反応の進行に伴い反応液のスラリー粘度は高まった。その後、エバポレーターにより溶媒等を除去、得られるスラリーをジエチルエーテルで洗浄し、さらに、ろ過、80℃で減圧乾燥を行い、副生塩であるヨウ化ナトリウムとともに42.1gの塩(副生塩を含め理論収量の99.1%を回収)を得た。
攪拌機、冷却管、滴下ロート、温度計、並びに固形物の投入が可能な投入口を附した200mlフラスコに、2−ジエチルアミノエタノール11.7g(100mmol)及びテトラヒドロフラン100mlを仕込み、攪拌下、水素化ナトリウム(60%、油性)4.2g(105mmol)を少量ずつ添加し、ヒドロキシル基のナトリウムアルコラート化を行った。反応により水素が発生、発熱するので、水冷により温度を40℃以下に保ちながら行った。水素化ナトリウム添加終了後、投入口を閉め、25〜40℃の間で30分間攪拌を行った後、続いて、ヨードメタン31.2g(220mmol)を滴下ロートより60分にわたり滴下した。アルコラート化反応時と同様水冷により温度を40℃以下に保ちながら行い、滴下終了後40℃で6時間反応を行った。生成した(2−メトキシエチル)ジエチルメチルアンモニウム・ヨーダイド、及び副生するヨウ化ナトリウムは析出し、反応の進行に伴い反応液のスラリー粘度は高まった。その後、エバポレーターにより溶媒等を除去、得られるスラリーをジエチルエーテルで洗浄し、さらに、ろ過、80℃で減圧乾燥を行い、副生塩であるヨウ化ナトリウムとともに42.1gの塩(副生塩を含め理論収量の99.1%を回収)を得た。
次いで、副生塩を含む(2−メトキシエチル)ジエチルメチルアンモニウム・ヨーダイド25.4g(60mmolに相当)をこれと等重量の水に溶解し、攪拌下、等モル量のリチウムビス(トリフルオロメチルスルホニル)イミド17.2gを含む50%水溶液を滴下した。滴下後さらに30分間激しく攪拌、熟成を行い、その後静置し、水相と有機相(目的物)に2相分離させた。さらに有機相を有機相と同体積の水で1回水洗を行い、その後含まれる水分を100℃、減圧下乾燥を行うことにより除去、室温(25℃)で液状の(2−メトキシエチル)ジエチルメチルアンモニウム・ビス(トリフルオロメタンスルホニル)イミド21.6g(収率84.5%)を得た。本常温溶融塩中には、Li 370ppm、Na 1200ppm、及びI 900ppmの無機不純物を含んでいた。
なお、アルカリ金属の定量は、湿式分解後、誘電結合型プラズマ発光分析(ICP)にて実施し、ハロゲンの定量は、密閉式燃焼で吸収液に溶解後イオンクロマトグラフィーにより実施した。なお、検出限界はアルカリ金属で1ppm、ハロゲンで10ppmである。
[参考例2] メチルプロピルピロリジニウム・ビス(トリフルオロメタンスルホニル)イミドの製造(カチオン種がカチオン中心以外にヘテロ原子を含まないもの)
参考例1と同様の装置を用い、N−メチルピロリジン8.5g(100mmol)及びテトラヒドロフラン100mlを仕込み、ヨードプロパン17.9g(105mmol)を滴下ロートより30分程度で滴下し、滴下終了後60℃で6時間反応を行った。生成したメチルプロピルピロリジニウム・ヨーダイドは析出し、反応の進行に伴い反応液のスラリー粘度は高まった。その後、ろ過により溶媒等を分離、さらに乾燥を行い、22.0gのメチルプロピルピロリジニウム・ヨーダイド22.0gを得た。
参考例1と同様の装置を用い、N−メチルピロリジン8.5g(100mmol)及びテトラヒドロフラン100mlを仕込み、ヨードプロパン17.9g(105mmol)を滴下ロートより30分程度で滴下し、滴下終了後60℃で6時間反応を行った。生成したメチルプロピルピロリジニウム・ヨーダイドは析出し、反応の進行に伴い反応液のスラリー粘度は高まった。その後、ろ過により溶媒等を分離、さらに乾燥を行い、22.0gのメチルプロピルピロリジニウム・ヨーダイド22.0gを得た。
次いで、副生塩を含むメチルプロピルピロリジニウム・ヨーダイド11.5g(45mmol)を等量の水に溶解し、等モル量のリチウムビス(トリフルオロメチルスルホニル)イミド12.9gを含む50%水溶液を攪拌しながら滴下した。以下、参考例と同様の操作を行い、液状のメチルプロピルピロリジニウム・ビス(トリフルオロメタンスルホニル)イミド16.2gを得た。本常温溶融塩中には、Li 180ppm、及びBr 270ppmの無機不純物を含んでいた。
以下、本発明の精製方法により、参考例1、2で得られた常温溶融塩に含まれるアルカリ金属及びハロゲン成分の除去を実施した。
[実施例1] 参考例1の常温溶融塩の0.2wt%アンモニア水溶液による洗浄
参考例1で得られた、Li 370ppm、Na 1200ppm、及びI 900ppmを含む常温溶融塩[(2−メトキシエチル)ジエチルメチルアンモニウム・ビス(トリフルオロメタンスルホニル)イミド]20.0gを100mlビーカーに入れ、これに0.2wt%アンモニア水溶液(pH11.4)20.0gを加え、マグネチックスターラーで、室温条件、15分間激しく攪拌した。終了後、分液を行い、アンモニア水溶液を除去、該常温溶融塩を、さらにもう1回20gの水と15分間激しく攪拌することで洗浄した。1時間以上分液を行った後、常温溶融塩を分取、100℃、減圧下乾燥を行い、Li 2ppm、Na 8ppm、及びI <10ppmを含む常温溶融塩18.2gを得た。
参考例1で得られた、Li 370ppm、Na 1200ppm、及びI 900ppmを含む常温溶融塩[(2−メトキシエチル)ジエチルメチルアンモニウム・ビス(トリフルオロメタンスルホニル)イミド]20.0gを100mlビーカーに入れ、これに0.2wt%アンモニア水溶液(pH11.4)20.0gを加え、マグネチックスターラーで、室温条件、15分間激しく攪拌した。終了後、分液を行い、アンモニア水溶液を除去、該常温溶融塩を、さらにもう1回20gの水と15分間激しく攪拌することで洗浄した。1時間以上分液を行った後、常温溶融塩を分取、100℃、減圧下乾燥を行い、Li 2ppm、Na 8ppm、及びI <10ppmを含む常温溶融塩18.2gを得た。
[実施例2] 参考例1の常温溶融塩の0.1N−硝酸による洗浄
0.1N−硝酸(pH1.3)20.0gを用いた以外は実施例1と同様に行い、Li 3ppm、Na 9ppm、及びI <10ppmを含む常温溶融塩17.6gを得た。なお、該硝酸処理により、常温溶融塩に若干の着色が生じた。
0.1N−硝酸(pH1.3)20.0gを用いた以外は実施例1と同様に行い、Li 3ppm、Na 9ppm、及びI <10ppmを含む常温溶融塩17.6gを得た。なお、該硝酸処理により、常温溶融塩に若干の着色が生じた。
[比較例1] 水洗のみによるアルカリ金属、ハロゲンの除去
参考例1で得られた常温溶融塩20.0gを、1回当たり20.0gの水を用い15分間、実施例1と同様マグネチックスターラーで激しく攪拌することによる水洗を3回繰り返した。水洗後実施例1と同様に処理、乾燥し、Li 90ppm、Na 350ppm、及びI 130ppmを含む常温溶融塩18.4gを得た。
参考例1で得られた常温溶融塩20.0gを、1回当たり20.0gの水を用い15分間、実施例1と同様マグネチックスターラーで激しく攪拌することによる水洗を3回繰り返した。水洗後実施例1と同様に処理、乾燥し、Li 90ppm、Na 350ppm、及びI 130ppmを含む常温溶融塩18.4gを得た。
[実施例3] メチルプロピルピロリジニウム・ビス(トリフルオロメタンスルホニル)イミドからのアルカリ金属、ハロゲンの除去(カチオン種がカチオン中心以外にヘテロ原子を含まない場合)
Li 180ppm、及びBr 270ppmを含むメチルプロピルピロリジニウム・ビス(トリフルオロメタンスルホニル)イミド20.0gを用いた以外は実施例1と同様に操作することで、Li<1ppm、及びBr<10ppmを含む常温溶融塩18.6gを得た。
Li 180ppm、及びBr 270ppmを含むメチルプロピルピロリジニウム・ビス(トリフルオロメタンスルホニル)イミド20.0gを用いた以外は実施例1と同様に操作することで、Li<1ppm、及びBr<10ppmを含む常温溶融塩18.6gを得た。
[比較例2] 水洗のみによるアルカリ金属、ハロゲンの除去(実施例3の比較)
実施例3で用いたLi 180ppm、及びBr 270ppmを含むメチルプロピルピロリジニウム・ビス(トリフルオロメタンスルホニル)イミド20.0gを、比較例1と同様、1回当たり20.0gの水を用いて2回洗浄を繰り返した。Li 3ppm、及びBr <10ppmの常温溶融塩18.5gを得た。
実施例3で用いたLi 180ppm、及びBr 270ppmを含むメチルプロピルピロリジニウム・ビス(トリフルオロメタンスルホニル)イミド20.0gを、比較例1と同様、1回当たり20.0gの水を用いて2回洗浄を繰り返した。Li 3ppm、及びBr <10ppmの常温溶融塩18.5gを得た。
Claims (6)
- 常温溶融塩を酸水溶液又はアルカリ水溶液で洗浄することを特徴とする常温溶融塩の精製方法。
- アルカリ水溶液がアンモニア水溶液であることを特徴とする請求項1に記載の常温溶融塩の精製方法。
- アンモニア水溶液中のアンモニアの濃度が0.02〜0.5wt%であることを特徴とする請求項2に記載の常温溶融塩の精製方法。
- カチオンが、カチオン中心以外にヘテロ原子を有する官能基を含む、アンモニウム、イミダゾリウム、ピリジニウム、ホスホニウム、及びスルホニウムからなる群より選ばれる1種又は2種以上のカチオンであることを特徴とする請求項4に記載の常温溶融塩の精製方法。
- カチオン中心以外にヘテロ原子を有する官能基がアルコキシアルキル基であることを特徴とする請求項5に記載の常温溶融塩の精製方法。
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2004114327A JP2005298375A (ja) | 2004-04-08 | 2004-04-08 | 常温溶融塩の精製方法 |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2004114327A JP2005298375A (ja) | 2004-04-08 | 2004-04-08 | 常温溶融塩の精製方法 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| JP2005298375A true JP2005298375A (ja) | 2005-10-27 |
Family
ID=35330358
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2004114327A Pending JP2005298375A (ja) | 2004-04-08 | 2004-04-08 | 常温溶融塩の精製方法 |
Country Status (1)
| Country | Link |
|---|---|
| JP (1) | JP2005298375A (ja) |
Cited By (7)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2006278167A (ja) * | 2005-03-29 | 2006-10-12 | Dai Ichi Kogyo Seiyaku Co Ltd | 超高純度イオン性液体 |
| WO2009025246A1 (ja) | 2007-08-17 | 2009-02-26 | Asahi Glass Company, Limited | 精製された含フッ素ビススルホニルイミドのアンモニウム塩の製造方法 |
| JP2014040369A (ja) * | 2009-03-31 | 2014-03-06 | Mitsubishi Materials Corp | ビス(フルオロスルホニル)イミド塩の製造方法 |
| WO2014171196A1 (ja) * | 2013-04-19 | 2014-10-23 | 住友電気工業株式会社 | 溶融塩電解質及びナトリウム溶融塩電池 |
| US9156692B2 (en) | 2009-03-31 | 2015-10-13 | Mitsubishi Materials Electronic Chemicals Co., Ltd. | Method for producing bis(fluorosulfonyl)imide salt, method for producing fluorosulfate, and method for producing bis(fluorosulfonyl)imide onium salt |
| JP2016178064A (ja) * | 2015-03-23 | 2016-10-06 | Tdk株式会社 | リチウムイオン二次電池用電解液およびこれを用いたリチウムイオン二次電池 |
| CN109641837A (zh) * | 2016-07-26 | 2019-04-16 | 东曹精细化工株式会社 | 卤化物得以减少的具有聚合性官能团的磺酰亚胺的有机溶剂溶液 |
-
2004
- 2004-04-08 JP JP2004114327A patent/JP2005298375A/ja active Pending
Cited By (11)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2006278167A (ja) * | 2005-03-29 | 2006-10-12 | Dai Ichi Kogyo Seiyaku Co Ltd | 超高純度イオン性液体 |
| WO2009025246A1 (ja) | 2007-08-17 | 2009-02-26 | Asahi Glass Company, Limited | 精製された含フッ素ビススルホニルイミドのアンモニウム塩の製造方法 |
| JPWO2009025246A1 (ja) * | 2007-08-17 | 2010-11-25 | 旭硝子株式会社 | 精製された含フッ素ビススルホニルイミドのアンモニウム塩の製造方法 |
| US7989635B2 (en) | 2007-08-17 | 2011-08-02 | Asahi Glass Company, Limited | Method for producing purified ammonium salt of fluorinated bis-sulfonylimide |
| JP2014040369A (ja) * | 2009-03-31 | 2014-03-06 | Mitsubishi Materials Corp | ビス(フルオロスルホニル)イミド塩の製造方法 |
| US9156692B2 (en) | 2009-03-31 | 2015-10-13 | Mitsubishi Materials Electronic Chemicals Co., Ltd. | Method for producing bis(fluorosulfonyl)imide salt, method for producing fluorosulfate, and method for producing bis(fluorosulfonyl)imide onium salt |
| WO2014171196A1 (ja) * | 2013-04-19 | 2014-10-23 | 住友電気工業株式会社 | 溶融塩電解質及びナトリウム溶融塩電池 |
| JPWO2014171196A1 (ja) * | 2013-04-19 | 2017-02-16 | 住友電気工業株式会社 | 溶融塩電解質及びナトリウム溶融塩電池 |
| JP2016178064A (ja) * | 2015-03-23 | 2016-10-06 | Tdk株式会社 | リチウムイオン二次電池用電解液およびこれを用いたリチウムイオン二次電池 |
| CN109641837A (zh) * | 2016-07-26 | 2019-04-16 | 东曹精细化工株式会社 | 卤化物得以减少的具有聚合性官能团的磺酰亚胺的有机溶剂溶液 |
| JPWO2018021185A1 (ja) * | 2016-07-26 | 2019-05-16 | 東ソー・ファインケム株式会社 | ハロゲン化物が低減された重合性官能基を有するスルホンイミドの有機溶剤溶液 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP6964595B2 (ja) | リチウムビス(フルオロスルホニル)イミドの新規の製造方法 | |
| CN102405189B (zh) | 氟磺酰亚胺盐以及氟磺酰亚胺盐的制备方法 | |
| US7641807B2 (en) | Direct process for the manufacture of tetraalkylammonium tetrafluoroborate-containing electrolyte compositions | |
| CN101980955B (zh) | 磺酰亚胺盐及其制备方法 | |
| JP5402634B2 (ja) | 精製された含フッ素ビススルホニルイミドのアンモニウム塩の製造方法 | |
| JP6370852B2 (ja) | ジスルホニルアミド塩の顆粒または粉末 | |
| CN1298698C (zh) | 四级烷基铵盐的精制方法及四级烷基铵盐 | |
| JP5135926B2 (ja) | 4−フルオロ−1,3−ジオキソラン−2−オンの製造方法 | |
| WO2009105881A1 (en) | Ionic liquids comprising ligands containing positively charged heterocyclic ring useful as catalyst and for metal extractions | |
| JP2005139100A (ja) | 常温溶融塩 | |
| CN115477308B (zh) | 一种一步法常温制备四氟硼酸钠的方法 | |
| JP2005298375A (ja) | 常温溶融塩の精製方法 | |
| JP4322073B2 (ja) | イオン性液体の精製方法 | |
| JP5595543B1 (ja) | 有価金属抽出方法 | |
| WO2014061482A1 (ja) | イオン液体 | |
| JP2005325067A (ja) | 第四級アンモニウム塩の精製方法及び該方法により調製された第四級アンモニウム塩 | |
| US8501138B2 (en) | Production method of high purity silver tetrafluoroborate | |
| CN106674261A (zh) | 草酸二氟硼酸锂的提纯方法 | |
| WO2016160855A1 (en) | N-substituted glycinium bis(fluorosulfonyl)imide ionic liquid | |
| JP2016027030A (ja) | 精製イオン性錯体の製造方法 | |
| CN118125403B (zh) | 一种资源化再利用处理多元醇醚精馏残液的方法 | |
| JP4993262B2 (ja) | 第四級アンモニウムテトラフルオロボレートの精製方法及びそれを用いた電気二重層キャパシタ | |
| JP2016027029A (ja) | 精製イオン性錯体の製造方法及びイオン性錯体 | |
| KR101402523B1 (ko) | 수용액 중에서 테트라플루오로보레이트 음이온을 제거하고 테트라플루오로보레이트 음이온을 포함하는 이온성 액체를 얻는 방법 | |
| JP2003335739A (ja) | 有機オニウムのフッ化物塩、その製造方法、及びそれを用いたテトラフルオロアルミネートの有機オニウム塩の製造方法 |