JP2005295825A - 袋状湿度供給容器 - Google Patents
袋状湿度供給容器 Download PDFInfo
- Publication number
- JP2005295825A JP2005295825A JP2004113146A JP2004113146A JP2005295825A JP 2005295825 A JP2005295825 A JP 2005295825A JP 2004113146 A JP2004113146 A JP 2004113146A JP 2004113146 A JP2004113146 A JP 2004113146A JP 2005295825 A JP2005295825 A JP 2005295825A
- Authority
- JP
- Japan
- Prior art keywords
- bag
- humidity supply
- humidity
- tissue culture
- supply container
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Withdrawn
Links
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 claims abstract description 67
- 238000011109 contamination Methods 0.000 claims abstract description 52
- 230000035699 permeability Effects 0.000 claims abstract description 40
- 239000000463 material Substances 0.000 claims abstract description 33
- 238000012136 culture method Methods 0.000 claims abstract description 6
- 238000000034 method Methods 0.000 claims description 18
- 230000001580 bacterial effect Effects 0.000 claims description 13
- 239000012528 membrane Substances 0.000 claims description 11
- -1 polyethylene Polymers 0.000 claims description 11
- 239000004698 Polyethylene Substances 0.000 claims description 10
- 229920000690 Tyvek Polymers 0.000 claims description 10
- 239000004775 Tyvek Substances 0.000 claims description 10
- 229920000573 polyethylene Polymers 0.000 claims description 10
- 230000004927 fusion Effects 0.000 claims description 8
- 239000004745 nonwoven fabric Substances 0.000 claims description 7
- VGGSQFUCUMXWEO-UHFFFAOYSA-N Ethene Chemical compound C=C VGGSQFUCUMXWEO-UHFFFAOYSA-N 0.000 claims description 6
- 239000005977 Ethylene Substances 0.000 claims description 6
- 101000925662 Enterobacteria phage PRD1 Endolysin Proteins 0.000 claims description 5
- 230000005251 gamma ray Effects 0.000 claims description 5
- 239000000758 substrate Substances 0.000 claims description 5
- 230000002265 prevention Effects 0.000 claims description 4
- 229920001410 Microfiber Polymers 0.000 claims description 3
- 230000010354 integration Effects 0.000 claims description 2
- 239000000088 plastic resin Substances 0.000 claims description 2
- 241000894006 Bacteria Species 0.000 abstract description 16
- 230000004888 barrier function Effects 0.000 abstract description 10
- 230000000813 microbial effect Effects 0.000 abstract description 8
- 239000012298 atmosphere Substances 0.000 abstract description 2
- 238000009736 wetting Methods 0.000 abstract 1
- 238000002474 experimental method Methods 0.000 description 18
- 238000012360 testing method Methods 0.000 description 18
- 239000002609 medium Substances 0.000 description 16
- 229920001817 Agar Polymers 0.000 description 12
- 239000008272 agar Substances 0.000 description 12
- 238000005070 sampling Methods 0.000 description 9
- 238000007789 sealing Methods 0.000 description 8
- 230000001954 sterilising effect Effects 0.000 description 8
- 238000004659 sterilization and disinfection Methods 0.000 description 8
- 244000005700 microbiome Species 0.000 description 7
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 6
- 239000000853 adhesive Substances 0.000 description 5
- 230000001070 adhesive effect Effects 0.000 description 5
- 210000004027 cell Anatomy 0.000 description 5
- 244000052616 bacterial pathogen Species 0.000 description 3
- 239000003814 drug Substances 0.000 description 3
- 230000008020 evaporation Effects 0.000 description 3
- 238000001704 evaporation Methods 0.000 description 3
- 210000005260 human cell Anatomy 0.000 description 3
- 238000004519 manufacturing process Methods 0.000 description 3
- 230000002093 peripheral effect Effects 0.000 description 3
- 239000011734 sodium Substances 0.000 description 3
- 108090000790 Enzymes Proteins 0.000 description 2
- 102000004190 Enzymes Human genes 0.000 description 2
- UIIMBOGNXHQVGW-UHFFFAOYSA-M Sodium bicarbonate Chemical compound [Na+].OC([O-])=O UIIMBOGNXHQVGW-UHFFFAOYSA-M 0.000 description 2
- 238000004113 cell culture Methods 0.000 description 2
- 238000000151 deposition Methods 0.000 description 2
- 239000007789 gas Substances 0.000 description 2
- 238000011194 good manufacturing practice Methods 0.000 description 2
- 238000010438 heat treatment Methods 0.000 description 2
- 210000004962 mammalian cell Anatomy 0.000 description 2
- 229920003023 plastic Polymers 0.000 description 2
- 239000004033 plastic Substances 0.000 description 2
- 238000012545 processing Methods 0.000 description 2
- 238000003908 quality control method Methods 0.000 description 2
- 239000000126 substance Substances 0.000 description 2
- 239000010409 thin film Substances 0.000 description 2
- 241000283690 Bos taurus Species 0.000 description 1
- IAYPIBMASNFSPL-UHFFFAOYSA-N Ethylene oxide Chemical compound C1CO1 IAYPIBMASNFSPL-UHFFFAOYSA-N 0.000 description 1
- 241001465754 Metazoa Species 0.000 description 1
- 239000004743 Polypropylene Substances 0.000 description 1
- 239000004793 Polystyrene Substances 0.000 description 1
- 239000006087 Silane Coupling Agent Substances 0.000 description 1
- 210000004102 animal cell Anatomy 0.000 description 1
- 210000004666 bacterial spore Anatomy 0.000 description 1
- 238000005452 bending Methods 0.000 description 1
- 230000010261 cell growth Effects 0.000 description 1
- 230000004663 cell proliferation Effects 0.000 description 1
- 238000012258 culturing Methods 0.000 description 1
- 238000011161 development Methods 0.000 description 1
- 238000001035 drying Methods 0.000 description 1
- 230000000694 effects Effects 0.000 description 1
- 230000012010 growth Effects 0.000 description 1
- 239000001963 growth medium Substances 0.000 description 1
- 229920001903 high density polyethylene Polymers 0.000 description 1
- 239000004700 high-density polyethylene Substances 0.000 description 1
- GPRLSGONYQIRFK-UHFFFAOYSA-N hydron Chemical compound [H+] GPRLSGONYQIRFK-UHFFFAOYSA-N 0.000 description 1
- 230000036512 infertility Effects 0.000 description 1
- 238000005304 joining Methods 0.000 description 1
- 210000004698 lymphocyte Anatomy 0.000 description 1
- 230000002101 lytic effect Effects 0.000 description 1
- 235000015097 nutrients Nutrition 0.000 description 1
- 210000000056 organ Anatomy 0.000 description 1
- 230000035515 penetration Effects 0.000 description 1
- 238000007589 penetration resistance test Methods 0.000 description 1
- 238000011056 performance test Methods 0.000 description 1
- 229920001155 polypropylene Polymers 0.000 description 1
- 229920002223 polystyrene Polymers 0.000 description 1
- 239000004800 polyvinyl chloride Substances 0.000 description 1
- 229920000915 polyvinyl chloride Polymers 0.000 description 1
- 230000000644 propagated effect Effects 0.000 description 1
- 150000003839 salts Chemical class 0.000 description 1
- 210000002966 serum Anatomy 0.000 description 1
- 229910000030 sodium bicarbonate Inorganic materials 0.000 description 1
- 235000017557 sodium bicarbonate Nutrition 0.000 description 1
- 238000001228 spectrum Methods 0.000 description 1
- 238000003860 storage Methods 0.000 description 1
- 229920005992 thermoplastic resin Polymers 0.000 description 1
- 210000001519 tissue Anatomy 0.000 description 1
- 238000003466 welding Methods 0.000 description 1
Images
Landscapes
- Immobilizing And Processing Of Enzymes And Microorganisms (AREA)
- Micro-Organisms Or Cultivation Processes Thereof (AREA)
- Apparatus Associated With Microorganisms And Enzymes (AREA)
Abstract
【課題】組織培養に際し、培養装置内の雰囲気を加湿するに際し、加湿にともなう微生物汚染を容易に防止するための袋状湿度供給容器及び該容器を用いた簡便な組織培養方法並びに組織培養システムを提供すること。
【解決手段】本発明は、次のような袋状湿度供給容器を提供し発明を完成した。
気密性を有する基材によって調製された水を担持する袋体であって、その袋体の一部に通気性、透湿性を有しかつバクテリアバリア性の膜状基材によって調製された湿度供給部を有する袋状湿度供給容器。湿度供給状態におかれるまで、湿度供給部による袋体に担持された水による透湿性が阻止された袋状湿度供給容器。そしてこの容器を用いた簡便な組織培養方法及び培養システムを提供しようとするものである。
【解決手段】本発明は、次のような袋状湿度供給容器を提供し発明を完成した。
気密性を有する基材によって調製された水を担持する袋体であって、その袋体の一部に通気性、透湿性を有しかつバクテリアバリア性の膜状基材によって調製された湿度供給部を有する袋状湿度供給容器。湿度供給状態におかれるまで、湿度供給部による袋体に担持された水による透湿性が阻止された袋状湿度供給容器。そしてこの容器を用いた簡便な組織培養方法及び培養システムを提供しようとするものである。
Description
本発明は、湿度供給容器に関する。より詳細には、微生物汚染が制御された組織培養のための加湿手段に関し、組織培養装置内の湿度を過飽和に保つための通気性、透湿性に優れかつバクテリアバリア性を達成した袋状湿度供給容器に関する。
組織培養装置(CO2インキュベーター)を使用して、ヒト細胞を始め哺乳動物細胞等の組織培養がさかんに行われている。組織培養とは、ヒトや動物の組織、臓器、リンパ細胞を分離して、フラスコやシャーレ等の培養容器にて、細胞を増殖させる方法である。通常培養フラスコ、シャーレにはヒト由来細胞のほか、メディウム液(培地)と牛由来血清などを入れて細胞の増殖を行う。培養の条件としては、温度37℃、CO2濃度5%、湿度過飽和が一般的である。
組織培養装置(CO2インキュベーター)は、培養条件環境を維持するため開発された装置であり、例えば温度は、哺乳動物細胞が生理的に必要な増殖条件である。
CO2濃度は、細胞が増殖に必要な培養液のpHを安定に維持することを目的にしている。培養液中の水素イオン濃度を調整するため、炭酸水素ナトリウム(NaHCO3)を添加することで、2NaHCO3⇔Na2CO3+H2O+CO2となる。CO2が放出されると、Na2CO3濃度が増し培養液中のpHは7.4以上となり、細胞の培養にとって障害となる。これを防止するために組織培養装置(CO2インキュベーター)にCO2ガスを供給することでNa2CO3はNaHCO3に戻り、培養液中のpHは7.1から7.4にて平衡化することが可能となる。
CO2濃度は、細胞が増殖に必要な培養液のpHを安定に維持することを目的にしている。培養液中の水素イオン濃度を調整するため、炭酸水素ナトリウム(NaHCO3)を添加することで、2NaHCO3⇔Na2CO3+H2O+CO2となる。CO2が放出されると、Na2CO3濃度が増し培養液中のpHは7.4以上となり、細胞の培養にとって障害となる。これを防止するために組織培養装置(CO2インキュベーター)にCO2ガスを供給することでNa2CO3はNaHCO3に戻り、培養液中のpHは7.1から7.4にて平衡化することが可能となる。
湿度は、組織培養装置内のCO2ガスを培養フラスコに供給するために培養フラスコの蓋を閉めずに空気の出入りがあるよう、緩めておく必要がある。この時培養フラスコよりメディウムの水分が蒸発することで、培地の塩濃度が変わり細胞培養環境に著しい影響をおよぼす。この乾燥を防ぐ目的で、組織培養装置(CO2インキュベーター)の内部を加湿する必要がある。
通常の加湿方法は、組織培養装置(CO2インキュベーター)内のバットに水を入れ自然蒸発にて培養装置内を過飽和状態にするのが一般的である。しかし組織培養温度条件が37℃であるため、バットに入っている水は通常カビや細菌に汚染されている。組織培養フラスコ中には、細胞の増殖に必要な栄養成分を多く含んでおり、これら雑菌が培養フラスコに混入することで重大な汚染を発生させ、動物細胞を死滅させる危険がある。
通常の加湿方法は、組織培養装置(CO2インキュベーター)内のバットに水を入れ自然蒸発にて培養装置内を過飽和状態にするのが一般的である。しかし組織培養温度条件が37℃であるため、バットに入っている水は通常カビや細菌に汚染されている。組織培養フラスコ中には、細胞の増殖に必要な栄養成分を多く含んでおり、これら雑菌が培養フラスコに混入することで重大な汚染を発生させ、動物細胞を死滅させる危険がある。
また、組織培養装置(CO2インキュベーター)は、空気の流入が必要である。しかし、組織培養装置の空気吸引口と排気口から細菌、カビ等の微生物が混入し、装置内が汚染されてしまう問題があった。
よって、一般的な組織培養装置(CO2インキュベーター)の内は、空気吸引口と排気口からの混入した雑菌、蒸発バットで繁殖した雑菌、と無菌性を要求されている培養フラスコとが同居している状態である。
また、薬事法の改正により、ヒト細胞の製造に当たり、ヒト細胞も生物由来製剤と規定され医薬品の製造管理及び品質管理規制の対象となり、生物由来製剤としての安産性の確保について、より安全で厳格な実施を求められている。
「生物由来製剤としての安産性の確保」には、GLP(Good Laboratory Practice )医薬品の開発において試験データーの信頼性を求めるためのガイドラインや,GMP(Good Manufacturing Practice)医薬品の製造管理及び品質管理基準を考慮した組織培養方法が求められる。
「生物由来製剤としての安産性の確保」には、GLP(Good Laboratory Practice )医薬品の開発において試験データーの信頼性を求めるためのガイドラインや,GMP(Good Manufacturing Practice)医薬品の製造管理及び品質管理基準を考慮した組織培養方法が求められる。
以上により、組織培養装置内の加湿水による汚染、空気吸引口と排気口からの雑菌の混入の防止対策が重要な課題となっている(特許文献1)。
PCT/JP03/06994
本発明の課題は、組織培養に際し、培養装置内の雰囲気を加湿するに際し、加湿にともなう微生物汚染を容易に防止するための新規な湿度供給容器を提供することである。
本発明は、
「1.気密性を有する基材によって調製された水を担持する袋体であって、その袋体の一部に通気性、透湿性を有しかつバクテリアバリア性の膜状基材によって調製された湿度供給部を有する袋状湿度供給容器。
2.湿度供給状態におかれるまで、湿度供給部による袋体に担持された水による透湿性が阻止された前項1の袋状湿度供給容器。
3.湿度供給部の透湿性の阻止が、湿度供給部の袋体外面を気密性を有する基材のシールで覆うことによって達成される前項2の袋状湿度供給容器。
4.湿度供給部の透湿性の阻止が、袋状湿度供給容器を要時統合可能な条件で2分割し、一方の空隙に水の担持、他方の空隙の袋体に湿度供給部を設ける前項3の袋状湿度供給容器。
5.要時統合可能な条件で2分割する手段が、袋体の両面の熱融着による前項4の袋状湿度供給容器。
6.担持される水が、滅菌処理されている前項1〜5の何れか一に記載の袋状湿度供給容器。
7.容器全体が、ガンマ線照射により滅菌処理される前項1〜6の何れか一に記載の袋状湿度供給容器。
8.袋状湿度供給容器が、気密性を有する基材によって調製された外袋内に装填される2重袋状態にある前項1〜7の何れか一に記載の袋状湿度供給容器。
9.湿度供給部が、高密度エチレン系の不織布によって構成される前項1〜8の何れか一に記載の容器。
10.高密度エチレン系の不織布が、0.5〜10ミクロンの口径のポリエチレンの連続性極細繊維に高熱を加えて結合、調製されたタイベック(登録商標)である前項9に記載の容器 。
11.気密性を有する基材が、プラスチック樹脂である前項1〜10の何れか一に記載の容器。
12.前項2〜11の何れか一に記載の袋状湿度供給容器の湿度供給部における袋体に担持された水による透湿性の阻止を開放し、透湿性を可能にし、この袋状湿度供給容器を用いて組織培養装置内を加湿する方法。
13.前項12の方法を用いる組織培養方法。
14.以下の手段を備えた組織培養システム;
1)組織培養装置への湿度供給手段であって、組織培養装置内の湿度を過飽和状態に保つために約37℃の温度条件下で水の自然蒸発が可能である、前項1〜11の何れか一に記載の袋状湿度供給容器の設置による湿度の供給。
2)組織培養装置の空気吸引口と排気口からの雑菌混入防止手段として、装置の空気吸引口と排気口に、溶菌酵素を固定化した細菌透過制御性の膜の設置による空気の供給及び排出。」からなる。
「1.気密性を有する基材によって調製された水を担持する袋体であって、その袋体の一部に通気性、透湿性を有しかつバクテリアバリア性の膜状基材によって調製された湿度供給部を有する袋状湿度供給容器。
2.湿度供給状態におかれるまで、湿度供給部による袋体に担持された水による透湿性が阻止された前項1の袋状湿度供給容器。
3.湿度供給部の透湿性の阻止が、湿度供給部の袋体外面を気密性を有する基材のシールで覆うことによって達成される前項2の袋状湿度供給容器。
4.湿度供給部の透湿性の阻止が、袋状湿度供給容器を要時統合可能な条件で2分割し、一方の空隙に水の担持、他方の空隙の袋体に湿度供給部を設ける前項3の袋状湿度供給容器。
5.要時統合可能な条件で2分割する手段が、袋体の両面の熱融着による前項4の袋状湿度供給容器。
6.担持される水が、滅菌処理されている前項1〜5の何れか一に記載の袋状湿度供給容器。
7.容器全体が、ガンマ線照射により滅菌処理される前項1〜6の何れか一に記載の袋状湿度供給容器。
8.袋状湿度供給容器が、気密性を有する基材によって調製された外袋内に装填される2重袋状態にある前項1〜7の何れか一に記載の袋状湿度供給容器。
9.湿度供給部が、高密度エチレン系の不織布によって構成される前項1〜8の何れか一に記載の容器。
10.高密度エチレン系の不織布が、0.5〜10ミクロンの口径のポリエチレンの連続性極細繊維に高熱を加えて結合、調製されたタイベック(登録商標)である前項9に記載の容器 。
11.気密性を有する基材が、プラスチック樹脂である前項1〜10の何れか一に記載の容器。
12.前項2〜11の何れか一に記載の袋状湿度供給容器の湿度供給部における袋体に担持された水による透湿性の阻止を開放し、透湿性を可能にし、この袋状湿度供給容器を用いて組織培養装置内を加湿する方法。
13.前項12の方法を用いる組織培養方法。
14.以下の手段を備えた組織培養システム;
1)組織培養装置への湿度供給手段であって、組織培養装置内の湿度を過飽和状態に保つために約37℃の温度条件下で水の自然蒸発が可能である、前項1〜11の何れか一に記載の袋状湿度供給容器の設置による湿度の供給。
2)組織培養装置の空気吸引口と排気口からの雑菌混入防止手段として、装置の空気吸引口と排気口に、溶菌酵素を固定化した細菌透過制御性の膜の設置による空気の供給及び排出。」からなる。
本発明は、極めて効率的に微生物汚染制御状態で加湿処理及び空気の流入手段を提供でき、組織培養の実用上に極めて有用である。
本発明の一は、気密性を有する基材によって調製された水を担持する袋体であって、その袋体の一部に通気性、透湿性を有しかつバクテリアバリア性の膜状基材によって調製された湿度供給部を有する袋状湿度供給容器である。
本発明の特徴の一つは、湿度供給容器を袋状(バッグ状)にしたことである。これにより予め滅菌処理された水を含む湿度供給容器を、使用前はシート状に積み重ねて保存、運搬が可能であり、容易に流通に供することが可能になった。使用者は、滅菌状態で密閉された湿度供給容器を要時開放し、所望の装置例えば組織培養装置内で無菌の状態で湿度の供給を可能にする。
本発明の基本的な袋体は、気密性を有する基材によって調製された水を担持する袋体である。気密性を有する基材とは、通気性と透湿性がなく、バクテリアバリア性を有する基材を意味する。この材料としては、広くプラスチック容器として知られる熱可塑性の各種樹脂が使用できる。例えばポリ塩化ビニル系素材、ポリエチレン系素材、ポリプロピレン系素材、EVA系素材、ポリスチレン系素材等が用いられ、好適にはポリエチレン系素材が用いられる。ポリエチレン系素材は特に現在製造・市販されているものであれば特に限定されないが、好ましくは気密性を有し、ガンマー線照射に耐性があるものが好適である。
袋体の中に充填する水は、充填前に細菌の死滅条件下で加熱滅菌されていることが好ましい。また、袋体の中に充填後に湿度供給容器全体として滅菌処理をしてもよい。その場合、プラスチック容器は、60℃10時間から110℃1〜5分の加熱に耐えるものであれば適用可能である。
本発明において、通気性、透湿性を有しかつバクテリアバリア性の膜状基材によって調製された湿度供給部とは、通気性と透湿性を有することで、袋内に担持される水から蒸発される湿度成分が組織培養装置内に通過可能であることを意味する。さらに、該湿度供給部は少なくとも細菌、カビ等の微生物の通過を阻止しうるものであることが必須である。湿度供給部は、薄膜状体になっており、その面積は、湿度が組織培養室内に湿度成分が効率的にすみやかに供給可能なことが必要である。この膜状体としては、高密度エチレン系の不織布が市販されており、これを用いて加工すれば容易に目的は達成可能である。高密度エチレン系の不織布は、例えば0.5〜10ミクロンの口径のポリエチレンの連続性極細繊維に高熱を加えて結合、調製されたものである。市販品としては、例えば、タイベック(デュポン社の登録商標)が例示される。タイベック(登録商標)は、高密度ポリエチレン100%の不織布であり、通気性、透湿性にすぐれている。また、優れたバクテリアバリア性を持ちASTMF1608-95法(米国材料試験協会)によるバクテリア芽胞の浸透抵抗性テストでは、LRV5.7(Log10N0-Log10N1:N0=細菌投与量、N1=細菌透過量)、バクテリア浸透抵抗99.999%を示している。本発明において使用に好適な湿度供給部に使用する膜状基材は、タイベック(登録商標)のメディカル用途の1059B、1073B(品番号:デュポンタイベック総合技術資料参照)が好適である。
バクテリアバリア性とは、細菌、カビ等の微生物が、例え袋体内に担持された水に夾雑していても、これらを通過させないことを意味する。通気性と透湿性を有するとは、蒸発水分の通過は可能とする性質を意味する。このような性質を有する膜状基材は、水分供給効果と除菌の完全性の効率を判断して例えばタイベック(デュポン社の登録商標)の品番を変更することで、随時変更可能である。
本発明の袋状湿度供給容器は、湿度供給状態におかれるまで、湿度供給部による袋体に担持された水による透湿性が阻止されたものであることが好ましい。湿度供給状態におかれるとは、例えば組織培養室内で、室内の湿度供給がされる状態をいう。湿度供給部による袋体に担持された水による透湿性が阻止されたとは、袋体に担持された水が湿度供給部と接触しても、湿度供給部を介した水の透湿性の阻止、つまり水成分の膜通過がされないことを意味する。その手段は、湿度供給部を介した水の透湿性の阻止を可能とする限り特に限定されない。
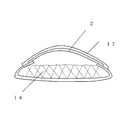
水の透湿性の阻止のためには、例えば湿度供給部(図5の2)の袋体外面を気密性を有する基材のシール(図5の17)で覆うことによって達成される。シールは、湿度供給部の袋体外面部を完全に覆い、しかも大きめのものがより効果を達成できる。シールは、前記気密性を有する基材を使うことによって効率的に達成できる。シールと湿度供給部の袋体外面の接着は、広く公知の要時剥離可能な接着剤を使えば容易に達成できる。接着剤は、湿度供給部の袋体外面部の湿度供給部外周部に接着可能なように塗布してもよいし、全面塗布でもよい。また、要時剥離可能なように湿度供給部の袋体外面部の湿度供給部外周部に気密性を有する基材同士を熱融着させてもよい。融着温度及び時間の調整により、適当な剥離強度が調整可能である。なお、剥離の際の容易性を確保するためには、シールに耳部をつくり、これを開放状態にしておくことで、これを引っ張ることで剥離が容易となる。
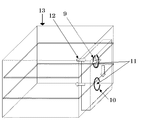
また、本発明の袋状湿度供給容器の一態様として、袋状湿度供給容器を要時統合可能な条件で2分割(図6)し、一方の空隙に水の担持(図6の14)、他方の空隙(図6の16)の袋体に湿度供給部(図6の2)を設けることができる。要時統合可能な条件で2分割するとは、所謂ダブルバッグであって、湿度供給状態に至るまでは、湿度供給部の空瞭側には水が担持されておらず、湿度供給状態にする時に、2分割されたバッグを一体化し、湿度供給部の空瞭側に水が移動し、結果湿度供給部を介した透湿性によって湿度の供給がなされるのである。そして、要時統合可能な条件で2分割する手段は、例えば袋体の横手方向に袋体の両内面を要時剥離可能な強度の熱融着(図6お15)をすることによって達成できる。剥離強度は、材質に応じた温度及び処理時間によって適宜調整可能である。なお、このような熱融着による場合、使用前の事故による剥離を排除するためには、融着部における袋体の重ね折をしておくことは有利である。
また、2分割のためには、融着によらず単なる物理的圧接であってもよい。簡便には、袋体外部両面を挟み具によって挟み込むことによっても達成できる。
また、2分割のためには、融着によらず単なる物理的圧接であってもよい。簡便には、袋体外部両面を挟み具によって挟み込むことによっても達成できる。
本発明の気密性を有する基材によって調製された水を担持する袋体は、滅菌処理された水を袋体に充填後、容器の口部を例えばシーラーにて熱着することで密封状況を作り出す。密封状況は必ずしも熱着法だけでなく、物理的な折り曲げ、粘着剤を用いた密着、或はチャック方式を組み合わせて密封状態を確保してもよい。
水を充填された本発明の袋体は、容器全体を滅菌処理に施す。滅菌方法は、エチレンオキサイド処理、ガンマー線照射、蒸気滅菌等公知の滅菌方法を適用できる。好適には、ガンマー線照射が推奨される。かくして、本発明の水が充填された袋状湿度供給容器は完全滅菌された状態となる。
水を充填された本発明の袋体は、容器全体を滅菌処理に施す。滅菌方法は、エチレンオキサイド処理、ガンマー線照射、蒸気滅菌等公知の滅菌方法を適用できる。好適には、ガンマー線照射が推奨される。かくして、本発明の水が充填された袋状湿度供給容器は完全滅菌された状態となる。
さらに本発明では、袋状湿度供給容器を、通気性及び透湿性を排除し、バクテリアバリア性をも担持した外袋内に装填し、外袋−内袋からなる2重袋のような形態で滅菌密封して製品化すれば要時使用可能な組織培養用湿度供給用キットとなる。外袋の密封には、熱着法だけでなく、物理的な折り曲げ、粘着剤を用いた密着、或はチャック方式を組み合わせて密封状態を確保してもよい。また、滅菌は、2重袋として密封後に、ガンマー線照射等によって行うことが効率的である。
本発明は、上記のように調製した袋状湿度供給容器の湿度供給部における袋体に担持された水による透湿性の阻止を開放し、透湿性を可能にすることで、この袋状湿度供給容器を用いて組織培養装置内を加湿する方法を提供する。水による透湿性の阻止を開放及び透湿性を可能にすることとは、前記の定義に準ずる。そしてこの組織培養装置内を加湿する方法は、組織培養方法として有用である。
さらに本発明は、以下の手段を備えた組織培養システムを提供する。その一の手段とは、組織培養装置への湿度供給手段であって、組織培養装置内の湿度を過飽和状態に保つために約37℃の温度条件下で水の自然蒸発が可能である、上記に記載の袋状湿度供給容器の透湿性が開放されたものを据え置きすることによる湿度の供給をすることである。水が無菌状態の水蒸気となって組織培養装置内に拡散され、組織培養装置内が湿度過飽和状態が保持される結果、組織培養が好適に行われる。
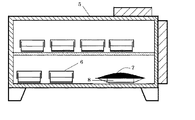
そしてその他の手段は、組織培養装置の空気吸引口と排気口からの雑菌混入防止手段として、装置の空気吸引口と排気口に、溶菌酵素を固定化した細菌透過制御性の膜の設置による空気の供給及び排出を可能とすることである。本発明における微生物汚染制御状態で空気循環可能な組織培養装置を図4にその一例を示す。該装置(13)は、空気吸引口(10)と排気口(9)に、溶菌酵素を固定化した細菌透過制御性の膜(11)が設置される。細菌透過制御性の膜とは、細菌、カビ等の微生物が、これらを通過しない口径であるが、空気の通過は可能とする膜を意味する。その膜の口径は一般的な除菌膜の口径である0.45好ましくは0.2ミクロン以下が好適である。本膜には、溶菌酵素が、空気中に通常存在する微生物を対象として溶菌スペクトルが設計され選択され、固定化される。固定化手段は、無機質と有機質を結びつける一般的なシランカップリング剤でおこなわれるが、これに限定されない。市販の溶菌酵素を固定化した殺菌・酵素フィルターとしては近藤化学工業株式会社のものがある。このような膜を使えば、微生物がフィルターに捕捉された後、捕捉された微生物を酵素の作用で溶菌をしてしまうので装置内の汚染がより確実に簡便に防止が可能となる。また、詳しくはPCT/JP03/06994記載の組織培養装置を参照することができる。
以下、本発明を実施例によりさらに具体的に説明するが、下記の実施例は本発明についての具体的認識を得る一助とみなすべきものであり、本発明の範囲は下記の実施例により何ら限定されるものではない。
(実施例1)
(実施例1)
袋状湿度供給容器の構成
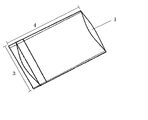
図1、2は、本発明に係る袋状水分保持具保存容器の一例を示す。図1では、湿度供給部位が背面図、図2では湿度供給部位(2)が正面図である。袋状湿度供給容器は、長方形型であり、水を充填可能な口部(1)を有する袋体形状である。袋状湿度供給容器の縦の長さ(3)は、約20cm、横の長さ(4)は約30cmである。しかし、組織培養装置内の容積と組織培養する細胞の用途に合わせて、適宜縦の長さ(3)、横の長さ(4)を調節することができる。また、湿度供給部(2)は、通気性、透湿性を有しかつバクテリアバリア性のタイベックで構成され、その他の部分は気密性を有するポリエチレン系素材で構成されている。袋状湿度供給容器の作成方法は、タイベックとポリエチレン系素材の周縁部同士を接合して袋体を形成するが、水を充填可能な口部(1)を有するために一方向を接合しないことにより達成できるが、これらに限定されることはなく、本発明に係るの構成を達成できる方法である限りは特に限定されない。また、タイベックとポリエチレン系素材の周縁部同士を接合する方法は、自体公知の接着剤(
)を使っておこなった。
別の実施例(図6)として、縦長の袋状湿度供給容器の一方の閉鎖側に湿度供給部(2)を設け、該湿度供給部を含まない縦長の袋状湿度供給容器略中心部付近で横手方向に袋状湿度供給容器の内壁面同士を熱融着(15)し、縦長の袋状湿度供給容器を2分割した。そして、他方の開放口(1)を有する端部から滅菌水(14)を充填し、その後該開放口を熱融着で閉鎖し、ダブルバッグ構造の袋状湿度供給容器を提供した。
さらに別の実施例(図5)として、縦長の袋状湿度供給容器の片面側に湿度供給部(2)を設け、この湿度供給部を完全に覆うかたちで気密性を有するポリエチレン系素材の薄膜(17)を要時剥離可能に接着させた。その後、袋状湿度供給容器の開放口から滅菌水(14)を充填し、さらに該開放口を熱融着で閉鎖し、ワンバッグ構造の袋状湿度供給容器を提供した。以上のように調製された袋状湿度供給容器は、さらに所望により、気密性を有するポリエチレン系素材の外袋内に装填し、開放口を閉鎖後、全体をγ線照射し、滅菌処理を施した。
(実施例2)
図1、2は、本発明に係る袋状水分保持具保存容器の一例を示す。図1では、湿度供給部位が背面図、図2では湿度供給部位(2)が正面図である。袋状湿度供給容器は、長方形型であり、水を充填可能な口部(1)を有する袋体形状である。袋状湿度供給容器の縦の長さ(3)は、約20cm、横の長さ(4)は約30cmである。しかし、組織培養装置内の容積と組織培養する細胞の用途に合わせて、適宜縦の長さ(3)、横の長さ(4)を調節することができる。また、湿度供給部(2)は、通気性、透湿性を有しかつバクテリアバリア性のタイベックで構成され、その他の部分は気密性を有するポリエチレン系素材で構成されている。袋状湿度供給容器の作成方法は、タイベックとポリエチレン系素材の周縁部同士を接合して袋体を形成するが、水を充填可能な口部(1)を有するために一方向を接合しないことにより達成できるが、これらに限定されることはなく、本発明に係るの構成を達成できる方法である限りは特に限定されない。また、タイベックとポリエチレン系素材の周縁部同士を接合する方法は、自体公知の接着剤(
)を使っておこなった。
別の実施例(図6)として、縦長の袋状湿度供給容器の一方の閉鎖側に湿度供給部(2)を設け、該湿度供給部を含まない縦長の袋状湿度供給容器略中心部付近で横手方向に袋状湿度供給容器の内壁面同士を熱融着(15)し、縦長の袋状湿度供給容器を2分割した。そして、他方の開放口(1)を有する端部から滅菌水(14)を充填し、その後該開放口を熱融着で閉鎖し、ダブルバッグ構造の袋状湿度供給容器を提供した。
さらに別の実施例(図5)として、縦長の袋状湿度供給容器の片面側に湿度供給部(2)を設け、この湿度供給部を完全に覆うかたちで気密性を有するポリエチレン系素材の薄膜(17)を要時剥離可能に接着させた。その後、袋状湿度供給容器の開放口から滅菌水(14)を充填し、さらに該開放口を熱融着で閉鎖し、ワンバッグ構造の袋状湿度供給容器を提供した。以上のように調製された袋状湿度供給容器は、さらに所望により、気密性を有するポリエチレン系素材の外袋内に装填し、開放口を閉鎖後、全体をγ線照射し、滅菌処理を施した。
(実施例2)
落下菌のコロニー数による袋状湿度供給容器(以下加湿バッグと記載)の性能試験(コンタミ試験)
加湿バックに無菌的に水を入れ、後天的に雑菌が混入するかどうかと、混入するとしたらどのくらいの期間で混入するのかを検討した。手を洗い、手袋を着用し、更に70%エタノール処理してからインキュベーター内を70%をエタノールで殺菌処理した。実験条件は、加湿バックを入れるインキュベーター内の条件として、37℃、CO2濃度5%に調整した。サンプリングしたシャーレを培養する温度は27℃である。
加湿バックに無菌的に水を入れ、後天的に雑菌が混入するかどうかと、混入するとしたらどのくらいの期間で混入するのかを検討した。手を洗い、手袋を着用し、更に70%エタノール処理してからインキュベーター内を70%をエタノールで殺菌処理した。実験条件は、加湿バックを入れるインキュベーター内の条件として、37℃、CO2濃度5%に調整した。サンプリングしたシャーレを培養する温度は27℃である。
対象実験1の方法は、以下のようにおこなった。インキュベーター内において、バットと加湿バックと無菌性能を比較するための実験をおこなった。乾燥処理した滅菌シャーレに減菌水を入れ、37℃のインキュベーターへ入れた後、蓋を開けた。3日後、これをサンプリングし、1週間寒天培地上27℃で培養した。更に2日後にサンプリングし、その後、一週間毎に雑菌が生えるまでサンプリングした。
対象実験2の方法は、以下のようにおこなった。無菌操作の正確性を証明するため、クリーンベンチ内で滅菌水をサンプリングし、一週間寒天培地上27℃で培養した。このサンプリングの操作は毎回の加湿バックのサンプリング時に行った。
加湿バックによるコンタミ試験、以下のようにおこなった。加湿バック内の水が無菌状態であることを確かめるためにインキュベーターに入れる前にサンプリングを行い、一週間寒天培地上27℃で培養した。インキュベーターへ入れた後、雑菌が生えるまで一週間毎にサンプリングを繰り返した。
対象実験2の方法は、以下のようにおこなった。無菌操作の正確性を証明するため、クリーンベンチ内で滅菌水をサンプリングし、一週間寒天培地上27℃で培養した。このサンプリングの操作は毎回の加湿バックのサンプリング時に行った。
加湿バックによるコンタミ試験、以下のようにおこなった。加湿バック内の水が無菌状態であることを確かめるためにインキュベーターに入れる前にサンプリングを行い、一週間寒天培地上27℃で培養した。インキュベーターへ入れた後、雑菌が生えるまで一週間毎にサンプリングを繰り返した。
(実験例1)
コンタミ試験として、加湿バック内の水が無菌状態であることを確かめるためにインキュベーターに入れる前に、手袋をし、エタノール消毒した手で、無菌的に400μlサンプリングした。これを一週間寒天培地上27℃で培養した。サンプリングの後、加湿バックをインキュベーターへ入れた。サンプリングの方法は、滅菌済みのシリンジにより、1ml抜き取り滅菌済みエッペンチューブへ入れることによっておこなった。そこから400μlとり、寒天培地へまいた。加湿バックはシーラーでシールして水漏れが無いことを確認してからサンプリング個所を70%エタノール処理を行った後、インキュベーターへ入れた。
対象実験1として、無菌的に滅菌シャーレに滅菌水を入れ蓋をせずに37℃のインキュベーターへ入れた。3日後、これを400μlサンプリングし、1週間寒天培地上27℃で培養した。
対象実験2として、実験操作上でコンタミが起こってないことを示すために滅菌水を400μl無菌的にサンプリングし、寒天培地上で一週間27℃で培養した。
結果:
コンタミ試験では、コンタミが見られないことから、加湿バック内の水が無菌状態であることが確認できた。対象実験1では、コンタミが見られないことから、インキュベーター内がまだ汚染されていないと考えられた。対象実験3では、コンタミが見られないことから、実験上の操作でコンタミが起こっていないことが確認できた。
コンタミ試験として、加湿バック内の水が無菌状態であることを確かめるためにインキュベーターに入れる前に、手袋をし、エタノール消毒した手で、無菌的に400μlサンプリングした。これを一週間寒天培地上27℃で培養した。サンプリングの後、加湿バックをインキュベーターへ入れた。サンプリングの方法は、滅菌済みのシリンジにより、1ml抜き取り滅菌済みエッペンチューブへ入れることによっておこなった。そこから400μlとり、寒天培地へまいた。加湿バックはシーラーでシールして水漏れが無いことを確認してからサンプリング個所を70%エタノール処理を行った後、インキュベーターへ入れた。
対象実験1として、無菌的に滅菌シャーレに滅菌水を入れ蓋をせずに37℃のインキュベーターへ入れた。3日後、これを400μlサンプリングし、1週間寒天培地上27℃で培養した。
対象実験2として、実験操作上でコンタミが起こってないことを示すために滅菌水を400μl無菌的にサンプリングし、寒天培地上で一週間27℃で培養した。
結果:
コンタミ試験では、コンタミが見られないことから、加湿バック内の水が無菌状態であることが確認できた。対象実験1では、コンタミが見られないことから、インキュベーター内がまだ汚染されていないと考えられた。対象実験3では、コンタミが見られないことから、実験上の操作でコンタミが起こっていないことが確認できた。
(実験例2)
コンタミ試験として、一週間37℃のインキュベーターへ入れた加湿バックを無菌的にサンプリングし、これを一週間27℃で培養した。インキュベーターのドアの開閉時間は加湿バックを取り出すときと入れるときであわせて15秒以内とした。
対象実験1のシャーレを無菌的にサンプリングし、これを一週間27℃で培養した。
対象実験2として、実験操作上でコンタミが起こってないことを示すために滅菌水を400μl無菌的にサンプリングし、寒天培地上で一週間27℃で培養した。
結果:
コンタミ試験では、コンタミが見られないことから、一週間インキュベーターに入れた加湿バックの水はまだ汚染されていないことがわかった。対象実験1では、コンタミが見られたことから、インキュベーター内がすでに汚染されていることがわかった。それと同時に、この結果からバットの水は一週間以内でコンタミすることが考えられる。対象実験2では、コンタミが見られないことから、実験上の操作でコンタミが起こっていないことが確認できた。
コンタミ試験として、一週間37℃のインキュベーターへ入れた加湿バックを無菌的にサンプリングし、これを一週間27℃で培養した。インキュベーターのドアの開閉時間は加湿バックを取り出すときと入れるときであわせて15秒以内とした。
対象実験1のシャーレを無菌的にサンプリングし、これを一週間27℃で培養した。
対象実験2として、実験操作上でコンタミが起こってないことを示すために滅菌水を400μl無菌的にサンプリングし、寒天培地上で一週間27℃で培養した。
結果:
コンタミ試験では、コンタミが見られないことから、一週間インキュベーターに入れた加湿バックの水はまだ汚染されていないことがわかった。対象実験1では、コンタミが見られたことから、インキュベーター内がすでに汚染されていることがわかった。それと同時に、この結果からバットの水は一週間以内でコンタミすることが考えられる。対象実験2では、コンタミが見られないことから、実験上の操作でコンタミが起こっていないことが確認できた。
(実験例3)
コンタミ試験として、二週間37℃のインキュベーターへ入れた加湿バックを無菌的にサンプリングし、これを一週間27℃で培養した。ドアの開閉時間は12秒かかった。
対象実験2として、実験操作上でコンタミが起こってないことを示すために滅菌水を無菌的にサンプリングし、寒天培地上で一週間27℃で培養した。
結果:
コンタミ試験ではコンタミが見られないことから、二週間インキュベーターに入れた加湿バックの水はまだ汚染されていないことがわかった。対象実験2では、コンタミが見られないことから、実験上の操作でコンタミが起こっていないことが確認できた。
コンタミ試験として、二週間37℃のインキュベーターへ入れた加湿バックを無菌的にサンプリングし、これを一週間27℃で培養した。ドアの開閉時間は12秒かかった。
対象実験2として、実験操作上でコンタミが起こってないことを示すために滅菌水を無菌的にサンプリングし、寒天培地上で一週間27℃で培養した。
結果:
コンタミ試験ではコンタミが見られないことから、二週間インキュベーターに入れた加湿バックの水はまだ汚染されていないことがわかった。対象実験2では、コンタミが見られないことから、実験上の操作でコンタミが起こっていないことが確認できた。
(実験例4)
コンタミ試験として、三週間37℃のインキュベーターへ入れた加湿バックを無菌的にサンプリングし、寒天培地上で一週間27℃で培養した。ドアの開閉時間は12秒かかった。
対象実験2として実験操作上でコンタミが起こってないことを示すために滅菌水を無菌的にサンプリングし、寒天培地上で一周間27℃で培養した。
結果:
コンタミ試験ではコンタミが見られないことから、三週間インキュベーターに入れた加湿バックの水はまだ汚染されていないことがわかった。対象実験2では、コンタミが見られないことから、実験上の操作でコンタミが起こっていないことが確認できた。
コンタミ試験として、三週間37℃のインキュベーターへ入れた加湿バックを無菌的にサンプリングし、寒天培地上で一週間27℃で培養した。ドアの開閉時間は12秒かかった。
対象実験2として実験操作上でコンタミが起こってないことを示すために滅菌水を無菌的にサンプリングし、寒天培地上で一周間27℃で培養した。
結果:
コンタミ試験ではコンタミが見られないことから、三週間インキュベーターに入れた加湿バックの水はまだ汚染されていないことがわかった。対象実験2では、コンタミが見られないことから、実験上の操作でコンタミが起こっていないことが確認できた。
(実験例5)
コンタミ試験として、四週間37℃のインキュベーターへ入れた加湿バックを無菌的にサンプリングし、これを一週間27℃で培養した。ドアの開閉時間は14秒かかった。
対象実験2として実験操作上でコンタミが起こってないことを示すために滅菌水を無菌的にサンプリングし、寒天培地上で一週間27℃で培養した。
結果:
コンタミ試験では、コンタミが見られない。対象実験2では、コンタミが見られないことから実験操作上でのコンタミは見られなかった。
コンタミ試験として、四週間37℃のインキュベーターへ入れた加湿バックを無菌的にサンプリングし、これを一週間27℃で培養した。ドアの開閉時間は14秒かかった。
対象実験2として実験操作上でコンタミが起こってないことを示すために滅菌水を無菌的にサンプリングし、寒天培地上で一週間27℃で培養した。
結果:
コンタミ試験では、コンタミが見られない。対象実験2では、コンタミが見られないことから実験操作上でのコンタミは見られなかった。
以上のコンタミ試験は、加湿バックに無菌的に水を入れ、後天的に殺菌が混入するかどうかと、混入するとしたらどのくらいの期間で混入するのかを調べる試験であり、一週間に一度のサンプリングにより試験を行った。その結果、いずれもコンタミを否定する結果であり、本発明からなる加湿バックの有用性が確認できた。
(実施例3)
(実施例3)
袋状湿度供給容器の湿度供給能試験
実施例で調製した袋状湿度供給容器(約400mlの水を担持)を湿度供給可能な状態にし、約80リットルの密閉室内で37℃にし、湿度の過飽和状態になるまでに時間を測定した。その結果、約1.5時間で室内は湿度が過飽和状態に達し、十分な湿度供給能を保有することを確認した。
実施例で調製した袋状湿度供給容器(約400mlの水を担持)を湿度供給可能な状態にし、約80リットルの密閉室内で37℃にし、湿度の過飽和状態になるまでに時間を測定した。その結果、約1.5時間で室内は湿度が過飽和状態に達し、十分な湿度供給能を保有することを確認した。
本発明は、極めて効率的に微生物汚染制御状態で加湿処理・空気循環可能な手段を提供でき、組織培養の実用上に極めて有用である。
1 口部
2 湿度供給部
3 縦の長さ
4 横の長さ
5 組織培養装置
6 培養フラスコ
7 袋状湿度供給容器
8 水分保持具
9 空気排気口
10 空気吸引口
11 細菌透過制御性の膜
12 空気の流れ(循環)を示す
13 微生物汚染制御状態で空気循環可能な組織培養装置
14 水
15 融着部
16 空隙
17 シール
2 湿度供給部
3 縦の長さ
4 横の長さ
5 組織培養装置
6 培養フラスコ
7 袋状湿度供給容器
8 水分保持具
9 空気排気口
10 空気吸引口
11 細菌透過制御性の膜
12 空気の流れ(循環)を示す
13 微生物汚染制御状態で空気循環可能な組織培養装置
14 水
15 融着部
16 空隙
17 シール
Claims (14)
- 気密性を有する基材によって調製された水を担持する袋体であって、その袋体の一部に通気性、透湿性を有しかつバクテリアバリア性の膜状基材によって調製された湿度供給部を有する袋状湿度供給容器。
- 湿度供給状態におかれるまで、湿度供給部による袋体に担持された水による透湿性が阻止された請求項1の袋状湿度供給容器。
- 湿度供給部の透湿性の阻止が、湿度供給部の袋体外面を気密性を有する基材のシールで覆うことによって達成される請求項2の袋状湿度供給容器。
- 湿度供給部の透湿性の阻止が、袋状湿度供給容器を要時統合可能な条件で2分割し、一方の空隙に水の担持、他方の空隙の袋体に湿度供給部を設ける請求項3の袋状湿度供給容器。
- 要時統合可能な条件で2分割する手段が、袋体の両面の熱融着による請求項4の袋状湿度供給容器。
- 担持される水が、滅菌処理されている請求項1〜5の何れか一に記載の袋状湿度供給容器。
- 容器全体が、ガンマ線照射により滅菌処理される請求項1〜6の何れか一に記載の袋状湿度供給容器。
- 袋状湿度供給容器が、気密性を有する基材によって調製された外袋内に装填される2重袋状態にある請求項1〜7の何れか一に記載の袋状湿度供給容器。
- 湿度供給部が、高密度エチレン系の不織布によって構成される請求項1〜8の何れか一に記載の容器。
- 高密度エチレン系の不織布が、0.5〜10ミクロンの口径のポリエチレンの連続性極細繊維に高熱を加えて結合、調製されたタイベック(登録商標)である請求項9に記載の容器 。
- 気密性を有する基材が、プラスチック樹脂である請求項1〜10の何れか一に記載の容器。
- 請求項2〜11の何れか一に記載の袋状湿度供給容器の湿度供給部における袋体に担持された水による透湿性の阻止を開放し、透湿性を可能にし、この袋状湿度供給容器を用いて組織培養装置内を加湿する方法。
- 請求項12の方法を用いる組織培養方法。
- 以下の手段を備えた組織培養システム;
1)組織培養装置への湿度供給手段であって、組織培養装置内の湿度を過飽和状態に保つために約37℃の温度条件下で水の自然蒸発が可能である、請求項1〜11の何れか一に記載の袋状湿度供給容器の設置による湿度の供給。
2)組織培養装置の空気吸引口と排気口からの雑菌混入防止手段として、装置の空気吸引口と排気口に、溶菌酵素を固定化した細菌透過制御性の膜の設置による空気の供給及び排出。
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2004113146A JP2005295825A (ja) | 2004-04-07 | 2004-04-07 | 袋状湿度供給容器 |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2004113146A JP2005295825A (ja) | 2004-04-07 | 2004-04-07 | 袋状湿度供給容器 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| JP2005295825A true JP2005295825A (ja) | 2005-10-27 |
Family
ID=35328123
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2004113146A Withdrawn JP2005295825A (ja) | 2004-04-07 | 2004-04-07 | 袋状湿度供給容器 |
Country Status (1)
| Country | Link |
|---|---|
| JP (1) | JP2005295825A (ja) |
Cited By (7)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2008005759A (ja) * | 2006-06-29 | 2008-01-17 | Sanyo Electric Co Ltd | インキュベータ及びインキュベータ用加湿皿 |
| JP2014054298A (ja) * | 2012-09-11 | 2014-03-27 | Toppan Printing Co Ltd | 滅菌用包装袋 |
| WO2016135988A1 (ja) * | 2015-02-28 | 2016-09-01 | ワケンビーテック株式会社 | 蒸気供給用保水容器 |
| JPWO2015111544A1 (ja) * | 2014-01-24 | 2017-03-23 | パナソニックヘルスケア株式会社 | インキュベータおよびこれを備えた細胞培養システム、加湿水の供給方法 |
| JP2017123786A (ja) * | 2016-01-12 | 2017-07-20 | ヤマト科学株式会社 | 加湿用バッグおよび加湿用バッグを備えるインキュベータ |
| WO2021095848A1 (ja) * | 2019-11-14 | 2021-05-20 | 富士フイルム株式会社 | 細胞の保存又は輸送器具及び細胞の輸送方法 |
| WO2021193780A1 (ja) * | 2020-03-25 | 2021-09-30 | 日産化学株式会社 | 放射線照射された樹脂成形物 |
-
2004
- 2004-04-07 JP JP2004113146A patent/JP2005295825A/ja not_active Withdrawn
Cited By (10)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2008005759A (ja) * | 2006-06-29 | 2008-01-17 | Sanyo Electric Co Ltd | インキュベータ及びインキュベータ用加湿皿 |
| JP2014054298A (ja) * | 2012-09-11 | 2014-03-27 | Toppan Printing Co Ltd | 滅菌用包装袋 |
| JPWO2015111544A1 (ja) * | 2014-01-24 | 2017-03-23 | パナソニックヘルスケア株式会社 | インキュベータおよびこれを備えた細胞培養システム、加湿水の供給方法 |
| WO2016135988A1 (ja) * | 2015-02-28 | 2016-09-01 | ワケンビーテック株式会社 | 蒸気供給用保水容器 |
| JPWO2016135988A1 (ja) * | 2015-02-28 | 2017-12-07 | ワケンビーテック株式会社 | 蒸気供給用保水容器 |
| JP2017123786A (ja) * | 2016-01-12 | 2017-07-20 | ヤマト科学株式会社 | 加湿用バッグおよび加湿用バッグを備えるインキュベータ |
| WO2021095848A1 (ja) * | 2019-11-14 | 2021-05-20 | 富士フイルム株式会社 | 細胞の保存又は輸送器具及び細胞の輸送方法 |
| JPWO2021095848A1 (ja) * | 2019-11-14 | 2021-05-20 | ||
| JP7265645B2 (ja) | 2019-11-14 | 2023-04-26 | 富士フイルム株式会社 | 細胞の保存又は輸送器具及び細胞の輸送方法 |
| WO2021193780A1 (ja) * | 2020-03-25 | 2021-09-30 | 日産化学株式会社 | 放射線照射された樹脂成形物 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| AU2020204234B2 (en) | Medical device packaging | |
| JP7043115B2 (ja) | 細胞培養用バッグアセンブリ | |
| JP5610312B2 (ja) | 包装容器 | |
| JP5662927B2 (ja) | 包装容器 | |
| US9222066B2 (en) | Incubator and method for decontaminating incubator | |
| KR102116633B1 (ko) | 미생물 배양용 배양백 | |
| WO2021021696A1 (en) | Devices and methods for solid-state fermentation and drying of microorganisms | |
| JP2016208866A (ja) | 自動培養装置 | |
| JP2005295825A (ja) | 袋状湿度供給容器 | |
| EP4483910A2 (en) | Apparatus and method for sterilization of an artcile | |
| JP2005278565A (ja) | 無菌培養方法及び無菌培養装置 | |
| JP2005278566A (ja) | 無菌培養方法及びその装置 | |
| CN109089412A (zh) | 封装的吸收剂及其短暂激活 | |
| JP2014083002A (ja) | 密閉容器、及びそれを用いた細胞の輸送及び/又は保管方法 | |
| JP3129610U (ja) | 袋状湿度供給容器 | |
| JP2017055723A (ja) | 細胞培養容器用包装袋 | |
| JP6354935B2 (ja) | 培養作業システム | |
| JP5592080B2 (ja) | 細胞培養方法、細胞培養システム | |
| JP2005087029A (ja) | 培養装置及び培養キット | |
| GB2436199A (en) | Sterile maggot production | |
| JP2023537847A (ja) | 無菌環境を細胞培養物のインキュベーションのために確保するための装置 | |
| CN201765122U (zh) | 植物样品采集袋 | |
| WO2021119486A1 (en) | Systems, devices and methods for engineered tissue construct transport and containment | |
| JP3223795U (ja) | 蒸気供給用保水容器 | |
| JP5962430B2 (ja) | アイソレータ内への物品の搬入方法と物品収容体 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A300 | Withdrawal of application because of no request for examination |
Free format text: JAPANESE INTERMEDIATE CODE: A300 Effective date: 20070703 |