JP2005110709A - 生体組織補填材 - Google Patents
生体組織補填材 Download PDFInfo
- Publication number
- JP2005110709A JP2005110709A JP2003344709A JP2003344709A JP2005110709A JP 2005110709 A JP2005110709 A JP 2005110709A JP 2003344709 A JP2003344709 A JP 2003344709A JP 2003344709 A JP2003344709 A JP 2003344709A JP 2005110709 A JP2005110709 A JP 2005110709A
- Authority
- JP
- Japan
- Prior art keywords
- bone
- main body
- cells
- communication
- holes
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Withdrawn
Links
Images
Abstract
【課題】 付着した細胞の成長を促進するとともに幹細胞の付着性が高い生体組織補填材を提供すること。
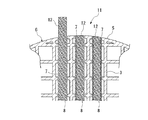
【解決手段】 本実施形態に係る骨補填材(生体組織補填材)1は、リン酸カルシウム(例えば、β−TCP)多孔体からなる足場材であって、中心軸Cに沿って一方向に延びる複数の貫通孔2を略同一厚さの隔壁部材3によって相互に区画して外周壁5で覆われるハニカム形状の本体6を備え、本体6には、一部の隔壁部材3を貫通する連通孔7が複数設けられ、本体6の外方と中央領域の貫通孔2とが複数の連通孔7を介して連通されている構成とした。
【選択図】 図1
【解決手段】 本実施形態に係る骨補填材(生体組織補填材)1は、リン酸カルシウム(例えば、β−TCP)多孔体からなる足場材であって、中心軸Cに沿って一方向に延びる複数の貫通孔2を略同一厚さの隔壁部材3によって相互に区画して外周壁5で覆われるハニカム形状の本体6を備え、本体6には、一部の隔壁部材3を貫通する連通孔7が複数設けられ、本体6の外方と中央領域の貫通孔2とが複数の連通孔7を介して連通されている構成とした。
【選択図】 図1
Description
本発明は、生体組織欠損部を再生する際に使用される生体組織補填材に関する。
近年、骨腫瘍摘出や外傷等により生じた骨等の生体組織の欠損部に、骨補填材等の生体組織補填材を補填することにより、骨を再生させて欠損部を修復することが可能になってきている。骨補填材としては、ハイドロキシアパタイト(HAP)やリン酸三カルシウム(TCP)が知られているが、体内に異物を残さないとする考え方から、例えば、β−TCPのようなリン酸カルシウム多孔体からなる足場材が使用される。β−TCPを骨欠損部の骨細胞に接触させておくと、破骨細胞がβ−TCPを食べ、骨芽細胞が新しい骨を形成する、いわゆるリモデリングが行われる。すなわち、骨欠損部に補填された骨補填材は、経時的に自家骨に置換されていくことになる。
一方、術後の骨欠損部の修復速度を高めるために、患者から採取した骨髄液に骨補填材を浸し、骨髄液に含まれる骨髄間葉系幹細胞を骨補填材とともに培養することにより製造される培養骨等の生体組織補填体を使用することが提案されている。培養されることにより骨補填材を足場にして増殖した多くの骨髄間葉系幹細胞を含む骨補填体を骨欠損部に補填するので、手術後に体内で細胞を増殖させる方法と比較すると、自家骨に置換されるまでの日数を大幅に短縮することができる(例えば、非特許文献1参照。)。
植村他2名,「生分解性β−TCP多孔材料を用いた骨におけるティッシュエンジニアリング−生体内で強度を増す新しい材料オスフェリオン−」,メディカル朝日,朝日新聞社,2001年10月1日,第三0巻,第10号,p.46−49
植村他2名,「生分解性β−TCP多孔材料を用いた骨におけるティッシュエンジニアリング−生体内で強度を増す新しい材料オスフェリオン−」,メディカル朝日,朝日新聞社,2001年10月1日,第三0巻,第10号,p.46−49
しかしながら、骨補填材として多孔体を用いても骨髄間葉系幹細胞は骨補填材表面に留まるのみとなってしまい、骨補填材内部まで骨髄間葉系幹細胞を十分に付着させることが困難であった。また、骨補填材の内部を貫通する一方向の貫通孔を形成させたものに細胞を付着させても、貫通孔の内部まで細胞の成長に必要な成分等が十分に浸透せず、一方、細胞老廃物が細胞周辺に貯留されてしまい細胞老廃物の円滑な交換や酸素供給が阻害されて骨髄間葉系幹細胞が死滅してしまう可能性があった。
本発明は上記事情に鑑みて成されたものであり、付着した細胞の成長を促進するとともに幹細胞の付着性が高い生体組織補填材を提供することを目的とする。
本発明は上記事情に鑑みて成されたものであり、付着した細胞の成長を促進するとともに幹細胞の付着性が高い生体組織補填材を提供することを目的とする。
本発明は、上記課題を解決するため、以下の手段を採用する。
本発明に係る生体組織補填材は、一方向に延びる複数の貫通孔を略同一厚さの隔壁部材によって相互に区画したハニカム形状の本体を備え、前記本体に、一部の前記隔壁部材を貫通する連通孔が複数設けられ、前記本体の外方と中央領域の前記貫通孔とが複数の前記連通孔を介して連通されていることを特徴とする。
本発明に係る生体組織補填材は、一方向に延びる複数の貫通孔を略同一厚さの隔壁部材によって相互に区画したハニカム形状の本体を備え、前記本体に、一部の前記隔壁部材を貫通する連通孔が複数設けられ、前記本体の外方と中央領域の前記貫通孔とが複数の前記連通孔を介して連通されていることを特徴とする。
この生体組織補填材は、上記の構成を備えているので、同じ体積でも大きな表面積を本体内部に得ることができ、より多くの細胞を本体内部の表面にまで付着させることができる。また、長い貫通孔であっても連通孔を通して本体内部の貫通孔まで細胞を付着させることができる。さらに、本体内部に付着させた細胞へ連通孔を通して老廃物交換や酸素供給を容易に行うことができる。
また、本発明に係る生体組織補填材は、前記生体組織補填材であって、一部の前記連通孔の中心軸が、前記本体の外方から中央領域に向けて直線上に配されていることが好ましい。
この生体組織補填材は、上記の構成を備えているので、本体外方と中央領域とを最短の距離で連通させることができ、細胞培養時に培養液を直接本体内部にムラ無く導入することができ、細胞への老廃物交換や酸素供給をより均等に行うことができる。
この生体組織補填材は、上記の構成を備えているので、本体外方と中央領域とを最短の距離で連通させることができ、細胞培養時に培養液を直接本体内部にムラ無く導入することができ、細胞への老廃物交換や酸素供給をより均等に行うことができる。
また、本発明に係る生体組織補填材は、前記生体組織補填材であって、前記連通孔に、多孔質部材が嵌合されていることが好ましい。
この生体組織補填材は、上記の構成を備えているので、連通孔の径が大きく細胞の付着性が低いものでも、多孔質部材を細胞の付着に好適な気孔率とすることによって細胞の付着を容易にすることができる。
この生体組織補填材は、上記の構成を備えているので、連通孔の径が大きく細胞の付着性が低いものでも、多孔質部材を細胞の付着に好適な気孔率とすることによって細胞の付着を容易にすることができる。
本発明によれば、初期の圧縮強度が必要な大きな骨欠損の部位に使用することができる。また、一方向の貫通孔のみならず外周壁からの複数の連通孔によって、生体組織補填材内部全体まで細胞が入りやすくなり、内部に付着させた細胞の老廃物交換が容易にできるため、細胞の成長を促進させることができる。
さらに、多孔質部材が複数の連通孔に嵌合されていることから、細胞を導入する際に多孔質部材に細胞を付着させることができ、細胞の流出を極力少なくすることができる。その結果、生体組織補填材内の細胞数を多くでき、細胞が成長することによって早期に生体組織に置換させることができる。
さらに、多孔質部材が複数の連通孔に嵌合されていることから、細胞を導入する際に多孔質部材に細胞を付着させることができ、細胞の流出を極力少なくすることができる。その結果、生体組織補填材内の細胞数を多くでき、細胞が成長することによって早期に生体組織に置換させることができる。
本発明に係る第1の実施形態について、図1から図3を参照しながら説明する。
本実施形態に係る骨補填材(生体組織補填材)1は、リン酸カルシウム(例えば、β−TCP)多孔体からなる足場材であって、中心軸Cに沿って一方向に延びる複数の貫通孔2を略同一厚さの隔壁部材3によって相互に区画して外周壁5で覆われるハニカム形状の本体6を備え、本体6には、一部の隔壁部材3を貫通する連通孔7が複数設けられ、本体6の外方と中央領域Aの貫通孔2とが複数の連通孔7を介して連通されている。
本実施形態に係る骨補填材(生体組織補填材)1は、リン酸カルシウム(例えば、β−TCP)多孔体からなる足場材であって、中心軸Cに沿って一方向に延びる複数の貫通孔2を略同一厚さの隔壁部材3によって相互に区画して外周壁5で覆われるハニカム形状の本体6を備え、本体6には、一部の隔壁部材3を貫通する連通孔7が複数設けられ、本体6の外方と中央領域Aの貫通孔2とが複数の連通孔7を介して連通されている。
本体6は、外形が円柱形状に形成されており、隔壁部材3によって貫通孔7が四角形状に区画されている。また、連通孔7は略円形状に形成されている。
本体6の中心軸Cに対して鉛直方向の、例えば断面P1上には、複数の連通孔7の中心軸が本体6の外方から中央領域に向けて直線L上に配されて仮想の連通路8が形成されており、これらが互いに平行に配されて一つの連通路群10を構成している。
連通路群10は、中心軸Cに沿って複数の断面上にそれぞれ配設されており、隣接する連通路群10の連通路8は、互いに異なる方向から中央領域Aに向かって延びている。
本体6の中心軸Cに対して鉛直方向の、例えば断面P1上には、複数の連通孔7の中心軸が本体6の外方から中央領域に向けて直線L上に配されて仮想の連通路8が形成されており、これらが互いに平行に配されて一つの連通路群10を構成している。
連通路群10は、中心軸Cに沿って複数の断面上にそれぞれ配設されており、隣接する連通路群10の連通路8は、互いに異なる方向から中央領域Aに向かって延びている。
次に、以上の構成からなる本実施形態に係る骨補填材1の製造方法について説明する。
まず、例えば、特開平5−237178号公報に開示されている方法によって、混合発泡させた水性の発泡スラリを調整したものにβ―TCPから作製した顆粒状成形体を混合してスラリ状に形成した原料を作製する。
続いて、例えば、特許第3405536号公報や特開平10−59784号公報に開示されている方法等によって押出し成形し、貫通孔2を備えるとともに外周壁5と隔壁部材3とが一体に形成されたハニカム形状の成形体を成形する。
この成形体を乾燥後、焼結炉を用いて所定の条件下で焼成して本体6を成形する。
この本体6は、長手方向に圧縮強度が15MPa以上とされる。
まず、例えば、特開平5−237178号公報に開示されている方法によって、混合発泡させた水性の発泡スラリを調整したものにβ―TCPから作製した顆粒状成形体を混合してスラリ状に形成した原料を作製する。
続いて、例えば、特許第3405536号公報や特開平10−59784号公報に開示されている方法等によって押出し成形し、貫通孔2を備えるとともに外周壁5と隔壁部材3とが一体に形成されたハニカム形状の成形体を成形する。
この成形体を乾燥後、焼結炉を用いて所定の条件下で焼成して本体6を成形する。
この本体6は、長手方向に圧縮強度が15MPa以上とされる。
この本体6に対し、例えば、ドリル加工によって、中心軸Cの鉛直方向外方から中央領域Aに向かって複数の貫通孔2を貫通するようにして外周壁5及び隔壁部材3を直線方向に貫通し、それぞれに連通孔7を形成する。この連通孔7は、細胞の付着性に好適な平均直径200μm程度とする。
このときに形成された連通孔7の中心軸は直線L上に配されるため、各連通孔7を連通する仮想の連通路8も直線状とされる。このような連通路8が互いに平行となるように断面P1上に連通路8を複数本配して連通路群10を形成する。
続いて、中心軸C上で一定間隔をおいた位置の断面P1と平行な他の断面(例えば断面P2)上に、連通路群10とは異なる方向から中央領域に向かって上述と同様の加工方法によって連通路8を加工して他の連通炉群10Aを形成する。本実施形態では、90度ずつ異なる方向から加工を行っている。
これを複数回繰り返して、骨補填材1を得る。
このときに形成された連通孔7の中心軸は直線L上に配されるため、各連通孔7を連通する仮想の連通路8も直線状とされる。このような連通路8が互いに平行となるように断面P1上に連通路8を複数本配して連通路群10を形成する。
続いて、中心軸C上で一定間隔をおいた位置の断面P1と平行な他の断面(例えば断面P2)上に、連通路群10とは異なる方向から中央領域に向かって上述と同様の加工方法によって連通路8を加工して他の連通炉群10Aを形成する。本実施形態では、90度ずつ異なる方向から加工を行っている。
これを複数回繰り返して、骨補填材1を得る。
こうして得られた骨補填材1に細胞を付与して骨補填体を作製する場合について説明する。
まず、腸骨等から骨髄液を抽出し、この骨髄液を遠心分離等の適宜の濃縮処理後、培養容器内にMEM(Minimal Essential Medium:最小必須培地)、FBS(Fetal Bovine Serum:ウシ胎児血清)等の成長因子を付加した培地を供給・混合して一次培養を行い、不要成分を除去した間葉系幹細胞を含む細胞濃縮液を作成する。
続いて、この細胞濃縮液を上述した方法によって製造した骨補填材1の全体に浸透させる。そして骨芽細胞への分化誘導因子であるデキサメタゾン等を含む骨形成培地に入れて二次培養する。
こうして、間葉系幹細胞から分化した骨芽細胞と産生された骨基質とを有し、骨形成作用が備えられた骨補填体を得る。
まず、腸骨等から骨髄液を抽出し、この骨髄液を遠心分離等の適宜の濃縮処理後、培養容器内にMEM(Minimal Essential Medium:最小必須培地)、FBS(Fetal Bovine Serum:ウシ胎児血清)等の成長因子を付加した培地を供給・混合して一次培養を行い、不要成分を除去した間葉系幹細胞を含む細胞濃縮液を作成する。
続いて、この細胞濃縮液を上述した方法によって製造した骨補填材1の全体に浸透させる。そして骨芽細胞への分化誘導因子であるデキサメタゾン等を含む骨形成培地に入れて二次培養する。
こうして、間葉系幹細胞から分化した骨芽細胞と産生された骨基質とを有し、骨形成作用が備えられた骨補填体を得る。
この骨補填材1によれば、ハニカム形状に形成されているので、同じ体積でも大きな表面積を本体6の内部に得ることができ、より多くの間葉系幹細胞を本体6内部の表面まで付着させることができる。また、貫通孔2が長い場合、連通孔7を通して本体6内部の貫通孔2まで間葉系幹細胞を付着させることができる。さらに、本体6内部に付着させた間葉系幹細胞へ連通孔7を通して老廃物交換や酸素供給を容易に行うことができ、細胞成長を増進させることができる。
また、本体6の外方と中央領域Aとを最短の距離で連通させることができ、細胞培養時に培養液を連通孔7を通して直接本体6の内部にムラ無く導入することができ、間葉系幹細胞への老廃物交換や酸素供給をより均等に行うことができる。
また、本体6の外方と中央領域Aとを最短の距離で連通させることができ、細胞培養時に培養液を連通孔7を通して直接本体6の内部にムラ無く導入することができ、間葉系幹細胞への老廃物交換や酸素供給をより均等に行うことができる。
次に、第2の実施形態について図4を参照しながら説明する。
なお、上述した第1の実施形態と同様の構成要素には同一符号を付すとともに説明を省略する。
第2の実施形態と第1の実施形態との異なる点は、第2の実施形態に係る骨補填材11の本体6の連通孔7に、多孔質部材12が嵌合されているとした点である。
多孔質部材12は、連通孔7に嵌合可能な外径を有する円柱状に形成されており、例えば気孔率が60〜80%程度とされ、本体6と同様にリン酸カルシウム(例えば、β−TCP)が主成分とされている。
なお、上述した第1の実施形態と同様の構成要素には同一符号を付すとともに説明を省略する。
第2の実施形態と第1の実施形態との異なる点は、第2の実施形態に係る骨補填材11の本体6の連通孔7に、多孔質部材12が嵌合されているとした点である。
多孔質部材12は、連通孔7に嵌合可能な外径を有する円柱状に形成されており、例えば気孔率が60〜80%程度とされ、本体6と同様にリン酸カルシウム(例えば、β−TCP)が主成分とされている。
本実施形態に係る骨補填材11の製造方法について、以下、説明する。
まず、第1の実施形態と同様の方法によって本体6を形成する。
次に、多孔質部材12を本体6の径方向外方から中央領域に向かって連通路8に嵌合させる。
こうして、骨補填材11を得る。
また、得られた骨補填材11に第1の実施形態と同様の方法によって細胞を付与して骨補填体を得る。
まず、第1の実施形態と同様の方法によって本体6を形成する。
次に、多孔質部材12を本体6の径方向外方から中央領域に向かって連通路8に嵌合させる。
こうして、骨補填材11を得る。
また、得られた骨補填材11に第1の実施形態と同様の方法によって細胞を付与して骨補填体を得る。
この骨補填材11によれば、上記第1の実施形態と同様の作用・効果を得ることができるが、本体6の連通孔7の径が、間葉系幹細胞の付着に好適な大きさである平均直径200μm程度を越えてしまったことにより付着性が低下した場合でも、間葉系幹細胞の付着に好適な気孔率を有する多孔質部材12を連通孔7に嵌合することによって、骨補填材11に対して間葉系幹細胞の付着を容易に行うことができる。
なお、本発明の技術範囲は上記実施の形態に限定されるものではなく、本発明の趣旨を逸脱しない範囲において種々の変更を加えることが可能である。
例えば、本体は円柱状に限らず、角柱形状であっても構わない。また、貫通孔の形状は四角形状に限られず、ハニカム形状である六角形や、三角形、或いは円形でも構わない。さらに、各貫通孔の大きさは均一である必要はなく、不均一な大きさであっても構わない。
また連通孔の加工はドリル加工等の機械加工に限らず、高温で溶ける円柱状の樹脂を貫通孔に対して垂直方向に立設してハニカム成形体を形成し、その後乾燥・焼結することによって、樹脂を溶融除去することによって連通孔を形成しても構わない。
例えば、本体は円柱状に限らず、角柱形状であっても構わない。また、貫通孔の形状は四角形状に限られず、ハニカム形状である六角形や、三角形、或いは円形でも構わない。さらに、各貫通孔の大きさは均一である必要はなく、不均一な大きさであっても構わない。
また連通孔の加工はドリル加工等の機械加工に限らず、高温で溶ける円柱状の樹脂を貫通孔に対して垂直方向に立設してハニカム成形体を形成し、その後乾燥・焼結することによって、樹脂を溶融除去することによって連通孔を形成しても構わない。
また、体液は、骨髄液に限らず、末梢血、さい帯血でも良く、ES細胞、体性幹細胞、骨細胞、軟骨細胞、神経細胞等の体細胞が含まれるものであれば良い。生体組織も、骨組織のみならず、軟骨組織、筋肉組織、あるいは皮下組織等任意の生体組織を再生するために利用することも可能である。
生体組織補填材としても、生体組織に親和性のある材料なら何でも良く、生体吸収性の材料なら更に良い。多孔体でも良い。
多孔体としては、β―TCPのみならず、スラリを形成することができるものであれば、リン酸カルシウム系セラミックス、コラーゲン、ヒアルロン酸等の天然高分子、ポリ乳酸、ポリグリコール酸等の合成高分子やこれらを組み合わせたものでも構わない。
生体組織補填材としても、生体組織に親和性のある材料なら何でも良く、生体吸収性の材料なら更に良い。多孔体でも良い。
多孔体としては、β―TCPのみならず、スラリを形成することができるものであれば、リン酸カルシウム系セラミックス、コラーゲン、ヒアルロン酸等の天然高分子、ポリ乳酸、ポリグリコール酸等の合成高分子やこれらを組み合わせたものでも構わない。
上記の実施形態に係る骨補填材を用いて、骨補填体としてラットの培養骨を作製した。
まず、ラットから骨髄液を抽出し、T型フラスコで10日間一次培養を行うことによって不要成分を除去した骨髄間葉系幹細胞を含む培養細胞を生成した。
一方、本実施形態に係る骨補填材を培養液、PBS(リン酸緩衝液)、生理食塩水等に浸漬する。
上記培養細胞をトリプシン処理後、骨補填材に播種する。培地にMEM、FBSの他にデキサメタゾンを混合して幹細胞の分化を開始しさらに2週間程度二次培養した。
こうして、骨髄間葉系幹細胞から分化した骨芽細胞を備える骨補填体を得た。
この骨補填体をラットの皮下に移植し、4週間後に再び取り出したところ、新しい骨組織の形成を確認することができた。
まず、ラットから骨髄液を抽出し、T型フラスコで10日間一次培養を行うことによって不要成分を除去した骨髄間葉系幹細胞を含む培養細胞を生成した。
一方、本実施形態に係る骨補填材を培養液、PBS(リン酸緩衝液)、生理食塩水等に浸漬する。
上記培養細胞をトリプシン処理後、骨補填材に播種する。培地にMEM、FBSの他にデキサメタゾンを混合して幹細胞の分化を開始しさらに2週間程度二次培養した。
こうして、骨髄間葉系幹細胞から分化した骨芽細胞を備える骨補填体を得た。
この骨補填体をラットの皮下に移植し、4週間後に再び取り出したところ、新しい骨組織の形成を確認することができた。
1、11 骨補填材(生体組織補填材)
2 貫通孔
3 隔壁部材
6 本体
7 連通孔
12 多孔質部材
2 貫通孔
3 隔壁部材
6 本体
7 連通孔
12 多孔質部材
Claims (3)
- 一方向に延びる複数の貫通孔を略同一厚さの隔壁部材によって相互に区画したハニカム形状の本体を備え、
前記本体に、一部の前記隔壁部材を貫通する連通孔が複数設けられ、前記本体の外方と中央領域の前記貫通孔とが複数の前記連通孔を介して連通されていることを特徴とする生体組織補填材。 - 一部の前記連通孔の中心軸が、前記本体の外方から中央領域に向けて直線上に配されていることを特徴とする請求項1に記載の生体組織補填材。
- 前記連通孔に、多孔質部材が嵌合されていることを特徴とする請求項1又は2に記載の生体組織補填材。
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2003344709A JP2005110709A (ja) | 2003-10-02 | 2003-10-02 | 生体組織補填材 |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2003344709A JP2005110709A (ja) | 2003-10-02 | 2003-10-02 | 生体組織補填材 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| JP2005110709A true JP2005110709A (ja) | 2005-04-28 |
Family
ID=34538255
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2003344709A Withdrawn JP2005110709A (ja) | 2003-10-02 | 2003-10-02 | 生体組織補填材 |
Country Status (1)
| Country | Link |
|---|---|
| JP (1) | JP2005110709A (ja) |
Cited By (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2007063820A1 (ja) | 2005-12-02 | 2007-06-07 | Sunstar Suisse Sa | エレクトロスピニング法により形成された生体適合性のナノ又はマイクロファイバー不織布を有する生体適合材、及びその製造方法 |
| WO2018061846A1 (ja) | 2016-09-27 | 2018-04-05 | 富士フイルム株式会社 | 細胞組織の製造方法、及び多孔フィルム |
| WO2018074429A1 (ja) | 2016-10-17 | 2018-04-26 | 国立大学法人九州大学 | 医療用ハニカム構造体 |
| JP2020515350A (ja) * | 2017-04-01 | 2020-05-28 | エイチディー ライフサイエンシズ エルエルシーHd Lifesciences Llc | インプラント用流体インターフェースシステム |
| WO2021177457A1 (ja) | 2020-03-05 | 2021-09-10 | 邦夫 石川 | 医用ハニカム構造体およびその製造方法、医用組織再建袋、成形型 |
-
2003
- 2003-10-02 JP JP2003344709A patent/JP2005110709A/ja not_active Withdrawn
Cited By (11)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2007063820A1 (ja) | 2005-12-02 | 2007-06-07 | Sunstar Suisse Sa | エレクトロスピニング法により形成された生体適合性のナノ又はマイクロファイバー不織布を有する生体適合材、及びその製造方法 |
| WO2018061846A1 (ja) | 2016-09-27 | 2018-04-05 | 富士フイルム株式会社 | 細胞組織の製造方法、及び多孔フィルム |
| US11633523B2 (en) | 2016-09-27 | 2023-04-25 | Fujifilm Corporation | Method for producing cell tissue, and porous film |
| WO2018074429A1 (ja) | 2016-10-17 | 2018-04-26 | 国立大学法人九州大学 | 医療用ハニカム構造体 |
| CN110087698A (zh) * | 2016-10-17 | 2019-08-02 | 国立大学法人九州大学 | 医疗用蜂窝结构体 |
| JPWO2018074429A1 (ja) * | 2016-10-17 | 2019-08-08 | 国立大学法人九州大学 | 医療用ハニカム構造体 |
| US11246708B2 (en) | 2016-10-17 | 2022-02-15 | Kyushu University, National University Corporation | Medical use honeycomb structure |
| JP7089284B2 (ja) | 2016-10-17 | 2022-06-22 | 国立大学法人九州大学 | 医療用ハニカム構造体 |
| JP2020515350A (ja) * | 2017-04-01 | 2020-05-28 | エイチディー ライフサイエンシズ エルエルシーHd Lifesciences Llc | インプラント用流体インターフェースシステム |
| JP7195005B2 (ja) | 2017-04-01 | 2022-12-23 | ナノハイブ メディカル エルエルシー | インプラント用流体インターフェースシステム |
| WO2021177457A1 (ja) | 2020-03-05 | 2021-09-10 | 邦夫 石川 | 医用ハニカム構造体およびその製造方法、医用組織再建袋、成形型 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| Kumar et al. | Biocompatibility and mechanical behaviour of three-dimensional scaffolds for biomedical devices: process–structure–property paradigm | |
| JP4504418B2 (ja) | 骨組織再生用生物活性人工器官装置の製造方法およびその人工器官装置 | |
| Mellor et al. | Fabrication and evaluation of electrospun, 3D-bioplotted, and combination of electrospun/3D-bioplotted scaffolds for tissue engineering applications | |
| Cordonnier et al. | Biomimetic materials for bone tissue engineering–state of the art and future trends | |
| JP4406283B2 (ja) | 組織再生用基材、移植用材料及びその製法 | |
| Whitehead et al. | High-porosity poly (ε-caprolactone)/mesoporous silicon scaffolds: calcium phosphate deposition and biological response to bone precursor cells | |
| Wang et al. | Biomimetic design strategy of complex porous structure based on 3D printing Ti-6Al-4V scaffolds for enhanced osseointegration | |
| JP2005160669A (ja) | 生体組織補填体の製造方法 | |
| JP2004008437A (ja) | 培養骨 | |
| CN213099717U (zh) | 一种具有互通微通道的牙槽骨再生材料 | |
| JP2005110709A (ja) | 生体組織補填材 | |
| KR101909328B1 (ko) | 조직 재생 컨스트럭트 및 조직 재생 컨스트럭트의 제조 방법 | |
| US10994050B2 (en) | High yield and high precision bone graft substitute from stem cells | |
| JP2004298407A (ja) | 生体組織補填材及びその製造方法 | |
| Kang et al. | Integrating Top‐Down and Bottom‐Up Scaffolding Tissue Engineering Approach for Bone Regeneration | |
| Thimm et al. | Biocompatibility studies of endothelial cells on a novel calcium phosphate/SiO2-xerogel composite for bone tissue engineering | |
| JP2006230817A (ja) | 生体組織補填材、生体組織補填体およびその製造方法 | |
| Fernandes et al. | Biopolymer‐based scaffolds for bone and tissue engineering | |
| JP2006230683A (ja) | 骨補填材、骨補填体および培養骨 | |
| JP4549016B2 (ja) | 生体用部材 | |
| JP3931134B2 (ja) | 生体組織再生用移植材とその製造方法 | |
| JP2005160668A (ja) | 生体組織補填体の製造方法 | |
| JP2004154308A (ja) | 生体組織補填材 | |
| JP2005124709A (ja) | 生体組織補填材及びその製造方法 | |
| JP4225491B2 (ja) | 軟骨形成用部材 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A300 | Withdrawal of application because of no request for examination |
Free format text: JAPANESE INTERMEDIATE CODE: A300 Effective date: 20061205 |