ES2833555T3 - Procedimiento para la preparación de una dispersión acuosa de una proteína vegetal poco dispersable - Google Patents
Procedimiento para la preparación de una dispersión acuosa de una proteína vegetal poco dispersable Download PDFInfo
- Publication number
- ES2833555T3 ES2833555T3 ES16715125T ES16715125T ES2833555T3 ES 2833555 T3 ES2833555 T3 ES 2833555T3 ES 16715125 T ES16715125 T ES 16715125T ES 16715125 T ES16715125 T ES 16715125T ES 2833555 T3 ES2833555 T3 ES 2833555T3
- Authority
- ES
- Spain
- Prior art keywords
- protein
- particles
- caseinate
- weight
- dispersion
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
- 239000006185 dispersion Substances 0.000 title claims abstract description 87
- 108010082495 Dietary Plant Proteins Proteins 0.000 title claims abstract description 52
- 238000000034 method Methods 0.000 title claims abstract description 36
- 238000002360 preparation method Methods 0.000 title claims abstract description 28
- 239000002245 particle Substances 0.000 claims abstract description 142
- 229940071162 caseinate Drugs 0.000 claims abstract description 130
- 102000004169 proteins and genes Human genes 0.000 claims abstract description 101
- 235000018102 proteins Nutrition 0.000 claims abstract description 100
- 108090000623 proteins and genes Proteins 0.000 claims abstract description 100
- 108010064851 Plant Proteins Proteins 0.000 claims abstract description 38
- 235000021118 plant-derived protein Nutrition 0.000 claims abstract description 38
- 239000012530 fluid Substances 0.000 claims abstract description 21
- 230000008569 process Effects 0.000 claims abstract description 19
- 238000011282 treatment Methods 0.000 claims abstract description 18
- 241000196324 Embryophyta Species 0.000 claims abstract description 8
- 241000209504 Poaceae Species 0.000 claims abstract description 5
- 235000007164 Oryza sativa Nutrition 0.000 claims description 40
- 235000009566 rice Nutrition 0.000 claims description 40
- 235000013339 cereals Nutrition 0.000 claims description 35
- 229940038580 oat bran Drugs 0.000 claims description 33
- 108010073032 Grain Proteins Proteins 0.000 claims description 21
- 240000008042 Zea mays Species 0.000 claims description 12
- 235000005824 Zea mays ssp. parviglumis Nutrition 0.000 claims description 12
- 235000002017 Zea mays subsp mays Nutrition 0.000 claims description 12
- 235000005822 corn Nutrition 0.000 claims description 12
- 235000007319 Avena orientalis Nutrition 0.000 claims description 11
- 244000075850 Avena orientalis Species 0.000 claims description 11
- 108010068370 Glutens Proteins 0.000 claims description 5
- 241000209140 Triticum Species 0.000 claims description 5
- 235000021307 Triticum Nutrition 0.000 claims description 5
- 244000025254 Cannabis sativa Species 0.000 claims description 3
- 240000005979 Hordeum vulgare Species 0.000 claims description 2
- 235000007340 Hordeum vulgare Nutrition 0.000 claims description 2
- 235000007238 Secale cereale Nutrition 0.000 claims description 2
- 244000082988 Secale cereale Species 0.000 claims description 2
- 240000006394 Sorghum bicolor Species 0.000 claims description 2
- 235000011684 Sorghum saccharatum Nutrition 0.000 claims description 2
- 235000021312 gluten Nutrition 0.000 claims description 2
- 240000007594 Oryza sativa Species 0.000 claims 3
- 235000013305 food Nutrition 0.000 description 48
- 239000000047 product Substances 0.000 description 39
- 241000209094 Oryza Species 0.000 description 37
- 239000000843 powder Substances 0.000 description 35
- 108010076119 Caseins Proteins 0.000 description 28
- 102000011632 Caseins Human genes 0.000 description 28
- 239000000203 mixture Substances 0.000 description 25
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 24
- IJGRMHOSHXDMSA-UHFFFAOYSA-N Atomic nitrogen Chemical compound N#N IJGRMHOSHXDMSA-UHFFFAOYSA-N 0.000 description 22
- 238000001246 colloidal dispersion Methods 0.000 description 22
- 239000005018 casein Substances 0.000 description 17
- BECPQYXYKAMYBN-UHFFFAOYSA-N casein, tech. Chemical compound NCCCCC(C(O)=O)N=C(O)C(CC(O)=O)N=C(O)C(CCC(O)=N)N=C(O)C(CC(C)C)N=C(O)C(CCC(O)=O)N=C(O)C(CC(O)=O)N=C(O)C(CCC(O)=O)N=C(O)C(C(C)O)N=C(O)C(CCC(O)=N)N=C(O)C(CCC(O)=N)N=C(O)C(CCC(O)=N)N=C(O)C(CCC(O)=O)N=C(O)C(CCC(O)=O)N=C(O)C(COP(O)(O)=O)N=C(O)C(CCC(O)=N)N=C(O)C(N)CC1=CC=CC=C1 BECPQYXYKAMYBN-UHFFFAOYSA-N 0.000 description 17
- 235000021240 caseins Nutrition 0.000 description 17
- 238000000265 homogenisation Methods 0.000 description 17
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 16
- 235000016709 nutrition Nutrition 0.000 description 13
- 235000019624 protein content Nutrition 0.000 description 13
- 239000000725 suspension Substances 0.000 description 13
- 239000011162 core material Substances 0.000 description 12
- 239000006228 supernatant Substances 0.000 description 12
- 229910052757 nitrogen Inorganic materials 0.000 description 11
- 238000005119 centrifugation Methods 0.000 description 10
- 235000013336 milk Nutrition 0.000 description 10
- 239000008267 milk Substances 0.000 description 10
- 210000004080 milk Anatomy 0.000 description 10
- 239000000126 substance Substances 0.000 description 10
- 229920002494 Zein Polymers 0.000 description 9
- 108010055615 Zein Proteins 0.000 description 9
- 150000001720 carbohydrates Chemical class 0.000 description 9
- 235000014633 carbohydrates Nutrition 0.000 description 9
- 230000000694 effects Effects 0.000 description 9
- 239000003925 fat Substances 0.000 description 9
- 235000019197 fats Nutrition 0.000 description 9
- 239000010410 layer Substances 0.000 description 9
- 239000000523 sample Substances 0.000 description 9
- 229940080237 sodium caseinate Drugs 0.000 description 9
- 239000005019 zein Substances 0.000 description 9
- 229940093612 zein Drugs 0.000 description 9
- 235000013361 beverage Nutrition 0.000 description 8
- 235000013365 dairy product Nutrition 0.000 description 8
- 239000002904 solvent Substances 0.000 description 8
- 102000014171 Milk Proteins Human genes 0.000 description 7
- 108010011756 Milk Proteins Proteins 0.000 description 7
- 238000001035 drying Methods 0.000 description 7
- 239000007788 liquid Substances 0.000 description 7
- 235000021239 milk protein Nutrition 0.000 description 7
- 238000002156 mixing Methods 0.000 description 7
- 239000007787 solid Substances 0.000 description 7
- 239000000243 solution Substances 0.000 description 7
- 238000001694 spray drying Methods 0.000 description 7
- RWRDLPDLKQPQOW-UHFFFAOYSA-N Pyrrolidine Chemical compound C1CCNC1 RWRDLPDLKQPQOW-UHFFFAOYSA-N 0.000 description 6
- HEMHJVSKTPXQMS-UHFFFAOYSA-M Sodium hydroxide Chemical compound [OH-].[Na+] HEMHJVSKTPXQMS-UHFFFAOYSA-M 0.000 description 6
- 238000002474 experimental method Methods 0.000 description 6
- JVTAAEKCZFNVCJ-UHFFFAOYSA-N lactic acid Chemical group CC(O)C(O)=O JVTAAEKCZFNVCJ-UHFFFAOYSA-N 0.000 description 6
- 235000020186 condensed milk Nutrition 0.000 description 5
- 235000020187 evaporated milk Nutrition 0.000 description 5
- 238000004519 manufacturing process Methods 0.000 description 5
- 241001465754 Metazoa Species 0.000 description 4
- 239000011575 calcium Substances 0.000 description 4
- 230000000052 comparative effect Effects 0.000 description 4
- 238000010438 heat treatment Methods 0.000 description 4
- 239000000463 material Substances 0.000 description 4
- 235000013384 milk substitute Nutrition 0.000 description 4
- 239000012071 phase Substances 0.000 description 4
- 235000000346 sugar Nutrition 0.000 description 4
- 238000012360 testing method Methods 0.000 description 4
- OYPRJOBELJOOCE-UHFFFAOYSA-N Calcium Chemical compound [Ca] OYPRJOBELJOOCE-UHFFFAOYSA-N 0.000 description 3
- GUBGYTABKSRVRQ-QKKXKWKRSA-N Lactose Natural products OC[C@H]1O[C@@H](O[C@H]2[C@H](O)[C@@H](O)C(O)O[C@@H]2CO)[C@H](O)[C@@H](O)[C@H]1O GUBGYTABKSRVRQ-QKKXKWKRSA-N 0.000 description 3
- 229910019142 PO4 Inorganic materials 0.000 description 3
- 239000002253 acid Substances 0.000 description 3
- 230000008901 benefit Effects 0.000 description 3
- 229910052791 calcium Inorganic materials 0.000 description 3
- 108010033929 calcium caseinate Proteins 0.000 description 3
- 230000001687 destabilization Effects 0.000 description 3
- 239000004310 lactic acid Substances 0.000 description 3
- 235000014655 lactic acid Nutrition 0.000 description 3
- 239000008101 lactose Substances 0.000 description 3
- 238000005259 measurement Methods 0.000 description 3
- 239000010452 phosphate Substances 0.000 description 3
- NBIIXXVUZAFLBC-UHFFFAOYSA-K phosphate Chemical compound [O-]P([O-])([O-])=O NBIIXXVUZAFLBC-UHFFFAOYSA-K 0.000 description 3
- 238000004062 sedimentation Methods 0.000 description 3
- 239000002356 single layer Substances 0.000 description 3
- 239000012265 solid product Substances 0.000 description 3
- 238000013112 stability test Methods 0.000 description 3
- 150000008163 sugars Chemical class 0.000 description 3
- 239000012134 supernatant fraction Substances 0.000 description 3
- 235000019871 vegetable fat Nutrition 0.000 description 3
- GUBGYTABKSRVRQ-XLOQQCSPSA-N Alpha-Lactose Chemical compound O[C@@H]1[C@@H](O)[C@@H](O)[C@@H](CO)O[C@H]1O[C@@H]1[C@@H](CO)O[C@H](O)[C@H](O)[C@H]1O GUBGYTABKSRVRQ-XLOQQCSPSA-N 0.000 description 2
- VTYYLEPIZMXCLO-UHFFFAOYSA-L Calcium carbonate Chemical compound [Ca+2].[O-]C([O-])=O VTYYLEPIZMXCLO-UHFFFAOYSA-L 0.000 description 2
- DGAQECJNVWCQMB-PUAWFVPOSA-M Ilexoside XXIX Chemical compound C[C@@H]1CC[C@@]2(CC[C@@]3(C(=CC[C@H]4[C@]3(CC[C@@H]5[C@@]4(CC[C@@H](C5(C)C)OS(=O)(=O)[O-])C)C)[C@@H]2[C@]1(C)O)C)C(=O)O[C@H]6[C@@H]([C@H]([C@@H]([C@H](O6)CO)O)O)O.[Na+] DGAQECJNVWCQMB-PUAWFVPOSA-M 0.000 description 2
- 208000025174 PANDAS Diseases 0.000 description 2
- 208000021155 Paediatric autoimmune neuropsychiatric disorders associated with streptococcal infection Diseases 0.000 description 2
- 240000004718 Panda Species 0.000 description 2
- 235000016496 Panda oleosa Nutrition 0.000 description 2
- CDBYLPFSWZWCQE-UHFFFAOYSA-L Sodium Carbonate Chemical compound [Na+].[Na+].[O-]C([O-])=O CDBYLPFSWZWCQE-UHFFFAOYSA-L 0.000 description 2
- CZMRCDWAGMRECN-UGDNZRGBSA-N Sucrose Chemical compound O[C@H]1[C@H](O)[C@@H](CO)O[C@@]1(CO)O[C@@H]1[C@H](O)[C@@H](O)[C@H](O)[C@@H](CO)O1 CZMRCDWAGMRECN-UGDNZRGBSA-N 0.000 description 2
- 229930006000 Sucrose Natural products 0.000 description 2
- 244000299461 Theobroma cacao Species 0.000 description 2
- 235000013351 cheese Nutrition 0.000 description 2
- 239000011248 coating agent Substances 0.000 description 2
- 238000000576 coating method Methods 0.000 description 2
- 235000013353 coffee beverage Nutrition 0.000 description 2
- 235000020247 cow milk Nutrition 0.000 description 2
- 230000007423 decrease Effects 0.000 description 2
- 238000001514 detection method Methods 0.000 description 2
- 238000005516 engineering process Methods 0.000 description 2
- 239000003797 essential amino acid Substances 0.000 description 2
- 235000020776 essential amino acid Nutrition 0.000 description 2
- 239000000706 filtrate Substances 0.000 description 2
- 238000001914 filtration Methods 0.000 description 2
- 239000012467 final product Substances 0.000 description 2
- -1 for example Chemical compound 0.000 description 2
- 230000036541 health Effects 0.000 description 2
- 230000003993 interaction Effects 0.000 description 2
- 239000012263 liquid product Substances 0.000 description 2
- 238000000386 microscopy Methods 0.000 description 2
- 235000021243 milk fat Nutrition 0.000 description 2
- 239000002105 nanoparticle Substances 0.000 description 2
- 239000003921 oil Substances 0.000 description 2
- 230000003287 optical effect Effects 0.000 description 2
- 239000002244 precipitate Substances 0.000 description 2
- 238000001556 precipitation Methods 0.000 description 2
- 238000012545 processing Methods 0.000 description 2
- 230000005855 radiation Effects 0.000 description 2
- 239000011734 sodium Substances 0.000 description 2
- 229910052708 sodium Inorganic materials 0.000 description 2
- 239000007921 spray Substances 0.000 description 2
- 239000007858 starting material Substances 0.000 description 2
- 238000003860 storage Methods 0.000 description 2
- 239000005720 sucrose Substances 0.000 description 2
- 239000008399 tap water Substances 0.000 description 2
- 235000020679 tap water Nutrition 0.000 description 2
- 238000002604 ultrasonography Methods 0.000 description 2
- 125000000979 2-amino-2-oxoethyl group Chemical group [H]C([*])([H])C(=O)N([H])[H] 0.000 description 1
- BXVSAYBZSGIURM-UHFFFAOYSA-N 2-phenoxy-4h-1,3,2$l^{5}-benzodioxaphosphinine 2-oxide Chemical compound O1CC2=CC=CC=C2OP1(=O)OC1=CC=CC=C1 BXVSAYBZSGIURM-UHFFFAOYSA-N 0.000 description 1
- 102000009027 Albumins Human genes 0.000 description 1
- 108010088751 Albumins Proteins 0.000 description 1
- 108050000244 Alpha-s1 casein Proteins 0.000 description 1
- 241000195940 Bryophyta Species 0.000 description 1
- 206010011224 Cough Diseases 0.000 description 1
- 235000019750 Crude protein Nutrition 0.000 description 1
- 241001669680 Dormitator maculatus Species 0.000 description 1
- 102000004190 Enzymes Human genes 0.000 description 1
- 108090000790 Enzymes Proteins 0.000 description 1
- 108010061711 Gliadin Proteins 0.000 description 1
- 102000006395 Globulins Human genes 0.000 description 1
- 108010044091 Globulins Proteins 0.000 description 1
- WQZGKKKJIJFFOK-GASJEMHNSA-N Glucose Natural products OC[C@H]1OC(O)[C@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-GASJEMHNSA-N 0.000 description 1
- 241000209510 Liliopsida Species 0.000 description 1
- 229920002774 Maltodextrin Polymers 0.000 description 1
- 101000895750 Oryctolagus cuniculus Alpha-S2-casein-like A Proteins 0.000 description 1
- FAPWRFPIFSIZLT-UHFFFAOYSA-M Sodium chloride Chemical compound [Na+].[Cl-] FAPWRFPIFSIZLT-UHFFFAOYSA-M 0.000 description 1
- 229920002472 Starch Polymers 0.000 description 1
- 235000009470 Theobroma cacao Nutrition 0.000 description 1
- 108060008539 Transglutaminase Proteins 0.000 description 1
- 238000003916 acid precipitation Methods 0.000 description 1
- 150000007513 acids Chemical class 0.000 description 1
- 238000007792 addition Methods 0.000 description 1
- 239000000654 additive Substances 0.000 description 1
- 238000013019 agitation Methods 0.000 description 1
- 150000001447 alkali salts Chemical class 0.000 description 1
- 125000003368 amide group Chemical group 0.000 description 1
- 239000012296 anti-solvent Substances 0.000 description 1
- 239000012736 aqueous medium Substances 0.000 description 1
- 239000008346 aqueous phase Substances 0.000 description 1
- 239000008122 artificial sweetener Substances 0.000 description 1
- 235000021311 artificial sweeteners Nutrition 0.000 description 1
- 235000015173 baked goods and baking mixes Nutrition 0.000 description 1
- WQZGKKKJIJFFOK-VFUOTHLCSA-N beta-D-glucose Chemical compound OC[C@H]1O[C@@H](O)[C@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-VFUOTHLCSA-N 0.000 description 1
- 230000005540 biological transmission Effects 0.000 description 1
- 235000020246 buffalo milk Nutrition 0.000 description 1
- 239000006227 byproduct Substances 0.000 description 1
- 235000015115 caffè latte Nutrition 0.000 description 1
- 235000010216 calcium carbonate Nutrition 0.000 description 1
- 229910000019 calcium carbonate Inorganic materials 0.000 description 1
- 238000004364 calculation method Methods 0.000 description 1
- 244000309466 calf Species 0.000 description 1
- 235000020248 camel milk Nutrition 0.000 description 1
- 235000015116 cappuccino Nutrition 0.000 description 1
- 125000003178 carboxy group Chemical group [H]OC(*)=O 0.000 description 1
- 239000007795 chemical reaction product Substances 0.000 description 1
- 235000019219 chocolate Nutrition 0.000 description 1
- 235000016213 coffee Nutrition 0.000 description 1
- 239000000084 colloidal system Substances 0.000 description 1
- 239000000470 constituent Substances 0.000 description 1
- 238000001816 cooling Methods 0.000 description 1
- 239000011258 core-shell material Substances 0.000 description 1
- 239000006071 cream Substances 0.000 description 1
- 235000015142 cultured sour cream Nutrition 0.000 description 1
- 235000011850 desserts Nutrition 0.000 description 1
- 235000013325 dietary fiber Nutrition 0.000 description 1
- 238000007865 diluting Methods 0.000 description 1
- 238000010790 dilution Methods 0.000 description 1
- 239000012895 dilution Substances 0.000 description 1
- 201000010099 disease Diseases 0.000 description 1
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 description 1
- 238000013455 disruptive technology Methods 0.000 description 1
- 239000012153 distilled water Substances 0.000 description 1
- 238000009826 distribution Methods 0.000 description 1
- VZFRNCSOCOPNDB-UHFFFAOYSA-N domoic acid Natural products OC(=O)C(C)C=CC=C(C)C1CNC(C(O)=O)C1CC(O)=O VZFRNCSOCOPNDB-UHFFFAOYSA-N 0.000 description 1
- 238000002036 drum drying Methods 0.000 description 1
- 230000009977 dual effect Effects 0.000 description 1
- 238000002296 dynamic light scattering Methods 0.000 description 1
- 239000008157 edible vegetable oil Substances 0.000 description 1
- 238000001493 electron microscopy Methods 0.000 description 1
- 239000003623 enhancer Substances 0.000 description 1
- 239000000796 flavoring agent Substances 0.000 description 1
- 235000019634 flavors Nutrition 0.000 description 1
- 235000013312 flour Nutrition 0.000 description 1
- 235000012041 food component Nutrition 0.000 description 1
- 239000005417 food ingredient Substances 0.000 description 1
- 235000013350 formula milk Nutrition 0.000 description 1
- 238000009472 formulation Methods 0.000 description 1
- 238000004108 freeze drying Methods 0.000 description 1
- ZZUFCTLCJUWOSV-UHFFFAOYSA-N furosemide Chemical compound C1=C(Cl)C(S(=O)(=O)N)=CC(C(O)=O)=C1NCC1=CC=CO1 ZZUFCTLCJUWOSV-UHFFFAOYSA-N 0.000 description 1
- 239000000499 gel Substances 0.000 description 1
- 235000021474 generally recognized As safe (food) Nutrition 0.000 description 1
- 235000021473 generally recognized as safe (food ingredients) Nutrition 0.000 description 1
- 239000011521 glass Substances 0.000 description 1
- 239000008103 glucose Substances 0.000 description 1
- ZDXPYRJPNDTMRX-UHFFFAOYSA-N glutamine Natural products OC(=O)C(N)CCC(N)=O ZDXPYRJPNDTMRX-UHFFFAOYSA-N 0.000 description 1
- 235000020251 goat milk Nutrition 0.000 description 1
- 235000012171 hot beverage Nutrition 0.000 description 1
- XLYOFNOQVPJJNP-UHFFFAOYSA-M hydroxide Chemical compound [OH-] XLYOFNOQVPJJNP-UHFFFAOYSA-M 0.000 description 1
- 235000015243 ice cream Nutrition 0.000 description 1
- 239000004615 ingredient Substances 0.000 description 1
- 229910052500 inorganic mineral Inorganic materials 0.000 description 1
- 150000002632 lipids Chemical class 0.000 description 1
- 235000012054 meals Nutrition 0.000 description 1
- 239000002609 medium Substances 0.000 description 1
- 239000012528 membrane Substances 0.000 description 1
- 239000000693 micelle Substances 0.000 description 1
- 230000002906 microbiologic effect Effects 0.000 description 1
- 239000011859 microparticle Substances 0.000 description 1
- 239000011707 mineral Substances 0.000 description 1
- 235000010755 mineral Nutrition 0.000 description 1
- 235000011929 mousse Nutrition 0.000 description 1
- 235000021096 natural sweeteners Nutrition 0.000 description 1
- 230000007935 neutral effect Effects 0.000 description 1
- 238000006386 neutralization reaction Methods 0.000 description 1
- 235000015097 nutrients Nutrition 0.000 description 1
- 239000003960 organic solvent Substances 0.000 description 1
- 235000014594 pastries Nutrition 0.000 description 1
- 229920001277 pectin Polymers 0.000 description 1
- 239000001814 pectin Substances 0.000 description 1
- 235000010987 pectin Nutrition 0.000 description 1
- 229920003023 plastic Polymers 0.000 description 1
- 239000004033 plastic Substances 0.000 description 1
- 239000011148 porous material Substances 0.000 description 1
- 230000008092 positive effect Effects 0.000 description 1
- 108060006613 prolamin Proteins 0.000 description 1
- XXRYFVCIMARHRS-UHFFFAOYSA-N propan-2-yl n-dimethoxyphosphorylcarbamate Chemical compound COP(=O)(OC)NC(=O)OC(C)C XXRYFVCIMARHRS-UHFFFAOYSA-N 0.000 description 1
- 230000009467 reduction Effects 0.000 description 1
- 239000013074 reference sample Substances 0.000 description 1
- 238000004007 reversed phase HPLC Methods 0.000 description 1
- 238000009666 routine test Methods 0.000 description 1
- 235000020254 sheep milk Nutrition 0.000 description 1
- 235000013570 smoothie Nutrition 0.000 description 1
- 235000017550 sodium carbonate Nutrition 0.000 description 1
- 229910000029 sodium carbonate Inorganic materials 0.000 description 1
- 239000011780 sodium chloride Substances 0.000 description 1
- 239000011343 solid material Substances 0.000 description 1
- 235000014347 soups Nutrition 0.000 description 1
- 235000011496 sports drink Nutrition 0.000 description 1
- 230000000087 stabilizing effect Effects 0.000 description 1
- 239000008107 starch Substances 0.000 description 1
- 235000019698 starch Nutrition 0.000 description 1
- 230000003068 static effect Effects 0.000 description 1
- 239000013589 supplement Substances 0.000 description 1
- 238000009210 therapy by ultrasound Methods 0.000 description 1
- 102000003601 transglutaminase Human genes 0.000 description 1
- 150000003626 triacylglycerols Chemical class 0.000 description 1
- UFTFJSFQGQCHQW-UHFFFAOYSA-N triformin Chemical compound O=COCC(OC=O)COC=O UFTFJSFQGQCHQW-UHFFFAOYSA-N 0.000 description 1
- 238000000108 ultra-filtration Methods 0.000 description 1
- 238000005199 ultracentrifugation Methods 0.000 description 1
- 235000013343 vitamin Nutrition 0.000 description 1
- 239000011782 vitamin Substances 0.000 description 1
- 229940088594 vitamin Drugs 0.000 description 1
- 229930003231 vitamin Natural products 0.000 description 1
- 238000004260 weight control Methods 0.000 description 1
- 239000008256 whipped cream Substances 0.000 description 1
- 235000008924 yoghurt drink Nutrition 0.000 description 1
- 235000021247 β-casein Nutrition 0.000 description 1
- 235000021246 κ-casein Nutrition 0.000 description 1
Classifications
-
- A—HUMAN NECESSITIES
- A23—FOODS OR FOODSTUFFS; TREATMENT THEREOF, NOT COVERED BY OTHER CLASSES
- A23J—PROTEIN COMPOSITIONS FOR FOODSTUFFS; WORKING-UP PROTEINS FOR FOODSTUFFS; PHOSPHATIDE COMPOSITIONS FOR FOODSTUFFS
- A23J3/00—Working-up of proteins for foodstuffs
- A23J3/14—Vegetable proteins
- A23J3/18—Vegetable proteins from wheat
-
- A—HUMAN NECESSITIES
- A23—FOODS OR FOODSTUFFS; TREATMENT THEREOF, NOT COVERED BY OTHER CLASSES
- A23C—DAIRY PRODUCTS, e.g. MILK, BUTTER OR CHEESE; MILK OR CHEESE SUBSTITUTES; MAKING THEREOF
- A23C11/00—Milk substitutes, e.g. coffee whitener compositions
- A23C11/02—Milk substitutes, e.g. coffee whitener compositions containing at least one non-milk component as source of fats or proteins
- A23C11/06—Milk substitutes, e.g. coffee whitener compositions containing at least one non-milk component as source of fats or proteins containing non-milk proteins
-
- A—HUMAN NECESSITIES
- A23—FOODS OR FOODSTUFFS; TREATMENT THEREOF, NOT COVERED BY OTHER CLASSES
- A23J—PROTEIN COMPOSITIONS FOR FOODSTUFFS; WORKING-UP PROTEINS FOR FOODSTUFFS; PHOSPHATIDE COMPOSITIONS FOR FOODSTUFFS
- A23J3/00—Working-up of proteins for foodstuffs
- A23J3/14—Vegetable proteins
-
- A—HUMAN NECESSITIES
- A23—FOODS OR FOODSTUFFS; TREATMENT THEREOF, NOT COVERED BY OTHER CLASSES
- A23L—FOODS, FOODSTUFFS, OR NON-ALCOHOLIC BEVERAGES, NOT COVERED BY SUBCLASSES A21D OR A23B-A23J; THEIR PREPARATION OR TREATMENT, e.g. COOKING, MODIFICATION OF NUTRITIVE QUALITIES, PHYSICAL TREATMENT; PRESERVATION OF FOODS OR FOODSTUFFS, IN GENERAL
- A23L2/00—Non-alcoholic beverages; Dry compositions or concentrates therefor; Their preparation
- A23L2/52—Adding ingredients
- A23L2/66—Proteins
-
- A—HUMAN NECESSITIES
- A23—FOODS OR FOODSTUFFS; TREATMENT THEREOF, NOT COVERED BY OTHER CLASSES
- A23L—FOODS, FOODSTUFFS, OR NON-ALCOHOLIC BEVERAGES, NOT COVERED BY SUBCLASSES A21D OR A23B-A23J; THEIR PREPARATION OR TREATMENT, e.g. COOKING, MODIFICATION OF NUTRITIVE QUALITIES, PHYSICAL TREATMENT; PRESERVATION OF FOODS OR FOODSTUFFS, IN GENERAL
- A23L33/00—Modifying nutritive qualities of foods; Dietetic products; Preparation or treatment thereof
- A23L33/10—Modifying nutritive qualities of foods; Dietetic products; Preparation or treatment thereof using additives
- A23L33/17—Amino acids, peptides or proteins
- A23L33/19—Dairy proteins
-
- A—HUMAN NECESSITIES
- A23—FOODS OR FOODSTUFFS; TREATMENT THEREOF, NOT COVERED BY OTHER CLASSES
- A23P—SHAPING OR WORKING OF FOODSTUFFS, NOT FULLY COVERED BY A SINGLE OTHER SUBCLASS
- A23P10/00—Shaping or working of foodstuffs characterised by the products
- A23P10/30—Encapsulation of particles, e.g. foodstuff additives
-
- A—HUMAN NECESSITIES
- A23—FOODS OR FOODSTUFFS; TREATMENT THEREOF, NOT COVERED BY OTHER CLASSES
- A23L—FOODS, FOODSTUFFS, OR NON-ALCOHOLIC BEVERAGES, NOT COVERED BY SUBCLASSES A21D OR A23B-A23J; THEIR PREPARATION OR TREATMENT, e.g. COOKING, MODIFICATION OF NUTRITIVE QUALITIES, PHYSICAL TREATMENT; PRESERVATION OF FOODS OR FOODSTUFFS, IN GENERAL
- A23L33/00—Modifying nutritive qualities of foods; Dietetic products; Preparation or treatment thereof
- A23L33/10—Modifying nutritive qualities of foods; Dietetic products; Preparation or treatment thereof using additives
- A23L33/17—Amino acids, peptides or proteins
- A23L33/185—Vegetable proteins
-
- A—HUMAN NECESSITIES
- A23—FOODS OR FOODSTUFFS; TREATMENT THEREOF, NOT COVERED BY OTHER CLASSES
- A23V—INDEXING SCHEME RELATING TO FOODS, FOODSTUFFS OR NON-ALCOHOLIC BEVERAGES AND LACTIC OR PROPIONIC ACID BACTERIA USED IN FOODSTUFFS OR FOOD PREPARATION
- A23V2002/00—Food compositions, function of food ingredients or processes for food or foodstuffs
Landscapes
- Life Sciences & Earth Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Polymers & Plastics (AREA)
- Food Science & Technology (AREA)
- Engineering & Computer Science (AREA)
- Nutrition Science (AREA)
- Health & Medical Sciences (AREA)
- Biochemistry (AREA)
- Mycology (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- General Preparation And Processing Of Foods (AREA)
- Non-Alcoholic Beverages (AREA)
- Grain Derivatives (AREA)
- Fodder In General (AREA)
- Colloid Chemistry (AREA)
- Peptides Or Proteins (AREA)
Abstract
Procedimiento para la preparación de una dispersión acuosa que comprende partículas proteicas coloidales dispersas en un fluido acuoso, cuyas partículas proteicas coloidales comprenden caseinato y una o más proteínas vegetales de una semilla de una planta de la familia Poaceae, comprendiendo el procedimiento a) proporcionar una dispersión intermedia de caseinato y partículas que comprenden dicha una o más proteínas vegetales en un fluido acuoso; y b) someter la dispersión intermedia a una etapa de presurización disruptiva que comprende el tratamiento en un homogeneizador a una presión de al menos 40 MPa, en el que las partículas que comprenden la una o más proteínas vegetales se rompen y se forma la dispersión acuosa que comprende las partículas proteicas coloidales.
Description
DESCRIPCIÓN
Procedimiento para la preparación de una dispersión acuosa de una proteína vegetal poco dispersable
La invención se refiere a un procedimiento para la preparación de una dispersión acuosa coloidal que comprende proteína vegetal.
Las proteínas vegetales son un subproducto abundante en la producción de otros nutrientes útiles, como aceites, carbohidratos digeribles y fibra dietética, a partir de material vegetal. Las proteínas vegetales pueden agruparse en base a la solubilidad en líquidos: agua (albúminas), soluciones salinas diluidas (globulinas), alcohol: mezclas de agua (prolaminas) y álcalis o ácidos diluidos (glutelinas). En particular, las semillas de ciertas monocotiledóneas, como las semillas de granos (cereales y pastos), como el arroz, maíz, trigo, avena, etc. tienen un alto contenido proteico que tienen una solubilidad intrínsecamente baja en agua (aproximadamente a pH neutro), y que también son poco dispersables en agua, como las prolaminas. La baja dispersabilidad en agua limita las posibilidades de usar estas proteínas en alimentos y otros productos a escala industrial. Esto no sólo es un inconveniente si el producto final es un producto acuoso, sino que también pone limitaciones al procesamiento de las proteínas poco dispersables con el fin de preparar un producto útil a partir de ellas. Por ejemplo, pueden ser necesarios líquidos orgánicos con el fin de dispersar las proteínas lo suficientemente bien para procesarlas.
Por ejemplo, Patel y otros ["Partículas coloidales de zeína estabilizadas con caseinato sódico. J. Agric. Food Chem.
58. (2010), 12497-12503] describen un procedimiento en el que se prepara una dispersión coloidal de zeína (una prolamina) mediante precipitación antisolvente mediante el uso de un solvente binario de etanol/agua en el que se disuelve la zeína. Luego, se forma una dispersión mezclando la zeína en etanol/agua con una preparación acuosa de caseinato. La concentración de zeína fue relativamente baja (2,5 % en peso/v). Con el fin de preparar una dispersión coloidal estable se necesitaba una cantidad relativamente alta de caseinato (una relación de zeína a caseinato de 1:0,3 como máximo). Se debe señalar que las proteínas de la leche (como la caseína y el caseinato) se están convirtiendo en un producto cada vez más escaso, ya que existe una demanda mundial creciente de productos lácteos. En particular, sería conveniente poder proporcionar una dispersión coloidal estable de una proteína vegetal que es poco dispersable en agua, que no requiera del uso de un solvente orgánico y/o para proporcionar partículas proteicas que comprenden dicha proteína vegetal que pueda dispersarse de forma estable en agua a una concentración superior a 2,5 % en peso/v.
Es un objeto de la presente invención para proporcionar una alternativa satisfactoria para las proteínas que se usan actualmente en alimentos o productos de alimentación comerciales u otros productos (de consumo), en particular para su uso en una dispersión.
En particular, es un objeto de la presente invención fabricar la proteína vegetal disponible para aplicaciones alimentarias humanas, cuya proteína vegetal está presente en fuentes o partes de las mismas que actualmente no se usan para la producción de alimentos o usados para alimentación animal.
En particular, un objeto de la presente invención es proporcionar una manera de mejorar la dispersabilidad y/o la estabilidad térmica de las proteínas vegetales en un medio acuoso, para proporcionar partículas que comprenden proteína vegetal que tienen una dispersabilidad mejorada en un fluido acuoso y para proporcionar un producto que comprende tales partículas.
Se ha descubierto ahora que uno o más de estos objetos se cumplen tratando partículas que comprenden una o más proteínas vegetales poco dispersables con una técnica específica en presencia de una proteína específica obtenida de la leche.
En consecuencia, la invención se refiere a un procedimiento para la preparación de una dispersión acuosa que comprende partículas proteicas coloidales dispersas en un fluido acuoso, cuyas partículas proteicas coloidales que comprenden caseinato y una o más proteínas vegetales de una semilla de una planta de la familia Poaceae, el procedimiento comprende
a) proporcionar una dispersión intermedia de caseinato y partículas que comprenden dicha una o más proteínas vegetales en un fluido acuoso; y
b) someter la dispersión intermedia a una etapa de presurización disruptiva, que comprende el tratamiento en un homogeneizador a una presión de al menos 40 MPa,
en el que las partículas que comprenden una o más proteínas vegetales se separan y se forma la dispersión acuosa que comprende las partículas proteicas coloidales.
Preferentemente, la proteína vegetal tiene una dispersabilidad en agua a 20 °C del 15 % o menos, preferentemente del 10 % o menos.
Se divulga una dispersión coloidal acuosa, preferentemente una dispersión que se obtiene mediante un procedimiento de acuerdo con la invención, que comprende partículas proteicas coloidales, las partículas comprenden un núcleo que es rico en una o más proteínas vegetales y una superficie que es rica en caseinato. Se divulga un procedimiento para preparar partículas proteicas híbridas que comprende un núcleo que es rico en una o más proteínas vegetales, y una superficie rica en caseinato, que comprende secar una dispersión acuosa (obtenida) de acuerdo con la invención.
Se divulgan partículas proteicas híbridas, preferentemente obtenibles mediante un procedimiento de acuerdo con la invención, que comprende un núcleo que consiste al menos sustancialmente en una o más proteínas vegetales y cuyo núcleo está al menos sustancialmente rodeado de caseinato.
Como se ilustra en los ejemplos, el tratamiento de partículas proteicas vegetales poco dispersables con presurización disruptiva en presencia de caseinato, mejora considerablemente la dispersabilidad de la proteína vegetal.
En una realización ventajosa, la dispersión acuosa de acuerdo con la invención presenta una estabilidad térmica mejorada.
Además, la invención proporciona un medio para reducir la necesidad de proteína de la leche, que se está volviendo cada vez más escasa debido a la creciente demanda mundial. Las partículas híbridas pueden usarse para reemplazar la proteína de la leche total o parcialmente. En particular, las capacidades funcionales de la proteína de la leche pueden ser absorbidas por partículas híbridas de la invención. Dado que sólo se necesita una fracción de proteína de la leche (caseinato), en comparación con un producto a base de proteína totalmente láctea, la invención ofrece una mayor eficacia al proporcionar un sustituto de la proteína de la leche.
Las proteínas lácteas son populares debido a la alta calidad nutricional de la proteína, lo que significa que los nueve aminoácidos esenciales están disponibles. Las proteínas de origen vegetal a menudo se consideran de menor calidad nutricional -porque- en función de la fuente de proteína de origen vegetal se reducen en uno o más aminoácidos esenciales. Las partículas proteicas híbridas pueden complementar una proteína vegetal de baja calidad con una proteína láctea de alta calidad.
A menos que se defina de cualquier otra manera, todos los términos técnicos y científicos que se usan en la presente memoria tienen el mismo significado que el que entiende comúnmente un experto en la técnica.
El término "sustancial(mente)" o "esencial(mente)" se usa generalmente en la presente memoria para indicar que tiene el carácter general o la función de lo que se especifica. Cuando se hace referencia a una característica cuantificable, estos términos se utilizan en particular para indicar que es al menos el 75 %, más en particular al menos el 90 %, incluso más en particular al menos el 95% del máximo de esa característica.
El término 'esencialmente libre' se usa generalmente en la presente memoria para indicar que una sustancia no está presente (más abajo del límite de detección alcanzable con tecnología analítica disponible en la fecha de presentación efectiva) o presente en una cantidad tan baja que no afecta significativamente la propiedad del producto que está esencialmente libre de dicha sustancia o que está presente en una cantidad tan baja (traza) que no necesita ser etiquetado en el producto envasado que está esencialmente libre de la sustancia. En la práctica, en términos cuantitativos, un producto generalmente se considera esencialmente libre de una sustancia, si el contenido de la sustancia es 0-0,1 % en peso, en particular 0-0,01 % en peso, más en particular 0- 0,005 % en peso, en base al peso total del producto en el que está presente.
El 'caseinato' es una proteína sin micelar derivada de la caseína, que se obtiene por precipitación ácida de un líquido que contiene caseína solubilizada (micelas de caseína) como la leche, y neutralización posterior con una base, como un hidróxido, por ejemplo, NaOH, Ko H, Mg(OH)2, Ca(OH)2 , NH4OH o una sal básica, por ejemplo, CaCO3, Na2CO3 o K2CO3 y mezclas de los mismos. El término caseinato también abarca caseinato modificado, por ejemplo, caseinato glicado o desamidado. El caseinato desamidado se puede obtener, por ejemplo, sometiendo el caseinato a la actividad desamidante de una enzima, por ejemplo, una desaminasa o transglutaminasa. Una parte de, o todos los grupos amida de las cadenas laterales de la glutamina y/o la asparagina se desamidan para formar grupos carboxilo. Al igual que la caseína, el caseinato se compone de una mezcla de cuatro tipos principales de caseína (alfa S1, alfa S2, beta y kappa caseína). Sin embargo, la caseína (micelar) contiene calcio y fosfato unidos a la estructura de la proteína, estabilizando la estructura micelar. El caseinato no necesita contener calcio ni fosfato, aunque una preparación de caseinato puede contener calcio o fosfato.
Preferentemente, el caseinato es caseinato de leche de vaca. Otras fuentes adecuadas incluyen leche de otros ungulados, en particular leche de ungulados con pezuñas, como leche de oveja, leche de cabra, yegua, camello y leche de búfalo.
Como se usa en la presente memoria, la "dispersabilidad" de una sustancia, en particular de partículas proteicas, se puede determinar mediante centrifugación a 1.360 g de 5 % en peso. % de mezcla de la sustancia en agua (agua destilada o agua del grifo, sin más aditivos) por una duración de 10 min. Esta prueba generalmente se lleva a cabo a unos 20 °C. La dispersabilidad de una proteína generalmente se calcula como:
100 % x la cantidad de nitrógeno de la proteína que queda en el sobrenadante dividida por la cantidad total de nitrógeno de la proteína.
Las partículas proteicas que permanecen en el sobrenadante bajo estas condiciones de prueba para determinar la dispersabilidad son generalmente partículas coloidales.
En particular, para la dispersabilidad de la proteína vegetal como constituyente de o a partir de las partículas híbridas, la dispersabilidad se puede determinar como se describe en los ejemplos. En la presente memoria se describe cómo se estima el contenido de nitrógeno de la proteína vegetal en el sobrenadante corrigiendo el contenido de nitrógeno de la fracción sobrenadante para la contribución de caseinato, asumiendo que el caseinato se distribuye proporcionalmente sobre el sobrenadante y el precipitado (residuo) y que la dispersabilidad del nitrógeno proteico vegetal se expresa como un porcentaje del nitrógeno proteico vegetal total.
El contenido de proteína se puede medir determinando el contenido de nitrógeno proteico, mediante el uso de la metodología Kjeldahl (TKN).
En particular se considera que una proteína tiene una dispersabilidad pobre (o baja) si la dispersabilidad es del 15 % o menos, preferentemente del 10 % o menos, con mayor preferencia del 5 % o menos, en particular del 3 % o menos. Cuando se hace referencia a una dispersabilidad en la presente memoria, se refiera a la dispersabilidad a un 20 °C, a menos que se especifique de cualquier otra manera.
Las partículas se han definido y clasificado de varias maneras diferentes en función de su estructura, tamaño o composición específica. Como se usa en la presente memoria, las partículas se definen ampliamente como partículas a micro o nanoescala que típicamente están compuestas por al menos un material sólido. Típicamente, el diámetro promedio en peso de tales partículas varía de aproximadamente 10 nm a aproximadamente 100 pm, como se puede determinar mediante microscopía (microscopía de luz o microscopía electrónica, en función del tamaño, como entenderá el experto en la materia).
En la dispersión coloidal, el diámetro promedio de partícula de las partículas coloidales normalmente es entre aproximadamente 0,01 pm y aproximadamente 4 pm, en particular entre aproximadamente 0,05 pm y aproximadamente 2 pm, más en particular aproximadamente 1,5 pm o menos, por ejemplo, aproximadamente 1 pm o menos. Preferentemente, el diámetro promedio de partícula es al menos 0,1 pm, con mayor preferencia de al menos 0,2 pm, con mayor preferencia al menos 0,4 pm, con mayor preferencia al menos 0,5 pm.
En la dispersión coloidal, las partículas coloidales generalmente tienen una distribución de tamaño de partícula (D(4,3) determinable por dispersión dinámica de luz (analizador Malvern Mastersize X), entre aproximadamente 0,01 pm y aproximadamente 4 pm. En particular, el D (4,3) es al menos aproximadamente 0,05 pm, más en particular al menos aproximadamente 0,1 pm. Preferentemente, el D (4,3) de las partículas coloidales es de al menos 0,2 pm, con mayor preferencia de al menos 0,3 pm, con mayor preferencia de al menos 0,4 pm, con mayor preferencia de al menos 0,5 pm. Preferentemente, el D (4,3) de las partículas coloidales es de aproximadamente 2 pm o menos, en particular de aproximadamente 1 pm o menos. En particular se han logrado buenos resultados con partículas que tienen un D (4,3) en el intervalo de 0,2 a 2 pm, más en particular de 0,5 a 1,5 pm.
Las partículas pueden tener una estructura homogénea o una estructura heterogénea. Las partículas homogéneas generalmente consisten en un material en una sola fase (estado de la materia). Las partículas con una estructura heterogénea, en la que se pueden distinguir dos o más estados de la materia (fases), se pueden referir a partículas jerárquicas. Las partículas jerárquicas en particular incluyen partículas que comprenden un núcleo interno y una capa exterior. La capa exterior puede estar formada por una capa de otra sustancia distinta del núcleo, por ejemplo, el caseinato puede formar un complejo en la superficie de la proteína vegetal de esta manera formando así una capa sobre al menos parte del núcleo compuesto por la proteína vegetal. La capa puede recubrir esencialmente el núcleo o puede estar presente como parches en partes del núcleo. La capa puede ser mono capa. También es posible que el núcleo esté al menos sustancialmente rodeado por una capa más gruesa que comprenda el caseinato, formando de esta manera un recubrimiento o envoltura o similar.
Como se usa en la presente memoria, "partículas proteicas" son partículas que consisten al menos sustancialmente en una o más proteínas. Preferentemente al menos 40 %, con mayor preferencia al menos 50 %, en particular al menos 80 %, más en particular al menos 90% del peso de las partículas está formado por una o más proteínas. Las partículas proteicas vegetales son preferentemente partículas que comprenden al menos 50 %, en base al peso total de las partículas de una o más proteínas vegetales poco dispersables, en particular al menos 80 %, más en particular al menos 90 %.
Las "partículas proteicas" pueden ser "partículas proteicas híbridas".
"Partículas proteicas híbridas" significa partículas que comprenden al menos una proteína vegetal como se define en la presente memoria, en particular al menos una proteína vegetal poco dispersable, como se define en la presente memoria, y caseinato. En particular, las partículas híbridas son partículas jerárquicas que tienen un núcleo rico en dicha proteína o proteínas vegetales y una fase circundante, rica en caseinato. Con "rica en proteína vegetal" se entiende en particular que dicha proteína es la proteína más abundante en el núcleo, y con "rica en caseinato" se entiende que la concentración de caseinato en la superficie es mayor que en el núcleo. En una realización específica, las partículas híbridas tienen un núcleo que consiste al menos sustancialmente en la proteína vegetal, y una capa circundante que consiste al menos sustancialmente en caseinato. Tal capa puede ser una monocapa de caseinato o un recubrimiento que tenga un grosor que exceda el grosor de una monocapa de caseinato. La capa también puede ser de naturaleza discontinua, lo que significa que la capa puede que no cubra toda la superficie de la proteína vegetal (partícula), pero está presente en "forma de parches".
pII se define como el pII aparente que se puede medir con un electrodo pII estándar, a 20 °C a menos que se especifique de cualquier otra manera.
El término "acuoso" se usa en la presente memoria para describir fluidos con agua como único o principal solvente. Generalmente, el contenido de agua de un fluido acuoso es superior al 50 % en peso. en base al peso total de los solventes (sustancias que están en estado líquido de la materia a 25 °C), preferentemente a 80-100 % en peso con mayor preferencia a 90-100 % en peso, en particular a 95-100 % en peso. Se han obtenido buenos resultados con un fluido que es esencialmente libre de solventes además del agua. Si están presentes uno o más solventes, estos generalmente son solventes GRAS, preferentemente solventes de grado alimenticio. En particular, el etanol puede estar presente en una cantidad menor. El otro solvente, tal como etanol, se puede añadir para facilitar la etapa de presurización disruptiva, por ejemplo, se puede reducir el número de ciclos de homogeneización o la presión de homogeneización mientras se logra un efecto similar. Si se usa, el contenido de etanol es generalmente al menos 5 % en peso, en particular 10-20 % en peso. Además, aparte del agua, un fluido acuoso puede comprender un aceite comestible, tal como un aceite de triglicéridos, aunque se han logrado buenos resultados con un fluido que está esencialmente libre de aceite.
Las partículas individuales que comprenden la proteína vegetal usadas como material de partida para fabricar la dispersión intermedia pueden estar compuestas por un único material homogéneo o pueden ser un aglomerado compuesto por una pluralidad de partículas más pequeñas, tales como nanopartículas.
Las partículas que comprenden la proteína vegetal, usadas como material de partida, pueden consistir al menos sustancialmente en una o más proteínas. Sin embargo, también es posible usar partículas que comprendan una cantidad sustancial de uno o más de otros componentes (vegetales). Por ejemplo, puede usarse harina de cereal. Generalmente, el contenido proteico de las partículas que comprenden la proteína vegetal es al menos aproximadamente 10 % en peso, en particular aproximadamente 25 % en peso o más, preferentemente al menos aproximadamente 40 % en peso, con mayor preferencia 50 % en peso, o más. Sin embargo, es una ventaja de la invención que también permite la preparación de una dispersión coloidal a partir de partículas proteicas relativamente crudas que contienen una cantidad sustancial de uno o más componentes distintos de las partículas proteicas, por ejemplo, un carbohidrato o un lípido. De este modo, en una realización específica las partículas proteicas contienen menos de aproximadamente 90 % en peso de proteína, más específicamente menos de aproximadamente 80 % en peso. Las partículas que comprenden la proteína vegetal son partículas que comprenden una proteína de las semillas de una planta de la familia Poaceae. Preferentemente, la proteína vegetal poco soluble es de un grano, con mayor preferencia de un cereal o pasto seleccionado del grupo de arroz, avena, trigo, maíz, cebada, centeno y sorgo, aún con mayor preferencia seleccionado de arroz, avena, trigo y maíz, más preferido de arroz, avena y maíz.
En una realización preferente, la proteína vegetal poco dispersable es seleccionada del grupo proteico de semillas de grano, como la proteína del grano de arroz; proteínas de salvado, como proteína de salvado de avena; partículas de gluten y prolaminas. Preferentemente, la prolamina es seleccionada del grupo de gliadina, hordeína, secalina, zeína, kafirina y avenina. Con mayor preferencia, la prolamina es zeína.
En el procedimiento de la invención, se prepara una dispersión intermedia a partir de las partículas que comprenden la proteína vegetal y el caseinato. Las partículas que comprenden la proteína vegetal para la dispersión intermedia pueden ser, pero no es necesario que sean partículas coloidales; pueden comprender partículas más grandes. En general, las partículas tienen un diámetro de hasta 1 mm. El D (4,3) es preferentemente hasta 400 pm, en particular en el intervalo de 1-200 pm, más en particular en el intervalo de 5-100 pm.
En una realización ventajosa, se preparan una preparación acuosa de la proteína vegetal y una preparación acuosa separada del caseinato. El pH de la preparación de caseinato se elige generalmente por encima de pH 5, en particular en el intervalo de pH 5,5-9, con el fin de proporcionar una preparación en el que el caseinato esté suficientemente solubilizado. Para la preparación de proteína vegetal el pH puede ser inferior a 5, pero por razones prácticas se prefiere que el pH también sea por encima de 5, en particular aproximadamente el mismo que para la
preparación de caseinato. La concentración de proteína total en dichas preparaciones generalmente está en el intervalo de 1-30 % en peso, en particular en el intervalo de 2-20 % en peso, más en particular en el intervalo de aproximadamente 3 a aproximadamente 15 % en peso. por ejemplo, aproximadamente 12 % en peso. o menos.
En una realización preferente, se realiza una etapa anterior de homogeneización disruptiva a alta presión de una dispersión de partículas que comprenden una o más proteínas vegetales y preferentemente sin caseinato en un fluido acuoso está hecho antes de la etapa a)
Preferentemente, la etapa anterior de homogeneización a alta presión implica una presión en un intervalo que es el mismo que los intervalos de presiones descritos para la etapa de homogeneización de la dispersión intermedia de caseinato y partículas que comprenden dicha una o más proteínas vegetales en un fluido acuoso. En una realización preferente específica, las presiones en la etapa anterior de homogeneización disruptiva a alta presión son aproximadamente las mismas que en la etapa a.
La dispersión intermedia de las partículas que comprenden la proteína vegetal y el caseinato se prepara ventajosamente mezclando la preparación acuosa de la proteína vegetal y la preparación acuosa del caseinato. Alternativamente, la dispersión intermedia se prepara mezclando un polvo que comprende la proteína vegetal y un polvo que comprende el caseinato y mezclando la combinación resultante con un líquido acuoso.
La temperatura a la que se prepara la dispersión intermedia se puede elegir dentro de amplios límites, y generalmente es en el intervalo de 5-90 °C, preferentemente en el intervalo de 10-70 °C, en particular en el intervalo de 15-65 °C. C, más en particular a aproximadamente temperatura ambiente o superior. Se puede lograr una mezcla adecuada con agitación (suave).
Generalmente, estas preparaciones se mezclan para obtener una dispersión intermedia en la que la relación peso a peso de dicha proteína vegetal con respecto a caseinato es 1:1 o más. Preferentemente dicha relación peso a peso es al menos 3:1, con mayor preferencia al menos 4:1, en particular al menos 5:1, al menos 6: 1 o al menos 7,1. Generalmente dicha relación peso a peso es 20:1 o menos, preferentemente 15:1 o menos, con mayor preferencia 12:1 o menos, en particular 10:1 o menos, más en particular 8:1 o menos.
El contenido de proteína total de la dispersión intermedia generalmente está en el intervalo de 1-30 % en peso. Preferentemente el contenido de proteína total es al menos 5 % en peso, con mayor preferencia al menos 8 % en peso, en particular aproximadamente 10 % en peso o más. Preferentemente, el contenido de proteína total es 25 % en peso o menos, con mayor preferencia 20 % en peso o menos, en particular aproximadamente 15 % en peso o menos, por ejemplo, aproximadamente 12 % en peso o menos.
El contenido total de proteínas vegetales que tienen poca dispersabilidad en agua, en la dispersión intermedia, generalmente es superior al 25 % en peso de la proteína total, preferentemente es al menos 50 % en peso del contenido de proteína total en la dispersión intermedia, con mayor preferencia al menos 65 % en peso, en particular aproximadamente 80 % en peso. o más. Preferentemente el equilibrio está formado al menos sustancialmente por caseinato.
La presurización disruptiva típicamente da como resultado una reducción del tamaño de las partículas que comprenden la proteína vegetal. La dispersión intermedia, sometida a la presurización disruptiva, generalmente tiene un pH por encima de 5. Se contempla que un pH por encima de 5 contribuya a una interacción suficiente del caseinato con las partículas que comprenden la proteína vegetal. En particular, el pII de la dispersión intermedia está en el intervalo de 5,5-9, preferentemente en el intervalo de 6,0-8, más específicamente en el intervalo de 6,3 a 7,5. Si se desea, el pH se ajusta con un ácido, por ejemplo, HCl, o una base, por ejemplo, NaOH.
La presurización disruptiva de la dispersión intermedia se lleva a cabo en un homogeneizador. La presión aplicada es 40 MPa o más, preferentemente 50 MPa o con mayor preferencia 75 MPa o más. En particular, se han logrado buenos resultados a una presión de aproximadamente 100 MPa o más. El límite superior de la presión se define generalmente por la presión máxima que se puede aplicar mediante el uso del dispositivo de presurización. Teniendo en cuenta la presión máxima conocida para los homogeneizadores disponibles comercialmente, en la práctica la presión máxima es generalmente de 500 MPa o menos. Se han obtenido buenos resultados a una presión considerablemente inferior. En particular, la presión aplicada puede ser 250 MPa o menos, más en particular 200 MPa o menos.
El tratamiento de presurización comprende 1 o más ciclos, preferentemente 2 o más ciclos, en particular 3 o más ciclos, más en particular 5 o más ciclos. El número de ciclos generalmente es 15 o menos, en particular 10 o menos, preferentemente 6 o menos.
La temperatura durante la presurización es generalmente menos de 100 °C, en particular menos de 90 ° C, preferentemente hasta 70 °C o hasta 60 °C. La temperatura de presurización generalmente se inicia aproximadamente a la temperatura ambiente, aunque puede iniciarse a una temperatura mayor o menor. Típicamente el tratamiento se inicia a una temperatura en el intervalo de 5-40 °C, en particular de 10-30 °C. Como
consecuencia de la presurización, la temperatura durante el tratamiento generalmente aumenta, también en presencia de enfriamiento activo. Generalmente, se puede permitir que la temperatura aumente a una temperatura de 40-90 °C, en particular 40-80 °C, más en particular 40-70 °C. Opcionalmente, la dispersión coloidal resultante se enfría activamente, en particular a una temperatura en el intervalo de aproximadamente 5 a aproximadamente 20 °C.
En una realización ventajosa, la presurización disruptiva se lleva a cabo con una intensidad energética (energía introducida en el producto por unidad de volumen) de al menos aproximadamente 10 MJ/m3de dispersión, preferentemente al menos 25 MJ/m3 de dispersión, en particular al menos 50 MJ/m3 de dispersión. El límite superior no es particularmente crítico y puede, por ejemplo, ser de hasta aproximadamente 2.000 MJ/m3 de dispersión, preferentemente alrededor de 1.500 MJ/m3 de dispersión o menos, en particular aproximadamente 1.000 MJ/m3 de dispersión o menos, más en particular aproximadamente 500 MJ/m3 de dispersión o menos.
En base a experimentos llevados a cabo por los inventores, se concluye que, durante la etapa de presurización de la dispersión intermedia, las partículas que comprenden la proteína vegetal se separan y se forma la dispersión acuosa que comprende las partículas proteicas coloidales. Sin estar limitados por la teoría, los inventores concluyen de los experimentos realizados que el caseinato interactúa con la superficie de las partículas y al menos rodea sustancialmente a las partículas después de la etapa de presurización disruptiva. De este modo, se proporciona una dispersión coloidal acuosa que comprende partículas proteicas coloidales, que comprende un núcleo que es rico en una o más proteínas vegetales que tiene una dispersabilidad en agua a 20 °C del 10 % o menos y una superficie que es rica en caseinato.
La dispersión coloidal acuosa se puede usar como tal, por ejemplo, en la preparación de una bebida u otro producto alimenticio o productos de alimentación, opcionalmente después de una etapa de dilución o una etapa de concentración, en la que la concentración de partículas coloidales disminuye o aumenta. En una realización, la dispersión coloidal acuosa se somete a una etapa en la que las partículas no coloidales se separan de la dispersión coloidal, antes de su uso posterior. Esto se puede hacer, por ejemplo, mediante filtración o centrifugación. De este modo, el contenido de partículas proteicas, el contenido proteico vegetal escasamente dispersable y el contenido de caseinato en la dispersión acuosa que comprende partículas proteicas coloidales que se obtienen no necesitan ser los mismos que en la dispersión intermedia a partir de la cual se prepara la dispersión. La concentración de proteína vegetal escasamente dispersable en la dispersión acuosa que comprende partículas proteicas coloidales es generalmente al menos 0,5 % en peso. Generalmente dicha concentración de proteína vegetal escasamente dispersable en la dispersión coloidal está en el intervalo de 0,5-50 % en peso. En principio, la dispersión coloidal acuosa puede prepararse a una concentración de proteína diferente a la concentración en el producto final, en particular un alimento o productos de alimentación, que se prepara con la dispersión coloidal acuosa. En una realización ventajosa, la dispersión coloidal acuosa se prepara a una concentración de proteína que es aproximadamente la misma que la concentración de proteína en el producto final. En una primera realización, la concentración de proteína vegetal está en el intervalo de 0,5-2,0 % en peso, en base al peso total, cuya dispersión es particularmente adecuada para preparar productos con un contenido de proteína relativamente bajo (típicamente menos del 3 % en peso o menos, en particular 0,5-2,0 % en peso de proteína total, en base al peso total del producto). En una segunda realización, la concentración de proteína vegetal está en el intervalo de 2,0-5,0 % en peso, en base al peso total, cuya dispersión que es particularmente adecuada para preparar productos con un contenido de proteína intermedio (típicamente hasta 6,5 % en peso, en particular 3,0-5,0 % en peso de proteína total, en base al peso total del producto). En una tercera realización, la concentración de proteína vegetal es 5,0 % en peso o más, en particular en el intervalo de 5,0-15 % en peso en base al peso total, cuya dispersión es particularmente adecuada para preparar productos con un contenido de proteína relativamente alto (generalmente más del 6,5 % en peso de proteína total, en base al peso total, en particular en el intervalo de 7,0-15 % en peso, en base al peso total).
Típicamente, al menos una parte sustancial de la proteína vegetal y el caseinato forman partículas coloidales en la dispersión acuosa. Preferentemente, en esencia la totalidad de al menos la proteína vegetal forma partículas coloidales.
Una dispersión coloidal acuosa tiene preferentemente una relación peso a peso de la proteína vegetal poco dispersable a caseinato de 3,5:1 o más, con mayor preferencia de 4:1 o más, en particular de 5:1 o más, más en particular de 6:1 o más, 7:1 o más, 8:1 o más o 9:1 o más. Dicha relación es preferentemente de 20:1 o menos - en particular en el intervalo de 4:1 a 20:1, con mayor preferencia de 15:1 o menos, en particular de 5:1 a 10:1,
La dispersión coloidal acuosa se puede usar como tal, por ejemplo, en la preparación de una bebida u otro producto alimenticio o productos de alimentación, o se pueden obtener partículas proteicas híbridas aisladas a partir de la dispersión coloidal. Las partículas híbridas se obtienen generalmente secando una dispersión acuosa de acuerdo con la invención. Para la etapa de secado, se pueden usar técnicas de secado generalmente conocidas, por ejemplo, secado en tambor, secado por pulverización o liofilización. Las partículas híbridas tienen una capacidad de dispersión mejorada en comparación con las partículas híbridas obtenidas secando un fluido acuoso que comprende proteína vegetal y caseinato que no se ha sometido a la etapa de presurización disruptiva. Una técnica de secado particularmente adecuada es el secado por pulverización. El secado por pulverización puede usarse en particular para obtener un polvo de partículas que tienen una morfología de núcleo-envoltura, en el que el núcleo consiste al
menos sustancialmente en la proteína vegetal y la envoltura consiste al menos sustancialmente en el caseinato. Esta técnica es generalmente conocida en la técnica y el experto en la técnica podrá llevar a cabo el secado por pulverización en base al conocimiento general común, la información divulgada en la presente memoria y opcionalmente una cantidad limitada de pruebas de rutina.
También se puede usar una técnica en la que las partículas se aíslan de la fase acuosa, por ejemplo, ultrafiltración, ultracentrifugación, o precipitación.
Las partículas proteicas híbridas (aisladas) de la invención son preferentemente un polvo.
La relación peso a peso de la proteína vegetal (escasamente dispersable) al caseinato de las partículas aisladas (tal como un polvo de las partículas) puede ser aproximadamente la misma que para la dispersión acuosa. Sin embargo, dependiendo de la técnica de preparación, también es posible proporcionar partículas con una relación peso a peso más baja de las proteínas vegetales al caseinato, por ejemplo, porque el caseinato que está presente en la mayor parte de la dispersión puede precipitar sobre las partículas coloidales en la dispersión durante el secado. La relación peso a peso de proteína vegetal escasamente dispersable a caseinato generalmente es 1:2 o más, en particular 1:1 o más, más en particular 2:1 o más, preferentemente 3,5:1 o más, con mayor preferencia 4:1 o más, más en particular 5:1 o más, más en particular 6:1 o más, 7:1 o más, 8:1 o más o 9:1 o más. Generalmente relación es 20:1 o menos, en particular 15:1 o menos, más en particular 10:1 o menos.
Es una ventaja de las partículas híbridas, en comparación con las partículas proteicas vegetales que carecen de caseinato y por lo tanto consisten esencialmente en el material del núcleo (partículas proteicas vegetales poco solubles) que se mejora la dispersabilidad (en base a la determinación de nitrógeno) en agua; la dispersabilidad en agua a 20 °C generalmente es más del 10 %, preferentemente 15 % o más, con mayor preferencia 20 % o más, en particular aproximadamente 25 % o más. En principio, la dispersabilidad puede ser de hasta el 100 %, al menos en realizaciones específicas. En la práctica, la dispersabilidad puede ser menor, en particular aproximadamente 70 % o menos, aproximadamente 65 % o menos, aproximadamente 50 % o menos, aproximadamente 40 % o menos, o aproximadamente 30% o menos.
La dispersión o partículas aisladas de la dispersión pueden usarse para proporcionar un producto alimenticio, productos de alimentación u otro producto, por ejemplo, un producto sanitario. El producto alimenticio es preferentemente adecuado para el consumo humano. El alimento o los productos de alimentación pueden ser un producto sólido, un producto semisólido, por ejemplo, un producto gelificado o un producto fluido (a la temperatura de su consumo deseada). El alimento o productos de alimentación se puede envasar como un producto alimenticio listo para usar, por ejemplo, una bebida, que se puede consumir al abrir el envase, o un alimento o productos de alimentación instantáneo.
Un producto se considera fluido si puede verterse desde de un envase lleno, cuando se mantiene en diagonal y la abertura de salida se mantiene hacia abajo. En particular, un producto se considera fluido si la viscosidad, medida con un viscosímetro Brookfield (husillo 5, 10 rpm, 7 °C), es 100 mPa.s o menos, más en particular 70 mPa.s o menos, más en particular 1-50 mPa.s.
Los productos sólidos y semisólidos son productos que son dimensionalmente estables en ausencia de una fuerza aplicada externamente. Típicamente los semisólidos suelen tener una consistencia más blanda que los sólidos (verdaderos), es decir, muestran un flujo reológico a una presión aplicada relativamente baja. Típicamente los semisólidos pueden tomarse con cuchara, lo que significa que el producto se puede tomar fácilmente con cuchara de un plato o un tazón. En particular, ejemplos de semisólidos son geles, mousses y cremas, en particular crema agria, crema batida, helados y requesón blando.
La dispersión o las partículas son particularmente adecuadas para el suministro de un producto bebible, como una sopa o una bebida. El alimento o productos de alimentación, en particular el producto bebible, puede ser un producto listo para usar o un producto instantáneo.
Los productos alimenticios preferidos incluyen productos alimenticios lácteos y sustitutos de productos alimenticios lácteos.
Es una ventaja de la invención que los alimentos o productos de alimentación puedan tratarse térmicamente para mejorar la calidad microbiológica. En consecuencia, la invención también se refiere a un producto alimenticio o productos de alimentación que estén esterilizados, pasteurizados o tratados con UHT.
Los productos alimenticios particularmente preferidos son seleccionados del grupo de bebidas nutricionales, bebidas similares a la leche; productos fermentados (similares a la leche), por ejemplo, yogures bebibles; batidos; licuados; bebidas de café, como café con leche, bebidas de capuchino; chocolate y otras bebidas a base de cacao.
Los productos alimenticios preferidos incluyen leche evaporada (EVAP) o productos de leche condensada azucarada (SCM) análogos.
EVAP y SCM como tal se conocen bien por el experto en la técnica; se trata de productos tradicionales que ya se usan desde hace mucho tiempo como blanqueadores para el café o la leche; o pueden consumirse como tal o en forma diluida. Dado que se usan con frecuencia en bebidas calientes, es particularmente útil, la estabilidad térmica mejorada que ofrece la invención. De acuerdo con la invención, los contenidos de los análogos son iguales o similares a EVAP respectivamente SCM, con la condición de que al menos una parte, preferentemente al menos una parte sustancial, en particular esencialmente toda la proteína láctea se sustituye con las partículas proteicas de la invención.
El análogo de EVAP se define en particular como un producto líquido esterilizado, que comprende aproximadamente 22-27 % de sólidos, de los cuales aproximadamente 7-11 % son azúcares, preferentemente lactosa; aproximadamente 6-8 % de grasa; y aproximadamente 5-8 % de proteína, la proteína que comprende las partículas proteicas coloidales de la invención.
La grasa puede ser grasa de leche y/o grasa vegetal.
El análogo de SCM se define en particular como un producto líquido esterilizado que comprende aproximadamente un 70-75 % de sólidos; de los cuales aproximadamente 6-10 % son grasas; aproximadamente 50-56 % de azúcares que comprenden sacarosa y lactosa; y aproximadamente 6-10 % de proteína, la proteína que comprende las partículas proteicas coloidales de la invención.
La grasa puede ser grasa de leche y/o grasa vegetal.
Las bebidas nutricionales son productos alimenticios fluidos que típicamente tienen una densidad energética de al menos 30 kcal/100 ml, en particular 50-150 kcal/100 ml, más en particular 60-100 kcal/100 ml. Preferentemente, la bebida nutricional tiene un contenido proteico y/o carbohidratos más alto que la leche de vaca. Además de proteínas y carbohidratos, la bebida nutricional puede contener en principio cualquier ingrediente alimentario adicional, en particular uno o más sabores, una o más vitaminas o uno o más minerales. En una realización específica, la bebida nutricional se prepara a partir de leche (desnatada), a la que se le han añadido partículas de la invención y opcionalmente uno o más ingredientes diferentes.
El contenido de proteína total de una bebida nutricional preferentemente es al menos aproximadamente 3,6 % en peso. La proteína es seleccionada preferentemente del grupo de proteínas lácteas y proteínas vegetales.
El contenido de grasa preferentemente es al menos aproximadamente 0,5 % en peso. En particular la grasa puede seleccionarse de grasas vegetales y grasas lácteas. El término grasa incluye grasas sólidas y líquidas, en particular triglicéridos sólidos y líquidos.
Opcionalmente están presentes uno o más carbohidratos digeribles. El contenido de carbohidratos generalmente es de 16 % en peso. o menos, preferentemente 0,5-12 % en peso. En una realización, la bebida nutricional está esencialmente libre de carbohidratos. En tal realización, preferentemente están presentes uno o más edulcorantes naturales o uno o más edulcorantes artificiales.
Ejemplos de carbohidratos son lactosa, sacarosa, glucosa, oligos azúcares, maltodextrinas y almidón.
En una realización específica, la bebida nutricional tiene una densidad energética de 70-114 kCal./ml, contiene 3,6-7 % en peso. de proteína, 0,5 - 3 % en peso de grasa, 0,5-16 % en peso de carbohidrato digerible.
En una realización adicional, el producto alimenticio es seleccionado del grupo de; coberturas; postres; productos de panadería; productos de repostería; productos de queso.
En una realización adicional, el producto alimenticio es una bebida deportiva.
En una realización adicional, el producto alimenticio es una fórmula infantil.
En una realización adicional, el producto alimenticio es una solución de control de peso.
En una realización preferente específica, el producto alimenticio es un producto alimenticio clínico, que puede ser una bebida nutricional clínica. Los alimentos clínicos son productos alimenticios que se usan para mejorar, mantener o restaurar la salud y/o prevenir una enfermedad, recetados por un profesional de la salud como un médico, enfermero o dietista, y destinados para y suministrados a personas que los necesiten. Una bebida nutricional clínica tiene preferentemente un contenido energético superior a 65 kcal/100 ml. Entonces se prefiere en particular una alta densidad de energía porque a menudo los pacientes tienen restricciones de volumen o les resulta difícil consumir grandes volúmenes de alimentos.
En una realización adicional, el producto alimenticio es una bebida de ácido láctico.
En una realización adicional, el producto alimenticio es un alimento para personas mayores (personas de 65 años o más) o personas enfermas. En particular una bebida o un preparado de una bebida para personas mayores o enfermas.
En una realización adicional, el alimento es una bebida de tipo yogur.
En una realización adicional, el producto alimenticio es un sustituto de comidas.
En una realización adicional, el producto alimenticio es una bebida instantánea en polvo.
En una realización adicional, el producto alimenticio es una barra nutricional.
En una realización adicional, el producto es un producto alimenticio para animales o un producto alimenticio para mascotas. Los productos de alimentación animal preferidos son los sustitutos de la leche. En particular, se pueden usar en un entorno agrícola. Los sustitutos de la leche preferidos para la alimentación de los animales son los sustitutos de la leche para terneros y los sustitutos de la leche para lechones.
La invención se ilustrará ahora mediante los siguientes ejemplos.
Ejemplo 1:
Se prepararon varias dispersiones de proteína de grano que comprenden 10 % en peso de polvo proteína de grano de arroz (RemyPro, Benco), 10 % en peso de polvo de proteína de salvado de avena (Proatein, Tate&Lyle) o 10 % de polvo de proteína de maíz (Zein F4400 FG, Flo Chemical) en agua a 20 °C y típicamente se agitaron durante 3 horas.
Además, un 10 % en peso de polvo de caseinato sódico (EM7 o NaCas S, FrieslandCampina DMV) se hizo una dispersión en agua a 20 °C y típicamente se agitó durante 3 horas (los contenidos típicos de proteína de los polvos fueron: caseinato sódico -92 %; grano de arroz -80-85 %; salvado de avena -51-54 %; proteína de maíz -88-96 %).
Las dispersiones se almacenaron a 5 °C hasta su posterior uso.
Después de almacenarla durante la noche, la dispersión se llevó a aproximadamente 20 °C. A partir de ahí, se prepararon dispersiones intermedias de polvo de proteína de grano y polvo de caseinato en diferentes proporciones de polvo de proteína de grano a polvo de caseinato mezclando las dos dispersiones en diferentes proporciones y desairadas (solo la proteína de maíz).
A partir de ahí, se determinó el pH de la dispersión y se ajustó a un pH en el intervalo de 6-9, si era necesario. Las dispersiones se sometieron a una etapa de homogeneización usando un homogeneizador Panda (GEA), un homogeneizador Stansted de sobremesa o un homogeneizador Stansted de alta presión de doble intensificador, que se hicieron funcionar de acuerdo con las instrucciones del proveedor. Durante la homogeneización, el aparato se enfrió con agua corriente del grifo y las muestras se mantuvieron en hielo. Las condiciones de homogeneización variaron de 50-330 MPa durante 1-10 ciclos.
Dispersibilidad
Para determinar el aumento de la dispersabilidad acuosa de la preparación de proteína de grano, las muestras se diluyeron al 5 % en peso. Se centrifugó la materia seca (MS) y 45 g de dispersión en tubos de plástico de 50 ml a 1.360 g durante 10 minutos a 20 °C. Las cantidades de sobrenadante y el residuo se determinaron en peso. Los sobrenadantes se recogieron para la determinación del contenido de nitrógeno (de acuerdo con el procedimiento de Kjeldahl; corregido por la contribución de la caseína al contenido de nitrógeno, asumiendo que el caseinato se distribuyó proporcionalmente sobre el sobrenadante y la fracción de residuo). Para determinar el aumento de la dispersabilidad acuosa de la preparación de proteína de grano, los resultados obtenidos para la mezcla se expresaron con relación al nitrógeno total del grano y se compararon con los de las dispersiones de polvo de grano (solamente) tratadas con homogeneización de polvo de grano en ausencia de caseinato y con los de las mezclas de polvo de grano y polvo de caseinato que no hubieran sido homogeneizados. Los resultados de los experimentos se resumen en la siguiente tabla.
En más detalle, la siguiente tabla muestra el efecto de aumentar la presión y/o el número de ciclos en el homogeneizador sobre la dispersabilidad de la proteína de grano de arroz (10 % de MS, relación de grano de arroz:caseinato 5:1, pH 7).
La siguiente tabla muestra el efecto de aumentar la presión y/o el número de ciclos en el homogeneizador sobre la dispersabilidad de la proteína de salvado de avena (10 % de MS, relación de salvado de avena:caseinato 20:1, pH 6,3).
La siguiente tabla ilustra que el aumento del pH de 7 a 8 tuvo un efecto positivo sobre la dispersabilidad de la proteína de grano de arroz (relación grano de arroz:caseinato 10:1; 150 MPa, 10 ciclos, 10 % de MS), en combinación con una etapa de presurización disruptiva.
La siguiente tabla ilustra que la variación de la proporción de grano de arroz: caseinato afecta la dispersabilidad de la proteína del grano (150 MPa, 10 ciclos, 10 % de MS, pH 7).
La siguiente tabla ilustra que al variar la relación de salvado de avena:caseinato afecta la dispersabilidad de la proteína del grano (100 MPa, 10 ciclos, 10 % de MS, pH 6,3).
La tabla más abajo ilustra que aplicando otro tipo de homogeneizador (homogeneizador Stansted de sobremesa) capaz de operar a presiones más altas; la etapa de presurización disruptiva es más efectiva que en un homogeneizador Panda (GEA) limitado a un funcionamiento a un máximo de 150 MPa.
De los resultados anteriores se concluyó que es posible mejorar significativamente la dispersabilidad de diferentes proteínas de granos mediante un procedimiento que involucra caseína y una tecnología disruptiva.
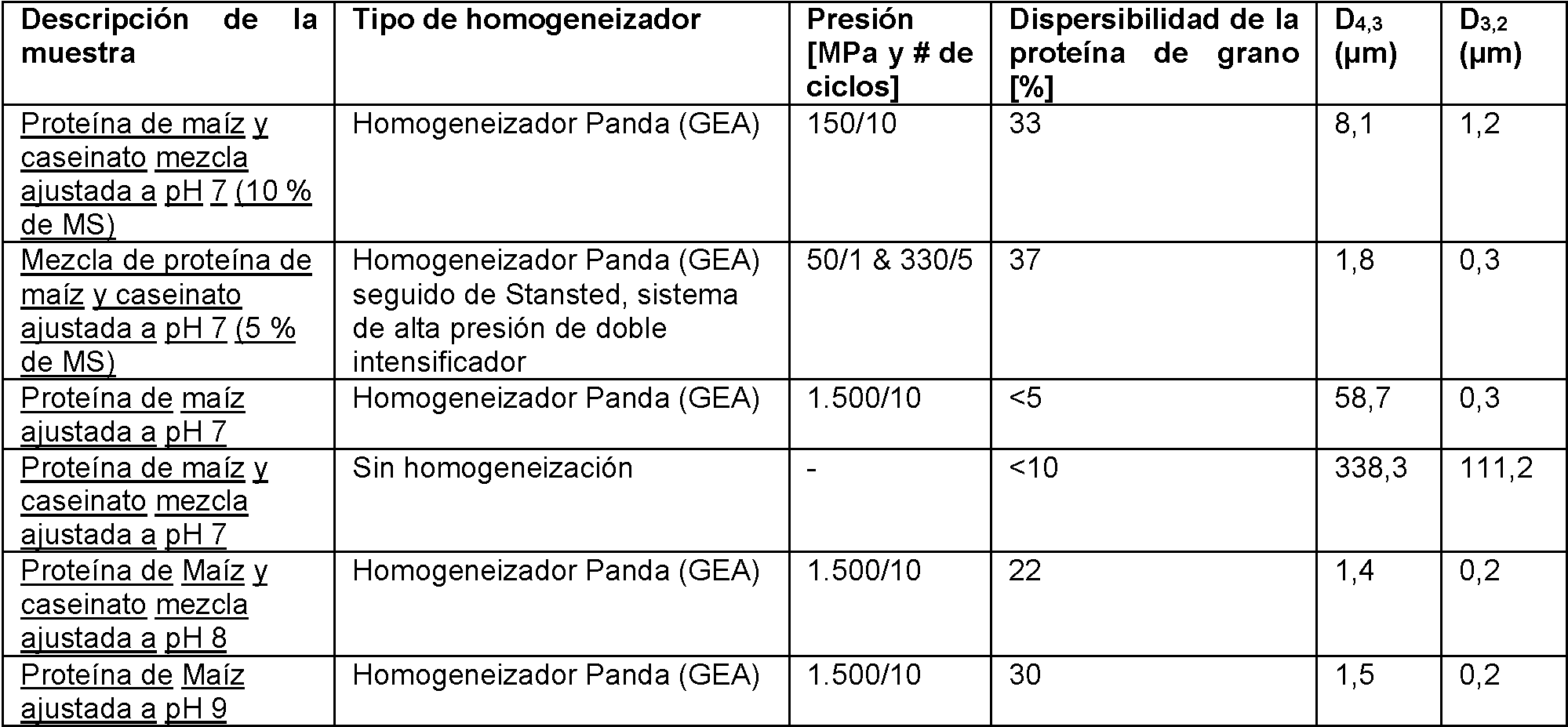
Tamaños de partículas
La tabla más abajo muestra algunos tamaños de partículas típicos medidos mediante el uso de un Malvern MastersizerX (Sysmex) operado de acuerdo con las instrucciones del fabricante. Las muestras se suspendieron en el Malvern Hydro 2000G en agua desmineralizada (bomba a 1.500 rpm, agitando a 300 rpm). Como puede verse en la tabla más abajo, la etapa de homogeneización dio como resultado una clara disminución del tamaño de partícula (valor promedio de 2 series de muestras medidas por duplicado). La centrifugación a 1.360 g dio como resultado la eliminación de la fracción de partículas más grandes dando como resultado una fracción sobrenadante que contiene partículas híbridas más pequeñas.
Estabilidad térmica
Un ensayo de estabilidad térmica en una dispersión coloidal de partículas híbridas de salvado de avena-caseinato (salvado de avena:caseinato 20:1, 10 % de MS, pH 6,3, 10*100 MPa) en comparación con proteína de salvado de avena homogeneizada en ausencia de caseinato (10 % de salvado de avena) y mezcla no homogeneizada de salvado de avena y caseinato (20:1). El ensayo de estabilidad térmica se realizó al 2,5 % de MS. Las dispersiones se mantuvieron a 90 °C durante 35 min. Posteriormente se centrifugaron (10 min de centrifugación a 1.360 g). Se determinó la estabilidad térmica expresada, como el porcentaje de proteína que quedaba en el sobrenadante. Las partículas híbridas eran más termoestables en comparación con el salvado de avena homogeneizado en ausencia de caseinato (10 % de salvado de avena) y mezcla no homogeneizada de salvado de avena y caseinato (20:1). Especialmente, las partículas híbridas de las que se eliminaron las partículas más grandes mediante centrifugación (10 min a 1.360 g) no mostraron visualmente sedimentación después del calentamiento.
La Figura 1 muestra imágenes de muestras calentadas durante 35 min a 90 °C, incubadas durante la noche a 4 °C (NO centrifugadas). De izquierda a derecha: mezcla no homogeneizada de salvado de avena y caseinato (20:1), mezcla homogeneizada de salvado de avena y caseinato (20:1), mezcla homogeneizada y centrifugada de salvado de avena y caseinato (20:1) y salvado de avena proteica homogeneizada en ausencia de caseinato (10 % de salvado de avena).
Además, se realizó una prueba de estabilidad térmica (2,5 % de MS, 30 min a 90 °C) en una dispersión coloidal de partículas híbridas de grano de arroz-caseinato (grano de arroz:caseinato 5:1, 10 % de MS, pH 7, 10*100 MPa) en comparación con la proteína de grano de arroz homogeneizada en ausencia de caseinato (10 % de grano de arroz) y mezcla no homogeneizada de grano de arroz y caseinato (20:1). La estabilidad térmica se realizó al 2,5 % de MS. Se vio claramente que las partículas híbridas eran más termoestables en comparación con el grano de arroz homogeneizado en ausencia de caseinato (10 % de grano de arroz) y mezcla no homogeneizada de grano de arroz y caseinato (5:1). Especialmente, las partículas híbridas de las que se eliminaron las partículas más grandes mediante centrifugación (10 min a 1.360 g) mostraron visualmente una pequeña sedimentación después del calentamiento. La Figura 2 muestra una imagen de muestras calentadas durante 30 minutos a 90 °C, centrifugadas a 1.360 g durante 10 min a TA. De izquierda a derecha: mezcla homogeneizada de grano de arroz y caseinato (5:1), mezcla homogeneizada y centrifugada de grano de arroz y caseinato (5:1), proteína de grano de arroz homogeneizada en ausencia de caseinato (10 % de grano de arroz) y mezcla no homogeneizada de grano de arroz y caseinato (5:1).
La tabla más abajo muestra la estabilidad térmica después de calentar durante 30 min a 90 °C (2,5 % de MS), expresada como el porcentaje de proteína que se determina en el sobrenadante (10 min de centrifugación a 1.360 g) en comparación con las muestras no calentadas. Puede verse claramente que para las partículas híbridas se mantiene más proteína en el sobrenadante después del calentamiento, lo que indica que las partículas híbridas son más termoestables que las muestras de control.
La estabilidad de las mezclas de caseinato de avena calentadas a (2.5 % de MS; 30 min 90 °C) (preparadas en una relación de salvado de avena: caseinato 10:1, 10 %, pH 6.3, 10*100 MPa) y las referencias también se determinaron mediante el uso de un Turbiscan™ AGS (formulación); las muestras analizadas fueron:
51 = Salvado de avena:caseinato 10:1, 10 % de MS, 10* 100 MPa, pH 6,3
52 = Sobrenadante de S1 (después de centrifugación durante 10 min a 1.360 g)
R1 = Salvado de avena: caseinato 10:1 sin tratamiento
R2 = salvado de avena, 10 % de MS, 10* 100 MPa, pH 6,3
R3 = 10 % de caseinato
Las mediciones se realizaron en celdas de medición de vidrio cilíndricas. La fuente de luz aplicada fue un LED infrarrojo cercano a pulso. Dos sensores ópticos simultáneos recibieron respectivamente la luz transmitida a través de la muestra (0° de la radiación incidente) y la luz retrodispersada por la muestra (135° de la radiación incidente). El cabezal de lectura óptico escaneó la longitud de la muestra, adquiriendo datos de transmisión y retrodispersión cada 40 pm. Las muestras se midieron cada dos horas durante 26 horas a 30 °C. Al comienzo de la medición Turbiscan, la muestra de referencia Salvado de avena.caseinato 10:1 sin tratamiento (R1), ya estaba separado en fases. Las otras muestras eran homogéneas al inicio de la medición.
Para comparar la desestabilización de las diferentes muestras, se utilizó el cálculo del Índice de Estabilidad de Turbiscan (TSI). El TSI suma todas las variaciones de la muestra, lo que da como resultado un número único que refleja la desestabilización de una muestra determinada. Cuanto mayor sea el TSI, más fuerte será la desestabilización de la muestra.
Se encontró que las partículas híbridas de salvado de avena-caseinato eran más estables que las referencias, mezcla no homogeneizada de salvado de avena y caseinato (R1) y salvado de avena homogeneizado (R2) (como se esperaba la solución de caseinato era estable (R3)). El más estable fue S2, la fracción del sobrenadante de la mezcla homogeneizada de caseinato de salvado de avena. Después de 22 horas, tenía un valor de TSI de 2, en comparación con 30 para R2, 8 para R1 y 4 para R3.
Más resultados para la proteína de maíz
Con más detalle, la siguiente tabla muestra el efecto del pH durante la homogeneización sobre la dispersabilidad de la proteína de maíz (relación de la proteína de maíz:caseinato 5:1).
• Guía del operador, capítulo 6, Malvern Mastersize X: D4,3 = diámetro medio del volumen y D3,2 = diámetro medio del área superficial, también conocido como la media de Sauter.
Ejemplo 2: Tecnologías de dispersión
En este ejemplo se probó la influencia de diferentes procedimientos de dispersión en la producción de dispersiones de proteínas vegetales con mejor estabilidad. Se produjeron cuatro dispersiones de partida:
A) 10 % de polvo de salvado de avena, 1 % de caseinato sódico
B) 10 % de polvo de grano de arroz, 1 % de caseinato sódico
C) 10 % de polvo de salvado de avena
D) 10 % de polvo de grano de arroz
Las suspensiones se usaron a su pH natural. Las dispersiones se sometieron a varios tratamientos.
Secado por pulverización (ejemplo comparativo)
El secado por pulverización se realizó mediante el uso de un secador piloto equipado con una boquilla de presión Schlick 121 que se hizo funcionar mediante el uso de una presión de pulverización de 80 bar. La temperatura de entrada y salida fue de 170 °C y 70 °C respectivamente. La temperatura del producto fue de 50 °C. Se produjeron dos variantes diferentes mediante el uso de la dispersión A: 1. La suspensión se seca por pulverización directamente 2. La suspensión se homogeneiza a una presión de 35 MPa antes del secado por pulverización. después de un día de almacenamiento los polvos producidos se disolvieron a una concentración del 10 %. Para dispersar adecuadamente el polvo las soluciones se sometieron a turrax durante 1 minuto mediante el uso de un turrax de laboratorio IKA a 14.000 rpm. Subsecuentemente, las soluciones se almacenaron durante la noche a 4 °C. La estabilidad de estas suspensiones se analizó diluyendo primero la dispersión por un factor de dos y luego centrifugando durante 10 min a 1.360 g. Los resultados se muestran en la tabla a continuación.
Dispax (ejemplo comparativo)
Los dispositivos rotor-estator se usan con frecuencia como herramientas de dispersión. Aquí usamos el reactor/homogeneizador IKA "DISPAX" para dispersar las dispersiones mencionadas anteriormente.
Las suspensiones se bombearon a 20 °C a través del Dispax a dos velocidades (10 L/h y 20 L/h, correspondientes con un tiempo de referencia dentro de la cámara de mezcla de aproximadamente 30 s y 15 s respectivamente). Durante el tratamiento con Dispax la temperatura ascendió a un máximo de 60 °C. Las suspensiones producidas se analizaron para determinar su estabilidad mediante el uso del procedimiento de centrifugación mencionado anteriormente. Los resultados se muestran en la tabla a continuación.
Los resultados muestran que Dispax es menos efectivo que la homogeneización repetida a alta presión para producir una suspensión estable. Esto se puede explicar por el hecho de que la homogeneización a alta presión generalmente introduce más energía en el producto que un Dispax (108 J/m3 en comparación con 107 J/m3).
Ultrasonido (ejemplo comparativo)
Se sabe que el ultrasonido es un procedimiento intensivo que consume mucha energía. Típicamente alrededor de 109 J/m3 se agrega durante el tratamiento con ultrasonido. Las pruebas se realizaron mediante el uso de la configuración de Cavitus US a escala de laboratorio con un volumen de aproximadamente 1 L. El dispositivo US rellenado con un producto (a 15 °C) y se aplicó US durante 2, 4, 8 o 12 min. Cada prueba se realizó con material nuevo. Se usó la potencia máxima, correspondiente a 900 W. Durante el tratamiento, la temperatura ascendió a 25 (2 min), 40 (4 min), 53 (8 min) y 60 °C (12 min). Las suspensiones producidas se analizaron para determinar su estabilidad mediante el uso del procedimiento de centrifugación mencionado anteriormente. Los resultados se muestran en la tabla a continuación.
A pesar de que el tratamiento de US consume mucha energía, la estabilidad de las suspensiones producidas es mucho menor que la de las suspensiones producidas mediante el uso de la homogeneización a alta presión (ver arriba). Dado que las partículas de sedimentación en las muestras tratadas con US parecían ser bastante voluminosas, especulamos que se produjeron partículas proteicas vegetales muy pequeñas que floculaban, lo que deshace parcialmente el efecto del tratamiento de US.
Molino coloidal (ejemplo comparativo)
Los molinos coloidales funcionan según el principio rotor-estator: un rotor gira a altas velocidades (2.000 - 18.000 rpm). Los altos niveles resultantes de cizallamiento hidráulico aplicados al líquido de proceso pueden romper las estructuras del fluido. Las muestras (AD) se trataron a temperatura ambiente y velocidad máxima mediante el uso de un IKA MagicLAB® (equipado con módulo MK/MKO). Como puede verse en la tabla más abajo no se observó ningún efecto significativo del tratamiento en presencia de caseinato (muestra A vs. C y muestra B vs. D).
Microfluidizador (procedimiento de acuerdo con la invención)
La microfluidización es otra pieza de dispersión que consume mucha energía. Los experimentos se realizaron mediante el uso de un Microfluidizador de Microfluidos Modelo M-110Y mediante el uso del disruptor tipo z (H30Z) con una dimensión interna de 200 micrones. Las suspensiones se pasaron a través del microfluidizador 3 veces. Al comienzo del experimento, las suspensiones estaban a temperatura ambiente. Después del tratamiento con el microfluidizador, la temperatura había aumentado a 30 °C o 45 °C cuando se usaba una presión de 40 MPa.
Los resultados muestran que la presencia de caseinato aumenta la estabilidad de la suspensión de avena.
Ejemplo 3
El siguiente experimento demuestra que el caseinato se une a las partículas proteicas vegetales durante la etapa disruptiva. Se prepararon partículas híbridas de proteína de grano de arroz y caseinato en una relación de polvo de grano de arroz:polvo de caseinato de 5:1, 10 % de MS, pH 6,9, 10* 100 MPa. Antes de su uso, la solución de caseinato se centrifugó al 10 % de MS durante 1 ha 100.000 g y subsequentemente se filtró (2x) a través de un filtro de 0,45 pm. Las dispersiones al 10% de MS de las partículas híbridas (homogeneizadas), la mezcla no homogeneizada de polvo de grano de arroz y caseinato, el polvo de grano de arroz homogeneizado en ausencia de caseinato y el caseinato se diluyeron al 5 % de MS y se centrifugaron durante 10 min a 1.360 g (20 °C).
Los sobrenadantes se filtraron subsecuentemente a través de filtros de 0,8 pm y se analizaron en cuanto al contenido de caseinato mediante el uso de la HPLC de fase inversa. La tabla más abajo muestra claramente que para las partículas híbridas (mezcla homogeneizada de grano de arroz y polvo de caseinato) está presente menos caseinato en el filtrado en comparación con las referencias, mezcla no homogeneizada y solución de caseinato. Esto indica claramente la interacción de la proteína de caseinato con la proteína del grano de arroz, evitando que parte del caseinato atraviese la membrana.
Como se esperaba en el filtrado de la dispersión de polvo de grano de arroz homogeneizado, no se pudo determinar caseinato u otras proteínas en el intervalo de detección. Como el contenido de caseína en el filtrado de la referencia de caseinato está de acuerdo con el valor estimado, el tamaño de poro seleccionado (0,8 pm) es completamente permeable para la proteína de caseinato.
Ejemplo 4: Bebida de ácido láctico
Se usaron partículas híbridas preparadas a partir de proteína de salvado de avena (relación granoproteína:caseinato = 10:1, 10*1.000 bar, pH 6,3) para la preparación de una bebida de ácido láctico (BAL) de acuerdo con una receta estándar. Se usó como referencia un bAl a base de lácteos.
Las recetas contenían azúcar, pectina y ácido y fueron tratadas con UHT. El producto se evaluó después de 1 semana de almacenamiento a 5 °C.
Se encontró que las dos variedades eran estables visual, física y microbiológicamente. La composición y el pH fueron bien comparables. Se determinó que el sabor, la textura y la sensación en la boca de todas las muestras eran buenos.
Ejemplo 5: efecto de los caseinatos vs. caseína micelar o leche en polvo
La siguiente tabla muestra el comportamiento de otro tipo de caseína(tos) en relación con el caseinato sódico sobre la dispersabilidad tanto del salvado de avena como de la proteína del grano de arroz (normalizada en caseinato sódico y corregida por la dispersabilidad en ausencia de caseína(caseinato)). Se realizaron diez ciclos de homogeneización a 100 MPa, 10 % en peso. de materia seca; relación peso a peso preparación de proteína vegetal: caseína(caseinato) 5:1 y pH 6,3 (salvado de avena) o pH 7 (grano de arroz). El rendimiento del caseinato sódico se comparó con el del caseinato de calcio (Excellion CaCasS, FrieslandCampina DMV; 92,6 % de proteína), aislado de caseína micelar (MCI 80, Refit, FrieslandCampina DOMO; 80,3 % de proteína), leche en polvo desnatada a temperatura media (SMP, 33,1 % proteína) y caseinato sódico desamidado *. En la configuración experimental, las adiciones de caseinato de calcio, MCI y SMP se estandarizaron en proteínas mediante el uso de caseinato como referencia. Claramente puede verse que de los diferentes tipos de preparaciones de caseína(caseinato), los caseinatos sódicos (desamidados) funcionan mejor. El caseinato de calcio funciona mejor que la caseína micelar y el SMP con proteína de salvado de avena.
Tabla: dispersabilidad (normalizada en caseinato sódico = 100 %)
Ejemplo 6: Efecto de la pre-homogeneización
Se homogeneizó una dispersión acuosa de MS al 10% de polvo de salvado de avena durante 9 ciclos a 100 MPa (R2). Subsecuentemente, se añadió caseinato para obtener una relación grano-proteína en polvo: polvo de caseinato de 10:1. A continuación, el lote se dividió en 4 partes iguales. Una parte se homogeneizó nuevamente durante 1 ciclo a 100 MPa (S1), a una parte se le dio un tratamiento estático de alta presión de 100 MPa (S2), una parte se calentó a 70 °C y se mantuvo a esa temperatura durante 1 h (S3), la cuarta parte no se trató nuevamente(S4). En la tabla más abajo se da la dispersabilidad de la proteína de grano después de las diferentes muestras tratadas.
continuación
Claims (9)
1. Procedimiento para la preparación de una dispersión acuosa que comprende partículas proteicas coloidales dispersas en un fluido acuoso, cuyas partículas proteicas coloidales comprenden caseinato y una o más proteínas vegetales de una semilla de una planta de la familia Poaceae, comprendiendo el procedimiento
a) proporcionar una dispersión intermedia de caseinato y partículas que comprenden dicha una o más proteínas vegetales en un fluido acuoso; y
b) someter la dispersión intermedia a una etapa de presurización disruptiva que comprende el tratamiento en un homogeneizador a una presión de al menos 40 MPa, en el que las partículas que comprenden la una o más proteínas vegetales se rompen y se forma la dispersión acuosa que comprende las partículas proteicas coloidales.
2. Procedimiento de acuerdo con la reivindicación 1, en el que la relación peso a peso de dicha proteína vegetal con respecto a caseinato en la dispersión intermedia está en el intervalo de 1:1 a 20:1, preferentemente en el intervalo de 3:1 a 15:1, en particular en el intervalo de 4:1 a 12:1, más en particular en el intervalo de 5:1 a 10:1.
3. Procedimiento de acuerdo con cualquiera de las reivindicaciones anteriores, en el que el contenido de proteína de la dispersión intermedia está en el intervalo de 1-30 % en peso. en particular en el intervalo de 5-25 % en peso, más en particular en el intervalo de 10-20 % en peso.
4. Procedimiento de acuerdo con cualquiera de las reivindicaciones anteriores en el que el contenido de dicha una o más proteínas vegetales en la dispersión intermedia es de al menos 25 % en peso, preferentemente al menos 50 % en peso del contenido de proteína total en la dispersión intermedia, con mayor preferencia al menos 65 % en peso, en particular al menos 80 % en peso.
5. Procedimiento de acuerdo con cualquiera de las reivindicaciones anteriores, en el que la presurización comprende el tratamiento en un homogeneizador a una presión de 50-500 MPa, en particular 100-250 MPa.
6. Procedimiento de acuerdo con cualquiera de las reivindicaciones anteriores, en el que el pH durante la presurización está en el intervalo de 5,5-9,0, preferentemente en el intervalo de 6,0-8,0, en particular en el intervalo de 6,3-7,5.
7. Procedimiento de acuerdo con cualquiera de las reivindicaciones anteriores, en el que dicha una o más proteínas vegetales son de un grano, preferentemente de un cereal o pasto seleccionado del grupo de arroz, avena, trigo, maíz, cebada, centeno y sorgo, con mayor preferencia de un cereal o pasto seleccionado del grupo de arroz, avena, trigo y maíz.
8. Procedimiento de acuerdo con la reivindicación 7, en el que una o más proteínas vegetales en la dispersión intermedia se seleccionan del grupo de proteínas del grano de arroz, proteínas de salvado de avena, partículas de gluten, y prolaminas.
9. Procedimiento de acuerdo con cualquiera de las reivindicaciones anteriores, en el que las partículas que comprenden dicha una o más proteínas vegetales en la dispersión intermedia tienen un D(4,3) en el intervalo de 1 pm a 1 mm, preferentemente en el intervalo de 5-400 pm y/o en el que las partículas coloidales tienen un D(4,3) en el intervalo de 0,2 pm a 4 pm, en particular de 0,4 a 2 pm, determinado por dispersión dinámica de la luz.
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| EP15154318 | 2015-02-09 | ||
| PCT/NL2016/050090 WO2016129998A1 (en) | 2015-02-09 | 2016-02-08 | Method for preparing an aqueous dispersion of a poorly dispersible plant protein |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| ES2833555T3 true ES2833555T3 (es) | 2021-06-15 |
Family
ID=52464248
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| ES16715125T Active ES2833555T3 (es) | 2015-02-09 | 2016-02-08 | Procedimiento para la preparación de una dispersión acuosa de una proteína vegetal poco dispersable |
Country Status (12)
| Country | Link |
|---|---|
| US (1) | US20180020695A1 (es) |
| EP (1) | EP3256002B1 (es) |
| JP (1) | JP6937246B2 (es) |
| CN (1) | CN107404932B (es) |
| BR (1) | BR112017016946B1 (es) |
| CA (1) | CA2975672C (es) |
| DK (1) | DK3256002T3 (es) |
| ES (1) | ES2833555T3 (es) |
| MX (1) | MX2017010221A (es) |
| PH (1) | PH12017550076A1 (es) |
| PL (1) | PL3256002T3 (es) |
| WO (1) | WO2016129998A1 (es) |
Families Citing this family (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP3256002B1 (en) | 2015-02-09 | 2020-09-23 | FrieslandCampina Nederland B.V. | Method for preparing an aqueous dispersion of a poorly dispersible plant protein |
| MX2019002109A (es) * | 2016-08-25 | 2019-12-05 | Perfect Day Inc | Productos alimenticios que contienen proteínas de la leche y proteínas no animales, y métodos para su producción. |
| US10806165B2 (en) | 2018-04-24 | 2020-10-20 | Stokely-Van Camp, Inc. | Ready-to-drink plant protein beverage product and methods for making same |
| US11191289B2 (en) | 2018-04-30 | 2021-12-07 | Kraft Foods Group Brands Llc | Spoonable smoothie and methods of production thereof |
| BE1027671B1 (nl) * | 2019-08-12 | 2021-05-10 | Anheuser Busch Inbev Sa | Poedervormige eiwitsamenstelling |
| AU2021481664A1 (en) * | 2021-12-30 | 2024-08-08 | Oatly Ab | Liquid oat composition and method for production thereof |
Family Cites Families (17)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| DE706115C (de) | 1939-02-22 | 1941-05-19 | Hermann Plauson | Herstellung von Milcheiweiss enthaltenden Getreideextraktionsprodukten |
| USRE32725E (en) | 1978-12-26 | 1988-08-02 | Central Soya Company, Inc. | Water-soluble vegetable protein aggregates |
| US5418010A (en) * | 1990-10-05 | 1995-05-23 | Griffith Laboratories Worldwide, Inc. | Microencapsulation process |
| US5736178A (en) * | 1995-05-02 | 1998-04-07 | Opta Food Ingredients, Inc. | Colloidal dispersions of gluten, method of making and use therefor |
| US6605311B2 (en) | 2000-06-22 | 2003-08-12 | The Procter & Gamble Company | Insoluble protein particles |
| US20030104033A1 (en) * | 2001-07-13 | 2003-06-05 | Lai Chon-Si | Enteral formulations |
| US7101585B2 (en) | 2004-04-15 | 2006-09-05 | Solae, Llc | Ultra high pressure homogenization process for making a stable protein based acid beverage |
| US7638155B2 (en) * | 2005-06-23 | 2009-12-29 | Solae, Llc | Process for making soy protein products having reduced off-flavor |
| DE102005031468A1 (de) * | 2005-07-04 | 2007-01-18 | Basf Ag | Wässrige Suspensionen schwer wasserlöslicher oder wasserunlöslicher Wirkstoffe und daraus hergestellte Trockenpulver |
| US7989592B2 (en) * | 2006-07-21 | 2011-08-02 | Mgp Ingredients, Inc. | Process for preparing hybrid proteins |
| WO2008143507A2 (en) * | 2007-05-21 | 2008-11-27 | Nizo Food Research B.V. | Oxidatively cross-linked protein-based encapsulates |
| EP2217088A1 (en) * | 2007-11-29 | 2010-08-18 | NIZO Food Research B.V. | Method for making protein-based encapsulates |
| CN101518350B (zh) * | 2009-03-27 | 2012-07-11 | 四川斯比泰饮料食品有限公司 | 双蛋白平衡乳酸菌饮料的制备方法 |
| US20110269849A1 (en) * | 2010-05-03 | 2011-11-03 | Yuan Yao | Emulsions and Methods for the Preparation Thereof, and Methods for Improving Oxidative Stability of Lipids |
| FR2995763B1 (fr) | 2012-09-21 | 2016-09-02 | Roquette Freres | Assemblage d'au moins une proteine vegetale et d'au moins une proteine laitiere |
| FR3019005B1 (fr) | 2014-03-26 | 2021-03-26 | Roquette Freres | Assemblage d'au moins une proteine vegetale et d'au moins une proteine laitiere, sa preparation et ses utilisations |
| EP3256002B1 (en) | 2015-02-09 | 2020-09-23 | FrieslandCampina Nederland B.V. | Method for preparing an aqueous dispersion of a poorly dispersible plant protein |
-
2016
- 2016-02-08 EP EP16715125.7A patent/EP3256002B1/en active Active
- 2016-02-08 ES ES16715125T patent/ES2833555T3/es active Active
- 2016-02-08 PL PL16715125T patent/PL3256002T3/pl unknown
- 2016-02-08 WO PCT/NL2016/050090 patent/WO2016129998A1/en active Application Filing
- 2016-02-08 BR BR112017016946-0A patent/BR112017016946B1/pt active IP Right Grant
- 2016-02-08 CN CN201680014517.3A patent/CN107404932B/zh active Active
- 2016-02-08 JP JP2017560459A patent/JP6937246B2/ja active Active
- 2016-02-08 CA CA2975672A patent/CA2975672C/en active Active
- 2016-02-08 DK DK16715125.7T patent/DK3256002T3/da active
- 2016-02-08 MX MX2017010221A patent/MX2017010221A/es unknown
- 2016-02-08 US US15/549,438 patent/US20180020695A1/en not_active Abandoned
-
2017
- 2017-08-08 PH PH12017550076A patent/PH12017550076A1/en unknown
Also Published As
| Publication number | Publication date |
|---|---|
| JP6937246B2 (ja) | 2021-09-22 |
| CA2975672C (en) | 2023-01-31 |
| EP3256002B1 (en) | 2020-09-23 |
| BR112017016946A2 (pt) | 2018-04-03 |
| CN107404932B (zh) | 2020-07-03 |
| DK3256002T3 (da) | 2020-12-14 |
| WO2016129998A1 (en) | 2016-08-18 |
| CA2975672A1 (en) | 2016-08-18 |
| BR112017016946B1 (pt) | 2022-09-20 |
| CN107404932A (zh) | 2017-11-28 |
| JP2018506303A (ja) | 2018-03-08 |
| PH12017550076A1 (en) | 2018-02-05 |
| PL3256002T3 (pl) | 2021-04-06 |
| MX2017010221A (es) | 2017-12-04 |
| EP3256002A1 (en) | 2017-12-20 |
| US20180020695A1 (en) | 2018-01-25 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| ES2833555T3 (es) | Procedimiento para la preparación de una dispersión acuosa de una proteína vegetal poco dispersable | |
| US11172691B2 (en) | Product analogs or components of such analogs and processes for making same | |
| Mäkinen et al. | Physicochemical and acid gelation properties of commercial UHT-treated plant-based milk substitutes and lactose free bovine milk | |
| US20240057651A1 (en) | Nutritional formulations such as a yoghurt, cream, cream dessert or frozen dessert, comprising a pea protein isolate, and the use of the formulation as a source of protein | |
| ES2628193T3 (es) | Polvo granulado que contiene proteínas vegetales y fibras, su procedimiento de obtención y sus utilizaciones | |
| ES2632178T3 (es) | Polvo granulado que contiene proteínas vegetales y maltodextrinas, su procedimiento de obtención y sus utilizaciones | |
| CN101410020B (zh) | 乳清蛋白微胶粒 | |
| JP6525213B2 (ja) | Cmp含有高タンパク変性ホエータンパク質組成物、それらを含む製品、およびその使用 | |
| CN101410024A (zh) | 富含蛋白质的冷冻甜点 | |
| BRPI0809949A2 (pt) | Pó de grãos aglomerados, secados por atomização, hidrolisados e produtos alimentícios bebíveis | |
| WO2020002454A1 (en) | Instant beverage powder based on blg | |
| ES2839455T3 (es) | Método de producción de agregados de proteínas de suero de leche gelificable con ácido concentrados o secos, y composiciones y productos alimenticios afines | |
| CN101410026B (zh) | 乳清蛋白微胶粒的原位制备 | |
| JP2022526283A (ja) | フィールドビーンタンパク質組成物 | |
| JP2019503694A (ja) | 乳清タンパク質系液体栄養組成物 | |
| JP2023017803A (ja) | 低下した粘度を有する高タンパク酸性液体乳製品、それを製造する方法及び関連する成分 | |
| CN108463113A (zh) | 用于制备奶精的方法 | |
| Devle et al. | Rheological characterization of milk during digestion with human gastric and duodenal enzymes | |
| CN106659174A (zh) | 制备酸性乳饮料的方法以及所述酸性乳饮料 |