ES2700784T3 - Extracto de partes aéreas de Gynandropsis gynandra o Cleome gynandra y composiciones cosméticas, dermatológicas o farmacéuticas que lo comprenden - Google Patents
Extracto de partes aéreas de Gynandropsis gynandra o Cleome gynandra y composiciones cosméticas, dermatológicas o farmacéuticas que lo comprenden Download PDFInfo
- Publication number
- ES2700784T3 ES2700784T3 ES11804695T ES11804695T ES2700784T3 ES 2700784 T3 ES2700784 T3 ES 2700784T3 ES 11804695 T ES11804695 T ES 11804695T ES 11804695 T ES11804695 T ES 11804695T ES 2700784 T3 ES2700784 T3 ES 2700784T3
- Authority
- ES
- Spain
- Prior art keywords
- extract
- skin
- agents
- advantageously
- composition according
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
- 239000000284 extract Substances 0.000 title claims abstract description 138
- 235000012469 Cleome gynandra Nutrition 0.000 title claims abstract description 59
- 239000002537 cosmetic Substances 0.000 title claims description 24
- 239000008194 pharmaceutical composition Substances 0.000 title claims description 5
- 241001406860 Gynandropsis gynandra Species 0.000 title abstract description 5
- 239000000203 mixture Substances 0.000 claims abstract description 73
- PEDCQBHIVMGVHV-UHFFFAOYSA-N Glycerine Chemical compound OCC(O)CO PEDCQBHIVMGVHV-UHFFFAOYSA-N 0.000 claims abstract description 36
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 claims abstract description 18
- 235000013824 polyphenols Nutrition 0.000 claims abstract description 17
- -1 flavonoids polyphenols Chemical class 0.000 claims abstract description 16
- 150000008442 polyphenolic compounds Chemical class 0.000 claims abstract description 15
- 229930003935 flavonoid Natural products 0.000 claims abstract description 14
- 235000017173 flavonoids Nutrition 0.000 claims abstract description 14
- LNTHITQWFMADLM-UHFFFAOYSA-N gallic acid Chemical compound OC(=O)C1=CC(O)=C(O)C(O)=C1 LNTHITQWFMADLM-UHFFFAOYSA-N 0.000 claims abstract description 14
- 150000002215 flavonoids Chemical class 0.000 claims abstract description 13
- 239000002904 solvent Substances 0.000 claims abstract description 13
- LYCAIKOWRPUZTN-UHFFFAOYSA-N Ethylene glycol Chemical compound OCCO LYCAIKOWRPUZTN-UHFFFAOYSA-N 0.000 claims abstract description 10
- ULWHHBHJGPPBCO-UHFFFAOYSA-N propane-1,1-diol Chemical compound CCC(O)O ULWHHBHJGPPBCO-UHFFFAOYSA-N 0.000 claims abstract description 10
- 239000000546 pharmaceutical excipient Substances 0.000 claims abstract description 8
- 229940074391 gallic acid Drugs 0.000 claims abstract description 7
- 235000004515 gallic acid Nutrition 0.000 claims abstract description 7
- WGCNASOHLSPBMP-UHFFFAOYSA-N hydroxyacetaldehyde Natural products OCC=O WGCNASOHLSPBMP-UHFFFAOYSA-N 0.000 claims abstract description 5
- 238000000956 solid--liquid extraction Methods 0.000 claims abstract description 3
- 244000227271 Cleome gynandra Species 0.000 claims description 55
- 238000000034 method Methods 0.000 claims description 32
- 208000002874 Acne Vulgaris Diseases 0.000 claims description 29
- 206010000496 acne Diseases 0.000 claims description 29
- 210000004400 mucous membrane Anatomy 0.000 claims description 23
- 239000003795 chemical substances by application Substances 0.000 claims description 20
- 238000004519 manufacturing process Methods 0.000 claims description 19
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 claims description 18
- 208000035475 disorder Diseases 0.000 claims description 18
- 230000002265 prevention Effects 0.000 claims description 17
- 102000004196 processed proteins & peptides Human genes 0.000 claims description 16
- 108090000765 processed proteins & peptides Proteins 0.000 claims description 16
- 244000025272 Persea americana Species 0.000 claims description 15
- 235000008673 Persea americana Nutrition 0.000 claims description 15
- 150000001875 compounds Chemical class 0.000 claims description 14
- 239000003921 oil Substances 0.000 claims description 14
- 241000196324 Embryophyta Species 0.000 claims description 13
- 230000035876 healing Effects 0.000 claims description 13
- 235000019198 oils Nutrition 0.000 claims description 13
- 230000003712 anti-aging effect Effects 0.000 claims description 10
- 241000219745 Lupinus Species 0.000 claims description 9
- 230000003020 moisturizing effect Effects 0.000 claims description 9
- 210000002374 sebum Anatomy 0.000 claims description 9
- 235000010469 Glycine max Nutrition 0.000 claims description 8
- 229930182558 Sterol Natural products 0.000 claims description 8
- 239000004480 active ingredient Substances 0.000 claims description 8
- 230000003110 anti-inflammatory effect Effects 0.000 claims description 8
- 239000003112 inhibitor Substances 0.000 claims description 8
- 235000003702 sterols Nutrition 0.000 claims description 8
- 235000000346 sugar Nutrition 0.000 claims description 8
- 150000008163 sugars Chemical class 0.000 claims description 8
- 206010033733 Papule Diseases 0.000 claims description 7
- 239000003963 antioxidant agent Substances 0.000 claims description 7
- 208000008742 seborrheic dermatitis Diseases 0.000 claims description 7
- 208000001840 Dandruff Diseases 0.000 claims description 6
- 206010015150 Erythema Diseases 0.000 claims description 6
- 240000000759 Lepidium meyenii Species 0.000 claims description 6
- 235000000421 Lepidium meyenii Nutrition 0.000 claims description 6
- 235000012902 lepidium meyenii Nutrition 0.000 claims description 6
- 239000003755 preservative agent Substances 0.000 claims description 6
- 230000008591 skin barrier function Effects 0.000 claims description 6
- 150000003432 sterols Chemical class 0.000 claims description 6
- 230000000475 sunscreen effect Effects 0.000 claims description 6
- 239000000516 sunscreening agent Substances 0.000 claims description 6
- 239000008158 vegetable oil Substances 0.000 claims description 6
- 235000013311 vegetables Nutrition 0.000 claims description 6
- 208000035484 Cellulite Diseases 0.000 claims description 5
- 240000006162 Chenopodium quinoa Species 0.000 claims description 5
- 206010049752 Peau d'orange Diseases 0.000 claims description 5
- 208000003251 Pruritus Diseases 0.000 claims description 5
- 229910052500 inorganic mineral Inorganic materials 0.000 claims description 5
- 239000002085 irritant Substances 0.000 claims description 5
- 230000004132 lipogenesis Effects 0.000 claims description 5
- 239000011707 mineral Substances 0.000 claims description 5
- 230000000485 pigmenting effect Effects 0.000 claims description 5
- 235000015112 vegetable and seed oil Nutrition 0.000 claims description 5
- 239000002677 5-alpha reductase inhibitor Substances 0.000 claims description 4
- 244000068988 Glycine max Species 0.000 claims description 4
- 239000013543 active substance Substances 0.000 claims description 4
- 239000003242 anti bacterial agent Substances 0.000 claims description 4
- 230000001914 calming effect Effects 0.000 claims description 4
- 239000003974 emollient agent Substances 0.000 claims description 4
- FREPJBZLNPPGDM-UHFFFAOYSA-N 4,4-dimethyl-2-undecyl-5h-1,3-oxazole Chemical compound CCCCCCCCCCCC1=NC(C)(C)CO1 FREPJBZLNPPGDM-UHFFFAOYSA-N 0.000 claims description 3
- SATHPVQTSSUFFW-UHFFFAOYSA-N 4-[6-[(3,5-dihydroxy-4-methoxyoxan-2-yl)oxymethyl]-3,5-dihydroxy-4-methoxyoxan-2-yl]oxy-2-(hydroxymethyl)-6-methyloxane-3,5-diol Chemical compound OC1C(OC)C(O)COC1OCC1C(O)C(OC)C(O)C(OC2C(C(CO)OC(C)C2O)O)O1 SATHPVQTSSUFFW-UHFFFAOYSA-N 0.000 claims description 3
- 229920000189 Arabinogalactan Polymers 0.000 claims description 3
- 239000001904 Arabinogalactan Substances 0.000 claims description 3
- 244000020551 Helianthus annuus Species 0.000 claims description 3
- 235000003222 Helianthus annuus Nutrition 0.000 claims description 3
- 241001465754 Metazoa Species 0.000 claims description 3
- 240000007594 Oryza sativa Species 0.000 claims description 3
- 235000007164 Oryza sativa Nutrition 0.000 claims description 3
- HCHKCACWOHOZIP-UHFFFAOYSA-N Zinc Chemical compound [Zn] HCHKCACWOHOZIP-UHFFFAOYSA-N 0.000 claims description 3
- 230000003266 anti-allergic effect Effects 0.000 claims description 3
- 235000019312 arabinogalactan Nutrition 0.000 claims description 3
- 239000012141 concentrate Substances 0.000 claims description 3
- 230000007803 itching Effects 0.000 claims description 3
- MQYXUWHLBZFQQO-QGTGJCAVSA-N lupeol Chemical compound C1C[C@H](O)C(C)(C)[C@@H]2CC[C@@]3(C)[C@]4(C)CC[C@@]5(C)CC[C@@H](C(=C)C)[C@@H]5[C@H]4CC[C@@H]3[C@]21C MQYXUWHLBZFQQO-QGTGJCAVSA-N 0.000 claims description 3
- PKGKOZOYXQMJNG-UHFFFAOYSA-N lupeol Natural products CC(=C)C1CC2C(C)(CCC3C4(C)CCC5C(C)(C)C(O)CCC5(C)C4CCC23C)C1 PKGKOZOYXQMJNG-UHFFFAOYSA-N 0.000 claims description 3
- 235000009566 rice Nutrition 0.000 claims description 3
- 238000007920 subcutaneous administration Methods 0.000 claims description 3
- 208000019553 vascular disease Diseases 0.000 claims description 3
- 229910052725 zinc Inorganic materials 0.000 claims description 3
- 239000011701 zinc Substances 0.000 claims description 3
- VBFBQEURBQANIX-UHFFFAOYSA-N (4-ethyl-2-undecyl-5h-1,3-oxazol-4-yl)methanol Chemical compound CCCCCCCCCCCC1=NC(CC)(CO)CO1 VBFBQEURBQANIX-UHFFFAOYSA-N 0.000 claims description 2
- JMQRHKPPXPCTGP-UHFFFAOYSA-N (4-methyl-2-undecyl-5h-1,3-oxazol-4-yl)methanol Chemical compound CCCCCCCCCCCC1=NC(C)(CO)CO1 JMQRHKPPXPCTGP-UHFFFAOYSA-N 0.000 claims description 2
- OYHQOLUKZRVURQ-NTGFUMLPSA-N (9Z,12Z)-9,10,12,13-tetratritiooctadeca-9,12-dienoic acid Chemical compound C(CCCCCCC\C(=C(/C\C(=C(/CCCCC)\[3H])\[3H])\[3H])\[3H])(=O)O OYHQOLUKZRVURQ-NTGFUMLPSA-N 0.000 claims description 2
- NHZLLKNRTDIFAD-UHFFFAOYSA-N 2,5-dihydro-1,3-oxazole Chemical compound C1OCN=C1 NHZLLKNRTDIFAD-UHFFFAOYSA-N 0.000 claims description 2
- CHAMUCPNQGNBLJ-VAWYXSNFSA-N 2-[(e)-heptadec-8-enyl]-4,4-dimethyl-5h-1,3-oxazole Chemical compound CCCCCCCC\C=C\CCCCCCCC1=NC(C)(C)CO1 CHAMUCPNQGNBLJ-VAWYXSNFSA-N 0.000 claims description 2
- 241001133760 Acoelorraphe Species 0.000 claims description 2
- 240000002791 Brassica napus Species 0.000 claims description 2
- 235000004977 Brassica sinapistrum Nutrition 0.000 claims description 2
- SNPLKNRPJHDVJA-ZETCQYMHSA-N D-panthenol Chemical compound OCC(C)(C)[C@@H](O)C(=O)NCCCO SNPLKNRPJHDVJA-ZETCQYMHSA-N 0.000 claims description 2
- 208000003367 Hypopigmentation Diseases 0.000 claims description 2
- 229940124091 Keratolytic Drugs 0.000 claims description 2
- 240000000894 Lupinus albus Species 0.000 claims description 2
- 235000010649 Lupinus albus Nutrition 0.000 claims description 2
- 235000019484 Rapeseed oil Nutrition 0.000 claims description 2
- 241001303601 Rosacea Species 0.000 claims description 2
- 206010039793 Seborrhoeic dermatitis Diseases 0.000 claims description 2
- 241000100615 Senegalia macrostachya Species 0.000 claims description 2
- 244000042314 Vigna unguiculata Species 0.000 claims description 2
- 235000010722 Vigna unguiculata Nutrition 0.000 claims description 2
- 240000008042 Zea mays Species 0.000 claims description 2
- 235000002017 Zea mays subsp mays Nutrition 0.000 claims description 2
- HCIRJRYSFLWMMS-ZHACJKMWSA-N [2-[(e)-heptadec-8-enyl]-4-methyl-5h-1,3-oxazol-4-yl]methanol Chemical compound CCCCCCCC\C=C\CCCCCCCC1=NC(C)(CO)CO1 HCIRJRYSFLWMMS-ZHACJKMWSA-N 0.000 claims description 2
- 150000001413 amino acids Chemical class 0.000 claims description 2
- 230000000843 anti-fungal effect Effects 0.000 claims description 2
- 229940121363 anti-inflammatory agent Drugs 0.000 claims description 2
- 239000002260 anti-inflammatory agent Substances 0.000 claims description 2
- 229940088710 antibiotic agent Drugs 0.000 claims description 2
- 229940121375 antifungal agent Drugs 0.000 claims description 2
- 235000021302 avocado oil Nutrition 0.000 claims description 2
- 239000008163 avocado oil Substances 0.000 claims description 2
- 125000000484 butyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 claims description 2
- 235000009508 confectionery Nutrition 0.000 claims description 2
- 150000001879 copper Chemical class 0.000 claims description 2
- 231100000321 erythema Toxicity 0.000 claims description 2
- 150000002240 furans Chemical class 0.000 claims description 2
- 229940087068 glyceryl caprylate Drugs 0.000 claims description 2
- 230000003425 hypopigmentation Effects 0.000 claims description 2
- 239000002955 immunomodulating agent Substances 0.000 claims description 2
- 229940121354 immunomodulator Drugs 0.000 claims description 2
- 239000002973 irritant agent Substances 0.000 claims description 2
- 230000001530 keratinolytic effect Effects 0.000 claims description 2
- 239000003410 keratolytic agent Substances 0.000 claims description 2
- 230000002366 lipolytic effect Effects 0.000 claims description 2
- 150000002918 oxazolines Chemical class 0.000 claims description 2
- 229940101267 panthenol Drugs 0.000 claims description 2
- 235000020957 pantothenol Nutrition 0.000 claims description 2
- 239000011619 pantothenol Substances 0.000 claims description 2
- 229940068065 phytosterols Drugs 0.000 claims description 2
- 235000013406 prebiotics Nutrition 0.000 claims description 2
- 239000006041 probiotic Substances 0.000 claims description 2
- 235000018291 probiotics Nutrition 0.000 claims description 2
- GHBFNMLVSPCDGN-UHFFFAOYSA-N rac-1-monooctanoylglycerol Chemical compound CCCCCCCC(=O)OCC(O)CO GHBFNMLVSPCDGN-UHFFFAOYSA-N 0.000 claims description 2
- 201000004700 rosacea Diseases 0.000 claims description 2
- 229940058349 sodium levulinate Drugs 0.000 claims description 2
- RDKYCKDVIYTSAJ-UHFFFAOYSA-M sodium;4-oxopentanoate Chemical compound [Na+].CC(=O)CCC([O-])=O RDKYCKDVIYTSAJ-UHFFFAOYSA-M 0.000 claims description 2
- 235000012424 soybean oil Nutrition 0.000 claims description 2
- 239000003549 soybean oil Substances 0.000 claims description 2
- LXMSZDCAJNLERA-ZHYRCANASA-N spironolactone Chemical compound C([C@@H]1[C@]2(C)CC[C@@H]3[C@@]4(C)CCC(=O)C=C4C[C@H]([C@@H]13)SC(=O)C)C[C@@]21CCC(=O)O1 LXMSZDCAJNLERA-ZHYRCANASA-N 0.000 claims description 2
- 229960002256 spironolactone Drugs 0.000 claims description 2
- 150000003722 vitamin derivatives Chemical class 0.000 claims description 2
- YEFOAORQXAOVJQ-UHFFFAOYSA-N wuweizischun A Natural products C1C(C)C(C)(O)CC2=CC(OC)=C(OC)C(OC)=C2C2=C1C=C(OC)C(OC)=C2OC YEFOAORQXAOVJQ-UHFFFAOYSA-N 0.000 claims description 2
- 150000003751 zinc Chemical class 0.000 claims description 2
- YLQBMQCUIZJEEH-UHFFFAOYSA-N Furan Chemical compound C=1C=COC=1 YLQBMQCUIZJEEH-UHFFFAOYSA-N 0.000 claims 2
- 235000016383 Zea mays subsp huehuetenangensis Nutrition 0.000 claims 1
- 235000020739 avocado extract Nutrition 0.000 claims 1
- 150000002148 esters Chemical class 0.000 claims 1
- ACCCMOQWYVYDOT-UHFFFAOYSA-N hexane-1,1-diol Chemical compound CCCCCC(O)O ACCCMOQWYVYDOT-UHFFFAOYSA-N 0.000 claims 1
- 235000009973 maize Nutrition 0.000 claims 1
- 210000003491 skin Anatomy 0.000 description 32
- 210000004027 cell Anatomy 0.000 description 25
- 210000002510 keratinocyte Anatomy 0.000 description 20
- 230000000694 effects Effects 0.000 description 18
- NTYJJOPFIAHURM-UHFFFAOYSA-N Histamine Chemical compound NCCC1=CN=CN1 NTYJJOPFIAHURM-UHFFFAOYSA-N 0.000 description 16
- 210000000440 neutrophil Anatomy 0.000 description 15
- 239000011149 active material Substances 0.000 description 13
- 239000000463 material Substances 0.000 description 13
- 241000186427 Cutibacterium acnes Species 0.000 description 12
- 230000005764 inhibitory process Effects 0.000 description 12
- 230000014509 gene expression Effects 0.000 description 11
- 238000011534 incubation Methods 0.000 description 11
- 150000002632 lipids Chemical class 0.000 description 11
- 238000000692 Student's t-test Methods 0.000 description 10
- 239000000047 product Substances 0.000 description 10
- 239000007791 liquid phase Substances 0.000 description 9
- 102000004890 Interleukin-8 Human genes 0.000 description 8
- 108090001007 Interleukin-8 Proteins 0.000 description 8
- 229960001340 histamine Drugs 0.000 description 8
- XKTZWUACRZHVAN-VADRZIEHSA-N interleukin-8 Chemical compound C([C@H](NC(=O)[C@H](CC(O)=O)NC(=O)[C@H](CC=1C2=CC=CC=C2NC=1)NC(=O)[C@@H](NC(C)=O)CCSC)C(=O)N[C@@H](CC(O)=O)C(=O)N[C@@H](CC(O)=O)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CC(N)=O)C(=O)N[C@@H](CC=1C=CC=CC=1)C(=O)N[C@@H]([C@@H](C)O)C(=O)NCC(=O)N[C@@H](CCSC)C(=O)N1[C@H](CCC1)C(=O)N1[C@H](CCC1)C(=O)N[C@@H](C)C(=O)N[C@H](CC(O)=O)C(=O)N[C@H](CCC(O)=O)C(=O)N[C@H](CC(O)=O)C(=O)N[C@H](CC=1C=CC(O)=CC=1)C(=O)N[C@H](CO)C(=O)N1[C@H](CCC1)C(N)=O)C1=CC=CC=C1 XKTZWUACRZHVAN-VADRZIEHSA-N 0.000 description 8
- 229940096397 interleukin-8 Drugs 0.000 description 8
- 230000005012 migration Effects 0.000 description 8
- 238000013508 migration Methods 0.000 description 8
- 230000008569 process Effects 0.000 description 8
- VNYSSYRCGWBHLG-AMOLWHMGSA-N leukotriene B4 Chemical compound CCCCC\C=C/C[C@@H](O)\C=C\C=C\C=C/[C@@H](O)CCCC(O)=O VNYSSYRCGWBHLG-AMOLWHMGSA-N 0.000 description 7
- 230000007170 pathology Effects 0.000 description 7
- 102000004169 proteins and genes Human genes 0.000 description 7
- 108090000623 proteins and genes Proteins 0.000 description 7
- 206010052428 Wound Diseases 0.000 description 6
- 208000027418 Wounds and injury Diseases 0.000 description 6
- VSCWAEJMTAWNJL-UHFFFAOYSA-K aluminium trichloride Chemical compound Cl[Al](Cl)Cl VSCWAEJMTAWNJL-UHFFFAOYSA-K 0.000 description 6
- 230000015572 biosynthetic process Effects 0.000 description 6
- 239000000839 emulsion Substances 0.000 description 6
- 238000000605 extraction Methods 0.000 description 6
- 210000004378 sebocyte Anatomy 0.000 description 6
- 102000044503 Antimicrobial Peptides Human genes 0.000 description 5
- 108700042778 Antimicrobial Peptides Proteins 0.000 description 5
- MHAJPDPJQMAIIY-UHFFFAOYSA-N Hydrogen peroxide Chemical compound OO MHAJPDPJQMAIIY-UHFFFAOYSA-N 0.000 description 5
- 206010039792 Seborrhoea Diseases 0.000 description 5
- 230000003078 antioxidant effect Effects 0.000 description 5
- 235000006708 antioxidants Nutrition 0.000 description 5
- 238000005119 centrifugation Methods 0.000 description 5
- 238000006243 chemical reaction Methods 0.000 description 5
- XEYBRNLFEZDVAW-ARSRFYASSA-N dinoprostone Chemical compound CCCCC[C@H](O)\C=C\[C@H]1[C@H](O)CC(=O)[C@@H]1C\C=C/CCCC(O)=O XEYBRNLFEZDVAW-ARSRFYASSA-N 0.000 description 5
- 229960002986 dinoprostone Drugs 0.000 description 5
- 238000001914 filtration Methods 0.000 description 5
- 210000003630 histaminocyte Anatomy 0.000 description 5
- 238000002360 preparation method Methods 0.000 description 5
- XEYBRNLFEZDVAW-UHFFFAOYSA-N prostaglandin E2 Natural products CCCCCC(O)C=CC1C(O)CC(=O)C1CC=CCCCC(O)=O XEYBRNLFEZDVAW-UHFFFAOYSA-N 0.000 description 5
- 239000000243 solution Substances 0.000 description 5
- 238000011200 topical administration Methods 0.000 description 5
- CIWBSHSKHKDKBQ-JLAZNSOCSA-N Ascorbic acid Chemical compound OC[C@H](O)[C@H]1OC(=O)C(O)=C1O CIWBSHSKHKDKBQ-JLAZNSOCSA-N 0.000 description 4
- 238000002965 ELISA Methods 0.000 description 4
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 4
- 206010061218 Inflammation Diseases 0.000 description 4
- XUMBMVFBXHLACL-UHFFFAOYSA-N Melanin Chemical compound O=C1C(=O)C(C2=CNC3=C(C(C(=O)C4=C32)=O)C)=C2C4=CNC2=C1C XUMBMVFBXHLACL-UHFFFAOYSA-N 0.000 description 4
- 210000001789 adipocyte Anatomy 0.000 description 4
- YZXBAPSDXZZRGB-DOFZRALJSA-N arachidonic acid Chemical compound CCCCC\C=C/C\C=C/C\C=C/C\C=C/CCCC(O)=O YZXBAPSDXZZRGB-DOFZRALJSA-N 0.000 description 4
- 230000004888 barrier function Effects 0.000 description 4
- 239000011575 calcium Substances 0.000 description 4
- PRQROPMIIGLWRP-BZSNNMDCSA-N chemotactic peptide Chemical compound CSCC[C@H](NC=O)C(=O)N[C@@H](CC(C)C)C(=O)N[C@H](C(O)=O)CC1=CC=CC=C1 PRQROPMIIGLWRP-BZSNNMDCSA-N 0.000 description 4
- 238000010908 decantation Methods 0.000 description 4
- 238000011156 evaluation Methods 0.000 description 4
- 230000004054 inflammatory process Effects 0.000 description 4
- 230000003859 lipid peroxidation Effects 0.000 description 4
- 238000005259 measurement Methods 0.000 description 4
- 230000008099 melanin synthesis Effects 0.000 description 4
- 239000000419 plant extract Substances 0.000 description 4
- 238000003756 stirring Methods 0.000 description 4
- 238000003786 synthesis reaction Methods 0.000 description 4
- QDZOEBFLNHCSSF-PFFBOGFISA-N (2S)-2-[[(2R)-2-[[(2S)-1-[(2S)-6-amino-2-[[(2S)-1-[(2R)-2-amino-5-carbamimidamidopentanoyl]pyrrolidine-2-carbonyl]amino]hexanoyl]pyrrolidine-2-carbonyl]amino]-3-(1H-indol-3-yl)propanoyl]amino]-N-[(2R)-1-[[(2S)-1-[[(2R)-1-[[(2S)-1-[[(2S)-1-amino-4-methyl-1-oxopentan-2-yl]amino]-4-methyl-1-oxopentan-2-yl]amino]-3-(1H-indol-3-yl)-1-oxopropan-2-yl]amino]-1-oxo-3-phenylpropan-2-yl]amino]-3-(1H-indol-3-yl)-1-oxopropan-2-yl]pentanediamide Chemical compound C([C@@H](C(=O)N[C@H](CC=1C2=CC=CC=C2NC=1)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CC(C)C)C(N)=O)NC(=O)[C@@H](CC=1C2=CC=CC=C2NC=1)NC(=O)[C@H](CCC(N)=O)NC(=O)[C@@H](CC=1C2=CC=CC=C2NC=1)NC(=O)[C@H]1N(CCC1)C(=O)[C@H](CCCCN)NC(=O)[C@H]1N(CCC1)C(=O)[C@H](N)CCCNC(N)=N)C1=CC=CC=C1 QDZOEBFLNHCSSF-PFFBOGFISA-N 0.000 description 3
- 108700034262 4-Nle-7-Phe-alpha- MSH Proteins 0.000 description 3
- JMGZEFIQIZZSBH-UHFFFAOYSA-N Bioquercetin Natural products CC1OC(OCC(O)C2OC(OC3=C(Oc4cc(O)cc(O)c4C3=O)c5ccc(O)c(O)c5)C(O)C2O)C(O)C(O)C1O JMGZEFIQIZZSBH-UHFFFAOYSA-N 0.000 description 3
- OYPRJOBELJOOCE-UHFFFAOYSA-N Calcium Chemical compound [Ca] OYPRJOBELJOOCE-UHFFFAOYSA-N 0.000 description 3
- 101000595923 Homo sapiens Placenta growth factor Proteins 0.000 description 3
- 102100035194 Placenta growth factor Human genes 0.000 description 3
- 102400000096 Substance P Human genes 0.000 description 3
- 101800003906 Substance P Proteins 0.000 description 3
- 102000016663 Vascular Endothelial Growth Factor Receptor-3 Human genes 0.000 description 3
- 108010053100 Vascular Endothelial Growth Factor Receptor-3 Proteins 0.000 description 3
- UAHFGYDRQSXQEB-LEBBXHLNSA-N afamelanotide Chemical compound C([C@@H](C(=O)N[C@@H](CO)C(=O)N[C@@H](CCCC)C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](CC=1NC=NC=1)C(=O)N[C@H](CC=1C=CC=CC=1)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CC=1C2=CC=CC=C2NC=1)C(=O)NCC(=O)N[C@@H](CCCCN)C(=O)N1[C@@H](CCC1)C(=O)N[C@@H](C(C)C)C(N)=O)NC(=O)[C@H](CO)NC(C)=O)C1=CC=C(O)C=C1 UAHFGYDRQSXQEB-LEBBXHLNSA-N 0.000 description 3
- 238000000540 analysis of variance Methods 0.000 description 3
- RJGDLRCDCYRQOQ-UHFFFAOYSA-N anthrone Chemical compound C1=CC=C2C(=O)C3=CC=CC=C3CC2=C1 RJGDLRCDCYRQOQ-UHFFFAOYSA-N 0.000 description 3
- 230000002225 anti-radical effect Effects 0.000 description 3
- 230000004071 biological effect Effects 0.000 description 3
- 229910052791 calcium Inorganic materials 0.000 description 3
- 210000002889 endothelial cell Anatomy 0.000 description 3
- IVTMALDHFAHOGL-UHFFFAOYSA-N eriodictyol 7-O-rutinoside Natural products OC1C(O)C(O)C(C)OC1OCC1C(O)C(O)C(O)C(OC=2C=C3C(C(C(O)=C(O3)C=3C=C(O)C(O)=CC=3)=O)=C(O)C=2)O1 IVTMALDHFAHOGL-UHFFFAOYSA-N 0.000 description 3
- 239000010200 folin Substances 0.000 description 3
- 210000004392 genitalia Anatomy 0.000 description 3
- CGIGDMFJXJATDK-UHFFFAOYSA-N indomethacin Chemical compound CC1=C(CC(O)=O)C2=CC(OC)=CC=C2N1C(=O)C1=CC=C(Cl)C=C1 CGIGDMFJXJATDK-UHFFFAOYSA-N 0.000 description 3
- 230000002401 inhibitory effect Effects 0.000 description 3
- 230000003902 lesion Effects 0.000 description 3
- 210000002752 melanocyte Anatomy 0.000 description 3
- 235000013336 milk Nutrition 0.000 description 3
- 210000004080 milk Anatomy 0.000 description 3
- 230000008520 organization Effects 0.000 description 3
- 230000001590 oxidative effect Effects 0.000 description 3
- 230000007310 pathophysiology Effects 0.000 description 3
- FDRQPMVGJOQVTL-UHFFFAOYSA-N quercetin rutinoside Natural products OC1C(O)C(O)C(CO)OC1OCC1C(O)C(O)C(O)C(OC=2C(C3=C(O)C=C(O)C=C3OC=2C=2C=C(O)C(O)=CC=2)=O)O1 FDRQPMVGJOQVTL-UHFFFAOYSA-N 0.000 description 3
- 239000012429 reaction media Substances 0.000 description 3
- ALABRVAAKCSLSC-UHFFFAOYSA-N rutin Natural products CC1OC(OCC2OC(O)C(O)C(O)C2O)C(O)C(O)C1OC3=C(Oc4cc(O)cc(O)c4C3=O)c5ccc(O)c(O)c5 ALABRVAAKCSLSC-UHFFFAOYSA-N 0.000 description 3
- IKGXIBQEEMLURG-BKUODXTLSA-N rutin Chemical compound O[C@H]1[C@H](O)[C@@H](O)[C@H](C)O[C@@H]1OC[C@H]1[C@H](O)[C@@H](O)[C@H](O)[C@@H](OC=2C(C3=C(O)C=C(O)C=C3OC=2C=2C=C(O)C(O)=CC=2)=O)O1 IKGXIBQEEMLURG-BKUODXTLSA-N 0.000 description 3
- 235000005493 rutin Nutrition 0.000 description 3
- 229960004555 rutoside Drugs 0.000 description 3
- 239000002453 shampoo Substances 0.000 description 3
- 239000007921 spray Substances 0.000 description 3
- PRAKJMSDJKAYCZ-UHFFFAOYSA-N squalane Chemical compound CC(C)CCCC(C)CCCC(C)CCCCC(C)CCCC(C)CCCC(C)C PRAKJMSDJKAYCZ-UHFFFAOYSA-N 0.000 description 3
- 230000000638 stimulation Effects 0.000 description 3
- 238000012360 testing method Methods 0.000 description 3
- 235000019154 vitamin C Nutrition 0.000 description 3
- 239000011718 vitamin C Substances 0.000 description 3
- GVEZIHKRYBHEFX-MNOVXSKESA-N 13C-Cerulenin Natural products CC=CCC=CCCC(=O)[C@H]1O[C@@H]1C(N)=O GVEZIHKRYBHEFX-MNOVXSKESA-N 0.000 description 2
- 208000034309 Bacterial disease carrier Diseases 0.000 description 2
- 102000000584 Calmodulin Human genes 0.000 description 2
- 108010041952 Calmodulin Proteins 0.000 description 2
- 102100038608 Cathelicidin antimicrobial peptide Human genes 0.000 description 2
- ZZZCUOFIHGPKAK-UHFFFAOYSA-N D-erythro-ascorbic acid Natural products OCC1OC(=O)C(O)=C1O ZZZCUOFIHGPKAK-UHFFFAOYSA-N 0.000 description 2
- RGHNJXZEOKUKBD-SQOUGZDYSA-M D-gluconate Chemical compound OC[C@@H](O)[C@@H](O)[C@H](O)[C@@H](O)C([O-])=O RGHNJXZEOKUKBD-SQOUGZDYSA-M 0.000 description 2
- 206010012434 Dermatitis allergic Diseases 0.000 description 2
- 206010012442 Dermatitis contact Diseases 0.000 description 2
- 238000001061 Dunnett's test Methods 0.000 description 2
- 102400001047 Endostatin Human genes 0.000 description 2
- 108010079505 Endostatins Proteins 0.000 description 2
- 102000004190 Enzymes Human genes 0.000 description 2
- 108090000790 Enzymes Proteins 0.000 description 2
- DHMQDGOQFOQNFH-UHFFFAOYSA-N Glycine Chemical compound NCC(O)=O DHMQDGOQFOQNFH-UHFFFAOYSA-N 0.000 description 2
- 101000741320 Homo sapiens Cathelicidin antimicrobial peptide Proteins 0.000 description 2
- 102000003855 L-lactate dehydrogenase Human genes 0.000 description 2
- 108700023483 L-lactate dehydrogenases Proteins 0.000 description 2
- DFPAKSUCGFBDDF-UHFFFAOYSA-N Nicotinamide Chemical compound NC(=O)C1=CC=CN=C1 DFPAKSUCGFBDDF-UHFFFAOYSA-N 0.000 description 2
- 208000002193 Pain Diseases 0.000 description 2
- 108010019674 Proto-Oncogene Proteins c-sis Proteins 0.000 description 2
- 102000007614 Thrombospondin 1 Human genes 0.000 description 2
- 108010046722 Thrombospondin 1 Proteins 0.000 description 2
- 102000002689 Toll-like receptor Human genes 0.000 description 2
- 108020000411 Toll-like receptor Proteins 0.000 description 2
- 206010047139 Vasoconstriction Diseases 0.000 description 2
- 229930003268 Vitamin C Natural products 0.000 description 2
- XLOMVQKBTHCTTD-UHFFFAOYSA-N Zinc monoxide Chemical compound [Zn]=O XLOMVQKBTHCTTD-UHFFFAOYSA-N 0.000 description 2
- 229920000392 Zymosan Polymers 0.000 description 2
- 230000009471 action Effects 0.000 description 2
- 230000032683 aging Effects 0.000 description 2
- 230000001772 anti-angiogenic effect Effects 0.000 description 2
- 229940114079 arachidonic acid Drugs 0.000 description 2
- 235000021342 arachidonic acid Nutrition 0.000 description 2
- 201000008937 atopic dermatitis Diseases 0.000 description 2
- GVEZIHKRYBHEFX-UHFFFAOYSA-N caerulein A Natural products CC=CCC=CCCC(=O)C1OC1C(N)=O GVEZIHKRYBHEFX-UHFFFAOYSA-N 0.000 description 2
- 230000001413 cellular effect Effects 0.000 description 2
- GVEZIHKRYBHEFX-NQQPLRFYSA-N cerulenin Chemical compound C\C=C\C\C=C\CCC(=O)[C@H]1O[C@H]1C(N)=O GVEZIHKRYBHEFX-NQQPLRFYSA-N 0.000 description 2
- 229950005984 cerulenin Drugs 0.000 description 2
- HVYWMOMLDIMFJA-DPAQBDIFSA-N cholesterol Chemical compound C1C=C2C[C@@H](O)CC[C@]2(C)[C@@H]2[C@@H]1[C@@H]1CC[C@H]([C@H](C)CCCC(C)C)[C@@]1(C)CC2 HVYWMOMLDIMFJA-DPAQBDIFSA-N 0.000 description 2
- 238000004140 cleaning Methods 0.000 description 2
- 239000000470 constituent Substances 0.000 description 2
- 239000012228 culture supernatant Substances 0.000 description 2
- 230000007123 defense Effects 0.000 description 2
- 230000035614 depigmentation Effects 0.000 description 2
- 238000011161 development Methods 0.000 description 2
- 230000018109 developmental process Effects 0.000 description 2
- UREBDLICKHMUKA-CXSFZGCWSA-N dexamethasone Chemical compound C1CC2=CC(=O)C=C[C@]2(C)[C@]2(F)[C@@H]1[C@@H]1C[C@@H](C)[C@@](C(=O)CO)(O)[C@@]1(C)C[C@@H]2O UREBDLICKHMUKA-CXSFZGCWSA-N 0.000 description 2
- 229960003957 dexamethasone Drugs 0.000 description 2
- 235000013399 edible fruits Nutrition 0.000 description 2
- 229940050410 gluconate Drugs 0.000 description 2
- 230000013632 homeostatic process Effects 0.000 description 2
- 238000010348 incorporation Methods 0.000 description 2
- 229960000905 indomethacin Drugs 0.000 description 2
- 230000007794 irritation Effects 0.000 description 2
- IYRMWMYZSQPJKC-UHFFFAOYSA-N kaempferol Chemical compound C1=CC(O)=CC=C1C1=C(O)C(=O)C2=C(O)C=C(O)C=C2O1 IYRMWMYZSQPJKC-UHFFFAOYSA-N 0.000 description 2
- MWDZOUNAPSSOEL-UHFFFAOYSA-N kaempferol Natural products OC1=C(C(=O)c2cc(O)cc(O)c2O1)c3ccc(O)cc3 MWDZOUNAPSSOEL-UHFFFAOYSA-N 0.000 description 2
- 239000007788 liquid Substances 0.000 description 2
- 239000006210 lotion Substances 0.000 description 2
- 238000012544 monitoring process Methods 0.000 description 2
- 238000001728 nano-filtration Methods 0.000 description 2
- 230000036407 pain Effects 0.000 description 2
- 201000001245 periodontitis Diseases 0.000 description 2
- 150000002989 phenols Chemical class 0.000 description 2
- 230000001023 pro-angiogenic effect Effects 0.000 description 2
- 230000004044 response Effects 0.000 description 2
- 238000003757 reverse transcription PCR Methods 0.000 description 2
- 230000037390 scarring Effects 0.000 description 2
- 210000001732 sebaceous gland Anatomy 0.000 description 2
- 230000028327 secretion Effects 0.000 description 2
- 230000037307 sensitive skin Effects 0.000 description 2
- 230000035882 stress Effects 0.000 description 2
- 239000000126 substance Substances 0.000 description 2
- 230000000699 topical effect Effects 0.000 description 2
- 238000000108 ultra-filtration Methods 0.000 description 2
- 230000002792 vascular Effects 0.000 description 2
- 230000025033 vasoconstriction Effects 0.000 description 2
- 239000003643 water by type Substances 0.000 description 2
- GMDUYWRBDHXKMS-UHFFFAOYSA-N (+-)-cleomin Natural products CCC1(C)CNC(=S)O1 GMDUYWRBDHXKMS-UHFFFAOYSA-N 0.000 description 1
- RSDFPCQESXIWFY-UHFFFAOYSA-N (2-heptadecyl-4-methyl-5h-1,3-oxazol-4-yl)methanol Chemical compound CCCCCCCCCCCCCCCCCC1=NC(C)(CO)CO1 RSDFPCQESXIWFY-UHFFFAOYSA-N 0.000 description 1
- GMDUYWRBDHXKMS-LURJTMIESA-N (5s)-5-ethyl-5-methyl-1,3-oxazolidine-2-thione Chemical compound CC[C@@]1(C)CNC(=S)O1 GMDUYWRBDHXKMS-LURJTMIESA-N 0.000 description 1
- YYGNTYWPHWGJRM-UHFFFAOYSA-N (6E,10E,14E,18E)-2,6,10,15,19,23-hexamethyltetracosa-2,6,10,14,18,22-hexaene Chemical compound CC(C)=CCCC(C)=CCCC(C)=CCCC=C(C)CCC=C(C)CCC=C(C)C YYGNTYWPHWGJRM-UHFFFAOYSA-N 0.000 description 1
- WRIDQFICGBMAFQ-UHFFFAOYSA-N (E)-8-Octadecenoic acid Natural products CCCCCCCCCC=CCCCCCCC(O)=O WRIDQFICGBMAFQ-UHFFFAOYSA-N 0.000 description 1
- 0 *C(C1O)=C(c(cc2O)ccc2O)Oc2c1c(O)cc(O)c2 Chemical compound *C(C1O)=C(c(cc2O)ccc2O)Oc2c1c(O)cc(O)c2 0.000 description 1
- LQJBNNIYVWPHFW-UHFFFAOYSA-N 20:1omega9c fatty acid Natural products CCCCCCCCCCC=CCCCCCCCC(O)=O LQJBNNIYVWPHFW-UHFFFAOYSA-N 0.000 description 1
- 229940113178 5 Alpha reductase inhibitor Drugs 0.000 description 1
- QSBYPNXLFMSGKH-UHFFFAOYSA-N 9-Heptadecensaeure Natural products CCCCCCCC=CCCCCCCCC(O)=O QSBYPNXLFMSGKH-UHFFFAOYSA-N 0.000 description 1
- QTBSBXVTEAMEQO-UHFFFAOYSA-M Acetate Chemical compound CC([O-])=O QTBSBXVTEAMEQO-UHFFFAOYSA-M 0.000 description 1
- 102000007469 Actins Human genes 0.000 description 1
- 108010085238 Actins Proteins 0.000 description 1
- 201000004384 Alopecia Diseases 0.000 description 1
- 241000894006 Bacteria Species 0.000 description 1
- 102100026887 Beta-defensin 103 Human genes 0.000 description 1
- SGNBVLSWZMBQTH-FGAXOLDCSA-N Campesterol Natural products O[C@@H]1CC=2[C@@](C)([C@@H]3[C@H]([C@H]4[C@@](C)([C@H]([C@H](CC[C@H](C(C)C)C)C)CC4)CC3)CC=2)CC1 SGNBVLSWZMBQTH-FGAXOLDCSA-N 0.000 description 1
- 241000873224 Capparaceae Species 0.000 description 1
- 206010007882 Cellulitis Diseases 0.000 description 1
- GHOKWGTUZJEAQD-UHFFFAOYSA-N Chick antidermatitis factor Natural products OCC(C)(C)C(O)C(=O)NCCC(O)=O GHOKWGTUZJEAQD-UHFFFAOYSA-N 0.000 description 1
- 208000032544 Cicatrix Diseases 0.000 description 1
- 241001116782 Cleome Species 0.000 description 1
- 102000004127 Cytokines Human genes 0.000 description 1
- 108090000695 Cytokines Proteins 0.000 description 1
- UBSCDKPKWHYZNX-UHFFFAOYSA-N Demethoxycapillarisin Natural products C1=CC(O)=CC=C1OC1=CC(=O)C2=C(O)C=C(O)C=C2O1 UBSCDKPKWHYZNX-UHFFFAOYSA-N 0.000 description 1
- 206010012438 Dermatitis atopic Diseases 0.000 description 1
- 206010013786 Dry skin Diseases 0.000 description 1
- 102400000686 Endothelin-1 Human genes 0.000 description 1
- 101800004490 Endothelin-1 Proteins 0.000 description 1
- MQYXUWHLBZFQQO-ISZJTHHZSA-N Epilupeol Chemical compound C1C[C@@H](O)C(C)(C)[C@@H]2CC[C@@]3(C)[C@]4(C)CC[C@@]5(C)CC[C@@H](C(=C)C)[C@@H]5[C@H]4CC[C@@H]3[C@]21C MQYXUWHLBZFQQO-ISZJTHHZSA-N 0.000 description 1
- 206010016936 Folliculitis Diseases 0.000 description 1
- 241000447437 Gerreidae Species 0.000 description 1
- 239000004471 Glycine Substances 0.000 description 1
- BTEISVKTSQLKST-UHFFFAOYSA-N Haliclonasterol Natural products CC(C=CC(C)C(C)(C)C)C1CCC2C3=CC=C4CC(O)CCC4(C)C3CCC12C BTEISVKTSQLKST-UHFFFAOYSA-N 0.000 description 1
- 206010019233 Headaches Diseases 0.000 description 1
- 102000002737 Heme Oxygenase-1 Human genes 0.000 description 1
- 108010018924 Heme Oxygenase-1 Proteins 0.000 description 1
- 206010020112 Hirsutism Diseases 0.000 description 1
- 102000000543 Histamine Receptors Human genes 0.000 description 1
- 108010002059 Histamine Receptors Proteins 0.000 description 1
- 101000912247 Homo sapiens Beta-defensin 103 Proteins 0.000 description 1
- 206010020751 Hypersensitivity Diseases 0.000 description 1
- XQFRJNBWHJMXHO-RRKCRQDMSA-N IDUR Chemical compound C1[C@H](O)[C@@H](CO)O[C@H]1N1C(=O)NC(=O)C(I)=C1 XQFRJNBWHJMXHO-RRKCRQDMSA-N 0.000 description 1
- OYHQOLUKZRVURQ-HZJYTTRNSA-N Linoleic acid Chemical compound CCCCC\C=C/C\C=C/CCCCCCCC(O)=O OYHQOLUKZRVURQ-HZJYTTRNSA-N 0.000 description 1
- FYYHWMGAXLPEAU-UHFFFAOYSA-N Magnesium Chemical compound [Mg] FYYHWMGAXLPEAU-UHFFFAOYSA-N 0.000 description 1
- 239000005913 Maltodextrin Substances 0.000 description 1
- 229920002774 Maltodextrin Polymers 0.000 description 1
- 241001413575 Moorea Species 0.000 description 1
- 239000005642 Oleic acid Substances 0.000 description 1
- ZQPPMHVWECSIRJ-UHFFFAOYSA-N Oleic acid Natural products CCCCCCCCC=CCCCCCCCC(O)=O ZQPPMHVWECSIRJ-UHFFFAOYSA-N 0.000 description 1
- 101100274508 Oryza sativa subsp. japonica CKI1 gene Proteins 0.000 description 1
- 102000003728 Peroxisome Proliferator-Activated Receptors Human genes 0.000 description 1
- 108090000029 Peroxisome Proliferator-Activated Receptors Proteins 0.000 description 1
- 206010034972 Photosensitivity reaction Diseases 0.000 description 1
- 102100040990 Platelet-derived growth factor subunit B Human genes 0.000 description 1
- 201000004681 Psoriasis Diseases 0.000 description 1
- ODHCTXKNWHHXJC-GSVOUGTGSA-N Pyroglutamic acid Natural products OC(=O)[C@H]1CCC(=O)N1 ODHCTXKNWHHXJC-GSVOUGTGSA-N 0.000 description 1
- 241000220317 Rosa Species 0.000 description 1
- 241000239226 Scorpiones Species 0.000 description 1
- 206010040925 Skin striae Diseases 0.000 description 1
- 208000031439 Striae Distensae Diseases 0.000 description 1
- 206010042496 Sunburn Diseases 0.000 description 1
- 235000019486 Sunflower oil Nutrition 0.000 description 1
- 208000033809 Suppuration Diseases 0.000 description 1
- BHEOSNUKNHRBNM-UHFFFAOYSA-N Tetramethylsqualene Natural products CC(=C)C(C)CCC(=C)C(C)CCC(C)=CCCC=C(C)CCC(C)C(=C)CCC(C)C(C)=C BHEOSNUKNHRBNM-UHFFFAOYSA-N 0.000 description 1
- 102000002933 Thioredoxin Human genes 0.000 description 1
- 241000394605 Viola striata Species 0.000 description 1
- 229930003571 Vitamin B5 Natural products 0.000 description 1
- 206010047642 Vitiligo Diseases 0.000 description 1
- 206010048222 Xerosis Diseases 0.000 description 1
- 235000005824 Zea mays ssp. parviglumis Nutrition 0.000 description 1
- QTBSBXVTEAMEQO-HQMMCQRPSA-N acetic acid Chemical compound C[14C](O)=O QTBSBXVTEAMEQO-HQMMCQRPSA-N 0.000 description 1
- NFXWJYUDIOHFAW-UHFFFAOYSA-N acetic acid;tetradecanoic acid Chemical compound CC(O)=O.CCCCCCCCCCCCCC(O)=O NFXWJYUDIOHFAW-UHFFFAOYSA-N 0.000 description 1
- ODHCTXKNWHHXJC-UHFFFAOYSA-N acide pyroglutamique Natural products OC(=O)C1CCC(=O)N1 ODHCTXKNWHHXJC-UHFFFAOYSA-N 0.000 description 1
- 210000000577 adipose tissue Anatomy 0.000 description 1
- 239000002671 adjuvant Substances 0.000 description 1
- 239000000556 agonist Substances 0.000 description 1
- 229930013930 alkaloid Natural products 0.000 description 1
- 208000002029 allergic contact dermatitis Diseases 0.000 description 1
- 231100000360 alopecia Toxicity 0.000 description 1
- 230000004075 alteration Effects 0.000 description 1
- 230000000202 analgesic effect Effects 0.000 description 1
- 238000004458 analytical method Methods 0.000 description 1
- 239000010775 animal oil Substances 0.000 description 1
- 235000010208 anthocyanin Nutrition 0.000 description 1
- 229930002877 anthocyanin Natural products 0.000 description 1
- 239000004410 anthocyanin Substances 0.000 description 1
- 150000004636 anthocyanins Chemical class 0.000 description 1
- 230000003255 anti-acne Effects 0.000 description 1
- 230000000844 anti-bacterial effect Effects 0.000 description 1
- 230000003627 anti-cholesterol Effects 0.000 description 1
- 230000000845 anti-microbial effect Effects 0.000 description 1
- 230000002141 anti-parasite Effects 0.000 description 1
- 239000003096 antiparasitic agent Substances 0.000 description 1
- 239000003125 aqueous solvent Substances 0.000 description 1
- 206010003246 arthritis Diseases 0.000 description 1
- 238000003556 assay Methods 0.000 description 1
- 238000000889 atomisation Methods 0.000 description 1
- 208000010668 atopic eczema Diseases 0.000 description 1
- 230000001580 bacterial effect Effects 0.000 description 1
- 230000009286 beneficial effect Effects 0.000 description 1
- 102000012265 beta-defensin Human genes 0.000 description 1
- 108050002883 beta-defensin Proteins 0.000 description 1
- 230000033228 biological regulation Effects 0.000 description 1
- 210000004369 blood Anatomy 0.000 description 1
- 239000008280 blood Substances 0.000 description 1
- 230000017531 blood circulation Effects 0.000 description 1
- 210000004204 blood vessel Anatomy 0.000 description 1
- 230000037396 body weight Effects 0.000 description 1
- 210000000481 breast Anatomy 0.000 description 1
- 235000014121 butter Nutrition 0.000 description 1
- DEGAKNSWVGKMLS-UHFFFAOYSA-N calcein Chemical compound O1C(=O)C2=CC=CC=C2C21C1=CC(CN(CC(O)=O)CC(O)=O)=C(O)C=C1OC1=C2C=C(CN(CC(O)=O)CC(=O)O)C(O)=C1 DEGAKNSWVGKMLS-UHFFFAOYSA-N 0.000 description 1
- FAPWYRCQGJNNSJ-UBKPKTQASA-L calcium D-pantothenic acid Chemical compound [Ca+2].OCC(C)(C)[C@@H](O)C(=O)NCCC([O-])=O.OCC(C)(C)[C@@H](O)C(=O)NCCC([O-])=O FAPWYRCQGJNNSJ-UBKPKTQASA-L 0.000 description 1
- 229960002079 calcium pantothenate Drugs 0.000 description 1
- SGNBVLSWZMBQTH-PODYLUTMSA-N campesterol Chemical compound C1C=C2C[C@@H](O)CC[C@]2(C)[C@@H]2[C@@H]1[C@@H]1CC[C@H]([C@H](C)CC[C@@H](C)C(C)C)[C@@]1(C)CC2 SGNBVLSWZMBQTH-PODYLUTMSA-N 0.000 description 1
- 235000000431 campesterol Nutrition 0.000 description 1
- 235000014633 carbohydrates Nutrition 0.000 description 1
- 150000001720 carbohydrates Chemical class 0.000 description 1
- POIUWJQBRNEFGX-XAMSXPGMSA-N cathelicidin Chemical compound C([C@@H](C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CCCCN)C(=O)N[C@@H](CO)C(=O)N[C@@H](CCCCN)C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](CCCCN)C(=O)N[C@@H]([C@@H](C)CC)C(=O)NCC(=O)N[C@@H](CCCCN)C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](CC=1C=CC=CC=1)C(=O)N[C@@H](CCCCN)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H]([C@@H](C)CC)C(=O)N[C@@H](C(C)C)C(=O)N[C@@H](CCC(N)=O)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H]([C@@H](C)CC)C(=O)N[C@@H](CCCCN)C(=O)N[C@@H](CC(O)=O)C(=O)N[C@@H](CC=1C=CC=CC=1)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CC(N)=O)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](C(C)C)C(=O)N1[C@@H](CCC1)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H]([C@@H](C)O)C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](CO)C(O)=O)NC(=O)[C@H](CC=1C=CC=CC=1)NC(=O)[C@H](CC(O)=O)NC(=O)CNC(=O)[C@H](CC(C)C)NC(=O)[C@@H](N)CC(C)C)C1=CC=CC=C1 POIUWJQBRNEFGX-XAMSXPGMSA-N 0.000 description 1
- 230000036232 cellulite Effects 0.000 description 1
- 229940106189 ceramide Drugs 0.000 description 1
- 150000001783 ceramides Chemical class 0.000 description 1
- 239000002975 chemoattractant Substances 0.000 description 1
- 230000003399 chemotactic effect Effects 0.000 description 1
- 239000005482 chemotactic factor Substances 0.000 description 1
- 229940107161 cholesterol Drugs 0.000 description 1
- 235000012000 cholesterol Nutrition 0.000 description 1
- 230000001684 chronic effect Effects 0.000 description 1
- 230000004087 circulation Effects 0.000 description 1
- 230000000052 comparative effect Effects 0.000 description 1
- 235000013409 condiments Nutrition 0.000 description 1
- 208000010247 contact dermatitis Diseases 0.000 description 1
- 238000011109 contamination Methods 0.000 description 1
- 235000005822 corn Nutrition 0.000 description 1
- 230000002596 correlated effect Effects 0.000 description 1
- 230000000875 corresponding effect Effects 0.000 description 1
- 239000006071 cream Substances 0.000 description 1
- 201000010251 cutis laxa Diseases 0.000 description 1
- 230000007812 deficiency Effects 0.000 description 1
- 210000003298 dental enamel Anatomy 0.000 description 1
- 238000011026 diafiltration Methods 0.000 description 1
- 239000006185 dispersion Substances 0.000 description 1
- 230000037336 dry skin Effects 0.000 description 1
- 238000001035 drying Methods 0.000 description 1
- 239000000975 dye Substances 0.000 description 1
- 230000002255 enzymatic effect Effects 0.000 description 1
- 210000002615 epidermis Anatomy 0.000 description 1
- 238000000684 flow cytometry Methods 0.000 description 1
- 239000007850 fluorescent dye Substances 0.000 description 1
- 239000004088 foaming agent Substances 0.000 description 1
- 230000003325 follicular Effects 0.000 description 1
- 235000013305 food Nutrition 0.000 description 1
- 238000004108 freeze drying Methods 0.000 description 1
- 235000011389 fruit/vegetable juice Nutrition 0.000 description 1
- 208000007565 gingivitis Diseases 0.000 description 1
- 239000003102 growth factor Substances 0.000 description 1
- 150000003278 haem Chemical class 0.000 description 1
- 231100000869 headache Toxicity 0.000 description 1
- 239000013003 healing agent Substances 0.000 description 1
- 230000000887 hydrating effect Effects 0.000 description 1
- 230000002519 immonomodulatory effect Effects 0.000 description 1
- 230000000977 initiatory effect Effects 0.000 description 1
- 230000015788 innate immune response Effects 0.000 description 1
- 230000000749 insecticidal effect Effects 0.000 description 1
- 230000003834 intracellular effect Effects 0.000 description 1
- 239000007928 intraperitoneal injection Substances 0.000 description 1
- QXJSBBXBKPUZAA-UHFFFAOYSA-N isooleic acid Natural products CCCCCCCC=CCCCCCCCCC(O)=O QXJSBBXBKPUZAA-UHFFFAOYSA-N 0.000 description 1
- 150000002540 isothiocyanates Chemical class 0.000 description 1
- 235000008777 kaempferol Nutrition 0.000 description 1
- 230000029774 keratinocyte migration Effects 0.000 description 1
- 238000002372 labelling Methods 0.000 description 1
- 239000010410 layer Substances 0.000 description 1
- OYHQOLUKZRVURQ-IXWMQOLASA-N linoleic acid Natural products CCCCC\C=C/C\C=C\CCCCCCCC(O)=O OYHQOLUKZRVURQ-IXWMQOLASA-N 0.000 description 1
- 235000020778 linoleic acid Nutrition 0.000 description 1
- 244000144972 livestock Species 0.000 description 1
- 210000004924 lung microvascular endothelial cell Anatomy 0.000 description 1
- IQPNAANSBPBGFQ-UHFFFAOYSA-N luteolin Chemical compound C=1C(O)=CC(O)=C(C(C=2)=O)C=1OC=2C1=CC=C(O)C(O)=C1 IQPNAANSBPBGFQ-UHFFFAOYSA-N 0.000 description 1
- LRDGATPGVJTWLJ-UHFFFAOYSA-N luteolin Natural products OC1=CC(O)=CC(C=2OC3=CC(O)=CC(O)=C3C(=O)C=2)=C1 LRDGATPGVJTWLJ-UHFFFAOYSA-N 0.000 description 1
- 235000009498 luteolin Nutrition 0.000 description 1
- 239000011777 magnesium Substances 0.000 description 1
- 229910052749 magnesium Inorganic materials 0.000 description 1
- 229940035034 maltodextrin Drugs 0.000 description 1
- 239000003550 marker Substances 0.000 description 1
- 239000000401 methanolic extract Substances 0.000 description 1
- 230000004089 microcirculation Effects 0.000 description 1
- 239000011785 micronutrient Substances 0.000 description 1
- 235000013369 micronutrients Nutrition 0.000 description 1
- 239000008267 milk Substances 0.000 description 1
- UXOUKMQIEVGVLY-UHFFFAOYSA-N morin Natural products OC1=CC(O)=CC(C2=C(C(=O)C3=C(O)C=C(O)C=C3O2)O)=C1 UXOUKMQIEVGVLY-UHFFFAOYSA-N 0.000 description 1
- 210000003205 muscle Anatomy 0.000 description 1
- JXTPJDDICSTXJX-UHFFFAOYSA-N n-Triacontane Natural products CCCCCCCCCCCCCCCCCCCCCCCCCCCCCC JXTPJDDICSTXJX-UHFFFAOYSA-N 0.000 description 1
- 229930014626 natural product Natural products 0.000 description 1
- 230000014399 negative regulation of angiogenesis Effects 0.000 description 1
- MQYXUWHLBZFQQO-UHFFFAOYSA-N nepehinol Natural products C1CC(O)C(C)(C)C2CCC3(C)C4(C)CCC5(C)CCC(C(=C)C)C5C4CCC3C21C MQYXUWHLBZFQQO-UHFFFAOYSA-N 0.000 description 1
- 230000007935 neutral effect Effects 0.000 description 1
- 229960003966 nicotinamide Drugs 0.000 description 1
- 235000005152 nicotinamide Nutrition 0.000 description 1
- 239000011570 nicotinamide Substances 0.000 description 1
- VOFUROIFQGPCGE-UHFFFAOYSA-N nile red Chemical compound C1=CC=C2C3=NC4=CC=C(N(CC)CC)C=C4OC3=CC(=O)C2=C1 VOFUROIFQGPCGE-UHFFFAOYSA-N 0.000 description 1
- WWZKQHOCKIZLMA-UHFFFAOYSA-N octanoic acid Chemical class CCCCCCCC(O)=O WWZKQHOCKIZLMA-UHFFFAOYSA-N 0.000 description 1
- 229960002378 oftasceine Drugs 0.000 description 1
- 239000002674 ointment Substances 0.000 description 1
- ZQPPMHVWECSIRJ-KTKRTIGZSA-N oleic acid Chemical compound CCCCCCCC\C=C/CCCCCCCC(O)=O ZQPPMHVWECSIRJ-KTKRTIGZSA-N 0.000 description 1
- 244000039328 opportunistic pathogen Species 0.000 description 1
- 239000007800 oxidant agent Substances 0.000 description 1
- 230000003647 oxidation Effects 0.000 description 1
- 238000007254 oxidation reaction Methods 0.000 description 1
- 230000004792 oxidative damage Effects 0.000 description 1
- 230000036542 oxidative stress Effects 0.000 description 1
- 238000007911 parenteral administration Methods 0.000 description 1
- 230000007918 pathogenicity Effects 0.000 description 1
- 239000002304 perfume Substances 0.000 description 1
- 208000028169 periodontal disease Diseases 0.000 description 1
- 230000000144 pharmacologic effect Effects 0.000 description 1
- 229940067631 phospholipid Drugs 0.000 description 1
- 150000003904 phospholipids Chemical class 0.000 description 1
- 230000030439 positive regulation of keratinocyte migration Effects 0.000 description 1
- 239000000843 powder Substances 0.000 description 1
- 230000003244 pro-oxidative effect Effects 0.000 description 1
- 229940055019 propionibacterium acne Drugs 0.000 description 1
- 230000001681 protective effect Effects 0.000 description 1
- 238000000746 purification Methods 0.000 description 1
- 230000002285 radioactive effect Effects 0.000 description 1
- 102000005962 receptors Human genes 0.000 description 1
- 108020003175 receptors Proteins 0.000 description 1
- 238000011084 recovery Methods 0.000 description 1
- 230000007115 recruitment Effects 0.000 description 1
- 230000002787 reinforcement Effects 0.000 description 1
- 230000008439 repair process Effects 0.000 description 1
- 238000011160 research Methods 0.000 description 1
- 108700022109 ropocamptide Proteins 0.000 description 1
- 229960001860 salicylate Drugs 0.000 description 1
- YGSDEFSMJLZEOE-UHFFFAOYSA-M salicylate Chemical compound OC1=CC=CC=C1C([O-])=O YGSDEFSMJLZEOE-UHFFFAOYSA-M 0.000 description 1
- 239000000523 sample Substances 0.000 description 1
- 235000015067 sauces Nutrition 0.000 description 1
- 231100000241 scar Toxicity 0.000 description 1
- 230000037387 scars Effects 0.000 description 1
- 238000000926 separation method Methods 0.000 description 1
- 230000011664 signaling Effects 0.000 description 1
- 239000002356 single layer Substances 0.000 description 1
- 208000017520 skin disease Diseases 0.000 description 1
- 230000000391 smoking effect Effects 0.000 description 1
- 235000014347 soups Nutrition 0.000 description 1
- 241000894007 species Species 0.000 description 1
- 238000002798 spectrophotometry method Methods 0.000 description 1
- 229940032094 squalane Drugs 0.000 description 1
- 229940031439 squalene Drugs 0.000 description 1
- TUHBEKDERLKLEC-UHFFFAOYSA-N squalene Natural products CC(=CCCC(=CCCC(=CCCC=C(/C)CCC=C(/C)CC=C(C)C)C)C)C TUHBEKDERLKLEC-UHFFFAOYSA-N 0.000 description 1
- 210000002784 stomach Anatomy 0.000 description 1
- 238000005728 strengthening Methods 0.000 description 1
- 239000002600 sunflower oil Substances 0.000 description 1
- 239000006228 supernatant Substances 0.000 description 1
- 239000000725 suspension Substances 0.000 description 1
- 239000002562 thickening agent Substances 0.000 description 1
- 108060008226 thioredoxin Proteins 0.000 description 1
- 229940094937 thioredoxin Drugs 0.000 description 1
- 229940126672 traditional medicines Drugs 0.000 description 1
- 238000009281 ultraviolet germicidal irradiation Methods 0.000 description 1
- 230000017260 vegetative to reproductive phase transition of meristem Effects 0.000 description 1
- 239000011782 vitamin Substances 0.000 description 1
- 229930003231 vitamin Natural products 0.000 description 1
- 235000013343 vitamin Nutrition 0.000 description 1
- 229940088594 vitamin Drugs 0.000 description 1
- 235000009492 vitamin B5 Nutrition 0.000 description 1
- 239000011675 vitamin B5 Substances 0.000 description 1
- 238000005406 washing Methods 0.000 description 1
- 229960001296 zinc oxide Drugs 0.000 description 1
- 239000011787 zinc oxide Substances 0.000 description 1
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K36/00—Medicinal preparations of undetermined constitution containing material from algae, lichens, fungi or plants, or derivatives thereof, e.g. traditional herbal medicines
- A61K36/18—Magnoliophyta (angiosperms)
- A61K36/185—Magnoliopsida (dicotyledons)
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K45/00—Medicinal preparations containing active ingredients not provided for in groups A61K31/00 - A61K41/00
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K8/00—Cosmetics or similar toiletry preparations
- A61K8/18—Cosmetics or similar toiletry preparations characterised by the composition
- A61K8/30—Cosmetics or similar toiletry preparations characterised by the composition containing organic compounds
- A61K8/60—Sugars; Derivatives thereof
- A61K8/602—Glycosides, e.g. rutin
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K8/00—Cosmetics or similar toiletry preparations
- A61K8/18—Cosmetics or similar toiletry preparations characterised by the composition
- A61K8/96—Cosmetics or similar toiletry preparations characterised by the composition containing materials, or derivatives thereof of undetermined constitution
- A61K8/97—Cosmetics or similar toiletry preparations characterised by the composition containing materials, or derivatives thereof of undetermined constitution from algae, fungi, lichens or plants; from derivatives thereof
- A61K8/9783—Angiosperms [Magnoliophyta]
- A61K8/9789—Magnoliopsida [dicotyledons]
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P17/00—Drugs for dermatological disorders
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P17/00—Drugs for dermatological disorders
- A61P17/02—Drugs for dermatological disorders for treating wounds, ulcers, burns, scars, keloids, or the like
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P17/00—Drugs for dermatological disorders
- A61P17/10—Anti-acne agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P9/00—Drugs for disorders of the cardiovascular system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61Q—SPECIFIC USE OF COSMETICS OR SIMILAR TOILETRY PREPARATIONS
- A61Q19/00—Preparations for care of the skin
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61Q—SPECIFIC USE OF COSMETICS OR SIMILAR TOILETRY PREPARATIONS
- A61Q19/00—Preparations for care of the skin
- A61Q19/06—Preparations for care of the skin for countering cellulitis
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61Q—SPECIFIC USE OF COSMETICS OR SIMILAR TOILETRY PREPARATIONS
- A61Q19/00—Preparations for care of the skin
- A61Q19/08—Anti-ageing preparations
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61Q—SPECIFIC USE OF COSMETICS OR SIMILAR TOILETRY PREPARATIONS
- A61Q5/00—Preparations for care of the hair
- A61Q5/006—Antidandruff preparations
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K2236/00—Isolation or extraction methods of medicinal preparations of undetermined constitution containing material from algae, lichens, fungi or plants, or derivatives thereof, e.g. traditional herbal medicine
- A61K2236/50—Methods involving additional extraction steps
- A61K2236/53—Liquid-solid separation, e.g. centrifugation, sedimentation or crystallization
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K2800/00—Properties of cosmetic compositions or active ingredients thereof or formulation aids used therein and process related aspects
- A61K2800/80—Process related aspects concerning the preparation of the cosmetic composition or the storage or application thereof
- A61K2800/805—Corresponding aspects not provided for by any of codes A61K2800/81 - A61K2800/95
Abstract
Composición que comprende a título de principio activo un extracto de partes aéreas de Gynandropsis gynandra, caracterizada por que el extracto comprende por lo menos un 3% en peso de polifenoles, expresado en equivalente de ácido gálico con respecto al peso del extracto seco, siendo dichos polifenoles ventajosamente unos flavonoides, típicamente con un contenido de por lo menos un 1% en peso de flavonoides, expresado en equivalente de rutina con respecto al peso del extracto seco, y llegado el caso, un excipiente apropiado, siendo dicho extracto susceptible de ser obtenido por extracción sólido-líquido de las partes aéreas de Gynandropsis gynandra en unas mezclas binarias de agua y de glicerol o de glicol tal como el propanodiol, conteniendo dicha mezcla binaria agua en unas proporciones comprendidas entre el 10 y el 50% con respecto al otro disolvente.
Description
DESCRIPCIÓN
Extracto de partes aéreas de Gynandropsis gynandra o Cleome gynandra y composiciones cosméticas, dermatológicas o farmacéuticas que lo comprenden.
La invención se refiere a una composición, preferentemente cosmética, dermatológica o farmacéutica, que comprende un extracto de partes aéreas de Gynandropsis gynandra, más ventajosamente hojas, y ventajosamente un excipiente apropiado.
Ventajosamente, el extracto de partes aéreas de Gynandropsis gynandra, en la composición, tiene un contenido comprendido entre el 0,01% y el 10% en peso con respecto al peso total dela composición.
La invención tiene también por objeto un procedimiento de extracción de un extracto de partes aéreas de Gynandropsis gynandra y más ventajosamente de hojas, así como el extracto susceptible de ser obtenido mediante dicho procedimiento.
La invención se refiere también a una composición de este tipo o a un extracto de este tipo para su utilización en la prevención o el tratamiento de los trastornos o patologías de la piel, de las mucosas o de los faneros, para su utilización en la prevención o el tratamiento de los trastornos vasculares y/o de los problemas relacionados con la hiperseborrea, o para su utilización como producto anti-acneico, anti-envejecimiento, cicatrizante, hidratante, adelgazante y/o anti-celulitis, anti-alérgico y pro-pigmentante. La invención se refiere por último a un procedimiento de cuidado cosmético de la piel, de los faneros o de las mucosas, para mejorar su estado o su aspecto, que consiste en administrar este tipo de composición o este tipo de extracto.
Gynandropsis gynandra es una planta de la familia de las capparaceas. Sus nombres botánicos son los siguientes: Gynandropsis gynandra (L.) Briq o Gynandropsis pentaphylla o Cleome gynandra. Se designa también bajo diversos nombres vernáculos, que varían en función de las zonas geográficas. Se podrán citar: * “wouin wouin” en Jula (Sudoeste de Burkina) y Kynebdo en Moorea (centro de Burkina Faso) y numerosas denominaciones diferentes en los diferentes países de África;
* Cleome, Gynandro, Mouzambre a fleurs blanches en francés;
* Cat's whiskers o spider flower en inglés; y
* Senfkapper, benzoinbaun en alemán.
Es una pequeña planta herbácea anual, planta cultivada de 15 a 30 cm de altura, que puede alcanzar 1,5 m de altura en su forma salvaje, de hojas pequeñas, tallos redondos, a veces rojizos. La floración está constituida por pequeñas flores azules a violetas pálidas. Los frutos son unas vainas alargadas de 4 a 6 cm de largo, que contienen numerosas semillas, minúsculas, negruzcas.
Se ha descrito que las hojas y los tallos contienen los compuestos siguientes:
■ Isotiocianato (cleomina),
■ Núcleos esterólicos (lupeol, campesterol, epi-lupeol),
■ Vitamina C (127 -484 mg/100g),
■ p-caroteno (6,7 -18,9 mg/100g),
■ Carbohidratos (4,4 - 6,4%),
■ Proteínas (3,1 - 7,7%),
■ Compuestos fenólicos (520 - 910 mg/100 g),
■ Calcio (213 - 434 mg/100 g), y
■ Magnesio (86 mg/100 g).
La presencia de alcaloides se menciona también por algunos autores, pero no por otros.
Se ha descrito que las hojas y los tallos contienen los compuestos siguientes:
■ un 29,5% de proteínas
■ un 28% de lípidos (un 59% ácido linoleico y aproximadamente un 20% de ácido oleico)
■ Esteroles
■ Compuestos fenólicos (kaempferol, luteolina).
Las partes aéreas (tallo y hojas) se utilizan tradicionalmente para administración por vía oral. Teniendo en cuenta su reputación como planta con alto contenido en vitaminas y micro-nutrientes, se utiliza generalmente como planta alimenticia, tanto en el adulto como en el niño y es muy recomendada para mujeres embarazadas como
condimento para salsas y también como vegetales en sopas generalmente.
Las partes aéreas y las tortas obtenidas después de la extracción del aceite de las semillas se pueden utilizar como forraje para el ganado.
Por otro lado, unas preparaciones de hojas, tallos y semillas, tendrían propiedades insecticidas, vermífugas, antiparasitarias y antimicrobianas, y antioxidantes cuando se consumen por vía oral. El jugo de hojas se utilizaría utilizado en lavados oculares. Las semillas, consumidas por vía oral, presentarían propiedades antivomitivas. En diferentes medicinas tradicionales (en particular en África o en India, la planta se utiliza por vía oral, esencialmente para el tratamiento de los dolores (dolores de cabeza, dolores relacionados con el parto, estómago), mordeduras de escorpión. Las hojas se pueden aplicar directamente sobre las heridas purulentas para prevenir la formación de pus.
Estudios farmacológicos recientes han reforzado algunos de estos usos tradicionales: actividad analgésica en el ratón por inyección intra-peritoneal de extractos de la planta (U.R. Ghogare et al., Natural Product Research, 23 (4): 327-333 (2009)); efecto anti-artritis en la rata por vía oral (R.T. Narendhirakannan et al., Molecular and Cellular Biochemistry, 276: 71-80 (2005)); efecto beneficioso anti-colesterol por vía oral (T. Johns, Journal of Ethnopharmocology, 66: 1-10 (1999)).
El documento Philippine medicinal plants: Apoi-apoian es un estudio botánico sobre la planta Gynandropsis Gynandra, que se puede utilizar para el tratamiento de diversas enfermedades de la piel.
El documento Narendhirakkannan et al. describe un extracto de hojas secas de Gynandropsis Gynandra obtenido con etanol al 95%.
El documento FR 2945943 se refiere a la utilización de un extracto vegetal rico en polifenoles como agente activo cosmético. Este documento se refiere más particularmente a la utilización de un extracto de rosa que presenta naturalmente un contenido elevado en antocianos, como agente anti-oxidante.
Por otro lado, la solicitud americana US 2004/0028643A1 describe la selección de numerosas plantas, para su utilización en composiciones anti-envejecimiento. Los resultados dados en los ejemplos de esta solicitud americana revelan que el extracto de planta de Cleome gynandra (extracto metanólico de una parte no definida o de la totalidad de la planta) no muestra resultados satisfactorios. En particular, tras el ensayo actividad anti-DPPH, el extracto no se ha conservado con una actividad significativa.
Por el contrario, los inventores han descubierto que los extractos de partes aéreas (hojas, tallos, flores, semillas) de Gynandropsis gynandra, y ventajosamente los extractos de hojas, presentaban propiedades cosméticas y dermatológicas nunca descritas hasta la fecha. Los siguientes ejemplos muestran que el extracto de acuerdo con la invención tiene una actividad anti-DPPH significativa.
Es la primera vez que se utilizan extractos de partes aéreas de Gynandropsis Gynandra como tales, por sus propiedades específicas.
La invención tiene por objeto una composición que comprende, a título de principio activo, un extracto de partes aéreas de Gynandropsis Gynandra (denominado en lo sucesivo extracto según la invención), ventajosamente de un extracto de hojas de Gynandropsis Gynandra, caracterizada por que el extracto comprende por lo menos un 3% en peso de polifenoles, expresado en equivalente de ácido gálico con respecto al peso del extracto seco. Ventajosamente, los polifenoles son unos flavonoides. Según este carácter particular, el extracto comprende por lo menos un 1% en peso de flavonoides, ventajosamente por lo menos un 3% en peso, expresado en equivalente de rutina con respecto al peso del extracto seco.
El extracto de Gynandropsis Gynandra, según la invención, está eventualmente en asociación con un excipiente apropiado en la composición.
La composición es ventajosamente una composición cosmética, dermatológica o farmacéutica.
La composición está destinada ventajosamente a ser aplicada por vía tópica externa sobre la piel, los faneros y/o las mucosas, en particular las pieles, los faneros y/o las mucosas sensibles o agredidas por el entorno, por ejemplo por los uV o la contaminación.
El extracto es ventajosamente un extracto de hojas de Gynandropsis Gynandra.
El extracto según la invención se caracteriza por su contenido en polifenoles (ensayo de Folin-Ciocalteu) que es de por lo menos un 3% en peso expresado en equivalente de ácido gálico con respecto al peso del extracto
seco.
Entre los polifenoles presentes en este extracto, los flavonoides son particularmente interesantes. Así, en una variante ventajosa de la invención, el extracto según la invención puede estar caracterizado por su contenido en flavonoides (ensayo con cloruro de aluminio), que es de por lo menos un 1% en peso de flavonoides expresado en equivalente rutina con respecto al peso del extracto seco. Preferentemente, estos flavonoides están constituidos principalmente por rutina y por sus derivados.
La rutina es un compuesto de fórmula (I):
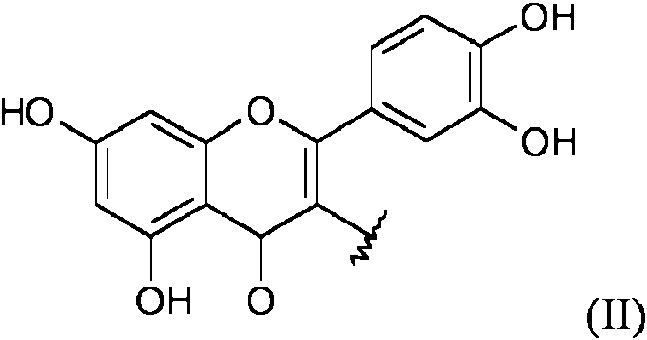
Los derivados de la rutina son ventajosamente los compuestos en los que se encuentra el residuo flavónico de la rutina, residuo de fórmula (II):
En los flavonoides contenidos en el extracto según la invención, se encuentra ventajosamente rutina y sus derivados en una proporción, en peso expresada en equivalente rutina con respecto al contenido en peso total de flavonoides, de por lo menos un 50%, ventajosamente por lo menos un 60%, más ventajosamente por lo menos un 70%, aún más ventajosamente por lo menos un 80%.
Según una variante ventajosa de la invención, el extracto contiene del 0% al 80%, ventajosamente del 10% al 80%, más ventajosamente del 30 al 70% de azúcares, expresándose los % en peso con respecto al peso del extracto seco.
El extracto según la invención contiene ventajosamente del 0 al 50% en peso, más ventajosamente del 0 al 20% en peso, aún más ventajosamente del 0 al 10% en peso de lípidos de Gynandropsis Gynandra; expresándose los % en peso con respecto al peso total del extracto.
El extracto según la invención contiene ventajosamente del 0 al 60% en peso, más ventajosamente del 0,5 al 30% en peso, aún más ventajosamente del 0,5 al 10% en peso de proteínas de Gynandropsis Gynandra; expresándose los % en peso con respecto al peso total del extracto (ensayo de Bradford).
Este extracto es susceptible de ser obtenido por extracción sólido-líquido de las partes aéreas, frescas o secas, de Gynandropsis Gynandra en un disolvente acuoso y glicólico y/o glicerólico. Las partes aéreas son ventajosamente las hojas.
El disolvente se selecciona de entre las mezclas binarias de agua con el glicerol, un glicol como el propanodiol, o sus mezclas, en proporciones comprendidas entre el 10% y el 50% de agua con respecto a los otros disolventes. Principalmente, se utilizan unas mezclas binarias de disolventes de tipo agua y un disolvente seleccionado de entre el glicerol o el propanodiol.
Más particularmente, se introducirá entre el 0,1 y el 50% en peso (en equivalente de materia seca) de partes de planta deseadas en el disolvente de extracción, y preferentemente entre el 1 y el 10% en peso, ventajosamente el 5% en peso (los % se expresan en peso de la materia seca con respecto al peso total utilizado). La parte seca de Gynandropsis Gynandra puede ser las hojas, los tallos, las flores, las semillas, solas o asociadas, y
preferentemente las hojas.
En presencia de glicerol, se seleccionará una proporción comprendida entre el 0 y el 100% de glicerol en agua, preferentemente entre el 30 y el 80%, y ventajosamente el 80% (los % se expresan en peso de glicerol con respecto al peso total agua+glicerol).
En presencia de glicol y más particularmente de propanodiol, se seleccionará una proporción comprendida entre el 0 y el 100% de propanodiol en agua, preferentemente entre el 10 y el 80%, y ventajosamente el 60% (los % se expresan en peso de propanodiol con respecto al peso total agua+propanodiol).
La temperatura de extracción está ventajosamente comprendida entre 4°C y 100°C, y preferentemente entre 10°C y 60°C, y más particularmente entre 15°C y 30°C.
La duración de extracción varía ventajosamente de 30 minutos a 4 horas, y preferentemente de 30 minutos a 2 horas, y más ventajosamente es de aproximadamente 1 hora.
Al final de la extracción, la materia seca residual se separa ventajosamente de la fase líquida, por ejemplo por filtración, decantación o centrifugación. La fase líquida así obtenida se puede filtrar con la ayuda de filtros de porosidad adecuada con el fin de obtener una solución límpida.
Estas primeras etapas de separación pueden ir seguidas de etapas de purificación, por ejemplo por ultrafiltración y/o nanofiltración, que permiten concentrar las moléculas de interés potenciales a costa de otras.
El extracto obtenido podrá presentarse en forma líquida pero también podrá secarse según los métodos conocidos por el experto en la técnica, la atomización o la liofilización, por ejemplo con o sin soporte, tal como la maltodextrina.
La invención tiene también por objeto un procedimiento de preparación de un extracto de partes aéreas de Gynandropsis Gynandra que comprende las etapas sucesivas siguientes:
(a) dispersión en fase líquida en un disolvente adecuado de las partes aéreas de Gynandropsis Gynandra, y ventajosamente de las hojas,
(b) sometimiento de la mezcla obtenida tras la etapa (a) a una extracción en un disolvente acuoso y/o glicólico y/o glicerólico;
(c) centrifugación y/o filtración del extracto obtenido tras la etapa (b);
(d) llegado el caso, ultrafiltración y/o diafiltración y/o nanofiltraxción del extracto obtenido tras la etapa (c); (e) tras la etapa (c) o (d), recuperación del extracto de partes aéreas de Gynandropsis Gynandra;
(f) secado eventual del extracto obtenido en la etapa (e) sobre un soporte o no.
Durante la etapa (a), se utilizan ventajosamente las hojas en las proporciones siguientes: entre el 0,1 y el 50% de materia seca de hojas, preferentemente entre el 5 y el 20%, y ventajosamente el 5%, expresándose los porcentajes en peso de la materia seca con respecto al peso total utilizado.
La etapa (b) se realiza ventajosamente bajo agitación. No se ha añadido ninguna enzima.
Durante la etapa (c), se utilizan ventajosamente los disolventes seleccionados de entre las mezclas binarias de agua con el glicerol, un glicol como el propanodiol, o sus mezclas en una proporción ventajosamente comprendida entre el 30 y el 90% de estos disolventes en agua y más ventajosamente entre el 50 y el 80% (los % se expresan en peso de disolvente con respecto al peso total disolvente+agua).
El extracto se utiliza ventajosamente como agente activo en una composición tal como una composición cosmética, dermatológica o farmacéutica, que puede comprender uno o varios excipientes apropiados. La composición puede comprender además por lo menos otro compuesto activo además del extracto de partes aéreas de Gynandropsis Gynandra. Este otro compuesto se puede seleccionar de entre todos los compuestos y sus equivalentes funcionales, enunciados anteriormente.
Este otro compuesto se puede seleccionar en particular de entre unos activos utilizados clásicamente en dermatología, farmacología o en cosmética y conocidos por el experto en la materia tales como los emolientes, los activos hidratantes, los queratorreguladores, los queratolíticos, los agentes cicatrizantes y/o reestructurantes de la barrera cutánea, los agonistas PPAR, RXR o LXR, los agentes seborreguladores, los agentes anti-irritantes y/o antiinflamatorios y/o calmantes, los agentes antioxidantes, los agentes antienvejecimiento, los agentes
despigmentantes o hipopigmentantes, los agentes pigmentantes, los agentes lipolíticos o inhibidores de la lipogénesis o también los agentes anti-celulíticos o adelgazantes, los filtros y pantallas solares minerales u orgánicas, los compuestos antifúngicos, los conservantes, los agentes anti-bacterianos, los pre y probióticos, los antibióticos, los inmunomoduladores.
Más particularmente, los agentes cicatrizantes y/o reestructurantes de la barrera cutánea que se pueden utilizar en asociación son ventajosamente el pantenol (vitamina B5), el arabinogalactano, el óxido de zinc, las ceramidas, el colesterol, el escualano y los fosfolípidos.
Los agentes seborreguladores que se pueden utilizar en asociación se seleccionan ventajosamente de entre el grupo constituido por los inhibidores de 5-alfareductasa. El zinc (y los derivados de zinc tal como sus sales gluconato, salicilato y ácido piroglutámico) y la espironolactona, presentan también una actividad sebosupresora.
Otros seborreguladores de origen lipídico que actúan sobre la calidad del sebo, como el ácido linoleico presentan un interés.
El agente antiinflamatorio y/o antiirritante y/o calmante puede ser el arabinogalactano.
Los activos protectores solares que se pueden utilizar en asociación son ventajosamente unos filtros o pantallas solares UVB y/o UVA; tales como las pantallas o filtros minerales y/u orgánicos conocidos por el experto en la materia que adaptará su elección y sus concentraciones en función del grado de protección buscado.
Los conservantes que se pueden utilizar en asociación son, por ejemplo, los utilizados generalmente en cosmética, las moléculas con actividad antibacteriana (pseudo-conservantes) tales como los derivados caprílicos, como por ejemplo la caproliol glicina o el caprilato de glicerilo; el hexanodiol, el levulinato sódico, y los derivados de zinc y de cobre (gluconato y PCA).
Entre los activos recomendados en asociación con el extracto según la invención, se pueden citar los extractos vegetales, en particular:
- los aceites vegetales tales como los aceites de soja y/o el aceite de colza (el aceite de aguacate (WO 2004/012496, WO 2004/012752, WO 2004/016106, WO 2007/057439), el aceite de altramuz, ventajosamente el aceite de altramuz blanco dulce (WO 98/47479), o una mezcla de estos aceites;
- el oleodestilado o los concentrados de aceite vegetal o animal, en particular de girasol, más ventajosamente unos concentrados de girasol linoleicos, tales como el aceite de girasol concentrado en insaponificables (Soline®) (véase la solicitud internacional WO 01/21150) comercializada por los laboratorios Expanscience, los aceites concentrados en insaponificable de tipo aceite de aguacate, de colza, de maíz o de palma, útiles en particular por su actividad hidratante y/o emoliente, cicatrizante y/o reestructurante de la barrera cutánea, anti-inflamatoria y/o antiirritante y/o calmante;
- los insaponificables de vegetales o de aceite vegetal, ventajosamente unos furanos de aguacate (Avocadofurane®), que se pueden obtener mediante el procedimiento descrito en la solicitud internacional WO 01/21605, los insaponificables de aguacate y/o de soja, más particularmente una mezcla de insaponificables de aguacate furánicos y de insaponificables de soja, ventajosamente en una relación respectiva de aproximadamente 1/3-2/3 (tal como Piasclédine®), los insaponificables de soja (tales como los obtenidos según el procedimiento descrito en la solicitud internacional WO 01/51596), los insaponificables esterólicos (típicamente unos insaponificables cuyo contenido en esteroles, en metilesteroles y en alcohol triterpénicos está comprendido entre el 20 y el 95% en peso, preferentemente del 45-65% en peso, con respecto al peso total del insaponificable), los fitosteroles, los ésteres de esteroles y los derivados vitamínicos, útiles en particular por su actividad cicatrizante y/o reestructurante de la barrera cutánea, antienvejecimiento, antiinflamatoria;
- los péptidos o complejos de aminoácidos vegetales, en particular los péptidos de aguacate (tales como los descritos en la solicitud internacional WO 2005/105123), los péptidos de altramuz (tales como los obtenidos según el procedimiento descrito en la solicitud WO 2005/102259), los péptidos de quinoa (tales como los descritos en la solicitud internacional WO 2008/080974), los péptidos de Maca tales como los descritos en la solicitud internacional WO 2004/112742), los péptidos de soja fermentada o no, los péptidos de arroz (tales como los descritos en la solicitud internacional WO 2008/009709), útiles en particular por su actividad hidratante y/o emoliente (aguacate), queratorreguladora (altramuz, quinoa), cicatrizante y/o reestructurante de la barrera cutánea (maca, quinoa, soja), antiinflamatoria y/o anti irritante y/o calmante (altramuz, quinoa), antioxidante (aguacate), antienvejecimiento (altramuz, maca) pigmentante (arroz), los péptidos de Schizandra (tales como los descritos en la solicitud de patente FR 0955 344), el extracto de semillas de Acacia macrostachya (tal como el descrito en la solicitud de patente FR 0 958 525) y unas semillas de Vigna unguiculata (tal como las descritas en la solicitud de
patente FR 0958529);
- los azúcares de vegetales, en particular los azúcares de aguacate (tales como los descritos en la solicitud WO 2005/115421), útiles en particular para sus propiedades queratorreguladora, cicatrizante y/o reestructurante de la barrera cutánea, antiinflamatoria y/o anti-irritante y/o calmante;
- el avocadato de butilo (5 alpha Avocuta®), inhibidor de la 5-alfa reductasa (véanse los documentos WO 01/52837 y WO 02/06205) y típicamente, regulador de la secreción seborrea que se encuentra aumentada en el acné o la caspa;
- los extractos ricos en polifenol, y más particularmente los extractos de frutos de aguacate (tales como los descritos en la solicitud FR 1061 055) y los extractos de hojas de Maca (tal como los descritos en la solicitud FR 1061047);
- el lupeol (FR 2822821, FR 2857596) útil en particular para favorecer la cicatrización;
- un extracto total de altramuz (tal como los descritos en la solicitud internacional WO 2005/102259), particularmente adaptado para el tratamiento de las irritaciones;
- una manteca de Cupuagu, particularmente apreciada por sus propiedades hidrantes.
Entre los activos recomendados en asociación con el extracto según la invención, se pueden citar las oxazolinas, en particular las seleccionadas de entre el grupo constituido por la 2-undecil-4-hidroximetil-4-metil-1,3-oxazolina, la 2-undecil-4,4-dimetil-1,3-oxazolina, la (E)-4,4-dimetil-2-heptadec-8-enil-1,3-oxazolina, la 4-hidroximetil-4-metil-2-heptadecil-1,3-oxazolina, la (E)-4-hidroximetil-4-metil-2-heptadec-8-enil-1,3-oxazolina, la 2-undecil-4-etil-4-hidroximetil-1,3-oxazolina, preferentemente la 2-undecil-4,4-dimetil-1,3-oxazolina (OX-100 o Cyclocéramide®; WO 2004050052, WO 2004050079, y WO 2004112741). Son particularmente útiles por su actividad antiinflamatoria y/o antiirritante y/o calmante, antioxidante, despigmentante, inmunomoduladora.
Entre los activos recomendados en asociación con el extracto según la invención, se pueden citar los inhibidores de 5-alfareductasa, tales como el avocadato de butilo (5 alpha Avocuta®).
Todas estas asociaciones comprenden por lo menos otro compuesto activo, además del extracto de partes aéreas de Gynandropsis gynandra, y pueden comprender dos, tres, cuatro o más compuestos activos tales como los descritos anteriormente.
La composición según la invención se puede formular en forma de diferentes preparaciones adaptadas para una administración tópica, para una administración oral, rectal, vaginal, nasal, auricular o bronquial, así como para una administración parenteral. La composición según la invención se formula ventajosamente en forma de diferentes preparaciones adaptadas para una administración tópica, más particularmente para aplicación sobre la piel, y/o los faneros y/o las mucosas.
Según una primera variante, las diferentes preparaciones son adecuadas para la administración tópica e incluyen en particular las cremas, las emulsiones, las leches, las pomadas, las lociones, los aceites, las soluciones acuosas o hidro-alcohólicas o glicólicas, los polvos, los parches, los espráis, los champús, los esmaltes o cualquier otro producto para la aplicación externa.
Los modos de administración, las posologías y las formas galénicas óptimas de los compuestos y composiciones según la invención se pueden determinar según los criterios tenidos en cuenta generalmente en el establecimiento de un tratamiento farmacéutico, en particular dermatológico, cosmético o veterinario adaptado a un paciente o a un animal como, por ejemplo, la edad o el peso corporal del paciente o del animal, la gravedad de su estado general, la tolerancia al tratamiento, los efectos secundarios constatados, el tipo de piel. En función del tipo de administración deseada, la composición y/o los compuestos activos según la invención pueden comprender además por lo menos un excipiente farmacéuticamente aceptable, en particular dermatológicamente aceptable, o un excipiente cosméticamente aceptable. Según la primera variante, se utiliza un excipiente adaptado para una administración por vía tópica externa. La composición según la presente invención puede comprender además por lo menos un adyuvante farmacéutico o cosmético conocido por el experto en la materia, seleccionado de entre los espesantes, los conservantes, los perfumes, los colorantes, unos filtros químicos o minerales, los agentes hidratantes, las aguas termales, etc.
La composición que comprende un extracto de partes aéreas de Gynandropsis gynandra que tiene las especificaciones indicadas está particularmente destinada a una utilización cosmética o dermatológica. La composición se formulará ventajosamente en forma de una preparación adaptada a una administración tópica. La invención tiene también por objeto la composición según la invención o un extracto de partes aéreas de Gynandropsis gynandra tal como se ha definido anteriormente, para su utilización como composición cosmética,
farmacéutica, dermatológica, ventajosamente cosmética o dermatológica.
Ventajosamente, la composición o el extracto según la presente invención se utilizan en la prevención y/o el tratamiento de los trastornos o patologías de la piel y/o de las mucosas y/o de los faneros.
En particular, la composición o el extracto según la presente invención se utilizan en la prevención y/o el tratamiento de los trastornos relacionados con el acné.
La fisiopatología del acné se asocia a diferentes factores iniciadores entre los cuales: la hiper-seborrea, la hiperqueratinización folicular (comedogenesis), y la colonización bacteriana por Propionibacterium acnes (P. acnes). Estos factores están intrincados e interactúan los unos con los otros (Bellew et al. 2011, 10(6): 582-585).
La producción de sebo por las glándulas sebáceas tiene un papel crucial en el desarrollo de las lesiones de acné. En efecto, la hiper-seborrea asociada con la alteración cualitativa del sebo genera unas señales que pueden inducir a la hiper-queratinización y crear, así, un entorno propicio para la multiplicación de P. acnés.
El acné se asocia también a un desarrollo excesivo de P. acnés. Esta bacteria comensal se comporta como un patógeno oportunista favorecido por el entorno del acné (hiper-seborrea/inflamación/obstrucción del folículo). P. acnés produce numerosos factores que contribuyen a agravar la comedogénesis y la inflamación: señalización mediante TLR (receptores de tipo Toll) para inducir y mantener la inflamación, liberar enzimas que conducen a la ruptura de la pared del folículo, producción de factores quimiotácticos para la atracción del neutrófilo.
La composición o el extracto según la presente invención se utilizan por lo tanto también en la prevención y/o el tratamiento de los trastornos relacionados con la hiper-seborrea, tal como la dermatitis seborreica (costra láctea), el acné y las pieles con tendencia acneica, y los estados de caspa.
La composición o el extracto según la invención son particularmente útiles en la prevención y/o el tratamiento de los trastornos vasculares, para la protección de los vasos sanguíneos y/o para actuar sobre la circulación sanguínea, en particular la microcirculación sanguínea.
La composición o el extracto según la invención se utilizan por lo tanto ventajosamente en la prevención y/o el tratamiento de la dilatación (crónica) de los capilares subcutáneos que se puede producir en las condiciones tales como la cuperosis, los eritemas cutáneos, la rosácea, el prurito, la piel y/o las mucosas reactivas, con enrojecimiento, que se deben en particular a una dilatación de los capilares subcutáneos.
La composición o el extracto según la invención se utiliza ventajosamente como producto anti-envejecimiento cronológico o foto-inducido en la prevención del envejecimiento, y del envejecimiento foto-inducido y, como producto cicatrizante, en la prevención y/o el tratamiento de los trastornos relacionados con la circulación y con la organización cutánea.
Se entiende por trastornos relacionados con la cicatrización y con la organización cutánea, los trastornos que resultan de los procesos de cicatrización y de organización cutánea de la piel tales como piel suelta, estrías, herpes, grietas, fisuras, en particular a nivel de los senos.
En particular, la composición o el extracto según la invención se utilizan como producto hidratante, que interviene en la prevención y/o el tratamiento de los trastornos de la barrera o de la homeostasis de la piel, de los faneros (cabellos y uñas) y/o de las mucosas (encías, periodontitis, mucosas genitales), inmadura(s), normal(es) o madura(s).
Se entiende por trastornos de la barrera de la piel, de los faneros y/o de las mucosas, los trastornos que intervienen a nivel de la capa externa de la epidermis.
Se entiende por trastornos de la homeostasis de la piel, de los faneros y/o de las mucosas, los trastornos que resultan de los procesos de renovación y de equilibrio de las células tales como la psoriasis, la dermatitis de contacto, la dermatitis atópica, la piel seca (xerosis), la piel deshidratada y la piel fotosensibilizada.
La composición o el extracto según la invención se utilizan también ventajosamente en el tratamiento y/o la prevención de las inflamaciones debida a los rayos de cualquier tipo, en particular quemaduras de sol.
La composición o el extracto según la presente invención pueden utilizarse también ventajosamente como producto adelgazante en la regulación del tejido adiposo, de la celulitis y más particularmente mediante la inhibición de la lipogénesis.
La composición o el extracto según la invención se utilizan como producto anti-alérgico en la prevención y/o en el tratamiento de las reacciones o patologías alérgicas tal como la dermatitis alérgica, la dermatitis de contacto, el eczema y el prurito.
Ventajosamente, la composición o el extracto según la invención se pueden utilizar como producto propigmentante en la prevención y/o el tratamiento de las reacciones, trastornos o patologías de la piel que presentan trastornos de la despigmentación, tal como la piel despigmentada (vitíligo).
Ventajosamente, la composición o el extracto según la invención se pueden utilizar para la prevención y/o el tratamiento de las reacciones, trastornos o patologías de la piel o de las reacciones, trastornos o patologías de los faneros tales como el cabello (alopecia, caspa, hirsutismos, foliculitis) o de las reacciones, trastornos o patologías de las mucosas tales como las encías y periodontitis que pueden presentar unas gingivitis (encías sensibles de los recién nacidos, problemas de higiene, debidos al tabaquismo u otros), periodontopatías, o de las mucosas genitales que pueden presentar unas irritaciones de las esferas genitales machos o hembras externas o internas, relacionadas con una deficiencia de la inmunidad innata (péptidos antimicrobianos) o adquirida (celular, humoral, citoquinas).
La invención se refiere también a un procedimiento de cuidado cosmético de la piel y/o de los faneros y/o de las mucosas, para mejorar su estado y/o su aspecto, que consiste en aplicar sobre la piel y/o los faneros y/o las mucosas de los pacientes que lo necesitan una composición o un extracto según la presente invención.
En un modo de realización del procedimiento cosmético según la invención, la piel y/o los faneros y/o las mucosas en cuestión son ventajosamente los que son sensibles, están irritados, atacados por el entorno (UV, contaminación), en particular las pieles sensibles. Las pieles sensibles presentan frecuentemente unos enrojecimientos (en particular de la cara), típicamente con tiranteces o picores diarios.
El procedimiento cosmético según la invención tiene en particular el objetivo de mejorar los pacientes que sufren de acné y que presentan pieles con tendencia acneica y también para mejorar los estados de caspa.
El procedimiento cosmético según la invención se caracteriza también por que la composición o el extracto es un producto antienvejecimiento cronológico o fotoinducido, hidratante, adelgazante y/o anticelulítico.
Ejemplo comparativo 1
Los tallos de Gynandropsis gynandra secados y triturados se ponen en suspensión bajo agitación al 5% en una mezcla etanol/agua 80/20 p/p durante 1 h a temperatura ambiente. La materia seca residual se separa de la fase líquida por filtración, decantación o centrifugación y la fase líquida así obtenida se puede filtrar con la ayuda de filtros de porosidad adaptada con el fin de obtener una solución límpida. El extracto obtenido presenta las características siguientes:
■ Azúcares totales (antrona): 41%/seco
■ Polifenoles totales (Folin - Ciocalteu) - eq. Ácido gálico: 7,7%/seco
■ Proteínas (evaluación de Bradford): 3,1%/seco.
Este extracto presenta una actividad anti-radicalaria, anti-DPPH “in tubo’’, para la cual se ha podido determinar la concentración inhibidora 50 (IC50) y es de 0,2 mg de extracto seco, lo cual representa 19 |jg de polifenoles en el medio de reacción.
Ejemplo 2
Los tallos con hojas de Gynandropsis gynandra secados y triturados se ponen en suspensión bajo agitación al 5% en una mezcla glicerol/agua 80/20 p/p durante 1 h a temperatura ambiente. La materia seca residual se separa de la fase líquida por filtración, decantación o centrifugación y la fase líquida así obtenida se puede filtrar con la ayuda de filtros de porosidad adaptada con el fin de obtener una solución límpida. El extracto obtenido presenta las características siguientes:
■ Azúcares totales (antrona): 65% /seco
■ Polifenoles totales (Folin - Ciocalteu) - eq. Ácido gálico: 6,4% /seco
■ Contenidos en flavonoides (AlCl3) - eq. rutina: 4%/seco
■ Proteínas (evaluación de Bradford): 4,0% /seco.
Este extracto presenta una actividad anti-radicalaria, anti-DPPH “in tubo’’, para la cual se ha podido determinar la concentración inhibidora 50 (IC50) y es de 0,09 mg de extracto seco, lo cual representa 7,1 jg de polifenoles en el medio de reacción.
Ejemplo 3
Los tallos con hojas de Gynandropsis gynandra secados y triturados se ponen en suspensión bajo agitación al 5% en una mezcla propanediol/agua 60/40 p/p durante 1 h a temperatura ambiente. La materia seca residual se
separa de la fase líquida por filtración, decantación o centrifugación y la fase líquida así obtenida se puede filtrar con la ayuda de filtros de porosidad adaptada con el fin de obtener una solución límpida. El extracto obtenido presenta las características siguientes:
■ Azúcares totales (antrona): 32% /seco
■ Polifenoles totales (Folin - Ciocalteu) - eq. ácido gálico: 7,6%/seco
■ Contenidos en flavonoides (AlCl3) - eq. rutina: 4,8%/seco
■ Proteínas: 1%.
Este extracto presenta una actividad anti-radicalaria, anti-DPPH “in tubo’’, para la cual se ha podido determinar la concentración inhibidora 50 (IC50) y es de 0,16 mg de extracto seco, lo cual representa 14 |jg de polifenoles en el medio de reacción.
Ejemplo 4: Composición para aplicación por vía tópica
Los inventores presentan a continuación varias composiciones para aplicación por vía tópica. Los extractos de partes aéreas de Gynandropsis gynandra se pueden incorporar a diversos productos cosméticos tales como aguas de limpieza, emulsiones aceite en agua, emulsiones agua en aceite, aceites, leches, lociones, champús, productos espumantes y espráis, cuyas composiciones se presentan a continuación. Los porcentajes representan el peso con respecto al peso total de la composición.
AGUA DE LIMPIEZA PARA PIEL SENSIBLE
EMULSION ANTI-ENVEJECIMIENTO
EMULSIÓN ANTI-ENROJECIMIENTOS
ESPRAY SOLAR SPF 50+
EMULSIÓN ANTI-ACNEICA
CHAMPU ANTICASPA
Ejemplo 5: Actividad biológica del extracto de
Gynandropsis gynandra
A. Actividad biológica en acné
A. 1. Acción sobre la hiper-seborrea: Inhibición de la síntesis de lípidos por unos sebocitos
- Material y métodos:
Se han tratado unos sebocitos humanos (línea SZ95), estimulados o no por el ácido araquidónico a 50 j M, mediante el extracto de Gynandropsis gynandra (GG) al 0,005%; al 0,01% y al 0,02% (p/v de materia activa) o por un inhibidor de referencia durante 24 o 48 horas.
Al final del tratamiento, los lípidos neutros se han cuantificado por medición de fluorescencia después del marcado con rojo de Nilo. Esta medición, expresada en unidad de fluorescencia (RFU) refleja la síntesis “de novo” de lípidos intracelulares por los sebocitos.
Los resultados se analizaron estadísticamente por un análisis de variancia (ANOVA) con un factor seguido de un ensayo de Dunnett.
- Resultados y conclusión:
El extracto de GG ha inhibido fuerte y significativamente la producción de lípidos por sebocitos en condición basal (síntesis constitutiva) y estimulados por el ácido araquidónico (tabla 1).
Estos resultados muestran que el extracto de GG presenta un interés para regular la producción de sebo que aumenta en el acné.
Tabla 1: síntesis de lípidos por sebocitos
m Cü ,
¡8 Ü GG 0,01% 45644,06 ±623,10 222 p<0,002 1 108301,22 ±4605,77 59 p<0,001 “o - £S
*
O¿ ' O
—
(ü
GG 0,02% 30823,73 ±1310,56 47 p<0
1 ,00 43726,41 ±1809,07 83 p<0,001 n o v i Inhibidor
w v o _
A.2. Acción sobre los factores agravantes del acné
1. Modelo de queratinocitos
- Material y métodos:
Se han preincubado unos queratinocitos humanos (línea NCTC-2544) o no (control) por el extracto de Gynandroposis gynandra (GG) al 0,01% y al 0,02% (p/v de materia activa) o las moléculas de referencia (dexametasona a 10-7M; indometacina a 10-6M) durante 24 horas. Se trataron después las células con PMA a 0,1 |jg/ml (Forbol Miristato acetato) durante 24 horas, todavía en presencia de GG o de las referencias.
Al final del tratamiento, las cantidades de IL8 (interleucina 8) y de PGE2 (prostaglandina E2) segregadas se midieron por ELISA en los sobrenadantes de cultivo. Los resultados se analizaron estadísticamente mediante un ensayo t de Student.
- Resultados y conclusión:
El extracto de GG ha inhibido fuerte y significativamente la producción de los mediadores que agravan el acné IL8 y PGE2 estimulada por PMA en queratinocitos (tabla 2).
El extracto de GG modula los factores agravantes precoces del acné.
Tabla 2: Producción de IL8 y de PGE2 por unos queratinocitos
IL8 (ng/ml)__________________Inhibición_____ Células controles 0,1 ± 0,0_______________________________ PMA 0,1 jg/ml______ 50,1 ± 1,8_______________________________ Dexametasona 10-7M 7,4 ± 0,8___________ 85%________ p<0,001 GG 0,01%_________ 28,3 ± 0,5____________ 44%________ p<0,001 GG 0,02% 17,6 ± 0,5____________ 65%________ p<0,001
PGE2 (ng/ml)_________________Inhibición_____ Células controles 0,039 ± 0,0______________________________ PMA 0,1 jg/ml 138,4 ± 10,6_____________________________ Indometacina 10-6M 0,039 ± 0,0___________ 100%________ p<0,001
GG 0,01% 24,1 ± 3,0 p<0,001 GG 0,02% 9,8 ± 0,0 93% p<0,001 2. Modulación del efecto de P. acnes sobre unos queratinocitos
- Material y métodos:
Se han preincubado unos queratinocitos humanos (línea HaCaT) durante 48 h en presencia del extracto de Gynandropsis gynandra (g G) al 0,0005%; al 0,002%; al 0,008% y al 0,031% (p/v de materia activa) o del inhibidor de referencia: nicotinamida.
Los queratinocitos se estimularon entonces por incubación durante 18 horas con una suspensión bacteriana de P. acnes (cepa ATCC6919).
Al final de la incubación, la cantidad de IL8 producida por los queratinocitos se midió en los sobrenadantes de cultivo mediante una técnica ELISA.
Los resultados se analizaron estadísticamente mediante un ensayo t de Student: ns p>0,05 (no significativo); *p<0,05; **p<0,01; ***p<0,001.
- Resultados y conclusión:
La figura 1 representa la producción de IL8, en pg/ml, por unos queratinocitos estimulados por P.acnes, en función de la concentración de activo en %.
El extracto de GG ha inhibido significativamente la producción de IL8 inducida por P. acnes sobre unos queratinocitos (figura 1).
El extracto de GG modula el impacto de P. acnes en la fisiopatología del acné.
3. Estimulación de la expresión de péptidos anti-microbianos
- Material y métodos:
Se han tratado unos queratinocitos humanos normales, cultivados en un medio enriquecido en Ca++, durante 24 horas por el extracto de Gynandropsis gynandra (GG) al 0,005% (p/v de materia activa).
Al final del tratamiento, la expresión génica de los péptidos anti-microbianos (beta-defensinas 2 y 3 -hBD2, hBD3-y catelicidina LL37) se ha analizado por RT-PCR cuantitativa en tiempo real.
Los resultados se analizaron estadísticamente mediante ANOVA con un factor seguido de un ensayo de Dunnett: ns p>0,05 (no significativo); ** p<0,01; ***p<0,001.
- Resultados y conclusión:
El extracto de GG ha estimulado la expresión de los péptidos anti-microbianos por los queratinocitos (tabla 3). Así, el extracto de GG permite limitar la colonización bacteriana de la piel y por lo tanto limitar la patogenicidad relacionada con P. acnes.
Tabla 3: Expresión génica de los péptidos anti-microbianos hBD2, hBD3, LL37 en queratinocitos (Cantidad Relativa)
HBD2 HBD3 LL37 Células controles 1,00 1,00 1,00
GG 0,005% 2,70 (+170% **) 1,85 (+85% ***) 1,51 (+51% ns) 4. Modulación de la migración de neutrófilos
El neutrófilo tiene un papel importante en la fisiopatología del acné. Está presente en una alta cantidad en la piel acneica debido en particular a numerosas sustancias quimiotácticas producidas por P. acnes.
- Material y métodos:
Se han pretratado unos neutrófilos humanos durante 30 minutos por el extracto de Gynandropsis gynandra al
0,001% y al 0,002% (p/v de materia activa) o por un inhibidor de referencia.
Las células se depositaron entonces en el sistema de migración “TransweN®”: los neutrófilos pretratados se depositaron en unos insertos posicionados en una placa receptora que contiene el quimioatrayente: fMLP (N-formil-Met-Leu-Phe) a 1 pM. Después de 2 horas de incubación, el número de neutrófilos que ha migrado se ha evaluado por medición de la actividad enzimática de la LDH (Lactato Deshidrogenasa).
Los resultados se analizaron estadísticamente mediante un ensayo t de Student.
- Resultados y conclusión:
La migración de los neutrófilos fue inhibida significativamente por el extracto de GG (tabla 4).
El extracto de GG impide por lo tanto el reclutamiento de neutrófilos en la piel descrito en el acné.
Tabla 4: Migración de neutrófilos
Migración (%) Inhibición con respecto a las células estimuladas por fMLP Células controles 1,89 ± 0,2
fMLP 25,1 ± 3,02
Inhibidor 6,4 ± 0,26 -74% (p<0,01)
GG 0,001% 8,65 ± 0,24 -66% (p<0,01)
GG 0,002% 14,05 ± 1,26 -44% (p<0,05)
5. Inhibición de la producción de leucotrieno B4 por unos neutrófilos
El leucotrieno B4 es producido y liberado masivamente por el neutrófilo, tiene un papel en las lesiones de acné e induce la secreción de sebo.
- Material y métodos:
Se han preincubado unos neutrófilos humanos durante 15 minutos en presencia del extracto de Gynandropsis gynandra (GG) al 0,002% y al 0,008% (p/v de materia activa). Se estimularon después las células por adición de zymosan opsonizado a 1 mg/ml.
Después de 10 minutos de incubación, el leucotrieno B4 (LTB4) liberado por las células se ha ensayado en los sobrenadantes de células mediante una técnica ELISA.
Los resultados se analizaron estadísticamente mediante un ensayo t de Student.
- Resultados y conclusión:
El extracto de GG ha inhibido significativamente la producción de LTB4 inducida por el zymosan opsonizado sobre neutrófilos (tabla 5).
Así, el extracto de GG modula el impacto del neutrófilo y de LTB4 en el acné.
Tabla 5: Producción de leucotrieno B4 por unos neutrófilos ___________________________________________LTB4 (pg/ml)___________________ Inhibición__________ Células controles____________________________ 81,45 ± 7,16______________________________________ Células estimuladas__________________________ 439,32 ± 3,01_____________________________________ GG 0,002%_________________________________199,17 ± 4,83____________ -54%_________ p<0,001 GG 0,008%_________________________________220,91 ± 1,75____________ -49%_________ p<0,001 6. Inhibición de la liberación de histamina por unos mastocitos
La histamina puede alterar la producción del sebo. En efecto, los sebocitos (células constitutivas de la glándula sebácea, responsables de la producción del sebo) presentan en su superficie unos receptores de histamina. - Material y métodos:
Se han preincubado unos mastocitos durante 30 minutos en presencia del extracto de Gynandropsis gynandra (GG) al 0,08% (p/v de materia activa) o de calcio a 10 mM (inhibidor de referencia de la liberación de histamina).
Los mastocitos fueron estimulados después por la sustancia P a 10 pM durante 15 minutos. Al final de la incubación, la histamina liberada se ha cuantificado por ELISA.
Los resultados se analizaron estadísticamente mediante un ensayo t de Student.
- Resultados y conclusión:
El extracto de GG ha inhibido fuerte y significativamente la liberación de histamina por unos mastocitos estimulados por la sustancia P (tabla 6).
El extracto de GG modula el efecto de la histamina en el acné.
Tabla 6: Liberación de histamina por unos mastocitos
Histamina (ng/ml)____________________Inhibición_____ Control_____ 20,1 ± 1,9____________________________________ Sustancia P 142,5 ± 9,6__________________________________ Calcio 10 mM 21,8 ± 1,0________________ -85%________ p<0,01 GG 0,08% 12,3 ± 1,3________________ -91%_________p<0,01 A.3. Estrés oxidante
En el acné, existe un estrés oxidante caracterizado por una fuerte producción de radicales libres oxigenados (RLO). La gravedad del acné está correlacionada con esta cantidad de RLO.
Por otro lado, el escualeno (constituyente lipídico del sebo) está oxidado en el acné.
1. Efecto antioxidante
- Material y métodos:
Se han tratado unos queratinocitos humanos normales durante 24 horas por el extracto de Gynandropsis gynandra (GG) al 0,032% (p/v de materia activa) o vitamina C a 10 pg/ml (referencia antioxidante) antes de la incorporación de la sonda H2DCF-DA (incubación de 45 minutos).
Los queratinocitos fueron estimulados después por peróxido de hidrógeno (H2O2) a 100 pM durante 20 minutos. La producción de ROS (Reactive Oxigen Species) se ha evaluado por medición de fluorescencia.
Los resultados se analizaron estadísticamente mediante un ensayo t de Student.
- Resultados y conclusión:
El extracto de GG ha inhibido la producción de ROS por unos queratinocitos en respuesta a un estrés oxidante inducido por H2O2 (tabla 7), presenta por lo tanto un efecto antioxidante.
Tabla 7: Producción de ROS en unos queratinocitos tratados por H
2 O2
ROS (Unidades de fluorescencia) Inhibición Células estimuladas (H2O2) 1474,5 ± 93,32
Referencia (Vit. C) 992,83 ± 93,96 33% p<0,05 GG 0,032% 981,33 ± 132,52 33% p<0,05 2. Protección contra la peroxidación lipídica
- Material y métodos:
Se han preincubado unas células de línea Jurkat durante 45 minutos en presencia del extracto de Gynandropsis gynandra (GG) al 0,02% (p/v de materia activa) o BHT a 100 pM (referencia) y en presencia de la sonda fluorescente C11 -fluor, específica de la peroxidación de los lípidos.
Las células se irradiaron después por unos UVA+B y después se incubaron durante 30 minutos en presencia de GG o de BHT.
Al final de la incubación, la cantidad de peróxidos lipídicos se ha evaluado por análisis en citometría de flujo de la
intensidad de fluorescencia (inversamente proporcional a la oxidación).
Los resultados se analizaron estadísticamente mediante un ensayo t de Student.
- Resultados y conclusión:
El extracto de GG ha protegido significativamente las células contra la peroxidación lipídica inducida por la irradiación con UV (tabla 8).
Tabla 8: Peroxidación de los lípidos inducida por UV
Peróxidos lipidíeos (% del control irradiado) Protección (%) Células irradiadas (UV) 100
BHT 100 j M 64 49% p < 0,01 GG 0,02% 83 23% p < 0,05 A.4. Acción cicatrizante: estimulación de la migración queratinocitaria
Las lesiones de acné pueden conducir a la formación de cicatrices poco agraciadas.
Asimismo, el tratamiento del acné puede acompañarse de una acción pro-cicatrizante.
- Material y métodos:
Se ha realizado una herida artificial sobre una alfombra de queratinocitos humanos normales en monocapa. Las células se han marcado con calceína y después se han incubado durante 72 horas en presencia del extracto de Gynandropsis gynandra (GG) al 0,001% y al 0,005% (p/v de materia activa) o por la referencia (EGF a 10 ng/ml).
A 0, 24, 48 y 72 horas, la migración de los queratinocitos se ha seguido por microfotografía y se ha cuantificado por medición de superficie de la herida.
La figura 2 representa unas fotografías de células controles o de células incubadas en presencia del extracto de gynandropsis gynandra (GG) al 0,001% y al 0,005% (p/v de materia activa) o por la referencia (EGF a 10 ng/ml) a 0 (T0), 24 (T24), 48 (t48) y 72 horas (T72); siendo T0 el instante en el que se ha realizado la herida.
Los resultados se analizaron estadísticamente mediante un ensayo t de Student.
- Resultados y conclusión:
El extracto de GG ha estimulado significativamente la migración de los queratinocitos (tabla 9, figura 2) con un recubrimiento total de la herida a partir de 48 horas.
El extracto de GG favorece por lo tanto el proceso de reepitelización durante la cicatrización cutánea.
Tabla 9: Evaluación de la migración de los queratinocitos
Zona de migración (% de recubrimiento de la herida)
24h 48h 72h Células control 62 68 71 Referencia (EGF) 95 (p<0,001) 99 (p<0,001) 100 (p<0,001) GG 0,001% 68 (ns) 96 (p<0,001) 99 (p<0,001) GG 0,005% 72 (ns) 99 (p<0,001) 99 (p<0,001) B. Otras actividades biológicas
B.1. Inhibición de la lioogénesis en adipocitos
- Material y métodos:
Se han incubado unos adipocitos humanos normales durante 1 hora en presencia del extracto de Gynandropsis gynandra (GG) al 0,02% (p/v de materia activa) o de la referencia (cerulenina a 20 j M). Después de la incubación, el marcador radioactivo [14C]-acetato se ha añadido y las muestras se han incubado durante la noche.
Al final de la incubación, se extraen los lípidos y se mide la radioactividad incorporada (que corresponde a la lipogénesis) por centelleo líquido.
Los resultados se analizaron estadísticamente mediante un ensayo t de Student.
- Resultados y conclusión:
El extracto de GG ha inhibido significativamente la neosíntesis de los lípidos por unos adipocitos (tabla 10). Así, este extracto presenta por lo tanto un efecto adelgazante.
Tabla 10: Evaluación de la lipogénesis en unos adipocitos
Incorporación de acetato (cpm) Inhibición Células controles 32895± 1358
Referencia (Cerulenina) 14934± 671 55% p<0,001 GG 0,02% 26573 ± 227 19% p<0,05 B.2. Aumento de la producción de melanina por unos melanocitos
- Material y métodos:
Se han cultivado unos melanocitos epidérmicos humanos normales durante 240 horas en presencia del extracto de Gynandropsis gynandra (GG) al 0,002% y al 0,01% (p/v de materia activa) y de NDP-MSH a 10-7M (estimulación de la síntesis de melanina).
Después de la incubación, se ha extraído la melanina de las células y se ha cuantificado por espectrofotometría. Los resultados se analizaron estadísticamente mediante un ensayo t de Student.
- Resultados y conclusión:
El extracto de GG ha estimulado significativamente y potencializado el efecto del NDP-MSH sobre la producción de melanina (tabla 11).
El extracto presenta por lo tanto un efecto pro-pigmentante.
Tabla 11: Producción de melanina por unos melanocitos
Melanina (|jg/ml) Estimulación Células controles 13,0 ± 1,1
GG 0,01% 41,2 ± 0,5 217% p<0,001
B.3. Monitorización de actividad sobre células endoteliales
- Material y métodos:
Se han tratado unas células endoteliales microvasculares humanas por el extracto de Gynandropsis gynandra (GG) al 0,01% y al 0,02% (p/v de materia activa) durante 24 horas.
Después de la incubación, se ha analizado la expresión génica de los diferentes marcadores por RT-PCR cuantitativa en tiempo real con la ayuda de un PCR array.
- Resultados y conclusión:
Los resultados de la monitorización sobre células endoteliales han permitido mostrar que el extracto de Gynandropsis gynandra (tabla 12):
- inhibe la expresión génica de las moléculas pro-angiogénicas: PGF (Placental Growth Factor), PDGF (Platelet Derived Growth Factor B subunit) y VEGFR3 (Vascular endothelial growth factor receptor 3). - estimula la expresión de moléculas anti-angiogénicas: trombospondina-1 y endostatina.
estimula la expresión de moléculas implicadas en la vasoconstricción: calmodulina y endotelina-1.
^ Estos efectos favorecen una inhibición de la angiogénesis y la dilatación vascular, y muestran por lo tanto una actividad anti-enrojecimiento de GG.
estimula la expresión de moléculas implicadas en el refuerzo y la elasticidad de los vasos: aSMA (aSmooth Muscle Actin) y troponina 1.
estimula la expresión de moléculas de defensa: Hemooxigenasa 1 (papel protector para evitar que el hemo libre participe en reacciones pro-oxidantes) y tioredoxina (reparación de los daños oxidativos en las proteínas).
^ Estos efectos favorecen una actividad de refuerzo y de protección de las paredes vasculares por GG.
Tabla 12: Selección de actividad en PCR array sobre células endoteliales
Expresión génica (Cantidad relativa en % con respecto a las células controles) Células controles_____________GG 0,01%______________ GG 0,02% Factores de crecimiento pro-angiogénicos_____________________ PGF 100______________________ 64__________________ 53 PDGFB 100______________________ 84__________________ 62 VEGFR3 100______________________ 57__________________ 65
_______Moléculas anti-angiogénicas__________________________ Trombospondina-1 100_____________________ 148__________________ 183 Endostatina 100_____________________ 112__________________ 220
___________ Vasoconstricción_______________________________ Calmodulina 100_____________________ 120__________________ 165 Endotelino 1 100_____________________ 127__________________ 169
____ Refuerzo de los vasos/Elasticidad________________________ aSMA 100_____________________ 127__________________ 183 Troponina 1 100_____________________ 177__________________ 184
Claims (14)
1. Composición que comprende a título de principio activo un extracto de partes aéreas de Gynandropsis gynandra, caracterizada por que el extracto comprende por lo menos un 3% en peso de polifenoles, expresado en equivalente de ácido gálico con respecto al peso del extracto seco, siendo dichos polifenoles ventajosamente unos flavonoides, típicamente con un contenido de por lo menos un 1% en peso de flavonoides, expresado en equivalente de rutina con respecto al peso del extracto seco, y llegado el caso, un excipiente apropiado, siendo dicho extracto susceptible de ser obtenido por extracción sólido-líquido de las partes aéreas de Gynandropsis gynandra en unas mezclas binarias de agua y de glicerol o de glicol tal como el propanodiol, conteniendo dicha mezcla binaria agua en unas proporciones comprendidas entre el 10 y el 50% con respecto al otro disolvente.
2. Composición según la reivindicación 1, caracterizada por que la composición está destinada a ser aplicada por vía tópica externa sobre la piel, los faneros y/o las mucosas, en particular las pieles, los faneros y/o las mucosas sensibles o agredidas por el entorno.
3. Composición según las reivindicaciones 1 o 2, caracterizada por que el extracto es un extracto de hojas de Gynandropsis gynandra.
4. Composición según cualquiera de las reivindicaciones anteriores, caracterizada por que las partes aéreas de Gynandropsis gynandra son frescas o secas, ventajosamente secas.
5. Composición según cualquiera de las reivindicaciones anteriores, que comprende además por lo menos otro activo, en particular seleccionado de entre el grupo constituido por los emolientes, los activos hidratantes, los queratorreguladores, los queratolíticos, los agentes cicatrizantes y/o reestructurantes de la barrera cutánea, los agentes seborreguladores, los agentes anti-irritantes y/o antiinflamatorios y/o calmantes, los agentes antioxidantes, los agentes antienvejecimiento, los agentes despigmentantes o hipopigmentantes, los agentes pigmentantes, los agentes lipolíticos o inhibidores de la lipogénesis o también los agentes anti-celulitis o adelgazantes, los filtros y pantallas solares minerales u orgánicas, los compuestos antifúngicos, los conservantes, los agentes anti-bacterianos, los pre y probióticos, los antibióticos, los inmunomoduladores.
6. Composición según la reivindicación 5, caracterizada por que el otro activo se selecciona de entre:
• los agentes cicatrizantes y/o reestructurantes de la barrera cutánea, preferentemente el pantenol,
• los agentes seborreguladores, seleccionados preferentemente de entre los inhibidores de 5-alfareductasa, los derivados de zinc, la espironolactona, y el ácido linoleico,
• los agentes antiinflamatorios y/o anti-irritantes y/o calmantes, preferentemente el arabinogalactano, • los filtros y pantallas solares minerales u orgánicos, preferentemente los filtros o pantallas solares UVB y/o UVA,
• los conservantes, seleccionados preferentemente de entre la capriloilglicina, el caprilato de glicerilo, el hexanodiol, el levulinato de sodio, los derivados de zinc y de cobre.
7. Composición según cualquiera de las reivindicaciones 1 a 4, que comprende además por lo menos otro activo seleccionado de entre el grupo constituido por:
• los aceites vegetales, preferentemente el aceite de soja, el aceite de colza, el aceite de aguacate, el aceite de altramuz y ventajosamente el aceite de altramuz blanco dulce, o una mezcla de estos aceites, • los oleodestilados o los concentrados de aceite vegetal o animal, preferentemente de girasol, de aguacate, de colza, de maíz y de palma y ventajosamente concentrados en insaponificables,
• los insaponificables de vegetales o de aceite vegetal, preferentemente los insaponificables de aguacates, los insaponificables de soja o sus mezclas, ventajosamente unos furanos de aguacate, y en particular una mezcla de insaponificables de aguacate furánicos y de insaponificables de soja en una relación respectiva de aproximadamente 1/3-2/3, los insaponificables esterólicos, los fitosteroles, los ésteres de esteroles y los derivados vitamínicos,
• los péptidos o complejos de aminoácidos vegetales, preferentemente los péptidos de aguacate, los péptidos de altramuz, los péptidos de quinoa, los péptidos de Maca, los péptidos de soja fermentados o no, los péptidos de arroz, los péptidos de Schizandra, un extracto de semillas de Acacia macrostachya y un extracto de semillas de Vigna unguiculata,
• los azúcares de vegetales, preferentemente los azúcares de aguacate,
• el avocadato de butilo,
• los extractos ricos en polifenoles, preferentemente los extractos de aguacate y los extractos de hojas de Maca,
• el lupeol,
• un extracto total de altramuz,
• las oxazolinas, preferentemente la 2-undecil-4-hidroximetil-4-metil-1,3-oxazolina, la 2-undecil-4,4-dimetil-1.3- oxazolina, la (E)-4,4-dimetil-2-heptadec-8-enil-1,3-oxazolina, la 4-hidroximetil-4-metil-2-heptadeciM,3-oxazolina, la (E)-4-hidroximetil-4-metil-2-heptadec-8-enil-1,3-oxazolina, la 2-undecil-4-etil-4-hidroximetil-1.3- oxazolina y la 2-undecil-4,4-dimetil-1,3-oxazolina, y
• sus mezclas.
8. Composición según cualquiera de las reivindicaciones anteriores, caracterizada por que se trata de una composición cosmética, dermatológica o farmacéutica.
9. Procedimiento de cuidado cosmético de la piel y/o de los faneros y/o de las mucosas, con vistas a mejorar su estado y/o su aspecto, que consiste en aplicar sobre la piel y/o faneros y/o mucosas de los pacientes que lo necesiten una composición según cualquiera de las reivindicaciones anteriores o un extracto de partes aéreas de Gynandropsis gynandra tal como se ha definido en cualquiera de las reivindicaciones 1 a 4.
10. Procedimiento de cuidado cosmético según la reivindicación 9 para las pieles, los faneros y/o las mucosas sensibles o agredidas por el entorno, o para las pieles, los faneros y/o las mucosas que presentan enrojecimientos, típicamente con tiranteces o picores diarios, o para regular la producción de sebo, o también los estados de caspa.
11. Procedimiento de cuidado cosmético según las reivindicaciones 9 o 10, caracterizado por que la composición o el extracto es un producto anti-envejecimiento cronológico o foto-inducido, o también un producto hidratante, adelgazante y/o anticelulitis.
12. Composición según cualquiera de las reivindicaciones 1 a 8, para su utilización en la prevención y/o el tratamiento de los trastornos relacionados con la hiperseborrea, preferentemente la dermatitis seborreica, o también del acné o de las pieles acneicas, o para su utilización como producto cicatrizante, anti-alérgico y/o propigmentante.
13. Composición según cualquiera de las reivindicaciones 1 a 8, para su utilización en la prevención y/o el tratamiento de los trastornos vasculares.
14. Composición según cualquiera de las reivindicaciones 1 a 8, para su utilización en la prevención y/o el tratamiento de las siguientes condiciones: la cuperosis, los eritemas cutáneos, la rosácea, el prurito, la piel y/o las mucosas reactivas, con enrojecimientos, en particular debidas a una dilatación de los capilares subcutáneos.
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| FR1061051A FR2969494B1 (fr) | 2010-12-22 | 2010-12-22 | Extrait de parties aeriennes de gynandropsis gynandra ou cleome gynandra et compositions cosmetiques, dermatologiques le comprenant |
| PCT/EP2011/073838 WO2012085230A1 (fr) | 2010-12-22 | 2011-12-22 | Extrait de parties aeriennes de gynandropsis gynandra ou cleome gynandra et compositions cosmetiques, dermatologiques ou pharmaceutiques le comprenant |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| ES2700784T3 true ES2700784T3 (es) | 2019-02-19 |
Family
ID=44260119
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| ES11804695T Active ES2700784T3 (es) | 2010-12-22 | 2011-12-22 | Extracto de partes aéreas de Gynandropsis gynandra o Cleome gynandra y composiciones cosméticas, dermatológicas o farmacéuticas que lo comprenden |
Country Status (10)
| Country | Link |
|---|---|
| US (1) | US9370541B2 (es) |
| EP (1) | EP2654762B1 (es) |
| KR (2) | KR102039846B1 (es) |
| CN (1) | CN103379910B (es) |
| BR (1) | BR112013014091A2 (es) |
| CA (1) | CA2819796A1 (es) |
| ES (1) | ES2700784T3 (es) |
| FR (1) | FR2969494B1 (es) |
| PL (1) | PL2654762T3 (es) |
| WO (1) | WO2012085230A1 (es) |
Families Citing this family (9)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP6523291B2 (ja) | 2013-12-24 | 2019-05-29 | ザ プロクター アンド ギャンブル カンパニーThe Procter & Gamble Company | スキンケア有効成分の高い浸透性を与える美容組成物及び方法 |
| CN104382967B (zh) * | 2014-11-29 | 2018-09-11 | 河南后羿实业集团有限公司 | 一种白花菜子油栓剂及其制备方法 |
| CN109996532A (zh) | 2016-10-04 | 2019-07-09 | 玫琳凯有限公司 | 用于处理萎缩纹的方法和组合物 |
| WO2019183494A1 (en) | 2018-03-23 | 2019-09-26 | Mary Kay Inc. | Topical compositions and methods |
| DE202019005710U1 (de) | 2018-12-14 | 2021-07-20 | Mary Kay Inc. | Kosmetikzusammensetzungen |
| CN110623000A (zh) * | 2019-09-09 | 2019-12-31 | 湖北工程学院 | 一种白花菜提取物及其制备方法和用途 |
| CN110711166A (zh) * | 2019-11-03 | 2020-01-21 | 广州悦荟化妆品有限公司 | 一种控油保湿功效的爽肤水 |
| CN111329799B (zh) * | 2020-02-18 | 2021-06-04 | 北京果素堂生物科技有限公司 | 无刺激性的白子菜活性物的制备方法及其应用 |
| GB202017114D0 (en) * | 2020-10-28 | 2020-12-09 | Givaudan Sa | Improvements in or relating to extracts |
Family Cites Families (9)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US4979938A (en) * | 1989-05-11 | 1990-12-25 | Iomed, Inc. | Method of iontophoretically treating acne, furuncles and like skin disorders |
| GB9802542D0 (en) * | 1998-02-05 | 1998-04-01 | Smithkline Beecham Plc | New use |
| JP4880816B2 (ja) * | 2000-12-15 | 2012-02-22 | 株式会社ヤクルト本社 | 皮膚老化防止剤 |
| FR2841470B1 (fr) * | 2002-06-27 | 2006-01-13 | Pharmascience Lab | Utilisation d'isoflavones pour la preparation de compositions topiques utiles pour favoriser l'amincissement et methode de traitement cosmetique associee |
| ES2422423T3 (es) | 2004-03-24 | 2013-09-11 | Cognis France Sas | Usos cosméticos y farmacéuticos de un extracto de las semillas de Buchholzia coriacea |
| NZ570920A (en) | 2006-03-03 | 2011-09-30 | Univ Aberdeen | Pest repellent comprising geranylacetone and sulcatone |
| GB0716605D0 (en) * | 2007-08-24 | 2007-10-03 | Univ Aston | Skin antiseptics |
| FR2937972B1 (fr) * | 2008-11-04 | 2013-03-29 | Galderma Res & Dev | Derives d'oxoazetidine, leur procede de preparation et leur utilisation en medecine humaine ainsi qu'en cosmetique |
| FR2945943B1 (fr) * | 2009-06-01 | 2015-04-03 | Lvmh Rech | Utilisation d'un extrait vegetal riche en polyphenols comme agent antioxydant en association avec un agent hydratant ou humectant |
-
2010
- 2010-12-22 FR FR1061051A patent/FR2969494B1/fr not_active Expired - Fee Related
-
2011
- 2011-12-22 EP EP11804695.2A patent/EP2654762B1/fr active Active
- 2011-12-22 KR KR1020187018766A patent/KR102039846B1/ko active IP Right Grant
- 2011-12-22 WO PCT/EP2011/073838 patent/WO2012085230A1/fr active Application Filing
- 2011-12-22 ES ES11804695T patent/ES2700784T3/es active Active
- 2011-12-22 BR BR112013014091A patent/BR112013014091A2/pt not_active IP Right Cessation
- 2011-12-22 KR KR1020137018864A patent/KR20140005204A/ko active Application Filing
- 2011-12-22 PL PL11804695T patent/PL2654762T3/pl unknown
- 2011-12-22 US US13/824,187 patent/US9370541B2/en active Active
- 2011-12-22 CN CN201180062295.XA patent/CN103379910B/zh active Active
- 2011-12-22 CA CA2819796A patent/CA2819796A1/fr not_active Abandoned
Also Published As
| Publication number | Publication date |
|---|---|
| EP2654762A1 (fr) | 2013-10-30 |
| PL2654762T3 (pl) | 2019-05-31 |
| BR112013014091A2 (pt) | 2016-09-20 |
| KR20140005204A (ko) | 2014-01-14 |
| KR102039846B1 (ko) | 2019-11-01 |
| CN103379910A (zh) | 2013-10-30 |
| EP2654762B1 (fr) | 2018-09-26 |
| FR2969494B1 (fr) | 2013-11-08 |
| CA2819796A1 (fr) | 2012-06-28 |
| FR2969494A1 (fr) | 2012-06-29 |
| KR20180078344A (ko) | 2018-07-09 |
| CN103379910B (zh) | 2018-10-02 |
| US9370541B2 (en) | 2016-06-21 |
| WO2012085230A1 (fr) | 2012-06-28 |
| US20130171082A1 (en) | 2013-07-04 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| ES2700784T3 (es) | Extracto de partes aéreas de Gynandropsis gynandra o Cleome gynandra y composiciones cosméticas, dermatológicas o farmacéuticas que lo comprenden | |
| ES2727832T3 (es) | Extracto de partes aéreas de Maca rico en polifenoles y composición que lo comprende | |
| ES2704665T3 (es) | Extracto de pulpa y/o de piel de aguacate rico en polifenoles y composiciones cosméticas, dermatológicas y nutracéuticas que lo comprenden | |
| US10688142B2 (en) | Methods of treatment using a lipid extract of Passiflora seeds concentrated in its unsaponifiable fraction | |
| ES2665313T3 (es) | Extracto de semillas de pasiflora y composiciones cosméticas, farmacéuticas, dermatológicas o nutracéuticas que lo comprenden | |
| ES2942766T3 (es) | Extracto de flores de ceiba y composiciones cosméticas, farmacéuticas o dermatológicas que lo contengan | |
| BR112016007843B1 (pt) | Uso cosmético não-terapêutico de um extrato de hamamelis virginiana, e, método de cuidados cosméticos | |
| BR102014018002A2 (pt) | composições compreendendo extrato de malva neglecta | |
| BR102014018008A2 (pt) | método de tratamento de uma condição de pele com malva neglecta | |
| US10406096B2 (en) | Compositions comprising extracts of Bursera simaruba | |
| JP6591459B2 (ja) | 皮膚美白用化粧品組成物 | |
| BR102014025813A2 (pt) | composições compreendendo extratos de madeira de paulownia tomentosa e usos das mesmas |