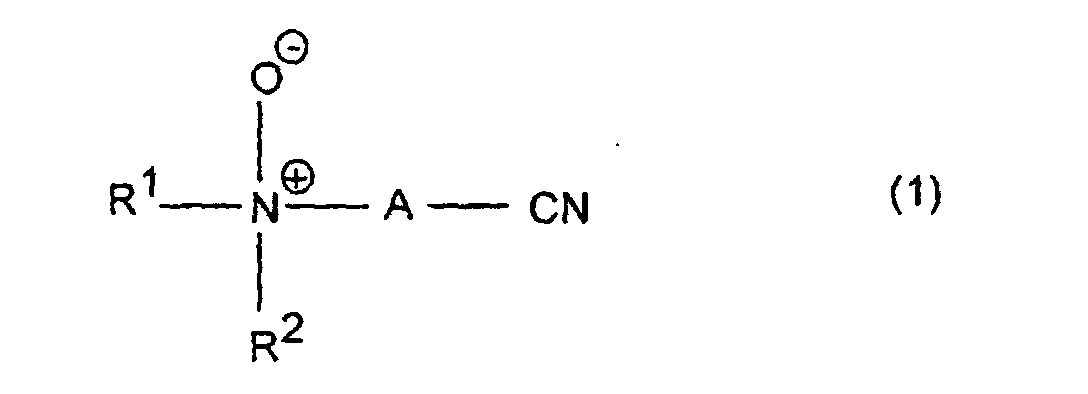EP0909810B1 - Verwendung von Aminonitril-N-oxiden als Bleichaktivatoren - Google Patents
Verwendung von Aminonitril-N-oxiden als Bleichaktivatoren Download PDFInfo
- Publication number
- EP0909810B1 EP0909810B1 EP98117813A EP98117813A EP0909810B1 EP 0909810 B1 EP0909810 B1 EP 0909810B1 EP 98117813 A EP98117813 A EP 98117813A EP 98117813 A EP98117813 A EP 98117813A EP 0909810 B1 EP0909810 B1 EP 0909810B1
- Authority
- EP
- European Patent Office
- Prior art keywords
- aminonitrile
- formula
- oxide
- alkyl
- detergent
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Expired - Lifetime
Links
- 239000007844 bleaching agent Substances 0.000 title claims description 28
- 239000012190 activator Substances 0.000 title claims description 25
- -1 aminonitrile N-oxides Chemical class 0.000 claims description 48
- 239000003599 detergent Substances 0.000 claims description 24
- 238000004061 bleaching Methods 0.000 claims description 15
- 150000001875 compounds Chemical class 0.000 claims description 10
- 150000003839 salts Chemical class 0.000 claims description 9
- 125000001997 phenyl group Chemical group [H]C1=C([H])C([H])=C(*)C([H])=C1[H] 0.000 claims description 8
- OAKJQQAXSVQMHS-UHFFFAOYSA-N Hydrazine Chemical compound NN OAKJQQAXSVQMHS-UHFFFAOYSA-N 0.000 claims description 6
- WKBOTKDWSSQWDR-UHFFFAOYSA-N Bromine atom Chemical group [Br] WKBOTKDWSSQWDR-UHFFFAOYSA-N 0.000 claims description 5
- ZAMOUSCENKQFHK-UHFFFAOYSA-N Chlorine atom Chemical group [Cl] ZAMOUSCENKQFHK-UHFFFAOYSA-N 0.000 claims description 5
- 239000000460 chlorine Chemical group 0.000 claims description 5
- 125000000753 cycloalkyl group Chemical group 0.000 claims description 5
- 239000004753 textile Substances 0.000 claims description 5
- GDTBXPJZTBHREO-UHFFFAOYSA-N bromine Chemical group BrBr GDTBXPJZTBHREO-UHFFFAOYSA-N 0.000 claims description 4
- 229910052794 bromium Inorganic materials 0.000 claims description 4
- 125000003178 carboxy group Chemical group [H]OC(*)=O 0.000 claims description 4
- 229910052801 chlorine Inorganic materials 0.000 claims description 4
- 125000004093 cyano group Chemical group *C#N 0.000 claims description 4
- 229910052757 nitrogen Inorganic materials 0.000 claims description 4
- 125000004433 nitrogen atom Chemical group N* 0.000 claims description 4
- CIHOLLKRGTVIJN-UHFFFAOYSA-N tert‐butyl hydroperoxide Chemical compound CC(C)(C)OO CIHOLLKRGTVIJN-UHFFFAOYSA-N 0.000 claims description 4
- 150000005840 aryl radicals Chemical class 0.000 claims description 3
- 125000004432 carbon atom Chemical group C* 0.000 claims description 3
- 229910052739 hydrogen Inorganic materials 0.000 claims description 3
- 125000000843 phenylene group Chemical group C1(=C(C=CC=C1)*)* 0.000 claims description 3
- 125000006732 (C1-C15) alkyl group Chemical group 0.000 claims description 2
- 125000006527 (C1-C5) alkyl group Chemical group 0.000 claims description 2
- 125000006833 (C1-C5) alkylene group Chemical group 0.000 claims description 2
- 125000006701 (C1-C7) alkyl group Chemical group 0.000 claims description 2
- FRIBMENBGGCKPD-UHFFFAOYSA-N 3-(2,3-dimethoxyphenyl)prop-2-enal Chemical compound COC1=CC=CC(C=CC=O)=C1OC FRIBMENBGGCKPD-UHFFFAOYSA-N 0.000 claims description 2
- 239000011737 fluorine Substances 0.000 claims description 2
- 229910052731 fluorine Inorganic materials 0.000 claims description 2
- 125000001153 fluoro group Chemical group F* 0.000 claims description 2
- 239000001257 hydrogen Substances 0.000 claims description 2
- 125000004435 hydrogen atom Chemical group [H]* 0.000 claims description 2
- 125000002496 methyl group Chemical group [H]C([H])([H])* 0.000 claims description 2
- 125000004430 oxygen atom Chemical group O* 0.000 claims description 2
- 125000005342 perphosphate group Chemical group 0.000 claims description 2
- AQLJVWUFPCUVLO-UHFFFAOYSA-N urea hydrogen peroxide Chemical compound OO.NC(N)=O AQLJVWUFPCUVLO-UHFFFAOYSA-N 0.000 claims description 2
- 125000004178 (C1-C4) alkyl group Chemical group 0.000 claims 1
- MWNQXXOSWHCCOZ-UHFFFAOYSA-L sodium;oxido carbonate Chemical compound [Na+].[O-]OC([O-])=O MWNQXXOSWHCCOZ-UHFFFAOYSA-L 0.000 claims 1
- 239000000203 mixture Substances 0.000 description 16
- 239000000126 substance Substances 0.000 description 10
- 229910052708 sodium Inorganic materials 0.000 description 9
- 239000011734 sodium Substances 0.000 description 9
- 239000000344 soap Substances 0.000 description 8
- DGAQECJNVWCQMB-PUAWFVPOSA-M Ilexoside XXIX Chemical compound C[C@@H]1CC[C@@]2(CC[C@@]3(C(=CC[C@H]4[C@]3(CC[C@@H]5[C@@]4(CC[C@@H](C5(C)C)OS(=O)(=O)[O-])C)C)[C@@H]2[C@]1(C)O)C)C(=O)O[C@H]6[C@@H]([C@H]([C@@H]([C@H](O6)CO)O)O)O.[Na+] DGAQECJNVWCQMB-PUAWFVPOSA-M 0.000 description 7
- 239000007788 liquid Substances 0.000 description 7
- YMWUJEATGCHHMB-UHFFFAOYSA-N Dichloromethane Chemical compound ClCCl YMWUJEATGCHHMB-UHFFFAOYSA-N 0.000 description 6
- 239000007795 chemical reaction product Substances 0.000 description 6
- KRKNYBCHXYNGOX-UHFFFAOYSA-N citric acid Chemical compound OC(=O)CC(O)(C(O)=O)CC(O)=O KRKNYBCHXYNGOX-UHFFFAOYSA-N 0.000 description 6
- 235000014113 dietary fatty acids Nutrition 0.000 description 6
- 239000000194 fatty acid Substances 0.000 description 6
- 229930195729 fatty acid Natural products 0.000 description 6
- IAYPIBMASNFSPL-UHFFFAOYSA-N Ethylene oxide Chemical compound C1CO1 IAYPIBMASNFSPL-UHFFFAOYSA-N 0.000 description 5
- 239000012459 cleaning agent Substances 0.000 description 5
- 150000004665 fatty acids Chemical class 0.000 description 5
- 238000005406 washing Methods 0.000 description 5
- 150000001298 alcohols Chemical class 0.000 description 4
- 125000000217 alkyl group Chemical group 0.000 description 4
- 125000000129 anionic group Chemical group 0.000 description 4
- 238000006243 chemical reaction Methods 0.000 description 4
- 239000008187 granular material Substances 0.000 description 4
- 150000002825 nitriles Chemical class 0.000 description 4
- VLQQSXBQOCOZGJ-UHFFFAOYSA-N 4-(dimethylamino)benzonitrile oxide Chemical compound CN(C)C1=CC=C(C#[N+][O-])C=C1 VLQQSXBQOCOZGJ-UHFFFAOYSA-N 0.000 description 3
- XSVSPKKXQGNHMD-UHFFFAOYSA-N 5-bromo-3-methyl-1,2-thiazole Chemical compound CC=1C=C(Br)SN=1 XSVSPKKXQGNHMD-UHFFFAOYSA-N 0.000 description 3
- UHOVQNZJYSORNB-UHFFFAOYSA-N Benzene Chemical class C1=CC=CC=C1 UHOVQNZJYSORNB-UHFFFAOYSA-N 0.000 description 3
- OYPRJOBELJOOCE-UHFFFAOYSA-N Calcium Chemical compound [Ca] OYPRJOBELJOOCE-UHFFFAOYSA-N 0.000 description 3
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 3
- LYCAIKOWRPUZTN-UHFFFAOYSA-N Ethylene glycol Chemical compound OCCO LYCAIKOWRPUZTN-UHFFFAOYSA-N 0.000 description 3
- HEMHJVSKTPXQMS-UHFFFAOYSA-M Sodium hydroxide Chemical compound [OH-].[Na+] HEMHJVSKTPXQMS-UHFFFAOYSA-M 0.000 description 3
- BGRWYDHXPHLNKA-UHFFFAOYSA-N Tetraacetylethylenediamine Chemical compound CC(=O)N(C(C)=O)CCN(C(C)=O)C(C)=O BGRWYDHXPHLNKA-UHFFFAOYSA-N 0.000 description 3
- 239000001083 [(2R,3R,4S,5R)-1,2,4,5-tetraacetyloxy-6-oxohexan-3-yl] acetate Substances 0.000 description 3
- 239000002253 acid Substances 0.000 description 3
- 229910052783 alkali metal Inorganic materials 0.000 description 3
- 239000003945 anionic surfactant Substances 0.000 description 3
- 125000003118 aryl group Chemical group 0.000 description 3
- 239000011575 calcium Substances 0.000 description 3
- 229910052791 calcium Inorganic materials 0.000 description 3
- 230000000694 effects Effects 0.000 description 3
- 239000004615 ingredient Substances 0.000 description 3
- 238000000034 method Methods 0.000 description 3
- 239000002736 nonionic surfactant Substances 0.000 description 3
- 150000002978 peroxides Chemical class 0.000 description 3
- 239000007787 solid Substances 0.000 description 3
- 150000003871 sulfonates Chemical class 0.000 description 3
- 239000004094 surface-active agent Substances 0.000 description 3
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 3
- LULAYUGMBFYYEX-UHFFFAOYSA-N 3-chlorobenzoic acid Chemical class OC(=O)C1=CC=CC(Cl)=C1 LULAYUGMBFYYEX-UHFFFAOYSA-N 0.000 description 2
- QGZKDVFQNNGYKY-UHFFFAOYSA-O Ammonium Chemical compound [NH4+] QGZKDVFQNNGYKY-UHFFFAOYSA-O 0.000 description 2
- 244000060011 Cocos nucifera Species 0.000 description 2
- 235000013162 Cocos nucifera Nutrition 0.000 description 2
- KCXVZYZYPLLWCC-UHFFFAOYSA-N EDTA Chemical class OC(=O)CN(CC(O)=O)CCN(CC(O)=O)CC(O)=O KCXVZYZYPLLWCC-UHFFFAOYSA-N 0.000 description 2
- 102000004190 Enzymes Human genes 0.000 description 2
- 108090000790 Enzymes Proteins 0.000 description 2
- PEDCQBHIVMGVHV-UHFFFAOYSA-N Glycerine Chemical compound OCC(O)CO PEDCQBHIVMGVHV-UHFFFAOYSA-N 0.000 description 2
- MHAJPDPJQMAIIY-UHFFFAOYSA-N Hydrogen peroxide Chemical compound OO MHAJPDPJQMAIIY-UHFFFAOYSA-N 0.000 description 2
- KFZMGEQAYNKOFK-UHFFFAOYSA-N Isopropanol Chemical compound CC(C)O KFZMGEQAYNKOFK-UHFFFAOYSA-N 0.000 description 2
- 229910019142 PO4 Inorganic materials 0.000 description 2
- NBIIXXVUZAFLBC-UHFFFAOYSA-N Phosphoric acid Chemical compound OP(O)(O)=O NBIIXXVUZAFLBC-UHFFFAOYSA-N 0.000 description 2
- PMZURENOXWZQFD-UHFFFAOYSA-L Sodium Sulfate Chemical class [Na+].[Na+].[O-]S([O-])(=O)=O PMZURENOXWZQFD-UHFFFAOYSA-L 0.000 description 2
- UAOKXEHOENRFMP-ZJIFWQFVSA-N [(2r,3r,4s,5r)-2,3,4,5-tetraacetyloxy-6-oxohexyl] acetate Chemical compound CC(=O)OC[C@@H](OC(C)=O)[C@@H](OC(C)=O)[C@H](OC(C)=O)[C@@H](OC(C)=O)C=O UAOKXEHOENRFMP-ZJIFWQFVSA-N 0.000 description 2
- 150000007513 acids Chemical class 0.000 description 2
- 239000000654 additive Substances 0.000 description 2
- 239000003513 alkali Substances 0.000 description 2
- 150000003863 ammonium salts Chemical class 0.000 description 2
- 239000011230 binding agent Substances 0.000 description 2
- 239000003054 catalyst Substances 0.000 description 2
- 229940088598 enzyme Drugs 0.000 description 2
- 238000002474 experimental method Methods 0.000 description 2
- 239000004744 fabric Substances 0.000 description 2
- 230000007062 hydrolysis Effects 0.000 description 2
- 238000006460 hydrolysis reaction Methods 0.000 description 2
- 150000002500 ions Chemical class 0.000 description 2
- SUMDYPCJJOFFON-UHFFFAOYSA-N isethionic acid Chemical compound OCCS(O)(=O)=O SUMDYPCJJOFFON-UHFFFAOYSA-N 0.000 description 2
- YDSWCNNOKPMOTP-UHFFFAOYSA-N mellitic acid Chemical class OC(=O)C1=C(C(O)=O)C(C(O)=O)=C(C(O)=O)C(C(O)=O)=C1C(O)=O YDSWCNNOKPMOTP-UHFFFAOYSA-N 0.000 description 2
- BDAGIHXWWSANSR-UHFFFAOYSA-N methanoic acid Natural products OC=O BDAGIHXWWSANSR-UHFFFAOYSA-N 0.000 description 2
- 150000004965 peroxy acids Chemical class 0.000 description 2
- 235000021317 phosphate Nutrition 0.000 description 2
- CDBYLPFSWZWCQE-UHFFFAOYSA-L sodium carbonate Substances [Na+].[Na+].[O-]C([O-])=O CDBYLPFSWZWCQE-UHFFFAOYSA-L 0.000 description 2
- 229910052938 sodium sulfate Inorganic materials 0.000 description 2
- 235000011152 sodium sulphate Nutrition 0.000 description 2
- 239000007790 solid phase Substances 0.000 description 2
- 239000000243 solution Substances 0.000 description 2
- 239000004711 α-olefin Substances 0.000 description 2
- CIOXZGOUEYHNBF-UHFFFAOYSA-N (carboxymethoxy)succinic acid Chemical class OC(=O)COC(C(O)=O)CC(O)=O CIOXZGOUEYHNBF-UHFFFAOYSA-N 0.000 description 1
- CFPOJWPDQWJEMO-UHFFFAOYSA-N 2-(1,2-dicarboxyethoxy)butanedioic acid Chemical class OC(=O)CC(C(O)=O)OC(C(O)=O)CC(O)=O CFPOJWPDQWJEMO-UHFFFAOYSA-N 0.000 description 1
- YTWUZAQZEVOPGG-UHFFFAOYSA-N 3-acetyl-1-phenylimidazolidine-2,4-dione Chemical compound O=C1N(C(=O)C)C(=O)CN1C1=CC=CC=C1 YTWUZAQZEVOPGG-UHFFFAOYSA-N 0.000 description 1
- FAGGUIDTQQXDSJ-UHFFFAOYSA-N 3-benzoylazepan-2-one Chemical compound C=1C=CC=CC=1C(=O)C1CCCCNC1=O FAGGUIDTQQXDSJ-UHFFFAOYSA-N 0.000 description 1
- NHQDETIJWKXCTC-UHFFFAOYSA-N 3-chloroperbenzoic acid Chemical compound OOC(=O)C1=CC=CC(Cl)=C1 NHQDETIJWKXCTC-UHFFFAOYSA-N 0.000 description 1
- OSWFIVFLDKOXQC-UHFFFAOYSA-N 4-(3-methoxyphenyl)aniline Chemical compound COC1=CC=CC(C=2C=CC(N)=CC=2)=C1 OSWFIVFLDKOXQC-UHFFFAOYSA-N 0.000 description 1
- JYMNQRQQBJIMCV-UHFFFAOYSA-N 4-(dimethylamino)benzonitrile Chemical compound CN(C)C1=CC=C(C#N)C=C1 JYMNQRQQBJIMCV-UHFFFAOYSA-N 0.000 description 1
- 102000013142 Amylases Human genes 0.000 description 1
- 108010065511 Amylases Proteins 0.000 description 1
- 102000005701 Calcium-Binding Proteins Human genes 0.000 description 1
- 108010045403 Calcium-Binding Proteins Proteins 0.000 description 1
- 102000005575 Cellulases Human genes 0.000 description 1
- 108010084185 Cellulases Proteins 0.000 description 1
- 229920000742 Cotton Polymers 0.000 description 1
- FBPFZTCFMRRESA-FSIIMWSLSA-N D-Glucitol Natural products OC[C@H](O)[C@H](O)[C@@H](O)[C@H](O)CO FBPFZTCFMRRESA-FSIIMWSLSA-N 0.000 description 1
- FBPFZTCFMRRESA-JGWLITMVSA-N D-glucitol Chemical compound OC[C@H](O)[C@@H](O)[C@H](O)[C@H](O)CO FBPFZTCFMRRESA-JGWLITMVSA-N 0.000 description 1
- PIICEJLVQHRZGT-UHFFFAOYSA-N Ethylenediamine Chemical compound NCCN PIICEJLVQHRZGT-UHFFFAOYSA-N 0.000 description 1
- UFHFLCQGNIYNRP-UHFFFAOYSA-N Hydrogen Chemical compound [H][H] UFHFLCQGNIYNRP-UHFFFAOYSA-N 0.000 description 1
- 239000004367 Lipase Substances 0.000 description 1
- 102000004882 Lipase Human genes 0.000 description 1
- 108090001060 Lipase Proteins 0.000 description 1
- SUZRRICLUFMAQD-UHFFFAOYSA-N N-Methyltaurine Chemical compound CNCCS(O)(=O)=O SUZRRICLUFMAQD-UHFFFAOYSA-N 0.000 description 1
- 102000035195 Peptidases Human genes 0.000 description 1
- 108091005804 Peptidases Proteins 0.000 description 1
- 229930182556 Polyacetal Natural products 0.000 description 1
- 229920000388 Polyphosphate Polymers 0.000 description 1
- GOOHAUXETOMSMM-UHFFFAOYSA-N Propylene oxide Chemical compound CC1CO1 GOOHAUXETOMSMM-UHFFFAOYSA-N 0.000 description 1
- 239000004365 Protease Substances 0.000 description 1
- DWAQJAXMDSEUJJ-UHFFFAOYSA-M Sodium bisulfite Chemical compound [Na+].OS([O-])=O DWAQJAXMDSEUJJ-UHFFFAOYSA-M 0.000 description 1
- KDYFGRWQOYBRFD-UHFFFAOYSA-N Succinic acid Natural products OC(=O)CCC(O)=O KDYFGRWQOYBRFD-UHFFFAOYSA-N 0.000 description 1
- ULUAUXLGCMPNKK-UHFFFAOYSA-N Sulfobutanedioic acid Chemical class OC(=O)CC(C(O)=O)S(O)(=O)=O ULUAUXLGCMPNKK-UHFFFAOYSA-N 0.000 description 1
- QAOWNCQODCNURD-UHFFFAOYSA-N Sulfuric acid Chemical class OS(O)(=O)=O QAOWNCQODCNURD-UHFFFAOYSA-N 0.000 description 1
- 244000269722 Thea sinensis Species 0.000 description 1
- ZYPMNZKYVVSXOJ-YNEHKIRRSA-N [(2r,3s,4r)-2,3,4-triacetyloxy-5-oxopentyl] acetate Chemical compound CC(=O)OC[C@@H](OC(C)=O)[C@H](OC(C)=O)[C@@H](OC(C)=O)C=O ZYPMNZKYVVSXOJ-YNEHKIRRSA-N 0.000 description 1
- DPXJVFZANSGRMM-UHFFFAOYSA-N acetic acid;2,3,4,5,6-pentahydroxyhexanal;sodium Chemical compound [Na].CC(O)=O.OCC(O)C(O)C(O)C(O)C=O DPXJVFZANSGRMM-UHFFFAOYSA-N 0.000 description 1
- 230000002378 acidificating effect Effects 0.000 description 1
- 239000013543 active substance Substances 0.000 description 1
- 150000001335 aliphatic alkanes Chemical class 0.000 description 1
- 125000001931 aliphatic group Chemical group 0.000 description 1
- 150000001340 alkali metals Chemical class 0.000 description 1
- 239000012670 alkaline solution Substances 0.000 description 1
- 150000001336 alkenes Chemical class 0.000 description 1
- 125000002877 alkyl aryl group Chemical group 0.000 description 1
- 229920013820 alkyl cellulose Polymers 0.000 description 1
- 125000002947 alkylene group Chemical group 0.000 description 1
- 229910052782 aluminium Inorganic materials 0.000 description 1
- PNEYBMLMFCGWSK-UHFFFAOYSA-N aluminium oxide Inorganic materials [O-2].[O-2].[O-2].[Al+3].[Al+3] PNEYBMLMFCGWSK-UHFFFAOYSA-N 0.000 description 1
- 229910000147 aluminium phosphate Inorganic materials 0.000 description 1
- 150000001412 amines Chemical class 0.000 description 1
- 125000005219 aminonitrile group Chemical group 0.000 description 1
- 239000002280 amphoteric surfactant Substances 0.000 description 1
- 235000019418 amylase Nutrition 0.000 description 1
- 229940025131 amylases Drugs 0.000 description 1
- 239000007864 aqueous solution Substances 0.000 description 1
- 125000000732 arylene group Chemical group 0.000 description 1
- 230000015572 biosynthetic process Effects 0.000 description 1
- CODNYICXDISAEA-UHFFFAOYSA-N bromine monochloride Chemical compound BrCl CODNYICXDISAEA-UHFFFAOYSA-N 0.000 description 1
- ONANWDUDFJIIGP-UHFFFAOYSA-N carbamoyl carbamoperoxoate Chemical compound NC(=O)OOC(N)=O ONANWDUDFJIIGP-UHFFFAOYSA-N 0.000 description 1
- 239000001768 carboxy methyl cellulose Substances 0.000 description 1
- 150000007942 carboxylates Chemical class 0.000 description 1
- 125000002091 cationic group Chemical group 0.000 description 1
- 239000003795 chemical substances by application Substances 0.000 description 1
- 238000004587 chromatography analysis Methods 0.000 description 1
- 238000004140 cleaning Methods 0.000 description 1
- 239000003240 coconut oil Substances 0.000 description 1
- 235000019864 coconut oil Nutrition 0.000 description 1
- 125000002993 cycloalkylene group Chemical group 0.000 description 1
- 239000000645 desinfectant Substances 0.000 description 1
- VTIIJXUACCWYHX-UHFFFAOYSA-L disodium;carboxylatooxy carbonate Chemical compound [Na+].[Na+].[O-]C(=O)OOC([O-])=O VTIIJXUACCWYHX-UHFFFAOYSA-L 0.000 description 1
- 238000007580 dry-mixing Methods 0.000 description 1
- 239000000975 dye Substances 0.000 description 1
- 230000007613 environmental effect Effects 0.000 description 1
- 230000032050 esterification Effects 0.000 description 1
- 238000005886 esterification reaction Methods 0.000 description 1
- 150000002148 esters Chemical class 0.000 description 1
- 150000002170 ethers Chemical class 0.000 description 1
- 150000002191 fatty alcohols Chemical class 0.000 description 1
- 239000000835 fiber Substances 0.000 description 1
- 239000006260 foam Substances 0.000 description 1
- 239000004088 foaming agent Substances 0.000 description 1
- 235000019253 formic acid Nutrition 0.000 description 1
- 235000011187 glycerol Nutrition 0.000 description 1
- 239000008233 hard water Substances 0.000 description 1
- 239000003112 inhibitor Substances 0.000 description 1
- 239000002563 ionic surfactant Substances 0.000 description 1
- 229940045996 isethionic acid Drugs 0.000 description 1
- 235000019421 lipase Nutrition 0.000 description 1
- 229940057995 liquid paraffin Drugs 0.000 description 1
- 150000004668 long chain fatty acids Chemical class 0.000 description 1
- 229930014626 natural product Natural products 0.000 description 1
- 238000006386 neutralization reaction Methods 0.000 description 1
- MGFYIUFZLHCRTH-UHFFFAOYSA-N nitrilotriacetic acid Chemical compound OC(=O)CN(CC(O)=O)CC(O)=O MGFYIUFZLHCRTH-UHFFFAOYSA-N 0.000 description 1
- JRZJOMJEPLMPRA-UHFFFAOYSA-N olefin Natural products CCCCCCCC=C JRZJOMJEPLMPRA-UHFFFAOYSA-N 0.000 description 1
- 150000002894 organic compounds Chemical class 0.000 description 1
- 150000001451 organic peroxides Chemical class 0.000 description 1
- 150000004028 organic sulfates Chemical class 0.000 description 1
- 239000007800 oxidant agent Substances 0.000 description 1
- MPQXHAGKBWFSNV-UHFFFAOYSA-N oxidophosphanium Chemical group [PH3]=O MPQXHAGKBWFSNV-UHFFFAOYSA-N 0.000 description 1
- 239000003346 palm kernel oil Substances 0.000 description 1
- 235000019865 palm kernel oil Nutrition 0.000 description 1
- 235000011837 pasties Nutrition 0.000 description 1
- 239000002304 perfume Substances 0.000 description 1
- NFBAXHOPROOJAW-UHFFFAOYSA-N phenindione Chemical compound O=C1C2=CC=CC=C2C(=O)C1C1=CC=CC=C1 NFBAXHOPROOJAW-UHFFFAOYSA-N 0.000 description 1
- 150000003013 phosphoric acid derivatives Chemical class 0.000 description 1
- 239000002798 polar solvent Substances 0.000 description 1
- 229920000642 polymer Polymers 0.000 description 1
- 229920005862 polyol Polymers 0.000 description 1
- 150000003077 polyols Chemical class 0.000 description 1
- 229920006324 polyoxymethylene Polymers 0.000 description 1
- 239000001205 polyphosphate Substances 0.000 description 1
- 235000011176 polyphosphates Nutrition 0.000 description 1
- 229920001296 polysiloxane Polymers 0.000 description 1
- 230000008092 positive effect Effects 0.000 description 1
- 159000000001 potassium salts Chemical class 0.000 description 1
- 239000002243 precursor Substances 0.000 description 1
- 239000000047 product Substances 0.000 description 1
- 229920006395 saturated elastomer Polymers 0.000 description 1
- 229910000029 sodium carbonate Inorganic materials 0.000 description 1
- 235000019812 sodium carboxymethyl cellulose Nutrition 0.000 description 1
- 229920001027 sodium carboxymethylcellulose Polymers 0.000 description 1
- 235000010267 sodium hydrogen sulphite Nutrition 0.000 description 1
- QSKQNALVHFTOQX-UHFFFAOYSA-M sodium nonanoyloxybenzenesulfonate Chemical compound [Na+].CCCCCCCCC(=O)OC1=CC=CC=C1S([O-])(=O)=O QSKQNALVHFTOQX-UHFFFAOYSA-M 0.000 description 1
- 229960001922 sodium perborate Drugs 0.000 description 1
- 239000012418 sodium perborate tetrahydrate Substances 0.000 description 1
- 229940045872 sodium percarbonate Drugs 0.000 description 1
- 159000000000 sodium salts Chemical class 0.000 description 1
- 235000019832 sodium triphosphate Nutrition 0.000 description 1
- PHIMXFJEDZOCMI-UHFFFAOYSA-M sodium;2-hexanoyloxy-3,4,5-trimethylbenzenesulfonate Chemical compound [Na+].CCCCCC(=O)OC1=C(C)C(C)=C(C)C=C1S([O-])(=O)=O PHIMXFJEDZOCMI-UHFFFAOYSA-M 0.000 description 1
- IBDSNZLUHYKHQP-UHFFFAOYSA-N sodium;3-oxidodioxaborirane;tetrahydrate Chemical compound O.O.O.O.[Na+].[O-]B1OO1 IBDSNZLUHYKHQP-UHFFFAOYSA-N 0.000 description 1
- OVONNAXAHAIEDF-UHFFFAOYSA-M sodium;4-benzoyloxybenzenesulfonate Chemical compound [Na+].C1=CC(S(=O)(=O)[O-])=CC=C1OC(=O)C1=CC=CC=C1 OVONNAXAHAIEDF-UHFFFAOYSA-M 0.000 description 1
- YKLJGMBLPUQQOI-UHFFFAOYSA-M sodium;oxidooxy(oxo)borane Chemical compound [Na+].[O-]OB=O YKLJGMBLPUQQOI-UHFFFAOYSA-M 0.000 description 1
- 239000002904 solvent Substances 0.000 description 1
- 239000000600 sorbitol Substances 0.000 description 1
- 238000001694 spray drying Methods 0.000 description 1
- 239000003381 stabilizer Substances 0.000 description 1
- 125000000547 substituted alkyl group Chemical group 0.000 description 1
- 230000001180 sulfating effect Effects 0.000 description 1
- 150000003462 sulfoxides Chemical class 0.000 description 1
- 150000003467 sulfuric acid derivatives Chemical class 0.000 description 1
- 238000003786 synthesis reaction Methods 0.000 description 1
- 239000003760 tallow Substances 0.000 description 1
- 150000003512 tertiary amines Chemical class 0.000 description 1
- RYFMWSXOAZQYPI-UHFFFAOYSA-K trisodium phosphate Chemical compound [Na+].[Na+].[Na+].[O-]P([O-])([O-])=O RYFMWSXOAZQYPI-UHFFFAOYSA-K 0.000 description 1
- 239000010457 zeolite Substances 0.000 description 1
- 239000002888 zwitterionic surfactant Substances 0.000 description 1
Classifications
-
- C—CHEMISTRY; METALLURGY
- C11—ANIMAL OR VEGETABLE OILS, FATS, FATTY SUBSTANCES OR WAXES; FATTY ACIDS THEREFROM; DETERGENTS; CANDLES
- C11D—DETERGENT COMPOSITIONS; USE OF SINGLE SUBSTANCES AS DETERGENTS; SOAP OR SOAP-MAKING; RESIN SOAPS; RECOVERY OF GLYCEROL
- C11D3/00—Other compounding ingredients of detergent compositions covered in group C11D1/00
- C11D3/39—Organic or inorganic per-compounds
- C11D3/3902—Organic or inorganic per-compounds combined with specific additives
- C11D3/3905—Bleach activators or bleach catalysts
- C11D3/3907—Organic compounds
- C11D3/3917—Nitrogen-containing compounds
- C11D3/3925—Nitriles; Isocyanates or quarternary ammonium nitriles
-
- D—TEXTILES; PAPER
- D06—TREATMENT OF TEXTILES OR THE LIKE; LAUNDERING; FLEXIBLE MATERIALS NOT OTHERWISE PROVIDED FOR
- D06L—DRY-CLEANING, WASHING OR BLEACHING FIBRES, FILAMENTS, THREADS, YARNS, FABRICS, FEATHERS OR MADE-UP FIBROUS GOODS; BLEACHING LEATHER OR FURS
- D06L4/00—Bleaching fibres, filaments, threads, yarns, fabrics, feathers or made-up fibrous goods; Bleaching leather or furs
- D06L4/10—Bleaching fibres, filaments, threads, yarns, fabrics, feathers or made-up fibrous goods; Bleaching leather or furs using agents which develop oxygen
-
- D—TEXTILES; PAPER
- D21—PAPER-MAKING; PRODUCTION OF CELLULOSE
- D21H—PULP COMPOSITIONS; PREPARATION THEREOF NOT COVERED BY SUBCLASSES D21C OR D21D; IMPREGNATING OR COATING OF PAPER; TREATMENT OF FINISHED PAPER NOT COVERED BY CLASS B31 OR SUBCLASS D21G; PAPER NOT OTHERWISE PROVIDED FOR
- D21H21/00—Non-fibrous material added to the pulp, characterised by its function, form or properties; Paper-impregnating or coating material, characterised by its function, form or properties
- D21H21/14—Non-fibrous material added to the pulp, characterised by its function, form or properties; Paper-impregnating or coating material, characterised by its function, form or properties characterised by function or properties in or on the paper
- D21H21/32—Bleaching agents
Definitions
- peroxidic bleaching agents such as perborates, Percarbonates, persilicates and perphosphates
- Bleach activators are called.
- nitrile bleach activators and their use as bleach activators in Bleaching agents are described, for example, in EP 303 520, GB 802 035, US 4,883,917, US 5 478 356, US 5 591 378, WO 9 606 912 and WO 9 640 661.
- aminonitrile N-oxides or thereof derived salts have a better bleaching effect than bleach activators according to the state of the art.
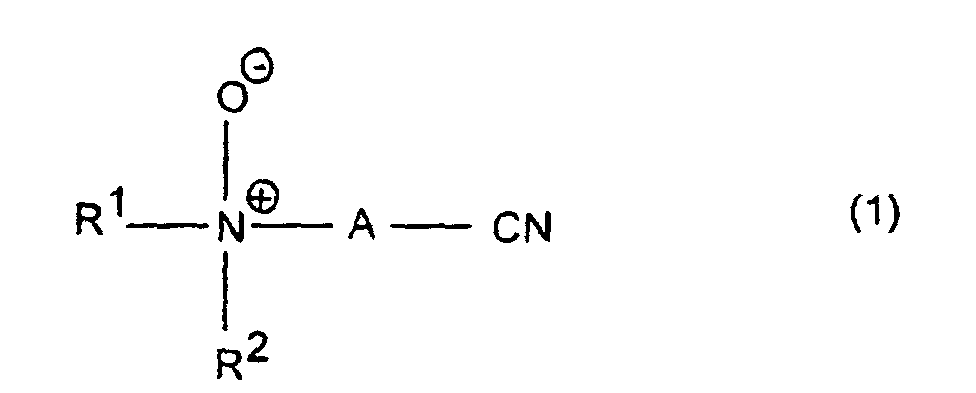
- Aminonitrile N-oxides or their salts of the formula 1 are preferred, in which R 1 and R 2 are C 1 -C 4 -alkyl, in particular methyl, and A is phenylene.
- the aminonitrile N-oxides or the salts derived therefrom are easily accessible by reacting aminonitriles with oxidizing agents; Such reactions are described, for example, in J. Backes "Amine", Methods of Organic Chemistry (Houben-Weyl), D. Klamann (ed.) Vol. E 16d (1992), pp. 1235-1329 and the literature cited therein.
- the invention also relates to the use of these bleach activators in bleaching detergents and cleaning agents as well as in paper and textile bleaching.
- the detergents and cleaning agents contain a peroxide compound and the bleach activator usually also surface-active compounds and other known ingredients.
- Bleach activators and other suitable bleach activators e.g. TAED, Tetraacetylglycoluril, glucose pentaacetate, sodium nonanoyloxybenzenesulfonate, Benzoylcaprolactam or nitrile activators may be included.
- TAED Tetraacetylglycoluril
- glucose pentaacetate glucose pentaacetate
- sodium nonanoyloxybenzenesulfonate Benzoylcaprolactam or nitrile activators
- Benzoylcaprolactam or nitrile activators may be included.
- These additional Bleach activators can be present in an amount of 1 to 10% by weight.
- the surfactant can be derived from natural products such as Soap, or is a synthetic compound from the group of anionic, non-ionic, amphoteric, zwitterionic or cationic surface-active Substances, or mixtures of these.
- suitable substances commercially available, and are described in the literature, for example in "Surface active agents and detergents", Vol. 1 and 2, by Schwartz, Perry and Berch.
- the total proportion of surface-active compounds can be up to 50 % By weight, preferably 1% by weight to 40% by weight, in particular 4% by weight up to 25% by weight.
- Synthetic anionic surfactants are common water-soluble alkali metal salts of organic sulfates and sulfonates with alkyl radicals from about 8 to 22 carbon atoms, the term "alkyl” being the Includes alkyl substituents of higher aryl groups.
- Examples include sodium and ammonium alkyl sulfates, especially the sulfates obtained by sulfating higher (C 8 -C 18 ) alcohols; Sodium and ammonium alkylbenzenesulfonates with an alkyl radical from C 9 to C 20 , in particular linear secondary sodium alkylbenzenesulfonates with an alkyl radical from C 10 to C 15 ; Sodium alkyl glycerol ether sulfates, especially the esters of the higher alcohols derived from tallow and coconut oil; the sodium sulfates and sulfonates of the coconut fatty acid monoglycerides; Sodium and ammonium salts of the sulfuric acid esters of higher (C 9 to C 18 ) oxalkylated, especially the fatty alcohols alkoxylated with ethylene oxide; the reaction products of the esterification of fatty acids with isethionic acid and subsequent neutralization with sodium hydroxide; Sodium and ammonium salts of the
- nonionic surface-active compounds which are preferably used together with anionic surface-active compounds, are in particular the reaction products of alkylene oxides (usually ethylene oxide) with alkylphenols (alkyl radicals from C 5 to C 22 ), the reaction products generally 5 to 25 ethylene oxide (EO ) Units contained in the molecule; the reaction products of aliphatic (C 8 to C 18 ) primary or secondary, linear or branched alcohols with ethylene oxide, generally with 6 to 30 EO, and the addition products of ethylene oxide with reaction products of propylene oxide and ethylenediamine.
- Other nonionic surface active compounds are alkyl polyglycosides, long chain tertiary amine oxides, long chain tertiary phosphine oxides and dialkyl sulfoxides.
- Amphoteric or zwitterionic surfactants can also be used can be used in the compositions according to the invention, but what is usually not desired because of its high cost. If amphoteric or zwitterionic compounds are used, so this usually happens in small amounts in compositions that are mainly anionic and contain nonionic surfactants.
- the detergents and cleaning agents generally also contain a builder.
- Builders come into consideration: calcium binding substances, precipitants, calcium-specific Ion exchangers and their mixtures.
- calcium binders include alkali metal polyphosphates such as sodium tripolyphosphate; Nitrilotriacetic acid and its water-soluble salts; the alkali metal salts of Carboxymethyloxy succinic acid, ethylenediaminetetraacetic acid, Oxydisuccinic acid, mellitic acid, benzene polycarboxylic acids, citric acid and Polyacetal carboxylates as described in U.S. Pat. 4,144,226 and 4,146,495.
- precipitants are sodium orthophosphate, sodium carbonate and Long chain fatty acid soaps.
- ion exchangers specific for calcium are various types of water-insoluble, crystalline or amorphous Aluminum silicates, of which the zeolites are the best known representatives.
- the washing and Detergents contain each of the conventional additives in amounts that one usually finds in such means.
- additives are Foaming agents, such as alkanolamides, especially the monoethanolamides Palm kernel oil fatty acids and coconut fatty acids; foam-preventing substances such as alkyl phosphates and silicones; Graying inhibitors and the like Auxiliaries such as sodium carboxymethyl cellulose and alkyl or substituted alkyl cellulose ethers; Stabilizers such as ethylenediaminetetraacetic acid; softener for textiles; inorganic salts such as sodium sulfate; and, usually small Quantities, fluorescent substances, perfumes, enzymes such as proteases, cellulases, Lipases and amylases, disinfectants and dyes.
- the bleach activators of this invention can be used in a variety of laundry and Detergents are used. These include laundry detergents, Textile bleach, surface cleaners, toilet cleaners, Dishwasher cleaner, and also denture cleaner.
- the detergents can be in solid or liquid form. It is for the sake of stability and Manageability advantageous to the bleach activators in the form of granules use that contain a binder in addition to the bleaching catalyst.
- Various methods for producing such granules are in the patent literature described, for example, in Canada Pat. No.
- the granules containing the bleach activators are generally the Detergent composition along with the other dry Components such as enzymes, inorganic peroxide bleach added.
- the detergent composition to which the catalyst granules are added can be obtained in several ways, such as Dry mixing, extruding, spray drying.
- the bleach activators according to the invention are Particularly suitable for non-aqueous, liquid detergents, together with a bleaching peroxide compound, such as sodium perborate, around the detergent great cleaning ability for fabrics and textiles.
- aqueous, liquid detergents, pasty and gelatinous Including detergent compositions are well known in the art are known, and are described, for example, in US 2,864,770, US 2,940,938, US 4,772,412, US 3 368 977, GB-A-1 205 711 GB-A-1 370 377, GB-A-1 270 040, GB-A-1 292 352, GB-A-2 194 536, DE-A-2 233 771, EP-A-0 028 849.
- compositions in the form of a non-aqueous, liquid medium in which a solid phase can be dispersed can be a liquid, surface-active substance, preferably a nonionic surfactant; a non polar liquid medium such as liquid paraffin; a polar solvent such as Polyols, for example glycerin, sorbitol, ethylene glycol, possibly in combination with low molecular weight monohydric alcohols such as ethanol or isopropanol; or Mixtures of these.
- the solid phase can consist of builder substances, alkalis, abrasive substances, Polymers and other solid ionic surfactants, bleaches fluorescent substances and other common solid ingredients.
- a lead composition was prepared by combining 200 ml of an aqueous solution of reference detergent WMP (laundry research Krefeld, 5 g / l in water with 15 ° dH) solution, 150 mg of sodium perborate monohydrate and 50 mg of the respective activator.
- WMP laundry research Krefeld, 5 g / l in water with 15 ° dH
- tissue pieces soiled with the standard soiling BC-1 tea were subjected to a treatment at a temperature of 40 ° C. under isothermal washing conditions in a Linitest device (Heraeus).
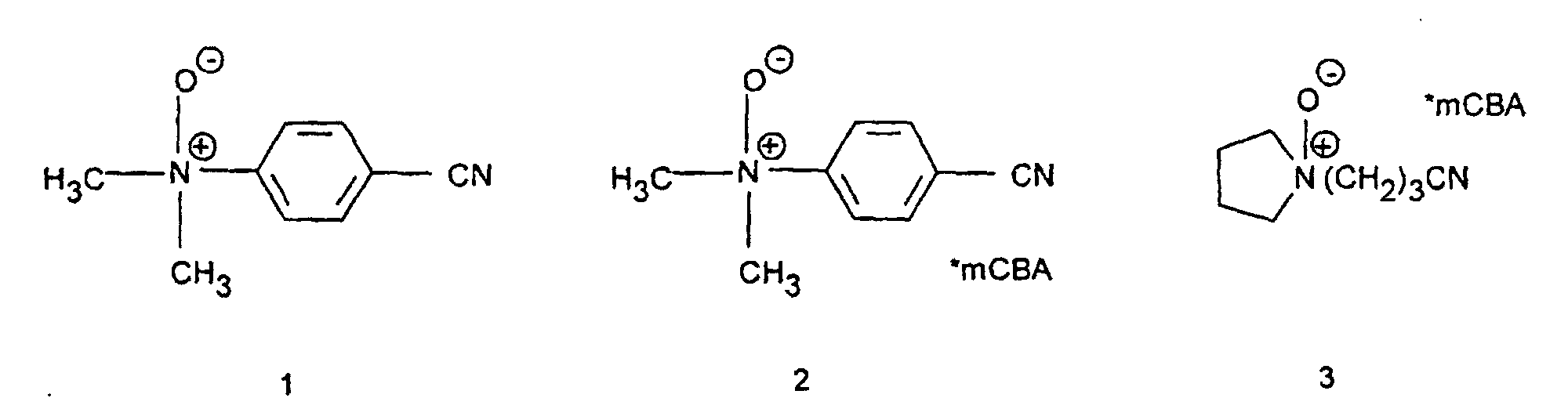
- Connections 1-5 are: 1 2 3 4 5 ⁇ R 1.0 0.7 1.2 0.3 0.1 mCBA: meta-chlorobenzoic acid salt
- the washing experiments show that the aminonitrile N-oxides according to the invention have good bleaching performance. Further advantageous properties of the complexes described are low color damage and low fiber damage.
Landscapes
- Chemical & Material Sciences (AREA)
- Engineering & Computer Science (AREA)
- Inorganic Chemistry (AREA)
- Life Sciences & Earth Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Oil, Petroleum & Natural Gas (AREA)
- Wood Science & Technology (AREA)
- Organic Chemistry (AREA)
- Textile Engineering (AREA)
- Detergent Compositions (AREA)
- Paper (AREA)
Description
- R1, R2
- unabhängig voneinander substituierte oder unsubstituierte C1-C15-Alkyl-, Cycloalkyl- oder Arylreste bedeuten, die durch Fluor, Chlor, Brom, C1-C5-Alkoxy, C1-C5-Alkoxycarbonyl, Amino, Ammonium, Carboxyl, Cyano oder Cyanamino substituiert sein können, oder zusammen mit dem Stickstoffatom, an das sie gebunden sind, einen Ring mit 4 bis 6 Kohlenstoffatomen bilden, der durch C1-C5-Alkyl, C1-C5-Alkoxy, C1-C5-Alkanoyl, Phenyl, Amino, Ammonium, Cyano, Cyanamino, Chlor oder Brom substituiert sein kann und wobei dieser Ring zusätzlich zum Stickstoffatom anstelle von -CH2-Gruppen ein oder zwei Sauerstoffatome oder eine Gruppe enthalten kann, worin R3 Wasserstoff, C1-C7-Alkyl oder Cycloalkyl, Phenyl oder C7-C9-Alkylaryl ist, und
- A
- für einen C1-C5-Alkylen-, einen C5-C10-Cycloalkylen- oder einen Arylenrest steht
Weitere vorteilhafte Eigenschaften der beschriebenen Komplexe sind geringe Farbschädigung und geringe Faserschädigung.
Claims (8)
- Verwendung von Aminonitril-N-oxiden der allgemeinen Formel (1) worin
- R1, R2
- unabhängig voneinander substituierte oder unsubstituierte C1-C15-Alkyl-, Cycloalkyl- oder Arylreste, die durch Fluor, Chlor, Brom, C1-C5-Alkoxy, C1-C5-Alkoxycarbonyl, Amino, Ammonium, Carboxyl, Cyano oder Cyanamino substituiert sein können, oder zusammen mit dem Stickstoffatom, an das sie gebunden sind, einen Ring mit 4 bis 6 Kohlenstoffatomen bilden, der durch C1-C5-Alkyl, C1-C5-Alkoxy, C1-C5-Alkanoyl, Phenyl, Amino, Ammonium, Cyano, Cyanamino, Chlor oder Brom substituiert sein kann und wobei dieser Ring zusätzlich zum Stickstoffatom anstelle von -CH2-Gruppen ein oder zwei Sauerstoffatome oder eine Gruppe enthalten kann, worin R3 Wasserstoff, C1-C7-Alkyl oder Cycloalkyl, Phenyl oder C7-C9-Alkylaryl ist,
- A
- für einen C1-C5-Alkylen-, einen C5-C10-Cycloalkylen- oder einen Arylenrest steht,
- Verwendung von Aminonitril-N-oxiden oder deren Salzen der Formel (1) nach Anspruch 1, dadurch gekennzeichnet, daß man eine Verbindung der Formel (1) verwendet, worin R1 und R2 C1-C4-Alkyl, insbesondere Methyl und A Phenylen bedeuten.
- Wasch- und Reinigungsmittel enthaltend eine Peroxidverbindung und ein Aminonitril-N-oxid der Formel (1) nach Anspruch 1.
- Wasch- und Reinigungsmittel enthaltend eine Peroxidverbindung und 0,05 bis 20 Gew.-% eines Aminonitril-N-oxids der Formel 1 nach Anspruch 1.
- Wasch- und Reinigungsmittel enthaltend 1 bis 60 Gew.-% einer Peroxidverbindung und ein Aminonitril-N-oxid der Formel (1) nach Anspruch 1.
- Wasch- und Reinigungsmittel enthaltend ein Aminonitril-N-oxid der Formel (1) nach Anspruch 1 und ein Perborat, Percarbonat, Perphosphat, Persilikat, Monopersulfat, Hamstoffperoxid, Cumolhydroperoxid oder tert.-Butylhydroperoxid.
- Wasch- und Reinigungsmittel enthaltend eine Peroxidverbindung, ein Aminonitril-N-oxid der Formel (1) nach Anspruch 1 sowie einen Bleichaktivator, der kein Aminonitril-N-oxid ist.
- Wasch- und Reinigungsmittel enthaltend eine Peroxidverbindung, ein Aminonitril-N-oxid der Formel (1) nach Anspruch 1 und oberflächenaktive Verbindungen.
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| DE19746290 | 1997-10-20 | ||
| DE19746290A DE19746290A1 (de) | 1997-10-20 | 1997-10-20 | Verwendung von Aminonitril-N-oxiden als Bleichaktivatoren |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| EP0909810A1 EP0909810A1 (de) | 1999-04-21 |
| EP0909810B1 true EP0909810B1 (de) | 2004-12-22 |
Family
ID=7846054
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| EP98117813A Expired - Lifetime EP0909810B1 (de) | 1997-10-20 | 1998-09-19 | Verwendung von Aminonitril-N-oxiden als Bleichaktivatoren |
Country Status (5)
| Country | Link |
|---|---|
| US (2) | US6007583A (de) |
| EP (1) | EP0909810B1 (de) |
| JP (1) | JP4021075B2 (de) |
| BR (1) | BR9804057A (de) |
| DE (2) | DE19746290A1 (de) |
Families Citing this family (14)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| ATE311432T1 (de) * | 1999-08-27 | 2005-12-15 | Procter & Gamble | Stabile substanzen, zusammensetzungen und waschverfahren zu deren verwendung |
| JP2003508581A (ja) * | 1999-08-27 | 2003-03-04 | ザ、プロクター、エンド、ギャンブル、カンパニー | 処方成分の制御された有効化法、それを使用する組成物および洗濯方法 |
| BR0013616B1 (pt) * | 1999-08-27 | 2011-12-27 | composiÇço de alvejamento e composto catalisador orgÂnico de lavanderia. | |
| US6821935B1 (en) | 1999-08-27 | 2004-11-23 | Procter & Gamble Company | Color safe laundry methods employing zwitterionic formulation components |
| US6825160B1 (en) | 1999-08-27 | 2004-11-30 | Procter & Gamble Company | Color safe laundry methods employing cationic formulation components |
| US6903060B1 (en) | 1999-08-27 | 2005-06-07 | Procter & Gamble Company | Stable formulation components, compositions and laundry methods employing same |
| BR0013610A (pt) * | 1999-08-27 | 2002-07-16 | Procter & Gamble | Componentes de formulções de ação rápida,composições e métodos para lavar roupa empregando os mesmos |
| US6818607B1 (en) | 1999-08-27 | 2004-11-16 | Procter & Gamble Company | Bleach boosting components, compositions and laundry methods |
| US7109156B1 (en) | 1999-08-27 | 2006-09-19 | Procter & Gamble Company | Controlled availability of formulation components, compositions and laundry methods employing same |
| DE10064636A1 (de) * | 2000-12-22 | 2002-07-04 | Henkel Kgaa | Flüssiges Wasch-und/oder Reinigungsmittel |
| US7557076B2 (en) * | 2002-06-06 | 2009-07-07 | The Procter & Gamble Company | Organic catalyst with enhanced enzyme compatibility |
| US7169744B2 (en) * | 2002-06-06 | 2007-01-30 | Procter & Gamble Company | Organic catalyst with enhanced solubility |
| US20050113246A1 (en) * | 2003-11-06 | 2005-05-26 | The Procter & Gamble Company | Process of producing an organic catalyst |
| AR051659A1 (es) * | 2005-06-17 | 2007-01-31 | Procter & Gamble | Una composicion que comprende un catalizador organico con compatibilidada enzimatica mejorada |
Family Cites Families (11)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| BE548769A (de) * | 1955-07-08 | |||
| DE2346504A1 (de) * | 1973-09-15 | 1975-04-24 | Hoechst Ag | Verfahren zum faerben von textilmaterial aus polyesterfaser-/cellulose-mischungen |
| US4883917A (en) * | 1985-10-01 | 1989-11-28 | Ethyl Corporation | Quaternary ammonium compounds |
| US4915863A (en) * | 1987-08-14 | 1990-04-10 | Kao Corporation | Bleaching composition |
| GB9011618D0 (en) * | 1990-05-24 | 1990-07-11 | Unilever Plc | Bleaching composition |
| US5478356B1 (en) * | 1994-05-10 | 1997-11-18 | Clorox Co | Cyanoimides and compositions useful for bleaching |
| US5591378A (en) * | 1994-07-06 | 1997-01-07 | The Clorox Company | Substituted benzonitriles and compositions useful for bleaching |
| JP3811508B2 (ja) * | 1994-08-31 | 2006-08-23 | ジョンソン株式会社 | 過酸化物の活性化方法およびその組成物 |
| US5739327A (en) * | 1995-06-07 | 1998-04-14 | The Clorox Company | N-alkyl ammonium acetonitrile bleach activators |
| DE19605526A1 (de) * | 1996-02-15 | 1997-08-21 | Hoechst Ag | Ammoniumnitrile und deren Verwendung als Bleichaktivatoren |
| US5739096A (en) * | 1996-05-06 | 1998-04-14 | S. C. Johnson & Son, Inc. | Cyanopyridine N-oxide peroxide bleach activators |
-
1997
- 1997-10-20 DE DE19746290A patent/DE19746290A1/de not_active Withdrawn
-
1998
- 1998-09-19 DE DE59812405T patent/DE59812405D1/de not_active Expired - Fee Related
- 1998-09-19 EP EP98117813A patent/EP0909810B1/de not_active Expired - Lifetime
- 1998-10-19 JP JP29697798A patent/JP4021075B2/ja not_active Expired - Fee Related
- 1998-10-19 US US09/174,841 patent/US6007583A/en not_active Expired - Fee Related
- 1998-10-19 BR BR9804057-0A patent/BR9804057A/pt not_active Application Discontinuation
-
1999
- 1999-10-06 US US09/413,831 patent/US6120557A/en not_active Expired - Fee Related
Also Published As
| Publication number | Publication date |
|---|---|
| JPH11199894A (ja) | 1999-07-27 |
| JP4021075B2 (ja) | 2007-12-12 |
| US6120557A (en) | 2000-09-19 |
| BR9804057A (pt) | 1999-12-07 |
| US6007583A (en) | 1999-12-28 |
| DE19746290A1 (de) | 1999-04-22 |
| DE59812405D1 (de) | 2005-01-27 |
| EP0909810A1 (de) | 1999-04-21 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| DE3886969T2 (de) | Quartäre Ammonium- oder Phosphonium-Peroxycarbonsäure-Prekursoren und ihre Verwendung in Detergensbleichmittelzusammensetzungen. | |
| DE69021129T2 (de) | Bleichaktivierung und Bleichmittel-Zusammensetzungen. | |
| DE19605526A1 (de) | Ammoniumnitrile und deren Verwendung als Bleichaktivatoren | |
| DE69222620T2 (de) | Bleichaktivierung unter Verwendung einer Mangan- verbindung und einem organischen Ligand | |
| DE69417435T2 (de) | Quarternäre oxaziridinsalze als bleichmittelverbindungen | |
| DE68908439T2 (de) | Quatenäre-Ammonium-Verbindungen zur Verwendung in Bleich-Systemen. | |
| EP0869171B1 (de) | Bleichaktive Metall-Komplexe | |
| EP0909810B1 (de) | Verwendung von Aminonitril-N-oxiden als Bleichaktivatoren | |
| DE2060762A1 (de) | Mittel zur Herstellung von Kaltbleichflotten,insbesondere von kaltbleichwirksamen Waschlaugen | |
| DE19633305A1 (de) | Sulphonylimin-Derivate als Bleichkatalysatoren | |
| EP0877078B1 (de) | Bleichaktive Metall-Komplexe | |
| CH642677A5 (de) | Bleich- und reinigungsmittel. | |
| DE10211389A1 (de) | Ammoniumnitrile und deren Verwendung als hydrophobe Bleichaktivatoren | |
| EP0930358B1 (de) | Verwendung von Formamidinium-Salzen als Bleichaktivatoren | |
| EP0816336A1 (de) | Quartäre Ammoniumverbindungen als Bleichaktivatoren und deren Herstellung | |
| EP0889050A2 (de) | Metall-Komplexe als Bleichaktivatoren | |
| DE19629159A1 (de) | Nitril-Betaine als Bleichaktivatoren und deren Herstellung | |
| DE19738274A1 (de) | Verwendung von Cyanpyridin-N-oxiden als Bleichaktivatoren | |
| EP0806473A2 (de) | Cyanopyridinium-Verbindungen als Bleichaktivatoren | |
| EP0698661A2 (de) | Aktivatoren für anorganische Peroxoverbindungen und sie enthaltende Mittel | |
| DE19629162A1 (de) | Salze von Cyanamiden als Bleichaktivatoren | |
| DE19614822A1 (de) | Isocyanate als Bleichaktivatoren | |
| DE102004041760A1 (de) | Diethylmethyl-Ammoniumnitrile und Wasch- und Reinigungsmittel, enthaltend diese Ammoniumnitrile | |
| DE102005037761A1 (de) | Wasch- und Reinigungsmittel enthaltend 1,3,5-Triacetyl-2,4-dioxo-1,3,5-hexahydrotriazin als Bleichaktivator | |
| DE102005009135A1 (de) | Ammoniumnitrile und deren Verwendung als Bleichaktivatoren |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| PUAI | Public reference made under article 153(3) epc to a published international application that has entered the european phase |
Free format text: ORIGINAL CODE: 0009012 |
|
| AK | Designated contracting states |
Kind code of ref document: A1 Designated state(s): AT BE CH DE DK ES FR GB IT LI NL PT SE |
|
| AX | Request for extension of the european patent |
Free format text: AL;LT;LV;MK;RO;SI |
|
| 17P | Request for examination filed |
Effective date: 19991021 |
|
| AKX | Designation fees paid |
Free format text: AT BE CH DE DK ES FR GB IT LI NL PT SE |
|
| GRAP | Despatch of communication of intention to grant a patent |
Free format text: ORIGINAL CODE: EPIDOSNIGR1 |
|
| RBV | Designated contracting states (corrected) |
Designated state(s): DE FR GB IT |
|
| GRAS | Grant fee paid |
Free format text: ORIGINAL CODE: EPIDOSNIGR3 |
|
| GRAA | (expected) grant |
Free format text: ORIGINAL CODE: 0009210 |
|
| AK | Designated contracting states |
Kind code of ref document: B1 Designated state(s): DE FR GB IT |
|
| REG | Reference to a national code |
Ref country code: GB Ref legal event code: FG4D Free format text: NOT ENGLISH |
|
| REF | Corresponds to: |
Ref document number: 59812405 Country of ref document: DE Date of ref document: 20050127 Kind code of ref document: P |
|
| GBT | Gb: translation of ep patent filed (gb section 77(6)(a)/1977) |
Effective date: 20050309 |
|
| PLBE | No opposition filed within time limit |
Free format text: ORIGINAL CODE: 0009261 |
|
| STAA | Information on the status of an ep patent application or granted ep patent |
Free format text: STATUS: NO OPPOSITION FILED WITHIN TIME LIMIT |
|
| 26N | No opposition filed |
Effective date: 20050923 |
|
| ET | Fr: translation filed | ||
| REG | Reference to a national code |
Ref country code: FR Ref legal event code: CD |
|
| PGFP | Annual fee paid to national office [announced via postgrant information from national office to epo] |
Ref country code: IT Payment date: 20080826 Year of fee payment: 11 Ref country code: FR Payment date: 20080813 Year of fee payment: 11 |
|
| PGFP | Annual fee paid to national office [announced via postgrant information from national office to epo] |
Ref country code: GB Payment date: 20080915 Year of fee payment: 11 |
|
| PGFP | Annual fee paid to national office [announced via postgrant information from national office to epo] |
Ref country code: DE Payment date: 20080808 Year of fee payment: 11 |
|
| GBPC | Gb: european patent ceased through non-payment of renewal fee |
Effective date: 20090919 |
|
| REG | Reference to a national code |
Ref country code: FR Ref legal event code: ST Effective date: 20100531 |
|
| PG25 | Lapsed in a contracting state [announced via postgrant information from national office to epo] |
Ref country code: FR Free format text: LAPSE BECAUSE OF NON-PAYMENT OF DUE FEES Effective date: 20090930 Ref country code: DE Free format text: LAPSE BECAUSE OF NON-PAYMENT OF DUE FEES Effective date: 20100401 |
|
| PG25 | Lapsed in a contracting state [announced via postgrant information from national office to epo] |
Ref country code: GB Free format text: LAPSE BECAUSE OF NON-PAYMENT OF DUE FEES Effective date: 20090919 |
|
| PG25 | Lapsed in a contracting state [announced via postgrant information from national office to epo] |
Ref country code: IT Free format text: LAPSE BECAUSE OF NON-PAYMENT OF DUE FEES Effective date: 20090919 |