EP0000061B1 - Phosphorhaltige Carbonsäure-Derivate, Verfahren zu deren Herstellung, sowie ihre Verwendung - Google Patents
Phosphorhaltige Carbonsäure-Derivate, Verfahren zu deren Herstellung, sowie ihre Verwendung Download PDFInfo
- Publication number
- EP0000061B1 EP0000061B1 EP78100104A EP78100104A EP0000061B1 EP 0000061 B1 EP0000061 B1 EP 0000061B1 EP 78100104 A EP78100104 A EP 78100104A EP 78100104 A EP78100104 A EP 78100104A EP 0000061 B1 EP0000061 B1 EP 0000061B1
- Authority
- EP
- European Patent Office
- Prior art keywords
- radicals
- compounds
- optionally
- alkyl
- acid
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Expired
Links
- 238000000034 method Methods 0.000 title claims description 17
- OAICVXFJPJFONN-UHFFFAOYSA-N Phosphorus Chemical compound [P] OAICVXFJPJFONN-UHFFFAOYSA-N 0.000 title claims description 10
- 229910052698 phosphorus Inorganic materials 0.000 title claims description 8
- 239000011574 phosphorus Substances 0.000 title claims description 8
- 150000001732 carboxylic acid derivatives Chemical class 0.000 title claims description 5
- 150000001875 compounds Chemical class 0.000 claims description 37
- -1 ammonium ions Chemical class 0.000 claims description 19
- 150000003254 radicals Chemical class 0.000 claims description 17
- WSFSSNUMVMOOMR-UHFFFAOYSA-N Formaldehyde Chemical compound O=C WSFSSNUMVMOOMR-UHFFFAOYSA-N 0.000 claims description 16
- 125000004178 (C1-C4) alkyl group Chemical group 0.000 claims description 10
- 229910052736 halogen Inorganic materials 0.000 claims description 10
- 150000002367 halogens Chemical class 0.000 claims description 10
- 239000003054 catalyst Substances 0.000 claims description 9
- 229910052794 bromium Inorganic materials 0.000 claims description 8
- 229910052708 sodium Inorganic materials 0.000 claims description 8
- 239000011734 sodium Substances 0.000 claims description 8
- 125000000217 alkyl group Chemical group 0.000 claims description 7
- 239000000460 chlorine Substances 0.000 claims description 7
- 229910052801 chlorine Inorganic materials 0.000 claims description 7
- 229910052739 hydrogen Inorganic materials 0.000 claims description 7
- 125000001997 phenyl group Chemical group [H]C1=C([H])C([H])=C(*)C([H])=C1[H] 0.000 claims description 7
- 229910052783 alkali metal Inorganic materials 0.000 claims description 6
- 150000001340 alkali metals Chemical class 0.000 claims description 6
- CBOIHMRHGLHBPB-UHFFFAOYSA-N hydroxymethyl Chemical compound O[CH2] CBOIHMRHGLHBPB-UHFFFAOYSA-N 0.000 claims description 5
- 229910052700 potassium Inorganic materials 0.000 claims description 5
- 125000003837 (C1-C20) alkyl group Chemical group 0.000 claims description 4
- 239000008139 complexing agent Substances 0.000 claims description 4
- 150000002825 nitriles Chemical class 0.000 claims description 4
- 239000004033 plastic Substances 0.000 claims description 4
- 229920003023 plastic Polymers 0.000 claims description 4
- 239000004014 plasticizer Substances 0.000 claims description 4
- QGZKDVFQNNGYKY-UHFFFAOYSA-O Ammonium Chemical compound [NH4+] QGZKDVFQNNGYKY-UHFFFAOYSA-O 0.000 claims description 3
- 125000004432 carbon atom Chemical group C* 0.000 claims description 3
- 150000001768 cations Chemical class 0.000 claims description 3
- 239000001257 hydrogen Substances 0.000 claims description 3
- 229910052744 lithium Inorganic materials 0.000 claims description 3
- 229910021645 metal ion Inorganic materials 0.000 claims description 3
- 125000002496 methyl group Chemical group [H]C([H])([H])* 0.000 claims description 3
- 229920000915 polyvinyl chloride Polymers 0.000 claims description 3
- 239000004800 polyvinyl chloride Substances 0.000 claims description 3
- VEXZGXHMUGYJMC-UHFFFAOYSA-M Chloride anion Chemical compound [Cl-] VEXZGXHMUGYJMC-UHFFFAOYSA-M 0.000 claims description 2
- 125000003917 carbamoyl group Chemical group [H]N([H])C(*)=O 0.000 claims description 2
- 125000001495 ethyl group Chemical group [H]C([H])([H])C([H])([H])* 0.000 claims description 2
- 125000004435 hydrogen atom Chemical group [H]* 0.000 claims description 2
- 239000012442 inert solvent Substances 0.000 claims description 2
- 239000000463 material Substances 0.000 claims description 2
- 239000004753 textile Substances 0.000 claims description 2
- WKBOTKDWSSQWDR-UHFFFAOYSA-N Bromine atom Chemical compound [Br] WKBOTKDWSSQWDR-UHFFFAOYSA-N 0.000 claims 3
- GDTBXPJZTBHREO-UHFFFAOYSA-N bromine Substances BrBr GDTBXPJZTBHREO-UHFFFAOYSA-N 0.000 claims 3
- ZAMOUSCENKQFHK-UHFFFAOYSA-N Chlorine atom Chemical compound [Cl] ZAMOUSCENKQFHK-UHFFFAOYSA-N 0.000 claims 2
- DGAQECJNVWCQMB-PUAWFVPOSA-M Ilexoside XXIX Chemical compound C[C@@H]1CC[C@@]2(CC[C@@]3(C(=CC[C@H]4[C@]3(CC[C@@H]5[C@@]4(CC[C@@H](C5(C)C)OS(=O)(=O)[O-])C)C)[C@@H]2[C@]1(C)O)C)C(=O)O[C@H]6[C@@H]([C@H]([C@@H]([C@H](O6)CO)O)O)O.[Na+] DGAQECJNVWCQMB-PUAWFVPOSA-M 0.000 claims 2
- 125000003368 amide group Chemical group 0.000 claims 2
- WHXSMMKQMYFTQS-UHFFFAOYSA-N Lithium Chemical compound [Li] WHXSMMKQMYFTQS-UHFFFAOYSA-N 0.000 claims 1
- YNPNZTXNASCQKK-UHFFFAOYSA-N Phenanthrene Natural products C1=CC=C2C3=CC=CC=C3C=CC2=C1 YNPNZTXNASCQKK-UHFFFAOYSA-N 0.000 claims 1
- ZLMJMSJWJFRBEC-UHFFFAOYSA-N Potassium Chemical compound [K] ZLMJMSJWJFRBEC-UHFFFAOYSA-N 0.000 claims 1
- DGEZNRSVGBDHLK-UHFFFAOYSA-N [1,10]phenanthroline Chemical compound C1=CN=C2C3=NC=CC=C3C=CC2=C1 DGEZNRSVGBDHLK-UHFFFAOYSA-N 0.000 claims 1
- 125000003262 carboxylic acid ester group Chemical group [H]C([H])([*:2])OC(=O)C([H])([H])[*:1] 0.000 claims 1
- 229920002678 cellulose Polymers 0.000 claims 1
- 239000001913 cellulose Substances 0.000 claims 1
- 125000002603 chloroethyl group Chemical group [H]C([*])([H])C([H])([H])Cl 0.000 claims 1
- 239000011591 potassium Substances 0.000 claims 1
- 239000003340 retarding agent Substances 0.000 claims 1
- 238000006243 chemical reaction Methods 0.000 description 23
- 239000000243 solution Substances 0.000 description 23
- 239000000203 mixture Substances 0.000 description 22
- OKKJLVBELUTLKV-UHFFFAOYSA-N Methanol Chemical compound OC OKKJLVBELUTLKV-UHFFFAOYSA-N 0.000 description 21
- YXFVVABEGXRONW-UHFFFAOYSA-N Toluene Chemical compound CC1=CC=CC=C1 YXFVVABEGXRONW-UHFFFAOYSA-N 0.000 description 18
- 239000003513 alkali Substances 0.000 description 16
- VEXZGXHMUGYJMC-UHFFFAOYSA-N Hydrochloric acid Chemical compound Cl VEXZGXHMUGYJMC-UHFFFAOYSA-N 0.000 description 15
- 239000002253 acid Substances 0.000 description 13
- 150000002148 esters Chemical class 0.000 description 13
- WQDUMFSSJAZKTM-UHFFFAOYSA-N Sodium methoxide Chemical compound [Na+].[O-]C WQDUMFSSJAZKTM-UHFFFAOYSA-N 0.000 description 10
- 238000001816 cooling Methods 0.000 description 10
- NLHHRLWOUZZQLW-UHFFFAOYSA-N Acrylonitrile Chemical compound C=CC#N NLHHRLWOUZZQLW-UHFFFAOYSA-N 0.000 description 9
- NLXLAEXVIDQMFP-UHFFFAOYSA-N Ammonia chloride Chemical compound [NH4+].[Cl-] NLXLAEXVIDQMFP-UHFFFAOYSA-N 0.000 description 9
- HEMHJVSKTPXQMS-UHFFFAOYSA-M Sodium hydroxide Chemical compound [OH-].[Na+] HEMHJVSKTPXQMS-UHFFFAOYSA-M 0.000 description 9
- 239000004744 fabric Substances 0.000 description 9
- 239000003063 flame retardant Substances 0.000 description 9
- RNFJDJUURJAICM-UHFFFAOYSA-N 2,2,4,4,6,6-hexaphenoxy-1,3,5-triaza-2$l^{5},4$l^{5},6$l^{5}-triphosphacyclohexa-1,3,5-triene Chemical compound N=1P(OC=2C=CC=CC=2)(OC=2C=CC=CC=2)=NP(OC=2C=CC=CC=2)(OC=2C=CC=CC=2)=NP=1(OC=1C=CC=CC=1)OC1=CC=CC=C1 RNFJDJUURJAICM-UHFFFAOYSA-N 0.000 description 8
- VNWKTOKETHGBQD-UHFFFAOYSA-N methane Chemical compound C VNWKTOKETHGBQD-UHFFFAOYSA-N 0.000 description 8
- 239000000047 product Substances 0.000 description 8
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 7
- 239000002904 solvent Substances 0.000 description 7
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 7
- MEJXGECPYZGPPN-UHFFFAOYSA-N 2-methylphosphonoyloxypropane Chemical compound CC(C)OP(C)=O MEJXGECPYZGPPN-UHFFFAOYSA-N 0.000 description 6
- QTBSBXVTEAMEQO-UHFFFAOYSA-N Acetic acid Chemical compound CC(O)=O QTBSBXVTEAMEQO-UHFFFAOYSA-N 0.000 description 6
- CSCPPACGZOOCGX-UHFFFAOYSA-N Acetone Chemical compound CC(C)=O CSCPPACGZOOCGX-UHFFFAOYSA-N 0.000 description 6
- OKTJSMMVPCPJKN-UHFFFAOYSA-N Carbon Chemical compound [C] OKTJSMMVPCPJKN-UHFFFAOYSA-N 0.000 description 6
- BAPJBEWLBFYGME-UHFFFAOYSA-N Methyl acrylate Chemical compound COC(=O)C=C BAPJBEWLBFYGME-UHFFFAOYSA-N 0.000 description 6
- WPYMKLBDIGXBTP-UHFFFAOYSA-N benzoic acid Chemical compound OC(=O)C1=CC=CC=C1 WPYMKLBDIGXBTP-UHFFFAOYSA-N 0.000 description 6
- 230000000694 effects Effects 0.000 description 6
- 229920000742 Cotton Polymers 0.000 description 5
- RTZKZFJDLAIYFH-UHFFFAOYSA-N Diethyl ether Chemical compound CCOCC RTZKZFJDLAIYFH-UHFFFAOYSA-N 0.000 description 5
- JIGUQPWFLRLWPJ-UHFFFAOYSA-N Ethyl acrylate Chemical compound CCOC(=O)C=C JIGUQPWFLRLWPJ-UHFFFAOYSA-N 0.000 description 5
- PNJWIWWMYCMZRO-UHFFFAOYSA-N pent‐4‐en‐2‐one Natural products CC(=O)CC=C PNJWIWWMYCMZRO-UHFFFAOYSA-N 0.000 description 5
- 238000007127 saponification reaction Methods 0.000 description 5
- 239000007787 solid Substances 0.000 description 5
- QGZKDVFQNNGYKY-UHFFFAOYSA-N Ammonia Chemical compound N QGZKDVFQNNGYKY-UHFFFAOYSA-N 0.000 description 4
- KFZMGEQAYNKOFK-UHFFFAOYSA-N Isopropanol Chemical compound CC(C)O KFZMGEQAYNKOFK-UHFFFAOYSA-N 0.000 description 4
- 150000007513 acids Chemical class 0.000 description 4
- 125000003118 aryl group Chemical group 0.000 description 4
- 125000006297 carbonyl amino group Chemical group [H]N([*:2])C([*:1])=O 0.000 description 4
- 150000001735 carboxylic acids Chemical class 0.000 description 4
- 239000000706 filtrate Substances 0.000 description 4
- 238000010992 reflux Methods 0.000 description 4
- 150000003839 salts Chemical class 0.000 description 4
- 238000003756 stirring Methods 0.000 description 4
- RYHBNJHYFVUHQT-UHFFFAOYSA-N 1,4-Dioxane Chemical compound C1COCCO1 RYHBNJHYFVUHQT-UHFFFAOYSA-N 0.000 description 3
- STJWVOQLJPNAQL-UHFFFAOYSA-N 1-[diethoxyphosphorylmethyl(ethoxy)phosphoryl]oxyethane Chemical compound CCOP(=O)(OCC)CP(=O)(OCC)OCC STJWVOQLJPNAQL-UHFFFAOYSA-N 0.000 description 3
- RAMHKESLQNRVOC-UHFFFAOYSA-N 3,3-diphosphonoheptanedioic acid Chemical class OC(=O)CCCC(P(O)(O)=O)(P(O)(O)=O)CC(O)=O RAMHKESLQNRVOC-UHFFFAOYSA-N 0.000 description 3
- 239000005711 Benzoic acid Substances 0.000 description 3
- 229960000583 acetic acid Drugs 0.000 description 3
- 230000002378 acidificating effect Effects 0.000 description 3
- 125000005396 acrylic acid ester group Chemical group 0.000 description 3
- 235000019270 ammonium chloride Nutrition 0.000 description 3
- 150000003863 ammonium salts Chemical class 0.000 description 3
- 239000002585 base Substances 0.000 description 3
- 235000010233 benzoic acid Nutrition 0.000 description 3
- 150000001733 carboxylic acid esters Chemical group 0.000 description 3
- 239000012230 colorless oil Substances 0.000 description 3
- YJSXLGKPMXKZJR-UHFFFAOYSA-N ethoxy-oxo-phenylphosphanium Chemical compound CCO[P+](=O)C1=CC=CC=C1 YJSXLGKPMXKZJR-UHFFFAOYSA-N 0.000 description 3
- 239000012362 glacial acetic acid Substances 0.000 description 3
- 229910052602 gypsum Inorganic materials 0.000 description 3
- 239000010440 gypsum Substances 0.000 description 3
- 238000010438 heat treatment Methods 0.000 description 3
- 150000004678 hydrides Chemical class 0.000 description 3
- 125000000896 monocarboxylic acid group Chemical group 0.000 description 3
- 239000003921 oil Substances 0.000 description 3
- 238000005406 washing Methods 0.000 description 3
- 125000006704 (C5-C6) cycloalkyl group Chemical group 0.000 description 2
- FVIFCZPHBXSWSB-UHFFFAOYSA-N 2-hydroxyheptanedinitrile Chemical compound N#CC(O)CCCCC#N FVIFCZPHBXSWSB-UHFFFAOYSA-N 0.000 description 2
- XOLXBWQACCVPIA-UHFFFAOYSA-N 3,3-bis(diethoxyphosphoryl)heptanedioic acid Chemical compound CCOP(=O)(OCC)C(P(=O)(OCC)OCC)(CC(O)=O)CCCC(O)=O XOLXBWQACCVPIA-UHFFFAOYSA-N 0.000 description 2
- LXFLHRNHTQZONO-UHFFFAOYSA-N 3,3-bis(methylphosphanyl)heptanedioic acid Chemical compound CPC(CCCC(=O)O)(CC(=O)O)PC LXFLHRNHTQZONO-UHFFFAOYSA-N 0.000 description 2
- 125000004648 C2-C8 alkenyl group Chemical group 0.000 description 2
- HEDRZPFGACZZDS-UHFFFAOYSA-N Chloroform Chemical compound ClC(Cl)Cl HEDRZPFGACZZDS-UHFFFAOYSA-N 0.000 description 2
- UFHFLCQGNIYNRP-UHFFFAOYSA-N Hydrogen Chemical compound [H][H] UFHFLCQGNIYNRP-UHFFFAOYSA-N 0.000 description 2
- MHAJPDPJQMAIIY-UHFFFAOYSA-N Hydrogen peroxide Chemical compound OO MHAJPDPJQMAIIY-UHFFFAOYSA-N 0.000 description 2
- OFBQJSOFQDEBGM-UHFFFAOYSA-N Pentane Chemical compound CCCCC OFBQJSOFQDEBGM-UHFFFAOYSA-N 0.000 description 2
- WYURNTSHIVDZCO-UHFFFAOYSA-N Tetrahydrofuran Chemical compound C1CCOC1 WYURNTSHIVDZCO-UHFFFAOYSA-N 0.000 description 2
- 150000007933 aliphatic carboxylic acids Chemical class 0.000 description 2
- 150000001447 alkali salts Chemical class 0.000 description 2
- 150000001408 amides Chemical class 0.000 description 2
- 229910021529 ammonia Inorganic materials 0.000 description 2
- 238000009835 boiling Methods 0.000 description 2
- 125000005521 carbonamide group Chemical class 0.000 description 2
- 150000003857 carboxamides Chemical class 0.000 description 2
- 230000003197 catalytic effect Effects 0.000 description 2
- 239000007795 chemical reaction product Substances 0.000 description 2
- DIOQZVSQGTUSAI-UHFFFAOYSA-N decane Chemical compound CCCCCCCCCC DIOQZVSQGTUSAI-UHFFFAOYSA-N 0.000 description 2
- 150000005690 diesters Chemical class 0.000 description 2
- 239000006185 dispersion Substances 0.000 description 2
- 230000008030 elimination Effects 0.000 description 2
- 238000003379 elimination reaction Methods 0.000 description 2
- 125000004494 ethyl ester group Chemical group 0.000 description 2
- 230000007062 hydrolysis Effects 0.000 description 2
- 238000006460 hydrolysis reaction Methods 0.000 description 2
- 238000005470 impregnation Methods 0.000 description 2
- XEEYBQQBJWHFJM-UHFFFAOYSA-N iron Substances [Fe] XEEYBQQBJWHFJM-UHFFFAOYSA-N 0.000 description 2
- MBKDYNNUVRNNRF-UHFFFAOYSA-N medronic acid Chemical compound OP(O)(=O)CP(O)(O)=O MBKDYNNUVRNNRF-UHFFFAOYSA-N 0.000 description 2
- VLKZOEOYAKHREP-UHFFFAOYSA-N n-Hexane Chemical compound CCCCCC VLKZOEOYAKHREP-UHFFFAOYSA-N 0.000 description 2
- 230000003472 neutralizing effect Effects 0.000 description 2
- WLJVNTCWHIRURA-UHFFFAOYSA-N pimelic acid Chemical compound OC(=O)CCCCCC(O)=O WLJVNTCWHIRURA-UHFFFAOYSA-N 0.000 description 2
- 230000002035 prolonged effect Effects 0.000 description 2
- 230000000717 retained effect Effects 0.000 description 2
- QDRKDTQENPPHOJ-UHFFFAOYSA-N sodium ethoxide Chemical compound [Na+].CC[O-] QDRKDTQENPPHOJ-UHFFFAOYSA-N 0.000 description 2
- 239000000126 substance Substances 0.000 description 2
- DREPONDJUKIQLX-UHFFFAOYSA-N 1-[ethenyl(ethoxy)phosphoryl]oxyethane Chemical compound CCOP(=O)(C=C)OCC DREPONDJUKIQLX-UHFFFAOYSA-N 0.000 description 1
- KGRVJHAUYBGFFP-UHFFFAOYSA-N 2,2'-Methylenebis(4-methyl-6-tert-butylphenol) Chemical compound CC(C)(C)C1=CC(C)=CC(CC=2C(=C(C=C(C)C=2)C(C)(C)C)O)=C1O KGRVJHAUYBGFFP-UHFFFAOYSA-N 0.000 description 1
- LYFNCKPMTCSLBV-UHFFFAOYSA-N 2-hydroxyheptanedioic acid Chemical compound OC(=O)C(O)CCCCC(O)=O LYFNCKPMTCSLBV-UHFFFAOYSA-N 0.000 description 1
- DDOAOFQKHIPFFJ-UHFFFAOYSA-N 2-methyl-1-methylphosphonoyloxypropane Chemical compound CC(C)COP(C)=O DDOAOFQKHIPFFJ-UHFFFAOYSA-N 0.000 description 1
- VGUWZCUCNQXGBU-UHFFFAOYSA-N 3-[(4-methylpiperazin-1-yl)methyl]-5-nitro-1h-indole Chemical compound C1CN(C)CCN1CC1=CNC2=CC=C([N+]([O-])=O)C=C12 VGUWZCUCNQXGBU-UHFFFAOYSA-N 0.000 description 1
- ZJQVSRSTKURISF-UHFFFAOYSA-N 3-methylphosphanyl-3-phosphonoheptanedioic acid Chemical compound CPC(CCCC(=O)O)(CC(=O)O)P(=O)(O)O ZJQVSRSTKURISF-UHFFFAOYSA-N 0.000 description 1
- HRPVXLWXLXDGHG-UHFFFAOYSA-N Acrylamide Chemical compound NC(=O)C=C HRPVXLWXLXDGHG-UHFFFAOYSA-N 0.000 description 1
- 241001136792 Alle Species 0.000 description 1
- IGJXEWFUGUJTNX-UHFFFAOYSA-N C1(=CC=CC=C1)P(OCCCCCCCC)=O Chemical compound C1(=CC=CC=C1)P(OCCCCCCCC)=O IGJXEWFUGUJTNX-UHFFFAOYSA-N 0.000 description 1
- IOPIMTCNBFTMDS-UHFFFAOYSA-N C=[P] Chemical class C=[P] IOPIMTCNBFTMDS-UHFFFAOYSA-N 0.000 description 1
- QPPRSMODGGENNE-UHFFFAOYSA-N CCOP(=O)CCCl Chemical compound CCOP(=O)CCCl QPPRSMODGGENNE-UHFFFAOYSA-N 0.000 description 1
- MLWHWVPMTLJDQS-UHFFFAOYSA-N CCOP(=O)CO Chemical compound CCOP(=O)CO MLWHWVPMTLJDQS-UHFFFAOYSA-N 0.000 description 1
- DRSHXJFUUPIBHX-UHFFFAOYSA-N COc1ccc(cc1)N1N=CC2C=NC(Nc3cc(OC)c(OC)c(OCCCN4CCN(C)CC4)c3)=NC12 Chemical compound COc1ccc(cc1)N1N=CC2C=NC(Nc3cc(OC)c(OC)c(OCCCN4CCN(C)CC4)c3)=NC12 DRSHXJFUUPIBHX-UHFFFAOYSA-N 0.000 description 1
- MYSWFUBOALATLA-UHFFFAOYSA-N CP(=O)OCCCl Chemical compound CP(=O)OCCCl MYSWFUBOALATLA-UHFFFAOYSA-N 0.000 description 1
- 208000006558 Dental Calculus Diseases 0.000 description 1
- ZAFNJMIOTHYJRJ-UHFFFAOYSA-N Diisopropyl ether Chemical compound CC(C)OC(C)C ZAFNJMIOTHYJRJ-UHFFFAOYSA-N 0.000 description 1
- YFPJFKYCVYXDJK-UHFFFAOYSA-N Diphenylphosphine oxide Chemical compound C=1C=CC=CC=1[P+](=O)C1=CC=CC=C1 YFPJFKYCVYXDJK-UHFFFAOYSA-N 0.000 description 1
- BDAGIHXWWSANSR-UHFFFAOYSA-N Formic acid Chemical compound OC=O BDAGIHXWWSANSR-UHFFFAOYSA-N 0.000 description 1
- GYCMBHHDWRMZGG-UHFFFAOYSA-N Methylacrylonitrile Chemical compound CC(=C)C#N GYCMBHHDWRMZGG-UHFFFAOYSA-N 0.000 description 1
- CNCOEDDPFOAUMB-UHFFFAOYSA-N N-Methylolacrylamide Chemical compound OCNC(=O)C=C CNCOEDDPFOAUMB-UHFFFAOYSA-N 0.000 description 1
- IOVCWXUNBOPUCH-UHFFFAOYSA-N Nitrous acid Chemical compound ON=O IOVCWXUNBOPUCH-UHFFFAOYSA-N 0.000 description 1
- CTQNGGLPUBDAKN-UHFFFAOYSA-N O-Xylene Chemical compound CC1=CC=CC=C1C CTQNGGLPUBDAKN-UHFFFAOYSA-N 0.000 description 1
- XYFCBTPGUUZFHI-UHFFFAOYSA-N Phosphine Natural products P XYFCBTPGUUZFHI-UHFFFAOYSA-N 0.000 description 1
- NBIIXXVUZAFLBC-UHFFFAOYSA-N Phosphoric acid Chemical compound OP(O)(O)=O NBIIXXVUZAFLBC-UHFFFAOYSA-N 0.000 description 1
- 239000004952 Polyamide Substances 0.000 description 1
- CDBYLPFSWZWCQE-UHFFFAOYSA-L Sodium Carbonate Chemical compound [Na+].[Na+].[O-]C([O-])=O CDBYLPFSWZWCQE-UHFFFAOYSA-L 0.000 description 1
- 229910000831 Steel Inorganic materials 0.000 description 1
- JQALNNOQTGZTJZ-UHFFFAOYSA-N [[4,6-bis[bis(methoxymethyl)amino]-1,3,5-triazin-2-yl]-(methoxymethyl)amino]methanol Chemical compound COCN(CO)C1=NC(N(COC)COC)=NC(N(COC)COC)=N1 JQALNNOQTGZTJZ-UHFFFAOYSA-N 0.000 description 1
- FKYVWTXHUKOZMA-UHFFFAOYSA-N [butoxy(oxido)phosphaniumyl]benzene Chemical compound CCCCOP(=O)C1=CC=CC=C1 FKYVWTXHUKOZMA-UHFFFAOYSA-N 0.000 description 1
- 238000005903 acid hydrolysis reaction Methods 0.000 description 1
- 238000007259 addition reaction Methods 0.000 description 1
- 150000001298 alcohols Chemical class 0.000 description 1
- 125000001931 aliphatic group Chemical group 0.000 description 1
- 150000001338 aliphatic hydrocarbons Chemical class 0.000 description 1
- 229910001420 alkaline earth metal ion Inorganic materials 0.000 description 1
- 150000001350 alkyl halides Chemical class 0.000 description 1
- 125000002947 alkylene group Chemical group 0.000 description 1
- 150000001412 amines Chemical class 0.000 description 1
- 235000011114 ammonium hydroxide Nutrition 0.000 description 1
- 239000011260 aqueous acid Substances 0.000 description 1
- 239000007864 aqueous solution Substances 0.000 description 1
- 150000004945 aromatic hydrocarbons Chemical class 0.000 description 1
- 125000004429 atom Chemical group 0.000 description 1
- 239000011230 binding agent Substances 0.000 description 1
- 230000015572 biosynthetic process Effects 0.000 description 1
- XAVFZUKFLWOSOS-UHFFFAOYSA-N bis(dimethoxyphosphoryl)methane Chemical compound COP(=O)(OC)CP(=O)(OC)OC XAVFZUKFLWOSOS-UHFFFAOYSA-N 0.000 description 1
- 239000006227 byproduct Substances 0.000 description 1
- 239000003795 chemical substances by application Substances 0.000 description 1
- 235000015218 chewing gum Nutrition 0.000 description 1
- 238000004140 cleaning Methods 0.000 description 1
- 238000009833 condensation Methods 0.000 description 1
- 230000005494 condensation Effects 0.000 description 1
- 239000000470 constituent Substances 0.000 description 1
- 239000002178 crystalline material Substances 0.000 description 1
- 208000002925 dental caries Diseases 0.000 description 1
- 239000003599 detergent Substances 0.000 description 1
- FQSYWBNOGJDGQC-UHFFFAOYSA-N dibutyl 2-methylheptanedioate Chemical compound CCCCOC(=O)CCCCC(C)C(=O)OCCCC FQSYWBNOGJDGQC-UHFFFAOYSA-N 0.000 description 1
- MIWBXKJLAATBKH-UHFFFAOYSA-N diethyl 2-ethyl-3,3-bis(phenylphosphanyl)heptanedioate Chemical compound CCC(C(=O)OCC)C(CCCC(=O)OCC)(PC1=CC=CC=C1)PC2=CC=CC=C2 MIWBXKJLAATBKH-UHFFFAOYSA-N 0.000 description 1
- 125000004177 diethyl group Chemical group [H]C([H])([H])C([H])([H])* 0.000 description 1
- LKKOGZVQGQUVHF-UHFFFAOYSA-N diethyl heptanedioate Chemical compound CCOC(=O)CCCCCC(=O)OCC LKKOGZVQGQUVHF-UHFFFAOYSA-N 0.000 description 1
- 239000003085 diluting agent Substances 0.000 description 1
- COIZGMOWEOXWMI-UHFFFAOYSA-N dimethylphosphane;methane Chemical compound C.CPC.CPC COIZGMOWEOXWMI-UHFFFAOYSA-N 0.000 description 1
- DYEIUQNFHMLHTL-UHFFFAOYSA-N dimethylphosphoryloxymethane;methane Chemical compound C.COP(C)(C)=O DYEIUQNFHMLHTL-UHFFFAOYSA-N 0.000 description 1
- SBOQCPPINFMCBH-UHFFFAOYSA-N diphenylphosphane;methane Chemical compound C.C=1C=CC=CC=1PC1=CC=CC=C1.C=1C=CC=CC=1PC1=CC=CC=C1 SBOQCPPINFMCBH-UHFFFAOYSA-N 0.000 description 1
- 238000004821 distillation Methods 0.000 description 1
- AGWPTXYSXUNKLV-UHFFFAOYSA-N ethoxy-methyl-oxophosphanium Chemical compound CCO[P+](C)=O AGWPTXYSXUNKLV-UHFFFAOYSA-N 0.000 description 1
- 230000002349 favourable effect Effects 0.000 description 1
- 239000000835 fiber Substances 0.000 description 1
- 235000019253 formic acid Nutrition 0.000 description 1
- 150000004820 halides Chemical class 0.000 description 1
- 150000002500 ions Chemical class 0.000 description 1
- 229910052742 iron Inorganic materials 0.000 description 1
- 239000007788 liquid Substances 0.000 description 1
- 229910000103 lithium hydride Inorganic materials 0.000 description 1
- FQPSGWSUVKBHSU-UHFFFAOYSA-N methacrylamide Chemical compound CC(=C)C(N)=O FQPSGWSUVKBHSU-UHFFFAOYSA-N 0.000 description 1
- 125000000325 methylidene group Chemical group [H]C([H])=* 0.000 description 1
- 125000002560 nitrile group Chemical group 0.000 description 1
- 239000012299 nitrogen atmosphere Substances 0.000 description 1
- 239000004745 nonwoven fabric Substances 0.000 description 1
- 239000003960 organic solvent Substances 0.000 description 1
- MPQXHAGKBWFSNV-UHFFFAOYSA-N oxidophosphanium Chemical class [PH3]=O MPQXHAGKBWFSNV-UHFFFAOYSA-N 0.000 description 1
- AQSJGOWTSHOLKH-UHFFFAOYSA-N phosphite(3-) Chemical class [O-]P([O-])[O-] AQSJGOWTSHOLKH-UHFFFAOYSA-N 0.000 description 1
- ZJAOAACCNHFJAH-UHFFFAOYSA-N phosphonoformic acid Chemical class OC(=O)P(O)(O)=O ZJAOAACCNHFJAH-UHFFFAOYSA-N 0.000 description 1
- 229910000073 phosphorus hydride Inorganic materials 0.000 description 1
- 239000011505 plaster Substances 0.000 description 1
- 229920002647 polyamide Polymers 0.000 description 1
- 229920000728 polyester Polymers 0.000 description 1
- 239000002244 precipitate Substances 0.000 description 1
- 125000001453 quaternary ammonium group Chemical group 0.000 description 1
- 239000000376 reactant Substances 0.000 description 1
- 239000011541 reaction mixture Substances 0.000 description 1
- 230000001105 regulatory effect Effects 0.000 description 1
- 238000012552 review Methods 0.000 description 1
- 239000002453 shampoo Substances 0.000 description 1
- 229910000104 sodium hydride Inorganic materials 0.000 description 1
- 159000000000 sodium salts Chemical class 0.000 description 1
- 239000007858 starting material Substances 0.000 description 1
- 239000010959 steel Substances 0.000 description 1
- 238000010998 test method Methods 0.000 description 1
- YLQBMQCUIZJEEH-UHFFFAOYSA-N tetrahydrofuran Natural products C=1C=COC=1 YLQBMQCUIZJEEH-UHFFFAOYSA-N 0.000 description 1
- 229920002554 vinyl polymer Polymers 0.000 description 1
- 239000003039 volatile agent Substances 0.000 description 1
- 238000010626 work up procedure Methods 0.000 description 1
- 239000008096 xylene Substances 0.000 description 1
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07F—ACYCLIC, CARBOCYCLIC OR HETEROCYCLIC COMPOUNDS CONTAINING ELEMENTS OTHER THAN CARBON, HYDROGEN, HALOGEN, OXYGEN, NITROGEN, SULFUR, SELENIUM OR TELLURIUM
- C07F9/00—Compounds containing elements of Groups 5 or 15 of the Periodic System
- C07F9/02—Phosphorus compounds
- C07F9/28—Phosphorus compounds with one or more P—C bonds
- C07F9/38—Phosphonic acids RP(=O)(OH)2; Thiophosphonic acids, i.e. RP(=X)(XH)2 (X = S, Se)
- C07F9/40—Esters thereof
- C07F9/4003—Esters thereof the acid moiety containing a substituent or a structure which is considered as characteristic
- C07F9/4025—Esters of poly(thio)phosphonic acids
- C07F9/4046—Esters of poly(thio)phosphonic acids containing carboxylic acid or carboxylic acid derivative substituents
-
- C—CHEMISTRY; METALLURGY
- C02—TREATMENT OF WATER, WASTE WATER, SEWAGE, OR SLUDGE
- C02F—TREATMENT OF WATER, WASTE WATER, SEWAGE, OR SLUDGE
- C02F5/00—Softening water; Preventing scale; Adding scale preventatives or scale removers to water, e.g. adding sequestering agents
- C02F5/08—Treatment of water with complexing chemicals or other solubilising agents for softening, scale prevention or scale removal, e.g. adding sequestering agents
- C02F5/10—Treatment of water with complexing chemicals or other solubilising agents for softening, scale prevention or scale removal, e.g. adding sequestering agents using organic substances
- C02F5/14—Treatment of water with complexing chemicals or other solubilising agents for softening, scale prevention or scale removal, e.g. adding sequestering agents using organic substances containing phosphorus
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07F—ACYCLIC, CARBOCYCLIC OR HETEROCYCLIC COMPOUNDS CONTAINING ELEMENTS OTHER THAN CARBON, HYDROGEN, HALOGEN, OXYGEN, NITROGEN, SULFUR, SELENIUM OR TELLURIUM
- C07F9/00—Compounds containing elements of Groups 5 or 15 of the Periodic System
- C07F9/02—Phosphorus compounds
- C07F9/28—Phosphorus compounds with one or more P—C bonds
- C07F9/30—Phosphinic acids R2P(=O)(OH); Thiophosphinic acids, i.e. R2P(=X)(XH) (X = S, Se)
- C07F9/305—Poly(thio)phosphinic acids
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07F—ACYCLIC, CARBOCYCLIC OR HETEROCYCLIC COMPOUNDS CONTAINING ELEMENTS OTHER THAN CARBON, HYDROGEN, HALOGEN, OXYGEN, NITROGEN, SULFUR, SELENIUM OR TELLURIUM
- C07F9/00—Compounds containing elements of Groups 5 or 15 of the Periodic System
- C07F9/02—Phosphorus compounds
- C07F9/28—Phosphorus compounds with one or more P—C bonds
- C07F9/30—Phosphinic acids R2P(=O)(OH); Thiophosphinic acids, i.e. R2P(=X)(XH) (X = S, Se)
- C07F9/32—Esters thereof
- C07F9/3205—Esters thereof the acid moiety containing a substituent or a structure which is considered as characteristic
- C07F9/3235—Esters of poly(thio)phosphinic acids
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07F—ACYCLIC, CARBOCYCLIC OR HETEROCYCLIC COMPOUNDS CONTAINING ELEMENTS OTHER THAN CARBON, HYDROGEN, HALOGEN, OXYGEN, NITROGEN, SULFUR, SELENIUM OR TELLURIUM
- C07F9/00—Compounds containing elements of Groups 5 or 15 of the Periodic System
- C07F9/02—Phosphorus compounds
- C07F9/28—Phosphorus compounds with one or more P—C bonds
- C07F9/38—Phosphonic acids RP(=O)(OH)2; Thiophosphonic acids, i.e. RP(=X)(XH)2 (X = S, Se)
- C07F9/3804—Phosphonic acids RP(=O)(OH)2; Thiophosphonic acids, i.e. RP(=X)(XH)2 (X = S, Se) not used, see subgroups
- C07F9/3839—Polyphosphonic acids
- C07F9/3869—Polyphosphonic acids containing carboxylic acid or carboxylic acid derivative substituents
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07F—ACYCLIC, CARBOCYCLIC OR HETEROCYCLIC COMPOUNDS CONTAINING ELEMENTS OTHER THAN CARBON, HYDROGEN, HALOGEN, OXYGEN, NITROGEN, SULFUR, SELENIUM OR TELLURIUM
- C07F9/00—Compounds containing elements of Groups 5 or 15 of the Periodic System
- C07F9/02—Phosphorus compounds
- C07F9/28—Phosphorus compounds with one or more P—C bonds
- C07F9/50—Organo-phosphines
- C07F9/53—Organo-phosphine oxides; Organo-phosphine thioxides
- C07F9/5304—Acyclic saturated phosphine oxides or thioxides
- C07F9/5308—Acyclic saturated phosphine oxides or thioxides substituted by B, Si, P or a metal
- C07F9/5312—Acyclic saturated phosphine oxides or thioxides substituted by B, Si, P or a metal substituted by a phosphorus atom
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07F—ACYCLIC, CARBOCYCLIC OR HETEROCYCLIC COMPOUNDS CONTAINING ELEMENTS OTHER THAN CARBON, HYDROGEN, HALOGEN, OXYGEN, NITROGEN, SULFUR, SELENIUM OR TELLURIUM
- C07F9/00—Compounds containing elements of Groups 5 or 15 of the Periodic System
- C07F9/02—Phosphorus compounds
- C07F9/28—Phosphorus compounds with one or more P—C bonds
- C07F9/50—Organo-phosphines
- C07F9/53—Organo-phosphine oxides; Organo-phosphine thioxides
- C07F9/5329—Polyphosphine oxides or thioxides
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08K—Use of inorganic or non-macromolecular organic substances as compounding ingredients
- C08K5/00—Use of organic ingredients
- C08K5/49—Phosphorus-containing compounds
- C08K5/51—Phosphorus bound to oxygen
- C08K5/53—Phosphorus bound to oxygen bound to oxygen and to carbon only
- C08K5/5393—Phosphonous compounds, e.g. R—P(OR')2
-
- D—TEXTILES; PAPER
- D06—TREATMENT OF TEXTILES OR THE LIKE; LAUNDERING; FLEXIBLE MATERIALS NOT OTHERWISE PROVIDED FOR
- D06M—TREATMENT, NOT PROVIDED FOR ELSEWHERE IN CLASS D06, OF FIBRES, THREADS, YARNS, FABRICS, FEATHERS OR FIBROUS GOODS MADE FROM SUCH MATERIALS
- D06M13/00—Treating fibres, threads, yarns, fabrics or fibrous goods made from such materials, with non-macromolecular organic compounds; Such treatment combined with mechanical treatment
- D06M13/244—Treating fibres, threads, yarns, fabrics or fibrous goods made from such materials, with non-macromolecular organic compounds; Such treatment combined with mechanical treatment with compounds containing sulfur or phosphorus
- D06M13/282—Treating fibres, threads, yarns, fabrics or fibrous goods made from such materials, with non-macromolecular organic compounds; Such treatment combined with mechanical treatment with compounds containing sulfur or phosphorus with compounds containing phosphorus
- D06M13/288—Phosphonic or phosphonous acids or derivatives thereof
Definitions
- diphosphonates and polyphosphonates are to be used in the form of the Sn (II) salts in oral compositions for preventing tooth decay and tartar formation in oral care products, chewing gums, etc.
- esters of 3,3-diphosphonopimelic acid d.i. those di-adducts of the formula given for this purpose, in which A means only the — optionally halogen-substituted — alkyl radicals, but not H and the alkali metal or ammonium ions.
- the esters can be transesterified to other esters in a known manner.
- the free acid and the alkali and ammonium salts are obtained from the esters in a likewise known manner by acidic or alkaline saponification.
- the products obtained in this way are obtained in a suitable purity or can be easily cleaned by distillation after by-products have been removed.
- Suitable metalating agents are the alkali metals and their hydrides, in particular Li, Na, LiH, NaH.
- Strong bases such as e.g. Alkaline alcoholates, hydrides, amides, quaternary ammonium hydroxides used.
- Alkali alcoholates, alkali hydrides and amides are particularly preferred.
- the Na and K compounds are particularly preferred.
- a solvent or diluent are all organic solvents which are inert under the reaction conditions, such as aliphatic and aromatic hydrocarbons, e.g. n-pentane, n-hexane, decane, toluene, xylene, ether such as e.g. Tetrahydrofuran, diethyl ether,
- the reaction temperatures can be varied within a wide range; generally one works between about + 20 ° and + 100 ° C, especially between about + 40 ° and + 80 ° C. Since the addition reaction is exothermic, good cooling may be required.
- An excess of component III up to about 10% is possible; Larger quantities are possible, but without advantage.
- the basic catalyst e.g. sodium methylate in methanolic solution
- the basic catalyst generally about 0.01 to 0.25 mol per mol of compound II, is added.
- the reaction temperature or the reaction rate can be regulated both by external cooling and by the metering rate of the catalyst.
- the adducts I are formed in sufficient purity in accordance with the process according to the invention, so that they can be directly processed further after volatile components have been distilled off in vacuo.
- the removal of the catalyst components is expediently carried out by treatment with water / activated carbon and is necessary when using these adducts as plasticizers for PVC.
- the substituted carboxylic acids according to the invention optionally dissolved in hydrochloric acid or water, are present and can be obtained in anhydrous form by distilling off water and / or hydrochloric acid in vacuo and at temperatures up to about + 150.degree.
- Acidolysis can also be particularly advantageously analogous to the process proposed in patent application P 2719415.6 by heating with lower aliphatic.
- Carboxylic acids HCOOH, CH 3 COOH, C 2 H 5 COOH etc.
- benzoic acid HCOOH, CH 3 COOH, C 2 H 5 COOH etc.
- the compounds covered by Formula 1 can be converted into one another by known operations.
- R 2 COOH
- R 2 COOH
- R2 CN
- R2 CN
- the (substituted) carboxamides of the formula 1 can be obtained in a technically simple manner under gentle conditions by known processes from the analogous carboxylic acid nitriles by reaction with hydrogen peroxide / sodium hydroxide solution. Likewise, the reaction of the substituted carboxylic acid esters with ammonia or substituted amines at 20 ° -100 ° C, optionally under pressure, leads to the unsubstituted or substituted carboxamides.
- the compounds of the formula I are versatile, valuable products.
- the acids and salts of the formula I can be used as gypsum binders or complexing agents, in particular for metal ions such as iron or alkaline earth metal ions. They can therefore be used for water softening. Compounds with m + n + p + q ⁇ 2 are preferred for this.
- the compounds of the formula also have favorable properties as flame retardants, especially in the primer of pile carpets.
- Example (1) 10 g of a 33% are slowly added to a mixture of 114 g (0.5 mol) of diethyl methane-dimethylphosphinoxidophosphonate, 200 ml of absolute dioxane and 100 g (1.0 mol) of ethyl acrylate at 40 ° C. sodium methoxide solution dropped into methanol. After appropriate work-up, 197 g of a colorless liquid (92% of theory) remain.
- Example (3) Analogously to Example (3), 114 g (0.5 mol) of methane-dimethylphospinoxido-phosphonic acid diethyl ester in 200 ml of absolute dioxane with 53 g (1.0 mol) of acrylonitrile and 10 g of a 33% sodium methylate solution in methanol at a maximum of 60 ° C implemented. After working up, 160 g (96% of theory) of a yellowish oil remain.
- Example No. 11 As in Example No. 11, 88 g (0.25 mol) of methane-di- (phenylphosphinic acid ethyl ester), 50 g (0.5 mol) of ethyl acrylate and 2 g of 33% NaOCH 3 / CH 3 OH solution are reacted. After working up, 125 g of a yellow oil (90.5% of theory) are obtained.
- Test method Vicat method according to DIN 1168
- the squeezing effect is approx. 75%. After predrying at 100 ° ⁇ 110 ° C, the mixture is condensed at 170 ° C for 4 minutes. It is then washed with 2.3 g / l of soda for 5 minutes at 90 ° C and rinsed very well warm and cold until free of alkali and dried again at 100 ° C.
- the cotton fabric treated in this way shows very good flame-retardant properties, which are retained even after three further machine washings with 3 g / l of a commercially available detergent.
- the untreated cotton fabric continues to burn after the flame has been removed.
- the treated fabric shows a burn-in length of 6 cm after washing and 8 cm after a three-time machine wash.
- the handle After washing, the handle is soft and flowing.
- the squeezing effect on a two-roll foulard is approx. 70%. After predrying at 100 ° C, condensation is carried out at 150 ° C for 5 minutes.
- the needle punched fabric treated in this way is then dried at 145 ° C. for 30 minutes.
- the needle punched fabric shows good dimensional stability and good unrolling ability.
- the needle fleece shows very good flame retardant properties according to DIN 54 333.
- test specimen of the needle felt described above with a weight of 750 g per square meter is only treated with 300 g / l of the 40% plastic dispersion, it will continue to burn in a broad direction after the flame has been removed.
- the flame front runs through the test section of 10 cm in a time of 2 minutes and 55 seconds.
- the needle-punched non-woven fabric according to the invention does not continue to burn after the test flame has been removed. Outside the test section, an afterglow of only 8-10 seconds could be detected. After 3 shampoos, the flame retardant properties of the needle fleece are fully retained. The post-flame time increased to only 1 minute and 15 seconds.
Description
- Von russischen Autoren ist die Addition von Methandiphosphonsäuretetraäthylester an verschiedene olefinisch ungesättigte Verbindungen in Gegenwart alkalischer Katalysatoren - insbesondere von Natriumäthylat - beschrieben worden (A.N. Pudovik, G.E. Yastrebovs, Zh Obsch. Khim. 40, 499, 1970). Im Falle der Verwendung beispielsweise des Acrylnitrils als olefinisch ungesättigter Verbindung soll ein Addukt aus 1 Mol Methandiphosphonsäuretetraäthylester und 2 Mol Acrylnitril erhalten worden sein; mit anderen olefinisch ungesättigten Verbindungen wie etwa dem Vinylphosphonsäurediäthylester und dem Acrylsäuremethylester soll nur das Monoadditionsprodukt, also das Produkt aus 1 Mol Methandiphosphonsäuretetraäthylester und 1 Mol der ungesättigten Verbindung, entstanden sein. Wozu die erhaltenen Verbindungen verwendet werden, ist aus der russischen Arbeit nicht ersichtlich.
- Eine weitere russische Arbeit [T.Ya. Medved et al, Russian Chemical Reviews 44 (6), 1975, 468 bis 79] beschäftigt sich mit Alkylen-, insbesondere Methylen-diphosphin-dioxiden und mit deren Verwendung u.a. als Komplexbildner. Unter den Reaktionen des Methylen-bis-(diphenylphosphinoxids) ist u.a. die Reaktion mit Acrylsäuremethylester zu 4,4-Bis-diphenylphospinoxido-propionsäure-äthylester erwähnt.
- Mit dieser Verbindung nur entfernt ähnliche gem. Diphosphonate und Polyphosphonate sollen nach der DE-A 1 768 759 in Form der Sn(II)-Salze in oralen Zusammensetzungen zur Verhütung von Karies und Zahnsteinbildung in Mundpflegemitteln, Kaugummis etc. Verwendung finden.
- In dem Bestreben, die von den russischen Autoren beschriebene, interessant erscheinende Reaktion für synthetische Zwecke weiter auszubauen und auch sinnvolle Einsatzgebiete für die nach der Reaktion erhältlichen Verbindungen zu erschließen, wurde auch bereits vorgeschlagen (Patentanmeldung P 2647042.8 - HOE 76/F 248), unter dem Einfluß alkalischer katalysatoren ganz allgemein 1 Mol Methandiphosphonsäuretetraälkylester mit 2 Mol Acrylsäureester zur Reaktion zu bringen. Die erhaltenen Di-Addukte sind neue Phosphoncarbonsäurederivate, welche unter anderem ausgezeichnete Weichmacher für Polyvinylchlorid darstellen. Die entsprechenden freien Phosphoncarbonsäuren und ihre Salze, insbesondere die Alkali- und Ammoniumsalze, sind unter anderem wertvolle Gipsabbinde-Verzögerer und Komplexbildner für verschiedene Metallionen.
-
- Alkylreste,vorzugsweise solche mit 1-18, insbesondere solche mit 1-8,
C-Atomen, welche noch durch Halogen (vorz. CI und/oder Br) substituiert, vorzugsweise, 1-3 x substituiert sein können, - Wasserstoff,
- Alkali-(vorz. Na- und K-) und NH4-Ionen.
- Diese Verbindungen, welche als Derivate der 3,3-Diphosphonopimelinsäure aufzufassen sind, bzw. - wenn R=H- die 3,3-Diphosphonopimelinsäure selbst ist, werden nach dem in der genannten Patentanmeldung vorgeschlagenen Verfahren hergestellt durch Umsetzung von Methandiphosphonsäuretetraalkylestern der Formel
- die Reste A1' welche gleich oder verschieden sein können, die gleichen - gegebenenfalls halogensubstituierten - Alkylreste wie in der Formel der Di-Addukte für A angegeben, bedeuten,
- im Molverhältnis etwa 1:2
- in Gegenwart stark basischer Katalysatoren
- bei Temperaturen von etwa 0°-140°, vorzugsweise etwa 20°-100° und insbesondere etwa 40°-80°C.
-
- Man erhält so zunächst die Ester der 3,3-Diphosphono-pimelinsäure, d.i. diejenigen Di-Addukte der hierfür angegebenen Formel, bei denen A nur die - gegebenenfalls halogensubstituierten-Alkylreste, nicht aber H und die Alkali- oder Ammoniumionen bedeutet. Die Ester können gewünschtenfalls in bekannter Weise zu anderen Estern umgeestert werden. Die freie Säure sowie die Alkali- und Ammoniumsalze werden aus den Estern in ebenfalls bekannter Weise durch saure oder alkalische Verseifung erhalten.
- Die saure Verseifung wird besonders vorteiihaft nach dem in der Patentanmeldung P 2719415.6 = HOE 77/F 089 vorgeschlagenen Verfahren durch Erhitzen mit der mindestens etwa 6-fachen molaren Menge einer niederen aliphatischen Carbonsäure oder mit Benzoesäure, ggf. in Gegenw. katalytischer Mengen starker Säuren oder Basen, durchgeführt.
- Die saure Verseifung wird besonders vorteilhaft nach dem in der Patentanmeldung P 2719415.6 = HOE 77/F 089 vorgeschlagenen Verfahren durch Erhitzen mit der mindestens etwa 6-fachen molaren Menge einer niederen aliphatischen Carbonsäure oder mit Benzoesäure, ggf. in Gegenw. katalytischer Mengen starker Säuren oder Basen, durchgeführt.
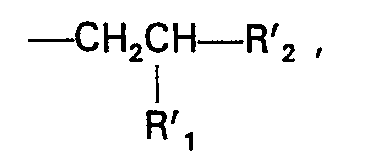
- In Fortführung der Arbeiten gemäß Patentanmeldung P 2647042.8 wurde nun durch eine weitere Variante der von den eingangs erwähnten russischen Arbeiten sowie der in der Patentanmeldung P 2647042.8 beschriebenen Reaktionen eine Anzahl neuer wertvoller phosphorhaltiger Verbindungen gefunden. Dies sind phosphorhaltige Carbonsäure-Derivate der allgemeinen Formel
- R = gleicheoder verschiedene Reste aus der Gruppe H,
- (C1-C21)-Alkyl, (C2―C8)-Alkenyl, beide gegebenenfalls substituiert, vorzugsweise bis zu dreimal, insbesondere einmal durch Halogen, insbesondere Cl, Br,
- (C5―C6)-Cycloalkyl,
- Phenyl oder Phen-(C1-C4)-alkyl, beide gegebenenfalls im Ring substituiert, vorzugsweise bis zu dreimal substituiert durch Halogen (vorzugsweise Cl, Br) oder (C1-C4)-Alkyl,
- ein Alkali- oder Ammonium-Kation, vorzugsweise Na, K,
- wobei jedoch R nicht H oder ein Kation ist, wenn das zugehörige m, n, p oder q = 0 ist,
- R, = H, (C1―C4)-Alkyl,
- R2 = CN, COOR4, CONR5R6, CONH2-x(CH2OH)x (x = 1 oder 2)
- R3 = H oder eine Gruppe
- R4 = Bedeutungen, wie für R beschrieben, hat und
- R5, R6 = H, (C1―C20)-Alkyl oder Phenyl, beide gegebenenfalls durch Halogen (vorzugsweise Cl, Br) und/oder (C1-C4)-Alkyl substituiert, vorzugsweise bis zu dreimal substituiert, und
- m, n, p, q = unabhängig voneinander die Zahlen 0 oder 1 mit der Einschränkung, daß für R2 = CN oder COOR4 nicht alle, m, n, p, q = 1 sein dürfen sowie daß für dne Fall R = C6H5 und m=n=p=q R3≠H.
- Bevorzugt sind, R, R4, R5, R6 = H oder Alkylgruppen.
- Bevorzugt sind unter den für die Reste R bis R6 genannten Alkylgruppen solche mit 1-4 C-Atomen, insbesondere Methyl und Aethyl sowie CI-Aethyl.
- Bevorzugt als Reste R2 bzw. R'2 sind CN, CONH2 und CONH2-x(CH2OH)x.
- Von den unter die Formel I fallenden Verbindungen werden in beispielhafter Weise folgende genannt:
- 3,3-Di-(methylphosphinsäureäthylester)-pimelinsäuredimethylester
- 3,3-Di-(2-chloräthylphosphinsäureäthylester)-pimelinsäuredi-isopropylester
- 3,3-Di-(phenylphosphinsäureäthylester)-pimelinsäuredi-n-oktylester
- 3,3-Di-(methylphosphinsäure-2-chloräthylesterl-pimelinsäurediäthylester
- 3,3-Di(methylphospinsäure-isobutylester)-pimelinsäuredi-decylester
- 3,3-Di-(phenylphosphinsäure-n-oktylester)-pimelinsäuredi-n-oktylester
- 3-Dimethylphosphinoxido-3-diäthylphosphono-pimelinsäuredimethylester
- 3-Diphenylphosphinoxido-3-diäthylphosphono-pimelinsäuredi-laurylester
- 3-Diphenylphosphinoxido-3-methylphosphinsäuremethyl-pimelinsäuredi-n-butylester
- 3-Dimethylphosphinoxido-3-phenylphosphinsäuremethyl-pimelinsäuredi-cetylester
- 3,3-Bis-dimethylphosphinoxido-pimelinsäuredilaurylester
- 3,3-Di-(methylphosphinsäureäthylester)-pimelinsäuredinitril
- 3,3-Di-(phenylphosphinsäure-n-butylester)-pimelinsäuredinitril
- 3-Diphenylphosphinoxido-3-dimethylphosphono-pimelinsäuredinitril
- 3-Dimethylphospinoxido-3-phenylphosphinsäure-n-butylester-pimelinsäuredinitril
- 3,3-Bis-diphenylphosphinoxido-pimelinsäuredinitril
- 3-Dimethyl-3-diphenylphosphinoxidopimelinsäuredinitril
- 3,3-Bis-(diäthylphosphono)-pimelinsäuredicarbonamid
- 3,3-Bis-(di-2-chloräthylphosphono)-pimelinsäure-N-methylcarbonamid
- 3,3-Bis-(diäthylphosphono)-pimelinsäuredi-N-phenylcarbonamid
- 3,3-Di-(methylphosphinsäureäthylester)-pimelinsäuredicarbonamid
- 3-Dimethylphosphinoxido-3-diäthylphosphono-pimelinsäuredicarbonamid
- 3-Diphenylphosphinoxido-3-phenylphosphinsäuremethylester-pimelinsäuredicarbonamid
- 3,3-Di-methylphospino-pimelinsäure
- 3-Methylphosphino-3-dimethylphosphinoxidopimelinsäure
- 3,3-Bis-(dimethylphosphinoxido)-pimelinsäure
- 3-Methylphosphino-3-phosphono-pimelinsäure
- 3-Dimethylphosphinoxido-3-phosphono-pimelinsäure
- 1 -Carbäthoxypropan-3,3-di-methylphosphinsäuremethylester
- 1-Carbäthoxypropan-3-diphenylphosphinoxido-3-phenylphosphinsäureäthylester
- 1-Carbonamidopropan-3-diäthylphosphono-3-dimethylphosphinoxid.
-
- Die neuen phosphorhaltigen Carbonsäurederivate werden erfindungsgemäß dadurch hergestellt, daß man Verbindungen der allgemeinen Formel
- Die als Ausgangsstoffe der Reaktion zu verwendenden Methylenverbindungen der allgemeinen Formel II (Me = H) können nach unterschiedlichen literaturbekannten Verfahren synthetisiert werden, z.B.
- a) durch Umsetzung von Trialkylphosphiten oder Alkyl-(Aryl)-phosphonigsäuredialkylestern mit Halogenmethanphosphinsäurealkyl-(aryl-)estern oder Halogenmethanphosphonsäureestern oder tertiären Halogenmethylphosphinoxiden unter Abspaltung der entsprechenden Alkylhalogenide, oder
- b) durch Reaktion von Alkalidialkyl-(aryl-)phosphiten bzw. Alkalidialkyl-(aryl-)phosphinoxiden mit Halogenmethanphosphonsäurediestern, Halogenmethanphosphinsäureestern und tertiären Halogenmethylphosphinoxiden unter Eliminierung der Alkalihalogenide.
- Die auf diese Weise erhaltenen Produkte fallen in geeigneter Reinheit an oder lassen sich nach Entfernung von Nebenprodukten destillativ leicht reinigen.
- Als Beispiele für Methylenphosphorverbindungen der Formel II seien im einzelnen genannt:
- Methandiphosphonsäuretetramethylester, -tetraäthylester, -tetra-2-chloräthylester, -tetrahexylester,
- Methan - bis - methylphosphinsäuremethylester, -bis - methylphosphinsäure - 2 - chloräthylester, -bisphenylphosphinsäure-isobutylester,
- Methanphosphonsäure-diäthyl-methylphosphinsäureester, -dihexylphenylphosphinsäure-2-chloräthylester,
- Methan - dimethylphosphinoxido - phosphonsäuredimethylester, -diphenylphosphinoxido - phosphonsäure-di-2-chloräthylester,
- Methan - dimethylphosphinoxido - methylphosphinsäureäthylester, -diphenylphosphinoxidophenylphosphinsäure-isobutylester,
- Methan-bis-dimethylphosphinoxid,
- Methan-bis-diphenylphosphinoxid.
- Zur Herstellung von Verbindungen der Formel II mit Me = Alkali werden die so erhaltenen Verbindungen in an sich bekannter Weise an der Methangruppierung metalliert. Geeignete Metallierungsmittel sind die Alkali-Metalle und ihre Hydride, insbesondere Li, Na, LiH, NaH.
- Die bei der Durchführung der Reaktion einzusetzenden olefinisch ungesättigten Verbindungen der allgemeinen Formel III sind bekannt und werden z.T. großtechnisch hergestellt. Als Beispiele seien im einzelnen genannt:
- Acrylsäuremethylester, -äthylester, -isopropylester, -nitril, Methacrylsäurenitril, Acrylsäureamid, Methacrylsäureamid.
- Als Reaktionskatalysatoren werden starke Basen wie z.B. Alkalialkoholate, -hydride, -amide, quartäre Ammoniumhydroxyde eingesetzt. Bevorzugt sind vor allem Alkalialkoholate, ferner Alkalihydride und -amide. Insbesondere bevorzugt sind die Na- und die K-Verbindungen. Bei Verwendung von Verbindungen der Formel II mit Me = Alkali erübrigt sich die Verwendung weiterer basischer Katalysatoren.
- Die erfindungsgemäße Umsetzung kann sowohl in Abwesenheit als auch in Gegenwart eines Lösungs- oder Verdünnungsmittels durchgeführt werden; geeignet als Lösungsmittel sind alle unter den Reaktionsbedingungen inerten organischen Lösungsmittel wie aliphatische und aromatische Kohlenwasserstoffe, z.B. n-Pentan, n-Hexan, Decan, Toluol, Xylol, Aether wie z.B. Tetrahydrofuran, Di- äthyläther, Diisopropyläther, Dioxan, und für Me = H auch Alkohole wie z.B. Methanol, Aethanol, Isopropanol.
- Die Reaktionstemperaturen können in einem größeren Bereich variiert werden; im allgemeinen arbeitet man zwischen etwa +20° und +100°C, speziell zwischen etwa +40° und +80°C. Da die Additionsreaktion exotherm verläuft, ist unter Umständen eine gute Kühlung erforderlich.
- Bei der Durchführung des erfindungsgemäßen Verfahrens werden die Reaktionspartner (11) und (111) vorzugsweise im Verhältnis von ca. 1:2 (Me = H) oder 1:1 (Me = Alkali) gemischt. Ein Überschuß der Komponente III bis ca. 10% ist möglich; größere Mengen sind möglich, aber ohne Vorteil. Anschließend wird (für Me = H) der basische Katalysator (z.B. Natriummethylat in methanolischer Lösung), im allgemeinen ca. 0,01 bis 0,25 Mol pro Mol Verbindung II, zugegeben.
- Die Reaktionstemperatur bzw. die Reaktionsgeschwindigkeit kann sowohl durch Außenkühlung als auch durch die Dosiergeschwindigkeit des Katalysators reguliert werden.
- Die Addukte I werden gemäß dem erfindungsgemäßen Verfahren in genügender Reinheit gebildet, so daß sie - nach Abdestillieren flüchtiger Anteile im Vakuum - direkt weiterverarbeitet werden können.
- Die Entfernung der Katalysatoranteile, insbesondere bei den langkettigen Carbonsäureestern erfolgt zweckmäßigerweise durch Behandeln mit Wasser/Aktivkohle und ist erforderlich bei der Verwendung dieser Addukte als Weichmacher für PVC. Die Verseifung der erhaltenen Verbindungen mit Me = Alkali zu den entsprechenden N-Verbindungen erfolgt in an sich bekannter Weise durch Behandeln mit Wasser oder wäßriger Säure. Diese Addukte mit Me=4 lassen sich mit einem weiteren Mol III in weitere Verbindungen 1* Die Überführung der Addukie (R2=CN, COOR4) im die substituierten Carbonsäuren erfolgt nach an sich bekannten Verfahren z.B. durch längere Einwirkung von wasserfreiem Chlorwasserstoff bei Temperaturen von etwa 130° bis 160°C, gegebenenfalls unter Druck, durch längeres Kochen mit wäßriger Salzsäure unter Rückflußbedingungen bei Temperaturen von etwa +70° bis +110°C, oder durch Umsetzung mit mindestens der stöchiometrisch erforderlichen Menge Wasser in Gegenwart der freien Säuren bei Temperaturen von etwa 160° bis 250°C unter Abdestillieren der gebildeten flüchtigen Anteile.
- Nach beendeter Acidolyse liegen die erfindungsgemäßen substituierten Carbonsäuren, gegebenenfalls gelöst in Salzsäure oder Wasser, vor und können durch Abdestillieren von Wasser und/oder Salzsäure im Vakuum und bei Temperaturen bis zu etwa +150°C in wasserfreier Form erhalten werden.
- Besonders vorteilhaft kann die Acidolyse auch analog dem in der Patentanmeldung P 2719415.6 vorgeschlagenen Verfahren durch Erhitzen mit niederen aliphat. Carbonsäuren (HCOOH, CH3COOH, C2H5COOH etc.) oder mit Benzoesäure durchgeführt werden.
- Die wäßrig-alkalische Verseifung der Ester der Formel I führt in an sich bekannter Weise zu den Salzen der Formel I (R, R4=Alkali, Ammonium), wobei auch eine stufenweise Verseifung möglich ist. Die unter die Formel 1 fallenden Verbindungen sind durch bekannte Operationen ineinander überführbar.
- Die im Formelbild I dargestellten substituierten Carbonsäuren (d.h. R2 = COOH) lassen sich z.B. durch saure Hydrolyse der Nitrile (R2 = CN) darstellen. Es ist jedoch schwierig, selektiv eine Hydrolyse der Nitrilgruppe durchzuführen, ohne daß gleichzeitig eine Hydrolyse der Phosphondiester- bzw. Phosphinestergruppierung erfolgt. Vorteilhaft wählt man deshalb ein Verfahren, das den Weg über das entsprechende Carbonsäureamid und die nachfolgende Behandlung mit salpetriger Säure nach dem folgenden Schema erforderlich macht:
- Die (substituierten) Carbonsäureamide der Formel 1 lassen sich in technisch einfacher Weise unter schonenden Bedingungen nach an sich bekannten Verfahren aus den analogen Carbonsäurenitrilen durch Umsetzung mit Wasserstoffperoxid/Natronlauge erhalten. Gleichfalls führt auch die Umsetzung der substituierten Carbonsäureester mit Ammoniak bzw. substituierten Aminen bei 20°―100°C, gegebenenfalls unter Druck, zu den unsubstituierten bzw. substituierten Carbonsäureamiden.
- Diese Produkte fallen durch diese Operation in hoher Reinheit an und können direkt weiterverwendet werden.
- Die Verbindungen der Formel I sind vielseitig verwendbare wertvolle Produkte. Die Ester der Formel 1 (wobei R und R4=die in der Legende zur Formel angegebenenorganischen Reste sind), insbesondere die langkettigen, lassen sich als Weichmacher für Kunststoffe, insbesondere für Polyvinyl- * überführen
chlorid, verwenden. Sie verleihen den so dotierten Massen zudem ausgezeichnete flammhemrr.ande bzw. selbstverlöschende Eigenschaften. - Die Säuren und Salze der Formel I (R und R4 = H, Alkali- und/oder Ammoniumionen) sind verwendbar als Gipsabbindemittel oder Komplexierungsmittel, insbesondere für Metallionen wie Eisen-oder Erdalkali-ionen. Sie können daher für die Wasserenthärtung eingesetzt werden. Bevorzugt sind hierfür Verbindungen mit m+n+p+q≧2.
- Auch als flammhemmende Mittel, insbesondere im Vorstrich von Florteppichen, besitzen die Verbindungen der Formel günstige Eigenschaften.
- Insbesondere sind jedoch die am Phosphor veresterten oder alkylierten Carbonsäureamide, bevorzugt in mono- oder di-methylolysierter Form, wenn in Formel I R = ggf. halogensubst. (C1-C20)-, vorzugsweise (C1-C4)-Alkylreste und R2 sowie ggf. auch R2'= CONH2-x(CH2OH)x (x = 1 oder 2), verwendbar für flammhemmende Ausrüstungen von cellulosehaltigem Material, insbesondere Textilien.
- Die folgenden Beispiele sollen der weiteren Erläuterung der Erfindung dienen, ohne diese jedoch in irgendeiner Weise zu beschränken.
-
- Zu einer Mischung aus 128 g (0,5 Mol) Methan-di-(methylphosphinsäure-isopropylester) und 86 g (1,0 Mol) Acrylsäuremethylester werden bei Raumtemperatur unter Rühren langsam 5 g einer 33%igen Natriummethylatlösung in Methanol eingetropft. Die Reaktion verläuft exotherm. Durch Kühlung wird die Innentemperatur auf maximal +60°C begrenzt. Nach beendetem Zutropfen wird das Gemisch noch 5 Stunden auf +60°C gehalten und dann im Vakuum von flüchtigen Anteilen befreit. Ausbeute: 205 (96% d. Th.).
-
- Entsprechend dem Beispiel (1) werden zu einer Mischung aus 114 g (0,5 Mol) Methan-dimethylphosphinoxido-phosphonsäure-diäthylester, 200 ml absolutem Dioxan und 100g (1,0 Mol) Acrylsäureäthylester bei 40°C langsam 10 g einer 33%igen Natriummethylatlösung in Methanol eingetropft. Nach entsprechender Aufarbeitung verbleiben 197 g einer farblosen Flüssigkeit (92% d. Th.).
-
- Zu einer Mischung aus 128 g (0,5 Mol) Methan-di-(methylphosphinsäure-isopropylester), 100 ml absolutem Toluol und 53 g (1,0 Mol) Acrylnitril werden bei Raumtemperatur unter Rühren langsam 5 g einer 33%igen Natriummethylatlösung in Methanol getropft. Die Reaktion verläuft stark exotherm. Die Innentemperatur wird durch Kühlung auf maximal +60°C gehalten. Anschließend wird noch 1 Stunde bei +50°C nachgerührt und im Vakuum andestilliert. Der verbleibende Rückstand wird nach Aufnehmen in 200 ml Chloroform mit etwas Aktivkohle behandelt, die Lösung filtriert und das Lösungsmittel im Vakuum entfernt. Es verbleiben 172 g eines farblosen Oeles (95% d. Th.), welches langsam kristallisiert.
-
- Analog dem Beispiel (3) werden 114 g (0,5 Mol) Methan-dimethylphospinoxido-phosphonsäurediäthylester in 200 ml absolutem Dioxan mit 53 g (1,0 Mol) Acrylnitril und 10 g einer 33%igen Natriummethylatlösung in Methanol bei maximal 60°C umgesetzt. Nach Aufarbeitung verbleiben 160 g (96% d. Th.) eines gelblich gefärbten Oeles.
-
- In eine Mischung aus 181 g (0,5 Mol) 3,3-Di-(methylphosphinsäureisopropylester)-pimelinsäuredinitril, 500 ml 95%igem Aethanol und 40 ml 6n Natronlauge werden innerhalb von 60 Minuten 400 ml 30%ige H102-Lösung eingetropft. Die Reaktion verläuft exotherm, durch außenkühlung wird die Temperatur unter +35°C gehalten. Anschließend wird noch 3 Stunden bei Raumtemperatur nachgerührt. Nach dem Neutralisieren mit Eisessig wird die Lösung filtriert und das Filtrat im Vakuum vom Lösungsmittel befreit. Der verbleibende Rückstand wird mit 200 ml Aceton heiß ausgerührt. Der verbleibende Festkörper wird abgetrennt und getrocknet. Ausbeute: 170 g Festkörper (85% d. Th.); Fp. 117°-120°C.
-
- In eine Mischung aus 197 g (0,5 Mol) 3,3-Di-(phosphonodiäthyl)-pimelinsäuredinitril, 550 ml 95%igem Aethanol und 40 ml 6n Natronlauge werden innerhalb von 60 Minuten 400 ml 30%ige H202-Lösung eingetropft. Die Reaktion verläuft exotherm, durch Außenkühlung wird die Temperatur unter +35°C gehalten. Anschließend wird noch 3 Stunden bei Raumtemperatur nachgerührt. Nach dem Neutralisieren mit Eisessig wird die Lösung filtriert und das Filtrat im Vakuum vom Lösungsmittel befreit, der verbleibende Rückstand wird mit 200 ml Aceton heiß ausgerührt. Der verbleibende Festkörper wird abgetrennt und getrocknet. Ausbeute: 168 g (78% d. Th.); Fp. 202°-204°C.
-
- In eine auf 0°C gehaltene gekühite Lösung von 230 g (0,5 Mol) 3,3-Di-(phosphonodiäthyl)-pimelinsäuredimethylester werden langsam 25,5 g (1,5 Mol) Ammoniak eingeleitet. Das Reaktionsgemisch wird nach dem Ueberführen in einen Stahlautoklaven 20 Stunden auf 55°-60°C erwärmt. Nach dem Abkühlen wird das Lösungsmittel im Vakuum entfernt und der verbleibende Rückstand mit 200 ml Aceton ausgekocht. Der ausfallende Festkörper wird abgetrennt und getrocknet. Ausbeute: 183 g (% d. Th.); Fp. 204°-205°C.
-
- 428 g (1,0 Mol) 3,3-Di-(methylphosphinsäure-isopropylester)-pimelinsäuredimethylester werden mit 2000 ml konzentrierter Salzsäure 15 Stunden unter Rückflußbedingungen gekocht. Flüchtige Anteile werden anschließend im Vakuum abgezogen, der Rückstand mit 500 ml Eisessig versetzt und auf Raumtemperatur gekühlt. Nach ca. 10-stündigem Stehen wird das kristalline Material abgetrennt und getrocknet. Ausbeute: 281 g (89% d. Th.); Fp. 187°-190°C.
-
- 214 g (0,5 Mol) 3-Dimethylphospinoxido-3-diäthylphosphono-pimelinsäurediäthylester werden mit 1000 ml konzentrierter Salzsäure 20 Stunden unter Rückflußbedingungen gekocht. Anschließend werden flüchtige Anteile am Rotationsverdampfer im Vakuum bei 120°C entfernt. Als Rückstand verbleibt eine glasig erstarrende Masse, die nach mehrfachem Auskochen mit Isopropanol kristallisiert: Der Festkörper wird abgetrennt und getrocknet. Ausbeute: 140 g (88,6% d. Th.); Fp. 128°-130°C.
-
- Zu einer Mischung aus 99 g (0.5 Mol) Methandimethylphosphinoxidomethylphosphinsäureäthylester, 100 m abs. Toluol und 53 g (1.0 Mol) Acrylnitril werden bei Raumtemperatur unter Rühren langsam 5 g einer 33%igen NaOCH3/CH30H-Lösung getropft. Durch Außenkühlung wird die stark exotherme Addition auf maximal +60°C gehalten. Anschließend wird noch 1 Stunde bei 50°C nachgerührt, durch Zugabe von Aktivkohle geklärt und filtriert. Das Filtrat wird im Vakuum vom Lösungsmittel und flüchtigen Anteilen befreit. Es verbleiben 140 g (92% d. Th.) eines leicht gelblichen Öles.
-
- Zu einer Mischung aus 99 g (0.5 Mol) Methandimethylphosphinoxidomethylphosphinsäureäthylester und 100 g (1.0 Mol) Acrylsäureäthylester werden bei Raumtemperatur langsam unter Rühren 5 g einer 33%igen Natriumethylatlösung in Methanol eingetropft. Die Reaktion verläuft stark exotherm und wird durch Außenkühlung auf maximal +50°C begrenzt. Nach dem Zutropfen wird das Gemisch noch 5 Stunden bei 80-90°C gerührt und dann im Vakuum von flüchtigen Anteilen befreit. Ausbeute 190 g (95,4% d. Th.).
-
- 199 g (0.5 Mol) 3-Dimethylphosphinoxido-3-methylphosphinoäthylpimelinsäurediäthylester werden mit 1000 ml konz. Salzsäure 20 Stunden unter Rückfluß gekocht. Anschließend werden flüchtige Anteile am Rotationsverdampfer im Vakuum bei maximal +120°C entfernt. Der verbleibende glasartige Rückstand wird in 500 ml Methanol aufgenommen und durch Zugabe von 82 g 33%iger NaOCH3/CH3OH-Lösung in das Natriumsalz überführt. Nach Einengen der Lösung wird das ausgefallene Produkt abgesaugt und getrocknet. Ausbeute 150 g (89% d. Th.).
-
-
-
-
-
- Wie vorstehend mehrfach beschrieben wurden 88 g (0.25 Mol) Methandiphenylphosphinoxidophosphonosäurediäthylester, 26,5 g (0.5 Mol) Acrylnitril mit 2 g 33%iger NaOCH3/CH3OH-Lösung in 100 ml abs. Toluol umgesetzt. Nach Aufarbeitung erhält man 100 g (87,3% d. Th.) eines farblosen Öles, das nach längerem Stehem erstarrt.
-
- Zu einem Gemisch aus 12 g (0.5 Mol) NaH in 200 ml abs. Toluol werden in einer Stickstoffatomosphäre bei Raumtemperatur langsam 114 g (0.5 Mol) Methan-dimethylphosphinoxidophosphonsäurediäthylester getropft. Das Gemisch wird anschließend solange bei Raumtemperatur gerührt, bis das NaH umgesetzt ist. Anschließend werden langsam 50 g (0.5 Mol) Acrylsäureäthylester under Außenkühlung bei 40-50°C eingetropft. Nach 2-stündigem Rühren bei 50°C wird das Gemisch durch vorsichtiges Eintropfen von konz. Salzsäure neutral gestellt und filtriert. Das Filtrat wird im Vakuum von flüchtigen Anteilen befreit und liefert 130 g (97% d. Th.) eines farblosen Öles.
- Prüfmethode: Vicat-Methode nach DIN 1168
-
- Ein Baumwollgewebe, köperbindig, mit einem Quadratmetergewicht von 240 g, wird auf einem Zweiwalzenfoulard mit folgender Imprägnierlösung behandelt:
- 450 g/I eines Umsetzungsproduktes von 2 Molen Formaldehyd mit 3,3-Di-(phosphonidiäthyl)-pimelinsäuredicarbonamid (das Produkt enthält 9,8% Phosphor)
- 60 g/1 Trimethylolmelamintrimethyläther (80%ig)
- 5 g/I Ammoniumchlorid.
- Der Abquetscheffekt beträgt ca. 75%. Nach einer Vortrocknung bei 100°―110°C wird 4 Minuten bei 170°C kondensiert. Anschließend wird mit 2,3 g/I Soda 5 Minuten bei 90°C nachgewaschen und sehr gut warm und kalt bis zur Alkalifreiheit gespült und wieder bei 100°C getrocknet.
- Das so behandelte Baumwollgewebe zeigt sehr gute flammhemmende Eigenschaften, die auch nach drei weiteren Maschinenkochwäschen mit 3 g/I eines handelsüblichen Waschmittels erhalten bleiben.
- Nach DIN 53 906 brennt das unbehandelte Baumwollgewebe nach Wegnahme der Flamme weiter. Das behandelte Gewebe zeigt eine Einbrennlänge von 6 cm nach der Nachwäsche und 8 cm nach einer dreifachen Maschinenkochwäsche.
- Der Warengriff ist nach der Nachwäsche weich und fließend.
- Das im Beispiel 1 beschriebene Baumwollgewebe wird mit nachstehender Impränierlösung behandelt:
- 380 g/I eines Ammoniumsalzes der 3,3-Di-(methylphosphino)-pimelänsäure (P = 11 %)
- 40 g/I Hexamethylolmelaminpentamethyläther (50%ig)
- 3 g/I Ammoniumchlorid.
- Der Abquetscheffekt auf einem Zweiwalzenfoulard beträgt ca. 70%. Nach der Vortrocknung bei 100°C wird 5 Minuten bei 150°C kondensiert.
- Das behandelte Baumwollgewebe zeigt nach DIN 53 906 einen sehr guten flammhemmenden Effekt. Die Einbrennlänge beträgt 5 cm. Der Flammhemmende Effekt überdauert 5 chemische Reinigungen. Zu gleich guten Effekten kommt man, wenn man
- 450 g/I 3-Dimethylphosphinoxido-3-diäthylphosphono-pimelinsäure dinitril einsetzt.
- Eine Nadelvliesauslegeware, die aus einem Polyesterfaserkern und aus einer Polyamidlauffläche im Mischungsverhältnis 65:35 besteht, wird auf einem Zweiwalzenfoulard (Abquetscheffekt ca. 105%) mit einer wäßrigen Lösung folgender Zusammensetzung behandelt:
- 400 g/I eines Umsetzungsproduktes von 2,0 Molen Formaldehyd mit 3,3-Di-(phosphonodiäthyl)-pimelinsäure dicarbonamid (das Produkt enthält 9,8% Phosphor),
- 50 g/I Trimethylolmelamintrimethyläther (80%ig)
- 5 g/I Ammoniumchlorid
- 300 g/I einer 40%igen Kunststoffdispersion aus Äthylacrylat/Acrylnitril/N-Methylolacrylamid im Verhältnis 6:3:1.
- Die so behandelte Nadelvliesauslegeware wird anschließend 30 Minuten bei 145°C getrocknet.
- Die Nadelvliesauslegeware zeigt eine gute Formstabilität und ein gutes Abrollvermögen.
- Der Nadelvlies zeigt nach DIN 54 333 sehr gute flammhemmende Eigenschaften.
- Wird ein Prüfling des oben beschriebenen Nadelvlieses mit einem Quadratmetergewicht von 750 g nur mit 300 g/I der 40%igen Kunststoffdispersion behandelt, so brennt er nach Wegnahme der Flamme in breiter Front weiter. Die Flammfront durchläuft in einer Zeit von 2 Minuten und 55 Sekunden die Prüfstrecke von 10 cm.
- Die erfindungsgemäß ausgerüstete Nadelvliesauslegeware brennt dagegen nach Wegnahme der Prüfflamme nicht weiter. Außerhalb der Prüfstrecke konnte lediglich ein Nachflammen von 8-10 Sekundenfestgestellt werden. Nach 3 Shampoonierungen bleiben die flammhemmenden Eigenschaften des Nadelvlieses voll erhalten. Die Nachflammzeit hat sich lediglich auf 1 Minute und 15 Sekunden erhöht.
Claims (8)
Me Wasserstoff oder ein Alkaliatom (vorzugsweise Li, Na) bedeutet, gegebenenfalls in einem inerten Lösungsmittel mit Verbindungen der Formel
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| CH729977 | 1977-06-14 | ||
| CH7299/77 | 1977-06-14 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| EP0000061A1 EP0000061A1 (de) | 1978-12-20 |
| EP0000061B1 true EP0000061B1 (de) | 1980-10-15 |
Family
ID=4322957
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| EP78100104A Expired EP0000061B1 (de) | 1977-06-14 | 1978-06-06 | Phosphorhaltige Carbonsäure-Derivate, Verfahren zu deren Herstellung, sowie ihre Verwendung |
Country Status (4)
| Country | Link |
|---|---|
| EP (1) | EP0000061B1 (de) |
| JP (1) | JPS545922A (de) |
| DE (1) | DE2860216D1 (de) |
| IT (1) | IT1096642B (de) |
Families Citing this family (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| DE3027040A1 (de) * | 1980-07-17 | 1982-02-25 | Hoechst Ag, 6000 Frankfurt | Dimethylphosphinyl-alkanphosphonsaeuren, ein verfahren zu ihrer herstellung und ihre verwendung als gipsabbindeverzoegerer |
| DE3225469A1 (de) * | 1982-07-05 | 1984-01-05 | Schering AG, 1000 Berlin und 4709 Bergkamen | Diphosphonsaeure-derivate und diese enthaltende pharmazeutische praeparate |
| DE3512536A1 (de) * | 1985-04-06 | 1986-10-16 | Boehringer Mannheim Gmbh, 6800 Mannheim | Neue diphosphonsaeure-derivate, verfahren zu deren herstellung und diese verbindungen enthaltende arzneimittel |
| GB9615497D0 (en) | 1996-07-24 | 1996-09-04 | Exxon Chemical Patents Inc | Materials for use in oils and processes for their manufacture |
| WO2003021031A1 (en) * | 2001-09-01 | 2003-03-13 | Rhodia Consumer Specialties Limited | Phosphorus compounds |
Family Cites Families (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| DE1768759A1 (de) * | 1968-06-27 | 1972-01-13 | Procter & Gamble | Zinnsalze von Phosphonsaeuren |
| DE2602030C2 (de) * | 1976-01-21 | 1983-12-01 | Henkel KGaA, 4000 Düsseldorf | Diphosphonoalkancarbonsäuren und Verfahren zu deren Herstellung |
| NL7711307A (nl) * | 1976-10-19 | 1978-04-21 | Hoechst Ag | Fosforcarbonzuurverbindingen en hun bereiding. |
-
1978
- 1978-06-06 DE DE7878100104T patent/DE2860216D1/de not_active Expired
- 1978-06-06 EP EP78100104A patent/EP0000061B1/de not_active Expired
- 1978-06-12 IT IT24481/78A patent/IT1096642B/it active
- 1978-06-13 JP JP7046378A patent/JPS545922A/ja active Pending
Also Published As
| Publication number | Publication date |
|---|---|
| IT7824481A0 (it) | 1978-06-12 |
| DE2860216D1 (en) | 1981-01-22 |
| EP0000061A1 (de) | 1978-12-20 |
| IT1096642B (it) | 1985-08-26 |
| JPS545922A (en) | 1979-01-17 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| EP1217004B1 (de) | Verfahren zur Herstellung von Ethan-1,2-bis(alkylphosphinsäuren) | |
| DE2337289A1 (de) | Verfahren zur herstellung von n-phosphonomethylglycin | |
| EP0044470B1 (de) | Dimethylphosphinyl-alkanphosphonsäuren, ein Verfahren zu ihrer Herstellung und ihre Verwendung als Gipsabbindeverzögerer | |
| DE2423881C2 (de) | Verfahren zur Herstellung von Phosphonomethylenaminocarbonsäureverbindungen | |
| EP0000061B1 (de) | Phosphorhaltige Carbonsäure-Derivate, Verfahren zu deren Herstellung, sowie ihre Verwendung | |
| EP1016623A2 (de) | Verfahren zur Herstellung von Phosphinsäuren | |
| DE855567C (de) | Verfahren zur Herstellung von insektiziden Phosphorverbindungen | |
| DE1668707A1 (de) | Verfahren zur Herstellung von Phosphonoalkylenammoniumverbindungen | |
| EP1219627B1 (de) | Verfahren zur Herstellung von Ethylen-1,2-diphosphonsäuren | |
| CH617206A5 (en) | Process for the preparation of phosphonic and phosphinic acids. | |
| DE2511932C2 (de) | Verfahren zur Herstellung von tert.-Hydroxyalkylphosphinoxiden | |
| EP0170034B1 (de) | Verfahren zur Herstellung von Chlor-phenyl-phosphanen | |
| EP0144743B1 (de) | Verfahren zur Herstellung organischer Chlorphosphane | |
| DE1184758B (de) | Verfahren zur Herstellung von Azo-bis-alkylphosphonaten und den entsprechenden Saeuren | |
| EP0047461A1 (de) | Verfahren zur Herstellung von Vinylphosphonsäurederivaten | |
| EP0038466B1 (de) | Verfahren zur Herstellung von Vinylphosphonsäurederivaten | |
| DE942149C (de) | Verfahren zur Herstellung substituierter Glycinamide | |
| DE4416018A1 (de) | Verfahren zur Herstellung von Vinylphophonsäuren | |
| DE1793778C3 (de) | Neues sekundäres Phosphinoxyd | |
| DE2313355A1 (de) | Hydroxyalkan(thio)-phosphonsaeureester und hydroxyalkyl(thio)-phosphinsaeureester sowie verfahren zu deren herstellung | |
| DE1216278B (de) | Verfahren zur Herstellung von unsymmetrischen Phosphorigsaeure-O, O-diestern | |
| DE2647042A1 (de) | Neue phosphoncarbonsaeureverbindungen | |
| DE1943577A1 (de) | Verfahren zur Herstellung von Polyphosphinsaeuren und deren Estern und Salzen | |
| DE1257153B (de) | Verfahren zur Herstellung von neuen basischen Estern der phosphorigen, phosphonigen oder phosphinigen Saeure | |
| DE3046221A1 (de) | Verfahren zur herstellung von verbindungen mit einer p=n-p-gruppierung |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| PUAI | Public reference made under article 153(3) epc to a published international application that has entered the european phase |
Free format text: ORIGINAL CODE: 0009012 |
|
| AK | Designated contracting states |
Kind code of ref document: A1 Designated state(s): BE CH DE FR GB NL |
|
| 17P | Request for examination filed | ||
| GRAA | (expected) grant |
Free format text: ORIGINAL CODE: 0009210 |
|
| AK | Designated contracting states |
Kind code of ref document: B1 Designated state(s): BE CH DE FR GB NL Designated state(s): BE CH DE FR GB NL |
|
| PG25 | Lapsed in a contracting state [announced via postgrant information from national office to epo] |
Ref country code: CH Effective date: 19801015 |
|
| REF | Corresponds to: |
Ref document number: 2860216 Country of ref document: DE Date of ref document: 19810122 |
|
| PG25 | Lapsed in a contracting state [announced via postgrant information from national office to epo] |
Ref country code: BE Effective date: 19810606 |
|
| PG25 | Lapsed in a contracting state [announced via postgrant information from national office to epo] |
Ref country code: NL Effective date: 19820101 |
|
| REG | Reference to a national code |
Ref country code: CH Ref legal event code: PL |
|
| NLV4 | Nl: lapsed or anulled due to non-payment of the annual fee |
Effective date: 19820101 |
|
| PG25 | Lapsed in a contracting state [announced via postgrant information from national office to epo] |
Ref country code: DE Effective date: 19820501 |
|
| GBPC | Gb: european patent ceased through non-payment of renewal fee | ||
| PG25 | Lapsed in a contracting state [announced via postgrant information from national office to epo] |
Ref country code: FR Free format text: LAPSE BECAUSE OF NON-PAYMENT OF DUE FEES Effective date: 19830331 |
|
| REG | Reference to a national code |
Ref country code: FR Ref legal event code: ST |
|
| PG25 | Lapsed in a contracting state [announced via postgrant information from national office to epo] |
Ref country code: GB Effective date: 19881117 |
|
| PLBE | No opposition filed within time limit |
Free format text: ORIGINAL CODE: 0009261 |
|
| STAA | Information on the status of an ep patent application or granted ep patent |
Free format text: STATUS: NO OPPOSITION FILED WITHIN TIME LIMIT |