EP0000005B1 - Neue Cephalosporinderivate, Verfahren zu ihrer Herstellung und pharmazeutische Präparate - Google Patents
Neue Cephalosporinderivate, Verfahren zu ihrer Herstellung und pharmazeutische Präparate Download PDFInfo
- Publication number
- EP0000005B1 EP0000005B1 EP78100078A EP78100078A EP0000005B1 EP 0000005 B1 EP0000005 B1 EP 0000005B1 EP 78100078 A EP78100078 A EP 78100078A EP 78100078 A EP78100078 A EP 78100078A EP 0000005 B1 EP0000005 B1 EP 0000005B1
- Authority
- EP
- European Patent Office
- Prior art keywords
- salts
- formula
- compounds
- methyl
- hydrates
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Expired
Links
- 0 **(*[C@@]([C@@](C1*2)SCC(*(S*)=C)=C2C(O)=O)C1=S=C)=[N+][O-] Chemical compound **(*[C@@]([C@@](C1*2)SCC(*(S*)=C)=C2C(O)=O)C1=S=C)=[N+][O-] 0.000 description 1
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D501/00—Heterocyclic compounds containing 5-thia-1-azabicyclo [4.2.0] octane ring systems, i.e. compounds containing a ring system of the formula:, e.g. cephalosporins; Such ring systems being further condensed, e.g. 2,3-condensed with an oxygen-, nitrogen- or sulfur-containing hetero ring
- C07D501/14—Compounds having a nitrogen atom directly attached in position 7
- C07D501/16—Compounds having a nitrogen atom directly attached in position 7 with a double bond between positions 2 and 3
- C07D501/20—7-Acylaminocephalosporanic or substituted 7-acylaminocephalosporanic acids in which the acyl radicals are derived from carboxylic acids
- C07D501/24—7-Acylaminocephalosporanic or substituted 7-acylaminocephalosporanic acids in which the acyl radicals are derived from carboxylic acids with hydrocarbon radicals, substituted by hetero atoms or hetero rings, attached in position 3
- C07D501/36—Methylene radicals, substituted by sulfur atoms
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
- A61P31/04—Antibacterial agents
Definitions
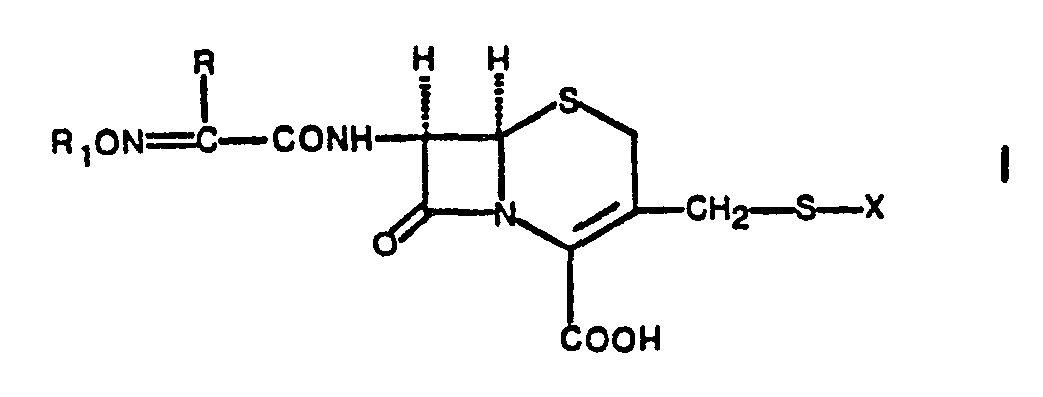
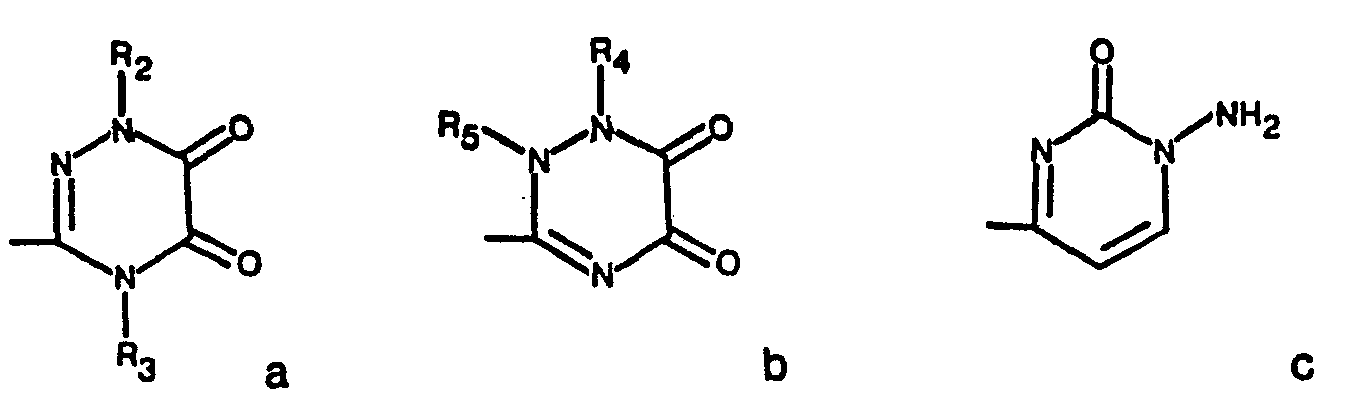
- the present invention relates to new acyl derivatives of the general formula in which R is furyl, thienyl or phenyl which is optionally substituted by halogen, hydroxy, lower alkoxy or lower alkyl, R 1 is lower alkyl or aminocarbonylmethyl and X is a group of the formulas in which one of the two radicals R 2 and R 3 or R 4 and R 5 is hydrogen and the other is lower alkyl, carboxymethyl or sulfomethyl, and salts of these compounds and hydrates of these salts.
- salts of the compounds of formula 1 are alkali metal salts such as the sodium and potassium salt; the ammonium salt; Alkaline earth metal salts such as the calcium salt; Salts with organic bases, such as salts with amines, e.g. Salts with N-ethyl-piperidine, procaine, dibenzylamine, N, N'-dibenzyl-ethyl-ethylenediamine, alkylamines or dialkylamines, and salts with amino acids, such as e.g. Salts with arginine or lysine.
- the salts can be mono-salts or also disalts.
- the second salt formation takes place on the tautomeric enol form of the triazine residue b, which has an acid character.
- the compounds of formula I also form addition salts with organic or inorganic acids.
- such salts are hydrohalides, for example hydrochlorides, hydrobromides; Hydroiodides, as well as other minor acid salts, such as sulfates, nitrates, phosphates and the like, alkyl and mono-aryl sulfonates, such as ethanesulfonates, toluenesulfonates, benzenesulfonates and the like, and also other organic acid salts, such as acetates, tartrates, maleates, citrates, benzoates, salic , Abscorbate and the like
- the salts of the compounds of formula I can be hydrated.
- the hydration can take place in the course of the production process or can occur gradually as a result of hygroscopic properties of an initially anhydrous salt of a compound of the formula I.
- lower alkyl groups are either straight chain or branched and can contain up to 7 carbon atoms, e.g. Methyl, ethyl, n-propyl, isopropyl, n-pentyl, n-heptyl, lower alkoxy groups have an analogous meaning.
- Halogen represents all four halogens, i.e. Fluorine, chlorine, bromine and iodine; chlorine and bromine are preferred.
- Preferred R groups are furyl, thienyl and phenyl, especially furyl. Methyl is preferred as R 1 .
- Preferred X groups are group (c) and groups (a) and (b), in which one of the two radicals R 2 and R 3 or R 4 and R 5 is hydrogen and the other is methyl. Particularly preferred X groups are the 1,2,5,6-tetrahydro-2-methyl-5,6-dioxo-as-triazin-3-yl and the 1,4,5,6-tetrahydro-4-methyl - 5,6-dioxo-as-triazin-3-yl group.
- Preferred compounds are (7R) - 7 - [2 - (2 - furyl) - 2 - (methoxyimino) acetamido] - 3 - / [(1,2,5,6 - tetrahydro - 2 - methyl - 5,6 - dioxo - as - triazin - 3 - yl) thio] methyl / - 3 - cephem - 4 - carboxylic acid and its salts and the hydrates of these salts.
- the compounds of the formula I and their salts or hydrates of the salts can be in the synisomeric form or in the anti-isomeric form or as mixtures of these two forms.
- the syn-isomeric form or mixtures in which the syn-isomeric form predominates is preferred.
- the carboxy groups present in the starting compounds of formulas II and IV can optionally be protected, e.g. by esterification to an easily cleavable ester such as a silyl ester, e.g. the trimethylsilyl ester.
- the carboxy group can also be protected by salt formation with an inorganic or tertiary organic base such as triethylamine.
- Suitable reactive functional derivatives of acids of the formula III are e.g. Halides, i.e. Chlorides, bromides and fluorides; Azides; Anhydrides, especially mixed anhydrides with stronger acids; reactive esters, e.g. N-hydroxy succinimide esters, and amides, e.g. Imidazolides.
- Halogens e.g. Chlorine, bromine or iodine
- acyloxy residues e.g. lower alkanoyl radicals, such as acetoxy, lower alkyl or arylsulfonyloxy radicals, such as mesyloxy or tosyloxy, or the azidorest in question.
- a free acid of formula III can be condensed with one of the esters corresponding to formula II by means of a carbodiimide, such as dicyclohexylcarbodiimide, in an inert solvent, such as ethyl acetate, acetonitrile, dioxane, chloroform, methylene chloride, benzene or dimethylformamide, and then the ester group is split off .
- carbodiimides can be as Condensing agents also use oxazolium salts, for example N-ethyl-5-phenyl-isoxazolium-3'-sulfonate.
- an acid halide preferably the chloride of an acid of the formula III
- the reaction is preferably carried out in the presence of an acid binding agent, e.g. in the presence of aqueous alkali, preferably sodium hydroxide solution, or also in the presence of an alkali metal carbonate, such as potassium carbonate, or in the presence of a lower alkylated amine, such as triethylamine.
- an acid binding agent e.g. in the presence of aqueous alkali, preferably sodium hydroxide solution, or also in the presence of an alkali metal carbonate, such as potassium carbonate, or in the presence of a lower alkylated amine, such as triethylamine.
- Water is preferably used as the solvent; but it can also be in an aprotic organic solvent such as e.g. Dimethylformamide, dimethyl sulfoxide, or hexamethylphosphoric triamide can be worked.
- reaction of a compound of formula II with a compound of formula III or a reactive functional derivative thereof can be advantageously carried out at temperatures between about -40 ° C and room temperature, for example at about 0-10 o C, take place.
- reaction of a compound of formula IV with a thiol of formula V can be carried out in a manner known per se, e.g. at a temperature between about 40 and 80 ° C, suitably at about 60 ° C, in a polar solvent, for example in an alcohol, e.g. in a lower alkanol such as ethanol, propanol and the like, in dimethylformamide or dimethyl sulfoxide, preferably in water or in a buffer solution with a pH of about 6 to 7, preferably 6.5.
- a polar solvent for example in an alcohol, e.g. in a lower alkanol such as ethanol, propanol and the like, in dimethylformamide or dimethyl sulfoxide, preferably in water or in a buffer solution with a pH of about 6 to 7, preferably 6.5.
- the protective group is a silyl group (silyl ester), this group can be split off particularly easily by treating the reaction product with water. If the carboxyl group of an acid of formula IV is protected by salt formation (e.g. with triethylamine), this salt-forming protective group can be split off by treatment with acid.
- the acid can be e.g. Hydrochloric acid, sulfuric acid, phosphoric acid or citric acid can be used.
- the 7-amino compounds of the formula 11 used as starting products can be started from a compound of the formula in which Y represents a leaving group and the carboxy group can be in protected form, are prepared with a thiol of the formula V.
- the reaction can be carried out under the same conditions as those of the starting compounds IV and V.
- syn / anti mixture of a compound of the formula I obtained can be separated into the corresponding syn and anti forms in the customary manner, for example by recrystallization or by chromatographic methods using a suitable solvent or solvent mixture.
- 2,275,215 and 2,280,381 cephalosporin derivatives which can carry a substituted thiomethyl radical of the present type ⁇ CH 2 ⁇ S ⁇ X in the 3-position. It has now been found that the new cephalosporin derivatives of the formula I and their salts and the hydrates of these salts, in which the substituents mentioned in positions 7 and 3 are present simultaneously for the first time, have valuable antibiotic, in particular bactericidal activity.
- ß-lactamase-forming staphylococci and various ß-lactamase-forming gram-negative bacteria, such as, for example, Haemophilus influenzae, Escherichia coli, Proteus and Klebsiella species.
- the compounds of formula I can be used for the treatment and prophylaxis of infectious diseases.
- a daily dose of approximately 1 g to approximately 4 g is suitable for the adult.
- the parenteral administration of the compounds according to the invention is particularly preferred.
- mice are infected intraperitoneally with an aqueous suspension of Proteus mirabilis.
- the test substance is applied subcutaneously one hour after the infection.
- the number of surviving animals is determined on the 4th day.
- Different doses are applied and the dose at which 50% of the test animals survived (CD sa , mg / kg) is determined by interpolation.
- compositions can contain the compounds of formula I, their salts or hydrated forms of these salts, possibly in a mixture with another therapeutically valuable substance. They are expediently mixed with a pharmaceutical, inorganic or organic inert carrier material which is particularly suitable for parenteral administration, such as e.g. with water, gum arabic.
- the pharmaceutical preparations are preferably in liquid form, e.g. as solutions, suspensions or emulsions. If necessary, they are sterilized and / or contain auxiliaries, such as preservatives, stabilizers, wetting agents or emulsifiers, salts for changing the osmotic pressure or buffers.
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Health & Medical Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Life Sciences & Earth Sciences (AREA)
- General Chemical & Material Sciences (AREA)
- Medicinal Chemistry (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Communicable Diseases (AREA)
- Pharmacology & Pharmacy (AREA)
- Oncology (AREA)
- Animal Behavior & Ethology (AREA)
- General Health & Medical Sciences (AREA)
- Public Health (AREA)
- Veterinary Medicine (AREA)
- Cephalosporin Compounds (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Saccharide Compounds (AREA)
Description
- Die vorliegende Erfindung betrifft neue Acylderivate der allgemeinen Formel
sowie Salze dieser Verbindungen und Hydrate dieser Salze. - Beispiele von Salzen der Verbindungen der Formel 1 sind Alkalimetallsalze, wie das Natrium- und Kaliumsalz; das Ammoniumsalz; Erdalkalimetallsalze, wie das Calciumsalz; Salze mit organischen Basen, wie Salze mit Aminen, z.B. Salze mit N-Aethyl-piperidin, Procain, Dibenzylamin, N,N'-Dibenzyl- äthyl-äthylendiamin, Alkylaminen oder Dialkylaminen, sowie Salze mit Aminosäuren, wie z.B. Salze mit Arginin oder Lysin. Die Salze können Monosalze oder auch Disalze sein. Die zweite Salzbildung erfolgt an der tautomeren Enolform des Triazinrestes b, welche sauren Charakter hat.
- Die Verbindungen der Formel I bilden ebenfalls Additionssalze mit organischen oder anorganischen Säuren. Beispiele solcher Salze sind Hydrohalogenide, beispielsweise Hydrochloride, Hydrobromide; Hydrojodide, sowie andere Minderalsäuresalze, wie Sulfate, Nitrate, Phosphate und dgl., Alkyl- und Mono-arylsulfonate, wie Aethansulfonate, Toluolsulfonate, Benzolsulfonate und dgl. und auch andere organische Säuresalze, wie Acetate, Tartrate, Maleate, Citrate, Benzoate, Salicylate, Abscorbate und dgl.
- Die Salze der Verbindungen der Formel I können hydratisiert sein. Die Hydratisierung kann im Zuge des Herstellungsverfahrens erfolgen oder allmählich als Folge hygroskopischer Eigenschaften eines zunächst wasserfreien Salzes einer Verbindung der Formel I auftreten.
- Die vorstehend genannten niederen Alkylgruppen sind entweder geradkettig oder verzweigt und können bis zu 7 Kohlenstoffatome enthalten, z.B. Methyl, Aethyl, n-Propyl, Isopropyl, n-Pentyl, n-Heptyl, Niedere Alkoxygruppen haben analoge Bedeutung. Halogen stellt alle vier Halogene dar, d.h. Fluor, Chlor, Brom und Jod; bevorzugt sind Chlor und Brom.
- Bevorzugte R-Gruppen sind Furyl, Thienyl und Phenyl, insbesondere Furyl. Als R1 ist Methyl bevorzugt. Bevorzugte X-Gruppen sind die Gruppe (c) sowie die Gruppen (a) und (b), worin einer der beiden Reste R2 und R3 bzw. R4 und R5 Wasserstoff und der andere Methyl darstellt. Besonders bevorzugte X-Gruppen sind die 1,2,5,6-Tetrahydro-2-methyl-5,6-dioxo-as-triazin-3-yl- und die 1,4,5,6 - Tetrahydro - 4 - methyl - 5,6 - dioxo - as - triazin - 3 - yl - gruppe.
- Bevorzugte Verbindungen sind (7R) - 7 - [2 - (2 - Furyl) - 2 - (methoxyimino)acetamido] - 3 - /[(1,2,5,6 - tetrahydro - 2 - methyl - 5,6 - dioxo - as - triazin - 3 - yl)thio]methyl/ - 3 - cephem - 4 - carbonsäure und deren Salze sowie die Hydrate dieser Salze.
-
- Die Acylderivate der Formel I sowie deren Salze bzw. Hydrate dieser Salze werden erfindungsgemäss durch ein Verfahren hergestellt, welches dadurch gekennzeichnet ist, dass man
- a) eine Verbindung der allgemeinen Formel
- b) eine Verbindung der allgemeinen Formel
- Die in den Ausgangsverbindungen der Formeln II and IV vorhandenen Carboxygruppen können wahlweise geschützt sein, z.B. durch Veresterung zu einem leicht spaltbaren Ester, wie einem Silylester, z.B. dem Trimethylsilylester. Die Carboxygruppe kann auch durch Salzbildung mit einer anorganischen oder tertiären organischen Base, wie Triäthylamin, geschützt werden.
- Als reaktionsfähige funktionelle Derivate von Säuren der Formel III kommen z.B. Halogenide, d.h. Chloride, Bromide und Fluoride; Azide; Anhydride, insbesondere gemischte Anhydride mit stärkeren Säuren; reaktionsfähige Ester, z.B. N-Hydroxy-succinimidester, und Amide, z.B. Imidazolide, in Betracht.
- Als austretende Gruppe Y einer Verbindung der Formel IV kommen beispielsweise Halogene, z.B. Chlor, Brom oder Jod, Acyloxyreste, z.B. niedere Alkanoylreste, wie Acetoxy, niedere Alkyl- oder Arylsulfonyloxyreste, wie Mesyloxy oder Tosyloxy, oder der Azidorest in Frage.
- Die Umsetzung einer Verbindung der Formel II mit einer Säure der Formel III oder einem reaktionsfähigen funktionellen Derivat davon kann in an sich bekannter Weise durchgeführt werden. So kann man z.B. eine freie Saüre der Formel III mit einem der erwähnten Ester entsprechend Formel II mittels eines Carbodiimids, wie Dicyclohexylcarbodiimid, in einem inerten Lösungsmittel, wie Essigester, Acetonitril, Dioxan, Chloroform, Methylenchlorid, Benzol oder Dimethylformamid kondensieren und anschliessend die Estergruppe abspalten. Anstelle von Carbodiimiden lassen sich als Kondensationsmittel auch Oxazoliumsalze, z.B. N-Aethyl-5-phenyl-isoxazolium-3'-sulfonat, verwenden.
- Nach einer anderen Ausführungsform setzt man ein Salz einer Säure der Formel 11, z.B. ein Trialkylammoniumsalz, mit einem reaktionsfähigen funktionellen Derivat einer Säure der Formel III wie oben erwähnt in einem inerten Lösungsmittel, z.B. einem der oben genannten, um.
- Nach einer weiteren Ausführungsform wird ein Säurehalogenid, vorzugsweise das Chlorid einer Säure der Formel 111 mit dem Amin der Formel II umgesetzt. Die Umsetzung erfolgt vorzugsweise in Gegenwart eines säurebindenden Mittels, z.B. in Gegenwart von wässrigem Alkali, vorzugsweise Natronlauge, oder auch in Gegenwart eines Alkalimetallcarbonats, wie Kaliumcarbonat, oder in Gegenwart eines nieder-alkylierten Amins, wie Triäthylamin. Als Lösungsmittel wird vorzugsweise Wasser verwendet; es kann aber auch in einem aprotischen organischen Lösungsmittel, wie z.B. Dimethylformamid, Dimethylsulfoxid, oder Hexamethylphosphorsäuretriamid, gearbeitet werden.
- Die Umsetzung einer Verbindung der Formel II mit einer Verbindung der Formel III oder einem reaktionsfähigen funktionellen Derivat davon kann zweckmässig bei Temperaturen zwischen etwa -40°C und Zimmertemperatur, beispielsweise bei etwa 0-10oC, erfolgen.
- Die Umsetzung einer Verbindung der Formel IV mit einem Thiol der Formel V kann in an sich bekannter Weise, z.B. bei einer Temperatur zwischen etwa 40 und 80°C, zweckmässig bei etwa 60°C, in einem polaren Lösungsmittel, beispielsweise in einem Alkohol, wie z.B. in einem niederen Alkanol, wie Aethanol, Propanol und dgl., in Dimethylformamid oder Dimethylsulfoxid, vorzugsweise in Wasser oder in einer Pufferlösung mit einem pH von etwa 6 bis 7, vorzugsweise 6,5, durchgeführt werden.
- Nach erfolgter Umsetzung einer Verbindung der Formel 11 oder IV mit einer Verbindung der Formel II bzw. V wird die allenfalls vorhandene Schutzgruppe abgespalten.
- Wenn die Schutzgruppe eine Silylgruppe darstellt (Silylester), kann diese Gruppe besonders leicht durch Behandlung des Umsetzungsproduktes mit Wasser abgespalten werden. Wenn die Carboxylgruppe einer Säure der Formel IV durch Salzbildung (z.B. mit Triäthylamin) geschützt ist, so kann die Abspaltung dieser salzbildenen Schutzgruppe durch Behandlung mit Säure erfolgen. Als Säure kann hierbei z.B. Salzsäure, Schwefelsäure, Phosphorsäure oder Citronensäure verwendet werden.
- Die als Ausgangsprodukte verwendeten 7-Aminoverbindungen der Formel 11 können ausgehend von einer Verbindung der Formel
- Ein allenfalls erhaltenes syn/anti-Gemisch einer Verbindung der Formel I kann in die entsprechenden syn- und anti-Formen in üblicher Weise getrennt werden, beispielsweise durch Umkristallisation oder durch chromatographische Methoden unter Verwendung eines geeigneten Lösungsmittels bzw. Lösungsmittelgemisches.
- Aus der französischen Patentpublikation No. 2.137.899 sind Cephalosporinderivate bekannt, welche in 7-Stellung u.a. einen Substituenten des vorliegenden Typs R,ON=CR-CONH- tragen können. Andererseits sind aus den französischen Patentpublikationen Nos. 2.275.215 und 2.280.381 Cephalosporinderivate bekannt, welche in 3-Stellung einen substituierten Thiomethylrest des vorliegenden Typs ―CH2―S―X tragen können. Es wurde nun gefunden, daß die neuen Cephalosporinderivate der Formel I sowie deren Salze und die Hydrate dieser Salze, in welchen erstmals die erwähnten Substituenten in den Stellungen 7 und 3 gleichzeitig vorliegen, wertvolle antibiotische, insbesondere bakterizide Wirksamkeit besitzen. Sie besitzen ein breites Wirkungsspektrum gegen Grampositive und Gram-negative Mikroorganismen, einschließlich ß-Lactamase bildende Staphylokokken und verschiedene ß-Lactamase bildende Gram-negative Bakterien, wie z.B. Haemophilus influenzae, Escherichia coli, Proteus- und Klebsiella-Spezies.
- Die Verbindungender Formel I sowie die pharmazeutisch verträglichen Salze und hydratisierten Formen davon können zur Behandlung und Prophylaxe von Infektionskrankheiten verwendet werden. Für den Erwachsenen kommt eine Tagesdosis von etwa 1 g bis etwa 4 g in Betracht. Die parenterale Verabreichung der erfindungsgemäßen Verbindungen ist besonders bevorzugt.
-
- Gruppen von 10 Mäusen werden mit einer wässrigen Suspension von Proteus mirabilis intraperitoneal infiziert. Eine Stunde nach der Infektion wird die Prüfsubstanz subcutan appliziert. Die Zahl der überlebenden Tiere wird am 4. Tag bestimmt. Es werden verschiedene Dosierungen appliziert, und durch Interpolation wird diejenige Dosis bestimmt, bei der 50% der Versuchstiere überlebten (CDsa, mg/kg).
- Pharmazeutische Präparate, vorzugsweise Trockenampullen, können die Verbindungen der Formel I, ihre Salze oder hydratisierte Formen dieser Salze, eventuell in Mischung mit einem anderen therapeutisch wertvollen Stoff enthalten. Zweckmässig sind sie mit einem insbesondere für die parenterale Applikation geeigneten pharmazeutischen, anorganischen oder organischen inerten Trägermaterial vermischt, wie z.B. mit Wasser, Gummi arabicum. Die pharmazeutischen Präparate leigen vorzugsweise in flüssiger Form vor, z.B. als Lösungen, Suspensionen oder Emulsionen. Gegebenenfalls sind sie sterilisiert und bzw. oder enthalten Hilfsstoffe, wie Konservierungs-, Stabilisierungs-, Netz- oder Emulgiermittel, Salze zur Veränderung des osmotischen Druckes oder Puffer.
- Herstellung des Natriumsalzes der (7R) - 7 - [2 - (2 - Furyl) - 2 - -(methoxyimino)acetamido] - 3 - /[(1,2,5,6 - tetrahydro - 2 - methyl - 5,6 - dioxo - as - triazin - 3 - yl)thio]methyl/ - 3 - cephem - 4 - carbonsäure:
- 5,60 2-Methoxyimino-2-furyl-essigsäure (syn/anti-Gemisch 80:20) werden in 150 ml Benzol gelöst und unter Stickstoff-Begasung bei 5-10°C mit 4,2 ml Triäthylamin, 2,6 ml Oxalylchlorid und 6 Tropfen Dimethylformamid versetzt. Das Gemisch wird 1 Stunde bei 5-10°C und 1/2 Stunde bei 25°C unter Stickstoff-Begasung gerührt und danach im Vakuum bei 40°C eingedampft. Der Rückstand wird in 150 ml Aceton suspendiert und bei 0°C mit einer Lösung von 11,2 g (7R) - 7 - Amino - 3 - desacetoxy - 3 - [(1,2,5,6 - tetrahydro - 2 - methyl - 5,6 - dioxo - as - triazin - 3 - yl) - thio] - cephalosporansäure in 150 ml Wasser, welche zuvor mittels 2-n wässriger Natronlauge auf ph 7,5 eingestellt worden war, versetzt. Das Reaktionsgemisch wird 2 1/2 Stunden unter Stickstoff und bei 0-10°C gerührt, wobei das pH mittels Zugabe von 2-n wässriger Natronlauge zwischen 7,5 und 8,0 gehalten wird. Dann werden 500 ml Essigester zugegeben und das pH mit 2-n wässriger Salzsäure auf 1,5 eingestellt. Nach dem Abtrennen der organischen Phase wird die wässrige Phase einmal mit Essigester extrahiert. Die vereinigten organischen Phasen werden zweimal mit gesättigter wässriger Kochsalz-Lösung gewaschen, über Natriumsulfat getrocknet und auf ein Volumen von ca. 100 ml eingeengt. Der Rückstand wird von Ungelöstem abfiltriert ud das erhaltene orangegefärbte Filtrat mit 1000 ml Aether verdünnt. Die dabei amorph ausgefallene (7R) - 7 - [2 - (2 - furyl) - 2 - (methoxyimino)acetamido] - 3 - /[(1,2,5,6 - tetrahydro - 2 - methyl - 5,6 - dioxo - as - triazin - 3 - yl)thio]methyl/ - 3 - cephem - 4 - carbonsäure wird abgenutscht und mit Aether sowie tiefsiedendem Petroläther gewaschen. Das erhaltene beige-farbene Produkt wird in 250 ml Essigester gelöst und von Ungelöstem abfiltriert. Das orangefärbte Filtrat wird mit 10 ml einer 2-n Lösung von 2-Aethylcapronsäure-Natriumsalz in Essigester versetzt, wobei das Natriumsalz der (7R) - 7 - [2 - (2 - Furyl) - 2 - (methoxyimino)acetamido] - 3 - /[(1,2,5,6 - tetrahydro - 2 - methyl - 5,6 - dioxo - as - triazin - 3 - yl)thio]methyl/ - 3 - cephem - 4 - carbonsäure ausfällt. Dieses wird abgenutscht, mit Essigester und tiefsiedendem Petroläther gewaschen und 2 Tage im Vakuum bei 25°C getrocknet. Das erhaltene Produkt ist ein beigefarbenes Pulver (syn/anti-Gemisch 80:20). (c = 0,5 in Wasser). Rf-Wert = 0,10 (DC auf Kieselgel-F254-Fertigplatten im System Butanol/Eisessig/Wasser 4:1:1; Sichtbarmachung mit UV-Licht).
- Herstellung des Natriumsalzes der (7R) - 7 - [2 - (2 - Furyl) - 2 - (methoxyimino)acetamido] - 3 - -/[1 - amino - 1,2 - dihydro - 2 - oxo - 4 - pyrimidinyl)thio] - methyl/ - 3 - cephem - 4 - carbonsäure:
- Diese Verbindung wird analog Beispiel 1 aus 3,4 g 2-Methoxyimino-2-furyl-essigsäure und 7,11 g g (7R) - 7 - Amino - 3 - desacetoxy - 3 - [(1 - amino - 1,2 - dihydro - 2 - oxo - 4 - pyrimidinyl) - thio] - cephalosporansäure hergestellt. Das Produkt stellt ein beiges Pulver dar (syn/anti-Gemisch 70:30), R,-Wert = 0,40 (DC auf Kieselgel-F254―Fertigplatten im System Butanol/Eisessig/Wasser 4:1;1; Sichtbarmachung mit UV-Licht).
- Herstellung des Natriumsalzes der (7R) - 7 - [2 - (Phenyl) - 2 - (methoxyimino)acetamido] - 3 - /[(1,2,5,6 - tetrahydro - 2 - methyl - 5,6 - dioxo - as - triazin - 3 - yl)thio]methyl/ - 3 - cephem - 4 - carbonsäure:
- Diese Verbindung wird analog Beispiel 1 aus 1,8 g 2-Methoxyimino-phenyl-essigsäure (syn/anti-Gemisch 90:10) und 3,73 g (7R) - 7 - Amino - 3 - desacetoxy - 3 - [(1,2,5,6 - tetrahydro - 2 - methyl - 5,6 - dioxo - as - triazin - 3 - yl) - thio] - cephalosporansäure hergestellt. Das Produkt ist ein beiges Pulver (syn/anti-Gemisch 90:10). (c = 0,5 in Wasser). Rf-Wert = 0,17 (DC auf Kieselgel-F254-Fertigplatten im System Butanol/Eisessig/Wasser 4:1:1, Sichtbarmachung mit UV-Licht).
- Herstellung des Natriumsalzes der (7R) - 7 - [2 - (2 - Furyl) - 2 - (methoxyimino)acetamido] - 3 - /[(1,4,5,6 - tetrahydro - 4 - methyl - 5,6 - dioxo - as - triazin - 3 - yl)thio]methyl/ - 3 - cephem - 4 - carbonsäure:
- Diese Verbindung wird analog Beispiel 1 aus 3,4 g 2-Methoxyimino-2-furyl-essigsäure (syn/anti-Gemisch 80:20) und 7,46 g (7R) - 7 - Amino - 3 - desacetoxy - 3 - [(1,4,5,6 - tetrahydro - 4 - methyl - 5,6 - dioxo - as - triazin - 3 - yl) - thio] - cephalosporansäure hergestellt. Das Produkt ist ein beiges Pulver (syn/anti-Gemisch 80:20). (c = 0,5 in Wasser). Rf-Wert = 0,34 (DC auf Kieselgel-F254-Fertigplatten im System Butanol/Eisessig/Wasser 4:1:1; Sichtbarmachung mit UV-Licht).
- Herstellung des Natriumsalzes der (7R) - 7 - [2 - (Methoxyimino) - 2 - (2 - thienyl)acetamido] - 3 - /[1,2,5,6 - tetrahydro - 2 - methyl - 5,6 - dioxo - as - triazin - 3 - yl)thio]methyl/ - 3 - cephem - 4 - carbonsäure:
- Diese Verbindung wird analog Beispiel 1 aus 1,85 g 2-Methoxyimino-2-thienyl-essigsäure (syn/anti-Gemisch ca. 70:30) und 3,71 g (7R) - 7 - Amino - 3 - desacetoxy - 3 - [(1,2,5,6 - tetrahydro - 2 - methyl - 5,6 - dioxo - as - triazin - 3 - yl)thio] - cephalosporansäure hergestellt. Das Produkt ist ein beiges Pulver (syn/anti-Gemisch ca. 70:30). (c = 0.5 in Wasser). Rf-Wert s 0,21 (DC auf Kieselgel-F254-Fertigplatten im System Butanol/Eisessig/Wasser 4:1:1, Sichtbarmachung mit UV-Licht).
- Herstellung des Dinatriumsalzes der (7R) - 7 - [2 - (2 - Furyl) - 2 - (methoxy imino)acetamido] - 3 - /[(2,5 - dihydro - 2 - methyl - 5 - oxo - 6 - hydroxy - as - triazin - 3 - yi)thio]methy)/ - 3 - cephem - 4 - carbonsäure:
- Diese Verbindung wird analog Beispiel 1 aus 10,12 g 2-Methoxyimino-2-furyl-essigsäure (syn-Isomer) und 18,7 g (7R) - 7 - Amino - 3 - desacetoxy - 3 - [(1,2,5,6 - tetrahydro - 2 - methyl - 5,6 - dioxo - as - triazin - 3 - yl)thio] - cephalosporansäure hergestellt. Bei der Salzbildung werden 20 ml (2 Aequiv.) einer 2-n Lösung von 2-Aethylcapronsäure-Natriumsalz in Essigester verwendet. Das Produkt is ein praktisch farbloses Pulver (syn-Isomer). (c0,5 in Wasser). Rf-Wert=0,14 (DC auf Kieselgel-F254-Fertigplatten im System Butano)/Eisessig/Wasser 4:1:1, Sichtbarmachung mit UV-Licht).
- Herstellung des Natriumsalzes der (7R) - 3 -/[(1-Aethyl - 1,4,5,6 - tetrahydro - 5,6 - dioxo - as - triazin - 3 - yl)thio]methyl/ - 7 - [2 - (2 - furyl) - 2 - (methoxyimino)acetamido] - 3 - cephem - 4 - carbonsäure:
- Diese Verbindung wird analog Beispiel 1 aus 1,69 g 2-Methoxyimino-2-furyl-essigsäure (syn-Isomer) und 3,85 g (7R) - 7 - Amino - 3 - desacetoxy - 3 - [(1 - äthyl - 1,4,5,6 - tetrahydro - 5,6 - dioxo - as - triazin - 3 - yl)thioJ - cephalosporansäure hergestellt. Das Produkt ist ein beiges Pulver (syn/anti-Gemisch ca. 70:30).
- Herstellung des Natriumsalzes der (7R) - 7 - /2 - [(Carbamoyl - methoxy)imino] - 2 - (2 - furyl)acetamido/ - 3 - /[1,4,5,6 - tetrahydro - 4 - methyl - 5,6 - dioxo - as - triazin - 3 - yl)thio]methyl/ - 3 - cephem - 4 - carbonsäure:
- 9,76 g /α - [(Carbamoylmethoxy)imino]furfuryl/cephalosporin Natriumsalz (syn/anti-Gemisch ca. 70:30) werden zusammen mit 4,77 g 1,4,5,6-Tetrahydro-4-methyl-5,6-dioxo-3-mercapto-as-triazin in 200 ml Phosphatpuffer mit pH 6,4 suspendiert. Unter Sticksoffbegasung wird das pH mittels 1-n Natronlauge auf 6,4 gestellt, wobei eine dunkle Lösung entsteht. Diese Lösung wird 6 Stunden bei 55-60°C unter Stickstoffbegasung bei pH 6,4-6,5 gerührt, wobei das pH mit Hilfe eines Autotitrators unter Zugabe von 1-n Natronlauge konstant gehalten wird. Die Reaktionslösung wird auf 0-5°C abgekühlt und das pH mit 2-n Salzsäure auf 2 gestellt, wobei das Reaktionsprodukt als Säure ausfällt. Dieses wird abgenutscht, mit Eiswasser gewaschen und über Nacht im Vakuum bei 40°C getrocknet. Man erhält das Endprodukt in Form der rohen Säure. Zur Reinigung wird diese in 150 ml Methanol gelöst und die Lösung 2 Minuten mit Aktivkohle gekocht. Das Gemisch wird durch ein Faltenfilter filtriert und das orangefarbige Filtrat im Vakuum eingeengt. Das dabei ausgeschiedene Harz wird abgetrennt und verworfen. Die konzentrierte methanolische Lösung wird auf Aether gegossen. Die dabei ausgefallene Säure wird abgenutscht, mit Aether und tiefsiedendem Petroläther gewaschen. Man erhält das Endprodukt in Form der gereinigten Säure, die, zwecks Ueberführung in das Natriumsalz, in 100 ml Methanol gelöst wird und mit 5 ml einer 2-n Lösung von 2-Aethylcapronsäure-Natriumsalz in Essigester versetzt wird. Es wird von wenig Ungelöstem abfiltriert und das orangefarbige Filtrat im Vakuum bei 40°C eingeengt. Dieser konzentrierten Lösung wird Aethanol zugegeben, wobei das Natriumsalze ausfällt. Dieses wird abgenutscht, mit Aethanol und tiefsiedendem Petroläther gewaschen und über Nacht im Vakuum bei 40°C getrocknet. Man erhält das Natriumsalz der (7R) - 7 - /2 - [(Carbamoylmethoxy)imino] - 2 - (2 - furyl)acetamido/ - 3 - /[1,4,5,6 - tetrahydro - 4 - methyl - 5,6 - dioxo - as - triazin - 3 - yl)thio]methyl/ - 3 - cephem - 4 - carbonsäure als beiges Pulver (syn/anti-Gemisch ca. 70:30). (c=1 1 in Wasser), Rf=0,29 (DC auf Kieselgel-F254-Fertigplatten im System Butanol/Eisessig/Wasser 4:1:1, Sichtbarmachung mit UV-Licht).
- Ersetzt man die Ausgangsverbindungen durch äquivalente Mengen /α - [(Methoxy)imino]furfu- ryl/cephalosporin und 1,2,5,6 - Tetrahydro - 2 - methyl - 5,6 - dioxo - 3 - mercapto - as - triazin, so erhält man unter sonst gleichen Bedingungen das Natriumsalz der (7R) - 7 - [2 - (2 - Furyl) - 2 - (methoxyimino)acetamido] - 3 - /[1,2,5,6 - tetrahydro - 2 - methyl - 5,6 - dioxo - as - triazin - 3 - yl)thio]methyl/ - 3 - cephem - 4 - carbonsäure. Das Produkt ist mit der gemäss Beispiel 1 erhaltenen Verbindung identisch.
- Es wird in üblicher Weise ein Lyophilisat von 1 g des Natriumsalzes der (7R) - 7 - [2 - (2 - Furyl) - 2 - (methoxyimino)acetamido] - 3 - /[1,2,5,6 - tetrahydro - -2 - methyl - 5,6 - dioxo - as - triazin - 3 - yl)thio]methyl/ - 3 - cephem - carbonsäure hergestellt und in eine Ampulle abge- .füllt. Vor der Verabreichung wird letzteres mit 2,5 ml einer 2%igen wässrigen Lidocainhydrochlorid-Lösung versetzt.
Claims (17)
Applications Claiming Priority (4)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| LU77485 | 1977-06-03 | ||
| LU77485 | 1977-06-03 | ||
| CH314278 | 1978-03-22 | ||
| CH3142/78 | 1978-03-22 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| EP0000005A1 EP0000005A1 (de) | 1978-12-20 |
| EP0000005B1 true EP0000005B1 (de) | 1980-10-29 |
Family
ID=25692293
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| EP78100078A Expired EP0000005B1 (de) | 1977-06-03 | 1978-06-01 | Neue Cephalosporinderivate, Verfahren zu ihrer Herstellung und pharmazeutische Präparate |
Country Status (26)
| Country | Link |
|---|---|
| EP (1) | EP0000005B1 (de) |
| JP (1) | JPS5412394A (de) |
| AR (1) | AR225134A1 (de) |
| AT (2) | AT362501B (de) |
| AU (1) | AU518648B2 (de) |
| BR (1) | BR7803565A (de) |
| CA (1) | CA1114808A (de) |
| CU (1) | CU21118A (de) |
| DE (2) | DE2860248D1 (de) |
| DK (1) | DK246878A (de) |
| ES (2) | ES470442A1 (de) |
| FI (1) | FI781754A7 (de) |
| FR (1) | FR2393000A1 (de) |
| GB (1) | GB1599232A (de) |
| GR (1) | GR73554B (de) |
| HU (1) | HU182498B (de) |
| IE (1) | IE46903B1 (de) |
| IL (1) | IL54803A (de) |
| IT (1) | IT1098306B (de) |
| MC (1) | MC1195A1 (de) |
| NL (1) | NL7805715A (de) |
| NO (1) | NO781934L (de) |
| NZ (1) | NZ187392A (de) |
| PH (1) | PH14653A (de) |
| PT (1) | PT68134A (de) |
| SE (1) | SE7806465L (de) |
Families Citing this family (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US4200745A (en) * | 1977-12-20 | 1980-04-29 | Eli Lilly And Company | 7[2-(2-Aminothiazol-4-yl)-2-alkoxyimino]acetamido 3[4-alkyl-5-oxo-6-hydroxy-3,4 dihydro 1,2,4-triazin 3-yl]thio methyl cephalosporins |
| FR2432521A1 (fr) * | 1978-03-31 | 1980-02-29 | Roussel Uclaf | Nouvelles oximes o-substituees derivees de l'acide 7-amino thiazolyl acetamido cephalosporanique, leur procede de preparation et leur application comme medicaments |
| MC1259A1 (fr) * | 1978-05-30 | 1980-01-14 | Hoffmann La Roche | Derives acyles |
| NO782998L (no) * | 1978-07-19 | 1980-01-22 | Hoffmann La Roche | Cephalosporinestere og -etere. |
| US4472574A (en) * | 1981-05-22 | 1984-09-18 | Hoffman-La Roche Inc. | Process for the manufacture of a cephem carboxylic acid derivative |
| US4698338A (en) * | 1986-02-19 | 1987-10-06 | Eli Lilly And Company | 7[2-(2-aminothiazol-4-yl)-2-benzyloximino]acetamido-3[4-alkyl-5-oxo-6-hydroxy-3,4-dihydro-1,2,4-triazin-3-yl]thiomethyl cephalosporins |
Family Cites Families (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| GB1399086A (en) * | 1971-05-14 | 1975-06-25 | Glaxo Lab Ltd | Cephalosporin compounds |
| CH609989A5 (en) * | 1974-06-21 | 1979-03-30 | Hoffmann La Roche | Process for the preparation of acyl derivatives |
| CA1100129A (en) * | 1974-08-02 | 1981-04-28 | William H.W. Lunn | Cephalosporin compounds |
| GB1555471A (en) * | 1975-06-19 | 1979-11-14 | Glaxo Lab Ltd | 7 carbamoylalkoxyimino acetamido 3 em 4 carboxylic acidsand derivatives thereof |
| GB1576625A (en) * | 1976-04-12 | 1980-10-08 | Fujisawa Pharmaceutical Co | Syn isomer 3,7 disubstituted 3 cephem 4 carboxylic acid compounds and processes for the preparation thereof |
| GB1596278A (en) * | 1976-11-30 | 1981-08-26 | Glaxo Operations Ltd | 7-(-oxyimino-acetamino)cephalosporin derivatives |
-
1978
- 1978-05-25 NL NL7805715A patent/NL7805715A/xx not_active Application Discontinuation
- 1978-05-25 GB GB22499/78A patent/GB1599232A/en not_active Expired
- 1978-05-26 IE IE1056/78A patent/IE46903B1/en unknown
- 1978-05-26 MC MC781305A patent/MC1195A1/fr unknown
- 1978-05-26 NZ NZ187392A patent/NZ187392A/en unknown
- 1978-05-29 IL IL54803A patent/IL54803A/xx unknown
- 1978-05-29 AU AU36588/78A patent/AU518648B2/en not_active Expired
- 1978-05-31 HU HU78HO2077A patent/HU182498B/hu unknown
- 1978-06-01 SE SE7806465A patent/SE7806465L/xx unknown
- 1978-06-01 FR FR7816468A patent/FR2393000A1/fr active Granted
- 1978-06-01 GR GR56409A patent/GR73554B/el unknown
- 1978-06-01 EP EP78100078A patent/EP0000005B1/de not_active Expired
- 1978-06-01 DE DE7878100078T patent/DE2860248D1/de not_active Expired
- 1978-06-01 DE DE19782824065 patent/DE2824065A1/de not_active Withdrawn
- 1978-06-01 JP JP6501078A patent/JPS5412394A/ja active Pending
- 1978-06-01 FI FI781754A patent/FI781754A7/fi not_active Application Discontinuation
- 1978-06-02 AT AT403578A patent/AT362501B/de not_active IP Right Cessation
- 1978-06-02 BR BR787803565A patent/BR7803565A/pt unknown
- 1978-06-02 NO NO781934A patent/NO781934L/no unknown
- 1978-06-02 CA CA304,644A patent/CA1114808A/en not_active Expired
- 1978-06-02 AR AR272437A patent/AR225134A1/es active
- 1978-06-02 PH PH21225A patent/PH14653A/en unknown
- 1978-06-02 IT IT24165/78A patent/IT1098306B/it active
- 1978-06-02 DK DK246878A patent/DK246878A/da not_active Application Discontinuation
- 1978-06-02 ES ES470442A patent/ES470442A1/es not_active Expired
- 1978-06-02 PT PT68134A patent/PT68134A/pt unknown
- 1978-07-03 CU CU7834929A patent/CU21118A/es unknown
-
1979
- 1979-02-27 ES ES478115A patent/ES478115A1/es not_active Expired
-
1980
- 1980-07-02 AT AT0345980A patent/AT365197B/de not_active IP Right Cessation
Also Published As
| Publication number | Publication date |
|---|---|
| IE781056L (en) | 1978-12-03 |
| ES478115A1 (es) | 1979-06-01 |
| IT7824165A0 (it) | 1978-06-02 |
| ES470442A1 (es) | 1979-10-01 |
| IL54803A0 (en) | 1978-07-31 |
| CA1114808A (en) | 1981-12-22 |
| GR73554B (de) | 1984-03-14 |
| EP0000005A1 (de) | 1978-12-20 |
| DE2824065A1 (de) | 1978-12-14 |
| BR7803565A (pt) | 1979-02-20 |
| NO781934L (no) | 1978-12-05 |
| NL7805715A (nl) | 1978-12-05 |
| CU21118A (es) | 1983-04-06 |
| HU182498B (en) | 1984-01-30 |
| AU518648B2 (en) | 1981-10-15 |
| ATA403578A (de) | 1980-10-15 |
| JPS5412394A (en) | 1979-01-30 |
| GB1599232A (en) | 1981-09-30 |
| IL54803A (en) | 1982-01-31 |
| FI781754A7 (fi) | 1978-12-04 |
| AT362501B (de) | 1981-05-25 |
| AT365197B (de) | 1981-12-28 |
| ATA345980A (de) | 1981-05-15 |
| NZ187392A (en) | 1984-05-31 |
| AR225134A1 (es) | 1982-02-26 |
| DK246878A (da) | 1978-12-04 |
| MC1195A1 (fr) | 1979-02-23 |
| IT1098306B (it) | 1985-09-07 |
| PT68134A (en) | 1978-07-01 |
| FR2393000B1 (de) | 1982-10-29 |
| SE7806465L (sv) | 1978-12-04 |
| AU3658878A (en) | 1979-12-06 |
| FR2393000A1 (fr) | 1978-12-29 |
| IE46903B1 (en) | 1983-11-02 |
| PH14653A (en) | 1981-10-14 |
| DE2860248D1 (en) | 1981-01-29 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| DE2462736C2 (de) | 7-Aminothiazolylacetamido-3-cephem-4-carbonsäuren und Verfahren zur Herstellung derselben | |
| CH630632A5 (de) | Verfahren zur herstellung neuer cephalosporinderivate. | |
| CH634578A5 (de) | Verfahren zur herstellung von neuen cephalosporinderivaten. | |
| EP0030294B1 (de) | Verfahren zur Herstellung von Cephalosporinderivaten; Zwischenprodukte und deren Herstellung | |
| DE2922036C2 (de) | 7-[2-(2-Amino-4-thiazolyl)-2-methoxyimino-acetamido]- cephalosporansäure-Derivate | |
| CH633558A5 (de) | Verfahren zur herstellung neuer cephalosporinderivate. | |
| DE2555858A1 (de) | 3-thiosubstituierte cephalosporinverbindungen und verfahren zu ihrer herstellung | |
| CH639666A5 (de) | Cephalosporansaeurederivate, diese verbindungen enthaltende arzneimittel und verfahren zu ihrer herstellung. | |
| CH655118A5 (de) | Cephalosporinverbindungen, verfahren zu ihrer herstellung und antibakterielle mittel, die diese verbindungen enthalten. | |
| CH641468A5 (de) | Cephemderivate. | |
| DE2736471C2 (de) | ||
| DE3307550C2 (de) | ||
| EP0000005B1 (de) | Neue Cephalosporinderivate, Verfahren zu ihrer Herstellung und pharmazeutische Präparate | |
| EP0049855A2 (de) | Neue Cephalosporinderivate, Verfahren zu ihrer Herstellung und Zwischenprodukte dafür sowie entsprechende pharmazeutische Präparate | |
| DE69109913T2 (de) | Cephalosporinzwischenverbindungen, Verfahren zu ihrer Herstellung sowie zur Herstellung ihrer Endprodukte. | |
| DE2527291C2 (de) | ||
| DE2521063A1 (de) | Phenylacetamidocephalosporin- derivate | |
| EP0029966A2 (de) | Cephalosporinderivate, und deren Herstellung sowie entsprechende pharmazeutische Präparate | |
| EP0553792B1 (de) | Verfahren zur Herstellung von Ceftriaxon-dinatriumsalzhemiheptahydrat | |
| EP0036652A2 (de) | Cephalosporinderivate, entsprechende Präparate, die Verwendung dieser Produkte bei der Behandlung von Krankheiten, die Herstellung der Wirkstoffe sowie dabei anfallende Zwischenprodukte | |
| CH666037A5 (de) | Verfahren zur herstellung von cephalosporin-syn-isomeren. | |
| EP0008372B1 (de) | Leicht hydrolisierbare Cephalosporinester und -äther, deren Herstellung und pharmazeutische Präparate enthaltend solche Ester und Äther | |
| CH634326A5 (de) | 2-hydroxyiminoacetamido-cephemcarbonsaeuren und ihre herstellung. | |
| EP0049499B1 (de) | Neue Cephalosporinderivate, Verfahren zu ihrer Herstellung und Zwischenprodukte dafür sowie entsprechende pharmazeutische Präparate | |
| DD201142A5 (de) | Verfahren zur herstellung von bistetrazolyl-methylsubstituierten cephalosporiantibiotika |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| PUAI | Public reference made under article 153(3) epc to a published international application that has entered the european phase |
Free format text: ORIGINAL CODE: 0009012 |
|
| AK | Designated contracting states |
Kind code of ref document: A1 Designated state(s): BE CH DE FR LU NL SE |
|
| 17P | Request for examination filed | ||
| GRAA | (expected) grant |
Free format text: ORIGINAL CODE: 0009210 |
|
| AK | Designated contracting states |
Kind code of ref document: B1 Designated state(s): BE CH DE FR LU NL SE |
|
| REF | Corresponds to: |
Ref document number: 2860248 Country of ref document: DE Date of ref document: 19810129 |
|
| PG25 | Lapsed in a contracting state [announced via postgrant information from national office to epo] |
Ref country code: LU Free format text: LAPSE BECAUSE OF NON-PAYMENT OF DUE FEES Effective date: 19810630 |
|
| PGFP | Annual fee paid to national office [announced via postgrant information from national office to epo] |
Ref country code: FR Payment date: 19821220 Year of fee payment: 6 |
|
| PGFP | Annual fee paid to national office [announced via postgrant information from national office to epo] |
Ref country code: DE Payment date: 19831212 Year of fee payment: 7 |
|
| PGFP | Annual fee paid to national office [announced via postgrant information from national office to epo] |
Ref country code: LU Payment date: 19840104 Year of fee payment: 7 |
|
| PGFP | Annual fee paid to national office [announced via postgrant information from national office to epo] |
Ref country code: CH Payment date: 19840507 Year of fee payment: 7 |
|
| PGFP | Annual fee paid to national office [announced via postgrant information from national office to epo] |
Ref country code: SE Payment date: 19840630 Year of fee payment: 7 Ref country code: NL Payment date: 19840630 Year of fee payment: 7 Ref country code: BE Payment date: 19840630 Year of fee payment: 7 |
|
| PG25 | Lapsed in a contracting state [announced via postgrant information from national office to epo] |
Ref country code: SE Effective date: 19850602 |
|
| PG25 | Lapsed in a contracting state [announced via postgrant information from national office to epo] |
Ref country code: CH Effective date: 19850630 Ref country code: BE Effective date: 19850630 |
|
| BERE | Be: lapsed |
Owner name: F. HOFFMANN-LA ROCHE & CO. A.G. Effective date: 19850601 |
|
| PG25 | Lapsed in a contracting state [announced via postgrant information from national office to epo] |
Ref country code: NL Effective date: 19860101 |
|
| PG25 | Lapsed in a contracting state [announced via postgrant information from national office to epo] |
Ref country code: FR Free format text: LAPSE BECAUSE OF NON-PAYMENT OF DUE FEES Effective date: 19860228 |
|
| REG | Reference to a national code |
Ref country code: CH Ref legal event code: PL |
|
| PG25 | Lapsed in a contracting state [announced via postgrant information from national office to epo] |
Ref country code: DE Effective date: 19860301 |
|
| NLV4 | Nl: lapsed or anulled due to non-payment of the annual fee | ||
| REG | Reference to a national code |
Ref country code: FR Ref legal event code: ST |
|
| PGFP | Annual fee paid to national office [announced via postgrant information from national office to epo] |
Ref country code: GR Payment date: 19911230 Year of fee payment: 6 |
|
| EUG | Se: european patent has lapsed |
Ref document number: 78100078.1 Effective date: 19860728 |
|
| PLBE | No opposition filed within time limit |
Free format text: ORIGINAL CODE: 0009261 |
|
| STAA | Information on the status of an ep patent application or granted ep patent |
Free format text: STATUS: NO OPPOSITION FILED WITHIN TIME LIMIT |