-
Neurodegenerative
Erkrankungen stellen eine heterogene Gruppe genetischer und erworbener
neurologischer Störungen
dar, die zu einer schweren und fortschreitenden kognitiven und motorischen
Beeinträchtigung
führen,
welche im mittleren bis späten
Lebensalter einsetzt (1). Die häufigste
Ursache der Demenz ist die Alzheimer-Krankheit (Alzheimer's disease, AD). Bei
weniger als 5% der Fälle
der Alzheimer-Krankheit sind genetische Faktoren beteiligt, der
Rest der Fälle
tritt sporadisch auf.
-
Tau-Protein
ist das im Zentralnervensystem exprimierte Protein und spielt im
Neuronen-Gerüst
eine wesentliche Rolle, indem es das intrazelluläre Mikrotubulus-Netzwerk stabilisiert.
Eine Beeinträchtigung
der physiologischen Rolle des Tau-Proteins entweder durch Trunkierung,
Hyperphosphorylierung oder durch Störung des Gleichgewichts zwischen
den sechs natürlich
vorkommenden Tau-Isoformen führt
zur Bildung der neurofibrillären
Bündel
(„neurofibrillary
tangles", NFT),
dystrophischen Neuriten und Neuropilfäden. Diese Gebilde stellen
ultrastrukturelle Kennzeichen der Alzheimer-Krankheit dar. Die wichtigste
Protein-Untereinheit dieser
Gebilde ist das Mikrotubulus-assoziierte Protein Tau (2, 3). Die
Menge des bei Autopsien von AD-Patienten festgestellten NFT korreliert
mit klinischen Symptomen, einschließlich des intellektuellen Verfalls.
Daher spielt das Tau-Protein
eine wesentliche Rolle bei der Pathologie der AD. Die jüngste Entdeckung
der Kosegregation spezifischer Mutationen im Tau-Gen mit der Krankheit
frontotemporale Demenz bei Parkinsonismus in Verbindung mit dem
Chromosom 17 (FTDP-17) bestätigte,
dass bestimmte Abnormitäten
im Tau-Protein eine primäre
Ursache der Neurodegeneration und der Demenz bei betroffenen Individuen
sein kann (4, 5). Es gibt jedoch kein Versuchsmodell, das sich direkt
mit den Details hinsichtlich der Rolle des Tau-Proteins bei der Pathogenese
der AD befassen würde.
-
Jüngste transgene
Modelle der AD basieren auf der Expression von Proteinen, die mit
FAD verbunden sind (APP, PS1, ApoE usw.), die mutiert sind oder
auch nicht. Zu diesen zählen
Tiere, die hinsichtlich eines einzigen oder mehrerer Gene humanisiert
sind. Keines der Modelle fasst beide Merkmale der AD zusammen, gewöhnlich weisen
sie keine neurofibrilläre
Pathologie auf, und keines davon inkludiert die Möglichkeit
der Untersuchung der Funktion von Umwelt-Risikofaktoren, die bei
der Entwicklung der AD eine wesentliche Rolle spielen.
-
Derzeit
verfügbare
Tiermodelle, die gewisse neurofibrilläre Veränderungen aufweisen, basieren
einzig auf der transgenen Expression von mutiertem Tau, das aus
mit dem Chromosom 17 verbundener frontotemporaler Demenz stammt
(FTDP17). Ein typisches Beispiel für diese Gruppe ist die JNPL3-transgene
Maus (6). Weitere Beweise für
die Rolle von mutiertem Tau wurden kürzlich von Goedert und Spillantini
veröffentlicht
(7).
-
Bei
einem anderen transgenen Tiermodell wurde eine Überexpression des 4-Repeat-Tau-Proteins
untersucht. Eine markante Axonopathie in Gehirn und Rückenmark
wurde berichtet, und es wurde gezeigt, dass eine Überexpression
der 4-Repeat-Tau-Protein-Isoform genügt, um die Physiologie von
Neuronen zu verändern.
Im Modell wurden Axonen-Dilatationen mit einer Ansammlung von Neurofilamenten
in den Neuronen des Zentralnervensystems dokumentiert, jedoch ohne
Bildung von intraneuronalen neurofibrillären Bündeln (8).
-
Die
transgene Maus wurde auch hergestellt, um die normale Zellfunktion
von Tau und seine Rolle bei der Pathogenese zu untersuchen. Die
transgene Maus überexprimiert
ein genomisches Tau-Transgen und auch Tau-cDNA-Transgen. Der Vergleich
der beiden Modelle zeigt, dass die Verteilung von Tau bei beiden transgenen
Linien ähnlich
ist. Tau-immunreaktive axonale Schwellungen wurden im Rückenmark
der cDNA-Mäuse
gefunden, was mit einer Abnormität
der hinteren Gliedmaßen
korrelierte, wogegen bei den genomischen Mäusen keine Neuropathologie
festgestellt wurde (9).
-
Trotz
des Vorteils der Ratte im Vergleich zur Maus als Versuchsmodell
in der Neurobiologie überrascht es,
dass kein Tautransgenes Modell für
eine neurofibrilläre
Pathologie erzeugt wurde. Bisher wurde allgemein eine beträchtlich
geringere Menge an transgenen Rattenmodellen der Neurodegeneration
erzeugt. Jedoch keine davon fasst die Tau-Pathologie zusammen, die
für AD
typisch ist.
-
Czech
C. et al (12) beschreiben ein transgenes Rattenmodell, welches Mutationen
in dem für
Presenilin 1 (SP1) codierten Gen aufweist. PS1 wird als Ursache
für die
Mehrheit der Fälle
der früh
einsetzenden familiären
Alzheimer-Krankheit angesehen, jedoch zeigte das veröffentlichte
Modell nicht genügend
Anzeichen für
eine mit AD verbundene Pathologie. Echeverria V. und Cuello AC.
(13) kommentieren die Rolle der intrazellulären Ansammlung von Beta-Amyloid
und der möglichen
neuropathologischen Rolle ei ner intrazellulären Amyloid-beta-Ansammlung
bei der Alzheimer-Krankheit.
Sie präsentieren
jüngste
Beobachtungen aus einem transgenen Rattenmodell mit einem Phänotyp einer
intrazellulären
Ansammlung von A-beta-Fragmenten in Neuronen des Hippocampus und
der Cortex, jedoch ohne Plaque- und NFT-Bildung. Daher gilt für Ratten,
die das am zweithäufigsten
verwendete Tier bei transgenen Untersuchungen sind, dasselbe wie
für Mäuse: in
der wissenschaftlichen Literatur ist keine transgene Ratte beschrieben,
die trunkiertes Tau-Protein exprimieren würde und eine NFT-Bildung zeigte.
-
Bisher
gibt es kein Versuchsmodell zur Untersuchung der Ätiologie
der AD in Verbindung mit Hypertonie oder anderen Risikofaktoren,
wie Diabetes und Dislipidämie,
die mit der AD verbunden sind. Der genetische Hintergrund der transgenen
Versuchstiere spielt eine Rolle bei der Entwicklung eines entsprechenden transgenen
Modells.
-
Es
ist wohlbekannt, dass AD mit bestimmten Umwelt-Risikofaktoren verbunden
ist. Bei epidemiologischen Untersuchungen wurde gezeigt, dass Risikofaktoren
für Gefäßerkrankungen
und Schlaganfall mit einer kognitiven Schädigung und Alzheimer-Krankheit
in Verbindung stehen; außerdem
verstärkt
das Vorliegen einer zerebrovaskulären Erkrankung das Vorhandensein
und die Schwere der klinischen Symptome der Alzheimer-Krankheit
(14). Eine weitere Verbindung zwischen Hypertonie und Demenz vom
AD-Typ ist in einer Rotterdamer Studie aufgezeigt (15).
-
Die
WO 01/53340 A betrifft
transgene Mäuse,
die humanes Tau-Protein
exprimieren. Das humane Tau-Protein können entweder die 6-Isoformen
oder verschiedene Mutanten davon sein.
-
Die
WO 01/65252 A betrifft
ebenfalls ein transgenes Mausmodell, welches mindestens eine Isoform des
humanen Tau-Proteins exprimiert.
-
Die
WO 01/02552 A betrifft
ein transgenes Tiermodell, welches Tau-Protein exprimiert, wobei
die Hyperphosphorylierung von Tau verbessert oder inhibiert wird.
-
Lewis
et al. (Science 293(2001): 1487–1491)
offenbaren die Kreuzung von zwei verschiedenen transgenen Mäusen, einer,
die ein mutiertes Tau-Protein (P30lL Mutante) aufweist, und einer
mutierten APP-Maus, was zu einer doppeltmutierten Nachkommenschaft
führt.
-
Die
WO 96/307366 A betrifft
einen Screening-Test für
Mittel, die die Tau-Tau-Assoziierung modulieren oder inhibieren,
u. a. durch Bestimmung der Bindung von Tau an Tubulin.
-
Novak
et al. (EMBO J. 12(1)(1993): 365–370) offenbaren verschiedene
Tau-Isoformen.
-
Die
WO 01/18546 A offenbart
mehrere trunkierte Formen von Tau-Peptiden.
-
Daher
ist es wichtig, ein Versuchsmodell für AD zu entwickeln, welches
die pathologischen Hauptmerkmale der Krankheit nachahmen würde und
zugleich eine Expression von Umweltfaktoren ermöglicht, verbunden mit der AD-Ätiologie.
-
Es
ist daher ein Ziel der vorliegenden Erfindung, ein Versuchsmodell,
welches die Kennzeichen der AD so genau wie möglich wiedergibt, und auch
das Testsystem für
Substanzen zur Behandlung, Prävention und
Diagnose von AD vorzusehen.
-
Die
vorliegende Erfindung betrifft ein transgenes, nicht-menschliches Tier,
das ein von cDNA codiertes Alzheimer-Tau-Protein im Gehirn der transgenen
Tiere exprimiert. Diese Tiere weisen eine pathologische NF-Aktivität im Gehirn
auf. Die Erfindung betrifft weiters ein transgenes Tier, welches
als Screening-Test-System
beim Verfahren zur Identifizierung von Substanzen verwendet werden
kann, welche das Lernen und Gedächtnis
verbessern, die Neurodegeneration inhibieren und die Rate der Bildung
von neurofibrillären
Bündeln (NFT)
verringern und ihre Eliminierung aus dem Gehirn. Die Tiere können für die Identifizierung
von Substanzen zur Prävention,
Behandlung und Diagnose neurodegenerativer Krankheiten, vorzugsweise
Tauopathien und AD, verwendet werden. Die transgenen Tiere können auch
zur Untersuchung des Einflusses von mit AD verbundenen Risikofaktoren
auf die Entstehung von AD verwendet werden. Eine andere Verwendung
der Tiere liegt im Verfahren zur Identifizierung von Arzneistoff-Zielen.
-
Die
vorliegende Erfindung beschreibt das Herstellen transgener Tiere,
wobei AD-Veränderungen
erzeugt werden, die durch ein spezifisches Transgen induziert werden,
was einer Alzheimer-Krankheit
in diesen Tieren ähnlich
ist. Dies liefert ein Untersuchungswerkzeug für die Entdeckung und Entwicklung
von Arzneistoffen und die Diagnose und für die weitere Untersuchung
der Rolle normaler und erkrankter Tau-Proteine in vivo.
-
Die
vorliegende Erfindung beruht auf einer Induktion einer NF-pathologischen
Aktivität
im Gehirn von Tieren einzig durch Expression von Alzheimer-Tau-Protein
in den Gehirnen transgener Tiere. Merkmale der AD werden in Tieren
induziert, die zur Induktion von mit der Ätiologie von AD verbundenen
Risikofaktoren neigen, was ein weiterer Vorteil der vorliegenden
Erfindung ist.
-
Alle
bei der Beschreibung bevorzugter Ausführungsformen verwendeten technischen
und wissenschaftlichen Ausdrücke
haben – sofern
nicht anders angegeben – dieselbe
Bedeutung wie sie allgemein auf dem Fachgebiet, zu welchem diese
Erfindung gehört,
verstanden werden. Die bevorzugten Methoden, die Laborverfahren
bei der Zellkultur, Molekulargenetik, Biochemie und Nukleinsäurechemie
und Materialien sind in der Erfindung beschrieben, aber jegliche
Methoden und Materialien, die ähnlich
oder äquivalent
sind, können beim
Testen der vorliegenden Erfindung verwendet werden. Für Verfahren
wie die rekombinante Nukleinsäure-Herstellung,
biochemische Analyse, Zellkultur und transgene Einarbeitung, wie
die Elektroporation, Lipofektion und Mikroinjektion, werden Standardtechniken
verwendet.
-
Der
Ausdruck „Alzheimer-Tau" bezieht sich auf
die Gruppe spezifisch trunkierter Isoformen von Tau-Protein, die
genetisch hergestellt wurden, welche jenen entspricht, die ausschließlich im
an AD erkrankten Gehirn vorhanden sind. Das Alzheimer-Tau kann eine
NF-Aktivität
selbst oder in Kombination mit anderen Molekülen im Gehirn induzieren. Wie
hierin verwendet, bezieht sich der Ausdruck Alzheimer-Tau-Protein
auf die Gruppe trunkierter Tau-Formen, die im humanen Hirngewebe
mit Alzheimer-Krankheit vorhanden ist.
-
Der
Ausdruck „transgen" wird hierin verwendet,
um genetisches Material zu beschreiben, das künstlich in das Genom einer
Zelle, insbesondere einer Säuger-Zelle,
insertiert wurde zwecks Implantation in ein lebendes Tier. Für bestimmte
Länder
kann es notwendig sein, einen bestimmten Gegenstand aus diesem Aspekt spezifisch
auszuschließen,
wie humane totipotente Stammzellen als solche oder Verfahren, die
zu solchen Zellen führen,
die unter Art. 6 (1) und (2) der EU-Richtlinie 98/44/EC fallen.
-
Mit „Alzheimer-Krankheit" (hierin als „AD" abgekürzt) ist
ein Zustand gemeint, der mit der Bildung von neurofibrillären Bündeln und
Beta-Amyloid-Plaques sowie mit der Beeinträchtigung sowohl des Lernens
als auch des Gedächtnisses
verbunden ist. Wie hierin verwendet, soll „AD" sowohl AD als auch AD-artige Pathologien
umfassen, d. h. Erkrankungen des Zentralnervensystems mit Symptomen,
die der AD ähnlich
sind.
-
Mit „neurofibrillärer Aktivität" (hierin als „NF"-Aktivität abgekürzt) ist
ein Zustand gemeint, der mit der Bildung von neurofibrillären Bündeln im
Zentralnervensystem mit Symptomen, die der AD ähnlich sind, verbunden ist.
-
Mit „der AD ähnlichen
Symptonen" und „mit AD
verbundenem Phänomen" ist eine strukturelle,
molekulare oder funktionelle, mit der AD verbundene Begebenheit
gemeint, insbesondere eine solche Begebenheit, die in einem Tiermodell
leicht beurteilbar ist. Zu solchen Begebenheiten gehören – ohne Einschränkung darauf – neurofibrilläre Pathologie,
Lern- und Gedächtnisdefizite
und andere mit der AD verbundene Merkmale.
-
Mit „transgenem
Tier" ist ein nicht-menschliches
Tier, gewöhnlich
ein Säugetier
(z. B. eine Maus, eine Ratte, ein Kaninchen, ein Hamster usw.) gemeint,
das eine nicht-endogene (d. h. heterologe) Nukleinsäuresequenz
hat, die als extrachromosomales Element in einem Teil seiner Zelle
vorliegt oder stabil integriert ist in seine Keimbahn-DNA (d. h.
in der Genom-Sequenz der meisten oder aller seiner Zellen). Heterologe
Nukleinsäure
wird in die Keimbahn solcher transgener Tiere mittels Genmanipulation
von beispielsweise Embryonen des Wirtstieres eingeführt.
-
Mit „Konstrukt" ist eine rekombinante
Nukleinsäuresequenz,
im Allgemeinen rekombinante DNA-Sequenzen gemeint, die mit einem
gewebespezifischen oder allgemeinen Promotor funktionell verknüpft sind, welcher
erzeugt wird zum Zweck der Expression von (einer) spezifischen Nukleotidsequenz(en)
in Säugerzellen,
oder welcher bei der Konstruktion anderer rekombinanter Nukleotidsequenzen
verwendet werden soll.
-
Die
vorliegende Erfindung sieht die Struktur, Sequenz und das Verfahren
zur Erzeugung von DNA-Konstrukten zur Verwendung für die Herstellung
von transgenen Tieren vor, gekennzeichnet durch die folgenden Merkmale:
Ein
transgenes, nicht-menschliches Tier, dessen Keim- und/oder Soma-Zellen ein DNA-Konstrukt
aufweisen, das eine Codierregion enthält, welche zur Expression eines
N- und C-terminal trunkierten Tau-Moleküls führt, wobei
- – die Codierregion
zumindest 30 Nukleotide stromabwärts
vom Start-Codon trunkiert und zumindest 30 Nukleotide stromaufwärts vom
Stop-Codon der Gesamtlängen-Tau-cDNA-Sequenz,
die für
4-repeat bzw. 3-repeat-Tau-Protein codiert, trunkiert ist,
- – der
minimal trunkierte Tau-Kern ein Proteinfragment umfasst, das durch
SEQ ID Nr. 9 codiert ist,
- – das
DNA-Konstrukt für
ein Protein codiert, welches eine eine neurofibrilläre (NF)
Krankheit erzeugende Aktivität
aufweist, wenn es in Hirnzellen des Tiers exprimiert wird.
-
Diese
NF-Pathologie-erzeugende Aktivität
kann durch Zählungen
der neurofibrillären
Bündel
pro ausgewählter
Hirnregion, d. h. unter Verwendung eines Stereologie-Ansatzes, quantifiziert
werden. Alternativ können
neurobehaviorale Tests für
die verlässliche
Evaluierung kognitiver Werte bei lernenden Gedächtnisaufgaben verwendet werden.
-
Besonders
bevorzugte Tau-DNA-Konstrukte gemäß der vorliegenden Erfindung
umfassen eine Nukleotidsequenz ausgewählt aus der Gruppe der SEQ
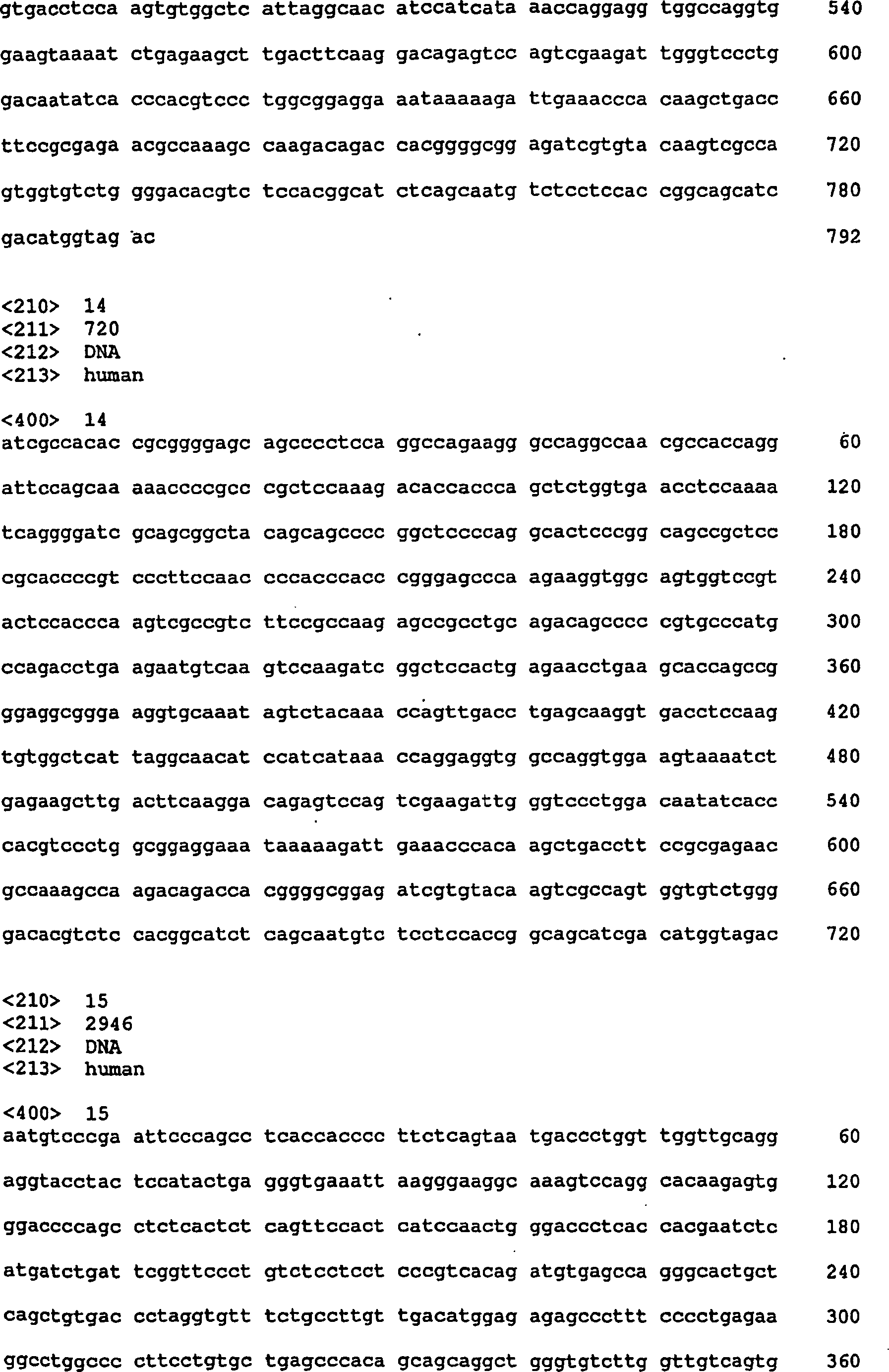
ID Nr. 1 bis 14. Die Sequenzen sind in 1 dargestellt.
-
Bei
einer bevorzugten Ausführungsform
der Erfindung stellen diese DNA-Konstrukte eine Gruppe von N- und
C-terminal doppelttrunkierten cDNAs dar, die die folgenden Nukleotid-Sequenzen
umfassen (Derivate von 4-Repeat-Tau (Tau 43) sind mit R4 bezeichnet,
und Derivate von 3-Repeat-Tau (Tau 44) sind mit R3 bezeichnet).
Die hier verwendete Nummerierung stammt von der in Goedert et al.
(24) beschriebenen Gesamtlängen-Tau-cDNA:
-
Die
trunkierten Tau-Sequenzen können
wegen der spezifischen Wirtszelle, in welche das Konstrukt transferiert
wird, adaptiert werden (Codon-Verwendung, Codon-Präferenzen,
Homolog-Adaptationen (Austauschen eines oder mehrerer der humanen
Codons mit dem Wirtszellen-Codon, wenn Unterschiede vorliegen)).
-
Bevorzugte Merkmale der Konstrukte:
-
Die
obigen cDNA-Sequenzen sind mit regulatorischen Sequenzen verbunden,
um eine Expression von trunkiertem Tau-Protein im Gehirn anzutreiben.
Die Modifikation des Thy-1-Gens (25) erfolgte so, dass die regulatorische
Sequenz, die eine Expression in T-Zellen lenkt, deletiert und eine trunkierte
cDNA-Sequenz zwischen die Spe-I und die Xho-Restriktionsstellen
eingeführt
wurde. Das modifizierte Konstrukt wurde von prokaryontischen Sequenzen
befreit und über
eine Mikroinjektion in einen männlichen
Pronukleus eingeführt.
Jegliche funktionellen Promotoren oder Promotor-Verstärker-Komplexe
können
für die
Expression der oben beschriebenen trunkierten Tau-cDNAs verwendet
werden.
-
Die
vorliegende Erfindung offenbart auch ein Verfahren zur Herstellung
und zum Testen von Molekülen gemäß der vorliegenden
Erfindung, gekennzeichnet durch die folgenden Schritte:
- (a) Konstruieren eines rekombinanten Prokaryonten-Klonierplasmids,
das Codiersequenzen für
ein doppelttrunkiertes Tau-Molekül
mit Deletionen trägt,
die sich zumindest auf die ersten 30 und die letzten 30 Nukleotide
von 3- oder 4-Repeat-Tau-cDNA-Molekülen erstrecken,
- (b) Konstruieren eines eukaryontischen Expressionsplasmids,
das geeignete Promotoren für
eine Gehirn-Expression oder für
eine ubiquitäre
Expression und entsprechende cDNA-Sequenzen von trunkierten Tau-Molekülen und
die Kombinationen davon tragen,
- (c) Züchten
von Bakterien, die diese Plasmide enthalten, und Amplifizieren der
Plasmide und ihre Extraktion in großen Mengen,
- (d) Transfizieren der Gen-Konstrukte in COS-7-Zellen und ihre
Analyse unter Verwendung der Western-Blot-Technik,
- (e) Isolieren und Reinigen des Gen-Konstrukts, so dass alle
prokaryontischen Sequenzen ausgeschlossen werden, und Verdünnen von
Transgenen in einem Puffer in einer für Mikroinjektion geeigneten
Konzentration (vgl. Beispiel 1),
- (f) Verifizieren der für
eine Mikroinjektion bestimmten Gen-Konstrukte.
-
Dies
erfolgt mittels Restriktionsanalyse, Gensequenzierung und Protein-Analyse
nach transienten Transfektionen in Säugetier-Zellen, wonach die
korrekte Größe der Proteine
und ihre Reaktivität
mit spezifischen monoklonalen Antikörpern evaluiert wird (vgl.
Beispiel 1, 2.b).
-
Die
vorliegende Erfindung sieht daher ein transgenes, nicht-menschliches Tier
vor, dessen Keim- und/oder Soma-Zellen das DNA-Konstrukt aufweisen,
welches für
Alzheimer-Tau-Protein codiert, und welches als geeignetes Tiermodell
der Alzheimer-Krankheit
verwendet werden kann.
-
Es
ist daher ein Ziel der vorliegenden Erfindung, ein transgenes, nicht-menschliches
Tier vorzusehen, dessen gesamte Keim- und/oder Soma-Zellen die humanen trunkierten
Tau-cDNA-Moleküle
aufweisen. Die klonierte humane Alzheimer-Tau-cDNA-Sequenz ist mit
einer Promotor-Sequenz verbunden, welche die Expression des Alzheimer-Tau
in gewebespezifischer Weise oder ubiquitär lenkt.
-
Transgene
Tiere der Erfindung werden hergestellt, indem man die wohlbekannten
regulären
Verfahren einer Mikroinjektion in den männlichen Pronukleus von einen
Tag alten fruchtbaren Embryonen von Ratten verwendet. Die Transgene
können
auch mittels anderer, auf dem Gebiet bekannter Methoden, einschließlich Transfektion,
Lipofektion, Elektroporation und mit Hilfe von Retroviren oder mit
anderen Mitteln in Embryo-Zellen eingeführt werden. Embryonen, die
das Transgen tragen, können
dann in scheinschwangere Tiere implantiert werden.
-
Es
ist daher ein Ziel der Erfindung, ein Verfahren zur Genotypisierung
von neugeborenen Tieren vorzusehen. Die PCR-Analyse unter Verwendung
von spezifischen Oligonukleotiden, die eine Amplifikation von Ziel-Sequenzen
des Transgens ermöglichen,
wird daher für
diesen Zweck eingesetzt. Für
die Genotypisierung verwendete Oligonukleotide wurden auf eine Weise
entworfen, dass die Transkriptions-Initiierungsstelle des Transgens
einschließlich
des ATG-Codons und der Kozak-Sequenz schließlich mittels DNA-Sequenzierung des
PCR-Produkts verifiziert werden konnten (Primer-Paar A). Außerdem lagert
sich ein Primer an den heterogenen Promotor an, und ein anderer
Primer lagert sich an die für
Alzheimer-Tau-Protein codierende Nukleotid-Sequenz an. Ähnliche
Gestaltungskriterien wurden für
das Stop-Codon angewendet (Primer-Paar B). Die Integrität des Transgens
kann daher auf diese Weise überwacht
werden. Sequenzen der diagnostischen Oligonu kleotide sind daher
wie folgt:
-
Die
erwartete Größe des PCR-Produkts
ist 438 Nukleotide.
-
Das
Vorhandensein des PCR-Fragments ist daher für Tiere spezifisch, die das
Transgen ins Genom integriert haben (vgl. Beispiel 2).
-
Die
Gründer-Tiere
(„founder
animals") können zum
Züchten
mit Wildtyp-Tieren verwendet werden, um die F1-Generation der Tiere
zu erzeugen, die für
das Transgen heterozygot sind. Bei weiteren Ausführungsformen können diese
heterozygoten Tiere untereinander gekreuzt werden, um lebensfähige transgene
Embryonen zu erhalten, deren Soma- und Keim-Zellen für die für das Alzheimer-Tau-Protein codierenden
Gene homozygot sind.
-
Ein
weiteres Ziel der vorliegenden Erfindung ist es, nicht-menschliche Tiere
vorzusehen, deren Keim- und Soma-Zellen das für das Alzheimer-Tau-Protein
codierende DNA-Konstrukt transient oder stabil exprimieren und die
eine NF-Pathologie im Gehirn aufweisen. Das bevorzugte Tier dieser
Erfindung ist eine Ratte, wobei das von den DNA-Molekülen codierte
Protein im Gehirn exprimiert wird.
-
Die
am meisten bevorzugte Ausführungsform
der vorliegenden Erfindung ist ein transgenes, nicht-menschliches
Tier, bei welchem das durch die DNA-Moleküle codierte Alzheimer-Tau-Protein
im Gehirn des Tiers exprimiert wird. Die Expression des Alzheimer-Tau
wurde mittels mehrerer monoklonaler Antikörper nachgewiesen, wie in Beispiel
3 beschrieben und in 3 dokumentiert. Die Expression
des Proteins in verschiedenen Hirnregionen der transgenen Abstammungslinie
ist in 4 dokumentiert.
-
Die
vorliegende Erfindung sieht daher ein transgenes, nicht-menschliches Tier
vor, bei welchem für das
Alzheimer-Tau-Protein codierende DNA-Moleküle in das Genom des Tiers stabil
integriert sind oder auf andere Weise im Zellkern anwesend sind,
damit sie transkribiert werden. Diese Tiere sind durch die folgenden Merkmale
gekennzeichnet:
- – Transgene werden auf nachfolgende
Generationen von Tieren gemäß den Mendelschen
Gesetzen übertragen,
wobei sie eine transgene Abstammungslinie bilden (vgl. 4)
- – das
ererbte Transgen exprimiert trunkierte Proteine in den Gehirnen
der Gründer-Tiere
und der Nachkommenschaft, wie in Beispiel 3, 4 gezeigt.
-
Die
vorliegende Erfindung sieht daher die transgenen, nicht-menschlichen Tiere
vor, welche eine neurofibrilläre
Pathologie im Zentralnervensystem (ZNS) aufweisen. Diese Tiere sind
durch die folgenden Merkmale gekennzeichnet:
- – Expression
trunkierter Tau-Proteine fördert
die Bildung der neurofibrillären
Pathologie (Beispiel 5).
- – PHF-1-immunreaktive
NFTs zeigten, dass endogenes normales Ratten-Tau an der Bildung
von NFTs beteiligt ist (Beispiel 5).
- – Neurofibrilläre Bündel sind
als intrazelluläre
Einschlüsse
und Filamente in den Neuronen des ZNS vorhanden und sind homolog
zu NFT in humanen, an AD erkrankten Gehirnen.
- – Immunfluoreszenz
zeigte das Vorhandensein kleiner, stabartiger Strukturen ähnlich jenen,
die bei präklinischer
Alzheimer-Krankheit
im humanen Hirngewebe beobachtet werden (vgl. Beispiel 5).
-
Bei
der bevorzugten Ausführungsform
der Erfindung weisen transgene Tiere Neuropathologien wie neurofibrilläre Bündel, Geisterfibrillen
(„ghost
tangles") und Neuropil-Fäden, die
ameisensäureempfindlich sind,
auf. Neurofibrilläre
Bündel
sind aus einer abnormen Ansammlung intraneuronaler Filamente zusammengesetzt.
Die Bündelbestandteile
bestehen aus Alzheimer-Tau sowie aus normalen Tau-Molekülen. Solche transgene
Tiere dienen als geeignetes Modellsystem zur Untersuchung der Alzheimer-Krankheit
und Entwicklung therapeutischer, präventiver und diagnostischer
Substanzen.
-
Die
Erfindung sieht ein transgenes Tier vor, das eine NF-Pathologie
entwickelt und einen genetischen Hintergrund hat, der die Induktion
von mit AD verbundenen Risikofaktoren ermöglicht, wodurch es ein Krankheitsmodell
für Menschen
darstellt.
-
Die
vorliegende Erfindung sieht daher ein transgenes, nicht-menschliches Tier
vor, bei welchem der genetische Hintergrund, in welchem die DNA-Moleküle im Genom
spontan hypertoner Tiere stabil integriert oder in anderer Weise
im Zellkern vorhanden sind, damit sie innerhalb des spezifischen
genetischen Hintergrunds transkribiert werden.
-
Ein
anderer Aspekt der Erfindung ist das Vorsehen eines Tiermodells,
umfassend die Kombination genetischer Faktoren und anderer, mit
AD verbundener Risikofaktoren wie folgt:
- – Hypertonie,
die der häufigste
Risikofaktor der AD ist,
- – Diabetes,
die durch die Ernährung
induziert sein kann (Diabetes ist ein wichtiger Risikofaktor der
AD),
- – Hypercholesterinämie, die
durch die Ernährung
induziert sein kann (ein weiterer wichtiger Risikofaktor der AD).
-
Diese
pathologischen Situationen können
im vorgesehenen Tiermodell leicht induziert werden. Geeignete Beispiele
wurden früher
in der Literatur berichtet (z. B. in 26, 27, 28).
-
Außerdem ist
das vorgesehene Tiermodell das erste Tiermodell, welches neurofibrilläre Pathologie
auf dem genetischen Hintergrund von SHR exprimiert.
-
Gemäß einem
anderen Aspekt sieht die vorliegende Erfindung ein Tier vor, welches
ein Versuchsmodell für
sporadische Alzheimer-Krankheit darstellt, wobei das Modell eine
Beurteilung der Rolle von mit der AD-Entwicklung verbundenen Risikofaktoren
gestattet. Risikofaktoren spielen bei der großen Mehrheit der AD-Fälle eine wesentliche Rolle,
das Modell kann daher als ein Modell for sporadische AD angesehen
werden, welche 90% aller Fälle
der AD-Neurodegenerationen ausmacht.
-
Bei
einer anderen bevorzugten Ausführungsform
sieht die vorliegende Erfindung ein Verfahren zum Screenen und zur
Validierung von Substanzen für
die Behandlung, Prävention
und Diagnose von Alzheimer-Krankheit, zur Behandlung und Prävention
von Tauopathien, vorzugsweise AD, zur Entwicklung diagnostischer
Marker und Sonden für
die Detektion von Tauopathien, vorzugsweise AD, und für Substanzen
zur Behandlung der Hypertonie, Diabetes, Dislipidämie und
Hypercholesterinämie
in Verbindung mit Tauopathien, vorzugsweise AD, vor, welches umfasst:
- – Evaluieren
der Substanzen durch:
- – Nachweisen
von Veränderungen
einer neurofibrillären
Krankheit bei den Tieren,
- – Messen
der neurobehavioralen Veränderungen
bei transgenen Tieren,
- – Messen
des kognitiven Werts bei transgenen Tieren,
- – chemisches
Messen von AD-spezifischen Markern in Tiergeweben und Körperflüssigkeiten.
-
Die
vorliegende Erfindung sieht daher einen In-vivo-Test zur Bewertung
der Wirksamkeit von Substanzen oder von Therapien, insbesondere
von NFT-reduzierenden oder verhindernden Therapien, vor. Die Tiere können zum
Screenen von Substanzen oder Therapien für neurodegenerative Erkrankungen,
insbesondere Tauopathien, vorzugsweise AD und andere neurodegenerative
Erkrankungen, die mit der Bildung von neurofibrillären Bündeln einhergehen,
verwendet werden.
-
Daher
sieht die vorliegende Erfindung ein Modellsystem vor, das aus transgenen
Tieren, Zellen und Tests besteht, die bei der Untersuchung der Ätiologie
und Behandlung der Alzheimer-Krankheit nützlich sind. Die Tests sind
auch zum Screenen auf Substanzen, die die Bildung einer neurofibrillären Pathologie
inhibieren, und anderer therapeutischer Wirkungen der Substanzen
nützlich.
-
Gemäß einem
anderen Aspekt sieht die vorliegende Erfindung eine nicht-menschliche
totipotente Zelllinie vor, die ein Konstrukt umfasst, das, wie oben
erwähnt,
für trunkiertes
Tau codiert.
-
Die
transgenen Tiere der vorliegenden Erfindung und davon abstammende
Tierzellen werden zum Screenen von Verbindungen hinsichtlich einer
möglichen
Wirkung bei der Behandlung der Alzheimer-Krankheit unter Verwendung
von Standard-Methodiken verwendet. Die Verbindung wird über einen
Zeitraum und in verschiedenen Dosierungen den Tieren verabreicht
oder in die Kulturmedien eingebracht, danach werden die Tiere oder
die Tierzellen auf Veränderungen
in der Histopathologie bzw. in der Expression von Alzheimer-Tau untersucht.
Weiters ermöglicht
die Durchführbarkeit
neurobehavioraler Tests an den transgenen Tieren eine Überwachung
der kognitiven Funktion nach der Behandlung mit potentiellen therapeutischen
Mitteln. Das Screenen von Verbindungen führt zur Selektion bestimmter
Mittel für
die Verhinderung oder Behandlung oder Diagnose der Alzheimer-Krankheit.
Dem Fachmann sind viele Variationen von Screening-Methoden bekannt und
können
im Rahmen der vorliegenden Erfindung angewendet werden.
-
Das
transgene Tiermodell der vorliegenden Erfindung kann auch zum Entschlüsseln der
molekularen Kaskade von Ereignissen, die zu einer Neurodegeneration
und zur Alzheimer-Krankheit führen,
verwendet werden, so dass therapeutische Ziele identifizert werden
können.
-
Noch
ein anderer Aspekt der Erfindung ist das Vorsehen eines In-vitro-Tests
auf der Basis von Zelllinien, die von einem transgenen Tier stammen,
oder einer Zelllinie, die von einem transgenen Ratten-Embryo der
vorliegenden Erfindung stammt, wobei der Test auch als ein Screening-
und Validierungswerkzeug für
die Entdeckung und Entwicklung der Alzheimer-Diagnose und von Alzheimer-Markern
verwendet wird. Dieser In-vitro-Test basiert auf den Zelllinien
und kann auch als Screening- und Validierungswerkzeug zur Entdeckung therapeutischer
und präventiver
Anti-Alzheimer-Arzneimittel verwendet werden.
-
Die
folgenden Beispiele werden zur Illustration angeführt, und
weil verschiedene andere Ausführungsformen
für den
Fachmann offensichtlich sind, ist das Folgende nicht als Einschränkung des
Umfangs der Erfindung auszulegen.
-
KURZE BESCHREIBUNG DER FIGUREN
-
1:
Schema von für
die Erzeugung von Gen-Expressions-Konstrukten verwendeten Alzheimer-Tau-Protein-cDNAs,
die bei der Produktion transgener Tiere der vorliegenden Erfindung
verwendet wurden.
-
2:
Herstellung und Verifizierung von für die Produktion transgener
Tiere verwendeten Gen-Konstrukten. Die Konstruktion transgener Tiere
wurde über
die pronukleare Mikroinjektion klonierter Gen-Konstrukte, die die
Codiersequenz für
Alzheimer-Tau enthielten, durchgeführt. Die Gen-Konstrukte wurden
durch Restriktionsanalyse und PCR unter Verwendung Transgen-spezifischer
Primer (Tafel A, Agarose-Gel von PCR-amplifiziertem DNA-Fragment)
sowie mittels DNA-Sequenzierung für eine Kontrolle auf potentielle
Mutationen verifiziert. Auf die Verifizierung folgte eine Reinigung
der Gen-Konstrukte (Tafel B, Agarose-Gel des reinen Transgen-Fragments)
und transiente Transfektionen in Sängerzellen (Tafel C, Western-Blot-Verifizierung der
Protein-Expression).
Nachdem die Tests fertiggestellt waren, wurden die Konstrukte von
prokaryontischen Sequenzen befreit und in einen Tag alte Ratten-Embryonen
injiziert. Das untere Flussdiagramm zeigt eine vereinfachte Vorgangsweise
der Produktion transgener Tiere.
-
3:
Genotypisierung der transgenen Gründer-Tiere und der F1-Generation
der transgenen Tiere. Tafel „A" zeigt Kontrollen
für das
Genotypisier-Experiment (+C: positive Kontrolle; NAC: keine Amplifikationskontrolle;
NTC: keine Matrizen-Kontrolle). Tafel „B" ziegt Ergebnisse der PCR-Genotypisierung.
Probe Nr. 12 stellt ein Transgen-positives Tier dar. Tafel „C" umreißt die Zuchtversuche,
die durchgeführt
wurden, um die Gründer-Tiere
zu bestätigen.
Weiters zeigt die Tafel die transgene Linie der vorliegenden Erfindung,
die das Transgen auf die nachfolgenden Generationen gemäß der Mendelschen
Gesetze übertragen
hat..
-
4:
Expression des Alzheimer-Tau-Proteins im Gehirn der transgenen Ratte.
Die linke Tafel zeigt eine Western-Blot-Analyse, und die rechte
Tafel zeigt die Gesamtmenge der pro Bahn geladenen Proteine. Das
Alzheimer-Tau-Protein wandert mit der Größe von 35 kD (Bahn 1, Pfeil),
durch den monoklonalen pan-Tau-Antikörper DC25
nachgewiesen. Für
den Western-Blot wurde eine ECL-Technik verwendet, und ein spezifisches
Signal wurde nach 1-minütiger Einwirkung
beobachtet. Die 7,5 μg
des Gesamt-Protein-Extrakts aus
den Gehirn-Lysaten des transgenen Tiers wurden geladen (Bahn 1),
wogegen 25 μg
Proteine von Wildtyp-Kontroll-Tieren geladen wurden. M: Molekülgrößen-Marker.
-
5:
Expression von Alzheimer-Tau-Protein in verschiedenen Hirnregionen
der transgenen Ratte. Western-Blot-Analyse der Gesamt-Protein-Lysate
aus Hirnregionen der transgenen Ratte. Bahn 1, vollständiges Gehirn-Lysat
des Gründer-Tiers
(Generation F0) – 10 μg Proteine;
Bahn 2: Gesamt-Gehirn-Lysat eines transgenen Tiers der F2-Generation;
Bahnen 3–6:
Protein-Lysate eines transgenen Tiers der F2-Generation. 3 – Hippocampus,
4 – subkortikale
Fläche,
5 – Großhirnrinde,
6 – Rückenmark
und Medulla; Bahnen 7–8
repräsentieren
Gehirn-Lysate aus nicht-transgenen Kontroll-Nachkommen desselben
Wurfs der F2-Generation: 7 – Cortex,
8 – Cerebellum
(die gesamte Protein-Beladung pro Bahnen 2–8 betrug 20 μg).
-
6:
Silberfärbung
der Gehirn-Schnitte vom transgenen Tier und nicht-transgenen Wildtyp-Kontrolltier.
Intrazelluläre
Einschlüsse
und neurofibrilläre
Filamente wurden in den Neuronen des ZNS der transgenen Ratte nachgewiesen
(Bahn B und C: transgenes Tier). Wildtyp-Ratten zeigen diese Strukturen
im homologen Hirnbereich nicht (A: Wildtyp-Kontrolle). Vergrößerung:
200 × (A
und B), 400 × (C).
-
7:
Detektion neurofibrillärer
Bündel
unter Verwendung des monoklonalen pan-Tau-Antikörpers DC 25 im Zentralnervensystem
des transgenen Tiers mAk DC25 erkennt NFTs in den Neuronen von AD-Patienten.
Die äquivalenten
Strukturen werden im Gehirn der transgenen Ratte erkannt (Tafeln
B und D). Wildtyp-Ratten wiesen keine ähnlichen Strukturen im homologen
Hirnbereich auf (A, C). Vergrößerung:
100 × (A, B),
200 × (C,
D).
-
8:
Detektion neurofribrillärer
Bündel
mittels monoklonalem Antikörper
PHF-1 im Zentralnervensystem des transgenen Tiers. PHF-1 ist der
spezifische Marker für
Tau-Phosporylierung. Eine Immunreaktivität mit diesem Antikörper zeigt,
dass bei der Expression von Alzheimer-Tau endogenes Tau im Prozess
der Bildung von NFTs beteiligt ist. Weiters zeigt die Immunfluoreszenz-Färbung kleine stabartige Strukturen, ähnlich jenen,
die im Hirngewebe bei präklinischer
Alzheimer-Krankheit beobachtet wird. Vergrößerung: 100 × (A), 200 × (B), 1000 × (C, D).
-
9:
Neuronale Zellkultur als Screening-Testsystem zur Charakterisierung
von Therapie-Ansätzen („therapeutic
leads") und Arzneimittel-Anwärtern. Primärkulturen
transgener und nicht-transgener
Ratten-Neuronen können
zu diesem Zweck nach Züchtung
in vitro verwendet werden, und die Wirkung der Arzneimittel-Anwärter auf
den mitochondrialen Transport kann unter Verwendung der Videomikroskopie
ausgewertet werden. Neuronen der Cortex (C ×) und des Hippocampus (Hipp),
die mit Vitalfarbstoff (z. B. Mito-trek) beladen wurden, sind nach
3 Tagen In-vitro-Züchtung
(3DIV) gezeigt. Die Mitochondrien (MT) sind sichtbar gemacht.
-
10:
Histopathologische Merkmale der Alzheimer-Krankheit, zusammengefasst
im transgenen Tier der vorliegenden Erfindung. Die dargestellte
neurofibrilläre
Pathologie ist eines der wesentlichen Merkmale der Alzheimer-Krankheit. 10 zeigt
einen Vergleich der durch Gallyas-Silbertechnik (A, C) und auch
durch Immunhistochemie (E) im menschlichen Gehirn mit AD nachgewiesenen
neurofibrillären
Bündel
mit im transgenen Tier der vorliegenden Erfindung beobachteten äquivalenten
pathologischen Strukturen. Die immunochemische Färbung erfolgte mit dem monoklonalen
Antikörper
7.51, der das generische Tau-Epitop in der Tandem-Repeat-Region
erkennt (29).
-
BEISPIELE:
-
BEISPIEL 1: Design von Gen-Konstrukten,
die eine DNA-Sequenz enthalten, die für Alzheimer-Tau-Protein codiert – humanes
trunkiertes Tau-Gen; Herstellung und Verifizierung der Gen-Konstrukte
für ubiquitäre und Gewebe-spezifische
Expression in transgenen Tieren.
-
Die
Konstruktion der Alzheimer-Tau-Expressionsvektoren besteht aus Maßnahmen,
welche inkludieren:
- – das Entwerfen einer Codiersequenz,
insbesondere Deletionen und Trunkierungen sind in 1 gezeigt;
- – diese
Teile des Tau-Gens wurden PCR-amplifiziert mit Hilfe der „proofreading"-DNA-Polymerase und
von Oligonukleotiden, die mit geeigneten Restriktionssequenzen ausgestattet
waren, so dass sie sie unter allgemeinen oder gewebespezifischen
Promotoren in einen eukaryontischen Expressionsvektor kloniert werden
können;
die Klonierung erfolgte unter Verwendung von Standard-Methoden in
gewöhnlichen
Bakterienstämmen;
- – Verifizierung
der klonierten Gene wurde durchgeführt, um die Ausrichtung des
insertierten Gens zu überprüfen, welche
durch Restriktionsverdaue und/oder PCR-Analyse bestätigt wurde
( 2A). Außerdem wurden die Konstrukte
teilweise sequenziert, um die möglichen
mutierten Formen auszuschließen;
- – Reinigung
des für
die Mikroinjektion bestimmten Fragments (2B);
- – Verifizierung
der Protein-Expression unter Verwendung von Transfektionen des Transgens
in Säuger-Zellen,
hauptsächlich
COS-7 und C6- Ratten-Gliom-Zellen, und Analyse der Expression der
Proteine in eukaryontischen Zellen mit der Western-Blot-Methode
(2C).
-
Alle
Methoden sind in einem Handbuch beschrieben: Sambrook et al., Molecular
Cloning, A Laboratory Manual, Cold spring Harbor Laboratory Press,
1989 (14).
-
BEISPIEL 2: Erzeugung der transgenen Ratte
-
Das
klonierte Gen-Konstrukt, das die für Alzheimer-Tau codierende
Sequenz enthielt, wurde in den männlichen
Pronukleus von einen Tag alten Embryonen injiziert. Befruchtete
Eier wurden aus den weiblichen SHR-Donor-Tieren in separaten Versuchen
unter Verwendung von Routine-Techniken extrahiert (15). Nach der
Mikroinjektion der DNA wurden die Zygoten in vitro im CO2-Inkubator etwa 12 Stunden lang gezüchtet und in
die Eileiter von scheinschwangeren Ziehmüttern implantiert. Die Gründer wurden
mittels PCR der transgen-spezifischen Zielsequenz von Genom-DNA
identifiziert. Um die Tau-Genotypen zu bestimmen, wurde Genom-DNA
von etwa 0,5 cm des Schwanzes, die von jeder Ratte entnommen wurden,
gereinigt. Die PCR-Analyse wurde zur Identifizierung der Nachkommenschaft,
die das Transgen enthielt, verwendet. Oligonukleotide für diagnostisches
PCR-Screening wurden so entworfen, dass die Integrität des Transgens
leicht bestimmt werden konnte. Zur Bestimmung der Anzahl der in
das Ratten-Genom integrierten Transgen-Kopien wurde eine Echtzeit-PCR-Analyse
verwendet.
-
Beispielsweise
enthielt die Tg-Linie #318 4 Kopien des Transgens, was mittels Echtzeit-PCR
unter Verwendung der Sybre-Green-Methode
und des BioRad-PCR-Geräts
bestimmt wurde.
-
BEISPIEL 3: Genotypisierung von Tieren,
die nach Embryo-Implantation in Ziehmütter geboren wurden, Identifizierung
transgener Tiere und Beurteilung der Übertragung des Transgens an
nachfolgende Generationen
-
Aus
Schwanzspitzen extrahierte DNA: Genom-DNA wurde mit dem DNeasy tissue
kit, Quiagen, extrahiert.
-
Genotypisierung:
Eine spezifische Amplifizierung von Transgenen, die für doppelttrunkierte
Tau-Formen codieren, wurde an Genom-DNA durchgeführt, die von der Eltern-Generation
transgener Tiere stammte und ist in den 3A und 3B gezeigt. Eine weitere Analyse der Genom-DNA
der F1-Generation zeigte, dass Transgene erblich sind, da sie auch
in der Nachkommenschaft der Eltern-Generation identifiziert wurden. Transgene,
die für
Alzheimer-Tau codieren,
sind daher in der chromosomalen DNA der Tiere fixiert. Die Genotypisierung
erfolgte mit zwei positiven (Plasmid und TG-positive Genom-DNA)
und zwei negativen Kontrollen (keine Amplifizierungskontrolle heterologer
Genom-DNA; keine Matrizen-Kontrolle
für die
Kontrolle von Chemikalien), wie in 3A gezeigt.
-
Analyse
der Transgen-Expression: Die Expression von mRNA, die von den Transgenen
stammte, wurde mittels RT-PCR-Analyse beurteilt, wobei allgemein
bekannte Methoden, einschließlich
RT-PCR und Agarose-Gelelektrophorese
angewendet wurden. RNA wurde aus schockgefrorenem Gewebe transgener
Tiere extrahiert und einer reversen Transkription, gefolgt von einer
spezifischen Amplifikation der cDNA, unterzogen.
-
Rattenzüchtung und
Erzeugung heterozygoter und homozygoter Ratten: Transgen-positive
Ratten wurden mit Wildtyp-SHR gezüchtet. Die Keimbahn-Übertragung
wurde in mehreren Linien erreicht. In diesem Beispiel ist die Tg-Linie
#318 gezeigt. Männliche
und weibliche transgene Ratte, von welchen jede vier Kopien des
trunkierten humanen Tau-Protein-Gens enthielt, wurden miteinander
und mit Wildtyp-SHR-Ratte gepaart, um die transgene Kolonie zu vergrößern. In
der Nachkommenschaft wurden Mendelsche Aufteilungsverhältnisse
des Transgens beobachtet (3C).
-
Die
transgenen Tiere der vorliegenden Erfindung können zum Kreuzen mit transgenen
Tieren verwendet werden, welche die humanes APP enthaltende familiäre Alzheimer-Krankheit
(FAD)-Mutation oder PS1 überexprimieren
(13). Die resultierende Ratte exprimiert sowohl APP als auch PS1
mit oder ohne FAD-Mutation auf einem hypertonen genetischen Hintergrund.
Die Wirkung von PS1 und APP auf die NFT-Bildung kann sowohl in vivo
als auch in vitro untersucht werden. Insbesondere können der
Beginn und die Schwere der AD-verbundenen Pathologien mittels Immunohistochemie
untersucht werden.
-
BEISPIEL 4: Expression des Alzheimer-Tau-Proteins
im Gehirn transgener Ratten
-
Die
Protein-Expression wurde mit Hilfe der Western-Blot-Analyse unter
Verwendung von für
Tau-Protein spezifischen monoklonalen Antikörpern vorgenommen. Es wurden
Hirngewebe von Ratten analysiert, die für das Transgen positiv waren
und das Transgen auf nachfolgende Generationen übertragen konnten. Versuche
wurden durch gleichzeitige Analyse von Hirnextrakten aus Transgennegativen,
im Alter dazu passenden Ratten und Transgen-negativen Nachkommen
desselben Wurfs kontrolliert.
-
Gewebeproben-Herstellung:
etwa 2 mg frisch isoliertes Hirngewebe wurde mechanisch in 30 μl modifiziertem
Hunt-Lysepuffer (20 mM Tris, pH 8,0, 100 mM NaCl, 1 mM EDTA, 0,5%
Igepal CA630, 0,5% Triton X-100) homogenisiert, welcher die Protease-Inhibitor-Mischung
Complete-EDTA free (Roche) enthielt. 170 μl Lysepuffer wurden zugegeben,
das Homogenat wurde mit Spritze und Nadel (22 G) trituriert und
in flüssigem Stickstoff
gefroren. Nach langsamem Auftauen auf Eis wurde das Lysat mit Schall
behandelt und 15 Minuten lang zentrifugiert, 10000 g bei +4°C. Der Proteingehalt
in den Proben wurde mit dem Bradford-Test unter Verwendung eines
Beckman-Spektrophotometers bestimmt.
-
PAGE
und Western Blot. Die Proteine wurden auf einem 12% denaturierenden
Polyacrylamid-Gel mit 0,1% (Gew./Vol.) SDS getrennt. Die Elektrophorese
wurde in Tris-Glycin-Puffer (25 mM Tris, 192 mM Glycin, 0,1% SDS)
durchgeführt.
Der Proteintrennung folgte ein Halbtrocken-Blotten. Ein Tris-Glycin-Isopropanol-Puffersystem
(25 mM Tris, 192 mM Glycin, 20% Isopropanol) wurde verwendet. Die
Tau-Proteine wurden mit monoklonalen Anti-Tau-Antikörpern DC25
gefärbt,
welche Tau-Proteine gleichermaßen
wie ein mAk 7.51 erkennen (29), und auch mit mAk Tau-1 (21). Das
positive Signal wurde unter Verwendung des Anti-Maus-HRP-Antikörpers und
der ECL-Methode bestimmt. Die Effizienz des Blot-Verfahrens wurde mittels Ponceau-Färbung kontrolliert.
Die Proteinanalyse offenbarte die spezifische Expression von Alzheimer-Tau-Protein im gesamten Protein-Extrakt
des Gehirns der transgenen Ratte (4) und auch
eine Expression von Alzheimer-Tau-Protein in verschiedenen Hirnregionen
der transgenen Ratte (5).
-
BEISPIEL 5: Immunohistochemische Analyse
des Gehirns der transgenen Ratte
-
Um
eine immunohistochemsiche Analyse der transgenen Ratte durchzuführen wurden
mehrere für Tau-Protein
und Alzheimer spezifische monoklonale Antikörper verwendet. Eine kurze
Beschreibung der in diesen Untersuchungen verwendeten monoklonalen
antikörper
umfasst PHF 1, das das phosphorylierte Epitop Ser 396–Ser 404
erkennt; mAk DC 25 erkennt Phosphat-unabhängiges Epitop Lys 347–Ile 353;
mAk AT 8 erkennt phosphoryliertes Epitop Ser 198–Ser 202; mAk Tau 1 erkennt
nicht-phosphoryliertes Epitop, mAk Tau 5 erkennt Phosphat-unabhängiges Epitop
(15, 16, 17, 18, 19, 20, 21, 22).
-
Lichtmikroskopie und Immunfluoreszenz:
-
Gewebe
wurden hergestellt und wie folgt geschnitten. Transgene und Kontroll-Tiere
wurden mit Ether anästhesiert
und sofort intrakardial mit gepuffertem 4% Paraformaldehyd perfundiert,
die Gehirne wurden entfernt, mit 20% Saccharose kryogeschützt, rasch
gefroren und mittels Kryostat zu 50 μm Dicke geschnitten. Einige
der Schnitte wurden mit 70% Ameisensäure vor dem Färbevorgang
kurz vorbehandelt. Die Rattenhirn-Gewebeschnitte wurden mit 1% H2O2 in PBS inkubiert,
und die unspezifischen Bindungsstellen wurden durch Inkubation mit
Blockier-Medium (PBS, 0,1% Triton, 5% normales Pferdeserum) blockiert.
Die Immunfärbung
erfolgte unter Verwendung von oben angeführten Antikörpern, danach wurde mit biotinyliertem
Pferd-anti-Maus-Antikörper
inkubiert, gefolgt von Avidin-Biotin-Komplex, und es wurde mit VIP
und DAB-Lösung
sichtbar gemacht. Die Gewebeschnitte wurden auf mit Gelatine beschichteten
Objektträgern
montiert, getrocknet, mit abgestuften Alkoholen, Xylol behandelt
und mit Entellan oben bedeckt.
-
Silberfärbung:
-
Die
Gallyas-Silberfärbungsmethode,
die früher
beschrieben wurde (23), wurde für
frei schwebende 50 μm-Schnitte
mit Goldtönung
(„gold
toning") adaptiert.
-
Immunfluoreszenzfärbung:
-
Zur
indirekten Immunfluoreszenz-Markierung wurden Schnitte mit 1% NaHBO4 30 min lang vorbehandelt, um die Autofluoreszenz
des Hirngewebes zu verringern; dann mit primären Antikörpern bei 4°C über Nacht gefärbt, mit
biotinyliertem Pferd-anti-Maus-Antikörper inkubiert, gefolgt von
Streptavidin-Alexa 488-Konjugat.
-
Der
Vergleich der NF-Pathologie, wie man sie in den Gehirnen von Patienten
mit AD sieht, mit jener, die man im Gehirn des transgenen Tiers
der vorliegenden Erfindung beobachtet, ist in 10 gezeigt.
-
BEISPIEL 6: Ein Screening-Testsystem für Arzneimittel-Ansätze und
Arzneimittel-Anwärter
für die
Behandlung und Prävention
der Alzheimer-Krankheit.
-
Die
transgenen Tiere der vorliegenden Erfindung können als Zell-Quelle für die Zellkultur
verwendet werden. Sowohl Tiere als auch Zellen können bei Tests dieser Erfindung
verwendet werden. Beispielsweise können Zellen vor Hirngewebe,
die trunkiertes Tau-Gen exprimieren, unter Verwendung von Standard-Züchtungstechniken verwendet
werden. Die Tiere und die gezüchteten
Zellen können
als In-vivo- und In-vitro-Systeme für die Untersuchung der Rolle
der Arzneimittel-Anwärter
auf das Zeltgerüst,
die Zellteilung und die Apoptose sowie auf eine Morphologie der
primären
gezüchteten
Neuronen, das Sprossen von Neuriten, Axon-Verzweigung und Axon-Verlängerung
in den Primärkulturen
und auch für
die Untersuchung der Organellen-Bewegung verwendet werden (9).
Sie können
auch als Testsystem für
neurotrophe Wirkungen von getesteten Substanzen verwendet werden.
-
Eine
Studie kann entworfen werden, um auf quantitative oder qualitative
Veränderungen
bei einer Wechselwirkung von Tau und Tubulin und auch bei einer
Wechselwirkung mit Organellen-Austausch („trafficking"), der durch die
getesteten Substanzen moduliert werden kann, zu screenen.
-
Es
kann auch eine Studie entworfen werden, um auf Verbindungen zu screenen,
die die Expression oder Aktivität
der Zellskelett-Proteine im Prozess des Aufbaus von synaptischen
Verbindungen modulieren.
-
Eine
Studie kann auch entworfen werden, um auf jene Verbindungen zu screenen,
die die NFT-Bildung oder die Protein-Protein-Interaktion beeinflussen
können,
was schließlich
zur Verlangsamung, Inhibierung oder Eliminierung der NFT-Bildung
führen
könnte,
und dies könnte
ein nützlicher
Test zum Screenen auf Substanzen sein, die potentielle Therapeutika
für Tauopathien
und andere neurodegenrative Erkrankungen, vorzugsweise AD, sein
könnten.
Die Wirkung der Verbindungen kann in Zellkulturen und auch in vivo
an den Tieren mittels neuropathologischer, neurophysiologischer
und behavioraler Analyse evaluiert werden. Viele Variationen der
Screening-Methoden sind dem Fachmann bekannt und können im
Rahmen der vorliegenden Erfindung angewendet werden.
-
Diese
Beispiele beschreiben besondere Aspekte und Ausführungsformen der Erfindung
zu illustrativen Zwecken und schränken den Umfang der Erfindung,
wie er durch die nachfolgenden Patentansprüche angegeben ist, nicht ein.
-
Literaturstellen:
-
- 1. Martin, J.B., (1999) N. Engl. J. Med. 340, 1970–1980.
- 2. Wischik CM, Novak M, Edwards PC, Klug A, Tichelaar W, Crowther
RA (1988a) Proc Natl Acad Sci USA 85: 4884–4888
- 3. Wischik CM, Novak M, Trogersen HC, Edwards PC, Runswick MJ,
Jake R, Walker JE, Milstein C, Roth M, Klug A(1988b) Proc Natl Acad
USA 85: 4506–4510
- 4. Hutton N, Lendon CL, Rizzu P, Baker N, Froelich S., Houlden
H, Pickering-Brown S, Chackraverty S, Isaacs A, Grover A (1998)
Nature 393, 702–705
- 5. Spillantini NG, Murrell JR, Goedert M, Farlow MR, Klug A,
Ghetti B (1998) Proc Natl Acad Sci USA 95, 7737–7741.
- 6. Lewis J, Dickson DW, Lin WL, Chisholm L, Corral A, Jones
G, Yen SH, Sahara N, Skipper L, Yager D, Eckman C, Hardy J, Hutton
N, McGowan E.: Science 2001 Aug 24;293(5534): 1487–1491
- 7. Goedert M, Spillantini MG.: Biochem Soc Symp 2001; 67: 59–71
- 8. Spittaels, K., C. Van den Haute, et al.: Am J Pathol (1999),
155 (6): 2153–65.
- 9. Duff, K., H. Knight, et al.: Neurobiol Dis (2000) 7 (2):
87–98.
- 10. Czech C, Lesort M, Tremp G, Terro F, Blanchard V, Schombert
B, Carpentier N, Dreisler S, Bonici B, Takashima A, Moussaoui S,
Hugon J, Pradier L.: Neuroscience (1998) Nov; 87 (2): 325–36
- 11. Echeverria V and Cuello AC.: Mol Neurobiol (2002) Oct-Dec;
26(2–3):
299–316
- 12. Breteler, MMB.: Neurobiology of Aging 21 (2000) 153–160
- 13. in't Veld
B.A., A. Ruitenberga, A. Hofmana, B.H.Ch. Stricke ra, M.M.B. Bretelera,:
Neurobiology of Aging 22 (2001) 407–412
- 14. Sambrook et al., Molecular Cloning, A Laboratory Manual,
Cold Spring Harbor Laboratory Press, 1989
- 15. Hogan, B. et al. Manipulating the Mouse Embryo, a Laboratory
Manual. Cold Spring Harbor Laboratory, 1986
- 16. Bramblett GT, Goedert M, Jakes R, Merrick SE, Trojanowski
JQ, Lee VM.: Neuron (1993) 10: 1089–99
- 17. Biernat J, Mandelkow EM, Schroter C, Lichtenberg-Kraag B,
Steiner B, Berling B, Meyer H, Mercken M, Vandermeeren A, Goedert
M, et al.: EMBO J (1992) Apr; 11(4): 1593–7
- 18. Braak E. Braak H, Mandelkow EM: Acta Neuropathol (Berl).
(1994); 87(6): 554–67.
- 19. Goedert M, Jakes R, Vanmechelen E.: Neurosci Lett (1995)
Apr
- 21; 189(3): 167–9
- 20. Szendrei GI, Lee VM, Otvos L Jr.: J Neurosci Res (1993)
Feb 1; 34(2): 243–9
- 21. Binder LI, Frankfurter A, Rebhun LI. J: Cell Biol (1985)
Oct; 101(4): 1371–8
- 22. LoPresti P, Szuchet S, Papasozomenos SC, Zinkowski RP, Binder
LI.: Proc Natl Acad Sci USA (1995) Oct 24; 92(22): 10369–73
- 23. Gallyas, F.: Acta Morphol. Acad. Sci. Hung. (1971) 19, 1–8.
- 24. Goedert M, Spillantini MG, Jakes R, Rutherford D, Crowther
RA (1989) Neuron 4, 519.
- 25. Gordon JW, Chesa PG, Nishimura H, Rettig WJ, Maccari JE,
Endo T, Seravalli E, Seki T, Silver J.: Cell. 1987 Jul 31; 50(3):
445–52.
- 26. Damiano PF, Roson MI, Armando I, Nowicki S, Dascal E, Cuni berti
L, Albornoz LE, de la Riva IJ. Potential role of glycerol leading
to rat fructose hypertension. Hypertension 1999 Oct; 34 (4Pt 2):
1007–11;.
- 27. Jackson B, Fabris B, Paxton D, Franze L, Johnston CI. High
salt diet ameliorates effects of angiotension converting enzyme
inhibition in spontaneously hypertensive streptozotocin diabetic
rats. Clin Exp Pharmacol Physiol. 1990 Mar; 17(3); 229–34.
- 28. Turley SD, Hansen CT. Rates of sterol synthesis in the liver
and extrahepatic tissues of the SHR/N-corpulent rat, an animal with
hyperlipidemia and insulin-independent diabetes. J Lipid Res. 1986-May;
27(5): 486–96.
- 29. Novak M, Jakes R, Edwards PC, Milstein C, Wischik CM.: Proc
Natl Acad Sci USA. 1991 Jul 1; 88(13): 5837–41.
-
-
-
-
-
-
-
-
-